Изобретение относится к комбинированным фармацевтическим препаратам, пригодным для лечения заболеваний системы кровообращения и содержащих ингибитор системы ренин - ангиотензин (ингибитор RAS) и антагонист эндотелина.
Система ренин - ангиотензин играет важную роль в регуляции кровяного давления. Эту систему можно представить в виде протеолитического каскада, состоящего из следующих ступеней:
1. Фермент ренин расщепляет ангиотензиноген на ангиотензин I, который является биологически неактивным.
2. Ангиотензин I преобразуется с помощью фермента ACE (Angiotensin Converting Enzyme - фермент, преобразующий ангиотензин) в ангиотензин II.
3. Ангиотензин II связывает на рецепторы в мембране эффекторных клеток и обусловливает биологическую реакцию.
Такие биологические реакции весьма разнообразны. Это может проявляться, например, в сокращении кровеносных сосудов, биосинтезе альдостерона и стимулировании роста сосудов после какого-либо повреждения.
Систему ренин - ангиотензин можно ингибировать на всех трех описанных выше ступенях, а именно: на первой ступени - путем применения ингибитора ренина, на второй - путем применения ингибитора ACE и на третьей - путем применения антагониста рецептора ангиотензина II.
При лечении высокого кровяного давления и сердечной недостаточности ингибиторы ACE приобрели большое значение. Прототипом веществ этого класса является каптоприл. Ингибиторов ренина и антагонистов рецептора ангиотензина II до настоящего времени в продаже нет, однако работы по их созданию ведутся во всем мире.
Эндотелин представляет собой открытый лишь несколько лет тому назад пептидный гормон [см. Yanagisawa et al., Nature 332. 411-415 (1988)], проявивший себя до сих пор как наиболее сильный вазоконстриктор. Эндотелин выделяется эндотелиальными клетками, выстилающими внутреннюю поверхность кровеносных сосудов. И хотя его концентрация в плазме крови очень низка, можно исходить из того, что локальные концентрации между эндотелиальными клетками и соседними гладкими мышечными клетками сосудов значительно выше.
Повышенный уровень эндотелина в плазме крови отмечается при целом ряде заболеваний сердечно-сосудистой системы, таких как гипертония, сердечная недостаточность, ишемия (сердце, мозг, желудочно-кишечный тракт, почки), или при спазмах сосудов. У пациентов, страдающих астмой, отмечается повышенная концентрация эндотелина в секрете бронх. Точно так же повышается уровень эндотелина в плазме крови при приступах мигрени.
Эндотелин связывает на специфические рецепторы эффекторных клеток. На сегодняшний день имеется описание по крайней мере двух подтипов таких рецепторов, а именно рецептор эндотелина A и рецептор эндотелина B [см. Lin et al., Proc. Natl. Acad. Sci., США 88, 3185-3189 (1991) и Sakamoto et al., Biochen. Biophys. Res. Commun. 178. 656-663 (1991)]. Эндотелин A вызывает сужение сосудов, что же касается эндотелина B, то его роль до настоящего времени полностью еще не выявлена.
Так как патофизиологическое значение эндотелина велико, то существует потребность в создании соответствующего антагониста эндотелина. Так, например, в европейских патентных публикациях EPA 405421, 436189, 457195, 460679 и 496452, а также Journ. Antibiotics 45, 74 (1992), FEBS 305, 41 (1992) и Biochem. Biophys. Res. Commun. 185, 630 (1992) описывается ряд соединений, ингибирующих связывание эндотелина с рецептором. Правда, речь идет здесь либо о веществах, обнаруженных в бродильных отварах, получить которые химическим путем практически невозможно, либо о пептидах, которые, по всей видимости, по причине недостаточной надежности в биологическом отношении непригодны для орального введения человеку. В отличие от этого описанные в EPA 510526 и 526708 и в заявке WO 93/08799 антагонисты эндотелина имеют простую химическую структуру и обладают тем преимуществом, что могут вводиться оральным путем.
Комбинированный препарат для лечения гипертонии, содержащий ингибитор ACE цилазаприл и антагонист ионов кальция - нитрендипин (Nitrendipin) описан в патенте США 4859665.
В рамках настоящего изобретения удалось установить, что при введении предлагаемой согласно изобретению композиции, содержащей ингибитор системы ренин - ангиотензин в сочетании с антагонистом эндотелина, не только суммарно улучшаются снижающие кровяное давление свойства и повышается продолжительность действия отдельных компонентов, но и неожиданным образом эти факторы усиливаются, благодаря чему эффективные дозы обоих компонентов могут быть существенно уменьшены.
В соответствии с этим композиция согласно изобретению обладает тем преимуществом, что вводимые количества биологически активных веществ могут быть значительно снижены, а нежелательные побочные явления полностью исключены или по крайней мере существенно ограничены.
Благодаря этому предлагаемая согласно изобретению композиция может применяться в качестве средства для лечения заболеваний, связанных с сужением сосудов или обусловленных каким-либо другим биологическим эффектом эндотелина и/или ангиотензина II. Примерами таких заболеваний являются высокое кровяное давление, коронарная болезнь, сердечная недостаточность, почечная и миокардиальная ишемия, почечная недостаточность, диализ, субарахноидальное кровоизлияние, синдром Рейно и легочное высокое давление. Сюда же относится лечение язвы желудка и двенадцатиперстной кишки, а также варикозной язвы, т. е. заболеваний, обусловленных сужением сосудов.
Названные средства могут использоваться также при атеросклерозе и для предупреждения рестеноза после индуцированного вздутием легких расширения сосудов.
Согласно настоящему изобретению предлагается фармацевтический препарат, содержащий ингибитор системы ренин - ангиотензин - цилазаприл и антагонист эндотелина - 4-трет. бутил-N- [6-(2-гидроксиэтокси)-5-(2-метоксифенокси)-2,2'-бипиримидин-4- ил]бензолсульфонамид при массовом соотношении соответственно 1:1 - 1:100.
Предпочтительно суточная доза вводимой композиции составляет 2,5-10 мг ингибитора RAS и 250-1000 мг антагониста эндотелина. Как правило, общее количество вводимых ингибитора RAS и антагониста эндотелина составляет максимум 550 мг в день. При использовании гидрата или применимой в фармацевтике соли указанные выше значения должны быть соответственно изменены.
Соотношение между массой ингибитора RAS и массой антагониста эндотелина можно выбирать и в пределах от 1:1 до 1:500.
Таким образом, исходя из сказанного, настоящее изобретение описывает:
- композицию из ингибитора RAS и антагониста эндотелина,
- фармацевтический препарат, содержащий ингибитор RAS и антагонист эндотелина,
- получение фармацевтической композиции из смеси, содержащей ингибитор RAS и антагонист эндотелина в виде лечебного средства, в виде галеновой формы препарата,
- применение композиции из ингибитора RAS и антагониста эндотелина, соответственно фармацевтического препарата, содержащего ингибитор RAS и антагонист эндотелина, для проведения одновременного, раздельного или же через определенные интервалы времени лечения заболеваний, связанных с сужением сосудов или с каким-либо другим биологическим воздействием эндотелина и/или ангиотензина II, прежде всего заболеваний системы кровообращения, в особенности при терапии, соответственно предупреждении гипертензии и вызываемых ею осложнений, а также при лечении сердечной недостаточности.
В качестве ингибитора системы ренин - ангиотензин можно рассматривать ингибиторы ренина, ингибиторы ACE и антагонисты ангиотензина II. Предпочтительно применять ингибиторы ACE. Пригодными для достижения поставленной в настоящем изобретении цели могут быть такие ингибиторы ACE, как Alacepril, Benazepril, Captopril, Cilazapril, Cilazaprilat, Delapril, Enalapril, Enalaprilat, Fosinopril, Lisinopril, Perindopril, Quinapril, Ramipril, Spirapril, Zofenopril и MC 838 [кальциевая соль (R-(R,S)-1-(3-((2-((циклогексилкарбонил)амино)-1-оксопропил)тио)-2- метил-1-оксопропил)-L-пролина] , а также аналоги указанных соединений, описанные в европейских патентных публикациях EPA-7477, 12401, 50800, 51391, 53902, 65301, 72352, 94095, 172552, 211220 и 271795, в патентах США 4105776 и 4316906, в патенте Великобритании 2102412, а также в Tetrahedron Letters, 23, 1677-1680 (1982). К предпочтительным ингибиторам ACE относятся соединения, которые в приведенных публикациях выделены особо. Особенно предпочтительными ингибиторами ACE являются названные выше соединения. Наиболее предпочтителен среди них Cilazapril, описанный в DE-OS 2117571.
Пригодными для целей настоящего изобретения ингибиторами ренина могут быть следующие соединения:
Ciprokiren
(S)-2-бензил-N-[(S)-1-[(1S, 2R, 3S)-1-циклогексилметил-3-циклопропил- 2,3-дигидроксипропилкарбамоил] -2-(имидазол-4-ил)этил] -3-[1-метил-1- (морфолин-4-илкарбонил)этилсульфонилметил]пропионамид;
Ditekiren
Boc-Pro-Phe-N-His-Leu-(CHOH-CH2)-Val-Ile-Asp;
Enalkiren
[1S-(1R*, 2S*,3R*)]-N-(3-амино-3-метил-1- оксобутил)-O-метил-L-тирозил-N-[1-(циклогексилметил)-2,3-дигидрокси-5 -метилгексил]-L-гистидинамид;
Remikiren
(S)-2-тpeт. бутилcульфoнилмeтил-N-[(S)-1-[(1S,2R,3S)-1- циклогексилметил-3-циклопропил-2,3-дигидроксипропилкарбамоил] -2- (1H-имидазол-4-ил)метил] -3-фенилприонамид;
Terlakiren
[R-(R*,S*)]-N-(4-морфолинилкарбонил)-L-фенилаланил- N-[1-(циклогексилметил)-2-гидрокси-3-(1-метилэтокси)-3-оксопропил]- S-метил-L-цистеинамид;
A 65 317
1(S)-циклогексилметил-2(R)-гидрокси-2-[3-этил-2-оксооксазолидин- 5(S)-ил] этиламид N-[2(R)-бензил-N-[2-[2-(2-метоксиэтокси)метокси] этил] - N-метилсукцинамоил]гистидина;
A 72 517
1(S)-(циклогексилметил)-2(R), 3(S)-дигидрокси-5-метилгексиламид N-[2(S)-бензил-3-(4-метил-1-пиперазинилсульфонил)пропаноил] -3-(4- тиазолил)-L-аланина;
A 70 461
N-[2(S)-амино-1-циклогексил-3(R), 4(S)-дигидрокси-6-метилгепт- 1-ил] -2(S)-[1(S)-[4-(метоксиметокси)пиперидин-1-илкарбонил] - 2-фенилэтокси]гексанамид;
A 74 273
6-циклогексил-4(S)-гидрокси-2(S)-изопропил-5(S)-[2(S)-[1 (S)-[4-(метоксиметокси)пиперидин-1-илкарбонил]-2-фенилэтокси] гексанамидо]-N-(3-морфолинопропил)гексанамид;
A 82 110
6-циклoгeкcил-4(S)-гидpoкcи-2(S)-изoпpoпил-5(S)-[N-[1 (S)-[4-(метоксиметокси)пиперидин-1-илкарбонил] -2-фенилэтил] -L-норлейциламино]-N-(2-метил-2-морфолинопропил)гексанамид;
WAY 121 604
метиловый эфир (3S)-4-циклогексил-2-гидрокси-3-[[(2S)-4- метил-2-[[(2S)-2-(1-оксо-1,3-дигидроизоиндол-2-ил)-3-фенилпропионил] амино] пентаноил]амино]масляной кислоты;
SQ 31 844
[R-(R*,S*)]-N-(4-морфолинилкарбонил)-L-фенилаланил]- N-[1-(циклогексилметил)-2-гидрокси-2-(1H-имидазол-2-ил)этил]-L- гистидинамид;
SQ 33 800
[1S-[1R*(R*), 2S*, 3S*]]-[2-(трет. бутилсульфонилметил)-1-оксо-3-фенилпропил] -N-[4-[(бутиламино) сульфонил] -1-(циклогексилметил)-2,3-дигидроксибутил]-L-гистидинамид- монометаносульфонат;
GR 70 982
[1S-(1R*, 2R*, 4S*)] -N-[(1,1-диметилэтокси) карбонил]-L-фенилаланил-N-[5-[(4-аминобутил)амино] -1-(циклогексилметил)- 2-гидрокси-5-оксо-4-(4-пиридинилметил)пентил]-L-гистидинамид;
ICI 219 623
(2S, 4S,5S)-N-бутил-6-циклогексил-4-гидрокси-2-изопропил-5-[2- [8-пропил-6-(3-пиридил)-1,2,4-триазоло[4,3-а] пиразин-3-ил] -3-(3-пиридил) пропионамидо]-гексанамид;
L 157 119
4-(Boc-Phe-His-ACHPA-Lys-NH-CH2)пиридин;
CP 71 362
[2R-(2R*, 4S*, 5S*)] -N-[N2-[6-циклогексил-5- [[N-[N-[(1,1-диметилэтокси)-карбонил] -L-фенилаланил] -L-гистидил] амино]- 4-гидрокси-2-(2-метилпропил)-1-оксогексил]-L-лизил]-L-фенилаланин- диацетат;
ES 8 891
5-циклогексил-2,4,5-тридеокси-N-гексил-4-[[N-[3-(1-нафталенил)- N-(4-морфолинилацетил)-L-аланил] -3-(4-тиазолил)-L-аланил] амино]- L-треопентанамид;
ES 1 005
[1S-[1R*(R*), 2R*, 4[R*(R*)] ] ] - N-[4-[[1-[[(5-амино-6-гидроксигексил)амино] -карбонил]-3- метилбутил]амино]-2-гидрокси-1-(2-метилпропил)- 4-оксобутил] -α-[[3-(1- нафталенил)-2-(1-нафталенилметил)- 1-оксопропил]амино] -1H-имидазол-4-пропанамид;
PD 132 002
[1S-(1R*, 2S*, 3R*)] -N-(4-морфолинилсульфонил)- L-фенилаланил-N-[1-(циклогексилметил)-2,3-дигидрокси-5-метилгексил] - O-метил-3-оксо-D- либо L-серинамид;
PD 134 674
([1S-(1R*, 2S*, 3R*)] )-N-(4-мopфoлинилcульфoнил)- L-фeнилaлaнил-3-(2-амино-4-тиазолил)-N-[(циклогексилметил)-2,3- дигидрокси-5-метилгексил]-L-аланинамид;
YM 21 095
N-[2-[[1-(циклогексилметил)-2-гидрокси-3-[(1-метил-1H- тетразол-5-ил)тио] пропил] амино] -1-(1H-имидазол-4-илметил)-2- оксоэтил]-α-(1-нафталенилметил)-γ-оксо-4-морфолинобутанамид;
FK 906
1(S)-(циклогексилметил)-2(S)-гидрокси-5-метилгексиламид N-метил-N-[2(S)-[N-метил-N-[2-[N-метил-N-(морфолинокарбонил)амино] этил]карбамоил]-3-фенилпропионил]-L-гистидина;
FK 744
этиловый эфир [1S-[1R*[R*(R*)],2R*]]-метил-[3-(4- морфолинил)-3-оксопропил] -2-[[2-[[1-(циклогексилметил)-2- гидрокси-5-метилгексил] амино] -1-(1H-имидазол-4-илметил)-2- оксоэтил] метиламино]-2-оксо-1-(фенилметил) карбаминовой кислоты;
S 89-2864
1(S)-(циклогексилметил-2(R), 3(S)-дигидрокси-5-(2-пиридил) пентиламид 3-(4-аминопиперидин-1-илкарбонил)-2(R)-бензилпропионил- L-гистидина, ацетат;
MDL 73 323
1-(циклогексилметил)-3,3-дифторо-4-(3-метилбутирамидо)-2- оксобутиламид 3-амино-3-метилбутирил-(4-O-метил)-L-тирозил-L- норвалина, гидрохлоридгидрат; и
JTP 3 071
1H-индол-2-илкарбонил-L-гистидин-1(S)-(циклогексилметил)- 2(S),4(S)-дигидрокси-5-метилгексиламид.
Пригодными для целей настоящего изобретения антагонистами ангиотензина II являются следующие:
Losartan
калиевая соль 2-бутил-4-хлор-1-[[2'-(1H-тетразол-5-ил)-[1,1'- бифенил] -4-ил]метил]-1H-имидазол-5-метанола;
Valsartan
N-(1-оксопентил)-N-[[2'-(1H-тетразол-5-ил)[1,1'-бифенил] -4-ил] метил]-L-валин;
BIBS 39
4'-[(2-n-бутил-6-циклогексиламинокарбониламинобензимидазол-1-ил) метил] бифенил-2-карбоновая кислота;
BIBS 222
2-n-бутил-1-[4-(6-карбокси-2,5-дихлорбензоиламино)бензил] -6- N-(метиламинокарбонил)-n-пентиламинобензимидазол;
BIBR 277
4'-[(1,4'-диметил-2'-пропил-[2,6'-би-1H-бензимидазол] -1'-ил) метил] -[1,1'-бифенил]-2-карбоновая кислота;
DuP 532
4-(пентафторэтил)-2-пропил-1-[[2'-(1H-тетразол-5-ил) [1,1'-бифенил]-4-ил]метил]-1H-имидазол-5-карбоновая кислота;
EXP 7 711
4'-[[2-бутил-4-хлор-5-(гидроксиметил)-1H-имидазол-1-ил] метил] -[1,1'-бифенил]-2-карбоновая кислота;
D 6 888
2-этил-5,6,7,8-тетрагидро-4-([2'-(1H-тетразол-5-ил)бифенил-4-ил] метокси)-хинолин;
D 8 731
2-этил-4-[(2'-(1H-тетразол-5-ил)бифенил-4-ил)метокси] хинолин- гидрохлорид;
GR 117 289
1-((3-бром-2-(2-(1H-тетразол-5-ил)фенил)-5-бензофуранил)метил)- 2-бутил-4-хлор-1H-имидазол-5-карбоновая кислота;
GR 138 950
1-[[3-бром-2-[2-[[(трифторметил)сульфонил] амино]фенил]-5- бензофуранил] метил]-4-циклопропил-2-этил-1H-имидазол-5-карбоксамид;
L 158 809
5,7-диметил-2-этил-3-(2'-(1H-тетразол-5-ил)(1,1'-бифенил)-4-ил) метил)-3H-имидазо-(4,5-b)пиридин;
SC 50 560
5-[4'-(3,5-дибутил-1,2,4-триазол-1-илметил)бифенил-2-ил]-1H- тетразол;
SC 51 895
1,4-дибутил-3-[2'-(1H-тетразол-5-ил)бифенил-4-илметил] -2,3-дигидро- 1H-имидазол-2-он;
SR 47 436
2-n-бутил-4-спироциклопентан-1-[(2'-(1H-тетразол-5-ил)бифенил- 4-ил)метил]-2-имидазолин-5-он;
SKF 108 566
(E)-α-[[2-бутил-1-[(4-карбоксифенил)метил] -1H-имидазол-5-ил] метилен]-2-тиофенпропановая кислота;
TCV 116/CV 11 974
1-[[(циклогексилокси)карбонил] окси]этиловый эфир 2-этокси-1-[[2'- (1H-тетразол-5-ил)-[1,1'-бифенил] -4-ил] метил] -1H-бензимидазол- 7-карбоновой кислоты;
CI 996
2-пропил-4-[(3-трифторацетил)пиррол-1-ил] -1-[[2'-(2H-тетразол- 5-ил)[1,1'-бифенил]4-ил]метил]-1H-имидазол-5-карбоновая кислота; и
YM 358
калиевая соль 2,7-диэтил-5-[[2'-(1H-тетразол-5-ил)[1,1'-бифенил]- 4-ил] метил]-5H-пиразоло[1,5-b][1,2,4]триазола.
В качестве антагонистов эндотелина могут быть использованы различные пептидные и непептидные производные, причем из-за упоминавшейся выше плохой бионадежности, присущей пептидным производным, предпочтительны непептидные производные. Особенно предпочтительными среди непептидных производных являются те из них, которые могут с эффективностью использоваться орально. Примерами пептидных производных являются следующие:
FR 139 317
пергидроазепин-1-илкарбонил-L-лейцил-(1-метил)-D-триптофил- [3-(2-пиридил)]-D-аланин;
FR 901 367
2-ацетамидо-3-[[1,4,4a,5,6,6a,7,12,12a,12b-декагидро-4a,8,12a, 12b-тетрагидрокси-3-метил-1,7,12-триоксобенз[α]антрацен-6a-ил] тио]пропионовая кислота;
BE 18 257 B
цикло(-D-Trp-D-Glu-L-Ala-алло-D-Ile-L-Leu-);
BQ 123
цикло(-D-Trp-D-Asp-L-Pro-D-Val-L-Leu-);
пергидроазепин-1-илкарбонил-L-лейцил-D-триптофил-D-триптофан;
Cochinmicin I;
эфир мирицерон-кофейной кислоты и
PD 142 893
ацетил-(3,3-дифенил-D-аланин)-L-Leu-L-Asp-L-Ile-L-Ile-L-Trp.
Пригодными для целей настоящего изобретения непептидными антагонистами эндотелина являются, например, сульфонамиды и производные индана и индена, описанные в европейских патентных публикациях EPA 510526 и 526708 и в заявке WO 93/08799, в частности следующие соединения:
4-трет. бутил-N-[6-(2-гидроксиэтокси)-5-(2-метоксифенокси)- 2,2'-бипиримидин-4-ил]бензолсульфонамид (описан в EPA 526708);
(1RS, 2SR, 3SR)-1-(4-метоксифенил)-3-(3,4-метилендиоксифенил) индан-2-карбоновая кислота;
(1RS, 2RS, 3SR)-5-гидрокси-3-(4-метоксифенил)-1-(3,4- метилендиоксифенил)индан-2-карбоновая кислота;
(1RS, 2RS, 3SR)-5-метокси-3-(4-метоксифенил)-1-(3,4- метилендиоксифенил)индан-2-карбоновая кислота;
(1RS, 2RS,3SR)-1,3-бис(3,4-метилендиоксифенил)-5-гидроксииндан- 2-карбоновая кислота;
(1RS, 2RS, 3RS)-3-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота;
(1RS, 2RS, 3SR)-3-(2-карбоксиметокси-4-метоксифенил)-1-(2-метокси- 4,5-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота;
бисдициклогексиламиновая соль (1RS,2RS,3RS)-3-[2-(1-карбоксиэт- 2-илокси)-4-метоксифенил] -1-(3,4-метилендиоксифенил)-5-(проп-1-илокси) индан-2-карбоновой кислоты;
(1RS,2RS,3SR)-[2-[(E)-2-карбоксиэтен-1-ил]-4-метоксифенил]-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота;
(1RS, 2RS,3SR)-3-[2-(2-карбоксиэт-1-ил)-4-метоксифенил]-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота; и
(1RS, 2RS,3RS)-3-[2-(3-карбоксифенил)-4-метоксифенил]-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота.
Предлагаемая согласно изобретению комбинация из 4-трет.бутил-N- [6-(2-гидроксиэтокси)-5-(2-метоксифенокси) -2,2'-бипиримидин-4-ил] бензолсульфонамида (называемого ниже также "соединение A") и Cilazapril'a является наиболее оптимальной.
Благодаря применению комбинированного препарата согласно изобретению с помощью небольших доз биологически активных веществ удается достичь регулярного и продолжительного действия по снижению кровяного давления.
Предпочтительный сверхсуммарный эффект по снижению кровяного давления, равно как и увеличение продолжительности действия, композиции согласно изобретению по сравнению с названными факторами обоих компонентов в отдельности поясняется на описанных ниже опытах.
Снижение кровяного давления у спонтанно гипертензивных крыс.
Одна из первых серий экспериментов проводилась на крысах. При этом использовали крыс рода SHRSP (вес около 300 г и возраст 18-20 недель). SHRSP (spontaneously hypertensive rats, stroke prone - спонтанно гипертензивные крысы, ударозаторможенные) - общепринятое название спонтанно гипертензивных крыс, у которых с возрастом развивается склонность к кровоизлиянию в мозг. В возрасте 18 недель кровяное давление у этих крыс стабилизировалось.
Артериальное кровяное давление у этих крыс измеряли с помощью телеметрического метода. Создателем этой телеметрической системы является фирма Data Scienses, Inc., Сан-Поль, Миннесотта, США. Измерение кровяного давления осуществляли заполненным жидкостью катетером, который заранее был имплантирован в брюшную аорту. Имплантацию осуществляли под наркозом короткого действия (15-20 мин) с помощью Evipan® (100 мг/кг, внутрибрюшинно). Катетер был соединен с минипередатчиком в брюшной полости, от которого на передатчик, расположенный вне клетки, поступали сигналы, соответствовавшие колебаниям кровяного давления. Таким путем обеспечивалась возможность непрерывного измерения на свободно перемещавшихся подопытных животных в течение продолжительного времени.
Эксперименты проводились на группе из 9 крыс по Cross-Over-методике, т. е. каждой из этих крыс один раз не вводили никакой субстанции (только растворители), один раз вводили соединение A, один раз Cilazapril и один раз композицию из соединения A и Cilazapril. Временной интервал между отдельными введениями составлял по крайней мере 48 часов. Дозировка составляла 100 мг/кг орально для соединения A и 1 мг/кг орально для Cilazapril. Введение осуществляли с помощью желудочного зонда.
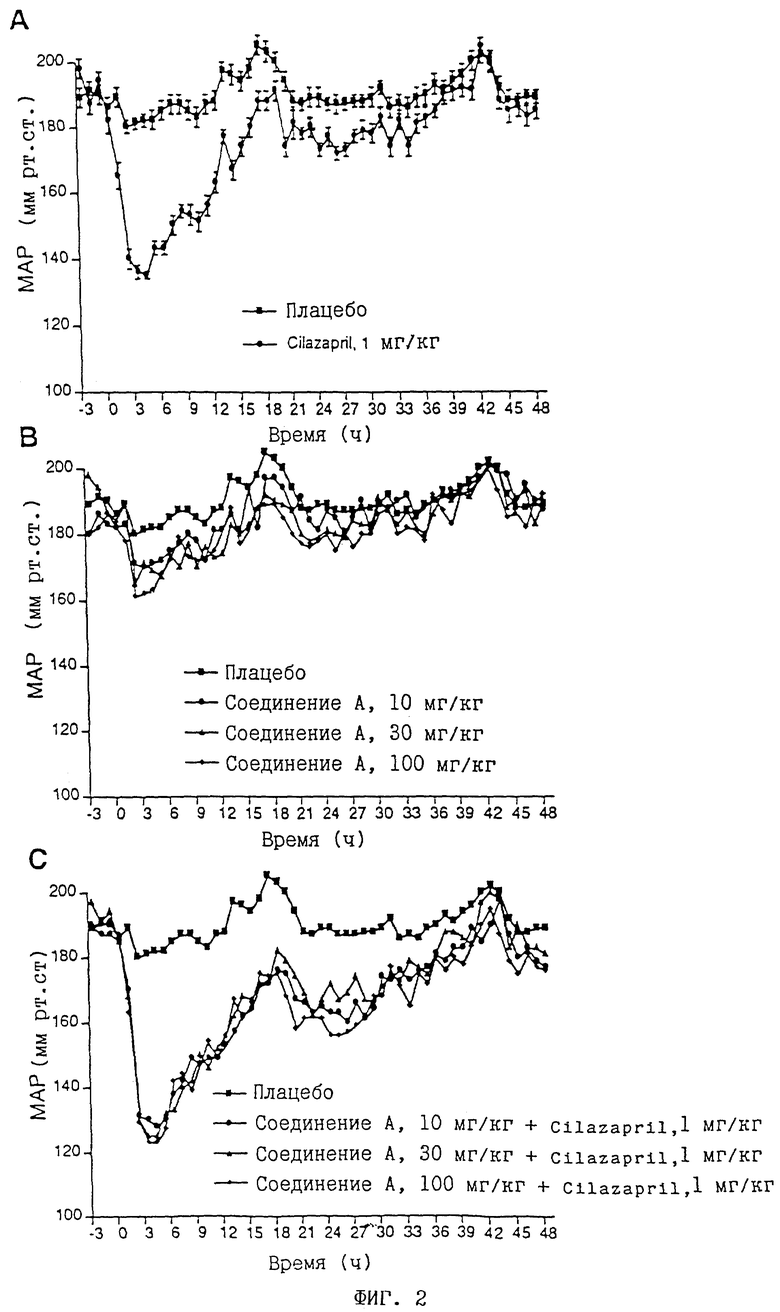
На фиг. 1 представлены результаты этой первой серии экспериментов, иллюстрирующие эффективность Cilazapril (1 мг/кг перорально) и соединения A (100 мг/кг перорально), вводившихся раздельно, и эффективность одновременного введения тех же доз обеих субстанций (n = 9 крыс).
Для подтверждения достоверности полученных результатов был проведен ряд других экспериментов, в которых подопытным животным вводили соединение A в двух других дозировках, а именно 10 и 30 мг/кг перорально, тогда как доза Cilazapril составляла, как и в первой серии опытов, 1 мг/кг перорально (фиг. 1C). Полученные результаты представлены на фиг.2, причем данные по одному только Cilazapril, равно как и при его введении со 100 мг/кг соединения A, включены в фиг. 2 из предыдущей серии.
Приведенные на фиг. 1 и 2 значения представляют собой средние значения кровяного давления у 9 подопытных животных, полосы границ погрешности указывают стандартную погрешность. Так как дальнейшие пояснения не требуются, эти полосы на фиг. 2B и 2C опущены.
Соединение A немного снижало среднее артериальное кровяное давление (MAP), причем максимальный эффект составлял 20 мм ртутного столба (фиг. 2B). Cilazapril подтвердил ожидаемое снижение давления, сохранявшееся примерно в течение 20 часов (максимальный эффект: снижение кровяного давления приблизительно на 45 мм ртутного столба (фиг. 2A)). При введении композиции кровяное давление снижалось максимально на примерно 60 мм ртутного столба, причем следует отметить, что через 20 часов все еще можно было наблюдать очевидный эффект, а еще через 40 часов этот эффект был таким же, как и через 20 часов после введения одного Cilazapril (фиг. 2C). Обе более низкие дозы соединения А оказывали примерно такое же воздействие, что и высокая доза (фиг. 2B). Указанные данные подтверждают увеличение продолжительности действия.
Снижение кровяного давления у обезьян с нормальным давлением.
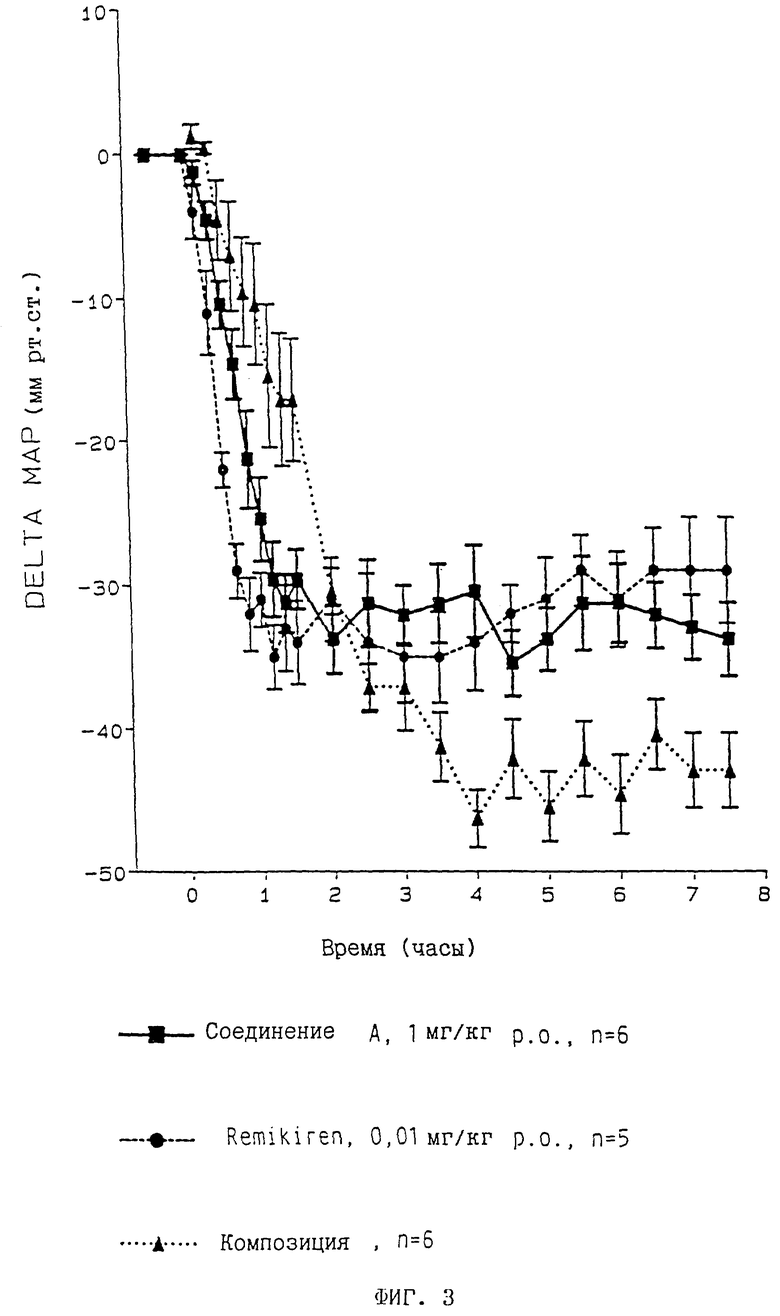
Во второй серии экспериментов исследовали эффективность соединения A в комбинации с ингибитором ренина Remikiren. В этой серии опыты проводились на обезьянах, так как Remikiren обладает специфическим действием именно по отношению к ренину приматов и поэтому не может применяться на крысах. Remikiren представляет собой активный ингибитор ренина, пригодный для орального введения (см. Fischli et al., Hypertension 18, 22-31 (1991)).
Измеряемой величиной являлось артериальное кровяное давление, которое измеряли также телеметрическим путем. Обезьяны вида Saimiri sciureus (саймири-белка или squirrel monkeys) весили от 400 до 700 г. В результате выведения натрия реактивность кровяного давления по отношению к ингибитору RAS повышается. Выведение натрия достигалось подкожной инъекцией 5 мг/кг фуросемида (Lasix®), которую проводили за 66, 42 и 18 часов до начала эксперимента. В ночь перед экспериментом животные не получали никакого корма. Во время опытов обезьяны содержались в изолированном помещении и за ними велось наблюдение с помощью видеокамер, что диктовалось необходимостью избежать колебаний кровяного давления, которые могли быть обусловлены стрессом, вызванным экспериментаторами.
На фиг. 3 представлены результаты этих опытов, причем указаны собственно изменения среднего кровяного давления, составлявшего 100 мм ртутного столба. В результате введения соединения A в дозировке 1 мг/кг перорально (n=6 обезьян) и 0,01 мг/кг Remikiren (n=5 обезьян) кровяное давление снижалось соответственно на примерно 30 мм ртутного столба. Введением композиции достигали заметно большего эффекта. Поскольку требования по охране животных не позволяли содержать обезьян в клетке более 8 часов, не представлялось возможным определить продолжительность действия препаратов.
Сердечная недостаточность.
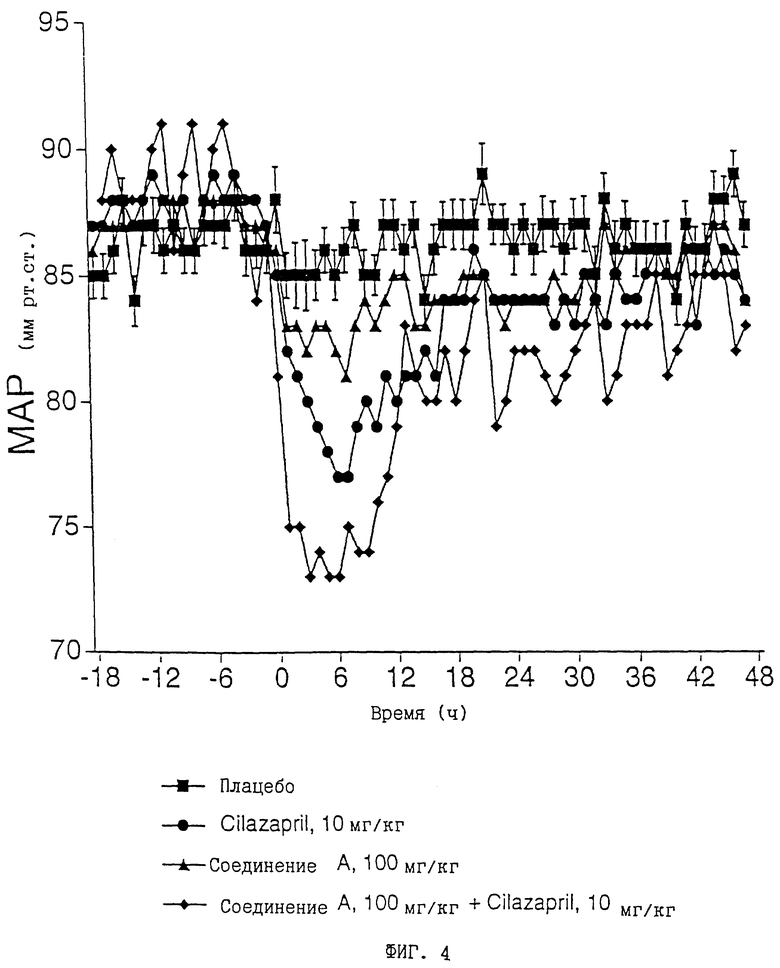
Так как ингибиторы ACE в настоящее время обычно используются в терапии пациентов, страдающих сердечной недостаточностью, соединение A и Cilazapril, вводившиеся раздельно и в сочетании друг с другом, испытывались также на животных на эффективность против сердечной недостаточности.
Эксперименты проводили на крысах, у которых через 8 недель после коронарной лигатуры (A. circumflex) проявились симптомы полной сердечной недостаточности. Артериальное давление измеряли описанным выше телеметрическим путем. Результаты этих опытов представлены на фиг. 4. По соображениям большей наглядности полосы границ погрешности представлены только для кривой плацебо. На этой модели животных также подтвердились более высокая эффективность композиции и увеличение продолжительности ее действия по сравнению с компонентами, вводимыми раздельно.
Экспериментальные данные неожиданным образом свидетельствуют о высоких положительных свойствах предлагаемых согласно изобретению композиций. Эти композиции согласно изобретению вводят преимущественно оральным путем, например в виде таблеток, лаковых таблеток, драже, твердо- и мягкожелатиновых капсул, растворов, эмульсий либо суспензий. Введение может осуществляться также ректально, например в виде суппозиториев, или же парентерально, например в виде инъекционных растворов. Введение биологически активных веществ можно осуществлять в виде препаратов, содержащих оба биологически активных вещества в виде дозиметрических единиц, таких как таблетки или капсулы, или раздельно с использованием композиции в виде тех же дозиметрических единиц, одновременно либо через определенные интервалы времени.
Для изготовления таблеток, лаковых таблеток, драже и твердожелатиновых капсул в композицию согласно изобретению могут добавляться инертные в фармацевтическом отношении, неорганические либо органические эксципиенты.
В качестве таковых могут использоваться, например, для таблеток, драже и твердожелатиновых капсул лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота либо ее соли и т.п. В качестве эксципиентов для мягкожелатиновых капсул пригодны, например, растительные масла, воск, жиры, полутвердые и жидкие полиолы и т.п.; однако в зависимости от специфических свойств биологически активного вещества для мягкожелатиновых капсул вообще не требуется никаких эксципиентов.
Для изготовления растворов и сиропов в качестве эксципиентов пригодны, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.п.
В качестве эксципиентов для инъекционных растворов пригодны, например, вода, спирты, полиолы, глицерин, растительные масла и т.д.
В качестве эксципиентов для суппозиториев пригодны, например, природные или отвержденные масла, воск, жиры, полужидкие или жидкие полиолы и т.п.
Фармацевтические композиции могут содержать, кроме того, еще и консерванты, вещества, способствующие растворимости, стабилизаторы, вещества с высокой поверхностной активностью, эмульгаторы, сладкие вещества, красители, ароматические вещества, соли для изменения осмотического давления, буферы, оболочки или антиокислители. Они могут содержать также и другие ценные в терапевтическом отношении вещества.
Ниже изобретение поясняется на примерах.
Пример 1.
Получение лаковых таблеток, имеющих следующий состав, мг:
Ядро лаковой таблетки:
а. Соединение A - 500,0
б. Cilazapril - 5,0
в. Безводная лактоза - 30,0
г. Микрокристаллическая целлюлоза - 30,0
д. Поливинилпирролидон - 20,0
е. Стеарат магния - 5,0
Вес ядра одной лаковой таблетки - 590,0
Лаковая оболочка:
ж. Гидроксипропилметилцеллюлоза - 3,5
з. Этилцеллюлоза - 3,5
и. Полиэтиленгликоль 6000 - 0,8
к. Окись железа желтая - 1,2
л. Двуокись титана - 0,3
м. Тальк - 0,7
Вес лаковой оболочки - 10,0
Общий вес одной лаковой таблетки - 600,0
Способ изготовления.
Изготовление ядра лаковых таблеток.
Соединение A, Cilazapril, лактозу, целлюлозу и поливинилпирролидон перемешивают и пропускают через сито. Смесь гранулируют во влажном состоянии, сушат и просеивают. Просеянный гранулят перемешивают со стеаратом магния, после чего из пластичной массы прессуют ядра овальной формы весом по 590,0 мг каждое.
Изготовление лаковой оболочки.
Из ингредиентов ж-м приготавливают водную лаковую суспензию и соответствующим образом с помощью способа лакирования в дражировочном котле или в какой-либо другой аппаратуре для лакирования покрывают этой суспензией ядра до получения лаковых таблеток с конечным весом 600 мг каждая.
Пример 2.
Изготовление твердожелатиновых капсул, имеющих следующий состав, мг:
а. Соединение A - 250,0
б. Cilazapril - 2,5
в. Крист. лактоза - 18,0
г. Поливинилпирролидон - 15,0
д. Микрокристаллическая целлюлоза - 17,5
е. Натрий-карбоксиметиловый крахмал - 10,0
ж. Тальк - 9,0
з. Стеарат магния - 3,0
Вес одной капсулы - 325,0
Способ изготовления.
Соединение A, Cilazapril, лактозу, поливинилпирролидон и целлюлозу просеивают через сито и перемешивают. Смесь гранулируют во влажном состоянии и сушат. Гранулят перемешивают с натрий-карбоксиметиловым крахмалом, тальком и стеаратом магния и из полученной смеси изготавливают твердожелатиновые капсулы размером 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИПОТЕНЗИВНОЕ СРЕДСТВО | 1992 |
|
RU2084225C1 |
| СУЛЬФОНАМИДНЫЕ ПРОИЗВОДНЫЕ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1996 |
|
RU2173317C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 1997 |
|
RU2184112C2 |
| СУЛЬФОНАМИДЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2151767C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ | 1998 |
|
RU2222328C2 |
| ПРОИЗВОДНЫЕ СУЛЬФОНИЛПИРРОЛИДИНА | 2001 |
|
RU2272026C2 |
| НОВЫЕ ОБРАТНЫЕ АГОНИСТЫ РЕЦЕПТОРА СВ1 | 2003 |
|
RU2339618C2 |
| СУЛЬФОНАМИДОКАРБОКСАМИДЫ, ИХ ГИДРАТЫ И ФИЗИОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1993 |
|
RU2133739C1 |
| ПРОИЗВОДНЫЕ АРИЛ- И ГЕТЕРОАРИЛСУЛЬФОНАМИДОВ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1995 |
|
RU2163598C2 |
| ЛИГАНДЫ Х-РЕЦЕПТОРА РЕТИНОЕВОЙ КИСЛОТЫ | 1995 |
|
RU2146241C1 |
Изобретение относится к комбинированному препарату. Оно может быть использовано для лечения заболеваний системы кровообращения. Препарат содержит ингибитор системы ренин - ангиотензин - цилазаприл и антагонист эндотелина - 4-трет. бутил-N- [6-(2-гидроксиэтокси)-5-(2-метоксифенокси)- 2,2'-бипиримидин-4-ил] бензолсульфонамид. Их массовое соотношение соответственно 1:1-1: 100. В частности, препарат содержит 2,5-10 мг цилазаприла и 250 -1000 мг антагониста эндотелина. Общая масса двух компонентов в препарате может составлять 550 мг. Совместное введение двух компонентов препарата приводит к синергическому эффекту. Благодаря этому эффективные дозы обоих компонентов могут быть существенно уменьшены. Это снижает побочные эффекты. 2 з.п.ф-лы, 4 ил.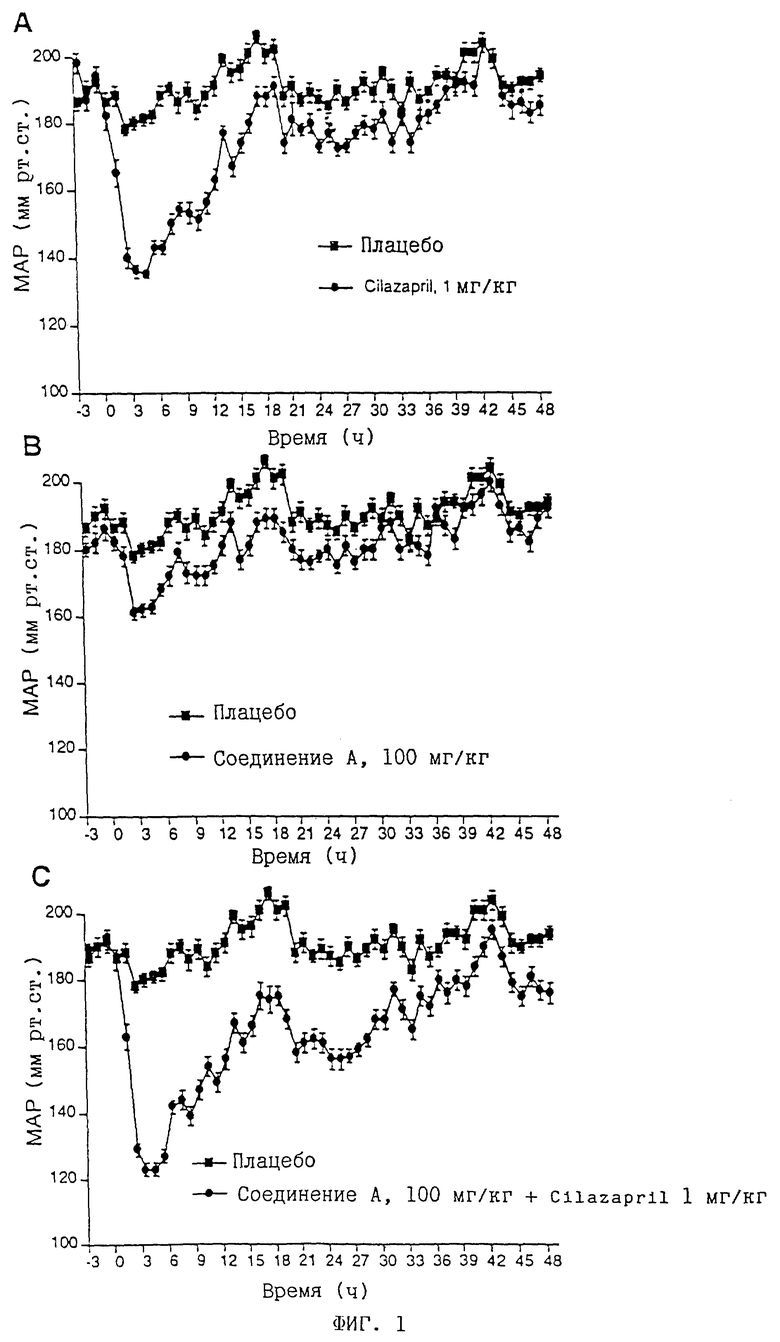
| ОТВЕРТКА | 1996 |
|
RU2117571C1 |
| Релейный реверсивный распределитель | 1973 |
|
SU526708A1 |
| Визуальный количественный спектральный метод анализа мартеновских и доменных шлаков | 1951 |
|
SU94095A1 |
| US 4316906 A, 1982 | |||
| US 3642785 A, 1972 | |||
| ГИПОТЕНЗИВНОЕ СРЕДСТВО | 1992 |
|
RU2084225C1 |
Авторы
Даты
2000-03-20—Публикация
1994-07-14—Подача