Изобретение относится к последовательностям ДНК, расположенным в 3'-5'-направлении, и их использованию для управления экспрессией генов в развивающихся семенах растений и применению последних.
Изучение экспрессии генов растений позволило сделать ряд общих выводов относительно элементов, которые контролируют экспрессию. Растения, как и другие организмы, как прокариоты, так и эукариоты, содержат консервативные или консенсусные последовательности в 5'-направлении от сайта инициации транскрипции гена, который, видимо, способен регулировать скорости транскрипции. В эукариотах эти последовательности включают фрагмент, обычно составляющий 25 п.н., в 5'-направлении от участка инициации транскрипции, который имеет последовательность TATAA/TAA/T, так что его называют TATA-блок.
Роль этого TATA-блока, видимо, заключается в определении начала транскрипции для РНК-полимеразы II. Вторую последовательность в обратном направлении называют CAAT-блок. Он обычно содержит около 75 п.н. в обратном направлении от участка инициации транскрипции и связан с регулированием частоты инициации транскрипции. У растений консенсусные последовательности могут иметь вид CCAAT или иногда AGGA. Однако необязательно любая из этих альтернативных консенсусных последовательностей должна присутствовать во всех генах растений. Указанные фрагменты последовательностей и связанный с ними участок ДНК, содержащий 7-90 нуклеотидов в обратном направлении от участка инициации транскрипции, часто называют промотором. В общем случае в 5'-направлении от участка промотора, а наиболее часто в пределах приблизительно 2000 нуклеотидов от него, располагаются цис-активные элементы, которые варьируют свойства промоторов и способны модулировать транскрипционную активность как конститутивным, так и неконститутивным образом. Указанные цис-активные последовательности можно называть усилителями (если они отвечают за ускорение транскрипции) или глушителями (если они отвечают за подавление транскрипции). Усилители и глушители часто являются сайтами, к которым присоединяются или с которыми взаимодействуют белки ядер. Модулирующие белки ядер называют транс-активными факторами. Они, как считается, являются очень важными для неконститутивных или регулируемых экспрессий, и могут оказаться решающим фактором активности гена в конкретных тканях или органах или же они могут откликаться на внешнее стимулирующее воздействие. Связь между присоединением указанных белков и элементом усилитель/глушитель может определять транскрипционную активность. Выделение генов, которые активируются теплом, светом или действием химических соединений, таких как эндогенные гормоны, или активируются в специфических органах, таких как семена, листья или цветки, позволяет провести анализ факторов, которые помогают выявить, каким образом регулируется экспрессия. Во многих, но не во всех, случаях было показано, что конструирование химерных генов, которые содержат промоторы и необязательно цис-элементы, из данного регулируемого гена и кодирующей последовательности репортерного белка, не связанного, как правило, с указанным промотором, приводит к регулируемой экспрессии репортерного гена. Были предприняты лишь отдельные попытки использовать промоторы из семяспецифичных генов при экспрессии последовательностей генов в семени, которые либо обычно не экспрессируются семяспецифичным образом, либо требуют применения измененной схемы экспрессии. Во всех случаях в химерных генах, разработанных для семяспецифичной экспрессии, используют регуляторные сигналы и промоторы для запасных (storage) белков семян. Однако из работ по экспрессии генов запасных белков стало очевидно, что экспрессия начинается на сравнительно поздней стадии эмбрионального развития, а именно как только эмбрион достигает (для двудольных растений) классической формы жгутика. Таким образом, хотя запасные белки экспрессируются на высоких уровнях и их регулирование часто является транскрипционным, время и уровень экспрессии могут не оказаться идеальными для применений, зависящих от типа семян. По этой причине представляет интерес выявление других семяспецифичных промоторов и усилителей, обладающих временной или клеточной специфичностью, отличной от запасных белков семян, таких как белки олеозинов.
Далее приводятся орган- или тканеспецифичные регуляторные последовательности, которые используют для орган- или тканеспецифичной экспрессии в трансформированных растениях. В настоящее время известно несколько ставших "классическими" примеров регулируемой экспрессии гена белка хлоралефемиколацетилтрансферазы, которая может быть экспрессирована зависимым от света и органспецифичным образом в трансгенных растениях, если кодирующую последовательность репотерного белка сливают с промотором и предшествующей последовательностью гена гороха, кодирующего рибулоза-бифосфаткарбоксилазу (Fluhr., Science, 1986, vol. 232, p. 1106-1112).
Sengupta-Gopalan et al., Proc. Natl. Acad. Sci. USA, 1985, vol. 82, p. 3320-3324, сообщают об экспрессии основного запасного белка французского гороха, называемого бета-фазеолином, в растениях табака. Ген экспрессируется именно в семенах и лишь незначительно в других частях растения. Однако конструкции, которые применили Sengupta-Gopalan et al., не были химерными. Был использован полный ген бета-фазеолина, включающий нативную 5'-фланкирующую последовательность. Последующие эксперименты с другими образцами (Radke et al. , Theor. App. Genet., 1988, vol. 75, p. 685-694) или другими генами (L. Perez-Grau, R. B. Goldberg, Plant Cell, vol. 1, p. 1095-1109) показали, что экспрессия является семяспецифичной как в случае Arabidopsis, так и Brassica; Radke et al. (1988, см. выше) использовали "меченый" ген, т.е. полный ген напина плюс нетранслируемую "метку".
В случае орган- и тканеспецифичной экспрессии можно привести ряд примеров, которые показывают, что последовательности, расположенные в обратном направлении от участка инициации транскрипции, можно использовать для придания орган/тканеспецифичности гену, введенному в растения методами генной инженерии. Примеры включают регулирование методами генной инженерии семяспецифичных генов (Radke et al., 1988, см. выше); Bustos et al., Plant Cell, 1989, vol. 1, p. 839-853). В обоих примерах последовательности в 3'-5'-направлении от кодирующих последовательностей белков семян присоединяют к репортерной метке (либо в виде РНК, либо в виде белка), и семяспецифичность подтверждают экспрессией репортерного гена. Во всех случаях это были гены запасных белков, отличные от олеозина.
Фрагменты ДНК, которые могут приводить к семяспецифичной экспрессии, являются в настоящее время объектом многих исследований. Marcotte et al. (W.R. Marcotte, I.S. Russel, R.S. Quantrano, Plant Cell, 1989, vol. 1, p. 969-976) изучали Em-ген пшеницы и предложили два фрагмента, названные "Em-блоками", которые могут играть роль консенсусных последовательностей для семяспецифичной экспрессии. Интересно отметить, что один из указанных блоков, получивший название EM-2, аналогичен блоку, найденному в других генах однодольных (тритицин из пшеницы) и даже двудольных (бета-конглицинин из сои). Hatzopoulos et al. Plant Cell, 1990, vol. 2, p. 457-467) исследовали последовательности, управляющие эмбрионспецифичной экспрессией гена белка липидных тел моркови. Был выявлен ряд фрагментов, содержащих большое число звеньев AT, которые защищены от расщепления во время обработки ДНКазой преимущественно с помощью транс-активных белков. Однако не было показано, что выделенные фрагменты являются консенсными фрагментами для других семяспецифичных генов.
DeClercq et al., Plant Physiol., 1990, vol. 94, p. 970-979 использовали промотор 2S альбумина растения Arabidopsis и комбинированные кодирующие последовательности 2S альбуминов Arabidopsis и бразильского ореха. Слияние осуществляли по участкам с низкой консервативностью. Трансформации как табака, так и Brassica napus приводят к семяспецифичной экспрессии и точной аккумуляции модифицированных запасных белков. Уровни экспрессии составляли от 0,05 до 0,3% от общего клеточного белка.
Другим примером этой формы семяспецифичной экспрессии чужеродной последовательности является экспрессия лей-энкефалинов в семенах. Для получения семяспецифичной экспрессии химерную последовательность ДНК, кодирующую 2S альбумин, и короткий олигонуклеотид, кодирующий лей-энкефалин (пентапептид), вводят в кодирующую альбумин последовательность между 6-м и 7-м цистеинами нативного белка (Vanderkerhove et al. , Bio/Technology, 1989, vol. 7, p. 929-932). Указанный ген вновь экспрессирует семяспецифичным образом, позволяя накапливать до 50 пмол лей-энкефалина на каждый грамм семян.
Геномные клоны, кодирующие белки масличных тел, со связанными с ними участками, расположенными в обратном направлении, описаны для двух образцов - кукурузы (Zea mays, Bowman-Vance and Huang, J. Biol. Chem., 1987, vol. 262, p. 11275-11279; Qu and Huang, J. Biol. Chem. 1990, vol. 265, p. 2238-2243) и моркови (Hatzopoulos et al., Plant Cell., 1990, vol. 2, p. 357-467). кДНК и геномные клоны также приводятся для одного культивируемого масличного растения Brassica napus (Murphy et al., Biochem. Biophys. Acta, 1991, vol. 1088, p. 86-94; Lee and Huang, Plant Physiol., 1991, vol. 96, p. 1395-1397). Появились и другие сообщения об экспрессии этих генов белков масличных тел в развивающихся семенах. В случае Zea mays транскрипция генов, кодирующих изоформы белков масличных тел, начинается уже на самых ранних стадиях развития семян и легко обнаруживается на 18-й день после опыления. В неэндоспермных семенах, таких как семена двудольного растения Brassica napus (Canol), экспрессия генов белков масличных тел, видимо, начинается на гораздо более поздних, чем у кукурузы, стадиях развития семян (Murphy et al., Biochem. J., 1989, vol. 258, p. 285-293).
Краткое описание изобретения.
Описываются способы и композиции для использования регуляторной последовательности транскрипции белков масличных тел и необязательно соседствующей с ней в 5'-направлении нетранслируемой лидерной последовательности для семяспецифичной экспрессии гетерологичного гена. Способ включает стадии трансформации клетки растения с помощью ДНК-конструкции, включающей регуляторную последовательность и ДНК-последовательность, отличную от нативной открытой рамки считывания, по отношению к регуляторной последовательности, генерацию растения из трансформированной клетки и выращивание его в условиях, при которых возможно образование семян и осуществляется экспрессия последовательности ДНК под транскрипционным контролем регуляторного участка. Указанные последовательности представляют ценность в тех случаях, когда необходимо модифицировать, усилить или подавить экспрессию продукта семени. Они также могут использоваться для получения модифицированных семян, содержащих чужеродные белки, с целью усиления качества семян.
На фиг. 1 приведена схематичная диаграмма вектора pPAW4, включающего регуляторную последовательность олеозина, инициирующий кодон, чужеродную ДНК, которая должна экспрессироваться, терминаторную последовательность олеозина и ген устойчивости к ампициллину.
На фиг. 2A показана последовательность ДНК геномного клона Arabidopsis (посл. ид. N 1), кодирующего 18 кДа белок масличного тела. Открытая рамка считывания прерывается коротким интроном (помечен), а два экзона транслируются и обозначаются однобуквенными символами, принятыми Международным союзом теоретической и прикладной химии (ИЮПАК) для аминокислот.
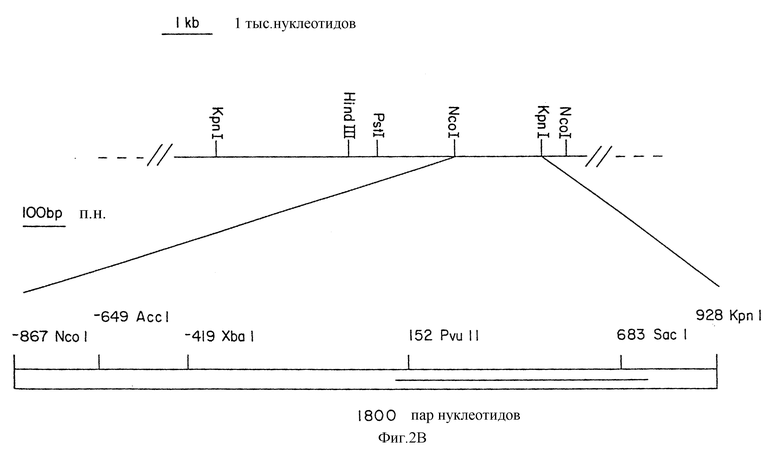
На фиг. 2B приведен рестрикционный фрагмент из геномной библиотеки Agrobacterium EMBL3, который включает кодирующую последовательность 18 кДа белка масличного тела. Выделено приблизительно местоположение кодирующего участка.
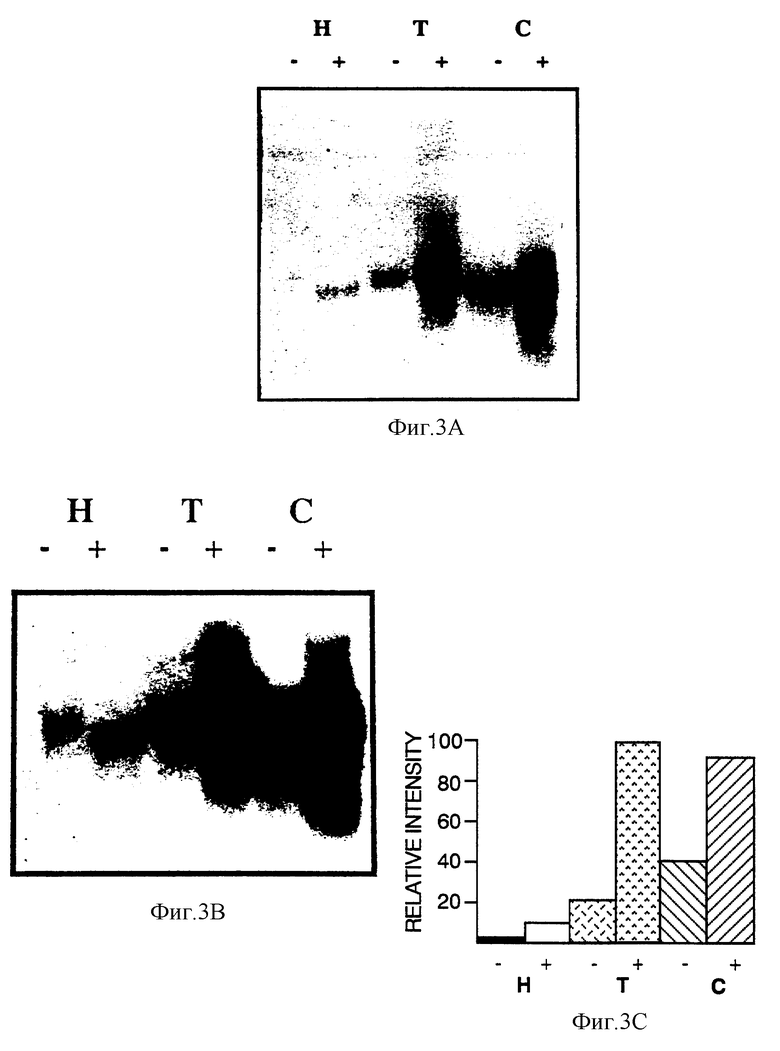
На фиг. 3 показаны воздействия 19 мкМ абсцизовой кислоты (ABA) на эволюционную экспрессию мРНК олеозина методом Нозерн-блот анализа всей РНК. A) (70 мкг на дорожку) с использованием в качестве зонда 50 нг OB990, меченного с помощью 32PgЦТФ (с удельной активностью ДНК 109 распадов в минуту). Зародыши на стадии ядра (H) (13-й день), жгутика (T) (17-й день) и семядоли (C) (21-25-й день), выращенные из микроспор и обработанные (+) и необработанные (-) 10 мкМ абсцизовой кислоты в течение 48 ч. Пятно экспонируют на пленку Kodak XAR5 при 70oC в течение 20 мин. Кажущиеся различия в размере мРНК на разных дорожках вызваны влиянием различного количества крахмала в разных препаратах мРНК. На все дорожки наносят одинаковое количество соединений, что определяют по измерению содержания OD260 и по окрашиванию с помощью бромида этидия. B) Экспонирование фиг. 3A в течение 4,5 ч. C) Относительная интенсивность накопления мРНК, определяемая методом сканирующей денситометрии.
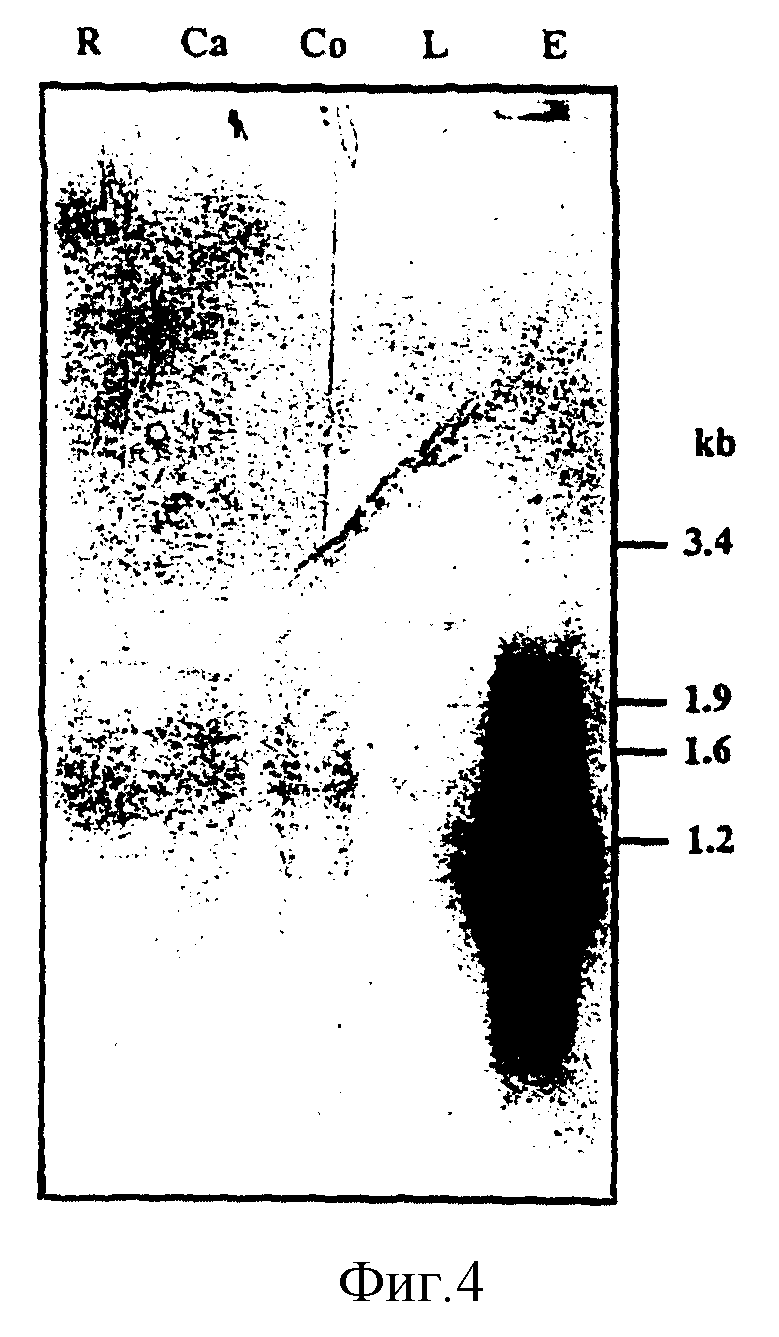
На фиг. 4 показана тканевая специфичность олеозина. 50 мкг поли(A)+РНК из корней (R), каллуса (Ca), семядоль (Co), листьев (L) и зиготных эмбрионов (E) через 24 дня после цветения исследуют действием 50 нг OB990, меченного 32PgЦТФ (с удельной активностью ДНК 108 распадов в минуту).
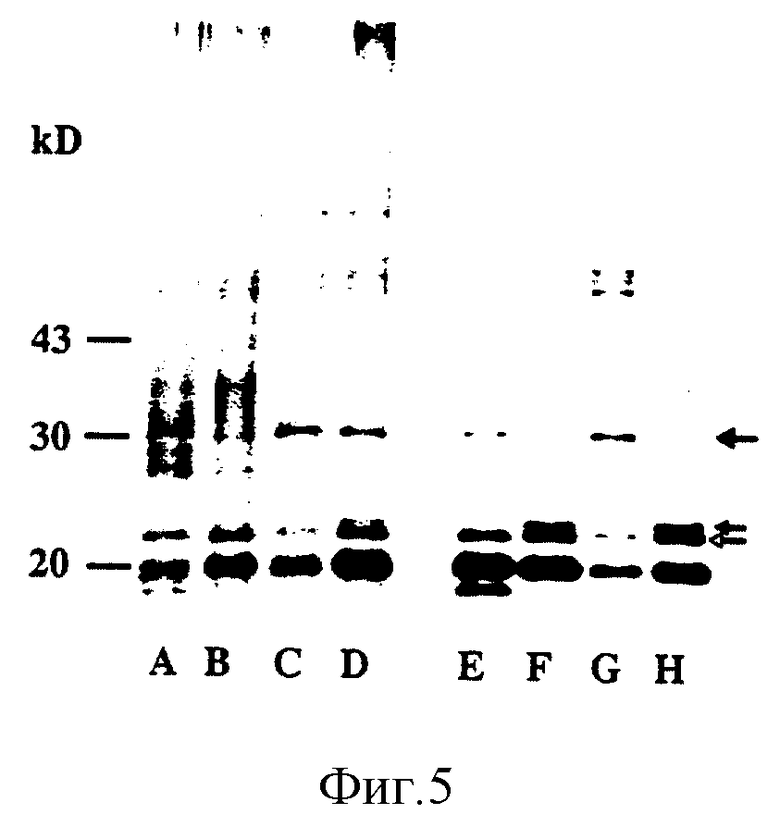
На фиг. 5 показана эволяционная чувствительность синтеза белков масличных тел от применения абсцизовой кислоты. Парные контрольные образцы (дорожки A, C, E, G) и образцы, обработанные с помощью абсцизовой кислоты (дорожки B, D, F, H) помещают в ячейку с приблизительной удельной активностью 10000 распадов в минуту на ячейку. Все образцы обрабатывают в течение двух дней абсцизовой кислотой, а затем помечают в течение 4 ч с помощью [32S]-метионина с активностью 1,85 МБк/мл. Дорожки A и B - 10-дневные культуры, просеянные на сите с размером ячеек 62 мкм, с целью выделения глобулярных эмбрионов. Дорожки C и D - 13-дневные культуры, просеянные на сите с размером ячеек 125 мкм, с целью выделения эмбрионов на стадии образования ядра. Дорожки E и F - 17-дневные культуры, просеянные на сите с размером ячеек 250 мкм, с целью выделения эмбрионов от стадии образования жгутика до стадии образования семядоли. Дорожки G и H - 25-дневные культуры, просеянные на сите с размером ячеек 500 мкм, с целью выделения эмбриона на стадии образования семядоли.
В соответствии с настоящим изобретением заявляются ДНК-конструкции, которые позволяют осуществить модуляцию фенотипа растения в семенах, в частности во время ранних стадий эмбрионального развития. Заявляются ДНК-конструкции для регулирования транскрипции в семенах с использованием нетранслированных последовательностей генов в 5'-направлении, которые активны в течение развития от поздней глобулярной стадии до созревания семян (стадия семядоли). В прямом направлении под участком инициации транскрипции гена белка масличных тел должна располагаться нужная ДНК-последовательность, которая будет получена и которая позволяет интегрировать транскрипционную кассету в геном клетки растения. Таким образом, в прямом направлении от участка инициации семяспецифичной транскрипции может быть включен множественный клонирующий сайт, так что для разнообразных ДНК-последовательностей можно эффективно использовать интеграционную конструкцию.
Особый интерес представляет регуляторная последовательность гена белков масличных тел, преимущественно ген белка масличных тел, экспрессируемый в масличных семенах двудольных растений. Сообщается, что белки масличных тел накапливаются значительно позднее, чем другие масла (триглицериды) или запасные белки. Эта поздняя экспрессия ограничивает ценность любых промоторов, связанных с указанными генами для семяспецифичной экспрессии, поскольку их нельзя использовать для модификации экспрессии генов на ранних стадиях эмбриогенеза. Однако неожиданно было обнаружено, что экспрессия указанных генов в семенах двудольных масличных культур наблюдается значительно ранее, чем считалось до настоящего времени. Таким образом, промоторы и элементы указанных генов, расположенные в обратном направлении, представляют ценность для широкого применения, включая модификацию метаболизма на различных фазах эмбриогенеза, которые предшествуют накоплению запасных белков.
Белки масличных тел идентифицированы у широкого круга таксономически различных видов (см. , например, Moreau et al., Plant Physiol., 1980, vol. 65, p. 1176-1180; Qu et al., Biochem. J., 1986, vol. 235, p. 57-65). Указанные белки локализованы лишь в масличных телах и не обнаруживаются в органеллах тканей овощей. В Braccica napus (рапс) имеются по крайней мере три полипептида, связанныx с масличными телами развивающихся семян (Taylor et al. , 1990, Planta, vol. 181, p. 19-26). Количества и размеры белков, связанных с масличными телами, могут изменяться от образца к образцу. В кукурузе, например, имеются четыре иммунологически различных полипептида, которые встречаются в масличных телах (Bowman-Vance and Huang, J. Biol. Chem., 1988, vol. 263, p. 1476-1481). Было показано, что олеозины включают участки с чередующейся гидрофильностью, гидрофобностью, гидрофильностью (Bowman-Vance and Huang, J. Biol. Chem., 1987, vol. 262, p. 11275-11279). Были получены последовательности аминокислот олеозинов, выделенных из кукурузы, рапса и моркови (cм. соответственно Qu and Huang, J. Biol. Chem., 1990, vol. 265, p. 2238-2243, Hatzopoulos et al., Plant Cell, 1990, vol. 2, p. 457-467). В масличных растениях, таких как рапс, содержание олеозина может составлять от 8% (Taylor et al., Planta., 1990, vol. 181, p. 18-26) до 20% (Murphy et al., Biochem. J., 1989, vol. 258, p. 285-293) от общего количества белка в семенах. Этот уровень сравним с количествами, найденными для других запасных белков.
Особый интерес представляет участок инициации транскрипции, связанный с ранними стадиями эмбриогенеза, в частности с периодом, предшествующим экспрессии запасных белков, так что на ранних стадиях семян он обеспечивает необходимый уровень транскрипции представляющей интерес ДНК-последовательности. Обычный процесс эмбриогенеза растения проходит ряд определенных фаз. Для двудольных семян процесс эмбрионального развития включает следующие фазы: глобулярную фазу, фазу ядра, фазу жгутика и фазу семядоли. В настоящем описании используются определения указанных терминов, взятые из книги Ray, Steves and Fultz, Botany (Saunders College Publishing), глава 17, с. 294. Обычно участок инициации транскрипции можно получить из гена, который экспрессируется на ранних стадиях образования семени. Участок инициации транскрипции предпочтительно сохраняет свою активность от поздней глобулярной стадии вплоть до стадии образования семядоли, а еще более предпочтительно сохраняет активность от глобулярной стадии через стадии образования ядра, жгутика и семядоли процесса эмбрионального развития. Под этим участком инициации транскрипции понимают участок инициации транскрипции, имеющий последовательность нуклеотидов, в значительной степени схожую с последовательностью участка инициации транскрипции гена белка природного масличного тела, который был бы способен обеспечивать транскрипцию на ранних стадиях формирования семени. Эта последовательность может быть природной, синтетической или частично синтетической.
Участок инициации транскрипции белка масличного тела обычно входит в кассету, которая включает в 5'-3'-направлении транскрипции участок инициации транскрипции, представляющую интерес ДНК-последовательность и участок терминации транскрипции, при этом регуляторные участки транскрипции присоединяются операбельно и способны функционировать в клетках растений. Может присутствовать также один или большее количество интронов. После каждой манипуляции ДНК, которая будет использоваться в конечной конструкции, может быть ограничена и операбельно присоединена к другой ДНК, которая будет использоваться в конечной конструкции, где каждая из частичных конструкций может быть клонирована на той же или разных плазмидах. В предпочтительном способе осуществления изобретения кодирующая последовательность с совместимым сайтом рестрикции может быть лигирована в положение, соответствующее кодону 1 гена белка масличного тела. Схематичная диаграмма такого замещения представлена на фиг. 1. Рекомбинантная кодирующая последовательность может быть встроена таким образом, что она полностью замещает кодирующую последовательность гена белка масличного тела и, таким образом, фланкирована на ее 3'-конце терминатором гена белка масличного тела и сигналом полиаденилирования. По другому способу можно осуществить амплификацию с помощью цепной полимеразной реакции (ЦРП) с целью получения ДНК-фрагментов, содержащих участок инициации транскрипции, который удобно соседствует с сайтами рестрикции. Скопированные фрагменты могут быть присоединены к последовательности, кодирующей нужный полипептид путем транскрипционного или трансляционного "слияния", например с целью получения химерного гена, в котором кодирующая последовательность нужного полипептида транскрибируется под контролем участка инициации транскрипции на фрагменте, амплифицированном с помощью ЦРП.
Участок инициации транскрипции может быть нативным или гомологичным по отношению к клетке-хозяину или чужеродным или гетерологичным по отношению к клетке-хозяину. Под чужеродным понимают то, что участок инициации транскрипции не встречается в клетке-хозяине дикого типа, в которую помещают конструкцию, содержащую участок инициации транскрипции. Как правило, регуляторная последовательность включает ДНК размером до 15000 нуклеотидов в 5'-направлении от сайта инициации трансляции гена белка масличного тела. Эту последовательность можно модифицировать в положении, соответствующем первому кодону представляющего интерес белка, путем сайт-направленного мутагенеза (T.A. Kukel, Proc. Natl. Acad. Sci. USA, 1985, vol. 82, p. 488-492) или введения удобного линкерного олигонуклеотида путем лигирования, если рядом с N-концевым кодоном находится подходящий сайт рестрикции.
В некоторых случаях желательно осуществить экспрессию нужной ДНК-последовательности в виде белка слияния, в частности в виде белка слияния с белком масличного тела. Нужную ДНК-последовательность можно ввести по обычной методике в последовательность, кодирующую белок маличного тела (в рамке с последовательностью, кодирующей белок масличного тела), так что транскрипция химерного гена приведет к получению белка слияния. Белок слияния преимущественно содержит кодирующий участок для аминокислот с номерами от 44 до 122 в белке масличного тела Arabidopsis, как показано на фиг. 2A, или эквивалентный участок из белка масличного тела видов, отличных от Arabidopsis, с целью обеспечить транспорт масличного тела тогда, когда это желательно.
Чтобы отделить последовательности, кодирующие белки масличного тела от других видов, можно пойти по крайней мере двумя путями. Первый заключается в использовании клона Arabidopsis, описанного в примерах, в качестве зонда в геномной библиотекe других растительных видов. Этот клон легко гибридизируется с клонами олеозина из близкородственных видов, в частности практически всех крестоцветных растений. Для образцов, которые эволюционно отличны от Arabidopsis, например пасленовых, бобовых и всех однодольных, альтернативный метод заключается в использовании антитела, вырабатываемого против генного продукта клона олеозина, такого как клон Arabidopsis. Это антитело можно применить для скрининга произведенной из семян кДНК - экспрессирующей библиотеки, например используя лямбда gtII; Huynh et al., cDNA Cloning, vol. 1, A Practical Approach (Ed. Grover), 1985, IRL Pres, p. 49-78. Этим путем можно получить клон кДНК олеозина для новых видов, который можно использовать для выделения геномного клона из геномной библиотеки указанных видов стандартными методами гибридизации ДНК.
Представляющие интерес последовательности ДНК могут являться любой открытой рамкой считывания, кодирующей нужный пептид, например фермент, или последовательностью, комплементарной последовательности генома, при этом геномная последовательность может являться одной из открытых рамок считывания интроном, некодирующей лидерной последовательностью или любой другой последовательностью, в которой комплементарная последовательность подавляет транскрипцию, процессинг матричной РНК, например сплайсинг или трансляцию. Представляющая интерес последовательность ДНК может быть синтетической, выделяемой из природного источника или их комбинацией. В зависимости от природы представляющей интерес последовательности ДНК может быть желательно синтезировать последовательность с предпочтительными кодонами растения. Предпочтительные кодоны растения можно определить по кодонам с наибольшей частотой в белках, экспрессированных в наибольшем количестве в конкретных видах растений, представляющих интерес.
Нужная последовательность ДНК может кодировать любое разнообразие рекомбинантных белков. Примеры рекомбинантных белков, которые могут экспрессироваться указанным способом, включают антикоагулянты, такие как гирудин, лимфокины, такие как лимфокины семейства интерлейкинов, пептидные гормоны, такие как гонадотропин-выделяющие гормоны, иммунологические реагенты, такие как одноцепочечные антитела, и множество имеющих промышленное значение ферментов, таких как протеазы, липазы и полиглюкангидролазы.
Используемым участком терминации является в первую очередь наиболее удобный, поскольку участки терминации являются относительно взаимозаменяемыми. Участок терминации может быть нативным по отношению к нужной последовательности ДНК или же может быть получен из другого источника. Удобные участки терминации доступны и включают 3'-конец терминатора гена белка масличного тела и сигнала полиаденилирования того же самого гена, из которого получен 5'-регуляторный участок. По другому способу с тем же успехом можно использовать отличный терминатор и сигнал полиаденилирования, например терминатор гена нопалинсинтетазы Agrobacterium.
Кассета экспрессии может дополнительно включать средства для идентификации трансформированных клеток и/или селекции трансформированных клеток. Например, рекомбинантный ген может быть связан с конститутивно экспрессируемым селективным маркером, таким как ген, придающий свойство биолюминесценции или окрашиваемости трансформированным клеткам.
Нужная последовательность ДНК, фланкированная по ее 5'-концу промотором белка масличного тела и регуляторной последовательностью, и фланкированная терминатором по ее 3'-концу, может быть введена в подходящий вектор трансформации, включая Ti - или бинарную плазмиду Agrobacterium или простую плазмиду для клонирования (в частности, pC19, pBP322) для прямого введения ДНК в клетки растений методами микроинъекции, электропорации, опосредованного полиэтиленгликолем поглощения или баллистического метода. Эти способы хорошо известны специалистам в области трансформации растений (cм., например, Horsch et al., Science, 1985, vol. 227, p. 1229-1231; Newhaus and Spangenberg, Physiol. Plant, 1990, vol, 79, p. 213-217; Sandford et al., Physiol. Plant, 1990, vol. 79, p. 206-209.
Трансформированные растения можно получить из трансформированных клеток, используя стандартные методики выращивания (см., например, Moloney et al., Plant Cell Rep., 1989, vol. 8, p. 238-242), совместимые с методами трансформации.
Кассета экспрессии, которую конструируют как указано ранее, в основном предпочтительно экспрессируется в развивающихся семенах. Поэтому клетки растения, которые трансформировались с помощью подходящего белка слияния, выращивают в виде растения в соответствии с известными способами и дают им возможность сформировать семена (cм., например, McCormick et al., Plant Cell Rep. , 1986, vol. 5, p. 81-84). Можно вырастить два или больше поколений и опылить их тем же трансформированным штаммом или другими штаммами, определяя полученный гибрид, обладающий нужным фенотипическими характеристиками, с тем чтобы убедиться, что изучаемые фенотипические характеристики стабильно сохраняются и наследуются, а затем собирают семена для выделения нужных белков или для использования в качестве посевного материала с новыми фенотипическими свойствами. Затем регенерированные растения культивируют в идентичных условиях с нерекомбинантными растениями в ростовых камерах, парниках или на поле и выявляют семяспецифичную экспрессию рекомбинантного гена на уровне мРНК, а часто на уровне полипептида или белка.
Полипептид/белок может представлять ценность сам по себе, и его можно экстрагировать и, если потребуется, подвергнуть дальнейшей очистке. Иначе полипептид/белок или же саму мРНК можно использовать для введения нового биохимического
фенотипа в развивающиеся семена. Новые фенотипы могут включать такие модификации, как изменение состава белка или состава масел семян, увеличение воспроизводства уже существующих нужных веществ или пептидов и ослабление и даже подавление образования нежелательных генных продуктов с использованием десенсибилизации, рибозимной технологии или совместной супрессии (Izant and Weintraub, Cell, 1984, vol. 36, p. 1007-1015, десенсибилизация; Hazelhoff and Gerlach, Nature, 1988, vol. 334, p. 585-591, рибозимная технология; Napoli et al., Plant Cell, 1990, vol. 2, p. 279-289, совместная супрессия).
Если трансформацию проводят с целью получения новых белков или пептидов семян, для выделения которых необходима экстракция, то ее осуществляют, используя водные растворы, содержащие небольшие количества поверхностно-активных веществ, таких как не приводящие к денатурации количества додецилсульфата натрия, Triton X-100, Tween 20, MEGA-8, или любого другого поверхностно-активного вещества, которое не приводит к необратимой дезактивации нужного белка. Для того чтобы провести экстракцию белка или полипептида сухие семена измельчают вручную или в механическом гомогенизаторе для получения водной суспензии или взвеси. Полученную смесь можно разделить на три фазы (отдельные частицы, растворимая в воде фаза, гидрофобная фаза) путем центрифугирования, например с ускорением 50000 x g. В зависимости от типа продукта его можно затем очистить в составе каждой из указанных фаз и селективно осадить после солюбилизации действием сульфата аммония или очистить с помощью колоночной хроматографии, например используя ионный обмен, гель-фильтрацию или аффинную матрицу.
Хотя идеальным хозяином описываемой здесь регуляторной последовательности могло бы быть растение семейства крестоцветных, можно использовать указанные промоторы для широкого круга образцов растений с относительно высокой степенью консервации олеозина в генах. Главным препятствием на пути использования указанных промоторов являются однодольные и двудольные растения. Для трансформаций, включающих указанную специфическую экспрессию в однодольных, необходимо использовать регуляторную последовательность олеозина однодольных. Для семяспецифичной экспрессии двудольных необходимо использовать регуляторную последовательность олеозина двудольных. Рассматриваемая последовательность может использоваться для широкого круга двудольных растений, в том числе всех членов вида Brassica и крестоцветных в целом. Пасленовые, такие как табак и помидоры, также распознают эту последовательность и демонстрируют корректное регулирование экспрессии в развивающихся семенах.
Можно ожидать, что нужные белки будут экспрессироваться во всех тканях эмбриона, несмотря на то что в различных тканях жилки эмбриона и семядолях можно обнаружить различные клеточные экспрессии. Настоящее изобретение имеет многочисленные применения, которые включают повышение качества семян растений за счет накопления ими измененных полипептидов или новых рекомбинантных полипептидов или путем включения или исключения стадий метаболизма. В наиболее простом варианте его осуществления использование настоящего изобретения может привести к повышению качества белка (например, к повышенной концентрации важных или редких аминокислот), улучшенному качеству жидкости за счет модификации состава жирных кислот или улучшенному составу углеводов или повышению их количества. Примеры включают экспрессию богатых серой белков, таких как белки, содержащиеся в люпинах или бразильских орехах, в семенах, дефицитных по серусодержащим остаткам аминокислот. Аналогично может экспрессироваться жирный ацил кофермент A - фермент семейства трансфераз, способный модифицировать относительные содержания жирных кислот в триглицеридах (запасных липидах). Если рекомбинантному белку позволяют накапливаться в семенах, белок также может представлять собой пептид, имеющий ценность для фармацевтического и технического применения или для использования в пище. В этом случае пептид можно экстрагировать из семян и использовать в сырой или очищенной форме в зависимости от предполагаемого применения. Пептид может быть действительно чужеродным пептидом растительному миру, например животным гормоном, ферментом, лимфокином, антикоагулянтом и т.п., который способен экспрессироваться в семенах. Гетерологичные белки затем можно экстрагировать из семян и после частичной или полной очистки использовать в исследовательских целях, в пищевой или фармацевтической промышленности.
Следующие примеры приводятся для иллюстрации, но не ограничивают настоящее изобретение.
Пример 1
Ген белка масличного тела из Arabidopsis изолируют для получения вставки размером 15 тыс. нуклеотидов, присутствующей в клоне из геномной библиотеки Arabidopsis thaliana v. Columbia в фаге EMBL3A путем гибридизации с клоном олеозина B. napus. Фрагмент, имеющий 1800 нуклеотидов и содержащий приблизительно 868 пар нуклеотидов в 3'-5'-направлении от участка инициации трансляции, субклонируют в плазмидном векторе. Ген олеозина Arabidopsis размером 18 кДа удобно клонировать в виде фрагмента величиной 1803 п.н., фланкированного сайтами NcoI и KpnI в векторе, называемом pPAW4 (см. фиг. 1). Для превращения фрагмента в кассету экспрессии с целью использования для широкого круга чужеродных/альтернативных генов необходимо осуществить две модификации. Вначале, применяя методику сайт-специфичного мутагенеза (Kunkel, см. ранее), вводят мутации в положениях -2, -1 и +4 с использованием неправильно спаренных олигонуклеотидов. Требуемые мутации заключаются в замене A на T (-2), A на C (-1) и G на A (+4). Результатом указанных мутаций является образование сайта BspHI в положении от -2 до +4. Сайт BspHI (T/CATGA) включает кодон инициации ATG и образует рецессированный конец, совместимый с NcoI. Вторая модификация включает расщепление с помощью EcoRV и MscI, в результате которого выделяется фрагмент размером 658 п.н., содержащий большую часть кодирующей последовательности нативного олеозина. После указанной операции остаются тупые края на сайтах разрыва, которые при отделении вектора и вспомогательной последовательности из фрагмента EcoRv-MscI обеспечивают рециркуляцию комбинации вектор-промотор-терминатор. Эту рециркуляцию осуществляют в присутствии олигонуклеотидного линкера, содержащего сайт рестрикции, который отсутствует в оригинальном фрагменте размером 1803 тыс. нуклеотидов.
В процессе рециркуляции получают плазмиду, содержащую все предшествующие последовательности гена олеозина, сайт инициации транскрипции и инициирующий кодон, встроенный в сайт BspHI. Его фрагмент в прямом направлении, содержащий 31 основание, представляет собой короткий полилинкер, содержащий одно или несколько уникальных сайтов рестрикции. Для введения какой-либо последовательности ДНК в эту кассету чужеродная последовательность должна иметь или должна быть соответствующим образом модифицирована, чтобы содержать сайт BspHI или McoI в исходной ATG позиции. Если последовательность будет экспрессироваться в виде белка, это обеспечивает сохранение расстояния между "сар"-сайтом и инициирующим кодоном.
Последовательность ДНК, которую необходимо ввести, должна заканчиваться когезивным концом сайта рестрикции, который отсутствует в плазмиде. Этот сайт следует учитывать при выборе полилинкера, который вводят в кассету экспрессии. Расщепление плазмиды с помощью BspHI и подходящего фермента рестрикции для 3'-конца чужеродной последовательности обеспечивает направленное клонирование нужного фрагмента ДНК. Используя подходящие условия лигирования, выдерживают совместно кассету экспрессии плазмиды с BspHI и сайт, совместимый с нужным фрагментом ДНК, и получают лигированный продукт, как это показано на фиг. 1.
Законченную конструкцию из NcoI-KpnI затем отсекают и вводят в подходящий вектор трансформации растения, такой как плазмида Agrobacterium. Для введения конструкции в обычные плазмиды Agrobacterium, такие как Bin 19 (Bevan, Nucl. Acid Reseach, 1984, vol. 12, p. 8711-8721) может потребоваться использование дополнительного сайта рестрикции в плазмиде pPAW4. По одной из методик плазмиду можно разрезать с помощью SmaI и KpnI. Полученный очищенный фрагмент лигируют к KpnI олигонуклеотидному и расщепляют с помощью KpnI. В результате получают ненаправленный KpnI фрагмент для введения в Bin 19. Иным способом конструкцию можно вырезать с помощью KpnI и BamHI и лигировать непосредственно в pBin19, предварительно разрезанную теми же самыми ферментами рестрикции. Полученную бинарную плазмиду Agrobacterium мобилизуют в штамм Agrobacterium путем трехстороннего спаривания (Ditta et al., PNAS, 1980, vol. 77, p. 7347-7351) или ДНК-трансформацией компетентных Agrobacterium (An, Plant Mol. Biology Manual, 1988, vol. A3, p. 1-19, Kluwer Academic, Dordrecht, Netherlands).
Agrobacterium, которая несет рекомбинантную Bin 19, используют для трансформации любого способного воспринимать изменения растения, в частности Brassica sp., путем стандартного культивирования вне растения (Horsch et al. , см. ранее). Трансформированные клетки подвергают селекции в культуре с помощью канамицина, используя введенный совместно ген устойчивости (неомицин фосфотрансфераза), который также содержится между границами Т-ДНК pBin. Указанные трансформированные клетки вносят для выращивания целого растения, используя стандартные процедуры (в частности, масличного растения, такого как рапс, см. Moloney et al., Plant Cell Rep., 1989, vol. 8, p. 238-242). Регенерированным растениям дают зацвести и подвергают самоопылению (или перекрестному опылению). В тех случаях, когда чужеродная ДНК в конструкции кодирует способный транслироваться продукт, его можно выделить из водных экстрактов созревших семян с последующим фракционированием суспензии на центрифуге (30 мин с ускорением 100000 x g). В зависимости от желаемого продукта он может распределиться в одной из трех полученных фаз. Он может находиться в таблетке, растворимой в воде фазе и липидной пленке на поверхности подвергнутого центрифугированию образца.
Если целью экспрессии является изменение метаболизма в семени и изменение таким образом фенотипа семян (в частности, путем изменения размера или цвета семян, изменения соотношения между остатками жирных кислот в семенах или запрещения определенной стадии метаболизма, которая, как считается, приводит к менее ценным семенам), экстракцию продукта проводить необязательно. Указанные стадии обмена веществ могут включать производство не пригодных для употребления в пищу вторичных продуктов, присутствие которых снижает ценность семян или являeтся нежелательным. В таких случаях семена просто собирают и используют в соответствии с принятой практикой.
Пример 2
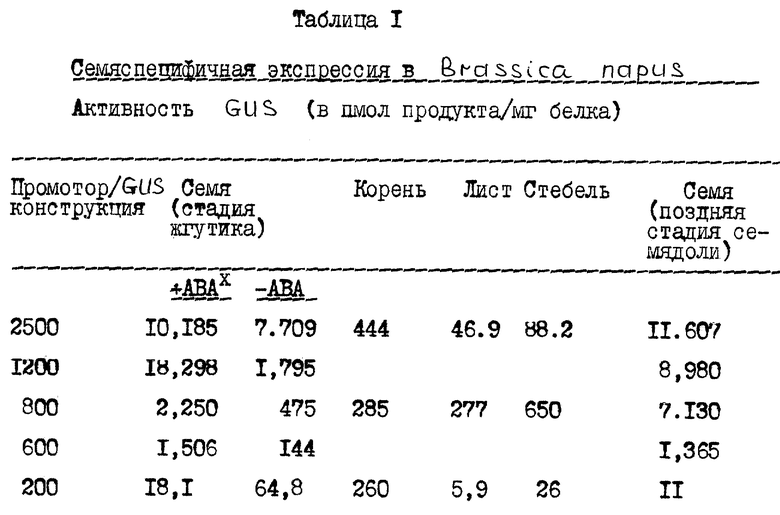
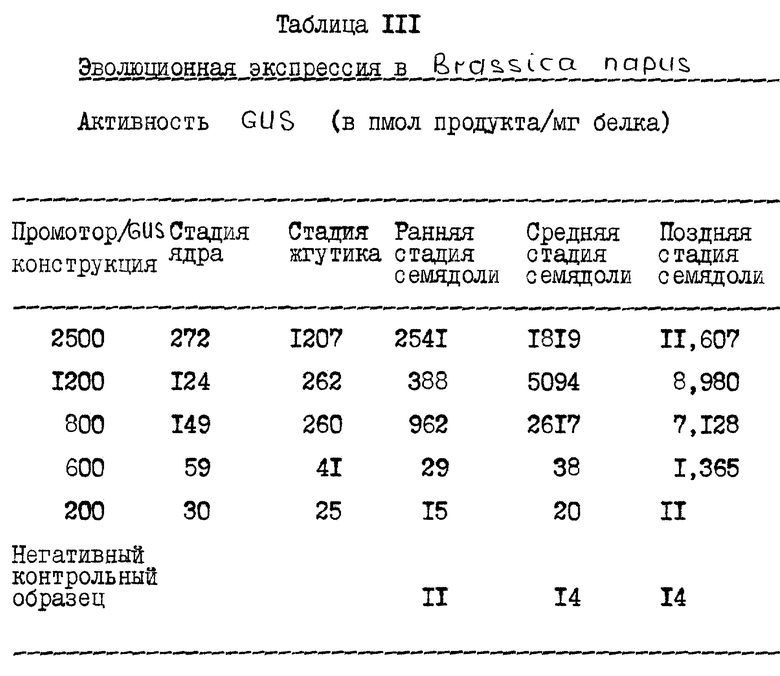
Методом ПЦР получают ряд конструкций, содержащих различные количества последовательностей ДНК в 3'-5'-направлении от участка инициации траскрипции гена олеозина Arabidopsis, операбельно присоединенных к кодирующему участку бета-глюкуронидазы (GUS). Конструкции обозначают в соответствии с величиной 5'-участка олеозина, так, например, конструкция 2500 содержит приблизительно 2500 п.н. 5'-участка олеозина. Конструкции вводят в Brassica napus и табак и оценивают экспрессию гена бета-глюкуронидазы, как это подробно описано далее. Результаты экспрессии GUS пяти конструкций - конструкции 2500, 1200, 800, 600 и 200 - в трансформированных растениях Brassica napus представлены в таблице I. Приведены также данные для негативного контрольного образца (нетрансформированного растения). Результаты экспрессии GUS двух конструкций - конструкции 2500 и конструкции 800 - в трансформированных растениях табака представлены в таблице II. В таблице III приведены данные о развитии экспрессии промотора олеозина в трансгенных эмбрионах.
Конструкции получают, используя стандартные методики молекулярной биологии, включая расщепление ферментом рeстрикции, лигирование и полимеразную цепную реакцию (ПЦР). Для пояснения использованной методики подробно описывается конструкция 800.
Для получения фрагмента ДНК, содержащего приблизительно 800 п.н. в 5'-направлении от участка инициации транскрипции гена олеозина Arabidopsis с конфигурацией, удобной для связывания с кодирующей последовательностью GUS, используют методику, основанную на ПЦР. Она включает применение полимеразной цепной реакции для амплификации точных последовательностей, которые необходимы для анализа экспрессии. Для проведения необходимой ПЦР амплификации синтезируют два олигонуклеотидных праймера (Milligen-Biosearch. Cyclon DNA synthetizer), содержащих следующие последовательности:
PstI последовательность олеозина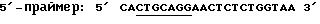
(GVR 10) (посл. ид. N 2)
Основания, помеченные шрифтом "италик", соответствуют нуклеотидам в позициях от -833 до -817 в последовательности, приведенной на фиг. 2A. Дополнительные нуклеотиды в 5'-направлении этой последовательности не идентичны в праймере гену олеозина, однако их включают с целью размещения сайта PstI у 5'-конца продукта амплификации. Сайт PstI не выделен.
Синтезируют второй (3') праймер, который имеет следующую последовательность:
3' праймер (APL I) последовательность олеозина
последовательность олеозина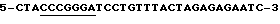 (посл. ид. N 3)
(посл. ид. N 3)
Smal
Этот праймер содержит точный комплемент (выделен шрифтом "италик") последовательности, приведенной на фиг. 2A от оснований -13 до -30. Далее он включает еще 13 оснований у 5'-конца. Указанная последовательность не является комплементарной гену олеозина, однако введена для получения двух (перекрывающихся) сайтов рестрикции, Smal и BamHI, у 3'-конца продукта амплификации с целью облегчения клонирования ПЦР фрагмента.
Эти два праймера используют в ПЦР реакции амплификации для получения фрагмента ДНК, содержащего последовательность между нуклеотидами -833 и -13 гена олеозина с сайтом Pstl на 5'-конце и сайтами Smal и BamHI на 3'-конце. Амплификацию с помощью ПЦР осуществляют, используя фермент Taq-полимеразу (Perkin-Elmer-Cetus) в условиях, рекомендованных производителем фермента по следующей температурной программе: 92oC (денатурация) 1 мин, 55oC (восстановление двойной спирали) 1 мин и 72oC (элонгация) 1 мин. В качестве матрицы используют геномный клон олеозина, приведенный в верхней части фиг. 2B, который в оригинальной библиотеке веществ, выделенных из природного сырья, содержал приблизительно 15000 нуклеотидов ДНК из Arabidopsis.
Продукт амплификации (OLEO p800) очищают в геле 0,7% агарозы, выделяют, используя метод стеклянных шариков (Vogelstein and Gillespie, Preparative and analytical purification of DNA from agarose-Proc. Natl. Acad. Sci. USA, 1979, vol. 76, p. 615-619), и расщепляют Pstl. Продукт расщепления очищают на геле и дополняют конец, используя фрагмент Кленова ДНК-полимеразы, а затем разрезают Smal, получая фрагмент с тупым краем. Его клонируют на Smal сайте pUC19 и получают плазмиду pUC OLEOp800. Применяя асимметричное положение сайта AccI во вставке (в положении, соответствующем -649 гена олеозина, приведенного на фиг. 2B), можно селектировать обе ориентации вставки в векторе pUC. Клон, имеющий вставку, ориентированную таким образом, что крайний 5'-конец амплифицированного фрагмента (в направлении транскрипции) расположен ближе к единственному сайту Hind III в векторе клонирования puC19, а крайний 3'-конец амплифицированного фрагмента расположен ближе к единственному сайту EcoRI в векторе pUC19.
Полученную плазмиду затем разрезают с помощью BamHI и выделяют фрагмент OLEOp800, фланкированный сайтами BamHI. Указанный фрагмент, BamHI-OLEOp800, клонируют в сайты BamHI расщепленной с помощью BamHI плазмиды, которую обозначают HspGUS 1559. HspGUS 1559 является плазмидой, которая используется в качестве бинарного вектора в Agrobacterium и образуется из вектора pCGN 1559 (MacBride and Summerfeldt, Plant Molecular Biology, 1990, N 14, p. 269-276) путем введения вставки, содержащей промотор генов теплового шока (фланкированный сайтами BamHI), открытую рамку считывания бета-глюкуронидазы и терминатор нопалинсинтетазы (получаемый из pBI221, R.A.Jefferson, в книге "Cloning' Vetors" 1988, Eds. P.Pouwels, B.E.Enger-Valk, W.J.Brammer, Elsevier Science Pub BV, Amsterdam section VIC, Aill). Расщепление HspGUS 1559 с помощью BamHI приводит к высвобождению промотора генов теплового шока и позволяет осуществить инсерцию любого другого фрагмента BamHI. В это место лигируют фрагмент BamHI-OLEOp800 и получают Agrobacterium pOLEOp800 GUS 1559. Указанную плазмиду используют для трансформации E.coli, и амплифицированную плазмиду вводят в Agrobacterium (штамм EHA101) методом электропорации, как описано ранее (Rogers et al., Plant Molecular Biology Manual, 1988, vol. A2, p. 1-12, Eds. S.Gelvin and R.Schilperoort, Kluwer Academic, Dordrecht, Netherlands).
Полученный штамм Agrobacterium (EHA 101 x pOLEOp800 GUS 1559) используют для трансформации растений Brassica napus по методу Молони и др. (M.M.Moloney, J. M.Walker, K.K.Sharma, Plant Cell Reports, 1989, vol. 8, p. 238-242) или растений табака по методу Хорша и др. (Horsch et al., Science, 1985, vol. 227, p. 1299-1302). Образовавшимся трансгенным растениям дают возможность образовать семена и проводят анализ экспрессии GUS (R.A.Jefferson, Plant Mol. Biol. Rep. , 1987, N 5, p. 387-405) в развивающихся семенах, а также непродуктивных частях растений, используемых в качестве контрольных образцов. Приведенные величины экспрессии являются средними значениями, которые получают в среднем из пяти семян от каждого из приблизительно пяти различных трансгенных растений.
Другие конструкции получают аналогичным методом ПЦР, указанным ранее, используя подходящие праймеры для амплификации -2500 фрагменты, -1200 фрагмента, -600 фрагмента или -200 фрагмента. Результаты для Brassica napus, выраженные в виде удельной активности фермента GUS, представлены в таблице I. Данные для табака приведены в таблице II.
Полученные результаты показывают, что олеозиновый фрагмент от -833 до -813, который используют в конструкции 800, содержит достаточно информации для прямой семяспецифичной экспрессии репортерного гена в трансгенном эмбрионе Brassica napus, начиная уже со стадии ядра, а промотор олеозина Arabidopsis способен направлять транскрипцию в растениях, отличных от Arabidopsis. Эти эксперименты также показывают, что последовательности, содержащиеся в конструкции промотора, содержат цис-элементы, необходимые для усиления транскрипции в ответ на добавление абсцизовой кислоты, что является характерным для промотора нативного олеозина.
Следует отметить, что семяспецифичная экспрессия, которая продемонстрирована в настоящем описании, не зависит от взаимодействий с нативными терминаторами у 3'-конца гена олеозина. В данном примере 3'-концевой терминатор олеозина заменен терминатором, выделенным из гена нопалинсинтетазы Agrobacterium. Таким образом, конструкция 800 достаточна для осуществления необходимого профиля экспрессии независимо от вспомогательных последовательностей.
Все публикации и патентные заявки, на которые даются ссылки в настоящем описании, приведены здесь для справки в той мере, в какой каждая индивидуальная публикация или патентная заявка была специально и индивидуально указана в качестве ссылки.
После того как изобретение полностью описано, для специалиста становится очевидным, что в него могут быть внесены многие изменения и модификации, которые не приводят к изменению сущности и изобретения, и объема притязаний, изложенного в прилагаемой формуле изобретения.
Описание последовательностей
(2) Информация для последовательности с номером идентификации: 1
(i) Характеристики последовательности:
(A) Длина: 1803
(B) Тип: нуклеиновая кислота
(C) Вид цепи: двойная
(D) Топология: линейная
(xi) Описание последовательности:
последовательность с номером идентификации 1 (см. в конце описания).
(2) Информация для последовательности с номером идентификации: 2
(i) Характеристики последовательности:
(A) Длина: 22
(B) Тип: нуклеиновая кислота
(C) Вид цепи: двойная
(D) Топология: линейная
(xi) Описание последовательности:
последовательность с номером идентификации 2:
CACTGCAGGA ACTCTCTGGT AA 22
(2) Информация для последовательности с номером идентификации: 3
(i) Характеристики последовательности:
(A) Длина: 31
(B) Тип: нуклеиновая кислота
(C) Вид цепи: двойная
(D) Топология: линейная
(xi) Описание последовательности:
последовательность с номером идентификации 3:
CTACCCGGGA TCCTGTTTAC TAGAGAGAAT C 31





Изобретение может быть использовано при селекции растений. Изолированный из гена белка масличного тела Brassica napus или Arabidopsis регуляторный участок транскрипции применен в качестве регулятора экспрессии гетерологичного гена в семенах. Экспрессия содержащих этот регуляторный участок конструкции ДНК и кассеты экспрессии в растении обеспечивает продукцию в его семенах желаемых запасных белков. 5 с. и 12 з.п. ф-лы, 3 табл., 5 ил.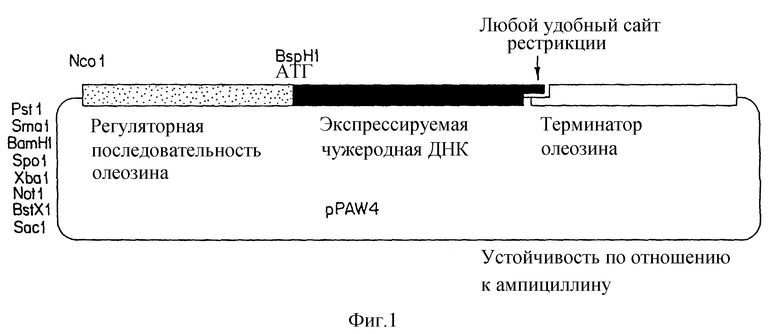
| Огнетушитель | 0 |
|
SU91A1 |
| БИОХИМИЯ РАСТЕНИЙ | |||
| Пер | |||
| с англ | |||
| - М.: Мир, 1968, с | |||
| Телефонная трансляция | 1922 |
|
SU465A1 |
Авторы
Даты
2000-05-10—Публикация
1993-04-02—Подача