Изобретение относится к приготовлению представляющих интерес ферментов в семенах трансгенных растений и применению подготовленных таким образом семян и производственных процессах при отсутствии необходимости экстракции или изоляции фермента.
Ферменты применяются в технологических процессах многих отраслей промышленности. Сюда входят изготовление поверхностно-активных веществ, тканей, молочных продуктов, еды и напитков, кормов, а также другие отрасли промышленности.
В настоящее время ферменты в промышленном масштабе приготавливаются посредством процессов ферментации или изолируются от растительных или животных источников. Ферменты, приготавливаемые с помощью бактерий, включают протеазы, амилазы, пектиназы, фитазы и др. Приготовление ферментов посредством процесса ферментации высокоэффективно, уровни производства могут достигать 10 г на 1 л культуральной среды.
Возможность применения трансгенных растений в качестве ценных белков уже предлагалась ранее. Примерами этого могут послужить приготовление интерферона в табаке (Goodman и др. , 1987), приготовление инкефалинов в табаке, "Brassica napus" и "Arabidopsis thaliana" (Vandekerckhove и др., 1989), приготовление антител в табаке (Hiatt и др., 1990) и приготовление сывороточного альбумина для человека в табаке и картофеле (Sijmons и др., 1990).
На практике, преобразование нарастающего количества видов растений, особенно - видов двудольных растений (например, табака, картофеля, помидоров, "Petunia", "Brassica") стало обычным делом для квалифицированных в данной области специалистов (Klee и др., 1987; Gasser и Fraley, 1989). Стратегии экспрессии инородных генов в растениях разработаны достаточно хорошо (Gasser и Fraley, 1989). Регулярные последовательности их генов растений идентифицировались по их применению в конструкции химерных генов, которые могут быть функционально выражены в растениях и растительных клетках.
Для введения генных структур в растения имеются различные технологии, например - преобразование с новообразованиями агробактерий или с ризогенами агробактерий. С помощью такой стратегии было использовано в рассматриваемых целях обширное множество тканей растений, причем выбор в значительной степени определялся видами растений и их податливостью в культуре клеток ткани. Удачными примерами являются преобразование протопластов, микроспор или пыльцы и таких эксплантатов, как листовые, стеблевые, корневые, гиподольные и дольные. Более того, применяется непосредственное введение ДНК в протопласты и растительные клетки или ткани - микроинжекция, электропорация, бомбардировка частицами и непосредственное поглощение ДНК (Gasser и Fraley, 1989).
Белки можно приготавливать в семенах растений с помощью множества систем экспрессии. К примеру, использование такого составного промотора, как промотор 35S вируса мозаики цветной капусты (CaMV) (Guilley и др., 1982) скажется в накоплении экспрессированного белка в семенах внутри трансгенного растения. И наоборот, можно применять промоторы из генов, кодируя запасные белки семян. Запасные белки семян экспрессируются способом задания весьма специфичных тканей и весьма специфичных стадий процесса (Higgins, 1984; Shotwell и Larkins, 1989), т.е. гены экспрессируются только в семенах и только на стадии развития семян.
Запасной белок семян (рассматривавшийся в работах Higgins, 1984, Shotwel и Larkins, 1989) определяется как любой белок, накапливающийся в значительных количествах (от 90% общего количества белка семян) в развивающихся семенах и гидролизующийся при прорастании, чтобы обеспечить питательную среду на ранних стадиях роста ростков. Белки помещаются во внутриклеточном участке между двумя перегородками, называемом телом белка или вакуолью запасной. Это тело белка содержит ингибиторы протеазы и создает свободную от протеазы окружающую среду. Протеазы, которые разлагают запасные белки семян, становятся активными через (3-6) дней после прорастания (Larkins, 1981).
Были изолированы и характеризованы многие гены в запасных белках семян, а также области их 5'- и 3'- экспозиции (рассмотрены Casey и Domoney, 1987). Примерами глобулинов и альбуминов являются гены глицинина и конглицинина сои культурной (Ficher и Goldberg, 1982; Harada и др., 1989), гены легумина и винилина из гороха (Lycett и др., 1984); Higgins и др., 1988), ген фасоли полевой 11S (Baumlein и др., 1986), ген фазолина 7S из "Phaseolus" (Doyle и др. , 1986), гены круциферина и напина из "Brassica" (Ryan и др., 1989; Scofield и Crough, 1987; Radke и др., 1988), ген гелиантина из подсолнуха (Vonder Haar и др., 1988; Jordano и др., 1989) и гены альбумина 2S и круциферина из "Arabidopsis thaliana" (Vandekerckhove и др., 1989; Pang и др., 1988). Другие примеры можно обнаружить среди генов, кодирующих проламины и глютерины (Casey и Domoney, 1987). Вообще говоря, запасные белки кодируются многогенными семействами.
Гены запасного белка семян передавались семенам табака, петунии и рапса (Okamura и др., 1986; Beachy и др., 1984; Sengupta-Gopalan и др., 1985; Higgins и др. , 1988; Ellis и др., 1988; Barker и др., 1988; Vandekerckhove и др. , 1989; Altenbach и др., 1989). Последовательная восходящая область 5'-бета фазолина из гороха применялась для непосредственной экспрессии бета-глюкуронидазы (Bustos и др., 1989), фитогемаглютинина (Voelker и др., 1989), люциферазы (Riggs и др. , 1989) и зеина (Hoffman и др., 1987) в табаке. Промотор гена альбумина 2S "Arabidopsis thaliana" применили для непосредственной экспрессии модифицированного альбумина 2S тех же самых видов табака, "Brassica napus" и "Arabidopsis thaliana" (Vandekerckhove и др., (1989). Упомянутые выше гены были экспрессированы способом задания весьма специфичных тканей и последовательного проведения, т.е. - в семенах во время развития семян. Во всех рассмотренных работах уровни экспрессии варьировались, но достигнутые уровни соответствовали 1,7% общего содержания белков в семенах (Voelker и др. , 1989). Было обнаружено, что комплементарная ДНК (кДНК) может заменять геномную ДНК, содержащую интроны как базис получения функционирующей и стабильной матричной РНК (мРНК) при гетерологичной экспрессии (Chee и др. , 1986). Эти результаты демонстрируют, что специалист, квалифицированный в области молекулярной биологии тканей, может разработать стратегии создания специфической экспрессии в семенах требуемого гена заданных видов растений, которые поддаются технологии преобразования.
Во время развития семян двудольных растений, значительная часть общего количества синтезированного белка направлена в вакуоли или в белковые тела клеток запасной паренхимы. Чтобы управлять этим процессом, белки, вообще говоря, синтезируются как предшественники. Белки-предшественники снабжаются гидрофобными сигнальными пептидами, обычно - с амино-концами (N-концами), которые дробятся на заданных этапах процесса. Значительное количество сигнальных пептидов запасного белка уже описано (Doyle и др., 1986; Pang и др., 1988; Vonder Haar и др., 1988; Iturriaga и др., 1989; Dorel и др., 1989; Voelker и др., 1989; Hattori и др., 1985; Lycett и др., 1983; Smith и Raikhel, 1989).
Вообще, кажется, что применимость сигнальных пептидов в системах гетерологичной экспрессии (например, Sijmons и др., 1990; Vitale и Bollini, 1986; Slightom и др., 1986; Della-Cioppa и др., 1987) подтверждает идею, что слияние сигнального пептида с гетерологичным "пассажирским белком" может быть применена для переноса и обработки пассажирского белка. Труды различных авторов подтверждают, что множество потенциальных "пассажирских белков" являются кандидатами в такую систему экспрессии.
Тем не менее, несмотря на притягивательность и значимость применения растений как биореакторов, системы рассматриваемого типа не избавлены от трудностей. В описанных выше примерах растение используется как биореактор, а представляющий интерес белок после этого изолируется от материала трансгенного растения, т. е. - от тканей, содержащих наиболее высокие уровни представляющего интерес белка. Изоляция белка, представляющего интерес, из семян, в которых он приготавливается, прямо приводит к таким осложнениям, как дополнительные затраты (Krebbers и Vandekerckhove, 1990).
Возможным решением этой проблемы может быть исключение необходимости экстракции экспрессированного белка из материала растения. В патенте ГДР N DD 275704 раскрывается сущность конструкции для экспрессии термоустойчивой бета-глюканазы в непроросших семенах преобразованных ячменных растений и применения этих семян в процессах сбраживания. Тем не менее, остававшаяся проблема обработки посевов злаков с малыми зернами состояла не только в преобразовании протопластов хлебных злаков, но и в регенерации преобразованных растений, что не раскрывается в описании указанного патента. Таким образом, с помощью процесса, описанного в рассмотренном патенте, нельзя получить ферментосодержащие семена.
Согласно данному изобретению обеспечиваются семена, содержащие по крайней мере один представляющий интерес фермент, которые могут быть использованы в промышленных процессах или в производстве еды или кормов в качестве катализаторов реакций пищеварения при отсутствии необходимости первичной экстракции и/или изоляции ферментов.
Обеспечиваются конструкции ДНК для преобразования растений, которые в свою очередь способны к экспрессии множества представляющих интерес ферментов в семенах. В указанных конструкциях применяются сигнальные последовательности, оперативно соединенные с последовательностью ДНК и кодирующие желаемый для экспрессии фермент. Такие конструкции управляются регулярными последовательностями, которые способны направлять экспрессию ферментов в семенах.
Данное изобретение предназначено также для обеспечения применения семян трансгенных растений в качестве стабильной и управляемой формы запасов ферментов. Ферменты поддерживаются в осушенной среде с низкой активностью протеазы и, таким образом, защищены от разложения.
Кроме того, применение семян для хранения ферментов обеспечивает устойчивое средство транспортирования, которое легко пакуется и перевозится, а также легко обрабатывается в ходе применения.
Кроме этого, данное изобретение обеспечивает жизнеспособный раствор для проведения дорогостоящего и трудно реализуемого процесса экстракции ферментов, представляющих интерес, из семян, в которых они приготовлены. Ферменты остаются устойчивыми внутри семян и, таким образом, могут быть использованы в качестве замены чистого фермента. Это преимущество, вместе с дешевизной выращивания семяпроизводящих растений, обеспечивает экономическую основу применения таких ферментов. Таким образом, данное изобретение позволяет снизить затраты, связанные с приготовлением, хранением и применением множества ферментов.
На фиг. 1 изображена стратегия клонирования фитазы кДНК.
На фиг. 2 изображен бинарный вектор pMOG23.
На фиг. 3 изображена геномная последовательность запасенного в семенах гена круциферина из "Brassica napus".
На фиг. 4 изображены дуплексы синтетических олигонуклеотидов, используемых для различных конструкций.
На фиг. 5 изображена плазмида pMOG429. Бинарный вектор pMOG23, содержащий часть кДНК фитазы, кодирующую нисходящие созревшие ферменты последовательности ДНК, кодирующей сигнальный пептид круциферина.
На фиг. 6 изображены эффекты добавления семян из грунта, содержащих фитазу, на высвобождение неорганического фосфора из фитата.
На фиг. 7 изображена геномная последовательность гена альфа-амилазы "Bacillus licheniformis" как присутствующая в векторе pPROM54.
На фиг. 8 изображена плазмида pMOG29. Плазмида pUC18, содержащая кассету экспрессии для неуправляемой экспрессии в растениях и последовательность, кодирующую сигнальный пептид табака.
На фиг. 9 изображена плазмида pMOG227. Бинарный вектор, содержащий часть гена альфа-амилазы, кодирующую нисходящие созревшие ферменты последовательности табака, кодирующей сигнальный пептид табака в кассете экспрессии для неуправляемой экспрессии.
На фиг. 10 изображено связанное с дозой соотношение фитазы "Aspergillus" в лабораторной модели гидролитического разложения.
На фиг. 11 изображено связанное с дозой соотношение фитазы "Aspergillus" и фитазы, содержащейся в семенах табака, в лабораторной модели гидролитического разложения.
На фиг. 12 проведено сравнение образцов олигосахаридов, полученных при гидролизе картофельного крахмала с применением: A) семян табака, преобразованных геном, кодирующим альфа-амилазу "Bacillus licheniformis"; B) альфа-амилазы "Bacillus licheniformis" и C) альфа-амилазы "Bacillus amyloliquefaciens".
На фиг. 13 проведено сравнение образцов олигосахаридов, полученных при гидролизе крахмала злаков с применением: A) семян табака, преобразованных геном, кодирующим альфа-амилазу "Bacillus licheniformis"; B) альфа-амилазы "Bacillus licheniformis" и C) альфа-амилазы "Bacillus amyloliquefaciens".
Подробное описание предпочтительных примеров осуществления данного изобретения
Представляющие интерес ферменты, которые могут быть получены по данному изобретению, включают любые ферменты, применяемые в производственных процессах.
Представляющие интерес ферменты включают ферменты, которые гетерологичны растению (т.е. не присущи конкретным видам растений), в котором они приготавливаются. Сюда также входят ферменты, гомологичные растениям (т.е. присущие конкретным видам растений), в которых они приготавливаются, и с избытком экспрессированные посредством методов применения рекомбинатной ДНК.
Такие ферменты выбираются из таких гидролаз, как протеазы, целлюлазы, гемицеллюлазы, фосфатазы, липазы, пектиназы, амидазы, лизоцимы, пуллулуназы и хитаназы, таких лиаз, как пектинлиаза, и таких изомераз, как изомераза глюкозы.
Предпочтительными ферментами являются фитаза, альфа-амилаза, целлобиогидролаза, эндоглюканаза, эндоксиланаза, эндогалактаназа, альфа-галактозидаза, арабинаназа, серинпротеазы, химозин, папаин, гастролипазы, пектинлиаза и глюкозоизомераза.
Промышленными считаются процессы, в которых экстрагированные и/или изолированные ферменты обычно включаются в смесь реактивов при реакции в естественных или искусственных условиях, содержащую по меньшей мере один субстрат, в котором ферменты способы катализировать такую реакцию субстрата (субстратов) таким образом, чтобы производить желаемые эффекты или продукты.
В число примеров таких промышленных процессов входят (но не исчерпывают их число) лабораторные процессы типа применения фитаз при обработке сои или осуществлении таких производственных процессов, как влажное перемалывание с целью изготовления инозитола или инозитолфосфатов из фитата. Гемицеллюлазы и целлюлазы можно также применять, вообще говоря, в качестве разлагаемых ферментов с ячеистой стенкой. Аналогично, альфа-амилазы можно использовать в хлебопекарной промышленности, чтобы улучшать качество выпечки и ее консистенцию; альфа-амилаза, амидоглюкозидаза, ксиланазы и/или глюкозоизомераза могут использоваться при разжижении крахмала; лигниназы и/или ксиланазы могут быть использованы в производстве бумаги; глюканазы, пектиназы и/или целлюлазы могут применяться в производстве еды и напитков, например - в процессах ферментации или сбраживания.
Помимо упомянутого выше воздействия ферментов в искусственных процессах, запасенные в семенах ферменты могут быть использованы для катализа реакций разложения в естественных процессах. В этом случае ферменты облегчают выделение питательных веществ из пищевых продуктов, которые не смогли бы попасть в пищу животного другим способом.
Ферменты, используемые в таких естественных процессах, включают (но этим их число не ограничивается) фитазы, целлюлазы, гемицеллюлазы, пектиназы и амилазы. Ферменты приведут к улучшению переваривания пищевых продуктов. Ферменты как пищеварительные добавки могут также использоваться и для нужд человека, например, в таких случаях заболеваний, как муковисцидоз или в других случаях панкреатического заболевания. Липазы, протеазы и целлюлазы, содержащиеся в семенах, могут быть использованы в терапевтических добавках, облегчающих трудности пищеварения, связанные с указанными заболеваниями.
Согласно данному изобретению желаемый фермент приготавливается в семенах трансгенных растений. Подготовленные таким образом семена используются в промышленном процессе, требующем применения фермента при отсутствии необходимости первичной экстракции и/или изоляции фермента.
Теми, кто сведущ в данной области, будет по достоинству оценено, что семена, содержащие ферменты и предназначенные для применения в промышленности, могут быть использованы в таких процессах непосредственно, или могут сначала быть подготовлены к такому применению посредством помола их до заданной консистенции. В любом случае все или перемолотые семена могут быть введены в такой желаемый процесс при отсутствии необходимости дальнейшей экстракции и/или изоляции фермента, а также без потерь активности фермента.
Как определено в контексте данного изобретения, трансгенные растения включают растения и их потомство, которое генетически модифицировано с целью создания или увеличения приготовления по меньшей мере одного представляющего интерес фермента в их семенах. Таким образом, приготовление представляющих интерес ферментов увеличивается по сравнению с уровнем, обнаруживаемым в дикорастущих растениях.
В контексте данного изобретения фраза "семена, содержащие увеличенное количество фермента" относится, в основном, к статистически значимому количеству семян, которые, в среднем, содержат статистически значимое большее количество фермента по сравнению со средним количеством фермента в равном количестве немодифицированных семян.
Роды растений, способные к производству представляющего интерес фермента в своих семенах и подходящие для реализации данного изобретения, включают (но этим их число не исчерпывается) такие, как "Nicotiana" (например, "tabacum"), "Brassica" (например, "napus" и "oleracea"), "Arabidopsis, Glycine" (например, "max"), "Zea" (например, "mays"), "Amaranthus, Hordeum" (например, "vulgarum") и "Pisum" (например, "sativum"), "Juglans" (например, "regia"), "Arachis" (например, "hypogeae"), "Medicago" (например, "sativa"), "Phaseolus" (например, "vulgaris"), "Pisum" (например, "sativum"), "Triticum" (например, "aestivum"), "Panicum L. , Helianthus" (например, "annus"), "Avena" (например, "sativa") и "Oryza" (например, "sativa").
Предпочтительно, чтобы выбираемые виды растений могли давать большую производительность семени на растение за год и чтобы химические и физические свойства семян были совместимы с промышленным процессом, для которого приготавливается фермент. Например, в некоторых случаях, когда эти семена (после преобразования родительского растения) включаются в пищевые продукты, можно выбрать виды растений, которые производят семена с низким содержанием таннинов или других антипищевых особенностей. В других случаях способность трансгенных семян к помолу до желаемой консистенции может служить критерием выбора, когда семена применяются в качестве добавок, например - в муку. В еще одном примере осуществления данного изобретения семена, содержащие представляющие интерес ферменты, могут быть введены в желаемый процесс непосредственно (например - при производстве пищевых продуктов), чему может предшествовать очистка и/или осушение по завершении сбора семян.
Выбор наиболее подходящих видов растений может быть основан на экспериментах по воспроизведению. Представляющий интерес фермент может быть добавлен вместе с широко распространенными семенами в смесь реактивов промышленного процесса, для которого в конечном счете будут подготовлены трансгенные семена.
Генетическая модификация вышеописанных семяпроизводящих растений подразумевает, что конструкция экспрессии, включающей ген, кодирующий представляющий интерес фермент, вводится в целевое растение. Эта конструкция экспрессии может включать ген, гетерологичный растению, который находится под управлением промотора, и терминирующие области, способные регулировать экспрессию гена, кодирующего представляющий интерес фермент в семенах растения. Также вводится ген, гомологичный растению, который находится под управлением регулируемой области, способной воздействовать на перепроизводство представляющего интерес фермента. Посредством перепроизводтва вводится производство представляющего интерес фермента на уровнях, которые превышают обнаруживаемые у множества дикорастущих растений.
Имеется несколько способов введения конструкции экспрессии, содержащей последовательность ДНК, кодирующую представляющий интерес фермент, в целевые растения. Такие способы включают (но этим их число не ограничивается) преобразование протопластов с помощью метода применения кальция/полиэтиленгликоля, электропорацию и микроинжекцию или бомбардировку (покрытыми) частицами (Potrykus, 1990).
Кроме этих так называемых методов непосредственного преобразования ДНК, широко распространены системы преобразования, включающие векторы, например векторы вирусов (начиная, к примеру, с вируса мозаики цветной капусты (CaMV)), и векторы бактериальные (например, из рода "Agrobacterium") (Potrykus, 1990). После отбора и/или поиска в мутантных средах, протопласты, клетки или части растений, которые претерпели преобразование, могут быть регенерированы в целые растения с помощью известных в рассматриваемой области методов (Horsh R.B. и др., 1985). Выбор способов преобразования и/или регенерации не критичен для данного изобретения.
Для двудольных растений, в предпочтительном примере осуществления данного изобретения используется принцип системы бинарного вектора (Hoekema и др. , 1983; Schilperoort и др., 1984), в которой используются штаммы "Agrobacterium", содержащие vir-плазмиду с вирулентными генами и совместимую плазмиду, содержащую конструкцию гена, подлежащую преобразованию. Этот вектор может воспроизводиться как в спирали фермента, так и в "Agrobacterium" и выводится из бинарного вектора Bin19 (Bevan, 1984), который изменяется в деталях, не относящихся к данному изобретению. Используемые в этом примере бинарные векторы содержат между левой и правой граничными последовательностями Т-ДНК тот же ген NPTII, кодирующий устойчивость к канамицину (Bevan, 1984) и место клонирования, чтобы клонировать требуемые конструкции генов.
Преобразование и регенерация однодольных культур не является стандартной процедурой. Тем не менее, достигнутый за последние годы прогресс в науке показывает, что в принципе однодольные культуры поддаются преобразованию и что из преобразованных клеток могут быть регенерированы плодоносящие трансгенные растения. Разработка систем, воспроизводящих культурные ткани для этих культур, наряду с разработкой мощных методов введения генетического материала в клетки растений, облегчила преобразование. В настоящее время среди методов, выбираемых для осуществления преобразования однодольных культур, имеются бомбардировка эксплантатов микрочастицами или бомбардировка клеток суспензии микрочастицами, а также непосредственное поглощение ДНК или электропорация протопластов. Например, трансгенные растения риса были успешно получены с помощью бактериального гена hph кодирующего устойчивость к гидромицину, в качестве маркера селекции. Этот ген был введен посредством электропорации (Shim и др. , 1989). Трансгенные растения кукурузы были получены введением гена "Streptomyces hygroscopicus bar", кодирующего ацетилентрансферазу, фосфинотрицина (фермент, дезактивирующий гербицид фосфинотрицин), в эмбриогенные клетки культуры кукурузной суспензии методом бомбардировки микрочастицами (Gordon-Kamm и др., 1990). Введение генетического материала в протопласты алейрона таких других однодольных культур, как пшеница и ячмень, тоже отражено в научных работах (Lee и др., 1989). Растения пшеницы регенерировались из культуры эмбриогенной суспензии путем выбора только состарившейся плотной части культуры и тканей клубенькового эмбриогенного каллюса для установления культур эмбриогенной суспензии (Vasil и др., 1990). Сочетание этих культур с системами преобразования обусловливает возможность применения данного изобретения к преобразованию монодольных растений. Эти методы могут применяться и для преобразования и регенерации двудольных растений.
Экспрессия рекомбинантных генов в растениях включает такие детали, как транскрипцию гена полимеразами растения, трансляцию матричной РНК (мРНК) и т. д., что хорошо известно специалистам, квалифицированным в области методов применения рекомбинантной ДНК. Ниже обсуждаются только те подробности рассмотренных процессов, которые относятся к способствующим лучшему пониманию данного изобретения.
Регуляторные последовательности, которые известны или находятся путем вызывания достаточно высокой экспрессии (в целях особых приложений, как обсуждается ниже) рекомбинантной ДНК в семенах, могут быть применены в данном изобретении. Такие регулярные последовательности можно получить из растений или от вирусов растений, или синтезировать химическим путем. Такие регуляторные последовательности являются промоторами, действуют во время непосредственной транскрипции в семенах. В их число входят (но не исчерпывают его) промоторы из генов особых семян, особенно - генов запасных белков, типа cruA-промотора "Brassica napus" (Ryan и др., 1989) или промоторов генов составной экспрессии типа промотора 35S вируса мозаики цветной капусты (CaMV) (Guilley и др. , 1982). Другими регуляторными последовательностями являются терминирующие последовательности и сигналы полиаденилирования, включающие каждую последовательность, функционирующую в растениях в качестве указанных выше последовательностей; примерами являются область экспозиции 3' гена нопалинсинтазы "Agrobacterium tumefaciens" или область экспозиции 3' cruA-гена "Brassica napus". Регуляторные последовательности могут также включать такие последовательности энхансера, как обнаруженные в промоторе 35S в CaMV и такие стабилизирующие мРНК последовательности, как лидерная последовательность мономерных остатков вируса мозаики люцерны (AlMV) RNA4 (Brederode и др., 1980) или любые другие последовательности, функционирующие как указанные.
Представляющий интерес белок должен быть в окружающей среде, которая обеспечивает оптимальную устойчивость белка во время созревания семян. Выбор таких составных частей клетки, как цитозоль, эндоплазматический ретикулум, вакуоль, белковое тело или периплазматическое пространство может быть использован в данном изобретении для создания указанной стабильной окружающей среды, в зависимости от биофизических параметров, в которые входят (но не исчерпывают его) оптимальное значение pH, чувствительность к протеазам или чувствительность к молярности предварительно заданной составной части. Хотя предпочтительнее гомологичные сигнальные последовательности, могут применяться и гетерологичные сигнальные последовательности. Особо предпочтительными являются сигнальные последовательности, полученные из запасных белков семян.
Запасные белки семян можно разделить на четыре основных класса, основанных на характеристиках растворимости.
1. Альбумины. Растворимы воде и подразделяются на два основных класса (12S и 2S). Класс 12S включает лектины, изолированные из гороха и различных бобовых культур, например альбумины 2S из "Brassica napus", "Arabidopsis thaliana", "Ricinus communis" (касторовые бобы), "Bertholletia exelsa" (бразильский орех), фасоли, редиса и подсолнечника.
2. Глобулины. Растворимы в растворах солей и могут быть класса 7S или класса 8S, например - фазолины из "Phaseolus", вицилины из фасоли, конглицинины из соевых бобов, вицилины из овса и глобулины класса 7S из других культур, или такие представители классов 11S-14S, как легумины из фасоли, глицинины из соевых бобов, гелиантины из подсолнечника, круциферины из рапса или белки классов 11S-14S из таких других видов, как "Arabidopsis" и бобовые культуры.
3. Проламины. Растворимы в разведенном в воде спирте. Например - зеины из злаков, гордеины из ячменя, глиадины, изолированные из пшеницы и кафирины из сорго.
4. Глутелины. Растворимы в кислотных или щелочных растворах и могут быть изолированы из пшеницы.
Хотя существуют исключения, основные запасные белки в семенах двудольных растений - это глобулины, а для однодольных растений - проламины и глутелины.
Все составные части, относящиеся к конструкциям ДНК (промоторы; регуляторные, стабилизирующие, сигнальные или терминирующие последовательности) и соответствующие данному изобретению, могут быть по желанию модифицированы, чтобы изменить их управляющие характеристики, с помощью методов, известных специалистам в данной области. Количество рекомбинантного белка ("уровень экспрессии"), необходимое в семени, должно быть очень высоким, чтобы использовать трансгенное семя как незначительную добавку (рассчитываемую на основе объемных, весовых или стоимостных характеристик) для всех предпочтительных случаев осуществления данного изобретения.
С целью получения трансгенных растений, семена которых содержат более одного представляющего интерес фермента, можно использовать целый ряд методов. В их число входят (но не исчерпывают его):
a) перекрестная подкормка трансгенных растений, экспрессирующих один или более представляющих интерес ферментов;
b) преобразование растений фрагментами ДНК или плазмидами, содержащими многочисленные гены, кодирующие представляющие интерес ферменты с помощью необходимых регуляторных последовательностей;
c) преобразование растений различными фрагментами ДНК или плазмидами одновременно, причем каждый из фрагментов или каждая плазмида содержат ген представляющих интереса фермента, с помощью необходимых регуляторных последовательностей;
d) последовательное преобразование тканей с использованием на каждой стадии фрагмента ДНК или плазмиды, кодирующих различные ферменты, представляющие интерес, под управлением необходимых регуляторных последовательностей;
e) сочетание указанных выше методов.
Метод, который фактически применяется для получения семян, содержащих один или более представляющих интерес ферментов, не критичен применительно к цели данного изобретения.
Подчеркиваем, что семена, содержащие увеличенные количества ферментов, могут быть получены с помощью процессов, известных специалистам в данной области и отличающихся от упоминавшихся выше рекомбинантных процессов тем, что они обеспечивают получение семян с увеличенными содержаниями ферментов по сравнению с семенами дикорастущих растений. Например, было бы возможно получать такие семена с помощью методов обеспечения сомаклональных изменений. Далее такие методы могли бы быть использованы непосредственно или в сочетании с методами отбора, в которых используется концепция цитоплазматической мужской стерильности (CmS), или ядерной мужской стерильности (NmS) (Mariani и др., 1990). Такие способы, как сомаклональная вариация или перекрестное скрещивание с помощью CmS или NmS могли бы быть использованы в сочетаниях с упоминавшимися выше рекомбинантными способами, чтобы еще больше увеличить количества имеющихся внутри семян ферментов. Что касается нерекомбинантных методов, которые могли бы быть использованы для увеличения количества ферментов в семенах, то можно сослаться на патент США N 4378655, изданный 07.04.83; в данном описании ссылка на этот патент приводится с целью раскрытия содержания таких способов. Подчеркнем, что существуют многочисленные публикации, в которых описаны способы селекции, включающие цитоплазматическую мужскую стерильность, открытую в 1968 г., и с применением соответствующих доминантных генов, восстанавливающих фертильность (Rf) (M.L. Kinmar и др., 1970). В последние годы было описано применение концепции ядерной мужской стерильности (Mariani и др., 1990). Более обобщенные описания, касающиеся скрещивания растений, обсуждаются в работе James R. Welsh "Основы генетики растений и скрещивание", 1981, а также в работе J.M. Poehlman. "Скрещиваемые полевые культуры", 1959.
В одном из примеров осуществления данного изобретения двуцепочечная ДНК, кодирующая фитазу, приготавливается из мРНК, изолированной из "Aspergillus ficuum" (van Gorcom и др., 1991). Конструкция ДНК находится под управлением регуляторных последовательностей, состоящих из запасного белка класса 12S-круциферина из "Brassica napus". Затем эта конструкция ДНК субклонируется в бинарный вектор типа pMOG23 (в штамме DH5 α E.coli K-12, депонированном в Центральном бюро культур штаммов в Берне, Нидерланды, с 29.01.90 под номером CBS 102.90). Этот вектор вводится в "Agrobacterium tumefaciens", где содержится обезвреженная плазмида, индуцирующая образование галлов у растений. Клетки бактерий, содержащие эту конструкцию, сокультивируются с тканями из табака или растений вида "Brassica", а клетки преобразованного растения отбираются с помощью питательной среды, содержащей антибиотики и индуцируемой в различные растения, чтобы регенерировать на базе такой среды нужные клетки. Получаемые в результате растения дают семена, которые содержат и экспрессируют конструкцию ДНК.
В другом примере осуществления данного изобретения кодирующая фитазу конструкция ДНК находится под управлением регуляторных последовательностей из промотора вируса мозаики цветной капусты (CaMV). Далее эта конструкция субклонируется в бинарный вектор. Затем этот вектор вводится в "Agrobacterium tumefaciens", где содержится обезвреженная плазмида, индуцирующая образование галлов у растений. Клетки бактерий, содержащие эту конструкцию, сокультивируются с тканями из табака или растений вида "Brassica", а клетки преобразованных растений отбираются с помощью питательной среды, содержащей антибиотики и индуцируемой в различные растения, чтобы регенерировать на базе такой среды нужные клетки. Получаемые в результате растения дают семена, которые содержат и экспрессируют составную конструкцию ДНК.
Деятельность фермента фитазы трансгенных семян может быть описана многочисленными методами (причем конкретный метод не критичен применительно к данному изобретению) типа ферментного иммуносорбентного анализа, вестерн-блотирования или прямых ферментативных методов анализа с использованием приемов калориметрии или приемов анализа природного геля.
Семена, содержащие подготовленную таким образом фитазу, могут быть использованы в промышленных процессах в качестве кормовых добавок для животных, не относящихся к жвачным, при обработке сои или в производстве инозитола или инозитолфосфатов из фитата. При необходимости или при желании можно сначала перемолоть семена до нужной консистенции (в зависимости от природы промышленного процесса) при отсутствии необходимости последующей экстракции и/или изоляции фитазы. В этом случае любой специалист в данной области сможет определить, нужны ли такие подготовительные стадии.
Произведенная в семенах фитаза может быть использована и в процессе замачивания зерен злаков или сорго. Семена могут быть перемолоты перед добавкой в замоченные зерна злаков. Освобожденная от семян фитаза может воздействовать на фитин, который присутствует во многих препаратах злаков. Разложение фитина в замоченном зерне злаков выгодно для получения дополнительного коммерческого объема кукурузного экстракта, который применяется в качестве корма для животных или в качестве питательной среды в реакциях бактериальной ферментации. Более того, разложение фитина поможет избежать проблем, связанных с накоплением остатков в фильтрах, трубах, емкостях реакторов и т.д. при сгущении, транспортировании и хранении кукурузного экстракта (Vaara и др. , 1989). Действие фитазы может также ускорить процесс замачивания и процессы разделения, входящие в технологию перемалывания влажных зерен.
В еще одном примере осуществления данного изобретения фрагмент геномной ДНК, кодирующий альфа-амилазу из "Bacillus licheniformiis", находится под управлением промотора 35S CaMV и последовательностей энхансера. Сюда входят как стабилизирующая мРНК лидерная последовательность многомерных остатков RNA4 из AlMV, так и терминирующие и сигнальные последовательности полиаденилирования гена нопалинсинтазы "Agrobacterium tumefaciens". Далее вся конструкция субклонируется в бинарный вектор. Этот вектор вводится в "Agrobacterium tumefaciens", где содержится обезвреженная плазмида, индуцирующая образование галлов у растений. Клетки бактерий, содержащие эту конструкцию, сокультивируются с тканями растений табака, а клетки преобразованного растения отбираются с помощью питательной среды, которая содержит антибиотики и индуцируется, чтобы регенерировать в различных растениях нужные клетки на базе такой среды. Полученные в результате растения дают семена, которые содержат и экспрессируют конструкцию ДНК.
Действие фермента альфа-амилазы трансгенных семян может быть описано различными методами, что не критично применительно к данному изобретению; например - методами непосредственного ферментативного анализа с использованием приемов калориметрии или приемов анализа природного геля.
Семена можно использовать в качестве источника альфа-амилазы, которую можно прямо использовать в промышленных процессах типа приготовления сиропов крахмала. Предпочтительнее сначала перемолоть семена; всю (перемолотую) смесь можно использовать в процессе, что может определить любой квалифицированный в данной области специалист.
Следующие далее примеры предназначены для того, чтобы дать обычному специалисту в данной области описание и полное представление о том, как выполнить работу по данному изобретению и как применить ее результаты; приведенное описание не ограничивает объем, который, по мнению авторов, охватывается изобретением. Были предприняты все усилия, чтобы гарантировать точность использованных данных (например, количеств, температуры, pH и т.д.), но следует учесть, что при этом имели место некоторые методические погрешности экспериментов и отклонения.
Если нет других указаний, то температура указывается в градусах Цельсия, а давление равно атмосферному или близко к нему.
Пример 1
Изоляция поли-A+-РНК от "Aspergillus ficuum"
Штамм "Aspergillus ficuum" NRRL 3135 выращивается в среде, содержащей кукурузную муку в концентрации 22,72 г/л (амилазу, обработанную при pH 7, температуре 85oC, в течение пятнадцати минут), глюкозу в концентрации 9,36 г/л, KNO3 в концентрации 2,9 г/л, KCl в концентрации 0,142 г/л, MgSO4•7H2O в концентрации 0,142 г/л и FeSO4•7H2O в концентрации 56,8 мг/л. Через 6 суток была получена плесень.
Высушенная плесень в количестве 0,5 г замораживалась жидким азотом и перемалывалась. Затем ее гомогенизовали с ультратарраксом (на полной скорости в течение одной минуты) при температуре 0oC в трехмолярном LiCl шестимолярной мочевине и с вечера всю ночь выдерживалась при температуре 4oC, как описывали Auffray и Rougeon (1980). Вся клеточная РНК получалась после центрифугирования при 16000g за которым следовали две последовательные экстракции с применением реактива фенол:хлороформ:изоамиловый спирт = (50:48:2). РНК осаждается этанолом и вновь растворяется в 1 мл 10-миллимолярного Tris-HCl (pH 7,4), 0,5% SDS. Для отбора поли-A+ весь образец РНК нагревается в течение пяти минут при температуре 65oC, доводится до 0,5-молярного раствора NaCl и последовательно вносится в колонке олиго -(αT)- целлюлозы. После нескольких промывок раствором, содержащим 10-миллимолярный Tris (pH 7,0), 1-миллимолярную этилендиаминтетрауксусную кислоту и 0,1-миллимолярный NaCl, поли-A+-РНК собирается посредством элюции 10-миллимолярным Tris (pH 7,0) и 1-миллимолярной этилендиаминтетрауксусной кислотой.
Пример 2
Приготовление и клонирование кДНК, кодирующей фитазу
Для синтеза первичного штамма кДНК, 5 мкг поли-A+-РНК, изолированной по примеру 1, растворяется в 16,5 мкл H2O, а затем добавляют следующие компоненты: 2,5 мкл рибонуклеазина (30 единиц на мкл), 10 мкл буфера, содержащего 50-миллимолярный Tris-HCl (pH 7,6), 6-миллимолярный MgCl2 и 2 мкл одномолярного KCl, 5 мкл 0,1-молярного 4,4-дихлордифенилтрихлорэтана (DDT), 0,5 мкл олиго -(αT)12-18 (2,5 мг/мл), 5 мл 8-миллимолярной смеси αNT,5 мл BSA (1 мг/мл) и 2,5 мл обратной транскриптазы MLV Moloney (200 единиц на микролитр). Смесь инкубируется в течение тридцати минут при 37oC, а остановка реакции производится путем добавления 10 мл 0,2-молярной этилендиаминтетрауксусной кислоты (EDTA) и 50 мл H2O. Экстракция осуществляется с помощью 110 мл хлороформа, а после центрифугирования в течение пяти минут в водный слой добавляют пятмолярный NH4Ac и 440 мл неразбавленного этанола (-20oC). Осаждение проводится в растворе сухого льда в этаноле в течение тридцати минут. После центрифугирования (в течение десяти минут при 0oC) таблетка кДНК/мРНК промывается семидесятипроцентным этанолом, охлажденным льдом. Таблетка высушивается и растворяется в 20 мл H2O.
Изоляция фитазы, кодируемой кДНК, осуществляется посредством цепной полимеразной реакции (PCR) в двух фрагментах. Оба фрагмента комбинируются с помощью помещения BamHI внутри гена, чтобы создать кДНК полной длины. Стратегия клонирования кДНК фитазы показана на фиг. 1.
Программирование гена фитазы (Van Gorcom и др., 1991) проявляет присутствие сайта BamHI в примерно 800 комплементарных парах оснований от инициирующего кодона. Последовательность нуклеотидов вокруг сайта BamHI, как и последовательность нуклеотидов, предшествующая инициирующему кодону, и последовательность нуклеотидов после терминирующего кодона гена фитазы, используются для построения олигонуклеотидов для цепной полимеразной реакции (PCR).
Полимеразная цепная реакция осуществляется в соответствии с источником Taq-полимеразы (Cetus), путем использования 1,5 мл раствора, содержащего продукт реакции первого синтеза и по 0,5 мг каждого из олигонуклеотидов. Амплификация осуществляется в амплификаторе ДНК Перкина-Элмера-Цетуса. Через 25 циклов, в которые входят 2 минуты при 94o, 2 минуты при 55oC и 3 минуты при 72oC, из реагирующей смеси удаляются белки посредством последовательных экстракций фенолом и хлороформом. ДНК осаждается, повторно растворяется в буфере, содержащем 10-миллимолярный Tris (pH 7) и 0,1-миллимолярную EDTA, и затем гидролизуется с соответствующей рестрикцией ферментов.
Для амплификации фрагмента, кодирующего часть - отростка белка используются два следующих олигонуклеотида:
Олиго 1:
5'GGGTAGAATTCAAAAATGGGCGTCTCTGCTGTTCTA 3';
Олиго 2:
5'AGTGACGAATTCGTGCTGGTGGAGATGGTGTCG 3'.
Амплифицированный фрагмент разлагается гидролитически с помощью EcoRI и клонируется в сайт EcoRI pTZ18R (заимствованного из фармакологии). Картографирование места рестрикции и расшифровка последовательности нуклеотидов демонстрируют достоверность фрагмента. Полученная в результате плазмида названа pGB925.
Для амплификации второго фрагмента используются следующие два олигонуклеотида:
Олиго 3:
5'GAGCACCAAGCTGAAGGATCC 3';
Олиго 4:
5'AAACTGCAGGCGTTGACTGTGATTGTTTAAAGGG 3'.
Амплифицированный фрагмент разлагается гидролитически с помощью BamHI и PstI, а затем клонируется в pTZ18R, который уже гидролитически разложен с помощью BamHI и PstI. Картографирование мест рестрикции и расшифровка последовательности нуклеотидов показывает, что изолирован правильный фрагмент. результирующая плазмида называется pGB926.
Чтобы изолировать кДНК на всю полную длину, pGB925 гидролитически разлагается с помощью EcoRI и BamHI, в результате чего изолируется фрагмент, содержащий фитазу, кодированную ДНК. Этот фрагмент клонируется в плазмиду pGB926, которая уже гидролитически разложена с помощью EcoRI и BamHI, полученная в результате плазмида называется pGB927. Плазмида pGB927 содержит кДНК полной длины, кодирующую фитазу, с приближенным размером 1,8 тысячи пар оснований.
Пример 3
Построение бинарного вектора pMOG23
В этом примере описывается построение бинарного вектора pMOG23 в штамме DH5α E.coli K-12, депонированном в Центральном бюро культур штаммов в Берне, Нидерланды, с 29.01.90, номер для доступа - CBS 102.90).
Бинарный вектор pMOG23 (фиг. 2) - это производная вектора Bin19 (Bevan, M. , 1984). Чтобы получить pMOG23, вектор Bin19 изменяется способом, который не существенен для данного изобретения; методы такого изменения известны специалистам в данной области молекулярной биологии.
Во-первых, положения левой границы (LB) и правой границы (RB) заменяют на ген неомицинфосфотрансферазы II (ген NPTII). Во-вторых, ориентация гена NPTII изменяется на обратную, задавая транскрипцию в направлении LB. И наконец, полилинкер из Bin19 замещается полилинкером со следующими распознаваемыми сайтами рестрикционных ферментов: EcoRI, KpnI, SmaI, BamHI, XbaI, Sacl, XhoI и HindIII.
Пример 4
Клонирование кДНК фитазы "Aspergillus ficuum" в конструкцию экспрессии для получения конститутивной экспрессии в растениях
Ген фитазы из "Aspergillus ficuum" приспосабливается и клонируется в конструкции экспрессии, чтобы обеспечить неуправляемую экспрессию в них для промотора 35S вируса мозаики цветной капусты. Конструкция экспресссии содержит также кодовую информацию для сигнальной последовательности пептидов области начала репликации растения.
кДНК фитазы клонируется в конструкцию экспрессии так, будто обеспечивается присутствие плазмиды pMOG29 (описанной ниже в подразделе a) данного примера). Затем вся конструкция вводится в бинарный вектор pMOG23 и передается в штамм LBA4404 "Agrobacterium fumefaciens"
a) Конструкция вектора экспрессии pMOG29
Конструкция экспрессии ROKI (Baulcombe и др., 1986) клонируется как фрагмент EcoRI/HindIII в pUI18. Эта конструкция содержит промотор 35S вируса мозаики цветной капусты (CaMV) на фрагменте EcoRI/BamHI и терминатор транскрипции нопалинсинтазы (nos) на фрагменте BamHI/HindIII. Фрагмент промотора содержит последовательность промотора 35S CaMV от -800 до +1. Положение +1, включенное в эту последовательность, является местом инициации транскрипции (Guilley и др., 1982). Восходящая последовательность сайта NcoI в положении -512 удаляется и этот сайт заменяется на сайт EcoRI. Это делается разрезанием конструкции экспрессии, присутствующей в pUC18, с помощью NcoI, заполнением концов единичных цепочек полимеразой Кленова и сшиванием линкером EcoRI. Полученная в результате плазмида разрезается с помощью EcoRI, что вызывает отбрасывание фрагмента EcoRI, несущего последовательности восходящего промотора 35S сайта первоначального NcoI. Фрагмент BamHI/HindIII, содержащий терминатор nos замещается фрагментом синтетической ДНК (дуплекс A олигонуклеотидов, фиг. 4), содержащим лидерную последовательность мономерных остатков RNA4 вируса мозаики люцерны (AlMV) (Brederode и др., 1980). Это осуществляется расщеплением с помощью BamHI, за которым следует расщепление с помощью HindIII и сшивание фрагмента синтетической ДНК. Сайт BamHI и три восходящих нуклеотида исключаются посредством сайт-специфического мутагенеза. В получающейся в результате плазмиде воспроизводится фрагмент BamHI/HindIII, содержащий терминирующую последовательность nos. Ген, кодирующий β-глюциронидазу (происходящую из плазмиды pPAJ275; Jefferson, 1987), расщеплялся как фрагмент NcoI/BamHI, в результате чего образовывалась плазмида pMOG14. Из литературы известно, что дупликация последовательности между -343 и -90 увеличивает активность промотора 35S (Kay и др., 1987). Чтобы удвоить фрагмент промотора, т.е. получить так называемую последовательность энхансера, надо выполнить следующие шаги, известные специалистам в данной области. Из плазмиды pMOG14 фрагмент энхансера изолируется на фрагмент AccI/EcoRI и затем его концы тупятся полимеразой Кленова. Полученный фрагмент вводится в pMOG14, разрезается с помощью EcoRI и тупится таким образом, что граница между затупленным сайтом EcoRI и сайтом AccI дает новый сайт EcoRI. Получающаяся в результате плазмида (pMOG18) содержит промотор 35S с двойной последовательностью энхансера, лидерную последовательность мономерных остатков RNA4 из AlMV, а nos-терминатор в конструкции экспрессии по-прежнему присутствует на фрагменте EcoRI/HindIII. И наконец, фрагмент NcoI/BamHI, кодирующий бета-глюциронидазу, замещается фрагментом B синтетической ДНК (фиг. 4), производимым из PROB12 кДНК (Cornelissen и др., 1986). Этот фрагмент B кодирует последовательность сигнального пептида PR-S белка PR из табака "SamsunNN". Сайт SphI создается в кодируемой ДНК сигнальной последовательности пептидов заменой одного нуклеотида. Эта замена не изменяет последовательность аминокислот кодируемого сигнального пептида PR-S. Получающаяся в результате плазмида называется pMOG29 (фиг. 8).
b) Клонирование гена фитазы из "Aspergillus ficuum" в бинарный вектор
Дуплекс C олигонуклеотидов (фиг. 4) клонируется в плазмиду pMOG29, гидролитически разлагается с помощью SphI и BamHI, в результате получается плазмида pMOG407. Дуплекс олигонуклеотидов содержит кодирующую информацию для двух последних аминокислот сигнального пептида PR-S за которыми следуют первые 6 аминокислот созревшей фитазы.
Плазмида pGB927, которая содержит кДНК фитазы полной длины, гидролитически разлагается с помощью XhoI (частично) и PstI. Фрагмент XhoI/PstI, содержащий последовательности ДНК, кодирующие созревшую фитазу из шести первых аминокислот, клонируется в плазмиду pMOG417. Вся конструкция, содержащая химерный ген фитазы, вводится в качестве фрагмента EcoRI/HindIII и бинарный вектор pMOG23, линеаризованный посредством EcoRI и HindIII. Получающаяся в результате бинарная плазмида pMOG413 мобилизуется при трехродительском скрещивании со штаммом RK2013 E. coli K-12, содержащим плазмиду pRK2013 (Ditta и др., 1980), в штамм LBA4404 "Agrobacterium tumefaciens" содержащий плазмиду с вирулентными генами, необходимыми для передачи ДНК растению.
Пример 5
Переходная экспрессия химерного гена фитазы в протопласты табака
Протопласты табака трансформируются с помощью ДНК плазмиды, несущей химерный ген фитазы под управлением составного промотора 35S CaMV. Через 72 часа обработанные протопласты испытываются с целью обеспечения переходной экспрессии введенного гена фитазы посредством проверки активности фитазы.
Протопласты приготавливаются из должным образом выращивавшихся растений табака возраста 1-2 месяца ("Nicotiana tabacum" SRI). Вся процедура описана Rodenburg и др. (1989). Для осуществления преобразования, 5•105 протопластов электропорировали с помощью 40 мкг ДНК плазмиды pMOG417. После электропорации протопласты повторно разводятся в суспензию с помощью 3 мл вещества K3G. Чтобы проверить активность фитазы, протопласты формируются в таблетки, а надосадочная жидкость всю ночь диализуется во избежание избытка воды. Диализат вымораживается и повторно разводится избытка воды. Диализат вымораживается и повторно разводится в 300 мл 25-миллимолярного ацетата натрия (pH 5,5). Затем выполняется анализ, подробности которого описаны в примере 10, за одним исключением - вместо буфера из 250-миллимолярного глицина и HCl (pH 2,5) используется буфер ацетата натрия 1,5-миллимолярного (при 37oC, pH 5,5).
В этих экспериментах одна единица фитазы определялась как 1-микромолярный фосфат, выделенный из раствора 1,5-миллимолярного ацетата натрия за минуту при 37oC и pH 5,5.
В необработанных протопластах не обнаружена активность фитазы. Протопласты, электропорированные с помощью pMOG417, проявляют активность в 0,26 (RTU (единиц фитазы, см. пример 10) на миллиграмм белка в надосадочной жидкости.
Пример 6
Устойчивая экспрессия химерного гена фитазы в растения табака под управлением промотора 35S CaMV
Табак преобразуется посредством сокультивации тканей растения со штаммом LBA4404 "Agrobacterium tumefaciens", содержащим бинарный вектор pMOG413 с химерным геном фитазы под управлением промотора 35S CaMV. Преобразование выполняется посредством сокультивации табака ("Nicotiana tabacum" SRI) в листовых дисках согласно Horsch и др., 1985. Трансгенные растения регенерируются из всходов, которые проращиваются в выбранной для этого среде (канамицин в концентрации 100 мг/л), укореняются и перемещаются в грунт. Молодые растения проверяются на активность гена NPTII (стойкость к канамицину), растут до созревания и до тех пор, пока не окажутся способными к самоопылению, а затем дают семена.
Чтобы определить обнаруженную в трансгенных семенах активность фитазы, берется почти 50 мг семян и гомогенизуется с помощью пестика в охлажденном льдом рабочем растворе объемом 1 мл 25-миллимолярного буфера ацетата натрия (pH 5,5). После центрифугирования надосадочная жидкость анализируется, как описано для случая переходной экспрессии. В тридцати двух независимо друг от друга преобразованных растениях табака максимальный уровень экспрессии фитазы составил 0,4% от общего растворенного белка семян. В непреобразованных растениях не наблюдалась активность фитазы.
На основе их высоких уровней экспрессии фитазы в семенах (приблизительно 0,4%) были отобраны две линии трансгенных растений: 413,25 и 413,32.
Пример 7
Клонирование кДНК фитазы "Aspergillus ficuum" в конструкцию семяспецифичной экспрессии
Конструкция экспрессии создается таким образом, что получается семяспецифичная экспрессия, использующая последовательности круциферина - гена запасного белка класса 12S из "Brassica napus" (cruA; Ryan и др., 1989). Эти последовательности могут быть замещены последовательностями аналогичных семяспецифичных генов для достижения той же самой цели, что и цель данного изобретения.
кДНК фитазы клонируется в конструкцию экспрессии. В конце концов, вся конструкция вводится в "Agrobacterium tumefaciens", что используется для преобразования. В случае любого другого представляющего интерес белка, клонирование гена или кДНК делается абсолютно тем же способом, что описан здесь для кДНК фитазы.
Для преобразования спирали фермента в данном примере используется штамм DH5α E.coli K-12.
a) Построение конструкции экспрессии
Чтобы построить конструкцию экспрессии, способную к семяспецифичной экспрессии, синтезируются последовательности промотора и терминатора из гена круциферина A (cruA) "Brassica napus" cv. "Jet Neuf" с помощью технологии PCR с изолированной геномной ДНК (Mettler, I.J., 1987) в качестве матрицы. Этот ген проявляет семяспецифичную экспрессию, а его кодовые и экспозиционные последовательности уже определены (Ryan и др., 1989).
Синтезируются два набора олигонуклеотидов. Один - чтобы обеспечить амплификацию области экспозиции cruA 5' и часть сигнального пептида, кодирующего последовательность как фрагмент EcoRI/NcoI:
5'GTTCGGAATTCGGGTTCCGG 3' и
5' AACTGTTGAGCTGTAGAGCC 3'.
Другой набор олигонуклеотидов предназначен для амплификации последовательности экспозиции 3' как фрагмента BglII/HindIII:
5'CTTAAGATCTTACCCAGTGA 3' и
5'CGGAGAAGCTTGCATCTCGT 3'.
Олигонуклеотиды предназначены для того, чтобы создать соответствующие сайты рестрикции экспрессии после гидролитического разложения фрагментов ферментами рестрикции.
Фрагмент 5' гена cruA, включающий 54 нуклеотида последовательности, кодируемой сигнальным пептидом, клонируется в вектор pMOG445 (дуплекс E олигонуклеотидов (фиг. 4), клонированный в вектор pUC18, линеаризованный с помощью SstI и EcoRI), разрывается с помощью EcoRI и NcoI, в результате чего получается вектор pMOG424. Синтезированный дуплекс D олигонуклеотидов (фиг. 4), содержащий последние 5 кодирующих триплетов для сигнальной последовательности круциферина "Brassica napus", последовательность, кодирующую аминокислоты созревшей фитазы с первой по шестую, и сайт множественного клонирования, клонируется в вектор pMOG424, разрезанный NcoI и HindIII. Полученный в результате вектор называется pMOG425. Фрагмент 3' cruA PCR клонируется как фрагмент BglII/HindIII в pMOG425, гидролитически разложенный с помощью BglII и HindIII, в результате чего получается pMOG426.
b) Клонирование гена фитазы из "Aspergillus ficuum" в бинарный вектор
Плазмида pGB927, содержащая полную кодирующую последовательность для фитазы "Aspergillus ficuum", гидролитически разлагается с помощью XhoI (частично) и PstI. Фрагмент XhoI/PstI, содержащий последовательности ДНК, кодирующие созревшую фитазу из шести последних аминокислот, клонируется в вектор pMOG42, разорванный XhoI и PstI. Из полученного в результате вектора pMOG428 вся конструкция, содержащая химерный ген фитазы вводится как фрагмент EcoRI/HindIII в бинарный вектор pMOG23, линеаризованный EcoRI и HindIII. Полученный в результате бинарный вектор pMOG429 (фиг. 5) мобилизуется при трехродовом скрещивании со штаммом RK2013 E.coli K-12, содержащим плазмиду pRK2013 (Ditta и др., 1980 г.), в штамм LBA4404 Agrobacterium (Hoekema и др. , 1983), содержащий плазмиду с вирулентными генами, необходимыми для передачи Т-ДНК растению.
Пример 8
Устойчивая семяспецифичная экспрессия фитазы в семенах табака под управлением промотора круциферина
Штамм LBA4404 "Agrobacterium", содержащий бинарный вектор pMOG429 с кДНК фитазы под управлением промотора круциферина, применяется в экспериментах по преобразованию. Преобразование табака ("Nicotiana tabacum" SRI) выполняется посредством сокультивации листовых дисков согласно процедуре, которую описали Horsch и др. (1985). Трансгенные растения регенерируются из ростков, которые прорастают в отобранной для этого среде (канамицин в концентрации 100 мг/л). Молодые растения испытываются на активность гена NPTII (устойчивость к канамицину), выращиваются до созревания и до тех пор, пока они не будут способны самоопыляться, и дают семена. Семена отдельных трансформантов группируются, и часть образцов семян проверяется на наличие фитазы. Из клонов с наивысшими уровнями экспрессии (по сравнению с непреобразованными контрольными растениями), оставшиеся семена проращиваются в среде канамицина (2000 мг/л) (а значит, тоже являются трансгенными для фитазы) и отбираются и применяются с целью массового распространения растений, способных давать наивысшие количества фитазы на своих семенах. Затем эти растения могут быть использованы, например, в экспериментах по гидролитическому разложению.
Чтобы определить активность фитазы, обнаруживаемой в трансгенных семенах, около 50 мг семян было гомогенизировано с помощью пестика в охлажденном льдом рабочем растворе объемом 1 мл 25-миллимолярного буфера ацетата натрия (pH 5,5). После центрифугирования, надосадочная жидкость испытывается, как описано в случае проверки для переходной экспрессии. В 55 независимо преобразованных растениях табака был обнаружен максимальный уровень экспрессии фитазы величиной 0,15% общего количества растворенного в семенах белка. В стеблях, корнях и листьях трансгенных растений активность фитазы не выявлена. Не смогли обнаружить активность фитазы и в непреобразованных растениях.
Пример 9
Преобразование семян рапса
В этом примере описывается преобразование семян рапса посредством сокультивации ткани растения с "Agrobacterium tumefaciens", содержащим бинарный вектор с химерным геном фитазы. Трансгенные растения можно отбирать по стойкости к антибиотикам. Трансгенные растения можно проверить на активность фитазы. Экспрессоры более высокого уровня можно проанализировать более тщательно и использовать в дальнейших экспериментах с растениями.
Та же самая химерная конструкция фитазы в бинарном векторе (pMOG429) мобилизуется в штамм LBA4404 "Agrobacterium tumefaciens" тем же самым способом, который описан в примере 7. Этот штамм может быть использован для преобразования семян рапса ("Brassica napus" cv. "Westar"). С этой целью сегменты стеблей со стерилизованной поверхностью, взятые из растений возрастом 5-6 недель, как раз перед цветением, предварительно обрабатываются в течение двадцати четырех часов в MS-среде (Fry и др., 1987) с помощью бактериальной щелочной фосфотазы (BAP) концентрации 1 мг/л, а затем сокультивируются в течение сорока восьми часов с "Agrobacterium" в новых чашках для засева культур с той же самой средой. Трансгенные саженцы можно регенерировать из ростков, которые растут в избранной среде (карбенициллин концентрации 500 мг/л, паромицин концентрации 40 мг/л) и далее анализировать, как описано в примере 8 для табака.
Пример 10
Проверка активности фитазы
В общей сложности 25 мг семян растения "Nicotiana tabacum" линии 413,25, в которой общее содержание составляло примерно 0,25 PTU, были измельчены (PTU - единицы фитазы. Одна единица активности фитазы определяется как количество фермента, которое выделяет неорганический фосфор из 1,5-молярного фитата натрия со скоростью 1 мкмоль/мин при температуре 37oC и pH 2,5).
Размельченные семена инкубируются в буферный раствор 250-миллимолярного глицина/HCl общим объемом 50 мл и с pH 2,5, причем общее содержание фитата натрия 11 H2O в буфере составляет 0,86 г. Хотя экспрессия фитазы "Aspergillus" дает оптимумы pH на уровнях 2,5 и 5,5, выбирается нижнее значение pH, чтобы пресечь активность фитазы в растении.
Результирующая смесь инкубируется в течение (15-60) минут при температуре 37oC. Реакцию прекращают путем добавления 5 мл инкубата в 5 мл десятипроцентной трихлоруксусной кислоты (TCA). Далее 10 мл реактива индикатора (3,66 г FeSO4•7H2O в 50 мл раствора молибдата аммония - 2,5 г (NH4)6Mo7O24•4H2O и 8 мл концентрированной H2SO4, разбавленной до объема 250 мл деминерализованной водой) добавляются в заторможенный раствор фермента. Интенсивность голубого цвета измеряется спектрофотометрически на длине волны 700 нм.
В качестве контрольного раствора служит раствор с содержанием неорганического фосфата, соответствующим T = 0.
Измерения показывают количество фосфата относительно соответствующего калибровочной кривой количества фосфата в диапазоне 0-1-миллимолярного раствора.
Пример 11
Инкубация размельченных семян Nicotiana tabacum с кормами
В типичном эксперименте 0,25 г растворенной вытяжки соевой муки инкубируется с 25 мг перемолотых семян "Nicotiana tabacum" (линия растения 413,25), содержащих 0,25 pTU в соответствии со сказанным выше, за исключением добавки фитата натрия. В этом случае добавочный агент инкубации состоит из смеси буфера объемом 410 мл и 90 мл деминерализованной воды.
В фактически идентичном эксперименте были получены аналогичные результаты для корма из пшеничной клейковины в качестве питательной среды. Результаты показаны на фиг. 6.
В отсутствие измельченных семян активность не наблюдалась, как и при добавке семян, которые не содержали активной фитазы.
Пример 12
Тестирование трансгенных семян, содержащих фитазу, в лабораторных условиях, подобных условиям пищеварительного тракта домашней птицы
Чтобы проверить эффективность фитазы, приготовленной в трансгенных семенах табака, активность фитазы из "Aspergillus" определялась в модели, воспроизводящей условия, обнаруженные в пищеварительном тракте домашней птицы.
Обычный образец корма домашней птицы сначала инкубировали в количестве 1 г на 15 мл деминерализованной воды в течение 60 мин при 39oC, чтобы воспроизвести условия в зобу птиц. Затем 5 мл раствора пепсина (Merck: 5,28 г/л, pH 3,0, доводится до кондиции HCl) добавляли в образец, доводили pH с помощью HCl до 3,0 и продолжали инкубацию в течение еще 90 мин при той же самой температуре, чтобы воспроизвести условия в желудке. В течение инкубационного периода брали пробы, чтобы определить количество фосфата, выделявшегося из-за присутствия фитата в корме.
Воздействие грибковой фитазы можно пояснить фиг. 10. Повышение дозировки фитазы с 250 PTU/кг корма до 1000 PTU/кг корма сказывается в увеличении выделения фосфата из пробы корма.
Когда образец семени трансгенного табака (линии 413,25 или 413,32; после измельчения в рабочем растворе) добавляли вместо грибковой фитазы, наблюдалось аналогичное выделение повышенного количества фосфата (фиг. 11). Тестировали и контрольное семя табака, не содержащее фитазу. В нем не было обнаружено выделение фосфата по сравнению с контрольным раствором.
Сравнение результатов эксперимента для корма, в котором содержание семени трансгенного табака составляло 50 г/кг, с результатами эксперимента, в котором содержание фитазы в корме составляло 500 PTU/кг и 750 PTU/кг, показывает, что 1 г семени табака эквивалентен 12 PTU в этой in vitro-модели пищеварения домашней птицы.
Пример 13
Тестирование животных
Чтобы показать эффективность фитазы, экспрессированной в семенах растений, а также отсутствие какого бы то ни было негативного эффекта семян табака на эсотехнические результаты, были поставлены эксперименты на бройлерах.
Были собраны семена табака с экспрессией фитазы и контрольные семена. Семена просеивали порциями по 100 г (в мельнице с выдачей порции помола ZMI) через сито с отверстиями размером 500 мкм, позаботившись о поддержании семян в охлажденном состоянии.
В один из дней самцов бройлерных цыплят ("Hybro") поместили в клетки с двумя ярусами батарей (0,45 м2). В течение первых двух дней температура составляла 32oC, а затем в течение первой недели понижалась на 4oC. Каждую последующую неделю температуру понижали на 2oC. Цыплят держали в режиме: 1 час на свету и 3 часа в темноте.
В возрасте одного дня птицу вакцинировали от болезни Нью Кастла с помощью вакцины "Клон 30". Во время экспериментов бройлеров держали на экспериментальной диете, причем все корма давались в виде кашицы в любом количестве. Рост и соотношения "корм/прибавка в весе" измерялись в течение периода экспериментов. Заметное наличие общего количества фосфора измерялось в течение трех дней, во время которых замерялось потребление кормов как сухой дозы вводимого вещества, а также оценивались количественно испражнения.
Применялись контролируемые диеты без добавки фитазы (см. табл. А)
В диету 1 (основную) не добавляли улучшающую подкормку фосфата. Кальций и фосфор из смеси безводного вторичного фосфата кальция и моноаммонийфосфат в соотношении 5:1 добавляли в диеты 2 и 3. Все экспериментальные диеты получали путем введения добавок в основную диету (см. табл. 1).
В экспериментальную диету 4 входят микробная фитаза в концентрации 400 PTU/кг корма, приготовленная так, как описали Van Gorcom и др. (1991).
Экспериментальная диета 5 подобна диете 4, но в кормовую смесь добавлены измельченные семена нетрансгенного табака до достижения конечного соотношения 3 кг/90 кг корма.
Экспериментальная диета 6 также подобна диете 4, но в кормовую смесь общим весом 90 кг добавлено 3 кг измельченных семян трансгенного табака (линия 413,25), чтобы получить конечную концентрацию фитазы 400 PTU/кг корма.
Эксперимент ставили на 176 бройлерах в 16-ти клетях с бактериями (по 11 бройлеров в клети с батареями) до тех пор, пока возраст бройлеров не составил 24 дня. Режимы (диеты) повторяли дважды и распространяли случайным образом в пределах каждого яруса клетей.
Наличие фосфора измеряли при возрасте птицы (21-24) дня.
Результаты, относящиеся к наличию фосфора и прибавки в весе, соответствующей диетам 4, 5 и 6, показывают для каждой диеты положительный эффект добавки фитазы (табл. 2). Сравнение диет 4, 5 и 6 также демонстрирует, что введение семян табака в корм сравнимо с воздействием микробной фитазы на желудочно-кишечный тракт разводимой на ферме домашней птицы типа бройлеров, и не выявляет никакого негативного влияния на зоотехнические результаты.
Пример 14
Клонирование гена альфа-амилазы "Bacillus licheniformis" в кассету экспрессии для осуществления конститутивной экспрессии
В этом примере ген альфа-амилазы из "Bacillus licheniformis" пришивается и клонируется в кассету экспрессии для осуществления конститутивной экспрессии, которая тоже содержит информацию о сигнальной последовательности пептидов области начала репликации растения. На последней стадии вся конструкция клонируется в бинарный вектор, переданный штамму LBA4404 "Agrobacterium tumefaciens", который применяется, чтобы преобразовать представляющее интерес растение. Так же, как здесь описано для гена альфа-амилазы, можно клонировать любой другой ген или кДНК.
Все преобразования в этом примере делаются в штамме DH5α E.coli K-12.
a) Пришивание гена альфа-амилазы "Bacillus licheniformis"
Ген альфа-амилазы из "Bacillus licheniformis" (фиг. 7), присутствующий в векторе "Bacillus" pPROM54 (депонирован в Центральном бюро культур штаммов с 05.11.85, номер доступа CBS 696.85) гидролитически разлагается с помощью XbaI и BclI. Фрагмент XbaI/BclI клонируется в плазмиду pUC18, линеаризованную с помощью XbaI и BamHI, в результате чего получается плазмида pMOG318. Фрагмент SalI/BamHI синтезируется с помощью PCR-технологиии (технологии цепных полимеразных реакций) с pMOG318 в качестве матрицы, создавая сайт BamHI с помощью несоответствующей затравки (указан на фиг. 7). PCR-фрагмент SalI/BamHI клонируется в плазмиду pIC-19R (Marsh и др., 1984), гидролитически разлагается с помощью SalI и BamHI, в результате чего получается плазмида pMOG319. Фрагмент SalI содержащий конец 5' гена альфа-амилазы, из pMOG318 (используя присутствие сайта SalI и PUC18) клонируется в pMOG319, линеаризованный с помощью SalI. В результате получается плазмида pMOG320, которая содержит весь ген альфа амилазы.
b) Построение вектора pMOG29
Вектор pMOG29 был построен в соответствии с описанием примера 4(a).
c) Клонирование гена альфа-амилазы из "Bacillus licheniformis" в бинарный вектор
Плазмида pMOG320 гидролитически разлагается с помощью HgaI и BamHI. Фрагмент HgaI/BamHI, кодирующий созревшую альфа-амилазу из девяти последних аминокислот, клонируется при трехстороннем лигировании с синтетическим дуплексом F олигонуклеотидов (фиг. 5) в pMOG29, линеаризованный с помощью SphI и BamHI в результате чего получается плазмида pMOG321. Дуплекс олигонуклеотидов имеет кодовую информацию о последних двух аминокислотах сигнального пептида PR-S и о первых девяти аминокислотах созревшей альфа-амилазы. Вся конструкция, содержащая химерный ген альфа-амилазы, вводится как EcoRI/HindIII в бинарный вектор pMOG23, линеаризованный с помощью EcoRI и HindIII. Полученная в результате бинарная плазмида pMOG227 (фиг. 9) мобилизуется при трехродительском скрещивании со штаммом RK2013 E. coli K-12 (содержащим плазмиду pRK2013) (Ditta и др., 1980) в штамм LBA4404 "Agrobacterium", содержащий плазмиду с вирулентными генами, необходимыми для передачи Т-ДНК растению.
Пример 15
Устойчивая экспрессия альфа-амилазы "Bacillus licheniformis" в табаке
В этом примере табак преобразуется путем сокультивации ткани растения с "Agrobacterium tumefaciens", содержащей бинарный вектор с химерным геном альфа-амилазы. Трансгенные растения отбираются по критерию устойчивости к антибиотикам. Семена трансгенных растений проверяются на активность альфа-амилазы. Экспрессоры высокого уровня анализируются более тщательно и используются в дальнейших экспериментах.
Штамм LBA4404 "Агробактериум" (pMOG227) используется в экспериментах по преобразованию. Преобразование табака ("Nicotiana tabacum" SRI) выполняется посредством сокультивации листовых дисков в соответствии с процедурой, которую описали Хорш. и др. (1985). Трансгенные растения регенерируются из всходов, проросших в отобранной для этого среде (канамицин, концентрация 100 мг/л). Молодые растения проверяются на активность гена NPTII, выращиваются до созревания, самоопыления и выдачи семян. Семена отдельных трансформантов группируются, и часть пробы семян испытывается на присутствие альфа-амилазы. Оставшиеся семена клонов с наивысшими уровнями экспрессии (по сравнению с непреобразованными контрольными семенами) проращиваются в среде канамицина (200 мг/л) (а значит тоже трансгенными для альфа-амилазы) и отбираются и применяются для массового распространения растений, способных давать наивысшие количества альфа-амилазы в производимых ими семенах. Максимальный наблюдавшийся уровень экспрессии фитазы составил 0,4% от общего количества растворенного в семенах белка. Эти семена можно затем использовать, например, в экспериментах по гидролитическому разложению и пищеварению.
Пример 16
Применение сформировавшейся в семенах альфа-амилазы с целью разжижения крахмала
Альфа-амилаза "Bacillus licheniformis", экспрессированная в семенах табака, применялась при разжижении крахмала следующим образом: были собраны по 100 г семян с экспрессией альфа-амилазы и контрольных семян табака. Семена просеивали через сито (в мельнице с выдачей порции помола ZMI), имеющее размеры пор 250 мкм, позаботившись об охлаждении семян. Чтобы определить содержание в них альфа-амилазы, перемолотые семена экстрагировали в десяти объемах 0,5-молярного буфера глицина (pH 9,0) с 10-миллимолярным CaCl2 в течение 30 минут при 0oC. Надосадочную жидкость использовали для определения количества альфа-амилазы методом Фадебаса (принятым в фармацевтической диагностике). Единицы содержания термоустойчивой альфа-амилазы называются TAU.
Тесты на разжижение выполняли следующим образом: суспензию крахмала (состав: 3,3 кг крахмала злаков или картофеля с содержанием сухого крахмала 88% (2,904 кг крахмала); 5,45 л H2O; содержание сухого крахмала в суспензии доводили до 33%, pH корректировали до величины 6,5 с помощью однонормального раствора сернистой кислоты или однонормального раствора NaOH; и перемолотые семена, и микробная альфа-амилаза добавлялись до количества, эквивалентного соотношению: 4,4 TAU на грамм сухого крахмала) нагревали как можно быстрее до температуры 100oC и выдерживали при этой температуре в течение десяти минут. Затем суспензию доводили до температуры 95oC и выдерживали в течение двух часов. Далее образцы подкисляли с помощью H2SO4, чтобы добиться pH 3,5, и помещали в ванну с кипящей водой, чтобы прекратить деятельность фермента до определения декстрозных эквивалентов (DE) и эталона гидролиза посредством жидкостной хроматографии высокого давления (HPLC). Для анализа посредством HPLC использовали колонну "BIORAD HPX-42A" с деминерализованной водой в качестве элюента. Эталон олигосахарида получали при гидролизе крахмала картофеля и злаков с помощью: A) семян преобразованных растений; B) "Maxamyl®" (альфа-амилазы "Bacillus licheniformis", полученной от "Gist-brocades N.V., Delf, The Netherlands); и C) "Dexlo® CL" (альфа-амилазы "Bacillus licheniformis", полученной от "Gist-brocades"). Полученные результаты сравнивали (фиг. 12 и 13). Образец олигосахарида, полученного из семян преобразованных растений, идентичен образцу, полученному с помощью "Maxamyl®", и оба указанных образца отличаются от образца, полученного с помощью "Dexlo®", подтверждая, что альфа-амилаза "Bacillus licheniformis" производится в семенах растений. Величины декстрозного эквивалента (DE), полученные на семенах растений (табл. 3) находятся в коммерчески приемлемом диапазоне (DE≥12, преимущественно DE≥16) (Reilly, 1985).
Хотя данное изобретение описано со ссылками на приводимые здесь варианты осуществления данного изобретения, для любого специалиста в данной области должно быть ясно, что могут быть внесены многочисленные изменения и модификации без хотя бы частичного отступления от духа и объема изобретения. Помимо этого, многие модификации могут быть проделаны для того, чтобы адаптировать конкретную ситуацию, материал, растение, семена, процесс, стадию или стадии процесса применительно к цели, духу и объему данного изобретения. Все такие модификации считаются входящими в объем данного изобретения, освещаемый прилагаемой формулой изобретения.
References
Altenbach, S.B., Pearson, K.W., Meeker, G., Staraci, L.C. & Sun, S.S.M. (1989) Plant Mol. Biol. 13. 513.
Auffray & Rougeon (1980) Eur. J. Biochem. 107, 303-314.
Barker, S. J. , Harada, J.J. & Goldberg, R.B. (1988) Proc. Natl. Acad. Sci. USA 85, 458.
Baulcombe, D.C., Saunders, G.R., Bevan, M.W., Mayo, M.A. & Harrison, B. D. (1986) Nature 321. 446.
Baumlein, H., Wobus, U., Pastell, J., & Kafatos, F.C. (1986) Nucl. Acids Res. 14, 2707.
Beachy, R.N., Chen, Z.- L., Horsch, R.B., Rogers, S.G., Hoffmann, N.J. & Fraley, R.T. (1985) EMBO J. 4., 3047.
Bevan, M. (1984) Nucl. Acids Res. 12, 8711.
Brederode, F. T. , Koper-Zwarthoff, E.G. & Bol, J.F. (1980) Nucl. Acids Res. 8, 2213.
Bustos, M. M. , Guiltinan, M.J., Jordano, J., Begum, D., Kalkan, F.A. & Hall, T.C. (1989) Plant Cell 1, 839.
Casey, R. & Domoney, C. (1987) Plant Mol. Biol. Reporter 5, 261.
Chee, В.В., Klassy, R.C. & Slightom, J.L. (1986) Gene 41, 47.
Cornelissen, B. J.C., Hooft van Huijsduijnen, R.A.M. & Bol, J.F. (1986) Nature 321, 531.
Della-Cioppa, G., Kishore, G.M., Beachy, R.N. & Fraley, R.T. (1987) Plant Physiol. 84, 965.
Ditta, G., Stanfield, S., Corbin, D. & Helinski, D.R. (1980) Proc. Natl. Acad. Sci. USA 77. 7347.
Dorel, С., Voelker, Т.A., Herman, E.M. & Chrispeels, M.J. (1989) J. Cell Biol. 108. 327.
Doyle, J. J. , Schuler, M.A., Godette, W.D., Zenger, V., Beachy, R.N. & Slightom, J.L. (1986) J. Biol. Chem. 261, 9228.
Ellis, J.R., Shirsat, A.H., Hepher, A., Yarwood, J.N., Gatehouse, J.A., Croy, R.R.D. & Boulter, D. (1988) Plant Mol. Biol. 10. 203.
Fischer, R.L. & Goldberg, R.B. (1982) Cell 29, 651.
Fry, J. & Barnason, A. & Horsch, R.B. (1987) Plant Cell Reports 6, 321.
Gasser, C.S. & Fraley, R.T. (1989) Science 244, 1293.
Goodman, R. M. , Knauf, V. C. , Houck, C.M. & Comai, L. (1987) PCT/WO 87/00865.
Gordon-Kamn, W.J., Spencer, T.M., Mangano, M.L, Adams, T.R., Daines, R. J., Start, W.G., O'Brien, J.V., Chambers, S.A., Adams Jr., W.R., Willets, N. G. , Rice, T. B., Mackey, C.J., Krueger, R.W., Kausch, A.P. & Lemaux, P.G. (1990) The Plant Cell 2., 603.
Guilley, H. , Dudley, R. K. , Jonard, G., Balazs, E. & Richards, K.E. (1982) Cell 30. 763.
Harada, J.J., Barker, S.J. & Goldberg, R.B. (1989) Plant Cell 1, 415.
Hattori, Т. , Nakagawa, Т. , Maeshima, M., Nakamura, K>, & Asahi, T. (1985) Plant Mol. Biol. 5, 313.
Hiatt, A., Cafferkey, R. & Boedish, K. (1989) Nature 342, 76.
Higgins, T.J.V., (1984) Annu. Rev. Plant Physiol. 35, 191.
Higgins, T. J.V., Newbigin, E.J., Spencer, D., Llewellyn, D.J. & Craig, S. (1988) Plant Mol. Biol. 11, 683.
Hoekema, A., Hirsch, P.R., Hooykaas, P.J.J. & Schilperoort, R.A. (1983) Nature 303. 179.
Hoffman, L.M., Donaldson, D.D., Bookland, R., Rashna, K. & Herman, E.M. (1987) EMBO J. 6, 3213.
Horsch, R. B., Fry, J.E., Hoffmann, N.L., Eichholtz, D., Rogers, S.G. & Fraley, R.T. (1985) Science 227, 1229.
Iturriaga, G., Jefferson, R.A. & Bevan, M.W. (1989) Plant Cell 1, 381.
Jefferson, R.A. (1987) Plant Mol. Biol. Reporter 5, 387.
Jordano, J., Almoguera, C. & Thomas, T.L. (1989) Plant Cell 1, 855. Kay, R., Chan, A., Dayly, M. & McPherson, J. (1987) Science 236. 1299.
Klee, H. , Horsch, R. & Rogers, S. (1987) Annu. Rev. Plant Physiol. 38, 467.
Krebbers, E. & Vandekerckhove, J. (1990) TIBTECH, 8, 1.
Larkins, M. A. (1981) In: The biochemistry of plants Vol. 6 (Academic Press, San Diego: Stumpf, P.K. & Conn, E.E., eds.). Chapter 11. p. 471.
Lee, B. , Murdoch, K. , Topping, J., Kreis, M. & Jones, M.G.K. (1989) Plant Mol. Biol. 13, 21.
Lycett, G.W., Delauney, A.J., Gatehouse, J.A., Gilroy, J., Croy, R.R.D. & Boulter, D. (1983) Nucl. Acids Res. 11, 2367.
Lycett, G. W. , Croy, R.R.D., Shirsat, A.H. & Boulter, D. (1984) Nucl. Acids Res. 12, 4493.
Mariani, С., de Beuckeleer, M., Truettner, J., Leemans, J., & Goldberg, R.B. (1990) Nature 347. 737.
Marsh, J.L., Erfle, M. & Wykes, E.J. (1984) Gene 32, 481.
Mettler, I.J. (1987) Plant Mol. Biol. Rep. 5, 346.
Okamura, J. K. , Jokufu, K.D. & Goldberg, R.B. (1986) Proc. Natl. Acad. Sci. USA 83, 8240.
Pang, P.P., Pruitt, R.E. & Meyerowitz, E.M. (1988) Plant Mol. Biol. 11, 805.
Potrykus, I. (1990) Bio/Technol. 8., 535.
Radke, S. E., Andrews, B.M., Moloney, M.M., Crough, M.L., Kridi, J.C. & Knauf, V.C. (1988) Theor. Appl. Genet. 75. 685.
Reilly, P. J. (1985) In: Starch Conversion Technology (Marcel Dekker, Inc., New York: Van Beynum, G.M.A. & Roels, J.A., eds.). Chapter 5, p. 101.
Riggs, С. D. , Hunt, D.C., Lin, J. & Chrispeels, M.J. (1989) Plant Sci. 63, 47.
Rodenburg, K.W., DeGroot, M.J.A., Schilperoort, R.A. & Hooykaas, P.J.J. (1989) Plant Mol. Biol., 13. 711.
Ryan, A.J., Royal, C.L., Hutchinson, J. & Shaw, C.H. (1989) Nucl. Acids Res. 17, 3584.
Scofield, S.R. & Crouch, M.L. (1987) J. Biol. Chem. 262. 12202.
Schilperoort, R. A., Hoekema, A. & Hooykaas, P.J.J. (1984) European Patent Application N 0120516.
Sengupta-Gopalan, С. , Reichert, N.A., Barker, R.F., Hall, T.C. & Kemp, J.D. (1985) Proc. Natl. Acad. Sci. USA 82. 3320.
Shimamoto, К. , Terada, R., Izawa, T. & Fujimoto, H. (1989) Nature 338, 274.
Shotwell, M. A. & Larkins, B.A. (1989) In: The biochemistry of plants Vol. 15 (Academic Press, San Diego: Stumpf, P.K. & Conn, E.E., eds.). Chapter 7. p. 297.
Sijmons, P.C., Dekker, B.M.M., Schrammeijer, B., Verwoerd, T.C., van den Elzen, P.J.M. & Hoekema, A. (1990) Bio/Technol. 8, 217.
Slightom, J. L., Schaber, M.D. & Kramer, R.A. (1986) In: Molecular biology of seed storage proteins and lectins (Waverley Press, Baltimore: Shannon, L.M. & Chrispeels, M.J., eds.) Am. Soc. Plant Physiol. p. 183.
Smith, J.J. & Raikhel, N.V. (1989) Plant Mol. Biol. 13., 601.
Vaara, Т. , Vaara, M., Simell, M., Lehmussaari, A. & Caransa, A. (1989) European Patent Application 0321004.
Vandekerckhove, J. , VanDamme, J., VanLijsebettens, M., Botterman, J., DeBlock, M>, DeClerq, A., Leemans, J., Van Montagu, M. & Krebbers, E. (1989) Bio/Technol. 7, 929.
van Gorcom, R.F.M., van Hartingsveldt, W., van Paridon, P.A., Veenstra, A. E. , Luiten, R. G.M., Selten, G.C.M. (1991) European Patent Application 89202436.5, Publication N 0420358, filed September 27, 1989.
Vasil, V., Redway, F. & Vasil, I. К. (1990) Bio/Technol. 8, 429.
Vitale, A. & Bollini, R. (1986) In: Molecular biology of seed storage proteins and lectins (Waverley Press, Baltimore: Shannon, L.M. & Chrispeels, M.J., eds.) Am. Soc. Plant Physiol. p. 175.
Voelker, T.A., Herman, E.M. & Chrispeels, M.J. (1989) Plant Cell 1, 95.
Vonder Haar, R.A., Alien, R.D., Cohen, E.A., Nessler, C.L. & Thomas, T. L. (1988) Gene 74, 433.
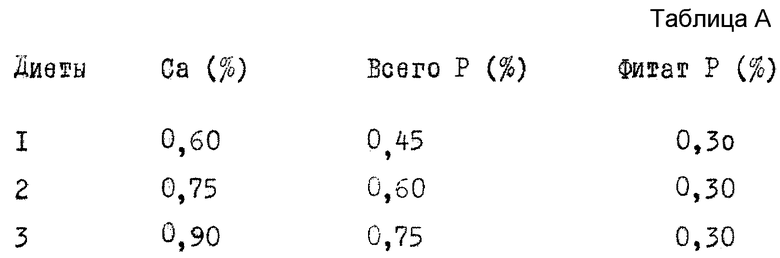


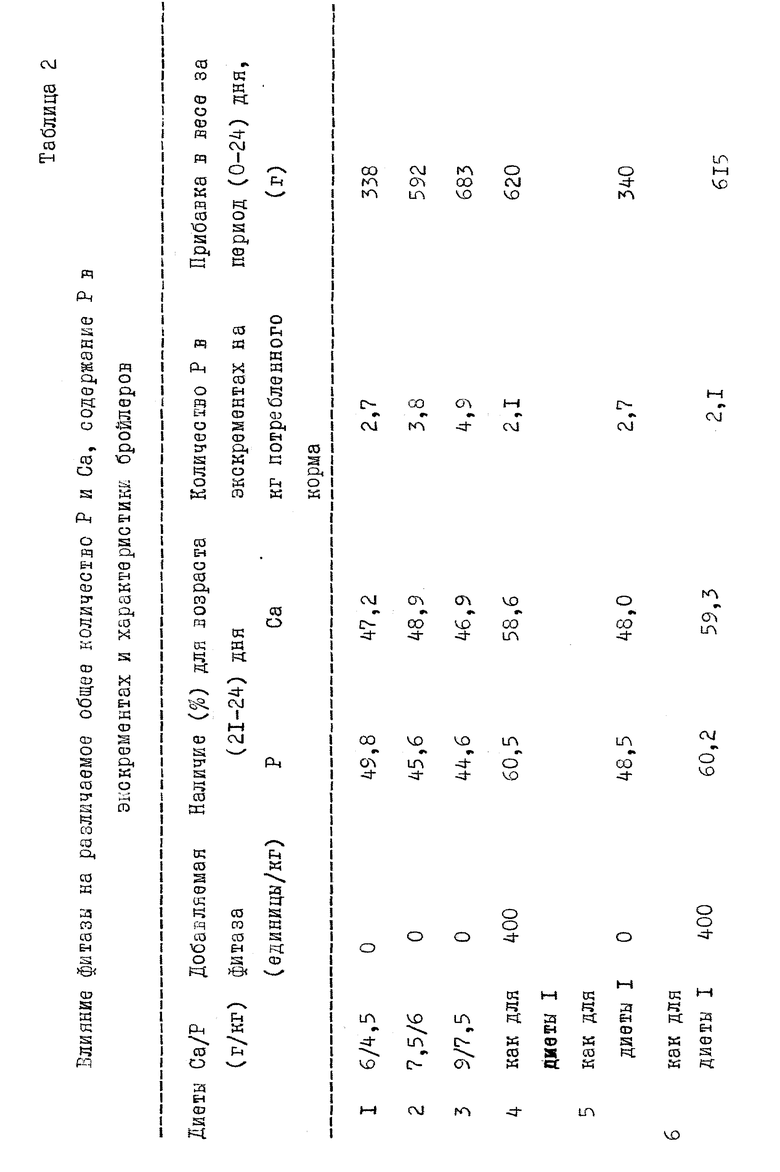

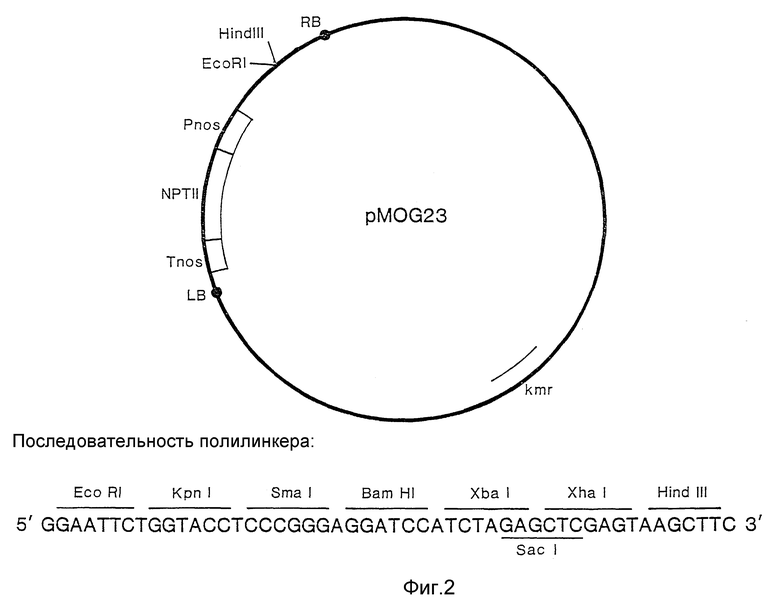



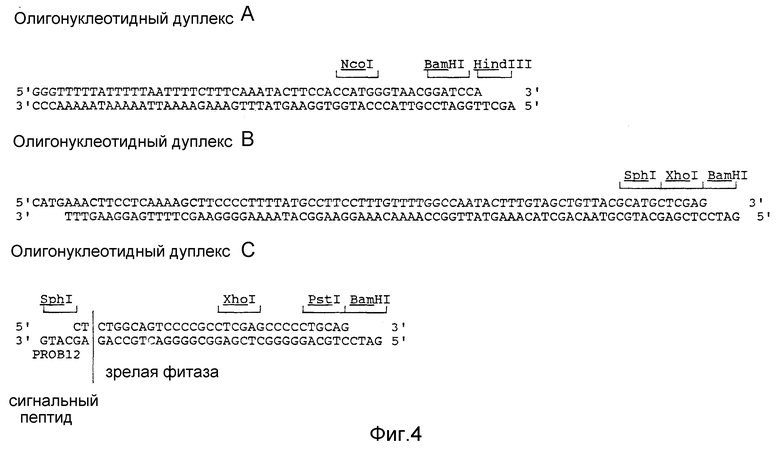
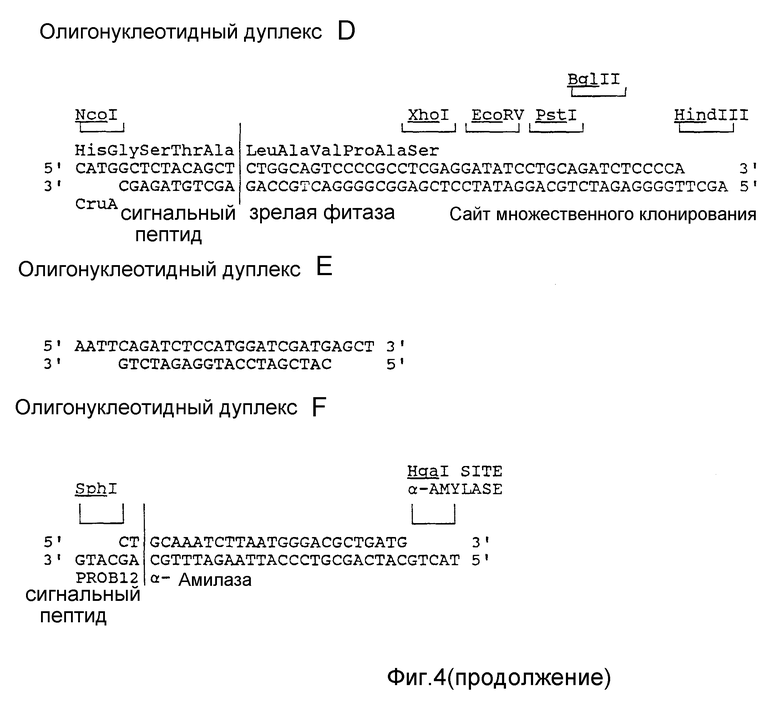
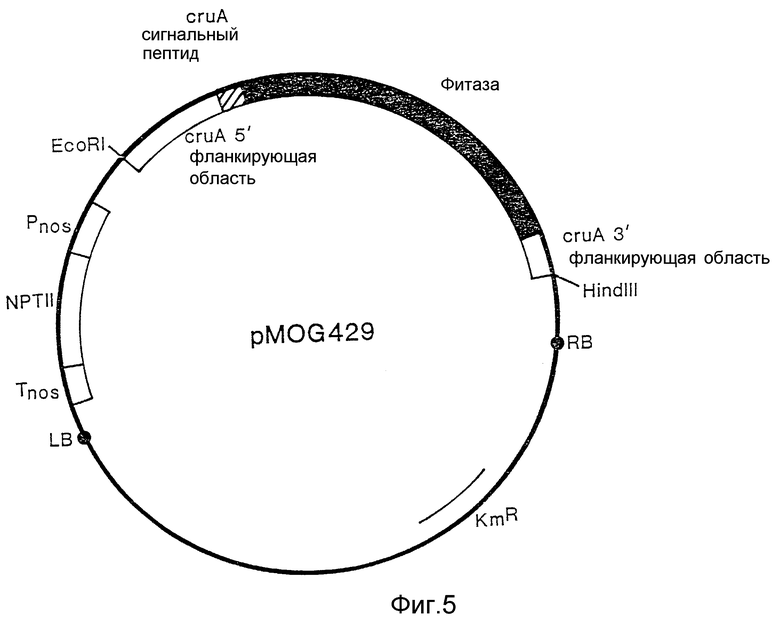
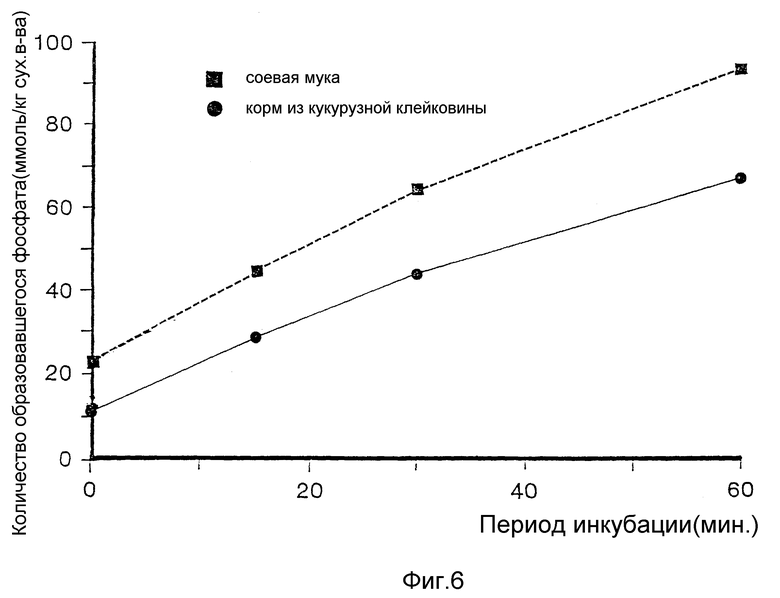


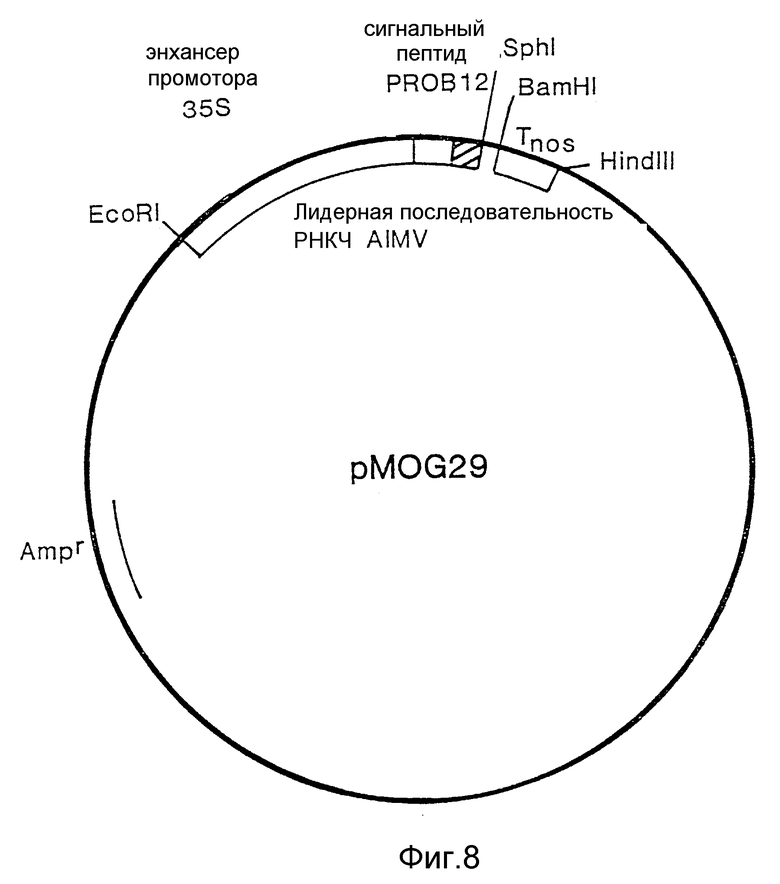
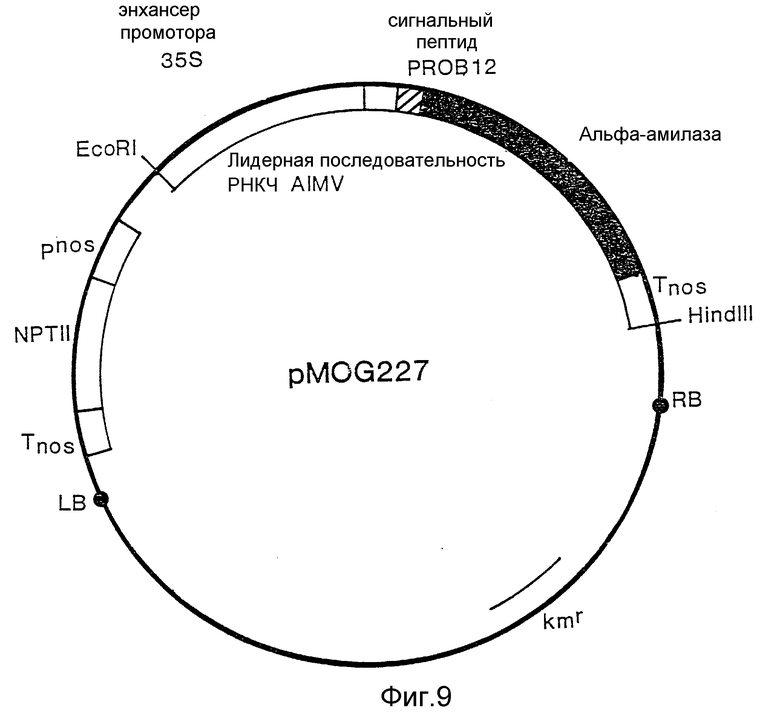
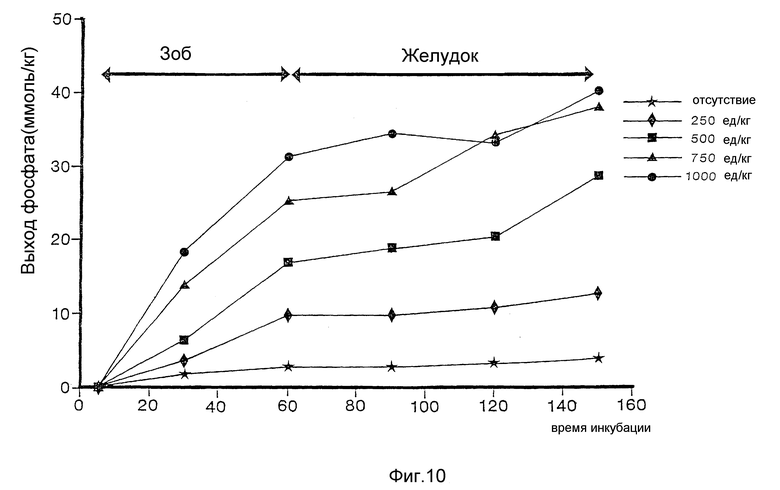
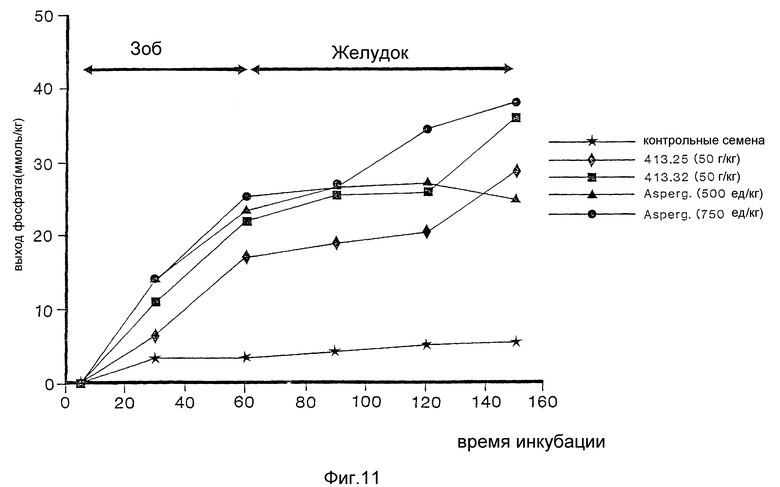
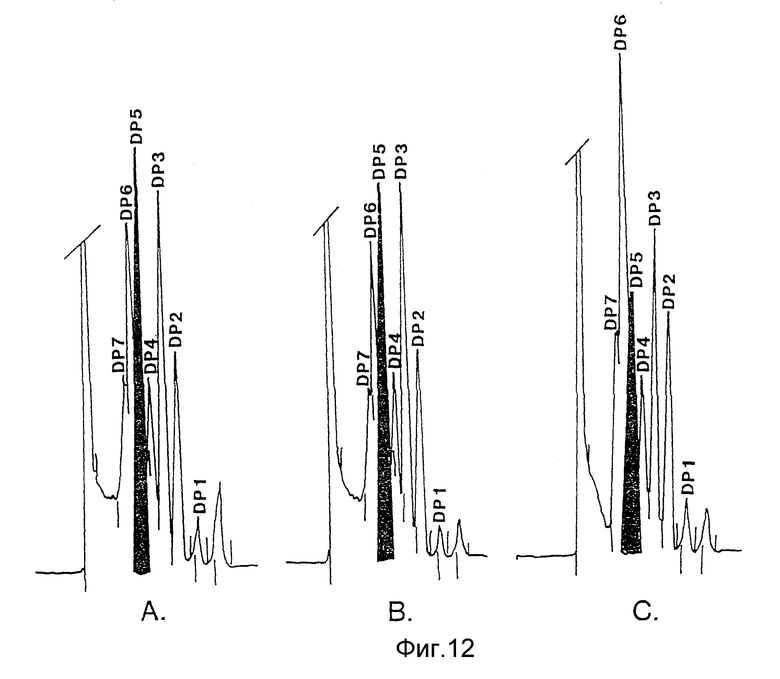
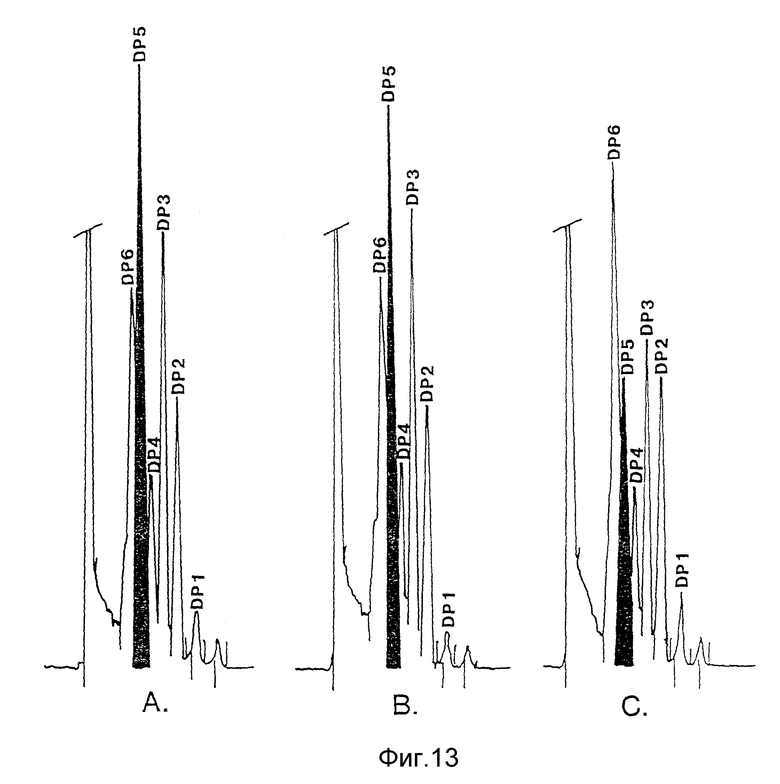
Изобретение может быть использовано в генетической инженерии для получения ферментов и в кормопроизводстве. Получают трансгенные растения и их семена добавляют в реагирующую смесь субстрата и фермента. Непосредственная добавка семян преимущественно в размолотом виде существенно снижает затраты на производство фермента за счет увеличения скорости ферментации, упрощения экстракции и очистки продукта. Форма продукта позволяет его использовать для лечения в виде пищевого рациона. Для получения трансгенных растений используют плазмиды. 5 с. и 11 з.п. ф-лы, 13 ил., 4 табл.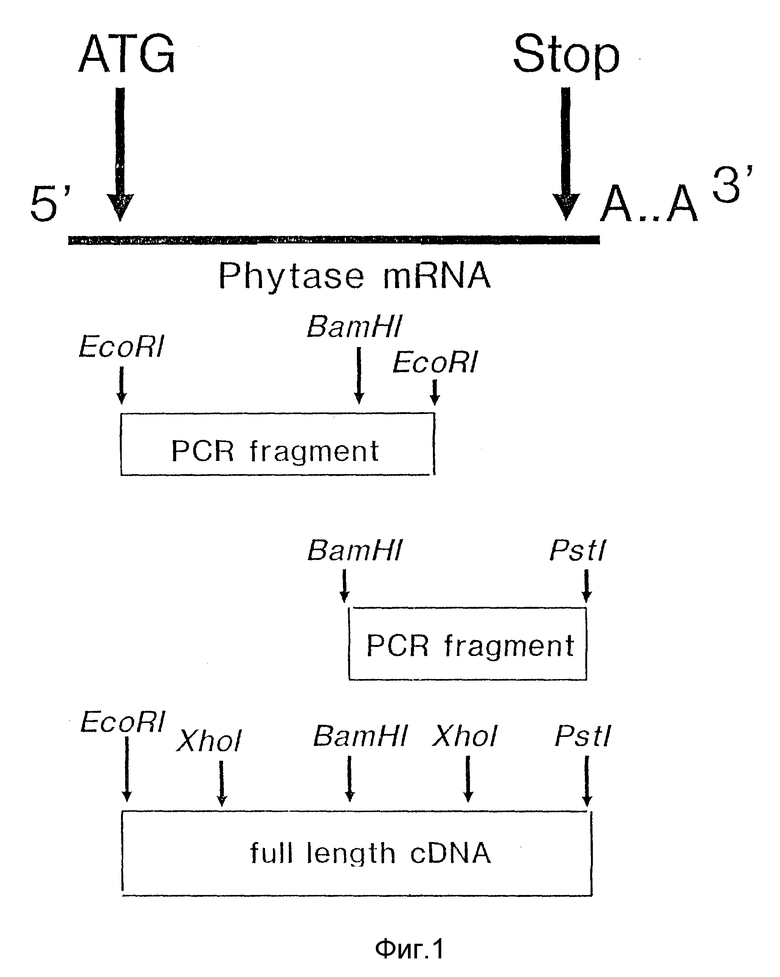
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| DD 275704 C, 30.01.90 | |||
| Брухман Э.Э | |||
| прикладная биохимия.-М.: Легкая и пищевая промышленность, 1981, с.152-164. | |||
Авторы
Даты
1999-04-27—Публикация
1991-03-25—Подача