Изобретение относится к органической химии, конкретно к способу получения 1,3-дигидро-7-нитро-5-фенил-2Н-1,4-бензодиазепин-2-она (нитразепама) формулы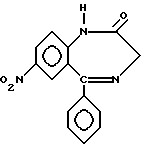
Нитразепам (Nitrazepamum) - психотропный лекарственный препарат, он оказывает успокаивающее действие на центральную нервную систему, обладает снотворным действием, вызывает мышечную релаксацию, обладает противосудорожной активностью.
Нитразепам относится к лекарственным препаратам из класса 1,4-бензодиазепин-2-онов, которые хорошо известны из уровня техники. Наиболее распространенный способ их получения заключается в синтезе 2-хлор- 5-нитробензофенона, обмене хлора на аминогруппу, получении 2-(2-хлор-ацетамидо-нитробензофенона с последующей его циклизацией с гексаметилентетрамином (a.с. N 550980, кл. C 07 D 243/16; пат. США 4155904, кл. 260-239, oпубл. 1977 г.).
Менее распространенным является способ получения 1,4-бензодиазепин-2-онов путем последовательного построения бензодиазепиновой структуры (например, из 2-хлор-5-нитробензофенона) с последующим окислением метиленовой группы до карбонильной.
Так, известен способ получения бензодиазепиновых соединений формулы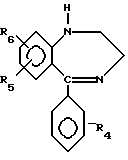
где R4; R5 и R6 выбраны из группы -H; Hal; CF3; NO2; NH2... (пат. США N 3222359, кл. 540-574, oпубл. 1965 г., авторы Reeder Е., Sternbach L.H.), включающий реакцию соединения формулы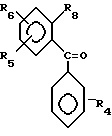
где R4; R5 и R6 указаны выше; R8 - галоген,
с соединением формулы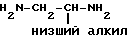
Синтез 2,3-дигидро-7-нитро-5-фенил-1Н-1,4-бензодиазепина (R4 и R6=H, R5= -NO2) осуществляют следующим образом: бензофенон, содержащий галоген в o-положении к C=O группе и активирующий электроотрицательный заместитель в положении 5 обрабатывают этилендиамином в среде пиридина при повышенной температуре (115-117oC). Затем растворитель отгоняют в вакууме, к остатку добавляют метанол, и сырой реакционный продукт отфильтровывают.
Выход целевого продукта в патенте не указан. Отмечено только, что добавочное количество продукта можно получить дополнительной обработкой фильтрата, выделив и подвергнув циклизации непрореагировавшие соединения с открытой цепью.
Недостатками способа являются трудоемкость выделения конечного продукта (вакуумная отгонка досуха смеси пиридина и этилендиамина, большие потери целевого продукта при высаживании метанолом), значительное количество примесей в конечном продукте, что вызывает необходимость дополнительной его очистки.
Способ получения 2,3-дигидро-7-нитро-5-фенил-1Н-1,4-бензодиазепина взаимодействием 2-хлор-5-нитробензофенона и этилендиамина в среде пиридина известен также из статьи (Sternbach L.Н., Reeder E., Archer G.A., J. Org. Chem. , 28, 3013-3016, 1963). Нагревание реакционной смеси приводит к нуклеофильному замещению атома хлора в бензофеноне и циклизации исходных реагентов в целевой продукт.
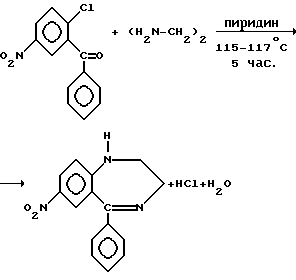
Способ осуществляют следующим образом. Раствор 960 г 2-хлор-5-нитробензофенона в смеси 2,0 л пиридина и 800 мл этилендиамина кипятят 5 ч. Растворитель отгоняют при атмосферном давлении, затем досуха под вакуумом.
После проведения реакции массу упаривают под вакуумом, и целевой продукт высаживают из остатка обработкой его метиловым спиртом. Выход 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина - 60%. Кислый гидролиз маточника с последующей обработкой кипящим пиридином приводит к получению добавочного количества целевого продукта до 30%. (После перекристаллизации из ацетона to пл= 211-212oC).
По мнению авторов статьи, проведение реакции циклизации в вышеуказанных условиях приводит к тому, что в реакционной массе образуются соединения формулы (основания Шиффа)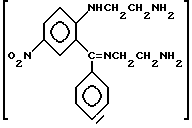
не выделенные в кристаллическом виде и образующие при гидролизе соединение формулы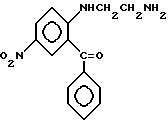
которое в свою очередь после циклизации в пиридине образует целевой продукт, что и обуславливает дополнительное повышение выхода на 30%.
Недостатками данного метода являются:
- недостаточно высокий выход целевого продукта;
- необходимость проведения дополнительных операций по выделению непрореагировавших соединений с открытой цепью, их гидролиз в кислой среде с последующим выделением и повторная циклизация в пиридине;
- трудоемкость выделения целевого продукта;
- значительное количество в конечном продукте примеси 2,2'-этилендиминобис (5-нитробензофенона) формулы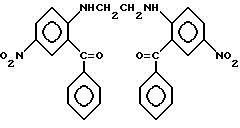
который очень устойчив в условиях кислого гидролиза (перекристаллизация из ацетона не понижает его содержание в конечном продукте);
- повышенная токсичность растворителей пиридина и метилового спирта;
- использование в процессе реакции высоких температур.
Полученный одним из вышеперечисленных методов 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин окисляют для получения 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она (нитразепама).
Известен способ получения (пат. США N 3247187, кл. 540-504, опубл. 1966 г., авторы Sternbach L.H., Fryer R.I.) соединений формулы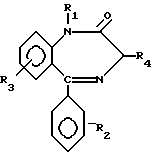
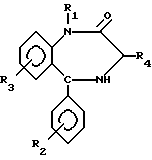
где R1 и R4 - H; низший алкил;
R2 и R3 - H; низший алкил, галоген, -NO2; -CF3,
включающий окисление агентом, содержащим кислород в комбинации с металлом с валентностью высшей, чем основная, выбранным из группы V, Cr, Mn, Pb соединений формулы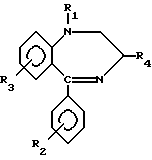
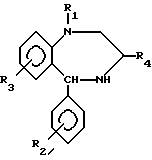
В патенте рассматривается возможность получения соединений, в том числе нитразепама окислением 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина "хроматным агентом" (CrO3-H2SO4) в среде ацетона или ледяной уксусной кислоты. Выход нитразепама не указан. Отмечено, что при проведении реакции окисления в ацетоне (также и в уксусной кислоте) выделено наряду с нитразепамом большое количество непрореагировавшего исходного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина.
Недостатками данного способа являются низкий выход целевого продукта, загрязнение его значительным количеством примесей, удаление которых возможно только путем хроматографического разделения полученной смеси веществ.
За прототип принят способ получения нитразепама, приведенный в статье "Хиназолины и 1,4-бензодиазепины. Окисление хромовой кислотой производных 1,4-бензодиазепина" (Sternbach L.Н. и др., J. Org. Chem., 30, p. 1308-1310, 1965).
В данной статье приведена схема получения различных производных 1,4-бензодиазепин-2-онов, в том числе нитразепама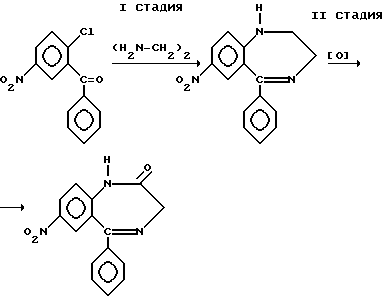
Что касается первой стадии процесса получения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина взаимодействием 2-хлор-5-нитробензофенона с этилендиамином в среде пиридина, то авторы делают отсылку к своей предыдущей работе, где подробно описан этот процесс (Sternbach L.Н. и др., J. Org. Chem., 28, p. 3013-3016, 1963).
2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин получают обработкой 2-хлор-5-нитробензофенона этилендиамином в среде пиридина с последующим кипячением смеси при 115-117oC в течение 5 ч. Выход целевого продукта - 60%. Кислый гидролиз маточника и последующая его обработка кипящим пиридином позволяет получить еще 30% целевого вещества (см. выше).
Полученный по этому способу 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин окисляют "хроматным агентом" в среде ацетона при 56oC в течение 1 ч. В качестве "хроматного агента" используют соединение шестивалентного хрома - окиси хрома в концентрированной серной кислоте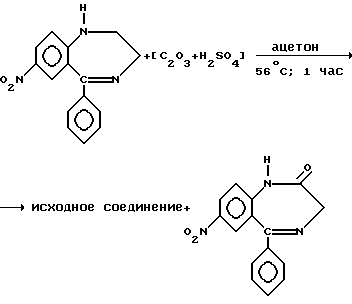
Процесс проводят следующим образом: 1,0 г 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина добавляют в 250 мл специально очищенного ацетона, затем в раствор дозируют 0,936 мл заранее приготовленного "хроматного агента" (CrO3-H2SO4). Мольные соотношения реагирующих компонентов составляют 1: 910:0,334:1,41 соответственно.
Смесь нагревают и кипятят при 56oC 1 ч в атмосфере сухого азота. Затем в реакционную массу добавляют 1,5 л холодной воды, экстрагируют полученную смесь продуктов хлороформом. Далее экстракт промывают, сушат и отгоняют хлороформ.
Перекристаллизация остатка из метанола приводит к осаждению желтых кристаллических призм исходного продукта (2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина) в количестве 0,75 г (возврат 75%). Перекристаллизация оставшегося продукта из эфира приводит к получению 25 мг (выход 2,4%) целевого нитразепама - кристаллов белого цвета с зеленоватым отливом. Следует отметить, что схожесть химических структур исходного и целевого продуктов приводит к невозможности их полного разделения методом кристаллизации.
Недостатками способа-прототипа являются:
на стадии синтеза 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина:
- недостаточно высокий выход целевого продукта (до 90% и только при условии проведения дополнительных операций - выделения непрореагировавших соединений с открытой цепью, их гидролиза и повторной циклизации в пиридине);
- повышенная токсичность растворителей пиридина и метилового спирта;
- значительное количество трудноудаляемых примесей в конечном продукте, главным образом 2,2'-этилендииминобис (5-нитробензофенона);
на стадии окисления 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина:
- низкий выход нитразепама, большое количество примесей в нем;
- сложность и трудоемкость выделения нитразепама из реакционной массы;
- большой расход растворителей и реагентов (для получения 1 кг нитразепама необходимо израсходовать более 1000 л только ацетона, не учитывая хлороформ, метанол, эфир);
- использование высоких температур при проведении реакции;
- опасность работы с таким соединением шестивалентного хрома, как CrO3.
Недостатки, присущие обеим стадиям получения 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она (нитразепама), делают этот процесс нетехнологичным и как следствие непригодным для организации промышленного производства.
В основу настоящего изобретения положена техническая задача разработки промышленного способа получения 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она (нитразепама), который отличался бы технологичностью, доступным сырьем, позволял бы получить конечный продукт с высоким выходом без трудноудаляемых примесей.
Поставленная техническая задача достигается двумя вариантами.
По первому варианту поставленная техническая задача достигается тем, что в способе получения 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она (нитразепама), заключающемся в обработке 2-хлор-5-нитробензофенона этилендиамином в среде органического растворителя для получения 2,3-дигидро-7-нитро-5- фенил-1H-1,4-бензодиазепина и последующем его окислении в целевой продукт соединениями хрома шестивалентного в концентрированной серной кислоте в среде растворителя, согласно изобретению для получения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина в качестве органического растворителя используют изопропиловый спирт, окисление полученного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина проводят в среде ацетона или ацетонитрила, при этом в качестве соединений хрома шестивалентного используют насыщенный водный раствор бихромата натрия (калия) при следующем мольном соотношении компонентов 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия (калия) : концентрированная серная кислота : ацетон или ацетонитрил 1 : (0,92-1,02) : (7,5-8,5) : (72-76), а процесс окисления проводят при температуре 18-20oC. После образования конечного продукта смесь солей отфильтровывают, суспендируют в воде, обрабатывают раствором щелочи до pH=3,0-3,5, выпавший нитразепам отфильтровывают.
Сущность изобретения заключается в следующем.
2-хлор-5-нитробензофенон обрабатывают этилендиамином в среде растворителя изопропилового спирта (ИПС)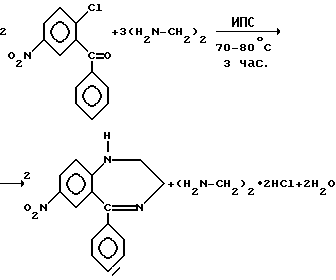
К изопропиловому спирту добавляют этилендиамин, смесь нагревают до 70oC, нагрев отключают. При интенсивном перемешивании дозируют 2-хлор-5-нитробензофенон в течение 1 ч при температуре 70-75oC.
После окончания дозировки реагентов дают выдержку 3 ч при температуре 70-80oC. Затем к реакционной массе прибавляют воду, выдерживают 1 ч при кипении, охлаждают до 10-15oC и фильтруют. Получают 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин с выходом 98%, to пл= 210-212oC.
В отличие от прототипа на этой стадии используют растворитель ИПС, который обеспечивает не только хорошую растворимость в нем реагирующих веществ, но и протекание реакции циклизации в нужном направлении с выделением конечного продукта с высоким выходом непосредственно из реакционной массы. Конечный продукт не требует дополнительной очистки, что очень существенно при получении фармакопейного нитразепама.
При взаимодействии 2-хлор-5-нитробензофенона с этилендиамином могут протекать следующие реакции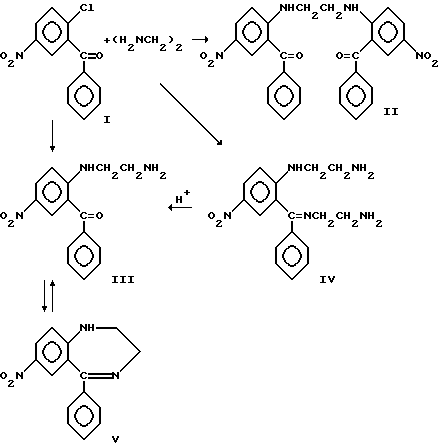
При недостаточном количестве этилендиамина происходит преимущественное образование диарилпроизводного II. При избытке этилендиамина образуются значительные количества оснований Шиффа IV, для перевода которых в целевую структуру необходим кислый гидролиз. И только образование продукта III позволяет получить целевую бензодиазепиновую структуру V. Проведение реакции по этому пути требует одновременно и создания оптимальных условий для реакции циклизации (для предотвращения побочных реакций продукта с открытой цепью). Необходимо учитывать и значительный тепловой эффект реакции нуклеофильного замещения атома хлора, что на фоне индукционного эффекта приводит к невозможности контролировать температуру и преобладанию побочных реакций.
Проведение реакции циклизации в среде ИПС в указанных условиях позволяет обойти все эти ограничения. Эндо-эффект при растворении 2-хлор-5-нитробензофенона ИПС компенсирует экзо-эффект проходящих химических реакций без значительного индукционного периода только в этом температурном интервале, что резко снижает вероятность протекания побочных реакций с образованием соединений II и IV.
Использование в качестве растворителя ИПС, проведение реакции циклизации при температуре 70-80oC, с последующим разбавлением водой позволяeт получить непосредственно из реакционной массы с количественным выходом целевой продукт практически без примесей. Следует отметить, что попытка заменить в реакции ИПС на ацетонитрил, метанол, этанол приводит к образованию значительного количества соединений структуры II, а на ацетон - к основаниям Шиффа.
Выделенный из реакционной массы 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин обрабатывают окислительной смесью насыщенный водный раствор Na2Cr2O7(K2C2O7) - концентрированная H2SO4 в среде растворителя ацетона или ацетонитрила при температуре 18-20oC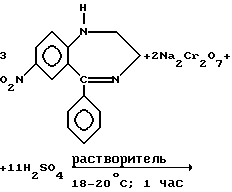
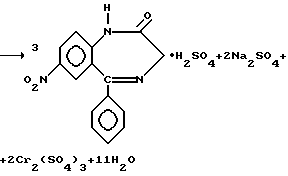
По окончании реакции реакционную массу сливают на вакуум-воронку и отфильтровывают смесь солей. Осадок суспендируют в воде, полученный раствор нейтрализуют до pH= 3-3,5, выпавший осадок отжимают и сушат. Выход 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она - 90-93%, содержание основного вещества - 99,9-99,95%.
В отличие от прототипа для обеспечения максимального выхода целевого продукта в предлагаемом способе в качестве растворителя используют ацетон или ацетонитрил, в качестве соединений шестивалентного хрома - насыщенный водный раствор Na2Cr2O7 (K2C2O7), причем его вводят в реакцию в три раза больше, чем необходимо по формальной стехиометрии, а процесс окисления проводят при 18-20oC.
Использование насыщенного раствора Na2Cr2O7 (или K2C2O7 - в данном способе для достижения технической задачи они абсолютно равнозначны) позволяет проводить реакцию окисления в нужном направлении из-за соотношения растворимостей исходного и конечного продукта в достаточно кислых растворах.
Кроме того, использование насыщенного раствора соли шестивалентного хрома, не снижая окислительной способности Cr+6, гораздо безопаснее, чем использование CrO3.
Проведение реакции в среде ацетона и ацетонитрила обусловлено тем, что они хорошо смешиваются с водой. Благодаря этому факту образующиеся при реакции неорганические соли переходят в маточник, а сульфат 2,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она выпадает в осадок. Выводя из зоны реакции нитразепам, ацетон и ацетонитрил способствуют сдвигу реакции в сторону образования конечного продукта. Далее осадок промывают водой, суспендируют в ней, обрабатывают до pH=3-3,5. При этом нитразепам остается в осадке, а сульфосоль исходного продукта переходит в раствор. Отфильтровав осадок и промыв его водой, получают целевой продукт.
Для протекания реакции окисления предпочтительны следующие мольные соотношения реагирующих компонентов: исходный 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия (калия) : серная кислота : ацетон или ацетонитрил 1 : (0,92-1,02) : (7,5-8,5) : (72-76). Данное соотношение реагентов является оптимальным.
Уменьшение количества растворителя приводит к увеличению вязкости реакционной массы и загрязнению целевого продукта исходным, а повышение приводит к уменьшению выхода. Уменьшение количества окислителя - соединений хрома и серной кислоты - приводит к накоплению в продуктах реакции исходного бензодиазепина из-за его неполного окисления, а увеличение приводит к образованию комплекса исходного бензодиазепина и хромовой кислоты, выпадающего в осадок, что также приводит к накоплению в продуктах реакции исходного продукта. Следует отметить, что несоблюдение соотношения по серной кислоте дополнительно приводит к образованию нерастворимых продуктов исходного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина с хромовой кислотой, что приводит к прекращению реакции в нужном направлении. Повышение температуры проведения реакции при данных соотношениях компонентов выше 18-20oC приводит к снижению выхода целевого продукта, уменьшение температуры технологически невыгодно и намного замедляет скорость протекания процесса окисления.
Данное изобретение по варианту 1 иллюстрируется следующими примерами конкретного выполнения.
Пример 1.
В аппарат с рубашкой и мешалкой заливают 100 л (1307 моль) изопропилового спирта и дозируют 25,0 (374 моль) этилендиамина, массу нагревают до 70oC и отключают нагрев. При интенсивном перемешивании дозируют 25,0 кг (95,54 моль) 2-хлор-5-нитробензофенона в течение 1 ч при поддержании температуры реакционной массы 70-75oC.
После окончания дозировки дают выдержку 3 ч при температуре 78-80oC, к реакционной массе приливают 200 л воды, нагретой до температуры 75-80oC, дают выдержку при этой температуре 1 ч, затем реакционную массу охлаждают до 10-15oC, выпавший осадок отфильтровывают, промывают водой, сушат. Вес полученного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина - 25,03 кг (98%), to пл = 210-212oC. По результатам потенциометрического титрования содержание основного вещества 99,90-99,95%.
В аппарат с рубашкой и мешалкой заливают 20 л (272,04 моль) ацетона. Включают охлаждение. При перемешивании приливают 1,7 л (31,81 моль) серной кислоты. Затем дозируют в течениe 1 ч 1 кг (3,74 моль) 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина и насыщенный раствор бихромата натрия, приготовленного заранее из 1 кг (3,82 моль) Na2Cr2O7 0,6 л (33,30 моль) воды при температуре не выше 20oC (предпочтительно 18-20oC).
По окончании дозировки реакционную массу выдерживают 1 ч при перемешивании и температуре не выше 20oC, затем сливают на вакуум-воронку и отфильтровывают выпавший осадок.
Отжатый на воронке осадок загружают в аппарат с мешалкой в 20 л воды, перемешивают. Полученную суспензию нейтрализуют раствором щелочи до pH=3-3,5, затем сливают ее на вакуум-воронку и фильтруют. Отфильтрованный осадок промывают водой, отжимают, сушат.
Выход полученного нитразепама 0,947 кг (90%), to пл = 226-228,5oC.
Мольное соотношение реагентов на этой стадии 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия : серная кислота : ацетон 1 : 1,02 : 8,50 : 72,7.
Это соотношение реагентов является предпочтительным при использовании ацетона в качестве растворителя. Контроль за содержанием примесей показывает отсутствие примеси исходного вещества. Содержание основного вещества 99,9%.
Пример 2.
Получение 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина проводят аналогично примеру 1. Выход целевого продукта 98%, to пл = 210-212oC. Затем в аппарат с рубашкой и мешалкой заливают 15 л (283,92 моль) ацетонитрила, включают охлаждение и при перемешивании приливают 1,5 л (28,06 моль) концентрированной H2SO4. При температуре не выше 20oC засыпают 1 кг (3,74 моль) 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина и после полного его растворения дозируют в течение 1 ч насыщенный раствор бихромата Na или К в воде (0,9 кг Na2Cr2O7 + 0,54 л H2O). Дают выдержку в течение 1 ч при перемешивании и температуре реакционной массы не выше 20oC.
Реакционную массу сливают на вакуум-воронку и отфильтровывают выпавший осадок, загружают в аппарат в 20 л H2O, перемешивают. Полученную суспензию нейтрализуют раствором щелочи до pH=3-3,5, сливают на вакуум-воронку и фильтруют. Отфильтрованный осадок промывают водой, сушат. Выход полученного нитразепама 0,979 кг (93%). Мольное соотношение реагентов на этой стадии 1: 0,92: 7,50: 75,9. Контроль на содержание примесей показывает их отсутствие, to пл = 226-228,5oC.
Пример 3.
Последовательность операций и количественное соотношение аналогично примеру 2, за исключением количества бихромата натрия, добавленного на стадии окисления. Зависимость выхода нитразепама от мольного соотношения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия приведена в табл. 1.
Пример 4.
Последовательность операций и количественное соотношение аналогично примеру 2, за исключением количества растворителя, используемого на стадии окисления. Зависимость выхода нитразепама от мольного соотношения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : растворитель приведена в табл. 2.
Пример 5.
Последовательность операций и количественное соотношение аналогично примеру 1, за исключением количества серной кислоты, используемой на стадии окисления. Зависимость выхода нитразепама от мольного соотношения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : серная кислота приведена в табл. 3.
По второму варианту поставленная техническая задача достигается тем, что в способе получения 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она (нитразепама), заключающемся в обработке 2-хлор-5-нитробензофенона этилендиамином в среде органического растворителя для получения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина и последующем его окислении в целевой продукт соединениями хрома шестивалентного в концентрированной серной кислоте в среде растворителя, согласно изобретению для получения 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина в качестве органического растворителя используют изопропиловый спирт, окисление полученного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина проводят в водной среде, при этом в качестве соединений хрома шестивалентного используют насыщенный водный раствор бихромата натрия (калия) при следующем мольном соотношении компонентов 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия (калия) : концентрированная серная кислота : вода 1 : (0,80-0,84) : (14-16) : (44-45), а процесс окисления проводят при температуре 18-20oC. После образования конечного продукта смесь солей отфильтровывают, суспендируют в воде, обрабатывают раствором щелочи до pH=3,0-3,5, выпавший нитразепам отфильтровывают.
Сущность изобретения по варианту 2 заключается в использовании в качестве соединений шестивалентного хрома насыщенного водного раствора бихромата натрия (калия), проведении процесса окисления при 18-20oC и использовании в качестве растворителя воды.
Первую стадию - получение 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин - осуществляют взаимодействием 2-хлор-5-нитробензофенона с этилендиамином в среде ИПС аналогично варианту 1. Выход целевого продукта 98%, to пл= 210-212oC.
Полученный 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин обрабатывают окислительной смесью состава Na2Cr2O-H2SO4 (K2Cr2O7-H2SO4) в среде растворителя - воды.
По окончании реакции массу сливают на вакуум-воронку, выпавшие сульфатные соли отделяют от маточника, суспендируют в воде. Затем полученную массу обрабатывают водным раствором щелочи до pH=3-3,5, выпавшие кристаллы целевого продукта отжимают и сушат. Выход 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она - 92-93%.
В данном способе в качестве растворителя используют воду. Как и в способе по первому варианту, выводя целевой продукт в виде его сульфосоли из зоны реакции, она способствует сдвигу реакции в сторону образования конечного продукта. Использование в качестве окислителя насыщенного раствора Na2Cr2O7 (K2Cr2O7)-H2SO4 обусловлено теми же соображениями, что и в способе по варианту 1.
Для протекания реакции окисления необходимо применять следующие мольные соотношения реагирующих компонентов - исходный 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия (калия) : серная кислота : вода 1 : (0,80-082) : (14-16) : (44-45). Данное соотношение реагентов является оптимальным.
Уменьшение количества растворителя приводит к увеличению вязкости реакционной массы и загрязнению целевого продукта исходным, а повышение приводит к уменьшению выхода. Уменьшение количества окислителя - соединений хрома и серной кислоты - приводит к накоплению в продуктах реакции исходного бензодиазепина из-за его неполного окисления, а увеличение приводит к образованию комплекса исходного бензодиазепина и хромовой кислоты, выпадающего в осадок, что также приводит к накоплению в продуктах реакции исходного продукта. Следует отметить, что несоблюдение соотношения по серной кислоте дополнительно приводит к образованию нерастворимых продуктов исходного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина с хромовой кислотой, что приводит к прекращению реакции в нужном направлении. Повышение температуры проведения реакции при данных соотношениях компонентов выше 18-20oC приводит к снижению выхода целевого продукта, уменьшение температуры технологически невыгодно и намного замедляет скорость протекания процесса окисления.
Изобретение по варианту 2 иллюстрируется следующими примерами конкретного исполнения.
Пример 6.
В аппарат с рубашкой и мешалкой заливают 100 л (1307 моль) изопропилового спирта и дозируют 25,0 (374 моль) этилендиамина, массу нагревают до 70oC и отключают нагрев. При интенсивном перемешивании дозируют 25,0 кг (95,54 моль) 2-хлор-5-нитробезофенона в течение 1 ч при поддержании температуры реакционной массы 70-75oC.
После окончания дозировки дают выдержку 3 ч при температуре 78-80oC, к реакционной массе примешивают 200 л воды, нагретой до температуры 75-80oC, дают выдержку при этой температуре 1 ч, затем реакционную массу охлаждают до 10-15oC, выпавший осадок отфильтровывают, промывают водой, сушат. Вес полученного 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепина - 25,03 кг (98%), to пл - 210-212oC. По результатам потенциометрического титрования содержание основного вещества 99,90-99,95%.
В аппарат с рубашкой и мешалкой заливают 2,5 л (138,74 моль) воды. Включают охлаждение и при перемешивании приливают 3 л (56,13 моль) 96% H2SO4. Приливают раствор бихромата натрия в воде (0,8 кг Na2Cr2O7 (3,05 моль) и 0,5 кг H2O (27,75 моль)). Дозируют равномерно в течение 1 ч 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин при температуре не выше 20oC. После окончания дозировки выдерживают реакционную массу в течение 1 ч при перемешивании при температуре 20oC. Далее процесс выделения проводят аналогично примеру 2.
Мольное соотношение реагентов на этой стадии 2,3-дигидро-7-нитро-5-фенил-1H-1,4-бензодиазепин : бихромат натрия : серная кислота : вода 1 : 0,82 : 15 : 44,5. Получают 0,968 кг нитразепама (выход 92%).
Предлагаемый способ позволяет получить как по варианту 1, так и по варианту 2 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензо-диазепин-2-он с высоким выходом, практически не содержащий примесей, после фармакопейной его очистки получают лекарственный препарат нитразепам. Использование в качестве растворителя ацетона, ацетонитрила или воды в указанных пределах определяется только возможностями предприятия-изготовителя.
Нитразепам представляет собой светло-желтый с зеленоватым отливом кристаллический порошок без запаха. Он практически не растворим в воде, мало растворим в спиртах, эфире, умеренно растворим в хлороформе.
Таким образом, разработанный способ получения 1,3-дигидро-7-нитро-5-фенил-2H-1,4-бензодиазепин-2-она, характеризующийся совокупностью предлагаемых стадий проведения процесса, их последовательностью и количественным соотношением реагентов, позволяет
- организовать промышленное производство нитразепама на базе доступного химического сырья и стандартизированного технологического оборудования;
- повысить выход целевого продукта, упростить процесс его выделения, снизить количество примесей в нем.
Способ может найти применение в химической и фармацевтической промышленности для получения лекарственных препаратов из ряда 1,4-бензодиазепинонов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА НИТРАЗЕПАМА-1,3-ДИГИДРО-5-ФЕНИЛ-7- НИТРО-2Н-1,4-БЕНЗОДИАЗЕПИН-2-ОНА | 1996 |
|
RU2136285C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-БЕНЗОДНАЗЕПИНОНА-2 ИЛИ ИХ СОЛЕЙ | 1970 |
|
SU417948A3 |
| ПРОИЗВОДНЫЕ 4-АРИЛ-6-АМИНО-НИКОТИНОВОЙ КИСЛОТЫ И ИХ СОЛИ | 1995 |
|
RU2154635C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АМИНО-5-НИТРОБЕНЗОФЕНОНА | 1992 |
|
RU2061678C1 |
| Способ получения 2-ациламинометил-1Н-2,3-дигидро-1,4-бензодиазепинов или их солей присоединения кислот | 1980 |
|
SU1253430A3 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ АРИТМИИ | 1994 |
|
RU2155587C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2,3-ДИГИДРО-1Я-1,4-БЕНЗОДИАЗЕПИНА | 1972 |
|
SU337991A1 |
| Способ получения производных 1-полифторалкил-1,4-бензодиазепина | 1971 |
|
SU437295A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ЭТИЛГЕКСИЛНИТРАТА НЕПРЕРЫВНЫМ МЕТОДОМ | 2004 |
|
RU2259348C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3-АЦИЛАМИНО-5-ФЕНИЛ-1,4-БЕНЗОДИАЗЕПИН-2-ОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРОМЕЖУТОЧНЫЙ ПРОДУКТ | 1995 |
|
RU2142948C1 |


Описывается способ получения 1,3-дигидро-7-нитро-5-фенил-2Н-1,4-бензодиазепин-2-она путем взаимодействия 2-хлор-5-нитробензофенона с этилендиамином в среде органического растворителя при нагревании с последующим окислением полученного 2,3-дигидро-7-нитро-5-фенил-1Н-1,4-бензодиазепина соединением шестивалентного хрома в концентрированной серной кислоте в среде растворителя и выделением целевого продукта, при этом взаимодействие-2-хлор-5-нитробензофенона с этилендиамином осуществляют в изопропиловом спирте при 70-80°С, окисление 2,3-дигидро-7-нитро-5-фенил-1Н-1,4-бензодиазепина проводят в среде ацетона или ацетонитрила при 18-20°С насыщенным водным раствором бихромата натрия (калия) при мольном соотношении компонентов 2,3-дигидро-7-нитро-5-фенил-1Н-1,4-бензодиазепин : бихромат натрия (калия) : концентрированная серная кислота : ацетон или ацетонитрил 1 : (0,92-1,02) : (7,5-8,5) : (72-76), а выделение целевого продукта осуществляют отделением осадка от реакционной массы и обработкой последнего в водной среде раствором щелочи до рН 3,0-3,5. Технический результат - повышение технологичности и выхода целевого продукта. 2 c.п. ф-лы, 3 табл.
| SU, 359819, 1973 | |||
| SU, 550980, 1977 | |||
| SU, 650505, 1979 | |||
| J.Org | |||
| Chem | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| J.Org | |||
| Chem | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
Авторы
Даты
2000-06-10—Публикация
1998-01-06—Подача