Изобретение относится к защите стальных деталей, машин, конструкций сооружений, эксплуатируемых в водно-солевых средах (замкнутые системы охлаждения, технологические среды химических и других производств, резервуары для хранения углеводородных топлив), а также в почвах и морской воде, от коррозионного разрушения под воздействием среды и бактериальных клеток сульфатредуцирующих бактерий (СРВ) и предотвращения (уменьшения) водородного охрупчивания конструкций и деталей машин, выполняющих ответственные в них функции, и таким образом, нацелено на то, чтобы повышать их надежность и долговечность.
Известны ингибиторы наводороживания стали [1], применяемые в кислой среде в процессе катодной обработки, однако, недостатком этого ингибитора является то, что он не обладает биоцидными свойствами по отношению к СРБ.
Наиболее близким к изобретению по технической сущности и достигаемому результату является ингибитор, состоящий из серусодержащих бис-четвертичных солей, соответствующий формуле (N+ CH2CH2)2 Z2X-, где N - четвертичная аминогруппа; Z - серусодержащая группа, например S, SO, SO2; X- - анион [2]. Однако данный известный ингибитор не предохраняет металл, корродирующий под действием СРБ от водородного охрупчивания.
Целью данного изобретения является способ применения ингибитора коррозии, сочетающего в себе одновременно свойства биоцида и ингибитора наводороживания стали. Указанная цель достигается тем, что используются соединения общей формулы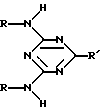
где R: -CH3; -CH2-CH3; -CH2-CH2-CH3; 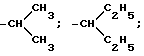
R': -H; -Cl; -Br; -S-CH3.
Введение таких ингибиторов в количестве 5-15 мМоль/л позволяет предотвратить коррозию и наводороживание стали в водно-солевых средах в присутствии сульфатредуцирующих бактерий.
Введение в молекулу триазинов линейных и/или разветвленных алкильных заместителей, обладающих электронодонорным характером, приводит к увеличению электронной плотности на атомах азота, непосредственно связанных с кольцом триазана и на самом кольце, что в свою очередь отражается в упрочнении адсорбционной связи таких молекул с поверхностными атомами стали, корродирующей в водно-солевой среде.
В соответствии с представлением физической органической химии увеличение длины алкильной цепи заместителя от - СН3 до -C3H7 повышает электронную плотность на реакционном центре. Однако дальнейшее ее удлинение такого действия не оказывает. Поэтому предложенные нами соединения ограничиваются кругом заместителей, указанных в формуле изобретения.
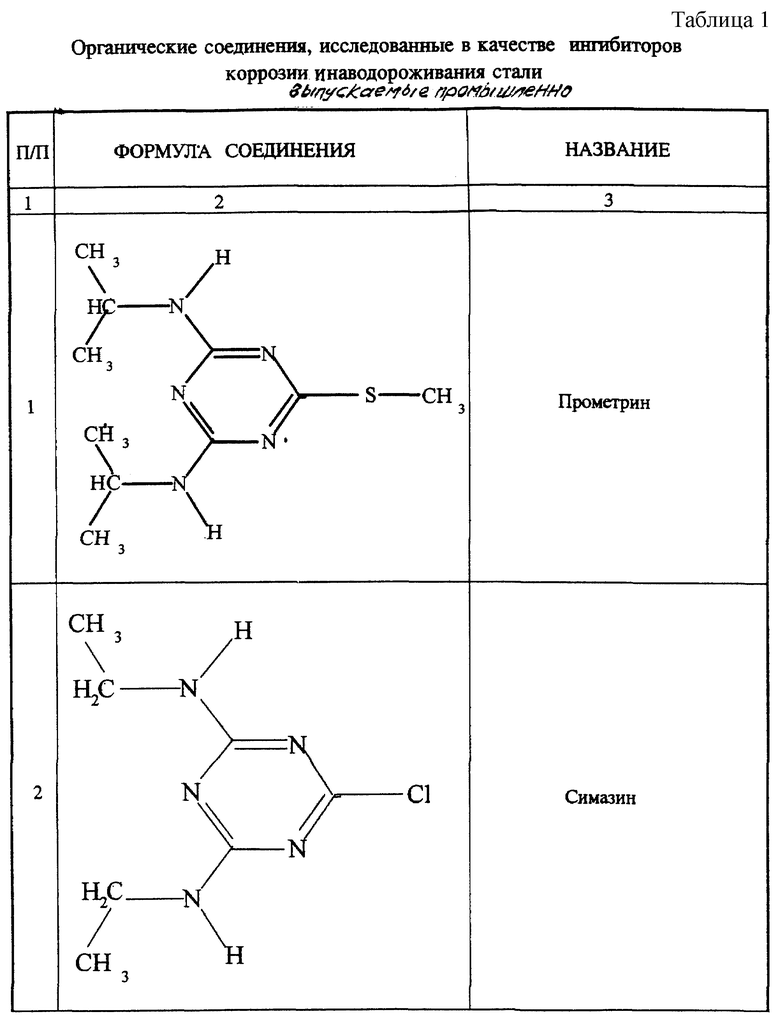
Некоторые из исследованных нами веществ легко доступны, так как производятся промышленно - прометрин, симазин и зеазин, были рекомендованы и нашли применение для борьбы с сорной растительностью (табл. 1).
Из строения молекулы прометрина следует, что в орто- и параположениях у атома азота кольца находятся три заместителя, оказывающих электронодонорное действие. Группа -SCH3 оказывает электроноакцепторное влияние, но атом серы передает лишь частично на бензольное кольцо электронную плотность от заместителя -CH3 (эффект "сульфидного мостика"). Способность адсорбироваться на металле и образовывать защитную пленку обеспечивается активностью адсорбционных центров - гетероатомов азота кольца и связанных с ним двух групп - NH. Следовательно, у прометрина должна проявиться высокая "кроющая способность" поверхности стали. У симазина и зеазина Cl оказывает некоторое смягчающее действие. Симазин имеет также два неразветвленных этиламинорадикала, оказывающих электронодонорное воздействие на систему сопряженных связей, увеличивая адсорбционную активность гетероатомов на поверхности металла.
Для испытания производных триазина использовали их растворы в водно-солевой среде Портгейта "Б" состава, приведенного в табл. 2, в 1 мл которой содержалось 4,0 • 107 мл-1 клеток СРБ.
CPB являются анаэробной культурой, то есть растворенный в среде кислород вызывает их переход в латентное состояние.
Коррозионные процессы на стали изучали гравиметрическим, потенциометрическим и потенциостатическим методами.
Наблюдения за жизнедеятельностью СРБ велись путем учета численности микроорганизмов нефелометрическим методом. Концентрацию сульфатного остатка определяли иодометрическим титрованием по калибровочному графику. Величины pH и редокс-потенциала сред определяли потенциометрически. Содержание водорода определяли методом послойного растворения стальных образцов.
Сущность метода заключается в определении убыли концентрации растворенного в электролите кислорода, взаимодействующего в присутствии платинового катализатора с выделяющимся при анодном растворении водородом. Концентрацию растворенного в электролите кислорода до и после анодного растворения определяли фотометрически по методу Ковальцева и Алесковского с применением в качестве реагента на кислород сафранина T.
После подготовки поверхности образец изолировали так, чтобы рабочая поверхность составляла 1,8 см2. Затем образец анодно растворяли при строго поддерживаемой плотности тока D ± 0,02 A/см2 (1 = 0,36 мА). Пробы анолита отбирали через каждые 20 минут и заполняли кювету. Добавляя 0,4 мл лейкосафранина, перемешивали раствор в кювете. Измеряли оптическую плотность и по результатам измерений определяли содержание водорода в растворенном слое металла по графику, полученному на основании формулы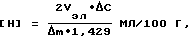
где Vэл - объем электролита, мл;
1,429 - масса 1 мл O2, мг;
Δm - масса растворенного слоя металла, мг;
ΔC - изменение концентрации кислорода в анолите после растворения поверхностного слоя, по сравнению с концентрацией кислорода в анолите до растворения.
Толщину слоя адсорбированного водорода определяли по формуле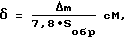
где Δm - масса растворенного слоя металла, г;
S - площадь стального образца, см2;
d = 7,8 г/cм3 - плотность стали.
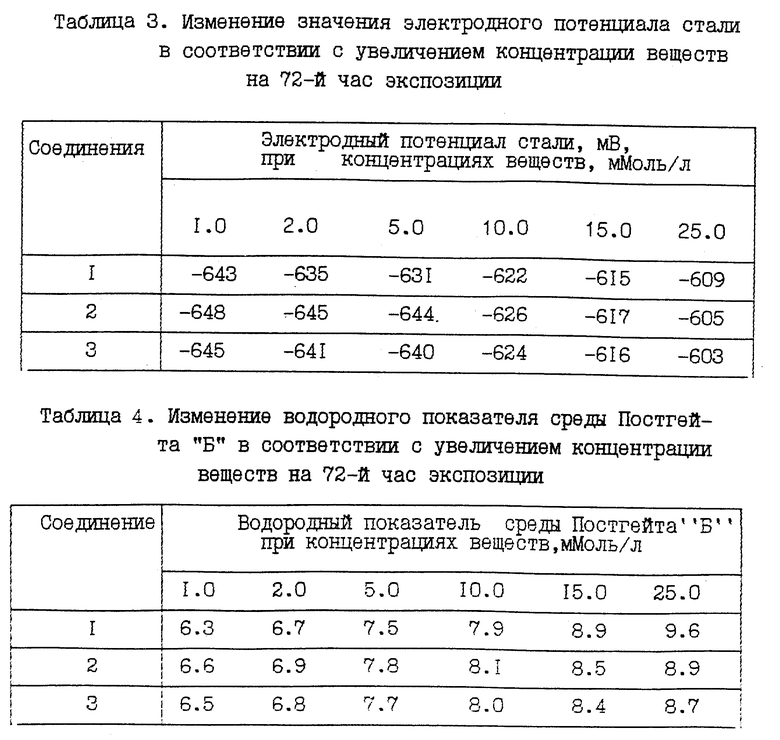
При изучении изменения значений электродного потенциала (ϕ) стали через одни сутки после введения в коррозионную среду заявляемых веществ установлено его резкое облагораживание значений на несколько десятков милливольт, причем оно, как правило, тем сильнее, чем больше концентрация органических веществ. Так, прометрин приводит к смещению ϕ не более 80 мВ. В присутствии всех органических веществ после резкого облагораживания ϕ наблюдается его постепенное смещение в отрицательную сторону обычно на несколько десятков милливольт и после 6 суток экспозиции ϕ принимает практически постоянное значение. Из триазинов наибольшее смещение ϕ вызвал прометрин, а наименьшее - симазин (табл. 3).
Спустя сутки после введения органических веществ наблюдали смещение значений водородного показателя (pH) среды в сторону слабокислотных значений по сравнению с контрольной серией. Прометрин вызывает наибольшее смещение pH от 8,4 до 5,8 при С = 1,0 мМоль/л, а при больших концентрациях (С = 10,0 мМоль/л и С = 15,0 мМоль/л) до значений 6,9-7,2. В дальнейшем, начиная с пятых суток экспозиции, во всех случаях, кроме прометрина, зеазина и симазина, в присутствии исследованных органических веществ pH монотонно смещался в сторону щелочных значений. Происходит подщелачивание среды. Наиболее активное смещение pH среды в щелочную область наблюдали в средах с прометрином (табл.4).
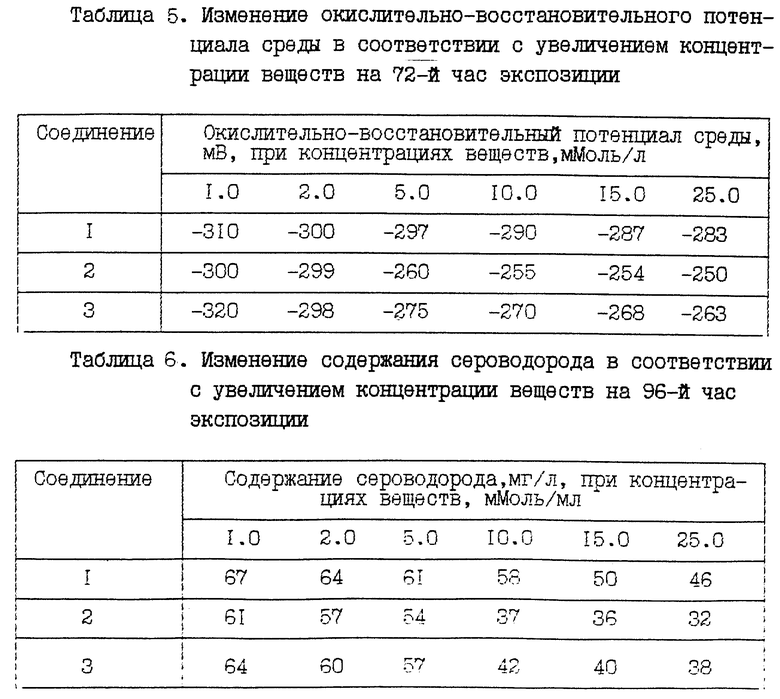
В ходе работы производилось измерение окислительно-восстановительного потенциала коррозионной среды (Eh), значения которого на 4-е сутки после инокуляции среды смещались в сторону положительных значений, и тем сильнее, чем больше концентрация органических веществ. Затем, начиная с 5-х суток эксперимента значения, Eh незначительно смещались в сторону более отрицательных значений. Причем наиболее электроотрицательные значения Eh наблюдались в присутствии прометрина (табл. 5).
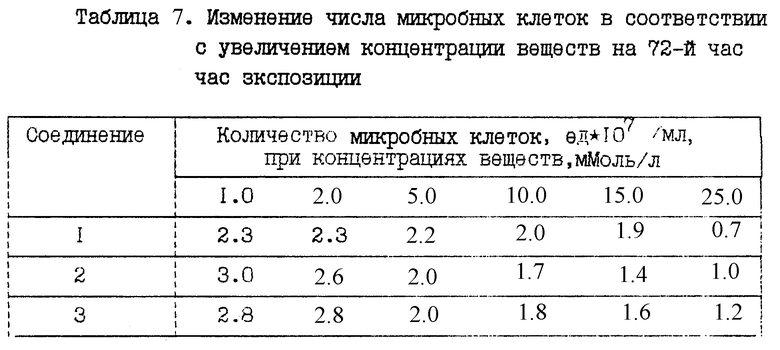
При определении концентрации сероводорода отмечено наименьшее содержание основного метаболита бактерий в случае такого органического соединения, как прометрин (табл. 6). Он приводит и к значительному уменьшению числа бактериальных клеток (табл. 7).
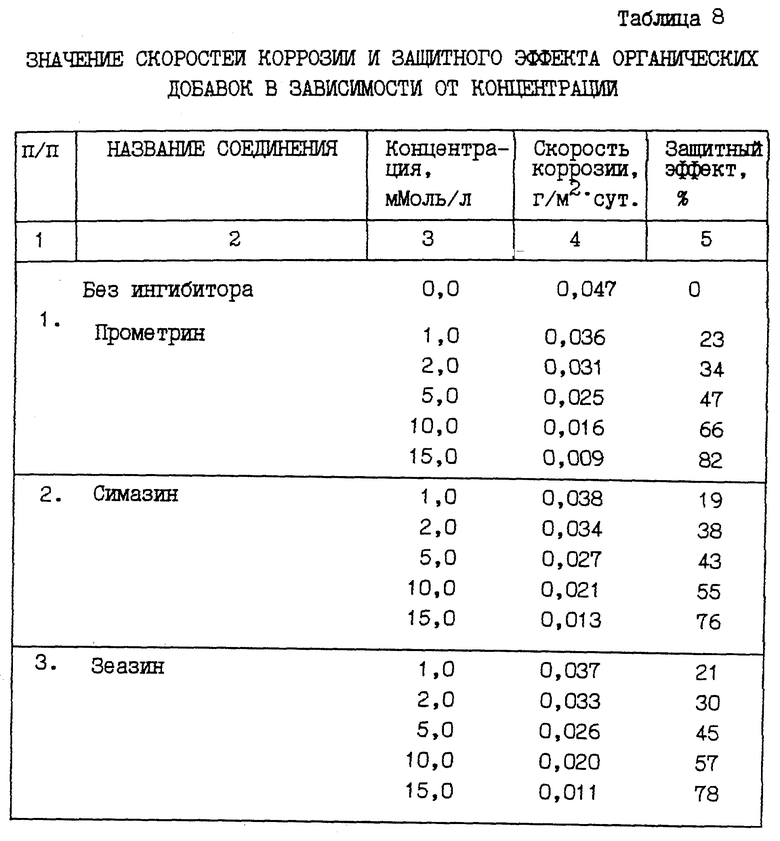
При обобщении экспериментальных данных по влиянию органических добавок на скорость коррозии стали в присутствии СРБ замечено, что соединения, показавшие себя как вещества с лучшими ингибирующими и биоцидными свойствами, снижали скорость коррозии до двух раз по сравнению с контрольной серией (табл. 8).
При рассмотрении зависимости содержания водорода в приповерхностных слоях стали от концентрации органических веществ наглядно видно преимущественное накопление поглощенного водорода в относительно тонком приповерхностном слое стали (10-15 мкм).
Так, на фиг. 1 представлены результаты послойного растворения образцов стали Ст. 3, корродировавшей в среде с СРБ в присутствии прометрина, симазина и зеазина. Водород концентрируется в слое 10-15 мкм. Замечено, что с увеличением концентрации ингибитора уменьшается содержание водорода в приповерхностном слое стальных образцов (фиг.1).
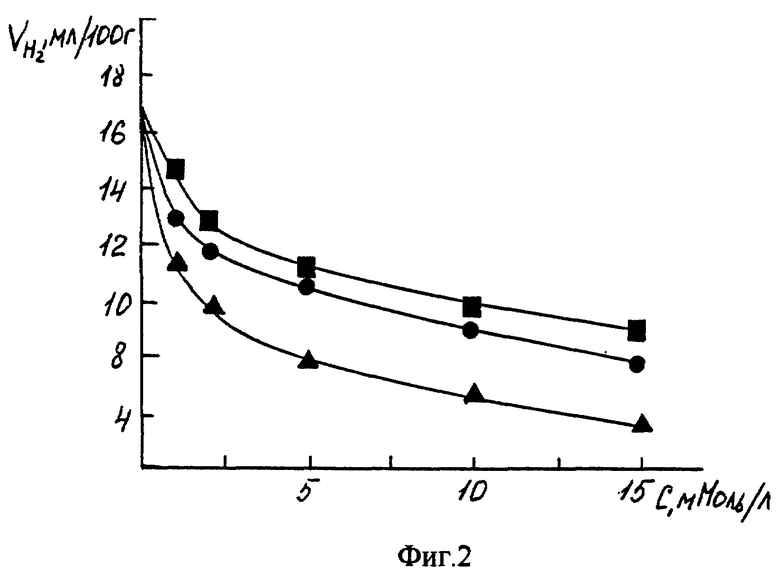
Можно отметить, что с увеличением концентрации ингибитора содержание водорода в приповерхностном слое стали 30 мкм уменьшается. Об эффективности ингибитора можно судить по количеству адсорбированного сталью водорода. При рассмотрении зависимости интегрального содержания водорода в приповерхностных слоях стали от концентрации ингибиторов в коррозионной среде обнаружено, что триазины являются очень эффективными ингибиторами наводороживания и лучшим из них - прометрин. Интегральное водородосодержание в его присутствии составило 10,7-5,2 мл/100 г при концентрациях 1-15 мМоль/л (фиг. 2). При введении в коррозионную среду данных органических веществ происходит резкое уменьшение интегрального водородосодержания в приповерхностном слое стали, которое продолжается и при увеличении Cинг до 2 мМоль/л. Затем уменьшение интегрального водородосодержания становится менее резким, интегральное водородосодержание находится в прямой зависимости от Cинг.
Замечено, что в отсутствии ингибиторов объем абсорбированного водорода линейно возрастает со скоростью коррозионного разрушения стали. В присутствии всех ингибиторов коррозии, обладающих бактерицидными свойствами, во всем исследованном интервале скоростей коррозии объем поглощенного сталью водорода в меньшей степени зависит от скорости коррозии. Обнаружено, что между объемом Hаб и скоростью коррозии для всех ингибиторов существует зависимость.
Связь между количеством бактерий и водородосодержанием стали, корродировавшей в присутствии исследуемых органических веществ, позволила судить о бактерицидном действии органических соединений. Так, при рассмотрении соотношения между бактерицидным и ингибирующим наводороживанием действием симазина, зеазина и прометрина (фиг. 3) при C = 1 мМоль/л лучшим бактерицидным свойством обладает прометрин, который также является лучшим ингибитором наводороживания, а худшим ингибитором наводороживания является симазин, который и худший биоцид. При 2 и 5 мМоль/л бактерицидное действие добавок одинаково, а при 10 и 15 мМоль/л происходят некоторые изменения. Теперь лучшим бактерицидным действием обладает симазин, который является худшим ингибитором наводороживания, а худшим бактерицидом оказывается прометрин, который лучше ингибирует наводороживание стали.
Во всех случаях применения органических соединений скорость коррозии закономерно уменьшалась с увеличением их концентрации в коррозионной среде. А в присутствии лучшего ингибитора - прометрина скорость коррозии снижалась на 84% (при Cинг = 15,0 мМоль/л) по сравнению с контрольной серией. При этом величина защитного эффекта для прометрина составляла 66% (Cинг =10,0 мМоль/л) и 82% (Cинг = 15,0 мМоль/л). Незначительно ниже величина защитного эффекта зеазина Z = 78% (С = 15,0 мМоль/л) и симазина Z = 76% (табл.6).
Исследования триазинов проводили при концентрациях в среде С = 1,25 мМоль/л, но учитывая высокую эффективность заявляемых веществ, из экономических соображений целесообразно применение их в качестве ингибиторов коррозии и наводороживания стали при средних концентрациях внутри указанного интервала.
Перечень фигур
Фиг. 1. Распределение водорода по глубине стальных образцов в зависимости от концентрации ингибитора (мМоль/л): • - коррозионная среда без добавки; • - С=1,0; Δ - С=2,0; □ - C = 5,0; о-C = 10,0; а - Доб.1; б - Доб.2; в - Доб.3.
Фиг. 2. Влияние концентрации добавок на интегральное водородосодержание в приповерхностном слое стали 30 мкм: Δ - прометрин; о - симазин; □ - зеазин.
Фиг. 3. Связь между количеством бактерий, сохранивших свою жизнедеятельность спустя 48 ч после введения ингибитора и интегральным содержанием водорода, абсорбированного сталью в процессе коррозии: □ - симазин; о - зеазин; Δ - прометрин.
Цифры у точек соответствуют концентрации ингибитора (мМоль/л).
Литература
1. Авторское свидетельство СССР N 503942, кл. С 25 F 3/06, 1975.
2. Патент США, N 4057390, P.M. Quinlan, Nov. 8, 1977.




Изобретение относится к защите стальных деталей, машин, конструкций и сооружений, эксплуатируемых в водно-солевых средах (замкнутые системы охлаждения, технологические среды химических и других производств, резервуары для хранения углеводородных топлив), а также в почвах и морской воде, от коррозионного разрушения под воздействием среды и бактериальных клеток сульфатредуцирующих бактерий и предотвращения (уменьшения) водородного охрупчивания конструкций и деталей машин, выполняющих ответственные в них функции. В качестве ингибиторов микробиологической коррозии и наводороживания стали в водно-солевой среде, содержащей сульфатредуцирующие бактерии, применяются производные триазина, сочетающие в себе свойства ингибиторов коррозии и наводороживания стали в количестве 5-15 мМоль/л и общей формулы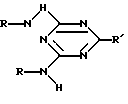
где R - -CH3; -CH2-CH3; -CH2-CH2-CH3; 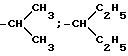
R' - -H; -Cl; Br; -S-CH3.
Таким образом достигаются повышение их надежности и долговечности и в конечном итоге экономия металла и уменьшение загрязнения среды продуктами коррозии. 7 табл., 3 ил.
Способ защиты от коррозии и наводороживания стали в водно-солевых средах, содержащих сульфатредуцирующие бактерии, путем введения ингибиторов, отличающийся тем, что в качестве ингибиторов используют производные триазина в количестве 5 - 15 мМоль/л общей формулы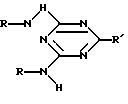
где R- -CH3, -CH2-CH3, -CH2-CH2-CH3, 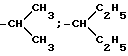
R' - -H, -Cl, -Br, -S-CH3\
| US 4057390 A, 08.11.1977 | |||
| Механизированная установка для очистки отливок | 1973 |
|
SU511163A1 |
| US 4830827 A, 16.05.1989 | |||
| РЕАГЕНТ ДЛЯ ПОДАВЛЕНИЯ РОСТА СУЛЬФАТВОССТАНАВЛИВАЮЩИХ БАКТЕРИЙ И ПРЕДОТВРАЩЕНИЯ СЕРОВОДОРОДНОЙ КОРРОЗИИ | 1989 |
|
SU1839779A3 |
Авторы
Даты
2000-06-27—Публикация
1997-09-03—Подача