Изобретение относится к защите деталей, машин, конструкций и сооружений из кадмированных углеродистых и низколегированных сталей, которые по условиям эксплуатации контактируют с водными растворами солей, кислот, с промышленными и хозяйственно-бытовыми сточными водами, морской водой, а также увлажненными почвами. В этих случаях на поверхности стали с Cd-покрытием часто складываются анаэробные условия, способствующие развитию сульфатредуцирующих бактерий (СРБ). Специфичность коррозионной среды, формируемой при участии СРБ состоит в том, что они выделяют в нее сероводород и органические кислоты. Эти продукты метаболизма СРБ сильно ускоряют коррозионное разрушение как тонкого электрохимически нанесенного Cd - покрытия, так и стали после ее обнажения хотя бы на отдельных участках поверхности, а сероводород является к тому же еще и сильным стимулятором абсорбции водорода сталью, приводящей к выраженному проявлению водородной хрупкости стали, которая проявляется тем сильнее, чем больше содержание углерода в ней, то есть чем выше уровень прочности стали.
Из описания к патенту РФ №2279455 известно «Применение МоО3 в качестве ингибитора коррозии и композиции для покрытия, содержащие такой ингибитор коррозии», МПК C09D 5/08, заявл. 2001.11.12, опубл. 2004.12.10. Данный ингибитор применяют в качестве агента для усиления антикоррозионных свойств композиции для антикоррозионного покрытия на основе дисперсного металла. По мнению авторов, подобный ингибитор позволяет улучшить стойкость композиции к воздействию солевого тумана.
Однако данный ингибитор недостаточно эффективен в водонефтяных средах, содержащих сероводород.
Наиболее близким к предложенному изобретению по технической сущности и достигаемому результату является ингибитор коррозии в водонефтяных сероводородсодержащих средах, включающий смесь производных карбоновых кислот [авт. свид. №1202291, МКИ С23F 11/00, 1995 г.]. Однако данный известный ингибитор не предохраняет сталь от водородного охрупчивания, возникающего при абсорбции водорода приповерхностными слоями металла.
Целью данного изобретения является применение ингибитора коррозии, сочетающего в себе свойства биоцида и ингибитора наводороживания стали одновременно.
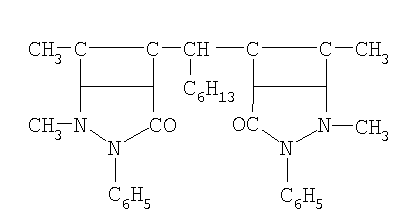
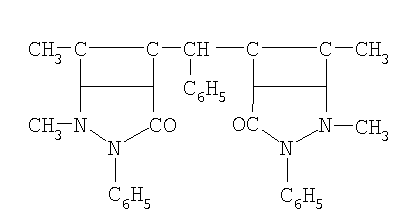
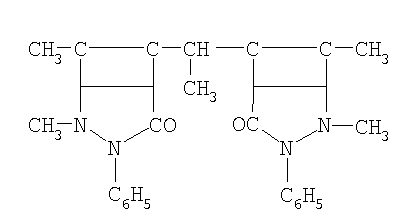
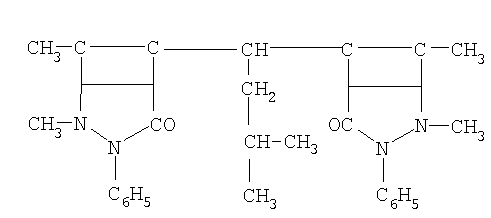
Указанная цель достигается тем, что в качестве ингибиторов коррозии кадмированной, в их присутствии, стали в водно-солевой среде, содержащей сульфатредуцирущие бактерии применяются производные антипирина, включенные в электроосадок кадмия, общей формулы:
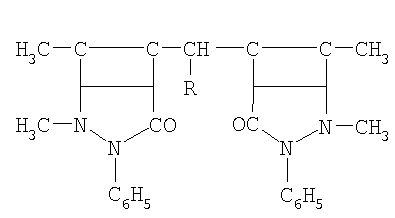
где R: -Н; -СН3; -С2Н5; -С3Н7; -С4Н9; -С5Н11; -С6Н5; -С6Н13.
Технический результат - улучшение коррозионной стойкости стали с кадмиевым покрытием, с включенными в него в процессе электроосаждения производными антипирина, к воздействию сульфатредуцирующих бактерий в водно-солевой среде.
Для исследования ингибирующего коррозию действия были выбраны соединения - производные антипирина (таблица 1). Антипирин является производным гетероциклического соединения - пиразола. Несмотря на наличие пятичленного кольца с двумя атомами азота, пиразол и его гомологи относятся к высокопрочным соединениям.
Диантипирилметан-4,4'-метилен-бис-(1,2-дигидро-1,5-диметил-2-фенил-3-пиразолон) (ДАМ) - типичное слабое двухосновное основание. Реакция протона с ДАМ даже в слабокислой среде касается обеих карбонильных групп. Образует комплексы со многими металлами состава: [MeDAMn]Xm, а также ионные
Органические соединения, исследованные в качестве ингибиторов микробиологической коррозии кадмированной в разных режимах стали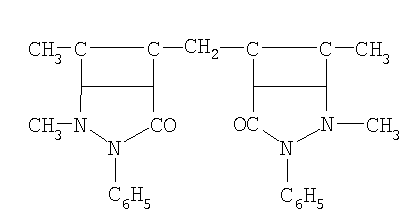
ассоциаты (DAMH)n-m[MeX]n, где Me - металл, X - однозарядный анион, m - степень окисления металла. Высокая эффективность предлагаемого ингибитора подтверждается следующим образом: при использовании производных диантипирилметана в качестве ингибитора коррозии и наводороживания стали в водно-солевых средах имеет место образование адсорбционных связей между молекулами ингибитора и поверхностными атомами Cd-покрытия и Fe-стали, которое носит хемосорбционный характер и сила этой связи зависит от электронной плотности на гетероатомах молекулы, а также от взаимодействия π-электронов ароматических колец с металлической поверхностью.
Кроме того, заявленные органические соединения в кислых средах ведут себя как катионактивные. При попадании в водно-солевую среду в результате разрушения Cd-покрытия они частично (в большей или меньшей степени - в зависимости от рН среды и рК-соединения) диссоциируют с образованием органических катионов. Поверхность углеродистых сталей в коррозионной среде, формирующейся в результате жизнедеятельности СРБ, из-за образования сульфидных мостиков приобретает обычно отрицательный заряд. Это создает предпосылки для электростатического взаимодействия (электросорбции) частиц ингибитора в катионной форме с поверхностью стали, обнажающейся после растворения Cd-покрытия с анодных участков локальных коррозионных элементов.
Синтез азотсодержащего соединения (диантипирилметана) осуществляют следующим образом: 500 г антипирина растворяют в 1 л 0.1 М серной кислоты, приливают 250 мл 35-40%-ного раствора формалина (профильтрованного через бумажный фильтр) и нагревают прикрытый часовым стеклом стакан на водяной бане (таблица 2). После начала выделения кристаллов продолжают нагревание еще 30-40 мин, затем охлаждают реакционную смесь и отфильтровывают выделившийся продукт на воронке Бюхнера. После промывки водой осадок отжимают и для более полной очистки, в основном, от формалина переносят в стакан, заливают 800-900 мл дистиллированной воды, добавляют 4-5 мл концентрированного раствора аммиака и нагревают на водяной бане при периодическом перемешивании в течение 2 часов. После охлаждения и фильтрования обработку дистиллированной водой, но без добавления аммиака повторяют, нагревая на водяной бане 2 часа. Отфильтрованный, промытый еще раз на воронке Бюхнера водой и тщательно отжатый реагент высушивают на воздухе или в термостате при 80-90°С. Для ускорения высушивания можно пропустить через находящийся на воронке реагент небольшую порцию диэтилового эфира. Полученный продукт обычно не требует дополнительной очистки и может быть применен в анализе. Выход количественный. В некоторых случаях при высушивании в термостате или длительном хранении (особенно, если в атмосфере содержится значительное количество диоксида серы) реагент может слегка пожелтеть. В этом случае его следует растворить в 0.25 М растворе серной кислоты, снова осадить разбавленным аммиаком и повторить операцию очистки (нагревание с водой и фильтрование).
Условия синтеза различных R-диантипирилметанов
Для испытания заявляемых соединений в качестве коррозионной среды использовали водно-солевую среду, обеспечивающую как интенсивное развитие СРБ, так и высокую скорость коррозионного разрушения Cd-покрытия и стальной основы (таблица 3).
Состав коррозионной среды
СРБ являются анаэробной культурой, то есть растворенный в среде кислород вызывает переход бактериальных клеток в латентное состояние. Для устранения посторонней микрофлоры и создания анаэробных условий, необходимых для жизнедеятельности СРБ, среду стерилизовали кипячением, затем инокулировали накопительной культурой СРБ, полученной многократным пересевом пробы, отобранной из природного источника. Сульфатредуцирующие бактерии были культивированы в виде чистой культуры на среде Постгейта «Б». В момент загрузки образцов 1 мл такой среды содержал 3,9·107 клеток сульфатредуцирующих бактерий рода Desulfovibrio.
В предварительно простерилизованные при Т=433К в течение 1,5 ч стеклянные пробирки с 100 мл коррозионной среды и 2 мл чистой культуры сначала помещали плоские образцы 50×20×1,5 мм стали марки Ст.3. Образцы перед внесением в среду шлифовали тонкой шкуркой на полотне, обезжиривали ацетоном, облучали под ртутно-кварцевой лампой ОКН-11 по 10 мин с каждой стороны. Пробирки плотно закрывали стерилизованными резиновыми пробками и выдерживали в термостате при 310К. На вторые сутки с начала эксперимента (что было достаточно для увеличения численности клеток СРБ) образцы из стали заменяли на стальные образцы с Cd-покрытием, полученным в результате электроосаждения в сульфатном электролите кадмирования в присутствии заявляемых веществ. Кадмирование проводилось без перемешивания при комнатной температуре и плотностях тока 1,0; 2,0 и 3,0 А/дм2 в сернокислом электролите следующего состава:
Для приготовления электролита растворяли отдельно каждое вещество в дистиллированной воде в концентрациях 1,0; 2,0 и 5,0 мМоль/л. Перед началом электролиза электролит прорабатывали 4 ч для удаления примесей других металлов.
Коррозионные процессы изучали гравиметрическим, потенциометрическим и потенциостатическим методами.
Подсчет числа клеток сульфатредукторов производился под микроскопом «БИОЛАМ ЛОМО», снабженным фазовоконтрастным устройством ФК-2 в камере Горяева для определения титра бактерий, по которому можно судить о жизнедеятельности изучаемых организмов.
Общее число бактерий в единице объема коррозионной среды (бактериальный титр) определяли по формуле:

где α - среднее число клеток в квадрате камеры Горяева;
n - глубина камеры (0,1 мм);
S - площадь квадрата сетки в камере (1/400 мм2).
Ежедневно проводили измерения редокс-потенциала с Pt-электродом, рН коррозионной среды со стеклянным электродом и электродного потенциала стального образца на универсальном иономере ЭВ-74.
Цикл развития сульфатредуцирующих бактерий составляет 8 сут. Поэтому по истечении 7 сут образцы извлекали из коррозионной среды, отмывали жесткой щеткой от продуктов коррозии и взвешивали. Скорость коррозии измеряли гравиметрически, определяя потерю массы Δm на каждом из трех образцов в параллельных опытах.

где Δm - изменение массы образца, г;
S - поверхность образца, м2 (1×10-3м2);
τ - время проведения опыта, сутки (7 сут).
Результаты измерений в трех параллельных опытах усредняли.
Защитный ингибирующий эффект органических добавок определяли по формуле:
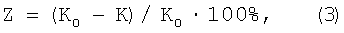
где К0 - скорость коррозии в среде без ингибитора;
К - скорость коррозии в присутствии ингибитора.
В процессе развития сульфатредуцирующих бактерий происходило выделение в коррозионную среду биогенного сероводорода, который взаимодействовал с кадмиевым покрытием образцов, осажденным в сульфатном электролите кадмирования в присутствии заявляемых соединений, с образованием сульфидов кадмия и железа. Сначала на поверхности образца появлялся осадок сульфидов кадмия и железа, наблюдалось помутнение среды, затем можно было обнаружить налет продуктов коррозии на стенках пробирки и на ее дне, что особенно проявлялось на 4 сут эксперимента. Затем в коррозионной среде происходила флокуляция сульфидов и некоторое просветление раствора. При неизменной температуре (37°С) на 6-7 сут среда становилась почти прозрачной, на дне пробирок появлялся осадок из продуктов коррозии и отмерших клеток СРБ, что свидетельствовало об истощении питательной среды и гибели культуры СРБ.
Биогенный сероводород определяли каждые сутки методом осадительного йодометрического титрования.
При выполнении эксперимента соблюдали необходимые способы предосторожности для сохранения сероводорода в коррозионной среде: минимальное время взятия пробы, плотно закрытые пробки. Перед началом титрования для определения концентрации сероводорода после тщательного перемешивания среды отбирали пробу объемом 5 мл, проводили осаждение ацетатом свинца (II). Отфильтрованный и промытый горячей водой осадок помещали в колбу с 25 мл 0,05 н. раствора йода, подкисленного серной кислотой, и титровали 0,05 н. раствором тиосульфата натрия до характерного цвета. Концентрацию биогенного сероводорода определяли по формуле:
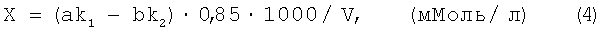
где а - объем прибавленного раствора йода, мл;
b - объем раствора тиосульфата, мл;
V - объем пробы исследуемого раствора, мл;
k1 - поправочный коэффициент для приведения концентрации йода к 0,05 н.;
k2 - поправочный коэффициент для приведения концентрации раствора тиосульфата натрия к 0,05 н.
Наблюдения за жизнедеятельностью СРБ вели путем ежедневного подсчета под микроскопом в фазовом контрасте численности микроорганизмов с помощью камеры Горяева. Концентрацию сульфатного остатка определяли йодометрическим титрованием по калибровочному графику. Величины рН и редокс-потенциала сред определяли потенциометрически.
Обезжиренные и облученные ртутно-кварцевой лампой стальные образцы с Cd-покрытием, полученным в процессе формирования электроосадка в сульфатном электролите кадмирования в присутствии заявляемых веществ вводили в коррозионную среду спустя 48 ч после инокуляции культурой СРБ, необходимых для их развития в коррозионной среде, и сразу же снимали первые показания физико-химических параметров: электродного потенциала поверхности образца, окислительно-восстановительного потенциала и водородного показателя рН коррозионной среды, концентрации биогенного сероводорода, количества бактериальных клеток (бактериальный титр).
Значения электродного потенциала (ε) стального образца с Cd-покрытиями (таблица 4), электроосажденными в присутствии всех заявляемых органических соединений, на 4-е сут эксперимента смещаются в сторону более положительных значений. Наибольшее облагораживание ε наблюдается в присутствии соединения 5, введенного в электролит в процессе осаждения кадмия при плотности катодного тока Дк=1 А/дм2 (таблица 4). Наименьший сдвиг значений ε вызвало соединение 1, введенное в электролит в процессе осаждения кадмия при Дк=3 А/дм2.
Величина электродного потенциала в коррозионной среде образцов, полученных из электролитов с различной концентрацией заявляемых соединений при трех Дк (экспозиция 96 ч)
На 3-4 сут эксперимента наблюдалось смещение окислительно-восстановительного потенциала (εh) в сторону более положительных значений по сравнению с контрольной серией. Причем сдвиг εh был тем сильнее, чем больше концентрация заявляемых веществ была в электролите электроосаждения кадмия. Наибольший сдвиг 8h наблюдался в присутствии соединения 5, вводимого в электролит в процессе осаждения при Дк=1 А/дм2, а наименьший - при введении соединения 1, введенного в электролит в процессе осаждения при Дк=3 А/дм2 (таблица 4а). В присутствии в коррозионной среде всех заявляемых органических веществ, переходящих в нее в результате коррозионного разрушения Cd, в последние сутки жизненного цикла микроорганизмов значения εh незначительно смещаются в сторону более отрицательных значений.
Окислительно-восстановительный потенциал коррозионной среды при коррозии кадмированной в электролите с заявляемыми соединениями стали (экспозиция 96 ч)
Вводимые в коррозионную среду образцы (таблица 5) со встроенными в осадок Cd исследуемыми органическими соединениями приводят к смещению рН среды в сторону менее кислых значений по сравнению с контрольной серией.
Водородный показатель коррозионной среды после 96 ч экспозиции стальных образцов, кадмировавшихся при трех плотностях тока в электролите с исследуемыми соединениями в трех концентрациях
При этом сдвиг рН уменьшается при уменьшении плотности катодного тока в процессе осаждения кадмия с введенными в электролит органическими веществами и увеличением концентрации вводимого органического соединения. Наименьшее смещение значений водородного показателя на 4 сут эксперимента в сторону кислых значений наблюдается при введении в коррозионную среду стальных образцов с Cd-покрытиями, полученными при Дк=1 А/дм2. Так соединение 5 вызывает смещение рН коррозионной среды до 5,75 (при С=1,0 мМоль/л) и до 5,89-5,90 (при С=2,0 и 5,0 мМоль/л), а добавка 1 до 5,66 (при С=1,0 мМоль/л) и до 5,77 (при С=5,0 мМоль/л) - таблица 5.
На 3-4 сут эксперимента в стерильной среде наблюдался "всплеск" численности СРБ. В пробах с заявляемыми соединениями, наоборот, уже через 1 сут после введения исследуемых веществ численность клеток резко уменьшалась.
Количество микробных клеток в коррозионной среде в зависимости от концентрации заявляемых соединений в электролите для осаждения Cd в конце экспозиции (96 ч)
Спустя 48 ч экспозиции наблюдалось незначительное увеличение количества клеток СРБ, что связано со способностью бактерий приспосабливаться к измененным условиям среды. Затем по мере истощения питательных свойств среды численность СРБ снижалась монотонно. Соединения 5 и 4 вызывают большее уменьшение численности микроорганизмов (таблица 6).
Изменение содержания сероводорода в среде после экспозиции образцов, кадмированных в электролите с органическими соединениями (экспозиция 96 ч)
На вторые сутки экспозиции в коррозионной среде кадмированных стальных образцов, полученных из электролита с добавками заявляемых соединений - производных антипирина, наблюдали уменьшение в ней основного метаболита бактерий - сероводорода. По мере завершения жизненного цикла СРБ, концентрация сероводорода в среде принимает относительно постоянное значение. Соединение 5 вызвало наибольшее снижение концентрации сероводорода в коррозионной среде (таблица 7). Из таблицы 8, приведенной ниже, видно, что скорость коррозии кадмированной в присутствии заявляемых веществ стали монотонно снижается с увеличением концентрации вводимых в электролит кадмирования органических соединений, достигая довольно небольших значений. Образец, кадмированный в присутствии соединения 5, имел наименьшую скорость коррозии, что соответствует его действию на рН, εh, CH2S, nкл.
Величины скорости коррозии кадмированной стали и защитного эффекта встроенных в Cd-покрытие органических добавок в зависимости от их концентрации в сульфатном электролите кадмирования
2
5
0,07
0,06
0,13
0,13
0,19
0,18
81
84
67
67
54
56
По степени защиты кадмированной стали от коррозии описываемые производные антипирина можно расположить в ряд: №5>№4>№3>№2>№1. Соединения 5 и 4 обладают наилучшими из описываемых заявляемых веществ ингибирующими коррозию Cd-стали и биоцидными свойствами.
Соединение 5 отличалось от остальных заявляемых соединений также по действию на электродный потенциал при выделении кадмия на катоде, которое было наиболее интенсивным. Это связано с появлением у молекул этого соединения наибольшей способности к адсорбции на поверхности металла катода (сталь, кадмий) в процессе электроосаждения, повлекшей за собой наибольшее среди исследуемых органических соединений включение (по массе органического вещества) в растущий электроосадок кадмия. Кроме того, повышенная адсорбционная способность соединения 5 на металле катода повлекла за собой и большее ингибирование коррозии кадмированной стали (таблица 8), поскольку ингибирование коррозии, протекающей по электрохимическому механизму, происходит, имея обязательную стадию - адсорбцию молекул органического соединения на поверхности корродирующего металла. Повышенная адсорбционная способность соединения 5 объясняется наличием в молекуле этого соединения электронодонорной группы (изобутил), связанной с центральным атомом С, что должно приводить к увеличению электронной плотности на всех гетероатомах N и обоих карбонильных атомах О. Таким образом, устанавливающиеся хемосорбционные связи молекул соединения 5 с атомами Fe и Cd, находящимися на поверхности, обеспечивают эффективное экранирование большой поверхности металла от коррозионной среды, достаточное для торможения как анодного (ионизация металла), так и катодного (разряд Н3О+) процессов.
Заявляемые соединения проявляют также биоцидное действие на СРБ (таблица 6), особенно сильно выраженное у соединения 5, и в меньшей степени у соединения 1. Биоцидное действие соединений имеет своим следствием и подавление сероводородогенеза в коррозионной среде, инокулированной СРБ рода Desulfovibrio.
Из представленных данных в таблицах 5-8 видно также, что наибольший полезный эффект оказывают заявляемые соединения, будучи встроенными в электроосадки Cd из сульфатного электролита, формируемые при меньшей катодной плотности тока (1 А/дм2), которая фактически и применяется на отечественных машиностроительных, судостроительных, авиамоторных и радиотехнических заводах при кадмировании многочисленного ассортимента изделий.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ АНТИПИРИНА В КАЧЕСТВЕ ИНГИБИТОРОВ МИКРОМИЦЕТНОЙ КОРРОЗИИ И НАВОДОРОЖИВАНИЯ СТАЛИ В ВОДНО-СОЛЕВОЙ СРЕДЕ | 2008 |
|
RU2359068C1 |
| Способ защиты стали от коррозии и наводороживания органическими соединениями в средах, содержащих сульфатредуцирующие бактерии | 2016 |
|
RU2630149C1 |
| СПОСОБ ЗАЩИТЫ СТАЛИ ОТ КОРРОЗИИ И НАВОДОРОЖИВАНИЯ В СРЕДАХ, СОДЕРЖАЩИХ СУЛЬФАТРЕДУЦИРУЮЩИЕ БАКТЕРИИ | 2007 |
|
RU2338008C1 |
| СПОСОБ ЗАЩИТЫ ОТ КОРРОЗИИ И НАВОДОРОЖИВАНИЯ СТАЛИ В ВОДНО-СОЛЕВЫХ СРЕДАХ | 2005 |
|
RU2283369C1 |
| ИНГИБИТОРЫ МИКРОБИОЛОГИЧЕСКОЙ КОРРОЗИИ АЛЮМИНИЕВОГО СПЛАВА Д16 | 2000 |
|
RU2198960C2 |
| ИНГИБИТОРЫ МИКРОБИОЛОГИЧЕСКОЙ КОРРОЗИИ И НАВОДОРОЖИВАНИЯ СТАЛИ | 1997 |
|
RU2151819C1 |
| Ингибитор микромицетной коррозии стали Ст3 с гальваническим покрытием Cu-Zn | 2018 |
|
RU2674499C1 |
| СПОСОБ ЗАЩИТЫ СТАЛИ ОТ МИКРОБИОЛОГИЧЕСКОЙ КОРРОЗИИ И НАВОДОРОЖИВАНИЯ В ВОДНОЙ СРЕДЕ, СОДЕРЖАЩЕЙ Aspergillus niger | 2007 |
|
RU2386727C2 |
| ЭЛЕКТРОЛИТ БЛЕСТЯЩЕГО НИКЕЛИРОВАНИЯ | 2008 |
|
RU2363774C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ЭЛЕКТРООСАЖДЕНИЯ КАДМИЯ НА СТАЛЬ | 2008 |
|
RU2398917C1 |
Изобретение относится к защите от коррозии деталей машин, конструкций и сооружений из кадмированных углеродистых и низколегированных сталей, которые контактируют с водными растворами солей, кислот, сточными водами, морской водой, увлажненными почвами. В качестве ингибитора коррозии кадмированной в его присутствии стали в водно-солевой среде, содержащей сульфатредуцирующие бактерии, применяют производное антипирина общей формулы:
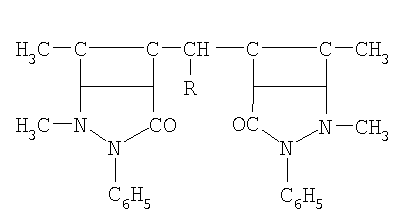
где R: -Н; -СН3; -С2Н5; -С3Н7; -С4Н9; -С5Н11; -С6Н5; -С6Н13. Технический результат: повышение коррозионной стойкости стали с кадмиевым покрытием, с включенным в него в процессе электроосаждения производным антипирина, к воздействию сульфатредуцирующих бактерий в водно-солевой среде. 9 табл.
Применение производного антипирина общей формулы
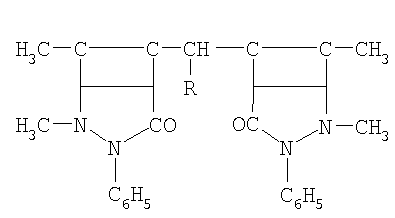
где R - -Н; -СН3; -С2Н5; -С3Н7; -С4Н9; -С5Н11; -С6Н5; -С6Н13,
в качестве ингибитора коррозии кадмированной в его присутствии стали в вводно-солевой среде, содержащей сульфатредуцирующие бактерии.
| ИНГИБИТОР КОРРОЗИИ МЕТАЛЛОВ В ВОДНО-НЕФТЯНЫХ СЕРОВОДОРОДСОДЕРЖАЩИХ СРЕДАХ | 1983 |
|
SU1202291A1 |
| Блескообразующая добавка к сернокислымэлЕКТРОлиТАМ КАдМиРОВАНия | 1979 |
|
SU829726A1 |
| ИНГИБИТОР ДЛЯ ЗАЩИТЫ СТРОИТЕЛЬНЫХ СТАЛЕЙ ОТ КОРРОЗИОННО-МЕХАНИЧЕСКОГО РАЗРУШЕНИЯ В СЕРОВОДОРОДСОДЕРЖАЩИХ МИНЕРАЛИЗОВАННЫХ СРЕДАХ | 2003 |
|
RU2230135C1 |
| Пирокатехилборат этиламина в качестве ингибитора сероводородной коррозии черных металлов в высокоминерализованной воде | 1980 |
|
SU967053A1 |
Авторы
Даты
2007-12-20—Публикация
2006-05-12—Подача