Изобретение относится к составам и терапевтическим способам снижения тяги к никотину и прекращения курения. В частности, предметом настоящего изобретения являются усовершенствованные составы никотинсодержащих таблеток и терапевтические способы обеспечения периодическими дозами никотина лиц, которые пытаются бросить курить.
Уровень техники
Терапия замены никотина как средство прекращения курения становится все более популярной. Никотинсодержащая жевательная резинка (никотиновый полакрилекс) и трансдермальный никотин представляют собой две из наиболее популярных форм замены никотина, имеющиеся на рынке. Стало, однако, ясно, что простая замена сигарет другим источником никотина может быть недостаточной для обеспечения успеха в терапии прекращения курения. В частности, обычная терапия замены никотина недостаточно учитывает симптомы, связанные с прекращением курения.
Из многих симптомов абстиненции от курения тяга к сигаретам является одной из самых трудных для облегчения. Как описано в Steuer, J.D. и Wewers, М. Е. в Oncology nursing Forum 1989, 16, 193-198, тяга к сигаретам является одним из наиболее стойких, наиболее тяжелых и самым первым из синдромов абстиненции, испытываемых теми, кто пытается прекратить курение. В некоторых сообщениях приводится, что пики тяги приходятся на период от первых 24 до 72 часов абстиненции, а затем они снижаются, хотя сообщалось и о случаях тяги к сигаретам после пяти лет воздержания.
Исследования нацелены на те факторы, которые понижают тягу, в попытке лучше понять и принять меры по отношению к проблеме рецидива. Некоторые исследователи полагают, что часть курильщиков намного более других подвержена ощущению симптомов тяги к курению, в частности при попытке бросить курить. На основе литературных данных и собственных исследований Harrington (в Br. J. Soc. Clin. Psychol. 1978, 17, 363-371) сообщал, что курильщики могут быть поделены по своему состоянию на имеющих тягу и на не имеющих тягу, и что эти категории имеют разные реакции на терапию прекращения курения. (В его исследовании лечение заключалось в различных поведенческих стратегиях и замена никотина не применялась). В частности, абстиненция во время лечения и успех в конце лечения в значительной степени были связаны с отсутствием тяги к курению.
Большинство продающихся веществ для замены никотина при лечении от курения не направлены конкретно на удовлетворение тяги к никотину. Вместо этого, как упомянуто выше, они обычно нацелены на достижение некоего минимального уровня никотина в крови. Есть доказательства того, что стойкие низкие уровни никотина в крови (которые достигаются с помощью трансдермального никотина или, в меньшей степени, с помощью никотинсодержащей жевательной резинки) облегчают некоторые из симптомов воздержания от никотина, но симптомы тяги к таковым не относятся (см. Russell, М.А.Н. в Nicotine Replacement: a Critical Evaluation; Pomerleau, O. F. and Pomerleau,C.S., Eds.; Alan R. Liss, Inc.: New York, 1988; pp 63-94). Это может быть вызвано тем, что курение сигареты дает сразу резкий рост содержания никотина в крови, что отсутствует в этих видах терапии замены никотина. Пик содержания никотина в крови, вызываемый сигаретами, одновременно выше (в пределах от 30 до 40 нг/мл) и острее (этот пик достигается в течение 10 минут), чем более умеренные уровни, получаемые от жевательной резинки или от трансдермальной системы. Расселл утверждает, что оптимальный устойчивый уровень для замены никотина составляет от 10 до 15 нг/мл, однако эффект быстрого роста, по-видимому, необходим для более полного избавления от тяги на самых ранних стадиях воздержания от сигарет. В его исследованиях указано, что повышение содержания никотина в крови по крайней мере на 10 нг/мл за 10 минут необходимо для получения постсинаптических эффектов на холинергических рецепторах никотина в центральной нервной системе и на вегетативных ганглиях. Эти постсинаптические эффекты могут быть ответственны за подобные наркотикам "высокие ощущения", такие как легкость в голове или головокружение, которые испытывают курильщики сигарет.
Как указано выше, никотинсодержащая жевательная резинка (полакрилекс никотина) представляет собой один из имеющихся на рынке источников никотина для терапии замены. Никотинсодержащая жевательная резинка фактически представляет собой ионообменную смолу, которая медленно выделяет никотин при жевании, а никотин, присутствующий во рту, выделяется непосредственно в большой круг кровообращения путем всасывания через рот. Однако много этого никотина остается в жевательной резинке из-за неполного изжевывания или в значительной мере пропадает зря из-за проглатывания, в результате чего соматическая биологическая доступность никотина из жевательной резинки низка и в среднем составляет только 30-40%. Кроме того, по сравнению с курением сигарет, никотинсодержащая резинка представляет собой медленный и неэффективный источник никотина.
Замена никотина через трансдермальные системы никотина представляет собой другой вид терапии, который стал коммерчески доступен. Эти никотинсодержащие пластыри обеспечивают низкий, стабильный уровень никотина в крови у потребителя и обходят воздействия первого прохождения на кишку и на печень. Системы с трансдермальным никотином могут быть предназначены для создания более высоких уровней стабильного состояния никотина в крови, но не способны создать пики или обеспечить быстрое повышение уровня никотина в крови. Таким образом, никотинсодержащая жевательная резинка и трансдермальный никотин конкурируют одна с другим как продукты, создающие уровни устойчивого состояния никотина в крови, но не удовлетворяют симптом тяги к сигарете у некоторых курильщиков.
Другие существующие или предложенные в литературе никотинзаменяющие вещества не представляют значительного интереса в терапии прекращения курения из-за проблем, связанных с их применением, а также из-за ограниченной способности удовлетворять тягу к сигарете. Пары никотина вводятся пациентам в виде аэрозоля, подобно технологии ингаляции, применяемой для введения лекарственных средств при бронхиальной астме, и из "бездымных сигарет", таких как выпускаемые фирмой Эдванст Тобаккоу Продактс под торговым названием Favor. Некоторые данные, однако, указывают на то, что эти варианты введения никотина не обеспечивают значительных уровней содержания никотина в крови у пациентов. Кроме того, ингаляция этих продуктов с парами никотина может оказаться слишком раздражающей для слизистой оболочки, чтобы это могли вытерпеть пациенты.
Другим бездымным способом попадания никотина на слизистую оболочку рта является жевание табака, вдыхание нюхательного табака через рот или табачные пакетики. Табачные пакетики, которые особенно популярны в Скандинавии и в США, содержат молотый табак в пакетиках, которые высасывают или держат во рту. Однако, как показано на фиг. 1 (уровни сигареты, никотинсодержащей жевательной резинки и пакетика с табаком из Russell, М.А.Н., Jarvis, M.J., et al. Lancet 1985, 2 1370), использование табачных пакетиков приводит к таким уровням содержания никотина в крови, которые более сравнимы с уровнями, получаемыми от жевательной резинки, чем при курении сигарет; т.е. они требуют примерно 30 минут для достижения максимального уровня примерно в 12 нг/мл, что меньше, чем половина пикового значения от выкуривания одной сигареты. Одной возможной причиной такого медленного поглощения никотина из табачных пакетиков является медленное выделение никотина в рот, как и при никотинсодержащей жевательной резинке: другая может состоять в том, что значительная часть никотина проглатывается и поэтому подвергается воздействию первого прохождения от желудка и печени. В любом случае эти оральные формы введения могут быть полезны для создания низких уровней содержания никотина в крови в стабильном состоянии, однако они не обеспечивают пиковых уровней, требуемых для удовлетворения сильной тяги.
В литературе описаны другие капсулы, таблетки и лепешки для орального введения никотина. Например, в заявке WO 88/03803 описана жевательная капсула, заполненная жидкостью, содержащей 0,1 - 10,0 мг никотина, вместе с добавками для улучшения вкусовых качеств и диспергирования. Капсулы имеют разные значения pH, что позволяет пациенту выбрать скорость поглощения никотина, и они специально предназначены как средство помощи при прекращении курения.
Другой состав никотинсодержащей капсулы описан авторами М.Е. Jarvik et al. (в Clin. Pharm. Ther. 1970, 11, 574-576) для приема внутрь в качестве вспомогательного средства для прекращения курения. Эти капсулы, однако, по всей очевидности проглатывались пациентами целиком в соответствии с теорией, что всасывание никотина в кишечнике может создавать значительные уровни содержания в крови. В этом исследовании показано небольшое, но заметное уменьшение количества сигарет, выкуриваемых пациентами, но не было получено количественных измерений уровней никотина в крови.
В литературе также описаны различные составы таблеток для выделения никотина в рот и в пищеварительную систему. В патенте Бельгии N 899037 в качестве вспомогательного средства для прекращения курения описывается таблетка, содержащая от 0,1 до 5 мг никотина в виде основания или водорастворимой кислой соли.
Wesnes и Warburton (в Psychopharmacology 1984, 82, 147-150; и Psychopharmacology 1986, 89, 55-59) обсуждают использование никотиновых таблеток в экспериментах по исследованию влияния никотина на учебу и на обработку информации. В ходе первого опыта никотин добавляли к таблеткам декстрозы с каплей острой приправы для маскировки вкуса никотина. Во втором опыте никотин добавляли к таблеткам гидроокиси магния, полагая, что щелочная среда во рту должна усилить внутриротовое поглощение. И вновь для маскировки вкуса никотина острую приправу добавляли как в активные, так и в контрольные таблетки. Пациентов инструктировали держать таблетки во рту в течение 5 минут до проглатывания, в целях обеспечения максимального контакта со слизистой оболочкой.
Шоу (например, в патентах Великобритании 2142822 и США 4.806.356) описывает никотинсодержащую таблетку, приготовленную холодным прессованием из смеси инертного наполнителя, связующего и либо чистого никотина, либо никотинсодержащего вещества. Таблетки предназначены для держания во рту, так как они медленно растворяются и постепенно выделяют никотин в ротовой полости.
В заявке WO 91/09599 описан никотинсодержащий продукт для перорального введения в форме комплекса включения никотина и циклодекстринового соединения. В этом патенте также обсуждается применение различных лекарственных сред и прямого прессования для изготовления этого продукта.
За последние годы на рынке Великобритании появилось несколько никотинсодержащих таблеток. Таблетки Resolution, производимые фирмой Феникс Фармасьютикэлз и реализуемые на рынке фирмой Эрнест Джексон, содержат 0,5 мг никотина вместе с витаминами A, C и E с антиоксидантами. Таблетки Stoppers, реализуемые на рынке фирмой Чарвелл Фармасьютикэлз, содержат 0,5 мг никотина и ароматические добавки шоколада, апельсина или перечной мяты.
Так как никотин имеет резкий, обжигающий вкус, то эти никотинсодержащие таблетки обычно готовят с сахаром в качестве основного компонента. Однако увеличение веса после прекращения курения было отмечено как серьезный фактор, способствующий возврату к курению. В недавнем опросе курильщиков, которые раньше пытались бросить курить, просили оценить важность некоторых возможных причин их возврата к курению. Двадцать семь процентов сообщили, что "реальное повышение веса" было "очень важной" или "достаточно важной" причиной, почему они возобновили курение; двадцать два процента сказали, что "возможность увеличения веса" была важной причиной для их возврата к курению. Cм. The Health Benefits of Smoking Cessation: A Report of the Surgeon General, Executive Summary (1990). Таким образом, составы таблеток на основе сахара могут быть неприемлемыми для программы прекращения курения для людей, обеспокоенных увеличением веса.
До настоящего времени было трудно вводить никотин с такими показателями, имитирующими достигаемые при постоянном курении уровни никотина в крови, чтобы удовлетворить острую тягу к никотину у людей, которые пытаются бросить курение, и таким образом обеспечить более надежную защиту от возврата к курению, чем при других видах терапии замены никотина для людей, пытающихся бросить курение. Поэтому желательно создать улучшенные составы таблеток и способы, при которых устранялись бы недостатки известных средств и способов ввода никотина, при обеспечении эффективного средства его введения.
Сущность изобретения.
Настоящее изобретение обеспечивает применение никотинсодержащих таблеток, содержащих непитательный подсластитель, в качестве способа ослабления острой тяги к никотину и терапии прекращения курения. В частности, настоящее изобретение представляет новый способ получения временных уровней содержания никотина в крови, имитирующих эффект курения сигареты, включающий в себя периодическое применение никотинсодержащих таблеток, предпочтительно включающих никотин, абсорбирующий наполнитель и непитательный подсластитель, и более предпочтительно сочетание непитательных подсластителей, для обеспечения быстрого введения никотина во внутриротовую слизистую оболочку. Никотинсодержащие таблетки предназначены для держания во рту и сосания, а также для выделения никотина в ротовую полость. В предпочтительном варианте осуществления никотин быстро выделяется, достигая максимальных уровней содержания никотина в крови через 2 - 30 минут после приема таблеток.
Таблетки содержат довольно низкие дозы, предпочтительно ниже 5 мг и более предпочтительно от 0,5 до 2,0 мг никотина. В особенно предпочтительных вариантах осуществления никотин диспергируют в манните или β- циклодекстрине, а таблетка представляет собой содержащий буферный раствор состав, предпочтительно с pH 6-11 и более предпочтительно с pH 7-9. В наиболее предпочтительном составе таблетка содержит непитательный подсластитель ксилит, известный своими некариесогенными свойствами, в сочетании с подсластителем глицирризинатом аммония.
Перечень фигур чертежей и иных материалов.
Фиг.1 диаграмма средних уровней содержания никотина в плазме (нанограммов (нг)/миллилитр (мл)), в результате применения сигарет, табачных пакетиков или никотинсодержащей жевательной резинки как функция от времени.
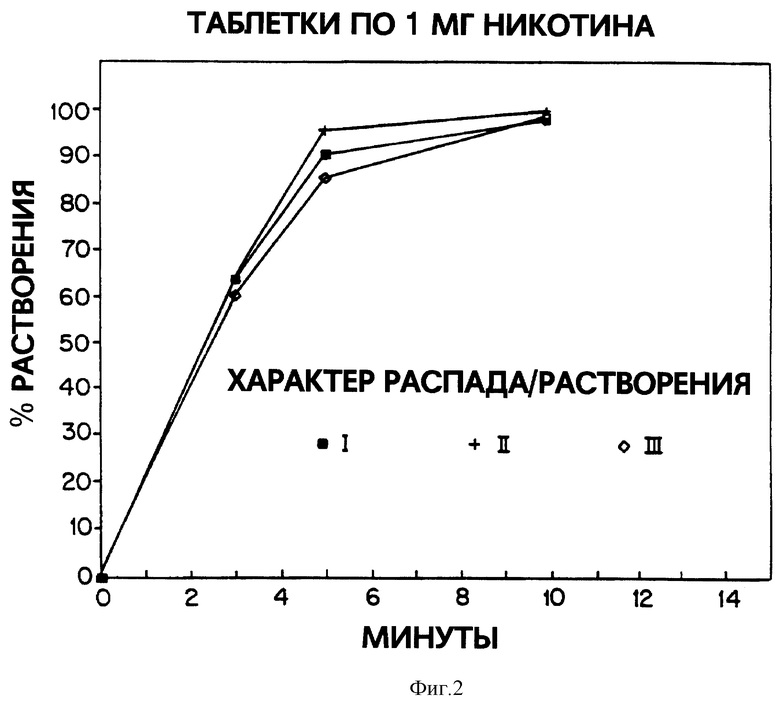
Фиг. 2 диаграмма профилей распада/растворения (растворение в весовых %) трех разных составов таблеток, каждый из которых содержит 1 мг никотина как функция от времени.
Сведения, подтверждающие возможность осуществления изобретения.
1. Терминология
Если не указано иное, термины, использованные далее в описании и в формуле изобретения, имеют следующие значения:
"Буккальный прием" относится к любой системе или средству для внутриротового приема пациентом лекарств, которые держат во рту и используют для введения лекарственного средства через слизистую оболочку рта в тело пациента. Этот термин включает, не будучи ограниченным этим, лепешки, капсулы и таблетки.
"Эфирное масло" означает натуральное масло с характерным запахом, выделяемое железками некоторых ароматических растений, содержащее терпены в качестве основного компонента. Примеры эфирных масел включают, не будучи ограничены этим, цитрусовые масла, цветочные масла (например, розы и жасмина) и гвоздичное масло.
"Никотин" относится к никотиновому свободному основанию, т.е. к соединению, имеющему формулу: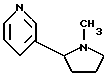
"Никотиновая соль" относится к любой моно- или бис- фармацевтически приемлемой соли присоединения кислоты или соли металла и никотина.
"Никотинсодержащая таблетка" означает любую лепешку, капсулу, таблетку или другое, средство для внутриротового выделения никотина.
"Непитательный подсластитель" означает синтетическое или натуральное вещество, сладость которого выше или сравнима со сладостью сахарозы и которое может иметь такие свойства как пониженная кариесогенность, полезные свойства для диабетиков или сниженную калорийную ценность по сравнению с сахарами.
"Фармацевтически приемлемая соль присоединения кислоты" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободных оснований и которые не являются нежелательными биологически или иным образом, и образованы неорганическими кислотами, такими как соляная, бромистоводородная, серная, азотная, фосфорная и подобные, и органическими кислотами, такими, как уксусная, пропионовая, гликолевая, пировиноградная, щавелевая, яблочная, малоновая, янтарная, малеиновая, фумаровая, винная, лимонная, бензойная, коричная, миндальная, ментансульфоновая, этансульфоновая, р-толуолсульфоновая, салициловая и тому подобные. Для описания фармацевтически приемлемых солей присоединения кислоты см. Bundgaard, Н., ed., (1985) Design of Prodrugs, Elsevier Science Publishers, Amsterdam.
"Фармацевтически приемлемая соль металла" относится к солям, сохраняющим биологическую эффекивность и свойства свободных оснований, которые не являются нежелательными биологически или иным образом, и образованы ионами щелочных металлов, таких как натрий или калий; ионами щелочноземельных металлов, таких как кальций и магний; и ионами других металлов, таких как цинк.
2. Таблетка
Согласно настоящему изобретению предлагаются таблетки, используемые для введения никотина пациенту в целях снижения его сильной тяги к никотину и для лечения от курения, и способы применения никотинсодержащих таблеток для этой цели, включая, но не будучи этим ограниченными, варианты осуществления и способы, описанные ниже. Никотинсодержащие таблетки по настоящему изобретению включают любые составы лепешек, таблеток или капсул, которые выделяют никотин в ротовую полость, включая никотин, диспергированный в абсорбирующем наполнителе, и непитательный подсластитель.
А. Никотин
Никотин представляет собой гетероциклическое соединение, которое существует как в форме свободного основания, так и соли. Свободное основание крайне летуче и легко поглощается через слизистые оболочки и неповрежденную кожу. Наибольшие проблемы, о которых сообщалось в отношении продуктов на базе свободного основания никотина, проистекают из летучести никотина, его резкого, обжигающего вкуса, раздражающего ощущения на слизистых оболочках и разложения никотина в присутствии кислорода. Ранее эти проблемы частично ослаблялись применением никотина в форме соли, т.е. в виде соли присоединения кислоты либо соли металла.
Неожиданно, описанные здесь таблетки могут изготовляться либо из свободного основания, либо из его фармацевтически приемлемой соли присоединения кислоты, либо из любого их сочетания. В приводимом в качестве примера варианте осуществления использован никотин, т.е. никотин в форме свободного основания.
Независимо от используемого состава таблетка содержит довольно низкие дозы никотина, предпочтительно от 0,5 до 5 мг, и наиболее предпочтительно от 0,5 до 2,0 мг, во избежание случайной передозировки при проглатывании таблетки в неразрушенном состоянии. Высокие дозы не требуются, так как назначение никотинсодержащей таблетки состоит в создании временного пика содержания никотина в крови.
Б. Абсорбирующий наполнитель
В соответствии с описанными здесь составами и способами никотин диспергируют в абсорбирующем наполнителе. Абсорбирующие наполнители представляют собой фармацевтически приемлемые вещества, которые способны: 1) снижать летучесть никотина, например, путем абсорбции или включения никотина как, например, в виде комплекса включения, и 2) подвергаться прессованию в виде лепешки или таблетки. Подходящие абсорбирующие наполнители включают, но не ограничены ими, маннит, циклодекстрины, включая α-, β- и γ- циклодекстрин, а также производные циклодекстринов, такие как триметил β- циклодекстрин, диметил β-циклодекстрин, гидроксиэтил β-циклодекстрин и гидроксипропил-β-диклодекстрин; препараты оксида кремния, такие как синтетический кремнезем, имеющийся на рынке под торговым наименованием Syloid фирмы У.Р.Грэйс Лимитед из Норт Дэйл Хаус, Норт Сэкьюлэ Роуд, Лондон (W.P. Grace Limited of North Dale House, North Circular Road, London); целлюлозные материалы, такие как микроцеллюлоза Avicel, изготовляемая фирмой ФМС Корпорейшн (FMC Corporation); и другие обычные связующие и наполнители, используемые в пищевой промышленности, такие как порошок акации, желатин, гуммиарабик и сорбит.
Согласно некоторым вариантам осуществления абсорбирующий наполнитель будет выполнять больше одной функции в составе таблетки. Например, маннит может действовать одновременно как непитательный подсластитель и как абсорбирующий наполнитель. Таким же образом, абсорбирующий наполнитель может служить в качестве ароматизатора, буферного вещества, смазывающего вещества или другого компонента таблетки.
Абсорбирующий наполнитель обычно присутствует в количестве от 5 до 25 вес. %, предпочтительно в количестве от 5 до 20 вес.%, и более предпочтительно в количестве от 5 до 15 вес.%.
В предпочтительном варианте осуществления абсорбирующий наполнитель содержит маннит или β- циклодекстрин.
В. Непитательный подсластитель
Таблетка также должна содержать непитательный подсластитель. Так как никотин имеет резкий, обжигающий вкус, то выбор подсластителя для никотинсодержащей таблетки может быть критичным, так как многие пациенты не находят приятным вкус никотина в форме таблетки. Обычно в описываемых таблетках будут использоваться непитательный подсластитель или сочетание подсластителей.
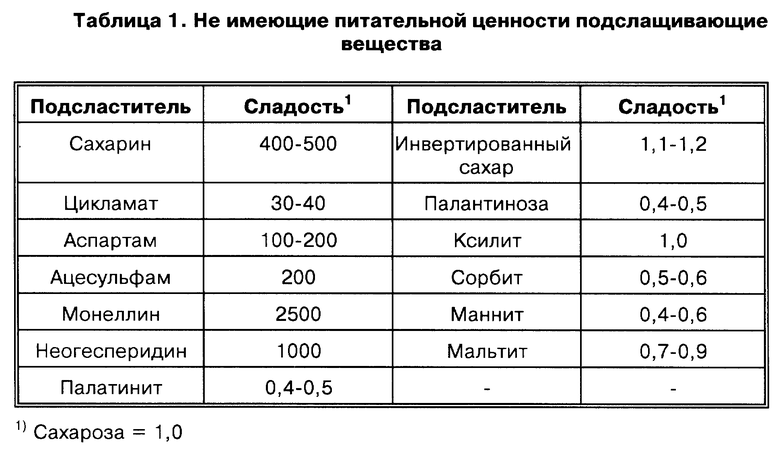
Непитательный подсластитель представляет собой синтетический или натуральный заменитель сахара, сладость которого выше или сравнима с сахарозой. В таблице 1 приводятся примеры непитательных подсластителей и их относительные величины сладости.
Таким образом, непитательный подсластитель должен иметь по сравнению с сахарозой относительную величину сладости примерно в пределах от 0,4 до 2500, более типично в пределах примерно от 0,4 до 500, предпочтительно в пределах от 0,4 до 200 и более предпочтительно в пределах от 0,4 до 2. Cм. Makinen (1988) Oral Health 78:57-66, включенный в настоящее описание путем ссылки.
В предпочтительном варианте осуществления непитательный подсластитель также является некариесогенным. Кариесогенность вещества зависит от его способности ферментироваться микроорганизмами Streptococcus mutans и другими ротовыми микроорганизмами. Исследователи-дантисты уже давно признали, что ферментируемые подсластители, такие как сахароза, глюкоза, крахмал и кукурузный сироп являются кариесогенными или вызывающими кариес. Полиольные непитательные подсластители, такие как ксилит, сорбит, фруктоза, инвертированный сахар, палантиноза, маннит, мальтит, палатинит и глицирризинат аммония, однако, в общем не ферментируются в сколь-нибудь значительной степени и менее кариесогенны, чем сахароза. Cм. Olinger, представленный на Конференции/Выставке Интерфекс-США (Interphex-USA), Нью-Йорк, 8-11 мая 1990 г.
Более конкретно, способность ксилита ингибировать развитие нового кариеса была продемонстрирована во многочисленных исследованиях in vivo и in vitro. Например, полевые испытания продуктов, принимаемых перорально, содержащих ксилит, показали, что замена сахарозы на ксилит в таких продуктах как жевательная резинка, может помочь в предупреждении зубного кариеса (см. Soderling, Е., и Scheinin, A., Proc. Finn. Dent. Soc. 1991, 87(2), 217-229). Исследованиями также было обнаружено, что когда употребляют ксилит-содержащие сласти как часть нормальной пищи вместе с принятой практикой гигиены рта, возникновение новых случаев кариеса уменьшается примерно на 50% и до 80%. См. выше Olinger.
Наряду с этим в литературе полагают, что непитательные подсластители и в частности ксилит могут быть полезны в качестве заменителя сахара для регулирования веса (см. патент США No 3.717.711), что ясно представляет собой серьезную обеспокоенность людей, которые бросают курить. В дополнение к этому, как было показано, ксилит удлиняет опорожнение желудка и уменьшает усвоение пищи у людей. Cм. Shafer et al. (1987) Am. J. Clin. Nutr. 45:744-47. Таким же образом, из-за того, что ксилит не метаболизируется как сахар, он имеет ценность для людей, которые должны ограничивать свое потребление сахара, таких как диабетики (см. Maukinen, К., Oral Health 1988, 78(9), стр. 60).
Ксилит также имеет охлаждающее воздействие, когда он растворяется во рту, что вызвано его отрицательной теплотой растворения. Теплота растворения ксилита составляет -36,6 кал/г по сравнению с -28,9 кал/г для маннита, -26,6 кал/г для сорбита и -4,3 кал/г для сахарозы (см. Olinger, P.M., представленный на Конференции/Выставке Интерфекс-США, Нью-Йорк, 8-11 мая 1990 г.). Следовательно, ксилит представляет собой великолепный выбор подсластителя и наполнителя для таблетки, которая должна удерживаться во рту в течение длительного периода времени и которую надо часто принимать каждый день для максимального терапевтического эффекта.
Часто необходимо использовать комбинацию непитательных подсластителей. Согласно одному варианту исполнения подсластитель, вызывающий временные ощущения, подобные сахарозе (т.е. время появления примерно 4 секунды и время затухания 13 секунд, например некоторые полиольные подсластители, сахарин, цикламат и аспартам), будут комбинироваться с подсластителем, сладость которого развивается медленнее или сохраняется дольше. Например, глицирризинат аммония, представляющий собой непитательный подсластитель с легким привкусом лакричника, имеет время появления или возникновения вкуса примерно 16 секунд для глицирризината аммония и время сохранения вкуса или время затухания 69 секунд.(Dubois и Lee (1983) Chem. Sens. 7:237-248). Другие примеры непитательных подсластителей с временными ощущениями, иными, чем у сахарозы, включают, но не ограничены ими, неогесперидиндигидрохалькон (время возникновения 9 секунд и время затухания 40 секунд) и стевиозид (время возникновения 4 секунды и время затухания 22 секунды).
Таким образом, в предпочтительном составе таблетка будет содержать непитательный подсластитель, такой как ксилит, сорбит, фруктоза, инвертированный сахар, палантиноза, маннит, мальтити палатинит, в чистом виде или в сочетании с другими непитательными ценности подсластителями. Более предпочтительно, будет использоваться ксилит, без добавок или в сочетании с непитательным подсластителем, имеющим время затухания длиннее, чем у сахарозы, таким как глицирризинат аммония, неогесперидиндигидрохалькон или стевиозид. В представленном в качестве примера варианте осуществления непитательный подсластитель будет включать ксилит и глицирризинат аммония.
Непитательный подсластитель обычно присутствует в количестве от 50 до 90 вес. %, предпочтительно в количестве от 70 до 90 вес.%, и более предпочтительно в количестве от 80 до 90 вес.%.
Г. Другие ингредиенты
Таблетка предпочтительно представляет собой состав с буфером для того, чтобы помочь в поглощении никотина в ротовой полости. Предпочтительный состав имеет pH примерно 6-11 и предпочтительно pH примерно 7-9. Предпочтительные составы с буфером будут включать в себя карбонат натрия, бикарбонат натрия, натрийфосфат, карбонат кальция, гидроксид магния, гидроксид калия, карбонат магния, гидроксид алюминия и другие вещества, известные специалистам, а также комбинации вышеупомянутых веществ. В наиболее предпочтительном составе в качестве буферных веществ таблетка будет содержать карбонат и бикарбонат натрия.
Буферные вещества (буферное вещество) должны присутствовать в количестве, достаточном для регулирования pH до величины между 6 и 11, обычно от 0,1 до 25 вес.%, предпочтительно в количестве от 0,1 до 10 вес.%, и более предпочтительно в количестве от 0,1 до 5 вес.%.
В дополнение к этому, таблетка может содержать ароматизатор, например, со вкусом шоколада, апельсина, ванили и тому подобного: эфирные масла перечной мяты, мяты курчавой и тому подобные; или другой ароматизатор, такой как анис, эвкалипт, 1-ментол, карвон, анетол и тому подобное, для маскирования вкуса никотина. Cм. Hall et al. Food Technol. 14:488 (1960); 15:20 (1961); 19:151 (1965); 24:25 (1970); 26:35 (1972); 27:64 (1973): 27:56 (1973): 28:76 (1974); 29: 70 (1974); 31:65 (1977); 32:60 (1978) и 33:65 (1979), каждый из которых включен в настоящее описание путем отсылки. Она также может содержать табачный ароматизатор для воспроизведения какой-то части ощущения курения для пользователя. Небольшое количество коллоидного диоксида кремния (менее чем 1 вес.%) обычно добавляют в таблетки, содержащие табачный ароматизатор, для помощи при изготовлении.
Стеарат магния и/или гидрогенизированное растительное масло также может добавляться к составу в качестве смазочного вещества. Обычно смазочное вещество присутствует в количестве от 0,1 до 25 вес.%, предпочтительно в количестве от 0,1 до 10 вес.%, и более предпочтительно в количестве от 0,1 до 5 вес.%.
Описываемые таблетки также могут содержать целый ряд других добавок. Например, при необходимости могут быть добавлены фармакологически активные ингредиенты, такие как монофторфосфат натрия, фторид натрия, декстраназа, мутаназа, хинокитиол, аллантоин, аминокапроновая кислота, транэксамовая кислота, азулен, производные витамина Е, хлорид натрия и тому подобные. Более конкретно, так как воздействие ксилита и фторида на гигиену зубов носит вспомогательный характер, вышеуказанное может значительно усилить эффективность традиционных видов лечения фтором. Таким образом, согласно одному варианту исполнения, фторид и более конкретно монофторфосфат натрия или фторид натрия будут включаться в состав таблеток, содержащих ксилит в качестве непитательного подсластителя.
В дополнение к этому таблетка может быть окрашена обычными, фармацевтически приемлемыми пищевыми красителями. Другие добавки, которые могут быть включены в описываемую здесь таблетку, включают в себя, не нося ограничительного характера, консерванты, антимикробные вещества и антиоксиданты.
Е. Способ изготовления
Способ изготовления таблеток может быть любым подходящим, известным в данной области, включая, но не будучи ограничен этим, добавление никотинсодержащего соединения к заранее изготовленным таблеткам; прессование в холодном состоянии инертного наполнителя, связующего и либо чистого никотина, либо никотинсодержащего вещества (как описано в патенте США N 4806356, включенном в настоящее описание путем отсылки); и расфасовка в капсулы никотина или никотинсодержащего соединения. См. патент США N 5135753, включенный в настоящее описание путем отсылки для примеров способов изготовления различных никотинсодержащих таблеток, подъязычных таблеток и желатиновых капсул. В предпочтительном варианте исполнения, таблетки формируют путем прямого прессования. См. пример 4 при описании способа изготовления, в котором никотин диспергируют в манните.
Согласно другому варианту осуществления, комплекс включения получают in situ из никотина и β-циклодекстрина, с применением технологии замешивания. В частности, небольшое количество раствора никотин-вода добавляется к циклодекстрину и замешивается или смешивается, см.SzezetIi в Cyclodextrins and Their Inclusion Complexes, Akademia Kiado: Budapest, 1992; стр. 109; включено в настоящее описание путем отсылки. Этот способ формирования комплекса включения никотин-циклодекстрин является предпочтительным, так как он сводит до минимума использование растворителей или разбавителей и таким образом устраняет этап очистки в процессе изготовления. См. также Пример 5 при описании применения технологии замешивания с никотином и β-циклодекстрином.
Еще один вариант осуществления настоящего изобретения обеспечивает получение комплексов включения как никотина, так и ароматизатора. Этот вариант применяется, например, когда в составе таблетки используют эфирное масло или другой летучий ароматизатор, такой как карвон или ментол. Как и в случае с описываемыми здесь комплексами включения никотина, включение ароматизатора в циклодекстрин снижает летучесть ароматизатора и повышает стабильность состава. Кроме того, так как ароматизатор медленно высвобождается из этого комплекса во время приема таблетки, он будет "оставаться" дольше, и таким образом уберет резкий вкус никотина на более длительные периоды времени.
Согласно этому варианту исполнения, смесь никотина и ароматизатора, и при необходимости воды, добавляют к циклодекстрину и замешивают. В качестве альтернативы, комплекс включения никотина и комплекс включения ароматизатора могут быть приготовлены раздельно, а затем смешиваться до приготовления состава таблеток.
Согласно еще одному варианту исполнения, часть непитательного подсластителя, предпочтительно ксилита, используется для твердого покрытия никотинсодержащей таблетки. Можно использовать традиционную технологию нанесения покрытия на боковые поверхности. Обычно увеличение веса примерно на 35% может быть осуществлено менее, чем за три часа (см. выше Olinger).
Таблетки могут быть упакованы таким образом, чтобы помочь поддерживать стабильность никотина. Предпочтительные методы упаковки включают в себя получение многослойной ленты из материала типа фольги, такого как Barex, или упаковку в шарики, используя материал типа Тефлона, такой как Aclar. См. также Hunt et al. (1991), патент США N 5077104.
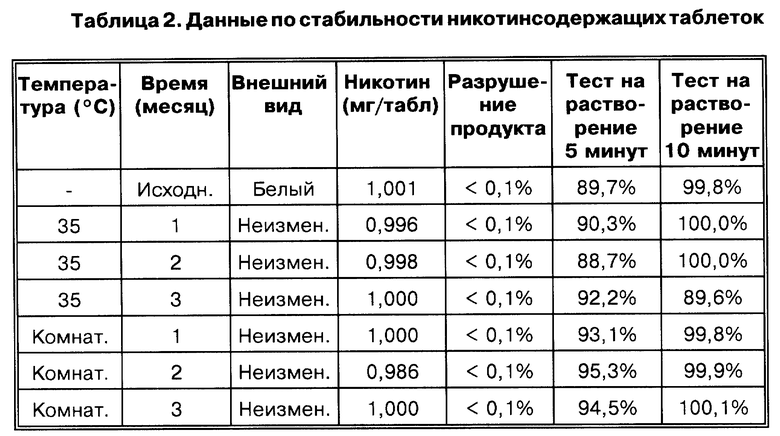
Как отмечено выше, никотин является летучим веществом. Сообщалось о кратковременном сроке хранения для никотинсодержащих таблеток из-за испарения никотина, в частности, когда окружающая температура выше 15o (см. Belcher et al. (1989) Brit. J. Med. 298:570. Описанные здесь таблетки, однако, стабильны в течение длительного времени при повышенных температурах, как показано в таблице 2 (см. Пример 6 при описании процедуры испытаний, использованной для определения стабильности.
Описываемые здесь таблетки в обычном случае будут иметь вес в пределах примерно от 70 до 1000 мг и будут содержать довольно низкие дозы никотина, предпочтительно менее 5 мг и наиболее предпочтительно от 0,5 до 2,0 мг.
3. Способ применения
Настоящее изобретение также относится к способу применения никотинсодержащих таблеток с целью создания периодических временных пиков содержания никотина в крови как средства снижения симптомов острой тяги к никотину. Обычно описываемые здесь таблетки будут использоваться по желанию пациентом для смягчения острой тяги к никотину по мере ее возникновения. Таким образом, данный способ обеспечивает пациенту средства для самостоятельного регулирования своих потребностей в приеме.
Более конкретно, острая тяга к никотину зависит частично от каждодневного характера стрессов, привычек ко сну и к еде, от веса тела, предшествующей интенсивности курения и тому подобного. Таким образом, желание к приему таблеток или потребность в них (сравнимые с желанием курить сигареты) обычно будут меняться в течение любого отдельного дня и день ото дня, также как и от пациента к пациенту. Описываемые здесь способы позволяют пациенту потреблять таблетки в таких количествах и в такое время, когда он сильнее всего чувствует тягу к никотину. Так как сильная тяга к никотину рассматривается некоторыми как наиболее устойчивый и наиболее важный фактор, препятствующий бросить курить, то возможность самостоятельного регулировать количество и, таким образом, снять тягу к никотину, повысит эффективность программы прекращения курения.
Для оценки степени тяги к никотину можно использовать целый ряд методов, включающих в себя, но не ограниченных этим, тест проверки тяги к никотину, описанный в Diagnostic and Statistical Manual of Mental Disorders, Revised Third Edition (DSM-III-R) (см. (1991) J. Am. Med. Assoc. 266:3133); подшкала тяги по Шиффману- Ярвику (см. O'Connel and Martin (1987) J. Consult. Clin. Psychol. 55: 367-371 и Steur and Wewers (1989) ONF 16:193-198, также описывающие параллельный визуальный аналоговый тест); West et al. (1984) Br. J. Addiction 79: 215-219: и Hughes et al. (1984) Psychopharmacology 83:82-87, каждый из которых специально включается в настоящее описание путем отсылки.
Предпочтительная шкала тяги к никотину включает шкалу, описанную выше в DSM-III-R. В соответствии с этой шкалой пациента просят оценить по степени серьезность его тяги к никотину на шкале от 0 до 4, где 0 означает отсутствие; 1 означает слабую; 2 означает среднюю; 3 означает умеренную и 4 означает сильную тягу. Используя описанные здесь составы и способы, пациент должен достичь снижения тяги к никотину по крайней мере на одну единицу и предпочтительно по крайней мере на две единицы, как замерено в протоколе, приведенном в DSM-III-R, через 2 - 30 минут после приема никотинсодержащей таблетки. Более предпочтительно, максимальное снижение тяги к никотину происходит примерно через 2 - 10 минут после приема никотинсодержащей таблетки.
Шкала силы тяги Шиффмана-Ярвика представляет собой шестипозиционный инструмент принудительного выбора и самостоятельной оценки, который измеряет тягу к сигаретам. Каждая позиция имеет семь возможных ответов, которые соответствуют цифрам в пределах от 1 (нет тяги) до 7 (сильная тяга). Средний результат получают для определения уровня тяги респондента к курению. Типичная цифра, замеренная через 48 часов после начала программы прекращения курения, находится в пределах от 4 до 5; в то время как шкала двухнедельного отслеживания тяги обычно дает результат примерно от 3 до 4. При использовании составов и способов, описываемых здесь, пациент должен достичь снижения своей тяги к никотину по крайней мере на одну единицу и предпочтительно по крайней мере на две единицы, как замерено в протоколе, составленном в шкале тяги Шиффмана-Ярвика, через 2 - 30 минут после введения никотинсодержащей таблетки. Более предпочтительно, когда максимальное уменьшение тяги к никотину произойдет через 2 - 10 минут после приема никотинсодержащей таблетки.
В шкале тяги "вопросник силы тяги" использует пятипозиционный вопросник, в котором пациентов просят оценить, как сильно им не хватало сигарет раньше, в какой степени они осознавали то, что не курят, насколько им было раньше трудно быть без сигарет, насколько они раньше были озабочены, думая о сигаретах и как сильна была раньше их тяга к сигаретам. Пациент отвечает на каждый вопрос цифрой от 1 до 3, где 1 означает мало, а 3 означает много. Цифры суммируют для получения единого показателя. Согласно этой шкале тяги комбинированный показатель в пределах от 9 до 12 является типичным. Используя описанные здесь составы и способы пациент должен достичь уменьшения тяги к никотину по крайней мере на три единицы и предпочтительно по крайней мере на четыре единицы, что замеряется протоколом, составляемым для использования с этим вопросником о силе тяги, через 2 - 30 минут после введения никотинсодержащей таблетки. Более предпочтительно, когда максимальное снижение тяги к никотину будет отмечено примерно через 2 - 10 минут после приема никотинсодержащей таблетки.
Конечно, таблетки также могут использоваться в соответствии с характером дозировки, предписанным врачом. Характер дозировки будет меняться вместе с показаниями. Например, в дополнение к использованию, в ходе терапии прекращения или уменьшения курения, вышеописанные никотинсодержащие таблетки могут быть использованы для лечения болезни Альцгеймера, язвенного колита и родственных состояний и болезней, связанных с пониженной центральной холинергической функцией, потерей холинергических нейронов, значительным снижением связывания рецептора никотина, нейродегенеративного слабоумия или снижения познавательной способности и памяти (см. Masterson (1991) патент США N 5069904; Wesnes и Warburton (1984) Psychopharmacology 82:147-150; и Warburton et al. (1986) Psychopharmacology 89:55-59.
Таблетка должна вводиться без наличия во рту какого-либо другого вещества, такого как пища или напиток. Особенно важно, чтобы кислые вещества или напитки, такие как фрукты, кофе, чай или фруктовые соки, не употреблялись непосредственно перед никотинсодержащей таблеткой или одновременно с ней с тем, чтобы обеспечить поддержание основной среды во рту.
Таблетку предпочтительно держат во рту в течение 2-10 минут, после чего она полностью растворяется и выделяет никотин в рот, а раствор с растворенным никотином должен удерживаться во рту максимально долго для поглощения никотина через слизистую оболочку.
В Примере 7 приводится протокол для измерения уровней никотина в крови у пациентов, использующих никотинсодержащую таблетку согласно настоящему изобретению. Применение таблетки приведет к получению временного пика уровня никотина в крови через 2 - 30 минут, и более предпочтительно через 2 - 10 минут, после помещения таблетки в рот.
На фиг.2 представлены профили дезинтеграции/растворения всехтрех составов, описанных в Примерах 1-3 (состав 1 содержит никотин, маннит, ксилит, мятный ароматизатор и другие наполнители: состав 2 содержит никотин, маннит, ксилит, вкусоароматическое вещество табака и другие наполнители, а состав 3 содержит никотин, циклодекстрин, ксилит и мятный ароматизатор). Как показано на фиг. 2, таблетки, имеющие состав согласно настоящему изобретению, будут растворены по крайней мере на 60% после 3-минутного держания во рту, по крайней мере 80% растворяется после 5 минут и примерно 100% растворяется спустя 10 минут.
Конкретные примеры состава согласно настоящему изобретению приведены ниже.
С целью более полного понимания описанного изобретения приведены нижеследующие примеры. Необходимо осознать, что эти примеры приведены только в целях иллюстрации и не должны толковаться как ограничивающие данное изобретение каким-либо образом.
Пример 1
Состав никотинсодержащей таблетки с ксилитом, маннитом и мятным ароматизатором
Ингредиенты - мг/таблетку
Никотин - 1,0
Маннит - 200,0
Ксилит - 1309,0
Мятный ароматизатор - 20,0
Глицирризинат аммония - 15,0
Карбонат натрия - 5,0
Бикарбонат натрия - 15,0
Гидрогенизированное растительное масло - 25,0
Стеарат магния - 10,0
Способ изготовления
Никотин диспергировали в манните. Порошки смешивали. Смесь прессовали с помощью подходящего чередующего таблеточного пресса с применением квадратного 16-миллиметрового штампа с дозировкой 1600 мг/таблетку.
Упаковка
Таблетки упаковывали в ленты из алюминия/барекса.
Пример 2
Состав никотинсодержащей таблетки с ксилитом, маннитом и вкусоароматической добавкой табака
Ингредиенты - мг/таблетку
Никотин - 1,0
Маннит - 200,0
Ксилит - 1316,5
Вкусоароматическая добавка табака - 6,0
Коллоидный кремнезем - 1,5
Глицирризинат аммония - 15,0
Карбонат натрия - 5,0
Бикарбонат натрия - 15,0
Гидрогенизированное растительное масло - 30,0
Стеарат магния - 10,0
Способ изготовления
Никотин диспергировали в манните. Порошки смешивали. Смесь спрессовывали с помощью подходящего чередующего таблеточного пресса с применением квадратного 16-миллиметрового штампа с дозировкой 1600 мг/таблетку.
Упаковка
Таблетки упаковывали в ленты из алюминия/барекса.
Пример 3
Состав никотинсодержащей таблетки с ксилитом, β-циклодекстрином и мятным ароматизатором
Ингредиенты - мг/таблетку
Никотин - 1,0
β-циклодекстрин - 109,0
Вода - 10,0
Ксилит - 1400,0
Мятный ароматизатор - 20,0
Глицирризинат аммония - 15,0
Карбонат натрия - 5,0
Бикарбонат натрия - 15,0
Гидрогенизированное растительное масло - 25,0
Стеарат магния - 10,0
Способ изготовления
Никотин диспергировали в β-циклодекстрине. Порошки смешивали. Смесь прессовали с помощью подходящего чередующего таблеточного пресса с применением квадратного 16-миллиметрового штампа с дозировкой 1600 мг/таблетку.
Упаковка
Таблетки упаковывали в ленты из алюминия/барекса.
Пример 4
Состав изготовления никотинсодержащей таблетки с ксилитом, маннитом и мятным ароматизатором
1) Приготовление смеси никотин-маннит
Один кг маннита просеивают через сито 50 меш и помещали в смеситель Тонацци. Затем медленно добавляли 10 г никотина при перемешивании в течение 10 минут. Смесь переносили в 2-литровую бутыль из стекла янтарного цвета и перемешивали в течение 15 минут в смесителе Турбула.
2) Приготовление гранулята
50,5 г смеси из вышеприведенного пункта (1) и 654,5 г Xilitab 200 (ксилит) просеивали с помощью сита 20 меш и затем смешивали с 50 г маннита, 5 г стеарата магния, 12,5 г Lubritab (гидрогенизированное растительное масло), 10 г мятного ароматизатора, 7,5 г глицирризината аммония, 7,5 г бикарбоната натрия и 2,5 г карбоната натрия и просеивали через сито 50 меш. Смесь переносили в 2-литровую бутыль из стекла янтарного цвета и перемешивали в течение 15 минут в смесителе Турбула.
3) Приготовление таблеток
Смесь таблетировали в чередующем прессе Беллони, используя штамп на 16 мм2. Вес таблеток составлял 1600 мг/таблетку.
4) Упаковка
Таблетки упаковывали в ленты из бумаги/алюминия/барекса.
Пример 5
Способ изготовления никотинсодержащих таблеток с ксилитом, β-циклодекстрином и мятным ароматизатором
1) Приготовление комплексного соединения никотин-β-циклодекстрин
Исходное количество в 56,76 г β-циклодекстрина помещали в 400-миллилитровый стакан и при перемешивании добавляли 5,68 г H2O (эквивалент 10% порошка). Воду добавляли в количествах по 1,9 г за каждый раз, с перемешиванием в течение 10 минут при каждом этапе. Порошок до добавления никотина был похож на влажный гранулят. Затем очень медленно, при перемешивании добавляли 6,37 г никотина и в конце этого процесса гранулят перемешивали в течение 10 минут. Полученный гранулят высушивали в печи при 35oC в течение 2 часов.
Затем проводили анализ пробы на содержание никотина.
2) Приготовление сухого гранулята
Общее количество из 5,25 г никотин β-циклодекстринового комплексного соединения, 50 г β-циклодекстрина, 5 г стеарата магния, 12,5 г LubritabR (гидрогенизированное растительное масло), 10 г мятного ароматизатора, 7,5 г глицирризината аммония, 7,5 г бикарбоната натрия и 2,5 г карбоната натрия просеивали сквозь сито 80 меш.
Затем сквозь сито 50 меш просеивали 700 г XilitabR 100 (ксилит). Смесь смешивали в смесителе Турбула в течение 20 минут.
3) Приготовление таблеток
Смесь из вышеприведенного пункта (2) таблетировали с помощью таблетирующего пресса Беллони, оснащенного квадратными штампами. Вес таблеток составлял 1600 мг/таблетку.
4) Упаковка
Таблетки помещали в ленты из бумаги/алюминия/барекса, имеющие следующий состав: бумага 50 г/м2, алюминий толщиной 12 мкм, 32 г/м2, барекс 35 г/м2.
Пример 6
Испытание стабильности никотинсодержащих таблеток
Одну никотинсодержащую таблетку растолкли и поместили в 50-миллилитровую мерную колбу. Затем в колбу добавили тетрагидрофуран (25 мл) и колбу перенесли в ультразвуковую ванну, где оставили на 20 минут. Добавили достаточное количество этилацетата для доведения раствора до 50 мл. Часть этого раствора (1 мл) отобрали и пометили в 25-миллилитровую мерную колбу. Затем в эту колбу добавили несколько миллилитров воды и 0,25 мл раствора согласно внутреннему стандарту, состоящего из 50 мг ацетанилида, разбавленного до 100 мл водой. Органические растворители удалили, используя слабый проток газообразного азота, что давало мутный раствор. Затем добавили достаточное количество воды к этому мутному раствору для доведения объема раствора до 25 мл. Раствор затем фильтровали через мембрану 0,22 мкм.
Количество никотина в образце определяли с использованием высокоэффективной жидкостной хроматографии (температура в колонке 30±1oC; подвижная фаза, буфер вода:метанол:ацетат (0,1 М, pH = 4,0):ацетонитрил 60:31:7:2, с доведением до pH = 6,82 триэтиламином, фильтрование и деаэрация; скорость протока подвижной фазы 1,0 мл/мин; твердая фаза Supelcosil LC1808 (5 мкм) 25 сантиметров (см) х4,6 миллиметров (мм), поставляемая фирмой Supelco Inc.; и аналитическая длина волны 254±1 нанометров (нм)). При таких условиях никотин и ацетанилид имели время удержания примерно 7,7 и 9,3 минут, соответственно. Соотношение компонентов в подвижной фазе может быть изменено для обеспечения подходящего времени элюирования для никотина и внутреннего стандарта.
Пример 7
Измерение in vivo выделения никотина из таблетки
Клинические испытания таблетки, описанной в примере 1, проводилось на шести пациентах, каждому из которых давали по одной таблетке на день исследования в 8: 00 утра. Перед каждым приемом отбирают пробу крови. Пациентов просят сосать таблетку. Пробы крови отбирают через 2,5, 5, 7,5, 10, 15, 20, 25, 30, 45, 60, 75, 90, 105, 120 и 240 минут. В дополнение к этому, сразу же после растворения таблетки он сообщает об этом медицинскому персоналу для регистрации времени растворения.
Пробы крови в 5 мл собирают в пробирки с литийгепаринатом. Сразу после сбора пробы охлаждают и центрифугируют при 4oC при 1500 об/мин в течение 15 минут. Затем плазму переносят в полипропиленовые пробирки и выдерживают при -30oC до анализа на никотин и котинин. Для анализа на никотин и котинин используют метод капиллярной газовой хроматографии. Предел обнаружения составляет 0,8 нг/мл для никотина и 5,0 нг/мл для котинина. Предел количественного определения составляет 1,0 нг/мл для никотина и 10 нг/мл для котинина.
Описания в данной заявке всех статей и ссылок, включая патентные документы, включены в настоящее описание путем отсылки.
Необходимо понимать, что вышеприведенное описание служит в качестве иллюстрации и не носит ограничительного характера. Для специалистов в данной области техники многие варианты осуществления будут очевидны при ознакомлении с вышеприведенным описанием. Поэтому рамки данного изобретения должны определяться не со ссылкой на вышеприведенное описание, а должны определяться со ссылкой на прилагаемую формулу изобретения, вместе со всем объемом эквивалентов, к которым относится эта формула изобретения.
Изобретение относится к области медицины, а именно к наркологии. Таблетка содержит никотин в количестве 0,5 - 5,0 мг, адсорбирующий наполнитель, непитательный подсластитель и целевые добавки. Таблетку вводят буккально и осуществляют контроль содержания никотина в крови на уровне 5 - 50 нг/мл. Способ позволяет повысить эффективность лечения. 2 с. и 21 з.п. ф-лы, 2 табл., 2 ил.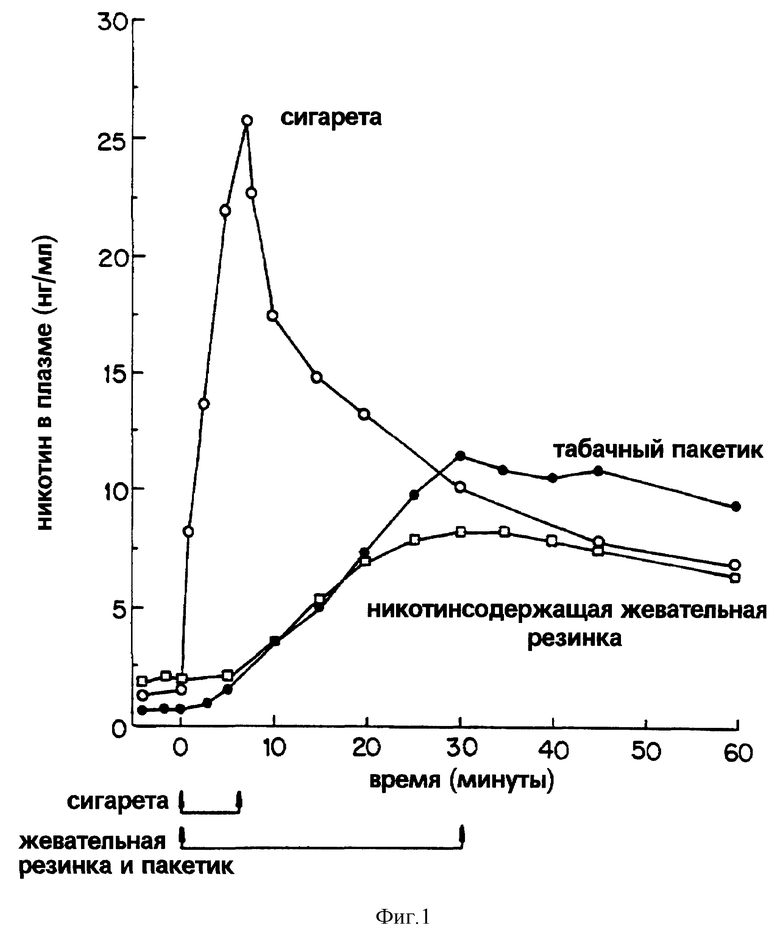
Абсорбирующий наполнитель - 5 - 15
Непитательный подсластитель - 80 - 90
Целевые добавки - Остальное
2. Никотинсодержащая таблетка по п.1, отличающаяся тем, что в качестве целевой добавки она содержит смазывающее вещество.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Огнетушитель | 0 |
|
SU91A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Смирнов В.К | |||
| Результаты клинического применения никоретта в практике лечения курящих табак лиц | |||
| - Вопросы туберкулеза, 1991, 7, стр.40 - 44. | |||
Авторы
Даты
2000-07-27—Публикация
1994-07-20—Подача