Проблема регенерации спинного мозга при его повреждении и дефектах - одна из самых актуальных и малорешенных. Всевозможные микрохирургические операции, направленные на прямое сшивание прерванных концов мозга или использование аутонервной пластики, не приводили к желаемому эффекту - регенерации спинного мозга не происходило. (Г.С. Юмашев "Возможны ли реконструктивные операции при повреждении спинного мозга". Ж. Ортопедия, травматология и протезирование. 1989, N 1, стр. 71 - 75; А.В. Лившиц "Хирургия спинного мозга". Монография. М. Медицина, 1990).
В связи с этим любые попытки каким-то образом способствовать регенерации спинного мозга привлекают внимание многих экспериментаторов и клиницистов.
Известен способ в реконструктивной хирургии спинного мозга с имплантацией сегментов периферического нерва в пространство между отрезками спинного мозга с ориентацией нервов в конец в отношении каждого из отрезков спинного мозга. (Из экспериментальных работ Као и др. 1983 и Дерлона и др. 1983 - цит. по А. В. Лифшиц "Хирургия спинного мозга". Монография. М. Медицина", 1990, стр. 313).
Однако при гистологическом исследовании не было установлено признаков регенерации элементов спинного мозга и констатированы некрозы и кавитация концов отрезков спинного мозга.
Этот способ принят нами за прототип.
Для достижения восстановления функции спинного мозга нами предложен и экспериментально апробирован принципиально новый способ при его повреждении с дефектом.
К моменту подачи заявки на изобретение эксперименты проведены на 62 белых крысах весом от 150 до 200 г. Способ осуществляют следующим образом. После дачи наркоза 1-ым раствором калипсола животное фиксируют на операционном столе в положении на животе. Операционное поле подготавливают в пределах нижней трети грудной клетки и поясничной области. Производят линейный разрез кожи и подкожной клетчатки по ходу остистых отростков от уровня десятого ребра до крестца. Затем производят ламинэктомию на уровне III - IV поясничных позвонков. Все этапы операции выполняют с помощью операционного микроскопа и микрохирургической техники. В рану предлежит спинной мозг. У всех животных спинной мозг резецируют на протяжении 5 мм. После этого производят тугую тампонаду спинно-мозгового канала с целью гемостаза. Из этого же разреза выделяют XI ребро, избегая травмировать плевральную полость. После забора ребра дефект в грудной клетке ушивают кетгутовыми швами.
I-ая серия опытов. Трансплантат длиной 7 мм помещают в образовавшийся дефект спинного мозга таким образом, чтобы проксимальный и дистальный концы спинного мозга упирались в трансплантат. После этого отверстие в спинно-мозговом канале укрывают костно-мышечным лоскутом, содержащим остистые отростки и часть дужек. Рану послойно ушивают наглухо после засыпания ее сухими антибиотиками.
В этой серии опытов на 18 животных использовали только один сегмент ауторебра.
II-ая серия опытов (34 животных). В дефект спинного мозга имплантировали два или три сегмента ауторебра.
III-я серия опытов - контрольная (10 экспериментов).
В этой серии опытов никакой аутопластики спинного мозга не производят, оставляя свободные концы спинного мозга после его резекции. В послеоперационном периоде животные никаких лекарственных препаратов не получают.
Результаты: в 1-й группе животных из 18 выжили только 2 крысы. У этих животных в первые 4-6 дней после операции были явления парапареза задних конечностей, а затем функция их полностью восстановлена в сроки наблюдения до 3 месяцев после операции.
Во 2-ой группе животных из 34 выжили также 2 животных.
Функция задних конечностей у этих животных восстановилась на 7-8 день после операции. В 3-й группе животных контрольной, где никакой пластики не производили, все животные погибли в течение 3 недель после операции.
Мы полагаем, что восстановление функции спинного мозга при наличии его дефекта с замещением реберным трансплантатом происходит потому, что костный трансплантат, упираясь в пересеченные концы спинного мозга, обеспечивает условия для роста нейроглии с прорастанием аксонов в дефект спинного мозга.
Последующее гистологическое исследование показало, что между концами резецированного участка спинного мозга обнаруживается ауторебро, представленное безостеоцитной тканью, а также пролиферирующие клеточные элементы рыхлой соединительной ткани, подверженной постепенному фиброзированию. В краевых участках повреждения спинного мозга обнаружены скопления нервных клеток с гиперпластическими изменениями, о чем свидетельствует значительно увеличенное ядро с формированием в нем нескольких ядрышек, увеличение объема цитоплазмы (фиг. 1). В этих нейронах при иммуногистохимическом исследовании выявляется резко выраженная экспрессия синаптофизина, проявляющаяся в виде интенсивного коричневого окрашивания цитоплазмы (фиг. 2).
Среди элементов постепенно фиброзирующейся соединительной ткани, расположенной между свободными концами поврежденного спинного мозга, встречаются позитивно окрашенные синаптофизином аксоны (фиг. 3). В некоторых участках они формируют ветвящиеся скопления, местами располагаются в виде единичных волокон (фиг. 4).
Таким образом, проведенное исследование дает основание предположительно высказаться о том, что в условиях данного эксперимента за счет внутриклеточной регенерации неповрежденных нейронов осуществляется аксоногенез в области повреждения спинного мозга.
Сама по себе методика операции доступна широкому кругу ортопедов и нейрохирургов, владеющих микротехникой. Она не является более травматичной или опасной в сравнении со многими признанными нейрохирургическими и ортопедическими операциями. И после наших уточняющих морфологических исследований, возможно, появятся достаточные основания для проведения ее у больных, которые по настоящим нашим возможностям являются безнадежными.
Данные об эксперименте.
Повреждение спинного мозга с образованием диастаза между его концами приводит к быстро нарастающим дегенеративно-дистрофическим изменениям и рубцеванию медуллярного вещества.
Одним из факторов, способствующих этим процессам, является оставленные без фиксации поврежденные концы спинного мозга.
Нами предложен метод фиксации концов спинного мозга костно-хрящевой распоркой из ауторебра.
Эксперименты проведены на 78 белых крысах, весом от 180 до 230 г, под 1%-ным калипсоловым наркозом выполняли ламинэктомию на уровне D 11- L 2. После чего резецировали 5 мм спинного мозга и в образовавшийся дефект вводили сегмент ауторебра длиной 7 мм, фиксируя тем самым оба конца пересеченного мозга.
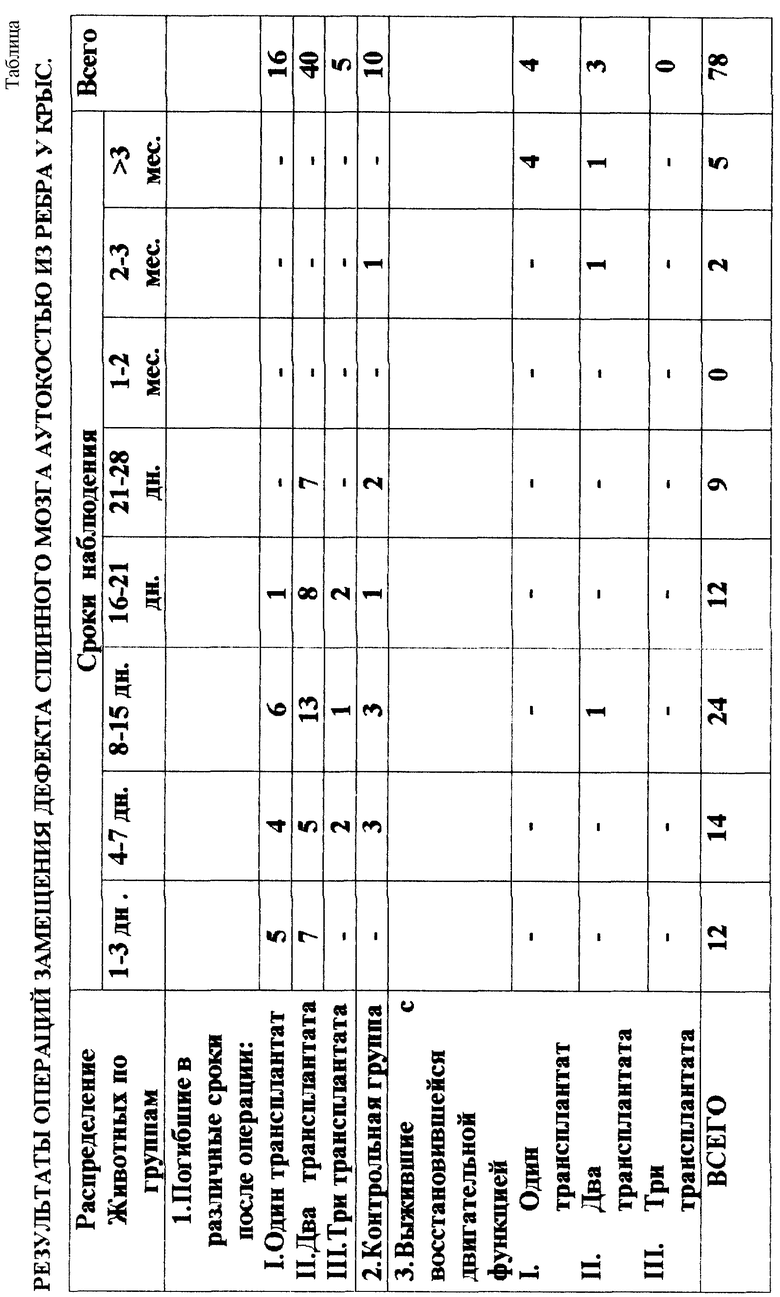
У всех животных сразу после операции развился паралич задних конечностей. 71 животное погибло в сроки до 1 месяца после операции в основном от прогрессирующего паралича задней половины тела. (Табл. 1).
Однако 7 животных выжили, и на 7-9 сутки после операции у них начали восстанавливаться движения в задних конечностях.
Эти животные были забиты в сроки от 9 дней до 3 месяцев.
Проводили гистологическое и иммуногистохимическое исследование области повреждения спинного мозга. Гистологическое исследование показало, что между концами резецированного участка спинного мозга обнаруживается ауторебро, представленное безостеоцитной тканью, а также пролиферирующие клеточные элементы рыхлой соединительной ткани, подверженной постепенному фиброзированию. В краевых участках повреждения спинного мозга обнаружены скопления нервных клеток с гиперпластическими изменениями, о чем свидетельствует значительно увеличенное ядро с формированием в нем нескольких ядрышек, увеличение объема цитоплазмы (фиг. 1). В этих нейронах при иммуногистохимическом исследовании выявляется резко выраженная экспрессия синаптофизина, проявляющаяся в виде интенсивного коричневого окрашивания цитоплазмы (фиг. 2).
Среди элементов постепенно фиброзирующейся соединительной ткани, расположенной между свободными концами поврежденного спинного мозга, встречаются позитивно окрашенные синаптофизином аксоны (фиг. 3). В некоторых участках они формируют ветвящиеся скопления, местами располагаются в виде единичных волокон (фиг. 4).
Таким образом, проведенное исследование дает основание предположительно высказаться о том, что в условиях данного эксперимента за счет внутриклеточной регенерации неповрежденных нейронов осуществляется аксоногенез в области повреждения спинного мозга.




Изобретение относится к области медицины, а именно к нейрохирургии. В дефект спинного мозга длиной 5 мм помещают аутотрансплантат из ребра длиной 7 мм, который плотно контактирует с проксимальным и дистальным его отрезками. Способ позволяет повысить эффективность восстановления функции спинного мозга. 1 табл., 4 ил.
Способ моделирования восстановления функции спинного мозга, включающий трансплантацию, отличающийся тем, что в дефект спинного мозга длиной 5 мм помещают плотно контактирующий с проксимальным и дистальным его отрезками аутотрансплантат из ребра длиной 7 мм.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЙ СПИННОГО МОЗГА | 1992 |
|
RU2050832C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ФУРБЕС С.С., ФРИЕРМАН Л.В | |||
| Способ восстановления проводимости спинного мозга, Невропатология и психиатрия им | |||
| С.С | |||
| Корсакова, 1958, N 8, с | |||
| Радиатор | 1925 |
|
SU857A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| ЯКОВЛЕВА Л.А | |||
| Замещение дефекта спинного мозга гомотрансплантатом седалищного нерва | |||
| Доклады АН СССР, 1954, 98, 6, с | |||
| ДОМКРАТ ДЛЯ ПЕРЕКАТКИ ВАГОНОВ | 1924 |
|
SU1041A1 |
Авторы
Даты
2000-08-20—Публикация
1997-10-22—Подача