Изобретение относится к области медицины, а именно к тканевой инженерии, регенеративной медицине, ортобиологии, экспериментальной травматологии, пластической и восстановительной хирургии и может быть использовано травматологических, ортопедических, хирургических и других стационарах.
Одной из актуальных проблем медицины является регенерация хрящевой ткани, большой практический интерес представляет восстановление любых дефектов гиалиновых хрящей, так как хрящевая ткань обладает крайне ограниченной способностью к спонтанной регенерации в условиях утраты надхрящницы или же при ее отсутствии в норме, например, у суставных гиалиновых хрящей нет надхрящницы. Значение надхрящницы как для физиологической, так и для репаративной регенерации, а также роста хрящей и хрящевых основ костей является основополагающим. В качестве примера, у детей и подростков надхрящница необходима для правильного формирования и роста хрящевой основы черепа (висцерального отдела), что должно обязательно учитываться при проведении реконструктивных операций в области головы и шеи с необходимостью восстановления целостности надхрящницы при хирургии этой области и лечении травм. Регенеративный потенциал надхрящницы - является перспективой для разработки новых стратегий тканевой инженерии хрящей и хрящевых тканей (Gvaramia D, Kern J, Jakob Y, Zenobi-Wong M, Rotter N. Regenerative Potential of Perichondrium: A Tissue Engineering Perspective. Tissue Eng Part В Rev. 2021 Jun 30. doi: 10.1089/ten.TEB.2021.0054. Epub ahead of print. PMID: 33966486).
Перспективными строительными блоками для разработки новых методов тканевой инженерии скелетных тканей являются клеточные сфероиды, которые представляют собой клеточные агрегаты округлой формы. При 3D культивировании клеток в составе сфероидов, например, некоторые стволовые клетки взрослых и клетки соединительной ткани синтезируют внеклеточный матрикс, воссоздавая в искусственных условиях выращивания новые структуры на тканевом уровне (клеточные агрегаты имеют способность накапливать внутри себя элементы внеклеточного матрикса). Сфероиды из стволовых клеток взрослых могут быть рассмотрены как органоиды, поскольку стволовые клетки повторяют пути дифференцировки, и являются перспективной живой моделью тех или иных тканей или органов вне организма для выявления новых молекулярных мишеней (биомаркеров) для диагностики и разработки новых методов терапии. Сфероиды представляют собой новый развивающийся и перспективный подход к клеточной трансплантации, установлено, что клетки, в составе сфероидов более успешно приживляются и интегрируют с организмом реципиента, сфероиды могут участвовать в регенеративных гистогенезах, что не характерно для клеточных трансплантатов в виде суспензии отдельных разрозненных клеток, для которых более характерно проявление паракринного эффекта на окружающие ткани реципиента в области пересадки - сценарий медицинских сигнальных клеток. Сфероиды могут быть непосредственно пересажены в область посттравматических дефектов, либо в комбинации с различными биоматериалами. Клетки, мигрирующие из сфероидов, могут выходить из сфероида и распространяться на поверхность каркаса, причем сфероиды могут взаимодействовать с каркасами (матрицами, скаффолдами) в разных условиях эксперимента in vitrum, в искусственных лабораторных условиях на тканевых или органных культурах, либо при закреплении каркаса-матрицы на реципиентной поверхности в организме-реципиента на живой модели. Сфероиды крайне важны для развития методов биопечати, являются для биопринтинга строительными блоками, продуктами тканевой инженерии, могут входить в состав биочернил. Образуемые конструкции, в которой сфероид взаимодействует со скаффолдом - каркасом, исследуются, уже доказано, что клетки сфероидов мигрируют в каркас от места прилипания сфероида, а сфероиды, например, из стволовых клеток взрослых вероятно могут быть использованы для оптимизации клеточной колонизации в скаффолдах для инженерии хрящей и костной ткани (Baptista LS, Kronemberger GS, Cortes I, Charelli LE, Matsui RAM, Palhares TN, Sohier J, Rossi AM, Granjeiro JM. Adult Stem Cells Spheroids to Optimize Cell Colonization in Scaffolds for Cartilage and Bone Tissue Engineering. Int J Mol Sci. 2018 Apr 25; 19(5): 1285. doi: 10.3390/ijms 19051285. PMID: 29693604; PMCID: PMC5983745).
Известен способ выращивания новой гиалиновой хрящевой ткани в искусственных условиях тканевой культуры, который может быть использован в качестве прототипа. В этом способе коллагеновые матрицы заворачивали в слой надхрящницы. Матрица служит носителем для обеспечения миграции клеток из надхрящницы в матрикс матрицы. Условия тканевого (3D) культивирования в питательной среде полученного конструкта стимулировали рост и пролиферацию клеток. Клетки мигрировали в поры матрикса (матрицы), где они выживали и синтезировали компоненты матрикса, включая коллаген 2-го типа. Было показано при гистологическом исследовании, что после 4 недель культивирования происходит увеличение количества клеточных слоев вокруг матрикса, а также количество клеток, мигрировавших в пористый матрикс самой матрицы. Иммуногистохимическое окрашивание этих культивируемых клеток показало экспрессию коллагена типа II, в том числе обнаруженного и внутриклеточно, что является одним из доказательств неохондрогенеза, так как процесс синтеза коллагена II типа является фенотипическими признаками хондроцита (van Lange JW, de Roo K, Middelkoop E, van den Bos T, Everts V, Nolst Trenite GJ. Perichondrium-wrapped collagenous matrices to induce chondroneogenesis: an in vitro study. Arch Facial Plast Surg. 2001 Apr-Jun; 3(2): 122-6. doi: 10.1001/archfaci.3.2.122. PMID: 11368666).
Известен способ неоморфогенеза хряща путем выращивания бычьих хондроцитов в тесной взаимосвязи с биоразлагаемыми полимерами, состоящими из полигликолевой кислоты и поли-L-молочной кислоты. В этом способе полимерные матрицы засевают свежевыделенными бычьими суставными хондроцитами, а затем имплантируют подкожно голым (иммунодефицитным) мышам. Макроскопическое исследование вырезанных образцов через 12 недель после имплантации (ксенотрансплантации клеток на носителе) выявило наличие нового гиалинового хряща примерно тех же размеров, что и исходная конструкция для подкожного введения из биоразлагаемого полимера. Этот хрящ не проявлял признаков резорбции или разрастания в течение 12 недель эксперимента (Kim W.S., Vacanti J.P., Cima L., Mooney D., Upton J., Puelacher W.C., Vacanti C.A. Cartilage engineered in predetermined shapes employing cell transplantation on synthetic biodegradable polymers. Plast Reconstr Surg. 1994 Aug; 94(2):233-7; discussion 238-40. PMID: 8041813).
На настоящий момент установлено, что спонтанное восстановление хряща на месте его посттравматического дефекта часто отсутствует или является неполным, это обычно медленно текущий процесс. Причины неспособности хрящевой ткани к репаративной регенерации исследуются, считают, что вероятно связаны с особенностями структуры и физиологической природы этой бессосудистой и узкоспециализированной скелетной ткани, содержащей ограниченное количество хондроцитов с медленным их обновлением при физиологической регенерации, как клеточной составляющей. Медленно обновляется и матрикс гиалинового хряща. Продолжаются разработки имплантатов с живыми аутологичными клетками, которые, во-первых, должны быть доступно для практического здравоохранения получаемыми; во-вторых, должны обладать, как минимум, всеми преимуществами аутогенного хряща, например, как при мозаичной хондропластике. Подобные более совершенные, но полученные искусственным путем, тканеинженерные конструкции или живые эквиваленты хрящей активно разрабатываются.
Один из важнейших способов добиться результата в регенеративной медицине скелетных тканей - изучить спонтанную репаративную регенерацию скелета, условия - специальные искусственные условия, при которых она возможна, и попробовать воспроизвести в процессе разработки и осуществления биомедицинской технологии, это, так называемый, биомиметический подход. При этом подходе создаются устройства и способы, в которых достижение технических результатов по восстановлению тканей возможны на основе заимствований идей и основных элементов осуществления механизмов органо-типичной репаративной, либо физиологической регенерации из живой природы.
В гистологии и хирургии давно известно, что реберный хрящ человека способен к полноценной регенерации при определенных условиях. Условием реализации способности гиалинового хряща к полноценному восстановлению на месте посттравматических дефектов с утратой части хрящевой массы этой части ребра является сохранение целостности надхрящницы, покрывающей реберный хрящ в виде чехла, либо наложение швов, восстанавливающих анатомическую форму надхрящницы этот самый покровный чехол, что очень важно для предотвращения врастания регенератов окружающих мягких тканей под надхрящницу. При наличии крупных отверстий в надхрящнице регенераты мягких тканей вместе с новообразованными сосудами быстро заполняют дефект хряща, постепенно превращаясь из рыхлой волокнистой ткани в атипичный соединительнотканный регенерат - рубец, при этом нормальная структура и функции реберного хряща не восстанавливаются, пожизненно остается дефект этого органа. Для регенерации хряща под надхрящницей важно наличие и поддержание свободного пространства для развития полноценного репаративного регенерата. Создание специальных пространств, в которых происходит развитие регенератов, часто осуществляется с помощью ин виво биореакторов.
Регенерация хряща под надхрящницей осуществляется благодаря наличию в ней камбиальных элементов. Содержащиеся в надхрящнице стволовые клетки и прехондробласты активируются, пролиферируют и дифференцируются в хондробласты, которые вырабатывают межклеточное вещество хряща, постепенно заполняющее образовавшийся дефект полноценным регенератом. Очень важно сохранять надхрящницу во время хирургического вмешательства для адекватного послеоперационного заживления и сохранения целостности хряща, как органа. Надо отметить, что клеточные и молекулярно-генетические механизмы полноценной репаративной регенерации реберного хряща человека исследованы недостаточно полно.
Известна животная модель посттравматического восстановления реберного хряща на примере реберного хряща у лабораторных мышей. В известных исследованиях показано, что полная замена резецированного хряща происходит быстро (в течение 1-2 месяцев), клетки регенерата правильно дифференцируются, но обращено внимание, что восстановление происходит спонтанно только при сохранении надхрящницы специальными хирургическими приемами в ходе создания экспериментального дефекта реберного хряща (Srour М.K., Fogel J.L., Yamaguchi K.T., Montgomery A.P., А.K Izuhara, A.L Misakian, S. Lam, Lakeland D.L., M.M Urata, J.S Lee, F.V Mariani Natural Large-Scale Regeneration of Rib Cartilage in a Mouse Model/ J Bone Miner Res. 2015 Feb; 30(2):297-308. https://doi.org/10.1002/ibmr.2326).
В экспериментах на крысах установлено, что надхрящница, пересаженная в дефекты суставного хряща, не только стимулировала регенерацию, но и сама интегрировалась в состав регенератов на хрящевых суставных поверхностях. Трансплантаты надхрящницы развились в суставоподобный гиалиновый хрящ (Dou Z, Muder D, Baroncelli M, Bendre A, Gkourogianni A, Ottosson L, Vedung T, Nilsson O. Rat perichondrium transplanted to articular cartilage defects forms articular-like, hyaline cartilage. Bone. 2021 Oct; 151:116035. doi: 10.1016/j.bone.2021.116035. Epub 2021 Jun 8. PMID: 34111644).
Известна группа изобретений, в которой трансплантат в виде клеточных сфероидов из надхрящницы ребра субъекта, обладает выраженным регенерационным потенциалом и используется для восстановления хряща. Недостатком известного способа является необходимость заполнения всего пространства посттравматических дефектов хряща клеточными сфероидами и их удержанием на месте, что требует подготовки большого количества биомассы аутологичных клеточных культур и решения вопроса об удержании сфероидов в необходимом пространстве определенной формы для восстановления нормальной анатомической структуры хряща в восстанавливаемой части тела. Толщина суставного хряща составляет несколько миллиметров, объем небольшой и легко заполняем, дно дефекта жесткое и надежно держит форму, поэтому данное изобретение направлено в больше степени на ремонт суставного хряща (Ковалев А.В., Родионов С.А. Способ производства клеточных сфероидов для восстановления хрящей. Патент на изобретение 2731314 С1, 01.09.2020. Заявка №2019134905 от 30.10.2019 г.).
Таким образом, несмотря на имеющиеся способы восстановления хрящей, все они характеризуются рядом недостатков и ограничений, а также остается много препятствий, в том числе, связанных с приживлением, участием в тканеспецифической полноценной репаративной регенерации, достаточным питанием и дыханием пересаженных клеток в конструктах, а также удержанием сфероидов в нужном для восстановления тканей месте и формирования регенерата правильной формы и объема в живом организме, это важно для восстановления анатомически правильной формы травмированных органов, восстановления их функций, поэтому сохраняется необходимость в разработке и создании новых способов и подходов к решению указанных проблем.
Задачей изобретения является создание трансплантата - тканеинженерной надхрящницы для восстановления хряща субъекта.
Техническим результатом является обеспечение восстанавление структуры и формы хрящей на месте посттравматических дефектов хрящей за счет инициации репаративной регенерации хрящевой ткани под трансплантатом-тканеинженерной надхрящницей, причем источником клеточной регенерации хряща являются трансплантированные внутри сфероидов клетки, входящих в конструкт, участвующие в регенерационном хондрогенезе.
Технический результат при осуществлении изобретения достигается тем, что предложен трансплантат - тканеинженерная надхрящница для восстановления хряща субъекта, включающий скаффолд и живые клетки, отличающийся тем, что скаффолд представлен пластом донорской децеллюляризованной надхрящницы, на верхней части которого расположены клеточные сфероиды, причем клеточные сфероиды представлены трехмерными агрегатами в форме сфер, состоящими из контактирующих друг с другом аутологичных, предварительно культивированных адгезивных клеток камбиального слоя надхрящницы в количестве 8000 клеток на сфероид, частично слившихся между собой и погруженных в скаффолд, сверху конструкт покрыт слоем геля на основе гиалуроновой кислоты с сурамин содержащими липосомами толщиной 250-500 мкм. При этом субъект представляет собой человека. При этом клеточные сфероиды состоят из аутологичных культивированных мультипотентных мезенхимальных стромальных клеток костного мозга в количестве 6000-8000 клеток на сфероид. При этом гель на основе гиалуроновой кислоты с сурамин содержащими липосомами размещен между скаффолдом с клеточными сфероидами и хрящевой тканью восстанавливаемого хряща, заполняя все свободное пространство. При этом донорская децеллюляризованная надхрящница с расположенными на ее поверхности клеточными сфероидами может быть свернута в форме трубы, где слой клеточных сфероидов расположен на ее внутренней цилиндрической поверхности, а внутреннее пространство трубы заполнено гелем на основе гиалуроновой кислоты с сурамин содержащими липосомами.
Настоящее изобретение также относится к трансплантату - тканеинженерной конструкции для восстановления эластических и гиалиновых хрящей в виде эластичной тонкой пластины на основе донорской децеллюлизированной надкостницы и клеточных сфероидов из аутологичных культивированных клеток надхрящницы, которые из прилипших к матрице надхрящницы сфероидов проникают в децеллюлизированной матрикс, причем при тканевом культивировании сфероиды укладываются со стороны камбиального слоя надхрящницы на ее поверхность, где сливаются между собой (тканевое слияние сфероидов), перед применением на тканеинженерную конструкцию наноситься гель на основе гиалуроновой кислоты с добавлением сурамина на сторону, свободную от сфероидов, тканеинженерная надхрящница может быть сформирована в виде трубы, где просвет трубы заполняется гелем, для восстановления краевых дефектов хрящей гель расположен в сторону реципиентной поверхности для эффективного восстановления хрящей, регенераты которых развиваются от слоя сфероидов.
Тканеинженерная надхрящница по данному устройству объединяет в себе достоинства клеточных сфероидов, которые имеют ряд преимуществ в сравнение с клеточной терапией - введения суспензий отдельных культивированных клеток. Недостатками терапии разрозненными культивированными клетками соединительной ткани являются быстрая гибель клеток после аутотрансплантации в живом организме, невозможность длительного удержания клеток на месте, потеря жизнеспособности из-за ограниченных передачи сигналов от клетки к клетке и взаимодействия клетки с клеточным матриксом, недостижение порога количества клеток, необходимого для хондрогенеза, необходимость длительного взаимодействия с организованным субстратом (внеклеточным матриксом) для целевой дифференцировки.
3D-системы культивирования, в том числе бесскаффолдные технологии, применяемые при выращивании сфероидов лучше воспроизводят межклеточную среду. Основные преимущества применения клеточных сфероидов в тканевой инженерии - это увеличение жизнеспособности клеток в составе сфероидов, микросреда в сфероидах частично приближается к ин виво межклеточному окружению; сфероиды характеризуются высокой клеточной емкостью для реконструкции; большей биосовместимостью; способностью к эффективной механотрансдукции; более выраженной способностью к биоинтеграции с организмом реципиента и способностью к большей пластичности и индуцируемой клеточной дифференцировке. Тканевое слияние сфероидов позволяет объединить сфероиды в более крупную бесскаффолдную тканеинженерную конструкцию, которая, однако, не обладает достаточной механической прочностью для хирургических манипуляций и проблематично удержать форму в течение срока достаточного для участия и реализации морфогенетических процессов, формирования органотипичных регенератов. Донорская обработанная надхрящница выполняет объединяющую роль для сфероидов, обладает свойствами индуктора дифференцировки, и является биоразлагаемым барьером для проникновения в область регенерации окружающих мягких тканей и предотвращает замещение восстанавливаемого пространства тканевого дефекта соединительнотканным рубцом. Толщина конструкции позволяет обеспечить клеточное дыхание и поступление питательных веществ путем диффузии от реципиентной поверхности при трансплантации в живой организм. Крайне важно обеспечить после трансплантации создать благоприятную локальную среду за счет формирования относительно изолированного пространства по типу ин виво биореактора и поддержку требуемого состава этой локальной среды регенерации, способствующей регенеративному хондрогенезу.
В качестве источника клеток для производства сфероидов выбрана надхрящница. Получение клеточной культуры и производство сфероидов из этих клеток осуществлялось согласно известному методу (патент РФ №2731314, «Способ производства клеточных сфероидов для восстановления хрящей»). Взятие надхрящницы осуществляли с реберного хряща в ходе амбулаторной операции под местной анестезией, для бережного отделения и забора надхрящницы от нижележащего хряща под надхрящницу с помощью иглы шприца вводили изотонический раствор, образуя своеобразный купол, который отсекался скальпелем и лоскут надхрящницы сразу переносился в пробирку с транспортной средой. Выделение клеток из надхрящницы реберного хряща производили путем предварительного механического измельчения с последующей ферментативной диссоциацией кусочков тканей. Выделенные клетки надхрящницы высевали в пластиковые культуральные флаконы для адгезивных клеточных культур с питательной средой следующего известного состава, пригодного для культивирования соединительнотканных клеток: DMEM 450 мл, L-глутамин 292 мг, эмбриональная телячья сыворотка 50 мл, пенициллин 100 ед/мл, стрептомицин 100 мкг/мл, при 100% влажности, температуре 37°С, 5% СО2 для получения первичной культуры клеток. Субкультивирование монослойной культуры клеток надхрящницы осуществляли до третьего пассажа со сменой среды каждые 2-3 дня. После третьего пассажа клетки снимали с дна пластиковых культуральных флаконов трипсином/ЭДТА. Полученную клеточную взвесь отмывали от трипсина/ЭДТА, в том числе средой DMEM с 10% сывороткой и с последующим центрифугированием при 200g в течение 10 минут, затем переносили в 81 -луночные агарозные планшеты с диаметром лунки 800 мкм в концентрации до 1,6 миллионов клеток на планшет. Внутри лунок формируются сфероиды в течение 6-7 суток.
Приготовление геля на основе гиалуроновой кислоты (ГК, НА) осуществлялась по известным методикам (Bulpitt, P., Aeschlimann, D. New strategy for chemical modification of hyaluronic acid: Preparation of functionalized derivatives and their use in the formation of novel biocompatible hydrogels (1999) J. Biomed. Матер. Рез. 47, 152-169). Гиалуроновая кислота (Genzyme) химически модифицировали так, чтобы он содержал альдегидные группы (HA-ALD) путем реакции с периодатом натрия и гидразидными группами (HA-ADH) в процессе взаимодействия с адипиновым дигидразидом. Гидрогели ГК получали смешиванием равных объемов 2% (мае. / Об.) водных растворов HA-ALD и HA-ADH. Сурамин (Bayer, Леверкузен, Германия) был включен в свободную (0,4 моль / литр) и инкапсулированную в липосомы (0,4 моль / литр) формы во время гелеобразования. Сураминсодержащие липосомы были получены с использованием ранее описанного метода (Kim S, Turker M.S., Chi E.Y., Sela S., Martin G.M. Preparation of multivesicular liposomes. Biochim Biophys Acta. 1983 Mar 9;728(3):339-48. doi: 10.1016/0005-2736(83)90504-7. PMID: 6824663; Hunziker EB, Driesang IM. Functional barrier principle for growth-factor-based articular cartilage repair. Osteoarthritis Cartilage. 2003 May; 11(5):320-7. doi: 10.1016/s 1063-4584(03)00031-1. PMID: 12744937). Такой гель, как известно, способствует регенеративному хондрогенезу внутри пространства ин виво биоректора, искусственно созданного под надкостницей (гель вводится под надкостницу диафиза длинной трубчатой кости, формируя дополнительное пространство между костью и надкостницей.
Скаффолд децеллюляризованного внеклеточного матрикса был получен из донорской надхрящницы (бык, овца, кролик) из реберного хряща. Такие скаффолды относят к биоматериалам, которые составляют органы или ткани человека или животных - это донорский материал с удалением иммуногенных клеточных компонентов с помощью одной из известных технологий децеллюляризации (Hinderer S. et al. ЕСМ and ECM-like materials - Biomaterials for applications in regenerative medicine and cancer therapy// Advanced Drug Delivery Reviews, Volume 97, 1 February 2016, Pages 260-269, https://doi.Org/10.1016/j.addr.2015.11.019). Каркасы децеллюляризованного внеклеточного матрикса в основном состоят из внеклеточного матрикса, который представляет собой трехмерный каркас, содержащий внеклеточные макромолекулы, такие как коллаген, эластин, фибронектин, ламинин и важные матрицеллюлярные белки. Особенностью подобных технологий является максимальное сохранение физико-химических сигналов и биологических характеристик такого матрикса после децеллюляризации, что обеспечивает получение полезного субстрата биологического происхождения как для механической поддержки, так и биологический 3D-носитель макромолекул для последующего выращивания клеток. Из надхрящницы получается удачный биоматериал, пригодный для пересадок в живой организм, хорошей механической поддержки 3D клеточных культур и при сохранении стабильности каркаса в живом организме на протяжении достаточно длительного времени. Пластинка из такой надхрящницы может быть надежно подшита к надхрящнице, окружающей дефект хряща в живом организме. Такой матрикс был получен методом детергентно-ферментативной децеллюляризации, использовался специальный детергент, содержащих ряд веществ: 1) натриевую соль лаурил-серной кислоты (анионоактивное поверхностно активное вещество, чистящее и смачивающее средство (SDS); 2) Triton X 100 - неионное поверхностно активное вещество (детергент для экстракции ДНК как часть литического буфера); 3) раствор кальция хлорида и магнезии сульфата для активации эндогенных нуклеаз; 4) диоксирибонуклеаза (эндонуклеаза, синтезируется в основном в тканях пищеварительного тракта). В стерильном растворе детергента надхрящница находилась на качающейся платформе 72 часа при 37°С, затем отмывалась в стерильном растворе Рингера и подвергалась ферментной обработке, с последующей отмывкой в стерильных апирогенных физиологических растворах натрия хлорида или Рингера. Скаффолд децеллюляризованного внеклеточного матрикса (ДЦМ) надхрящницы замораживался про -25°С, а затем подвергался сублимационной сушке, причем перед сушкой скаффолд растягивался на прямоугольной рамке для получения в виде расправленного листа. Важно не терять где находиться слой матрикса, ассоциированный с камбиальным слоем надхрящницы, и фиброзным слоем.
Для получения тканеинженерной конструкции ДЦМ укладывается на дно культурального флакона (матрасы для клеточных культур) с поддающейся повторной герметизации боковой крышкой с поверхностью роста 150 см2. Причем сторона ассоциированная с камбиальным слоем надхрящницы располагается сверху. Заливалась культуральная питательная среда температурой 37°С для смачивания и насыщения скаффолда раствором. На лист ДЦМ укладывается стерильное техническое приспособление в виде скрепленных под углом друг к другу четырех стержней прямоугольной формы (боковая сторона - 0,5 мм высотой и две стороны верха и низа по 4 мм длиной) скрепленных между собой под прямым углом из титана, в виде металлической рамы. Рама придавливает ДЦМ ко дну флакона, и образует ограниченное внутренними краями рамы пространство. Клеточные сфероиды в виде суспензии в культуральной питательной среде выливаются в получаемое пространство, ограниченное внутренними боковыми поверхностями рамы. С помощью планки, двигающейся по верхним поверхностям рамы, сфероиды аккуратно распределяются в один слой на ДЦМ под визуальным контролем с помощью лупы бинокулярной медицинской, излишек питательной среды смахивается планкой, сфероиды с помощью пипеток добавляются для формирования сплошного слоя из сфероидов, покрывающих всю верхнюю поверхность ДЦМ, ограниченную внутренними краями рамы из титана. Рама служит не только для сохранения формы ДЦМ, но и обеспечивает возможность в жидкой среде обеспечить плотное покрытие сфероидами ДЦМ, что необходимо для эффективного тканевого слияния клеточных сфероидов между собой. Внутрь культурального флакона для работы с адгезивными культурами клеток аккуратно добавляется культуральная питательная среда (ДМЕМ (или ДМЕМ/Ф12) 450 мл, L-глутамин 292 мг, эмбриональная телячья сыворотка 50 мл, пенициллин 100 ед/мл, стрептомицин 100 мкг/мл, при 100% влажности над слоем питательной среды внутри культурального флакона), в которую вноситься добавка культуральная MSCgo™ Chondro-genic Differentiation Supplement Mix, Biological Industries, в количестве 3 мл добавки на 100 мл питательной среды, что составляет 30% от рекомендуемого производителем количества для индукции хондрогенной дифференцировки мультипотентных стромальных клеток костного мозга). Условия культивирования включают инкубацию ткане-инженерной конструкции с постоянной температурой 37°С под тонким слоем культуральной среды во влажной воздушной атмосфере газовой фазы внутри культурального флакона с добавлением 5% углекислого газа в атмосферный воздух флакона внутри культурального флакона. Смена питательные среды проводят каждый день. Уровень культуральной питательной среды не менее, чем на 750 мкм должен превышать верхний край титановой рамы, удерживающей конструкцию. Количество на поверхности ДЦМ сфероидов зависит от их размера, при диаметре в 400-500 мкм размещают 4 сфероида на 1 мм2 ДЦМ. Культивируют сфероиды в хондрогенной среде в течение 4-6 суток, причем на дне культурального сосуда находится скаффолд, а сверху сфероиды. В этом варианте применения сфероиды представляют собой новый развивающийся подход к клеточной пересадке, и, клетки, мигрирующие из сфероидов, могут диссеминировать и распространяться на поверхность каркаса, в результате чего образуется цельная эластичная конструкция сфероид-каркас, достаточно прочно удерживающая слившиеся сфероиды на своей поверхности.
Клетки этого трансплантата является источником репаративной регенерации хряща, позволяющий воспроизводить биомиметический подход к восстановлению хряща, а именно естественный способ репаративной регенерации хряща под надхрящницей воспроизвести под тканеинженерной конструкцией в пространстве дефекта хрящевой ткани (само пространство дефекта заполняется гелем на основе гиалуроновой кислоты с сураминсодержащими липосомами). Со стороны слоя слившихся сфероидов матрицы надхрящницы должен быть размещен этот специальный гель на основе гиалуроновой кислоты. Такая конструкция позволяет свернуть себя в трубку и быть трансплантирована в живой организм, как в форме трубки, а если не сворачивать, то используется в форме заплатки, края тканеинженерной надхрящницы должны быть подшиты рассасывающимся хирургическим швом к краям надхрящницы вокруг хрящевого дефекта. В живом организме в пространстве, заполненном гелем, формируется регенерат хряща.
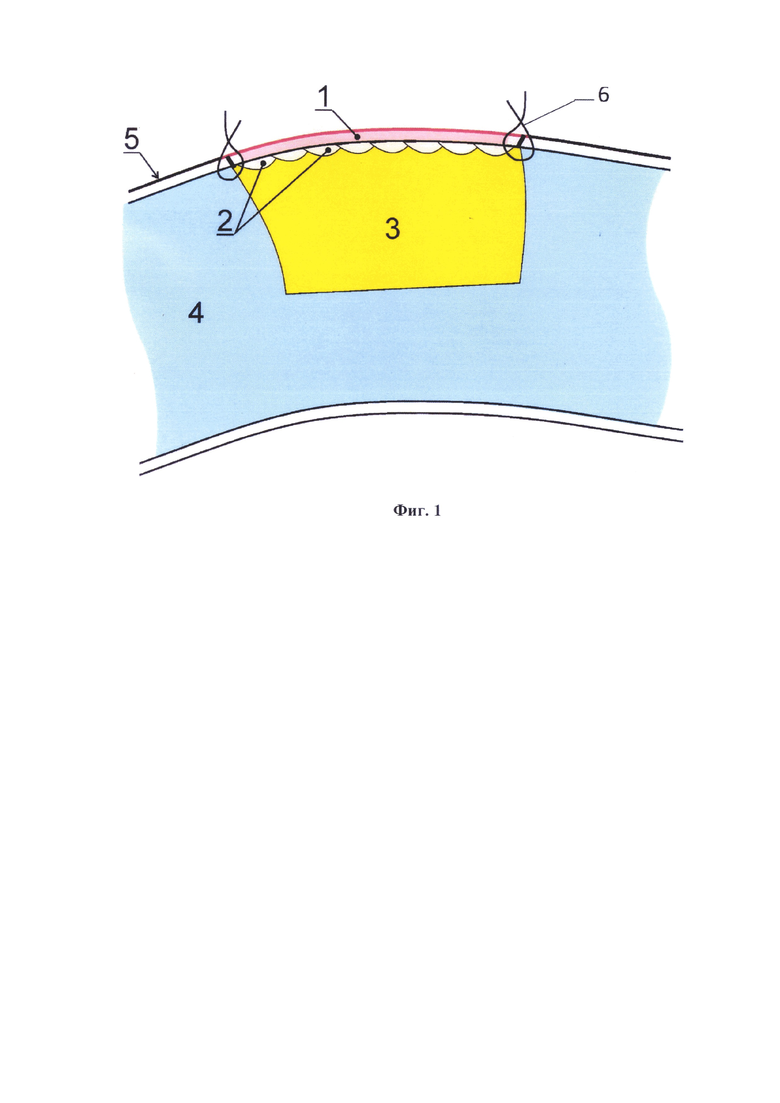
Сущность предложенного трансплантата - тканеинженерной надхрящницы для восстановления хряща субъекта поясняется чертежом, где на фиг. 1 показана принципиальная схема тканеинженерной надхрящницы для восстановления хрящей. На фиг. 1 цифрами обозначены следующие позиции: 1 - децел-люляризованная донорская надхрящница; 2 - аутологичные клеточные сфероиды; 3 - гель на основе гиалуроновой кислоты с добавлением сурамина, заполняющий пространство посттравматического дефекта хряща; 4 - реберный хрящ; 5 - интактная надхрящница вокруг посттравматического дефекта хряща; 6 - хирургический шов.
Сущность предложенного трансплантата - тканеинженерной надхрящницы для восстановления хряща субъекта поясняется примерами осуществления.
Пример 1. У кролика в ходе экспериментальной операции иссекли участок надхрящницы площадью 4 кв. см, провели механическое измельчение и выделение клеток из камбиального слоя надхрящницы собственного реберного хряща, путем ферментной обработки далее клетки выделили из внеклеточного матрикса и их перевели в культуру. В ходе той же операции из гребня подвздошной кости таза с помощью аспирационной иглы забрали костный мозг, выделили мононуклеары костного мозга на градиенте концентрации, затем перевели мультипотентные мезенхимальные стромальные клетки костного мозга в адгезивную культуру. Кролика оставили под наблюдением для последующего моделирования хрящевого дефекта и пересадки тканеинженерной конструкции для полноценного восстановления экспериментального повреждения хряща.
Выделенные клетки раздельно культивировали в адгезивных 2D культурах без хондрогенной дифференцировочной среды на протяжении четырех пассажей в течение 28 дней в базовой питательной среде с добавлением к этой среде 10% тромболизата (PLTGold®, Merck). Далее клетки двух полученных клеточных линий сняли с матрасов и перенесли в пластиковые лунки (неадгезивный пластик) NanoCulture® плиты для 3D-культивирования сфероидов (Corning®), причем на этом этапе перед началом 3D культивирования клетки суспензии клеток 2-х клеточных линий смешивают между собой в соотношении клеток надхрящницы к мультипотентным мезенхимальным клеткам костного мозга 2:1. Клеточный сфероид состоит из 8000 клеток, срок 3D культивирования клеток внутри лунок составляет 7 суток при ежедневном обновлении культуральной питательной среды.
На дно пластикового культурального флакона с боковой дверцей уложили децеллюляризованную и лиофиллизированную аллогенную надхрящницу кролика, сверху на лист этой приготовленной надхрящницы уложили стерильную титановую рама прямоугольной формы (боковая сторона сечения бруска рамы - 0,5 мм высотой и две стороны верха и низа по 4 мм длиной). Суспензию сфероидов в культуральной питательной среде перенесли в пространство ограниченное внутренними стенками металлической рамы, ее размеры позволяют уложить выращенные сфероиды в один ряд, постоянно добавляли суспензию сфероидов и смахивали планкой избыток питательной среды, при этом на 1 мм2 матрицы приходится около 4-х сфероидов. В культуральный флакон заливали питательную среду, состоящую из среда DMEM, без глутамина, сод. глюкозы 4,5 г/л, с HEPES, с пируватом Na 450 мл (ПанЭ-ко), L-глутамина 292 мг, эмбриональной телячьей сыворотки 50 мл, пенициллин 100 ед/мл, стрептомицин 100 мкг/мл, в которую вносили добавку культуральной MSCgo™ Chondrogenic Differentiation Supplement Mix (Biological Industries), для индуцирования хондрогенной дифференцировки в количестве 12,5 мл.
Культивировали сфероиды на ДЦМ аллогенной надхрящницы в хондрогенной среде в течение 4-6 суток, причем на дне культурального сосуда находится этот скаффолд, а сверху сфероиды участвуют во взаимном тканевом слиянии, часть клеток сфероидов проникает в глубь скаффолда, откладывает внеклеточный матрикс, включая коллагеновые фибриллы, что формирует объединяющий конструкцию волоконный остов, способствующий дополнительному удержанию распластанных сфероидов в тканеинженерной конструкции, фактически происходила матурация (дозревание) тканеинженерной конструкции.
Далее в ходе второй последовательной операции под медикаментозным наркозом тому же кролику провели пересадку тканеинженерной конструкции, клетки которой аутологичны для этого животного. Для этого осуществили доступ к хрящевой части ребра. Провели иссечение бокового фрагмента хряща с надхрящницей на 1/2 толщины реберного хряща длиной 1 см. По размеру удаленной надхрящницы произвели выкраивание лоскута тканеинженерной конструкции. Далее с помощью наложения хирургических швов тканеинженерная надхрящница подшили к краям надхрящницы, окружающей дефект хряща. Под подшитую тканеинженерную надхрящницу с помощью шприца пространство послеоперационного дефекта реберного хряща заполнили гелем на основе гиалуроновой кислоты с сурамин содержащими липосомами. Края надхрящницы, к которой подшивается тканеинженерная конструкция, пометили тушевыми метками - красящий пигмент вводили точечно и вдоль хирургических швов на расстоянии в 3 мм. Произвели послойное ушивание раны.
При резекции участка реберного хряща, ограниченного тушевыми метками, у этого же кролика через 4 месяца после пересадки отметили полное восстановление утраченной массы хрящевой ткани, форма хряща полностью восстановлена. При гистологическом исследовании подтвердили образование полноценного регенерата гиалинового хряща на месте послеоперационного дефекта.
Пример 2. Из полученной тканеинженерной надхрящницы иссекли два квадрата с длиной стороны 0,8 см, сшили под операционным микроскопом между собой тонкой шелковой хирургической нитью, соединенной с атравматической хирургической иглой, причем сшивание производили в чашке Петри, заполненной питательной средой DMEM, без глутамина, сод. глюкозы 4,5 г/л, с HEPES, с пируватом Na 450 мл (ПанЭко), L-глутамина 292 мг, 50 мл, пенициллин 100 ед/мл, стрептомицин 100 мкг/мл, с добавлением 50 мл 10% тромболизата (PLTGold®, Merck). Причем слои сфероидов были обращены друг к другу и находились во внутренней части конструкта. С помощью иглы шприца конструкт заполнили между двумя тканеинженерными надхрящницами гелем на основе гиалуроновой кислоты с сурамин содержащими липосомами.
Далее полученный конструкт перенесли в диффузную камеру (EMD Millipore's Diffusion Chamber, Merck) диаметром 13 мм, которую имплантируют под капсулу почки взрослого кролика в ходе экспериментальной операции, причем клетки тканеинженерной конструкции аутологичны для животного. При извлечении диффузной камеры из тела животного на 50 сутки провели гистологическое исследование образца. Обнаружили формирование гиалинового хряща внутри диффузной камеры с тканеинженерной надхрящницей.
Изобретение относится к области биомедицины и биотехнологии. Предложен трансплантат - тканеинженерная надхрящница для восстановления хряща субъекта, включающий скаффолд и живые клетки, отличающийся тем, что скаффолд представлен пластом донорской децеллюляризованной надхрящницы, на верхней части которого расположены клеточные сфероиды, представленные трехмерными агрегатами в форме сфер, состоящими из контактирующих друг с другом аутологичных предварительно культивированных адгезивных клеток камбиального слоя надхрящницы в количестве 8000 клеток на сфероид, частично слившихся между собой и погруженных в скаффолд, сверху конструкт покрыт слоем геля на основе гиалуроновой кислоты с сураминсодержащими липосомами толщиной 250-500 мкм. Изобретение обеспечивает восстановление структуры и формы хрящей на месте посттравматических дефектов хрящей за счет инициации репаративной регенерации хрящевой ткани. 4 з.п. ф-лы, 1 ил., 2 пр.
1. Трансплантат - тканеинженерная надхрящница для восстановления хряща субъекта, включающий скаффолд и живые клетки, отличающийся тем, что скаффолд представлен пластом донорской децеллюляризованной надхрящницы, на верхней части которого расположены клеточные сфероиды, причем клеточные сфероиды представлены трехмерными агрегатами в форме сфер, состоящими из контактирующих друг с другом аутологичных предварительно культивированных адгезивных клеток камбиального слоя надхрящницы в количестве 8000 клеток на сфероид, частично слившихся между собой и погруженных в скаффолд, сверху конструкт покрыт слоем геля на основе гиалуроновой кислоты с сураминсодержащими липосомами толщиной 250-500 мкм.
2. Трансплантат по п. 1, отличающийся тем, что субъект представляет собой человека.
3. Трансплантат по п. 1, отличающийся тем, что клеточные сфероиды аутологичных культивированных мультипотентных мезенхимальных стромальных клеток костного мозга - в количестве 6000-8000 клеток на сфероид.
4. Трансплантат по п. 1, отличающийся тем, что гель на основе гиалуроновой кислоты с сураминсодержащими липосомами размещен между скаффолдом с клеточными сфероидами и хрящевой тканью восстанавливаемого хряща, заполняя все свободное пространство.
5. Трансплантат по п. 1, отличающаяся тем, что донорская децеллюляризованная надхрящница с расположенными на ее поверхности клеточными сфероидами может быть свернута в форме трубы, где слой клеточных сфероидов расположен на ее внутренней цилиндрической поверхности, а внутреннее пространство трубы заполнено гелем на основе гиалуроновой кислоты с сураминсодержащими липосомами.
| LUO Z | |||
| et al | |||
| Comparison of various reagents for preparing a decellularized porcine cartilage scaffold, Am J Transl Res, 2019, vol | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| 1417-1427 | |||
| СПОСОБ ПРОИЗВОДСТВА КЛЕТОЧНЫХ СФЕРОИДОВ ДЛЯ ВОССТАНОВЛЕНИЯ ХРЯЩЕЙ | 2019 |
|
RU2731314C1 |
| РОДИОНОВ С | |||
| А | |||
| и др | |||
| Регенерация хряща в органной культуре с помощью тканевых сфероидов, сформированных из клеток надхрящницы ребра, Гены и Клетки, 2019, т | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
Авторы
Даты
2024-07-03—Публикация
2023-07-21—Подача