Изобретение относится к усовершенствованию способа региоселективной этерификации сахарозы с использованием сложного диэфира дистанноксана в качестве катализатора.
Искусственный подсластитель 4,1',6'-трихлор-4,1'6'-тридеоксигалактосахарозу ("сукралозу") получают из сахарозы путем замещения гидроксилов в положениях 4, 1' и 6' хлором (в способе изготовления подсластителя стереоконфигурация в положении 4 обращена - поэтому соединение является галактосахарозой). Направление атомов хлора только в требуемые положения является главной проблемой синтеза, так как гидроксилы, которые замещаются, обладают различающейся реакционной способностью; два являются первичными, а один является вторичным. Кроме того, синтез осложнен тем, что первичный гидроксил в положении 6 является незамещенным в конечном продукте.
Разработано несколько различных путей синтеза для получения сукралозы, в которых перед хлорированием гидроксилов в положениях 4, 1' и 6' вначале блокируют реакционноспособный гидроксил в положении 6, например, сложноэфирной группой, с последующим гидролизом для удаления сложноэфирного заместителя, чтобы получить сукралозу. Некоторые из таких путей синтеза включают олово-опосредованный (с использованием олова) синтез сложных эфиров сахарозы по положению 6. Иллюстрациями являются олово-опосредованные схемы, которые описаны Navia (патент США N 4 950 746), Neiditch et al. (патент США N 5 023 329) и Walkup et al. (патент США N 5 089 608).
В EP A 0 475 619, опубликованной 18 марта 1992 г., а также в патенте США N 5 470 969 (частичное продолжение заявки США, на которой была основана ЕРА 0 475 619) описан усовершенствованный способ получения сложного эфира сахарозы по положению 6. Данный способ включает проведение реакции сахарозы с ангидридом карбоновой кислоты в реакционной смеси, содержащей полярный апротонный растворитель и 1,3-диацилокси- 1,1,3,3-тетра(гидрокарбил) дистанноксан ("сложный диэфир дистанноксана" или "ДЭДС"), в течение времени и при температуре, которые достаточны для образования сложного эфира сахарозы по положению 6. В одном из своих важных аспектов катализируемый ДЭДС процесс включает стадии:
(1) приготовления первой реакционной смеси, содержащей сахарозу, полярный апротонный растворитель, второй растворитель, способный удалять воду путем совместной перегонки, и 1,3- диацилокси-1,1,3,3-тетра(гидрокарбил)дистанноксан;
(2) проведения совместной перегонки указанной первой реакционной смеси с целью удаления воды, образуя таким образом вторую реакционную смесь; и
(3) добавления ангидрида карбоновой кислоты к указанной второй реакционной смеси для образования третьей реакционной смеси и поддержания указанной третьей реакционной смеси при температуре и в течение времени, достаточных для того, чтобы получить сложный эфир сахарозы по положению 6.
Данное изобретение включает в себя усовершенствование данного аспекта катализируемого ДЭДС способа.
В широком смысле, в изобретении предлагается способ, который включает пропускание паров растворителя, способного удалять воду посредством совместной перегонки, через реакционную смесь, содержащую (a) полярный апротонный растворитель и (b) сахарозу и 1,3-диацилокси-1,1,3,3-тетра(гидрокарбил)дистанноксан и/или продукт реакции сахарозы с 1,3-диацилокси-1,1,3,3- тетра(гидрокарбил)дистанноксаном, в достаточных количествах и в течение времени, достаточного для удаления, по существу, всей воды из указанной реакционной смеси путем совместной перегонки.
По одному аспекту в изобретении предлагается способ, который содержит стадии:
(1) приготовления первой реакционной смеси, содержащей сахарозу и полярный апротонный растворитель, и необязательно нагревания указанной первой реакционной смеси путем пропускания паров второго растворителя, способного удалять воду путем совместной перегонки, через указанную первую реакционную смесь;
(2) добавления 1,3- диацилокси-1,1,3,3-тетра(гидрокарбил) дистанноксана в указанную первую реакционную смесь с образованием второй реакционной смеси;
(3) пропускания паров второго растворителя, способного удалять воду посредством совместной перегонки, через указанную вторую реакционную смесь, в достаточном количестве и в течение времени, достаточного для удаления, по существу, всей воды из указанной реакционной смеси путем совместной перегонки, с образованием посредством этого третьей реакционной смеси, содержащей указанный полярный апротонный растворитель и указанный второй растворитель, причем указанная вторая реакционная смесь, по существу, не содержит воду; и
(4) добавления ангидрида карбоновой кислоты к указанной третьей реакционной смеси для образования четвертой реакционной смеси и поддержания указанной четвертой реакционной смеси при температуре и в течение времени, достаточных для получения сложного эфира сахарозы по положению 6.
Способ по изобретению является усовершенствованным в одном важном аспекте способа, в котором проводят реакцию сахарозы с ангидридом карбоновой кислоты в реакционной смеси, содержащей полярный апротонный растворитель и сложный диэфир дистанноксана, в течение времени и при температуре, достаточных для получения сложного эфира сахарозы по положению 6. По данному способу (a) готовят первую реакционную смесь, которая содержит сахарозу и полярный апротонный растворитель. Первую реакционную смесь необязательно нагревают путем пропускания паров второго растворителя, способного удалять воду путем совместной перегонки, через первую реакционную смесь. На второй стадии (b) к первой реакционной смеси добавляют ДЭДС для образования второй реакционной смеси, (c) через вторую реакционную смесь пропускают пары второго растворителя (такого как циклогексан), способного удалять воду путем совместной перегонки, в достаточном количестве и в течение времени, достаточного для удаления воды, с образованием третьей реакционной смеси, содержащей полярный апротонный растворитель и второй растворитель, причем полученная третья реакционная смесь, по существу, не содержит воды, и (d) к третьей реакционной смеси добавляют ангидрид карбоновой кислоты с получением четвертой реакционной смеси, которую поддерживают при температуре и в течение времени, которые достаточны для получения сложного эфира сахарозы по положению 6.
Стехиометрическое отношение (моль:моль) ДЭДС:сахароза не является очень критичным. Например, можно использовать отношения в интервале от примерно 0.10 до примерно 1.5 мольных эквивалентов (на основе сахарозы), что приводит к выходам сложного эфира сахарозы по положению 6 в интервале от примерно 35% до примерно 80%. Лабораторные результаты показывают, что выходы сложного эфира сахарозы по положению 6 увеличиваются с ростом стехиометрического количества ДЭДС вплоть до примерного отношения сахароза: ДЭДС около 1:1. Было показано, что при применении в данном способе эффективными являются как 1,3-диацетокси-1,1,3,3- тетрабутилдистанноксан (дистанноксандиацетат или "ДСДА"), так и 1,3-дибензоилокси-1,1,3,3-тетрабутилдистанноксан (дистанноксандибензоат или "ДСДБ").
Полярные апротонные растворители, которые использовали, включают N,N-диметилформамид ("ДМФ") и N-метил-2-пирролидон. Другие пригодные растворители включают диметилсульфоксид, N,N-диметилацетамид и гексаметилфосфорамид.
Можно использовать стехиометрические отношения ангидрида карбоновой кислоты в интервале от примерно 1 до примерно 4 мольных эквивалентов (на основе сахарозы). Предпочтительные стехиометрические отношения находятся в интервале от примерно 1.1 до примерно 1.8 мольных эквивалентов. Стехиометрические отношения ниже примерно 1.1 мольного эквивалента могут привести к нежелательному количеству непрореагировавшей сахарозы в конечном продукте, в то время как отношения выше примерно 1.8 могут вызвать образование нежелательных сложных диэфиров сахарозы.
Было обнаружено, что пригодными являются температуры реакции ацилирования в интервале от примерно -10oC до примерно 60oC. Конкретные используемые температуры реакции не являются узким критическим аспектом изобретения, хотя температура реакции ацилирования влияет на скорость ацилирования, и излишне высокие температуры могут увеличить образование нежелательных сложных эфиров сахарозы. Предпочтительные температуры ацилирования находятся в интервале от примерно 0oC до примерно 45oC. В указанном температурном диапазоне от 0oC до 60oC реакция ацилирования обычно протекает от примерно 1/4 часа до примерно 6 часов.
Показано, что и уксусный ангидрид, и бензойный ангидрид являются эффективными ацилирующими агентами. Предпочтителен уксусный ангидрид в основном по экономическим причинам, а также потому, что для применения в реакции с сахарозой дистанноксандиацетат является предпочтительным над дистанноксандибензоатом (этот факт будет обсуждаться ниже более подробно). Ожидается, что в практике изобретения эффективно будут выступать многие другие ангидриды карбоновых кислот. Примерами таких других ангидридов являются ангидриды замещенной бензойной кислоты (например, 4-нитробензойная кислота, 3,5-динитробензойная кислота, и т.п.); алкановых кислот, таких как пропионовая кислота, масляная кислота, циклогексанкарбоновая кислота; длинноцепных жирных кислот, как насыщенных, так и ненасыщенных, таких как стеариновая кислота, олеиновая кислота, линолевая кислота, и т.п., имеющие, например, до 28 углеродных атомов; ненасыщенных кислот, таких как акриловая кислота и метакриловая кислота; замещенных кислот, таких как хлоруксусная кислота, цианоуксусная кислота, феноксиуксусная кислота, и т.п.
Скорость ацилирования зависит от нескольких переменных, которые включают стехиометрию катализатора (увеличение концентрации катализатора относительно сахарозы повышает скорость ацилирования). Активность катализатора (например, оказалось, что ДСДА является более активным катализатором, чем ДСДБ), реакционную способность ангидрида карбоновой кислоты (например, уксусный ангидрид является более реакционноспособным, чем бензойный ангидрид) и температуру реакции, а также относительную концентрацию реакционноспособных частиц (так как ацилирование является процессом множественного порядка).
ДЭДС можно регенерировать для повторного использования по способу Vernon et al. , патент США N 5 034 551. (В данном случае ДЭДС можно использовать в регенерированном виде; Vernon et al. предполагали превращение ДЭДС в диалкоксид дистанноксана или в оксид ди(гидрокарбол)олова). Смесь ацилирования обрабатывают небольшим количеством воды и ДЭДС экстрагируют, по существу, количественным образом путем контактирования смеси с углеводородом, таким как толуол, циклогексан, н-гептан, 2,2,4-триметилпентан или их смесями, или с простым эфиром, таким как диэтиловый эфир, ди-н-пропиловый эфир, метил-трет-бутиловый эфир, и т.п. Рециркулирование ДЭДС выгодно по экономическим причинам, поскольку большую долю разновидностей олова можно регенерировать для повторного применения, а также по технологическим причинам, поскольку уменьшается обращение с твердыми веществами (то есть ДЭДС регенерируется в растворе).
После удаления ДЭДС для рецикла реакционная смесь содержит сложный эфир сахарозы по положению 6, карбоновую кислоту (ту, которая образовалась путем реакции ангидрида карбоновой кислоты с сахарозой, плюс ту, которая может образоваться путем реакции избытка ангидрида с водой, которую добавили на вышеописанной стадии экстракции ДЭДС), некоторое количество непрореагировавшей сахарозы, небольшое количество других сложных эфиров сахарозы, а также полярный апротонный растворитель. Перед дальнейшей обработкой сложного эфира сахарозы по положению 6 предпочтительно удалить карбоновую кислоту из раствора сложного эфира сахарозы по положению 6 в полярном апротонном растворителе. Это можно осуществить, например, упариванием в вакууме, когда кислота является относительно летучей, такой как уксусная кислота. Если требуется дополнительно обрабатывать сложный эфир сахарозы по положению 6 в том же самом растворителе, то во время операции выпаривания можно добавлять свежий полярный апротонный растворитель. (Например, если растворителем является ДМФ и следующей стадией будет хлорирование по способу Walkup и др.). Затем требуемый сложный эфир сахарозы по положению 6 в оставшемся полярном апротонном растворителе можно использовать непосредственно в последующей обработке или, необязательно, его можно регенерировать по обычным методикам, таким как кристаллизация из растворителя, такого как метанол. Примеси углеводов, которые обычно присутствуют (непрореагировавшая сахароза и другие сложные эфиры сахарозы), не влияют вредным образом на хлорирование сложного эфира сахарозы по положению 6 с получением сложного эфира сукралозы по положению 6.
Вторые растворители, которые способны удалять воду посредством совместной перегонки, включают насыщенные углеводороды, ароматические углеводороды, хлорированные углеводороды, кетоны и простые эфиры. Очень широкий круг вторых растворителей пригоден для использования в изобретении. Основные категории для второго растворителя заключаются в том, чтобы он образовывал смесь с полярным апротонным растворителем, ДЭДС и сахарозой, которая кипит с обратным холодильником при внутренней температуре реакции в интервале от примерно 75oC до примерно 153oC (и предпочтительно ниже 100oC, для того, чтобы свести к минимуму термическое разложение сахарозы), чтобы он совместно перегонял воду, присутствующую в реакционной смеси, и чтобы он не делал нерастворимыми основные компоненты реакции (например, сахарозу).
Предпочтительны вторые растворители, которые не смешиваются с водой и которые образуют кипящий при минимальной температуре азеотроп постоянного состава с водой, однако для эффективного использования в изобретении второй растворитель не должен быть способен образовывать с водой азеотроп с постоянной точкой кипения и с постоянным составом. Также не является необходимым то, чтобы второй растворитель не смешивался с водой. Необходимо только, чтобы второй растворитель был способен совместно перегоняться с водой из реакционной среды. Источником воды во второй реакционной смеси являются малые количества воды, присутствующей в сахарозе и в полярном апротонном растворителе, и вода, которая образуется (путем реакции, которая не охарактеризована полностью) за счет взаимодействия сахарозы и ДЭДС. Несмотря на взаимодействие ДЭДС с сахарозой, в способе по изобретению, ДЭДС называется "катализатором", так как его можно регенерировать как ДЭДС в конце процесса.
Постулируется, что в способе по изобретению происходит следующая последовательность реакций, в которой для иллюстративных целей используется 1,3-диацетокси-1,1,3,3-тетрабутилдистанноксан (ДСДА) как сложный диэфир дистанноксана и уксусный ангидрид как ацилирующий агент.
Сахароза и ДСДА реагируют с образованием аддукта сахароза/станноксан (1) и гидроксида дибутилолова (2):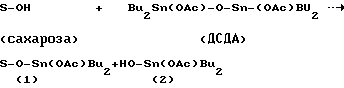
Известно, что гидроксиды алкилолова легко дегидратируются с образованием дистанноксанов. A.J.Bloodworth и A.G.Davies, Глава 4, в Organotin Compounds (Оловоорганические соединения), ред. А.К.Sawyer, Marcel Dekker, NY 1971. В результате, 1 мольный эквивалент (2) конденсируется с образованием по 1/2 мольному эквиваленту воды и ДСДА. Это является источником воды, образованной путем реакции сахарозы с ДЭДС. По завершении реакции сахарозы с ДСДА реакционную смесь охлаждают, добавляют ацилирующий агент, и происходит следующая реакция:
S-O-Sn(OAc)Bu2 + Ас2О --> S-6-A + Bu2Sn(OAc)2
(1) + уксусный ангидрид --> ацетат сахарозы по положению 6 + диацетат дибутилолова
Сообщается, что диацетатдибутил олова гидролизуется в воде и приводит к ДСДА и уксусной кислоте. M.G.Muralidhara и V. Chandrasekhar, Ind. J. Chem., 1991, 30, 487. Таким образом, если используют ДСДА и уксусный ангидрид (как в проиллюстрированной выше серии реакций), то ДСДА выделяется неизменным после добавления воды (гашения) к реакционной смеси после того, как реакция ацилирования завершена. Если, например, используют ДСДА и бензойный ангидрид, тогда выделяется монобензоилокси-, моноацетат оксисоединения дибутилолова (или его димер, аналог исходного сложного диэфира дистанноксана).
По соображениям химической стойкости, эффективности удаления воды, стоимости и температуре кипения предпочтительные вторые растворители включают толуол, циклогексан, н-гептан и изооктан (2,2,4-триметилпентан). Предпочтительная температура дегидратации находится в диапазоне от примерно 85oC до примерно 105oC. Температуры ниже примерно 85oC могут привести к излишне медленной дегидратации, в то время как температуры выше примерно 105oC могут привести к значительному разложению сахарозы.
Главным вкладом данного изобретения является стадия осуществления удаления воды путем пропускания (барботирования) второго растворителя в виде пара через вышеописанную вторую реакционную смесь в достаточном количестве и в течение времени, достаточного для удаления воды. Пары второго растворителя пропускают через вторую реакционную смесь, чтобы удалить, по существу, всю воду из этой реакционной смеси. Удаление воды продолжают до тех пор, пока, например, отношение олово/вода не будет между примерно 20/1 и примерно 35/1 вес/вес. Измерение для олова представляет собой % олова самого по себе, а не % ДЭДС, измеряемый методом рентгенофлуоресценции, а воду измеряют как % воды по анализу Карла Фишера.
Следующие эксперименты иллюстрируют изобретение.
Схема оборудования
Реакторная система (размера пилотной установки) включала перемешиваемый реактор с рубашкой, соединенный с петлей циркуляции, кипятильник для циклогексана, систему регенерации пара и систему подачи твердых веществ. Петля циркуляции состоит из насоса и теплообменника. Кипятильник для циклогексана состоит из автоклава, соединенного с петлей циркуляции, которая имеет насос и теплообменник, а также паровой линии, которая соединена через барботер с реактором. Система регенерации пара состоит из парового конденсатора и отстойного бака с насосами для отвода тяжелой и легкой фаз. Система подачи твердых веществ состоит из вибрирующей загрузочной воронки и шнекового транспортера.
Поток циклогексана в системе происходит следующим образом: циклогексан перегревают в кипятильнике до 20 фунт/кв. дюйм (138 кН/м2). Затем перегретые пары циклогексана поступают в реактор через барботер, контактируют с реакционной смесью и протекают сверху в конденсатор. (Пары циклогексана в данном случае перегреты, так как требуемая температура реакции превышает нормальную точку кипения циклогексана. Специалист сможет определить конкретную требуемую температуру пара второго растворителя в индивидуальных случаях, основываясь на требуемой температуре реакции, скоростях теплопереноса, удельной теплоемкости пара конкретного второго растворителя и других подобных факторов, которые хорошо известны инженерам-химикам и технологам). Сконденсированные пары протекают в отстойный бак, где разделяют две несмешивающиеся фазы [(1) вода/ДМФ - тяжелая; (2) циклогексан - легкая]. Извлеченный циклогексан перекачивают в кипятильник для циклогексана, а воду/ДМФ собирают в поддоне (то есть в переносном приемнике для сконденсированной жидкости).
Испытание
Циклогексан загружают в кипятильник и начинают циркуляцию. Реактор загружают 390 кг ДМФ и перемешивают. ДМФ нагревают до 45oC, используя 33% водный пропиленгликоль в рубашке в качестве теплообменной среды. Затем через систему подачи твердых веществ в реактор загружают 70 кг сахарозы. Реактор нагревают до 85oC и сахарозу оставляют растворяться. Как только сахароза была в растворе, реактор нагревают до 105oC (внутренняя температура), используя рубашку. Циклогексан перегревают в кипятильнике до 20 фунт/кв.дюйм (138 кН/м2). По достижении температуры пары циклогексана начинали подавать в реактор через барботер. Пары циклогексана из реактора конденсируют, собирают в отстойном баке и откачивают назад в кипятильник.
Когда реактор был при нужной температуре и к нему протекали пары, в реактор в течение примерно 15 минут добавляли концентрированный ДСДА в циклогексане (122,7 кг ДСДА; 74,66 вес.% ДСДА/25,44 вес.% циклогексана) при комнатной температуре и начинали отсчитывать время реакции. Во время добавления ДСДА температура упала до 94oC, однако она вернулась к температуре реакции 97oC в течение 10 минут. После этого линию концентрированного ДСДА промывали струей 51 кг ДМФ. Во время реакции расход циклогексана поддерживали при примерно 1400 кг/ч, а температуру реактора - при примерно 97oC. Взаимодействие между сахарозой и ДСДА завершалось (отслеживание по отношению олово/вода) через 60 минут. Благодаря временным задержкам при отборе проб и анализе реакция продолжалась 98 минут. После этого кипятильник для циклогексана закрывали, начинали перемешивание в реакторе и реактор охлаждали до 0oC с использованием цепи циркуляции, охлаждаемой 33% водным пропиленгликолем.
Когда реактор находился при 0oC, в цепь циркуляции реактора в течение 15 минут загружали 24,1 кг уксусного ангидрида. Реакцию ацетилирования поддерживали при 0oC в общей сложности 360 минут. В конце времени выдерживания раствор гасили 21,7 кг воды и выдерживали в течение 30 минут. Конечный профиль углеводов был следующим: 86,01% S-6-A/S-2-А (ацетат сахарозы по положению 6/ацетат сахарозы по положению 2), 11,75% S-D-A (диацетат сахарозы), 0,59% S-M-A (другие моноацетаты сахарозы) и 1,65% сахарозы.
Отношение S-6-A/S-2-A (ацетат сахарозы по положению 6/ацетат сахарозы по положению 2) обычно составляет около 18:1, что соответствует выходу S-6-A самого по себе около 81,5% и S-2-A - 4,5%.
Альтернативный способ
Другой способ получения S-6-A заключается в том, чтобы растворить сахарозу при 85oC, затем нагреть раствор до 105oC и добавить в течение примерно 15 минут концентрированный ДСДА. Во время добавления ДСДА температура реактора обычно падает до примерно 92oC и требуется нагрев обратно до температуры реакции 97oC с использованием рубашки. Когда реактор находится при требуемой температуре, начинают подавать пары циклогексана и отсчитывать время реакции. За протеканием реакции наблюдают путем отслеживания отношения олово/вода. Когда дегидратация завершена, реактор охлаждают и проводят ацетилирование при 0oC, а затем гасят, как обсуждалось выше. Хотя по данному способу достигаются сравнимые качество и выход продукта, происходит увеличение времени реакции сахароза/ДЭДС от 60 минут до примерно 90 минут и увеличивается общее время, в течение которого углеводы подвергаются воздействию повышенных температур.
Основное отличие между этими двумя способами относится к общему времени цикла реакции, на которое, в свою очередь, воздействует последовательность нагрева и используемый режим. По первому способу использовали введение паров циклогексана, для того, чтобы поддерживать внутреннюю температуру во время ввода оловоорганического соединения (ДЭДС). По второму способу систему барботирования включали только после введения всех реагентов и приведения их в равновесие при надлежащей температуре, что достигалось путем нагрева рубашки. Чистый результат состоит в том, что последний режим нагрева является более медленным. Хотя создается впечатление, что это не влияет отрицательно на выход или качество, имеет значение то, что за данное время на одном и том же оборудовании можно провести меньше загрузок, и поэтому затраты на оборудование для фиксированного объема производства соответственно увеличиваются.
Способ по уровню техники
Другой способ (способ уровня техники) получения S-6-А заключается в том, чтобы растворить сахарозу при 85oC, нагреть ее до 105oC, используя петлю циркуляции и нагрев паром, а затем добавить концентрированный ДСДА. Во время добавления ДСДА температура реактора обычно падает до примерно 90oC и требуется нагрев обратно до температуры реакции 97oC с использованием теплообменника. За ходом реакции наблюдают путем отслеживания отношения олово/вода. Когда дегидратация завершена (путем совместной перегонки с циклогексаном, но с использованием нагрева рубашкой, а не нагрева с помощью барботирования паров циклогексана через реакционную смесь), реакционную смесь охлаждают и ацетилируют, выдерживают в течение трех часов и гасят так, как обсуждалось выше.
Данный способ приводит к качеству продукта, который обычно содержит около > 3% оставшейся сахарозы, к небольшому снижению выхода, к увеличению времени реакции от 60 до 120 минут и к увеличению общего времени, в течение которого углеводы подвергаются воздействию повышенных температур.
Вследствие теплочувствительности и потенциальной обратимости реакции между ДЭДС и сахарозой вследствие реакции с водой продукта взаимодействия ДЭДС-сахароза существует необходимость мягкого нагрева и эффективной совместной перегонки для удаления воды. Эта потребность удовлетворяется путем энергичного контактирования паров растворителя для совместной перегонки, которые барботируют во вторую реакционную смесь. Кроме того, время, в течение которого реакционная смесь находится при повышенной температуре, определяет величину разложения углеводов. Путем регулирования порядка добавления (то есть, добавляя ДЭДС после того, как началось барботирование парами растворителя для совместной перегонки), что позволяет реакции протекать во время восстановления температуры реактора после добавления ДСДА, и в связи с идеей барботируемых паров, время пребывания при повышенной температуре значительно снижено, что имеет результатом достижение высокого более воспроизводимого выхода. В случае способа по уровню техники после добавления ДСДА система должна быть повторно нагрета до температуры реакции перед тем, как можно начинать удаление воды. Это приводило к увеличенным промежуткам времени пребывания при повышенной температуре.
Циклогексан (или другой растворитель для совместной перегонки) нагревают в кипятильнике и впрыскивают его в нижнюю часть реактора, содержащего раствор сахароза/ДМФ. Реакционную смесь нагревают до 105oC путем прямого контакта с циклогексаном. Затем в реактор в течение 15 минут добавляют концентрированный раствор ДСДА при комнатной температуре, что приводит к падению температуры до примерно 94oC. Отсчет времени реакции начинается с начала загрузки ДСДА. Реакция продолжается, пока температура повышается назад до 97oC. Во время реакции пары циклогексана контактируют с продуктами реакции, нагревая и совместно отгоняя образованную воду из системы. Удаление воды из системы является ограничивающей скорость стадией и определяет общее время реакции.
Затем раствор охлаждают до, например, 0oC и ацетилируют. Ацетилирование на холоду помогает гарантировать то, что количество непрореагировавшей сахарозы держится на минимальном уровне. Непрореагировавшая сахароза является нежелательной, так как она непосредственно влияет на выход S-6-A и образует нежелательные хлорированные соединения, которые трудно отделить от сукралозы-6-А во время последующей обработки. Общее время ацетилирования предпочтительно составляет около шести часов или более, чтобы позволить реакции пройти до завершения при низкой температуре.
После ацетилирования реакционную смесь гасят водой, чтобы прогидролизовать весь уксусный ангидрид и регенерировать ДЭДС (предположительно из присутствующего сложного диэфира диалкилолова, как обсуждалось выше). Это гашение осуществляют так, как описано в ЕР А 0 475 619, опубликованной 18 марта 1992 г., и в патенте США N 5 470 969, описания которых включены сюда как ссылки.
Преимуществами способа по данному изобретению являются следующие:
- снижение разложения углевода и увеличенное образование углеводного комплекса (с ДЭДС) посредством совместной перегонки воды с впрыскиваемыми парами растворителя для совместной перегонки, что приводит к снижению времени цикла, вызванному более плотным массопереносом; удаление воды в данном случае является важным фактором, определяющим скорость, и система барботирования удаляет воду более быстрым путем обеспечения более тесного контакта растворителя для совместной перегонки с реакционной массой;
- снижение времени, в течение которого углевод находится при повышенной температуре;
- улучшенное качество продукта;
- улучшенная селективность реакции (улучшенная селективность и улучшенное качество, вероятно, являются следствием лучшего образования комплекса ДЭДС/сахароза и уменьшенного разложения углевода, а не какого-либо улучшения реакции ацилирования);
- уменьшенное количество непрореагировавшей сахарозы.
Описывается способ, который включает 4 стадии: (1) приготовление первой реакционной смеси, содержащей сахарозу и полярный апротонный растворитель, (2) добавление 1,3-диацилокси-1,1,3,3-тетра(гидрокарбил)-дистанноксана в первую реакционную смесь с образованием второй реакционной смеси, (3) пропускание паров второго растворителя, способного удалять воду путем совместной перегонки, через вторую реакционную смесь, в достаточном количестве и в течение времени, достаточного для удаления, по существу, всей воды из указанной реакционной смеси путем совместной перегонки, с образованием посредством этого третьей реакционной смеси, содержащей указанные полярный апротонный растворитель и второй растворитель, причем вторая реакционная смесь, по существу, не содержит воду, и (4) добавление ангидрида карбоновой кислоты к третьей реакционной смеси для образования четвертой реакционной смеси и поддерживания четвертой реакционной смеси при температуре и в течение времени, достаточных для получения сложного эфира сахарозы по положению 6. Технический результат - упрощение процесса, улучшение качества целевого продукта и улучшение селективности процесса. 3 с. и 19 з.п. ф-лы.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО САХАРОЗА-6-ЭФИРА | 1991 |
|
RU2049791C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Радиоизотопный способ исследования материала | 1973 |
|
SU448413A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Шиберный затвор | 1973 |
|
SU454386A2 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения 6-сложных эфиров сахарозы | 1987 |
|
SU1639430A3 |
Авторы
Даты
2000-11-27—Публикация
1996-11-27—Подача