Изобретение касается замещенных производных тетрациклического азепина, обладающих антипсихотическим, сердечно-сосудистым и гастрокинетическим действием, и их приготовления; далее, оно касается содержащих их композиций, а также их использования в качестве лекарственного средства.
Соединения, имеющие подобную структуру, раскрываются в Патенте США 4039558, описывающем пирролидинодибензо-азепин, -оксазепин, - тиазепин и -диазепин производные, обладающие антигистаминным, седативным и антидепрессивным действием. EP-A-О 421823 описывает подобные производные дибензопиразино- или бензо-пиридо-пиразино- азепина, обладающие противоаллергическими и противоастматическими свойствами.
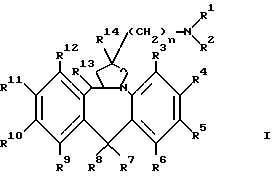
Данное изобретение касается соединений формулы (I)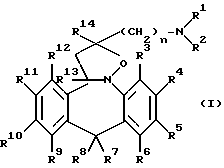
их фармацевтически приемлемых кислых или основных солей присоединения и их стереохимических изомерных форм, а также их N- оксидных форм, где
R1 и R2 каждый независимо представляет собой водород, C1-6алкил, C1-6алкилкарбонил, тригалометилкарбонил, C1-6-алкил, замещенный гидроксилом, C1-6алкоксил, карбоксил, C1-6алкилкарбонилокси, C1-6алкилоксикарбонил или арил; R1 и R2 вместе с азотным атомом, к которому они прикреплены, могут образовывать морфолиниловое кольцо или радикал формулы: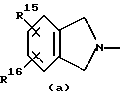



где R15, R16, R17 и R18 каждый независимо представляет собой водород, гало, трифторометил или C1-6алкил;
m представляет собой 1, 2 или 3;
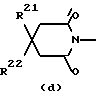
R19, R20, R21 и R22 каждый независимо представляет собой водород или C1-6алкил; или
R21 и R22 вместе могут образовывать двухвалентный радикал C4-5алкандиил;
R23 представляет собой водород, C1-6алкил, C1-6алкилкарбонил, тригалометилкарбонил, C1-6алкилоксикарбонил, арил, ди(арил)метил, C1-6алкил, замещенный гидроксилом, C1-6алкилокси, карбоксил, C1-6алкилкарбонилокси, C1-6алкилоксикарбонил или арил;
R3, R4, R5, R6, R9, R10, R11 и R12 каждый независимо представляет собой водород, гало, циано, гидрокси, трифторометил, трифторметокси, карбоксил, нитро, амино, моно- или ди(C1-6алкил)амино, C1-6алкилкарбониламино, аминосульфонил, моно- или ди(C1-6алкил)аминосульфонил, C1-6алкил, C1-6алкилокси, C1-6алкилкарбонил, C1-6алкилоксикарбонил;
R7 и R8 каждый независимо представляет собой водород, гидрокси, C1-6алкил, C1-6алкокси или R7 и R8 вместе могут образовывать моно- или ди(циано)метилен, двухвалентный радикал формулы -(CH2)2-, -(CH2)3-, -(CH2)4-, -(CH2)5-, -О-(CH2)2-O-, -O2-(CH2)3-О-, или карбонил вместе с атомом углерода, к которому они прикреплены, или
R7 и R8 вместе могут образовывать метилен,
R13 представляет собой водород, C1-6алкил или трифторометил,
n = 0, 1, 2, 3, 4, 5 или 6,
арил представляет собой фенил или фенил, замещенный 1, 2 или 3 заместителями, выбранными среди галогена, гидроксила, C1-6алкила и трифторометила.
В вышеуказанных определениях C1-6алкил представляет собой прямые или разветвленные насыщенные углеводородные радикалы, содержащие от 1 до 6 атомов углерода, такие как, например, метил, этил, пропил, бутил, 1-метилпропил, 1,1-диметилэтил, пентил, гексил; С4-5алкандиил представляет собой двухвалентные прямые или разветвленные насыщенные углеводородные радикалы, содержащие от 4 до 5 атомов углерода, такие, как, например, 1,4-бутандиил, 1,5-пентадиил; "галоген" является общим термином, относящимся к фтору, хлору, брому и йоду. Термин "моноцианометилен" обозначает радикал, имеющий формулу =CHCN, "дицианометилен" обозначает радикал, имеющий формулу =C(CN)2. В том случае, если R7 и R8 вместе образуют двухвалентный радикал, как указано выше, соединения формулы (1) представляют собой спиросоединения.
Термин "фармацевтически приемлемые кислые соли присоединения", указанный выше, означает терапевтически активные нетоксические формы кислых солей присоединения, которые могут быть образованы соединениями формулы (I). Указанные соли могут быть получены путем обработки основной формы соединений формулы (I) соответствующими кислотами, такими как неорганические кислоты, например, гидрогалоидная кислота: соляная, бромистоводородная, серная, азотная, фосфорная и т.п., или органические кислоты, такие как, например, уксусная, гидроксилуксусная, пропановая, молочная, пировиноградная, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, лимонная, метаносульфоновая, этаносульфоновая, бензолосульфоновая, р-толуолсульфоновая, цикламовая, салициловая, р-аминосалициловая, памоевая и т.п. кислота.
Подходящими кислотами являются щавелевая кислота, в частности (R)- или (S)-яблочная кислота и фумаровая кислота, особенно (S)-яблочная кислота.
Соединения формулы (I), содержащие кислотные протоны, могут также быть превращены в их терапевтически активные нетоксичные металлические или аминовые соли присоединения путем обработки соответствующими органическими и неорганическими основаниями. Соответствующие основные соли включают, например, соли аммония, соли щелочных и щелочно-земельных металлов, такие как соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, такие как соли бензатина, Н-метил-D-глюкамина, гидрабамина, и соли с аминокислотами, такие как, например, аргинин, лизин и т.п.
Обратным образом соли могут быть превращены в свободные формы путем обработки соответствующим основанием или кислотой.
Термин "соль присоединения", используемый выше, означает сольваты, которые могут образовывать соединения формулы (I), а также их соли. Такие сольваты включают, например, гидраты, алкоголяты и т.п.
Подразумевается, что N-оксидные формы соединений формулы (I) включают те соединения формулы (I), в которых один или несколько атомов азота окисляются до так называемого N-оксида, особенно те N-оксиды, в которых атом азота, несущий заместители R1 и R2, N-окисляется.
Термин "стереохимически изомерные формы", используемый выше и ниже, охватывает вое возможные изомерные формы, которые могут иметь соединения формулы (I). Если не указано иначе, химическое обозначение соединений означает смесь, особенно рацемическую смесь, всех возможных стереохимически изомерных форм, при этом указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. Предполагается, что стереохимически изомерные формы соединений формулы (I) и смеси таких форм со всей очевидностью представлены формулой (I).
Нумерация тетрациклической кольцевой системы соединений формулы (I), как указано в номенклатуре Химических Рефератов, показана в формуле (I').
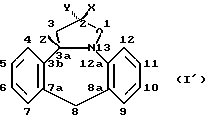
Соединения формулы (I) могут иметь вид "цис" и "транс" изомеров. Указанные термины относятся к положению заместителей на изоксазолидиновом кольце и соответствуют номенклатуре Химических Рефератов. Отличие заключается в том, что атом углерода 3b, являющийся частью кольцевой системы, не считается заместителем, имеющим отношение к атому углерода 3a. При установлении конфигурации принимаются во внимание заместитель на атоме углерода 3a (т.е. "Z") и наиболее приоритетный заместитель на атоме углерода 2 (т.е. "Z" или "Y"). Если "Z" и наиболее приоритетный заместитель на атоме углерода 2 находятся на одной и той же стороне средней плоскости, определяемой изоксазолидиновым кольцом, то конфигурация обозначается как "цис", если нет, то конфигурация обозначается как "транс".
Соединения формулы (I) имеют по крайней мере два симметричных центра, а именно, атом углерода 3а, несущий заместитель R13, и атом углерода 2, несущий заместитель R14. Указанные асимметричные центры и любые другие имеющиеся асимметричные центры, обозначаются буквами R и S. Если часть моноцианометилена присутствует в соединениях формулы (I), указанная часть может иметь конфигурацию E или Z.
Абсолютная стереохимическая конфигурация некоторых соединений формулы (I) не была установлена экспериментально. В таких случаях стереохимически изомерная форма, которая была выделена первой, обозначается как "А", а вторая как "В", без дальнейших ссылок на действительную стереохимическую конфигурацию.
Во всех случаях, описываемых ниже, термин "соединения формулы (I)" также охватывает фармацевтически приемлемые кислотные соли присоединения, основные соли присоединения и все стереоизомерические формы, а также N-оксидные формы.
Особыми группами соединений формулы (I) являются такие группы, к которым применимо одно или несколько следующих ограничений:
a) R1 представляет водород, C1-6алкил; R2 представляет собой водород, C1-6алкил, тригалометилкарбонил, C1-6алкил, замещенный гидроксилом, карбоксилом, C1-6алкилкарбонилоксилом; или R1 и R2 вместе с атомом азота, к которому они прикреплены, образуют радикал формулы (а), в котором R15 и R16 оба представляют собой водород, радикал формулы (b), в котором R17 и R18 оба представляют собой водород, радикал формулы (с), в котором R19 и R20 оба представляют собой водород, радикал формулы (d), в которой R21 и R22 вместе образуют радикал С4-5алкандиил, или радикал формулы (е), в которой R23 представляет собой водород, C1-6алкил, тригалометилкарбонил или арил;
R3, R4, R5 и R6 каждый по отдельности представляет собой водород, галоген, C1-6алкил;
в) R9, R10, R11 и R12 каждый по отдельности представляет собой водород, галоген, C1-6алкил или трифторметил;
г) R7 и R8 оба представляют собой метил или, в частности, водород;
д) R13 представляет собой метил или, в частности, водород;
е) R14 представляет собой метил или, в частности, водород;
ж) n = 1, 2, 3 или 4, в частности, 1;
з) R7 представляет собой метил и R8 представляет собой водород, или R7 и R8 вместе образуют метилен или цианометилен;
и) R1 и R2 вместе с атомом азота, к которому они прикреплены, образуют радикал формулы (е), в котором R23 представляет собой ди(арил)метил.
Особый интерес представляют те соединения формулы (I) или подгруппы, как указывалось выше, в которых один из ароматических заместителей R3, R4, R5, R6, R9, R10, R11 и R12 выбирается из группы, содержащей водород, галоген, C1-6алкил, при этом оставшимся ароматическим заместителем является водород.
Также особый интерес представляют те соединения формулы (I) или подгруппы, как указывалось выше, в которых два или более ароматических заместителей R3, R4, R5, R6, R9, R10, R11 и R12 выбираются из группы, содержащей фтор, хлор или бром, при этом оставшимися ароматическими заместителями является водород.
Наибольший интерес представляют те соединения, в которых ароматические заместители R4, R5 и R11 каждый в отдельности выбираются из группы, состоящей из водорода, фтора, хлора, брома, метила, при этом оставшимися ароматическими заместителями является водород.
Предпочтительными соединениями являются те соединения формулы (I) или подгруппы соединений формулы (I), как указывалось выше, в которых R1 и R2 оба представляют метил, а n=1 или 2.
Также предпочтительными являются те соединения формулы (I) или подгруппы соединений формулы (I), как указывалось выше, в которых R1 представляет собой водород, R2 представляет собой метил, а n=1 или 2.
Наиболее предпочтительными соединениями являются цио-2,3,3а,8-тетрагидро-N, N-диметилдибенз [с, f]изоксазоло[2,3-а]азепин-2-метанамин, их стереохимически изомерные формы и фармацевтически приемлемые кислые соли присоединения, а также их N-оксидные формы.
Далее наиболее предпочтительными являются соединения цис-2,3,3а,8-тетрагидро-N-метилдибенз[с, f] изоксазоло[2,3-а] -азепин-2- метанамин, их стереохимически изомерные формы и фармацевтически приемлемые кислые соли присоединения, а также их N-оксидные формы.
Среди наиболее предпочтительных соединений, указанных выше, особенно предпочтительным является (+)-(А-цис)-2,3,3а, 8-тетрагидро-N,N- диметилдибенз[с,а]изоксазоло[2,3-а]азепин-метанамин (S)-гидроксибутадиоат (1:1).
Интересно отметить, что соединения формулы (I) достаточно легко синтезируются. В общем, они могут быть приготовлены 1,3-диполярным циклодобавлением диенофила формулы (III) и промежуточного соединения формулы (II). В промежуточных соединениях (II) и (III) и в любых других промежуточных соединениях, упоминаемых ниже, если не указано иначе, R1-R14 и n имеют вышеуказанные значения. Указанное 1,3-диполярное циклодобавление может быть легко осуществлено путем смешивания реагентов, возможно, в реакционно-инертном растворителе, таком, например, как ароматический растворитель, т.е. толуол; кетон, т.е. 4-метил-2-пентанон, или в смеси таких растворителей. Помешивание и повышенная температура или высокое давление могут увеличить скорость реакции. Реакция промежуточного соединения (II) с промежуточным соединением (III) на практике местно-выборочным образованием соединений формулы (I).

В этой и последующих процедурах продукты реакции могут быть выделены из реакционной среды и при необходимости подвергнуты дальнейшему очищению в соответствии с общеизвестными методами, такими как, например, экстракция, кристаллизация, растирание в порошок и хроматография.
Соединения формулы (I) также могут быть превращены друг в друга в соответствии с известными превращениями. Например,
а) соединение формулы (I), в котором R1 и R2 вместе с атомом азота, к которому они прикреплены, образуют радикал формулы (b), может быть превращено в соответствующий первичный амин путем обработки гидразином или водной щелочью;
б) соединение формулы (I), где R1 или R2 представляют собой трифторметилкарбонил, может быть превращено в соответствующий первичный или вторичный амин путем гидролиза с помощью водной щелочи;
в) соединение формулы (I), где R1 или R2 представляют собой С1-6алкил, замещенный С1-6алкилкарбонилоксилом, могут быть гидролизованы в соединение формулы (I), где R1 или R2 представляют собой С1-6алкил, замещенный гидроксилом;
г) соединение формулы (I), где R1 или R2 оба представляют собой водород, могут быть алкилированы с помощью моно- или ди-N-алкила в соответствующий амин;
д) соединение формулы (I), где R1 или R2 оба представляют собой водород, могут быть ацилированы с помощью N-ацила в соответствующий амид.
Соединения формулы (I) также могут быть превращены в соответствующие N-оксидные формы в соответствии с известными процедурами превращения трехвалентного азота в его N-оксидную форму. Указанная реакция N-окисления обычно проводится путем реагирования исходного материала формулы (I) с 3-фенил-2-(фенилсульфонил)оксазиридином или с соответствующим органическим или неорганическим пероксидом. Соответствующие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных металлов или щелочно-земельных металлов, например, пероксид натрия, пероксид калия; соответствующие органические пероксиды могут включать перкислоты, такие как, например, бензолкарбопероксоидная кислота или галозамещенная бензолкарбопероксоидная кислота, пероксоалканоловые кислоты, например, пероксоуксусная кислота, алкил-гидропероксиды, например, трет-бутил гидропероксид. Подходящими растворителями являются, например, вода, низшие алканолы, например этанол и т.п., углеводороды, например, толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например дихлорметан, и смеси этих растворителей.
Промежуточные соединения формулы (II) могут быть приготовлены путем окисления соединения формулы (IV) с соответствующим окисляющим веществом, таким как, например, 2-бензол-сульфонил-3-фенил-оксазиридин, пероксид водорода, трет-бутил-гидроперекись или метахлорпербензойная кислота.
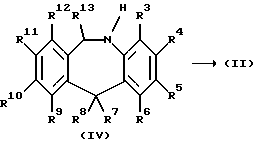
Указанное окисление проводится в реакционно-инертном растворителе при температуре в интервале между -20oC и 50oC, предпочтительно между 0oC и комнатной температурой. Подходящими растворителями являются, например, вода, хлорированные углеводороды, например, дихлорметан или хлороформ; ароматические углеводороды, например, толуол; спирты, такие как метанол; кетоны, например, 4-метил-2-пентанон; или смесь таких растворителей. При использовании пероксидного окислителя скорость реакции может быть увеличена посредством использования металлических катализаторов, таких как, например, Na2WO4, VO(ацетилацетонат)2, Ti(OBu)4, или MoO2(ацетилацетонат)2, возможно, в реакционно-инертной атмосфере, такой, например, как аргон.
Промежуточные соединения формулы (IV) могут быть образованы путем восстановления имина формулы (V) с помощью водорода в сочетании с подходящим катализатором, таким, например, как палладий или платина, нанесенным на древесный уголь; в реакционно-инертном растворителе, таком как, например, тетрагидрофуран, метанол или смесь этих растворителей. Образование имина формулы (V) описывается в J. Chem. Soс. Perk. 1 (1976), 1279.
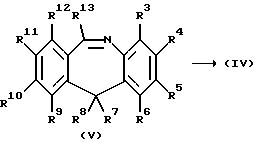
Промежуточные соединения формулы (IV) также могут быть приготовлены путем межмолекулярной циклизации промежуточных соединений формулы (VI) посредством добавления сильной кислоты, такой как, например, серная кислота или фосфорная кислота, возможно, в реакционно-инертном растворителе, к промежуточному соединению формулы (VI).

Чистые стереохимически изомерные формы соединений формулы (I) могут быть получены с использованием известных процедур. Диастереомеры могут быть отделены с помощью физических методов, таких как избирательная кристаллизация и хроматографические процедуры, например, противоточное распределение, жидкостная хроматография и т.п.
Соединения формулы (I), приготовленные в соответствии с вышеописанными процессами, обычно представляют собой рацемические смеси энантиомеров, которые могут быть отделены друг от друга с помощью известных процедур растворения. Рацемические соединения формулы (I), которые имеют достаточную степень основности или кислотности, могут быть превращены в соответствующие диастереометрические соли посредством реакции с соответствующей хиральной кислотой, такой как, например, ди-1,4-толуолил-D-винная кислота, или, соответственно, с подходящим хиральным основанием. Указанные диастереометрические соли затем разделяются, например, с помощью выборочной или фракционной кристаллизации, а энантиомеры высвобождаются с помощью щелочи или кислоты. Альтернативный способ отделения энантиомерических форм соединений формулы (I) включает жидкостную хроматографию с использованием хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы также могут быть получены из соответствующих чистых стереохимически изомерных форм соответствующих исходных материалов при условии, что реакция носит стереоспецифический характер. При получении специфического стереоизомера указанное соединение предпочтительно синтезируется с помощью стереоспецифических методов приготовления. При осуществлении таких методов предпочтительно используются энантиометрически чистые исходные материалы.
Соединения в соответствии с настоящим изобретением показывают сродство с рецепторами 5-НТ2, особенно с рецепторами 5-НТ2A и 5-НТ2C (номенклатура, описанная D. Hoyer в "Serotonin (5-НТ) in neurologic and psychiatric disorders", изданный М. Д.Феррари и опубликованный в 1994 г. Boerhaave Commission Лейденского университета). Далее, соединения в соответствии с настоящим изобретением проявляют интересную фармакологическую активность в "мСРР тесте с крысами", которая описывается ниже, и в (мХФП) "Elevated and Illuminated Plus Maze Test", описываемой в Drug Dev. Res. 18, 119-144 (1989). Кроме того, данные соединения проявляют интересную фармакологическую активность в "Tail Suspension Test", "Combined Apomorphine, Tryptamine, Norepinephrine Test on Rats", описываемых в Arch. Int. Pharnacodyn, 227, 238-253 (1977), a также в "LSD Drug Discrimination Test", описываемом в Drug Dev. Res. 18, 119-144 (1989). Другим интересным свойством соединений формулы (I) является подавление стереотипичного подавления поведения крыс, вызванного амфетамином.
С учетом этих фармакологических свойств, соединения формулы (I) могут быть использованы в качестве лекарственных средств для лечения или профилактики таких расстройств центральной нервной системы, как тревога, депрессия и легкая депрессия, биполярные расстройства, нарушения сна и сексуальные нарушения, психозы, пограничные психозы, шизофрения, мигрень, расстройства, связанные с изменением личности, или навязчиво-компульсивные расстройства, социальные фобии или приступы паники, умственные расстройства у детей, агрессия, расстройства памяти и поведенческие расстройства у пожилых людей, злоупотребления, ожирение, булимия и тому подобные расстройства. В частности, настоящие соединения могут использоваться в качестве анксиолитиков, антидепрессантов и средств, потенциально способных устранять свойства, вызывающие привыкание к лекарственным средствам.
Соединения формулы (I) также могут использоваться как терапевтические средства для лечения моторных расстройств. Предпочтительно использовать данные соединения в сочетании с классическими терапевтическими средствами для лечения подобных расстройств.
Соединения формулы (I) могут также служить для лечения или профилактики нарушений нервной системы, вызванных травмой, ударом, нейродегенеративными заболеваниями и т.п.; сердечно-сосудистыми нарушениями, такими как высокое кровяное давление, тромбоз, удар, и т.п.; и желудочно-кишечные расстройства, такие как дисфункция сократительной способности желудочно-кишечной системы и т. п. Данные соединения могут также быть использованы в качестве противоконвульсивных средств.
Из вышеописанного возможного применения соединений формулы (I) следует, что настоящее изобретение также обеспечивает метод лечения теплокровных животных, страдающих от вышеуказанных заболеваний, который заключается в систематическом введении терапевтического количества соединения формулы (I), действенной для лечения вышеописанных расстройств.
Таким образом, настоящее изобретение также относится к соединениям формулы (I), как указано выше, используемым в виде лекарственного средства, особенно для использования в качестве лекарственного средства для лечения вышеуказанных заболеваний.
Специалисты по лечению подобных заболеваний могут определить эффективное терапевтическое суточное количество, исходя из нижеизложенных результатов теста. Эффективное терапевтическое суточное количество составляет приблизительно от 0,001 мг/кг до приблизительно 10 мг/кг веса тела, предпочтительно, от приблизительно 0,005 мг/кг до приблизительно 1 мг/кг веса тела.
Для облегчения введения данные соединения могут иметь различные лекарственные формы в зависимости от способа введения. Для приготовления фармацевтической композиции согласно данному изобретению, терапевтически эффективное количество отдельного соединения, возможно, в виде соли присоединения, смешивается в качестве активного ингредиента в однородной смеси с фармацевтически приемлемым носителем, которая может иметь самые разнообразные формы в зависимости от желаемого способа введения. Такие фармацевтические композиции желательно должны иметь единичную лекарственную форму, пригодную предпочтительно для орального введения, ректального, через кожу или в виде парентеральных инъекций. Например, для приготовления композиций, имеющих оральную лекарственную форму, можно использовать любую обычную фармацевтическую среду, такую как, например, вода, гликоли, масла, спирты и т.п., для приготовления жидких оральных препаратов, таких как суспензии, сиропы, эликсиры и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазывающие и связующие вещества, вещества, вызывающие распад, и т.п. для приготовления порошков, пилюль, капсул и таблеток. Ввиду легкости введения, таблетки и капсулы представляют наиболее предпочтительную оральную единичную лекарственную форму, в этом случае очевидно использование твердых фармацевтических носителей. В парентеральных композициях носитель обычно содержит стерильную воду, по крайней мере, в основном, хотя он может включать также другие ингредиенты, например, ускоряющие растворимость. Также могут быть приготовлены растворы для инъекций, в которых носитель содержит солевой раствор, раствор глюкозы или смесь солевого и глюкозного раствора. Растворы для инъекций, содержащие соединения формулы (I), могут приготавливаться в масле с целью продления их действия. Для этого могут использоваться соответствующие масла, например арахисовое масло, сезамовое масло, хлопковое масло, кукурузное масло, соевое масло, синтетические глицериновые эфиры жирных кислот, имеющих длинные цепи, и смеси этих и других масел. Также могут быть приготовлены суспензии для инъекций, содержащие соответствующие жидкие носители, суспендирующие вещества и т.п. В композициях, предназначенных для введения через кожу, носитель может содержать вещество, усиливающее проникновение, и/или подходящее смачивающее вещество, возможно, соединенное в небольших пропорциях с подходящими добавками любого происхождения, которые не оказывают серьезного вредного воздействия на кожу. Подобные добавки могут облегчать введение через кожу и/или могут облегчить приготовление желаемых композиций. Эти композиции могут вводиться различными способами, например, с помощью трансдермальных накладок, пятен или в виде мази. Очевидно, что для приготовления водных композиций больше подходят кислые или основные соли присоединения благодаря их повышенной растворимости в воде.
С целью повышения растворимости и/или устойчивости соединений формулы (1) в фармацевтических композициях, предпочтительно могут использоваться α-, β- или γ- циклодекстрины или их производные, в частности, циклодекстрины, замещенные гидроксиалкилом, например, 2-гидроксипропил- β- -циклодекстрин. Растворимость и/или стабильность соединений формулы (I) в фармацевтических композициях может быть также улучшена с помощью растворителей, таких как спирты.
Особенно предпочтительно изготавливать вышеуказанные фармацевтические композиции в единичных лекарственных формах с целью облегчения введения и обеспечения равномерности дозировки. Термин "единичная лекарственная форма", используемый в описании изобретения и в формуле данного изобретения, относится к физически дискретным единицам, используемым в виде единичных лекарственных форм, при этом каждая единица содержит заданное количество активного ингредиента, необходимого для достижения желаемого терапевтического действия, в сочетании с необходимым фармацевтическим носителем. Примерами таких единичных лекарственных форм являются таблетки (включая таблетки с насечками или с покрытием), капсулы, пилюли, порошки, облатки, растворы или суспензии для инъекций, чайные ложки, столовые ложки и т.п., а также их разделенные части.
Следующие примеры предназначены для иллюстрации, а не для ограничения объема настоящего изобретения.
Экспериментальная часть
В дальнейшем "ДИПЭ" означает, диизопропилэфир, а "ЭтОАц" означает этилацетат.
А. Получение промежуточных соединений
Пример 1
Ангидрид трифторуксусной кислоты (12,7 мл) добавляют по каплям при 0oC к раствору N-метил-2-пропен-1-амина (5 г) и триэтиламина (14,7 мл) в диэтил эфире (50 мл) и смесь перемешивается при комнатной температуре в течение 6 часов, после чего растворитель выпаривается. Остаток растворяется в воде, экстрагируется с помощью CH2CH2 и растворитель выпаривается, давая 9,4 г (75%) 2,2,2-трифтор-N-метил-N-2-пропенилацетамида (промежуточное соединение 1).
Аналогичным образом получают 1-(2- пропенил)-4-(трифторацетил)пиперазин (промежуточное соединение 2).
Пример 2
а) Смесь N-метил-2-пропен-1-амина (2,7 мл), этил 3-бромопропаноата (4,5 мл) и карбоната калия (5,8 г) в 2-бутаноне (20 мл) перемешивается при 50oC в течение 4 часов. Смесь охлаждается при комнатной температуре, фильтруется, и фильтрат выпаривается. Остаток растворяется в воде, экстрагируется с помощью CH2CH2, и растворитель выпаривается. Остаток очищается посредством хроматографии на колонках с силикагелем (растворитель для элюирования: CH2Cl2/CH3OH 9,75/0,25). Очищенные фракции собираются и выпариваются, давая 3 г (63%) этил N-метил-N-2-пропенил- β- -аланина (промежуточное соединение 3).
Подобным образом получают следующие промежуточные соединения:
этил 4-[метил(2-пропенил)амино]бутаноат (промежуточное соединение 4),
этил 5-[метил(2-пропенил)амино]пентаноата (промежуточное соединение 5), и
2-[метил(2-метил-2-пропенил)амино] этанол ацетат (эфир) (промежуточное соединение 81).
б) Смесь промежуточного соединения 4 (14 г) в растворе соляной кислоты (35%) (38 мл), уксусной кислоты (38 мл) и воды (19 мл) перемешивается и дефлегмируется в течение 5 часов. Смесь охлаждается на ледяной бане, и к ней добавляется NaOH (50%) до тех пор, пока pH не достигнет приблизительно 6, после чего растворитель выпаривается. Остаток промывается с помощью CH2Cl2. Осадок отфильтровывается, и фильтрат выпаривается. Сироп (19,4 г) промывается толуолом, и растворитель выпаривается. Продукт использовался без дальнейшей очистки, давая 15 г (100%) 4-[метил(2-пропенил)амино]бутановой кислоты (промежуточное соединение 6).
Аналогичным образом из промежуточного соединения 5 приготавливается 5-[метил(2- пропенил)амино]пентановая кислота (промежуточное соединение 7).
Пример 3
Смесь 5-гексен-1-ола (5 г) и 8-азаспиро[4.5]декан-7,9-диона (14 мл) в триэтиламине (150 мл) охлаждается на ледяной бане. Хлорид метана-сульфонила (8,6 г) в триэтиламине (50 мл) добавляется к ней по каплям, и смесь перемешивается при комнатной температуре в течение 1 часа. Смесь отфильтровывается, и фильтрат выпаривается. К остатку добавляется дихлорметан (7,7 г), карбонат калия (7,6 г) и N,N-диметилформамид, и смесь перемешивается при 160oC в течение ночи. Смесь отфильтровывается, и фильтрат выпаривается. Остаток очищается с помощью хроматографии на коротких открытых колонках с силикагелем (растворитель для элюирования; CH2Cl2/CH3OH 100/0-98/2). Чистые фракции собираются и выпариваются, давая 1,5 г (13%) 8-(5-гексенил)-8-азаспиро[4.5]декан-7,9-дион (промежуточное соединение 8).
Пример 4
a) P2O5 (516,5 г) добавляется порциями к H3PO4 (247,5 мл) и перемешивается под струей N2 при комнатной температуре. Смесь перемешивается в течение 2 часов при 120oC, а затем охлаждается до 50oC. К ней добавляется p-ксилен (1810 мл), и перемешивание продолжается в течение 15 минут. Затем добавляется POCl3 (83,3 г), и перемешивание продолжается в течение 10 минут. N-[2-(фенилметил) фенил] формамид (приготовленный в соответствии с описанием, приведенным в Helv. Chim. Acta 47(5) 1163-72 (1964) (37,2 г) добавляется в виде порций. Смесь перемешивается в течение 30 минут при 60-70oC. Другая часть N-[2-(фенилметил)фенил]формамида (74,3 г) добавляется в виде порций, и реакционная смесь перемешивается в течение ночи при 100oC. Реакционная смесь охлаждается, и слой р-ксилена удаляется. Медленно добавляется вода (990 мл). Смесь охлаждается с помощью ледяной воды. В течение 2 часов добавляется раствор КОН (1073 г) в воде (2200 мл). По каплям добавляется CH2Cl2 (500 мл), и смесь энергично перемешивается в течение 15 минут. Органический слой отделяется. Водный слой дважды экстрагируется с помощью CH2Cl2. Объединенные органические слои высушиваются с помощью MgSO4, отфильтровываются, и растворитель выпаривается. Остаток очищается посредством дистилляции, давая смешанную фракцию. Смешанная фракция очищается еще два раза при помощи дистилляции, давая 1,4 г 11H-дибен[b,е]азепина (промежуточное соединение 9).
б) Смесь промежуточного соединения 9 (116 г) в метаноле (1000 мл) гидрируется с помощью палладия на активированном углероде (10%) (17,7 г), используемом в качестве катализатора. После отбора водорода (1 экв. часть) катализатор отфильтровывается, и фильтрат выпаривается. Остаток перемешивается в ДИПЭ (80%), осадок отфильтровывается и высушивается в вакууме при 45oC в течение 24 часов, давая 88,1 г (75,7%) 6,11- дигидро- 5H-дибенз[b,e]азепина (промежуточное соединение 10).
Подобным образом получают
3-хлор-6,11-дигидро-5H-дибенз [b,e]азепин (промежуточное соединение 11) и 2-хлор-6,11-дигидро-5H-дибенз[b,e]азепин (промежуточное соединение 12).
в) Бром (1,3 мл) добавляется по каплям к смеси промежуточного соединения 10 (5 г) в уксусной кислоте (12 мл), и смесь перемешивается при комнатной температуре в течение 4 часов. Растворитель выпаривается, остаток промывается с помощью NH4OH (10%) и растворяется в CH2Cl2. Органический слой высушивается с помощью Na2SO4, отфильтровывается и выпаривается. Остаток (8 г) очищается с помощью флеш-хроматографии с силикагелем (растворитель для элюирования: гексан/ЭтОАц 9/1). Очищенные фракции собираются и выпариваются, давая 4 г (56%) 2 бромо-6,11-дигидро-5Н-дибенз[b,e]азепин (промежуточное соединение 13).
Пример 5
a) 2-Амино-6-хлоробензойная кислота (25 г), растворенная в уксусном ангидриде (100 мл), перемешивается при 120oC в течение 2 часов. Смесь охлаждается до комнатной температуры и отфильтровывается. Осадок промывается водой и Na2CO3 (10%) и растворяется в CH2Cl2. Раствор высушивается с помощью Na2SO4, отфильтровывается и выпаривается. Остаток дважды кристаллизуется из бензола, давая 13 г (46%) 5-хлоро-2-метил-4H-3,1-бензоксазин-4-он, имеющий температуру плавления 148,7oC (промежуточное соединение 14).
б) Промежуточное соединение 14 (20 г) растворяется в тетрагидрофуране (200 мл), и смесь охлаждается на бане с ледяной водой в атмосфере N2. По каплям добавляется фенил магний бромид (34 мл) в тетрагидрофуране (100 мл), и смесь перемешивается при 10oC в течение 1 часа. Смесь резко охлаждается водой и HCl (2N) и дважды экстрагируется с помощью CH2Cl2. Объединенные органические слои высушиваются с помощью Na2SO4, отфильтровываются, а фильтрат выпаривается. Остаток очищается с помощью хроматографии на коротких открытых колонках с силикагелем (растворитель для элюирования: CH2Cl2). Очищенные фракции собираются и выпариваются, давая 24,5 г (87%) N(2-бензоил-3-хлорофенил)- ацетамид (промежуточное соединение 15).
в) Промежуточное соединение 15 (20 г), растворенное в уксусной кислоте (700 мл) и соляной кислоте (175 мл), перемешивается и дефлегмируется в течение 6 часов. Смесь охлаждается до комнатной температуры и растворитель выпаривается. Остаток разделяется между CH2CI2 и Na2СО3 10%. Органический слой высушивается с помощью Na2SO4, отфильтровывается и выпаривается. Остаток откристаллизовывается от ДИПЭ/ЭтОАц, давая 10,5 г (62%) (2-амино-6-хлорфенил)фенилметанон, имеющий температуру плавления 191,5oC (промежуточное соединение 16).
г) Промежуточное соединение 16 (10,5 г) и гидразин гидрат (8,8 мл) растворяются в 1,2-этандиоле (200 мл), и смесь перемешивается при 200oC в течение 2 часов. Смесь охлаждается до 60oC, к ней добавляется КОН (5,1 г), а затем смесь перемешивается при 200oC в течение ночи. Смесь охлаждается до комнатной температуры и разделяется между водой и CH2Cl2. Органический слой высушивается с помощью Na2SO4, отфильтровывается и выпаривается, давая 9 г (90%) 3-хлор-2-(фенилметил)-бензоламина (промежуточное соединение 17).
д) Смесь промежуточного соединения 17 (10 г), растворенного в муравьиной кислоте (100 мл), перемешивается и дефлегмируется в течение 2 часов. Смесь охлаждается до комнатной температуры и растворитель выпаривается. Na2CO3 (10%) добавляется к остатку, и эта водная смесь дважды экстрагируется с помощью CH2Cl2. Органический слой высушивается с помощью Na2SO4 отфильтровывается и выпаривается, давая 9,6 г (85%) N-[3-хлоро-2-(фенилметил)-фенил] формамида (промежуточное соединение 18).
е) Начиная от промежуточного соединения 18, 1-хлоро -6,11-дигидро-5Н-дибенз[b, e] азепин (промежуточное соединение 19) получают в соответствии с процедурой, описанной в Примере 4.
Аналогичным образом получают 6,11-дигидро-4-метил-5H- дибенз[b,e]азепин (промежуточное соединение 20).
Пример 6
а) Раствор 3-бромобензоламина (20 г) в 1,2-дихлорэтане добавляется по каплям в атмосфере N2 к раствору BCl3/ксилена (128 мл) в 1,2-дихлорэтане, охлажденного на льду. Цианобензол (12 г) в 1,2-дихлорэтане и AlCl3 (17 г) также добавлялись к нему, и смесь перемешивалась и дефлегмировалась в течение ночи. Смесь охлаждается, лед/HCl (2N) добавляется к ней при помешивании, затем смесь перемешивается и нагревается до 80oC в течение 30 минут. Смесь охлаждается, разбавляется водой и экстрагируется с помощью CH2Cl2. Органический слой высушивается с помощью Na2SO4, отфильтровывается и выпаривается. Остаток очищается с помощью хроматографии на коротких колонках с силикагелем (растворитель для элюирования: гексан/CH2Cl2/ЭтОАц 6/3/1). Очищенные фракции собираются и выпариваются, давая 13 г (41%) (4-бромо-2- аминофенил)фенил-метанон (промежуточное соединение 21).
б) Начиная с промежуточного соединения 21, 3-бромо-6,11-дигидро-5H-дибенз[b, e] азепин (промежуточное соединение 22) приготавливался аналогично тому, как приготавливалось промежуточное соединение 19 из промежуточного соединения 16, как описано в Примерах 5г, 5е и 5д.
Аналогичным способом приготавливались:
6,11-дигидро-3-метил-5Н-дибенз[b,e]азепин (промежуточное соединение 23);
6,11-дигидро-2-метил-5Н-дибенз[b,e]азепин (промежуточное соединение 24);
6,11-дигидро-10-метил-5Н-дибенз[b, e] азепин (промежуточное соединение 25), и
6,11-дигидро-8-метил-5Н-дибенз[b,e]азепин (промежуточное соединение 26).
Пример 7
2- [[(4-хлорфенил) метил] амино]бензолметанол (6,7 г) (приготовленный в соответствии с описанием, приведенным в J. Chem. Soc. Chem. Commun., 1989(1), 44-5) охлаждается в атмосфере N2 до -40oC. По каплям добавляется серная кислота (35 мл) при температуре приблизительно -10oC, и смесь перемешивается при комнатной температуре в течение 1 часа. Смесь выливается в ледяную воду и осторожно превращается в основание с помощью КОН. Смесь отфильтровывается, и осадок промывается водой и CH2CI2. Фильтрат и промывочная жидкость экстрагируются, высушиваются с помощью Na2SO4, отфильтровываются и выпариваются, давая 5,8 г (95%) 9- хлоро-6,11-дигидро-5Н-дибенз[b,e]азепин (промежуточное соединение 27).
Аналогичным способом получают 3-фтор-6,11-дигидро-5Н- дибенз[b,e]азепин (промежуточное соединение 28).
Пример 8
Процедура 1
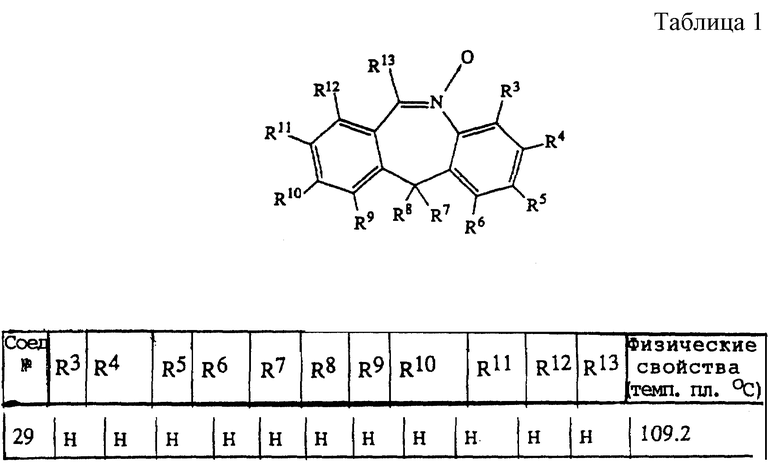
3-Фенил-2-(фенилсульфонил)оксазиридин (18,7 г) добавляется в виде порций к раствору промежуточного соединения 10 (7 г) в CHCl3 (120 мл), а затем перемешивается при комнатной температуре в течение 2 часов. Растворитель выпаривается, и остаток очищается с помощью хроматографии на коротких открытых колонках с силикагелем (растворитель для элюирования: CH2Cl2/CH3OH 97,5/2,5). Очищенные фракции собираются и выпариваются, давая 10 г (80%) 11Н- дибенз[b, e] азепин, 5-оксид, имеющий температуру плавления 109,2oC (промежуточное соединение 29).
Процедура 2
Раствор промежуточного соединения 10 (50 г) в CH2Cl2 (1282 мл) перемешивается и охлаждается до ±10oC. Раствор метахлоропербензойной кислоты (115,6 г) в CH2Cl2 (2430 мл) добавляется по каплям при <15oC. Реакционная смесь перемешивается в течение 1 часа. Смесь экстрагируется с помощью 10% водного раствора Na2SO3 (1 литр), затем с помощью 5% водного раствора Na2CO3. Органическая фаза высушивается, фильтруется, и растворитель выпаривается, давая 53,5 г (количественный выход) 11H-дибенз[b,e]азепин, 5-оксид (промежуточное соединение 29).
По аналогии с процедурой 2 получают следующие промежуточные продукты:
11-метилен-11H-дибенз[b,с]азепин, 5-оксид (промежуточное соединение 73); 2,3-диметил-11Н-дибенз[b, с]азепин, 5-оксид (промежуточное соединение 74), и 3-хлоро-2-метил-11-дибенз[b,с]азепин, 5-оксид (промежуточное соединение 75).
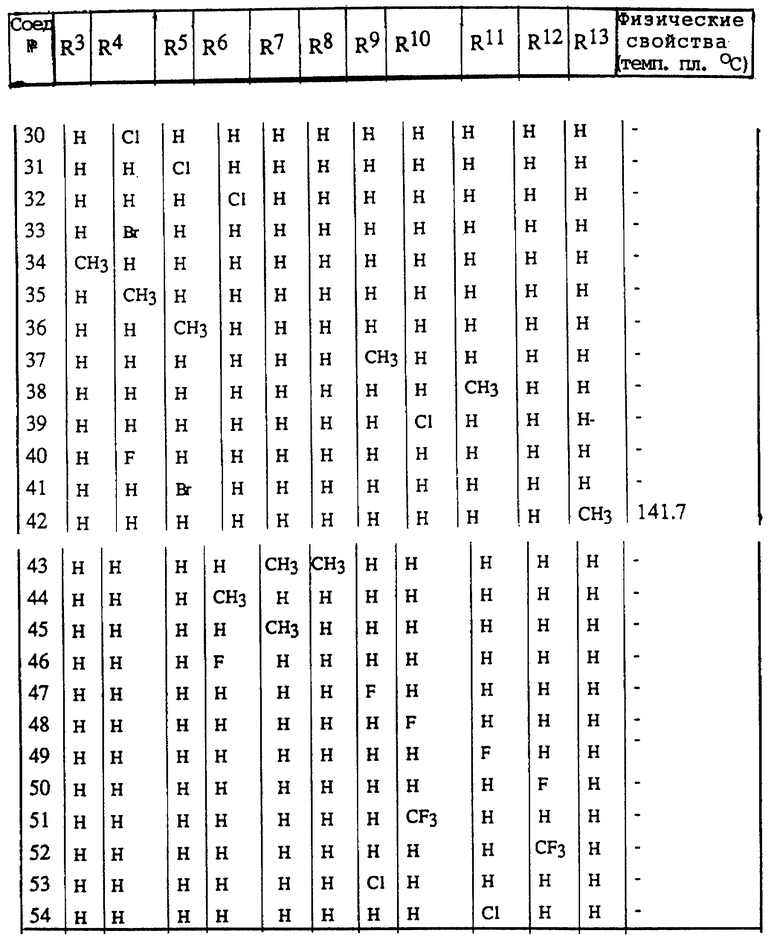
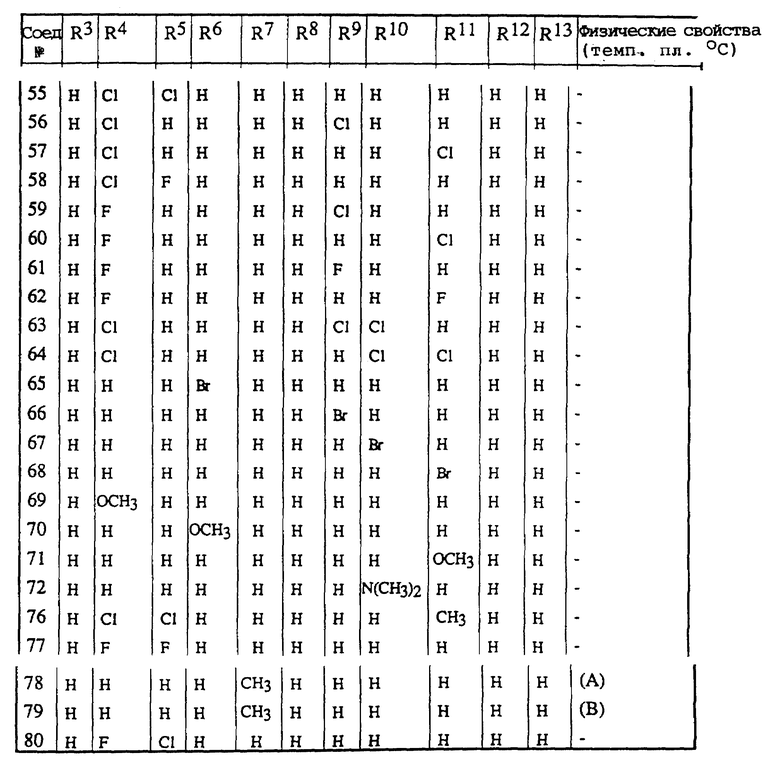
Соединения, приведенные в Таблице 1, получают по аналогии с процедурой 1.
В. Получение соединений формулы (I)
Пример 9
Смесь промежуточного соединения 29 (2,7 г) и N,N-диметил-2- пропен-1-амин (3 мл) в толуоле (60 мл) перемешивается при температуре 100oC в течение ночи. Растворитель выпаривается, и остаток очищается с помощью флеш-хроматографии на силикагеле (растворитель для элюирования: CH2Cl2/CH3OH 95/5). Очищенные фракции собираются и выпариваются. Остаток (3,1 г), содержащий свободное основание (±)-цис-2,3,3а, 8-тетрагидро-N, N- диметилдибенз[c,f] изоксазоло[2,3-а]азепин-2-метан-амин (промежуточное соединение 59), превращается в соль щавелевой кислоты (1:1) в С2H5ОН при комнатной температуре, давая 2,6 г (52%) (±)-цис-2,3,3а,8-тетрагидро-N,N-диметилдибенз [с, f]изоксазоло[2,3-а] азепин-2-метанамин этандионат (1:1), имеющий температуру плавления 139,5oC (соединение 1).
Пример 10
а) Следуя процедуре, описанной в Примере 9, но используя в качестве растворителя 4-метил-2-пентанон, получают (±)-цис- 2,3,3а,8-тетрагидро-2-(1-пирролидинил-метил)дибенз- [с,f]изоксазоло[2,3-а]азепин этандионат (1:1), имеющий температуру плавления 167,2oC (соединение 2).
б) Следуя процедуре, описанной в Примере 9, но используя в качестве растворителя тетрагидрофуран, получают (±)- цис-10,11-дихлоро-2,3,3a,8-тетрагидро-N, N, 5-триметил-дибенз [c,f]изоксазоло[2,3-а]азепин-2-метанамин, имеющий температуру плавления 103,2oC (соединение 98).
Пример 11
Используя процедуру, описанную в Примере 9, но перемешивая исходные материалы без растворителя в автоклаве Парра при 100oC в течение ночи, получают (±)-(цис+транс)-2,3,3а,8-тетрагидро-N, N, 3a-триметил-дибенз [c,f]изоксазоло[2,3-а]азепин-2-метанамин (соединение 3).
Пример 12
Соединение 59 (свободное основание соединения 1), приготовленное в соответствии с примером 9, превращается в фумарат (1:1) путем добавления в виде капель этанольного раствора фумаровой кислоты (0,215 г/мл) к смеси, охлажденной на ледяной бане, свободного основания в смеси этанола (8 мл) и диэтилэфира (30 мл). Образующийся осадок отфильтровывается и высушивается в вакууме, давая 1 г (71%) (±)-цис-2,3,3а,8-тетрагидро-N,N- диметилдибенз[c,f] изоксазоло[2,3-а]азепин-2-метанамин (Е)-2- бутендионат (1:1), имеющий температуру плавления 148,9oC (соединение 4).
Пример 13
а) Соединение 59 (свободное основание соединения 1), приготовленное в соответствии с Примером 9, разделяется и очищается с помощью хроматографии на колонке Chiralcel OJ (Daiсel, 250 г, 20 μм, длина - 23 см, обнаружение при 200 нм, скорость - 40 мл/мин, растворитель для элюирования: гексан/этанол 80/20, объем впрыскивания - 25 мл).
1) Целевые (А-цис)-фракции собираются, и растворитель выпаривается. Остаток (6,8 г) растворяется в этаноле (50 мл), перемешивается при комнатной температуре и превращается в соль щавелевой кислоты (1:1) с помощью раствора щавелевой кислоты (2,94 г) в этаноле (50 мл). Целевое соединение кристаллизуется, и осадок отфильтровывается и высушивается, давая 5,5 г (24,7%) (+)-(А-цис)-2,3,3а, 8-тетрагидро-N, N-диметилдибенз[с, f] изоксазоло[2,3-а] азепино-2-метанамин этандиоат (1:1), имеющего температуру плавления 167,0oC (соединение 5).
2) Целевые (В-цис)-фракции обрабатываются тем же способом, что и (А-цис)-фракции, давая 3,4 г (15,2%) (-)-(В-цис)-2,3, 3а, 8-тетрагидро-N,N-диметилдибенз [c, f] изоксазоло [2,3-а]-азепин-2-метанамин этандиоат (1:1), имеющего температуру плавления 152,4oC (соединение 6).
б) Соединение 1, полученное в соответствии с Примером 9, разделяется и очищается с помощью хроматографии на колонке Chiralcel OJ (Daicel, 250 г, 20 μм, длина - 23 см, обнаружение при 200 нм, скорость - 40 мл/мин, растворитель для элюирования: гексан/этанол 80/20; инжектирование: соединение 1 (0,55 г) растворяется в п-гексане/этаноле (1:1) (50 мл), объем инжектирования - 20 мл, концентрация -11,00 мг/мл). Две целевые фракционные группы (1) и (2) собираются, и их растворители выпариваются, давая 0,2 г (47,5%) (А-цис)-2,3, -3а,8-тетрагидро- N,N-диметилдибенз[с,f]изоксазоло[2,3-а]азепин-2-метанамина (соединение 7) и 0,19 г фракции (2). Фракция (2) содержит примесь (20%), которая отделяется с помощью хроматографии с обращенной фазой на колонках на RP-Кромасил С-18 (1 дюйм/2,54 см/, растворитель для элюирования: (0,2% NH4OAc в H2О)/CH3ОН 30/70). Очищенные фракции собираются, и органический растворитель выпаривается при комнатной температуре. Водный остаток экстрагируется с помощью CHCl3. Отделенный органический слой выпаривается, давая 0,110 г (26,1%) (В-цис) -2,3, 3а, 8-тетрагидро-N,N-диметилдибенз [c,f]изоксазоло-[2,3-а]азепин-2- метанамин (соединение 8).
Пример 14
Смесь (±)-цис-2-[(2,3,3а, 8-тетрагидродибенз[с,f]]изоксазоло[2,3-а]азепин-2-ил) -метил] -1H-изоиндол-1,3(2H)-диона (4 г), приготавливаемая в соответствии с процедурой, описываемой в Примере 1, и гидразин гидрат (0,5 мл) в этаноле (80 мл) перемешивается при 80oC в течение 4 часов. Осадок отфильтровывается и очищается с помощью хроматографии на открытых колонках с силикагелем (растворитель для элюирования CH2Cl2/2-пропанон 8/2). Очищенные фракции собираются и выпариваются. Остаток (1,6 г) превращается в соль щавелевой кислоты (1: 1) в C2H5OH при комнатной температуре. Остаток (0,8 г) очищается с помощью хроматографии на колонках с силикагелем (растворитель для элюирования: CH2Cl2/CH3OH 97,5/2,5-95/5). Очищенные фракции собираются и выпариваются, давая 0,6 г (22%) (±)-цис-2,3,3а, 8-тетрагидродибенз[с,f] иэоксазоло[2,3-а]азепин-2- метанамина (соединение 9).
Пример 15
Смесь (±)-цис-2,2,2-трифторо-N-метил-N-[(2,3,3а,8-тетрагидродибенз [c,f] изоксазоло [2,3-а]азепин-2-ил) метил] ацетамида (4 г), приготовленная в соответствии с процедурой, описанной в Примере 9, гидроксид натрия (1,06 г) в метаноле (60 мл) и вода (12 мл) перемешиваются при 60oC в течение 3 часов. Растворитель выпаривается, остаток разбавляется водой и экстрагируется с помощью CH2Cl2. Органический слой высушивается с помощью Na2SO4, отфильтровывается и выпаривается. Остаток (3,9 г) очищается с помощью хроматографии на открытых колонках с силикагелем (растворитель для элюирования: CH2Cl2/CH3OH 95/5). Очищенные фракции собираются и выпариваются. Остаток превращается в соль щавелевой кислоты (1:1) в C2H5OH при комнатной температуре, давая 3,2 г (82%) (±)-цис-2,3, 3а, 8-тетрагидро-N-метилдибенз [с,f] изоксазоло[2,3-а] азепин- -2-метанамин этандиоат (1:1), имеющий температуру плавления 134,0oC (соединение 10).
Пример 16
Смесь промежуточного соединения 29 (54,5 г) и N,N-диметил- 2-пропен-1-амин (35,8 г) в толуоле (1000 мл) перемешивалась в течение ночи при 100oC. Растворитель выпаривается. Остаток очищается с помощью хроматографии на колонках с силикагелем (растворитель для элюирования: CH2Cl2/CH3OH 97/3). Целевые фракции собираются, и растворитель выпаривается. Остаток очищается и разделяется на энантиомеры с помощью хроматографии на колонках с Chiralcel OJ (растворитель для элюирования: гексан/этанол 90/10). Очищенные фракции собираются, и растворитель выпаривается. Остаток растворяется в этаноле (100 мл, р. а.) и превращается в соль (S)-яблочной кислоты (1:1) путем добавления (-)-(8)-яблочной кислоты (9 г). Смесь перемешивается в течение ночи, получающийся осадок отфильтровывается, высушивается, перемешивается в этаноле (100 мл), промывается с помощью ДИПЭ и высушивается, давая 18,8 г (+)-(А-цис)-2,3, 3а, 8-тетрагидро-N, N-диметилдибенз [с,f]изоксазоло[2,3-а]азепинметанамина (S)-гидроксибутандиоата (1: 1), имеющего температуру плавления 154,2oC, α = 50,41 при 20oC для 100,58 мг в 10 мл метанола (соединение 58).
Пример 17
Раствор (+)-(R)-яблочной кислоты (0,67 г) в этаноле (10 мл) добавляется к раствору соединения 59 (1,47 г) в этаноле (10 мл) и перемешивается при комнатной температуре. Полученному прозрачному раствору была дана возможность кристаллизоваться. Осадок отфильтровывается и высушивается (вакуум, 50oC, 24 часа). Данная фракция вновь кристаллизуется из этанола (15 мл), отфильтровывается и высушивается (вакуум, 50oC), давая 0,76 г (±)-цис-2,3,3а, 8-тетрагидро-N, N-диметилдибенз [c,f] изоксазоло [2,3-а] азепинметанамин (R)-гидроксибутандиоата (1:1) (35,5%), имеющего температуру плавления 138,6oC, α = 13,86o при 20oC для 10,10 мг в 10 мл метанола (соединение 57).
Пример 18
Соединение 58 (2,1 г) превращают в свободное основание путем обработки водным аммиаком (при 0oC). Эта смесь экстрагируется с помощью CH2Cl2 (100 мл). Отделенный органический слой высушивается, фильтруется, и фильтрат объединяется в 3-фенил-2- (фенилсульфонил)оксазиридином (1,3 г). Эта смесь перемешивается в течение 24 часов при комнатной температуре. Растворитель выпаривается, и остаток очищается с помощью хроматографии на колонках с силикагелем (растворитель для элюирования: CH2Cl2/(CH3ОН/NH3) 90/10). Очищенные фракции собираются, и растворитель выпаривается. Остаток растирается в ДИПЭ, отфильтровывается и высушивается, давая 0,85 г (55%) (А- цис)-2,3,3а,8-тетрагидро-N,N-диметилдибенз[с,f]изоксазоло-[2,3- а]азепинметанамин, N-оксид моногидрата, имеющего температуру плавления 170oC (соединение 96).
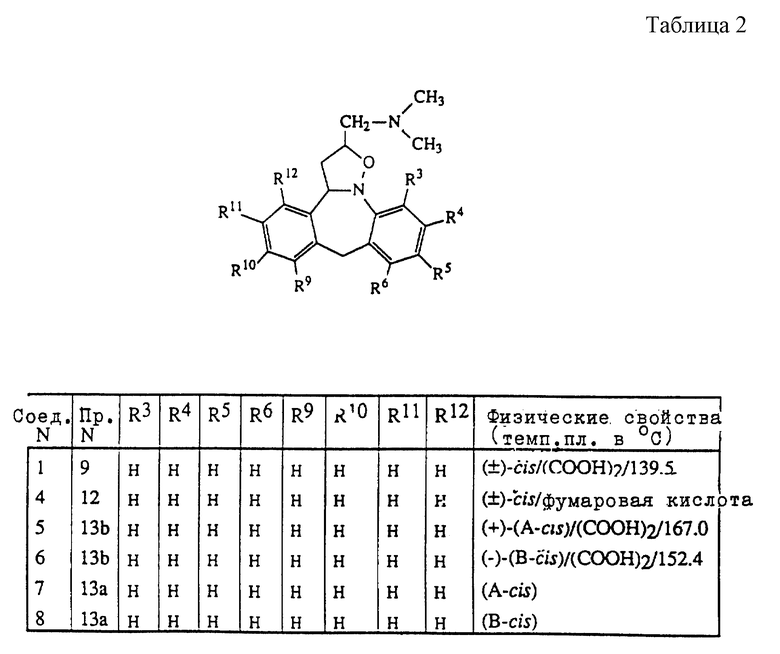
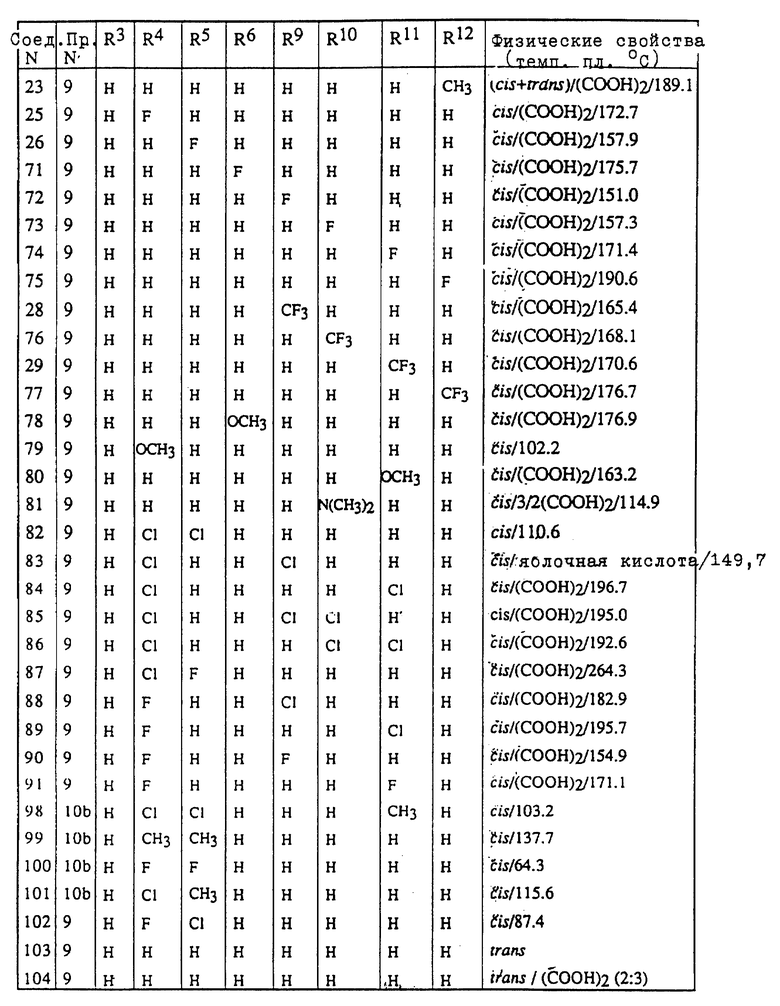
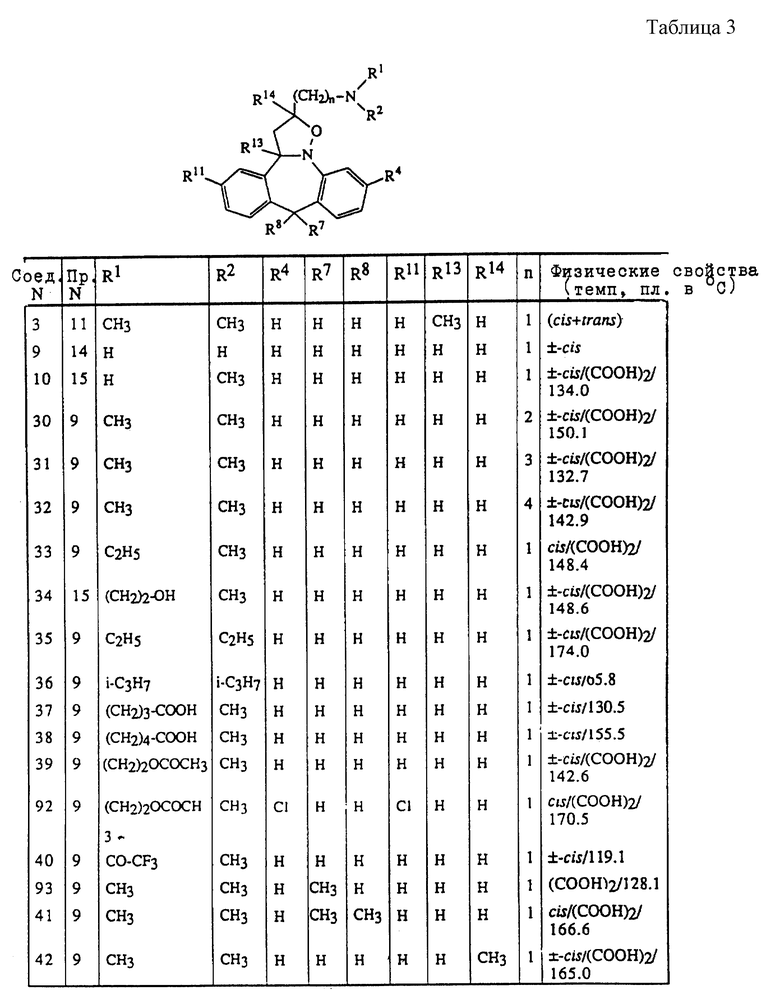
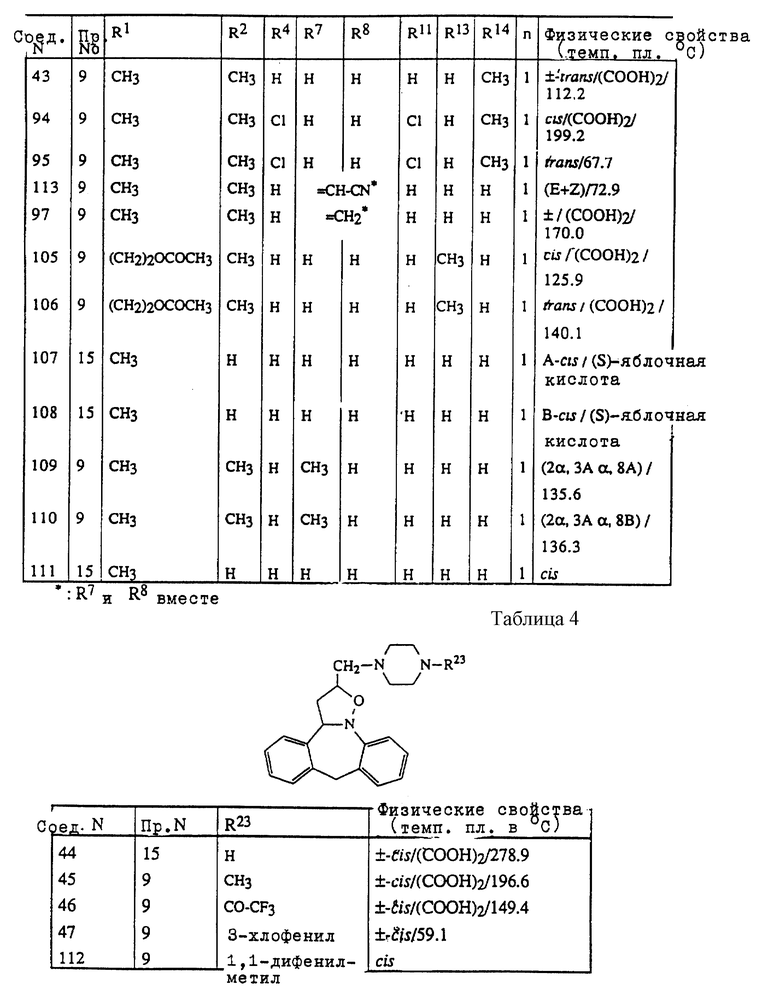
Таблицы 2-6 включают соединения, полученные способом, описанным в одном из вышеуказанных примеров.
С. Фармакологический пример
Пример 19: "Тест мСРР на крысах" (мХФП)
Крысам вводилось испытуемое соединение в дозе, составляющей 0,0025-40 мг/кг веса тела, при этом время Т перед тестированием составляло от 5 до 480 минут, и 1 мг/кг мХФП (метахлорофенилпиперазин) вводится внутривенно за 15 минут до теста. После истечения предварительного времени Т обработанные крысы подвергались "Открытому полевому тесту на крысах", описанному в Drug Dev. Res. 18, 119-144 (1989), только вместо источника света KleverluxR (12V/20W) использовался инфракрасный источник света. Доза, при которой 40% испытуемых крыс показали подавление действия, вызванного мХФП, т.е. антагонизм мХФП, определялась как активная доза. Диапазон активности испытуемого соединения определялся по разнице ВАД (высшей активной дозы) и НАД (низшей активной дозы). Соединения 1, 4-7, 10, 15, 18, 25, 26, 30, 39, 57, 58, 77, 84, 89 и 91 имели разницу между ВАД и НАД, равную 16 или более, при этом предварительное время перед тестом Т составляло 60 минут. При предварительном времени перед тестом Т, составлявшем 60 минут, соединения 2, 8, 11-14, 16, 19, 21, 23, 24, 27, 29, 35, 42-45, 47, 48, 52, 54, 55, 65-75, 78, 79, 87, 88, 90 и 92-94 показали мХФП-антагонизм по крайней мере при одной тестируемой дозе.
Пример 20: Изучение сродства к связыванию на рецепторах 5-HT2A и 5-НТ2C in vitro
Взаимодействие соединений формулы (I) с рецепторами 5-НТ2A и 5-НТ2C оценивалось в экспериментах по связыванию радиоактивных лигандов in vitro.
В целом, низкая концентрация радиоактивного лиганда, имеющего сильное связывающее сродство с рецептором выдерживается в термостате с образцом ткани препарата, обогащенного определенным рецептором (1-5 мг ткани) в буферной среде (0,2-5 мл). Во время инкубирования радиоактивные лиганды связываются с рецептором. Когда достигается равновесие связывания, рецепторно-связывающая радиоактивность отделяется от несвязывающей радиоактивности и подсчитывается рецепторно-связывающая активность. Взаимодействие тестируемых соединений с рецепторами оценивается в экспериментах по соревновательному связыванию. Тестируемые соединения с различной концентрацией добавляются к культивируемой смеси, содержащей препарат ткани и радиолиганд. Связывание радиолиганда ингибируется тестируемым соединением в пропорции к его связывающему сродству и его концентрации.
Радиолигандом, используемым для связывающего сродства 5-НТ2A, является 3H-кетансерин, а используемой тканью является переднее корковое вещество крысы. Соединения 1-5, 7, 9, 10, 12-14, 16-20, 27, 30, 31, 33-35, 39, 42, 45, 52, 54, 57-59, 62-64, 67, 68, 70-72, 74, 77, 79, 82, 84, 87, 88, 89, 91, 96, 97, 100, 101 и 108 ингибируют более 40% рецептора 5-НТ2A при концентрации теста, составляющей 10-8М. Соединения 6, 8, 22, 32, 36-38, 43, 46, 55, 61, 65, 76, 80, 86, 92-94, 98, 99, 105 и 107 ингибируют более 40% рецептора 5-НТ2A при концентрации теста, составляющей 10-7М. Остальные соединения либо не подвергались тестированию, либо ингибировали менее 40% рецептора 5-НТ2A при концентрации теста, составляющей 10-7М. Радиолигандом, используемым для связывающего сродства 5-НТ2C, является 3H-месулергин, а используемой тканью является хориоидальное сплетение свиньи. Соединения 1-3, 5, 7, 9-19, 21, 22, 24-27, 29, 30, 33-35, 42, 52, 54, 57-59, 64, 66, 68, 70-72, 74, 77, 79, 80, 82, 84, 86-93, 96, 98, 100, 101 и 108 ингибируют более 40% рецептора 5-HT2C при концентрации теста, составляющей 10-8М. Соединения 4, 6, 8, 20, 23, 31, 32, 38, 39, 41, 45, 55, 61- 63, 65, 67, 75, 76, 81, 94, 95, 99, 107 и 113 ингибируют более 40% рецептора 5-НТ2C при концентрации теста, составляющей 10-7М. Остальные соединения либо не подвергались тестированию, либо ингибировали менее 40% рецептора 5-НТ2C при концентрации теста, составляющей 10-7М.
Д. Примеры композиции
Термин "активный ингредиент" (А.И.), используемый в примерах, относится к соединениям формулы (I), фармацевтически приемлемой кислой соли присоединения, его стереохимически изомерной форме или его N-оксидной форме.
Пример 21: ОРАЛЬНЫЕ КАПЛИ
500 г активного ингредиента (соединение примера 16) растворяются в 0,5 л 2-гидроксипропановой кислоте и 1,5 л полиэтиленгликоля при 60-80oC. После охлаждения до 30-40oC добавляется 35 л полиэтиленгликоля, и смесь хорошо перемешивается. Затем добавляется раствор 1750 г сахарина натрия в 2,5 л очищенной воды и при перемешивании к ним добавляются 2,5 л корригента какао и полиэтиленгликоль в таком количестве, чтобы общий объем составил 50 л, при условии, что раствор оральных капель содержит 10 мг/мл активного ингредиента. Готовый раствор расфасовывается в подходящие флаконы.
Пример 22: ОРАЛЬНЫЙ РАСТВОР
3 г метил 4-гидроксилбензоата и 1 г пропил 4-гидроксибензоата растворяются в 4 л кипящей очищенной воды. В 3 л этого раствора растворяются первые 10 г 2,3-дигидроксибутандиоевой кислоты, а затем 20 г активного ингредиента (соединение примера 16). Этот раствор объединяется с оставшейся частью предыдущего раствора, и к нему добавляются 12 л 1,2,3-пропантриола и 3 л 70% раствора сорбита. 40 г сахарина натрия растворяются в 0,5 л воды, и 2 мл малеиновой эссенции и 2 мл крыжовниковой эссенции добавляются к нему. Последний раствор объединяется с предыдущим, к ним добавляется вода в таком количестве, чтобы общий объем составил 20 л, при условии, что оральный раствор содержит 5 мг активного ингредиента на столовую ложку (5 мл). Готовый раствор расфасовывается в подходящие флаконы.
Пример 23: ТАБЛЕТКИ С ПЛЕНОЧНЫМ ПОКРЫТИЕМ
Приготовление сердцевины таблетки
Смесь 100 г активного ингредиента (соединение примера 16), 570 г глактозы и 200 г крахмала хорошо перемешивается, а затем увлажняется с помощью раствора 5 г сульфата додецила натрия и 10 г поливинилпирролидона приблизительно в 200 мл воды. Влажная порошковая смесь просеивается, высушивается и вновь просеивается. Затем к ней добавляются 100 г микрокристаллической целлюлозы и 15 г гидрогенизированного растительного масла. Вся масса хорошо перемешивается и прессуется в таблетки, при этом получается 10000 таблеток, и каждая таблетка содержит 10 мг активного ингредиента.
Покрытие
К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляется раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем к нему добавляются 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляются и растворяются в 75 мл дихлорметана. Этот раствор добавляется к предыдущему раствору, и к ним добавляется 2,5 г октандеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной цветовой суспензии, затем вся смесь гомогенизируется. Сердцевины таблеток покрываются смесью, полученной таким образом, в аппарате для покрытия таблеток оболочкой.
Пример 24: РАСТВОР ДЛИ ИНЪЕКЦИЙ
1,8 г метил 4-гидроксибензоата и 0,2 г пропил 4-гидроксибензоата растворяются приблизительно в 0,5 л кипящей воды для инъекций. После охлаждения приблизительно до 50oC к раствору при помешивании добавляются 4 г молочной кислоты, 0,05 г пропилен гликоля и 4 г соединения примера 16. Раствор охлаждается до комнатной температуры, и к нему добавляется вода для инъекций в таком количестве, чтобы общий объем составил 1 л, при этом получается раствор, содержащий 4 мг/мл активного ингредиента. Раствор стерилизуется путем фильтрации и расфасовывается в стерильные емкости.


Изобретение описывает соединения общей формулы I, их приемлемые кислые аддитивные соли, их стереохимические изомерные формы, их N-оксиды, где R1 представляет водород, C1-6алкил; R2 представляет водород, C1-6алкил, тригалометилкарбонил, С1-6алкил, замещенный гидроксилом, карбоксилом, C1-6алкилкарбонилокси группой; R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют морфолиновое кольцо, или гетероцикл; R15, R16, R17, R18, R20 каждый представляет водород; R21 и R22 вместе представляют двухвалентный радикал C4-5 алкандиил; R23 представляет водород, C1-6алкил, тригалометилкарбонил, арил, ди(арил)метил, и арил представляет фенил, незамещенный или монозамещенный галогеном; R3 и R5 каждый представляет водород, галоген, C1-6алкил; R4 и R6 представляет водород, C1-6алкил, галоген, C1-6алкилокси; R7, R8, R13, R14 каждый представляет водород, C1-6алкил или R7 и R8, взятые вместе, образуют моно(циано)-метилен или метилен; R9 представляет собой водород, галоген, C1-6алкил или трифторметил; R10 представляет водород, C1-6алкил, галоген, трифторметил, ди(C1-6алкил)амино; R11 представляет водород, C1-6алкил, галоген, C1-6алкилокси, трифторметил; R12 представляет водород, C1-6алкил, трифторметил. Эти соединения тестировались как мХФП-антагонисты на крысах. Соединения формулы I используются как терапевтические средства для лечения или профилактики расстройств ЦНС, сердечно-сосудистых расстройств или желудочно-кишечных расстройств. Описывается также способ получения соединений формулы I, фармацевтическая композиция на их основе, промежуточный продукт и способ его получения. 5 с. и 6 з.п. ф-лы, 6 табл.
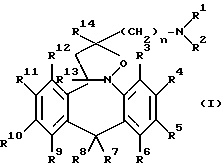
или их фармацевтически приемлемые кислые аддитивные соли, ил их стереохимические изомерные формы, или их N-оксиды, где R1 представляет водород, C1-6алкил; R2 представляет водород, C1-6алкил, тригалометилкарбонил, C1-6алкил, замещенный гидроксилом, карбоксилом, C1-6алкилкарбонилокси группой; R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют радикал формулы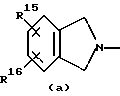
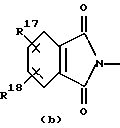

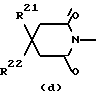

где R15, R16, R17, R18, R19, R20 каждый представляет водород;
m = 1, 2;
R21 и R22 вместе представляют двухвалентный радикал C4-5алкандиил;
R23 представляет водород, C1-6алкил, тригалометилкарбонил, арил, ди(арил)метил и арил представляет фенил, незамещенный или монозамещенный галогеном;
R3 и R5 каждый представляет водород, галоген, C1-6алкил;
R4 и R6 каждый представляет водород, C1-6алкил, галоген, C1-6алкилокси;
R7, R8, R13, R14 каждый представляет водород, C1-6алкил или R7 и R8, взятые вместе, образуют моно(циано)-метилен или метилен;
R9 представляет собой водород, галоген, C1-6алкил или трифторметил;
R10 представляет водород, C1-6алкил, галоген, трифторметил, ди(C1-6алкил)амино;
R11 представляет водород, C1-6алкил, галоген, C1-6алкилокси, трифторметил;
R12 представляет водород, C1-6алкил, трифторметил;
n = 1, 2, 3, 4.
где R3 - R13 имеют значения, указанные в п.1, его кислые аддитивные соли и его стереохимическая изомерная форма.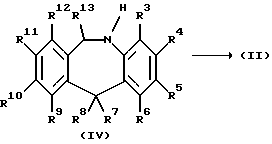
11. Способ получения соединения по п.1, отличающийся тем, что включает взаимодействие диенофила формулы (III) с промежуточным соединением формулы (II)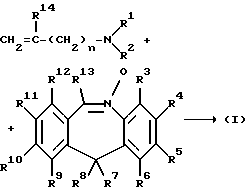
где R1 - R14 и n в промежуточных соединениях (II) и (III) имеют значения, указанные в п.1,
и, при необходимости, осуществляют одну из следующих стадий: а) полученное соединение формулы (I), в котором R1 и R2, вместе с атомом азота, к которому они прикреплены, образуют радикал формулы (b), превращают в соответствующий первичный амин обработкой гидразином или водной щелочью; б) соединение формулы (I), где R2 представляет трифторметилкарбонил, превращают в соответствующий первичный или вторичный амин гидролизом с водной щелочью; в) соединение формулы (I), где R2 представляет C1-6алкил, замещенный C1-6алкилкарбонилоксилом, гидролизом превращают в соединение формулы (I), где R2 представляет C1-6алкил, замещенный гидроксилом; г) соединение формулы (I), где R1 и R2 оба представляют водород, алкилированием моно- или ди-N-алкилом превращают в соответствующий амин; д) соединение формулы (I), где R1 и R2, оба представляют водород, ацилированием с помощью N-ацила превращают в соответствующий амид, с последующим превращением, при желании, любого из полученных соединения формулы (I) в терапевтически активную нетоксичную кислую аддитивную соль путем обработки кислотой, или, наоборот, кислая аддитивная соль может быть превращена в свободное основание путем обработки щелочью и, при желании, получают стереохимически изомерную или N-оксидную форму полученного соединения формулы I.
Приоритет по пунктам и признакам:
02.11.1994 - по пп.1 - 8 - за исключением п.1, когда R7 и R8 вместе образуют метилен, а также в случае N-оксидных форм соединений;
31.05.1995 - по пп. 9 - 11 - N-оксидные формы соединений формулы I и соединений, в которых R7 и R8 вместе образуют метиленовую группу.
| РАСПЫЛИТЕЛЬ | 2015 |
|
RU2647114C2 |
| МАГНИТНЫЙ СДВИГОВЫЙ РЕГИСТР | 0 |
|
SU318166A1 |
| US 5512563 A1, 30.04.96 | |||
| Способ получения 4,1-бензоксазепинов или их тиааналогов | 1979 |
|
SU936815A3 |
| ВСЕСОЮЗНАЯ ПАиНТВ04[Хп:Г!ЕСШБИБЛИОТЕКА | 0 |
|
SU352442A1 |
| Способ получения производных 1,4-диазепина | 1975 |
|
SU648104A3 |
Авторы
Даты
2001-02-20—Публикация
1995-10-25—Подача