Изобретение относится к способу удаления восстановленных соединений серы из потока газа посредством промывания газа водной промывной жидкостью и обработки отработанной промывной жидкости сульфидоокисляющими бактериями в присутствии акцептора электронов в реакторе и повторного использования обработанной жидкости в качестве промывной жидкости.
Подобный способ известен, например, из W0 92/10270, W0 92/29227 и W0 96/30110. В этих способах предшествующего уровня техники в качестве акцептора электронов используют кислород. Кислород подают при ограниченной скорости, так чтобы направлять окисление сульфидов предпочтительнее до элементарной серы, чем до сульфата. Однако, использование кислорода в качестве акцептора электронов требует присутствия системы аэрации, включающей в себя компрессор, систему трубопроводов, барботеры и в большинстве случаев отдельный реактор. Расходы по инвестированию для подобной системы являются относительно высокими, особенно в случаях, когда необходимо очистить небольшие объемы воды или газа или когда, например, необходимо провести десульфурирование природного газа под большим давлением.
В соответствии с изобретением отработанную промывную жидкость, содержащую восстановленные соединения серы, обрабатывают сульфидокисляющими бактериями в интегрированном скруббере биореакторе при использовании нитрата в качестве акцептора электронов.
В настоящем контексте понятие "восстановленное соединение серы" применяется для описания любого газообразного или летучего соединения серы, в котором сера имеет степень окисления -2. К подобным соединениям относятся сероводород, низший алкил-меркаптаны, такие как метантиол, (низший алкилсульфиды и дисульфиды, такие как диметилсульфид, карбонилсульфид (COS) и сероуглерод (CS2). Наиболее значимыми являются H2S, COS и CS2.
Реакции биологического окисления сероводорода посредством бесцветных серных бактерий, таких как представители рода Thiobacillus, в частности, вид T. denitrificans, с использованием нитрата в качестве акцептора электронов являются следующими:
H2S + ОН- ---> HS- + Н2O (1)
H2S + HCO3- ---> HS- + H2O + CO2 (1a)
5HS- + 2NO3- + H2O ---> 5S0 + N2 + 7OH- (2)
5HS- + 8NO3- ---> 5SO42- + 41N2 + 3ОН- + H2O (3)
5H2S + 2NO3- ---> 5S0 + N2 + 2OH- + 4H2O (1+2)
5H2S + 8NO3- + 2OH- ---> 5SO42- + 4N2 + 6H2) (1+3)
Реакция (1) обозначает предварительную реакцию, например, протекающую в газоочистителе, в которой газообразный сероводород растворяется в виде гидросульфидных анионов. Реакция (2) показывает бескислородное окисление сульфида до элементарной серы, тогда как реакция (3) представляет собой полное окисление сульфида до серной кислоты. Реакция (1+2) является полной общей реакцией превращения сероводорода до элементарной серы.
Карбонилсульфид и сероуглерод могут быть гидролизованы до сероводорода в соответствии с нижеследующими реакциями или их анионными эквивалентами:
COS + H2O ---> H2S + CO2 (4)
CS2 + 2H2O ---> 2H2S + CO2 (5)
Альтернативно или дополнительно, COS и CS2 могут быть окислены непосредственно, в соответствии со следующими реакциями:
5COS + 2NO3- + H2O ---> 5CO2 + +5So + N2 + 2OH- (2')
5COS + 8NO3- + H2O ---> 5CO2 + 5SO42- + 4N2 + 2OH- (3')
5CS2 + 4NO3- + 2H2O ---> 5CO2 + 10S0 + 2N2 + 4OH- (2'')
5CS2 + 16NO3- + 2H2O ---> 5CO2 + 10SO42- + 8N2 + 4H+ (3'')
Реакции, включающие в себя окисление тиосульфата с использованием нитрата в качестве акцептора электронов, являются следующими:
5S2O32- + 8NO3- + 2OH- ---> 10SO42- + 4N2 + H2O (6)
5S2O32- + 2NO3- + H2O ---> 5S0 + 5SO42- + N2 + 2OH- (7)
Нитрат может быть добавлен в виде твердой соли, но предпочтительно его добавляют в виде концентрированного раствора, например, нитрата калия или смеси нитрата с азотной кислотой. Так как превращение H2S и других восстановленных соединений серы в элементарную серу производит щелочь (уравнение 1+2/2'/2''), а превращение H2S и других восстановленных соединений серы в сульфат потребляет такое же количество щелочи (уравнение 1+3/3'/3''), кислоту (предпочтительно азотную кислоту, замещающую часть нитрата) необходимо добавлять в предпочтительном случае, когда сульфид преимущественно превращается в серу. Нитрат (и азотную кислоту) предпочтительно добавляют по существу в стехиометрическом количестве для окисления восстановленного соединения серы главным образом до серы, т.е. примерно 0,4 моль нитрата на моль H2S или COS с необязательным допущением незначительного окисления до сульфата, т.е. 0,4-0,9, в частности, 0,4-0,6 моль нитрата на моль H2S или COS, и в удвоенном количестве для CS2. Следует избегать слишком большой дозы нитрата потому, что это ведет к дестабилизации процесса вследствие накопления нитрита (NO2-). Концентрация нитрита должна оставаться ниже 1 мМ, предпочтительно ниже 0,5 мМ.
Добавление нитрата можно регулировать, используя окислительно-восстановительный потенциал водного раствора, как описано в WO 98/04503. Так, окислительно-восстановительный потенциал среды окисления устанавливают при величине ниже -150 мВ (против электрода сравнения Ag/AgCI, в частности, ниже -250 мВ. Предпочтительный диапазон окислительно-восстановительного потенциала находится в пределах от -300 до -390 мВ, более предпочтительно от -320 до -360 мВ (против электрода сравнения Ag/AgCI). Диапазон -300/-390 мВ против Ag/AgCI соответствует диапазону в -97/-187 мВ против электрода сравнения H2 при 30oC. Величины установленных точек окислительно-восстановительного потенциала относятся к температуре 30oC и pH 8.
Температура биологического окисления находится между 10 и 85oC, причем оптимум находится между 20 и 50oC, в особенности при 30oC. Оптимум pH находится в пределах от 7 до 9. Если раствор не содержит питательных веществ, как в случае промывания газа, их также необходимо добавлять. Это может быть сделано одновременно с подачей нитрата. Электрическую проводимость промывной жидкости предпочтительно поддерживают между 30 и 100 мс/см.
Бактерии для использования в настоящем способе могут быть взяты из общепринятых сульфидокисляющих культур. Эти бактерии являются предпочтительно нейтрофильными бактериями и, как правило, включают в себя виды Thiobacillus, в особенности T.denitrificans.
Способ данного изобретения может быть использован для обработки газов, содержащих также углекислый газ. Углекислый газ участвует в допустимой нагрузке H2S промывной жидкости, в особенности при высоких давлениях. В качестве примера, допустимая нагрузка H2S промывной жидкости для промывания находящегося под давлением газа (95 бар), имеющего содержание CO2 1,1 об./%, равна 200 - 300 г/м3. Углекислый газ может быть также использован в качестве источника углерода для сульфидокисляющих бактерий.
В способе данного изобретения для удаления сероводорода и других восстановленных соединений серы из газовых потоков, раствор рециркулируется после окисления восстановленных соединений серы до элементарной серы с использованием одного и того же реактора для промывания и для бескислородной биологической обработки. Рециркуляция жидкости между различными давлениями не является необходимой. Дальнейшие преимущества состоят в том, что оборудование может быть относительно простым и недорогим, и что коэффициент рециркуляции и, следовательно, время пребывания жидкости в зоне реакции, может быть достаточно высоким, так что любая потеря биомассы компенсируется бактериальным ростом. При необходимости, бактерии могут быть иммобилизированы на носителе, который в свою очередь может быть объединен с наполнителем в скруббере. Для простой операции такой иммобилизацией можно пренебречь.
Способ может быть выполнен в установке, изображенной на чертеже. Газовый скруббер/реактор 1 снабжен системой 2 подачи сульфидсодержащего газа и системой 3 выхода очищенного газа. Промывная жидкость рециркулируется через трубопровод 4 без перепада давления и избыток жидкости выпускается через трубопровод 5. Скруббер содержит наполнитель 6 для улучшения контакта между газом и промывной жидкостью. Добавочную (подпиточную) воду, содержащую питательные вещества и микроэлементы, вводят через линию 7. Нитрат (акцептор электронов) подают через 8, но он также может быть добавлен к добавочной воде линии 7. Азотная кислота может быть использована для регуляции pH и добавлена через линии 7 или 8 или отдельно. Отделитель 9 расположен в потоке 5 выпускаемого газа, где суспензия серы отделяется и удаляется через трубопровод 10. Осветленная жидкость 11 может быть повторно использована в качестве добавочной воды в линиию 7. Альтернативно, отделитель серы может быть помещен в обводном рециркуляционном трубопроводе 4. Предпочтительно, чтобы элементарная сера не была полностью отделена: остаточный уровень 0,1-5 мас.%, в особенности 0,3-3 мас. %, является выгодным для улучшенной абсорбции сульфидов промывной жидкостью и улучшения буферного действия. Уровень серы в скруббере/реакторе может быть отрегулирован установкой коэффициента нециркуляции (потока трубопровода 4 относительно потока трубопровода 5) и/или корректировкой эффективности отделения в отделителе серы.
Способ данного изобретения может быть выгодно применен для обработки небольших потоков биогаза, подобных производящем менее 100 кг серы в день. Для подобных потоков стоимость добавления нитрата является более, чем компенсированной, за счет экономии в инвестициях как результата отказа от использования дорогих компрессоров, барботеров и других приспособлений, необходимых для подачи кислорода.
Способ также может быть использован для очистки вентиляционного воздуха, содержащего сероводород, такого как воздух, генерируемый в анаэробных очистных реакторах, насосных станциях и отстойниках. Если подобный вентилирующий воздух содержит недостаточное количество кислорода или если переход кислорода в водную фазу недостаточен, нитрат успешно выступает в качестве (дополнительного) акцептора электронов.
Способ данного изобретения пригоден также для очистки природного газа и других газовых потоков высокого давления, например, 50 бар или выше. Обычно такие высокие давления делают непривлекательной биологическую очистку природного газа вследствие высоких энергетических затрат из-за необходимости подачи промывной жидкости в газоочиститель под высоким давлением и снижения давления жидкости для поступления в аэрируемый аэробный реактор. Способы предшествующего уровня техники удаления сероводорода и других восстановленных соединений серы из природного газа включают в себя: (1) обратимую химическую или физическую абсорбцию, основанную на алканоламине или карбонатных растворителях; для этих способов необходимы высокие температуры и перепады давления; кроме того, часть дорогого раствора амина теряется с выпускаемым потоком; (2) прямую конверсию через абсорбцию и окисление, например, основанную на окислительно-восстановительной реакции между H2S и Fe3+, в которой восстановленный металл повторно окисляется кислородом; недостатками таких способов являются тенденция к закупориванию конгломератами серы и использование дорогих хелатов коррозионных металлов; (3) необратимую абсорбцию, при которой сероводород абсорбируется, например, на активированный уголь или губчатое железо, которые систематически заменяются и ликвидируются "выбрасываются".
В настоящем способе стадии увеличения/уменьшения давления могут быть опущены, поскольку биологическая обработка не требует наличия газообразного кислорода, и, следовательно, промывание газа может быть интегрировано с биореактором.
К другим газам, которые могут быть очищены по способу данного изобретения, относятся газы, связанные с нефтяным светильным газом и природным (нефтяным) газом, газ из стабилизационной колонны, газ из установок глубокого вакуума, топливный газ, газ из агрегатов HDS, газ из молекулярных сит, синтез-газ, содержащий сероводород, из газовых потоков CO2.
Пример 1
В установке, изображенной на чертеже, имеющей объем скруббера 10 м3, природный газ под давлением 95 бар, содержащий 100 об.м.д. H2S и 1,1 об.% CO2, обрабатывается при 25000 Нм3 в день с использованием промывной жидкости, имеющей pH около 8,5, и с использованием биомассы, содержащей Thiobacillus denitrificans. Нитрат калия и азотная кислота подаются в количестве 50-200 г/час и 50-200 г/час соответственно. Используют скорость рециркуляции жидкости 0,5-5 м3/час. Содержание H2S в очищенном газе составляет 2 об.м.д. (эффективность десульфуризации: 98%).
Пример 2
Установку, показанную на чертеже, состоящую из интегрированного скруббера и биореактора, использовали для удаления H2S из вентиляционного воздуха, содержащего как H2S, так и кислород. Поток обрабатываемого воздуха достигает 900 м3/час с концентрацией H2S между 500 и 800 м.д. pH промывной жидкости поддерживали между 8,5 и 9 с удельной электропроводностью 40 мс/см. Нитрат добавляли при 0,3 кг/час из комбинации азотной кислоты и нитрата калия так, чтобы pH поддерживался в указанном диапазоне. Отношение нитрата к сульфиду было 0,25 моль/моль, что гораздо ниже теоретически ожидаемого отношения 0,4-1,6 моль/моль. Причиной этого является то, что вентиляционный воздух содержит кислород, который также действует в качестве акцептора электронов. В течение всего испытательного периода не был детектирован H2S в отходящем газе тогда, как концентрация нитрата была менее 10 м.д. Остаточную элементарную серу в выпускаемом потоке декантировали и извлекали.
Данное изобретение относится к способу удаления сульфидов, в том числе сероводорода, карбонилсульфида и сероуглерода из газового потока. Способ применим, в частности, для десульфуризации газа при высоком давлении, такого как природный газ. Восстановленные соединения серы удаляют посредством промывания газа водной промывной жидкостью и обработки промывной жидкости сульфидоокисляющими бактериями в присутствии акцептора электронов и повторного использования этой обработанной жидкости в качестве промывной жидкости, при этом промывание газа и бактериальную обработку проводят в одном и том же реакторе и в качестве акцептора электронов используют нитрат. Способ позволяет снизить расходы по инвестированию, исключив систему аэрации, которая необходима, если в качестве акцептора электронов используют кислород. 8 з.п. ф-лы, 1 ил.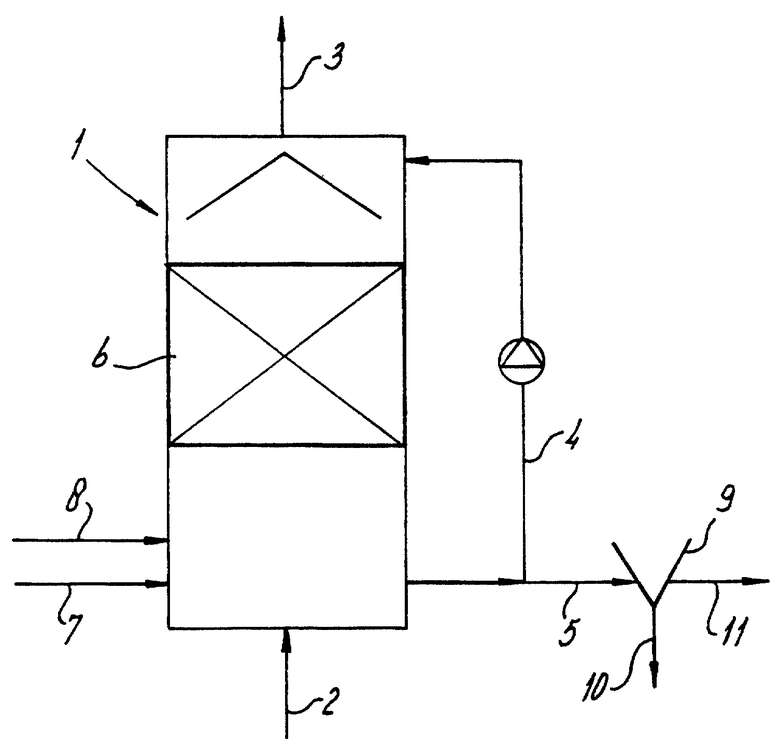
| WO 9630110 A1, 03.10.1996 | |||
| ЛИНИЯ ЗАДЕРЖКИ | 0 |
|
SU218958A1 |
| WO 9429227 A1, 22.12.1994 | |||
| 0 |
|
SU402704A1 | |
| US 5236677 A, 17.08.1993 | |||
| Способ очистки многокомпонентных парогазовых смесей | 1989 |
|
SU1701349A1 |
| Способ очистки коксового газа от сероводорода | 1978 |
|
SU704649A1 |
Авторы
Даты
2001-01-10—Публикация
1997-11-26—Подача