Область техники
Настоящее изобретение относится к получению сероводорода из элементарной серы в мягких условиях и к применению сероводорода для извлечения металлов.
Предпосылки
Сероводород представляет собой дорогостоящий химический реагент, используемый в металлургической и добывающей промышленности, а также в электронной промышленности. Его используют, например, при добыче никеля, цинка и меди и в металлургических процессах для селективного извлечения и выделения металлов из водных выщелачивающих потоков, из продувочных потоков установки по производству кислоты, электролитных сливов при нефтепереработке и сливов установки по производству благородных металлов. Обычно необходимый сульфид:
(i) производят на месте каталитическим восстановлением элементарной серы при повышенных давлении и температуре (выше 150° С) или переносят в нужное место позже в виде сжиженного сероводорода (H2S); подобные способы получения химического реагента сероводорода известны, например, из патентов США 4094961, 4146580 и 4332774;
(ii) переносят в нужное место в виде раствора гидросульфида натрия (NaHS); или
(iii) производят на месте биологическим восстановлением сульфата из разбавленных потоков сточных вод (смотри, например, WO 97/29055, патент США 5587079).
Недостатки этих способов заключаются в том, что они являются относительно дорогостоящими, нуждаются в катализаторах, введении больших загрузок соли, щелочи или кислоты и требуют больших мер безопасности.
В WO 92/17410 описан способ выделения соединений серы из воды при анаэробной обработке восстанавливающими серу бактериями при высоких температурах.
Описание изобретения
В настоящее время найден улучшенный способ получения сероводорода. В способе настоящего изобретения используют элементарную серу, которую биологически восстанавливают в сероводород. По сравнению с вышеупомянутыми способами данный способ имеет следующие преимущества:
(a) Биологическое восстановление элементарной серы можно осуществлять при умеренных температуре и давлении. По сравнению с каталитическим восстановлением на месте биологическое восстановление намного безопаснее и дешевле. Еще одно преимущество нового способа заключается в том, что производство сульфида возможно на основе потребности. Биологическое производство сульфида можно запустить и прекратить очень легко.
(b) По сравнению с добавлением раствора гидросульфида натрия (NaHS) в способах, в которых необходим сульфид, полученный биологическим способом сульфид менее дорогой, и он имеет преимущество в том, что в рассматриваемые процессы не вводят натрий. Очень часто в металлургических операциях необходимо низкое значение рН, что подразумевает то, что при добавлении в процесс, кроме того, натрия потребуется добавить большее количество кислоты. Кроме того, натрий попадает в поток сточных вод в виде сульфата натрия, который необходимо отвести или обработать. Однако в этом случае при традиционной обработке известью сульфаты не удастся удалить так же эффективно, как ранее, из-за присутствия натрия.
(с) По сравнению с биологическим производством сульфида из разбавленного сульфатсодержащего потока сточных вод способ данного изобретения имеет несколько преимуществ. Он намного менее дорогостоящий благодаря тому, что для восстановления элементарной серы требуется лишь 25% количества донора электронов (газообразного водорода или органических соединений) по сравнению с восстановлением сульфата. Следующее преимущество заключается в том, что в биореакторе можно поддерживать низкий уровень рН, что дает возможность более эффективно выделять полученный сероводород из жидкости. Кроме того, в способе изобретения воду можно использовать повторно, что минимизирует выходной поток сульфидсодержащей жидкости до нуля. В случае получения сульфида из сульфата, находящегося в разбавленном потоке сточной воды, обычно требуется последующая обработка для окисления растворенного сульфида, находящегося в выходном потоке анаэробного реактора. Следующее преимущество состоит в том, что благодаря тому, что не требуется отвода жидкости, бактерии, таким образом, могут сохраняться в реакторе без необходимости в системе удерживания биомассы. Это значительно повышает концентрацию активной биомассы и приводит к более высоким скоростям производства сульфида.
Способ данного изобретения можно осуществить с использованием биореактора, в который подают концентрированный поток элементарной серы и донор электронов для биологического восстановления серы с получением сероводорода. В качестве донора электронов можно использовать газообразные компоненты, например водород и монооксид углерода, а также органические соединения, такие как этанол, метанол, уксусную кислоту и другие жирные кислоты.
Биологические характеристики
Бактерии: биологическое восстановление серы осуществляют с помощью смешанной культуры неидентифицированных восстанавливающих серу бактерий, таких как виды из родов: виды Desulforomonas (мезофильный), Desulfotomaculum KT7 (термофильный), вид Desulforolobus ambivalens, Acidianus infernus, Acidianus brierley, Stygiolobus azoricus (мезофильный), Thermoproteus neutrophilus, Thermoproteus tenax, Thermodiscus maritimus (термофильный), Pyrobaculum islandicum, Pyrodictium occultum, Pyrodictium brockii (гипертермофильный) и другие виды родов Desulfovibrio, Desulfotomaculum, Desulfomonas, Desulfobulbus, Desulfobacter, Desulfococcus, Desulfonema, Desulfosarcina, Desulfobacterium и Desulforomas (мезофильный), и виды серовосстанавливающих метаногенных бактерий, например, таких, которые составляют рода Methanococcus и Methanobacterium.
Донор электронов: газообразный водород, монооксид углерода, спирты (например, этанол, метанол), жирные кислоты (например, уксусная кислота) или другие легко разлагаемые органические соединения.
Биологические превращения:
Газообразный водород в качестве донора электронов:
H2+S° → Н2S.
Органическое соединение, например этанол, в качестве донора электронов:
C2H5OH+6 S° +3 Н2О → 6 Н2S+2 СО2.
Температура: Способ можно осуществлять в мезофильных условиях (15-40° С) или в термофильных условиях (40-90° С). Предпочтительными интервалами температур являются 25-75° С. Мезофильные температуры для использования с водородом являются особым аспектом данного изобретения.
рН: работа в интервале от рН 5 до 9, предпочтительно от 6 до 8,5, наиболее предпочтительно от 6 до 8.
Можно извлекать металлы, такие как медь, цинк, никель, кобальт, олово, свинец, кадмий, висмут, ртуть, серебро, железо, марганец, хром, ванадий и титан, при контакте сероводорода, полученного в соответствии с настоящим изобретением, с жидкостью, содержащей указанные металлы, и осаждении металлов в виде их сульфидов. Такие металлы можно также извлекать селективно, используя, например, варьирование значений рН, как описано в WO 97/29055.
После осушки концентрированный шлам сульфида металла можно обработать с использованием обычных металлургических способов для выделения чистого металла. Например, сульфиды меди и цинка можно перевести в элементарные медь и цинк способами обжига и плавления в сочетании с электролитическим выделением. Особенно подходящим для выделения меди и свинца является способ ECUPREX®-EW, поскольку в этом способе в качестве побочного продукта образуется элементарная сера и этот побочный продукт можно использовать вновь для получения требуемого сероводорода. Этот способ описан в ЕР-А-411687. Таким образом, медь и свинец можно извлекать из сточных вод или технологических потоков путем осаждения сероводородом в виде нерастворимых сульфида меди или сульфида свинца в соответствии с
1. CuSO4+H2S → CuS+H2SO4.
Согласно способу ECUPREX®-EW эти сульфиды металлов осаждают и сушат, а затем приводят их в контакт с фтороборным выщелачивающим раствором, в котором металл растворяется, а сульфид окисляется до элементарной серы в соответствии с
2. CuS+2 Fе(ВF4)3 →Сu(ВF4)3+2 Fe(BF4)2+S° .
После отделения элементарной серы используют электролиз для получения чистой меди на катоде и для повторного окисления железа на аноде в соответствии с
3. Cu(BF4)2+2е- →Сu+2 BF
2 Fe(BF4)2+2BF
После сушки полученный на стадии выщелачивания (стадия 2) осадок можно использовать для биологического производства сероводорода, а полученный сероводород используют вновь для осаждения металла на стадии 1. Таким образом был разработан идеальный цикл серы, в котором не нужно покупать никаких сернистых соединений для получения сероводорода, необходимого для осаждения металлов на стадии 1.
Инженерные характеристики
Проект способа
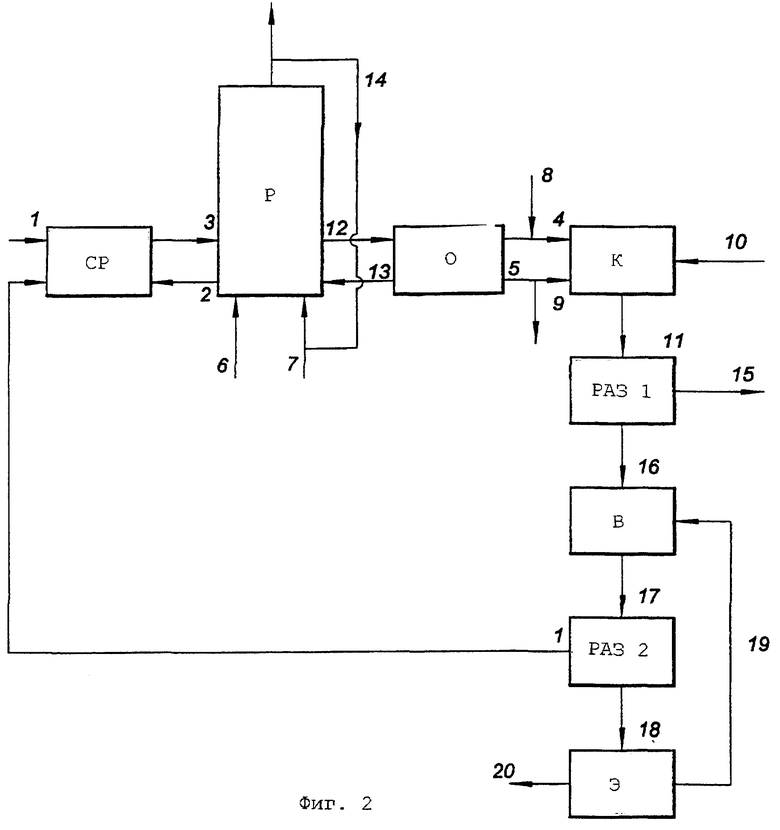
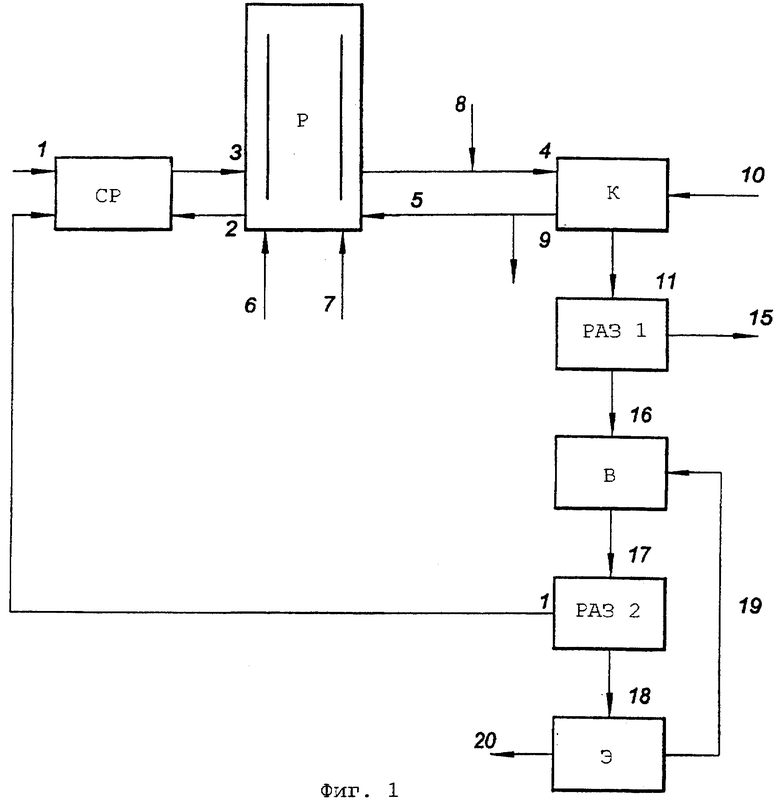
На фиг.1 показана возможная схема способа. Элементарную серу (1) предпочтительно прибавляют в виде измельченных частиц, которые либо непосредственно вносят в реактор, либо предпочтительно суспендируют в смесительном резервуаре (СР), используя для этой цели часть жидкости из реактора (3) перед добавлением (2) в биореактор (Р). В анаэробный биореактор прибавляют донор электронов (органическое соединение (6) или водород/монооксид углерода (7)) и восстанавливают элементарную серу с получением сероводорода в умеренных условиях. В биореакторе осуществляют хорошее перемешивание для суспендирования биомассы и частиц серы в реакторе и создания между ними эффективного контакта. Кроме того, перемешивание предотвращает градиенты концентрации растворенного сульфида и рН внутри реактора. Перемешивание можно осуществлять различными способами, хотя предпочтительно перемешивать содержимое реактора с использованием потока оборотного газа (4, 5). В этом случае предпочтительно использовать реактор аэролифтного циркуляционного типа для оптимизации характеристик перемешивания реактора. Оборотный газ предпочтителен для перемешивания, поскольку он обеспечивает простой способ контролирования рН в реакторе и удаление полученного сероводорода из реактора при контакте оборотного газа с технологическим потоком, в котором необходим сероводород. Другая возможная схема заключается в том, что часть жидкого стока (12) анаэробного биореактора поступит к отдельной сульфидной отпарной колонне (О) с рециркуляцией (13) и сульфид из этого потока удаляют при контакте его либо с потоком технологического газа (14), либо с потоком оборотного газа (4, 5) через контактор (К). Это показано на фиг.2. Однако недостаток этой блок-схемы заключается в том, что сероводород не удаляется из жидкости в самом реакторе. Использование аналогичного рН в биореакторе будет означать, что рН в отпарной колонне повысится вследствие удаления сероводорода, что приведет к тому, что для переноса того же количества сероводорода потребуется больший поток оборотного газа через контактор.
Контактор (К) представляет собой устройство, в котором сероводородсодержащий оборотный газ приводят в контакт с технологическим потоком (10) для переноса сероводорода из оборотного газа в технологический поток. Проектировка контактора и связанных с ним технологических потоков может различаться для разных применений. Например, контактор мог бы представлять собой колонну открытого типа с орошением распыленной жидкостью, в которой металлсодержащий технологический поток приводят в контакт с оборотным газом. Металлы осядут в виде сульфидов металлов и могут быть отделены от технологического потока после контактора.
Технологический поток (10) может предпочтительно представлять собой металлсодержащий поток (10), в который переносят сероводород из оборотного газа. Металлы осядут, а осадки можно будет отделить от жидкости после (11) контактора в разделителе для твердых веществ (РАЗ 1). Проектировка газожидкостного контактора зависит, главным образом, от скорости газового потока, скорости потока жидкости, концентрации сероводорода в газе и концентрации металла в жидкости. Для этой цели можно, например, использовать колонну открытого типа с орошением распыленной жидкостью или насадочную колонну. После осаждения сульфидов металлов обработанную воду (15) отводят, а сульфиды металлов (16) сушат и после этого их можно обработать с использованием обычных металлургических способов для выделения чистого металла. В случае способа ECUPEX-EW осушенный шлам сульфида меди или свинца приводят в контакт с фтороборным выщелачивающим раствором (19) в реакторе выщелачивания (В). Во втором разделителе для жидкостей-твердых веществ (РАЗ 2) элементарную серу (1) отделяют от потока (17) и возвращают в биореактор (Р). Содержащий растворенные металлы раствор (18) направляют в электролизер (Э), в котором получают чистый металл (20) и регенерируют фтороборный выщелачивающий раствор (19).
Вместо металлсодержащей жидкости подаваемый в контактор (К) технологический поток (10) может также представлять собой жидкость, которая абсорбирует сероводород для транспортировки его в регенерационную колонну для концентрирования сероводорода в газовый поток с более высоким процентным содержанием (>90%). Сероводородный газовый поток можно использовать для различных промышленных назначений сероводорода. Кроме того, контактор (К) может также представлять собой мембранную установку, в которой сероводород селективно выделяют и концентрируют для получения, кроме того, газового потока более высокой концентрации для использования для различных промышленных целей. Можно также отогнать сероводород непосредственно из биореактора (Р) или из отпарной колонны (О) с использованием потока технологического газа вместо того, чтобы использовать оборотный газ для переноса сероводорода в поток жидкости.
Контроль процесса
Для достижения высоких скоростей производства сероводорода следует осуществлять тщательное контролирование процесса. Важным фактором является контроль рН в водной системе (водная система включает в себя реактор и необязательную отпарную колонну и соединительные трубопроводы). Биологическое восстановление элементарной серы с использованием газообразного водорода, монооксида углерода или органических соединений в качестве донора электронов приводит к получению в биореакторе кислот сероводорода и двуокиси углерода. В принципе, это может понизить рН в реакторе до низкого уровня, что способно ингибировать биологические реакции. Поскольку любой спуск потока жидкости из водной системы нежелателен, повышение рН в реакторе путем постоянного прибавления щелочных компонентов, таких как гидроксид натрия, нежелательно, так как концентрация натрия постепенно возрастет до неприемлемых значений, что вызовет отвод потока жидкости до некоторого уровня. Значение рН системы контролируют путем удаления кислот из жидкости при отгонке либо непосредственно из реактора (фиг.1), либо из выходного потока реактора (фиг.2) в сочетании с удалением кислотных компонентов из оборотного газа. Отсутствие отвода жидкости соответствует длительному гидравлическому времени удерживания, составляющему, по меньшей мере, 1 день, предпочтительно, по меньшей мере, 5 дней, вплоть до 1 месяца или более, в зависимости от количества воды, введенной с элементарной серой.
Процесс является непрерывно действующей системой и весь полученный сероводород в конечном итоге удаляют из жидкости. Однако рН и концентрацию растворенного сероводорода в реакторе можно выбирать свободно. Их можно установить на определенном уровне, отрегулировав подачу донора электронов для удаления сероводорода в контактор. Концентрацию сероводорода в газе поддерживают высокой, чтобы иметь возможность уменьшить поток оборотного газа для переноса сероводорода и увеличить массоперенос в контакторе. Концентрация сероводорода в газе составляет, по меньшей мере, 1 об.%, предпочтительно, по меньшей мере, 3 об.%, более предпочтительно, по меньшей мере, 10 об.%. Поскольку отвод жидкости из системы биореактора небольшой или отсутствует, концентрацию активной биомассы легко можно увеличить без установки системы удерживания биомассы. Это предусматривает более высокие допустимые концентрации растворенного сероводорода в газе. Концентрации растворенного сульфида в биореакторе предпочтительно составляют, по меньшей мере, 300 мг/л, в особенности, по меньшей мере, от 600 до 3000 мг/л. Концентраций растворенного сероводорода, превышающих 3000 мг/л (больше 20% в газе) можно достигнуть без потери мощности производства сульфида в биореакторе. Биологическое производство сероводорода можно мгновенно прекратить, прервав удаление сероводорода из контактора. Тогда концентрация сероводорода повысится и, в конечном итоге, подавит производство сероводорода. Данный процесс обратим. Так, после повторного начала удаления сероводорода концентрация в биореакторе снизится и производство сероводорода немедленно возобновится. Другой способ мгновенного прекращения и запуска производства заключается в прекращении и возобновлении подачи донора электронов.
Сероводород удаляют в виде кислоты в контакторе (К), а полученную двуокись углерода удаляют путем отдувки части газа (9) из системы рециркуляции газа. Количество удаленной двуокиси углерода можно контролировать путем регулировки количества инертного газа, например газообразного азота (8), добавленного с этой целью к оборотному газу. Добавочный газ, полученный из продувки двуокиси углерода, отделяют от сероводорода и затем удаляют.
Пример 1
В 5-литровый аэролифтный циркуляционный реактор прибавляли 1,25 г/ч элементарной серы путем нагнетания насосом из резервуара, в котором измельченную серу смешали с жидкостью из биореактора. В качестве донора электронов для биологического восстановления добавили газообразный водород. Добавочную воду не использовали и отвода жидкости не было. Реактор эксплуатировали при 35° С, а рН в реакторе поддерживали при 7,5, отгоняя сероводород из жидкости с оборотным газом. Оборотный газ приводили в контакт с выщелачивающей водой (7 л/ч), содержащей медь, выделяя сероводородную кислоту из оборотного газа и извлекая медь из выщелачивающей воды в виде сульфида меди. Были зарегистрированы концентрации растворенного сероводорода вплоть до 2000 мг/л. Концентрация сероводорода в газе достигла 15%.
Пример 2
В 8-литровый лабораторный реактор ежедневно добавляли 80 грамм измельченной элементарной серы, а в качестве донора электронов для восстановления непрерывно добавляли этанол. Реактор эксплуатировали при 30° С, а рН регулировали на уровне рН 7, используя оборотный газ для отгонки сероводорода и двуокиси углерода. Сероводород выделяли из оборотного газа при контакте данного газа с раствором, содержащим сульфат меди, в барботажной колонне. Двуокись углерода удаляли при добавлении к оборотному газу небольшого количества газообразного азота, создавая поток продувочного газа, содержащего азот, двуокись углерода и небольшое количество сероводорода. Были зарегистрированы концентрации растворенного сероводорода вплоть до 1500 мг/л. Концентрация сероводорода в газе достигла 20%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БИОГЕННОГО СЕРОВОДОРОДА | 2014 |
|
RU2577114C1 |
| СПОСОБ ОБРАБОТКИ ВОДЫ, СОДЕРЖАЩЕЙ ИОНЫ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1997 |
|
RU2178391C2 |
| СПОСОБ ОБРАБОТКИ ЗАГРЯЗНЕННОГО МАТЕРИАЛА | 1995 |
|
RU2133632C1 |
| СПОСОБ ОЧИСТКИ ОТХОДЯЩЕГО ИЛИ ДЫМОВОГО ГАЗА, СОДЕРЖАЩЕГО ОКИСЛЫ АЗОТА | 1996 |
|
RU2146964C1 |
| СПОСОБ УДАЛЕНИЯ СОЕДИНЕНИЙ СЕРЫ ИЗ ВОДЫ (ВАРИАНТЫ) И СПОСОБ ОБРАБОТКИ СЕРУСОДЕРЖАЩЕГО ДЫМОВОГО ГАЗА | 1993 |
|
RU2108982C1 |
| СПОСОБ ПРЕОБРАЗОВАНИЯ СОЕДИНЕНИЯ СЕРЫ | 2019 |
|
RU2780483C2 |
| СПОСОБ ДЕСУЛЬФУРИЗАЦИИ ГАЗОВ | 2000 |
|
RU2241527C2 |
| СПОСОБ ОБРАБОТКИ ГАЗОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1996 |
|
RU2164167C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕМЕНТАРНОЙ СЕРЫ | 2018 |
|
RU2764882C2 |
| СПОСОБ ПРЕВРАЩЕНИЯ БИСУЛЬФИДА В ЭЛЕМЕНТАРНУЮ СЕРУ | 2018 |
|
RU2769804C2 |
Способ предусматривает восстановление элементарной серы в жидкой среде с использованием микроорганизмов и газообразного водорода, моноокиси углерода или органических соединений в качестве донора электронов. При этом гидравлическое время удерживания жидкой среды составляет по меньшей мере 1 день, а рН 5-9. Затем осуществляют отгонку сероводорода с получением газа, содержащего не менее 1 об.% сероводорода. Полученный сероводород могут направлять на взаимодействие с потоком, содержащим тяжелые металлы, после чего осуществляют осаждение сульфидов. Способы получения сероводорода и обработки тяжелых металлов являются менее дорогостоящими и имеют преимущества в безопасности. 2 н. и 10 з.п.ф-лы, 2 ил.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| US 5670123 А, 23.09.1997 | |||
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФИДА МЕТАЛЛА | 1996 |
|
RU2112743C1 |
| ХОМЧЕНКО Г.П | |||
| Химия для подготовительных отделений | |||
| - М.: Высшая школа, 1989, с.173 и 174. | |||
Авторы
Даты
2004-09-10—Публикация
1999-11-16—Подача