Изобретение относится к производным дифенилметиленпиперидина, к содержащим их фармацевтическим композициям, к способу их получения и к способу лечения и профилактики психотических расстройств.
Из уровня техники известны родственные производные дифенилметиленпиперидина. В особенности родственные соединения описаны в патенте США 4,540,780 и в выделенном из него патенте США 4,666,905, в которых упоминаются производные дифенилметиленпиперидина, пригодные как противорвотные, антигистаминные, легочные и противоспазмолитические средства.
Настоящее изобретение относится к производным дифенилметиленпиперидина формулы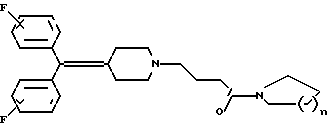
где n равно 1 или 2, или к их фармацевтически приемлемым солям.
Более предпочтительно, чтобы производные дифенилметиленпиперидина по изобретению имели оба атома фтора, присоединенные в пара-положении к бензольным кольцам.
Предпочтительным соединением является производное дифенилметиленпиперидина, имеющее формулу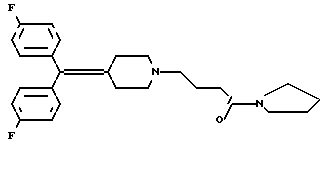 или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
Производные дифенилметиленпиперидина по изобретению являются антагонистами рецептора допамина, которые обладают сильной антипсихотической активностью, как было продемонстрировано in vivo в испытании на лазанье при воздействии апоморфина (ИЛА) (apomorhine climbing test, ACT). Способность антагонистов рецептора допамина подавлять поведенческие эффекты у грызунов, вызванные агонистами допамина, такими как апоморфин, является хорошо установленным критерием для предсказания антипсихотической эффективности этих лекарств у человека (например, см. W.C. Bowman и M.J. Rand, Textbook of Pharmacology (Учебник по фармакологии), 2 изд., 1980, 15, 6). Особенно подходящим тестом в этом отношении является ИЛА, в котором измеряется способность антагониста допамина подавлять поведение с лазаньем у мышей, вызванное подкожным введением апоморфина. Активность в данном испытании широко используют для предсказания антипсихотической активности, то есть антишизофренической активности (например, см. J.T. Strupczewski и др., J.Med. Chem., 1995, 38, 1119).
Соединения по данному изобретению (позиции 1 и 2) сравнивали с различными родственными производными дифенилметиленпиперидина в соответствии с патентом США 4,540,780 (позиции 3-15), и результаты приведены в следующей таблице 1.
Пять соединений из таблицы 1, которые имели наибольшую активность после подкожного введения, испытывали в ИЛА после перорального введения. Результаты приведены в таблице 2.
Как продемонстрировано в таблице 2, соединения по данному изобретению имеют хорошую пероральную активность в сравнении с производными дифенилметиленпиперидина в соответствии с патентом США 4,540,780. Более того, заявляемые здесь соединения не приводят к проявлению каталепсии, что предсказывает отсутствие у них нежелательных экстрапирамидальных побочных эффектов.
Соединения по изобретению можно получить методами, известными на уровне техники, например с помощью методов, аналогичных получению, описанному в патенте США 4,540,780. Подходящий способ получения заключается в конденсации 4-бис(2-, 3- или 4-фторфенил)метиленпиперидина или его соли (например, гидрохлорида), синтез которого описан в патенте США 4,50,780, с 1-(4-гало-1-оксобутил)пирролидином (n=1) или с 1-(4-гало-1-оксобутил)пиперидином (n=2), где гало представляет подходящий атом галогена, такой как хлор, бром или иод, после чего полученное соединение необязательно превращают в фармацевтически приемлемую соль.
Новые соединения по изобретению можно выделить из реакционной смеси в форме фармацевтически приемлемой соли. Фармацевтически приемлемые соли также могут быть получены путем обработки свободного основания формулы I органической или неорганической кислотой, такой как HCl, HBr, Hl, H2SO4, H3PO4, уксусная кислота, пропионовая кислота, гликолевая кислота, малеиновая кислота, малоновая кислота, метансульфоновая кислота, фумаровая кислота, янтарная кислота, винная кислота, лимонная кислота, бензойная кислота и аскорбиновая кислота.
Соединен по изобретению можно вводить энтерально или парентерально, и предпочтительно при дневной дозе для человека 0,001-10 мг на кг веса тела. Будучи смешанными с фармацевтически пригодными вспомогательными веществами, например, с описанными в стандартной ссылке Gennaro и др., Remington's Pharmaceutical Sciences (18 изд., Mack Publishing Company, 1990, см. Особенно часть 8: фармацевтические препараты и их изготовление), соединения можно спрессовать в твердые дозировочные единицы, такие как пилюли, таблетки, или же переработать их в капсулы или суппозитории. Кроме того, с помощью фармацевтически пригодных жидкостей соединения можно использовать как препарат для инъекций в форме раствора, суспензии, эмульсии или в виде аэрозоля, например аэрозоля для носа.
Для изготовления дозировочных единиц, например таблеток, предвидится использование обычных добавок, таких как наполнители, красители, полимерные связующие и т.п.. В общем, можно использовать любую фармацевтически приемлемую добавку, которая не мешает действию активных соединений. К подходящим носителям, с которыми можно вводить композиции, относятся лактоза, крахмал, производные целлюлозы и т.п. или их смеси, используемые в подходящих количествах.
Далее изобретение иллюстрируется следующими примерами.
Пример 1.
Получение этилового эфира 1-(трифенилметил)-4-пиперидин-карбоновой кислоты
Раствор этилизонипекотата (25 г, 0,165 моль) в дихлорметане (250 мг) и триэтиламин (50 мл) охлаждали в водяной бане и порциями добавляли трифенилметилхлорид (48,7 г, 0,175 моль). Вскоре после окончания добавления образовался осадок. Смесь перемешивали при комнатной температуре в течение 24 часов, после чего ее промыли водой, сушили над сульфатом натрия и выпаривали досуха с получением желтого масла (74,0 г). Это масло растирали с метанолом и получили продукт в виде кристаллов кремового цвета с выходом 97% (61,9 г); т.пл. 164oC.
Получение α,α-бис-(4-фторфенил)-1-(трифенилметил)-4-пиперидинметанола
1-Бром-4-фторбензол (154 мл, 1,402 моль) в безводном эфире (640 мл) добавляли к суспензии магниевых стружек (34,1 г, 1,404 моль) в безводном эфире (250 мл), и смесь перемешивали в атмосфере азота со скоростью, приводящей к легкому кипению с обратным холодильником. Раствор охладили, перемешивали при комнатной температуре в течение 45 минут, а затем охлаждали в ледяной бане. К этому раствору в течение 40 мин по каплям прибавляли раствор этилового эфира 1-(трифенилметил)-4-пиперидинкарбоновой кислоты (90 г, 0,225 моль) в безводном тетрагидрофуране (1,2 л). Спустя 1 час охлаждающую баню удалили и реакцию оставляли стоять при комнатной температуре в течение ночи. После этого реакционную смесь нагревали с обратным холодильником в течение 30 минут, вылили в воду со льдом, и продукт экстрагировали в этилацетат. Экстракт фильтровали для удаления нерастворимых веществ, промыли водой, сушили над сульфатом натрия и выпаривали с получением масла, которое при растирании с горячим н-гексаном привело к продукту в виде кристаллов (68,0 г). т.пл. 243oC.
Получение гидрохлоридной соли 4-[бис-(4-фторфенил)-метилен]-пиперидина
α,α-Бис-(4-фторфенил)-1-(трифенилметил)-4-пиперидинметанол (67 г, 0,123 моля) растворили в соляной кислоте (1 л, 2 моль/л), и раствор нагревали с обратным холодильником в течение 2 часов. Раствор охладили, выпавшее в осадок твердое вещество собирали фильтрованием и суспендировали в безводном диэтиловом эфире. Смесь перемешивали в течение 1 часа, фильтровали, и твердое вещество кристаллизовали из метанола/эфира с получением продукта (28,3 г) в виде белых кристаллов, т.пл. 83oC.
Получение гидрохлоридной соли 1-[4-[4-бис-(фторфенил)метилен]-1-пиперидинил-1-оксобутил]-пирролидина
Раствор 4-хлорбутирилхлорида (0,68 мл, 6,07 ммоль) в безводном дихлорметане (10 мл) по каплям добавляли к охлажденному льдом и перемешиваемому раствору пирролидина (0,57 мл, 6,83 ммоль) и триэтиламина (1 мл) в безводном дихлорметане (10 мл). Спустя 1 час добавляли воду и дихлорметановый раствор разделили, промыли водой, сушили над сульфатом натрия и выпаривали досуха с получением 1-(4-хлор-1-оксобутил)-пирролидина, который вместе с гидрохлоридом 4-[бис-(4-фторфенил)-метилен] -пиперидина (2,0 г, 6,2 ммоль) и карбонатом калия (2,15 г, 15,55 ммоль) растворили в диметилформамиде, и смесь нагревали при 100oC в течение 2 часов. Раствор вылили в воду, и продукт экстрагировали диэтиловым эфиром. Органический экстракт промыли водой, сушили над сульфатом натрия и выпаривали досуха с получением 1-[4-[4-[бис-(4-фторфенил)метилен] -1-пиперидинил-1-оксоубутил] -пирролидина в виде оранжево-желтой смолы (2,33 г). Этот продукт растворили в метаноле, добавили щавелевую кислоту (0,73 г), и раствор оставили кристаллизоваться с получением этандиоатной соли 1-[4-[4-[бис-(4-фторфенил)метилен] -1-пиперидинил]-1-оксобутил] -пирролидина. Этот материал кристаллизовали из метанола/эфира с получением материала (0,85 г), который был повторно превращен в свободное основание, и его хроматографировали на диоксиде кремния. Элюирование дихлорметаном/метанолом привело к чистому материалу, который растворяли в эфире и обрабатывали газообразным хлористым водородом. Осадок кристаллизовали из метанола/эфира с получением гидрохлоридной соли 1-[4-[4-[бис-(4-фторфенил)метилен]-1-пиперидинил-1-оксобутил]-пирролидина (0,40 г); т.пл. 107oC.
Аналогичным образом, очищенное свободное основание растворили в эфире/метаноле (55/3, об/об), и перемешиваемый раствор обрабатывали раствором метансульфоновой кислоты (1,05 моль-эквив.) в эфире. Продукт осаждался в виде смолы, которая кристаллизовалась при перемешивании. После добавления дополнительного количества эфира твердое вещество отфильтровывали и сушили с получением метансульфонатной соли 1-[4-[4-[бис-(4-фторфенил)-метилен]-1-пиперидинил-1-оксобутил]-пирролидина; т.пл. 157-158oC.
Пример 2
Получение (E)-2-бутандиоатной (1: 1) соли 1-[4-[4-[бис-(4-фторфенил)метилен]-1-пиперидинил-1-оксобутил]пиперидина
4-Хлорбутирилхлорид в дихлорметане добавляли к охлажденному льдом раствору пиперидина (1,8 мл, 17,6 ммоль) и триэтиламина (2,5 мл) в дихлорметане (40 мл) в атмосфере азота. Смесь перемешивали в течение 5 минут до ее охлаждения, а затем перемешивали при температуре окружающей среды в течение 3 часов. Раствор промыли водой, сушили над сульфатом натрия и выпаривали с получением 1-(4-хлор-1-оксобутил)пиперидина в виде бледно-желтого масла (2,1 г). Смесь гидрохлорида 4-[бис(4-фторфенил)метилен] пиперидина (3,5 г, 11 ммоль), полученного так, как описано в предыдущем примере, вышеупомянутого 1-(4-хлор-1-оксобутил)-пиперидина (2,1 г, 11 ммоль) и карбоната калия (3,3 г, 24 ммоль) в диметилформамиде (40 мл) нагревали при 80oC в течение 6 часов, и реакционную смесь вылили в воду. Продукт экстрагировали эфиром и экстракт промыли водой, сушили над сульфатом натрия и выпаривали с получением смолы, которую хроматографировали на диоксиде кремния. Элюирование дихлорметаном/метанолом/аммиаком привело к продукту в виде свободного основания, которое растворили в этилацетате и добавили раствор фумаровой кислоты (0,25 г) в метаноле. Раствор оставили стоять при 5oC до тех пор, пока не произошла кристаллизация, образовавшиеся кристаллы собрали с получением продукта (0,88 г), т.пл. 145oC.
Пример 3
Испытание на лазанье при воздействии апоморфина на мышах
Мыши, обработанные апоморфином HCl, стремятся принять вертикальное положение вдоль стенки цилиндра из проволочной сетки, стоя или лазая. Предполагают, что поведение с лазаньем получается путем опосредованного апоморфином стимулирования рецепторов допамина. На поведение с лазаньем влияют многие лекарства, однако обычно антагонисты допамина подавляют его в дозах, которые не мешают спонтанной двигательной активности и/или двигательной координации у мышей. Испытываемые соединения, которые модулируют это поведение с лазаньем, могут обладать антипсихотической активностью.
Различные обработки случайным образом распределены среди мышей. Каждый эксперимент состоит из 1+n групп обработки:
1 является контрольной группой из 12 мышей, принимающих подкожно апоморфин и среду, или же контрольной группой из 12 мышей, принимающих подкожно апоморфин и перорально - среду; n (обычно 4) являются группами из 12 мышей, принимающих подкожно апоморфин и испытываемое соединение, или же группами из 12 мышей, принимающих подкожно апоморфин и перорально - испытываемое соединение.
Эксперименты проводятся в 3 серии, по 20 мышей в каждом.
Мышей помечают и взвешивают, подкожно вводят испытываемое соединение или среду, и мышей помещают в небольшие клетки Macrolon размером 17х11х13 см, по 5 мышей в клетку; или же испытываемое соединение или среду вводят перорально и мышей помещают в клетки Macrolon размером 29х11х13 см, по 5 мышей в клетку. Спустя 30 минут мышам, обработанным подкожно средой или испытываемым соединением, вводят 0,75 мг/кг апоморфина HCl или же 0,75 мг/кг апоморфина HCl вводят подкожно мышам, обработанным перорально средой или испытываемым соединением, и мышей помещают индивидуально в цилиндр из проволочной сетки (диаметр 12 см, высота 14 см). Спустя 10 минут после обработки апоморфином наблюдают за поведением с лазаньем для каждой мыши и выражают его в баллах в соответствии со следующей градацией:
4 лапы на полу - балл 0
1 или 2 лапы держатся за стену - балл 1
3 или 4 лапы держатся за стенку - балл 2
Спустя 20 минут после обработки апоморфином наблюдают за поведением с лазаньем и снова выражают его в баллах.
Для каждой группы обработки определяют средний балл на мышь. Балл контрольной группы должен быть по меньшей мере 1,0, а если это не так, то испытание отбрасывают. Конечный результат на группу выражают в процентах в сравнении с контрольной группой.
Результаты данного испытания для настоящих испытываемых соединений приведены в таблице 1 (подкожное введение испытываемого соединения) и в таблице 2 (пероральное введение испытываемого соединения).
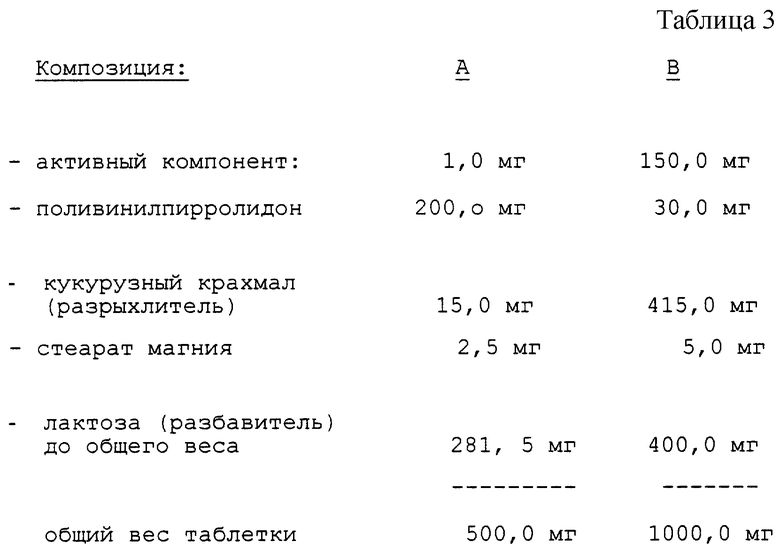
Примеры композиций в форме таблеток, содержащих в качестве активного компонента соединение примера 1 - метансульфонатную соль 1-[4-[4-[бис-(4-фторфенил)метилен-1-пиперидинил] -1-оксобутил]-пирролидина, обозначенное как Org 23366, приведены в табл. 3.
Для определения максимально переносимой дозы (МПД) соединение Org 23366 перорально вводили поросятам в возрастающих дозах 3, 10 и 30 мг/кг/день. При этом не наблюдалось никаких, вызванных введением лекарства макро- или микроскопических изменений органов и тканей. Только у животного, получившего дозу 30 мг/кг/день, отмечалась тахикардия, продолжавшаяся менее 6 часов, без гистопатологических изменений сердечно-сосудистой системы. МПД перероральная доза для поросят была оценена, приблизительно, как 20 мг/кг/день.
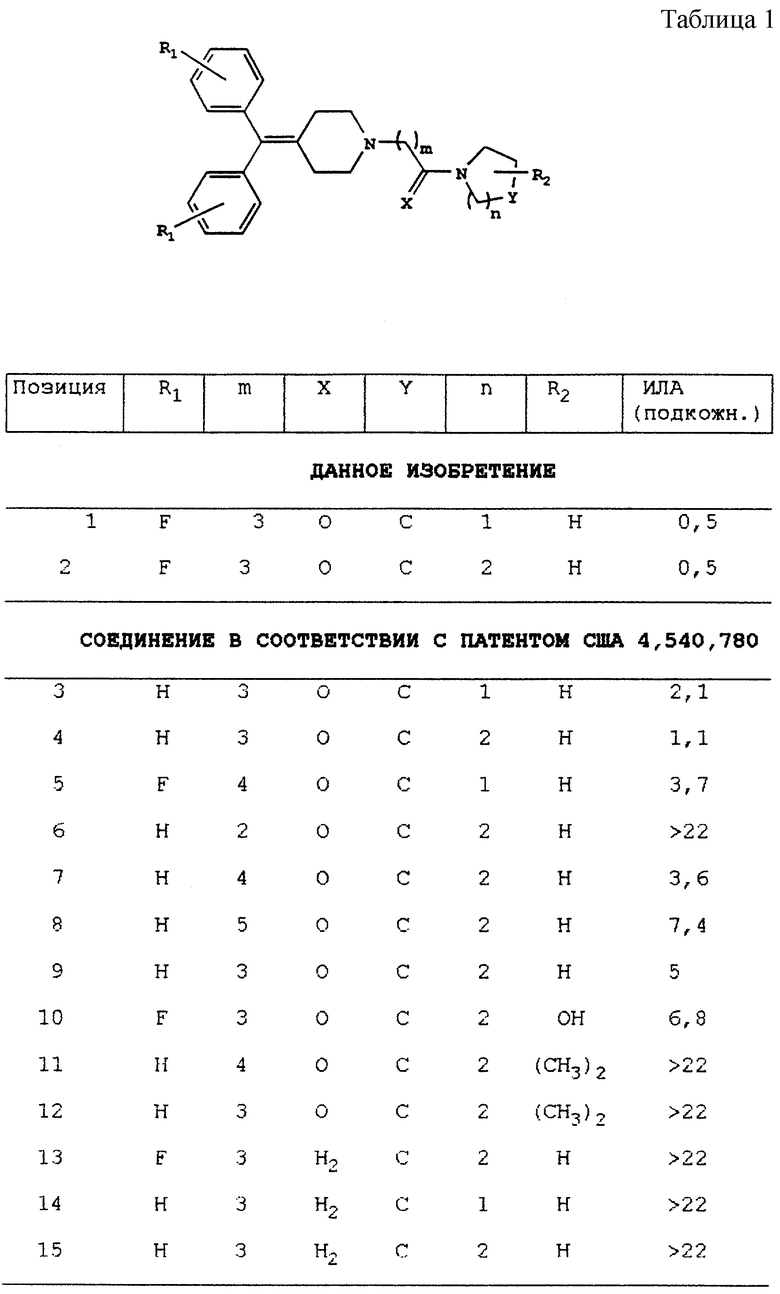
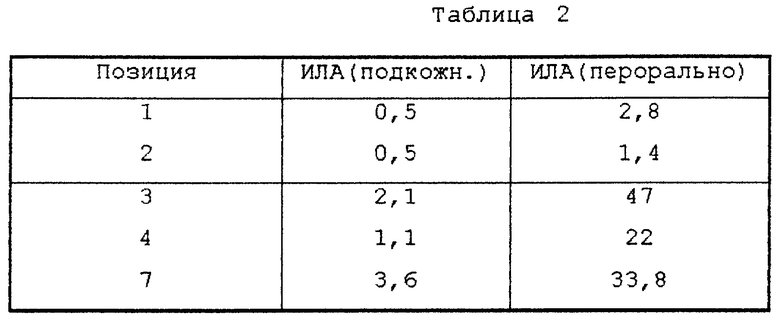
Изобретение относится к производным дифенилметиленпиперидина формулы I, где n равно 1 или 2, или их фармацевтически приемлемым солям. Соединения формулы I и их соли являются антагонистами рецептора допамина, обладают сильной антипсихотической активностью и могут найти применение в медицине. 3 с. и 3 з.п.ф-лы, 3 табл.
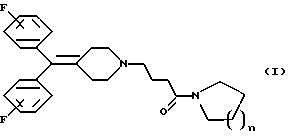
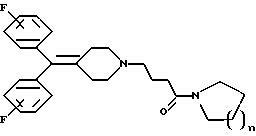
где n равно 1 или 2,
или их фармацевтически приемлемые соли.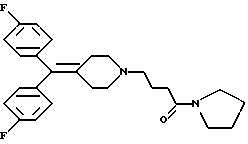
или его фармацевтически приемлемая соль.
| US 4666905 A, 19.05.1987 | |||
| US 4540780 A, 10.09.1985 | |||
| US 4180583 A, 25.12.1979 | |||
| Способ получения пиперазинилгетероциклических соединений или их фармацевтически приемлемых кислотно-аддитивных солей | 1988 |
|
SU1644716A3 |
Авторы
Даты
2001-02-10—Публикация
1996-07-09—Подача