Изобретение относится к новому полипептидному соединению и его фармацевтически приемлемой соли, которые могут быть использованы в качестве лекарственного средства.
В патенте США N 5376634 раскрывается полипептидное соединение и его фармацевтически приемлемая соль, которые обладают противомикробной активностью (в частности, противогрибковой активностью).
Настоящее изобретение относится к новому полипептидному соединению и его фармацевтически приемлемой соли.
Более конкретно, настоящее изобретение относится к новому полипептидному соединению и его фармацевтически приемлемой соли, которые обладают противомикробной активностью (в частности, противогрибковой активностью, направленной против таких грибков, как Aspergillus, Cryptococcus, Candida, Mucor, Actinomyces, Histoplasma, Dermatophyte, Malassezia, Fusarium и т.п.), активностью, ингибирующей β-1,3-глюкансинтазу, и которые, как предполагается, могут быть использованы для профилактики и/или терапевтического лечения инфекций, вызываемых Pneumocysitis carinii (например, пневмонии, вызываемой Pneumocystis carinii), у человека или животных; и кроме того, настоящее изобретение относится к способу получения указанного соединения, к фармацевтической композиции, содержащей это соединение, и к способу предупреждения и/или терапевтического лечения инфекционных заболеваний, включая инфекции Pneumocystis carinii (например, пневмония, вызываемая Pneumocystis carinii), у человека или животных. Целевое полипептидное соединение, используемое в настоящем изобретении является новым и может быть представлено следующей общей формулой (I)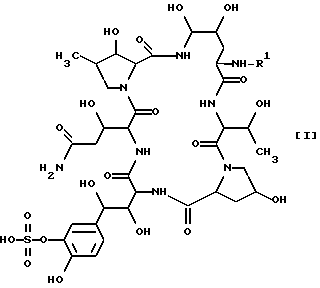
где R1 - обозначает низший алканоил, замещенный ненасыщенной 6-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей;
низший алканоил, замещенный 1,2,3,4-тетрагидроизохинолином, который может иметь один или несколько подходящих заместителей;
низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей по крайней мере один атом кислорода, которая может иметь один или несколько подходящих заместителей;
низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 1-3 атома серы, которая может иметь один или несколько подходящих заместителей;
низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 2 или более атомов азота, которая может иметь один или несколько подходящих заместителей;
низший алканоил, замещенный насыщенной 3-8-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей;
ар(низший)алкеноил, замещенный арилом, который может иметь один или несколько подходящих заместителей;
нафтил(низший)алкеноил, который может иметь один или несколько высших алкокси;
низший алкиноил, который может иметь один или несколько подходящих заместителей;
(C2-C6)алканоил, замещенный нафтилом, имеющим высший алкокси;
ар(C2-C6)алканоил, замещенный арилом, имеющим один или несколько подходящих заместителей, где ар(C2-C6)алканоил может иметь один или несколько подходящих заместителей;
ароил, замещенный гетероциклической группой, которая может иметь один или несколько подходящих заместителей, где указанный ароил может иметь один или несколько подходящих заместителей;
ароил, замещенный арилом, имеющим гетероциклил(высший)алкокси, где гетероциклическая группа может иметь один или несколько подходящих заместителей;
ароил, замещенный арилом, имеющим низший алкокси(высший)алкокси;
ароил, замещенный арилом, имеющим низший алкенил(низший)алкокси;
ароил, замещенный 2 низшими алкокси;
ароил, замещенный арилом, имеющим низший алкил;
ароил, замещенный арилом, имеющим высший алкил;
арилокси(низший)алканоил, который может иметь один или несколько подходящих заместителей;
ар(низший)алкокси(низший)алканоил, который может иметь один или несколько подходящих заместителей;
ариламино(низший)алканоил, который может иметь один или несколько подходящих заместителей;
низший алканоил, замещенный пиразолилом, который имеет низший алкил и арил, имеющий высший алкокси;
низший алкокси(высший)алканоил, где высший алканоил может иметь один или несколько подходящих заместителей;
ароил, замещенный арилом, имеющим гетероциклилокси, где гетероциклилокси может иметь один или несколько подходящих заместителей;
ароил, замещенный цикло(низшим)алкилом, имеющим низший алкил;
индолилкарбонил, имеющий высший алкил;
нафтоил, имеющий низший алкил;
нафтоил, имеющий высший алкил;
нафтоил, имеющий низший алкокси(высший)алкокси;
ароил, замещенный арилом, имеющим низший алкокси(низший)алкокси(высший)алкокси;
ароил, замещенный арилом, имеющим низший алкокси(низший)алкокси;
ароил, замещенный арилом, который имеет арил, содержащий низший алкокси;
ароил, замещенный арилом, который имеет арил, содержащий низший алкокси(низший)алкокси;
ароил, замещенный арилом, имеющим гетероциклилокси(высший)алкокси;
ароил, замещенный, арилом, имеющим арилокси(низший)алкокси;
ароил, замещенный арилом, имеющим гетероциклилкарбонил(высший)алкокси;
низший алканоил, замещенный оксазолилом, который имеет арил, содержащий высший алкокси;
низший алканоил, замещенный фурилом, который имеет арил, замещенный арилом, содержащим низший алкокси;
низший алканоил, замещенный триазолилом, который имеет оксо и арил, содержащий высший алкил;
высший алканоил, имеющий гидрокси;
высший алканоил, имеющий ар(низший)алкил и гидрокси;
3-метил-тридеценоил; или
(C2-C6)алканоил, замещенный арилом, содержащим высший алкокси, где (C2-C6)алканоил может иметь амино или защищенную амино.
Новое полипептидное соединение (I) и его фармацевтически приемлемая соль могут быть получены способом, проиллюстрированным в реакционной схеме (Способ 1), представленной в конце описания, либо они могут быть получены с помощью реакции элиминирования аминозащитной группы в R1, где R1 определен выше.
Подходящими фармацевтически приемлемыми солями целевого полипептидного соединения (I) являются обычные нетоксичные соли, которые могут представлять собой соль с основанием или кислотную соль присоединения, такую как соль с неорганическим основанием, например соль щелочного металла (например, натриевая соль, калиевая соль и т. п. ), соль щелочно-земельного металла (например, кальциевая соль, магниевая соль и т.п.); соль аммония; соль с органическим основанием, например соль органического амина (например, триэтиламиновая соль, пиридиновая соль, пиколиновая соль, этаноламиновая соль, триэтаноламиновая соль, дициклогексиламиновая соль, N,N'-дибензил-этилендиаминовая соль и т.п.); соль присоединения неорганической кислоты (например, гидрохлорид, гидробромид, сульфат, фосфат и т.п.); соль присоединения органической карбоновой сульфоновой кислоты (например, формат, ацетат, трифторацетат, малеат, тартрат, фумарат, метансульфонат, бензолсульфонат, толуолсульфонат и т. п. ); соль с основной или кислотной аминокислотой (например, такой как аргинин, аспарагиновая кислота, глутаминовая кислота и т.п.).
Ниже приводится подробное объяснение и подходящие иллюстративные примеры различных определений, имеющихся в настоящем описании и входящих в объем настоящего изобретения.
Если это не оговорено особо, то термин "низший" относится к группе, имеющей 1-6 атомов углерода.
Если это не оговорено особо, то термин "высший" относится к группе, имеющей 7-20 атомов углерода.
При указании числа "один или более" подходящим примером может служить число 1-6, а предпочтительно 1-3.
Подходящим примером "низшего алканоила" может служить прямой или разветвленный низший алканоил, такой как формил, ацетил, 2-метилацетил, 2,2-диметилацетил, пропионил, бутирил, изобутирил, пентаноил, 2,2-диметилпропионил, гексаноил, и т.п.
Примером "подходящего заместителя (подходящих заместителей)" в таких группах, как "низший алканоил, замещенный ненасыщенной 6-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота,
которая может иметь один или несколько подходящих заместителей", "низший алканоил, замещенный 1,2,3,4- тетрагидроизохинолином, который может иметь один или несколько подходящих заместителей" и т.п., может служить низший алкокси, упомянутый ниже; высший алкокси, упомянутый ниже; низший алкил, упомянутый ниже; высший алкил, упомянутый ниже; высший алкокси(низший)алкил; низший алкоксикарбонил; оксо; арил, который может иметь один или несколько низших алкокси; арил, который может иметь один или несколько высших алкокси; арил, который может иметь один или несколько низших алкилов; арил, который может иметь один или несколько высших алкилов; арил, замещенный арилом, который может иметь один или несколько низших алкокси; арил, замещенный арилом, который может иметь один или несколько высших алкокси; арил, замещенный арилом, который может иметь один или несколько низших алкилов; арил, замещенный арилом, который может иметь один или несколько высших алкилов; ароил, который может иметь один или несколько низших алкокси; ароил, который может иметь один или несколько высших алкокси;
ароил, который может иметь один или несколько низших алкилов; ароил, который может иметь один или несколько высших алкилов; гетероциклическая группа, которая может иметь один или несколько низших алкокси; гетероциклическая группа, которая может иметь один или несколько высших алкокси; арил, имеющий гетероциклил(высший)алкокси; гетероциклическая группа, которая может иметь арил, содержащий высший алкокси; гетероциклическая группа, которая может иметь арил, содержащий низший алкокси(высший)алкокси; гетероциклическая группа, которая может иметь арил, содержащий низший алкокси; низший алкокси(низший)алкил, галоген(низший)алкокси; низший алкенилокси; галоген(высший)алкокси; низший алкокси(высший)алкокси; арил, который может иметь один или несколько низших алкокси(низший)алкокси; гетероциклическая группа; арил, который может иметь один или несколько низших алкокси(высший)алкокси; арил, который может иметь один или несколько высших алкенилокси; цикло(низший)алкил, который может иметь арил; арил, замещенный гетероциклической группой, которая может иметь низший алкил и оксо; цикло(низший)алкил, который может иметь один или несколько низших алкилов; арил, который может иметь цикло(низший)алкил; арил, который может иметь гетероциклическую группу; и т.п.
Подходящим примером "низшего алкокси" может служить прямой или разветвленный низший алкокси, такой как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, трет-бутокси, пентилокси, трет-пентилокси, нео-пентилокси, гексилокси, изогексилокси, и т.п.; при этом предпочтительными могут быть метокси, этокси, пропокси, бутокси, пентилокси, гексилокси и изогексилокси.
Подходящим примером "высшего алкокси" может служить прямой или разветвленный высший алкокси, такой как гептилокси, октилокси, 3,5-диметилоктилокси, 3,7-диметилоктилокси, нонилокси, децилокси, ундецилокси, додецилокси, тридецилокси, тетрадецилокси, гексадецилокси, гептадецилокси, октадецилокси, нонадецилокси, икозилокси и т.п., при этом предпочтительными могут быть (C7-C14)алкокси, а более предпочтительными гептилокси и октилокси.
Подходящим примером "низшего алкила" может служить прямой или разветвленный низший алкил, имеющий 1-6 атомов углерода, такой как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, трет-пентил, нео-пентил, гексил, изогексил и т.п., при этом предпочтительными могут быть метил, пентил, гексил и изогексил.
Подходящим примером "высшего алкила" может служить прямой или разветвленный алкил, имеющий 7-20 атомов углерода, такой как гептил, октил, 3,5-диметилоктил, 3,7-диметилоктил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, нонадецил, икозил и т.п., при этом предпочтительным высшим алкилом может быть (C7-C14)алкил, а более предпочтительным высшим алкилом может быть гептил, октил, нонил и децил.
Подходящим примером "арила" или радикала "ар" может служить фенил, который может иметь низший алкил (например, фенил, мезитил, толил и т.п.), нафтил, антрил и т.п., при этом предпочтительными могут быть фенил и нафтил.
Подходящим примером "ароила" может служить бензоил, толуолил, нафтоил, антрилкарбонил и т.п., при этом предпочтительными являются бензоил и нафтоил.
Подходящим примером "гетероциклической группы" и "гетероциклической" части может служить:
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-4 атома азота, например пирролил, пирролинил, имидазолил, пиразолил, пиридил, дигидропиридил, пиримидил, пиразинил, пиридазинил, триазолил (например, 4H-1,2,4-триазолил, 1H-1,2,3-триазолил, 2H-1,2,3-триазолил и т. п. ), тетразолил (например, 1H-тетразолил, 2H-тетразолил и т.п.), и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-4 атома азота, например пирролидинил, имидазолидинил, пиперидил, пиперазинил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-4 атома азота, например индолил, изоиндолил, индолинил, индолизинил, бензимидазолил, хинолил, изохинолил, индазолил, бензотриазолил и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота, например оксазолил, изоксазолил, оксадиазолил (например, 1,2,4-оксадиазолил; 1,3,4-оксадиазолил; 1,2,5-оксадиазолил и т.п.) и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота, например морфолинил, сиднонил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота, например бензоксазолил, бензоксадиазолил и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома серы и 1-3 атома азота, например тиазолил, изотиазолил, тиадиазолил (например, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,3,4-тиадиазолил, 1,2,5-тиадиазолил и т.п.) и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома серы и 1-3 атома азота, например тиазолидинил и т.п.
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома серы, например тиенил, дигидродитиинил, дегидродитионил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-2 атома серы и 1-3 атома азота, например бензотиазолил, бензотиадиазолил и т. п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая атом кислорода, например, такая как фурил и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая атом кислорода, например тетрагидрофуран, тетрагидропиран и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5 или 6-членная) гетеромоноциклическая группа, содержащая атом кислорода и 1-2 атома серы, например дигидрооксатиинил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-2 атома серы, например бензотиенил, бензодитиинил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая атом кислорода и 1-2 атома серы, например бензоксатиинил и т.п., и т.п.
Подходящим примером "галогена" может служить фтор, хлор, бром и йод.
Подходящим примером "низшего алкенилокси" может служить винилокси, 1- (или 2-) пропенилокси, 1- (или 2-, или 3-) бутенилокси, 1- (или 2-, или 3-, или 4-) пентенилокси, 1-(или 2-, или 3-, или 4-, или 5-) гексенилокси и т.п. , при этом предпочтительным может быть (С2-С6)алкенилокси, а наиболее предпочтительным 5-гексенилокси.
Подходящим примером "высшего алкенилокси" может служить (С7-С20)алкенилокси, при этом предпочтительным может быть 6-гептенилокси и 7-октенилокси.
Подходящим примером "цикло(низший)алкила" может служить циклопропил, циклобутил, циклопентил, циклогексил и т.п., при этом предпочтительным может быть цикло(С4-С6)алкил, а наиболее предпочтительным может быть циклогексил.
Подходящим примером "высшего алканоила" может служить гептаноил, октаноил, нонаноил, деканоил, удеканоил, лауроил, тридеканоил, тетрадеканоил, пентадеканоил, гексадеканоил, гептадеканоил, октадеканоил, нонадеканоил, икозаноил и т.п., при этом предпочтительным может быть (С7-С20)алканоил, а наиболее предпочтительным может быть гексадеканоил.
Подходящим примером "ар(низший)алкила" может служить бензил, фенетил, фенилпропил, фенилбутил, фенилпентил, фенилгексил, нафтилметил, нафтилэтил, нафтилпропил, нафтилбутил, нафтилпентил, нафтилгексил и т.п., при этом предпочтительным может быть фенил(C1-C4)алкил, а наиболее предпочтительным может быть бензил.
Подходящим примером "защищенной амино" может служить низший или высший алкоксикарбониламино (например, метоксикарбониламино, этоксикарбониламино, т-бутоксикарбониламино, т-пентилоксикарбониламино, гептилоксикарбониламино и т.п.), ар(низший)алкоксикарбониламино [например, фенил(низший)алкоксикарбониламино (например, бензилоксикарбониламино и др.) и т. п. ] , аминогруппа, замещенная стандартной защитной группой, такой как ар(низший)алкил, который может иметь подходящего(их) заместителя(ей) (например, бензил, тритил и т.п.) и т.п., при этом предпочтительной аминогруппой может быть фенил(низший)алкоксикарбониламино, а наиболее предпочтительной может быть бензилоксикарбониламино.
Подходящим примером "низшего алканоила", указанного в термине "низший алканоил, замещенный ненасыщенной 6-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько заместителей" могут быть примеры, упомянутые выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а более предпочтительным формил.
Подходящим примером "ненасыщенной 6-членной гетеромоноциклической группы, содержащей по крайней мере один атом азота" в термине "низший алканоил, замещенный ненасыщенной 6-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей" может служить пиридил, дигидропиридил, пиримидил, пиразинил, пиридазинил, триазинил (например, 4H-1,2,4-триазинил, 1H-1,2,3-триазинил и т. п.), тетразинил (например, 1,2,4,5-тетразинил, 1,2,3,4-тетразинил и т. п.) и т.п., при этом предпочтительной может быть ненасыщенная 6-членная гетеромоноциклическая группа, содержащая 1-3 атома азота, а наиболее предпочтительной пиридил и пиридазинил.
Примером "подходящих заместителей, упомянутых в термине "низший алканоил, замещенный ненасыщенной 6-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "подходящих заместителей", при этом предпочтительными могут быть высший алкокси; высший алкокси(низший)алкил; гетероциклическая группа, которая может иметь арил, имеющий высший алкокси; арил, который может иметь один или более высших алкокси; арил, замещенный арилом, который может иметь низший алкокси; гетероциклическая группа, которая может иметь арил, содержащий низший алкокси(высший)алкокси; и гетероциклическая группа, которая может иметь арил, имеющий низший алкокси; более предпочтительными могут быть (C7-C14)алкокси(C7-C14)алкокси, (C1-C4)алкил; 3-8-членная насыщенная гетеромоноциклическая группа, содержащая по крайней мере один атом азота, которая может иметь фенил, имеющий 1-3 (C7-C14)алкокси; фенил, который может иметь 1-3 (C7-C14)алкокси; фенил, замещенный фенилом, который может иметь 1-3 (C3-C6)алкокси; 3-8-членная насыщенная гетеромоноциклическая группа, содержащая по крайней мере один атом азота, которая может иметь фенил, имеющий (C1-C4)алкокси(C1-C14)алкокси; и 3-8-членная насыщенная гетеромоноциклическая группа, содержащая по крайней мере один атом азота, которая может иметь фенил, содержащий 1-3 (C3-C6)алкокси, и наиболее предпочтительными могут быть октилокси, октилоксиметил, пиперазинил, который имеет фенил, содержащий гептилокси или октилокси; фенил, имеющий гептилокси; фенил, замещенный фенилом, имеющим бутокси; пиперазинил, который содержит фенил, имеющий метоксиоктилокси; и пиперазинил, который содержит фенил, имеющий гексилокси.
Подходящим примером "низшего алканоила" в группе, обозначенной термином "низший алканоил, замещенный 1,2,3,4-тетрагидроизохинолином, который может иметь один или несколько подходящих заместителей" могут быть примеры, упомянутые выше для "низшего алканоила", при этом предпочтительным может быть (С1-С4)алканоил, а более предпочтительным может быть формил.
Примером "подходящих заместителей" в группе, обозначенной термином "низший алканоил, замещенный 1,2,3,4-тетрагидроизохинолином, который может иметь один или несколько подходящих заместителей", при этом предпочтительными могут быть низший алкокси, высший алкокси, низший алкил, высший алкил и низший алкоксикарбонил; более предпочтительными могут быть (C7-C14)алкокси и (C1-C4)алкоксикарбонил, а наиболее предпочтительными могут быть октилокси и трет-бутоксикарбонил.
Подходящим примером "низшего алканоила", обозначенного термином "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей по крайней мере атом кислорода, которая может иметь один или несколько подходящих заместителей" могут служить примеры, упомянутые выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а более предпочтительным формил.
Подходящим примером "ненасыщенной конденсированной гетероциклической группы, содержащей по крайней мере один атом кислорода" в термине "низший алканоил, замещенный ненасыщенной конденсированной группой, содержащей по крайней мере один атом кислорода, которая может иметь один или несколько подходящих заместителей", может служить ненасыщенная конденсированная гетероциклическая группа, содержащая один или несколько атомов кислорода, и необязательно, другой гетероатом (гетероатомы), кроме атома кислорода, при этом предпочтительными могут быть ненасыщенная конденсированная гетероциклическая группа, содержащая 1-3 атомов кислорода; ненасыщенная конденсированная гетероциклическая группа, содержащая 1-2 атома кислорода и 1-2 атома серы; и ненасыщенная конденсированная гетероциклическая группа, содержащая 1-3 атома кислорода и 1-3 атома азота; более предпочтительными могут быть бензо[b] фуранил, изобензофуранил, хроменил, ксантенил, бензоксазолил, бензоксадиазолил, дигидрооксатиинил, феноксатиинил и т.п.; а наиболее предпочтительными могут быть бензо[b]фуранил, хроменил и бензоксазолил.
Примером "подходящих заместителей" в группе, обозначенной термином "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей по крайней мере один атом кислорода, которая может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "подходящих заместителей", при этом предпочтительными могут быть низший алкокси, высший алкокси, низший алкил, высший алкил, оксо, арил, который может иметь один или несколько низших алкокси, гетероциклическая группа, которая может иметь один или несколько высших алкокси, и арил, замещенный арилом, который может иметь один или несколько низших алкилов; более предпочтительными могут быть (C7-C14)алкокси, (C7-C14)алкил, (C7-C14)алкил, оксо, фенил, который может иметь 1-3 (C3-C6)алкокси, ненасыщенная 6-членная гетеромоноциклическая группа, содержащая по крайней мере один атом азота, которая может иметь 1-3 (C7-C14)алкокси, и фенил, замещенный фенилом, который может иметь 1-3 (C3-C6)алкилов; а наиболее предпочтительными могут быть октилокси, метил, нонил, оксо, фенил, имеющий гексилокси, пиридил, имеющий октилокси, и фенил, замещенный фенилом, имеющим гексил.
Подходящим примером "низшего алканоила" в термине "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 1-3 атома серы, которая может иметь один или несколько заместителей" могут служить примеры, упомянутые выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а более предпочтительным формил.
Подходящим примером "ненасыщенной конденсированной гетероциклической группы, содержащей 1-3 атома серы" в термине "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 1-3 атома серы, которая может иметь один или несколько подходящих заместителей" может служить ненасыщенная конденсированная гетероциклическая группа, содержащая только 1-3 атома серы, предпочтительно такая, как бензотиенил и бензодитиинил, а наиболее предпочтительно бензотиенил.
Подходящим примером "подходящих заместителей" в термине "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 1-3 атома серы, которая может иметь один или несколько подходящих заместителей" могут служить примеры, упомянутые выше для "подходящих заместителей", при этом предпочтительными могут быть низший алкокси, высший алкокси, низший алкил и высший алкил, более предпочтительным может быть (C7-C14)алкокси, а наиболее предпочтительным октилокси.
Подходящим примером "низшего алканоила" в термине "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 2 или более атомов азота, которая может иметь один или несколько подходящих заместителей" могут служить примеры, упомянутые выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а наиболее предпочтительным формил.
Подходящим примером "ненасыщенной конденсированной гетероциклической группы, содержащей 2 или более атомов азота" в термине "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 2 или более атомов азота, которая может иметь один или несколько подходящих заместителей" может служить 1H-индазолил, пуринил, фталазинил, бензоимидазолил, нафтиридинил, хиноксалинил, хиназолил, циннолинил, петеридинил и т.п., при этом наиболее предпочтительным является бензоимидазолил.
Подходящим примером "подходящих заместителей" в термине "низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей 2 или более атомов азота, которая может иметь один или несколько подходящих заместителей" могут служить примеры, упомянутые выше для "подходящих заместителей", при этом предпочтительными могут быть низший алкокси, высший алкокси, низший алкил, высший алкил, арил, который может иметь один или несколько низших алкокси, и арил, который может иметь один или несколько высших алкокси; более предпочтительными могут быть (C7-C14)алкил и фенил, который может иметь 1-3 (C1-C6)алкокси; а наиболее предпочтительными могут быть нонил и фенил, который может иметь гексилокси.
Подходящим примером "низшего алканоила" в термине "низший алканоил, замещенный насыщенной 3-8-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей" могут служить примеры, указанные выше для "низшего алканоила", при этом предпочтительным может быть (С1-С4)алканоил, а более предпочтительным может быть формил.
Подходящим примером "насыщенной 3-8-членной гетеромоноциклической группы, содержащей по крайней мере один атом азота" в термине "низший алканоил, замещенный насыщенной 3-8-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей" могут служить пирролидинил, имидазолидинил, пиперидил, пиперазинил, пиразолидинил, морфолинил, тиоморфолинил и т.п., при этом предпочтительными могут быть пиперидил и пиперазинил.
Примером "подходящих заместителей" в термине "низший алканоил, замещенный насыщенной 3-8-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей" могут служить низший алкокси, высший алкокси, высший алкокси(низший)алкил, низший алкил, высший алкил, оксо, арил, который может иметь один или несколько низших алкокси; арил, который может иметь один или несколько высших алкокси; арил, который может иметь один или несколько низших алкилов, арил, который может иметь один или несколько высших алкилов; ароил, который может иметь один или несколько низших алкокси; ароил, который может иметь один или несколько высших алкокси; ароил, который может иметь один или несколько низших алкилов; ароил, который может иметь один или несколько высших алкилов, и т. п., при этом предпочтительными могут быть арил, который может иметь один или несколько низших алкокси; арил, который может иметь один или несколько высших алкокси; ароил, который может иметь один или несколько низших алкокси; ароил, который может иметь один или несколько высших алкокси; более предпочтительными могут быть арил, который может иметь 1-3 высших алкокси, и ароил, который может иметь 1-3 высших алкокси; еще более предпочтительными могут быть фенил, который может иметь 1-3 (С7-С14)алкокси и нафтоил, который может иметь 1-3 (С7-С14)алкокси; а наиболее предпочтительными могут быть фенил, который может иметь октилокси, и нафтоил, который может иметь гептилокси.
Подходящим примером "ар(низший)алкеноила" в термине "ар(низший)алкеноил, замещенный арилом, который может иметь один или несколько подходящих заместителей" могут служить фенил(низший)алкеноил (например, 3-фенилакрилоил, (2-, или 3-, или 4-) фенил-(2- или 3-) бутеноил, 3-фенилметакрилоил, (2-, или 3-, или 4-, или 5-) фенил-(2-, или 3-, или 4-)пентаноил, (2-, или 3-, или 4-, или 5-, или 6-) фенил-(2-, или 3-, или 4-, или 5-) -гексаноил и т.п. ), нафтил(низший)алкеноил (например, 3-нафтилакрилоил, (2-, или 3-, или 4-) нафтил- (2- или 3-) бутеноил, (2-, или 3-, или 4-, или 5-) нафтил-(2-, или 3-, или 4- ) пентаноил, (2-, или 3-, или 4-, или 5-, или 6-) нафтил- (2-, или 3-, или 4-, или 5-) гексаноил, и т.п.) и т.п., при этом предпочтительными могут быть 3-фенилакрилоил и 3-метил-3-фенилакрилоил.
Примером "подходящих заместителей" в термине "ар(низший)алкеноил, замещенный арилом, который может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "подходящих заместителей", при этом предпочтительными могут быть низший алкокси, низший алкил, высший алкил, низший алкокси(низший) алкил, галоген(низший) алкокси, низший алкенилокси, галоген(высший) алкокси, и низший алкокси(высший) алкокси, более предпочтительными могут быть (С1-С6)алкокси, (С1-С6)алкил, (С7-С17)алкил, (С1-С4)алкокси(С3-С6)алкил, галоген(С3-С6)алкокси, (С3-С6)алкенилокси,
галоген(С7-С14)алкокси и (С1-С4)алкокси(С7-С14)алкокси, а наиболее предпочтительными могут быть пентилокси, гептил, пентил, метоксигексил, фторгексилокси, изогексилокси, 5-гексенилокси, галогенгептилокси, метоксигептилокси, метоксиоктилокси и бутилокси.
Подходящим примером "нафтил(низший) алкеноила" в термине "нафтил(низший) алкеноил, который может иметь один или несколько высших алкокси" могут служить 3-нафтилакрилоил, (2-, или 3-, или 4-) нафтил-(2- или 3-) бутеноил, (2-, или 3-, или 4-, или 5-) нафтил- (2-, или 3-, или 4-)пентаноил, (2-, или 3-, или 4-, или 5-, или 6-) нафтил- (2-, или 3-, или 4-, или 5-) гексаноил и т. п., при этом предпочтительным может быть 3-нафтилакрилоил.
Подходящим примером "низшего алкиноила" в термине "низший алкиноил, который может иметь один или несколько подходящих заместителей" могут служить 2-пропиноил, (2- или 3-)бутиноил, (2-, или 3-, или 4-) пентиноил, (2-, или 3-, или 4-, или 5-)гексеноил и т.п., при этом предпочтительным может быть 2-пропиноил.
Примером "подходящих заместителей" в термине "низший алканоил, который может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "подходящих заместителей", при этом предпочтительными могут быть арил, который может иметь один или несколько низших алкокси; арил, который может иметь один или несколько высших алкокси; арил, замещенный арилом, который может иметь один или несколько низших алкилов; и арил, замещенный арилом, который может иметь один или несколько высших алкилов; более предпочтительными могут быть арил, замещенный арилом, который может иметь 1-3 низших алкилов; и арил, который может иметь 1-3 высших алкокси; еще более предпочтительными могут быть фенил, замещенный фенилом, который может иметь 1-3 (С1-С6)алкилов, и фенил, который может иметь 1-3 (С7-С14)алкокси; а наиболее предпочтительными могут быть фенил, замещенный фенилом, который может иметь пентил, и нафтил, который может иметь гептилокси.
Подходящим примером "ар(С2-С6)алканоила" в термине "ар(С2-С6)алканоил, замещенный арилом, имеющим один или несколько подходящих заместителей, где ар(С2-С6)алканоил может иметь один или несколько подходящих заместителей" могут служить, фенил(С2-С6)алканоил (например, фенилацетил, (2- или 3-) фенилпропаноил, (2-, или 3-, или 4-) фенилбутаноил, (2-, или 3-, или 4-, или 5-) фенилпентаноил, (2-, или 3-, или 4-, или 5-, или 6-)-фенилгексаноил и т. п. ), нафтил (С2-С6)алканоил (например, нафтилацетил, (2- или 3-) нафтилпропаноил, (2-, или 3-, или 4-) нафтилбутаноил, (2-, или 3-, или 4-, или 5-) нафтилпентаноил, (2-, или 3-, или 4-, или 5-, или 6-) нафтилгексаноил и т.п. ) и т.п., при этом предпочтительными могут быть 2-фенилацетил и 3-фенилпропаноил.
Примером "подходящих заместителей" в термине "ар(С2-С6)алканоил, замещенный арилом, имеющим один или несколько подходящих заместителей, где ар(С2-С6)алканоил может иметь один или несколько подходящих заместителей" могут служить низший алкокси; высший алкокси; низший алкил; высший алкил, высший алкокси(низший)алкил; оксо; арил, имеющий один или несколько низших алкокси; арил, имеющий один или несколько высших алкокси; арил, имеющий один или несколько низших алкилов; арил, имеющий один или несколько высших алкилов; арил, замещенный арилом, имеющим один или несколько низших алкокси; арил, замещенный арилом, имеющим один или несколько высших алкокси; арил, замещенный арилом, имеющим один или несколько низших алкилов; арил, замещенный арилом, имеющим один или несколько высших алкилов; арил, имеющий один или несколько низших алкокси(низший)алкокси и т.п., при этом предпочтительными могут быть низший алкокси, высший алкокси, низший алкил, высший алкил, и фенил, имеющий 1-3 низших алкокси(низший)алкокси; более предпочтительными могут быть (С1-С6)алкокси, (С1-С6)алкил, (С7-С14)алкил и фенил, имеющий (С1-С4)алкокси (С3-С6)алкокси; а наиболее предпочтительными могут быть пентилокси, пентил, гептил и фенил, имеющий метоксипентилокси.
Примером "подходящих заместителей", упомянутых в выражении "где ар(С2-С6)алканоил может иметь один или несколько подходящих заместителей" могут служить гидрокси, оксо, амино и нижеупомянутые "защищенные амино".
Подходящим примером "(С2-С6)алканоила", упомянутого в термине "(С2-С6)алканоил, замещенный нафтилом, имеющим высший алкокси" могут служить ацетил, пропаноил, бутаноил, пентаноил, гексаноил и т.п., при этом предпочтительным может быть пропаноил.
Подходящим примером "высшего алкокси", упомянутого в выражении "(С2-С6)алканоил, замещенный нафтилом, имеющим высший алкокси" могут служить примеры, указанные выше для "высших алкокси", при этом предпочтительным примером может служить (С7-С14)алкокси, а наиболее предпочтительным - гептилокси.
Подходящим примером "ароила", упомянутого в выражении "ароил, замещенный гетероциклической группой, которая может иметь один или несколько подходящих заместителей, где указанный ароил может иметь один или несколько подходящих заместителей" могут служить бензоил, толуоил, нафтоил и т.п., при этом предпочтительным может быть бензоил.
Подходящим примером "гетероциклической группы", упомянутой в выражении "ароил, замещенный гетероциклической группой, которая может иметь один или несколько подходящих заместителей" может служить ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-4 атома азота, например, такая как пирролил, пирролинил, имидазолил, пиразолил, пиридил, дигидропиридил, пиримидил, пиразинил, пиридазинил, триазолил (например, 4H-1,2,4-триазолил, 1H-1,2,3-триазолил, 2H-1,2,3- триазолил и т.п.), тетразолил (например, 1H-тетразолил, 2H-тетразолил и т.п. ) и т. п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-4 атома азота, например пирролидинил, имидазолидинил, пиперидил, пиперазинил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-4 атома азота, например индолил, изоиндолил, индолинил, индолизинил, бензимидазолил, хинолил, изохинолил, индазолил, бензотриазолил и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота, например оксазолил, изоксазолил, оксадиазолил (например, 1,2,4-оксадиазолил, 1,3,4-оксадиазолил, 1,2,5-оксадиазолил и т.п.) и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота, например морфолинил, сиднонил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота, например бензоксазолил, бензоксадиазолил, и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома серы и 1-3 атома азота, например тиазолил, изотиазолил, тиадиазолил (например, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,3,4- тиадиазолил, 1,2,5-тиадиазолил и т.п.), дигидротиазинил и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома серы и 1-3 атома азота, например тиазолидинил и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая 1-2 атома серы, например тиенил, дигидродитиинил, дигидродитионил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, 1-2 атома серы и 1-3 атома азота, например бензотиазолил, бензотиадиазолил и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая атом кислорода, например фурил и т.п.;
насыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая атом кислорода, например тетрагидрофуран, тетрагидропиран и т.п.;
ненасыщенная 3-8-членная (более предпочтительно 5- или 6-членная) гетеромоноциклическая группа, содержащая атом кислорода и 1-2 атома серы, например дигидрооксатиинил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая 1-2 атома серы, например бензотиенил, бензодитиинил и т.п.;
ненасыщенная конденсированная гетероциклическая группа, содержащая атом кислорода и 1-2 атома серы, например бензоксатиинил и т.п., и т.п.;
при этом предпочтительными могут быть насыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-4 атома азота; ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота;
ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-4 атома азота; и
ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-2 атома серы и 1-3 атома азота;
а наиболее предпочтительными могут быть пиперазинил, изоксазолил, оксадиазолил, тиадиазолил, пиразолил, пиперидил, оксазолил и пиримидил.
Примером "подходящих заместителей", упомянутых в выражении "ароил, замещенный гетероциклической группой, которая может иметь один или несколько подходящих заместителей, где указанный ароил может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "подходящих заместителей", при этом предпочтительными могут быть арил, который может иметь 1-3 высших алкокси; арил, который может иметь 1-3 низших алкокси, высших алкилов, гетероциклических групп; арил, который может иметь 1-3 низших алкокси(высший)алкокси; арил, который может иметь высший алкенилокси; гетероциклическая группа, которая может иметь арил, содержащий низший алкокси; цикло(низший)алкил, который может иметь арил; арил, который может иметь 1-3 низших алкилов; арил, который может иметь цикло(низший)алкил; арил, который может иметь высший алкенилокси; арил, замещенный гетероциклической группой, которая может иметь низший алкил и оксо; цикло(низший)алкил, который может иметь низший алкил; арил, замещенный арилом, который может иметь 1-3 низших алкокси; и арил, который может иметь гетероциклическую группу; более предпочтительными примерами могут служить фенил, который может иметь 1-3 (C7-C14)алкокси; фенил, который может иметь 1-3 (C3-C6)алкокси, (C7-C14)алкил, насыщенную 3-8-членную гетеромоноциклическую группу, содержащую 1-4 атома азота; фенил, который может иметь 1-3 (C1-C4)алкокси(C7-C14)алкокси; фенил, который может иметь (C7-C14)алкенилокси; насыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-4 атома азота, замещенная фенилом, имеющим (C3-C6)алкокси; цикло(C3-C6)алкил, который может иметь фенил; фенил, который может иметь 1-3 (C3-C6)алкила; фенил, который может иметь цикло(C3-C6)алкил; фенил, который может иметь (C7-C14)алкенилокси; фенил, замещенный гетероциклической группой, которая может иметь (C3-C6)алкил и оксо; цикло(C3-C6)алкил, который может иметь (C3-C6) алкил; фенил, замещенный фенилом, который может иметь 1-3 (C1-C4)алкокси; и фенил, который может иметь 3-8-членную гетеромоноциклическую группу, содержащую 1-4 атома азота; а наиболее предпочтительными могут быть фенил, имеющий октилокси; фенил, имеющий пентилокси; фенил, имеющий гексилокси; гептил, пиперидил; фенил, имеющий изогексилокси; фенил, имеющий гептилокси; фенил, имеющий метоксигептилокси; фенил, имеющий метоксиоктилокси; фенил, имеющий 6-гептенилокси; пиперидил замещенный фенилом, имеющим гексилокси; циклогексил, имеющий фенил; фенил, имеющий гексил; фенил, имеющий циклогексил; фенил, имеющий 7-октенилокси; фенил, замещенный триазолилом, имеющий низший алкил и оксо; циклогексил, имеющий пентил; фенил, имеющий метоксиоктилокси; нонил, фенил, замещенный фенилом, имеющим пропокси, и фенил, имеющий пиперидин.
Примером "подходящих заместителей", упомянутых в выражении "где ароил может иметь один или несколько подходящих заместителей", может служить галоген, при этом предпочтительными могут быть фтор и хлор.
Подходящим примером "ароила", упомянутого в выражении "ароил, замещенный арилом, имеющим гетероциклил(высший)алкокси, где гетероциклическая группа может иметь один или несколько подходящих заместителей", может служить бензоил, толуоил, нафтоил, антрилкарбонил и т.п.; при этом предпочтительным может быть бензоил.
Подходящим примером "гетероциклического" радикала ("гетероциклила"), упомянутого в выражении "ароил, замещенный арилом, имеющим гетероциклил(высший)алкокси, где гетероциклическая группа может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "гетероциклической группы", упомянутой в выражении "ароил, замещенный гетероциклической группой, которая может иметь один или несколько подходящих заместителей"; при этом предпочтительными могут быть ненасыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-4 атома азота, и насыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-2 атома кислорода и 1-3 атома азота; а наиболее предпочтительными могут быть триазолил, тетразолил и морфолинил.
Подходящим примером группы "(высший)алкокси", упомянутой в выражении "ароил, замещенный арилом, имеющим гетероциклил(высший)алкокси, где гетероциклическая группа может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "высшего алкокси", при этом предпочтительным может быть (C7-C14)алкокси, а наиболее предпочтительным октилокси.
Подходящим примером "арила", упомянутого в выражении "ароил, замещенный арилом, содержащим гетероциклил(высший)алкокси, где гетероциклическая группа может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Примером "подходящих заместителей", упомянутых в выражении "где гетероциклическая группа может иметь один или несколько подходящих заместителей", может служить низший алкил, а предпочтительно метил.
Подходящим примером "ароила", упомянутого в выражении "ароил, замещенный арилом, имеющим низший алкокси(высший)алкокси", может служить бензоил, толуоил, нафтоил, антрилкарбонил и т.п., при этом предпочтительным может быть бензоил.
Подходящим примером "арила", упомянутого в выражении "ароил, замещенный арилом, имеющим алкокси(высший)алкокси" могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "низшего алкокси(высший)алкокси" в выражении "ароил, замещенный арилом, имеющим алкокси(высший)алкокси" могут служить метоксигептилокси, метоксиоктилокси, метоксинонилокси, метоксидецилокси, этоксигептилокси, этоксиоктилокси, этоксинонилокси, этоксидецилокси, этоксиундецилокси, пропоксиундецилокси, бутоксидодецилокси, пентилокситридецилокси, гексилокситетрадецилокси, пропоксигептилокси, пропоксиоктилокси, пропоксинонилокси, бутоксидецилокси или т. п., при этом предпочтительным может быть (C1-C6)алкилокси (C7-C14)алкокси, а наиболее предпочтительным может быть метоксиоктилокси.
Подходящим примером "ароила", упомянутого в выражении "ароил, замещенный арилом, имеющим низший алкенил(низший)алкокси" могут служить бензоил, толуоил, нафтоил, антрилкарбонил и т.п., при этом предпочтительным может быть бензоил.
Подходящим примером "арила", упоминаемого в выражении "ароил, замещенный арилом, имеющим низший алкенил(низший)алкокси", могут служить примеры, указанные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "низшего алкенил(низший)алкокси", упомянутого в выражении "ароил, замещенный арилом, имеющим низший, алкенил(низший)алкокси" могут служить винилметокси, винилэтокси, винилпропокси, винилбутокси, винилпентилокси, винилгексилокси, 1- (или 2-) пропенилметокси, 1- (или 2-) пропенилэтокси, 1- (или 2-) пропенилпропокси, 1- (или 2-) пропенилбутокси, 1- (или 2-) пропенилпентилокси, 1- (или 2-) пропенилгексилокси, 1- (или 2-, или 3-) бутенилбутокси, 1-(или 2-, или 3-) бутенилгексилокси, 1- (или 2-, или 3-, или 4-) пентенилпентилокси, 1- (или 2-, или 3-, или 4-) пентенилгексилокси, 1- (или 2-, или 3-, или 4-, или 5-) гексенилбутокси, 1- (или 2-, или 3-, или 4-, или 5-) гексенилгексилокси или т.п.; при этом предпочтительным может быть (C2-C6)алкенил(C1-C6)алкокси, а наиболее предпочтительным может быть винилгексилокси.
Подходящим примером "ароила, замещенного 2 низшими алкокси" могут служить бензоил, замещенный 2 низшими алкокси, и нафтоил, замещенный 2 низшими алкокси; при этом предпочтительным может быть бензоил, замещенный 2 (C1-C6)алкокси, а наиболее предпочтительным может быть бензоил, замещенный 2 пентилокси.
Подходящим примером "ароила, замещенного арилом, имеющим низший алкил" могут служить бензоил, замещенный фенилом, имеющим низший алкил; бензоил, замещенный нафтилом, имеющим низший алкил; нафтоил, замещенный фенилом, имеющим низший алкил; нафтоил, замещенный нафтилом, имеющим низший алкил, и т. п. ; при этом предпочтительным может быть бензоил, замещенный фенилом, имеющим (C1-C6)алкил; а наиболее предпочтительными могут быть бензоил, замещенный фенилом, имеющим гексил; и бензоил, замещенный фенилом, имеющим пентил.
Подходящим примером "ароила, замещенного арилом, имеющим низший алкил" могут служить бензоил, замещенный фенилом, имеющим высший алкил; бензоил, замещенный нафтилом, имеющим высший алкил; нафтоил, замещенный фенилом, имеющим высший алкил; нафтоил, замещенный нафтилом, имеющим высший алкил, и т. п. ; при этом предпочтительным может быть бензоил, замещенный фенилом, имеющим (C7-C14)алкил; а наиболее предпочтительным может быть бензоил, замещенный фенилом, имеющим гептил.
Подходящим примером "арилокси"-части, упомянутой в выражении "арилокси(низший)алканоил, который может иметь один или несколько подходящих заместителей" могут служить фенокси, мезитилокси, толилокси, нафтилокси, антрилокси и т.п.; при этом предпочтительным может быть фенокси.
Подходящим примером "низшей алканоильной" части, упомянутой в выражении "арилокси (низший) алканоил, который может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "низшего алканоила", при этом предпочтительными могут быть формил, ацетил, 2,2-диметилацетил, пропионил, бутирил, изобутирил, пентаноил и гексаноил; более предпочтительными могут быть (C1-C6)алканоил; а наиболее предпочтительными могут быть формил, ацетил, пропионил и 2,2-диметилацетил.
Примером "подходящих заместителей", упомянутых в выражении "арилокси(низший)алканоил, который может иметь один или несколько заместителей", могут служить примеры, приведенные выше для "подходящих заместителей"; при этом предпочтительным может быть (C7-C14)алкокси, а более предпочтительным октилокси.
Подходящим примером "ар(низший)алкокси"-части, упомянутой в выражении "ар(низший)алкокси(низший)алканоил, который может иметь один или несколько подходящих заместителей", могут служить фенил(низший)алкокси (например, фенилметокси, (1- или 2-) фенилэтокси, фенилпропокси, 2-фенил-1-метилпропокси, 3-фенил-2,2-диметилпропокси, (1-, или 2-, или 3-, или 4-) фенилбутокси, (1-, или 2-, или 3-, или 4-, или 5-) фенилпентилокси, (1-, или 2-, или 3-, или 4-, или 5-, или 6-) фенилгексилокси и т.п., нафтил (низший) алкокси (например, нафтилметокси, (1- или 2-) нафтилэтокси, 1-нафтилпропокси, 2-нафтил-1-метил-пропокси, 3-нафтил-2,2-диметилпропокси, (1- или 2- или 3- или 4-) нафтилбутокси, (1-, или 2-, или 3-, или 4-, или 5-) нафтилпентилокси, (1-, или 2-, или 3-, или 4-, или 5-, или 6-) нафтилгексилокси и т.п.) и т.п. ; при этом предпочтительным может быть нафтил (C1-C4)алкокси, а более предпочтительным нафтилметокси.
Подходящим примером группы "(низший)алканоил", упомянутой в выражении "ар(низший)алкокси(низший)алканоил, который может иметь один или несколько подходящих заместителей", могут служить примеры, приведенные выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а более предпочтительным может быть формил.
Примером "подходящих заместителей", упомянутых в выражении "ар(низший)алкокси(низший)алканоил, который может иметь один или несколько подходящих заместителей", могут служить примеры, приведенные выше для "подходящих заместителей"; при этом предпочтительными могут быть низший алкокси, высший алкокси, низший алкил и высший алкил; более предпочтительным может быть высший алкокси, еще более предпочтительным может быть (C7-C14)алкокси, а наиболее предпочтительным может быть гептилокси.
Подходящим примером "ариламино"-группы, упомянутой в выражении "ариламино(низший)алканоил, который может иметь один или несколько подходящих заместителей", могут служить фениламино, мезитиламино, толиламино, нафтиламино, антриламино и т.п.; при этом предпочтительными могут быть фениламино и нафтиламино.
Подходящим примером группы "низший алканоил", упомянутой в выражении "ариламино (низший) алканоил, который может иметь один или несколько подходящих заместителей", могут служить примеры, приведенные выше для "низшего алканоила"; при этом предпочтительным может быть (C1-C4) алканоил, а более предпочтительным формил.
Подходящим примером "подходящих заместителей", упомянутых в выражении "ариламино(низший)алканоил, который может иметь один или несколько подходящих заместителей", могут служить примеры, приведенные выше для "подходящих заместителей"; при этом предпочтительными могут быть низший алкокси; высший алкокси; низший алкил; высший алкил; арил, который может иметь 1-3 низших алкокси; и арил, который может иметь 1-3 высших алкокси; более предпочтительными могут быть (C7-C14)алкокси и фенил, который может иметь 1-3 (C7-C14)алкокси; а наиболее предпочтительными могут быть гептилокси и фенил, который может иметь гептилокси.
Подходящим примером "низшего алканоила", упомянутого в выражении "низший алканоил, замещенный пиразолилом, который может содержать низший алкил и арил, имеющий высший алкокси", могут служить примеры, приведенные выше для "низшего алканоила"; при этом предпочтительным может быть (C1-C4)алканоил, а наиболее предпочтительным может быть формил.
Подходящим примером "низшего алкила", упомянутого в выражении "низший алканоил, замещенный пиразолилом, который имеет низший алкил и арил, содержащий высший алкокси", могут служить примеры, приведенные выше для "низшего алкила"; при этом предпочтительным может быть (C1-C4)алкил, а наиболее предпочтительным может быть метил.
Подходящим примером "арила", упомянутого в выражении "низший алканоил, замещенный пиразолилом, который имеет низший алкил и арил, содержащий высший алкокси", могут служить примеры, приведенные для вышеуказанного "арила"; при этом предпочтительным может быть фенил.
Подходящим примером "высшего алкокси", упомянутого в выражении "низший алканоил, замещенный пиразолилом, который имеет низший алкил и арил, содержащий высший алкокси" могут служить примеры, приведенные ранее для вышеупомянутого "высшего алкокси", при этом предпочтительным может быть (C7-C14)алкокси, а наиболее предпочтительным может быть октилокси.
Подходящим примером "низшего алкокси(высший)алканоила", упомянутого в выражении "низший алкокси(высший)алканоил, где высший алканоил может иметь один или несколько подходящих заместителей", может служить метоксиоктадеканоил.
Примером "подходящих заместителей", упомянутых в выражении "низший алкокси(высший)алканоил, где высший алканоил может иметь один или несколько подходящих заместителей", могут служить амино и вышеупомянутая "защищенная амино"; при этом предпочтительными могут быть амино и ар(низший)алкоксикарбониламино, а наиболее предпочтительными могут быть амино и бензилоксикарбониламино.
Подходящим примером "ароила" в выражении "ароил, замещенный арилом, содержащим гетероциклилокси, где гетероциклилокси может иметь один или несколько заместителей" может служить вышеупомянутый "ароил", при этом предпочтительным может быть бензоил.
Подходящим примером "арила", упомянутого в выражении "ароил, замещенный арилом, содержащим гетероциклилокси, где гетероциклилокси может иметь один или несколько подходящих заместителей" может служить вышеупомянутый "арил"; при этом предпочтительным может быть фенил.
Подходящим примером "гетероциклической" части, упомянутой в выражении "ароил, замещенный арилом, содержащим гетероциклилокси, где гетероциклилокси может иметь один или несколько подходящих заместителей" могут служить примеры, приведенные выше для "гетероциклической" части; при этом предпочтительной может быть 3-8-членная гетеромоноциклическая группа, содержащая 1-4 атома азота, а наиболее предпочтительной может быть пиридазинил.
Примером "подходящих заместителей", упомянутых в выражении "ароил, замещенный арилом, содержащим гетероциклилокси, где гетероциклилокси может иметь один или несколько подходящих заместителей", может служить арил; при этом предпочтительным может быть фенил.
Подходящим примером "ароила" в выражении "ароил, замещенный цикло(низшим)алкилом, содержащим низший алкил" могут служить примеры, приведенные выше для "ароила", где предпочтительным может быть бензоил.
Подходящим примером "цикло(низший)алкила", упомянутого в выражении "ароил, замещенный цикло(низшим)алкилом, содержащим низший алкил", могут служить примеры, приведенные выше для "цикло(низшего)алкила", где предпочтительным может быть циклогексил.
Подходящим примером "низшего алкила", упомянутого в выражении "ароил, замещенный цикло(низшим)алкилом, содержащим низший алкил", могут служить примеры, приведенные выше для "низшего алкила", где предпочтительным может быть пентил.
Подходящим примером "высшего алкила", упомянутого в выражении "индолилкарбонил, имеющий высший алкил", могут служить примеры, приведенные выше для "высшего алкила", где предпочтительным может быть децил.
Подходящим примером "низшего алкила", упомянутого в выражении "нафтоил, содержащий низший алкил", могут служить примеры, приведенные выше для "низшего алкила", где предпочтительным может быть гексил.
Подходящим примером "высшего алкила", упомянутого в выражении "нафтоил, содержащий высший алкил", могут служить примеры, приведенные выше для "высшего алкила", где предпочтительным может быть гептил.
Подходящим примером "низший алкокси(высший)алкокси", упомянутого в выражении "нафтоил, содержащий низший алкокси (высший) алкокси", может служить (C1-C4)алкокси(C7-C14)алкокси, при этом предпочтительным может быть метоксиоктилокси.
Подходящим примером "ароила", упомянутого в выражениях "ароил, замещенный арилом, имеющим низший алкокси(низший)алкокси(высший)алкокси", "ароил, замещенный арилом, имеющим низший алкокси(низший)алкокси", "ароил, замещенный арилом, который имеет арил, содержащий низший алкокси", "ароил, замещенный арилом, который имеет арил, содержащий низший алкокси(низший)алкокси", "ароил, замещенный арилом, имеющим гетероциклилокси(высший)алкокси", "ароил, замещенный арилом, содержащим арилокси(низший)алкокси", "ароил, замещенный арилом, имеющим гетероциклилкарбонил(высший)алкокси", могут служить примеры, приведенные выше для "ароила", при этом предпочтительным может быть бензоил.
Подходящим примером "арила", упомянутого в вышеуказанных терминах, могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "низшего алкокси(низший)алкокси(высший)алкокси", упомянутого в выражении "ароил, замещенный арилом, имеющим низший алкокси(низший)алкокси(высший)алкокси" может служить (C1-C4)алкокси(C1-C4)алкокси(C7-C14)алкокси; при этом предпочтительным может быть этоксиэтоксиоктилокси.
Подходящим примером "низшего алкокси(низший)алкокси", упомянутого в выражении "ароил, замещенный арилом, имеющим низший алкокси(низший)алкокси", может служить (C1-C4)алкокси(C3-C6)алкокси, при этом предпочтительным может быть пропоксигексилокси.
Подходящим примером "низшего алкокси", упомянутого в выражении "ароил, замещенный арилом, который имеет фенил, содержащий низший алкокси", может служить (C3-C6)алкокси, при этом предпочтительным может быть бутокси.
Подходящим примером "низшего алкокси(низший)алкокси", упомянутого в выражении "ароил, замещенный арилом, который имеет фенил, содержащий низший алкокси(низший)алкокси" может служить(C1-C4)алкокси(C3-C6)алкокси; при этом предпочтительными могут быть метоксипентилокси и метоксигексилокси.
Подходящим примером "гетероциклической" части, упомянутой в выражении "ароил, замещенный арилом, содержащим гетероциклилокси (высший) алкокси" могут служить примеры, приведенные выше для "гетероциклической" части; при этом предпочтительной может быть насыщенная 3-8-членная гетеромоноциклическая группа, содержащая атом кислорода, а наиболее предпочтительной может быть тетрагидропиранил.
Подходящим примером "высшей алкокси"-части, упомянутой в выражении "ароил, замещенный арилом, содержащим гетероциклилокси(высший)алкокси" может служить (C7-C14)алкокси, при этом предпочтительным может быть октилокси.
Подходящим примером "арилокси(низший)алкокси", упомянутого в выражении "ароил, замещенный арилом, имеющим арилокси(низший)алкокси", может служить фенокси(C3-C6)алкокси; при этом предпочтительным может быть феноксипентилокси.
Подходящим примером "гетероциклической" части, упомянутой в выражении "ароил, замещенный арилом, имеющим гетероциклилкарбонил(высший)алкокси", могут служить примеры, приведенные выше для "гетероциклической" части; при этом, предпочтительной может быть насыщенная 3-8-членная гетеромоноциклическая группа, содержащая 1-4 атома азота; а наиболее предпочтительным может быть пиперидил.
Подходящим примером "высшей алкокси"-части, упомянутой в выражении "ароил, замещенный арилом, имеющим гетероциклилкарбонил(высший)алкокси", могут служить примеры, приведенные выше для "высшего алкокси"; при этом предпочтительным может быть (C7-C14)алкокси; а наиболее предпочтительным может быть гептилокси.
Подходящим примером "низшего алканоила", упомянутого в выражении "низший алканоил, замещенный оксазолилом, который имеет арил, содержащий высший алкокси", могут служить примеры, приведенные выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а наиболее предпочтительным может быть формил.
Подходящим примером "арила", упомянутого в выражении "низший алканоил, замещенный оксазолилом, который имеет арил, содержащий высший алкокси", могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "высшего алкокси", упомянутого в выражении "низший алканоил, замещенный оксазолилом, который имеет арил, содержащий высший алкокси", могут служить примеры, приведенные выше для "высшего алкокси", при этом предпочтительным может быть (C7-C14)алкокси, а наиболее предпочтительным октилокси.
Подходящим примером "низшего алканоила", упомянутого в выражении "низший алканоил, замещенный фурилом, который имеет арил, замещенный арилом, содержащим низший алкокси", могут служить примеры, приведенные выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а наиболее предпочтительным может быть формил.
Подходящим примером "арила", упомянутого в выражении "низший алканоил, замещенный фурилом, который имеет арил, замещенный арилом, содержащим низший алкокси", могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "низшего алкокси", упомянутого в выражении "низший алканоил, замещенный фурилом, который имеет арил, содержащий низший алкокси", могут служить примером, приведенным выше для "низшего алкокси", при этом предпочтительным может быть (C1-C4)алкокси, а наиболее предпочтительным может быть бутокси.
Подходящим примером "низшего алканоила", упомянутого в выражении "низший алканоил, замещенный триазолилом, которые имеет оксо и арил, содержащий высший алкил", могут служить примеры, приведенные выше для "низшего алканоила", при этом предпочтительным может быть (C1-C4)алканоил, а наиболее предпочтительным может быть формил.
Подходящим примером "высшего алкила", упомянутого в выражении "низший алканоил, замещенный триазолилом, который имеет оксо и арил, содержащий высший алкил", могут служить примеры, приведенные выше для "высшего алкила", при этом предпочтительным может быть (C7-C14)алкил, а наиболее предпочтительным может быть октил.
Подходящим примером "арила", упомянутого в выражении "низший алканоил, замещенный триазолом, который может иметь оксо и арил, содержащий высший алкил", могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "высшего алканоила", упомянутого в выражении "высший алканоил, имеющий гидрокси", могут служить примеры, приведенные выше для "высшего алканоила", при этом предпочтительным может быть (C7-C20)алканоил, а наиболее предпочтительным может быть гексадеканоил.
Подходящим примером "высшего алканоила", упомянутого в выражении "высший алканоил, имеющий ар(низший)алкил и гидрокси", могут служить примеры, приведенные выше для "высшего алканоила", при этом предпочтительным может быть (C7-C20)алканоил, а наиболее предпочтительным может быть гексадеканоил.
Подходящим примером "ар(низший)алкила", упомянутого в выражении "высший алканоил, имеющий ар(низший)алкил и гидрокси", могут служить примеры, приведенные выше для "ар(низший)алкила", при этом предпочтительным может быть фенил(C1-C4)алкил, а наиболее предпочтительным может быть бензил.
Подходящим примером "(C2-C6)алканоила", упомянутого в выражении "(C2-C6)алканоил, замещенный арилом, содержащим высший алкокси, где (C2-C6)алканоил может иметь амино или защищенный амино", могут служить ацетил, пропаноил, бутаноил, пентаноил, гексаноил и т.п., при этом предпочтительными могут быть ацетил и пропаноил.
Подходящим примером "арила", упомянутого в выражении "(C2-C6)алканоил, замещенный арилом, содержащим высший алкокси, где (C2-C6)алканоил может иметь амино или защищенный амино", могут служить примеры, приведенные выше для "арила", при этом предпочтительным может быть фенил.
Подходящим примером "высшего алкокси", упомянутого в выражении "(C2-C6)алканоил, замещенный арилом, имеющим высший алкокси, где (C2-C6)алканоил может иметь амино или защищенный амино", могут служить примеры, приведенные выше для "высшего алкокси", при этом предпочтительным может быть (C7-C14)алкокси, а наиболее предпочтительным может быть октилокси.
Подходящим примером "защищенной амино", упомянутой в выражении "(C2-C6)алканоил, замещенный арилом, имеющим высший алкокси, где (C2-C6)алканоил может иметь амино или защищенную амино" могут служить примеры, приведенные выше для "защищенной амино", при этом предпочтительной может быть ар(низший)алкоксикарбониламино, а наиболее предпочтительно может быть бензилоксикарбониламино.
Ниже более подробно описан способ получения целевого полипептидного соединения (I) настоящего изобретения или его соли.
Способ 1
Целевое полипептидное соединение (I) или его соль могут быть получены посредством реакции соединения (II) или его реакционноспособного производного по аминогруппе или его соли с соединением (III) или его реакционноспособным производным по карбоксигруппе или его солью.
Подходящим реакционноспособным производным по карбоксигруппе соединения (III) может быть галоидангидрид, ангидрид кислоты, активированный амид, активированный сложный эфир, и т.п. Подходящими примерами реакционноспособных производных могут служить хлорангидрид; азид кислоты; смешанный ангидрид кислоты с такой кислотой, как замещенная фосфорная кислота (например, диалкилфосфорная кислота, фенилфосфорная кислота, дифенилфосфорная кислота, дибензилфосфорная кислота, галогенированная фосфорная кислота и т.п.), диалкилфосфорная кислота, сернистая кислота, тиосерная кислота, серная кислота, сульфоновая кислота (например, метансульфоновая кислота, и т.п.), алифатическая карбоновая кислота (например, уксусная кислота, пропионовая кислота, масляная кислота, изомасляная кислота, пивалиновая кислота, пентановая кислота, изопентановая кислота, 2-этилмасляная кислота, трихлоруксусная кислота и т.п.), или ароматическая карбоновая кислота (например, бензойная кислота и т. п.); симметричный ангидрид кислоты; активированный амид с имидазолом, 4-замещенным имидазолом, диметилпиразолом, триазолом, тетразолом или 1-гидрокси-1Н-бензотриазолом; или активированный сложный эфир (например, цианометиловый эфир, метоксиметиловый эфир, диметилиминометиловый 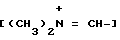 эфир, виниловый эфир, пропаргиловый эфир, н-нитрофениловый эфир, 2,4-динитрофениловый эфир, три-хлорфениловый эфир, пентахлорфениловый эфир, мезил-фениловый эфир, фенилазофениловый эфир, фениловый тиоэфир, п-нитрофениловый тиоэфир, п-крезиловый тиоэфир, карбоксиметиловый тиоэфир, пираниловый эфир, пиридиловый эфир, пиперидиловый эфир, 8-хинолиловый тиоэфир и т.п.), или сложный эфир N-гидроксисоединением (например, N,N-диметилгидроксиламин, 1-гидрокси-2- (1H)-пиридон, N-гидроксисукцинимид, N-гидрокси-фталамид, 1- гидрокси-1H-бензотриазол и т.п.) и т.п. Указанные реакционноспособные производные могут быть, но необязательно, выбраны из вышеприведенных соединений с учетом природы соединения (III), которое необходимо использовать.
эфир, виниловый эфир, пропаргиловый эфир, н-нитрофениловый эфир, 2,4-динитрофениловый эфир, три-хлорфениловый эфир, пентахлорфениловый эфир, мезил-фениловый эфир, фенилазофениловый эфир, фениловый тиоэфир, п-нитрофениловый тиоэфир, п-крезиловый тиоэфир, карбоксиметиловый тиоэфир, пираниловый эфир, пиридиловый эфир, пиперидиловый эфир, 8-хинолиловый тиоэфир и т.п.), или сложный эфир N-гидроксисоединением (например, N,N-диметилгидроксиламин, 1-гидрокси-2- (1H)-пиридон, N-гидроксисукцинимид, N-гидрокси-фталамид, 1- гидрокси-1H-бензотриазол и т.п.) и т.п. Указанные реакционноспособные производные могут быть, но необязательно, выбраны из вышеприведенных соединений с учетом природы соединения (III), которое необходимо использовать.
Подходящими солями соединения (III) и его реакционноспособного производного могут быть соединения, примеры которых приведены выше для получения целевого полипептидного соединения (I).
Реакцию обычно осуществляют в стандартном растворителе, таком, как вода, спирт (например, метанол, этанол, и т.п.), ацетон, диоксан, ацетонитрил, хлороформ, метиленхлорид, этиленхлорид, тетрагидрофуран, этилацетат, N,N-диметилформамид, пиридин или любой другой органический растворитель, который не оказывает неблагоприятного воздействия на реакцию. Указанные стандартные растворители могут быть также использованы в смеси с водой.
В случае, когда соединение (III) используют в свободной кислотной форме или в форме его соли, то эту реакцию предпочтительно осуществляют в присутствии стандартного конденсирующего агента, такого как N,N-дициклогексилкарбодиимид, N-циклогексил-N'-морфолин-этилкарбодиимид, N-циклогексил-N'- (4-диэтиламиноциклогексил) карбодиимид, N,N'-диэтилкарбодиимид, N,N'-диизопропилкарбодиимид, N-этил-N'-(3-диметиламино- пропил)карбодиимид, N,N -карбонилбис-(2-метилимидазол), пентаметиленкетен-N-циклогексилимин, дифенилкетен-N- циклогексилимин, этоксиацетилен, 1-алкокси-2-хлорэтилен, триалкилфосфит, этилполифосфат, изопропилполифосфат, оксихлорид фосфора (фосфорилхлорид), трихлорид фосфора, тионилхлорид, оксалилхлорид, (низший алкил) галогенформат (например, этилхлороформат, изопропилхлороформат и т.п.), трифенилфосфин, 2-этил-7-гидроксибензизоксазолиевая соль; гидроксид 2-этил-5- (м-сульфофенил) изоксазолия (внутримолекулярная соль), 1-(п- хлоробензол-сульфонилокси)-6-хлор-1Н-бензотриазол, так называемый реагент Вильсмайера, полученный с помощью реакции N, N-диметилформамида с тионилхлоридом, фосгеном, трихлорметилхлороформатом, оксихлоридом фосфора, метансульфонилхлоридом и т.п.; и т.п.
Эта реакция может быть также осуществлена в присутствии неорганического или органического основания, такого как карбонат щелочного металла, бикарбонат щелочного металла, три (низший) алкиламин, пиридин, ди (низший) алкиламинопиридин (например, 4-диметил- аминопиридин и т.п.), N-(низший)алкилморфолин, N,N- ди (низший) алкилбензиламин, или т.п.
Реакционная температура не имеет решающего значения, и реакция может быть осуществлена как при охлаждении, так и при нагревании.
Исходное соединение (II) является известным соединением. Оно может быть получено путем ферментации и способом синтеза, описанного в ЕР 0462531 A2.
Культура Coleophoma sp. F-11899, которую использовали в указанном процессе ферментации, была депонирована Национальным институтом биологических наук и технологии человека при Агентстве промышленных наук и технологии (прежнее название: Научно-исследовательский институт по ферментации при Агентстве промышленных наук и технологии) (1-3, Higashi 1-chome, Tsukubashi, IBARAKI 305, JAPAN) 26 октября 1989 под номером допуска FERM ВР-2635.
Соединения, полученные вышеуказанным Способом 1, могут быть выделены и очищены стандартным методом, таким как пульверизация, перекристализация, колоночная хроматография, высокоразрешающая жидкостная хроматография (ВРЖХ), переосаждение и т.п.
В вышеуказанном Способе 1, соединения могут быть получены в виде их гидратов, которые также входят в объем настоящего изобретения.
При этом следует отметить, что каждое из целевых соединений (I) может существовать в виде одного или нескольких стереоизомеров, таких как оптический(е) изомер(ы) и геометрический(е) изомер(ы), благодаря присутствию в этих соединениях асимметрического(их) атома(ов) углерода и двойной(ых) связи(ей), причем все указанные изомеры и их смеси входят в объем настоящего изобретения.
Биологические свойства полипептидного соединения (I) настоящего изобретения
Для иллюстрации эффективности полипептидного соединения (I) настоящего изобретения ниже приводятся биологические данные, полученные при испытаниях характерного соединения (I).
Испытание 1 (Противомикробная активность):
Противомикробную активность in vitro соединения Примера 17, указанную ниже, определяли методом двухкратного разведения в планшете с агаром, как описано ниже.
Метод испытаний
Одну петлю с ночной культурой каждого испытуемого микроорганизма в среде Сабуро, содержащей 2% глюкозу (105 жизнеспособных клеток на 1 мл), наносили штрихом на азотсодержащий декстрозный агар (YNBDA) с дрожжевым экстрактом, включающий ступенчато возрастающие концентрации целевого полипептидного соединения (I), и после инкубирования в течение 24 часов при 30oC определяли минимальную ингибирующую концентрацию (МIС), которую выражали в мкг/мл.
Результаты испытаний
МIС (мкг/мл)
Микроорганизм - Испытуемое соединение Соединение Примера 17
Candida albicans FP-633 - 0,2
Результаты испытаний свидетельствуют о том, что целевое полипептидное соединение (I) настоящего изобретения обладает противомикробной активностью (в частности, противогрибковой активностью).
Фармацевтическая композиция настоящего изобретения может быть использована в виде фармацевтического препарата, например в виде твердой, полутвердой или жидкой лекарственной формы, которая содержит целевое полипептидное соединение (I) или его фармацевтически приемлемую соль в качестве активного ингредиента в смеси с органическим или неорганическим носителем или наполнителем, подходящим для ректального введения, пульмонального введения (путем интраназальной или трансбуккальной ингаляции), введения путем закапывания в глаза, наружного (местного) применения, перорального введения, парентерального введения (подкожного, внутривенного и внутримышечного введения), введения путем инсуффляции (включая применение аэрозолей с помощью ингалятора с дозируемым высвобождением лекарственного средства, с помощью распылителя или с помощью инсуффлятора для вдувания порошкообразных лекарственных средств).
Активный ингредиент может быть смешан, например, с обычными нетоксичными фармацевтически приемлемыми носителями с получением твердой лекарственной формы, такой как гранулы, таблетки, драже, пилюли, пастилки, капсулы или суппозитории; кремы, мази, аэрозоли, порошки для инсуффляции; жидкой лекарственной формы, такой как растворы, эмульсии или суспензии для инъекций; для приема вовнутрь и для глазных капель; а также любой другой лекарственной формы, приемлемой для использования. В вышеуказанные препараты, если это необходимо, могут быть включены добавки, такие как стабилизирующие, загущающие, смачивающие и эмульгирующие агенты, красители, отдушки или буфер, или любые другие обычно используемые добавки.
Целевое полипептидное соединение (I) или его фармацевтически приемлемую соль вводят в фармацевтическую композицию в количестве, достаточном для продуцирования нужного противомикробного эффекта в зависимости от течения и тяжести заболевания.
Предпочтительным способом введения композиции человеку является внутривенное, внутримышечное, пульмональное или пероральное введение, либо введение путем инсуффляции.
Доза терапевтически эффективного количества целевого полипептидного соединения (I) может варьироваться и зависит от возраста и состояния пациента, но, в основном, для лечения или предупреждения инфекционных заболеваний суточная доза целевого полипептидного соединения ((I)) может составлять в случае внутривенного введения 0,01-20 мг, в случае внутримышечного введения 0,1-20 мг; а в случае перорального введения 0,5-50 мг на кг веса человека.
Что касается лечения или предупреждения инфекции, вызываемой Pneumocystis carinii, то можно, в частности, указать следующее.
Для введения путем ингаляции соединение настоящего изобретения может быть изготовлено в виде порошка для доставки путем аэрозольного распыления под давлением, и полученная порошкообразная композиция может быть введена с помощью инсуффлятора. Предпочтительной системой доставки лекарственного средства является аэрозоль для дозированной ингаляции, который может быть изготовлен в виде суспензии или раствора соединения в соответствующем диспергаторе, таком как фторуглерод или углеводород.
Поскольку непосредственная обработка легких и бронхов является особенно желательной в данном случае, то метод введения с помощью аэрозолей является предпочтительным методом. Предпочтительным является также введение путем инсуффляции, особенно в случае распространения инфекции на уши и другие полости организма.
Альтернативно, может быть также применено парентеральное введение путем капельного внутривенного вливания.
Нижеследующие Получения и Примеры приводятся в целях более наглядной иллюстрации настоящего изобретения.
Получение 1
К суспензии, содержащей 1-(4-гидроксифенил)-4- трет-бутоксикарбонилпиперазин (3 г) и карбонат калия (0,82 г) в N,N-диметилформамиде (15 мл), добавляли октилбромид (1,87 мл). Полученную смесь перемешивали в течение 10 часов при температуре 70oC. Затем, реакционную смесь добавляли к смеси воды и этилацетата. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния, фильтрат выпаривали при пониженном давлении. Остаток подвергали колоночной хроматографии на силикагеле и элюировали гексаном/этилацетатом (9:1). Фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении, в результате чего получали 1- (4-н-октилоксифенил)-4-трет-бутокси-карбонилпиперазин (2,71 т).
ИК (KBr): 1687, 1513, 1241 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.2 Hz), 1.2-1.4 (10H, m), 1.48 (9H, s), 1.65-1.85 (2H, m), 3.00 (4H, t, J= 5.2 Hz), 3.57 (4H, t, J= 5.2 Hz), 3.90 (2H, t, J= 6.5 Hz), 6.83 (2H, dd, J= 6.4 and 2.1 Hz), 6.89 (2H, dd, J=6.4 and 2.1 Hz)
Получение 2
Раствор 1-(4-н-октилоксифенил)-4-трет-бутокси- карбонилпиперазина (2,61 г) в трифторуксусной кислоте (20 мл) перемешивали в течение четырех часов при комнатной температуре. Полученную реакционную смесь выпаривали при пониженном давлении и к остатку добавляли смесь, содержащую водный раствор 1 н. гидроксида натрия и этилацетат. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали 1-(4-н- октилоксифенил) пиперазин (0,86 г).
ИК (KBr): 2923, 1513, 1259, 831 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.4 Hz), 1.2-1.53 (10H, m), 1.65-1.85 (2H, m), 3.03 (4H, s), 3.90 (2H, t, J=6.5 Hz), 6.83 (2H, dd, J=6.4 and 2.9 Hz), 6.90 (2H, dd, J=6.4 and 2.9 Hz)
АПХИ (APCI)-МС: m/z = 291 (M++1).
Получение 3
К суспензии, содержащей 1-(4-н-октилокси-фенил) пиперазин (1 г) и карбонат калия (0,476 г) в N,N-диметилформамиде (1 мл), добавляли пара-фторбензонитрил (0,347 г) и эту суспензию перемешивали в течение 5 часов при температуре 160oC. Полученную реакционную смесь добавляли к смеси воды и этилацетата. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния, фильтрат выпаривали при пониженном давлении, в результате чего получали 4-[4-(4-н-октилоксифенил) пиперазин-1-ил]бензонитрил (0,93 г).
ИК (KBr): 2848, 2217, 1604, 1511, 1241 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.53 (10H, m), 1.65-1.85 (2H, m), 3.20 (4H, t, J=5.4 Hz), 3.48 (4H, t, J=5.4 Hz), 3.91 (2H, t, J=6.5 Hz), 6.8- 7.0 (6H, m), 7.52 (2H, d, J=8.9 Hz)
АПХИ-МС: m/z = 392 (M++1).
Получение 4
Смесь, содержащую 2,4-дигидроксибензальдегид (5,52 г), карбонат калия (6,08 г) и октилбромид (7,73 г) в ацетонитриле (55 мл), перемешивали в течение 16 часов при температуре 60oC. Растворитель реакционной смеси удаляли при пониженном давлении, а затем остаток растворяли в этилацетате и промывали водой и рассолом.
Отделенный органический слой осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. Остаток подвергали колоночной хроматографии на силикагеле и элюировали (гексан: этилацетат = 9:1), в результате чего получали 2-гидрокси-4-октилоксибензальдегид (6,73 г).
ЯМР (CDCl3, δ): 0.8 (3H, t, J=8.8 Hz), 1.2-1.5 (10H, m), 1.8-2.0 (2H, m), 4.0-4.2 (2H, m), 6.42 (1H, s), 6.52 (1H, d, J=8.7 Hz), 7.79 (1H, d, J= 8.7 Hz), 10.33 (1H, s)
АПХИ-МС: m/z = 257 (M++1).
Нижеследующее соединение получали способом, описанным в Получении 4.
Получение 5
Метил 3,4-дипентилоксибензоат
ЯМР (CDCl3, δ): 0.93 (6H, t, J=6.0 and 9.0 Hz), 1.3-2.0 (12H, m), 3.88 (3H, s), 4.04 (4H, m), 6.86 (1H, d, J= 8.4 Hz), 7.53 (1H, d, J= 2.0 Hz), 7.63 (1H, dd, J=8.4 and 2.0 Hz)
АПХИ-МС: m/z= 309 (M++1).
Получение 6
Смесь, содержащую 4-бром-4'-пентилбифенила (5,04 г), триметилсилилацетилена (2,4 мл), тетракис(три-фенилфосфин) палладий (0,96 г), трифенилфосфин (0,22 г) и йодид меди (I) (95 мг) в пиперидине (10 мл), нагревали в течение одного часа при атмосферном давлении азота при 90oC. Реакционную смесь выливали в смесь холодной воды и этилацетата, а затем доводили до pH=1 путем добавления 6 н. соляной кислоты. Отделенный органический слой промывали водой и рассолом, а затем осушали сульфатом магния. После этого сульфат магния отфильтровывали, и фильтрат выпаривали при пониженном давлении, в результате чего получали неочищенный 2-[4- (4-пентилфенил)фенил]-1-триметилсилилацетилен, который использовали в последующей реакции без дополнительной очистки. Неочищенную смесь растворяли в смеси дихлорметана (10 мл) и метанола (10 мл), и к полученному раствору добавляли карбонат калия (2,75 г) при температуре 0oC. Затем смесь оставляли для нагревания до комнатной температуры и перемешивали еще 2 часа. Реакционную смесь выливали в смесь холодной воды и этилацетата, и полученный осадок отфильтровывали. Фильтрат доводили до pH 7 путем добавления 1 н. соляной кислоты, промывали рассолом, и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали неочищенный порошок, который подвергали колоночной хроматографии на силикагеле (300 мл) и элюировали смесью гексана и этилацетата (99:1-97:3, об/об) с получением 2,09 г 4-(4-пентилфенил)фенилацетилена.
ИК ("Нуджол"): 3274, 1490 см-1
ЯМР (CDCl3, δ ): 0.90 (3H, t, J=6.4 Hz), 1.30-1.50 (4H, m), 1.50-1.80 (2H, m), 2.64 (2H, t, J=7.6 Hz), 7.20-7.30 (2H, m), 7.45-7.60 (6H, m)
АПХИ-МС: m/z =281 (М++1+MeOH).
Нижеследующее соединение получали способом, описанным в Получении 6.
Получение 7
6-Гептилоксинафталин-2-ил-ацетилен
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.20-1.60 (8H, m), 1.70-1.90 (2H, m), 3.10 (1H, s), 4.07 (2H, t, J=6.5 Hz), 7.08 (1H, d, J=2.5 Hz), 7.15 (1H, dd, J=2.5 and 8.9 Hz), 7.47 (1H, dd, J=1.6 and 8.5 Hz), 7.64 (1H, d, J= 7.3 Hz), 7.68 (1H, d, J=8.5 Hz), 7.94 (1H, d, J=1.6 Hz)
АПХИ-МС: m/z=267 (M++1).
Получение 8
К раствору 4-(4-пентилфенил)фенилацетилена (2,09 г) в тетрагидрофуране (30 мл) по капле добавляли раствор диизобутиламида лития в смеси тетрагидрофурана и н-гексана (1,60 М, 5,6 мл) при температуре - 75oC, и полученную смесь перемешивали в течение одного часа при температуре -78oC. К этой смеси добавляли метилхлорформат (0,72 мл) и реакционную смесь нагревали до комнатной температуры. Полученный раствор разводили этилацетатом, последовательно промывали водой и рассолом, а затем осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении и получали неочищенный продукт, который подвергали колоночной хроматографии на силикагеле (150 мл) и элюировали (элюент: смесь н-гексана и этилацетата = 100: 0 -9: 1, об/об), в результате чего получали метил 3-[4-(4-пентилфенил) фенил]пропионат (2,20 г).
ИК ("Нуджол"): 2225, 1712 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.25-1.50 (4H, m), 1.52-1.80 (2H, m), 2.64 (2H, t, J=7.6 Hz), 3.85 (3H, s), 7.20-7.35 (2H, m), 7.40-7.70 (6H, m)
АПХИ-МС: m/z = 307 (M++1).
Нижеследующее соединение получали способом, описанным в Получении 8.
Получение 9
Метил 3-(6-гептилоксинафталин-2-ил) пропионат
ИК ("Нуджол"): 2219, 1704, 1621 см-1.
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.20-1.60 (8H, m), 1.70-2.00 (2H, m), 3.86 (3H, s), 4.08 (2H, t, J= 6.5 Нz), 7.10 (1H, d, J=2.5 Hz), 7.17 (1H, dd, J=2.5 and 8.9 Hz), 7.52 (1H, dd, J=1.6 and 8.5 Hz), 7.68 (1H, d, J= 7.3 Hz), 7.72 (1H, d, J=8.5 Hz), 8.06 (1H, d, J=1.6 Hz)
АПХИ-МС: m/z =325 (M++1).
Получение 10
Смесь, содержащую 4-бром-4-пентилбифенил (5,0 r), метилакрилат (2,2 мл), ацетат палладия (0,11 г) и трис(о-толил)фосфин (0,60 г) в триэтиламине (16 мл), нагревали с обратным холодильником в течение 15 часов в атмосфере азота. Полученную реакционную смесь выливали в смесь холодной воды и этилацетата и доводили до pH 1,5 путем добавления 6 н. соляной кислоты. Отделенный органический слой последовательно промывали водой и рассолом, а затем осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали неочищенный порошок, который" подвергали колоночной хроматографии на силикагеле (200 мл) и элюировали (н-гексан: этилацетат = 100:0- 94:6, об/об) с получением метил-3-[4-(4-пентилфенил)фенил] акрилата (4,48 г).
ИК ("Нуджол"): 1718, 1637 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J=6.7 Hz), 1.20-1.50 (4H, m), 1.50-1.80 (2H, m), 2.65 (2H, t, J=7.4 Hz), 3.82 (3H, s), 6.47 (1H, d, J=16.0 Hz), 7.20-7.35 (2H, m), 7.45-7.68 (6H, m), 7.73 (1H, d, J=16.0 Hz)
АПХИ-МС: m/z = 309 (M++1).
Нижеследующие соединения (Получения 11-13) были получены способом, описанным в Получении 10.
Получение 11
Метил 3-(6-гептилоксинафталин-2-ил)акрилат
ИК ("Нуджол"): 1716, 1625, 1459 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.20-1.65 (8H, m), 1.76-1.93 (2H, m), 3.82 (3H, s), 4.07 (2H, t, J=6.5 Hz), 6.49 (1H, a, J=16.0 Hz), 7.05-7.20 (2H, m), 7.55-7.90 (5H, m)
АПХИ-МС: m/z = 327 (M++1).
Получение 12
Метил 3-[4-(4-гептилфенил) фенилакрилат
ЯМР(CDCl3, δ): 0.88 (3H, t, J=6.5 Hz), 1.15-1.50 (8H, m), 1.50- 1.75 (2H, m), 2.64 (2H, t, J=7.6 Hz), 3.81 (3H, s), 6.46 (1H, d, J=16.0 Hz), 7.26 (2H, d, J= 8.2 Hz), 7.52 (2H, d, J=8.2 Hz), 7.59 (6H, s), 7.73 (1H, d, J= 16.0 Hz)
АПХИ-МС: m/z = 337 (M++1).
Получение 13
Метил 3-[4-(4-пентилоксифенил)фенил]акрилат
ЯМР (CDCl3, δ): 0.94 (3H, t, J=7.0 Hz), 1.30-1.60 (4H, m), 1.70-1.93 (2H, m), 3.82 (3H, s), 4.00 (2H, t, J=6.7 Hz), 6.45 (1H, d, J=16.0 Hz), 6.90-7.05 (2H, m), 7.48-8.65 (6H, m), 7.72 (1H, d, J=16.0 Hz)
АПХИ-МС: m/z = 325 (M++1)
Получение 14
Смесь 6-гептилоксинафталин-2-карбоновой кислоты (1,00 грамм) и тионилхлорида (5 мл) перемешивали в течение 18 часов при комнатной температуре, а затем концентрировали при пониженном давлении, в результате чего получали неочищенный 6- гептилокси-2-нафтоилхлорид. К смеси этилизонипекотината (605 мг), триэтиламина (425 мг) и N,N-диметиламинопиридина (10 мл) в дихлорметане (10 мл) добавляли неочищенный 6-гептилокси-2- нафтоилхлорид и эту смесь размешивали в течение двух часов при комнатной температуре, а затем разбавляли дихлорметаном. Полученную смесь промывали водой, 1 н. соляной кислотой и рассолом, а затем осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. Остаток подвергали колоночной хроматографии на силикагеле и элюировали (элюент: н-гексан: этилацетат = 3:1), в результате чего получали 4-этоксикарбонил-1-(6-гептилокси-2-нафтоил)пиперидин (1,20 г).
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.6 Hz), 1.2-2.0 (19H, m), 2.5-2.7 (1H, m), 3.0-3.2 (2H, m), 4.1-4.3 (4H, m), 7.1-7.2 (2H, m), 7.44 (1H, dd, J=8.4 and 1.7 Hz), 7.72 (1H, d, J=3.9 Hz), 7.77 (1H, d, J=3.9 Hz), 7.82 (1H, s)
АПХИ-МС: m/z = 426 (M++1).
Получение 15
К смеси метил-3,4-диаминобензоата (1,91 г) и триэтиламина (0,56 г) в N, N-диметилформамиде (20 мл) добавляли деканоилхлорид (2,31 г) и полученную смесь перемешивали в течение одного часа при температуре 0oC. Реакционную смесь разводили этилацетатом, а затем промывали водой и рассолом. Отделенный органический слой осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. Образовавшийся остаток растворяли в метаноле (20 мл), а затем добавляли 0,05 мл концентрированной серной кислоты и полученную смесь размешивали в течение шести часов при температуре 60oC. После охлаждения реакционную смесь выпаривали при пониженном давлении. Остаток разводили этилацетатом и промывали водой и рассолом. Отделенный органический слой осушали сульфатом магния. После этого сульфат магния отфильтровывали, а фильтрат выпаривали при пониженном давлении. Образовавшийся остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: н-гексан/этилацетат = 3:1), в результате чего получали 5-метоксикарбонил-2- нонилбензимидазол (1,40 г).
ИК (таблетка KBr): 2923, 1718, 1623, 1544, 1438, 1413, 1288, 1213, 1085, 750 см-1
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J=6.7 Hz), 1.1-1.4 (12H, m), 1.7-1.9 (2H, m), 2.83 (2H, t, J=7.4 Hz), 7.56 (1H, d, J=8.4 Hz), 7.78 (1H, c, J=8.4 Hz), 8.07 (1H, s)
АПХИ-МС: m/z = 303 (M++1).
Получение 16
К смеси, содержащей диметилмалонат (4 мл), 2-гидрокси-4-октилоксибензальдегид (2,50 г) и пиперидин (0,1 мл) в метаноле (10 мл), добавляли уксусную кислоту (0,01 мл), и смесь размешивали в течение 3 часов при температуре 70oC. После удаления растворителей при пониженном давлении, остаток растворяли в этилацетате, а затем раствор промывали 0,5 н. соляной кислотой, водой и рассолом и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, и образовавшийся осадок собирали путем фильтрации, промывали н-гексаном, а затем осушали, в результате чего получали метил 7-октилоксикумарин-3-карбоксилат (0,94 г).
ЯМР (DMSO-d6, δ): 0.86 (3H, m), 1.2-1.6 (10H, m), 1.7- 1.8 (2H, m), 3.81 (3H, s), 4.11 (2H, t, J=6.4 Hz), 6.9-7.1 (2H, m), 7.83 (1H, d, J=9.0 Hz), 8.75 (1H, s)
АПХИ-МС: m/z = 333 (M++1).
Получение 17
К смеси гидрида натрия (423 мг) и 4-октилфенола (2,06 грамм) в тетрагидрофуране (16 мл) по капле добавляли этил 2-хлорацетоацетат при комнатной температуре. Полученную смесь размешивали в течение шести часов при температуре 70oC в атмосфере азота, а затем выливали в насыщенный водный раствор хлорида аммония. После этого раствор экстрагировали этилацетатом, а органический слой промывали водой и рассолом и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. Остаток добавляли к 10 мл концентрированной серной кислоты при 0oC и смесь размешивали в течение десяти минут. Реакционную смесь выливали в воду со льдом и доводили до pH=7,0 путем добавления 1 н. водного раствора гидроксида натрия, а затем экстрагировали этилацетатом. Органический слой промывали водой и рассолом, а затем осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. Остаток подвергали колоночной хроматографии на силикагеле и элюировали гексаном/этилацетатом (95: 5). Фракции, содержащие нужный продукт, объединяли и выпаривали при пониженном давлении, в результате чего получали этил 3-метил-5-октил-бензо[b]фуран-2-карбоксилат (1,44 г).
ИК (чистый): 2925, 2854, 1712, 1596, 1463, 1292, 1149, 1089 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 1.44 (3H, t, J= 7.1 Hz), 1.6-1.8 (2H, m), 2.58 (3H, s), 2.71 (2H, t, J=8.0 Hz), 4.45 (2H, t, J=7.1 Hz), 7.2-7.5 (3H, m)
АПХИ-МС: m/z = 317 (M++1).
Получение 18
К раствору этил 3-амино-4-гидроксибензоата (1,81 г) и триэтиламина (1,53 мл) в дихлорметане (20 мл) по капле добавляли деканоилхлорид (2,01 мл) при температуре 0oC. Реакционную смесь размешивали в течение 48 часов при комнатной температуре, а затем промывали водой, 0,5 н. соляной кислотой, снова водой и рассолом. Отделенный органический слой осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. К остатку, растворенному в ксилоле (30 мл), добавляли моногидрат паратолуолсульфоновой кислоты (0,5 г) и смесь перемешивали в течение четырех часов при температуре 130oC. К смеси добавляли этилацетат и эту смесь промывали водой и рассолом. Отделенный органический слой осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: н-гексан/этилацетат = 9:1, об/об), в результате чего получали этил 2-нонилбензо [b]оксазол-6-карбоксилат (2,36 г).
ИК (KBr таблетка): 2914, 1722, 1621, 1575, 1470, 1429, 1365, 1290, 1203, 1151, 1115, 1081, 1022 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.7 Hz), 1.2-1.4 (12H, m), 1.42 (3H, t, J= 7.2 Hz), 1.90 (2H, m), 2.95 (2H, t, J=7.4 Hz), 4.40 (2H, q, J=7.0 Hz), 7.50 (1H, d, J=8.5 Hz), 8.06 (1H, d, J=8.5 Hz), 8.37 (1H, s)
АПХИ-МС: m/z= 318 (M++1).
Получение 19
Смесь метил 3,4-диаминобензоата (1,84 г) и 4-гексилоксибензальдегида (2,30 г) в нитробензоле (40 мл) размешивали в течение 48 часов при температуре 145oC. После охлаждения смесь выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: н-гексан/этилацетат = 2:1), в результате чего получали 5-метоксикарбонил-2-(4-гексил- оксифенил) бензимидазол (1,19 г).
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.4 Hz), 1.2-1.9 (8H, m), 3.92 (3H, s), 3.90-4.1 (2H, m), 6.93 (2H, d, J=8.9 Hz), 7.5-7.8 (1H, br), 7.94 (1H, dd, J= 8.5 and 1.5 Hz), 8.03 (1H, d, J=8.9 Hz), 8.2-8.4 (1H, br)
АПХИ-МС: m/z= 353 (M++1).
Получение 20
Смесь метил 3-[4-(4-пентилфенил)фенил]акрилата (2,0 г) и 10% палладия на угле (50 мас.%, 0,2 г) в тетрагидрофуране (20 мл) перемешивали в течение 8 часов при атмосферном давлении водорода при комнатной температуре. После отфильтровывания катализатора фильтрат выпаривали при пониженном давлении, в результате чего получали метил 3-[4-(4-пентилфенил)фенил]пропионат (1,93 г).
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.8 Hz), 1.25-1.50 (4H, m), 1.50-1.75 (2H, m), 2.55-2.75 (4H, m), 2.99 (2H, t, J=8.0 Hz), 3.68 (3H, s), 7.10-7.30 (4H, m), 7.40-7.60 (4H, m)
АПХИ-МС: m/z= 311 (M++1).
Получение 21
Смесь метил 3-[4-(4-пентилоксифенил) фенил] акрилата (2,70 г) и оксида платины (0,41 г) в тетрагидрофуране (40 мл) размешивали в течение 8 часов при атмосферном давлении водорода при комнатной температуре. После отфильтровывания катализатора фильтрат выпаривали при пониженном давлении, в результате чего получали метил 3-[4-(4-пентилоксифенил) фенил] пропионат (2,70 г).
ЯМР (CDCl3, δ): 0.94 (3H, t, J=7.0 Hz), 1.28-1.60 (4H, m), 1.60-1.95 (2H, m), 2.55-2.78 (2H, m), 2.98 (2H, t, J=7.8 Hz), 3.98 (2H, t, J=6.5 Hz), 6.85-7.05 (2H, m), 7.05-7.30 (2H, m), 7.40-7.55 (4H, m)
АПХИ-МС: m/z= 327 (M++1).
Нижеследующее соединение получали способом, описанным в Получении 21.
Получение 22
Метил 3-(6-гептилоксинафталин-2-ил) пропионат
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.20-1.70 (8H, m), 1.70-1.93 (2H, m), 2.70 (2H, t, J=7.7 Hz), 3.07 (2H, t, J=7.7 Hz), 3.67 (3H, s), 4.05 (2H, t, J=6.5 Hz), 7.02-7.20 (2H, m), 7.20- 7.38 (2H, m), 7.55 (1H, s), 7.66 (1H, dd, J=3.0 and 8.5 Hz)
АПХИ-МС: m/z= 329 (M++1).
Получение 23
К смеси, метил 3-[4-(4-пентилфенил)фенил]акрилата (0,41 грамм) в тетрагидрофуране (5 мл) добавляли водный раствор 3 н. гидроксида натрия (1,3 мл) и полученную смесь нагревали в течение десяти часов при 85oC. Реакционную смесь выливали в смесь холодной воды и этилацетата, а затем доводили до pH=2 путем добавления 6 н. соляной кислоты. Отделенный органический слой последовательно промывали водой и рассолом, а затем осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали 3-[4-(4-пентилфенил)фенил]акриловую кислоту (0,41 г).
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J=7.5 Hz), 1.15-1.46 (4H, m), 1.48-1.70 (2H, m), 2.61 (2H, t, J=7.4 Hz), 6.56 (1H, d, J=16.0 Hz), 7.29 (2H, d, J=8.2 Hz), 7.60 (2H, d, J=4.0 Hz), 7.66 (2H, d, J=4.0 Hz), 7.68-7.85 (3H, m)
АПХИ-МС: m/z= 295 (M++1).
Нижеследующие соединения (Получения 24-31) были получены способом, описанным в Получении 23.
Получение 24
3-[4-(4-Пентилоксифенил)фенил] пропионовая кислота
ИК ("Нуджол"): 1697, 1606, 1500 см-1
ЯМР (CDCl3, δ): 0.94 (3H, t, J=7.1 Hz), 1.25-1.60 (4H, m), 1.70-1.95 (2H, m), 2.72 (2H, t, J=7.5 Hz), 3.00 (2H, t, J=7.5 Hz), 3.99 (2H, t, J=6.5 Hz), 6.95 (2H, dd, J=2.1 and 6.7 Hz), 7.25 (2H, d, J=8.2 Hz), 7.40-7.60 (4H, m)
АПХИ-МС: m/z= 313 (M++1).
Получение 25
3-[4-(4-Гептилфенил)фенил]пропионовая кислота
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.8 Hz), 1.15-1.50 (8H, m), 1.50-1.78 (2H, m), 2.65 (2H, t, J=7.6 Hz), 6.48 (1H, d, J=16.0 Hz), 7.27 (2H, d, J=8.2 Hz), 7.53 (2H, d, J=8.2 Hz), 7.63 (4H, m), 7.83 (1H, d, J=16.0 Hz)
АПХИ-МС: m/z= 323 (M++1).
Получение 26
3-[4-(4-Пентилфенил)фенил]пропионовая кислота
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.4 Hz), 1.20- 1.50 (4H, m), 1.50-1.75 (2H, m), 2.64 (2H, t, J=8.0 Hz), 2.67 (2H, t, J=9.6 Hz), 3.00 (2H, t, J=8.0 Hz), 7.15-7.38 (4H, m), 7.38-7.60 (4H, m)
АПХИ-МС: m/z= 297 (M++1).
Получение 27
3-(6-Гептилоксинафталин-2-ил)пропионовая кислота
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.20-1.65 (8H, m), 1.75-2.00 (2H, m), 2.75 (2H, t, J=7.7 Hz), 3.09 (2H, t, J=7.7 Hz), 4.06 (2H, t, J=6.5 Hz), 7.05-7.15 (2H, m), 7.15-7.35 (2H, m), 7.50-7.73 (2H, m)
АПХИ-МС: m/z= 315 (M++1).
Получение 28
3-(6-Гептилоксинафталин-2-ил)акриловая кислота
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.15-1.60 (8H, m), 1.75-1.95 (2H, m), 4.09 (2H, t, J=6.5 Hz), 6.51 (1H, d, J=16.0 Hz), 7.09-7.30 (2H, m), 7.65-3.00 (5H, m)
Получение 29
3-[4-(4-Пентилфенил)фенил]пропионовая кислота
ЯМР (CDCl3, δ): 0.91 (3H, t, J=6.5 Hz), 1.23-1.50 (4H, m), 1.50- 1.80 (2H, m), 2.65 (2H, t, J=7.6 Hz), 7.27 (2H, d, J=8.2 Hz), 7.51 (2H, d, J=8.2 Hz), 7.58-7.80 (4H, m)
АПХИ-МС: m/z= 325 (M++1+MeOH).
Получение 30
3-(6-Гептилоксинафталин-2-ил) пропионовая кислота
ИК ("Нуждол"): 2645, 2198, 1670, 1627 см-1
ЯMP (DMSO-d6, δ): 0.85 (3H, t, J=6.5 Hz), 1.10-1.60 (8H, m), 1.65-1.90 (2H, m), 4.10 (2H, t, J=6.5 Hz), 7.24 (1H, dd, J=2.4 and 8.9 Hz), 7.39 (1H, d, J=2.5 Hz), 7.55 (1H, dd, J=1.6 and 8.5 Hz), 7.8-8.0 (2H, m), 8.22 (1H, d, J=1.6 Hz)
АПХИ-МС: m/z= 343 (M++1+MeOH).
Получение 31
4-[5-(4-Пентилоксифенил)изоксазолил-3-ил]бензойная кислота
ИК (KBr): 2939, 2867, 1681, 1614, 1429, 1255, 1178, 821 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J=7.1 Hz), 1.3-1.5 (4H, m), 1.6-1.8 (2H, m), 4.04 (2H, t, J=6.5 Hz), 7.11 (2H, d, J=8.9 Hz), 7.54 (1H, s), 7.85 (2H, d, J=8.9 Hz), 7.98 (2H, d, J=8.6 Hz), 8.11 (2H, d, J=8.6 Hz)
АПХИ-МС: m/z= 352 (M+H)+
Получение 32
К раствору этил 3-метил-5-октилбензо[b]фуран-2-карбоксилата (1,44 г) в этаноле (20 мл) добавляли 10% водный раствор гидроксида натрия (2,2 мл), и полученную смесь перемешивали в течение 2 часов при комнатной температуре, а затем выпаривали при пониженном давлении. Остаток доводили до pH=3,0 путем добавления 1 н. соляной кислоты, и экстрагировали этилацетатом. Органический слой промывали рассолом и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали 3-метил-5-октилбензо[b]фуран-2-карбоновую кислоту (1,00 г).
ИК (KBr таблетка): 2923, 1689, 1664, 1581, 1456, 1319, 1159, 933 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 1.5-1.8 (2H, m), 2.49 (3H, s), 2.69 (2H, t, J=7.9 Hz), 7.32 (1H, dd, J=8.5 and 1.7 Hz), 7.52 (1H, d, J=8.5 Hz), 7.54 (1H, d, J=1.7 Hz), 13.2-13.5 (1H, br)
АПХИ-МС: m/z= 289 (M++1).
Нижеследующие соединения (Получения 33-39) получали способом, описанным в Получении 32.
Получение 33
3,4-Дипентилоксибензойная кислота
ЯМР (DMSO-d6, δ): 0.89 (6H, t, J=6.8 Hz), 1.2-1.5 (8H, m), 1.6-1.8 (4H, m), 3.9-4.1 (4H, m), 7.02 (1H, d, J=8.4 Hz), 7.43 (1H, d, J=1.7 Hz), 7.53 (1H, dd, J=8.4 and 1.7 Hz)
АПХИ-МС: m/z= 295 (M++1).
Получение 34
1- (6-Гептилокси-2-нафтоил) пиперидин-4-карбоновая кислота
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J=6.7 Hz), 1.2-2.0 (14H, m), 2.5-2.6 (1H, m), 2.9-3.2 (2H, br), 3.25 (2H, s), 4.09 (2H, t, J=6.5 Hz), 7.20 (1H, dd, J= 8.9 and 2.4 Hz), 7.36 (1H, d, J=2.3 Hz), 7.43 (1H, dd, J=8.4 and 1.5 Hz), 7.8-8.0 (3H, m), 12.30 (1H, br)
АПХИ-МС: m/z= 398 (M++1).
Получение 35
7-Октилоксикумарин-3-карбоновая кислота
ИК (KBr): 1748, 1625, 1558, 1467, 1430, 1386, 1360, 1257, 1217, 1120 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.6-1.8 (2H, m), 4.11 (2H, t, J=6.4 Hz), 6.9-7.1 (2H, m), 7.82 (1H, d, J=8.9 Hz), 8.72 (1H, s), 12.98 (1H, br)
АПХИ-МС: m/z= 319 (M++1).
Получение 36
4-(4-Пентилоксифенил) коричная кислота
ИК ("Нуджол"): 2923, 1675, 1500, 1290, 1223, 985, 821 см-1.
ЯМР (DMSO-d6, δ): 0.90 (3H, t, J=7.0 Hz), 1.3-1.5 (4H, m), 1.6-1.8 (2H, m), 4.01 (2H, t, J=6.5 Hz), 6.54 (1H, d, J=16.0 Hz), 7.02 (2H, d, J=8.8 Hz), 7.5-7.8 (7H, m)
АПХИ-МС: m/z= 311 (M++1).
Получение 37
2-Нонилбензоксазол-6-карбоновая кислота
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J=6.7 Hz), 1.2-1.5 (12H, m), 1.7-1.9 (2H, m), 2.96 (2H, t, J=7.4 Hz), 7.76 (1H, d, J=8.4 Hz), 7.98 (1H, d, J=8.4 Hz), 8.19 (1H, s)
АПХИ-МС: m/z= 290 (M++1).
Получение 38
2-(4-Гексилоксифенил) бензимидазол-5-карбоновая кислота
ЯМР (DMSO-d6, δ): 0.8-1.0 (3H, m), 1.3-1.6 (6H, m), 1.7-1.8 (2H, m), 4.06 (2H, t, J= 6.4 Hz), 7.12 (2H, d, J=8.8 Hz), 7.6-7.9 (2H, m), 8.1-8.2 (3H, m), 13.00 (1H, br)
АПХИ-МС: m/z= 339 (M++1).
Получение 39
2-Нонилбензимидазол-5-карбоновая кислота
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J=6.7 Hz), 1.1-1.4 (12H, m), 2.7-2.9 (2H, m), 2.96 (2H, t, J=7.6 Hz), 3.6-5.2 (1H, br), 7.66 (1H, d, J=8.4 Hz), 7.90 (1H, d, J=8.4 Hz), 8.15 (1H, s)
АПХИ-МС: m/z= 289 (M++1).
Получение 40
Раствор 4-[4-(4-октилоксифенил) пиперазин-1-ил] бензонитрила (0,5 г) в 20%-ном водном растворе серной кислоты (30 мл) и уксусной кислоте (20 мл) нагревали с обратным холодильником в течение девяти часов. Реакционную смесь обрабатывали водой. Образовавшийся осадок собирали путем фильтрации и добавляли к смеси, содержащей воду, тетрагидрофуран и этилацетат, а затем доводили до pH=2,5 посредством добавления водного раствора 1 н. гидроксида натрия. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали 4-[4-(4-октилоксифенил)пиперазин-1-ил]бензойную кислоту (388 мг).
ИК (KBr): 2929, 1664, 1600, 1510, 1240 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.6 Hz), 1.2-1.5 (10H, m), 1.5-1.8 (2H, m), 3.13 (4H, t, J=5.3 Hz), 3.44 (4H, t, J=5.3 Hz), 3.88 (2H, t, J=6.5 Hz), 6.83 (2H, d, J=9.2 Hz), 6.94 (2H, d, J=9.2 Hz), 7.02 (2H, d, J=9.0 Hz), 7.79 (2H, d, J=9.0 Hz)
АПХИ-МС: m/z= 411 (M++1).
Получение 41
К суспензии гидрида натрия (60% суспензия в минеральном масле) (0,296 г) в N, N-диметилформамиде (14 мл) добавляли 1,2,4-триазол (0,511 г) и 4-[4-(8-бромоктилокси)фенил] бензойную кислоту (1 г) и смесь перемешивали в течение 5 часов при температуре 120oC. Полученную реакционную смесь добавляли к смеси воды и этилацетата, а затем доводили до pH=2,5 путем добавления концентрированной соляной кислоты. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали 4-[4-[8-(1,2,4- триазол-1-ил)октилокси]фенил]бензойную кислоту (0,81 г).
ИК (KBr): 2940, 1689, 1604, 1297, 1189 см-1
ЯМР (DMSO-d6, δ): 1.1-1.53 (8H, m), 1.6-1.9 (4H, m), 4.00 (2H, t, J=6.3 Hz), 4.16 (2H, t, J=7.0 Hz), 7.03 (2H, d, J=8.7 Hz), 7.67 (2H, d, J=8.7 Hz), 7.75 (2H, d, J=8.4 Hz), 7.95 (1H, s), 7.99 (2H, d, J=8.4 Hz), 8.51 (1H, s), 12.9 (1H, s)
АПХИ-МС: m/z= 394 (M++1).
Получение 42
Смесь, содержащую 2-карбамоил-5-метоксибензо[b]тиофен (2,0 г), уксусную кислоту (5 мл) и 48%-ную бромисто-водородную кислоту (20 мл), перемешивали в течение 16 часов при температуре 110oC, а затем выливали в воду со льдом. Полученный осадок собирали путем фильтрации и осушали, в результате чего получали 5-гидроксибензо[b]тиофен-2- карбоновую кислоту (1,66 г).
ЯМР (DMSO-d6, δ): 7.03 (1H, dd, J=8.8 and 0.6 Hz), 7.31 (1H, d, J=0.6 Hz), 7.81 (1H, d, J=8.8 Hz), 7.96 (1H, s), 9.64 (1H, s), 13.32 (1H, s)
АПХИ-МС: m/z= 195 (M++1).
Получение 43
Раствор (S)-2-трет-бутоксикарбонил-1,2,3,4-тетрагидро-7- гидроксиизохинолин-3-карбоновой кислоты (1 г) в смеси 10% водного раствора гидроксида натрия (2,73 мл) и диметилсульфоксида (11 мл) размешивали в течение 0,5 часа при температуре 80oC. Затем к смеси добавляли октилбромид (0,589 мл) и эту смесь размешивали в течение 4 часов при температуре 660oC. Реакционную смесь добавляли к смеси воды и этилацетата, а затем доводили до pH=2,5 путем добавления концентрированной соляной кислоты. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали (S) -2-трет-бутоксикарбонил-1,2,3,4-тетрагидро-7- октил-оксиизохинолин-3-карбоновую кислоту (1,30 г).
ИК (чистый): 2929, 1743, 1704, 1164 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.1 Hz), 1.1-1.6 (10H, m), 1.41 + 1.51 (9H, s, cis + trans), 1.75 (2H, quint, J=6.5 Hz), 3.10 (2H, m), 3.90 (2H, t, J= 3.9 Hz), 4.42 (1H, d, J=16.8 Hz), 4.65 (1H, d, J=16.8 Hz), 4.74 + 5.09 (1H, m, cis + trans), 6.5-6.8 (2H, m), 7.03 (1H, d, J=8.3 Hz)
АПХИ-МС: m/z= 306 (M++1-Boc).
Нижеследующие соединения (Получения 44-45) были получены способом, описанным в Получении 43.
Получение 44
5-Октилоксибензо [b] тиoфeн-2-кapбoнoвaя кислота
ИК (Kbr): 1673, 1666, 1600, 1517, 1409, 1267, 1214, 1153, 865 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 1.7-1.9 (2H, m), 4.02 (2H, t, J=6.4 Hz), 7.13 (1H, dd, J=8.9 and 0.6 Hz), 7.51 (1H, d, J= 0.6 Hz), 7.90 (1H, d, J=9.0 Hz), 7.99 (1H, s)
АПХИ-МС: m/z= 307 (M++1).
Получение 45
4-[4-(4-Гексилоксифенил)пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1668, 1600, 1510, 1228 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J=6.9 Hz), 1.2-1.5 (6H, m), 1.6-1.9 (2H, m), 3.0-3.2 (4H, m), 3.3-3.5 (4H, m), 3.88 (2H, t, J=6.3 Hz), 6.83 (2H, d, J=9 Hz), 6.9-7.1 (4H, m), 7.79 (2h, d, J=8.8 Hz), 12.32 (1H, s)
АПХИ-МС: m/z = 383 (M+H+).
Получение 46
К суспензии диметилтерефталата (1,94 г) и т-бутоксида калия (2,24 г) в тетрагидрофуране (30 мл) по капле добавляли 4-пентилоксиацетофенон (1,59 г) в тетрагидрофуране (10 мл) при температуре 70oC. Полученную смесь нагревали с обратным холодильником в течение 30 минут, а затем выливали в 1 н. соляную кислоту (50 мл). Затем смесь экстрагировали этилацетатом (100 мл), а органический слой промывали 100 миллилитрами H2O и 100 миллилитрами рассолом, после чего выпаривали при пониженном давлении. Остаток растирали с ацетонитрилом (20 мл), собирали путем фильтрации и осушали при пониженном давлении, в результате чего получали 1-(4-метоксикарбонилфенил)-3-(4-пентилоксифенил) пропан-1,3-дион (2,41 г) в виде желтого твердого вещества.
ИК (KBr): 3475, 2956, 2923, 1720, 1606, 1508, 1284, 1176, 1108, 769 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t,J=7.0 Hz), 1.3-1.5 (4H, m), 1.7-2.0 (2H, m), 3.96 (3H, s), 4.04 (2H, t, J=6.5 Hz), 6.82 (1H, s), 6.96 (2H, d, J=8.9 Hz), 8.0-8.1 (4H, m), 8.14 (2H, m, J=8.7 Hz), 12-13 (1H, br)
АПХИ-МС: m/z = 369 (M+H+).
Получение 47
Раствор 1-(4-метоксикарбонилфенил)-3-(4-пентилоксифенил) пропан-1,3-диона (1,00 г) и гидрохлорида гидроксиламина (567 мг) в метаноле (10 мл) нагревали с обратным холодильником в течение 10 часов. Реакционную смесь разводили 50 миллилитрами этилацетата, а затем промывали водой (50 мл x 2) и рассолом (50 мл). Органический слой осушали сульфатом магния, и растворители удаляли при пониженном давлении. Образовавшийся остаток растирали с ацетонитрилом (10 мл), собирали путем фильтрации, и осушали при пониженном давлении, в результате чего получали метил 4-[5-(4-пентилоксифенил)изоксазол-3-ил]бензоат (0,74 г).
ИК (KBr): 2942, 2873, 1716, 1616, 1508, 1280, 1108 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J=6.9 Hz), 1.3-1.6 (4H, m), 1.8-2.0 (2H, m), 3.95 (3H, s), 4.02 (2H, t, J=6.5 Hz), 6.74 (1H, s), 6.99 (2H, d, J=8.8 Hz), 7.76 (2H, d, J=8.8 Hz), 7.93 (2H, d, J=8.5 Hz), 8.14 (2H, d, J=8.5 Hz)
АПХИ-МС: m/z = 366 (M+H)+.
Получение 48
Раствор 4-[4-(8-бромоктилокси)фенил] бензойной кислоты (1 г) в смеси метилата натрия (28% раствор в метаноле) (10 мл) и N,N-диметилформамида (5 мл) нагревали с обратным холодильником в течение пяти часов. Затем реакционную смесь добавляли к смеси воды и этилацетата и доводили до pH = 2,0 путем добавления концентрированной соляной кислоты. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении, в результате чего получали 4-[4-(8-метоксиоктилокси)фенил]бензойную кислоту (0,77 г).
ИК (KBr): 2935, 1685, 835, 773 см-1
ЯМР (CDCl3, δ): 1.27-1.7 (10H, m), 1.7-1.95 (2H, m), 3.34 (3H, s), 3.38 (2H, t, J=6.4 Hz), 4.01 (2H, t, J=6.5 Hz), 6.99 (2H, d, J=8.7 Hz), 7.58 (2H, d, J=8.7 Hz), 7.66 (2H, d, J=8.4 Hz), 8.15 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 339 (M+ + H - H2O).
Получение 49
К суспензии 1-гидроксибензотриазола (0,283 г) и 6-октилоксиметилпиколиновой кислоты (0,505 г) в дихлорметане (15 мл) добавляли гидрохлорид 1-этил-3-(3'-диметиламинопропил)карбодиимида (WSCD · HCl) (0,473 г) и размешивали в течение 3 часов при комнатной температуре. Затем реакционную смесь выливали в воду. Органический слой отделяли и осушали сульфатом магния. Сульфат магния отфильтровывали, и фильтрат выпаривали при пониженном давлении, в результате чего получали 1-(6-октилоксиметилпиколиноил)бензотриазола 3-оксид (737 мг).
ИК (чистый): 1793, 1654, 1591, 1039 см-1
Нижеследующие соединения (Получения 50-66) были получены способом, аналогичным способу, описанному в Получении 49.
Получение 50
1-[4-(4-Октилоксифенил)пиперазин-1-ил)бензоил]-бензотриазола 3-оксид
ИК (KBr): 1783, 1600, 1511, 1232, 1184 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.6 Hz), 1.2-1.65 (10H, m), 1.65- 1.9 (2H, m), 3.24 (4H, t, J=5.3 Hz), 3.62 (4H, t, J=5.3 Hz), 3.93 (2H, t, J=6.5 Hz), 6.8-7.1 (6H, m), 7.35-7.63 (3H, m), 8.0-8.25 (3H, m)
Получение 51
1-[4-[4-[8-(1,2,4-Тpиaзoл-1-ил)октилокси] фенил] бензоил] бензотриазола 3-оксид
ИК (KBr): 1776, 1600, 1193, 983 см-1
ЯМР (CDCl3, δ): 1.2-2.0 (12H, m), 4.03 (2H, t, J=6.4 Hz), 4.18 (2H, t, J=7.1 Hz), 7.02 (2H, d, J=8.7 Hz), 7.4-7.63 (3H, m), 7.63 (2H, d, J=8.7 Hz), 7.79 (2H, d, J=8.3 Hz), 7.95 (1H, s), 8.06 (1H, s), 8.12 (1H, d, J=7.7 Hz), 8.32 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 511 M++1.
Получение 52
1-[2-Метил-2-(4-октилоксифенокси)пропионил]бензотриазола 3-оксид
ИК (чистый): 2927, 1810, 1504, 1047 см-1
Получение 53
1-[2-(4-Октилоксифенокси)пропионил]бензотриазола 3-оксид
ИК (KBr): 2954, 1812, 1513, 1232 см-1
Получение 54
1-[(S)-2-трет-Бутоксикарбонил-1,2,3,4-тетрагидро-7- oктилoкcиизoxинoлин-3-ил-кapбoнил] бензотриазола 3-оксид
ИК (чистый): 2929, 1816, 1739, 1704, 1392 см-1
Получение 55
Сукцинимид-4-(4-н-октилоксифенил) пиперазин-1 -карбоксила
ИК (KBr): 2925, 1758, 1743, 1513, 1241 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.65-1.85 (2H, m), 2.83 (4H, s), 3.0-3.2 (2H, m), 3.6-3.85 (2H, m), 3.91 (2H, t, J=6.5 Hz), 6.84 (2H, dd, J=8.5 and 2.7 Hz), 6.90 (2H, dd, J= 8.5 and 2.7 Hz)
АПХИ-МС: m/z = 432 (M++1).
Получение 56
(6-Гептилокси-2-нафтил) метилсукцинимида карбонат
ИК (KBr): 1878, 1832, 1787, 1735, 1209 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.2 Hz), 1.2-1.6 (8H, m), 1.73-2.0 (2H, m), 2.83 (4H, s), 4.07 (2H, t, J=6.5 Hz), 5.44 (2H, s), 7.13 (1H, d, J=2.4 Hz), 7.17 (1H, dd, J= 8.8 and 2.4 Hz), 7.44 (1H, dd, J=8.4 and 1.6 Hz), 7.67-7.85 (3H, m)
Получение 57
1-(3,4-Дипентилоксибензоил) бензотриазола 3-оксид
ИК (KBr): 2952, 1774, 1594, 1515, 1430, 1272, 1147, 1089 см-1
ЯМР (CDCl3, δ): 0.9-1.1 (6H, m), 1.3-1.6 (8H, m), 1.8-2.1 (4H, m), 4.0-4.2 (4H, m), 6.99 (1H, d, J=8.5 Hz), 7.4-7.6 (3H, m), 7.68 (1H, d, J=2.0 Hz), 7.92 (1H, dd, J=8.5 and 2.0 Hz), 8.10 (1H, d, J=8.5 Hz)
АПХИ-МС: m/z = 412 (M++1).
Получение 58
1-(7-Октилоксикумарин-3-ил-карбонил)бензотриазола 3-оксид
ИК (KBr): 2925, 1754, 1716, 1610, 1548, 1282, 1199, 1172, 1139, 1064, 781, 750 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=7.8 Hz), 1.2-1.5 (10H, m), 1.6-1.8 (2H, m), 4.11 (2H, t, J=6.5 Hz), 6.9-7.1 (2H, m), 7.41 (1H, t, J=7.2 Hz), 7.54 (1H, t, J=7.2 Hz), 7.72 (1H, d, J=8.3 Hz), 7.82 (1H, d, J=8.3 Hz), 7.99 (1H, d, J=8.3 Hz), 8.72 (1H, s)
АПХИ-МС: m/z = 436 (M++1).
Получение 59
1-[4-(4-Пентилоксифенил)циннамоил]бензотриазола 3-оксид
ИК ("Нуджол"): 2854, 1778, 1708, 1620, 1597, 1494, 1459, 1434, 1377, 1350, 1250, 1188, 1138, 1086, 978 см-1
Получение 60
1 - (5-Октилоксибензо [b] тиoфeн-2-ил-кapбoнил)бензотриазола 3-оксид
ИК (KBr): 2950, 1776, 1517, 1342, 1211, 1151 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 1.7-1.9 (2H, m), 4.01 (2H, t, J=6.4 Hz), 7.13 (1H, dd, J=8.8 and 2.4 Hz), 7.42 (1H, d, J= 7.1 Hz), 7.5-7.6 (3H, m), 7.72 (1H, d, J=8.4 Hz), 7.89 (1H, d, J=8.8 Hz), 7.9-8.1 (2H, m)
АПХИ-МС: m/z = 424 (M++1).
Получение 61
1-(3-Метил-5-октилбензо [b] фуран-2-ил-карбонил)бензотриазола 3-оксид
ИК (KBr): 1776, 1575, 1469, 1363, 1324, 1276, 1114, 1027 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 2.6-2.8 (2H, m), 2.71 (3H, s), 2.76 (2H, t, J=7.4 Hz), 7.4-7.6 (6H, m), 8.12 (1H, s)
АПХИ-МС: m/z = 406 (M++1).
Получение 62
1- (2-Нонилбензоксазол-5-ил-карбонил)бензотриазола 3-оксид
ИК (KBr): 2980, 1783, 1623, 1573, 1276, 1151, 1091, 989 см-1
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J=6.8 Hz), 1.1-1.4 (12H, m), 1.81 (2H, t, J= 7.2 Hz), 2.96 (3H, t, J=7.4 Hz), 7.41 (1H, t, J=7.0 Hz), 7.54 (1H, t, J= 7.0 Hz), 7.74 (2H, t, J=7.0 Hz), 7.98 (2H, d, J=7.0 Hz), 8.19 (1H, s)
АПХИ-МС: m/z = 407 (M++1).
Получение 63
1-[2- (4-Гексилоксифенил) бензимидазол-5-ил- карбонил] бензотриазола 3-оксид
ИК (KBr): 3160, 2931, 2863, 1778, 1612, 1502, 1448, 1388, 1294, 1247, 1174, 1097, 1010, 732 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.7 Hz), 1.2-1.5 (6H, m), 1.7-1.8 (2H, m), 4.08 (2H, t, J=6.4 Hz), 7.16 (2H, d, J=8.7 Hz), 7.6-8.4 (9H, m), 8.3-8.6 (1H, br)
АПХИ-МС: z/m = 456 (M++1).
Получение 64
1-[4-[4-(8-Метоксиоктилокси) фенил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2931, 1793, 1770, 1600 см-1
ЯМР (CDCl3, δ): 1.2-1.7 (10H, m), 1.7-1.93 (2H, m), 3.34 (3H, s), 3.38 (2H, t, J=6.4 Hz), 4.03 (2H, t, J=6.5 Hz), 7.03 (2H, d, J=8.8 Hz), 7.4-7.7 (3H, m), 7.63 (2H, d, J=8.8 Hz), 7.79 (2H, d, J=8.6 Hz), 8.12 (1H, d, J=8.2 Hz), 8.32 (2H, d, J=8.6 Hz)
Получение 65
1-[4-[4-(4-Гексилоксифенил)пиперазин-1-ил]бензоил] бензотриазола 3-оксид
ИК (KBr): 1770, 1604, 1510, 1232, 1186 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J=6.6 Hz), 1.2-1.6 (6H, m), 1.6-1.9 (2H, m), 3.1-3.3 (4H, m), 3.5-3.7 (4H, m), 3.93 (2H, t, J=6.5 Hz), 6.87 (2H, d, J= 9.2 Hz), 6.96 (2H, d, J=9.2 Hz), 7.00 (2H, d, J=9.0 Hz), 7.3-7.7 (3H, m), 8.10 (1H, d, J=8.2 Hz), 8.15 (2H, d, J=9.0 Hz)
АПХИ-МС: m/z = 500 (M+H+).
Получение 66
1-[4-[5-(4-Пентилоксифенил)изоксазол-3-ил]бензоил] бензотриазола 3-оксид
ИК (KBr): 2950, 2837, 1774, 1616, 1508, 1452, 1251, 1006 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J=7.1 Hz), 1.3-1.5 (4H, m), 1.8-2.0 (2H, m), 4.04 (2H, t, J=6.5 Hz), 6.81 (1H, s), 7.0-7.1 (3H, m), 7.4-7.6 (3H, m), 7.80 (2H, d, J=8.8 Hz), 8.0-8.2 (3H, m), 8.40 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 469 (M+H)+.
Получение 67
К суспензии 1-гидроксибензотриазола (0,20 г) и 4-(4-пентилфенил) коричной кислоты (0,40 г) в дихлорметане (12,0 мл) добавляли гидрохлорид 1-этил-3-(3'-диметил- аминопропил)карбодиимида (0,33 г) (WSCD· HCl) и полученную смесь размешивали в течение 12 часов при комнатной температуре. Затем реакционную смесь разбавляли дихлорметаном, промывали рассолом и осушали сульфатом магния. Фильтрат магния отфильтровывали, а фильтрат выпаривали и растирали с ацетонитрилом, в результате чего получали 3-оксид 1-[4-(4-пентилфенил) циннамоил] бензотризола (0,24 г).
ЯМР (CDCl3, δ): 0.91 (3H, t, J=6.6 Hz), 1.20-1.50 (4H, m), 1.50-1.75 (2H, m), 2.66 (2H, t, J=8.0 Hz), 7.20-8.25 (11H, m), 8.55 (1H, d, J=8.4 Hz)
АПХИ-МС: m/z = 412 (M++1).
Нижеследующие соединения (Получения 68-73) были получены способом, аналогичным способу, описанному в Получении 67.
Получение 68
1-[3-[4-[(4-Пентилоксифенил)фенил]-2-пропаноил]бензотриазола 3-оксид
ЯМР (CDCl3, δ): 0.90-1.05 (3H, m), 1.30-1.65 (4H, m) 1.70-1.95 (2H, m), 3.10-3.60 (4H, m), 3.90-4.10 (2H, m), 6.88-7.08 (2H, m), 7.20-8.50 (10H, m)
АПХИ-МС: m/z = 430 (M++1).
Получение 69
1-[4-(4-Гептилфенил)циннамоил]бензотриазола 3-оксид
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.7 Hz), 1.20-1.50 (8H, m), 1.50-1.80 (2H, m), 2.66 (2H, t, J=7.6 Hz), 6.70-8.60 (12H, m)
АПХИ-МС: m/z = 440 (M++1).
Получение 70
1-[3-[4-(4-Пентилфенил)фенил]-2-пропаноил]бензотриазола 3-оксид
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.8 Hz), 1.20-1.50 (4H, m), 1.50-1.76 (2H, m), 2.63 (2H, t, J=7.4 Hz), 3.21 (2H, t, J=7.3 Hz), 3.51 (2H, t, J=7.3 Hz), 7.20-7.45 (4H, m), 7.45-7.70 (5H, m), 7.78 (1H, dt, J=1.0 and 7.2 Hz), 8.00 (1H, d, J=8.2 Hz), 8.42 (1H, d, J=8.4 Hz)
АПХИ-МС: m/z = 414 (M++1).
Получение 71
1-[3-(6-Гептилоксинафталин-2-ил)пропаноил]бензотриазола 3-оксид
ЯМР (CDCl3, δ): 0.80-1.10 (3H, m), 1.20-1.70 (8H, m), 1.70-2.00 (2H, m), 3.10-3.70 (4H, m), 4.00- 4.18 (2H, m), 6.80-8.50 (10H, m)
АПХИ-МС: m/z = 432 (M++1).
Получение 72
1-[3-(6-Гептилоксинафталин-2-ил)пропеноил]-бензотриазола 3-оксид
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.20-1.65 (8H, m), 1.75-1.95 (2H, m), 4.10 (2H, d, J=6.5 Hz), 6.75-8.62 (8H, m)
АПХИ-МС: m/z = 430 (M++1)
Получение 73
1-(4-Гексилфенилбензоил)бензотриазола 3 -оксид
ЯМР (CDCl3, δ): 0.90 (3H, t, J=4.4 Hz), 1.2-1.5 (6H, m), 1.6-1.8 (2H, m), 2.68 (2H, t, J=8.0 Hz), 7.32 (2H, d, J=8.2 Hz), 7.4-7.7 (5H, m), 7.81 (2H, d, J=6.6 Hz), 8.10 (2H, d, J=8.1 Hz), 8.32 (2H, d, J=7.6 Hz)
АПХИ-МС: m/z = 400 (M++1).
Получение 74
К раствору 4-октилоксифенола (1 г) в диметилформамиде (10 мл) и пиридине (0,364 мл) добавляли N,N'-дисукцинимидилкарбоната (1,16 г). Полученную смесь размешивали в течение 12 часов при комнатной температуре. Затем реакционную смесь добавляли к смеси воды и этилацетата. Органический слой отделяли и осушали сульфатом магния. Сульфат магния отфильтровывали и фильтрат выпаривали при пониженном давлении, в результате чего получали 4-октилоксифенилсукцинимидилкарбонат (0,59 г).
ИК (KBr): 2927, 1876, 1832, 1735 см-1
ЯМР (CDCl2, δ): 0.89 (3H, t, J=6.3 Hz), 1.2-1.55 (10H, m), 1.67-1.87 (2H, m), 2.87 (4H, s), 3.94 (2H, t, J=6.5 Hz), 6.89 (2H, d, J=9.2 Hz), 7.17 (2H, d, J=9.2 Hz)
АПХИ-МС: m/z = 364 (М++1).
Нижеследующие соединения (Получения 75-88) были получены способом, описанным в Получении 1.
Получение 75
Метил 4-[4-(6-фенилпиридазин-3-ил-окси)фенил]бензоат
ИК (KBr): 1708, 1427, 1280, 1187, 1112 см-1
ЯМР (CDCl3, δ): 3.95 (3H, s), 7.2-7.7 (10H, m), 7.92 (1H, d, J=9.2 Hz), 8.0-8.2 (4H, m)
АПХИ-МС: m/z = 383 (M+H)+.
Получение 76
Метил 4-[4-(5-бромпентилокси)фенил]бензоат
ИК (KBr): 2946, 2871, 1716, 1602, 1294, 1199, 1112, 837 см-1
ЯМР (CDCl3, δ): 1.7-2.0 (6H, m), 3.45 (2H, t, J=6.7 Hz), 3.93 (3H, s), 4.02 (2H, t, J=6.1 Hz), 6.97 (2H, d, J=8.7 Hz), 7.56 (2H, d, J=8.7 Hz), 7.61 (2H, d, J=8.3 Hz), 8.07 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 378 (M+H)+.
Получение 77
Метил 4-[4-(5-феноксипентилокси) фенил]бензоат
ИК (Kbr): 2944, 2931, 1720, 1600, 1492, 1197, 1110 см-1
ЯМР (CDCl3, δ): 1.6-1.8 (2H, m), 1.8-2.0 (4H, m), 3.93 (3H, s), 4.00 (2H, t, J=6.3 Hz), 4.04 (2H, t, J=6.3 Hz), 6.9-7.1 (5H, m), 7.3-7.4 (2H, m), 7.56 (2H, d, J=8.7 Hz), 7.62 (2H, d, J=8.3 Hz), 8.07 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 391 (M+H)+.
Получение 78
1-[2-(4-Циклогексилфениламино)этил]-2-оксазолидона гидрохлорид
ИК (KBr): 2923,6; 2852,2; 1747,2; 1683,6 см-1
ЯМР (DMSO-d6, δ): 1.1-1.5 (6H, m), 1.6-1.9 (4H, m), 2.3-2.6 (1H, m), 3.3-3.5 (4H, m), 3.58 (2H, dd, J=9.4 and 7.4 Hz), 4.22 (2H, dd, J=9.4 and 7.4 Hz), 7.1-7.4 (4H, m)
Получение 79
Метил 4-[4-(8-гидроксиоктилокси)фенил] бензоат
ИК (KBr): 3250, 2933, 2856, 1724, 1602, 1436, 1292, 1199 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (12H, m), 3.6-3.8 (2H, br), 3.93 (3H, s), 4.00 (2H, t, J=6.7 Hz), 4.82 (1H, s), 7.68 (2H, d, J=8.7 Hz), 7.56 (2H, d, J=8.7 Hz), 7.62 (2H, d, J=8.3 Hz), 8.07 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 357 (M+H+).
Получение 80
Метил 4-[4-(6-бромгексилокси)фенил]бензоат
ИК (KBr): 2937, 2861, 1724, 1602, 1529, 1436, 1292, 1199, 1112 см-1
ЯМР (CDCl3, δ): 1.5-2.0 (8H, m), 3.43 (2H, t, J=6.8 Hz), 3.93 (3H, s), 4.02 (2H, t, J=6.3 Hz), 6.98 (2H, d, J=8.8 Hz), 7.56 (2H, d, J=8.8 Hz), 7.62 (2H, d, J=8.4 Hz), 8.07 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 391 (M+H+).
Получение 81
4-[4-(5-Бромпентилокси)фенил]бромбензол
ИК (KBr): 2942, 2867, 1604, 1515, 1477, 1286 см-1;
ЯМР (CDCl3, δ): 1.5-2.0 (6H, m), 3.44 (2H, t, J=6.7 Hz), 3.99 (2H, t, J= 6.2 Hz), 6.95 (2H, d, J=8.7 Hz), 7.3-7.6 (6H, m)
АПХИ-МС: m/z = 399 (М+Н+).
Получение 82
8-[4-(4-Метоксикарбонилфенил)фенокси]октаноилпиперидин
ИК (KBr): 2935, 2852, 1720, 1639, 1604, 1438, 1292 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (16H, m), 2.34 (2H, d, J=7.6 Hz), 3.4-3.6 (4H, m), 3.93 (3H, s), 3.99 (2H, t, J=6.4 Hz), 6.97 (2H, d, J=8.8 Hz), 7.55 (2H, d, J=8.8 Hz), 7.61 (2H, d, J=8.6 Hz), 8.07 (2H, d, J=8.6 Hz)
АПХИ-МС: m/z = 438 (M+H+).
Получение 83
Метил 6-[4-(4-н-гептилоксифенил)пиперазин-1-ил] никотинат
ИК (KBr): 2933, 2859, 1726, 1608, 1513, 1430, 1280, 1245 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.7 Hz), 1.2-1.8 (10H, m), 3.17 (4H, t, J= 4.9 Hz), 3.8-4.0 (9H, m), 6.65 (1H, d, J=9.1 Hz), 6.86 (2H, d, J=9.1 Hz), 6.96 (2H, d, J=9.1 Hz), 8.05 (1H, dd, J=9.1 and 2.3 Hz), 8.82 (1H, d, J=2.3 Hz)
АПХИ-МС: m/z = 412 (M+H+).
Получение 84
Метил 6-[4-[4-(8-бромоктилокси)фенил]пиперазин-1-ил]никотинат
ИК (KBr): 2933, 2861, 1724, 1608, 1513, 1430, 1280 см-1
ЯМР (CDCl3, δ): 1.2-2.0 (12H, m), 3.17 (4H, t, J=5.0 Hz), 3.40 (2H, t, J= 6.8 Hz), 3.8-4.0 (9H, m), 6.64 (1H, d, J=9.0 Hz), 6.85 (2H, d, J=9.1 Hz), 6.96 (2H, d, J= 9.1 Hz), 8.05 (1H, dd, J=9.0 and 2.2 Hz), 8.82 (1H, d, J=2.2 Hz)
АПХИ-МС: m/z = 504 (M+H+).
Получение 85
4-[4-(7-Бромгептилокси)фенил]бромбензол
ИК (KBr): 2935,1; 2856,1; 1604,5 см-1
ЯМР (CDCl3, δ): 1.18-1.65 (6H, m), 1.70-2.02 (4H, m), 3.41 (2H, t, J=6.8 Hz), 3.99 (2H, t, J=6.4 Hz), 6.95 (2H, d, J=8.6 Hz), 7.40 (2H, d, J=8.6 Hz), 7.46 (2H, d, J=8.6 Hz), 7.52 (2H, d, J=8.6 Hz)
Получение 86
4-[4-(8-Бромоктилокси)фенил]бромбензол
ЯМР (CDCl3, δ): 1.22-1.65 (8H, m), 1.65-1.95 (4H, m), 3.41 (2H, t, J=6.8 Hz), 3.99 (2H, t, J=6.4 Hz), 6.95 (2H, d, J=8.6 Hz), 7.40 (2H, d, J=8.6 Hz), 7.46 (2H, d, J=8.6 Hz), 7.52 (2H, d, J=8.6 Hz)
Получение 87
Метил (E)-3-[4-[4-(5-гексенилокси)фенил]фенил]акрилат
ЯМР (CDCl3, δ): 1.50-1.72 (2H, m), 1.72-1.95 (2H, m), 2.05-2.14 (2H, m), 3.82 (3H, s), 4.01 (2H, t, J=6.3 Hz), 4.95-5.10 (2H, m), 5.70-5.93 (1H, m), 6.46 (1H, d, J=16 Hz), 6.97 (2H, d, J=8.7 Hz), 7.54 (2H, d, J=8.7 Hz), 7.58 (4H, s), 7.72 (1H, d, J=16 Hz)
АПХИ-МС: m/z = 337 (M++1).
Получение 88
4-Бром-4'-(4-метилпентилокси) бифенил
ИК (KBr) : 2956,3; 2871,5; 1606,4 см-1
ЯМР (CDCl3, δ): 0.93 (6H, d, J=6.6 Hz), 1.25-1.45 (2H, m), 1.62 (1H, sept, J=6.6 Hz), 1.72-1.93 (2H, m), 3.98 (2H, t, J=6.6 Hz), 6.95 (2H, d, J= 8.6 Hz), 7.30- 7.60 (6H, m)
АПХИ-МС: m/z = 332, 334 (М+, М++2).
Нижеследующие соединения (Получения 89-90) были получены способом, аналогичным способу, описанному в Получении 2.
Получение 89
N-[4-[2-(4-Метилпентил) -2,3-дигидро-4H-1,2,4-триазол-3-он-4-ил] фенил] пиперазина дитрифторацетат
ИК (KBr): 1668,1; 1519,6; 1203,4; 1176,4; 1130,1 см-1
ЯМР (DMSO-d6, δ): 0.86 (6H, d, J=6.6 Hz), 1.1-1.3 (2H, m), 1.4-1.8 (3H, m), 3.1-3.3 (4H, m), 3.3-3.5 (4H, m), 3.70 (2H, t, J=7.0 Hz), 7.11 (2H, d, J=9.0 Hz), 7.53 (2H, d, J=9.0 Hz), 8.35 (1H, s), 8.90 (2H, s)
Получение 90
1-(4-Фенилциклогексил) пиперазина дитрифторацетат
ИК (KBr): 1677,8; 1197,6; 1133,9 см-1
ЯМР (DMSO-d6, δ): 1.4-1.8 (4H, m), 1.8-2.25 (4H, m), 2.4- 2.7 (1H, m), 3.2-3.7 (9H, m), 4.54 (2H, br s), 7.0-7.4 (5H, m), 9.32 (1H, br s)
АПХИ-МС: m/z = 245 (M++H).
Нижеследующие соединения (Получения 91-103) были получены способом, аналогичным способу, описанному в Получении 3.
Получение 91
Метил 6-[4-(4-октилоксифенил)пиперазин-1-ил]никотинат
ИК (KBr): 2923, 1726, 1608, 1515, 1278, 1116 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.7-1.8 (2H, m), 3.1-3.2 (4H, m), 3.8-4.0 (9H, m), 6.64 (1H, d, J=9.0 Hz), 6.8-7.0 (4H, m), 8.04 (1H, dd, J=9.0 and 2.4 Hz), 8.81 (1H, d, J=2.4 Hz)
АПХИ-МС: m/z = 426 (M+H+).
Получение 92
4-[4-[4-[2-(4-Метилпентил)-2,3-дигидро-4H-1,2,4-триазол-3-он- 4-ил] фенил]пиперазин-1-ил]бензонитрил
ИК (KBr): 2217,7; 1685,5 см-1
ЯМР (CDCl3, δ): 0.90 (6H, d, J=6.6 Hz), 1.2-1.4 (2H, m), 1.5-2.0 (3H, m), 3.3-3.4 (4H, m), 3.4-3.6 (4H, m), 3.83 (2H, t, J=7.4 Hz), 6.92 (2H, d, J= 9.0 Hz), 7.01 (2H, d, J=9.0 Hz), 7.43 (2H, d, J=9.0 Hz), 7.54 (2H, d, J= 9.0 Hz), 7.62 (1H, s)
Получение 93
3-Фтор-4-[4-(4-метоксифенил)пиперазин-1-ил] бензонитрил
ИК (KBr): 2225,5; 1510,0; 1240,0 см-1
ЯМР (CDCl3, δ): 3.1-3.55 (8H, m), 3.79 (3H, s), 6.7-7.1 (6H, m), 7.3-7.5 (1H, m)
Получение 94
3-Хлор-4-[4-(4-н-гексилоксифенил)пиперазин- 1-ил] бензонитрил
ИК (KBr): 2223,5; 1592,9; 1510,0; 1490,7; 1236,1 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.7 Hz), 1.3-1.6 (6H, m), 1.7-1.9 (2H, m), 3.2-3.4 (8H, m), 3.92 (2H, t, J=6.6 Hz), 6.85 (2H, d, J=9.3 Hz), 6.94 (2H, d, J=9.3 Hz), 7.08 (1H, d, J=8.4 Hz), 7.53 (1H, dd, J=8.4 and 1.9 Hz), 7.64 (1H, d, J=1.9 Hz)
АПХИ-МС: m/z = 398 (M++ H).
Получение 95
Этил 3-[4-(4-н-гексилоксифенил)пиперазин-1-ил]-6-пиридазинкарбоксилат
ИК (KBr): 1729,8; 1587,1; 1511,9; 1245,8 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.2-1.4 (6H, m), 1.44 (3H, t, J= 7.1 Hz), 1.65-1.85 (2H, m), 3.1- 3.25 (4H, m), 3.8- 4.0 (6H, m), 4.46 (2H, q, J=7.1 Hz), 6.8-7,0 (5H, m), 7.91 (1H, d, J=9.6 Hz)
АПХИ-МС: m/z = 413 (М++Н).
Получение 96
4-(4-Пиперидинопиперидин-1-ил)бензонитрил
ИК (KBr): 2217,7; 1602,6; 1511,9 см-1
ЯМР (CDCl3, δ): 1.35-1.75 (8H, m), 1.92 (2H, d, J=12.9 Hz), 2.3-2.6 (5H, m), 2.86 (2H, td, J=12.8 and 2.6 Hz), 3.90 (2H, d, J=12.8 Hz), 6.84 (2H, d, J=9.1 Hz), 7.46 (2H, d, J=9.1 Hz)
АПХИ-МС: m/z = 270 (M++H).
Получение 97
5-[4-(4-н-Гексилоксифенил)пиперазин-1-ил] пиколинонитрил
ИК (KBr): 2223,5; 1575,6; 1511,9; 1241,9 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.2-1.55 (6H, m), 1.7-1.85 (2H, m), 3.22 (4H, t, J=5.1 Hz), 3.52 (4H, t, J=5.1 Hz), 3.92 (2H, t, J=6.5 Hz), 6.86 (2H, d, J=9.4 Hz), 6.93 (2H, d, J=9.4 Hz), 7.13 (1H, dd, J=8.8 and 3.0 Hz), 7.53 (1H, d, J=8.8 Hz), 8.35 (1H, d, J= 3.0 Hz)
АПХИ-МС: m/z = 365 (M++H).
Получение 98
4-[4-(4-Циклoгeкcилфeнил)пиперазин-1-ил]бензонитрил
ИК (KBr): 2219,7; 1606,4; 1513,8; 1238,1 см-1
ЯМР (CDCl3, δ): 1.1-1.5 (6H, m), 1.65-2.0 (4H, m), 2.44 (1H, m), 3.30 (4H, t, J=5.1 Hz), 3.46 (4H, t, J=5.1 Hz), 6.90 (4H, d, J=8.9 Hz), 7.14 (2H, d, J=8.9 Hz), 7.52 (2H, d, J=8.9 Hz)
АПХИ-МС: m/z = 346 (М++Н).
Получение 99
4-[4-(4-н-Гексилфенил)пиперазин-1-ил] бензонитрил
ИК (KBr): 2925,5; 2850,3; 2213,9; 1604,5; 1513,8; 1234,2; 944,9 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.4 Hz), 1.2-1.45 (6H, m), 1.45- 1.7 (2H, m), 2.54 (2H, t, J=7.6 Hz), 3.2- 3.4 (4H, m), 3.4-3.6 (4H, m), 6.89 (2H, d, J= 8.5 Hz), 6.91 (2H, d, J=8.9 Hz), 7.11 (2H, d, J=8.5 Hz), 7.52 (2H, d, J= 8.9 Hz)
Получение 100
1-[2-(4-н-Гексилфениламино)этил]-2-оксазолидона гидрохлорид
ИК (KBr) : 2925,5; 2852,2; 1753,0; 1729,8; 1267,0 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J=6.5 Hz), 1.1-1.4 (6H, m), 1.45-1.7 (2H, m), 2.56 (2H, t, J=7.6 Hz), 3.3-3.53 (4H, m), 3.57 (2H, t, J=7.9 Hz), 4.24 (2H, t, J=7.9 Hz), 7.24 (4H, s)
АПХИ-МС: m/z = 291 (M++H).
Получение 101
4-[4-(4-Фенилциклогексил)пиперазин-1-ил]бензонитрил
ИК (KBr): 2212,0; 1602,6; 1513,8; 1249,6 см-1
ЯМР (CDCl3, δ): 1.3-1.8 (4H, m), 1.9-2.2 (4H, m), 2.3-2.6 (2H, m), 2.75 (4H, t, J=5.0 Hz), 3.34 (4H, t, J=5.0 Hz), 6.86 (2H, d, J=8.9 Hz), 7.1-7.4 (5H, m), 7.49 (2H, d, J=8.9 Hz)
АПХИ-МС: m/z = 346 (M++H).
Получение 102
Метил 6-[4-(4-гидроксифенил)пиперазин-1-ил]никотинат
ИК (KBr): 3411, 1691, 1602, 1510, 1432, 1249, 1147 см-1
ЯМР (DMSO-d6, δ): 3.0-3.1 (4H, m), 3.7-3.9 (7H, m), 6.67 (2H, d, J=8.8 Hz), 6.84 (2H, d, J=8.8 Hz), 6.93 (1H, d, J=9.1 Hz), 7.97 (1H, dd, J=2.4 and 9.1 Hz), 8.66 (1H, d, J=2.4 Hz), 8.88 (1H, s)
АПХИ-МС: m/z = 314 (M+H)+.
Получение 103
1-н-Децилиндол-5-карбоновая кислота
ИК (KBr): 2921, 2854, 1679, 1612, 1427, 1313, 1199 см-1
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J=6.8 Hz), 1.1-1.3 (14H, m), 1.6-1.8 (2H, m), 4.19 (2H, t, J=6.9 Hz), 6.57 (1H, s), 7.4-7.8 (3H, m), 8.23 (1H, s), 12.40 (1H, s)
АПХИ-МС: m/z = 302 (M+H+).
Нижеследующие соединения (Получения 104-111) были получены способом, описанным в Получении 10.
Получение 104
(Е)-Метил 4-(4-н-бутоксифенил) циннамат
ИК (KBr): 2958, 2939, 2873, 1720, 1637, 1498, 1313, 1195, 1170 см-1
ЯМР (CDCl3, δ): 0.98 (3H, t, J=7.3 Hz), 1.4-1.8 (4H, m), 3.81 (3H, s), 4.00 (2H, t, J= 6.4 Hz), 6.45 (1H, d, J=16.0 Hz), 6.97 (2H, d, J=8.7 Hz), 7.5-7.7 (6H, m), 7.72 (1H, d, J=16.0 Hz)
АПХИ-МС: m/z = 311 (M+H+).
Получение 105
Метил (E)-3-[4-[4-(4-метилпентилокси)фенил]фенил] акрилат
ИК (KBr): 2956,3; 2873,4; 1720; 1635,3; 1600,6 см-1
ЯМР (CDCl6, δ): 0.93 (6H, d, J=6.5 Hz), 1.28-1.50 (2H, m), 1.50-1.95 (3H, m), 3.82 (3H, s), 3.99 (2H, t, J=6.6 Hz), 6.44 (1H, d, J=16.0 Hz), 6.97 (2H, d, J=8.7 Hz), 7.49-7.65 (6H, m), 7.71 (1H, d, J=16 Hz)
АПХИ-МС: m/z = 339 (M++1).
Получение 106
Метил (E)-3-[4-[4-(6-фторгексилокси)фенил]фенил]акрилат
ЯМР (CDCl3, δ): 1.23-2.00 (8H, m), 3.81 (3H, s), 4.01 (2H, t, J=6.4 Hz), 4.47 (2H, dt, J=47.4 and 6.0 Hz), 6.45 (1H, d, J=16.0 Hz), 6.96 (2H, d, J= 8.8 Hz), 7.45-7.63 (6H, m), 7.72 (1H, d, J=16.0 Hz)
АПХИ-МС: m/z = 357 (М++1).
Получение 107
Метил (E)-3-[4-[4-(6-метоксигексилокси)фенил]фенил]акрилат
АПХИ-МС: m/z = 369 (M+).
Получение 108
Метил (E)-3-[4-[4-(8-метоксиоктилокси)фенил]фенил]акрилат
ИК (KBr): 2935,1; 2858,0; 1722,1; 1637,3; 1602,6 см-1
ЯМР (CDCl6, δ): 1.30-1.70 (10H, m), 1.70-1.92 (2H, m), 3.33 (3H, s), 3.37 (2H, t, J=6.5 Hz), 3.81 (3H, s), 4.00 (2H, t, J=6.5 Hz), 6.45 (1H, d, J= 16.0 Hz), 6.97 (2H, d, J=8.8 Hz), 7.46-7.78 (6H, m), 7.72 (1H, d, J=16.0 Hz)
АПХИ-МС: m/z = 397 (M++1).
Получение 109
Метил (E)-3-[4-(4-гидроксифенил)фенил]акрилат
ИК (KBr): 3409,5; 1695,1 см-1
ЯМР (DMSO-d6, δ): 3.73 (3H, s), 6.64 (1H, d, J=16 Hz), 6.85 (2H, d, J= 8.6 Hz), 7.50-7.83 (5H, m)
АПХИ-МС: m/z = 255 (M++1).
Получение 110
Метил (E)-3-[4-[4-(7-метоксигептилокси)фенил]фенил]акрилат
ЯМР (CDCl3, δ): 1.32-1.70 (8H, m), 1.70-1.92 (2H, m), 3.34 (3H, s), 3.38 (2H, t, J=6.4 Hz), 3.81 (3H, s), 4.00 (2H, t, J=6.5 Hz), 6.45 (1H, d, J=16.0 Hz), 6.97 (2H, d, J=8.8 Hz), 7.47-7.65 (6H, m), 7.70 (1H, d, J=16 Hz)
АПХИ-МС: m/z = 383 (M++1).
Получение 111
Метил (E)-3-[4-[4-(7-фторгептилокси)фенил]фенил]акрилат
ИК (KBr): 2937,1; 2861,8; 1722,1; 1637,3; 1600,6 см-1
Нижеследующее соединение получали способом, описанным в Получении 20.
Получение 112
Метил 3-[4-(4-гептилфенил)фенил]пропаноат
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.5 Hz), 1.15-1.50 (8H, m), 1.50-1.77 (2H, m), 2.52-2.73 (4H, m), 2.99 (2H, t, J=7.8 Hz), 3.68 (3H, s), 7.18-7.35 (4H, m), 7.40- 7.58 (4H, m)
АПХИ-МС: m/z = 339 (M++1).
Нижеследующие соединения (Получения 113-164) получали способом, описанным в Получении 32.
Получение 113
4-(4-Октилфенил)-2,4-дигидро-3H-1,2,4-триазол-3-он-2-ил-уксусная кислота
ИК (KBr): 2923,6; 1704,8; 1224,6 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J=6.7 Hz), 1.1-1.4 (10H, m), 1.4-1.7 (2H, m), 2.60 (2H, t, J=7.2 Hz), 4.38 (2H, s), 7.32 (2H, d, J=8.5 Hz), 7.58 (2H, d, J=8.5 Hz), 8.43 (1H, s)
Получение 114
1-Гептил-4-(4-карбоксифенил)пиразол
ИК (KBr): 3106, 2917, 1687, 1612, 1425, 1295, 1184, 952, 860, 773 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J=6.8 Hz), 1.1-1.4 (8H, m), 1.7-1.9 (2H, m), 4.11 (2H, t, J=7.0 Hz), 7.69 (2H, d, J=8.5 Hz), 7.91 (2H, d, J=8.5 Hz), 7.98 (1H, s), 8.32 (1H, s), 12.82 (1H, br)
АПХИ-МС: m/z = 287 (M+H+).
Получение 115
6-[4-(4-Октилоксифенил)пиперазин-1-ил] никотиновая кислота
ИК (таблетка KBr): 2919, 2854, 1697, 1608, 1515, 1429, 1263, 1245, 1228 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.7 Hz), 1.1-1.5 (10H, m), 1.6-1.8 (2H, m), 3.0-3.2 (4H, m), 3.7-3.9 (4H, m), 3.88 (2H, t, J=6.4 Hz), 6.7-7.0 (5H, m), 7.95 (1H, dd, J=9.0 and 1.1 Hz), 8.64 (1H, d, J= 1.1 Hz)
АПХИ-МС: m/z = 412 (M+H+).
Получение 116
2-(4-Гексилоксифенил)бензоксазол-5-карбоновая кислота
ИК (KBr): 2952, 1689, 1677, 1619, 1500, 1415, 1299, 1172, 1024 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.7 Hz), 1.2-1.5 (6H, m), 1.7-1.9 (2H, m), 4.09 (2H, t, J=6.5 Hz), 7.16 (2H, d, J=8.8 Hz), 7.84 (1H, d, J=8.5 Hz), 8.01 (1H, dd, J=8.5 and 1.5 Hz), 8.15 (2H, d, J=8.8 Hz), 8.26 (1H, d, J=1.5 Hz)
АПХИ-МС: m/z = 340 (M+H+).
Получение 117
4-[4-(4-н-бутоксифенил)фенил]бензойная кислота
ИК (KBr) : 2958, 2873, 1689, 1600, 1537, 1396 см-1
Получение 118
6-(4-Гептилоксифенил) никотиновая кислота
ИК (KBr): 2858, 1699, 1674, 1589, 1425, 1180, 1016, 781 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J=6.7 Hz), 1.2-1.5 (8H, m), 1.6- 1.8 (2H, m), 4.04 (2H, t, J=6.4 Hz), 7.06 (2H, d, J=8.9 Hz), 8.03 (1H, d, J=8.2 Hz), 8.13 (2H, d, J=8.9 Hz), 8.27 (1H, dd, J=8.2 and 2.2 Hz), 9.09 (1H, d, J=2.2 Hz), 13.31 (1H, br)
АПХИ-МС: m/z = 314 (M+H+).
Получение 119
5-(4-Октилоксифенил)изоксазол-3-карбоновая кислота
ИК (таблетка KBr): 2923, 2852, 1704, 1612, 1440, 1272, 1178 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.8 Hz), 1.2-1.6 (10H, m), 1.6-1.9 (2H, m), 4.03 (2H, t, J=6.5 Hz), 7.08 (2H, d, J=8.9 Hz), 7.25 (1H, s), 7.86 (2H, d, J=8.9 Hz)
АПХИ-МС: m/z = 318 (M+H+).
Получение 120
2-(2-Октилoкcипиpидин-5-ил)бензоксазол-5-карбоновая кислота
ИК (KBr): 2954, 2923, 2854, 1697, 1683, 1625, 1488, 1290 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=7.6 Hz), 1.2-1.5 (10H, m), 1.7-1.8 (2H, m), 4.36 (2H, t, J=6.6 Hz), 7.04 (1H, d, J=8.7 Hz), 7.88 (1H, d, J=8.5 Hz), 8.04 (1H, dd, J=8.5 and 1.6 Hz), 8.29 (1H, d, J=1.6 Hz), 8.43 (1H, dd, J=8.7 and 2.4 Hz), 8.99 (1H, d, J=2.4 Hz), 13.0-13.2 (1H, br)
АПХИ-МС: m/z = 369 (M+H+).
Получение 121
2-[4-(4-Гексилфенил)фенил]бензоксазол-5- карбоновая кислота
ИК (KBr): 2923, 2854, 1683, 1411, 1299, 1054 см-1
АПХИ-МС: m/z = 400 (M+H+).
Получение 122
6-[4-(4-н-бутоксифенил)фенил]никотиновая кислота
ИК (KBr): 3406, 2958, 1691, 1591, 1394, 1284, 1253 см-1
ЯМР (DMSO-d6, δ): 0.94 (3H, t, J=7.3 Hz), 1.4-1.8 (4H, m), 4.01 (2H, t, J= 6.4 Hz), 7.02 (2H, d, J=8.7 Hz), 7.57 (2H, d, J=8.7 Hz), 7.61 (2H, d, J= 8.2 Hz), 7.83 (2H, d, J=8.2 Hz), 8.05 (1H, d, J=8.5 Hz), 8.22 (1H, dd, J=8.5 and 1.6 Hz), 9.14 (1H, d, J=1.6 Hz)
АПХИ-МС: m/z = 348 (M+H+).
Получение 123
4-[4-(5-Феноксипентилокси)фенил]бензойная кислота
ЯМР (DMSO-d6, δ): 1.5-1.7 (2H, m), 1.7-1.9 (4H, m), 3.98 (2H, t, J=6.3 Hz), 4.05 (2H, t, J=6.1 Hz), 6.8-7.0 (3H, m), 7.05 (2H, d, J=8.6 Hz), 7.25 (2H, t, J=8.2 Hz), 7.68 (2H, d, J=8.5 Hz), 7.75 (2H, d, J=8.2 Hz), 7.98 (2H, d, J=8.2 Hz), 12.8-13.0 (1H, br s)
АПХИ-МС: m/z = 375 (M-H)-.
Получение 124
4-[5-(4-н-гексилоксифенил)-1,3,4-оксадиазол-2-ил] бензойная кислота
ИК (KBr): 2935, 2854, 1685, 1612, 1495, 1425, 1286, 1251 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.7 Hz), 1.2-1.5 (6H, m), 1.6-1.9 (3H, m), 4.12 (2H, t, J=6.4 Hz), 7.19 (2H, d, J=8.7 Hz), 8.08 (2H, d, J=8.7 Hz), 8.18 (2H, d, J=8.4 Hz), 8.24 (2H, d, J= 8.4 Hz)
АПХИ-МС: m/z = 367 (M+H)+.
Получение 125
4-[5-(4-н-гексилоксифенил)-1,3,4-тиадиазол-2-ил] бензойная кислота
ИК (KBr): 2952, 2586, 1699, 1604, 1517, 1432, 1251, 1174 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.7 Hz), 1.3-1.9 (8H, m), 4.04 (2H, t, J=6.3 Hz), 7.13 (2H, d, J=8.8 Hz), 7.97 (2H, d, J=8.8 Hz), 8.11 (4H, s)
АПХИ-МС: m/z = 383 (M+H)+.
Получение 126
5-(4-Октилоксифенил)-1-метилпиразол-3-карбоновая кислота
ИК (таблетка KBr): 2950, 2923, 1695, 1450, 1282, 1251, 956 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.6-1.8 (2H, m), 3.98 (2H, t, J=6.5 Hz), 4.10 (3H, s), 6.95 (1H, d, J=8.8 Hz), 7.18 (1H, s), 7.73 (2H, d, J=8.8 Hz), 13.37 (1H, br)
АПХИ-МС: m/z = 331 (M+H)+.
Получение 127
4-[3-(4-н-пентилоксифенил)пиразол-5-ил] бензойная кислота
ИК (KBr): 3224, 2956, 1692, 1614, 1506, 1251 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J=6.9 Hz), 1.3-1.5 (4H, m), 1.6-1.8 (2H, m), 4.00 (2H, t, J=6.5 Hz), 7.02 (2H, d, J=8.8 Hz), 7.19 (1H, s), 7.75 (2H, d, J=8.8 Hz), 7.95 (2H, d, J=8.7 Hz), 8.02 (2H, d, J=8.7 Hz), 12.8-13.3 (2H, br)
АПХИ-МС: m/z= 351 (M+H+).
Получение 128
5-[4-(4-н-бутоксифенил)фенил]фуран-2-карбоновая кислота
ИК (KBr): 2958, 2873, 1679, 1487, 1253, 1166 см-1
ЯМР (DMSO-d6, δ): 0.95 (3H, t, J=7.3 Hz), 1.3-1.8 (4H, m), 4.02 (2H, t, J= 6.3 Hz), 7.03 (2H, d, J=8.6 Hz), 7.17 (1H, d, J=3.6 Hz), 7.33 (1H, d, J= 3.6 Hz), 7.66 (2H, d, J=8.6 Hz), 7.74 (2H, d, J=8.4 Hz), 7.86 (2H, d, J=8.4 Hz), 13.1 (1H, br s)
АПХИ-МС: m/z = 337 (M+H)+.
Получение 129
3-(S)-гидроксигексадекановая кислота
ИК (KBr): 1679,7, 1467,6, 1224,6 см-1
ЯМР (CDCl6, δ): 0.88 (3H, t, J=6.4 Hz), 1.1-1.7 (24H, m), 2.35-2.65 (2H, m), 4.03 (1H, m), 5.41 (1H, br s)
Получение 130
6-[4-(4-н-гексилоксифенил)пиперазин-1-ил]пиридазин- 3-карбоновая кислота
ИК (KBr): 1697,1; 1589,1; 1515,8; 1448,3 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J=6.4 Hz), 1.2-1.5 (6H, m), 1.6- 1.8 (2H, m), 3.0-3.2 (4H, m), 3.7-4.0 (6H, m), 6.83 (2H, d, J=9.0 Hz), 6.95 (2H, d, J=9.0 Hz), 7.36 (1H, d, J=9.6 Hz), 7.86 (1H, d, J=9.6 Hz), 11.68 (1H, s)
Получение 131
4-[4-[1-(4-н-гексилоксифенил)пиперидин-4-ил] пиперазин-1-ил] бензойной кислоты гидрохлорид
ИК (KBr); 1699,0, 1608,3, 1513,8 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J=6.5 Hz), 1.2-1.5 (6H, m), 1.6- 1.8 (2H, m), 2.0-2.45 (3H, m), 3.2-3.8 (12H, m), 3.94 (2H, t, J=6.4 Hz), 4.03 (2H, d, J= 11 Hz), 6.95 (2H, d, J=8.7 Hz), 7.07 (2H, d, J=8.9 Hz), 7.32 (2H, br s), 7.83 (2H, d, J=8.9 Hz)
АПХИ-МС: m/z= 466 (M++H).
Получение 132
6-(8-метоксиоктилокси)-2-нафтойная кислота
ИК (KBr): 2937,1, 2854,1, 1677,8, 1211,1 см-1
ЯМР (DMSO-d6, δ): 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.20 (3H, s), 3.29 (2H, t, J=6.5 Hz), 4.11 (2H, t, J=6.4 Hz), 7.23 (1H, dd, J=9.0 and 2.3 Hz), 7.39 (1H, d, J=2.3 Hz), 7.85 (1H, d, J=8.7 Hz), 7.93 (1H, d, J=8.7 Hz), 7.99 (1H, d, J=9.0 Hz), 8.51 (1H, s), 12.9 (1H, s)
Получение 133
Смесь (E) и (Z)-3-[4-(4-гептилфенил)фенил]-2-бутеновой кислоты
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.6 Hz), 1.15-1.50 (8H, m), 1.52-1.75 (2H, m), 2.63 and 3.62 (total 3H, each s), 2.53-2.75 (2H, m), 6.24 and 5.68 (total 1H, each s), 7.19-7.35 (2H, m), 7.47-7.70 (6H, m)
АПХИ-МС: m/z = 337 (M++1), 351 (сложный метиловый эфир+ +1).
Получение 134
3-[4-(4-гептилфенил)фенил]пропановая кислота
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.6 Hz), 1.13-1.48 (8H, m) 1.48-1.75 (2H, m), 2.52-2.83 (4H, m), 3.00 (2H, t, J=7.8 Hz), 7.15-7.35 (4H, m), 7.40-7.60 (4H, m)
АПХИ-МС: m/z = 323 (M+-1).
Получение 135
4-(4-н-гептилфенил)бензоилкарбоновая кислота
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.6 Hz), 1.13-1.50 (8H, m), 1.50-1.75 (2H, m), 2.66 (2H, t, J= 7.7 Hz), 7.20-7.40 (2H, m), 7.50-7.66 (2H, m), 7.66-7.84 (2H, m), 8.40-8.60 (2H, m)
АПХИ-МС: m/z = 323 (M+-1).
Получение 136
6-Гексилнафталин-2-карбоновая кислота
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.15-1.53 (6H, m), 1.55-1.84 (2H, m), 2.80 (2H, t, J=7.6 Hz), 7.42 (1H, dd, J=1.7 and 8.4 Hz), 7.67 (1H, s), 7.84 (1H, d, J=8.6 Hz), 7.90 (1H, d, J=8.4 Hz), 8.09 (1H, dd, J=1.7 and 8.6 Hz), 8.68 (1H, s)
АПХИ-МС: m/z = 257 (M++1), 271 (сложный метиловый эфир+ +1).
Получение 137
3-(E)-[4-[4-(7-метоксигептилокси)фенил]фенил]акриловая кислота
ЯМР (DMSO-d6, δ): 1.20-1.60 (8H, m), 1.60-1.83 (2H, m), 3.21 (3H, s), 3.25-3.60 (2H, m), 4.01 (2H, t, J=6.4 Hz), 6.54 (1H, d, J=16.0 Hz), 7.02 (2H, d, J=8.8 Hz), 7.55-7.80 (7H, m)
АПХИ-МС: m/z = 369 (M++1).
Получение 138
3-(E)-[4[4-(8-метоксиоктилокси)фенил]фенил]акриловая кислота
ИК (KBr): 3037,3, 2933,2, 2858,0, 2551,4, 1706,7, 1677,8, 1629,6, 1602,6 см-1
ЯМР (DMSO-d6, δ): 1.18-1.55 (10H, m), 1.65-1.83 (2H, m), 3.18-3.45 (5H, m), 4.01 (2H, t, J=6.5 Hz), 6.53 (1H, d, J=16.0 Hz), 7.02 (2H, d, J=8.8 Hz), 7.50-8.80 (7H, m)
АПХИ-МС: m/z = 383 (M++1).
Получение 139
3-(E)-[4-[4-(5-гексенилокси)фенил]фенил]акриловая кислота
ЯМР (DMSO-d6, δ): 1.42-1.63 (2H, m), 1.63-1.85 (2H, m), 2.00-2.20 (2H, m), 4.03 (2H, t, J=6.3 Hz), 4.90- 5.15 (2H, m), 5.68-5.97 (1H, m), 6.54 (1H, d, J=16 Hz), 7.02 (2H, d, J=8.7 Hz), 7.50-7.80 (7H, m)
АПХИ-МС: m/z = 323 (M++1).
Получение 140
3-(E)-[4-[4-(4-метилпентилокси)фенил]фенил]акриловая кислота
ИК (KBr); 2956,3, 2869,6, 2713,4, 2599,6, 1689,3, 1627,6, 1602,6 см-1
ЯМР (DMSO-d6, δ): 0.89 (6H, d, J=6.5 Hz), 1.15-1.43 (2H, m), 1.48-1.90 (3H, m), 4.00 (2H, t, J=6.7 Hz), 6.54 (1H, d, J=16 Hz), 7.02 (2H, d, J=8.7 Hz), 7.50-7.90 (7H, m)
АПХИ-МС: m/z = 325 (M++1).
Получение 141
3-(E)-[4-[4-(6-Фторгексилокси)фенил]фенил]акриловая кислота
ЯМР (CDCl3, δ): 1.39-2.00 (8H, m), 4.01 (2H, t, J=6.5 Hz), 4.47 (2H, dt, J= 47.3 and 6.0 Hz), 6.49 (1H, d, J=15.9 Hz), 6.98 (2H, d, J=8.7 Hz), 7.40-7.70 (6H, m), 7.81 (1H, d, J=15.9 Hz)
АПХИ-МС: m/z = 343 (M++1).
Получение 142
3-(E)-[4-[4-(6-метоксигексилокси)фенил]фенил]акриловая кислота
ЯМР (DMSO-d6, δ): 1.22-1.63 (6H, m), 1.63-1.88 (2H, m), 3.21 (3H, s), 3.22-3.40 (2H, m), 4.00 (2H, t, J=6.5 Hz), 6.54 (1H, d, J=15.8 Hz), 7.02 (2H, d, J= 8.7 Hz), 7.50-7.84 (7H, m)
АПХИ-МС: m/z = 369 (сложный метиловый эфир, M++1).
Получение 143
4-[4-[8-(Тетрагидропиран-2-ил-окси) октилокси] фенил] бензойная кислота
ИК (KBr): 2935, 1697, 1683, 1604, 1303, 1290, 1197 см-1
ЯМР (DMSO-d6, δ): 1.2-1.8 (18H, m), 3.3-3.9 (4H, m), 4.01 (2H, t, J=6.3 Hz), 4.5-4.6 (1H, m), 7.03 (2H, d, J=8.7 Hz), 7.67 (2H, d, J=8.7 Hz), 7.74 (2H, d, J=8.3 Hz), 7.98 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 425 (M-H+).
Получение 144
4-[3-(4-н-гексилоксифенил)пиразол-5-ил] бензойная кислота
ИК (KBr): 2956, 2935, 1693, 1614, 1508, 1432, 1251, 1178 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.4 Hz), 1.2-1.5 (6H, m), 1.6-1.8 (2H, m), 4.00 (2H, t, J=6.4 Hz), 7.02 (2H, d, J=8.7 Hz), 7.12 (1H, s), 7.74 (2H, d, J=8.7 Hz), 7.95 (2H, d, J=8.8 Hz), 8.01 (2H, d, J=8.8 Hz), 13.17 (1H, s)
АПХИ-МС: m/z = 365 (M+H+).
Получение 145
4-[4-[4-(6-Метоксигексилокси)фенил]фенил]бензойная кислота
ИК (KBr): 2939, 2861, 1685, 1602, 1430, 1286, 1128 см-1
ЯМР (DMSO-d6, δ): 1.3-1.8 (8H, m), 3.21 (3H, s), 3.3-3.4 (2H, m), 4.01 (2H, t, J=6.5 Hz), 7.04 (2H, d, J=8.6 Hz), 7.66 (2H, d, J=8.6 Hz), 7.7-7.9 (6H, m), 8.03 (2H, d, J=8.2 Hz)
АПХИ-МС: m/z = 405 (М+H+).
Получение 146
4-[5-[4-(8-Метоксиоктилокси)фенил] -1,3,4-тиадиазол-2-ил] бензойная кислота
ИК (KBr): 2931, 2854, 1691, 1602, 1251 см-1
ЯМР (DMSO-d6, δ): 1.2-2.0 (12H, m), 3.20 (3H, s), 3.29 (2H, t, J=6.4 Hz), 4.04 (2H, t, J=6.4 Hz), 7.13 (2H, t, J=8.8 Hz), 7.9-8.2 (6H, m), 13.95 (1H, br)
АПХИ-МС: m/z = 441 (M+H+).
Получение 147
4-(4-н-бутоксифенил) коричная кислота
ИК (KBr): 2958, 2871, 1695, 1625, 1498, 1249 см-1
ЯМР (DMSO-d6, δ): 0.94 (3H, t, J=7.3 Hz), 1.44 (2H, tq, J=7.0 and 7.3 Hz), 1.71 (2H, tt, J=7.0 and 6.4 Hz), 4.01 (2H, t, J=6.4 Hz), 6.54 (1H, d, J=16.0 Hz), 7.02 (2H, d, J=8.7 Hz), 7.6-7.9 (7H, m)
АПХИ-МС: m/z = 297 (M+H+).
Получение 148
4-[5-(4-Циклогексилфенил)-1,3,4-тиадиазол-2-ил]бензойная кислота
ИК (KBr): 2925, 2850, 1683, 1429, 1292 см-1
ЯМР (DMSO-d6, δ): 1.1-1.5 (5H, m), 1.6-2.0 (5H, m), 2.4-2.6 (1H, m), 7.45 (2H, d, J=8.3 Hz), 7.96 (2H, d, J=8.3 Hz), 8.13 (4H, s)
АПХИ-МС: m/z = 365 (М+Н)+.
Получение 149
4-[5-[4-(Пиперидин-1-ил)фенил]-1,3,4-тиадиазол-2-ил] бензойная кислота
ИК (KBr): 2931, 2854, 1685, 1604, 1415, 1238 см-1
ЯМР (DMSO-d6, δ): 1.61 (6H, s), 3.31 (4H, s), 7.05 (2H, d, J=9.0 Hz), 7.83 (2H, d, J=9.0 Hz), 8.10 (4H, s)
АПХИ-МС: m/z = 366 (М+Н)+.
Получение 150
4-[5-[4-[4-н-пропилоксифенил)фенил] -1,3,4- оксадиазол-2-ил] бензойная кислота
ИК (KBr): 2939, 1689, 1606, 1488, 1429, 1290 см-1
ЯМР (DMSO-d6, δ): 1.00 (3H, t, J=7.3 Hz), 1.76 (2H, tq, J=6.5 and 7.3 Hz), 4.00 (2H, t, J=6.5 Hz), 7.07 (2H, d, J=8.8 Hz), 7.70 (2H, d, J=8.5 Hz), 7.78 (2H, d, J=8.8 Hz), 7.90 (2H, d, J=8.5 Hz), 8.0-8.4 (4H, m)
АПХИ-МС: m/z = 401 (M+H)+.
Получение 151
4-(5-н-Нонил-1,3,4-оксадиазол-2-ил) бензойная кислота
ИК (KBr): 2919, 2852, 1685, 1565, 1430, 1284 см-1
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J= 6.5 Hz), 1.2-1.5 (12H, m), 1.7-1.9 (2H, m), 2.94 (2H, t, J=7.4 Hz), 8.0-8.2 (4H, m), 13.35 (1H, s)
АПХИ-МС: m/z = 317 (M+H)+.
Получение 152
4-[3-(4-н-Гексилоксифенил)-1,2,4-оксадиазол-5-ил] бензойная кислота
ИК (KBr): 2942, 2869, 1695, 1421, 1251 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.8 (8H, m), 4.06 (2H, t, J= 6.5 Hz), 7.13 (2H, d, J=8.9 Hz), 8.03 (2H, d, J=8.9 Hz), 8.17 (2H, d, J= 8.5 Hz), 8.28 (2H, d, J=8.5 Hz)
АПХИ-МС: m/z = 367 (M+H)+.
Получение 153
4-[4-[4-(5-Метоксипентилокси)фенил]фенил]фенилуксусная кислота
ИК (КВг): 2939, 2861, 1699, 1253, 1182, 1124 см-1
ЯМР (DMSO-d6, δ): 1.4-1.9 (6H, m), 3.22 (3H, s), 3.39 (2H, t, J=6.2 Hz), 3.61 (2H, s), 4.01 (2H, t, J=6.4 Hz), 7.02 (2H, d, J=8.8 Hz), 7.35 (2H, d, J=8.2 Hz), 7.6-7.8 (8H, m)
АПХИ-МС: m/z = 405 (М+Н+).
Получение 154
4-[5-(4-н-Октилоксифенил)-1,3,4-тиадиазол-2-ил] бензойная кислота
ИК (KBr): 2921, 2856, 1691, 1432, 1251 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 1.7-1.9 (2H, m), 4.07 (2H, t, J=6.5 Hz), 7.13 (2H, d, J=8.9 Hz), 7.97 (2H, d, J=8.9 Hz), 8.12 (4H, s)
АПХИ-МС: m/z = 411 (М+Н+).
Получение 155
4-[5-(4-Транс-н-пентилциклогексил)-1,3,4- тиадиазол-2-ил] бензойная кислота
ИК (KBr) : 2919, 2848, 1677, 1430, 1294 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J=6.9 Hz), 1.0-1.4 (11H, m), 1.5-1.6 (2H, m), 1.8-2.0 (2H, m), 2.1-2.3 (2H, m), 3.1-3.3 (1H, m), 8.07 (4H, s)
АПХИ-МС: m/z = 359 (M+H+).
Получение 156
4-[3-(4-н-Пентилоксифенил)изоксазол-5-ил] бензойная кислота
ИК (KBr): 2925, 2869, 1699, 1687, 1612, 1432, 1251, 1178 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J=6.9 Hz), 1.2-1.5 (4H, m), 1.7-1.9 (2H, m), 4.04 (2H, t, J=6.5 Hz), 7.09 (2H, d, J=8.8 Hz), 7.69 (1H, s), 7.85 (2H, d, J=8.8 Hz), 8.01 (2H, d, J=8.5 Hz), 8.11 (2H, d, J=8.5 Hz)
АПХИ-МС: m/z = 352 (M+H+).
Получение 157
4-[5-[4-(8-Метоксиоктилокси)фенил] -1,3,4-оксадиазол-2-ил] бензойная кислота
ИК (KBr): 2967, 2937, 2877, 1687, 1290 см-1
ЯМР (DMSO-d6, δ): 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.20 (3H, s), 3.29 (2H, t, J=6.4 Hz), 4.08 (2H, t, J=6.5 Hz), 7.17 (2H, d, J=8.9 Hz), 8.07 (2H, d, J=8.9 Hz), 8.15 (2H, d, J=8.6 Hz), 8.24 (2H, d, J=8.6 Hz)
АПХИ-МС: m/z = 425 (M+H)+.
Получение 158
4-[4-(6-Фенилпиридазин-3-ил-окси)фенил] бензойная кислота
ИК (KBr): 1700, 1687, 1608, 1427, 1284, 1186 см-1
ЯМР (DMSO-d6, δ): 7.40 (2H, d, J=8.6 Hz), 7.5-7.7 (4H, m), 7.7-7.9 (4H, m), 7.9-8.1 (4H, m), 8.35 (1H, d, J=9.2 Hz), 12.99 (1H, br s)
АПХИ-МС: m/z = 369 (M+H)+.
Получение 159
4-[5-(4-н-Октилоксифенил)-1,3,4-оксадиазол-2-ил] бензойная кислота
ИК (KBr): 2921, 2852, 1685, 1612, 1496, 1425, 1288, 1251 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J=6.7 Hz), 1.2-1.5 (10H, m), 1.7-1.9 (2H, m), 4.08 (2H, t, J=6.4 Hz), 7.17 (2H, d, J=8.7 Hz), 8.07 (2H, d, J=8.7 Hz), 8.15 (2H, d, J=8.5 Hz), 8.24 (2H, d, J=8.5 Hz), 13.36 (1H, br)
АПХИ-МС: m/z = 395 (M+H+).
Получение 160
4-[2-(4-н-Гексилоксифенил)пиримидин-6-ил] бензойная кислота
ИК (KBr): 2944, 2863, 1697, 1585, 1415, 1386, 1253 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J=6.7 Hz), 1.2-1.6 (6H, m), 1.7-1.9 (2H, m), 4.07 (2H, t, J=6.6 Hz), 7.10 (2H, d, J=8.9 Hz), 8.00 (1H, d, J=5.2 Hz), 8.13 (2H, d, J=8.4 Hz), 8.44 (2H, d, J=5.9 Hz), 8.47 (2H, d, J=5.9 Hz), 8.95 (1H, d, J=5.2 Hz)
АПХИ-МС: m/z = 377 (M+H+).
Получение 161
4-[4-(7-Пиперидинокарбонилгептилокси)фенил]бензойная кислота
ИК (KBr): 2933, 2858, 1697, 1677, 1637, 1604, 1429, 1249 см-1
ЯМР (DMSO-d6, δ): 1.2-1.8 (16H, m), 2.26 (2H, t, J=7.5 Hz), 3.2-3.5 (4H, m), 4.01 (2H, t, J=6.4 Hz), 7.03 (2H, d, J=8.8 Hz), 7.67 (2H, d, J=8.8 Hz), 7.74 (2H, d, J=8.4 Hz), 7.98 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 424 (M+H+).
Получение 162
6-[4-(4-н-Гептилоксифенил)пиперазин-1-ил]никотиновая кислота
ИК (KBr): 2929, 2854, 1695, 1673, 1606, 1577, 1515, 1421, 1245 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J=6.7 Hz), 1.2-1.5 (8H, m), 1.6- 1,8 (2H, m), 3.0-3.2 (4H, m), 3.6-3.8 (4H, m), 3.87 (2H, t, J=6.5 Hz), 6.8-7.2 (5H, m), 7.95 (1H, dd, J=8.9, 2.3 Hz), 8.62 (1H, d, J=2.3 Hz)
АПХИ-МС: m/z = 398 (М+Н+).
Получение 163
6-[4-[4-(8-Метоксиоктилокси)фенил]пиперазин-1-ил]никотиновая кислота
ИК (KBr): 2933, 2856, 1697, 1672, 1605, 1511, 1421, 1245 см-1
ЯМР (DMSO-d6, δ): 1.2-1.8 (12H, m), 3.08 (4H, t, J=5.0 Hz), 3.20 (3H, s), 3.28 (2H, t, J=6.5 Hz), 3.78 (4H, t, J=4.6 Hz), 3.87 (2H, t, J=6.4 Hz), 6.8-7.0 (5H, m), 7.95 (1H, dd, J=9.0 and 2.2 Hz), 8.65 (1H, d, J=2.2 Hz), 12.54 (1H, s)
АПХИ-МС: m/z = 442 (M+H+).
Получение 164
4-[5-[4-(4-н-Пропилоксифенил)фенил] -1,3,4-тиадиазол-2-ил] бензойная кислота
ИК (KBr): 1685, 1537, 1423, 817 см-1
ЯМР (DMSO-d6, δ): 1.00 (3H, t, J=6.7 Hz), 1.6-1.8 (2H, m), 4.00 (2H, t, J=6.6 Hz), 7.0-7.2 (2H, d, J=8.6 Hz), 7.6-8.1 (10H, m)
АПХИ-МС: m/z = 417 (M+H)+.
Получение 165
К раствору этил 4-[5-(4-н-пентилоксифенил) изоксазол-3-ил]бензоата (6,33 г) в этаноле (60 мл) и тетрагидрофуране (90 мл) добавляли 2 н. водный раствор гидроксида натрия (12,5 мл) при 80oC. Полученную смесь нагревали в колбе с обратным холодильником в течение 1 часа и выливали в воду со льдом. С помощью 1 н. HCl pH суспензии доводили до 2,0. Осадок собирали путем фильтрации, промывали водой и осушали, в результате чего получали 4-[5-(4-н-пентилоксифенил)изоксазол- 3-ил] бензойную кислоту (5,80 г).
ИК (KBr): 2939, 2867, 1681, 1614, 1429, 1255, 1178, 821 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J=7.1 Hz), 1.3-1.5 (4H, m), 1.6- 1.8 (2H, m), 4.04 (2H, t, J=6.5 Hz), 7.11 (2H, d, J=8.9 Hz), 7.54 (1H, s), 7.85 (2H, d, J=8.9 Hz), 7.98 (2H, d, J=8.6 Hz), 8.11 (2H, d, J= 8.6 Hz)
АПХИ-МС: m/z = 352 (M+H)+.
Нижеследующие соединения (Получения 166-170) были получены способом, описанным в Получении 40.
Получение 166
5-[4-(4-н-Гексилоксифенил)пиперазин-1-ил] пиколиновой кислоты тригидрохлорид
ИК (KBr): 1689,3; 1577,5; 1511,9; 1241,9 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J=6.5 Hz), 1.15-1.5 (6H, m), 1.6-1.8 (2H, m), 3.1-3.25 (4H, m), 3.45-3.6 (4H, m), 3.89 (2H, t, J=6.4 Hz), 6.84 (2H, d, J= 9.1 Hz), 6.97 (2H, d, J=9.1 Hz), 7.43 (1H, dd, J=8.8 and 3.0 Hz), 7.90 (1H, dd, J=8.8 and 0.7 Hz), 8.41 (1H, dd, J=3.0 and 0.7 Hz)
АПХИ-МС: m/z = 384 (M++H).
Получение 167
4-[4-(4-Фенилциклогексил)пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1700,9, 1606,4, 1220,7, 1180,2 см-1
ЯМР (DMSO-d6, δ): 1.4-1.85 (4H, m), 1.9-2.05 (2H, m), 2.2-2.4 (2H, m), 3.1-3.5 (6H, m), 3.5-3.7 (2H, m), 3.9-4.2 (2H, m), 7.06 (2H, d, J=8.8 Hz), 7.1-7.4 (5H, m), 7.83 (2H, d, J=8.8 Hz)
АПХИ-МС: m/z = 365 (М++H).
Получение 168
4-(4-Транс-н-пентилциклогексил) бензойная кислота
ИК (KBr): 1681,6, 1423,2, 1290,1 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.6 Hz), 1.0-1.6 (13H, m), 1.89 (4H, d, J=10 Hz), 2.54 (1H, t, J=12 Hz), 7.30 (2H, d, J= 8.3 Hz), 8.03 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 274 (M++H).
Получение 169
4-(4-Пиперидинопиперидин-1-ил) бензойная кислота
ИК (KBr): 1710,6; 1403,9 см-1
ЯМР (DMSO-d6, δ): 1.6-2.1 (8H, m), 2.17 (2H, d, J=12 Hz), 2.7- 3.05 (4H, m), 3.2-3.5 (1H, m), 3.35 (2H, d, J=12 Hz), 4.05 (2H, d, J=13 Hz), 7.01 (2H, d, J=8.9 Hz), 7.77 (2H, d, J=8.9 Hz), 10.84 (1H, s)
АПХИ-МС: m/z = 289 (M++H).
Получение 170
3-Хлоро-4-[4-(4-н-гексилоксифенил)пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1712,5; 1598,7; 1513.8; 1251,6 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J=6.6 Hz), 1.2-1.5 (6H, m), 1.6- 1.8 (2H, m), 3.4-3.6 (8H, m), 3.98 (2H, t, J=6.4 Hz), 7.02 (2H, d, J=9.0 Hz), 7.32 (1H, d, J=8.1 Hz), 7.60 (2H, d, J=9.0 Hz), 7.89 (1H, d, J=8.1 Hz), 8.02 (1H, s)
АПХИ-МС: m/z = 417 (M++H).
Нижеследующие соединения (Получения 171-175) были получены способом, описанным в Получении 41.
Получение 171
Этил [4-(4-октилфенил)-2,3-дигидро-4H-1,2,4-триазол-3-он-2-ил] ацетат
ИК (KBr): 2921,6, 1764,5, 1715, 1197,6 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.7 Hz), 1.30 (3H, t, J=7.1 Hz), 1.2-1.4 (10H, m), 1.5-1.7 (2H, m), 2.63 (2H, t, J=7.9 Hz), 4.26 (2H, q, J=7.1 Hz), 4.64 (2H, s), 7.28 (2H, d, J=8.4 Hz), 7.44 (2H, d, J=8.4 Hz), 7.71 (1H, s)
Получение 172
4-[4-(4-трет-Бутоксикарбонилпиперазин-1-ил)фенил)-2-(4- метилпентил)-2,3-дигидро-4H-1,2,4-триазол-3-он
ИК (KBr): 1687,4 см-1
ЯМР (CDCl3, δ): 0.90 (6H, d, J=6.5 Hz), 1.1-1.4 (2H, m), 1.49 (9H, s), 1.4-1.9 (3H, m), 3.16 (4H, t, J=4.9 Hz), 3.59 (4H, t, J= 4.9 Hz), 3.82 (2H, t, J=7.3 Hz), 6.98 (2H, d, J=9.0 Hz), 7.41 (2H, d, J=9.0 Hz), 7.61 (1H, s)
Получение 173
Метил-6-(в-бромоктилокси)-2-нафтоат
ИК (KBr): 2933,2; 2856,1; 1720,2; 1294; 1209,1 см-1
ЯМР (CDCl3, δ): 1.3-1.6 (8H, m), 1.75-2.0 (4H, m), 3.42 (2H, t, J=6.8 Hz), 3.96 (3H, s), 4.09 (2H, t, J=6.5 Hz), 7.14 (1H, d, J=1.7 Hz), 7.19 (1H, dd, J=8.9 and 1.7 Hz), 7.73 (1H, d, J=8.7 Hz), 7.83 (1H, d, J=8.9 Hz), 8.01 (1H, dd, J=8.7 and 1.7 Hz), 8.51 (1H, d, J=1.7 Hz)
АПХИ-МС: m/z = 393 (M++H).
Получение 174
4-[4-(6-н-Пропилоксигексилокси)фенил]бензойная кислота
ИК (KBr): 2937, 2858, 1695, 1683, 1604, 1430, 1290, 1247, 1195 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J=7.4 Hz), 1.3-1.9 (10H, m), 3.2-3.4 (4H, m), 4.01 (2H, t, J=6.3 Hz), 7.04 (2H, d, J=8.7 Hz), 7.67 (2H, d, J=8.7 Hz), 7.74 (2H, d, J=8.3 Hz), 7.98 (2H, d, J=8.3 Hz), 12.9 (1H, s)
АПХИ-МС: m/z = 357 (M+H+).
Получение 175
4-[4-(6-бромгексилокси)фенил]бромбензол
ЯМР (CDCl3, δ): 1.40-1.65 (4H, m), 1.70-2.00 (4H, m), 3.43 (2H, t, J=6.7 Hz), 4.00 (2H, t, J=6.4 Hz), 6.95 (2H, d, J=8.8 Hz), 7.30-7.60 (6H, m)
Нижеследующие соединения (Получения 176-180) были получены способом, описанным в Получении 43.
Получение 176
4-[4-(4-н-Пентилоксифенил)пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1668,1; 1602,6; 1510.0; 1228,4 см-1
ЯМР (DMSO-d8, δ): 0.89 (3H, t, J=6.9 Hz), 1.2-1.5 (5H, m), 1.6-1.9 (2H, m), 3.0-3.2 (4H, m), 3.4-3.6 (4H, m), 3.88 (2H, t, J=6.4 Hz), 6.83 (2H, d, J=9 Hz), 6.9-7.1 (4H, m), 7.79 (2H, d, J=8.8 Hz), 12.32 (1H, s)
АПХИ-МС: m/z = 369 (M+H+).
Получение 177
4-[4-(4-н-Гептилоксифенил)пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1666,2; 1600,6; 1511,9 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.9 Hz), 1.2-2.0 (10H, m), 3.1-3.3 (4H, m), 3.4-3.6 (4H, m), 3.92 (2H, t, J=6.4 Hz), 6.8-7.1 (6H, m), 8.00 (2H, d, J=8.8 Hz)
Получение 178
4-[4-[4-(4-Метилпентиокси)фенил]пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1668,1; 1602,6; 1510,0; 1236,1 см-1
ЯМР (DMSO-d6, δ): 0.89 (6H, d, J=6.5 Hz), 1.2-1.4 (2H, m), 1.4- 1.8 (3H, m), 3.0-3.2 (4H, m), 3.3-3.5 (4H, m), 3.87 (2H, t, J=6.3 Hz), 6.83 (2H, d, J=9.0 Hz), 6.9-7.1 (4H, m), 7.79 (2H, d, J=8.8 Hz), 12.33 (1H, s)
АПХИ-МС: m/z = 383 (M+H+).
Получение 179
4-[4-[4-(8-бромоктилокси)фенил] пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1670,1; 1602,6; 1511,9; 1234,2 см-1
ЯМР (DMSO-d6, δ): 1.2-1.5 (8H, m), 1.6-1.9 (4H, m), 3.0-3.2 (4H, m), 3.2-3.5 (4H, m), 3.52 (2H, t, J=6.7 Hz), 3.88 (2H, 3t, J=6.4 Hz), 6.83 (2H, d, J= 9.1 Hz), 6.94 (2H, d, J=9.1 Hz), 7.02 (2H, d, J=8.9 Hz), 7.79 (2H, d, J=8.9 Hz)
Получение 180
3-Фтор-4-[4-(4-н-гексилоксифенил) пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1673,9; 1511,9; 1240 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J=6.5 Hz), 1.2-1.5 (6H, m), 1.6-1.8 (2H, m), 3.0-3.5 (8H, m), 3.88 (2H, t, J=6.4 Hz), 6.7- 7.2 (5H, m), 7.4-7.8 (2H, m), 12.82 (1H, s)
АПХИ-МС: m/z = 401 (М++Н).
Нижеследующее соединение было получено способом, описанным в Получении 46.
Получение 181
1-(4-Метоксикарбонилфенил)-3-(4-н-гексилоксифенил)пропан- 1,3-дион
ИК (KBr): 2956, 2927, 2856, 1722, 1511, 1284, 1108 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J=6.4 Hz), 1.2-2.0 (8H, m), 3.96 (3H, s), 4.04 (2H, t, J=6.5 Hz), 6.82 (1H, s), 6.97 (2H, d, J=8.7 Hz), 7.9-8.1 (4H, m), 8.14 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 383 (М+H+).
Нижеследующие соединения (Получения 182-185) были получены способом, описанным в Получении 47.
Получение 182
Метил 5- (4-октилоксифенил) -1-метилпиразол-3-карбоксилат
ИК (таблетка KBr): 2923, 1724, 1616, 1513, 1446, 1251, 1120 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.7-1.9 (2H, m), 3.90 (3H, s), 3.98 (2H, t, J=6.6 Hz), 4.20 (3H, s), 6.92 (2H, d, J=8.9 Hz), 7.04 (1H, s), 7.89 (2H, d, J=8.9 Hz)
АПХИ-МС: m/z = 345 (М+H+).
Получение 183
Метил 4-[5-(4-н-пентилоксифенил) пиразол-3-ил] бензоат
ИК (KBr): 3236, 2952, 2873, 1716, 1616, 1508, 1276, 1174, 1106 см-1
ЯМР (CDCl3, δ): 0.94 (3H, t, J=7.0 Hz), 1.3-1.5 (4H, m), 1.7-1.9 (2H, m), 3.92 (3H, s), 3.96 (2H, t, J=6.7 Hz), 6.78 (1H, s), 6.88 (2H, d, J=8.7 Hz), 7.55 (2H, d, J=8.7 Hz), 7.79 (2H, d, J=8.4 Hz), 8.02 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 365 (M+H+).
Получение 184
Метил 5-(4-октилоксифенил)изоксазол-3-карбоксилат
ИК (таблетка KBr): 2950, 2921, 1724, 1614, 1510, 1446, 1257, 1178, 1143, 1009 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 4.0-4.1 (5H, m), 6.80 (1H, s), 6.98 (2H, dd, J=6.9, 2.1 Hz), 7.73 (2H, dd, J=6.9 and 2.1 Hz)
АПХИ-МС: m/z = 332 (M+H+).
Получение 185
Метил 4-[3-(4-н-гексилоксифенил)пиразол-5-ил] бензоат
ИК (KBr): 2952, 1716, 1616, 1508, 1276, 1106 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J=6.3 Hz), 1.2-1.6 (6H, m), 1.7-1.9 (2H, m), 3.8-4.0 (5H, m), 6.76 (1H, s), 6.86 (2H, d, J=8.8 Hz), 7.54 (2H, d, J= 8.8 Hz), 7.77 (2H, d, J=8.4 Hz), 8.00 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 379 (M+H+).
Получение 186
Суспензию, содержащую 1-(4-н-пентилоксифенил)- 3-(4-этоксикарбонилфенил)-1-бутен-3-он (74,43 г), гидрохлорид гидроксиламина (28,23 г) и карбонат калия (56,11 г) в этаноле (400 мл), нагревали с обратным холодильником в течение 4 часов. Полученную смесь разводили этилацетатом, промывали водой (2 раза) и рассолом, а затем осушали сульфатом магния. Растворители удаляли при пониженном давлении, в результате чего получали неочищенный оксим. К раствору неочищенного оксима в дихлорэтане (500 мл) добавляли 200 г оксида марганца (IV). Реакционную смесь нагревали с обратным холодильником в течение 2 часов, а затем фильтровали. Остаток промывали дихлорметаном. После удаления растворителей при пониженном давлении остаток растирали с ацетонитрилом. Образовавшееся твердое вещество собирали путем фильтрации и осушали, в результате чего получали этил 4-[5-(4-н- пентилоксифенил)изоксазол-3-ил] бензоат (21,07 г).
ИК (KBr): 2945, 2872, 1717, 1615, 1508, 1280, 1108 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J=6.9 Hz), 1.3-1.9 (9H, m), 4.01 (2H, t, J= 6.5 Hz), 4.41 (2H, q, J=7.1 Hz), 6.74 (1H, s), 6.99 (2H, d, J=8.8 Hz), 7.76 (2H, d, J=8.8 Hz), 7.93 (2H, d, J=8.4 Hz), 8.15 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 380 (М+H+).
Нижеследующие соединения (Получения 187-190) были получены способом, описанным в Получении 48.
Получение 187
Метил 6-[4-[4-(8-метоксиоктилокси)фенил] пиперазин-1-ил]никотинат
ИК (KBr): 2933, 2858, 1722, 1608, 1513, 1432, 1405, 1278, 1245 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (12H, m), 3.16 (4H, t, J=5.0 Hz), 3.33 (3H, s), 3.36 (2H, t, J=6.5 Hz), 3.8- 4.0 (9H, m), 6.64 (1H, d, J=9.1 Hz), 6.85 (2H, d, J=9.2 Hz), 6.93 (2H, d, J=9.2 Hz), 8.04 (1H, dd, J=9.1 and 2.2 Hz), 8.81 (1H, d, J=2.2 Hz)
АПХИ-МС: m/z = 456 (M+H+).
Получение 188
4-[4-(5-Метоксипентилокси)фенил]бромбензол
ИК (KBr): 2940, 2856, 1604, 1479, 1286, 1255, 1124 см-1
ЯМР (CDCl3, δ): 1.5-1.9 (6H, m), 3.34 (3H, s), 3.41 (2H, t, J=6.1 Hz), 3.99 (2H, t, J=6.4 Hz), 6.95 (2H, d, J=8.7 Hz), 7.4-7.6 (6H, m)
АПХИ-МС: m/z = 349 (M+H+).
Получение 189
Метил 6-(8-метоксиоктилокси)-2-нафтоат
ЯМР (DMSO-d6, δ): 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.20 (3H, s), 3.29 (2H, t, J=6.4 Hz), 3.89 (3H, s), 4.11 (2H, t, J=6.4 Hz), 7.24 (1H, dd, J=9.0 and 2.4 Hz), 7.40 (1H, d, J=2.4 Hz), 7.88 (1H, d, J=8.7 Hz), 7.94 (1H, dd, J=8.7 and 1.5 Hz), 8.03 (1H, d, J=9.0 Hz), 8.55 (1H, d, J=1.5 Hz)
Получение 190
4-[4-[4-(8-Метоксиоктилокси)фенил] пиперазин-1-ил] бензойной кислоты дигидрохлорид
ИК (KBr): 1668,1, 1602,6, 1511,9, 1236,1 см-1
ЯМР (DMSO-d6, δ): 1.2-1.8 (12H, m), 3.05-3.2 (4H, m), 3.29 (2H, t, J=7.1 Hz), 3.33 (3H, s), 3.4-3.55 (4H, m), 3.88 (2H, t, J=6.4 Hz), 6.82 (2H, d, J= 9.0 Hz), 6.94 (2H, d, J=9.0 Hz), 7.02 (2H, d, J=8.8 Hz), 7.79 (2H, d, J=8.8 Hz), 12.31 (1H, s)
Нижеследующие соединения (Получения 191-254) были получены способом, описанным в Получении 49.
Получение 191
1-[4-[4-[4-[2-(4-Метилпентил)-2,3-дигидро-4H-1,2,4-триазол- 3-он-4-ил] фенил]пиперазин-1-ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 1766,5, 1693,2, 1600,6, 1519,6 см-1
Получение 192
1-[4-(4-Октилфенил)-2,3-дигидpo-4H-1,2,4-тpиaзoл-3-он-2-ил- ацетил] бензотриазола 3-оксид
ИК (KBr); 2921,6, 1753,0, 1720,0, 1423,2 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J=6.7 Hz), 1.2-1.4 (10H, m), 1.5-1.8 (2H, m), 2.65 (2H, t, J=7.5 Hz), 5.46 (2H, s), 7.30 (2H, d, J=8.5 Hz), 7.48 (2H, d, J=8.5 Hz), 7.62 (1H, t, J=8.3 Hz), 7.80 (1H, s), 7.82 (1H, t, J=8.3 Hz), 8.05 (1H, d, J=8.3 Hz), 8.37 (1H, d, J=8.3 Hz)
Получение 193
1-[4-[4-[4-(7-Метоксигептилокси)фенил] пиперазин-1-ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 1783,8, 1600,6, 1511,9, 1232,3, 1184,1 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (10H, m), 3.2-3.3 (4H, m), 3,34 (3H, s), 3.38 (2H, t, J=6.4 Hz), 3.5-3.7 (4H, m), 3.92 (2H, t, J=6.5 Hz), 6.87 (2H, d, J= 9.2 Hz), 6.95 (2H, d, J=9.2 Hz), 7.00 (2H, d, J=9.0 Hz), 7.3- 7.6 (3H, m), 8.09 (1H, d, J=8.2 Hz), 8.15 (2H, d, J=9.0 Hz)
Получение 194
1-[4-[4-(4-н-Гептилоксифенил) пиперазин-1-ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 1783,8, 1600,6, 1511,9, 1230,4, 1184,1 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.3 Hz), 1.2-1.6 (8H, m), 1.7-1.9 (2H, m), 3.2-3.3 (4H, m), 3.5-3.7 (4H, m), 3.93 (2H, t, J=6.5 Hz), 6.87 (2H, d, J=9.2 Hz), 6.95 (2H, d, J=9.2 Hz), 7.00 (2H, d, J=9.0 Hz), 7.3- 7.7 (3H, m), 8.09 (1H, d, J=8.2 Hz), 8.15 (2H, d, J=9.0 Hz)
Получение 195
1-[4-[4-[4-(4-Meтилпeнтилoкcи)фенил] пиперазин-1-ил] бензоил] бензотриазола 3-оксид
ЯМР (CDCl3, δ): 0.92 (6H, d, J=6.6 Hz), 1.2-1.4 (2H, m), 1.5-1.9 (3H, m), 3.1-3.3 (4H, m), 3.5-3.7 (4H, m), 3.92 (2H, t, J=6.6 Hz), 6.87 (2H, d, J=9.3 Hz), 6.96 (2H, d, J=9.3 Hz), 7.01 (2H, d, J=9.0 Hz), 7.4- 7.6 (3H, m), 8.10 (1H, d, J=8.2 Hz), 8.15 (2H, d, J=9.0 Hz)
Получение 196
1-[4-[4-(4-н-Пентилоксифенил)пиперазин-1- ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 1787,7, 1600,6, 1511,9, 1232,3, 1184,1 см-1
ЯМР (CDCl3, δ): 0.93 (3H, t, J=6.9 Hz), 1.3-1.6 (4H, m), 1.7-1.9 (2H, m), 3.1-3.4 (4H, m), 3.5-3.8 (4H, m), 3.93 (2H, t, J=6.6 Hz), 6.87 (2H, d, J= 9.2 Hz), 6.92 (2H, d, J=9.2 Hz), 7.01 (2H, d, J=9.1 Hz), 7.4-7.6 (3H, m), 8.10 (1H, d, J=8.2 Hz), 8.15 (2H, d, J=9.1 Hz)
Получение 197
1-[4-[4-[8-(1H-Тетразол-1-ил)октилокси]фенил]бензоил] бензотриазола 3-оксид и
1-[4-[4-[8-(2H-тетразол-2-ил)октилокси] фенил]бензоил]бензотриазола 3-оксид
ИК (KBr): 1778,0, 1602,6, 1189,9, 981,6 см-1
ЯМР (CDCl3, δ): 1.2-1.6 (8H, m), 1.7-1.9 (2H, m), 1.9-2.2 (2H, m), 4.02 (2H, t, J=6.4 Hz), 4.44 and 4.66 (2H, t, J=7.1 Hz), 7.02 (2H, d, J=8.8 Hz), 7.4- 7.6 (3H, m), 7.63 (2H, d, J=8.8 Hz), 7.79 (2H, d, J=8.6 Hz), 8.12 (1H, d, J=8.2 Hz), 8.32 (2H, d, J=8.6 Hz), 8.51 and 8.60 (1H, s)
Получение 198
1-[4-[4-[8-(2,6-Диметилморфолин-4-ил)октилокси]фенил]бензсил] бензотриазола 3-оксид
ИК (KBr): 1778,0, 1600,6, 977,7 см-1
ЯМР (CDCl3, δ): 1.18 (6H, d, J=6.3 Hz), 1.2-1.7 (10H, m), 1.7-2.0 (4H, m), 2.4-2.6 (2H, m), 2.9-3.2 (2H, m), 3.7- 3.9 (2H, m), 4.01 (2H, t, J=6.5 Hz), 7.02 (2H, d, J=8.8 Hz), 7.4-7.7 (3H, m), 7.63 (2H, d, J= 8.8 Hz), 7.79 (2H, d, J=8.5 Hz), 8.12 (1H, d, J=8.1 Hz), 8.32 (2H, d, J=8.5 Hz)
Получение 199
1-[6-[4-(4-Октилоксифенил)пиперазин-1-ил] никотиноил]бензотриазола 3-оксид
ИК (таблетка KBr): 2922, 2854, 1766, 1602, 1513, 1417, 1234, 1025, 950, 813 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.7-1.9 (2H, m), 3.1-3.3 (4H, m), 3.9-4.1 (6H, m), 6.75 (1H, d, J=9.2 Hz), 6.87 (2H, d, J= 9.2 Hz), 6.95 (2H, d, J=9.2 Hz), 7.4-7.6 (3H, m), 8.10 (1H, d, J=8.1 Hz), 8.19 (1H, dd, J=9.2 and 2.4 Hz), 9.04 (1H, d, J=2.4 Hz)
АПХИ-МС: m/z = 529 (M+H+).
Получение 200
1-(2-(4-Гексилоксифенил)бензоксазол-5-ил-карбонил]-бензотриазола 3-оксид
ИК (KBr): 2950, 1774, 1623, 1504, 1265, 1176 см-1
ЯМР (CDCl3, δ): 0.93 (3H, t, J=6.9 Hz), 1.3-1.6 (6H, m), 1.8-2.0 (2H, m), 4.07 (2H, t, J=6.5 Hz), 7.06 (2H, d, J=8.9 Hz), 7.4-7.6 (3H, m), 7.75 (1H, d, J=8.6 Hz), 8.13 (1H, d, J=8.2 Hz), 8.2-8.4 (3H, m), 8.67 (1H, d, J= 1.6 Hz)
АПХИ-МС: m/z = 457 (M+H+).
Получение 201
1-[4-[4-(4-н-Бутилоксифенил)фенил]бензоил]бензотриазола 3-оксид
ИК (KBr): 2958, 2871, 1776, 1600, 1398, 1255, 1211, 1037 см-1
ЯМР (CDCl3, δ): 1.00 (3H, t, J=7.2 Hz), 1.4-1.9 (4H, m), 4.03 (2H, t, J= 6.4 Hz), 7.01 (2H, d, J=8.3 Hz), 7.4-7.8 (9H, m), 7.87 (2H, d, J=8.1 Hz), 8.12 (1H, d, J=8.4 Hz), 8.36 (2H, d, J=7.9 Hz)
АПХИ-МС: m/z = 464 (M+H)+.
Получение 202
1-[2-(4 -Гептилоксифенил)пиридин-5-ил-карбонил]бензотриазола 3-оксид
ИК (KBr): 2944, 2867, 1793, 1770, 1589, 1471, 1321, 1093 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J=6.7 Hz), 1.2-1.6 (8H, m), 1.7-1.9 (2H, m), 4.05 (2H, t, J=6.5 Hz), 7.04 (2H, d, J=8.0 Hz), 7.4-7.6 (3H, m), 7.91 (1H, d, J= 8.5 Hz), 8.1-8.2 (3H, m), 8.51 (1H, dd, J=8.5 and 2.3 Hz), 9.47 (1H, d, J=2.3 Hz)
АПХИ-МС: m/z = 431 (M+H+).
Получение 203
1-[2-(2-Октилоксипиридин-5-ил)бензоксазол-5-ил-карбонил] бензотриазола 3- оксид
ИК (таблетка KBr): 2925, 2854, 1787, 1623, 1479, 1263, 989 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J=6.8 Hz), 1.2-1.5 (10H, m), 1.8-1.9 (2H, m), 4.42 (2H, t, J=6.7 Hz), 6.91 (1H, d, J=8.7 Hz), 6.4-6.6 (3H, m), 7.79 (1H, d, J=8.6 Hz), 8.13 (1H, d, J=8.2 Hz), 8.32 (1H, dd, J=8.6 and 1.7 Hz), 8.41 (1H, dd, J=8.7 and 2.4 Hz), 8.70 (1H, d, J=1.4 Hz), 9.07 (1H, d, J=1.9 Hz)
АПХИ-МС: m/z = 486 (M+H+).
Получение 204
1-[2-[4-(4-Гексилфенил)фенил] бензоксазол-5-ил-карбонил] бензотриазола 3-оксид
ИК (KBr); 2927, 2854, 1785, 1621, 1490, 1261, 1166, 1052 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J=6.5 Hz), 1.2-1.8 (8H, m), 2.68 (2H, t, J= 7.9 Hz), 7.31 (2H, d, J=8.2 Hz), 7.4-7.7 (5H, m), 7.79-7.81 (3H, m), 8.13 (1H, d, J=8.3 Hz), 8.3-8.4 (3H, m), 8.73 (1H, d, J= 1.3 Hz)
АПХИ-МС: m/z = 517 (M+H+).
Получение 205
1-[2-[4-(4-н-бутилоксифенил)фенил] пиридин-5-ил-карбонил] бензотриазола 3-оксид
ИК (KBr): 2956, 2933, 2871, 1774, 1650, 1591, 1471, 1251 см-1
ЯМР (CDCl3, δ): 1.00 (3H, t, J=7.2 Hz), 1.5-1.9 (4H, m), 4.03 (2H, t, J= 6.4 Hz), 7.02 (2H, d, J=8.6 Hz), 7.4-7.6 (3H, m), 7.54 (2H, d, J=7.3 Hz), 7.62 (2H, d, J=8.5 Hz), 8.02 (1H, d, J=8.3 Hz), 8.13 (1H, d, J=8.2 Hz), 8.21 (2H, d, J=7.9 Hz), 8.57 (1H, dd, J=8.3 and 2.0 Hz), 9.54 (1H, d, J=2.0 Hz)
АПХИ-МС: m/z = 465 (M+H)+.
Получение 206
1-[4-[4-(5-Феноксипентилокси)фенил]бензоил]бензотриазола 3-оксид
ИК (KBr): 2944, 2869, 1770, 1600, 1494, 1249, 1189 см-1
ЯМР (CDCl3, δ): 1.6-1.8 (2H, m), 1.8-2.0 (4H, m), 4.01 (2H, t, J=6.3 Hz), 4.07 (2H, t, J=6.2 Hz), 6.91 (2H, d, J=8.9 Hz), 7.04 (2H, d, J=8.7 Hz), 7.3-7.6 (4H, m), 7.63 (2H, d, J=8.6 Hz), 7.78 (2H, d, J=8.4 Hz), 8.12 (1H, d, J=8.1 Hz), 8.32 (2H, d, J=8.4 Hz)
АПХИ-МС: m/z = 494 (M+H)+.
Получение 207
1-[4-[5-(4-Гексилоксифенил)-1,3,4-оксадиазол-2-ил] -бензоил] бензотриазола 3-оксид
ИК (KBr): 2956, 2921, 2856, 1778, 1612, 1496, 1261, 1232, 1025 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J=6.7 Hz), 1.3-1.6 (6H, m), 1.8-2.0 (2H, m), 4.05 (2H, t, J=6.5 Hz), 7.05 (2H, d, J=8.7 Hz), 7.4-7.6 (3H, m), 8.10 (2H, d, J=8.7 Hz), 8.13 (1H, d, J=7.4 Hz), 8.37 (2H, d, J=8.5 Hz), 8.45 (2H, d, J=8.5 Hz)
АПХИ-МС: m/z = 484 (M+H)+.
Получение 208
1-[4-[5-(4-н-Гексилоксифенил)-1,3,4-тиадиазол-2-ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2952, 2873, 1774, 1602, 1261, 1230, 1176 см-1
ЯМР (CDCl3, δ): 0.93 (3H, t, J=6.8 Hz), 1.3-2.0 (8H, m), 4.04 (2H, t, J= 6.5 Hz), 7.02 (2H, d, J=8.7 Hz), 7.4-7.7 (3H, m), 7.98 (2H, d, J=8.7 Hz), 8.13 (1H, d, J=8.7 Hz), 8.25 (2H, d, J=8.3 Hz), 8.41 (2H, d, J=8.3 Hz)
АПХИ-МС: m/z = 500 (M+H)+.
Получение 209
1-[5-(4-Октилоксифенил)-1-метилпиразол-3-ил-карбонил] бензотриазола 3-оксид
ИК (таблетка KBr): 2939, 2852, 1776, 1687, 1612, 1448, 1249, 995 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.7 Hz), 1.3-1.5 (10H, m), 1.7-1.9 (2H, m), 4.01 (2H, t, J = 6.5 Hz), 4.25 (3H, s), 6.97 (2H, d, J = 6.8 Hz), 7.4-7.7 (4H, m), 7.78 (2H, d, J = 6.8 Hz), 8.14 (1H, d, J = 8.0 Hz)
АПХИ-МС: m/z = 448 (M+H)+.
Получение 210
1-[4-[5-(4-н-Пентилоксифенил)пиразол-3-ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 3251, 2956, 2869, 1780, 1612, 1506, 1232, 985 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 6.9 Hz), 1.3-1.6 (4H, m), 1.7-2.0 (2H, m), 4.01 (2H, t, J = 6.6 Hz), 6.90 (1H, s), 6.99 (2H, d, J = 8.7 Hz), 7.4-7.6 (5H, m), 8.0-8.2 (3H, m), 8.33 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 468 (M+H+).
Получение 211
1-[5-[4-(4-н-бутоксифенил)фенил] фуран-2-ил-карбонил] бензотриазола 3-оксид
ИК (KBr): 2958, 2871, 1781, 1678, 1603, 1535, 1479, 1265 см-1
ЯМР (CDCl3, δ ): 1.00 (3H, t, J = 7.3 Hz), 1.4-1.9 (4H, m), 4.02 (2H, t, J = 6.4 Hz), 6.9-7.1 (3H, m), 7.4-8.2 (11H, m)
АПХИ-МС: m/z = 351 (метиловый эфир).
Получение 212
1-(3-(S)-Гидрокси-2-бензилгексадеканоил)бензотриазола 3-оксид
ИК (чистый): 2854,1, 1814,7, 1459,8, 742,5 см-1
Получение 213
1-(3-(R)-Бензилоксикарбоксиламино-18-метоксиоктадеканоил)бензотриазола 3-оксид
ИК (KBr): 1805,0, 1729,8, 1695,1 см-1
ЯМР (DMSO-d6, δ): 1.1-1.65 (30H, m), 3.20 (3H, s), 3.28 (2H, t, J = 6.5 Hz), 4.01 (1H, m), 5.06 (2H, s), 7.32 (5H, m), 7.4-7.8 (3H, m), 8.12 (1H, d, J = 7 Hz)
Получение 214
1-(3-(S)-Гидроксигексадеканоил)бензотриазола 3-оксид
ИК (KBr): 1710,6, 1498,4, 1429,0, 771,4 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.4 Hz), 1.2-1.7 (24H, m), 2.00 (1H, s), 3.1-3.5 (2H, m), 4.30 (1H, m), 7.59 (1H, t, J = 7.8 Hz), 7.81 (1H, t, J = 7.8 Hz), 8.02 (1H, d, J = 8.3 Hz), 8.42 (1H, d, J = 8.3 Hz)
Получение 215
1-(3-Метил-2-тридеценоил)бензотриазола 3-оксид
ИК (KBr): 2927,4, 1791,5, 1633,4, 1081,9 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.3 Hz), 1.1-1.7 (20H, m), 2.25 (3H, s), 6.08 (1H, s), 7.3-7.6 (3H, m), 8.06 (1H, d, J = 8.2 Hz)
Получение 216
1-[4-[4-[4-(8-Метоксиоктилокси)фенил] пиперазин-1- ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 1780,0, 1600,6, 1511,9, 1234,2, 1184,1 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (12H, m), 3.24 (4H, t, J = 5.0 Hz), 3.33 (3H, s), 3.37 (2H, t, J = 6.8 Hz), 3.62 (4H, t, J = 5.0 Hz), 3.92 (2H, t, J = 6.5 Hz), 6.8-7.1 (6H, m), 7.35-7.65 (3H, m), 8.09 (1H, d, J = 8.2 Hz), 8.15 (2H, d, J = 9.0 Hz)
Получение 217
1-[3-Фтор-4-[4-(4-н-гексилоксифенил)пиперазин-1- ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 1778,0 см-1
Получение 218
1-[3-Хлор-4-[4-(4-н-гексилоксифенил)пиперазин-1- ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 1778,0, 1594,8, 1511.9, 1218,8 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J = 6.5 Hz), 1.2-1.6 (6H, m), 1.6-1.9 (2H, m), 3.29 (4H, t, J = 3.6 Hz), 3.44 (4H, t, J = 3.6 Hz), 3.93 (2H, t, J = 6.5 Hz), 6.87 (2H, d, J = 9.2 Hz), 6.97 (2H, d, J = 9.2 Hz), 7.19 (1H, d, J = 8.6 Hz), 7.4-7.7 (3H, m), 8.10 (1H, d, J = 6.4 Hz), 8.14 (1H, dd, J = 8.6 and 2.1 Hz), 8.27 (1H, d, J = 2.1 Hz)
АПХИ-МС: m/z = 534 (M++H).
Получение 219
1-[4-(4-Пиперидинопиперидин-1-ил)бензоил]бензотриазола 3-оксид
ИК (KBr): 1758,8, 1602,6, 1186,0 см-1
ЯМР (CDCl3, δ): 1.35-1.8 (8H, m), 1.96 (2H, d, J = 13 Hz), 2.45-2.7 (5H, m), 2.97 (2H, td, J = 12.8, 2.6 Hz), 4.04 (2H, d, J = 13 Hz), 6.93 (2H, d, J = 9.2 Hz), 7.35-7.6 (3H, m), 8.1-8.4 (3H, m)
Получение 220
1-[3-[4-(4-н-Гексилоксифенил)пиперазин-1-ил] пиридазин-6-ил- карбонил] бензотриазола 3-оксид
ИК (KBr): 1787,7, 1585,2, 1511,9, 1240,0 см-1
Получение 221
1-[5-[4-(4-н-Гексилоксифенил)пиперазин-1-ил] пиколиноил] бензотриазола 3-оксид
ИК (KBr): 1766,5, 1575,6, 1511,9, 1232,3 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J = 6.5 Hz), 1.2-1.6 (6H, m), 1.65-1.9 (2H, m), 3.27 (4H, t, J = 5.1 Hz), 3.66 (4H, t, J = 5.1 Hz), 3.93 (2H, t, J = 6.5 Hz), 6.88 (2H, d, J = 9.2 Hz), 6.95 (2H, d, J = 9.2 Hz), 7.25 (1H, dd, J = 7.6 and 2.9 Hz), 7.35-7.6 (3H, m), 8.09 (1H, d, J = 8.2 Hz), 8.18 (1H, d, J = 8.9 Hz), 8.52 (1H, d, J = 2.9 Hz)
АПХИ-МС: m/z = 501 (M++H).
Получение 222
1-[4-[4-(4-Циклогексилфенил)пиперазин-1-ил)бензоил]бензотриазола 3-оксид
ИК (KBr): 1770,3, 1602,6, 1515,8, 1232,3, 1186,0 см-1
ЯМР (CDCl3, δ): 1.15-1.5 (6H, m), 1.65-2.0 (4H, m), 2.45 (1H, m), 3.33 (4H, t, J = 5.1 Hz), 3.62 (4H, t, J = 5.1 Hz), 6.92 (2H, d, J = 8.7 Hz), 6.99 (2H, d, J = 9.2 Hz), 7.16 (2H, d, J = 8.7 Hz), 7.35-7.65 (3H, m), 8.09 (1H, d, J = 8.2 Hz), 8.15 (2H, d, J = 9.2 Hz)
Получение 223
1-[4-[4-(4-н-Гексилфенил)пиперазин-1-ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 1768,4, 1602,6, 1515,8, 1230,4, 1184,1 см-1
ЯМР (CDCl3, δ ): 0.89 (3H, t, J = 6.5 Hz), 1.2-1.45 (6H, m), 1.5-1.7 (2H, m), 2.55 (2H, t, J = 7.6 Hz), 3.2-3.4 (4H, m), 3.5-3.7 (4H, m), 6.91 (2H, d, J = 8.6 Hz), 7.00 (2H, d, J = 9.1 Hz), 7.13 (2H, d, J = 8.5 Hz), 7.35-7.6 (3H, m), 8.09 (1H, d, J = 8.2 Hz), 8.15 (2H, d, J = 9.1 Hz)
Получение 224
1-[4-[4-(4-Фенилциклогексил)пиперазин-1-ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 1780,0, 1762,6, 1602,6, 1234,2, 1182,2 см-1
ЯМР (CDCl3, δ): 1.3-1.7 (4H, m), 1.95-2.15 (4H, m), 2.35-2.6 (2H, m), 2.79 (4H, t, J = 5.0 Hz), 3.49 (4H, t, J = 5.0 Hz), 6.95 (2H, d, J = 9.0 Hz), 7.1-7.35 (5H, m), 7.35-7.6 (3H, m), 8.08 (1H, d, J = 7.1 Hz), 8.12 (2H, d, J = 9.0 Hz)
Получение 225
1-[4-[4-[1-(4-н-Гексилоксифенил)пиперидин-4-ил] пиперазин-1- ил]бензоил] бензотриазола 3-оксид
ИК (KBr): 1768,4, 1602,6, 1511,9, 1234,2 см-1
ЯМР (CDCl3, δ ): 0.90 (3H, t, J = 6.5 Hz), 1.2-1.55 (6H, m), 1.6-1.9 (4H, m), 1.96 (2H, d, J = 11 Hz), 2.44 (1H, m), 2.64 (2H, d, J = 1.1 Hz), 2.77 (4H, t, J = 5.0 Hz), 3.48 (4H, t, J = 5.0 Hz), 3.59 (2H, d, J = 11 Hz), 3.91 (2H, t, J = 6.5 Hz), 6.7-7.05 (6H, m), 7.35-7.6 (3H, m), 8.08 (1H, d, J = 6.9 Hz), 8.12 (2H, d, J = 7.7 Hz)
Получение 226
1-[4-(4-Транс-н-пентилциклогексил)бензоил]бензотриазола 3-оксид
ИК (KBr): 1799,3, 1778,0, 1608,3, 1228,4, 977,7 см-1
ЯМР (CDCl3, δ ): 0.91 (3H, t, J = 6.6 Hz), 1.0-1.7 (13H, m), 1.93 (4H, d, J = 9.8 Hz), 2.62 (1H, t, J = 12 Hz), 7.35-7.6 (5H, m), 8.09 (1H, d, J = 7.9 Hz), 8.19 (2H, d, J = 8.4 Hz)
Получение 227
1-(6-(8-Метоксиоктилокси)-2-нафтоил]бензотриазола 3-оксид
ИК (KBr): 2931,3, 2856,1, 1778,0, 1623,8 см-1
Получение 228
1-(E)-[3-[4-[4-(7-Фторгептилокси)фенил] фенил]акрилоил]бензотриазола 3-оксид
ИК (KBr): 3070,1, 2935,1, 2859,9, 1700,9, 1619,9, 1596,8 см-1
ЯМР (CDCl3, δ): 1.30-2.00 (10H, m), 4.02 (2H, t, J = 6.4 Hz), 4.45 (2H, dt, J = 47.5 and 6.2 Hz), 6.70-8.65 (14H, m)
Получение 229
1-(6-Гептилнафталин-2-карбонил)бензотриазола 3-оксид
ЯМР (DMSO-d6, δ): 0.75-0.93 (3H, m), 1.10-1.45 (8H, m), 1.55-1.80 (2H, m), 2.68-2.90 (2H, m), 7.35-9.06 (10H, m)
АПХИ-МС: m/z = 388 (M++1).
Получение 230
1-(E)-[3-[4-[4-(8-Метоксиоктилокси)фенил] фенил] акрилоил] бензотриазола 3-оксид
Получение 231
1-(E)-[3-[4-[4-(5-гексенилокси)фенил] фенил] акрилоил] бензотриазола 3-оксид
ИК (KBr): 3072,0, 3033,5, 2939,0, 2865,7, 1780,0, 1693,2, 1619,9, 1596,8 см-1
ЯМР (DMSO-d6, δ): 1.43-1.66 (2H, m), 1.66-1.90 (2H, m), 2.02-2.23 (2H, m), 3.90-4.16 (2H, m), 4.90-5.13 (2H, m), 5.72-6.00 (1H, m), 6.93-8.30 (14H, m)
АПХИ-МС: m/z = 337 (метиловый эфир, M++1).
Получение 232
1-(E)-[3-[4-[4-(4-Метилпентилокси)фенил] фенил] акрилоил] бензотриазола 3-оксид
ИК (KBr): 3072,0, 3033,5, 2952,5, 2869,6, 1780,0, 1693,2, 1618,0, 1598,7 см-1
ЯМР (DMSO-d6, δ): 0.90 (6H, d, J = 6.5 Hz), 1.20-1.40 (2H, m), 1.50-1.90 (3H, m), 3.90-4.10 (2H, m), 6.40-8.30 (14H, m)
АПХИ-МС: m/z = 442 (M++1).
Получение 233
1-(E)-[3-[4-[4-(6-Фторгексилокси)фенил] фенил] акрилоил] бензотриазола 3 -оксид
ИК (KBr): 3074,0, 3033,5, 2939,0, 2865,7, 1780,0, 1697,1, 1598,7 см-1
ЯМР (DMSO-d6, δ): 1.25-1.83 (6H, m), 4.04 (2H, t, J = 6.5 Hz), 4.45 (2H, dt, J = 47.5 and 6.5 Hz), 6.9-8.3 (14H, m)
АПХИ-МС: m/z = 460 (M++1).
Получение 234
1-(E)-[3-[4-[4-(6-Метоксигексилокси)фенил] фенил] акрилоил]бензотриазола 3-оксид
ЯМР (DMSO-d6, δ): 1.30-1.65 (6H, m), 1.65-1.90 (2H, m), 3.22 (3H, s), 3.22-3.40 (2H, m), 4.02 (2H, t, J = 6.5 Hz), 6.5-8.3 (14H, m)
Получение 235
1-[4-[3-(4-н-гексилоксифенил)пиразол-5-ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 2935, 1780, 1610, 1506, 1249, 1232, 1178, 1087 см-1
ЯМР (CDCl3, δ): 0.91 (3H, d, J = 6.4 Hz), 1.2-1.6 (6H, m), 1.7-1.9 (2H, m), 3.98 (2H, t, J = 6.5 Hz), 6.8-7.0 (3H, m), 7.4-7.6 (5H, m), 8.00 (2H, d, J = 8.4 Hz), 8.10 (1H, d, J = 8.1 Hz), 8.28 (1H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 482 (M+H+).
Получение 236
1-[4-[4-[4-(6-Метоксигексилокси)фенил] фенил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2935, 2858, 1774, 1600, 1490, 1257, 1211 см-1
ЯМР (CDCl3, δ): 1.4-1.9 (8H, m), 3.35 (3H, s), 3.40 (2H, t, J = 6.3 Hz), 4.02 (21H, t, J = 6.4 Hz), 7.00 (2H, d, J = 8.7 Hz), 7.4-7.8 (7H, m), 7.87 (2H, d, J = 8.4 Hz), 8.12 (1H, d, J = 8.2 Hz), 8.36 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 522 (M+H+).
Получение 237
1-[4-[5-[4-(8-Метоксиоктилокси)фенил] -1,3,4-тиадиазол-2- ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2929, 2854, 1776, 1602, 1469, 1255 см-1
ЯМР (CDCl3, δ): 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.33 (3H, s), 3.37 (2H, d, J = 6.4 Hz), 4.03 (2H, d, J = 6.5 Hz), 7.00 (2H, d, J = 8.9 Hz), 7.4-7.6 (3H, m), 7.97 (2H, d, J = 8.9 Hz), 8.12 (1H, d, J = 8.2 Hz), 8.23 (2H, d, J = 8.7 Hz), 8.39 (2H, d, J = 8.7 Hz)
АПХИ-МС: m/z = 558 (M+H+).
Получение 238
1-[4-(4-н-Бутоксифенил)циннамоил]бензотриазола 3-оксид
ИК (KBr): 2952, 2867, 1778, 1598, 1496, 1249, 1186 см-1
ЯМР (CDCl3, δ): 0.99 (3H, t, J = 7.3 Hz), 1.55 (2H, tq, J = 7.0 and 7.3 Hz), 1.78 (2H, tt, J = 7.0 and 6.4 Hz), 4.02 (2H, t, J = 6.4 Hz), 6.75 (1H, d, J = 16.0 Hz), 7.00 (2H, d, J = 8.7 Hz), 7.4-8.2 (9H, m)
АПХИ-МС: m/z = 414 (M+H+).
Получение 239
1-[4-[5-(4-Циклогексилфенил)-1,3,4-тиадиазол-2-ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 2925, 2850, 1778, 1230, 989 см-1
ЯМР (CDCl3, δ): 1.2-1.6 (5H, m), 1.7-2.0 (5H, m), 2.5-2.7 (1H, m), 7.37 (2H, d, J = 8.3 Hz), 7.4-7.6 (3H, m), 7.97 (2H, d, J = 8.3 Hz), 8.13 (1H, d, J = 8.2 Hz), 8.26 (2H, d, J = 8.6 Hz), 8.42 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 482 (M+H)+.
Получение 240
1-[4-[5-[4-(4-н-Пропилоксифенил)фенил] -1,3,4-оксадиазол-2- ил]бензоил] бензотриазола 3-оксид
ИК (KBr): 1778, 1604, 1488, 1249, 1232, 998 см-1
ЯМР (CDCl3, δ): 1.07 (3H, t, J = 7.4 Hz), 1.85 (2H, tq, J = 6.5, 7.4 Hz), 7.02 (2H, d, J = 8.8 Hz), 7.4-7.7 (3H, m), 7.61 (2H, d, J = 8.8 Hz), 7.75 (2H, d, J = 8.5 Hz), 8.14 (1H, d, J = 8.2 Hz), 8.22 (2H, d, J = 8.5 Hz), 8.40 (2H, d, J = 8.8 Hz), 8.48 (2H, d, J = 8.8 Hz)
АПХИ-МС: m/z = 518 (M+H)+.
Получение 241
1-[4-(5-н-Нонил-1,3,4-оксадиазол-2-ил)бензоил]бензотриазола 3-оксид
ИК (KBr): 2919, 2850, 1780, 1565, 1415, 1251 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.7 Hz), 1.2-1.6 (12H, m), 1.8-2.0 (2H, m), 2.98 (2H, t, J = 7.7 Hz), 7.4-7.6 (3H, m), 8.12 (1H, d, J = 9.0 Hz), 8.28 (2H, d, J = 8.7 Hz), 8.42 (2H, d, J = 8.7 Hz)
АПХИ-МС: m/z = 434 (M+H+).
Получение 242
1-[4-[3-(4-н-Гексилоксифенил)-1,2,4-оксадиазол-5- ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 2946, 2869, 1780, 1251, 1230, 1001 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J = 6.8 Hz), 1.3-1.6 (6H, m), 1.8-1.9 (2H, m), 4.04 (2K, t, J = 6.5 Hz), 7.03 (2H, d, J = 8.9 Hz), 7.4-7.6 (3H, m), 8.0-8.2 (3H, m), 8.46 (4H, s)
АПХИ-МС: m/z = 484 (M+H+).
Получение 243
1-[4-[5-(4-н-Октилоксифенил)-1,3,4-тиадиазол-2-ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 2925, 2856, 1774, 1602, 1259, 1232, 989 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.7 Hz), 1.1-1.6 (10H, m), 1.7-1.9 (2H, m), 4.04 (2H, t, J = 6.5 Hz), 7.01 (2H, d, J = 8.9 Hz), 7.4-7.6 (3H, m), 7.97 (2H, d, J = 8.8 Hz), 8.12 (1H, d, J = 8.2 Hz), 8.24 (2H, d, J = 8.6 Hz), 8.40 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 528 (M+H+).
Получение 244
1-[4-[5-(4-Транс-н-пентилциклогексил)-1,3,4-тиадиазол-2- ил]бензоил]бензотриазола 3-оксид
ИК (KBr): 2952, 2919, 2848, 1785, 1444, 1226, 991 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.9 Hz), 1.0-1.7 (13H, m), 1,94 (2H, d, J = 12.0 Hz), 2.27 (2H, d, J = 12.0 Hz), 3.19 (1H, tt, J = 12.0 and 3.6 Hz), 7.4-7.6 (3H, m), 8.12 (1H, d, J = 8.0 Hz), 8.19 (2H, d, J = 8.6 Hz), 8.38 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 476 (M+H+).
Получение 245
1-[4-[3-(4-н-Пентилоксифенил)изоксазол-5-ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2948, 2867, 1776, 1610, 1436, 1253, 1002 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 7.1 Hz), 1.2-1.6 (4H, m), 1.7-1.9 (2H, m), 4.02 (2H, t, J = 6.5 Hz), 7.0-7.1 (3H, m), 7.4-7.6 (3H, m), 7.81 (2H, d, J = 8.8 Hz), 8.06 (2H, d, J = 8.6 Hz), 8.12 (1H, d, J = 8.0 Hz), 8.39 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 469 (M+H+).
Получение 246
1-[4-[5-[4-(8-Метоксиоктилокси)фенил] -1,3,4-оксадиазол-2- ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2923, 2854, 1787, 1608, 1494, 1255, 1228, 993 см-1
ЯМР (CDCl3, δ): 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.34 (3H, s), 3.38 (2H, t, J = 6.4 Hz), 4.05 (2H, t, J = 6.5 Hz), 7.04 (2H, d, J = 8.8 Hz), 7.4-7.6 (3H, s), 8.1-8.2 (3H, s), 8.36 (2H, d, J = 8.7 Hz), 8.45 (2H, d, J = 8.7 Hz)
АПХИ-МС: m/z = 542 (M+H+).
Получение 247
1-[4-[4-(6-Фенилпиридазин-3-ил-окси)фенил]бензоил]бензотриазола 3-оксид
ИК (KBr): 1783, 1604, 1423, 1284, 985 см-1
ЯМР (CDCl3, δ): 7.2-8.2 (15H, m), 8.12 (2H, d, J = 8.3 Hz), 8.36 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 486 (M++1).
Получение 248
1-[4-[5-(4-н-Октилоксифенил)-1,3,4-оксадиазол-2- ил] бензоил]бензотриазола 3-оксид
ИК (KBr): 2925, 2854, 1780, 1610, 1496, 1257, 1228, 1180 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.8 Hz), 1.2-2.0 (12H, m), 4.05 (2H, t, J = 6.5 Hz), 7.05 (2H, d, J = 8.7 Hz), 7.4-7.6 (3H, m), 8.0-8.2 (3H, m), 8.37 (2H, d, J = 8.6 Hz), 8.45 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 512 (M+H+).
Получение 249
1-[4-[2-(4-н-Гексилоксифенил)пиримидин-6-ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2948, 2861, 1780, 1552, 1413, 1378, 987 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J = 6.8 Hz), 1.2-1.6 (6H, m), 1.8-2.0 (2H, m), 4.06 (2H, t, J = 6.5 Hz), 7.04 (2H, d, J = 9.0 Hz), 7.4-7.6 (3H, m), 7.64 (1H, d, J = 5.2 Hz), 8.13 (1H, d, J = 8.2 Hz), 8.44 (4H, s), 8.55 (2H, d, J = 9.0 Hz), 8.90 (1H, d, J = 5.2 Hz)
АПХИ-МС: m/z = 494 (M+H+).
Получение 250
1-[4-[4-[8-(2-Этоксиэтокси)октилокси]фенил]бензоил]бензотриазола 3-оксид
ИК (KBr): 2933, 2861, 1778, 1598, 1247, 1186, 977 см-1
ЯМР (CDCl3, δ): 1.22 (3H, t, J = 7.0 Hz), 1.3-2.0 (14H, m), 3.4-3.6 (6H, m), 4.02 (2H, t, J = 6.5 Hz), 7.02 (2H, d, J = 8.8 Hz), 7.4-7.6 (3H, m), 7.62 (2H, d, J = 8.8 Hz), 7.78 (2H, d, J = 8.6 Hz), 8.10 (1H, d, J = 8.9 Hz), 8.31 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 532 (M+H+).
Получение 251
1-[4-[4-[7-(Пиперидин-1-ил-карбонил)гептилокси]фенил]бензоил] бензотриазола 3-оксид
ИК (KBr): 2935, 2856, 1774, 1631, 1598, 1255, 1191 см-1
ЯМР (CDCl3, δ): 1.3-2.0 (16H, m), 2.37 (2H, t, J = 7.6 Hz), 3.48 (4H, s), 4.02 (2H, t, J = 6.4 Hz), 7.02 (2H, d, J = 8.6 Hz), 7.4-7.6 (3H, m), 7.63 (2H, d, J = 8.6 Hz), 7.78 (2H, d, J = 8.3 Hz), 8.11 (1H, d, J = 8.1 Hz), 8.31 (2H, d, J = 8.3 Hz)
АПХИ-МС: m/z = 541 (M+H+).
Получение 252
1-[6-[4-(4-н-Гептилоксифенил)пиперазин-1-ил] никотиноил] бензотриазола 3-оксид
ИК (KBr); 2929, 2856, 1762, 1604, 1510, 1240 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.7 Hz), 1.2-1.9 (10H, m), 3.20 (4H, t, J = 5.0 Hz), 3.8-4.0 (6H, m), 6.75 (1H, d, J = 9.5 Hz), 6.86 (2H, d, J = 9.3 Hz), 6.95 (2H, d, J = 9.3 Hz), 7.3-7.6 (3H, m), 8.10 (1H, d, J = 8.2 Hz), 8.19 (1H, dd, J = 9.2 and 2.3 Hz), 9.05 (1H, d, J = 2.3 Hz)
АПХИ-МС: m/z = 515 (M+H+).
Получение 253
1-[6-[4-[4-(8-Метоксиоктилокси)фенил] пиперазин-1- ил]никотиноил]бензотриазола 3-оксид
ИК (KBr): 2929, 2854, 1766, 1602, 1510, 1419, 1234 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (12H, m), 3.2-3.3 (4H, m), 3.33 (3H, s), 3.36 (2H, t, J = 6.4 Hz), 3.92 (2H, t, J = 6.5 Hz), 4.0-4.2 (4H, m), 6.75 (1H, d, J = 9.1 Hz), 6.87 (2H, d, J = 8.9 Hz), 7.0-7.2 (2H, m), 7.4-7.6 (3H, m), 8.09 (1H, d, J = 8.1 Hz), 8.20 (1H, dd, J = 9.1 and 2.3 Hz), 9.05 (1H, d, J = 2.3 Hz)
АПХИ-МС: m/z = 559 (M+H+).
Получение 254
1-[4-[5-[4-(4-н-Пропилоксифенил)фенил] -1,3,4-тиадиазол-2- ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 1774, 1600, 1234, 985 см-1
ЯМР (CDCl3, δ): 1.07 (3H, t, J = 7.3 Hz), 1.85 (2H, tq, J = 6.5, 7.3 Hz), 3.99 (2H, t, J = 6.5 Hz), 7.01 (2H, d, J = 8.7 Hz), 7.4-7.7 (5H, m), 7.72 (2H, d, J = 8.7 Hz), 8.1-8.2 (2H, m), 8.28 (2H, d, J = 8.6 Hz), 8.44 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 534 (M+H)+.
Нижеследующие соединения (Получения 255-256) были получены способом, описанным в Получении 32.
Получение 255
6-Гептилнафталин-2-карбоновая кислота
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.6 Hz), 1.15-1.53 (8H, m), 1.58-1.88 (2H, m), 2.80 (2H, t, J = 7.6 Hz), 7.42 (1H, dd, J = 1.7 and 8.4 Hz), 7.67 (1H, s), 7.84 (1H, d, J = 8.6 Hz), 7.90 (1H, d, J = 8.4 Hz), 8.09 (1H, dd, J = 1.7 and 8.6 Hz), 8.68 (1H, s)
АПХИ-МС: m/z = 271 (M++1), 285 (метиловый эфир+-1).
Получение 256
3-(E)-[4-[4-(7-Фторгептилокси)фенил]фенил]акриловая кислота
ИК (KBr): 3037,3, 2935,1, 2861,8, 1679,7, 1633,4, 1600,6 см-1
ЯМР (DMSO-d6, δ ): 1.30-1.85 (10H, m), 4.01 (2H, t, J = 6.4 Hz), 4.44 (2H, dt, J = 47.6 and 6.1 Hz), 6.54 (1H, d, J = 15.9 Hz), 7.02 (2H, d, J = 8.7 Hz), 7.53-7.80 (7H, m)
Получение 257
К раствору 4-метилпентанола (3,0 мл) в пиридине (20 мл) добавляли по очереди, при комнатной температуре, п-толуолсульфонилхлорид (4,6 г) и 4-N, N-диметиламинопиридин (1,5 г). После размешивания при комнатной температуре, реакционную смесь растворяли в смеси этилацетата (100 мл) и воды (100 мл). Выделенный органический слой промывали по очереди соляной кислотой (1 н.), водой, водным раствором бикарбоната натрия и затем осушали сульфатом магния. После выпаривания получали 1-п-толуолсульфонилокси-4-метилпентан (5,30 г).
ЯМР (CDCl3, δ): 0.83 (6H, d, J = 6.6 Hz), 1.48 (1H, sept, J = 6.6 Hz), 1.50-1.70 (2H, m), 2.45 (3H, s), 4.00 (2H, t, J = 6.6 Hz), 7.34 (2H, d, J = 8.1 Hz), 7.79 (2H, d, J = 8.1 Hz)
АПХИ-МС: m/z = 257 (M++1).
Получение 258
К раствору 4-бром-4'-н-бутилоксибифенила (3,05 г) в тетрагидрофуране (60 мл), в течение 10 минут при -60oC добавляли 1,55 М н-бутиллития в н-гексане (7,74 мл). Полученный раствор размешивали в течение 1,5 часов при -30oC, а затем охлаждали до -60oC. После этого в течение 5 минут к раствору добавляли триизопропилборат (3,46 мл) и полученную смесь размешивали в течение 1,5 часов без охлаждения. К раствору добавляли 1 н. соляную кислоту (20 мл) и раствор размешивали в течение 30 минут, а затем экстрагировали этилацетатом.
Органический слой отделяли и промывали водой, рассолом и осушали сульфатом магния. Растворители удаляли при пониженном давлении и остаток растирали с н-гексаном. Твердое вещество собирали путем фильтрации и осушали при пониженном давлении, в результате чего получали 4-(4-н-бутилоксифенил)фенилбороновую кислоту (2,31 г).
ИК (KBr): 3398, 2956, 2919, 2871, 1604, 1531, 1392, 1257 см-1
ЯМР (DMSO-d6, δ): 0.94 (3H, t, J = 7.3 Hz), 1.4-1.8 (4H, m), 4.01 (2H, t, J = 6.3 Hz), 7.01 (2H, d, J = 8.7 Hz), 7.58 (2H, d, J = 7.9 Hz), 7.62 (2H, d, J = 8.7 Hz), 7.84 (2H, d, J = 7.9 Hz), 8.03 (2H, s)
Нижеследующие соединения (Получения 259-260) были получены способом, описанным в Получении 258.
Получение 259
4-[4-(6-Метоксигексилокси)фенил]фенилбороновая кислота
ИК (KBr): 3448, 3392, 2937, 2861, 1606, 1529, 1346, 1288 см-1
ЯМР (DMSO-d6, δ): 1.3-1.8 (8H, m), 3.21 (3H, s), 3.31 (2H, t, J = 6.3 Hz), 3.99 (2H, t, J = 6.4 Hz), 7.00 (2H, d, J = 8.7 Hz), 7.5-7.7 (4H, m), 7.84 (2H, d, J = 8.1 Hz), 8.03 (2H, s)
АПХИ-МС: m/z = 329 (M+H+).
Получение 260
4-[4-(5-Метоксипентилокси)фенил]фенилбороновая кислота
ИК (KBr): 3473, 3369, 3330, 2935, 2863, 1604, 1531, 1338, 1251 см-1
ЯМР (DMSO-d6, δ): 1.4-1.8 (6H, m), 3.22 (3H, S), 3.3-3.4 (2H, m), 3.99 (2H, t, J = 6.4 Hz), 7.00 (2H, d, J = 8.7 Hz), 7.58 (2H, d, J = 8.0 Hz), 7.61 (2H, d, J = 8.7 Hz), 7.84 (2H, d, J = 8.0 Hz), 8.04 (2H, s)
АПХИ-МС: m/z = 315 (M+H+).
Получение 261
К суспензии 4-метоксикарбонилфенилбороновой кислоты (648 мг), 4-йод-1-гептилпиразола (876 мг) и Pd(PPh3)4 (173 мг) в 1,2-диметоксиэтане (10 мл) добавляли 2 М Na2CO3 вод. (3,6 мл). Реакционную смесь размешивали 2 часа при 80oC в атмосфере азота, а затем выливали в воду со льдом и экстрагировали этилацетатом. Органический слой промывали рассолом и осушали сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток подвергали колоночной хроматографии на силикагеле 60 (Merk) и элюировали смесью н-гексана и этилацетата (80:20). Фракции, содержащие целевое соединение, объединяли и выпаривали при пониженном давлении, в результате чего получали 1-гептил-4-(4-метоксикарбонилфенил)пиразол (0,20 г).
ИК (таблетка KBr): 2952, 2920, 2848, 1712, 1610, 1288, 1114, 769 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.7 Hz), 1.1-1.4 (8H, m), 1.7-1.9 (2H, m), 3.85 (3H, s), 4.11 (2H, t, J = 7.0 Hz), 7.72 (2H, d, J = 8.5 Hz), 7.93 (2H, d, J = 8.5 Hz), 7.99 (1H, s), 8.34 (1H, s)
АПХИ-МС: m/z = 301 (M+H+).
Нижеследующие соединения (Получения 262-268) были получены способом, описанным в Получении 261.
Получение 262
Этил 4-[4-(4-н-бутилоксифенил)фенил]бензоат
ИК (KBr): 2958, 2935, 2871, 1714, 1602, 1396, 1280, 1108 см-1
ЯМР (CDCl3, δ): 0.99 (3H, t, J = 7.3 Hz), 1.4-2.0 (7H, m), 4.02 (2H, t, J = 6.4 Hz), 4.40 (2H, q, J = 7.1 Hz), 6.98 (2H, d, J = 6.8 Hz), 7.56 (2H, d, J = 6.8 Hz), 7.66 (4H, s), 7.68 (2H, d, J = 8.4 Hz), 8.12 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 375 (M+H)+.
Получение 263
Метил 6-(4-гептилоксифенил)никотинат
ИК (KBr): 2954, 2859, 1724, 1597, 1288, 1251, 1116, 783 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.6 Hz), 1.2-1.5 (8H, m), 1.7-1.9 (2H, m), 3.96 (3H, s), 4.03 (2H, t, J = 6.5 Hz), 7.00 (2H, d, J = 8.8 Hz), 7.75 (1H, d, J = 8.4 Hz), 8.02 (1H, d, J = 8.8 Hz), 8.30 (1H, dd, J = 8.4 and 2.2 Hz), 9.23 (1H, d, J = 2.2 Hz)
АПХИ-МС: m/z = 328 (M+H+).
Получение 264
Метил 6-[4-(4-н-бутилоксифенил)фенил]никотинат
ИК (KBr): 2956, 2933, 2871, 1724, 1598, 1282, 1118 см-1
ЯМР (CDCl3, δ): 1.00 (3H, t, J = 7.3 Hz), 1.4-1.9 (4H, m), 3.98 (3H, s), 4.02 (2H, t, J = 6.4 Hz), 7.00 (2H, d, J = 8.8 Hz), 7.59 (2H, d, J = 8.8 Hz), 7.70 (2H, d, J = 8.5 Hz), 7.86 (1H, d, J = 8.8 Hz), 8.13 (2H, d, J = 8.5 Hz), 8.37 (1H, dd, J = 8.8 and 1.6 Hz), 9.30 (1H, d, J = 1.6 Hz)
АПХИ-МС: m/z = 362 (M+H+).
Получение 265
Метил 5-[4-(4-н-бутилоксифенил)фенил]фурана 2-карбоксилат
ИК (KBr): 2958, 2933, 2873, 1716, 1483, 1303, 1139 см-1
ЯМР (CDCl3, δ): 0.99 (3H, t, J = 7.3 Hz), 1.5-1.9 (4H, m), 3.93 (3H, s), 4.01 (2H, t, J = 6.4 Hz), 6.75 (1H, d, J = 3.6 Hz), 6.98 (2H, d, J = 8.7 Hz), 7.26 (1H, d, J = 3.6 Hz), 7.56 (2H, d, J = 8.4 Hz), 7.61 (2H, d, J = 8.7 Hz), 7.83 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 351 (M+H)+.
Получение 266
Этил 4-[4-[4-(6-метоксигексилокси)фенил]фенил]бензоат
ИК (KBr): 2937, 2863, 1712, 1602, 1396, 1278, 1108 см-1
ЯМР (CDCl3, δ): 1.4-2.0 (11H, m), 3.34 (3H, s), 3.39 (2H, t, J = 6.4 Hz), 4.01 (2H, t, J = 6.4 Hz), 4.41 (2H, q, J = 7.1 Hz), 6.98 (2H, d, J = 8.7 Hz), 7.56 (2H, d, J = 8.7 Hz), 7.6-7.8 (6H, m), 8.12 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 433 (M+H+).
Получение 267
4-[4-[4-(5-Метоксипентилокси)фенил]фенил]бензойная кислота
ИК (KBr): 2939, 2859, 1679, 1587, 1396, 1321, 1292, 1126 см-1
ЯМР (DMSO-d6, δ): 1.3-1.8 (6H, m), 3.21 (3H, s), 3.2-3.4 (2H, m), 4.01 (2H, t, J = 6.5 Hz), 7.04 (2H, d, J = 8.6 Hz), 7.66 (2H, d, J = 8.6 Hz), 7.7-7.9 (6H, m), 8.03 (2H, d, J = 8.2 Hz)
АПХИ-МС: m/z = 391 (M+H+).
Получение 268
Метил 4-[4-[4-(5-метоксипентилокси)фенил]фенил]фенилацетат
ИК (KBr): 2937, 2863, 1739, 1604, 1492, 1255 см-1
ЯМР (CDCl3, δ): 1.5-2.0 (6H, m), 3.34 (3H, s), 3.42 (2H, t, J = 6.3 Hz), 3.68 (2H, s), 3.72 (3H, s), 4.02 (2H, t, J = 6.4 Hz), 6.97 (2H, d, J = 8.7 Hz), 7.36 (2H, d, J = 8.2 Hz), 7.5-7.7 (8H, m)
АПХИ-МС: m/z = 419 (M+H+).
Получение 269
Раствор гидрохлорида 3-[2-(4-гексилфениламино)этил]-2-оксо-оксазолидина (2,131 г) в 25% бромисто-водородной кислоте в уксусной кислоте (13,04 мл) размешивали в течение 96 часов при комнатной температуре. Реакционную смесь экстрагировали диизопропиловым эфиром. Осадок собирали путем фильтрации и добавляли к этанолу (15 мл). Раствор нагревали с обратным холодильником в течение 5 часов и экстрагировали диизопропиловым эфиром. Осадок собирали путем фильтрации и получали дигидробромид 1-(4-н-гексилфенил) пиперазина (2,413 г).
ИК (KBr): 2921,6; 2711,4; 2485,8; 1452,1; 1012,4 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.6 Hz), 1.1-1.4 (6H, m), 1.4-1.6 (2H, m), 2.49 (2H, t, J = 8.4 Hz), 3.1-3.4 (8H, m), 6.54 (2H, s), 6.90 (2H, d, J = 8.7 Hz), 7.08 (2H, d, J = 8.7 Hz), 8.78 (1H, s)
АПХИ-МС: m/z = 247 (M++H).
Нижеследующие соединения (Получения 270-274) были получены способом, описанным в Получении 269.
Получение 270
4-[4-(4-н-Гексилфенил)пиперазин-1-ил)бензойной кислоты дигидробромид
ИК (KBr): 2956,3; 1691,3; 1664,3; 1602,6; 1232,3 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.5 Hz), 1.2-1.4 (10H, m), 1.4-1.6 (2H, m), 2.51 (2H, t, J = 7.4 Hz), 3.2-3.6 (8H, m), 7.0-7.2 (6H,m), 7.81 (2H, d, J = 8.8 Hz)
АПХИ-МС: m/z = 367 (M++H).
Получение 271
1-(4-Циклогексилфенил)пиперазина дигидробромид
ИК (KBr): 2927,4; 1510,0; 1452,1 см-1
ЯМР (DMSO-d6, δ): 1.1-1.5 (6H, m), 1.6-1.9 (4H, m), 2.41 (1H, m), 3.1-3.4 (8H, m), 6.91 (2H, d, J = 8.7 Hz), 7.11 (2H, d, J = 8.7 Hz), 8.78 (1H, s)
АПХИ-МС: m/z = 245 (M++H).
Получение 272
4-[4-(4-Циклогексилфенил)пиперазин-1-ил]бензойной кислоты дигидробромид
ИК (KBr): 1668,1; 1602,6; 1230,4; 1189,9 см-1
АПХИ-МС: m/z = 365 (M++H).
Получение 273
3-Фтор-4-[4-(4-гидроксифенил)пиперазин-1-ил] бензойной кислоты дигидробромид
ИК (KBr): 1708,6; 1610,3 см-1
ЯМР (DMSO-d6, δ): 3.2-3.6 (8H, m), 6.81 (2H, d, J = 8.6 Hz), 7.0-7.4 (3H, m), 7.4-7.8 (2H, m)
АПХИ-МС: m/z = 317 (M++H).
Получение 274
4-[4-(4-Гидроксифенил)пиперазин-1-ил]бензойной кислоты дигидробромид
ИК (KBr): 1670,1; 1604,5; 1226,5; 775,2 см-1
ЯМР (DMSO-d6, δ): 3.0-3.2 (4H, m), 3.3-3.5 (4H, m), 6.68 (2H, d, J = 8.8 Hz), 6.85 (2H, d, J = 8.8 Hz), 7.02 (2H, d, J = 8.8 Hz), 7.79 (2H, d, J = 8.8 Hz), 8.86 (1H, s), 12.29 (1H, s)
АПХИ-МС: m/z = 299 (M+H+).
Получение 275
Смесь 4-н-гексилоксианилина (10 г), этилакрилата (56,1 мл), ледяной уксусной кислоты (19,25 мл) и хлорида меди (1,02 г) нагревали с обратным холодильником, размешивая в течение 26 часов в атмосфере азота. Раствор охлажденного продукта в эфире встряхивали с водой, а затем с водным раствором аммиака. Органический слой отделяли и осушали сульфатом магния. Сульфат магния отфильтровывали и фильтрат выпаривали при пониженном давлении. Остаток подвергали колоночной хроматографии на силикагеле и элюировали смесью гексана и этилацетата (9: 1). Фракции, содержащие целевое соединение, объединяли и выпаривали при пониженном давлении, в результате чего получали этил 3-[N-(2- этоксикарбонилэтил)-N-(4-гексилоксифенил)амино] пропионат (15,756 г).
ИК (чистый): 1733,7; 1513,8; 1241,9, 1182,2 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.5 Hz), 1.2-1.55 (6H, m), 1.24 (6H, t, J = 7.1 Hz), 1.65-1.85 (2H, m), 2.51 (4H, t, J = 7.2 Hz), 3.53 (4H, t, J = 7.2 Hz), 3.89 (2H, t, J = 6.5 Hz), 4.12 (4H, q, J = 7.1 Hz), 6.72 (2H, d, J = 9.3 Hz), 6.83 (2H, d, J = 9.3 Hz)
АПХИ-МС: m/z = 394 (M++H).
Получение 276
Суспензию метил-4-формилбензоата (4,92 г), гидрохлорида гидроксиламина (5,21 г) и ацетата натрия (6,15 г) в этаноле (50 мл) нагревали с обратным холодильником в течение 2 часов. Смесь выливали в воду и экстрагировали этилацетатом, а отделенный органический слой промывали рассолом и осушали MgSO4. Растворители удаляли при пониженном давлении, в результате чего получали 4-метоксикарбонилбензальдегида оксим (5,28 г).
ИК (KBr): 3291, 1727, 1438, 1284, 1112 см-1
ЯМР (CDCl3, δ): 3.93 (3H, s), 7.65 (2H, d, J = 8.3 Hz), 8.10 (2H, d, J = 8.3 Hz), 8.18 (1H, s), 8.27 (1H, s)
АПХИ-МС: m/z = 180.
Нижеследующее соединение было получено способом, описанным в Получении 276.
Получение 277
N-Гидрокси-4-н-гексилоксибензамидин
ИК (KBr): 3446, 3349, 2937, 2865, 1650, 1610, 1519, 1392, 1253 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.4 Hz), 1.2-1.8 (8H, m), 3.97 (2H, t, J = 6.5 Hz), 5.70 (2H, s), 6.90 (2H, d, J = 8.4 Hz), 7.58 (2H, d, J = 8.4 Hz), 9.43 (1H, s)
АПХИ-МС: m/z = 237 (M+H)+.
Получение 278
К раствору оксима 4-метоксикарбонилбензальдегида (896 мг) в N,N-диметилформамиде (10 мл) добавляли 4 н. соляную кислоту в 1,4-диоксане (1,38 мл) и оксон® (1,69 г). Суспензию размешивали при комнатной температуре в течение 16 часов и выливали в воду со льдом. Целевое соединение экстрагировали этилацетатом и органический слой промывали рассолом, а затем осушали сульфатом магния. Растворители удаляли при пониженном давлении и получали хлорид оксима 4-метоксикарбонилбензальдегида (1,05 г).
ИК (KBr): 3390, 1710, 1436, 1405, 1284, 1232, 1116, 1016 см-1
ЯМР (CDCl3, δ): 3.95 (3H, s), 8.93 (2H, d, J = 8.3 Hz), 8.10 (2H, d, J = 8.7 Hz), 8.39 (1H, s)
АПХИ-МС: m/z = 176 (M-H+-HCl).
Получение 279
Раствор этил-4-оксо-1-(4-н-гексилоксифенил)пиперидин-3-карбоксилата (1,437 г) в 20% соляной кислоте (7,2 мл) нагревали с обратным холодильником в течение 2 часов, затем охлаждали, подщелачивали 60%-ным водным раствором гидроксида натрия и экстрагировали этилацетатом. Органический слой отделяли и отфильтровывали, и фильтрат выпаривали при пониженном давлении, в результате чего получали 1-(4-н-гексилоксифенил)-4-пиперидон (0,959 г).
ИК (чистый): 2931,3; 1716,3; 1511,9; 1243,9; 825,4 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.5 Hz), 1.2-1.6 (6H, m), 1.65-1.85 (2H, m), 2.57 (4H, t, J = 6.1 Hz), 3.46 (4H, t, J = 6.1 Hz), 3.92 (2H, t, J = 6.5 Hz), 6.85 (2H, d, J = 9.3 Hz), 6.95 (2H, d, J = 9.3 Hz)
АПХИ-МС: m/z = 276 (M++H).
Получение 280
Раствор 4-[4-(7-бромгептилокси)фенил] бромбензола (0,25 г) в растворе фторида тетра-н-бутиламмония (тетрагидрофурановый раствор, 1 М, 2,9 мл) нагревали в течение 2 часов до 50oC. После охлаждения до комнатной температуры, раствор растворяли в смеси этилацетата (20 мл) и воды (20 мл). Отделенный органический слой промывали водой, рассолом и осушали сульфатом магния. После выпаривания получали остаток, который подвергали хроматографии на силикагеле (30 мл), элюируя смесью н-гексана и этилацетата (100:0-97:3, об/об). Фракции, содержащие целевое соединение, собирали, и остаток после выпаривания растирали с н-гексаном, в результате чего получали 4-[4-(7-фторгептилокси)фенил]бромбензол (104 мг).
ИК (KBr): 2937,1, 2859,9, 1606,4 см-1
ЯМР (CDCl3, δ): 1.20-1.90 (10H, m), 3.99 (2H, t, J = 6.4 Hz), 4.45 (2H, dt, J = 47.3 and 6.1 Hz), 6.95 (2H, d, J = 6.7 Hz), 7.40 (2H, d, J = 6.7 Hz), 7.47 (2H, d, J = 6.7 Hz), 7.52 (2H, d, J = 6.7 Hz)
Нижеследующее соединение было получено способом, описанным в Получении 280.
Получение 281
4-[4-(6-Фторогексилокси)фенил]бромбензол
ЯМР (CDCl3, δ): 1.40-1.95 (8H, m), 4.01 (2H, t, J = 6.4 Hz), 4.47 (2H, dt, J = 47.5 and 6.0 Hz), 6.95 (2H, d, J = 8.6 Hz), 7.35-7.59 (6H, m)
Получение 282
Раствор 4-[4-(8-бромоктилокси)фенил] бромбензола (3,7 г) в смеси метоксида натрия (4,9 М в метаноле, 17 мл), N,N-диметилформамида (20 мл) и тетрагидрофурана (8 мл) нагревали до 80oC в течение 3 часов. Реакционную смесь растворяли в смеси этилацетата (200 мл) и воды (100 мл). Отделенный органический слой по очереди промывали водой и рассолом, а затем осушали сульфатом магния. После выпаривания получали остаток, который подвергали колоночной хроматографии (силикагель, 100 мл), элюируя н-гексаном, в результате чего получали 4-[4-(8-метоксиоктилокси)фенил]бромбензол (2,73 г).
ИК (KBr): 2935,1, 2858,0, 1604,5 см-1
ЯМР (CDCl3, δ): 1.25-1.70 (10H, m), 1.70-1.95 (2H, m), 3.33 (3H, s), 3.37 (2H, t, J = 6.5 Hz), 3.99 (2H, t, J = 6.5 Hz), 6.95 (2H, d, J = 8.8 Hz), 7.35-7.66 (6H, m)
АПХИ-МС: m/z = 391 (M+).
Нижеследующие соединения (Получения 283-284) были получены способом, описанным в Получении 282.
Получение 283
4-[4-(6-Метоксигексилокси)фенил]бромбензол
ЯМР (CDCl3, δ): 1.50-1.70 (6H, m), 1.70-1.95 (2H, m), 3.34 (3H, s), 3.40 (2H, t, J = 6.2 Hz), 3.99 (2H, t, J = 6.5 Hz), 6.95 (2H, d, J = 8.7 Hz), 7.30-7.60 (6H, m)
АПХИ-МС: m/z = 365 (M++2).
Получение 284
4-[4-(7-Метоксигептилокси)фенил]бромбензол
ИК (KBr): 2935,1; 2854,1, 1604,5 см-1
ЯМР (CDCl3, δ): 1.25-1.70 (8H, m), 1.70, 1.95 (2H, m), 3.33 (3H, s), 3.37 (2H, t, J = 6.4 Hz), 3.98 (2H, t, J = 6.5 Hz), 6.95 (2H, d, J = 8.8 Hz), 7.35-7.56 (6H, m)
АПХИ-МС: m/z = 379 (M++2).
Получение 285
N-(4-октилфенил)-N'-аминомочевину, ацетат формамидина (12,76 г) и N-карбазоил-4-октиланилин (6,458 г) в N,N-диметилформамиде (19,4 мл) размешивали в течение 6 часов при 150oC. Реакционную смесь обрабатывали водой. Осадок собирали путем фильтрации и промывали водой, в результате чего получали 4-(4-октилфенил)-2,3-дигидро-4H-1,2,4-триазол-3-он (4,27 г).
ИК (KBr): 3214,8; 3085,5; 1704,8 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.7 Hz), 1.2-1.5 (10H, m), 1.5-1.8 (2H, m), 2.64 (2H, t, J = 7.9 Hz), 7.29 (2H, d, J = 8.5 Hz), 7.43 (2H, d, J = 8.5 Hz), 7.67 (1H, d, J = 1.3 Hz), 10.31 (1H, s)
АПХИ-МС: m/z = 274 (M+H+).
Нижеследующее соединение (Получение 286) получали способом, описанным в Получении 285.
Получение 286
4-[4-(4-трет-Бутоксикарбонилпиперазин-1-ил)фенил] -2,3-дигидро-4H- 1,2,4-триазол-3-он
ИК (KBr): 3200; 1699,0; 918,0 см-1
ЯМР (CDCl3, δ): 1.49 (9H, s), 3.17 (4H, t, J = 4.9 Hz), 3.60 (4H, t, J = 4.9 Hz), 7.00 (2H, d, J = 9.0 Hz), 7.40 (2H, d, J = 9.0 Hz), 7.63 (1H, s), 10.4 (1H, s)
АПХИ-МС: m/z = 346 (M+H+).
Получение 287
Смесь метил 6-(1-гептинил)нафталин-2-карбоксилата (4,51 г) и оксида платины (0,4 г) в тетрагидрофуране размешивали в течение 5 часов под давлением водорода в 3,5 атм. Затем катализатор отфильтровывали и фильтрат выпаривали, в результате чего получали метил 6-гептилнафталин-2-карбоксилат (4,40 г).
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.6 Hz), 1.16-1.50 (8H, m), 1.50-1.80 (2H, m), 2.78 (2H, t, J = 7.6 Hz), 3.97 (3H, s), 7.39 (1H, dd, J = 17 and 8.4 Hz), 7.64 (1H, s), 7.79 (1H, d, J = 8.6 Hz), 7.86 (1H, d, J = 8.4 Hz), 8.02 (1H, dd, J = 1.7 and 8.6 Hz), 8.57 (1H, s)
АПХИ-МС: m/z = 285 (M++1).
Нижеследующее соединение (Получение 288) получали способом, описанным в Получении 287.
Получение 288
Метил 6-гексилнафталин-2-карбоксилат
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.8 Hz), 1.17-1.53 (6H, m), 1.60-1.82 (2H, m), 2.79 (2H, t, J = 7.7 Hz), 3.97 (3H, s), 7.39 (1H, dd, J = 1.7 and 8.4 Hz), 7.64 (1H, s), 7.80 (1H, d, J = 8.6 Hz), 7.86 (1H, d, J = 8.4 Hz), 8.03 (1H, dd, J = 1.7 and 8.6 Hz), 8.57 (1H, s)
АПХИ-МС: m/z = 271 (M+1).
Получение 289
К размешанному раствору метил 6-гидроксинафталин-2-карбоксилата (3,0 г) в дихлорметане (40 мл) добавляли по очереди диизопропилэтиламин (3,9 мл) и ангидрид трифторуксускной кислоты (3,0 мл) при -40oC. После размешивания в течение 20 минут при -40oC смесь растворяли в смеси этилацетата и холодной воды, органический слой отделяли, промывали рассолом, осушали сульфатом магния, а затем подвергали вакуумной сушке. Остаток растворяли в пиперидине (20 мл) и к полученному раствору добавляли 1-гептин (4,0 мл) и тетракис(трифенилфосфин)палладий (0) (0,5 г). После нагревания в течение 1 часа в атмосфере азота при 85oC реакционную смесь выпаривали в вакууме. Остаток разбавляли этилацетатом, и раствор последовательно промывали соляной кислотой и рассолом а затем осушали сульфатом магния и выпаривали в вакууме. Остаток подвергали хроматографии на силикагеле (200 мл), элюируя смесью н-гексана и этилацетата (9:1, объем/объем), в результате чего получали метил 6-(1-гептинил)нафталин-2-карбоксилат (4,01 г).
ЯМР (CDCl3, δ): 0.94 (3H, t, J = 7.1 Hz), 1.30-1.70 (6H, m), 2.46 (2H, t, J = 7.0 Hz), 3.97 (3H, s), 7.50 (1H, dd, J = 1.7 and 8.6 Hz), 7.80 (1H, d, J = 8.6 Hz), 7.86 (1H, d, J = 8.6 Hz), 8.04 (1H, dd, J = 1.7 and 8.6 Hz), 8.55 (1H, s)
АПХИ-МС: m/z = 281 (M++1).
Нижеследующее соединение получали способом, описанным в Получении 289.
Получение 290
Метил 6-(1-гексинил)нафталин-2-карбоксилат
ЯМР (CDCl3, δ): 0.97 (3H, t, J = 7.1 Hz), 1.40-1.71 (4H, m), 2.47 (2H, t, J = 6.8 Hz), 3.98 (3H, s), 7.50 (1H, dd, J = 1.5 and 8.5 Hz), 7.79 (1H, d, J = 8.6 Hz), 7.85 (1H, d, J = 8.5 Hz), 7.92 (1H, s), 8.04 (1H, dd, J = 1.7 and 8.6 Hz), 8.55 (1H, s)
АПХИ-МС: m/z = 267 (M++1).
Получение 291
К раствору 4-октиланилина (5 мл) в смеси пиридина (12,5 мл) и хлороформа (40 мл) добавляли фенилхлороформиат (2,95 мл) и полученную смесь размешивали 1,5 часа при комнатной температуре. Затем реакционную смесь добавляли к смеси воды и этилацетата. Органический слой отделяли и осушали сульфатом магния. Сульфат магния отфильтровывали, и фильтрат выпаривали при пониженном давлении, в результате чего получали 4-октил-N-феноксикарбониланилин (4,51 г).
ИК (KBr): 3318,9; 1714,4; 1234,2 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.2 Hz), 1.2-1.4 (10H, m), 1.5-1.7 (2H, m), 2.57 (2H, t, J = 7.3 Hz), 6.88 (1H, s), 7.1-7.5 (9H, m)
Нижеследующие соединения (Получения 292-299) были получены способом, описанным в Получении 291.
Получение 292
4-(4-трет-Бутоксикарбонилпиперазин-1-ил)-N-феноксикарбониланилин
ИК (KBr): 3309,2; 1743,3; 1658,5; 1197,6 см-1
ЯМР (CDCl3, δ): 1.48 (9H, s), 3.08 (4H, t, J = 5.3 Hz), 3.58 (4H, t, J = 5.3 Hz), 6.87 (1H, s), 6.91 (2H, d, J = 9 Hz), 7.1-7.5 (7H, m)
АПХИ-МС: m/z = 398 (M+H+).
Получение 293
1-(4-Циклогексилбензоил)-2-(4-метоксикарбонилбензоил)гидразин
ИК (KBr): 3236, 2925, 2852, 1726, 1679, 1637, 1278, 1110 см-1
ЯМР (DMSO-d6, δ): 1.1-1.5 (5H, m), 1.6-2.0 (5H, m), 2.60 (1H, m), 3.90 (3H, s), 7.37 (2H, d, J = 8.0 Hz), 7.85 (2H, d, J = 8.0 Hz), 8.0-8.2 (4H, m), 10.48 (1H, s), 10.68 (1H, s)
АПХИ-МС: m/z = 381 (M+H)+.
Получение 294
1-[4-(Пиперидин-1-ил)бензоил]-2-(4-метоксикарбонилбензоил)гидразин
ИК (KBr): 3500, 3286, 2941, 2854, 1712, 1689, 1650, 1606, 1286, 1242 см-1
ЯМР (DMSO-d6, δ): 1.59 (6H, s), 3.33 (4H, s), 3.90 (3H, s), 6.97 (2H, d, J = 8.8 Hz), 7.79 (2H, d, J = 8.8 Hz), 8.02 (2H, d, J = 8.4 Hz), 8.09 (2H, d, J = 8.4 Hz), 10.23 (1H, s), 10.57 (1H, s)
АПХИ-МС: m/z = 382 (M+H)+.
Получение 295
1-[4-(4-н-Пропилоксифенил)бензоил]-2-(4-метоксикарбонилбензоил)гидразин
ИК (KBr): 3230, 1724, 1679, 1654, 1280, 1108 см-1
ЯМР (DMSO-d6, δ): 1.00 (3H, d, J = 7.5 Hz), 1.76 (2H, tq, J = 6.5 and 7.5 Hz), 3.91 (3H, s), 7.05 (2H, d, J = 8.7 Hz), 7.71 (2H, d, J = 8.7 Hz), 7.79 (2H, d, J = 8.5 Hz), 8.00 (2H, d, J = 8.5 Hz), 8.05 (2H, d, J = 8.6 Hz), 8.11 (2H, d, J = 8.6 Hz), 10.60 (1H, s), 10.72 (1H, s)
АПХИ-МС: m/z = 433 (M+H)+.
Получение 296
1-(4-Метоксикарбонилбензоил)-2-деканоилгидразин
ИК (KBr): 3220, 2919, 2850, 1724, 1643, 1600, 1567, 1479, 1284 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.8 Hz), 1.2-1.7 (14H, m), 2.18 (2H, t, J = 7.4 Hz), 3.89 (3H, s), 7.97 (2H, d, J = 8.5 Hz), 8.06 (2H, d, J = 8.5 Hz), 9.15 (1H, s), 10.49 (1H, s)
АПХИ-МС: m/z = 349 (M+H+).
Получение 297
1-(4-Метоксикарбонилбензоил)-2-(транс-4-н- пентилциклогексилкарбонил)гидразин
ИК (KBr): 3201, 2923, 2852, 1727, 1600, 1567, 1479, 1282 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.9 Hz), 0.9-1.0 (2H, m), 1.1-1.5 (11H, m), 1.7-1.9 (4H, m), 2.20 (1H, m), 3.88 (3H, s), 7.97 (2H, d, J = 8.6 Hz), 8.06 (2H, d, J = 8.6 Hz), 9.85 (1H, s), 10.46 (1H, s)
АПХИ-МС: m/z = 375 (M+H+).
Получение 298
1-[4-(8-Метоксиоктилокси)бензоил]-2-(4-метоксикарбонилбензоил]гидразин
ИК (KBr): 3213, 2935, 2856, 1718, 1600, 1567, 1465, 1282 см-1
ЯМР (DMSO-d6, δ): 1.2-1.8 (12H, m), 3.21 (3H, s), 3.29 (2H, t, J = 6.4 Hz), 3.90 (3H, s), 4.04 (2H, t, J = 6.5 Hz), 7.04 (2H, d, J = 8.8 Hz), 7.90 (2H, d, J = 8.8 Hz), 8.04 (2H, d, J = 8.7 Hz), 8.10 (2H, d, J = 8.7 Hz), 10.41 (1H, s), 10.64 (1H, s)
АПХИ-МС: m/z = 457 (M+H+).
Получение 299
1-(4-Октилоксибензоил)-2-(4-метоксикарбонилбензоил)гидразин
ИК (KBr): 3224, 2923, 2854, 1724, 1681, 1643, 1502, 1434, 1282, 1253, 1106 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.8 Hz), 1.2-1.5 (10H, m), 1.6-1.8 (2H, m), 3.89 (3H, s), 4.04 (2H, t, J = 6.3 Hz), 7.04 (2H, d, J = 8.7 Hz), 7.90 (2H, d, J = 8.7 Hz), 8.03 (2H, d, J = 8.6 Hz), 8.10 (2H, d, J = 8.6 Hz), 10.42 (1H, s), 10.64 (1H, s)
АПХИ-МС: m/z = 427 (M+H+).
Получение 300
Раствор метил 4-н-гексилоксибензоата (2,00 г) и гидрата гидразина (4,24 г) в этаноле (10 мл) нагревали с обратным холодильником в течение 6 часов. После охлаждения реакционную смесь выливали в воду. Осадок собирали путем фильтрации, промывали водой и осушали P2O5 при пониженном давлении, в результате чего получали N-(4-н-гексилоксибензоил) гидразин (1,96 г).
ИК (KBr): 3311, 2954, 2869, 1623, 1253 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.8 Hz), 1.2-1.5 (6H, m), 1.6-1.8 (2H, m), 4.00 (2H, t, J = 6.5 Hz), 4.40 (2H, s), 6.95 (2H, d, J = 8.6 Hz), 7.77 (2H, d, J = 8.6 Hz), 9.59 (1H, s)
АПХИ-МС: m/z = 237 (M+H)+.
Нижеследующие соединения (Получения 301-308) были получены способом, описанным в Получении 300.
Получение 301
N-(4-Октилфенил)-N'-аминомочевина
ИК (KBr): 3309,2; 1683,6; 1554,3 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.7 Hz), 1.1-1.4 (10H, m), 1.4-1.6 (2H, m), 2.48 (2H, t, J = 8.9 Hz), 4.32 (2H, s), 7.03 (2H, d, J = 8.4 Hz), 7.32 (1H, s), 7.38 (2H, d, J = 8.4 Hz), 8.50 (1H, s)
Получение 302
N-[4-(4-трет-Бутоксикарбонилпиперазин-1-ил)фенил]-N'-аминомочевина
ИК (KBr): 3237,9; 1695,1; 1670,1; 1540,8; 1230,4 см-1
ЯМР (DMSO-d6, δ ): 1.42 (9H, s), 2.97 (4H, t, J = 4.9 Hz), 3.44 (4H, t, J = 4.9 Hz), 4.30 (2H, s), 6.85 (2H, d, J = 9.0 Hz), 7.26 (1H, s), 7.36 (2H, d, J = 9.0 Hz), 8.41 (1H, s)
Получение 303
4-Циклогексилбензоилгидразин
ИК (KBr): 3318, 2925, 2852, 1625, 1606, 1527, 1326 см-1
ЯМР (DMSO-d6, δ): 1.1-1.5 (5H, m), 1.6-2.0 (5H, m), 2.4-2.6 (1H, m), 4.44 (2H, s), 7.27 (2H, d, J = 8.2 Hz), 7.73 (2H, d, J = 8.2 Hz), 9.66 (1H, s)
АПХИ-МС: m/z = 219 (M+H+).
Получение 304.
4-(пиперидин-1-ил)бензоилгидразин
ИК (KBr): 3263, 2852, 1612, 1504, 1245, 1124 см-1
ЯМР (DMSO-d6, δ): 1.57 (6H, s), 3.25 (4H, s), 4.35 (2H, s), 6.90 (2H, d, J = 9.0 Hz), 7.68 (2H, d, J = 9.0 Hz), 9.44 (1H, s)
АПХИ-МС: m/z = 220 (M+H+).
Получение 305
4-(4-н-Пропилоксифенил)бензоилгидразин
ИК (KBr): 3350, 3276, 1610, 1494, 1288, 978 см-1
ЯМР (DMSO-d3, δ): 0.99 (3H, t, J = 7.5 Hz), 1.75 (2H, tq, J = 6.5 and 7.5 Hz), 3.98 (2H, t, J = 6.5 Hz), 4.50 (2H, s), 7.03 (2H, d, J = 8.8 Hz), 7.65 (2H, d, J = 8.8 Hz), 7.69 (2H, d, J = 8.4 Hz), 7.88 (2H, d, J = 8.4 Hz), 9.79 (1H, s)
АПХИ-МС: m/z = 271 (M+H+).
Получение 306
4-Метоксикарбонилбензоилгидразин
ИК (KBr): 3322, 3250, 3018, 1727, 1658, 1621, 1565, 1432, 1280, 1110 см-1
ЯМР (DMSO-d6, δ): 3.87 (3H, s), 4.58 (2H, s), 7.93 (2H, dd, J = 8.6 and 3.1 Hz), 7.02 (2H, dd, J = 8.6 and 3.1 Hz), 9.97 (1H, s)
АПХИ-МС: m/z = 195 (M+H+).
Получение 307
Транс-4-н-пентилциклогексилкарбонилгидразин
ИК (KBr): 3303, 3199, 2954, 2925, 2850, 1639, 1619, 1533, 1457 см-1
ЯМР (DMSO-d6, δ): 0.8-1.0 (6H, m), 1.1-1.5 (10H, m), 1.6-2.2 (5H, m), 4.10 (2H, s), 8.85 (1H, s)
АПХИ-МС: m/z = 213 (M+H+).
Получение 308
4-(8-Метоксиоктилокси)бензоилгидразин
ИК (KBr): 3309, 2937, 2852, 1606, 1494, 1253 см-1
ЯМР (DMSO-d6, δ): 1.2-1.8 (12H, m), 3.20 (3H, s), 3.25 (2H, t, J = 6.5 Hz), 3.99 (2H, t, J = 6.5 Hz), 4.39 (2H, s), 6.95 (2H, d, J = 8.8 Hz), 7.77 (2H, d, J = 8.8 Hz), 9.58 (1H, s)
АПХИ-МС: m/z = 295 (M+H)+.
Получение 309
К размешанному раствору 4-бром-4'-н-гептилбифенила (2,71 г) в тетрагидрофуране (100 мл) при -78oC по капле добавляли раствор н-бутиллития в смеси диэтилового эфира и н-гексана (1,6 М, 5,1 мл). После размешивания в течение 30 минут при -78oC, полученную смесь добавляли к раствору диэтилоксалата (3,4 мл) в тетрагидрофуране (50 мл) при -78oC. Затем смесь нагревали в течение 1 часа до 0oC и к этой смеси добавляли уксусную кислоту (0,5 мл). После выпаривания получали остаток, который растворяли в смеси воды и этилацетата. Органический слой отделяли, промывали рассолом, осушали сульфатом магния. Остаток, полученный после выпаривания, подвергали хроматографии на силикагеле (200 мл), элюируя смесью н-гексана и этилацетата (10:0-95:5, V/V), в результате чего получали 1-этил-2-(4-н-гептилфенил)этандион (2,23 г).
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.6 Hz), 1.10-1.50 (8H, m), 1.44 (3H, t, J = 7.1 Hz), 1.50-1.80 (2H, m), 2.66 (2H, t, J = 7.7 Hz), 4.47 (2H, q, J = 7.1 Hz), 7.20-7.40 (2H, m), 7.50-7.64 (2H, m), 7.64-7.85 (2H, m), 8.00-8.20 (2H, m)
АПХИ-МС: m/z = 353 (M++1).
Получение 310
К суспензии гидрида натрия (60% в масле, 0,37 г) в тетрагидрофуране (40 мл) при комнатной температуре порциями добавляли 4-ацетил-4'-н-гептилбифенил (2,50 г). После размешивания в течение 1 часа при комнатной температуре к раствору добавляли триэтилфосфоноацетат (1,9 мл) и полученную смесь нагревали в течение 5 часов до температуры дефлегмации. После охлаждения до комнатной температуры к смеси добавляли уксусную кислоту (0,53 мл) и выпаривали. Остаток растворяли в смеси воды и этилацетата. Отделенный органический слой промывали рассолом, осушали сульфатом магния и выпаривали. Остаток хроматографировали на силикагеле (200 мл), элюируя смесью н-гексана и диизопропилового эфира (99:1-20:1, V/V), в результате чего получали этил (E)-[4-(4-гептилфенил)фенил]-2-бутеноат (2,19 г).
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.6 Hz), 1.13-1.48 (8H, m), 1.48-1.78 (2H, m), 2.61 (3H, s), 2.65 (2H, t, J = 7.4 Hz), 4.22 (2H, q, J = 7.1 Hz), 6.20 (1H, t, J = 2.7 Hz), 7.23-7.28 (2H, m), 7.50-7.63 (6H, m)
АПХИ-МС: m/z = 365 (M++1).
Получение 311
К раствору 4-бром-4'-н-гептилбифенила (5,1 г) в тетрагидрофуране (60 мл) добавляли при -60oС раствор н-бутиллития в смеси н-гексана и диэтилового эфира (1,6 M, 9,7 мл). После размешивания в течение 30 минут при -60oC к смеси добавляли N,N-диметилацетамид (4,3 мл), и реакционную смесь оставляли нагреваться до 0oC. Затем реакционную смесь растворяли в смеси холодной воды и этилацетата, и рН смеси доводили до 1 с помощью 1 н. соляной кислоты. Органический слой отделяли, промывали рассолом, осушали сульфатом магния и выпаривали. Остаток подвергали хроматографии на силикагеле (150 мл), элюируя смесью н-гексана и этилацетата (20:1, V/V), в результате чего получали 4-ацетил-4'-н-гептилбифенил (1,60 г).
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.6 Hz), 1.05-1.48 (8H, m), 1.48-1.75 (2H, m), 2.65 (2H, t, J = 7.6 Hz), 2.63 (3H, s), 7.20-7.31 (2H, m), 7.52-7.58 (2H, m), 7.65-7.70 (2H, m), 7.97-8.05 (2H, m)
АПХИ-МС: m/z = 295 (M+1).
Получение 312
К раствору метил 4-[4-(8-гидроксиоктилокси)фенил] бензоата (500 мг) и гидропирана (141 мг) в дихлорметане (15 мл) добавляли п-толуолсульфоновую кислоту (5 мл). Полученную смесь размешивали 10 минут при комнатной температуре, а затем разбавляли дихлорметаном и промывали водой и рассолом. Отделенный органический слой осушали сульфатом магния и выпаривали при пониженном давлении, в результате чего получали метил 4-[4-(8-тетрагидропиран-2-ил-оксиоктилокси)фенил]бензоат (616 мг).
ИК (KBr): 2935, 2856, 1722, 1602, 1438, 1290, 1199 см-1
ЯМР (CDCl3, δ): 1.3-2.0 (18H, m), 3.3-3.9 (4H, m), 3.93 (3H, s), 4.00 (2H, t, J = 6.5 Hz), 4.5-4.6 (1H, m), 6.98 (2H, d, J = 8.7 Hz), 7.56 (2H, d, J = 8.7 Hz), 7.62 (2H, d, J = 8.3 Hz), 8.07 (2H, d, J = 8.3 Hz)
Получение 313
К раствору хлорида титана (IV) (11,6 г) в дихлорметане (100 мл) по капле добавляли при 0oC 4-н-пентилоксиацетофенон (10,3 г) и метил 4-формилбензоат (8,21 г) в дихлорметане (50 мл). Затем к смеси добавляли триэтиламин (11,15 мл) в дихлорметане (30 мл). Смесь размешивали 30 минут при 0oC и разбавляли н-гексаном. Органический слой промывали водой (4 раза) и рассолом, а затем осушали сульфатом магния. Растворители удаляли при пониженном давлении и остаток растирали с изопропиловым эфиром. Твердое вещество собирали путем фильтрации и осушали, в результате чего получали 1-(4-метоксикарбонилфенил)-3-(4-н-пентилоксифенил)-1-пропен-3-он (4,02 г).
ИК (KBr): 2950, 2910, 2863, 1718, 1654, 1604, 1274, 1176 см-1
ЯМР (CDCl3, δ): 0.94 (3H, t, J = 6.9 Hz), 1.3-1.6 (4H, m), 1.8-2.0 (2H, m), 3.93 (3H, s), 4.04 (2H, t, J = 6.5 Hz), 6.97 (2H, d, J = 8.8 Hz), 7.60 (1H, d, J = 15.7 Hz), 7.68 (2H, d, J = 8.4 Hz), 7.80 (1H, d, J = 15.7 Hz), 8.0-8.2 (4H, m)
АПХИ-МС: m/z = 353 (M+H+).
Получение 314
К раствору хлорида титана (IV) (13,88 г) в дихлорметане (100 мл) по капле добавляли при 0oC этил 4-ацетилбензоат (11,53 г) и 4-н-пентилоксибензальдегид (12,69 г) в дихлорметане (50 мл). Затем к смеси добавляли триэтиламин (12,44 мл) в дихлорметане (30 мл). Смесь размешивали 30 минут при 0oC и разбавляли этилацетатом. Органический слой промывали водой (четыре раза) и рассолом, а затем осушали сульфатом магния. Растворители удаляли при пониженном давления и остаток растирали с н-гексаном. Твердый продукт собирали путем фильтрации и осушали, в результате чего получали 1-(4-н-пентилоксифенил)-3-(4-этоксикарбонилфенил)-1-пропен-3-он (13,45 г).
ИК (KBr): 2956, 2929, 2861, 1718, 1656, 1594, 1510, 1272 см-1
ЯМР (CDCl3, δ): 0.94 (3H, t, J = 7.1 Hz), 1.3-1.9 (9H, m), 4.01 (2H, t, J = 6.5 Hz), 4.42 (2H, q, J = 7.1 Hz), 6.93 (1H, d, J = 8.7 Hz), 7.37 (1H, d, J = 15.6 Hz), 7.60 (2H, d, J = 8.7 Hz), 7.81 (1H, d, J = 15.6 Hz), 8.03 (2H, d, J = 8.5 Hz), 8.16 (2H, d, J = 8.5 Hz)
АПХИ-МС: m/z = 367 (M+H+).
Нижеследующее соединение было получено способом, описанным в Получении 314.
Получение 315
Этил 4-оксо-1-(4-н-гексилоксифенил)пиперидин-3-карбоксилат
ИК (чистый): 1664,3; 1511,9; 1243,9; 1216,9 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.5 Hz), 1.2-1.5 (6H, m), 1.32 (3H, t, J = 7.1 Hz), 1.65-1.85 (2H, m), 2.51 (2H, t, J = 5.8 Hz), 3.31 (2H, t, J = 5.8 Hz), 3.76 (2H, s), 3.91 (2H, t, J = 6.5 Hz), 4.26 (2H, q, J = 7.1 Hz), 6.84 (2H, d, J = 9.2 Hz), 6.94 (2H, d, J = 9.2 Hz), 12.06 (1H, s)
АПХИ-МС: m/z = 348 (M++H).
Получение 316
К раствору 4-н-гексилоксибензоилгидразина (1,96 г) и пиридина (0,74 мл) в тетрагидрофуране (20 мл) по капле добавляли при 0oC раствор хлорида монометилового эфира терефталевой кислоты (1,56 г) в тетрагидрофуране (15 мл). Реакционную смесь размешивали 2 часа при комнатной температуре и выливали в воду. Осадок собирали путем фильтрации и промывали ацетонитрилом. Остаток осушали при пониженном давлении и получали 1-(4-н-гексилоксибензоил)-2-(4-метоксикарбонилбензоил)гидразин (2,99 г).
ИК (KBr): 3230, 3023, 2954, 2858, 1724, 1681, 1643, 1280, 1251, 1105 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.6 Hz), 1.2-1.5 (6H, m), 1.6-1.8 (2H, m), 3.90 (3H, s), 4.04 (2H, t, J = 6.4 Hz), 7.04 (2H, d, J = 8.7 Hz), 7.90 (2H, d, J = 8.7 Hz), 8.03 (2H, d, J = 8.4 Hz), 8.10 (2H, d, J = 8.4 Hz), 10.42 (1H, s), 10.65 (1H, s)
АПХИ-МС: m/z = 399 (M+H)+.
Получение 317
Смесь 1-(4-н-гексилоксифенил)-4-пиперидона (0,823 г), 1-(4-этоксикарбонилфенил)пиперазина (0,7 г) и изопропоксид титана (IV) (1,11 мл) размешивали при комнатной температуре. Через 1 час ИК-спектр смеси не обнаруживал полосу кетона, и вязкий раствор разбавляли абсолютным этанолом (3 мл). Затем добавляли цианоборогидрид натрия (0,121 г), и раствор размешивали в течение 3 часов. После этого, размешивая, добавляли воду (3 мл) и полученный органический осадок фильтровали, а затем промывали этанолом. Фильтрат экстрагировали этилацетатом. Органический слой отделяли и осушали сульфатом магния. Сульфат магния отфильтровывали и фильтрат выпаривали при пониженном давлении, в результате чего получали этил 4-[4-[1-(4-н-гексилоксифенил)пиперидин-4-ил]пиперазин-1-ил]бензоат (331 мг).
ИК (KBr): 1708,6; 1606,4; 1511,9; 1284,4; 1236,1 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.5 Hz), 1.2-1.55 (6H, m), 1.37 (3H, t, J = 7.1 Hz), 1.6-1.85 (4H, m), 1.95 (2H, d, J = 12 Hz), 2.41 (1H, m), 2.62 (2H, d, J = 11 Hz), 2.75 (4H, t, J = 5.0 Hz), 3.35 (4H, t, J = 5.0 Hz), 3.58 (2H, d, J = 11 Hz), 3.90 (2H, t, J = 6.5 Hz), 4.32 (2H, q, J = 7.1 Hz), 6.7-7.0 (6H, m), 7.92 (2H, d, J = 9.0 Hz)
АПХИ-МС: m/z = 494 (M++H).
Нижеследующее соединение получали способом, описанным в Получении 317.
Получение 318
1-трет-Бутоксикарбонил-4-(4-фенилциклогексил)пиперазин
ИК (KBr): 1697,1; 1245,8; 1170,6; 1124,3; 700 см-1
ЯМР (CDCl3, δ): 1.2-1.65 (17H, m), 1.9-2.1 (4H, m), 2.3-2.6 (2H, m), 2.55 (4H, t, J = 5.0 Hz), 3.44 (4H, t, J = 5.0 Hz), 7.1-7.4 (5H, m)
АПХИ-МС: m/z = 345 (M++H).
Получение 319
К суспензии 1-(N, N-диметиламино)-2-(4-этокси-карбонилбензоил)этилена (0,742 г) и 4-н-гексил-оксибензамидина гидрохлорида (0,847 г) в метаноле (10 мл) добавляли 28% метоксид натрия в метаноле (0,64 мл). Суспензию нагревали с обратным холодильником в течение 6 часов и распределяли между этилацетатом и водой. Органический слой промывали водой и рассолом, осушали сульфатом магния и выпаривали при пониженном давлении. Остаток растирали с ацетонитрилом, собирали путем фильтрации и осушали при пониженном давлении, в результате чего получали метил 4-[2-(4-н-гексилоксифенил)пиримидин-6-ил]бензоат (0,61 г).
ИК (KBr): 2931, 2861, 1722, 1606, 1558, 1251 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 6.7 Hz), 1.2-1.6 (6H, m), 1.8-2.0 (2H, m), 3.97 (3H, s), 4.05 (2H, t, J = 6.5 Hz), 7.02 (2H, d, J = 8.8 Hz), 7.56 (1H, d, J = 5.2 Hz), 8.18 (2H, d, J = 8.6 Hz), 8.28 (2H, d, J = 8.6 Hz), 8.52 (2H, d, J = 8.8 Hz), 8.83 (1H, d, J = 5.2 Hz)
АПХИ-МС: m/z = 391 (M+H+).
Получение 320
Раствор 1-(4-метоксикарбонилфенил)-3-(4-н-пентилоксифенил)-1- пропен-3-она (4,0 г) и гидрохлорида гидроксиламина (3,93 г) в этаноле (40 мл) нагревали с обратным холодильником в течение 4 часов. Смесь разбавляли этилацетатом, органический слой промывали водой (х 2) и рассолом и осушали сульфатом магния. Растворители удаляли при пониженном давлении и получали сырой оксим. К раствору сырого оксима в 1,2-дихлорэтане (20 мл) добавляли оксид активированного марганца (IV) (10,0 г). Реакционную смесь нагревали с обратным холодильником в течение 2 часов и фильтровали. Остаток промывали дихлорметаном. Растворители удаляли при пониженном давлении и остаток растирали с ацетонитрилом. Твердое вещество собирали путем фильтрации и осушали, в результате чего получали метил 4-[3-(4-н-пентилоксифенил)изоксазол-5-ил]бензоат (0,98 г).
ИК (KBr): 2940, 2871, 1720, 1612, 1278, 1249, 1178, 1108 см-1
ЯМР (DMSO-d6, δ): 0.94 (3H, t, J = 7.2 Hz), 1.2-1.6 (4H, m), 1.7-1.9 (2H, m), 3.95 (3H, s), 4.01 (2H, t, J = 6.5 Hz), 6.87 (1H, s), 6.98 (2H, d, J = 8.9 Hz), 7.79 (2H, d, J = 8.9 Hz), 7.89 (2H, d, J = 8.6 Hz), 8.15 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 366 (M+H+).
Получение 321
К раствору 4-метоксикарбонилфенилгидроксииминометилхлорида (16,98 г) и 4-н-пентилоксифенилацетилена (18,96 г) в тетрагидрофуране (170 мл) в течение 2 часов добавляли при 40oC триэтиламин (14,4 мл) в тетрагидрофуране (140 мл) и полученную смесь размешивали в течение 30 минут при 40oC. Затем смесь разбавляли дихлорметаном и промывали водой и рассолом. Отделенный органический слой осушали сульфатом магния и выпаривали при пониженном давлении. Остаток растирали с ацетонитрилом. Осадок собирали путем фильтрации и осушали, в результате чего получали метил 4-[5-(4-н-пентилоксифенил)изоксазол-3-ил]бензоат (24,56 г).
ИК (KBr): 2942, 2873, 1716, 1616, 1508, 1280, 1108 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 6.9 Hz), 1.3-1.6 (4H, m), 1.8-2.0 (2H, m), 3.95 (3H, s), 4.02 (2H, t, J = 6.5 Hz), 6.74 (1H, s), 6.99 (2H, d, J = 8.8 Hz), 7.76 (2H, d, J = 8.8 Hz), 7.93 (2H, d, J = 8.5 Hz), 8.14 (2H, d, J = 8.5 Hz)
АПХИ-МС: m/z = 366 (M+H+).
Получение 322
К раствору N-гидрокси-4-октилоксибензамидина (1,89 г) в пиридине (10 мл) добавляли по капле при 0oС хлорид монометилового эфира терефталевой кислоты (1,67 г) в тетрагидрофуране (15 мл). Смесь размешивали при комнатной температуре в течение 15 минут, а затем выливали в воду. Осадок собирали путем фильтрации, осушали и растворяли в пиридине (10 мл). Раствор нагревали с обратным холодильником в течение 1 часа. Реакционную смесь разбавляли этилацетатом и промывали 1 н. HCl, водой и рассолом. Отделенный органический слой осушали сульфатом магния и растворители удаляли при пониженном давлении. Остаток растирали с ацетонитрилом и собирали путем фильтрации. Твердый остаток осушали и получали в результате метил 4-[3-(4-н-гексилоксифенил)-1,2,4-оксадиазол-5-ил]бензоат (2,27 г).
ИК (KBr): 2950, 2925, 2863, 1720, 1280, 1255 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J = 6.6 Hz), 1.2-1.9 (8H, m), 3.97 (3H, s), 4.03 (2H, d, J = 6.5 Hz), 7.00 (2H, d, J = 8.9 Hz), 8.09 (2H, d, J = 8.9 Hz), 8.20 (2H, d, J = 6.6 Hz), 8.28 (2H, d, J = 6.6 Hz)
АПХИ-МС: m/z = 381 (M+H)+.
Получение 323
Суспензию 1-(4-н-гексилоксибензоил)-2-(4-метоксикарбонилбензоил)гидразина (1,00 г) в оксихлориде фосфора (5 мл) нагревали в течение 1 часа с обратным холодильником. После охлаждения раствор концентрировали при пониженном давлении. Остаток выливали в воду со льдом и экстрагировали дихлорметаном. Органический слой промывали водой, рассолом и осушали сульфатом магния. Растворители удаляли при пониженном давлении. Остаток растирали с ацетонитрилом, собирали путем фильтрации и осушали при пониженном давлении, в результате чего получали метил 4-[5-(4-н-гексилоксифенил)-1,3,4-оксадиазол-2-ил]бензоат (761 мг).
ИК (KBr): 2954, 2854, 1724, 1612, 1494, 1280, 1249 см-1
ЯМР (CDCl3, δ): 0.91 (3H, t, J = 6.6 Hz), 1.3-1.6 (6H, m), 1.7-1.9 (2H, m), 3.96 (3H, s), 4.04 (2H, t, J = 6.5 Hz), 7.02 (2H, d, J = 8.6 Hz), 8.07 (2H, d, J = 8.6 Hz), 8.19 (4H, m)
АПХИ-МС: m/z = 381 (M+H)+.
Нижеследующие соединения (получения 324-327) были получены способом, описанным в Получении 323.
Получение 324
Метил-4-[5-[4-(4-н-пропилоксифенил)фенил]-1,3,4-оксадиазол-2-ил]бензоат
ИК (KBr): 1720, 1614, 1496, 1280, 1103 см-1
ЯМР (CDCl3, δ ): 1.07 (3H, d, J = 7.5 Hz), 1.84 (2H, tq, J = 6.5 and 7.5 Hz), 3.98 (3H, s), 3.99 (2H, t, J = 6.5 Hz), 7.01 (2H, d, J = 8.8 Hz), 7.60 (2H, d, J = 8.8 Hz), 7.73 (2H, d, J = 8.5 Hz), 8.19 (2H, d, J = 8.5 Hz), 8.22 (4H, s)
АПХИ-МС: m/z = 415 (M+H+).
Получение 325
Метил 4-[5-(н-нонил)-1,3,4-оксадиазол-2-ил]бензоат
ИК (KBr): 2915, 2848, 1724, 1569, 1436, 1413, 1278 см-1
ЯМР (CDCl3, δ): 0.88 (3H, t, J = 6.4 Hz), 1.2-1.6 (12H, m), 1.8-2.0 (2H, m), 2.94 (2H, t, J = 7.6 Hz), 3.96 (3H, s), 8.11 (2H, d, J = 8.8 Hz), 8.17 (2H, d, J = 8.8 Hz)
АПХИ-МС: m/z = 331 (M+H)+.
Получение 326
Метил 4-[5-[4-(8-метоксиоктилокси)фенил]-1,2,4-оксадиазол-2-ил]бензоат
ИК (KBr): 2925, 2858, 1722, 1614, 1280, 1259 см-1
ЯМР (CDCl3, δ): 1.3-1.9 (12H, m), 3.36 (3H, s), 3.37 (2H, t, J = 6.4 Hz), 3.97 (3H, s), 4.04 (2H, t, J = 6.5 Hz), 7.02 (2H, d, J = 8.9 Hz), 8.07 (2H, d, J = 8.9 Hz), 8.20 (4H, s)
АПХИ-МС: m/z = 439 (M+H+).
Получение 327
Метил 4-[5-(4-н-октилоксифенил)-1,3,4-оксадиазол-2-ил]бензоат
ИК (KBr): 2923, 2856, 1722, 1614, 1496, 1282, 1103 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.8 Hz), 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.97 (3H, s), 4.04 (2H, t, J = 6.5 Hz), 7.03 (2H, d, J = 8.7 Hz), 8.07 (2H, d, J = 8.7 Hz), 8.19 (4H, m)
АПХИ-МС: m/z = 409 (M+H+).
Получение 328
Суспензию 1-(4-гексилоксибензоил)-2-(4-метоксикарбонилбензоил)гидразина (1,0 г) и дипентасульфида фосфора (1,28 г) в тетрагидрофуране (15 мл) размешивали в течение 3 часов при комнатной температуре. Полученную смесь разбавляли водой (30 мл), размешивали в течение 30 минут и экстрагировали дихлорметаном. Органический слой промывали рассолом, осушали сульфатом магния и выпаривали при пониженном давлении. Остаток растирали с ацетонитрилом. Твердое вещество собирали путем фильтрации и осушали при пониженном давлении, в результате чего получали метил 4-[5-(4-н-гексилоксифенил)-1,3,4-тиадиазол-2-ил]бензоат (816 мг).
ИК (KBr): 2925, 2871, 1722, 1608, 1436, 1276, 1106 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J = 6.6 Hz), 1.3-2.0 (8H, m), 3.96 (3H, s), 4.03 (2H, t, J = 6.5 Hz), 6.99 (2H, d, J = 8.6 Hz), 7.95 (2H, d, J = 8.4 Hz), 8.16 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 397 (M+H)+.
Нижеследующие соединения (Получения 329-334) были получены способом, описанным в Получении 328.
Получение 329
Метил 4-[5-[4-(8-метоксиоктилокси)фенил]-1,3,4-тиадиазол-2-ил]бензоат
ИК (KBr): 3210, 2935, 2856, 1718, 1600, 1465, 1280, 1110 см-1
ЯМР (CDCl3, δ): 1.3-1.6 (10H, m), 1.7-1.9 (2H, m), 3.33 (3H, s), 3.37 (2H, d, J = 6.4 Hz), 3.96 (3H, s), 4.03 (2H, t, J = 6.5 Hz), 6.99 (2H, d, J = 8.9 Hz), 7.94 (2H, d, J = 8.9 Hz), 8.07 (2H, d, J = 8.6 Hz), 8.16 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 455 (M+H+).
Получение 330
Метил 4-[5-(4-циклогексилфенил)-1,3,4-тиадиазол-2-ил]бензоат
ИК (KBr): 2925, 2850, 1716, 1432, 1274, 1108, 997 см-1
ЯМР (CDCl3, δ): 1.2-1.6 (5H, m), 1.7-2.0 (5H, m), 2.58 (1H, m), 3.96 (3H, s), 7.34 (2H, d, J = 8.2 Hz), 7.93 (2H, d, J = 8.2 Hz), 8.07 (2H, d, J = 8.6 Hz), 8.16 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 379 (M+H+).
Получение 331
Метил 4-[5-[4-(пиперидин-1-ил)фенил]-1,3,4-тиадиазол-2-ил]бензоат
ИК (KBr): 2940, 2848, 1720, 1602, 1436, 1415, 1276, 1108 см-1
ЯМР (CDCl3, δ): 1.68 (6H, br), 3.34 (4H, br), 3.96 (3H, s), 6.95 (2H, d, J = 8.7 Hz), 7.88 (2H, d, J = 8.7 Hz), 8.05 (2H, d, J = 8.6 Hz), 8.16 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 380 (M+H+).
Получение 332
Метил 4-[5-(4-н-октилоксифенил)-1,3,4-тиадиазол-2-ил]бензоат
ИК (KBr): 2927, 2858, 1720, 1606, 1434, 1276, 1106 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.8 Hz), 1.2-1.6 (10H, m), 1.7-1.9 (2H, m), 3.96 (3H, s), 4.03 (2H, t, J = 6.5 Hz), 7.00 (2H, d, J = 8.9 Hz), 7.95 (2H, d, J = 8.9 Hz), 8.06 (2H, d, J = 8.4 Hz), 8.16 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 425 (M+H+).
Получение 333
Метил 4-[5-(4-транс-н-пентилциклогексил)-1,3,4-тиадиазол-2-ил]бензоат
ИК (KBr): 2923, 2850, 1722, 1440, 1276, 1110 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.9 Hz), 1.0-1.8 (13H, m), 1.92 (2H, d, J = 13.4 Hz), 2.24 (2H, d, J = 12.2 Hz), 3.15 (1H, tt, J = 12.2 and 3.5 Hz), 3.95 (3H, s), 8.01 (2H, dd, J = 8.6, 2.0 Hz), 8.13 (2H, dd, J = 8.6, 2.0 Hz)
АПХИ-МС: m/z = 373 (M+H+).
Получение 334
Метил 4-[5-[4-(4-н-пропилоксифенил)фенил]-1,3,4-тиадиазол-2-ил]бензоат
ИК (KBr): 1720, 1540, 1508, 1282 см-1
ЯМР (CDCl3, δ): 1.07 (3H, t, J = 7.5 Hz), 1.85 (2H, m), 3.9-4.1 (5H, m), 7.01 (2H, d, J = 8.8 Hz), 7.59 (2H, d, J = 8.8 Hz), 7.70 (2H, d, J = 8.4 Hz), 8.07 (2H, d, J = 8.4 Hz), 8.1-8.2 (4H, m)
АПХИ-МС: m/z = 431 (M+H)+.
Получение 335
К суспензии 4-гексилоксибензойной кислоты в оксалилхлориде (10 мл) и дихлорметане (10 мл) добавляли N, N-диметилформамид (0,1 мл). Полученную смесь размешивали в течение 2 часов при комнатной температуре. Растворитель удаляли при пониженном давлении и получали сырой 4-гексилоксибензоилхлорид. К суспензии этил 3-амино-4-гидроксибензоата (733 мг) и триэтиламина (1,38 мл) и 4-диметиламинопиридина (DMAP, 10 мг) в метиленхлориде (10 мл) по капле добавляли (при 10oC) раствор 4-гексилоксибензоилхлорида в дихлорметане (5 мл), полученного выше. Реакционную смесь размешивали 1,5 часа при 10oC, а затем разбавляли дихлорметаном (20 мл). Раствор последовательно промывали водой (20 мл), 1 н. вод. HCl (20 мл х 2), водой (20 мл) и рассолом (20 мл). Органический слой осушали сульфатом магния и растворитель удаляли при пониженном давлении. К остатку добавляли толуол (15 мл) и п-толуолсульфоновую кислоту (10 мг). Смесь нагревали с обратным холодильником в течение 6 часов и растворитель удаляли при пониженном давлении. Остаток растирали с ацетонитрилом и осадок собирали путем фильтрации, после чего его осушали PO5 и получали 2-(4-гексилоксифенил)-5-этоксикарбонилбензоксазол (0,60 г).
ИК (KBr): 2952, 2871, 1712, 1623, 1500, 1294, 1255 см-1
ЯМР (CDCl3, δ): 0.92 (3H, t, J = 6.6 Hz), 1.3-1.6 (9H, m), 1.7-1.9 (2H, m), 4.05 (2H, t, J = 6.5 Hz), 4.42 (2H, q, J = 7.1 Hz), 7.03 (2H, d, J = 6.9 Hz), 7.57 (1H, d, J = 8.6 Hz), 8.08 (1H, dd, J = 8.6 and 1.7 Hz), 8.18 (2H, d, J = 6.9 Hz), 8.43 (1H, d, J = 1.7 Hz)
АПХИ-МС: m/z = 368 (M+H+).
Нижеследующие соединения (получения 336-337) были получены способом, описанным в Получении 335.
Получение 336
5-Этоксикарбонил-2-(2-октилоксипиридин-5-ил)бензоксазол
ИК (KBr): 2933, 2858, 1716, 1623, 1604, 1577, 1467, 1290, 1213, 1083 см-1
ЯМР (CDCl3, δ): 0.89 (3H, t, J = 6.7 Hz), 1.2-1.5 (10H, m), 1.43 (3H, t, J = 7.1 Hz), 1.7-1.9 (2H, m), 4.3-4.5 (4H, m), 6.87 (1H, d, J = 8.7 Hz), 7.60 (1H, d, J = 8.6 Hz), 8.11 (1H, dd, J = 8.6 and 1.6 Hz), 8.37 (1H, dd, J = 8.8 and 2.4 Hz), 8.45 (1H, d, J = 1.6 Hz), 9.03 (1H, d, J = 2.4 Hz)
АПХИ-МС: m/z = 397 (M+H+).
Получение 337
2-[4-(4-Гексилоксифенил)фенил]-5-этоксикарбонилбензоксазол
ИК (KBr): 2952, 2871, 1712, 1623, 1500, 1294, 1255, 1024 см-1
ЯМР (CDCl3, δ): 0.90 (3H, t, J = 6.6 Hz), 1.2-1.5 (6H, m), 1.44 (3H, t, J = 7.1 Hz), 1.6-1.8 (2H, m), 2.67 (2H, t, J = 7.3 Hz), 4.43 (2H, q, J = 7.1 Hz), 7.27 (1H, d, J = 3.7 Hz), 7.32 (1H, s), 7.5-7.7 (3H, m), 7.77 (2H, d, J = 8.6 Hz), 8.12 (1H, dd, J = 8.6 and 1.7 Hz), 8.32 (2H, d, J = 8.5 Hz), 8.48 (1H, d, J = 1.2 Hz)
АПХИ-МС: m/z = 428 (M+H+).
Получение 338
Суспензию 4-[4-(8-бромоктилокси)фенил] бензойной кислоты (1 г) в 2,6-диметилморфолине (3,06 мл) нагревали с обратным холодильником в течение 30 минут. Реакционную смесь добавляли к смеси воды и этилацетата и pH этой смеси доводили до 2,0 с помощью конц. HCl. Органический слой отделяли и осушали сульфатом магния. Затем сульфат магния отфильтровывали и фильтрат выпаривали при пониженном давлении, в результате чего получали гидрохлорид 4-[4-[8-(2,6-диметилморфолин-4-ил)октилокси] фенил] бензойной кислоты (0,95 г).
ИК (KBr): 2939,0; 1704,8; 1606,4; 1189,9 см-1
ЯМР (DMSO-d6, δ): 1.12 (6H, d, J = 6.3 Hz), 1.2-1.6 (10H, m), 1.6-1.9 (4H, m), 2.4-2.7 (2H, m), 2.9-3.1 (2H, m), 3.8-4.0 (2H, m), 4.02 (2H, t, J = 6.3 Hz), 7.04 (2H, d, J = 8.8 Hz), 7.68 (2H, d, J = 8.8 Hz), 7.75 (2H, d, J = 8.4 Hz), 7.99 (2H, d, J = 8.4 Hz)
АПХИ-МС: m/z = 440 (M+H+).
Получение 339
Гидрид натрия (60% суспензия в минеральном масле, 108 мг) добавляли к этоксиэтанолу (10 мл) и полученный раствор размешивали 20 минут при 60oC. Затем к раствору добавляли метил 4-[4-(8-бромоктилокси)фенил]бензоат (1,26 г) и реакционную смесь размешивали в течение 2 часов при 70oC. К реакционной смеси добавляли 10% водный раствор гидроксида натрия (2,4 мл) и раствор размешивали в течение 1 часа при 70oC. После охлаждения pH раствора доводили до 2,0 с помощью 1 н. соляной кислоты. Осадок собирали путем фильтрации и осушали, в результате чего получали 4-[4-[8-(2-этоксиэтокси)октилокси]фенил] бензойную кислоту (1,13 г).
ИК (KBr): 2933, 2858, 1685, 1604, 1434, 1294, 1132 см-1
ЯМР (DMSO-d6, δ): 1.09 (3H, t, J = 7.0 Hz), 1.2-1.9 (14H, m), 3.2-3.6 (6H, m), 4.01 (2H, d, J = 6.3 Hz), 7.04 (2H, d, J = 8.8 Hz), 7.67 (2H, d, J = 8.8 Hz), 7.74 (2H, d, J = 8.5 Hz), 7.98 (2H, d, J = 8.5 Hz)
АПХИ-МС: m/z = 415 (M+H+).
Нижеследующее соединение получали способом, описанным в Получении 300.
Получение 340
4-н-Пентилоксибензоилгидразин
ИК (KBr): 3182, 2937, 2869, 1645, 1618, 1571, 1251 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, d, J = 7.1 Hz), 1.2-1.8 (6H, m), 4.00 (2H, t, J = 6.5 Hz), 4.41 (2H, s), 6.96 (2H, d, J = 8.8 Hz), 7.78 (2H, d, J = 8.8 Hz), 9.59 (1H, s)
АПХИ-МС: m/z = 223 (M+H+).
Нижеследующее соединение было получено способом, описанным в Получении 291.
Получение 341
1-(4-Метоксикарбонилбензоил)-2-(4-н-пентилоксибензоил)гидразин
ИК (KBr): 3234, 2956, 2931, 1724, 1683, 1643, 1610, 1284, 1253 см-1
ЯМР (DMSO-d6, δ): 0.90 (3H, t, J = 6.9 Hz), 1.2-1.5 (4H, m), 1.6-1.8 (2H, m), 3.90 (3H, s), 4.04 (2H, t, J = 6.5 Hz), 7.04 (2H, d, J = 8.8 Hz), 7.90 (2H, d, J = 8.8 Hz), 8.03 (2H, d, J = 8.7 Hz), 8.10 (2H, d, J = 8.7 Hz), 10.42 (1H, s), 10.64 (1H, s)
АПХИ-МС: m/z = 385 (M+H+).
Нижеследующее соединение было получено способом, описанным в Получении 328.
Получение 342
Метил 4-[5-(4-н-пентилоксифенил)тиадиазол-2-ил]бензоат
ИК (KBr): 2940, 2871, 1720, 1606, 1438, 1280 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 7.1 Hz), 1.3-1.6 (4H, m), 1.3-2.0 (2H, m), 3.96 (3H, s), 4.03 (2H, t, J = 6.5 Hz), 6.99 (2H, d, J = 8.8 Hz), 7.94 (2H, d, J = 8.8 Hz), 8.06 (2H, d, J = 8.7 Hz), 8.16 (2H, d, J = 8.7 Hz)
АПХИ-МС: m/z = 383 (M+H+).
Нижеследующее соединение было получено способом, описанным в Получении 32.
Получение 343
4-[5-(4-н-Пентилоксифенил)тиадиазол-2-ил]бензойная
кислота
ИК (KBr): 2954, 2867, 1687, 1602, 1432, 1294, 1255 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J = 7.0 Hz), 1.3-1.5 (4H, m), 1.7-1.9 (2H, m), 4.07 (2H, t, J = 6.7 Hz), 7.13 (2H, d, J = 8.8 Hz), 7.97 (2H, d, J = 8.8 Hz), 8.07 (4H, s)
АПХИ-МС: m/z = 369 (M+H+).
Нижеследующее соединение было получено способом, описанным в Получении 49.
Получение 344
1-[4-[5-(4-н-Пентилоксифенил)тиадиазол-2-ил] бензоил] бензотриазола 3-оксид
ИК (KBr): 2948, 2873, 1770, 1602, 1257, 1232 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 7.1 Hz), 1.3-1.6 (4H, m), 1.8-2.0 (2H, m), 4.04 (2H, t, J = 6.5 Hz), 7.01 (2H, d, J = 8.1 Hz), 7.4-7.7 (3H, m), 7.97 (2H, d, J = 8.1 Hz), 8.12 (1H, d, J = 8.2 Hz), 8.24 (2H, d, J = 8.0 Hz), 8.40 (2H, d, J = 8.0 Hz)
АПХИ-МС: m/z = 486 (M+H*)*
Получение 345
К раствору хлорида оксима 4-бромбензальдегида (647 мг) и 4-н-пентилоксифенилацетилена (650 мг) в тетрагидрофуране (7 мл) по капле при 40oC добавляли триэтиламин (0,5 мл) в тетрагидрофуране. Полученный раствор размешивали в течение 30 минут при 40oC, выливали в воду и экстрагировали этилацетатом. Органический слой промывали водой и рассолом, а затем осушали сульфатом магния. Растворители удаляли при пониженном давлении и остаток растирали с ацетонитрилом. Осадок собирали путем фильтрации и осушали, в результате чего получали 4-[5-(4-н-пентилоксифенил)изоксазол-3-ил]бромбензол (0,59 г).
ИК (KBr): 2948, 2867, 1612, 1430, 1255 см-1
ЯМР (CDCl3, δ): 0.95 (3H, t, J = 6.9 Hz), 1.3-1.6 (4H, m), 1.7-1.9 (2H, m), 4.01 (2H, t, J = 6.5 Hz), 6.66 (1H, s), 6.98 (2H, d, J = 8.8 Hz), 7.60 (2H, d, J = 8.6 Hz), 7.7-7.9 (4H, m)
АПХИ-МС: m/z = 388 (M+H+).
Получение 346
К суспензии 4-[5-(4-н-пентилоксифенил)изоксазол-3-ил] бромбензола (386 мг) в тетрагидрофуране (5 мл) добавляли при -40oC в потоке N2 1,55 М н-бутиллития в гексане (0,84 мл) и раствор размешивали в течение 1 часа при -40oC. К этому раствору добавляли колотый сухой лед (1 г) и суспензию размешивали в течение 1 часа при -40oC. Указанную суспензию разбавляли водой и подкисляли 1 н. соляной кислотой. Осадок собирали путем фильтрации и осушали, в результате чего получали 4-[5-(4-н-пентилоксифенил)изоксазол-3-ил]бензойную кислоту (312 мг).
ИК (KBr): 2939, 2867, 1681, 1614, 1429, 1255, 1178, 821 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J = 7.1 Hz), 1.3-1.5 (4H, m), 1.6-1.8 (2H, m), 4.04 (2H, t, J = 6.5 Hz), 7.11 (2H, d, J = 8.9 Hz), 7.54 (1H, s), 7.85 (2H, d, J = 8.9 Hz), 7.98 (2H, d, J = 8.6 Hz), 8.11 (2H, d, J = 8.6 Hz)
АПХИ-МС: m/z = 352 (M+H+).
Исходное соединение в нижеприведенных Примерах 1-117 и целевые соединения (1)-(122) и (124) в нижеприведенных Примерах 1-122 и 124 могут быть представлены следующими химическими формулами.
Исходное соединение (соединение в Примерах 1-117)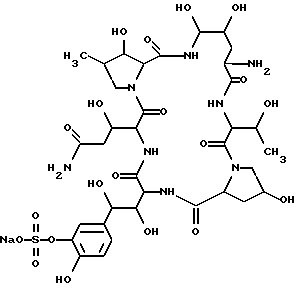
Целевые соединения (1)-(122) и (124)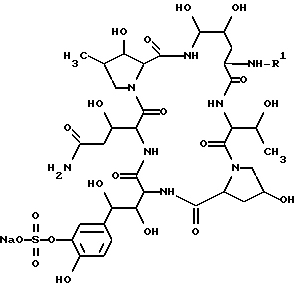
В Примерах (см. табл. 1) "целевое соединение (X)" (например, "целевое соединение (1)") означает целевое соединение Примера (X) (например, целевое соединение Примера (1)).
Пример 1
К раствору исходного соединения (1 г) и 3-оксида 1-(6-октил-оксиметилпиколиноил)бензотриазола (0,399 г) в N,N-диметилформамиде (10 мл) добавляли 4-(N, N-диметиламино)пиридин (0,140 г) и полученную смесь перемешивали в течение 12 часов при комнатной температуре. Затем реакционную смесь обрабатывали этилацетатом. Образовавшийся осадок собирали путем фильтрации и осушали при пониженном давлении. После этого порошок растворяли в воде и подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4) (торговая марка; поставляемой от Dow Chemical), используя в качестве элюента воду. Фракции, содержащие нужное соединение, объединяли и подвергали колоночной хроматографии на ODS (УМС-гель·ODS-AM·S-50) (торговая марка; от Yamamura Chemical Lab. ), используя в качестве элюента 50% водный раствор метанола. Фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления метанола. Остаток лиофилизовали, в результате чего получали целевое соединение (I).
ИК (KBr): 3347, 1664, 1629, 1517 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.98 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 6.0 Hz), 1.2-1.47 (10H, m), 1.47-1.67 (2H, m), 1.67-2.06 (3H, m), 2.06-2.5 (4H, m), 3.19 (1H, m), 3.53 (2H, t, J = 6.4 Hz), 3.5-3.85 (2H, m), 3.85-4.7 (13H, m), 5.35 (11H, m), 5.56 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.3 Hz), 6.83 (1H, d, J = 8.3 Hz), 6.89 (1H, s), 7.05 (1H, s), 7.11 (1H, s), 7.32 (1H, m), 7.43 (1H, d, J = 8.5 Hz), 7.63 (1H, d, J = 7.3 Hz), 7.85-8.13 (4H, m), 8.66 (1H, d, J = 7.8 Hz), 8.84 (1H, s)
FAB (FAB = бомбардировка быстрыми атомами) - масс-спектр: m/z = 1228 (M++Na).
Элементный анализ для C50H72N9O22SNa·6H2O:
Вычислено: C 45,49; H 6,44; N 9,59
Найдено: C 45,89; H 6,52; N 9,69.
Целевые соединения (2)-(25) были получены способом, описанным в Примере 1.
Пример 2
ИК (KBr): 3353, 1666, 1510, 1236 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.8 Hz), 1.2-1.5 (10H, m), 1.55-2.05 (5H, m), 2.11-2.7 (4H, m), 3.0-3.3 (5H, m), 3.3-3.5 (4H, m), 3.6-4.5 (15H, m), 4.6-5.6 (12H, m), 6.6-7.2 (10H, m), 7.2-7.5 (3H, m), 7.81 (2H, d, J = 8.8 Hz), 8.05 (1H, d, J = 8.7 Hz), 8.28 (1H, d, J = 8.7 Hz), 8.41 (1H, d, J = 6.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1373 (M++Na).
Элементный анализ для C60H83N10O22SNa·4H2O:
Вычислено: C 50,63; H 6,44; N 9,84
Найдено: C 50,59; H 6,59; N 9,79.
Пример 3
ИК (KBr): 3350, 1664, 1627, 1047 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.6 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.15-1.53 (8H, m), 1.55-2.1 (9H, m), 2.1-2.45 (3H, m), 2.5-2.7 (1H, m), 3.18 (1H, m), 3.6-3.83 (2H, m), 3.83-4.6 (17H, m), 4.7-5.4 (11H, m), 5.51 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.83 (1H, d, J = 8.2 Hz), 6.85 (1H, s), 7.03 (2H, d, J = 8.4 Hz), 7.05 (1H, s), 7.30 (1H, s), 7.2-7.5 (2H, m), 7.67 (2H, d, J = 8.4 Hz), 7.71 (2H, d, J = 7.4 Hz), 7.94 (1H, s), 7.96 (2H, d, J = 7.4 Hz), 8.06 (1H, d, J = 8.0 Hz), 8.25 (1H, d, J = 6.7 Hz), 8.50 (1H, s), 8.74 (1H, d, J = 6.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1356 (M++Na).
Элементный анализ для C58H76N11O22SNa·4H2O:
Вычислено: C 49,53; H 6,02; N 10,95
Найдено: C 49,26; H 6,22; N 10,77.
Пример 4
ИК (KBr): 3350, 1660, 1631, 1047 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.9 Hz), 0.97 (3H, d, J = 6.6 Hz), 1.09 (3H, d, J = 5.3 Hz), 1.2-1.5 (10H, m), 1.37 (6H, s), 1.55-2.0 (5H, m), 2.1-2.6 (4H, m), 3.16 (1H, m), 3.73 (2H, m), 3.89 (2H, t, J = 6.3 Hz), 3.95-4.49 (11H, m), 4.68-5.21 (10H, m), 5.25 (1H, d, J = 4.1 Hz), 5.53 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.75-6.85 (4H, m), 6.91 (1H, d, J = 8.2 Hz), 7.05 (1H, s), 7.15 (1H, s), 7.3-7.5 (2H, m), 7.9-8.2 (3H, m), 8.84 (1H, s)
FAB-МС: m/z = 1271 (M++Na).
Элементный анализ для C53H77N8O23SNa·4H2O:
Вычислено: C 48,18; H 6,48; N 8,48
Найдено: C 48,04; H 6,51; N 8,38.
Пример 5
ИК (KBr): 1666, 1629, 1222 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.6 Hz), 0.9-1.12 (6H, m), 1.12-1.52 (13H, m), 1.52-1.93 (5H, m), 2.08-2.55 (4H, m), 3.16 (1H, m), 3.6-5.3 (26H, m), 5.49 + 5.54 (1H, d, J = 5.8 Hz, mixture of diastereomer), 6.60-7.1 (7H, m), 7.04 (1H, s), 7.1 (1H, m), 7.2-7.5 (2H, m), 7.9-8.43 (3H, m), 8.83 (1H, s)
FAB-МС: m/z = 1257 (M++Na).
Элементный анализ для C52H75N8O23SNa·3H2O:
Вычислено: C 48,14; H 6,33; N 8,69
Найдено: C 48,16; H 6,51; N 8,53.
Пример 6
ИК (KBr): 3349, 1666, 1629, 1259 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.9 (3H, d, J = 5.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.1-1.55 (19H, m), 1.55-2.0 (5H, m), 2.0-2.47 (4H, m), 2.65-3.25 (3H, m), 3.5-5.13 (27H, m), 5.17 (1H, d, J = 3.2 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.38 (1H, d, J = 5.9 Hz), 6.5-6.9 (5H, m), 6.9-7.1 (3H, m), 7.2-7.46 (2H, m), 7.7-8.1 (3H, m), 8.83 (1H, s)
FAB-МС: m/z = 1368 (M++Na).
Элементный анализ для C58H84N9O24SNa·5H2O:
Вычислено: C 48,50; H 6,60; N 8,78
Найдено: C 48,47; H 6,83; N 8,78.
Пример 7
ИК (KBr): 3350, 1666, 1502, 1199 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.2-1.5 (10H, m), 1.55-2.0 (5H, m), 2.1-2.6 (4H, m), 3.17 (1H, m), 3.7-4.5 (15H, m), 4.7-5.22 (10H, m), 5.24 (1H, d, J = 4.4 Hz), 5.60 (1H, d, J = 5.9 Hz), 6.68-7.03 (8H, m), 7.04 (1H, s), 7.2-7.42 (2H, m), 7.85-8.1 (3H, m), 8.83 (1H, s)
FAB-МС: m/z = 1229 (M++Na).
Элементный анализ для C50H71N8O23SNa · 5H2O:
Вычислено: C 46,29; H 6,29; N 8,64
Найдено: C 46,39; H 6,05; N 8,72.
Пример 8
ИК (KBr): 3350, 1666, 1631, 1513 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.2 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.04 (3H, d, J = 5.7 Hz), 1.2-1.58 (8H, m), 1.58-2.0 (5H, m), 2.0-2.6 (4H, m), 3.17 (1H, m), 3.6-4.5 (15H, m), 4.63-5.33 (13H, m), 5.53 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.82 (1H, d, J = 8.2 Hz), 6.84 (1H, s), 6.95-7.52 (7H, m), 7.66 (1H, d, J = 7.6 Hz), 7.7-7.9 (3H, m), 8.05 (1H, d, J = 9.1 Hz), 8.15 (1H, d, J = 7.6 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1279 (M++Na).
Элементный анализ для C54H73N8O23SNa · 5H2O:
Вычислено: C 48,14; H 6,21; N 8,32
Найдено: C 48,43; H 6,28; N 8,30.
Пример 9
ИК (KBr): 3347, 2956, 1664, 1633, 1508, 1444, 1268, 1047 см-1
ЯМР (DMSO-d6, δ): 0.9-1.1 (9H, m), 1.06 (3H, d, J = 5.9 Hz), 1.3-1.5 (8H, m), 1.6-2.0 (7H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.6-4.4 (17H, m), 4.7-5.0 (8H, m), 5.09 (1H, d, J = 5.5 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.24 (1H, d, J = 4.5 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 6.98 (1H, d, J = 8.3 Hz), 7.05 (1H, d, J = 1.7 Hz), 7.3-7.6 (5H, m), 8.08 (1H, d, J = 8.9 Hz), 8.25 (1H, d, J = 8.4 Hz), 8.54 (1H, d, J = 7.5 Hz), 8.83 (1H, s)
FAB-МС: m/z = 1257 (M++Na).
Элементный анализ для C52H75N8O23SNa · 4H2O:
Вычислено: C 47,78; H 6,40; N 8,57
Найдено: C 47,88; H 6,71; N 8,53.
Пример 10
ИК (KBr): 3350, 2931, 1664, 1625, 1529, 1440, 1276, 1226, 1047 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.8 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.12 (3H, d, J = 5.9 Hz), 1.2-1.5 (10H, m), 1.6-2.1 (5H, m), 2.1-2.4 (4H, m), 3.1-3.3 (1H, m), 3.5-4.6 (15H, m), 4.7-5.0 (3H, m), 5.0-5.2 (7H, m), 5.27 (1H, d, J = 4.4 Hz), 5.55 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.0-7.2 (4H, m), 7.3-7.6 (2H, m), 7.90 (1H, d, J = 8.8 Hz), 8.0-8.2 (2H, m), 8.8-8.9 (2H, m), 9.06 (1H, d, J = 7.2 Hz)
FAB-МС: m/z = 1281 (M++Na).
Элементный анализ для C53H71N8O24SNa · 5H2O:
Вычислено: C 47,18; H 6,05; N 8,30
Найдено: C 46,97; H 6,27; N 8,22.
Пример 11
ЯМР (DMSO-d6, δ): 0.87-1.05 (6H, m), 1.10 (3H, d, J = 5.7 Hz), 1.3-1.5 (4H, m), 1.6-1.9 (5H, m), 2.2-2.5 (3H, m), 2.6 (1H, m), 3.1-3.2 (1H, m), 3.7-4.5 (15H, m), 4.8-5.1 (8H, m), 5.09 (1H, d, J = 5.64 Hz), 5.16 (1H, d, J = 3.2 Hz), 5.26 (1H, d, J = 4.2 Hz), 5.52 (1H, d, J = 6.0 Hz), 6.73 (2H, d, J = 8.4 Hz), 6.8-6.9 (2H, m), 7.0-7.1 (3H, m), 7.2-7.4 (4H, m), 7.6-7.8 (6H, m), 8.11 (1H, d, J = 8.4 Hz), 8.29 (1H, d, J = 8.4 Hz), 8.51 (1H, d, J = 7.7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1273 (M++Na).
Элементный анализ для C55H71N8O22SNa · 4H2O:
Вычислено: C 49,32; H 6,02; N 8,47
Найдено: C 49,79; H 6,14; N 8,45.
Пример 12
ИК (KBr): 3330, 2929, 1670, 1629, 1533, 1440, 1280, 1226, 1045, 804 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.9 Hz), 1.2-1.6 (10H, m), 1.6-2.0 (5H, m), 2.1-2.5 (4H, m), 3.1-3.3 (1H, m), 3.6-4.5 (15H, m), 4.8-5.1 (9H, m), 5.17 (1H, d, J = 3.0 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.56 (1H, d, J = 5.6 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.83 (1H, d, J = 6.8 Hz), 7.1-7.2 (3H, m), 7.3-7.5 (3H, m), 7.85 (1H, d, J = 8.8 Hz), 8.0-8.2 (3H, m), 8.84 (1H, s), 8.96 (1H, d, J = 7.2 Hz)
FAB-МС: m/z = 1269 (M++Na).
Элементный анализ для C52H71N8O22S2Na · 4H2O:
Вычислено: C 47,34; H 6,04; N 8,49
Найдено: C 47,21; H 5,96; N 8,41.
Пример 13
ИК (KBr): 3345, 2927, 1664, 1629, 1515, 1442, 1274, 1047 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.7 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.10 (3H, d, J = 5.9 Hz), 1.2-1.4 (10H, m), 1.5-2.5 (8H, m), 2.46 (3H, s), 2.69 (2H, t, J = 7.7 Hz), 3.1-3.4 (2H, m), 3.6-4.5 (17H, m), 4.8-5.2 (8H, m), 6.7-7.0 (3H, m), 7.05 (1H, d, J = 1.7 Hz), 7.14 (1H, s), 7.3-7.6 (5H, m), 8.0-8.2 (2H, m), 8.47 (1H, d, J = 7.0 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1251 (M++Na).
Элементный анализ для C53H73N8O22SNa · 3H2O:
Вычислено: C 49,61; H 6,21; N 8,73
Найдено: C 49,88; H 6,44; N 8,74.
Пример 14
ИК (KBr): 3340, 1672, 1627, 1542, 1513, 1440, 1268, 1045 см-1
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J = 6.7 Hz), 0.94 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 6.0 Hz), 1.2-1.4 (12H, m), 1.6-2.0 (5H, m), 2.1-2.4 (3H, m), 2.6 (1H, m), 2.96 (2H, t, J = 7.4 Hz), 3.1-3.3 (1H, m), 3.6-4.5 (13H, m), 4.7-5.2 (11H, m), 5.50 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 7.04 (1H, s), 7.2-7.5 (3H, m), 7.72 (1H,d, J = 8.5 Hz), 7.91 (1H, d, J = 8.4 Hz), 8.05 (1H, d, J = 8.4 Hz), 8.2-8.4 (1H, m), 8.80 (1H, d, J = 7.7 Hz), 8.83 (1H, s)
FAB-МС: m/z = 1252 (M++Na).
Элементный анализ для C52H72N9O22SNa · 6H2O:
Вычислено: C 46,67; H 6,33; N 9,42
Найдено: C 46,72; H 6,53; N 9,45.
Пример 15
ИК (KBr): 3350, 2935, 1664, 1627, 1517, 1446, 1251, 1045 см-1
ЯМР (DMSO-d6, δ): 0.90-1.1 (6H, m), 1.10 (3H, d, J = 5.9 Hz), 1.2-1.4 (6H, m), 1.6-2.4 (8H, m), 2.6-2.7 (1H, m), 3.1-3.3 (1H, m), 3.7-4.5 (16H, m), 4.7-5.4 (11H, m), 5.51 (1H, d, J = 5.6 Hz), 6.7-7.0 (3H, m), 7.0-7.6 (7H, m), 7.74 (1H, d, J = 8.6 Hz), 8.0-8.4 (5H, m), 8.7-8.8 (1H, m), 8.84 (1H, s)
FAB-МС: m/z = 1301 (M++Na).
Элементный анализ для C55H71N10O22SNa·6H2O:
Вычислено: C 47,62; H 6,03; N 10,01
Найдено: C 47,65; H 6,03; N 10,03.
Пример 16
ИК ("Нуджол"): 3353, 1668, 1627, 1540, 1515, 1500 см-1
ЯМР (DMSO-d6, δ): 0.80-1.00 (6H, m), 1.06 (3H, d, J = 5.9 Hz), 1.20-1.53 (4H, m), 1.60-1.95 (5H, m), 2.00-2.65 (8H, m), 2.80 (2H, t, J = 7.5 Hz), 3.05-3.45 (1H, m} , 3.50-3.85 (2H, m), 3.90-4.48 (11H, m), 4.65-5.38 (11H, m), 5.47 (1H, d, J = 6.0 Hz), 6.65-6.90 (2H, m), 6.90-7.10 (2H, m), 7.10-7.65 (11H, m), 7.90-8.25 (2H, m), 8.30 (1H, d, J = 7.8 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1275,3 (M++Na).
Элементный анализ для C55H73N8O22SNa·3H2O:
Вычислено: C 50,53; H 6,09; N 8,57
Найдено: C 50,48; H 6,39; N 8,57.
Пример 17
ИК ("Нуджол"): 3351, 1656, 1623, 1538, 1515 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.8 Hz), 1.15-1.40 (8H, m), 1.50-2.00 (5H, m), 2.10-2.48 (4H, m), 2.52-2.70 (2H, m), 3.05-3.28 (1H, m), 3.60-4.50 (13H, m), 4.70-5.20 (9H, m), 5.25 (1H, d, J = 4.6 Hz), 5.52 (1H, d, J = 6.0 Hz), 6.68-6.92 (4H, m), 7.04 (1H, d, J = 1.0 Hz), 7.22-7.50 (5H, m), 7.55-7.82 (7H, m), 8.14 (1H, d, J = 8.4 Hz), 8.31 (1H, d, J = 8.4 Hz), 8.54 (1H, d, J = 7.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1285 (M++Na).
Пример 18
ИК ("Нуджол"): 3351, 1668, 1627, 1540, 1515 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.8 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.8 Hz), 1.17-1.48 (4H, m), 1.50-1.95 (5H, m), 2.05-2.70 (8H, m), 2.70-2.95 (2H, m), 3.05-3.30 (1H, m), 3.60-3.90 (2H, m), 3.90-4.50 (11H, m), 4.65-5.10 (9H, m), 5.15 (1H, d, J = 3.2 Hz), 5.23 (1H, d, J = 4.2 Hz), 5.48 (1H, d, J = 6.0 Hz), 6.67-6.90 (3H, m), 7.03 (1H, d, J = 1.5 Hz), 7.15-7.80 (11H, m), 8.00-8.20 (2H, m), 8.29 (1H, d, J = 7.8 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1259 (M++Na).
Элементный анализ для C55H73N8O21SNa·6H2O:
Вычислено: C 50,30; H 6,52; N 8,53
Найдено: C 50,42; H 6,50; N 8,45.
Пример 19
ИК ("Нуджол"): 3351, 1668, 1652, 1623, 1540 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 6.0 Hz), 1.25-1.45 (4H, m), 1.50-2.00 (5H, m), 2.05-2.48 (4H, m), 2.50-2.75 (2H, m), 3.60-4.50 (13H, m), 4.68-5.25 (10H, m), 5.27 (1H, d, J = 4.5 Hz), 5.53 (1H, d, J = 6.0 Hz), 6.67-6.98 (4H, m), 7.05 (1H, d, J = 1.0 Hz), 7.22-7.58 (5H, m), 7.58-7.90 (7H, m), 8.16 (1H, d, J = 9.0 Hz), 8.34 (1H, d, J = 8.4 Hz), 8.57 (1H, d, J = 7.7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1258 (M++Na).
Элементный анализ для C55H71N8O21SNa·5H2O:
Вычислено: C 49,84; H 6,15; N 8,45
Найдено: C 49,77; H 6,27; N 8,39.
Пример 20
ИК ("Нуджол"): 3353, 1670, 1629, 1540, 1508 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.5 Hz), 0.97 (3H, d, J = 6.8 Hz), 1.04 (3H, d, J = 5.9 Hz), 1.20-1.58 (8H, m), 1.60-1.96 (5H, m), 2.08-2.60 (6H, m), 2.70-3.00 (2H, m), 3.00-3.40 (1H, m), 3.60-3.85 (2H, m), 3.85-4.50 (13H, m), 4.50-5.60 (12H, m), 6.65-6.90 (3H, m), 7.00-7.15 (3H, m), 7.18-7.50 (4H, m), 7.59 (1H, s), 7.62-7.78 (2H, m), 7.95-8.20 (2H, m), 8.30 (1H, d, J = 7.7 Hz), 8.83 (1H, s)
FAB-МС: m/z = 1277 (M++Na).
Элементный анализ для C55H75N8O22SNa·4H2O:
Вычислено: C 49,77; H 6,30; N 8,44
Найдено: C 49,67; H 6,31; N 8,40.
Пример 21
ИК ("Нуджол"): 3351, 1654, 1623, 1538, 1515 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.7 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.9 Hz), 1.20-1.58 (8H, m), 1.66-1.95 (5H, m), 2.10-2.60 (4H, m), 3.09-3.30 (1H, m), 3.58-4.60 (15H, m), 4.69-5.20 (10H, m), 5.24 (1H, d, J = 4.5 Hz), 5.51 (1H, d, J = 6.0 Hz), 6.68-6.95 (4H, m), 7.04 (1H, d, J = 1.0 Hz), 7.10-7.73 (7H, m), 7.73-7.90 (2H, m), 7.98 (1H, d, J = 1.9 Hz), 8.10 (1H, d, J = 8.4 Hz), 8.32 (1H, d, J = 8.4 Hz), 8.50 (1H, d, J = 7.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1275 (M++Na).
Элементный анализ для C55H73N8O22SNa·5H2O:
Вычислено: C 50,38; H 6,38; N 8,55
Найдено: C 49,98; H 6,37; N 8,41.
Пример 22
ИК (KBr): 3340, 2931, 1664, 1627, 1531, 1444, 1278, 1047 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.96 (3H, d, J = 6.8 Hz), 1.08 (3H, d, J = 5.9 Hz), 1.2-1.4 (6H, m), 1.5-1.7 (2H, m), 1.7-2.1 (3H, m), 2.2-2.4 (3H, m), 2.6-2.7 (3H, m), 3.1-3.2 (1H, m), 3.7-4.6 (13H, m), 4.78 (1H, d, J = 6.0 Hz), 4.8-5.1 (1H, m), 5.09 (1H, d, J = 5.6 Hz), 5.16 (1H, d, J = 3.2 Hz), 5.24 (1H, d, J = 4.4 Hz), 5.52 (1H, d, J = 6.0 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.83 (2H, d, J = 8.3 Hz), 7.05 (1H, s), 7.3-7.5 (5H, m), 7.65 (2H, d, J = 8.2 Hz), 7.74 (2H, d, J = 8.4 Hz), 7.98 (2H, d, J = 8.4 Hz), 8.11 (1H, d, J = 8.4 Hz), 8.31 (1H, d, J = 8.4 Hz), 8.79 (1H, d, J = 7.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1245 (M++Na).
Элементный анализ для C54H71N8O21SNa · 4H2O:
Вычислено: C 50,07; H 6,15; N 8,65
Найдено: C 50,26; H 6,44; N 8,67.
Пример 23
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.8 Hz), 1.05 (3H, d, J = 5.6 Hz), 1.2-1.5 (6H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.0-3.5 (9H, m), 3.6-4.5 (15H, m), 4.6-5.6 (11H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (4H, m), 6.95 (2H, d, J = 8.6 Hz), 7.02 (2H, d, J = 9.2 Hz), 7.04 (1H, s), 7.2-7.5 (3H, m), 7.82 (2H, d, J = 8.6 Hz), 8.06 (1H, d, J = 8 Hz), 8.25 (1H, d, J = 6.7 Hz), 8.43 (1H, d, J = 6.7 Hz), 8.85 (1H, s)
ИК (KBr): 3350, 1668, 1629, 1510 см-1
FAB-МС: m/z = 1345 (M+Na).
Элементный анализ для C58H79N10O22SNa·6H2O:
Вычислено: C 48,67; H 6,41; N 9,78
Найдено: C 48,80; H 6,46; N 9,82.
Пример 24
Главный продукт
ИК (KBr): 3350, 1668, 1631, 1047 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.2-1.6 (10H, m), 1.6-2.4 (8H, m), 2.5-2.7 (1H, m), 3.18 (1H, m), 3.21 (3H, s), 3.29 (2H, t, J = 6.4 Hz), 3.6-3.83 (2H, m), 3.83-4.6 (13H, m), 4.7-5.4 (11H, m), 5.51 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.83 (1H, d, J = 8.2 Hz), 6.85 (1H, s), 7.04 (2H, d, J = 8.4 Hz), 7.06 (1H, s), 7.31 (1H, s), 7.2-7.5 (2H, m), 7.67 (2H, d, J = 8.4 Hz), 7.71 (2H, d, J = 8.4 Hz), 7.96 (2H, d, J = 8.4 Hz), 8.06 (1H, d, J = 8 Hz), 8.25 (1H, d, J = 6.7 Hz), 8.74 (1H, d, J = 6.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1319 (M+Na).
Элементный анализ для C57H77N8O23SNa·4H2O:
Вычислено: C 49,99; H 6,26; N 8,18
Найдено: C 49,74; H 6,27; N 8,06.
Минорный продукт
ИК (KBr): 3350, 1668, 1631 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.2-1.6 (6H, m), 1.6-2.1 (7H, m), 2.1-2.5 (3H, m), 2.5-2.7 (1H, m), 3.18 (1H, m), 3.6-3.8 (2H, m), 3.8-4.6 (13H, m), 4.6-5.2 (12H, m), 5.26 (1H, d, J = 4.6 Hz), 5.53 (1H, d, J = 5.8 Hz), 5.6-6.0 (1H, m), 6.73 (1H, d, J = 8.2 Hz), 6.83 (1H, d, J = 8.3 Hz), 6.85 (1H, s), 7.04 (2H, d, J = 8.5 Hz), 7.06 (1H, s), 7.30 (1H, s), 7.2-7.5 (2H, m), 7.68 (2H, d, J = 8.5 Hz), 7.72 (2H, d, J = 8.5 Hz), 7.96 (2H, d, J = 8.5 Hz), 8.06 (1H, d, J = 8 Hz), 8.25 (1H, d, J = 6.7 Hz), 8.74 (1H, d, J = 6.7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1287 (M+Na).
Элементный анализ для C56H73N8O22S·7H2O:
Вычислено: C 48,34; H 6,30; N 8,05
Найдено: C 48,19; H 6,19; N 7,99.
Пример 25
ИК (KBr): 3350, 2935, 2873, 1668, 1629, 1538, 1506, 1438, 1257, 1049 см-1
ЯМР (DMSO-d6, δ): 0.9-1.0 (6H, m), 1.08 (3H, d, J = 5.7 Hz), 1.2-1.6 (4H, m), 1.6-2.0 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.6-4.6 (15H, m), 4.7-5.2 (10H, m), 5.26 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.9 Hz), 6.7-6.9 (3H, m), 7.0-7.6 (7H, m), 7.85 (2H, d, J = 8.6 Hz), 7.9-8.2 (4H, m), 8.26 (1H, d, J = 7.7 Hz), 8.8-9.0 (2H, m)
FAB-МС: m/z = 1314,3 (M+Na)+.
Элементный анализ для C56H70N9O23NaS·7H2O:
Вычислено: C 47,42; H 5,97; N 8,89
Найдено: C 47,33; H 5,85; N 8,73.
Пример 26
К раствору исходного соединения (1 г) и сукцинимидо 4-(4-октилоксифенил)пиперазин-1-карбоксилата (0,45 г) в N,N-диметилформамиде (10 мл) добавляли 4-диметиламинопиридин (0,141 г) и полученную смесь размешивали в течение пяти дней при температуре 50oC. Реакционную смесь обрабатывали этилацетатом. Осадок собирали путем фильтрации и осушали при пониженном давлении. Затем порошок растворяли в воде и подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4), используя воду в качестве элюента. Фракции, содержащие нужное соединение, объединяли и подвергали колоночной хроматографии на ODS (УМС-гель·ODS-AM·S-50), используя в качестве элюента 50% водный раствор ацетонитрила. Затем фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления ацетонитрила. Полученный остаток лиофилизовали, в результате чего получали целевое соединение (23). Неочищенное целевое соединение в виде порошка очищали посредством препаративной ВРЖХ на смоле C18 Bondapak (Waters Associates, Inc.) и элюировали при помощи системы растворителей (ацетонитрил / (pH = 3) фосфатный буфер = 40:60) на скорости потока 80 мл/минуту с использованием насоса LC-8A Shimadzu. Колонку контролировали посредством УФ-детектора при 240 мкм. После этого фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления ацетонитрила. Образовавшийся остаток подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4), используя в качестве элюента воду. Фракции, содержащие нужное соединение, объединяли и подвергали колоночной хроматографии на ODS (УМС-гель·ODS-AM·S-50), используя в качестве элюента 50% водный раствор ацетонитрила. Фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления ацетонитрила. Затем остаток лиофилизовали, в результате чего получали целевое соединение (23) (60 мг).
ИК (KBr): 3347, 1629, 1511, 1245 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.95 (3H, d, J = 6.8 Hz), 1.06 (3H, d, J = 5.9 Hz), 1.2-1.5 (10H, m), 1.55-1.92 (5H, m), 2.0-2.65 (4H, m), 2.8-3.05 (5H, m), 3.2-4.47 (17H, m), 4.6-5.6 (12H, m), 6.6-7.0 (7H, m), 7.03 (1H, s), 7.2-7.5 (3H, m), 7.9-8.3 (3H, m), 8.84 (1H, s)
FAB-МС: m/z = 1297 (M++Na).
Элементный анализ для C54H79N10O22SNa·6H2O·CH3CN:
Вычислено: C 47,22; H 6,65; N 10,82
Найдено: C 47,58; H 7,05; N 10,85.
Пример 27
К суспензии 1-гидроксибензотриазола (0,53 г) и 2-(4-октилоксифенокси)уксусной кислоты (1 грамм) в дихлорметане (30 мл) добавляли 1-этил-3-(3'-диметиламинопропил)карбодиимида гидрохлорид (WSCD HCl) (0,886 г) и полученную смесь перемешивали в течение трех часов при комнатной температуре. К смеси добавляли воду, а затем органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении и получали 1-[2-(4-октилоксифенокси)ацетил]бензотриазола 3-оксид (892 мг). К раствору исходного соединения (1,79 г) и 3-оксида 1-[2-(4-октилоксифенокси)ацетил] бензотриазола (892 мг) в N,N-диметилформамиде (18 мл) добавляли 4-(N,N-диметиламино)пиридин (0,297 г) и полученную смесь перемешивали в течение 12 часов при комнатной температуре. Затем реакционную смесь обрабатывали этилацетатом. Осадок собирали путем фильтрации и осушали при пониженном давлении. После этого порошок добавляли в воду и подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4), используя в качестве элюента воду. Фракции, содержащие нужное соединение, объединяли и подвергали колоночной хроматографии на ODS (УМС-гель·ODS-AM·S-50), элюируя 50% водным раствором метанола. Затем фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления метанола. После этого остаток лиофилизовали и получали целевое соединение (24) (1,75 г).
ИК (KBr): 3350, 1666, 1629, 1228 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.9 Hz), 0.95 (3H, d, J = 6.7 Hz), 1.04 (2H, d, J = 5.7 Hz), 1.15-1.5 (10H, m), 1.55-2.0 (5H, m), 2.05-2.5 (4H, m), 3.16 (1H, m), 3.72 (2H, m), 3.88 (3H, t, J = 6.3 Hz), 4.41 (2H, s), 3.93-4.6 (11H, m), 4.69-5.25 (10H, m), 5.28 (1H, d, J = 4.3 Hz), 5.57 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (5H, m), 7.04 (1H, s), 7.09 (1H, s), 7.3-7.4 (2H, m), 7.92-8.17 (2H, m), 8.29 (1H, d, J = 7.5 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1243 (M++Na).
Элементный анализ для C51H73N8O23SNa·4H2O:
Вычислено: C 47,36; H 6,31; N 8,66
Найдено: C 47,22; H 6,44; N 8,37.
Целевые соединения (28)-(31) были получены способом, описанным в Примере 27.
Пример 28
ИК (KBr): 3350, 2933, 1664, 1628, 1446, 1205, 1045 см-1
ЯМР (DMSO-d6, δ): 0.8-1.1 (9H, m), 1.2-2.0 (19H, m), 2.1-2.3 (3H, m), 3.6-3.8 (4H, m), 3.9-4.4 (13H, m), 4.6-5.0 (8H, m), 5.07 (1H, d, J = 5.6 Hz), 5.14 (1H, d, J = 3.2 Hz), 5.23 (1H, d, J = 4.3 Hz), 5.46 (1H, d, J = 6.7 Hz), 6.7-6.9 (3H, m), 7.04 (1H, s), 7.2-7.5 (6H, m), 7.8-8.0 (3H, m), 8.05 (1H, d, J = 8.4 Hz), 8.2-8.4 (2H, m), 8.83 (1H, s)
FAB-МС: m/z = 1360 (M++Na).
Элементный анализ для C59H80N9O23SNa·6H2O:
Вычислено: C 48,99; H 6,41; N 8,72
Найдено: C 48,92; H 6,37; N 8,64.
Пример 29
ИК (KBr): 3350, 2927, 1668, 1627, 1535, 1515, 1452, 1440, 1286, 1045 см-1
ЯМР (DMSO-d6, δ): 0.83 (3H, t, J = 6.7 Hz), 0.95 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.9 Hz), 1.2-1.4 (12H, m), 1.6-2.0 (5H, m), 2.1-2.4 (3H, m), 2.6 (1H, m), 2.82 (2H, t, J = 7.4 Hz), 3.1-3.2 (1H, m), 3.6-4.5 (13H, m), 4.7-5.2 (11H, m), 5.4-5.6 (1H, m), 6.72 (1H, d, J = 8.2 Hz), 6.82 (2H, d, J = 8.1 Hz), 7.03 (1H, s), 7.2-7.4 (3H, m), 7.47 (1H, d, J = 8.5 Hz), 7.69 (1H, d, J = 8.5 Hz), 8.1-8.2 (2H, m), 8.23 (1H, d, J = 8.4 Hz), 8.62 (1H, d, J = 7.8 Hz), 8.83 (1H, s)
FAB-МС: m/z = 1251 (M++Na).
Элементный анализ для C52H73N10O21SNa·5H2O:
Вычислено: C 47,34; H 6,34; N 10,61
Найдено: C 47,30; H 6,45; N 10,45.
Пример 30
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.8 Hz), 0.96 (3H, t, J = 6.7 Hz), 1.05 (3H, t, J = 5.8 Hz), 1.2-1.5 (10H, m), 1.6-2.0 (5H, m), 2.2-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.7-4.5 (15H, m), 4.7-5.0 (8H, m), 5.10 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.52 (1H, d, J = 5.8 Hz) 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (3H, m), 7.04 (1H, s), 7.2-7.4 (3H, m), 8.0-8.3 (3H, m), 8.68 (1H, d, J = 2.3 Hz), 8.7-8.8 (1H, m), 8.85 (1H, m)
FAB-МС: m/z = 1214 (M++Na).
Элементный анализ для C49H70N9O22SNa·4H2O:
Вычислено: C 46,55; H 6,22; N 9,97
Найдено: C 46,29; H 6,18; N 9,71.
Пример 31
ИК ("Нуджол"): 3342, 2210, 1668, 1623 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.7 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 6.7 Hz), 1.20-1.60 (8H, m), 1.60-2.00 (5H, m), 2.05-2.50 (4H, m), 3.05-3.30 (1H, m), 3.60-4.60 (15H, m), 4.65-5.18 (10H, m), 5.24 (1H, d, J = 4.5 Hz), 5.58 (1H, d, J = 6.0 Hz), 6.68-7.10 (4H, m), 7.15-7.65 (5H, m), 7.80-8.30 (6H, m), 8.84 (1H, s), 9.18 (1H, d, J = 7.7 Hz)
FAB-МС: m/z = 1273,5 (M++Na).
Пример 32
К раствору 6-гептилокси-2-нафтойной кислоты (0,358 г) и триэтиламина (0,174 мл) в N,N-диметилформамиде (10 мл) добавляли дифенилфосфорилазид (0,4 мл) и полученную смесь перемешивали в течение одного часа при комнатной температуре. Затем реакционную смесь перемешивали в течение одного часа при температуре 100oC. После охлаждения к реакционной смеси добавляли исходное соединение (1 г) и 4-(N,N-диметиламино)пиридин (0,140 г) и эту смесь перемешивали в течение десяти часов при комнатной температуре. После этого реакционную смесь обрабатывали этилацетатом. Осадок собирали путем фильтрации и осушали при пониженном давлении. Порошок растворяли в воде и подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4) с использованием воды в качестве элюента. Фракции, содержащие нужное соединение, объединяли и подвергали колоночной хроматографии на ODS (УМС-гель·ODS-AM·S-50) с использованием в качестве элюента 50% водного раствора ацетонитрила. Фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления ацетонитрила. Затем остаток лиофилизовали, в результате чего получали целевое соединение (29) (0,832 г).
ИК (KBr): 3350, 1664, 1629, 1546, 1240 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.9 Hz), 1.2-1.55 (8H, m), 1.55-2.0 (5H, m), 2.1-2.5 (4H, m), 3.18 (1H, m), 3.6-3.8 (3H, m), 3.9-4.5 (13H, m), 4.7-4.95 (3H, m), 5.0-5.3 (7H, m), 5.59 (1H, d, J = 5.8 Hz), 6.52 (1H, d, J = 8.1 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.83 (1H, d, J = 8.2 Hz), 6.90 (1H, s), 7.0-7.15 (3H, m), 7.20 (1H, s), 7.27-7.4 (3H, m), 7.6-7.7 (2H, m), 7.87 (1H, s), 7.95-8.2 (2H, m), 8.69 (1H, s), 8.85 (1H, s)
FAB-МС: m/z = 1264 (M++Na).
Элементный анализ для C53H72N9O22SNa·5H2O:
Вычислено: C 47,78; H 6,20; N 9,46
Найдено: C 47,65; H 6,42; N 9,34.
Целевое соединение (33) было получено способом, описанным в Примере 32.
Пример 33
ИК (KBr): 3350, 1666, 1629, 1537, 1240 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.7 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.8 Hz), 1.2-1.55 (8H, m), 1.55-2.0 (5H, m), 2.07-2.6 (4H, m), 3.18 (1H, m), 3.6-3.85 (3H, m), 3.9-4.5 (13H, m), 4.7-4.98 (3H, m), 5.0-5.3 (7H, m), 5.57 (1H, d, J = 5.9 Hz), 6.50 (1H, d, J = 8.1 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.82 (1H, dd, J = 8.2 and 1.7 Hz), 6.87 (1H, s), 6.97 (2H, d, J = 8.8 Hz), 7.05 (1H, d, J = 1.7 Hz), 7.10 (1H, s), 7.23-7.43 (2H, m), 7.38 (2H, d, J = 8.8 Hz), 7.50 (2H, d, J = 8.8 Hz), 7.52 (2H, d, J = 8.8 Hz), 8.0-8.15 (2H, m), 8.65 (1H, s), 8.84 (1H, s)
FAB-МС: m/z = 1290 (M++Na).
Элементный анализ для C55H74N9O22SN·7H2O:
Вычислено: C 47,38; H 6,36; N 9,04
Найдено: C 47,67; H 6,53; N 9,03.
Пример 34
Раствор исходного соединения (2,45 г), 3-[4-(4-пентилфенил)фенил]пропиоловой кислоты (0,90 г), 1-этил-3-(3'-диметиламинопропил)карбодиимида гидрохлорида (WSCD·HCl) (0,59 г) и триэтиламина (0,43 мл) в N,N-диметилформамиде (50 мл) размешивали в течение 15 часов при комнатной температуре. Реакционную смесь разводили этилацетатом, а затем полученный осадок собирали путем фильтрации, последовательно промывали этилацетатом и диизопропиловым эфиром и осушали при пониженном давлении. После этого порошок растворяли в воде и подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4*) с использованием воды в качестве элюента. Фракции, содержащие нужное соединение, объединяли и подвергали обращенно-фазовой хроматографии на ODS (УМС-гель, ODS·AM·S-50, 50 мл) с использованием в качестве элюента смеси воды и ацетонитрила (10:0-7:3, об/об). Фракции, содержащие целевое соединение, объединяли и выпаривали при пониженном давлении для удаления ацетонитрила. После этого остаток лиофилизовали, в результате чего получали целевое соединение (31) (1,53 г). (*Na форма, 50 мл)
ИК ("Нуджол"): 3351, 2212, 1668, 1627 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.5 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.8 Hz), 1.20-1.50 (4H, m), 1.50-2.00 (5H, m), 2.03-2.55 (4H, m), 2.62 (2H, t, J = 7.5 Hz), 3.17 (1H, t, J = 8.4 Hz), 3.55-4.57 (15H, m), 4.65-5.13 (9H, m), 5.16 (1H, d, J = 3.2 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.58 (1H, d, J = 5.8 Hz), 6.67-6.90 (3H, m), 6.93-7.10 (2H, m), 7.15-7.50 (4H, m), 7.50-7.90 (6H, m), 8.06 (1H, d, J = 8.4 Hz), 8.15 (1H, d, J = 7.7 Hz), 8.84 (1H, s), 9.19 (1H, d, J = 7.1 Hz)
FAB-МС: m/z = 1255 (M++Na).
Элементный анализ для C55H69N8O21SNa·4H2O:
Вычислено: C 50,61; H 5,95; N 8,58
Найдено: C 50,47; H 6,00; N 8,54.
Пример 35
К суспензии 1-гидроксибензотриазола (501 мг) и 4-(4-гептилфенил)бензойной кислоты (1 г) в дихлорметане (30 мл) добавляли 1-этил-3-(3'-диметиламинопропил) карбодиимида гидрохлорид (WSCD·HCl) (839 мг) и полученную смесь перемешивали влечение 3 часов при комнатной температуре. Затем реакционную смесь помещали в воду. Органический слой отделяли и осушали сульфатом магния. После отфильтровывания сульфата магния фильтрат выпаривали при пониженном давлении и получали 1-[4-(4-гептилфенил)бензоил]бензотриазола 3-оксид. К раствору исходного соединения (2,49 г) и 3-оксида 1-[4-(4-гептилфенил)бензоил] бензотриазола в N,N-диметилформамиде (25 мл) добавляли 4-(N, N-диметиламино)пиридин (381 мг) и полученную смесь размешивали в течение 12 часов при комнатной температуре. Затем реакционную смесь обрабатывали этилацетатом. Осадок собирали путем фильтрации и осушали при пониженном давлении. Полученный остаток растворяли в воде и подвергали колоночной хроматографии на ионообменной смоле (DOWEX-50WX4) с использованием воды в качестве элюента. Фракции, содержащие нужное соединение, объединяли и подвергали колоночной хроматографии на ODS (УМС-гель·ODS-AM·S-50) с использованием в качестве элюента 30% водного раствора ацетонитрила. Фракции, содержащие нужное соединение, объединяли и выпаривали при пониженном давлении для удаления ацетонитрила. После этого остаток лиофилизовали, в результате чего было получено целевое соединение (32) (1,99 г).
ИК ("Нуджол"): 3350, 2852, 1749, 1621, 1457, 1376, 1045 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.9 Hz), 1.5-1.7 (2H, m), 1.7-2.2 (3H, m), 2.2-2.5 (3H, m), 2.6-2.8 (3H, m), 3.1-3.2 (1H, m), 3.7-4.6 (13H, m), 4.7-5.2 (8H, m), 5.12 (1H, d, J = 5.5 Hz), 5.18 (1H, d, J = 2.9 Hz), 5.27 (1H, d, J = 4.4 Hz), 5.54 (1H, d, J = 5.8 Hz), 6.7-6.9 (3H, m), 7.05 (1H, s), 7.2-7.4 (5H, m), 7.65 (2H, d, J = 8.0 Hz), 7.74 (2H, d, J = 8.3 Hz), 7.98 (2H, d, J = 8.3 Hz), 8.11 (1H, d, J = 8.7 Hz), 8.28 (1H, d, J = 8.4 Hz), 8.78 (1H, d, J = 7.3 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1259 (M++Na).
Элементный анализ для C55H73N8O21SNa·5H2O:
Вычислено: C 49,77; H 6,30; N 8,44
Найдено: C 49,98; H 6,44; N 8,41.
Целевые соединения (36)-(107) были получены способом, описанным в Примере 1.
Пример 36
ИК (KBr): 3350, 1675,8, 1629,6, 1515,8 см-1
ЯМР (DMSO-d6, δ): 0.86 (6H, d, J = 6.6 Hz), 0.96 (3H, d, J = 6.6 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.1-1.3 (2H, m), 1.4-2.0 (6H, m), 2.0-2.7 (4H, m), 3.1-3.5 (9H, m), 3.66 (2H, t, J = 7.3 Hz), 3.6-4.5 (13H, m), 4.7-5.6 (12H, m), 6.73 (1H, d, J = 8.3 Hz), 6.82 (1H, d,
J = 8.3 Hz), 6.8-6.9 (1H, m), 7.02 (2H, d, J = 9.0 Hz), 7.04 (1H, s), 7.11 (2H, d, J = 9.0 Hz), 7.2-7.6 (3H, m), 7.50 (2H, d, J = 9.0 Hz), 7.82 (2H, d, J = 9.0 Hz), 8.1 (1H, d, J = 8.5 Hz), 8.28 (1H, d, J = 8.5 Hz), 8.33 (1H, s), 8.45 (1H, d, J = 7.0 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1412 (M+Na).
Элементный анализ для C60H80N13O22Na·9H2O:
Вычислено: C 46,42; H 6,36; N 11,73
Найдено: C 46,64; H 6,43; N 11,62.
Пример 37
ИК (KBr): 3350, 1668,1, 1629,6, 1268,9 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.6 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.9 Hz), 1.2-1.4 (10H, m), 1.4-2.0 (5H, m), 2.0-2.5 (4H, m), 2.61 (2H, t, J = 7.2 Hz), 3.1-3.3 (1H, m), 3.6-4.5 (13H, m), 4.40 (2H, s), 4.6-5.3 (11H, m), 5.60 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.82 (1H, d, J = 8.2 Hz), 6.6-6.9 (1H, m), 7.04 (1H, s), 7.0-7.1 (1H, m), 7.32 (2H, d, J = 8.5 Hz), 7.2-7.5 (2H, m), 7.58 (2H, d, J = 8.5 Hz), 7.93 (1H, d, J = 7 Hz), 8.04 (1H, d, J = 9.4 Hz), 8.41 (1H, s), 8.44 (1H, d, J = 9.4 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1294 (M++Na).
Элементный анализ для C53H74N11O22SNa·7H2O:
Вычислено: C 45,52; H 6,34; N 11,02.
Найдено: C 45,57; H 6,27; N 10,93.
Пример 38
Главный продукт
ИК (KBr): 3349,7, 1670,1, 1627,6, 1508,1 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.6 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.2-1.6. (8H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.0-3.2 (5H, m), 3.21 (3H, s), 3.30 (2H, t, J = 6.5 Hz), 3.3-3.5 (4H, m), 3.6-4.5 (15H, m), 4.7-5.3 (11H, m), 5.49 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.3 Hz), 6.8-6.9 (4H, m), 6.95 (2H, d, J = 9.2 Hz), 7.01 (2H, d, J = 8.5 Hz), 7.04 (1H, s), 7.20 (1H, s), 7.2-7.5 (2H, m), 7.81 (2H, d, J = 8.5 Hz), 8.09 (1H, d, J = 8.7 Hz), 8.28 (1H, d, J = 8.7 Hz), 8.45 (1H, d, J = 6.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1389 (M+Na).
Элементный анализ для C60H83N10O23SNa·8H2O:
Вычислено: C 47,68; H 6,60; N 9,27
Найдено: C 47,83; H 6,72; N 9,27.
Минорный продукт
ИК (KBr): 3338,2, 1646,9, 1511,9 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.3-1.6 (4H, m), 1.6-2.7 (11H, m), 3.0-3.2 (5H, m), 3.3-3.5 (4H, m), 3.6-4.5 (15H, m), 4.7-5.3 (13H, m), 5.48 (1H, d, J = 5.9 Hz), 5.7-6.0 (1H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (4H, m), 6.94 (2H, d, J = 9.3 Hz), 7.01 (2H, d, J = 8.6 Hz), 7.04 (1H, s), 7.2-7.5 (3H, m), 7.81 (2H, d, J = 8.6 Hz), 8.06 (1H, d, J = 8.7 Hz), 8.25 (1H, d, J = 8.7 Hz), 8.42 (1H, d, J = 6.7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1357 (M+Na).
Элементный анализ для C59H79N10O22SNa·9H2O:
Вычислено: C 47,32; H 6,53; N 9,35
Найдено: C 47,08; H 6,66; N 9,25.
Пример 39
ИК (KBr): 3350, 1670,1, 1631,5, 1510,0, 1234,2 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.6 Hz), 1.2-1.5 (8H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.0-3.3 (5H, m), 3.3-3.5 (4H, m), 3.6-3.8 (2H, m), 3.88 (2H, d, J = 6.4 Hz), 3.8-4.5 (11H, m), 4.7-5.1 (8H, m), 5.10 (1H, d, J = 5.6 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.48 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (4H, m), 6.94 (2H, d, J = 9.3 Hz), 7.01 (2H, d, J = 8.7 Hz), 7.04 (1H, s), 7.2-7.5 (3H, m), 7.81 (2H, d, J = 8.7 Hz), 8.06 (1H, d, J = 8 Hz), 8.25 (1H, d, J = 6.7 Hz), 8.43 (1H, d, J = 6.7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1359 (M+Na).
Элементный анализ для C59H81N10O22SNa·5H2O:
Вычислено: C 49,64; H 6,43; N 9,81
Найдено: C 49,49; H 6,54; N 9,72.
Пример 40
ИК (KBr): 3355,5, 1670,1, 1627,6, 1510,0 и 1236,1 см-1
ЯМР (DMSO-d6, δ): 0.89 (6H, d, J = 6.5 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.05 (3H, d, J = 5.7 Hz), 1.2-1.4 (2H, m), 1.5-2.1 (6H, m), 2.1-2.7 (4H, m), 3.0-3.6 (9H, m), 3.6-4.5 (15H, m), 4.5-5.4 (12H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (4H, m), 6.96 (2H, d, J = 9.6 Hz), 7.02 (2H, d, J = 8.7 Hz), 7.05 (1H, s), 7.2-7.5 (3H, m), 7.82 (2H, d, J = 8.7 Hz), 8.08 (1H, d, J = 8 Hz), 8.27 (1H, d, J = 6.7 Hz), 8.46 (1H, d, J = 6.7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1345 (M+Na).
Элементный анализ для C58H79N10O22SNa·8H2O
Вычислено: C 47,47; H 6,52; N 9,54
Найдено: C 47,47; H 6,54; N 9,51.
Пример 41
ИК (KBr): 3347,8, 1668,1, 1629,6, 1510,0, 1234,2 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J = 7.0 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.05 (3H, d, J = 5.8 Hz), 1.2-1.5 (4H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.0-3.6 (9H, m), 3.6-3.8 (2H, m), 3.8-4.5 (13H, m), 4.7-5.6 (12H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (4H, m), 6.96 (2H, d, J = 8.7 Hz), 7.02 (2H, d, J = 9.0 Hz), 7.04 (1H, s), 7.2-7.5 (3H, m), 7.82 (2H, d, J = 8.7 Hz), 8.07 (1H, d, J = 8 Hz), 8.27 (1H, d, J = 6.7 Hz), 8.45 (1H, d, J = 6.7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1331 (M+Na).
Элементный анализ для C57H77N10O22SNa·6H2O:
Вычислено: C 48,30; H 6,33; N 9,88
Найдено: C 48,20; H 6,58; N 10,03.
Пример 42
Продукт смеси ИК (KBr): 3344, 1670,1, 1631,5 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.9 Hz), 1.2-1.5 (8H, m), 1.6-2.1 (7H, m), 2.1-2.7 (4H, m), 3.1-3.3 (1H, m), 3.6-4.5 (15H, m), 4.45 and 4.70 (2H, t, J = 7.1 Hz), 4.6-5.3 (11H, m), 5.52 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.83 (1H, d, J = 8.2 Hz), 6.85 (1H, s), 7.03 (2H, d, J = 8.6 Hz), 7.05 (1H, s), 7.2-7.5 (3H, m), 7.68 (2H, d, J = 8.6 Hz), 7.71 (2H, d, J = 8.4 Hz), 7.96 (2H, d, J = 8.4 Hz), 8.12 (1H, d, J = 8.5 Hz), 8.30 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1357 (M+Na).
Элементный анализ для C57H75N12O22SNa·4H2O:
Вычислено: C 48,64; H 5,94; N 11,94.
Найдено: C 48,91; H 5,88; N 11,86.
Пример 43
ИК (KBr): 3350, 1666,2, 1651,5 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.05 (6H, d, J = 6.3 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.2-1.6 (10H, m), 1.6-2.1 (7H, m), 2.1-2.7 (6H, m), 2.8-3.0 (2H, m), 3.0-3.2 (1H, m), 3.4-3.7 (2H, m), 3.6-3.8 (2H, m), 3.8-4.5 (13H, m), 4.7-5.6 (12H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.03 (2H, d, J = 8.7 Hz), 7.06 (1H, s), 7.2-7.5 (3H, m), 7.67 (2H, d, J = 8.7 Hz), 7.71 (2H, d, J = 8.4 Hz), 7.96 (2H, d, J = 8.4 Hz), 8.04 (1H, d, J = 8.5 Hz), 8.31 (1H, d, J = 8.5 Hz), 8.73 (1H, d, J = 7.0 Hz), 8.90 (1H, s)
FAB-МС: m/z = 1402 (M+Na).
Пример 44
ИК (таблетка KBr): 3350, 2929, 2856, 1670, 1631, 1510, 1243, 1045 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.8 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.6-2.0 (5H, m), 2.2-2.5 (5H, m), 2.6-2.7 (1H, m), 3.0-3.3 (5H, m), 3.6-4.5 (19H, m), 4.77 (2H, d, J = 5.9 Hz), 4.8-5.1 (6H, m), 5.10 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.50 (1H, d, J = 5.8 Hz), 6.7-7.0 (8H, m), 7.04 (1H, s), 7.2-7.4 (3H, m), 8.0-3.2 (2H, m), 8.26 (1H, d, J = 8.0 Hz), 8.55 (1H, d, J = 7.3 Hz), 8.67 (1H, d, J = 1.2 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1374,3 (M+Na+).
Элементный анализ для C59H82N11O22SNa·5,5H2О:
Вычислено: C 48,82; H 6,46; N 10,61
Найдено: C 48,89; H 6,74; N 10,50.
Пример 45
ИК (KBr): 3350, 2935, 1668, 1623, 1538, 1257, 1174, 1047 см-1
ЯМР (DMSO-d6, δ): 0.8-1.1 (6H, m), 1.09 (3H, d, J = 5.7 Hz), 1.2-1.6 (6H, m), 1.7-2.1 (5H, m), 2.2-2.4 (3H, m), 2.5-2.6 (1H, m), 3.6-3.8 (2H, m), 3.8-4.6 (14H, m), 4.8-5.2 (7H, m), 5.18 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.54 (1H, d, J = 5.8 Hz), 6.7-7.5 (9H, m), 7.82 (1H, d, J = 8.5 Hz), 7.96 (1H, d, J = 8.7 Hz), 8.1-8.4 (5H, m), 8.8-9.0 (2H, m)
FAB-МС: m/z = 1302,6 (M+Na+).
Элементный анализ для C55H70N9O23SNa·6H2O:
Вычислено: C 47,58; H 5,95; N 9,08
Найдено: C 47,76; H 6,04; N 9,05.
Пример 46
ИК (KBr): 3355, 2958, 1670, 1627, 1521, 1247, 1047 см-1
ЯМР (DMSO-d6, δ): 0.9-1.0 (6H, m), 1.08 (3H, d, J = 5.6 Hz), 1.4-1.6 (2H, m), 1.7-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.7-3.8 (2H, m), 3.9-4.6 (13H, m), 4.8-5.1 (8H, m), 5.11 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.54 (1H, d, J = 5.9 Hz), 6.7-6.9 (3H, m), 7.0-7.2 (3H, m), 7.3-7.5 (3H, m), 7.7-7.9 (8H, m), 8.02 (2H, d, J = 8.4 Hz), 8.08 (1H, d, J = 8.4 Hz), 8.32 (1H, d, J = 7.7 Hz), 8.81 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1309,3 (M+Na)+.
Элементный анализ для C58H71N8O22NaS·6H2O:
Вычислено: C 49,92; H 6,00; N 8,03
Найдено: C 49,92; H 5,97; N 8,03.
Пример 47
ИК (KBr): 3350, 2933, 1668, 1629, 1517, 1249, 1045 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.8 Hz), 1.7-2.7 (8H, m), 3.1-3.3 (1H, m), 3.6-4.5 (16H, m), 4.7-5.2 (8H, m), 5.18 (1H, d, J = 3.1 Hz), 5.27 (1H, d, J = 4.5 Hz), 5.56 (1H, d, J = 5.8 Hz), 6.7-7.0 (3H, m), 7.0-7.2 (3H, m), 7.2-7.5 (3H, m), 8.0-8.4 (6H, m), 8.85 (1H, s), 8.96 (1H, d, J = 7.0 Hz), 9.07 (1H, s)
FAB-МС: m/z = 1276,6 (M+Na)+.
Элементный анализ для C54H72N9O22NaS·5H2O:
Вычислено: C 48,25; H 6,15; N 9,38
Найдено: C 48,10; H 6,14; N 9,30.
Пример 48
ИК (KBr): 3350, 2931, 1668, 1629, 1537, 1049 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.9 Hz), 0.9-1.5 (16H, m), 1.6-2.4 (8H, m), 2.5-2.7 (1H, m), 3.1-3.3 (1H, m), 3.5-5.6 (25H, m), 6.6-7.4 (8H, m), 7.8-8.4 (6H, m), 8.7-9.0 (2H, m), 9.00 (1H, d, J = 2.4 Hz)
FAB-МС: m/z = 1331,4 (M+Na+).
Элементный анализ для C56H73N10O23NaS·8H2O:
Вычислено: C 46,28; H 6,17; N 9,64
Найдено: C 46,50; H 6,27; N 9,65.
Пример 49
ИК (таблетка KBr): 3300, 2931, 1668, 1650, 1629, 1538, 1515, 12-68, 1049 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.10 (3H, d, J = 5.6 Hz), 1.2-1.4 (6H, m), 1.5-1.7 (2H, m), 1.7-2.1 (3H, m), 2.1-2.4 (3H, m), 2.6-2.7 (3H, m), 3.1-3.2 (1H, m), 3.7-3.9 (2H, m), 3.9-4.5 (12H, m), 4.8-5.1 (7H, m), 5.11 (1H, d, J = 5.5 Hz), 5.18 (1H, d, J = 3.1 Hz), 5.27 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.8 Hz), 6.7-7.0 (3H, m), 7.06 (1H, s), 7.3-7.5 (5H, m), 7.72 (2H, d, J = 8.2 Hz), 7.9-8.2 (5H, m), 8.3-8.4 (4H, m), 8.9-9.0 (2H, m)
FAB-МС: m/z = 1260,5 (M+Na)+.
Элементный анализ для C61H74N9O22SNa·6H2O:
Вычислено: C 50,58; H 5,98; N 8,70
Найдено: C 50,34; H 6,16; N 8,55.
Пример 50
ИК (KBr): 3369, 2958, 2935, 1670, 1629, 1525, 1473, 1247, 1047 см-1
ЯМР (DMSO-d6, δ): 0.95 (3H, t, J = 7.3 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.7 Hz), 1.3-1.6 (2H, m), 1.7-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.7-4.6 (15H, m), 4.7-5.1 (8H, m), 5.10 (1H, d, J = 5.6 Hz), 5.18 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.4 Hz), 5.56 (1H, d, J = 5.7 Hz), 6.7-7.0 (3H, m), 7.1-7.2 (3H, m), 7.2-7.4 (3H, m), 7.70 (2H, d, J = 8.6 Hz), 7.78 (2H, d, J = 8.4 Hz), 8.1-8.4 (6H, m), 8.85 (1H, s), 8.99 (1H, d, J = 7.0 Hz), 9.13 (1H, d, J = 1.6 Hz)
FAB-МС: m/z = 1310,1 (M+Na)+.
Элементный анализ для C57H70N9O22NaS·7H2O:
Вычислено: C 47,20; H 6,12; N 8,69
Найдено: C 47,42; H 6,19; N 8,92.
Пример 51
ИК (KBr): 3351, 2937, 2875, 1670, 1627, 1533, 1245, 1047 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.5-1.7 (2H, m), 1.7-2.1 (7H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.7-3.8 (2H, m), 3.9-4.6 (15H, m), 4.7-4.9 (3H, m), 5.0-5.1 (5H, m), 5.10 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.52 (1H, d, J = 5.9 Hz), 6.7-7.1 (9H, m), 7.2-7.5 (5H, m), 7.68 (2H, d, J = 8.2 Hz), 7.72 (2H, d, J = 6.7 Hz), 7.96 (2H, d, J = 8.2 Hz), 8.06 (1H, d, J = 8.4 Hz), 8.28 (1H, d, J = 7.7 Hz), 8.76 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1339,5 (M+Na+).
Элементный анализ для C59H73N8O23NaS·7H2O:
Вычислено: C 49,09; H 6,08; N 7,76
Найдено: C 49,04; H 6,08; N 7,82.
Пример 52
ИК (KBr): 3350, 2954, 2937, 1670, 1631, 1440, 1257, 1047 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J = 6.8 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.09 (2H, d, J = 5.8 Hz), 1.2-1.5 (6H, m), 1.7-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.7-4.6 (15H, m), 4.7-5.3 (11H, m), 5.5-5.6 (1H, m), 6.7-6.9 (1H, m), 7.0-7.5 (6H, m), 8.0-8.4 (8H, m), 8.85 (1H, s), 8.96 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1329,0 (M+Na)+.
Элементный анализ для C56H71N10O23NaS·6H2O:
Вычислено: C 47,52; H 5,91; N 9,90
Найдено: C 47,42; H 6,05; N 9,90.
Пример 53
ИК (KBr): 3350, 2952, 1666, 1629, 1537, 1519, 1255 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.4 Hz), 1.08 (3H, d, J = 5.6 Hz), 1.7-2.4 (8H, m), 2.5-2.6 (1H, m), 3.7-4.5 (15H, m), 4.7-5.1 (8H, m), 5.11 (1H, d, J = 5.5 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 3.1 Hz), 5.56 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.7-7.0 (2H, m), 7.05 (1H, s), 7.13 (2H, d, J = 8.7 Hz), 7.2-7.5 (3H, m), 7.97 (2H, d, J = 8.7 Hz), 8.1-8.4 (6H, m), 8.85 (1H, s), 8.92 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1345,3 (M+Na)+.
Элементный анализ для C56H71N10O22S2Na·8H2O:
Вычислено: C 45,84; H 5,98; N 9,55
Найдено: C 45,87; H 6,07; N 9,55.
Пример 54
ИК (таблетка KBr): 3350, 2931, 1670, 1652, 1628, 1442, 1247, 1047 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.8 Hz), 1.12 (3H, d, J = 6.8 Hz), 1.2-1.5 (10H, m), 1.7-2.0 (5H, m), 2.2-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.72 (2H, br), 3.8-4.5 (17H, m), 4.7-5.2 (9H, m), 5.26 (1H, d, J = 4.6 Hz), 5.57 (1H, d, J = 5.7 Hz), 6.7-7.1 (7H, m), 7.3-7.5 (3H, m), 7.66 (2H, d, J = 8.7 Hz), 8.10 (1H, d, J = 7.6 Hz), 8.17 (1H, d, J = 7.6 Hz), 8.76 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1293 (M+Na+).
Элементный анализ для C54H75N10O22NaS·7H2O:
Вычислено: C 46,41; H 6,42; N 10,02
Найдено: C 46,51; H 6,43; N 9,95.
Пример 55
ИК (KBr): 3345, 2937, 1650, 1511, 1249, 1047 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J = 7.0 Hz), 0.96 (3H, t, J = 7.8 Hz), 1.09 (3H, d, J = 6.8 Hz), 1.3-1.5 (4H, m), 1.6-2.1 (5H, m), 2.1-2.5 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.7-3.9 (2H, m), 3.9-4.6 (13H, m), 4.79 (2H, d, J = 5.9 Hz), 4.8-4.9 (1H, m), 4.9-5.2 (5H, m), 5.10 (1H, d, J = 5.9 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.6 Hz), 5.53 (1H, d, J = 5.9 Hz), 6.7-7.0 (3H, m), 7.0-7.2 (3H, m), 7.19 (1H, s), 7.3-7.5 (3H, m), 7.7-8.1 (6H, m), 8.08 (1H, d, J = 10.0 Hz), 8.26 (1H, d, J = 8.8 Hz), 8.77 (1H, m), 8.85 (1H, s), 13.32 (1H, s)
FAB-МС: m/z = 1314,0 (M+Na)+.
Элементный анализ для C56H71N10O22SNa·8H2O:
Вычислено: C 46,86; H 6,11; N 9,76
Найдено: C 46,93; H 5,87; N 9,74.
Пример 56
ИК (KBr): 3350, 2958, 2935, 2873, 1666, 1629, 1247, 1045 см-1
ЯМР (DMSO-d6, δ): 0.9-1.1 (6H, m), 1.03 (3H, d, J = 6.0 Hz), 1.4-1.6 (2H, m), 1.6-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (15H, m), 4.7-5.1 (8H, m), 5.10 (1H, d, J = 5.5 Hz), 5.17 (1H, d, J = 2.9 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.7 Hz), 6.7-6.9 (3H, m), 7.0-7.5 (8H, m), 7.68 (2H, d, J = 8.9 Hz), 7.73 (2H, d, J = 8.3 Hz), 8.01 (2H, d, J = 8.3 Hz), 8.10 (1H, d, J = 8.4 Hz), 8.26 (1H, d, J = 7.7 Hz), 8.8-9.0 (2H, m)
FAB-МС: m/z = 1299,5 (M+Na)+.
Элементный анализ для C56H69N8O23NaS·6H2O:
Вычислено: C 48,55; H 5,89; N 8,09
Найдено: C 48,52; H 5,94; N 8,07.
Пример 57
ИК (KBr): 3355,5, 1662,3, 1629,6, 1267,0 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.8 Hz), 0.93 (3H, d, J = 8.4 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.2-1.5 (4H, m), 1.5-1.95 (5H, m), 2.1-2.45 (4H, m), 2.5-2.7 (4H, m), 3.17 (1H, m), 3.55-4.45 (14H, m), 4.6-5.3 (13H, m), 5.56 (1H, d, J = 5.6 Hz), 6.72 (1H, d, J = 8.1 Hz), 6.75 (1H, s), 6.77 (1H, d, J = 8.1 Hz), 7.04 (1H, s), 7.10 (1H, s), 7.2-7.45 (10H, m), 7.53 (4H, d, J = 6.6 Hz), 7.85 (1H, d, J = 7 Hz), 7.92 (1H, d, J = 7 Hz), 8.05 (1H, d, J = 7 Hz), 8.22 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1408 (M+Na).
Пример 58
ИК (KBr): 3347,8, 1664,3, 1631,5, 1245,8 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.96 (3H, d, J = 6.6 Hz), 1.04 (3H, d, J = 5.7 Hz), 1.15-2.6 (21H, m), 3.16 (1H, m), 3.5-4.5 (16H, m), 4.6-5.4 (13H, m), 5.47 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz) 6.78-6.85 (4H, m), 7.05 (1H, s), 7.10 (1H, s), 7.18 (2H, d, J = 8.6 Hz), 7.25-7.45 (6H, m), 7.72 (1H, d, J = 7 Hz), 7.91 (1H, d, J = 7 Hz), 8.05 (1H, d, J = 9.3 Hz), 8.20 (1H, d, J = 7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1390 (M+Na).
Элементный анализ для C60H82N9O24SNa·5H2O:
Вычислено: C 49,41; H 6,36; N 8,64
Найдено: C 49,77; H 6,71; N 8,71.
Пример 59
ИК (KBr): 3353,6, 1670,1, 1627,6, 1247,7 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.5 Hz), 0.97 (3H, d, J = 6.8 Hz), 1.01 (3H, d, J = 5.4 Hz), 1.1-1.55 (12H, m), 1.55-1.95 (5H, m), 2.05-4.7 (4H, m), 3.16 (1H, m), 3.5-4.5 (16H, m), 4.6-5.3 (13H, m), 5.55 (1H, d, J = 5.6 Hz), 6.7-6.9 (5H, m), 7.05 (1H, s), 7.1 (1H, s), 7.15 (1H, d, J = 8.5 Hz), 7.25-7.5 (6H, m), 7.73 (1H, d, J = 8.4 Hz), 7.92 (1H, d, J = 7 Hz), 8.08 (1H, d, J = 8.4 Hz), 8.18 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1390 (M+Na).
Пример 60
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.6 Hz), 0.96 (3H, d, J = 6.6 Hz), 1.05 (3H, d, J = 5.6 Hz), 1.1-1.5 (22H, m), 1.5-2.5 (9H, m), 2.5-3.5 (4H, m), 3.5-4.45 (14H, m), 4.45-5.45 (12H, m), 6.72 (1H, d, J = 8.2 Hz), 6.79 (1H, s), 6.81 (1H, d, J = 8.2 Hz), 7.04 (1H, s), 7.05-7.5 (8H, m), 7.9-8.3 (3H, m), 8.84 (1H, s)
FAB-МС: m/z = 1325 (M+Na).
Элементный анализ для C58H89N8O22SNa·6H2O:
Вычислено: C 49,35; H 7,14; N 7,94
Найдено: C 49,33; H 7,04; N 7,87.
Пример 61
ИК (KBr): 3400, 1668,1, 1629,6, 1270,9 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.8 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.1-2.0 (33H, m), 2.1-2.5 (4H, m), 3.20 (3H, s), 3.23 (2H, t, J = 6.5 Hz), 3.1-3.3 (1H, m), 3.6-4.45 (14H, m), 4.6-5.3 (13H, m), 5.49 (1H, d, J = 6.1 Hz), 6.70 (1H, s), 6.72 (1H, d, J = 8.2 Hz), 6.80 (1H, d, J = 8.2 Hz), 7.03 (1H, s), 7.0-7.1 (1H, m), 7.15 (1H, s), 7.2-7.45 (6H, m), 8.0-3.3 (3H, m), 8.83 (1H, s)
FAB-МС: m/z = 1426 (M+Na).
Элементный анализ для C62H94N9O24SNa·5H2O:
Вычислено: C 49,82; H 7,01; N 8,43
Найдено: C 49,86; H 7,31; N 8,40.
Пример 62
ИК (KBr): 3355,5, 1668,1, 1629,6, 1274,7 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.5 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.04 (3H, d, J = 5.9 Hz), 1.1-2.6 (34H, m), 3.2 (1H, m), 3.6-4.55 (14H, m), 4.7-5.3 (11H, m), 5.47 (1H, d, J = 5.9 Hz), 6.72 (1H, d, J = 8.1 Hz), 6.79 (1H, s), 6.81 (1H, d, J = 3.1 Hz), 7.05 (1H, s), 7.11 (1H, s), 7.2-7.5 (2H, m), 8.0-8.15 (2H, m), 8.20 (1H, d, J = 8.0 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1235 (M+Na).
Элементный анализ для C51H81N8O22SNa·7H2O:
Вычислено: C 45,73; H 7,15; N 8,37
Найдено: C 45,55; H 7,24; N 8,23.
Пример 63
ИК (KBr): 3353,6, 1664,3, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.95 (3H, d, J = 6.7 Hz) 1.04 (3H, d, J = 5.7 Hz), 1.2-2.7 (30H, m), 3.16 (1H, m), 3.6-4.5 (13H, m), 4.7-5.3 (11H, m), 5.51 (1H, d, J = 6.0 Hz), 5.74 (1H, s), 6.72 (1H, d, J = 8.2 Hz), 6.75 (1H, s), 6.77 (1H, d, J = 8.2 Hz), 7.05 (1H, s), 7.2-7.5 (3H, m), 8.0-8.3 (3H, m), 8.85 (1H, s)
FAB-МС: m/z = 1204 (M+Na).
Элементный анализ для C50H77N8O21SNa·5H2O:
Вычислено: C 47,24; H 6,90; N 8,81
Найдено: C 46,98; H 7,12; N 8,72.
Пример 64
Главный продукт
ИК (KBr): 3400, 1675,8, 1631,5, 1511,9, 1234,2 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.6 Hz), 1.05 (3H, d, J = 5.8 Hz), 1.2-1.6 (10H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.05-3.2 (4H, m), 3.20 (3H, s), 3.29 (2H, t, J = 6.4 Hz), 3.3-3.5 (5H, m), 3.6-4.5 (15H, m), 4.7-5.3 (11H, m), 5.50 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.1 (9H, m), 7.2-7.5 (3H, m), 7.81 (2H, d, J = 8.6 Hz), 8.08 (1H, d, J = 8.2 Hz), 8.24 (1H, d, J = 7 Hz), 8.44 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1403 (M+Na).
Элементный анализ для C61H85N10O23SNa·9H2O:
Вычислено: C 47,47; H 6,73; N 9,07
Найдено: C 47,73; H 7,06; N 9,03.
Минорный продукт
ИК (KBr): 3350, 1668,1, 1631,5, 1511,9, 1234,2 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.6 Hz), 1.07 (3H, d, J = 5.8 Hz), 1.2-1.5 (6H, m), 1.55-2.1 (7H, m), 2.1-2.65 (4H, m), 3.0-3.6 (9H, m), 3.7-4.5 (15H, m), 4.7-5,6 (14H, m), 5.7-6.0 (1H, m), 6.72 (1H, d, J = 8.0 Hz), 6.75-7.1 (9H, m), 7.25-7.5 (3H, m), 7.81 (2H, d, J = 8.3 Hz), 8.08 (1H, d, J = 8.2 Hz), 8.25 (1H, d, J = 7 Hz), 8.45 (1H, d, J = 7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1371 (M+Na).
Элементный анализ для C60H81N10O22SNa·8H2O:
Вычислено: C 48,25; H 6,55; N 9,38
Найдено: C 48,10; H 6,81; N 9,40.
Пример 65
ИК (KBr): 3450, 1668,1, 1635,3 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.5 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 6 Hz), 1.2-1.5 (6H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.1-3.4 (9H, m), 3.6-4.5 (15H, m), 4.7-5.3 (11H, m), 5.49 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 6.83 (2H, d, J = 9.0 Hz), 6.94 (2H, d, J = 9.0 Hz), 7.04 (1H, s), 7.12 (1H, t, J = 8.4 Hz), 7.2-7.5 (3H, m), 7.65-7.8 (2H, m), 8.09 (1H, d, J = 8.4 Hz), 8.25 (1H, d, J = 7 Hz), 8.63 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1363 (M+Na).
Элементный анализ для C58H78FN10O22SNa·5H2O:
Вычислено: C 48,67; H 6,20; N 9,79
Найдено: C 48,83; H 6,15; N 9,74.
Пример 66
ИК (KBr): 3400, 1668,1, 1635,3, 1510,0, 1240,0 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.6 Hz), 1.2-1.5 (6H, m), 1.5-2.05 (5H, m), 2.1-2.65 (4H, m), 3.1-3.3 (9H, m), 3.6-4.5 (15H, m), 4.7-5.3 (11H, m), 5.51 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (4H, m), 6.94 (2H, d, J = 9.2 Hz), 7.04 (1H, s), 7.24 (1H, d, J = 8.5 Hz), 7.15-7.5 (3H, m), 7.86 (1H, dd, J = 8.6 and 2.1 Hz), 8.02 (1H, d, J = 2.1 Hz), 8.04 (1H, d, J = 8.4 Hz), 8.23 (1H, d, J = 7 Hz), 8.70 (1H, d, J = 7 Hz), 3.84 (1H, s)
FAB-МС: m/z = 1379 (M+Na).
Элементный анализ для C58H78ClN10O22SNa·6H2O:
Вычислено: C 47,52; H 6,19; N 9,55
Найдено: C 47,78; H 6,23; N 9,55.
Пример 67
ИК (KBr): 3400, 1670 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.05 (3H, d, J = 5.7 Hz), 1.4-2.65 (17H, m), 2.65-3.6 (8H, m), 3.6-4.5 (15H, m), 4.6-5.3 (11H, m), 5.44 (1H, d, J = 6.0 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.81 (1H, s), 6.83 (1H, d, J = 8.2 Hz), 6.98 (2H, d, J = 8.9 Hz), 7.05 (1H, s), 7.2-7.5 (3H, m), 7.80 (2H, d, J = 8.9 Hz), 8.05 (1H, d, J = 8.4 Hz), 8.26 (1H, d, J = 7 Hz), 8.39 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1229 (M+Na).
Элементный анализ для C52H74N10O21S·5H2O:
Вычислено: C 48,14: H 6,53; N 10,80
Найдено: C 48,29; H 6,33; N 10,95.
Пример 68
ИК (KBr): 3400, 1652,7, 1635,3, 1511,9, 1241,9 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.7 Hz), 1.2-1.5 (6H, m), 1.6-2.0 (5H, m), 2.1-2.6 (4H, m), 3.0-3.3 (5H, m), 3.6-4.6 (19H, m), 4.7-5.3 (11H, m), 5.53 (1H, d, J = 5.6 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.75-7.0 (2H, m), 6.83 (2H, d, J = 9.2 Hz), 6.95 (2H, d, J = 9.2 Hz), 7.05 (1H, s), 7.12 (1H, s), 7.25-7.5 (2H, m), 7.42 (1H, d, J = 9.5 Hz), 7.84 (1H, d, J = 9.5 Hz), 7.9-8.1 (2H, m), 8.71 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-MC: m/z = 1347 (M+Na).
Элементный анализ для C56H77N12O22SNa·7H2O:
Вычислено: C 46,34; H 6,32; N 11,58
Найдено: C 46,38; H 6,18; N 11,36.
Пример 69
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.8 Hz), 1.2-1.5 (6H, m), 1.6-2.05 (5H, m), 2.1-2.6 (4H, m), 3.0-3.3 (5H, m), 3.4-3.55 (4H, m), 3.7-4.6 (15H, m), 4.7-5.3 (11H, m), 5.52 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.1 Hz), 6.8-6.95 (2H, m), 6.83 (2H, d, J = 9.3 Hz), 6.95 (2H, d, J = 9.3 Hz) 7.05 (1H, s), 7.14 (1H, s), 7.3-7.6 (3H, m), 7.84 (1H, d, J = 8.6 Hz), 7.95-8.1 (2H, m), 8.40 (1H, s), 8.42 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1346 (M+Na).
Элементный анализ для C57H78N11O22SNa·5H2O:
Вычислено: C 48,40; H 6,27; N 10,89
Найдено: C 48,32; H 6,44; N 10,86.
Пример 70
ИК (KBr): 3400, 1668,1, 1629,6, 1511,9 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.7 Hz), 1.15-1.5 (6H, m), 1.6-2.0 (7H, m), 2.1-2.65 (5H, m), 3.1-3.5 (9H, m), 3.6-4.5 (13H, m), 4.7-5.3 (11H, m), 5.46 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.81 (1H, s), 6.84 (1H, d, J = 8.2 Hz), 6.91 (2H, d, J = 8.7 Hz), 6.95-7.05 (3H, m), 7.09 (2H, d, J = 8.7 Hz), 7.25-7.5 (3H, m), 7.81 (2H, d, J = 8.8 Hz), 8.09 (1H, d, J = 7 Hz), 8.25 (1H, d, J = 7 Hz), 8.04 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1327 (M+Na).
Элементный анализ для C58H77N10O21SNa·5H2O:
Вычислено: C 49,92; H 6,28; N 10,03
Найдено: C 49,75; H 6,41; N 10,25.
Пример 71
ИК (KBr): 3350, 1668,1, 1629,6, 1511,9, 1232,3 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.5 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 6.0 Hz), 1.2-1.4 (6H, m), 1.4-1.6 (2H, m), 1.7-2.1 (3H, m), 2.1-2.7 (6H, m), 3.1-3.5 (9H, m), 3.72 (2H, m), 3.8-4.5 (11H, m), 4.7-5.3 (11H, m), 5.47 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 6.91 (2H, d, J = 8.6 Hz), 6.95-7.15 (5H, m), 7.25-7.5 (3H, m), 7.81 (2H, d, J = 8.8 Hz), 8.09 (1H, d, J = 8.4 Hz), 8.26 (1H, d, J = 7 Hz), 8.40 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1329 (M+Na).
Элементный анализ для C58H79N10NaO21S·6H2O:
Вычислено: C 49,22; H 6,48; N 9,90
Найдено: C 49,33; H 6,67, N 9,89.
Пример 72
ИК (KBr): 3450, 1668,1, 1631,5, 1240,0 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.6 Hz), 1.05 (3H, d, J = 5.6 Hz), 1.3-1.7 (4H, m), 1.7-2.1 (7H, m), 2.1-2.73 (6H, m), 2.75-3.05 (4H, m), 3.05-4.5 (18H, m), 4.7-5.5 (12H, m), 6.72 (1H, d, J = 8.3 Hz), 6.77-6.9 (2H, m), 6.96 (2H, d, J = 8.6 Hz), 7.05 (1H, s), 7.1- 7.5 (8H, m), 7.80 (2H, d, J = 8.6 Hz), 8.06 (1H, d, J = 8.4 Hz), 8.28 (1H, d, J = 7 Hz), 8.41 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1305 (M+Na).
Элементный анализ для C58H78N10O21S·8H2O:
Вычислено: C 48,80; H 6,64; N 9,81
Найдено: C 48,88; H 6,50; N 9,81.
Пример 73
ИК (KBr): 1673,9, 1646,9, 1510,0 и 1238,1 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.4 Hz), 0.96 (3H, d, J = 6.6 Hz), 1.05 (3H, d, J = 5.6 Hz), 1.2-1.5 (6H, m), 1.5-2.0 (9H, m), 2.1-2.8 (11H, m), 3.1-3.4 (5H, m), 3.4-4.5 (17H, m), 4.6-5.5 (12H, m), 6.6-7.0 (9H, m), 7.04 (1H, s), 7.2-7.5 (3H, m), 7.78 (2H, d, J = 8.7 Hz), 8.05 (1H, d, J = 8.4 Hz), 8.24 (1H, d, J = 7 Hz), 8.39 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1326 (M+-SO3+Na).
Элементный анализ для C63H89N11O22S·9H2O:
Вычислено: C 48,92; H 6,97; N 9,96
Найдено: C 48,77; H 6,73; N 9,94.
Пример 74
ИК (KBr): 3450, 1670,1, 1631,5, 1280,5 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 7.0 Hz), 0.96 (3H, t, J = 6.8 Hz), 1.05 (3H, d, J = 5.6 Hz), 1.1-1.65 (13H, m), 1.65-2.1 (7H, m), 2.1-2.65 (5H, m), 3.17 (1H, m), 3.6-4.5 (13H, m), 4.7-5.3 (11H, m), 5.49 (1H, d, J = 5.9 Hz), 6.72 (1H, d, J = 8.2 Hz), 6.82 (1H, d, J = 8.2 Hz), 6.84 (1H, s), 7.04 (1H, s), 7.29 (2H, d, J = 8.3 Hz), 7.2-7.5 (3H, m), 7.80 (2H, d, J = 8.3 Hz), 8.10 (1H, d, J = 8.4 Hz), 8.26 (1H, d, J = 7 Hz), 8.65 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1237 (M+Na).
Элементный анализ для C53H75N8O21SNa·6H2O:
Вычислено: C 48,10; H 6,63; N 8,47
Найдено: C 48,26; H 6,62; N 8,46.
Пример 75
ИК (KBr): 3400, 1670,1, 1627,6, 1272,8 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 3.3 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.2-1.6 (10H, m), 1.6-2.1 (5H, m), 2.1-2.7 (4H, m), 3.0-3.3 (1H, m), 3.20 (3H, s), 3.29 (2H, t, J = 6.4 Hz), 3.73 (2H, m), 3.9-4.6 (13H, m), 4.7-5.3 (11H, m), 5.53 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.3 Hz), 6.83 (1H, d, J = 8.3 Hz), 6.91 (1H, s), 7.05 (1H, s), 7.23 (1H, dd, J = 9.0 and 2.3 Hz), 7.3-7.5 (4H, m), 7.8-8.0 (3H, m), 8.09 (1H, d, J = 8.4 Hz), 8.33 (1H, d, J = 7 Hz), 8.44 (1H, s), 8.80 (1H, d, J = 7 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1293 (M+Na).
Элементный анализ для C55H75N8O23SNa·6H2O:
Вычислено: C 47,89; H 6,36; N 8,12
Найдено: C 47,81; H 6,26; N 8,05.
Пример 76
ИК (KBr): 3361,3, 1668,1, 1635,3, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.8 Hz), 1.19-1.25 (8H, m), 1.25-2.00 (5H, m), 2.02-2.53 (4H, m), 2.44 (3H, s), 2.61 (2H, t, J = 7.6 Hz), 3.05-3.27 (1H, m), 3.55-4.50 (13H, m), 4.65-5.65 (12H, m), 6.42 (1H, s), 6.65-6.95 (3H, m), 7.05 (1H, d, J = 0.4 Hz), 7.13-7.50 (5H, m), 7.50-7.88 (6H, m), 8.10 (1H, d, J = 9.0 Hz), 8.25 (1H, d, J = 8.4 Hz), 8.40 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1299,3 (M+Na-1).
Элементный анализ для C58H77N8NaO21S·5H2O:
Вычислено: C 50,94; H 6,41; N 8,19
Найдено: C 50,99; H 6,40; N 8,15.
Пример 77
ИК ("Нуджол"): 3351,7, 1670,1, 1652,7, 1623,8 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.8 Hz), 1.13-1.45 (8H, m), 1.47-1.96 (5H, m), 2.06-2.66 (8H, m), 2.81 (2H, t, J = 7.6 Hz), 3.04-3.30 (1H, m), 3.53-4.50 (13H, m), 4.53-5.70 (12H, m), 6.64-6.88 (3H, m), 7.04 (1H, d, J = 0.4 Hz), 7.13-7.60 (11H, m), 8.10 (1H, d, J = 9.0 Hz), 8.18 (1H, d, J = 8.4 Hz), 8.30 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1287,4 (M+Na-1).
Элементный анализ для C57H77N8NaO21S·5H2O:
Вычислено: C 50,51; H 6,46; N 8,27
Найдено: C 50,84; H 6,60; N 8,33.
Пример 78
ИК (KBr): 3361,3, 1683,6, 1670,1, 1662,3, 1652,7, 1646,9, 1635,3, 1627,6, 1623,8 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.6 Hz), 1.28-2.00 (13H, m), 2.08-2.60 (4H, m), 3.07-3.30 (1H, m), 3.60-4.66 (17H, m), 4.66-5.12 (9H, m), 5.11 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.6 Hz), 5.52 (1H, d, J = 6.0 Hz), 6.62-6.95 (4H, m), 6.95-7.15 (3H, m), 7.20-7.50 (3H, m), 7.50-7.85 (7H, m), 8.12 (1H, d, J = 8.4 Hz), 8.35 (1H, d, J = 7.7 Hz), 8.53 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1319,7 (M+Na-1).
Элементный анализ для C57H74N8NaO22SF·8H2O:
Вычислено: C 47,49; H 6,29; N 7,77
Найдено: C 47,79; H 6,16; N 7,93.
Пример 79
ИК (KBr): 3354,9, 1668,1, 1662,3, 1654,6, 1646,9, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.7 Hz), 0.90-1.10 (6H, m), 1.10-1.40 (8H, m), 1.48-1.95 (5H, m), 2.05-2.46 (4H, m), 2.60 (2H, t, J = 7.6 Hz), 3.07-3.23 (1H, m), 3.55-4.45 (14H, m), 4.67-5.32 (11H, m), 5.48-5.63 (1H, m), 6.22 (1H, J = 5.3 Hz), 6.65-6.89 (3H, m), 6.97-7.15 (2H, m), 7.20-7.68 (10H, m), 7.85-8.20 (3H, m), 8.84 (1H, s)
FAB-МС: m/z = 1289,4 (M+Na-1).
Элементный анализ для C56H75N8NaO22S·3H2O:
Вычислено: C 50,90; H 6,18; N 8,48
Найдено: C 50,80; H 6,44; N 8,29.
Пример 80
ИК (KBr): 3361,3, 1664,3, 1631,5, 1600,6 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.98 (3H, d, J = 6.7 Hz), 1.16 (3H, t, J = 5.9 Hz), 1.20-1.45 (8H, m), 1.50-1.70 (2H, m), 1.70-2.05 (3H, m), 2.10-2.57 (4H, m), 2.63 (2H, t, J = 7.6 Hz), 3.10-3.30 (1H, m), 3.68-4.50 (13H, m), 4.78-5.32 (11H, m), 5.66 (1H, d, J = 5.7 Hz), 6.68-7.02 (3H, m), 7.04 (1H, a, J = 0.4 Hz), 7.25-7.48 (4H, m), 7.60-8.08 (7H, m), 8.10 (1H, d, J = 8.4 Hz), 8.28 (1H, d, J = 7.7 Hz), 8.85 (1H, s), 9.30 (1H, d, J = 7.1 Hz)
FAB-МС: m/z = 1287,5 (M+Na-1).
Элементный анализ для C55H73N8NaO22S·3H2O:
Вычислено: C 50,53; H 6,09; N 8,57
Найдено: C 50,66; H 6,01; N 8,22.
Пример 81
ИК (KBr): 3349,7, 1668,1, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.8 Hz), 1.18-1.48 (8H, m), 1.50-2.10 (5H, m), 2.10-2.45 (3H, m), 2.50-2.65 (1H, m), 2.77 (2H, t, J = 7.6 Hz), 3.05-3.25 (1H, m), 3.60-4.65 (13H, m), 4.67-5.60 (12H, m), 6.65-6.97 (3H, m), 7.05 (1H, d, J = 0.4 Hz), 7.21-7.43 (4H, m), 7.76 (1H, s), 7.83-8.05 (3H, m), 8.10 (1H, d, J = 9.0 Hz), 8.29 (1H, d, J = 8.4 Hz), 8.48 (1H, s), 8.64-9.03 (2H, m)
FAB-МС: m/z = 1233,0 (M+Na-1).
Элементный анализ для C53H71N8NaO20S·3H2O:
Вычислено: C 50,96; H 6,22; N 8,96
Найдено: C 50,62; H 6,40; N 8,92.
Пример 82
ИК (KBr): 3361,3, 1670,1, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 6.7 Hz), 0.96 (2H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.9 Hz), 1.18-1.43 (6H, m), 1.50-2.10 (5H, m), 2.10-2.69 (4H, m), 2.77 (2H, t, J = 7.6 Hz), 3.07-3.29 (1H, m), 3.60-4.62 (13H, m), 4.69-5.23 (10H, m), 5.27 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.9 Hz), 6.63-7.00 (3H, m), 7.05 (1H, d, J = 0.4 Hz), 7.25-7.53 (4H, m), 7.76 (1H, s), 7.84-8.05 (3H, m), 8.13 (1H, d, J = 8.4 Hz), 8.33 (1H, d, J = 7.7 Hz), 8.48 (1H, s), 8.73-9.00 (2H, m)
FAB-МС: m/z = 1219,4 (M+Na-1).
Элементный анализ для C52H69N8NaO21S·5H2O:
Вычислено: C 48,51; H 6,19; N 8,71
Найдено: C 48,67; H 6,34; N 8,74.
Пример 83
ИК (KBr): 3357,5, 1668,1, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 6.0 Hz), 1.20-1.62 (10H, m), 1.62-2.00 (5H, m), 2.10-2.65 (4H, m), 3.20 (3H, s), 3.08-3.45 (1H, m), 3.28 (2H, t, J = 6.5 Hz), 3.53-4.50 (15H, m), 4.68-5.13 (9H, m), 5.17 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.4 Hz), 5.53 (1H, d, J = 6.0 Hz), 6.68-6.95 (4H, m), 6.95-7.11 (3H, m), 7.20-7.52 (3H, m), 7.55-7.95 (7H, m), 8.13 (1H, d, J = 8.4 Hz), 8.30 (1H, d, J = 7.7 Hz), 8.52 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1345,2 (M+Na-1).
Элементный анализ для C59H79N8NaO23S·8H2O:
Вычислено: C 48,29; H 6,53; N 7,64
Найдено: C 48,44; H 6,58; N 7,75.
Пример 84
ИК (KBr): 3553,6, 1662,3, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.5 Hz), 1.40-1.65 (2H, m), 1.65-2.00 (5H, m), 2.00-2.67 (6H, m), 3.08-3.30 (1H, m), 3.50-4.50 (15H, m), 4.68-5.13 (11H, m), 5.18 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.53 (1H, d, J = 6.0 Hz), 5.70-6.00 (1H, m), 6.63-6.95 (4H, m), 6.95-7.13 (3H, m), 7.20-7.52 (3H, m), 7.52-7.95 (7H, m), 8.12 (1H, d, J = 8.4 Hz), 8.31 (1H, d, J = 7.7 Hz), 8.53 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1285,4 (M+Na-1).
Элементный анализ для C56H71N8O22SNa·8H2O:
Вычислено: C 47,79; H 6,23; N 7,96
Найдено: C 47,59; H 6,32; N 8,06.
Пример 85
ИК (KBr): 3363,2, 1670,1, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.89 (6H, d, J = 6.5 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.7 Hz), 1.22-1.41 (2H, m), 1.50-1.97 (6H, m), 2.11-2.65 (4H, m), 3.10-3.30 (1H, m), 3.60-4.50 (15H, m), 4.70-5.08 (8H, m), 5.10 (1H, d, J = 5.6 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.50 (1H, d, J = 5.9 Hz), 6.65-6.92 (4H, m), 6.92-7.12 (3H, m), 7.21-7.50 (3H, m), 7.52-7.90 (7H, m), 8.12 (1H, d, J = 8.4 Hz), 8.30 (1H, d, J = 7.7 Hz), 8.56 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1287,6 (M+Na-1).
Элементный анализ для C56H73N8NaO22S·6,5H2O:
Вычислено: C 48,66; H 6,27; N 8,11
Найдено: C 48,67; H 6,32; N 8,20.
Пример 86
ИК (KBr): 3361,3, 1683,6, 1670,1, 1654,6, 1635,3, 1623,8 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.6 Hz), 1.30-2.00 (11H, m), 2.10-2.70 (4H, m), 3.05-3.15 (1H, m), 3.55-4.70 (17H, m), 4.70-5.11 (9H, m), 5.16 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.52 (1H, d, J = 6.0 Hz), 6.65-6.95 (4H, m), 6.95-7.10 (3H, m), 7.10-7.50 (3H, m), 7.50-7.85 (7H, m), 8.12 (1H, d, J = 8.4 Hz), 8.30 (1H, d, J = 8.3 Hz), 8.52 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1305,2 (M+Na-1).
Элементный анализ для C56H72N8NaO22SF·6H2O:
Вычислено: C 48,34; H 6,09; N 8,05
Найдено: C 48,47; H 6,29; N 7,95.
Пример 87
ИК (KBr): 3359,4, 1668,1, 1654,6, 1625,7 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 6.0 Hz), 1.22-1.62 (6H, m), 1.62-2.00 (5H, m), 2.10-2.65 (4H, m), 3.20 (3H, s), 3.05-3.40 (1H, m), 3.31 (2H, t, J = 6.5 Hz), 3.60-4.55 (15H, m), 4.65-5.13 (9H, m), 5.16 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.4 Hz), 5.53 (1H, d, J = 6.0 Hz), 6.68-6.95 (4H, m), 6.95-7.20 (3H, m), 7.20-7.58 (3H, m), 7.58-7.90 (7H, m), 8.13 (1H, d, J = 8.4 Hz), 8.32 (1H, d, J = 7.7 Hz), 8.53 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1317,6 (M+Na-1).
Элементный анализ для C57H75N8NaO23S·7H2O:
Вычислено: C 48,16; H 6,31; N 7,88
Найдено: C 48,21; H 6,60; N 7,78.
Пример 88
ИК (KBr): 3350, 2954, 1668, 1629, 1538, 1511, 1454, 1249 см-1
ЯМР (DMSO-d6, δ): 0.88 (3H, t, J = 7.1 Hz), 0.96 (3H, d, J = 7.5 Hz), 1.08 (2H, d, J = 5.7 Hz), 1.2-1.5 (6H, m), 1.6-2.4 (8H, m), 2.6-2.7 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (19H, m), 4.7-5.3 (8H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.1 (5H, m), 7.19 (1H, s), 7.3-7.5 (3H, m), 7.75 (2H, d, J = 8.7 Hz), 7.8-8.0 (4H, m), 8.08 (1H, d, J = 8.9 Hz), 8.30 (1H, d, J = 7.7 Hz), 8.7-9.0 (3H, m)
FAB-МС: m/z = 1327 (M+Na+).
Элементный анализ для C57H73N10O22NaS·9H2O:
Вычислено: C 46,65, H 6,25; N 9,54.
Найдено: C 46,95; H 6,22; N 9,55.
Пример 89
ИК (KBr): 3376, 2931, 2858, 1662, 1631, 1521, 1444, 1245, 1047 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.9 Hz), 1.3-1.6 (6H, m), 1.7-2.1 (5H, m), 2.2-2.4 (3H, m), 2.5-2.6 (1H, m), 3.21 (3H, s), 3.2-3.4 (3H, m), 3.6-4.5 (16H, m), 4.79 (2H, d, J = 6.0 Hz), 4.9-5.2 (5H, m), 5.10 (1H, d, J = 3.6 Hz), 5.18 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.53 (1H, d, J = 6.0 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.0-7.2 (3H, m), 7.3-7.5 (3H, m), 7.6-7.9 (8H, m), 8.01 (2H, d, J = 8.4 Hz), 8.12 (1H, d, J = 8.4 Hz), 8.31 (1H, d, J = 7.7 Hz), 8.79 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1367 (M+Na+).
Элементный анализ для C61H77N8O23NaS·6,5H2O:
Вычислено: C 50,10; H 6,20; N 7,66
Найдено: C 50,09; H 6,17; N 7,62.
Пример 90
ИК (KBr): 3363, 2937, 2869, 1646, 1444, 1255 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.2-1.6 (10H, m), 1.7-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.7 (1H, m), 3.20 (3H, s), 3.2-3.4 (1H, m), 3.6-4.6 (16H, m), 4.7-5.2 (8H, m), 5.16 (1H, d, J = 3.1 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.54 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.1-7.4 (6H, m), 7.97 (2H, d, J = 8.8 Hz), 8.0-8.4 (6H, m), 8.84 (1H, s), 8.92 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1403,6 (M+Na+).
Элементный анализ для C59H77N10O23NaS2·6H2O:
Вычислено: C 47,58; H 6,02; N 9,40
Найдено: C 47,72; H 6,12; N 9,42.
Пример 91
ИК (KBr): 3350, 1668, 1654, 1625, 1537, 1521, 1245, 1047 см-1
ЯМР (DMSO-d6, δ): 0.9-1.1 (6H, m), 1.07 (3H, d, J = 5.7 Hz), 1.4-2.0 (7H, m), 2.2-2.5 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (16H, m), 4.7-5.1 (7H, m), 5.09 (1H, d, J = 5.6 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.4 Hz), 5.53 (1H, d, J = 6.0 Hz), 6.73 (1H, d, J = 8.4 Hz), 6.8-7.2 (6H, m) 7.2-7.5 (4H, m), 7.5-7.8 (6H, m), 8.11 (1H, d, J = 8.4 Hz), 8.32 (1H, d, J = 7.7 Hz), 8.54 (1H, d, J = 7.0 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1259 (M+Na+).
Элементный анализ для C54H69N8O22NaS·8H2O:
Вычислено: C 46,95; H 6,20; N 8,11
Найдено: C 47,20; H 6,23; N 8,28.
Пример 92
ИК (KBr): 3359, 2929, 2852, 1668, 1650, 1631, 1538, 1515 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 6.1 Hz), 1.2-1.6 (5H, m), 1.6-2.5 (10H, m), 2.5-2.6 (1H, m), 3.18 (1H, m), 3.7-4.5 (15H, m), 4.8-5.2 (8H, m), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.1 Hz), 6.81 (1H, s), 6.85 (1H, s), 7.05 (1H, s), 7.2-7.4 (3H, m), 7.45 (2H, d, J = 8.2 Hz), 7.96 (2H, d, J = 8.2 Hz), 8.0-8.2 (4H, s), 8.2-8.3 (1H, m), 8.85 (1H, s), 8.9-9.0 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1327,5 (M+Na)+.
Элементный анализ для C56H69N10O21S2Na·6H2O:
Вычислено: C 47,59; H 5,78; N 9,91
Найдено: C 47,89; H 5,76; N 9,93.
Пример 93
ИК (KBr): 3350, 1654, 1629, 1517, 1249, 1047 см-1
ЯМР (DMSO-d6, δ): 0.9-1.1 (6H, m), 1.11 (3H, d, J = 5.9 Hz), 1.6-2.0 (5H, s), 2.1-2.4 (3H, s), 2.6-2.7 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (16H, m), 4.7-5.2 (7H, m), 5.10 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.7 Hz), 6.7-6.9 (3H, m), 7.0-7.5 (6H, m), 7.74 (2H, d, J = 8.8 Hz), 7.91 (2H, d, J = 8.5 Hz), 8.1-8.4 (8H, m), 8.84 (1H, s), 8.97 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1363,5 (M+Na+).
Элементный анализ для C59H69N10O23SNa·5H2O:
Вычислено: C 49,51; H 5,56; N 9,79
Найдено: C 49,39; H 5,63; N 9,77.
Пример 94
ИК (KBr): 3355, 2929, 2856, 1664, 1631, 1519, 1440,
1282 см-1
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, t, J = 5.8 Hz), 1.2-1.5 (12H, m), 1.7-2.0 (5H, m), 2.2-2.4 (3H, m), 2.5-2.7 (1H, m), 2.94 (2H, t, J = 7.4 Hz), 3.1-3.3 (1H, m), 3.6-4.6 (14H, m), 4.8-5.2 (7H, m), 5.10 (1H, d, J = 3.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.0-7.5 (4H, m), 8.0-8.2 (5H, m), 8.27 (1H, d, J = 7.7 Hz), 8.85 (1H, s), 8.93 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1279 (M+Na+).
Элементный анализ для C53H73N10O22SNa·5,5H2O:
Вычислено: C 46,93, H 6,24; N 10,33
Найдено: C 46,93; H 6,46; N 10,31.
Пример 95
ИК (KBr): 3363, 1673, 1648, 1538, 1253 см-1
ЯМР (DMSO-d6, δ): 0.92 (3H, t, J = 6.8 Hz), 0.97 (3H, d, J = 6.8 Hz), 1.10 (3H, d, J = 5.8 Hz), 1.2-1.5 (6H, m), 1.7-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (16H, m), 4.7-5.1 (9H, m), 5.16 (1H, d, J = 3.1 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.54 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.4 (8H, m), 8.04 (2H, d, J = 8.8 Hz), 8.13 (2H, d, J = 8.6 Hz), 8.2-8.4 (4H, m), 8.84 (1H, s), 8.98 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1329,6 (M+Na+).
Элементный анализ для C56H71N10O23SNa·7H2O:
Вычислено: C 46,92; H 5,92; N 9,77;
Найдено: C 46,86, H 5,99; N 9,77
Пример 96
ИК (KBr): 3355, 2929, 1666, 1648, 1631, 1515, 1442, 1047 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.7 Hz), 0.97 (3H, d, J = 6.7 Hz), 1.10 (3H, d, J = 5.8 Hz), 1.2-1.5 (10H, m), 1.7-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.6-4.6 (16H, m), 4.79 (2H, d, J = 5.9 Hz), 4.8-5.2 (5H, m), 5.09 (1H, d, J = 5.5 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.23 (1H, d, J = 4.5 Hz), 5.53 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.0 Hz), 6.8-6.9 (2H, m), 7.0-7.5 (6H, m), 7.97 (2H, d, J = 8.8 Hz), 8.0-8.3 (6H, m), 8.83 (1H, s), 8.88 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1373,5 (M+Na)+.
Элементный анализ для C58H75N10O22S2Na·6H2O:
Вычислено: C 47,73; H 6,01; N 9,60
Найдено: C 47,57; H 5,92; N 9,53.
Пример 97
ИК (KBr): 3361, 2925, 2852, 1668, 1650, 1631, 1538, 1452, 1049 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.9 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.2-1.4 (11H, m), 1.4-1.6 (2H, m), 1.7-2.1 (5H, m), 2.1-2.5 (5H, m), 2.5-2.6 (1H, m), 3.1-3.3 (2H, m), 3.7-4.5 (14H, m), 4.7-5.0 (7H, m), 5.09 (1H, d, J = 5.6 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.54 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, d), 7.04 (1H, s), 7.2-7.5 (3H, m), 8.03 (4H, s), 8.0-8.3 (2H, m), 8.84 (1H, s), 8.95 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1321,9 (M+Na)+.
Элементный анализ для C55H75N10O21S2Na·5H2O:
Вычислено: C 47,54, H 6,17; N 10,08
Найдено: C 47,38; H 6,12; N 9,98.
Пример 98
ИК (KBr): 3374, 2937, 2875, 1658, 1629, 1531, 1436, 1255, 1047 см-1
ЯМР (DMSO-d6, δ): 0.9-1.11 (6H, m), 1.09 (3H, d, J = 5.7 Hz), 1.2-1.5 (4H, m), 1.7-2.1 (5H, m), 2.2-2.5 (3H, m), 2.6-2.7 (1H, m), 3.2-3.3 (1H, m), 3.6-4.5 (16H, m), 4.80 (2H, d, J = 5.8 Hz), 4.8-5.2 (5H, m), 5.10 (1H, d, J = 5.5 Hz), 5.17 (1H, d, J = 3.0 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.53 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.06 (1H, s), 7.10 (2H, d, J = 8.9 Hz), 7.2-7.5 (3H, m), 7.68 (1H, s), 7.86 (2H, d, J = 8.8 Hz), 8.0-8.4 (6H, m), 8.84 (1H, s), 8.90 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1314 (M+Na+).
Элементный анализ для C56H70N9O23NaS·6H2O:
Вычислено: C 48,03; H 5,90; N 9,00
Найдено: C 47,92; H 5,83; N 8,88.
Пример 99
ИК (KBr): 3345, 1646, 1633, 1531, 1257 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.11 (3H, d, J = 5.7 Hz), 1.2-1.6 (10H, m), 1.7-2.5 (8H, m), 2.6-2.7 (1H, m), 3.21 (3H, s), 3.3-3.4 (1H, m), 3.7-4.6 (16H, m), 4.8-5.2 (8H, m), 5.16 (1H, d, J = 3.1 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.7 Hz), 6.7-6.9 (3H, m), 7.0-7.5 (6H, m), 8.0-8.3 (8H, m), 8.84 (1H, s), 8.96 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1387,7 (M+Na+).
Элементный анализ для C59H77N10O24NaS·6H2O:
Вычислено: C 48,09; H 6,09; N 9,51
Найдено: C 47,81; H 5,83; N 9,38.
Пример 100
ИК (KBr): 3357, 1668, 1631, 1429, 1284, 1047 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.8 Hz), 1.8-2.4 (6H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.7-4.6 (14H, m), 4.7-5.2 (7H, m), 5.10 (1H, d, J = 5.5 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.24 (1H, d, J = 5.5 Hz), 5.53 (1H, d, J = 5.8 Hz), 6.75 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 7.05 (1H, s), 7.3-7.6 (9H, m), 7.8-7.9 (4H, m), 8.0-8.2 (5H, m), 8.2-8.3 (1H, m), 8.34 (1H, d, J = 9.3 Hz), 8.7-8.8 (1H, m), 8.85 (1H, s)
FAB-МС: m/z = 1332,7 (M+Na+).
Элементный анализ для C58H65N10O22SNa·8H2O:
Вычислено: C 47,93; H 5,62; N 9,64
Найдено: C 47,83; H 5,53; N 9,56.
Пример 101
ИК (KBr): 3353, 2929, 2856, 1666, 1631, 1612, 1496, 1440, 1259 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.5 Hz), 1.09 (3H, d, J = 5.9 Hz), 1.2-1.5 (10H, m), 1.7-2.1 (5H, m), 2.2-2.5 (3H, m), 2.6-2.7 (1H, m), 3.1-3.2 (1H, m), 3.6-4.5 (16H, m), 4.7-5.0 (3H, m), 5.0-5.2 (5H, m), 5.10 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.2 Hz), 5.56 (1H, d, J = 5.5 Hz), 6.73 (1H, d, J = 8.1 Hz), 6.8-7.0 (2H, m), 7.05 (1H, s), 7.1-7.5 (5H, m), 8.0-8.4 (8H, m), 8.85 (1H, s), 8.95 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1357,3 (M+Na+).
Элементный анализ для C58H75N10O23SNa·7H2O:
Вычислено: C 47,67; H 6,14; N 9,58
Найдено: C 47,63; H 6,42; N 9,52.
Пример 102
ИК (KBr): 3361, 1670, 1648, 1633, 1540, 1519, 1249 см-1
ЯМР (DMSO-d6, δ): 0.89 (3H, t, J = 7.0 Hz), 0.97 (3H, d. J = 6.8 Hz), 1.10 (3H, d, J = 5.7 Hz), 1.2-1.5 (6H, m), 1.6-2.4 (8H, m), 2.5-2.7 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (16H, m), 4.80 (2H, d, J = 5.8 Hz), 4.8-5.2 (5H, m), 5.10 (1H, d, J = 5.4 Hz), 5.18 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.3 Hz), 5.55 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.0-7.5 (6H, m), 8.02 (1H, d, J = 5.3 Hz), 8.0-8.4 (4H, m), 8.42 (2H, d, J = 8.4 Hz), 8.48 (2H, d, J = 8.9 Hz), 8.8-9.0 (3H, m)
FAB-МС: m/z = 1339,3 (M+Na+).
Элементный анализ для C58H73N10O22SNa·6H2O:
Вычислено: C 48,87; H 6,01; N 9,83
Найдено: C 49,16; H 5,92; N 9,86.
Пример 103
ИК (KBr): 3350, 2971, 2859, 1672, 1629, 1537, 1442, 1247, 1047 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.8 Hz), 1.0-1.2 (6H, m), 1.2-1.6 (12H, m), 1.7-2.5 (8H, m), 2.5-2.6 (1H, m), 3.2-3.6 (7H, m), 3.7-4.5 (16H, m), 4.76 (2H, d, J = 5.6 Hz), 4.8-5.1 (5H, m), 5.09 (1H, d, J = 5.5 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.23 (1H, d, J = 5.5 Hz), 5.51 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 7.0-7.1 (3H, m), 7.3-7.5 (3H, m), 7.67 (2H, d, J = 6.9 Hz), 7.71 (2H, d, J = 6.9 Hz), 7.95 (2H, d, J = 8.4 Hz), 8.05 (1H, d, J = 7.0 Hz), 8.23 (1H, d, J = 7.7 Hz), 8.70 (1H,d, J = 7.0 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1377,1 (M+Na+).
Элементный анализ для C60H83N8O24NaS·5H2O:
Вычислено: C 49,86, H 6,49; N 7,75
Найдено: C 49,74; H 6,73; N 7,68.
Пример 104
ИК (KBr): 3349, 2937, 2858, 1672, 1629, 1537, 1444, 1249, 1047 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.08 (3H, d, J = 5.6 Hz), 1.2-1.7 (14H, m), 1.7-2.1 (5H, m), 2.1-2.4 (5H, m), 2.5-2.6 (1H, m), 3.1-3.2 (1H, m), 3.4-3.6 (4H, m), 3.7-4.5 (16H, m), 4.77 (2H, d, J = 5.7 Hz), 4.8-5.2 (5H, m), 5.09 (1H, d, J = 5.6 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.24 (1H, d, J = 4.5 Hz), 5.51 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 7.0-7.1 (3H, m), 7.3-7.5 (3H, m), 7.6-7.8 (4H, m), 7.96 (2H, d, J = 8.4 Hz), 8.10 (1H, d, J = 8.4 Hz), 8.24 (1H, d, J = 7.7 Hz), 8.71 (1H, d, J = 7.0 Hz), 8.89 (1H, s)
FAB-МС: m/z = 1386,5 (M+Na+).
Элементный анализ для C61H82N9O23NaS·6H2O:
Вычислено: C 49,76; H 6,43; N 8,56
Найдено: C 49,99; H 6,39; N 8,52.
Пример 105
ИК (KBr): 3350, 2933, 2856, 1664, 1631, 1604, 1511, 1450, 1243, 1045 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.5 Hz), 1.05 (3H, d, J = 5.7 Hz), 1.2-1.5 (8H, m), 1.6-2.0 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.0-3.3 (5H, m), 3.6-4.4 (20H, m), 4.7-5.1 (7H, m), 5.10 (1H, d, J = 5.5 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.27 (1H, d, J = 4.5 Hz), 5.51 (1H, d, J = 6.0 Hz), 6.7-7.1 (9H, m), 7.2-7.5 (3H, m), 9.0-8.2 (2H, m), 8.2-8.4 (1H, m), 8.4-8.6 (1H, m), 8.66 (1H, d, J = 2.2 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1360 (M+Na+).
Элементный анализ для C58H80N11O22SNa·6H2O:
Вычислено: C 48,16; H 6,41; N 10,65
Найдено: C 47,91; H 6,31; N 10,56.
Пример 106
ИК (KBr): 3369, 3345, 2935, 1672, 1629, 1511, 1245, 1047 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.06 (3H, d, J = 5.8 Hz), 1.3-1.6 (10H, m), 1.6-2.0 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.20 (3H, s), 3.28 (2H, t, J = 6.4 Hz), 3.1-3.4 (5H, m), 3.7-4.5 (20H, m), 4.7-5.1 (7H, m), 5.08 (1H, d, J = 5.5 Hz), 5.15 (1H, d, J = 3.1 Hz), 5.23 (1H, d, J = 4.5 Hz), 5.48 (1H, d, J = 5.8 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.82 (2H, d, J = 9.1 Hz), 6.94 (2H, d, J = 9.1 Hz), 6.9-7.0 (1H, m), 7.04 (1H, s), 7.3-7.5 (3H, m), 8.0-8.1 (2H, m), 8.27 (1H, d, J = 7.7 Hz), 8.49 (1H, d, J = 7.0 Hz), 8.66 (1H, d, J = 2.2 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1404 (M+Na+).
Пример 107
ИК (KBr): 3357, 1647, 1631, 1537, 1444, 1249, 1049 см-1
ЯМР (DMSO-d6, δ): 0.9-1.1 (6H, m), 1.09 (3H, d, J = 5.9 Hz), 1.6-2.4 (8H, m), 2.4-2.5 (1H, m), 3.1-3.3 (1H, m), 3.6-4.5 (16H, m), 4.8-5.2 (7H, m), 5.10 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.9 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.0-7.6 (6H, m), 7.73 (2H, d, J = 8.7 Hz), 7.86 (2H, d, J = 8.5 Hz), 8.0-8.3 (8H, m), 8.84 (1H, s), 8.9-9.0 (1H, m)
FAB-МС: m/z = 1379,4 (M+Na)+.
Элементный анализ для C59H69N10O22S2Na·6H2O:
Вычислено: C 48,36; H 5,57; N 9,56
Найдено: C 48,18; H 5,60; N 9,36.
Целевые соединения (108)-(117) получали способом, описанным в Примере 27.
Пример 108
ИК (KBr): 3350, 2933, 1670, 1627, 1521, 1436, 1272, 1047 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 6.7 Hz), 0.92 (3H, d, J = 6.7 Hz), 1.1-1.4 (11H, m), 1.7-2.4 (9H, m), 3.1-3.2 (1H, m), 3.5-5.4 (27H, m), 6.6-7.2 (8H, m), 7.5-7.8 (3H, m), 7.8-8.0 (3H, m), 8.1-8.8 (3H, m)
FAB-МС: m/z = 1249,4 (M+Na+).
Элементный анализ для C52H71N10O21NaS·7H2O:
Вычислено: C 46,15; H 6,33; N 10,35
Найдено: C 46,12; H 6,35; N 10,24
Пример 109
ИК (таблетка KBr): 3361, 2933, 2856, 1670, 1652, 1616, 1540, 1508, 1448, 1261, 1047 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.97 (3H, d, J = 6.8 Hz), 1.12 (3H, d, J = 6.8 Hz), 1.2-1.5 (10H, m), 1.7-2.0 (5H, m), 2.2-2.6 (4H, m), 3.1-3.2 (1H, m), 3.7-4.4 (16H, m), 4.8-5.3 (10H, m), 5.59 (1H, d, J = 6.0 Hz), 6.7-6.9 (3H, m), 7.0-7.4 (7H, m), 7.8-8.2 (4H, m), 8.8-9.0 (2H, m)
FAB-МС: m/z = 1280,3 (M+Na+).
Элементный анализ для C54H72N9O23NaS·7H2O:
Вычислено: C 46,45; H 6,21; N 9,03.
Найдено: C 46,68; H 6,44; N 9,03.
Пример 110
ИК (KBr): 3350, 2931, 1670, 1627, 1540, 1436, 1276, 1047 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.8 Hz), 0.93 (2H, d, J = 8.8 Hz), 1.08 (2H, d, J = 5.9 Hz), 1.2-1.4 (4H, m), 1.5-1.7 (2H, m), 1.7-2.1 (3H, m), 2.1-2.4 (3H, m), 2.6-2.7 (3H, m), 3.1-3.3 (1H, m), 3.6-4.5 (17H, m), 4.7-5.4 (8H, m), 6.73 (1H, d, J = 8.2 Hz), 6.83 (2H, d, J = 8.2 Hz), 7.0-7.1 (1H, m), 7.2-7.5 (5H, m), 7.65 (2H, d, J = 8.2 Hz), 7.74 (2H, d, J = 8.4 Hz), 7.98 (2H, d, J = 8.4 Hz), 8.08 (1H, d, J = 8.5 Hz), 8.25 (1H, d, J = 8.5 Hz), 8.74 (1H, d, J = 7.6 Hz), 8.7-9.0 (1H, br)
FAB-МС: m/z = 1231,2 (M+Na+).
Элементный анализ для C53H69N8O21Na·3H2O:
Вычислено: C 50,39; H 5,98; N 8,87
Найдено: C 50,34; H 6,25; N 8,90.
Пример 111
ИК (KBr): 3353,6, 1670,1, 1652,7, 1623,8 см-1
ЯМР (DMSO-d6, δ): 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.6 Hz), 1.20-1.62 (8H, m), 1.62-2.00 (5H, m), 2.10-2.65 (4H, m), 3.20 (3H, s), 3.08-3.40 (1H, m), 3.30 (2H, t, J = 6.5 Hz), 3.53-4.50 (15H, m), 4.68-5.13 (9H, m), 5.16 (1H, d, J = 2.9 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.53 (1H, d, J = 5.9 Hz), 6.68-6.95 (4H, m), 6.95-7.11 (3H, m), 7.20-7.52 (3H, m), 7.55-7.95 (7H, m), 8.13 (1H, d, J = 8.4 Hz), 8.31 (1H, d, J = 7.7 Hz), 8.53 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1331,5 (M+Na-1).
Элементный анализ для C58H77N8NaO23S·6H2O:
Вычислено: C 49,15; H 6,33; N 7,91
Найдено: C 49,07; H 6,53; N 7,84.
Пример 112
ИК (KBr): 3350, 2937, 1673, 1646, 1631, 1538, 1519, 1456, 1247, 1049 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.6 Hz), 1.07 (3H, d, J = 5.7 Hz), 1.3-2.4 (25H, m), 2.5-2.6 (1H, m), 3.2-3.4 (1H, m), 3.5-4.6 (20H, m), 4.8-5.7 (11H, m), 6.73 (1H, d, J = 8.0 Hz), 6.9-7.0 (2H, m), 7.0-7.2 (3H, m), 7.3-7.6 (3H, m), 7.74 (2H, d, J = 8.5 Hz), 7.77 (2H, d, J = 8.3 Hz), 8.02 (2H, d, J = 8.3 Hz), 8.13 (1H, d, J = 8.4 Hz), 8.30 (1H, d, J = 7.7 Hz), 8.77 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1389 (M+Na+).
Элементный анализ для C61H83N8O24NaS·7H2O:
Вычислено: C 49,06; H 6,55; N 7,50
Найдено: C 49,03; H 6,54; N 7,56.
Пример 113
ЯМР (DMSO-d6, δ): 0.84 (3H, t, J = 6.7 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.07 (3H, d, J = 5.9 Hz), 1.1-1.3 (14H, m), 1.7-2.1 (5H, m), 2.2-2.5 (3H, m), 2.6-2.7 (1H, m), 3.1-3.3 (1H, m), 3.7-4.5 (16H, m), 4.7-5.1 (7H, m), 5.10 (1H, d, J = 5.5 Hz), 5.16 (1H, d, J = 3.1 Hz), 5.25 (1H, d, J = 4.5 Hz), 5.49 (1H, d, J = 5.7 Hz), 6.53 (1H, d, J = 3.1 Hz), 6.73 (1H, d, J = 8.2 Hz), 6.8-6.9 (2H, m), 7.05 (1H, m), 7.31 (1H, d, J = 8.1 Hz), 7.4-7.6 (4H, m), 7.70 (1H, d, J = 6.7 Hz), 8.08 (1H, d, J = 8.4 Hz), 8.18 (1H, s), 8.31 (1H, d, J = 7.7 Hz), 8.57 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1264 (M+Na+).
Элементный анализ для C54H76N9O21NaS·6H2O:
Вычислено: C 48,03; H 6,57; N 9,34
Найдено: C 48,02; H 6,61; N 9,28.
Пример 114
ИК (KBr): 3350, 2937, 1668, 1631, 1537, 1247, 1047 см-1
ЯМР (DMSO-d6, δ): 0.85 (3H, t, J = 7.4 Hz), 0.96 (3H, d, J = 6.5 Hz), 1.07 (3H, d, J = 5.7 Hz), 1.3-1.7 (7H, m), 1.7-2.1 (5H, m), 2.2-2.4 (3H, m), 2.6-2.7 (1H, m), 3.0-3.8 (16H, m), 3.8-4.6 (11H, m), 4.7-5.3 (6H, m), 6.73 (1H, d, J = 8.2 Hz), 6.8-7.0 (2H, m), 7.0-7.2 (3H, m), 7.3-7.5 (3H, m), 7.6-7.8 (4H, m), 7.96 (2H, d, J = 8.3 Hz), 8.11 (1H, d, J = 8.2 Hz), 8.26 (1H, d, J = 7.6 Hz), 8.6-9.0 (2H, m)
FAB-МС: m/z = 1319,4 (M+Na+).
Элементный анализ для C57H77N8O23NaS·8H2O:
Вычислено: C 47,50; H 6,50; N 7,77
Найдено: C 47,72; H 6,85; N 7,85.
Пример 115
ИК (KBr): 3350, 1666, 1631, 1546, 1276, 1247 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 7.5 Hz), 1.08 (3H, d, J = 5.7 Hz), 1.4-1.6 (4H, m), 1.6-2.1 (5H, m), 2.1-2.4 (3H, m), 2.5-2.6 (1H, m), 3.1-3.3 (1H, m), 3.23 (3H, s), 3.3-3.5 (2H, m), 3.7-4.5 (16H, m), 4.79 (2H, d, J = 6.2 Hz), 4.8-5.1 (5H, m), 5.11 (1H, d, J = 5.6 Hz), 5.18 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.4 Hz), 5.54 (1H, d, J = 5.7 Hz), 6.73 (1H, d, J = 8.1 Hz), 6.8-7.0 (2H, m), 7.0-7.1 (3H, m), 7.3-7.5 (3H, m), 7.6-7.9 (8H, m), 8.01 (2H, d, J = 8.4 Hz), 8.08 (1H, d, J = 8.4 Hz), 8.32 (1H, d, J = 7.7 Hz), 8.80 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1353,9 (M+Na+).
Элементный анализ для C60H75N8O23NaS·9,5H2O:
Вычислено: C 47,96, H 6,31; N 7,46
Найдено: C 47,97; H 6,25; N 7,41.
Пример 116
ИК (KBr): 3450, 2935, 1675, 1650, 1540, 1513, 1454, 1047 см-1
ЯМР (DMSO-d6, δ): 0.97 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.9 Hz), 1.60 (6H, s), 1.7-2.4 (6H, m), 2.5-2.6 (1H, m), 3.1-3.6 (5H, m), 3.7-4.5 (14H, m), 4.7-5.0 (3H, m), 5.0-5.2 (4H, m), 5.11 (1H, d, J = 5.5 Hz), 5.18 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.56 (1H, d, J = 6.0 Hz), 6.8-7.5 (9H, m), 7.84 (2H, d, J = 8.8 Hz), 8.0-8.4 (6H, m), 8.85 (1H, s), 8.91 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1328 (M+Na)+.
Элементный анализ для C55H68N11O21S2Na·8H2O:
Вычислено: C 45,55; H 5,84, N 10,62
Найдено: C 45,62; H 5,70; N 10,54.
Пример 117
ИК (KBr): 3350, 2939, 1664, 1627, 1531, 1446, 1249, 1049 см-1
ЯМР (DMSO-d6, δ): 0.8-1.0 (6H, m), 1.4-1.9 (9H, m), 2.0-2.5 (4H, m), 3.1-3.2 (1H, m), 3.22 (3H, s), 3.3-3.4 (2H, m), 3.51 (2H, s), 3.6-4.4 (16H, m), 4.7-5.2 (7H, m), 5.07 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.23 (1H, d, J = 4.5 Hz), 5.54 (1H, d, J = 5.9 Hz), 6.7-6.8 (3H, m), 7.0-7.4 (8H, m), 7.5-7.7 (4H, m), 7.70 (4H, s), 8.1-8.2 (2H, m), 8.51 (1H, d, J = 7.0 Hz), 8.83 (1H, s)
FAB-МС: m/z = 1367,6 (M+Na+).
Элементный анализ для C61H77N8O23SNa·6,5H2O:
Вычислено: C 50,01; H 6,20; N 7,66
Найдено: C 50,30; H 6,50; N 7,75.
Пример 118
К раствору целевого соединения (61) (0,25 г) в метаноле (50 мл) добавляли безводный 10% палладий на угле (0,2 г) и полученную смесь размешивали в течение 6 часов в атмосфере водорода. После отфильтровывания палладия на угле фильтрат выпаривали при пониженном давлении, в результате чего получали целевое соединение 118 (179 мг).
ИК (KBr): 3400, 1668,1, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.92 (3H, d, J = 6.7 Hz), 1.1-2.45 (40H, m), 3.20 (3H, s), 3.28 (2H, t, J = 6.5 Hz), 3.0-3.4 (1H, m), 3.5-4.7 (14H, m), 4.95-5.5 (12H, m), 6.55 (1H, d, J = 8.4 Hz), 6.84 (1H, s), 6.86 (1H, d, J = 8.4 Hz), 7.0-7.3 (4H, m), 7.9-8.3 (4H, m)
FAB-МС: m/z = 1292 (M+Na).
Элементный анализ для C54H88N9O22SNa·5H2O:
Вычислено: C 47,67; H 7,26; N 9,26
Найдено: C 47,72; H 7,35; N 8,95.
Целевые соединения (119)-(121) были получены способом, аналогичным описанному в Примере 118.
Пример 119
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 6.6 Hz), 1.00 (3H, d, J = 7.3 Hz), 1.03 (3H, d, J = 6.0 Hz), 1.2-1.5 (4H, m), 1.5-2.0 (5H, m), 2.1-2.7 (8H, m), 3.17 (1H, m), 3.6-4.5 (14H, m), 4.65-5.7 (12H, m), 6.72 (1H, d, J = 8.1 Hz), 6.75 (1H, s), 6.80 (1H, d, J = 8.1 Hz), 7.05 (1H, s), 7.1-7.7 (15H, m), 8.0-8.6 (4H, m), 8.85 (1H, s)
FAB-МС: m/z = 1274 (M+Na).
Элементный анализ для C55H74N9O21SNa·7H2O:
Вычислено: C 47,93; H 6,43; N 9,15.
Найдено: C 48,12; H 6,56; N 9,03.
Пример 120
ИК (KBr): 3355,5, 1672,0, 1629,6 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.98 (3H, d, J = 6.5 Hz), 1.03 (3H, d, J = 6.0 Hz), 1.2-2.6 (21H, m), 3.18 (1H, m), 3.6-4.5 (16H, m), 4.65-5.55 (12H, m), 6.6-7.5 (10H, m), 8.0-8.6 (4H, m), 8.89 (1H, s)
FAB-МС: m/z = 1256 (M+Na).
Пример 121
ИК (KBr): 3357,5, 1660,4, 1629,6, 1249,6 см-1
ЯМР (DMSO-d6, δ): 0.86 (3H, t, J = 6.6 Hz), 0.96 (3H, d, J = 6.8 Hz), 1.03 (3H, d, J = 6.0 Hz), 1.1-1.5 (12H, m), 1.6-2.0 (5H, m), 2.0-2.5 (4H, m), 3.07 (1H, m), 3.5-4.5 (16H, m), 4.6-5.6 (12H, m), 6.72 (1H, d, J = 8.1 Hz), 6.7-6.9 (4H, m), 7.04 (1H, s), 7.16 (1H, s), 7.1-7.5 (2H, m), 7.25 (2H, d, J = 8.6 Hz), 8.0-8.2 (3H, m), 8.46 (1H, d, J = 7 Hz), 8.84 (1H, s)
FAB-МС: m/z = 1256 (M+Na).
Элементный анализ для C52H76N9O22SNa·7H2O:
Вычислено: C 45,91; H 6,67; N 9,27
Найдено: C 45,98; H 6,67; N 9,10.
Пример 122
Раствор целевого соединения (11) (795 мг) в воде (16 мл) оставляли на 240 часов. После этого раствор подвергали колоночной хроматографии на ODS (УМС-гель, ODS-AM·S-50) и элюировали смесью 25% CH3CN/H2O. Фракции, содержащие целевое соединение, объединяли, а ацетонитрил удаляли при пониженном давлении. Затем остаток лиофилизовали, в результате чего получали целевое соединение (123) (38 мг).
ИК (KBr): 3361, 2956, 2875, 1668, 1627, 1521, 1249, 1047 см-1
ЯМР (DMSO-d6, δ): 0.8-1.5 (19H, m), 1.6-2.4 (13H, m), 3.1-3.2 (1H, m), 3.5-4.1 (12H, m), 4.1-4.7 (10H, m), 4.9-5.6 (5H, m), 5.98 (1H, d, J = 10.6 Hz), 6.36 (1H, d, J = 10.6 Hz), 6.7-7.3 (12H, m), 7.4-8.0 (7H, m)
FAB-МС: m/z = 1273,1 (M+Na+).
Элементный анализ для C55H71N8O22SNa·11H2O:
Вычислено: C 45,58; H 6,47; N 7,73
Найдено: C 45,83; H 6,26; N 7,75.
Целевое соединение (123) было получено способом, описанным в Примере 118.
Пример 123
ИК (KBr): 3349,7, 1670,1, 1627,6 см-1
ЯМР (DMSO-d6, δ): 0.87 (3H, t, J = 7.2 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.13 (3H, d, J = 5.7 Hz), 1.18-1.55 (10H, m), 1.58-2.08 (5H, m), 2.08-2.90 (4H, m), 2.90-3.30 (2H, m), 3.60-4.50 (17H, m), 4.70-5.70 (12H, m), 6.65-7.60 (11H, m), 7.80 (2H, br s), 7.95-8.23 (2H, m), 8.75 (1H, d, J = 7.0 Hz), 8.85 (1H, s)
FAB-МС: m/z = 1114,4 (M-SO4-2).
Элементный анализ для C52H77N9O21S·6H2O:
Вычислено: C 47,88; H 6,88; N 9,66
Найдено: C 47,60; H 6,74; N 9,53.
Нижеследующее соединение (124) было получено способом, описанным в Примере 1.
Пример 124
ИК (KBr): 3324, 2937, 2873, 1664, 1629, 1442, 1257 см-1
ЯМР (DMSO-d6, δ): 0.91 (3H, t, J = 7.1 Hz), 0.96 (3H, d, J = 6.7 Hz), 1.09 (3H, d, J = 5.7 Hz), 1.3-1.5 (4H, m), 1.7-2.6 (9H, m), 3.1-3.3 (1H, m), 3.7-4.6 (16H, m), 4.7-5.1 (7H, m), 5.11 (1H, d, J = 5.6 Hz), 5.17 (1H, d, J = 3.1 Hz), 5.26 (1H, d, J = 4.5 Hz), 5.55 (1H, d, J = 5.8 Hz), 6.7-6.9 (3H, m), 7.0-7.6 (6H, m), 7.97 (2H, d, J = 8.8 Hz), 8.0-8.4 (6H, m), 8.85 (1H, s), 8.92 (1H, d, J = 7.0 Hz)
FAB-МС: m/z = 1331 (M+Na+).
Элементный анализ для C55H69N10O22NaS2:
Вычислено: C 45,45; H 5,89; N 9,64
Найдено: C 45,71; H 5,68; N 9,60.
Испытание на активность против микроорганизмов
Методика испытания
Активность против микроорганизмов in vitro испытуемых соединений определяли методом двухкратного разведения в планшете с агаром.
Одну петлю с ночной культурой каждого испытуемого микроорганизма в среде Сабуро, содержащей 2% глюкозы (105 жизнеспособных клеток на 1 мл), наносили штрихом на агар Сабуро с декстрозой (SDA: декстроза 2%), включающий ступенчато возрастающие концентрации испытуемых соединений, и после инкубирования в течение 24 часов при 30oC определяли минимальную ингибирующую концентрацию (MIC), которую выражали в мкг/мл.
Испытуемый микроорганизм: C.albicans FP633
Результаты испытаний представлены в табл. 2.
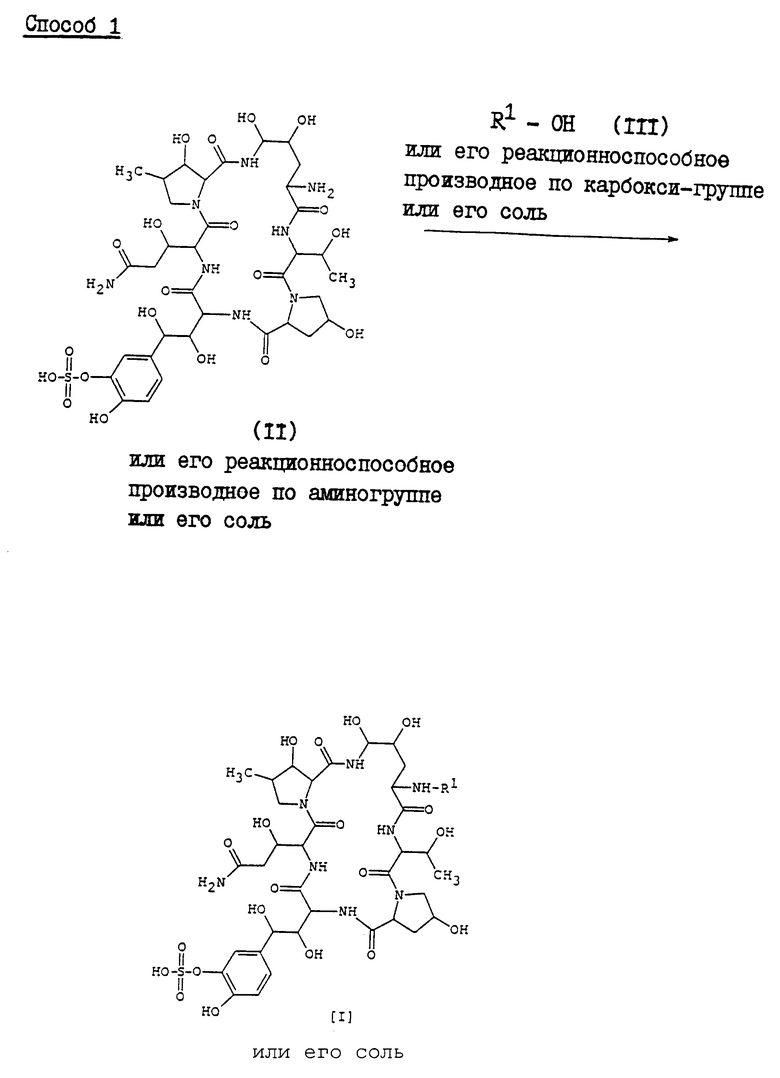
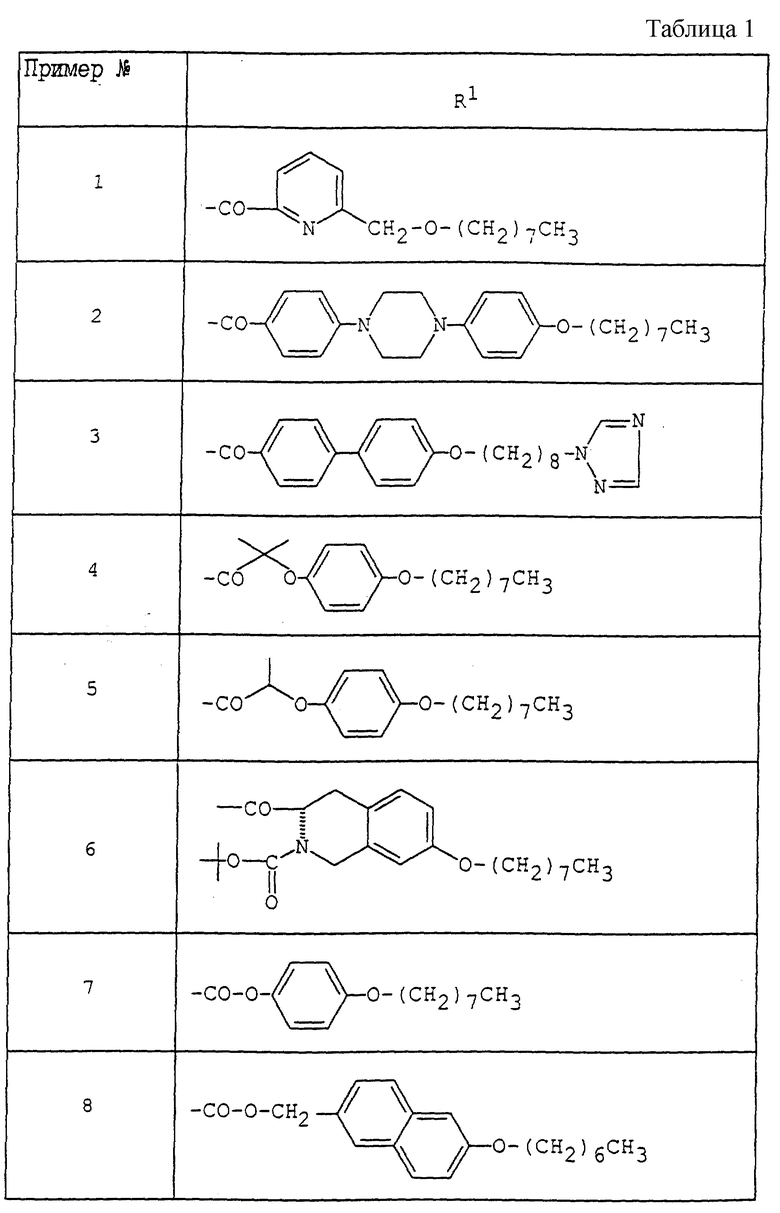
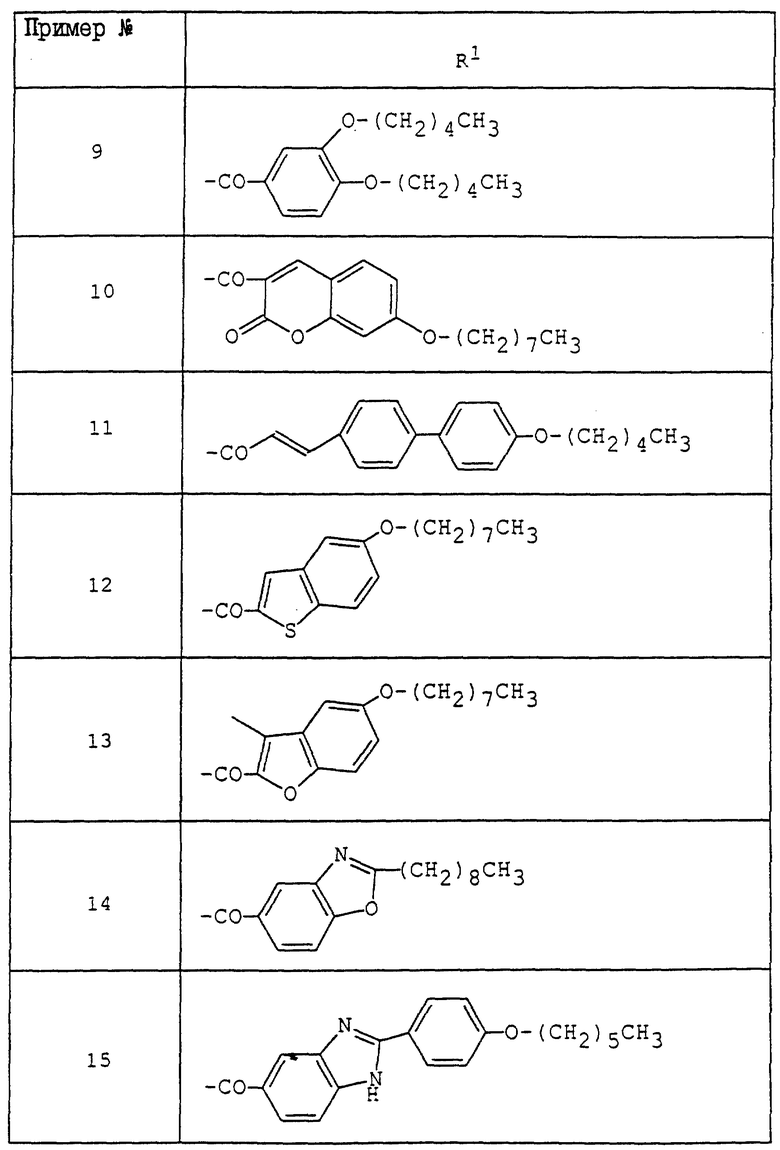
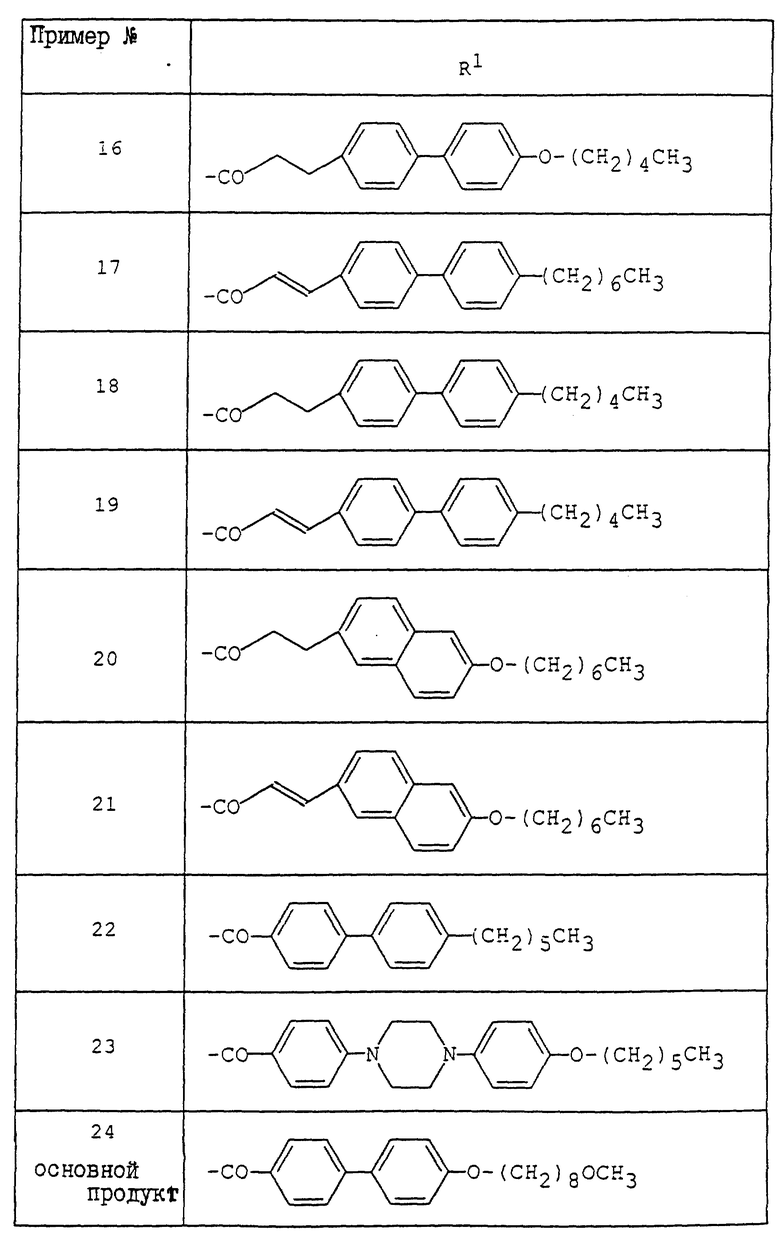
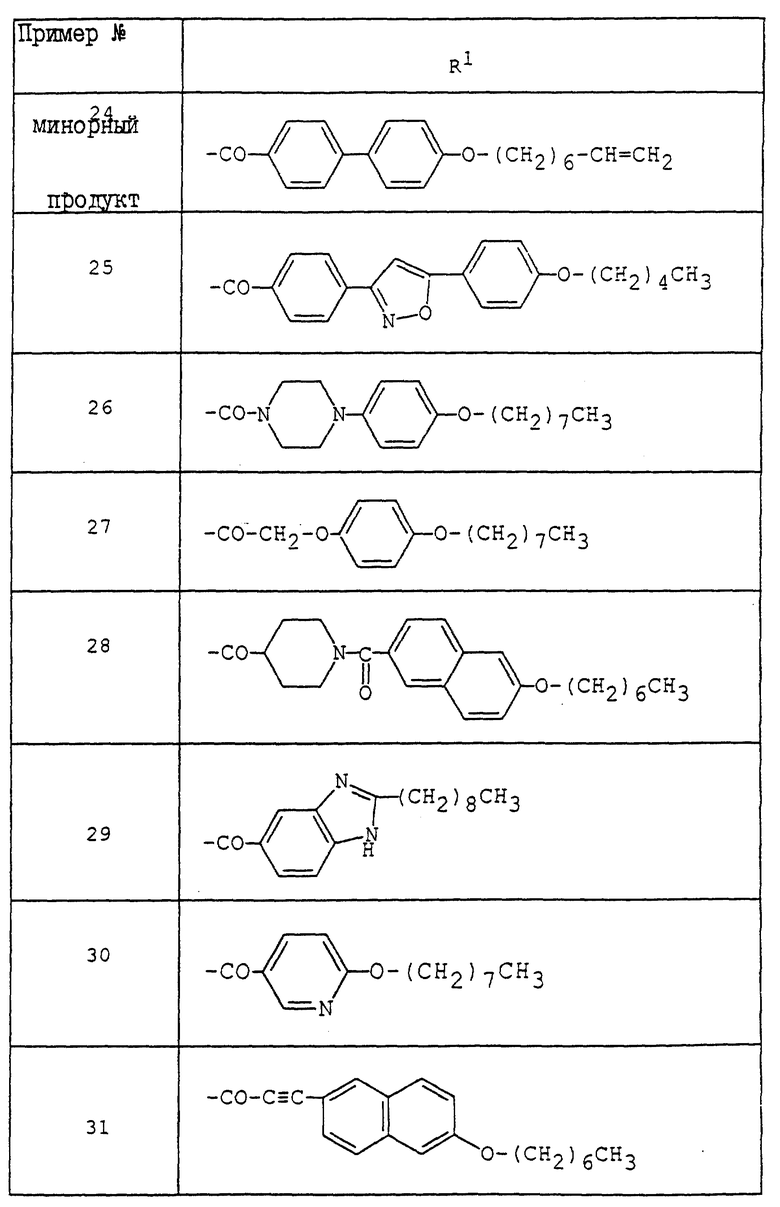
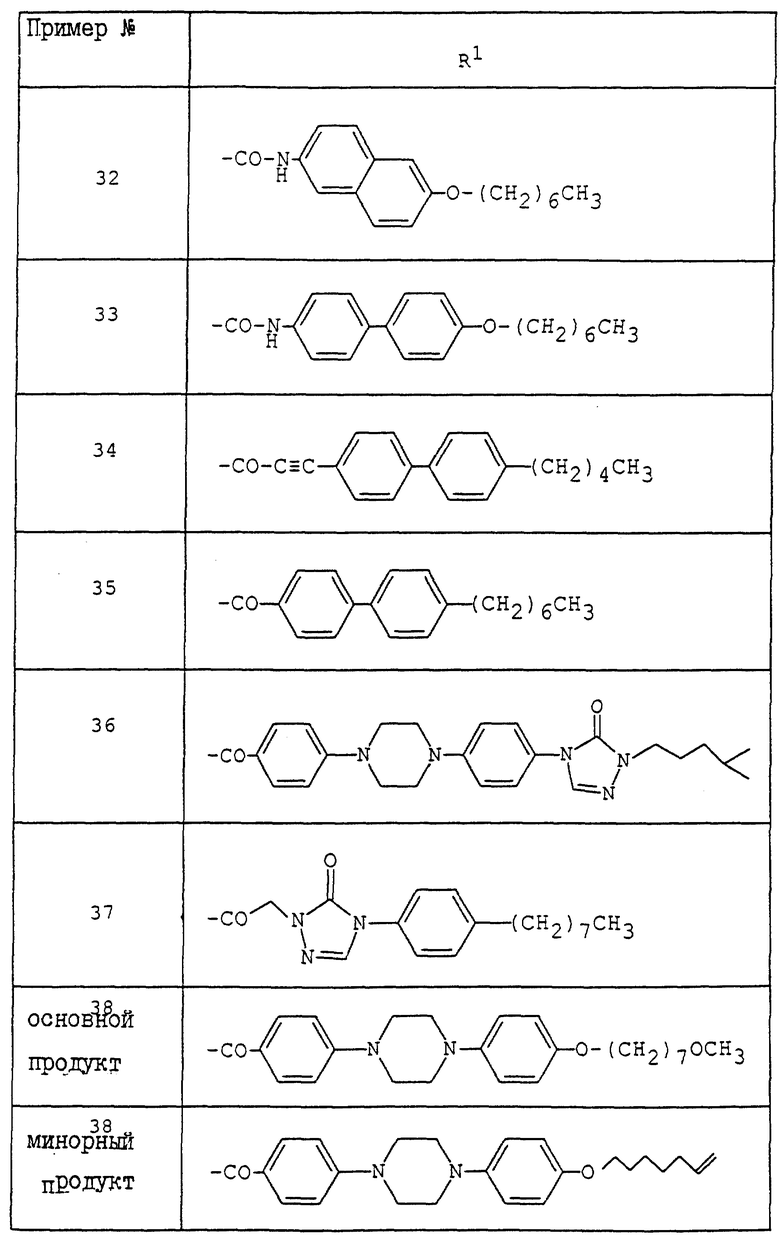
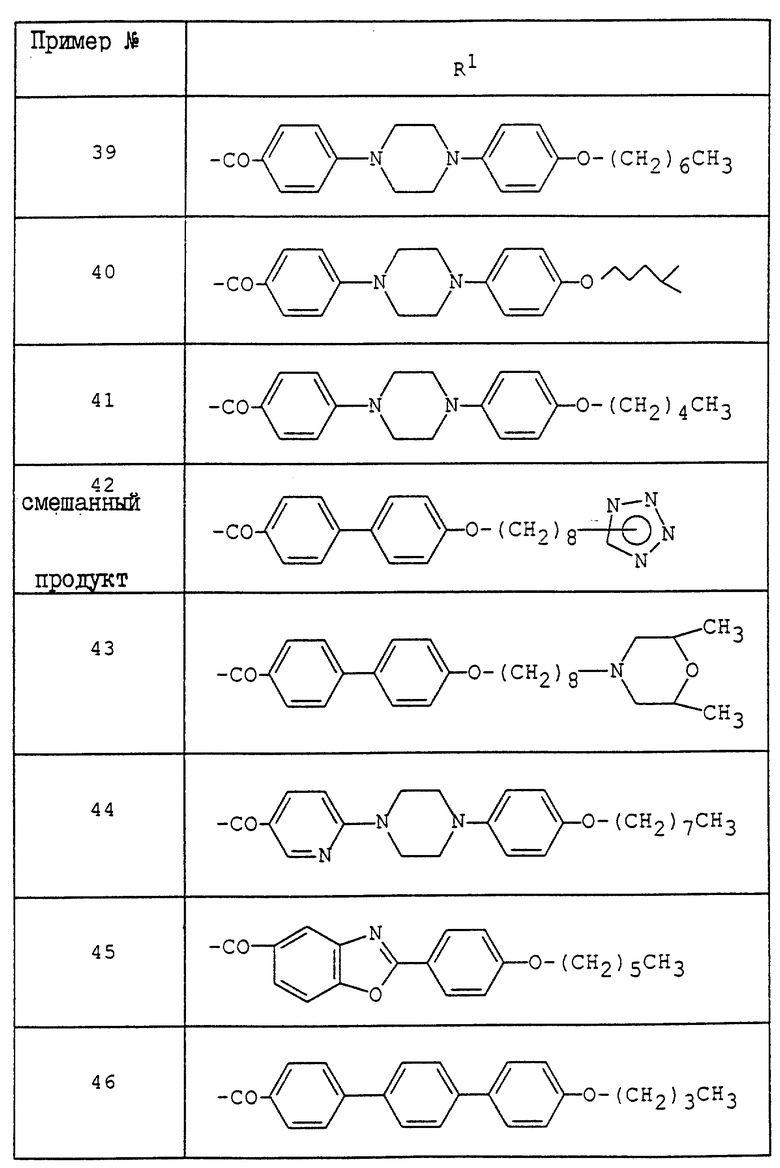
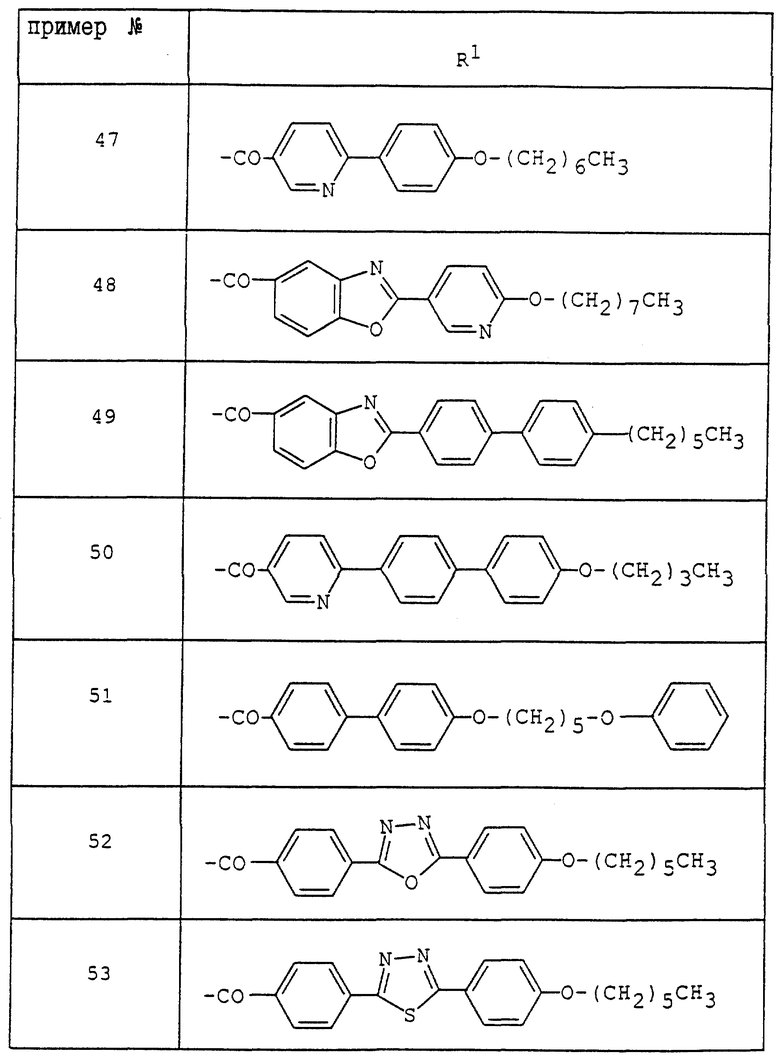
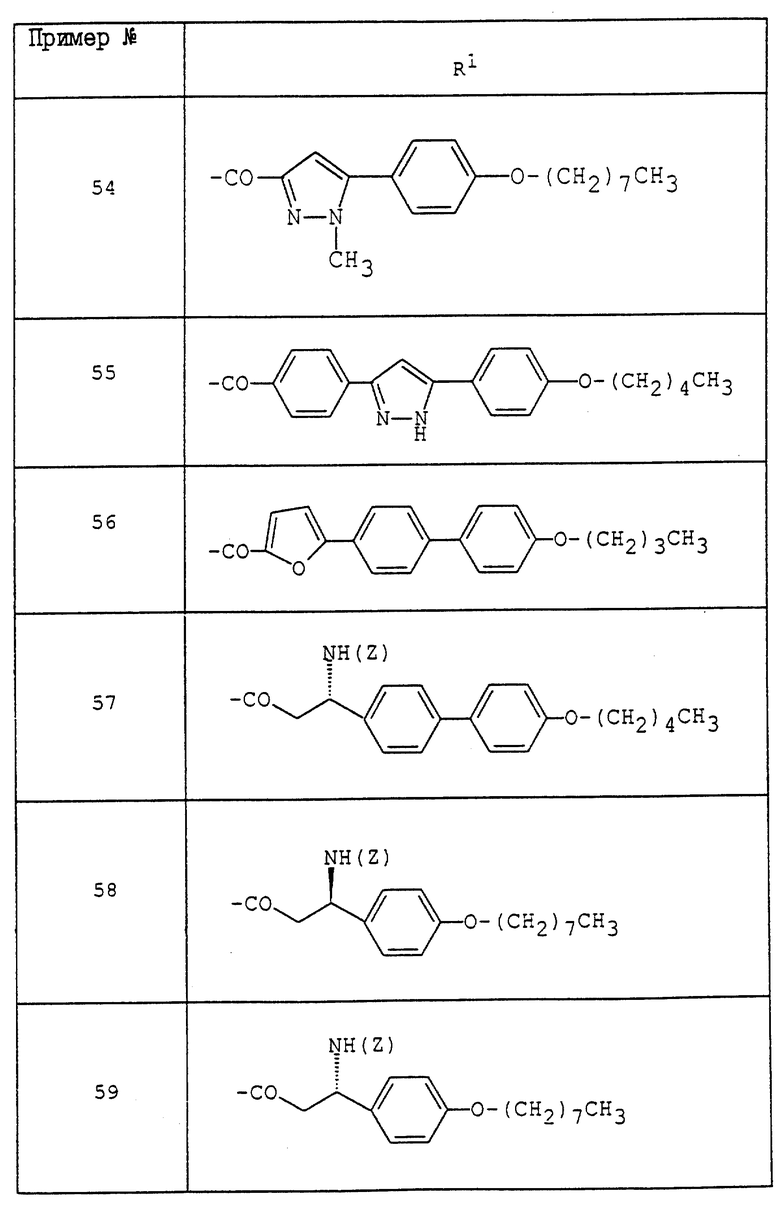
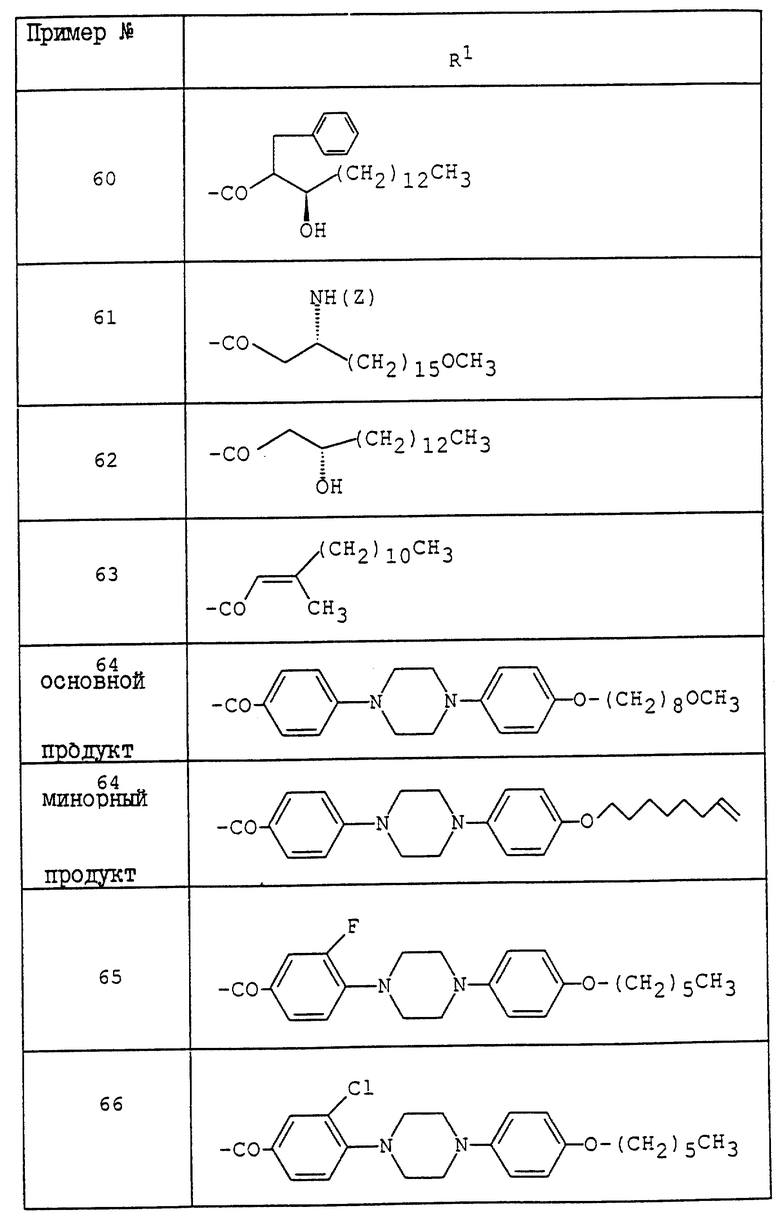
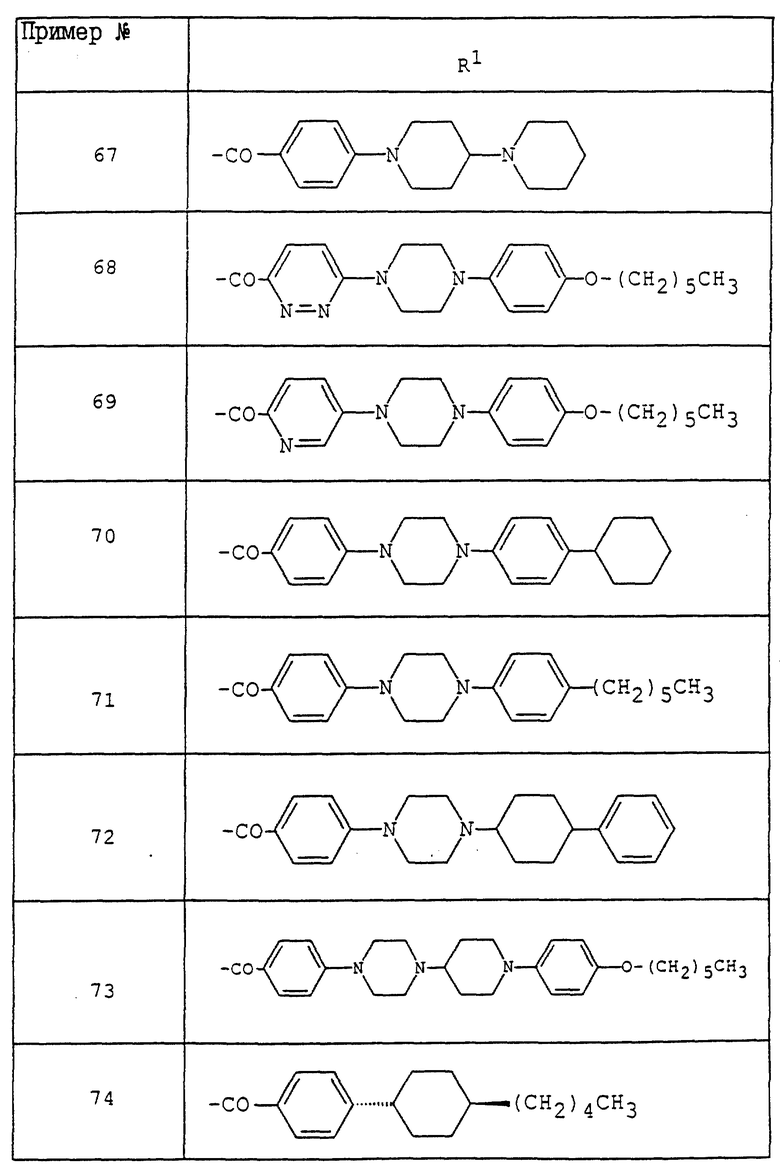
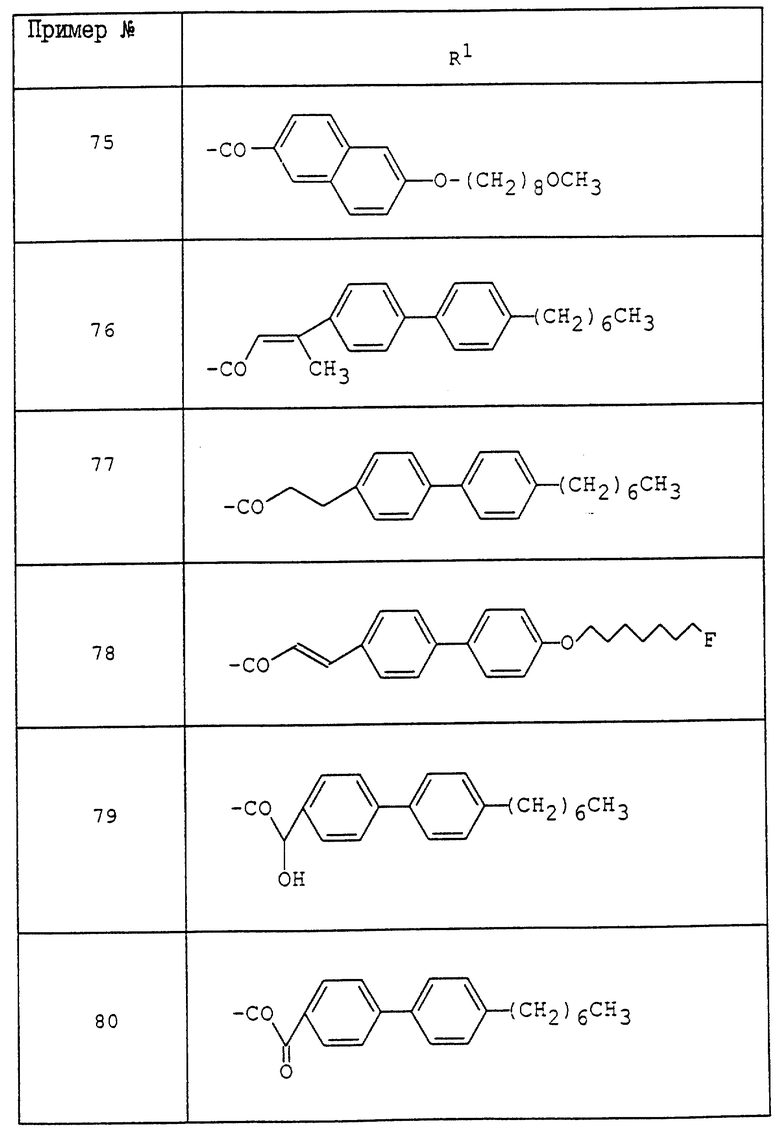
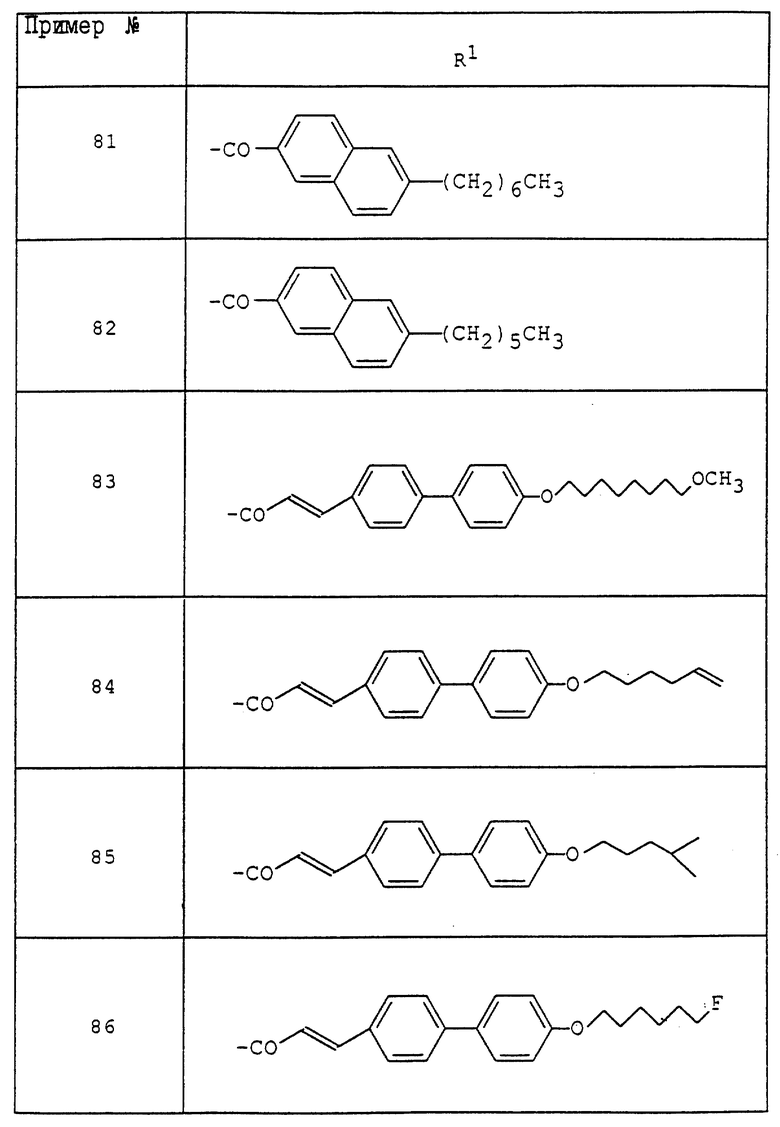
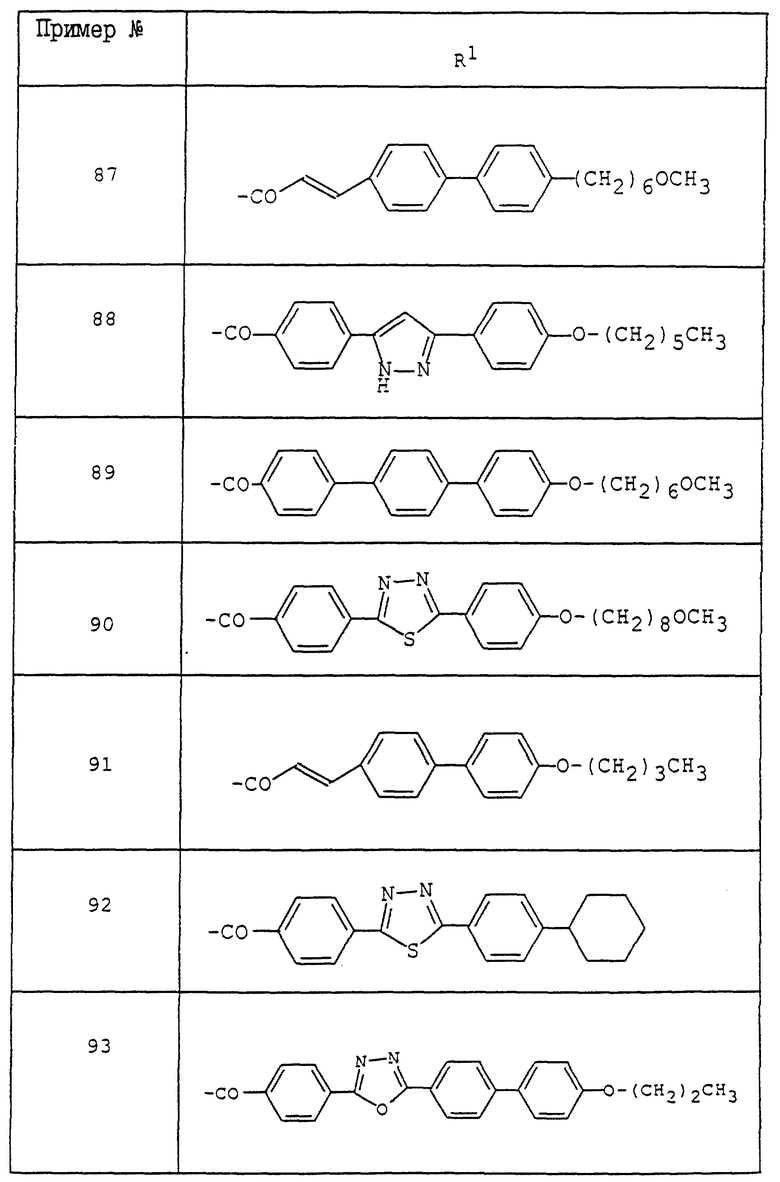
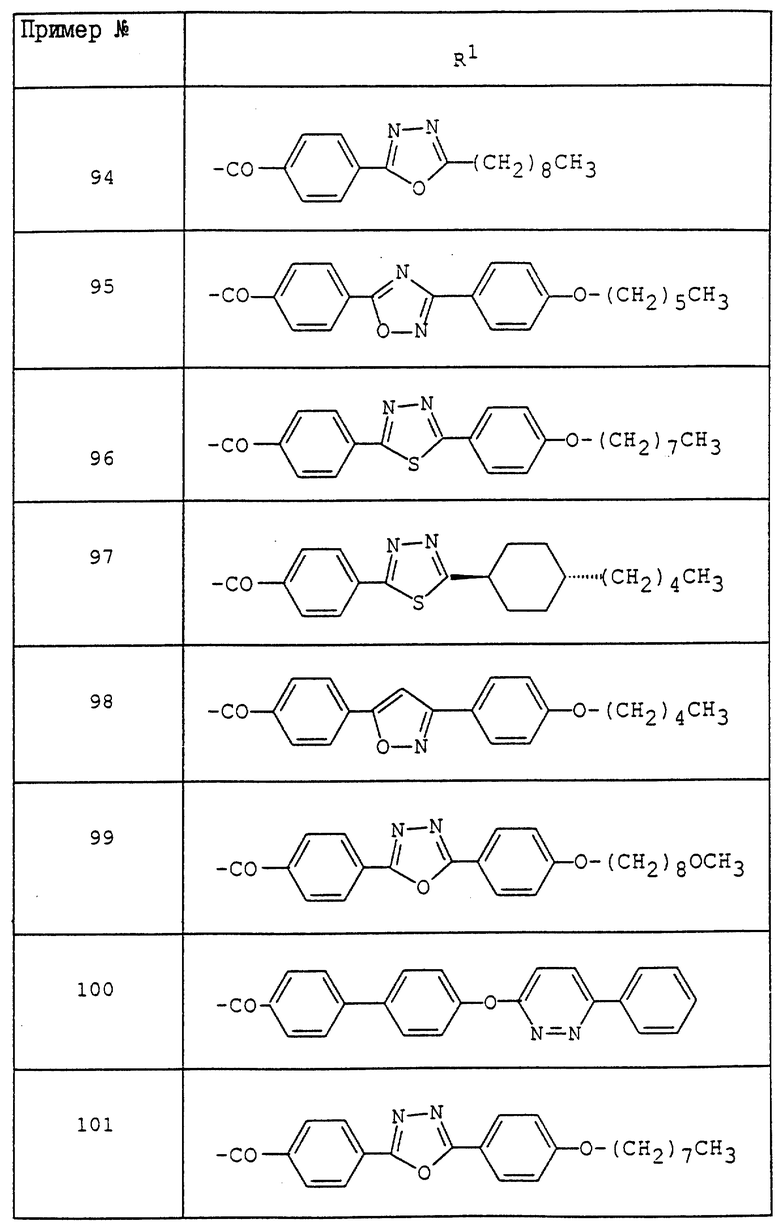
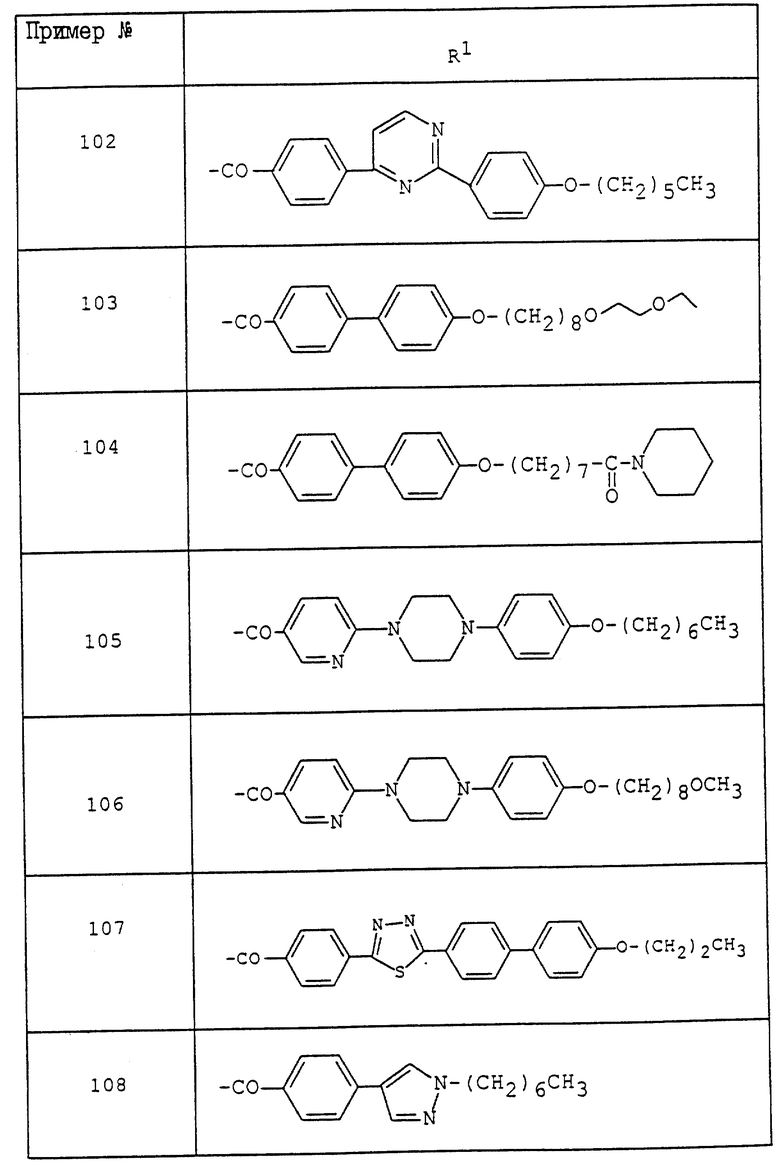
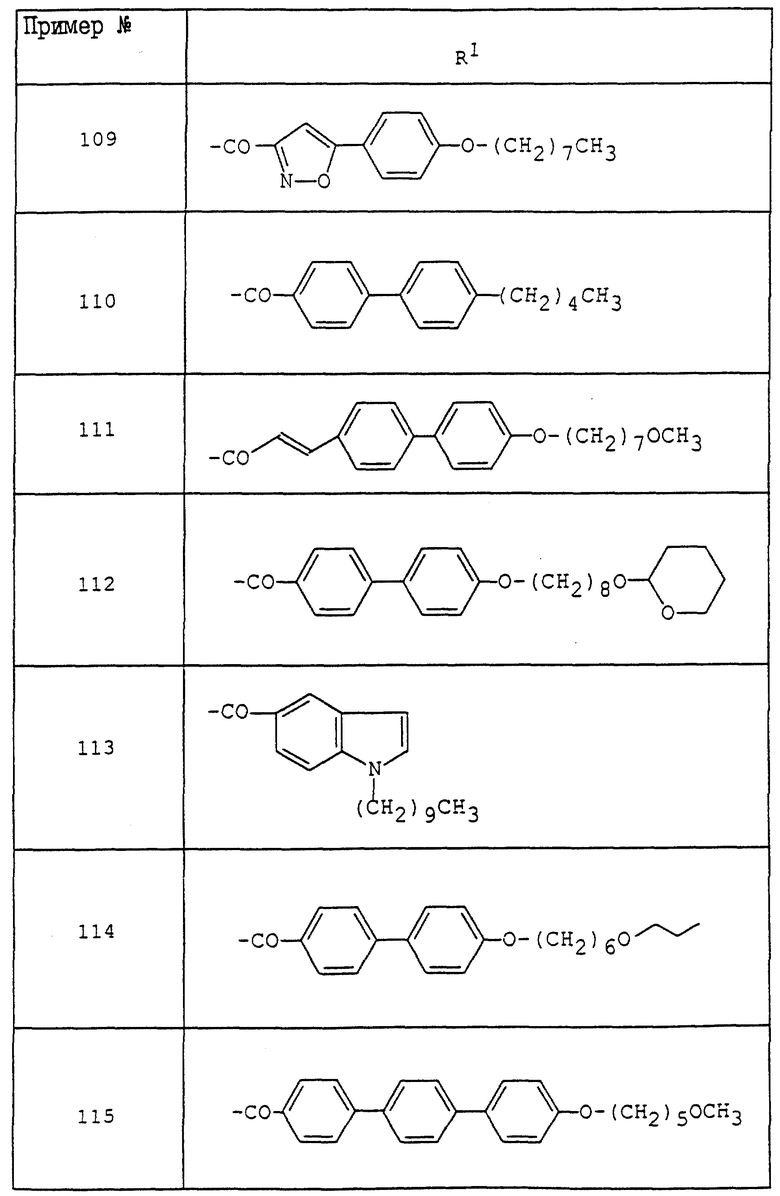
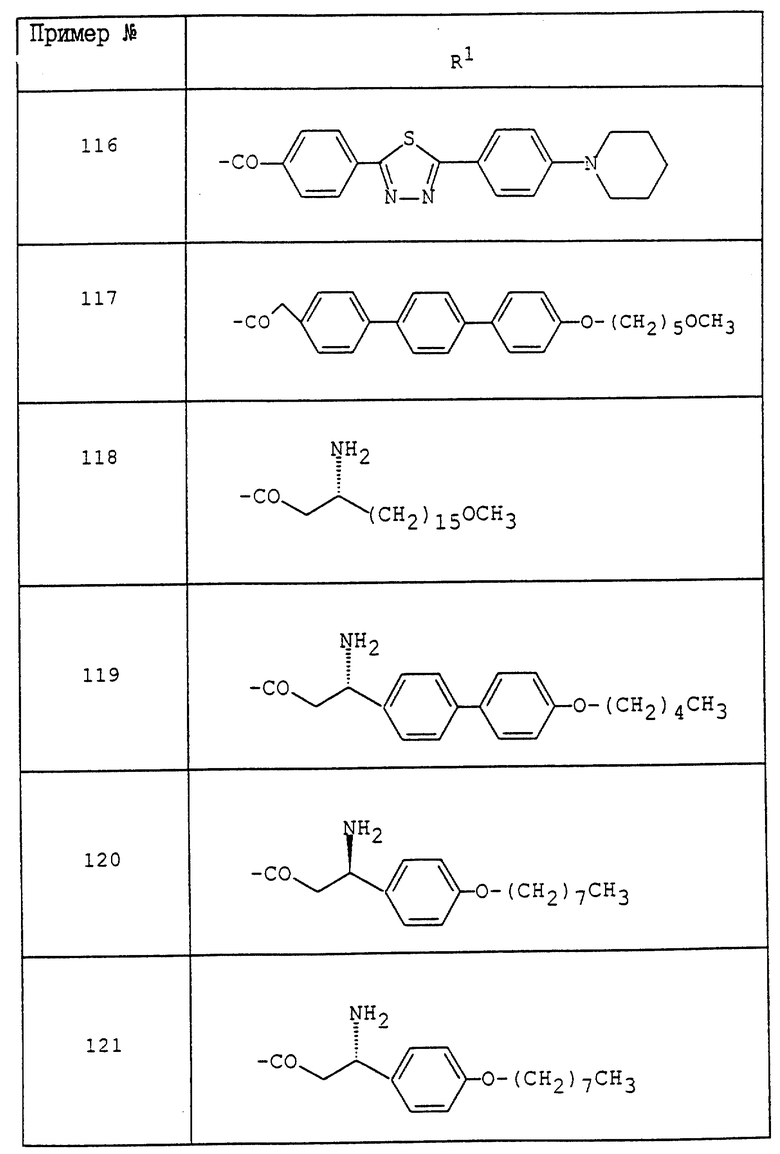
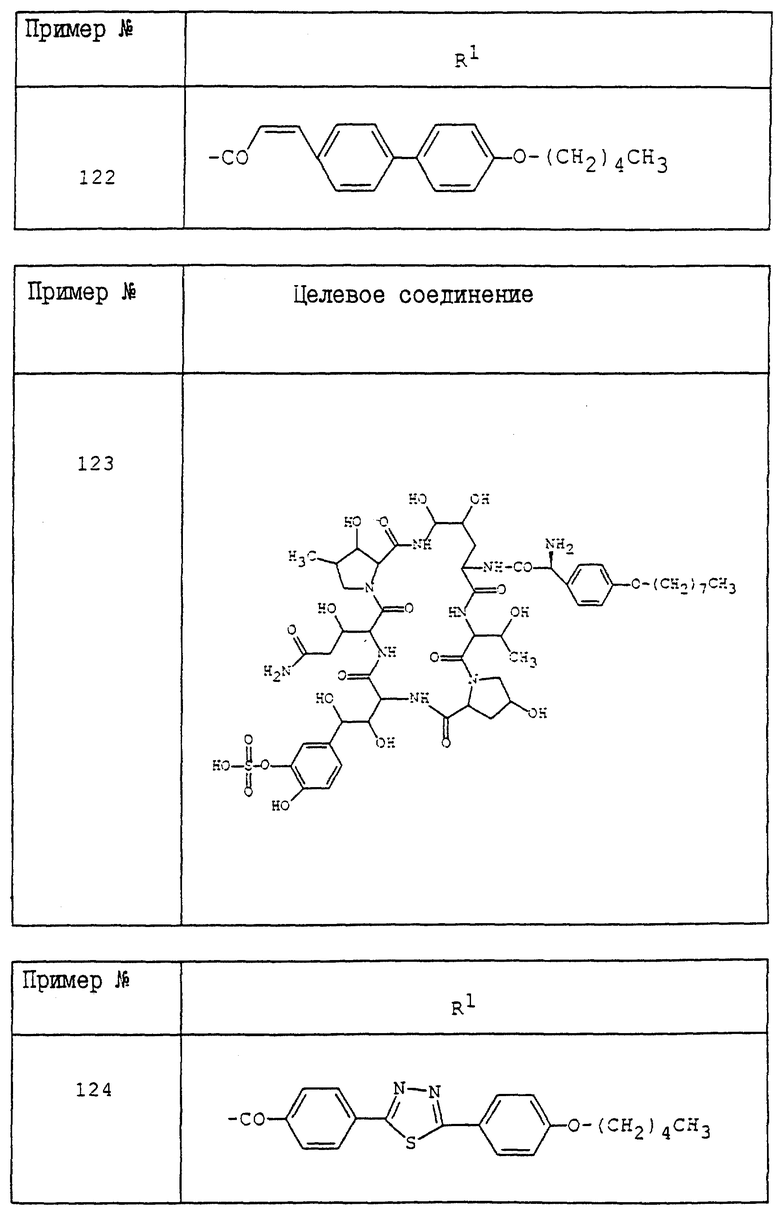
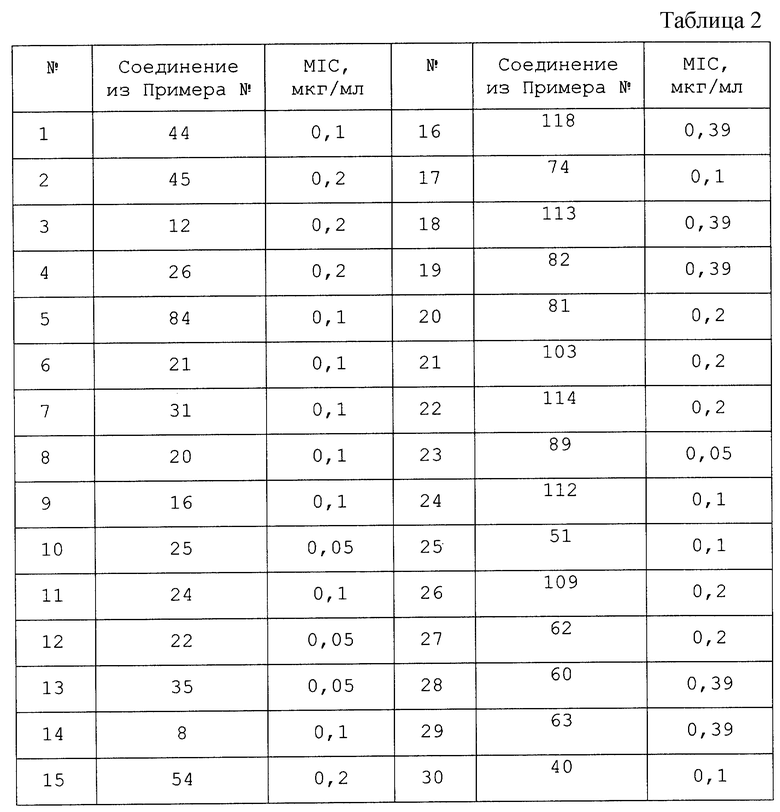
Изобретение относится к полипептидному соединению общей формулы I, где R1 обозначает низший алканоил, замещенный ненасыщенной 6-членной гетеромоноциклической группой, содержащей по крайней мере один атом азота, которая может иметь один или несколько подходящих заместителей; низший алканоил, замещенный 1,2,3,4-тетрагидроизохинолином, который может иметь один или несколько подходящих заместителей; низший алканоил, замещенный ненасыщенной конденсированной гетероциклической группой, содержащей по крайней мере один атом кислорода, которая может иметь один или несколько подходящих заместителей, или к их фармацевтически приемлемым солям. Соединения обладают противомикробной активностью (в частности, противогрибковой активностью) и активностью, ингибирующей действие β-1,3-глюкансинтазы. Кроме того, изобретение относится к способу получения указанных соединений, к фармацевтическим композициям, содержащим эти соединения. Соединения могут быть использованы для предупреждения и/или терапевтического лечения инфекционных заболеваний, включая инфекцию, вызываемую Pneumocystis carinii (например, пневмонию, вызываемую Pneumocystis carinii), у человека или животных. 3 с. и 5 з.п.ф-лы, 2 табл.
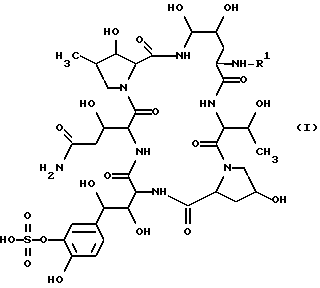
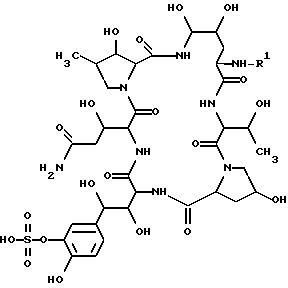
где R1 обозначает низший алканоил, замещенный пиридилом или пиридазинилом, каждый из которых может иметь 1-3 заместителя, выбранных из группы, включающей высший алкокси, высший алкокси(низший)алкил; фенил, имеющий высший алкокси; фенил, замещенный фенилом, имеющим низший алкокси; пиперазинил, замещенный фенилом, имеющим высший алкокси; пиперазинил, замещенный фенилом, имеющим низший алкокси(высший)алкокси; и пиперазинил, замещенный фенилом, имеющим низший алкокси; низший алканоил, замещенный 1,2,3,4-тетрагидроизохинолином, имеющим высший алкокси и низший алкоксикарбонил; низший алканоил, замещенный кумарином, который может иметь 1-3 заместителя, выбранных из группы, включающей высший алкокси и оксогруппу; низший алканоил, замещенный бензотиофенилом, который может иметь 1-3 высших алкокси; низший алканоил, замещенный бензо[b]фуранилом, который может иметь 1-3 заместителя, выбранных из группы, включающей высший алкокси и низший алкил; низший алканоил, замещенный бензооксазолилом, который может иметь 1-3 заместителя, выбранных из группы, включающей высший алкил; фенил, имеющий низший алкокси; фенил, замещенный фенилом, имеющим низший алкил; и пиридил, имеющий высший алкокси; низший алканоил, замещенный бензимидазолилом, который может иметь 1-3 заместителя, выбранных из группы, включающей высший алкил и фенил, имеющий низший алкокси; низший алканоил, замещенный пиперидилом или пиперазинилом, каждый из которых может иметь 1-3 заместителя, выбранных из группы, включающей фенил, имеющий высший алкокси, и нафтоил, имеющий высший алкокси; фенил(низший)алкеноил, замещенный фенилом, который может иметь 1-3 заместителя, выбранных из группы, включающей низший алкокси, низший алкил, высший алкил, низший алкокси(высший)алкил, галоген(низший)алкокси, низший алкенилокси, галоген(высший)алкокси, и низший алкокси(высший)алкокси; нафтил(низший)алкеноил, который может иметь 1-3 высших алкокси; низший алкиноил, который может иметь 1-3 заместителя, выбранных из группы, включающей нафтил, имеющий высший алкокси, и фенил, замещенный фенилом, имеющим низший алкил; фенил(C2-C6)алканоил, замещенный фенилом, который имеет 1-3 заместителя, выбранных из группы, включающей низший алкокси, высший алкокси, низший алкил, высший алкил и фенил, имеющий низший алкокси(низший)алкил; где указанный фенил(C2-C6)алканоил может иметь гидрокси-, оксо-, защищенную амино-, или аминогруппу; (C2-C6)алканоил, замещенный нафтилом, имеющим высший алкокси; фенилокси(низший)алканоил, который может иметь 1-3 высших алкокси; фенил(низший)алкокси(низший)алканоил, который может иметь 1-3 высших алкокси; фениламино(низший)алканоил, который может иметь 1-3 высших алкокси; бензоил, замещенный пиперазинилом, который может иметь 1-3 заместителя, выбранных из группы, включающей фенил, имеющий низший алкокси; фенил, имеющий высший алкокси; фенил, имеющий низший алкил; фенил, имеющий низший алкокси(высший)алкокси; фенил, имеющий высший алкенилокси; пиперидил, замещенный фенилом, имеющим низший алкокси; цикло(низший)алкил, имеющий фенил; фенил, имеющий цикло(низший)алкил; и фенил, замещенный триазолилом, имеющим оксо и низший алкил; где указанный бензоил может иметь галоген; бензоил, замещенный изоксазолилом, который может иметь 1-3 заместителя, выбранных из группы, включающей высший алкил; фенил, имеющий низший алкокси; фенил, имеющий высший алкокси; фенил, имеющий низший алкокси(высший)алкокси; и фенил, замещенный фенилом, имеющим низший алкокси; бензоил, замещенный фенилом, имеющим низший алкокси(высший)алкокси; бензоил, замещенный фенилом, имеющим низший алкил; бензоил, замещенный фенилом, имеющим высший алкил; фенил(низший)алкеноил, замещенный фенилом, который может иметь 1-3 заместителя, выбранных из группы, включающей низший алкокси, низший алкил, высший алкил; низший алкокси(низший)алкил, галоген(низший)алкокси, низший алкенилокси, галоген(высший)алкокси и низший алкокси(высший)алкокси; бензоил, замещенный тиадиазолилом, который может иметь 1-3 заместителя, выбранных из группы, включающей фенил, имеющий низший алкокси; фенил, имеющий высший алкокси; цикло(низший)алкил, имеющий низший алкил; фенил, замещенный фенилом, имеющим низший алкокси; фенил, имеющий цикло(низший)алкил; фенил, имеющий пиперидил; и фенил, имеющий низший алкокси(высший)алкокси; или бензоил, замещенный оксадиазолилом, который может иметь 1-3 заместителя, выбранных из группы, включающей фенил, имеющий низший алкокси; фенил, имеющий высший алкокси; фенил, имеющий низший алкокси(высший)алкокси; высший алкил и фенил, замещенный фенилом, имеющим низший алкокси,
или его фармацевтически приемлемая соль.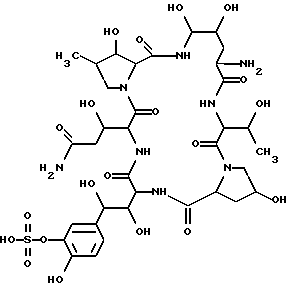
или его производное, реакционноспособное по аминогруппе, или его соль подвергают взаимодействию с соединением формулы III
R1-OH
где R1 определен в п.1, или с его производным, реакционноспособным по карбоксигруппе, или с его солью, в результате чего получают соединение формулы I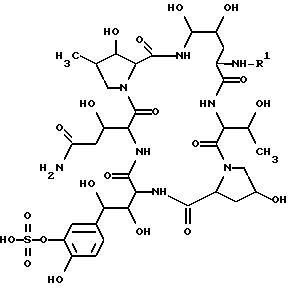
где R1 определен, как указано в п.1,
или его соль.
Приоритет по признакам:
07.10.94 все признаки изобретения, изложенные в п.1;
28.04.95 уточнение признаков.
| Устройство для определения величиныи точки приложения равнодействующейсил давления света на тело сложнойформы | 1974 |
|
SU509795A1 |
| SU, 1574603 A1, 30.06.1990 | |||
| EP, 349049 A3, 03.01.1990. | |||
Авторы
Даты
2001-04-20—Публикация
1995-09-29—Подача