Кальциевый обмен является одной из важнейших составляющих электролитно-водного баланса в организме. Узкие границы содержания кальция в сыворотке крови человека в норме (2,25 - 2,75 мМоль/л) свидетельствуют о том, что деятельность кальций регулирующих механизмов организма направлена на поддержание постоянства кальцемии. При различных видах патологии наблюдается как снижение концентрации кальция в сыворотке крови, так и гиперкальцемия. И то и другое состояние имеет большое диагностическое значение, особенно у пациентов со злокачественными опухолями [1, 3, 11].
Назначение и область применения:
Изобретение относится к области медицины, а именно к области лабораторной диагностики.
Уровень науки и техники:
Для фотометрического измерения концентрации кальция в растворах, сыворотке крови и других биологических жидкостях предложены различные реактивы: используются мурексид, глиоксаль-бис-оксианилид (ГБОА), ортокрезолфталеинкомплексон (о-КФК), метилтимоловый синий [2, 4, 11], реактивы группы арсеназо: Арсеназо-I, Нитразо C, Карбоназо и другие [8]. Из всех этих реактивов значительная часть по разным причинам не получила широкого распространения в силу каких-либо недостатков, часть реактивов, такие как мурексид, Нитразо C, карбоназо, используются в химическом анализе, но не используются в медицинской практике для измерения концентрации кальция в биологических жидкостях.
Практически для медицинских целей используются ГБОА, о-КФК, метилтимоловый синий. Они имеют также определенные недостатки. ГБОА, который использовался для обозначенных целей в прежние годы, неудобен тем, что должен применяться в виде свежего раствора в метаноле. Раствор не стойкий, требует постоянного обновления. Реактив также чувствителен к свету. Сохранность готового реактива не более 1 недели. Результаты измерения концентрации кальция с этим реактивом по причине его нестабильности весьма неудовлетворительны.
Реактив с метилтимоловым синим весьма сохранен, дает приемлемые результаты по стабильности, воспроизводимости, но имеет недостаточную избирательность, (сродство) к ионам кальция. В результате этот реактив дает несколько завышенные результаты концентрации кальция по сравнению с референсным методом измерения концентрации кальция в биологических жидкостях - ионизационно-плазменной фотометрией.
Реактив с о-КФК в настоящее время применяется наиболее широко в медицинской практике. Он имеет высокую избирательность к ионам кальция, обеспечивает высокую точность, хорошую коррекцию с референсным методом - ионизационно-плазменной фотометрией. Недостатком его является необходимость ежедневно готовить свежий раствор реагента (из компонентов), так как он может быть использован только в течение 3-4 ч.
Сущность изобретения:
Изобретательский уровень предлагаемого изобретения подтверждается тем, что нами предложен новый ранее не описанный состав реактива с комплексоном Арсеназо III и 8-оксихинолином. Арсеназо III - комплексон из группы арсеназо, синтезированный впервые в нашей стране В.Б. Саввиным и сотрудниками в 1959 году [6, 8, 9].
Задачей изобретения является разработка реактива для измерения концентрации кальция в сыворотке крови и других биологических жидкостях, удобного в использовании - однокомпонентного раствора стойкого при хранении (желательно при комнатной температуре), специфичного к иону кальция, сравнительно дешевого (из отечественных компонентов).
Указанная задача была реализована путем разработки реактива, в котором основными компонентами являются комплексообразующие соединения Арсеназо III, 8-оксихинолин и детергент Тритон-Х100.
Анализ известного уровня науки и техники показал новизну "Способа измерения концентрации кальция в сыворотке крови и других биологических жидкостях реактивом на основе комплексона Арсеназо III". Это подтверждает соответствие решения условию "изобретательский уровень" и "новизна".
Изобретательский уровень предлагаемого изобретения подтверждается тем, что нами предложен новый ранее не защищенный авторскими правами состав реактива с комплексоном Арсеназо III с 8-оксихинолином. Арсеназо III - металлокомплексон из группы диазокомплексообразователей. Всего таких реагентов известно более 100. Все они имеют разное сродство к различным ионам металлов. Арсеназо III не имеет определенной специфичности к одному иону и образует комплексы со многими ионами [5, 8]. Наибольшее сродство проявляется к ионам Th, UO
Интерференция с другими близкими ионами наблюдается при превышении концентрации натрия в 300 раз и более по сравнению с кальцием, калия и магния - примерно в 100 раз [8].
Рекомендуемый состав реактива:
Ацетатный буфер - 0,1 Моль/л, pH 4,75 (13,61 г натрия уксуснокислого, воды до 1000 мл, доводят уксусной кислотой до нужного значения pH);
Арсеназо III - 0,15 мМоль/л (116 мг/л);
8-оксихинолин - 2 мМоль/л (290 мг/л);
Детергент "Тритон Х100" - 0,04%.
Реактив представляет собой раствор темно-красного или вишневого цвета, с характерным запахом ацетатного буфера. При соединении с субстратом, содержащим ионы Ca2+, меняет окраску к синему цвету. Спектры поглощения исходного реактива и реактива в комплексе с кальцием приведены на фиг. 1.
Для калибровки измерения концентрации кальция необходим калибровочный раствор, который готовят по следующей методике:
навеску кальция углекислого (чистотой не ниже ЧДА), высушенного до постоянного веса - 250,22 мг/л, растворяют в 0,1 н. HCl, концентрация ионов Ca2+ в таком растворе 2,50 мМоль/л. Раствор хранится в плотно закрытой посуде неограниченно долго.
Реактив стабилен, постоянно готов к работе, чем выгодно отличается от реактива с о-КФК, ГБОА. Сохранность его не менее 6 мес при комнатной температуре, сохранность при 4-8oC не менее 1 года. Мы сохраняли готовый реактив и большее время - более двух лет, при этом свойства реактива несколько меняются, что требует периодической калибровки по калибровочному раствору, но он вполне пригоден для работы. Введение в состав реактива 8-оксихинолина предлагается нами впервые и, следовательно, является полностью приоритетной разработкой. Присутствие в растворе 8-оксихинолина улучшает метрологические характеристики реактива. При его наличии реактив имеет лучшую избирательность, линейность, воспроизводимость. Положительное влияние 8-оксихинолина в составе реактив можно пояснить тем, что этот реактив, являясь комплексообразователем (образует хелатные комплексы со многими ионами металлов, включая Mg, Fe, Al, Zn и другие), конкурентно связывается с ионами в растворе. Соединения 8-оксихинолина с ионами кальция в литературе не отмечено. Известно, что такие конкурентные взаимодействия повышают специфичность реакции и определения искомого иона, в данном случае кальция.
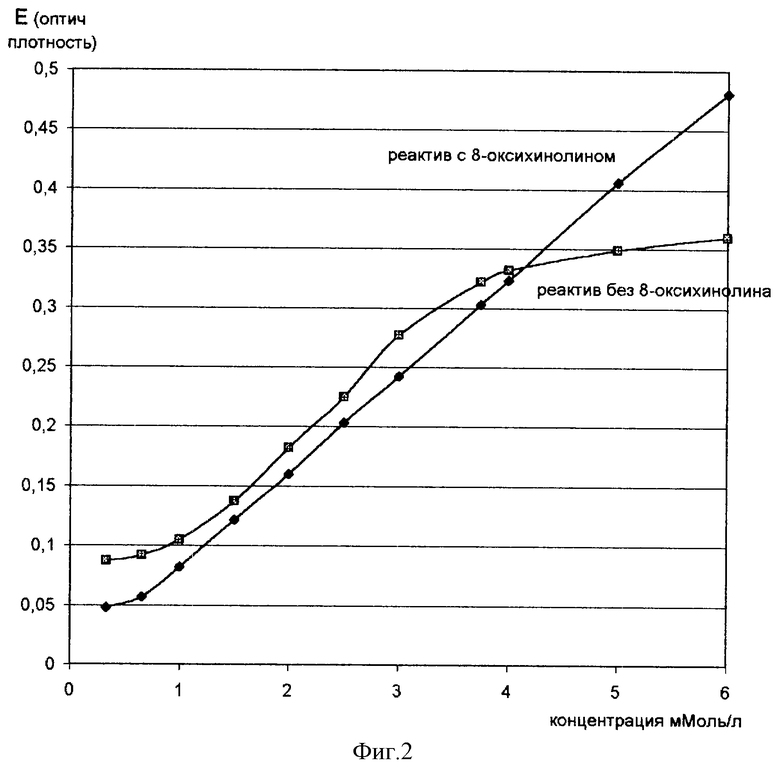
На фиг. 2 показаны типичные калибровочные графики определения кальция без и с 8-оксихинолином. Без 8-оксихинолина диапазон линейности 1,5 - 3,5 мМоль/л, с 8-оксихинолином диапазон линейности 1,0 - 5,0 мМоль/л. Также улучшается при наличии 8-оксихинолина в составе реактива стабильность измерения (разброс параллельных измерений одного образца). Это способствует уменьшению коэффициента вариации при измерениях.
Проведение измерения:
Оптимальное соотношение сыворотка: реакционная смесь 1:100. Например, 10 мкл сыворотки вносят в 1000 мкл реактива. Объемы могут быть изменены в соответствии с объемами кювет прибора. Параллельно измеряют калибровочный раствор Ca при таких же соотношениях калибровочного раствора и реактива.
Через 2 мин после смешивания замеряют оптическую плотность образцов против реактива в кюветах с длиной оптического пути 5 или 10 мм при длине волны 650 нм (620-670 нм). Оптическая плотность стабильна в течение длительного времени (несколько часов). Рассчитывать концентрацию следует по пропорции или по фактору, введенному в автоматические и полуавтоматические приборы.
Диапазон линейности: 1,0 - 5,0 мМоль/л.
Также может быть измерена концентрация кальция в плазме крови, но возможно использование только плазмы, взятой с гепарином в качестве антикоагулянта. Плазму, полученную с использованием цитрата или оксалата, использовать нельзя. Можно измерять концентрацию кальция в моче. Чаще требуется измерять концентрацию кальция в суточной моче для вычисления выведения кальция за сутки. Для этого собирают мочу в течение суток в одну посуду. Для предотвращения выпадения нерастворимых солей кальция в осадке мочу необходимо подкислить соляной кислотой (например, внести 10 мл 1 Моль/л раствора HCl на 1 л мочи). Концентрация кальция в моче может быть высокой и выходить за пределы линейности измерения. В этом случае необходимо мочу развести в 10 раз или больше 0,1 М раствором соляной кислоты. Концентрацию кальция вычисляют соответственно разведению.
Реактив очень удобен для автоматических приборов тем, что он однокомпонентный, длительно и постоянно готов к работе, может храниться в кюветах (картриджах) прибора при комнатной температуре.
Для лучшего понимания сущности заявленного изобретения, а также для подтверждения соответствия решения условию "промышленная применимость" проведены сравнительные испытания данного реагента с ближайшими аналогами и другие конкретные применения, которыми оно исчерпаться не может.
Так, при измерении в реальных условиях отделения лабораторной диагностики института одного и того же образца сыворотки крови изо дня в день (внутренний контроль качества) в течение 128 рабочих дней (за 6 месяцев) коэффициент вариации составил с реактивом на основе Арсеназо III - 5,75%, с реактивом на основе о-КФК - 6,8% (измерение проводилось на анализаторе FP-901M, Labsystems, Финляндия). Для сравнения при проведении аналогичных измерений с реактивом ГБОА коэффициент вариации составил 10,5% за 46 дней.
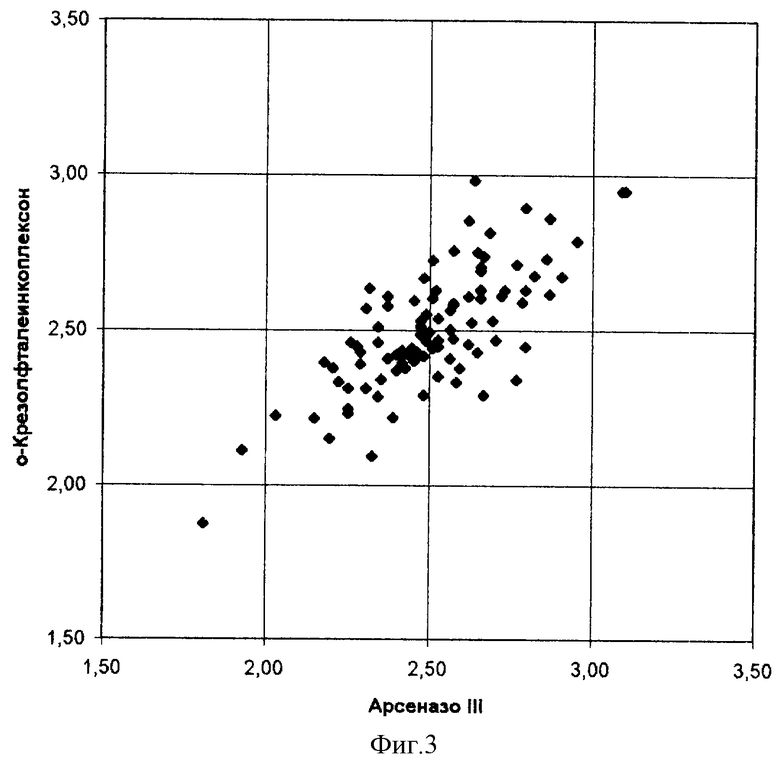
Мы провели также измерение концентраций кальция в сыворотке крови у больных клиники института двумя методами параллельно с реактивами о-КФК и Арсеназо III. Результаты представлены в таблице 1 и на графике (фиг. 3). Коэффициент корреляции составил 0,74. Проведение калибровки ежедневно не требуется. С реактивом о-КФК требуется ежедневное измерение калибратора, так как оптические плотности зависят в большей степени от внешних факторов - температуры, времени после приготовления реактива или его смешивания из двух компонентов, как это организовано во многих коммерческих наборах. Это же относится и к ГБОА реактиву.
Нами была предпринята попытка оценки нормальных (референсных) значений концентрации кальция в сыворотке крови, измеренных реактивом с Арсеназо III. На основании измерения концентрации кальция в 760 образцах сывороток сборной группы здоровых людей были вычислены значения референсных величин 2,15 - 2,75 мМоль/л для нашего реактива и использованной группы пациентов. Диаграмма распределения концентраций кальция, получения нами, представлена на фиг. 3. Мы использовали для расчета метод процентильной оценки. Для повышения достоверности использовали диапазон 5-95% после элиминации всех измерений, не укладывающихся в диапазоне М±2S [7, 16]. Среднее значение концентрации кальция в сыворотке - 2,47 мМоль/л, полученное в этом опыте, хорошо совпадает с цифрами, полученными в другом исследовании для жителей Дании, где методами атомно-абсорбционной фотометрии и о-КФК методом для 1213 получили среднее значение 2,40 мМоль/л [15].
Приведем также конкретные примеры актуальности измерения концентрация кальция из клинической практики.
Женщина 54 лет была пролечена по поводу опухоли щитовидной железы. В процессе лечения ей была проведена операция удаления опухоли с участками здоровой ткани щитовидной железы. При этом были удалены обе доли паращитовидной железы. Через некоторое время после операции у пациентки начались выраженные нарушения регуляции обмена кальция. Измерения концентрации кальция сыворотки крови показывали резкое снижение его уровня. Концентрация кальция снижалась и составляла 2,10, 2,05, 1,98, 1,65, 1,55 мМоль/л. Такие концентрации кальция в крови опасны для жизни. Потребовалось корректирующее гормональное лечение. После назначения гормонотерапии концентрация кальция в сыворотке крови начала возрастать до значений 1,95, 2,05, 2,20 мМоль/л.
Гиперкальцемия характерна для многих локализаций опухолей, в частности для лимфом и лейкозов. Так, у ребенка 10 лет с диагнозом неходжкинская лимфома неоднократно при измерениях в сыворотке обнаруживались высокие концентрации уровня кальция - 2,90 - 3,60 мМоль/л. Высокие концентрации кальция в крови также представляют опасность для жизни. После успешного лечения основного заболевания с применением химиотерапии, концентрации кальция в крови начали снижаться. Последующие измерения концентрации кальция при повторных поступлениях пациента для повторных курсов химиотерапии (в течение 9 мес) показали последовательно следующие значения - 2,86, 3,05, 2,68, 2,47, 2,44 мМоль/л, то есть концентрация кальция стала соответствовать нормальной.
Литература
1. Авдонин П.В., Ткачук В.А. // Рецепторы и внутриклеточный кальций. - М., Наука, 1994, 288 с.
2. Вишневская Т. М. , Ляшевская Т.И. // Лаб. дело. - 1976. - N 7. - С. 144.
3. Мерзон А.К., Коломиец В.В., Мерзон К.А., Дидина С.Е. // Лаб. дело. - 1985. - N 5. - С. 264-269.
4. Михайлова С. П. , Смирнова Г.А. // Лаб. дело. - 1978. - N 10. - С. 613-617.
5. Новикова К. Ф., Басаргин Н.Н., Цыганова М.Д. // Ж. аналит. химии. - 1961. т. 16. С. 348.
6. Петрова Т.В., Хакимходжаев Н., Саввин С.Б. // Известия АН СССР, Сер. химич. - 1970. N 2. - С. 259 - 265.
7. Общая теория статистики. / Ред. А.Я. Боярский, Г.Л. Громыко. - М., Изд. московского университета, 1985, 375 с.
8. Саввин С.Б. // Органические реактивы группы Арсеназо III. - М., Атомиздат. 1971, 562 с.
9. Саввин С.Б., Кузин Э.Л. // Электронные спектры и структура органических реагентов. - М., Наука, 1974, 277 с.
10. Словак З., Семенкова Л. // Лаб. дело. - 1974. - N 1. - С. 19-22.
11. Титов В.Н. // Клин. лаб. диагностика. - 1996. - N 2. - С. 23-26.
12. Айткен Дж. М. (Aitken J.M.) / в кн. Нарушения обмена кальция. Ред. Д.А. Хит, С. Дж. Маркс./ М., Медицина - 1985. - С. 65-90.
13. Bauer P.J. // Anal. Biochem. - 1981. - V. 110. - P. 61-72.
14. Reed A.H., Henry R.J., Mason W.B. // Clin. Chem. - 1971. - V. 17. - P. 275.
15. Thode J., Juul-Jorgensen B., Bhatia H.M. et all. // Scand. J. Clin. Invest. - 1989. - V. 49 - P. 217-223.
16. Young D.C., Pestaner L.E., Gibberman V. // Clin. Chem. - 1975. - V. 21. - N 5.
Изобретение относится к медицине, в частности к лабораторной диагностике. Способ обеспечивает повышение специфичности определения концентрации кальция в биологических жидкостях. Исследование проводят путем фотометрического измерения биологической жидкости в присутствии реактива, при этом в качестве реактива используют водный раствор состава: ацетатный буфер, рН 4,75 - 0,1 моль/л, комплексон Арсеназо III - 0,15 мМоль/л, 8-оксихинолин - 2,0 мМоль/л, детергент Тритон-Х100 - 0,04%, и этот раствор смешивают с сывороткой крови или другой биологической жидкостью в соотношении 100 : 1. 3 ил.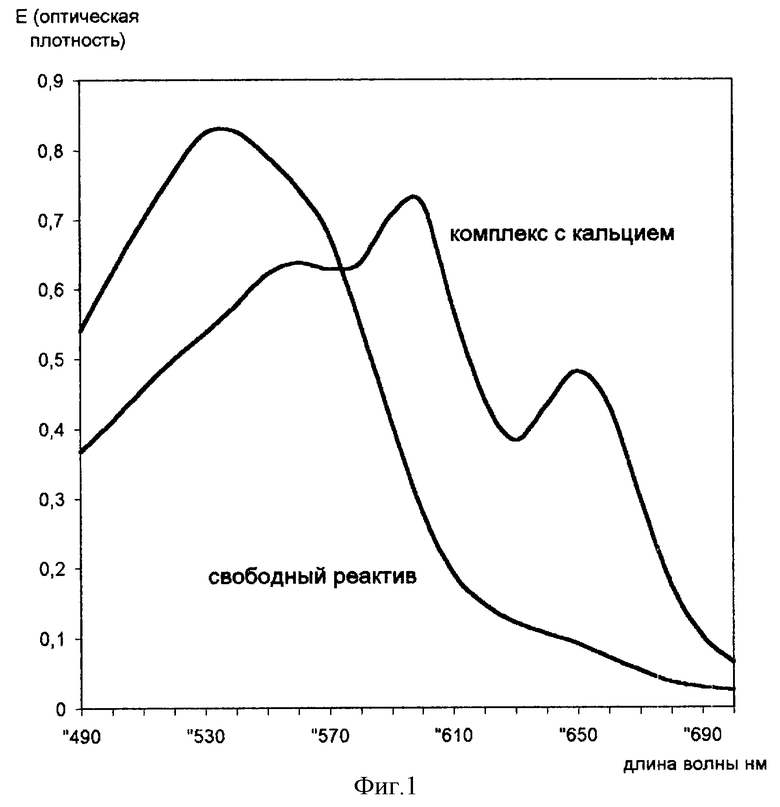
Способ определения концентрации кальция в сыворотке крови и других биологических жидкостях путем фотометрического измерения в присутствии реактива, отличающийся тем, что в качестве реактива используют водный раствор состава: ацетатный буфер, рН 4,75 0,1 моль/л, комплексон Арсеназо III 0,15 мМоль/л, 8-оксихинолин 2,0 мМоль/л, детергент Тритон-Х100 0,04% и этот раствор смешивают с сывороткой крови или другой биологической жидкостью в соотношении 100:1.
| САВВИН С.Б | |||
| Органические реактивы группы Арсеназо III | |||
| - М.: Атомиздат, 1971, с.562 | |||
| RU 94007098 А1, 27.10.1995 | |||
| УСТРОЙСТВО для ОПРЕДЕЛЕНИЯ КОЭФФИЦИЕНТА | 0 |
|
SU335136A1 |
| US 4382122 A, 03.05.1983. | |||
Авторы
Даты
2001-08-20—Публикация
2000-06-16—Подача