Изобретение относится к области медицины и может быть использовано для лечения гипогликемии, в частности гипогликемических состояний, вызванных повышенным содержанием в крови инсулина эндогенного или экзогенного происхождения.
Кроме того, изобретение может быть использовано в экспериментальной медицине или биологии в опытах in vivo или in vitro для блокады клеточных рецепторов инсулина без получения инсулиноподобного эффекта, а также в других случаях, где может быть необходим контринсулярный эффект.
В настоящее время во всем мире отмечается рост психоэмоционального напряжения, стресса. Среди стрессорно обусловленной патологии важное место занимают гипогликемические состояния, которые вызываются снижением уровня глюкозы в крови (ниже 50 - 70 мг %) и имеют различную этиологию. Различают:
1) гипогликемии, вызванные функциональной недостаточностью коры надпочечников (астеническое состояние), при которой скорость глюконеогенеза - образования глюкозы из неуглеводных продуктов (глюкогенных аминокислот) - существенно снижается;
2) гипогликемии печеночного типа, связанные с недостаточностью функции печени;
3) гипогликемии, вызванные усилением выделения глюкозы из организма (нарушением резорбции глюкозы в почках);
4) гипогликемии, вызванные усиленным распадом глюкозы в тканях (опухоли островков Лангерганса, гиперплазия и гипертрофия островков Лангерганса, преходящий гиперинсулинизм и др.) (Большая медицинская энциклопедия. - 1977. - Т.6. - С.198);
5) гипогликемии, возникающие в результате передозирования инсулина, вводимого с терапевтической целью, например, при диабете или при лечении психических заболеваний.
Непосредственной причиной гипогликемии является стимулируемое инсулином ускорение транспорта глюкозы из крови в ткани, тормозящее влияние инсулина на процессы глюконеогенеза и глюкозообразование в печени и почках с последующим замедлением поступления глюкозы из этих органов в кровяное русло, а при гипогликемии почечного происхождения - ускорением выделения глюкозы из крови в мочу (Большая медицинская энциклопедия. - 1977. - Т.5. - С.482 - 483).
Вышеперечисленные пять видов гипогликемии могут быть условно объединены в две группы:
I. Гипогликемии, вызванные недостаточным поступлением глюкозы в кровь или ускоренным выведением ее из организма (1 - 3).
II. Гипогликемии, вызванные усиленным транспортом глюкозы из крови в клетку из-за высокого содержания в крови инсулина экзогенного или эндогенного происхождения (4 - 5).
Существует ряд средств и методов для лечения гипогликемических состояний. Коррекция гипогликемии в острой форме может быть проведена с помощью внутримышечного или подкожного введения глюкагона (Машковский М.Д. - 1993. - Ч. 1. - С.652) либо глюкагона и амилина (пат. 5234906 США). При алиментарной гипогликемии, а также при болезни Гирке показан адреналин (1 мл 0,1%-ного раствоpa), который быстро мобилизует гликоген печени, обеспечивая поступление глюкозы в кровь (Большая медицинская энциклопедия. -1977. -Т.5. - С. 482-483). Во многих случаях при гипогликемических состояниях больным вводят глюкозу (Там же; машковский М.Д. Лекарственные средства. - 1993. - Ч.2. - С. 219).
Вышеприведенные способы коррекции гипогликемических состояний оказывают временное действие и не направлены на купирование гормонального эффекта инсулина. Применение их может быть эффективным в случаях 1 - 3. В случаях же 4 - 5, связанных с выраженным проявлением гормонального эффекта инсулина, они недостаточно эффективны. В этих случаях предпочтительнее было бы использовать предлагаемые в настоящей заявке пептиды с контринсулярным действием. Они могут быть применены как самостоятельно, так и в сочетании с вышеуказанными средствами. Например, при коррекции гипогликемического состояния путем введения глюкозы очень трудно подобрать адекватную дозу глюкозы, если у больного имеет место высокая чувствительность тканей к инсулину. Введенная глюкоза быстро переходит из крови в клетки под влиянием инсулина и опять наступает гипогликемическое состояние. Введение же глюкозы совместно с предлагаемыми контринсулярными пептидами способно было бы решить данную проблему.
В случае 4 при развитии гипогликемии на фоне опухолевого процесса введение одной глюкозы нецелесообразно, т.к. оно стимулирует рост опухоли. Здесь также более благоприятный эффект может быть получен при введении глюкозы совместно с контринсулярными пептидами, являющимися предметом данной заявки. Контринсулярные пептиды в данном случае будут оказывать цитостатический эффект.
Патентный поиск был проведен по рубрикам МКИ5 А 61 К 37/26 и С 07 К 7/40 - 7/42, а также по рубрикам МПК6 А 61 К 38/28 и С 07 К 14/62.
Анализ патентных документов, выявленных в данных рубриках, показал, что найденные патентные документы относятся к решению следующих задач:
- производство и очистка инсулина;
- получение аналогов и производных инсулина;
- разработка форм и способов введения инсулина в организм;
- инсулинотерапия (лечение сахарного диабета, психических заболеваний и проч.).
Было обнаружено несколько патентных документов, где описываются пептиды - фрагменты инсулина (а.с. 1149603 СССР, заявка 89825-91 Австралии, патент 915933 Финляндии). Однако во всех этих случаях решается задача создания пептидов с гипогликемической, т.е. инсулиноподобной активностью.
Обнаружены также патентные документы, где речь идет
- о гипергликемических препаратах (патент 5234906 США),
- о способе и препарате для лечения сахарного диабета и гипогликемии (патент 5321008 США).
В первом случае используется глюкагон с амилином, а во втором - инсулин с кальцитонином.
В изученной литературе отсутствуют сведения о создании пептидов - фрагментов инсулина, которые бы предлагались для коррекции гипогликемических состояний.
Сущность изобретения
Сущность предлагаемого изобретения состоит в том, что для коррекции гипогликемического состояния предлагаются синтезированные пептиды инсулина человека, содержащие часть аминокислотных остатков, входящих в сайт связывания инсулина с клеточным рецептором, причем при отсутствии инсулиноподобного действия синтезированные пептиды проявляют себя как активные конкуренты инсулина за клеточный рецептор, вследствие чего препятствуют транспорту глюкозы из крови в клетки и тормозят развитие гипогликемии. Данный механизм не используется ни в одном из существующих средств коррекции гипогликемического состояния.
Структура синтетических пептидов
1. С-концевой пептид "10" А-цепи инсулина:
S--L--Y--Q--L--E--N--Y--C-N
12 13 14 15 16 17 18 19 20 21
2. С-концевой пептид "14" В-цепи инсулина:
L--V--С--G--E--R--G--F--F--Y--Т--Р--К-Т
17 18 19 20 21 22 23 24 25 26 27 28 29 30
3. С-концевой пептид "16" В-цепи инсулина:
L--Y--L--V--C--G--E--R--G--F--F--Y--T--P--K-T
15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30
4. С-концевой пептид "23" В-цепи инсулина:
G--S--H--L--V--E--A--L--Y--L--V--C--G--E--R--G--F--F--Y-
8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26
Т--Р--К-Т
27 28 29 30
5. Димер, содержащий С-концевые пептиды А- и В-цепей инсулина: NYCN - С-концевой пептид из А-цепи (А 18 - А 21)
где S - серии, L - лейцин, Y - тирозин, Q - глутамин, Е -глутаминовая кислота, N - аспарагин, С - цистеин, V - валин, R -аргинин, F - фенилаланин, Т - треонин, Р - пролин, К - лизин, G - глицин, Н - гистидин, А - аланин.
Инсулин - небольшой глобулярный белок с известной первичной и третичной структурой, состоящий из двух пептидных цепей. А-цепь инсулина содержит 21 аминокислотный остаток, В-цепь - 30 аминокислотных остатков. Сайт связывания инсулина с рецептором, согласно литературным данным, представляет собой два сближенных в пространстве участка поверхности молекулы инсулина. Первый участок включает остатки В-цепи: Val-12, Tyr-16, Gly-23, Phe-24, Phe-25 и Туr-26. Второй участок включает аминокислоты А-цепи: Gly-1, Glu-4, Gln-5 и Asn-21. Показано, что мутантный инсулин с заменой Туr-В16 на His сохраняет лишь 43% активности нативного человеческого инсулина, а замена остатка Phe-B24 на серин приводит к полной утрате эффекта связывания.
Отсюда видно, что связывание инсулина с рецептором - сложный и тонкий процесс. Поэтому было неочевидно, будут ли садиться на рецептор и конкурировать с инсулином синтезированные пептиды, содержащие часть аминокислотных остатков, входящих в сайт связывания с рецептором, т.е. будут ли синтезированные пептиды проявлять контринсулярную активность.
Проведенные эксперименты показали, что предлагаемые пептиды действительно тормозят транспорт глюкозы из крови в клетки, проявляя себя как контринсулярные пептиды.
Предлагаемое изобретение соответствует, таким образом, критерию "изобретательский уровень".
Сведения, подтверждающие возможность осуществления изобретения
Пептиды синтезировали твердофазным методом. В работе применяли L-аминокислоты с шелочелабильной 2-(4-нитрофенилсульфонил)этоксикарбонильной (NSC) Nа-защитной группой. В качестве защиты боковых функций аминокислот использовали: для Glu, Туr, Thr - трет-бутиловые эфиры; для Arg - мезитиленсульфонильную группу; для Cys - тритильную; для Lys - трет-бутилоксикарбонильную; для Asn - ксантинильную защитную группу. Сборку пептидных цепей осуществляли в ручном синтезаторе на смоле Ванга (0,8 ммоль/г ОН-групп), используя в качестве конденсирующего агента ВОР - реагент Кастро по синтетическому протоколу, описанному ранее (Samukov V.V. et al.//Tetrahedron Lett. 1994. V.35. P. 7821-7824). Деблокирование и отщепление пептидов от полимера проводили по методу Тамма (Tam J.P.//Org. Chem. 1985. V.50. Р.5291-5298).
Очистку пептидов осуществляли полупрепаративной обращенно-фазовой ВЭЖХ с использованием хроматографа Pharmacia-LKB 2249 (Швеция) на колонке (10 х 250 мм), заполненной сорбентом LiChrosorb 100RP - 18 (10 мкм; Merck), в градиенте концентрации ацетонитрила (0-50%) в 0,1%-ной трифторуксусной кислоте за 60 мин при скорости потока 4 мл/мин. Объем фракции 4 мл. Фракции, содержащие пептиды с чистотой выше 90% по данным аналитической ВЭЖХ, объединяли, растворитель удаляли при пониженном давлении на ротационном испарителе при температуре бани 30oС. Остаток растворяли в ледяной уксусной кислоте, фильтровали через стеклянный фильтр, лиофилизировали. На полупрепаративную колонку наносили до 200 мг неочищенных пептидов. Аналитическую ВЭЖХ проводили на колонке (4,6 х 150 мм) с сорбентом Nucleosil 100 RP-18 (5 мкм). Детекцию осуществляли спектрофотометрически по поглощению при 226 нм. Аминокислотный состав пептидов определяли после гидролиза в 6 н. HCL (110oС, 24 ч; в запаянных ампулах) на аминокислотном анализаторе Biotronik LC 5001(ФРГ).
Получение димера. 10 мг лиофилизированного пептида NYCN со свободной сульфгидрильной группой растворяли в 5 мл дегазированной 50%-ной уксусной кислоты, добавляли 15 мг 2,2'-дипиридилдисульфида (Merck) и 3 ч перемешивали реакционную смесь без доступа воздуха. Ход реакции контролировали с помощью ВЭЖХ. Затем реакционную смесь наносили на колонку и NYC(Ps)N выделяли полупрепаративной обращенно-фазовой ВЭЖХ в хроматографических условиях, описанных выше. Выход лиофилизированного продукта 90%.
По 10 мг пептидов NYC(Ps)N и LVCGERGFFYTPKT растворяли в атмосфере аргона в 5 мл дегазированной 50%-ной уксусной кислоты. В ходе реакции, по данным ВЭЖХ, появлялся новый пик. После полного исчезновения исходного тетрадекапептида (5 ч) октадекапептид с дисульфидным мостиком выделяли из реакционной смеси с помощью ВЭЖХ. Фракции, содержащие целевой пептид с чистотой выше 95%, объединяли, удаляли растворитель при пониженном давлении, остаток растворяли в дегазированной воде, фильтровали и лиофилизировали. Выход лиофилизированного материала в расчете на тетрадекапептид 60%.
Все полученные в результате синтеза пептиды имели корректный аминокислотный состав.
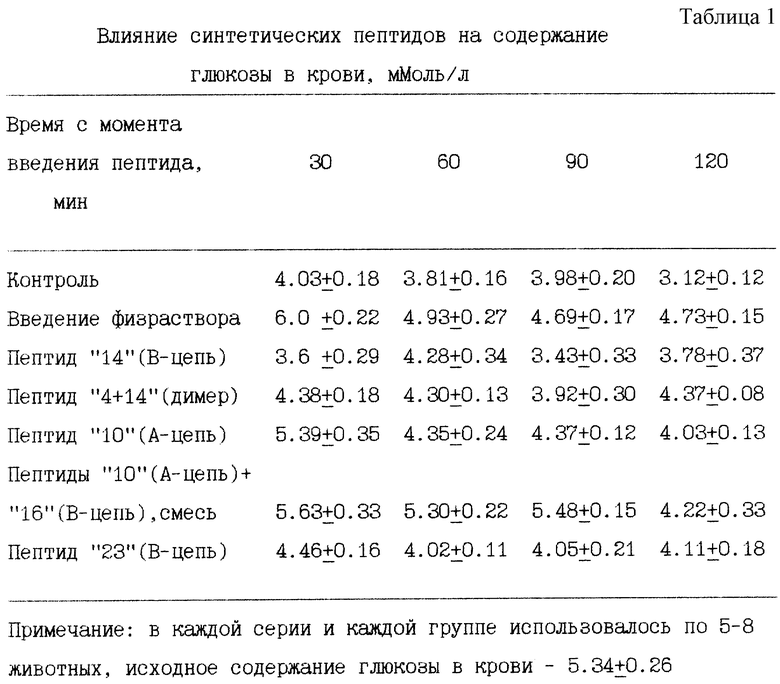
Синтезированные пептиды вводили мышам (гибриды СВА х С57 Black) внутрибрюшинно в эквимолярных количествах. Мышей забивали декапитацией через 30, 60, 90 и 120 мин после введения препаратов. Содержание сахара в крови определяли глюкозоксидазным методом с помощью набора реактивов "Новоглюк" производства "Вектор-Бест" (Новосибирск).
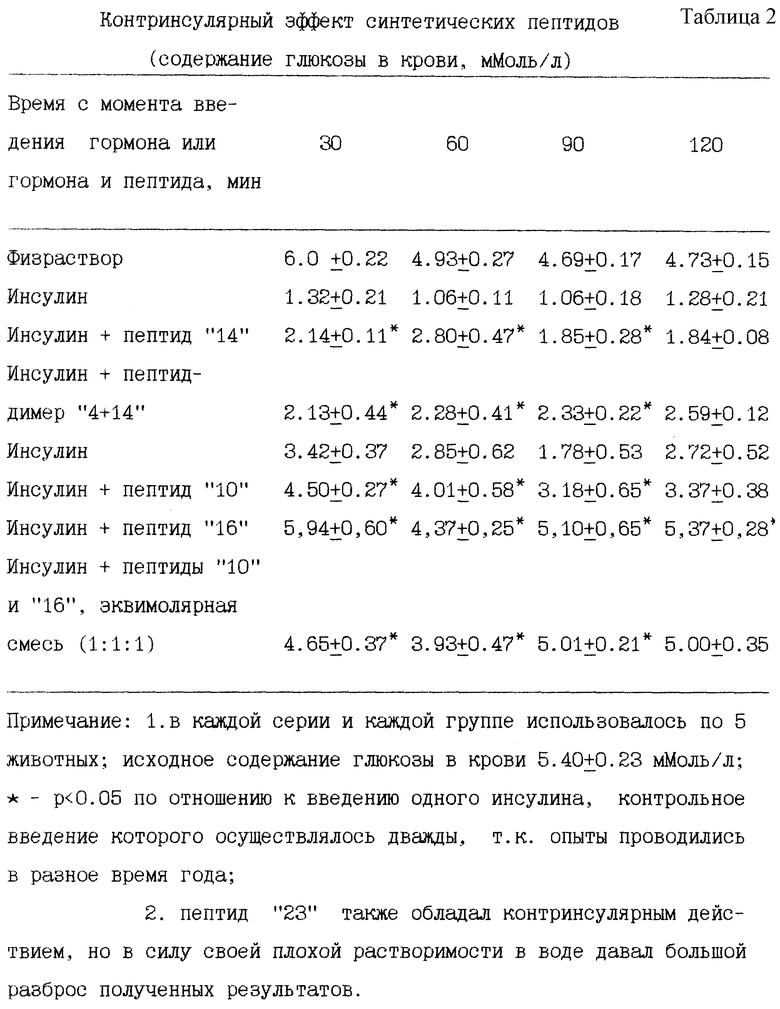
Полученные результаты представлены в табл.1 и 2. Из представленных данных видно, что все синтезированные нами пептиды не обладали гормональным (проинсулярным) эффектом (табл.1), но все обладали контринсулярным действием, задерживая поглощение глюкозы из крови под влиянием гормона (табл.2).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДНЫЙ ФРАГМЕНТ, ОБЛАДАЮЩИЙ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ ИНСУЛИНА | 1995 |
|
RU2078769C1 |
| АНАЛОГ-АГОНИСТ АМИЛИНА, ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ СВОЙСТВА АГОНИСТА АМИЛИНА | 1992 |
|
RU2130463C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2670106C2 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА, СОДЕРЖАЩАЯ КОНЪЮГАТ ИНСУЛИНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ И КОНЪЮГАТ ИНСУЛИНОТРОПНОГО ПЕПТИДА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ | 2012 |
|
RU2606840C2 |
| АНАЛОГИ ГЛЮКАГОНА, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ И СТАБИЛЬНОСТЬЮ В БУФЕРАХ С ФИЗИОЛОГИЧЕСКИМИ ЗНАЧЕНИЯМИ Ph | 2009 |
|
RU2560254C2 |
| ОКСИНТОМОДУЛИН ЧЕЛОВЕКА, ЕГО ПРИМЕНЕНИЕ, ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ЕГО ОСНОВЕ И СПОСОБ ПРИМЕНЕНИЯ ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГИПЕРГЛИКЕМИИ | 2009 |
|
RU2524204C2 |
| НОВЫЙ ВАРИАНТ ЭКСЕНДИНА И ЕГО КОНЪЮГАТ | 2010 |
|
RU2528734C2 |
| АНАЛОГИ ИНСУЛИНА С АЦИЛЬНОЙ И АЛКИЛЕНГЛИКОЛЕВОЙ ГРУППИРОВКОЙ | 2008 |
|
RU2514430C2 |
| ТЕТРАДЕКАПЕПТИДЫ, УЛУЧШАЮЩИЕ ВОССТАНОВИТЕЛЬНУЮ ФУНКЦИЮ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ПРИ ИШЕМИИ | 2017 |
|
RU2648846C1 |
| ИНГИБИТОР ДИПЕПТИДИЛПЕПТИДАЗЫ-4 ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА 2-ГО ТИПА | 2015 |
|
RU2628573C2 |
Изобретение относится к области медицины и может быть использовано для лечения гипогликемий, в частности гипогликемических состояний, вызванных повышенным содержанием в крови инсулина эндогенного или экзогенного происхождения. Для коррекции гипогликемического состояния предлагаются синтезированные пептиды инсулина человека, содержащие аминокислотные остатки, входящие в сайт связывания инсулина с клеточным рецептором, выбранные из группы: С - концевой пептид А-цепи инсулина (А12-А21), С - концевые пептиды В-цепи инсулина человека, содержащие 14-23 аминокислотных остатков, димер, содержащий С-концевой пептид А-цепи (А18-А21) и С-концевой пептид В-цепи (В17-В30), соединенные дисульфидным мостиком, а также их смеси. Предложенное средство оказывает более длительное действие. 2 табл.
Средство, обладающее контринсулярным действием, отличающееся тем, что оно представляет собой пептид, выбранный из группы: С - концевой пептид А-цепи инсулина, включающий 10 аминокислотных остатков (А12 - А21), С - концевые пептиды В-цепи инсулина, включающие 14-23 аминокислотных остатков, димер, содержащий соединенные дисульфидным мостиком С-концевой тетрапептид А-цепи (А18 - А21) и С-концевой тетрадекапептид В-цепи инсулина (В17 - В30), или их смеси.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ВСЕСОЮЗНАЯ [OATIihTHO-T[KH'r!EOH^J;| | 0 |
|
SU286147A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 4372884 A, 08.02.1983 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Панин Л.Е | |||
| и др | |||
| К механизму контринсулярного эффекта апопротеина В | |||
| Вопросы медицинской химии | |||
| - М., 1995, № 6, с | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| BAGRIACIK N | |||
| Диагностика и лечение гипогликемии | |||
| Диабетография | |||
| - М., 1995, № 4, с | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2002-05-20—Публикация
1998-05-13—Подача