Область, к которой относится изобретение
Изобретение относится к медицине, а именно к веществам, являющимся ингибиторами дипептидилпептидазы-4 из группы N-ацильных производных аминоацил-2-цианопирролидина для лечения сахарного диабета.
Уровень техники
По данным ВОЗ сахарный диабет (СД) 2-го типа выявлен приблизительно у 90% всех больных диабетом в мире. Во всем мире значительно увеличилось количество ранее редких случаев заболевания детей диабетом 2-го типа. В некоторых странах на него приходится почти половина новых диагностируемых случаев среди детей и подростков. По прогнозам ВОЗ в 2030 году диабет станет седьмой по значимости причиной смерти.
Сахарный диабет является одной из серьезнейших медико-социальных проблем в связи с высокой распространенностью, стремительным ростом заболеваемости, высокой частотой инвалидизации и сохраняющейся высокой летальностью из-за развития осложнений этого заболевания. В настоящее время на фармацевтическом рынке имеется ряд препаратов для коррекции состояния лиц, страдающих СД 2-го типа. Вместе с тем, прием большинства препаратов сопровождается серьезными побочными эффектами в виде гипогликемии, лактатацидоза, гепатотоксичности, тошноты, диареи и др., что существенно ухудшает качество жизни пациентов. В связи с этим особую актуальность приобретает разработка новых, более эффективных, патогенетически обоснованных подходов к терапии данного заболевания.
Одним из звеньев патогенеза СД 2-го типа является нарушение функции инкретинов - гормонов желудочно-кишечного тракта, вырабатываемых в ответ на прием пищи и вызывающих стимуляцию секреции инсулина (инкретин - от англ. INCRETIN - Intestine seCRETion of INsulin). В организме человека известны два основных инкретина: глюкозозависимый инсулинотропный полипептид (ГИП), также известный как гастроингибиторный пептид (ГИП1) или желудочный ингибиторный пептид (ЖИП), вырабатываемый К-клетками двенадцатиперстной и тощей кишки, а также глюкагонподобный пептид-1 (ГПП-1), секретируемый энтероэндокринными L-клетками. То есть оба гормона вырабатываются эндокринными клетками, расположенными в эпителии тонкой кишки, а их высвобождение регулируется аналогичным образом с другими гормонами желудочно-кишечного тракта. Увеличение концентрации вещества в просвете желудочно-кишечного тракта (в данном случае глюкозы) действует как триггер для секреции гормона.
Инкретины ГПП-1 и ГИП являются пептидными гормонами, которые выделяются из К- и L-клеток в тонком кишечнике после еды. Среди других действий, оба инкретина стимулируют глюкозозависимое высвобождение инсулина из панкреатических β-клеток, а ГПП-1 подавляет высвобождение глюкагона из панкреатических α-клеток. Действие обоих инкретинов имеет комбинированный эффект на гипергликемию, увеличивая поглощение глюкозы тканями и уменьшая высвобождение глюкозы из печени. ГПП-1 также влияет на гомеостаз глюкозы, задерживая опорожнение желудка. Дипептидилпептидаза-4 (ДПП-4) быстро расщепляет и инактивирует оба инкретина, обеспечивая период полураспада продолжительностью 1-2 минуты. У пациентов с СД 2-го типа действие ГИП в поджелудочной железе ослаблено, а продукция ГПП-1 после еды снижена.
Гормоны семейства инкретинов секретируются в кишечнике в течение суток, их уровень повышается в ответ на прием пищи. Появление глюкозы в тонком кишечнике стимулирует высвобождение инкретинов, функция которых осуществляется посредством их попадания в клетки-мишени - панкреатические α- и β-клетки. Стимуляция инкретинами β-клеток, например, приводит к увеличению ими секреции инсулина в ответ на сохраняющееся количество глюкозы в крови. К благоприятным эффектам инкретинов относится улучшение функции β-клеток, включая глюкозозависимую секрецию инсулина (ГИП и ГПП-1), подавление выработки глюкагона α-клетками (ГПП-1), а также ряд внепанкреатических свойств, таких как замедление опорожнения желудка и подавление аппетита (ГПП-1), увеличение потребления глюкозы тканями организма (ГИП), снижение высвобождения глюкозы из печени (ГПП-1).
У пациентов с сахарным диабетом 2-го типа эффект инкретина значительно снижен по сравнению со здоровыми людьми. У таких пациентов после перорального введения глюкозы инсулиновый ответ как отсрочен во времени, так и снижен. Кроме того, у больных СД 2-го типа нарушено не только количественное содержание инкретинов (ГПП-1), но и механизм их действия (ГИП).
Создание препаратов, влияющих на уровень инкретинов, дает возможность улучшить гликемический контроль путем воздействия на иные, в отличие от других групп антидиабетических препаратов, патогенетические звенья данного заболевания.
Известны ингибиторы дипептидилпептидазы-4, патенты РФ №2180901, №2251544 «n-замещенные 2-цианопирролидины», заявка US 20130204012.
Известен патент РФ №2286986 «Ингибиторы дипептидилпептидазы-4 на основе конденсированных циклопропилпирролидинов и способ их применения».

Известен патент РФ на изобретение №2443687, «Новые ингибиторы дипептидилпептидазы IV, способы их получения и содержащие их фармацевтические композиции».
Известен патент РФ 2483716.
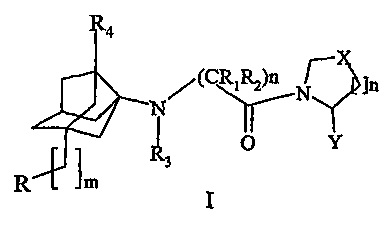
Изобретение относится к медицине и фармацевтической промышленности и касается фармацевтического состава, включающего ингибитор дипептидилпептидазы-4, предпочтительно вилдаглиптин от 1,5 до 20% и метформин от 80 до 98,5%. При этом активные ингредиенты составляют от 60 до 98% композиции. В качестве связующего вещества используются целлюлоза или ее производные в количестве от 1 до 20%.
Синтезировано новое амино-производное пирролидина в качестве ингибитора дипептидилпептидазы-4:
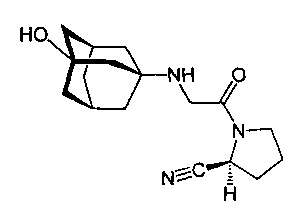
Известно изобретение по заявке US №20130023671 А1, в котором заявлен способ производства саксаглиптина - ингибитора дипептидилпептидазы-4, являющегося производным пирролидина.
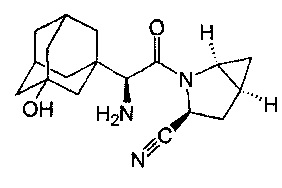
Саксаглиптин-селективный обратимый конкурентный ингибитор дипептидилпептидазы-4 (ДПП-4).
У пациентов с сахарным диабетом 2 типа прием саксаглиптина приводит к подавлению активности фермента ДПП-4 в течение 24 часов.
После приема внутрь ингибирование ДПП-4 приводит к 2-3-кратному увеличению концентрации глюкагоноподобного пептида-1 (ГПП-1) и глюкозозависимого инсулинотропного пептида (ГИП), уменьшению концентрации глюкагона и усилению глюкозозависимой ответной реакции бета-клеток, что приводит к повышению концентрации инсулина и С-пептида и, соответственно, к снижению гликемии натощак и постпрандиальной гликемии.
В качестве ингибиторов дипептидилпептидазы-4 на Российском рынке представлены: ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин - аминопроизводные пирролидина, обладающие несколько отличающимися свойствами.
На сегодняшний день есть необходимость в создании новых ингибиторов дипептидилпептидазы-4 для расширения линейки известных ингибиторов дипептидилпептидазы-4 с целью удовлетворения потребности в данном препарате.
Задачей заявляемого изобретения является создание ингибитора дипептидилпептидазы-4, обладающего активностью для снижения уровня гликемии у пациентов, больных сахарным диабетом 2-го типа, и являющегося стабильным.
Задача решена за счет того, что синтезирован ингибитор дипептидилпептидазы-4 из группы N-ацильных производных аминоацил-2-цианопирролидина, представляющий вещество:
(R/S)-3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-он (с молекулярной массой Mr = 380) в виде гидрохлорида (в пересчете на солевую форму Mr = 380+36.5 (HCl) = 416.5), соответствующее структурной формуле:
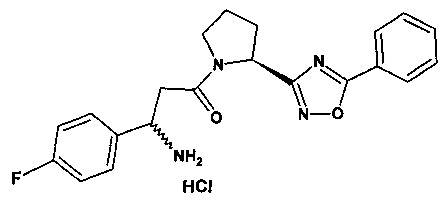
для лечения сахарного диабета 2-го типа.
Перечень чертежей
На фиг. 1 - результаты высокоэффективной жидкостной хроматографии полученного вещества (ВЭЖХ).
На фиг. 2 приведен анализ пика вещества, выявленного при ВЭЖХ.
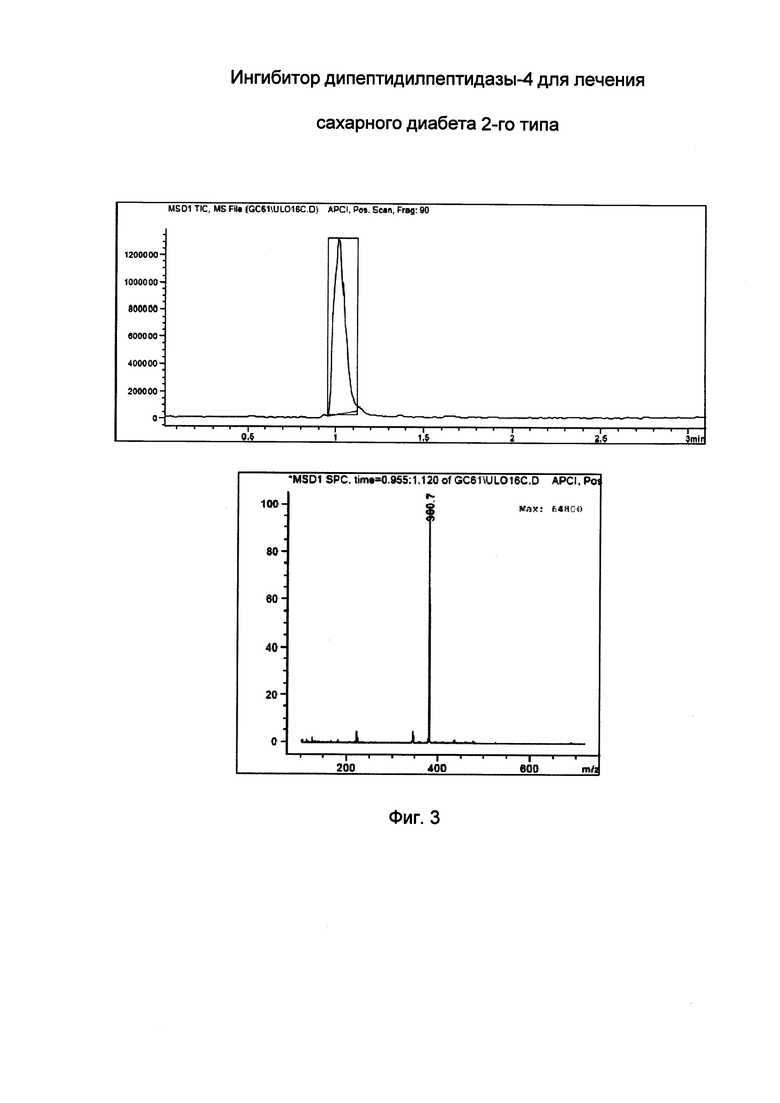
На фиг. 3 приведены результаты масс-спектрометрии полученного продукта.
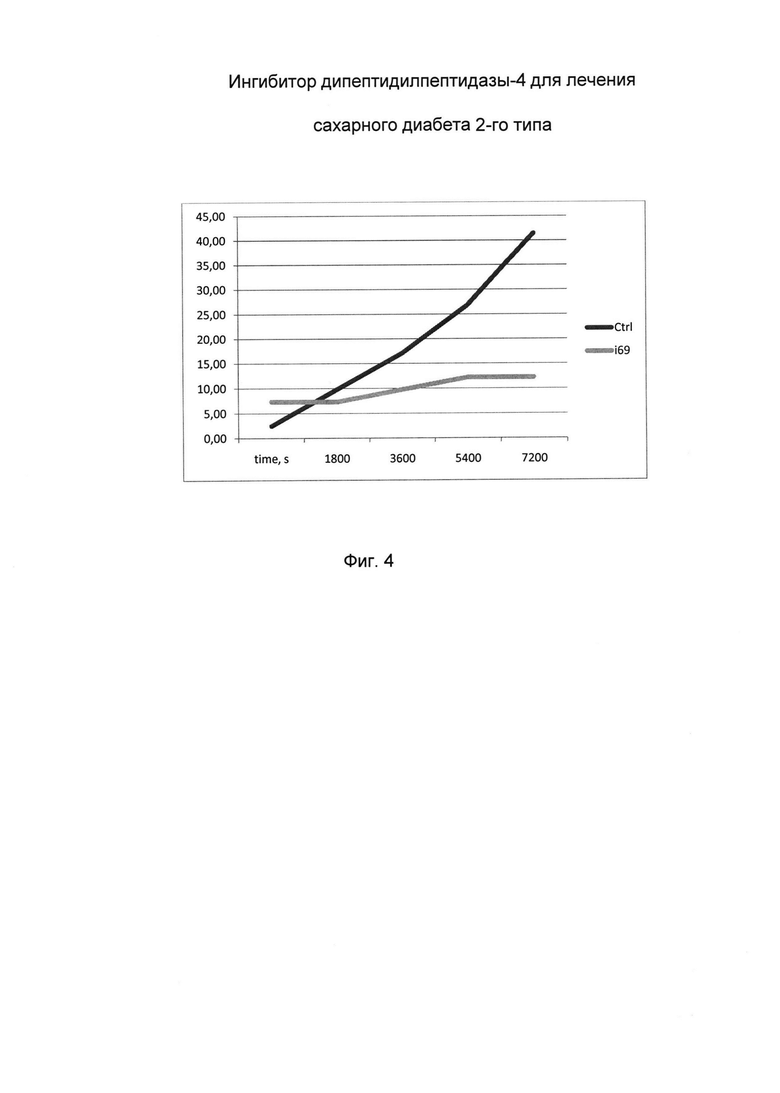
На фиг. 4 представлен график скорости реакции в присутствии ингибитора - полученного вещества, в концентрации, сопоставимой с концентрацией субстрата.
Раскрытие изобретения
Известно, что у больных СД 2-го типа нарушено не только количественное содержание инкретинов (ГПП-1), но и механизм их действия (ГИП), поэтому очевидна необходимость создания группы препаратов, влияющих на уровень инкретинов. Наличие подобных средств должно улучшить гликемический контроль путем воздействия на иные патогенетические звенья данного заболевания, в отличие от существующих групп антидиабетических препаратов.
Влияние дипептидилпептидазы-4. Снижение эффекта инкретинов, находящихся в кровеносном русле, является следствием их быстрого разрушения и выведения из организма. Причина деградации инкретинов и потери их функции кроется в их структуре - наличии остатка аланина (Ala) во 2-м с N-конца положении. Подобные аминокислотные последовательности являются субстратами для сериновой протеазы - дипептидилпептидазы-4 (ДПП-4).
Инкретины ГПП-1 и ГИП представляют собой пептидные гормоны, зрелые формы которых являются результатом расщепления предшественников в К- и L-клетках тонкого кишечника. ГИП состоит из 42 аминокислот и образуется в результате посттрансляционной модификации про-ГИП прогормон-протеазой РС1/3 в энтероэндокринных K-клетках. Форма ГИП является единственной известной активной формой ГИП у человека, крысы, мыши, свиньи и крупного рогатого скота. ГПП-1 представляет собой результат посттрансляционного расщепления прогормон-протеазой PC1/3 продукта гена проглюкагона в энтероэндокринных L-клетках. ГПП-1 и является основной формой биологически активного циркулирующего ГПП-1 в организме человека. В результате протеолитической обработки ГПП-1 и ГИП во 2-м N-концевом положении их последовательностей появляется остаток аланина. Получающиеся структуры являются субстратами для дипептидилпептидазы-4, отщепляющей от полипептидной цепи N-концевые дипептиды, содержащие остатки Pro или Ala во 2-м с N-конца положении.
Еще одним доказательством роли дипептидилпептидазы-4 в патогенезе сахарного диабета 2-го типа является влияние функции генов, регулирующих экспрессию гена ДПП-4. Генами, снижающими экспрессию указанного гена, являются печеночные ядерные транскрипционные факторы 1-α и 1-β, члены семейства гомеодоменсодержащих белков. Наличие мутаций, снижающих функцию любого из этих генов и, соответственно, повышающих уровень экспрессии ДПП-4, приводит к развитию сахарного диабета.
Понимание роли ДПП-4 в метаболизме инкретинов дало основание для создания препаратов, увеличивающих время действия эндогенных ГИП и ГПП-1 - ингибиторов ДПП-4. Результаты экспериментов на животных моделях продемонстрировали сохранение концентрации инкретинов в крови под влиянием ингибиторов ДПП-4.
Ингибиторы ДПП-4 имеют и другое преимущество перед применяющимися в настоящее время гипогликемическими препаратами. Так как инкретин-опосредованные эффекты на биосинтез и высвобождение инсулина являются глюкозозависимыми, при применении ингибиторов ДПП-4 риск возникновения гипогликемии значительно ниже, чем при применении инсулина, препаратов сульфонилмочевины или меглитинидов. Кроме того, в отличие от указанных препаратов, ингибиторы ДПП-4 не вызывают прибавку массы тела. Благодаря особенностям их действия, применение ингибиторов ДПП-4 представляет особый интерес на ранних стадиях СД 2-го типа, как в виде монотерапии, так и в комбинации с другими препаратами, так как они могут способствовать протекции β-клеток.
Экзопептидазная каталитическая активность дипептидилпептидазы-4, отщепляющей от полипептидной цепи определенные N-концевые дипептиды, содержащие остатки Pro или Ala во 2-м с N-конца положении, определяется строением ее активного центра.
ГПП-1 и ГИП обеспечивают от 60 до 70% общего 1, 3 инсулинового ответа после приема пищи (эффект инкретина) у здоровых людей. В клинических исследованиях пациентов с сахарным диабетом 2 типа эффект инкретина присутствовал, но был значительно снижен по сравнению со здоровыми людьми. У таких пациентов после перорального введения глюкозы инсулиновый ответ был не только отсрочен во времени, но и снижен.
Потенциальные лекарственные средства, ингибирующие каталитическую активность ДПП-4 и взаимодействующие с ее активным центром, должны отвечать следующим критериям:
- субструктуры, образованные остатком Ser630 в каталитическом центре фермента и соседние аминокислоты, как правило, связывают гидрофобные кольцевые группы, такие как три-фторбензил группа ситаглиптина или бензонитрил алоглиптина;
- обязательна стабилизация двух кислотных остатков -Glu205 и Glu206 - в сайте связывания ДПП-4 аминогруппой ингибитора;
- в дополнение к этим обязательным взаимодействиям, потенциальные ингибиторы могут содержать различные функциональные группы с целью усиления связывания с ДПП-4.
Согласно указанным выше критериям, эффективными ингибиторами ДПП-4 могут быть соединения, N-ацилированные альфа-аминокислотами производные цианопирролидина. Однако данная группа веществ в водных растворах при рН 7,4 способна к внутримолекулярной циклизации. Этот феномен приводит в естественных условиях человеческого организма к функциональной инактивации лекарственных средств - N-ацилированных альфа-аминокислотами производных цианопирролидина. Процесс циклизации таких цианопирролидинов отражен ниже:
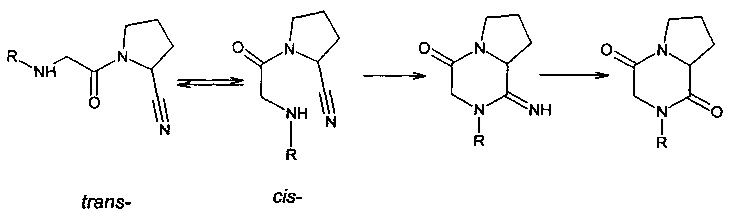
Показана внутримолекулярная циклизация из цис-формы N-ацилцианопирролидина.
Процесс внутримолекулярной циклизации N-ацилцианопирролидина в физиологических условиях, говорит о том, что при сохранении химической структуры потенциального лекарственного средства необходимо предотвратить данное свойство подобных производных цианопирролидина. Например, включать в соединения пространственно объемные группы, препятствующие быстрой циклизации или проводить модификацию циано-группы в пирролидине таким образом, чтобы циклизация оказалась невозможна. Это способы "защиты" функциональной активности ингибитора ДПП-4. Несмотря на наличие на рынке коммерческих противодиабетических средств - ингибиторов ДПП-4, есть необходимость в создании новых ингибиторов дипептидилпептидазы-4, сохраняющих свою химическую и пространственную структуру в естественных условиях человеческого организма. При этом соединение должно быть в первую очередь стабильным, даже при не очень высокой его активности, как ингибитора.
Пример 1
Получение 3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-она гидрохлорида
Обозначения реагентов:
NH2OH×HCl - гидроксиламина гидрохлорид;
DIC - N,N'-диизопропилкарбодиимид;
CH2Cl2 - хлористый метилен;
HCl - хлористый водород;
ВОР - (бензотриазол-1-илокси)трис(диметиламино)фосфоний гексафторфосфат;
DIPEA - диизопропилэтиламин;
МеОН - метанол;
Boc2O - ди-трет-бутилдикарбонат.
Получение 3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-она гидрохлорида заключается в последовательности процедур, включающей на первой стадии обработку защищенного по азоту трет-бутилоксикарбонильной группой 2-цианопирролидина (I) гидроксиламином. Полученное соединение (II) далее ацилировали бензойной кислотой в присутствии диизопропилкарбодиимида и далее осуществляли термическую циклизацию продукта с образованием соединения (III). После снятия трет-бутилоксикарбонильной защитной группы получали (S)-2-(5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин в виде гидрохлорида (IV). Далее полученное соединение (IV) ацилировали защищенной по аминогруппе трет-бутилоксикикарбонильной защитой 3-амино-3-(4-фторфенил) пропановой кислотой в присутствии (бензотриазол-1-илокси)-трис-(диметиламино)-фосфоний гексафторфосфата и диизопропиламина. После снятия трет-бутилоксикарбонильной защитной группы получали искомое соединение 3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-она гидрохлорид (V).
Пример 2
Получение продукта II
(S)-1-N-трет-бутоксикарбонил-2-(N-гидроксикарбамимидоил)-пирролидин (II)
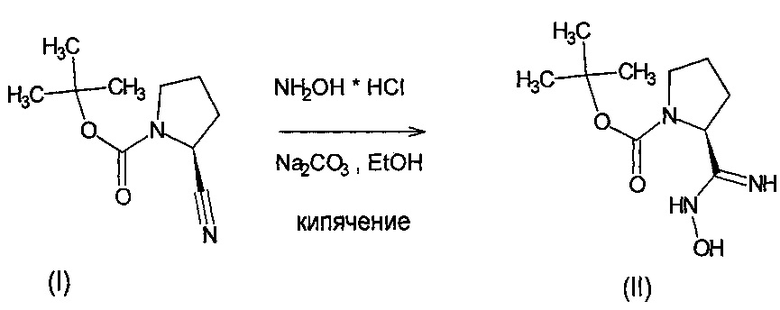
К перемешиваемому раствору 5,00 г (0,0255 моль, 1 экв) (S)-1-трет-бутоксикарбонил-2-цианопирролидина (I) в 100 мл этанола последовательно добавили 7,03 г (0,066 моль, 2,6 экв) карбоната натрия и 4,59 г (0,066 моль, 2,6 экв.) гидрохлорида гидроксиламина. Реакционную смесь нагрели до кипения и выдержали при кипении и перемешивании в течение суток. Затем реакционную смесь охладили до комнатной температуры и отфильтровали. Осадок на фильтре промыли 50 мл этанола. Полученный фильтрат упарили на роторном испарителе досуха. К полученному остатку добавили 50 мл воды и продукт экстрагировали хлористым метиленом (3⋅50 мл). Объединенные органические слои промыли 50 мл 5%-ного раствора лимонной кислоты. Водный слой нейтрализовали насыщенным раствором карбоната натрия и экстрагировали 50 мл смеси хлороформа и изопропанола в соотношении 1:5. Хлороформно-изопропанольный слой объединили с раствором хлористого метилена, полученного после промывки раствором лимонной кислоты. Объединенный органический слой высушили над безводным сульфатом натрия и упарили досуха на роторном испарителе.
Полученный продукт (сырой амидоксим) II (2,1 г) без очистки использовали в следующей стадии.
Пример 3
Получение продукта III
(S)-1-N-трет-бутоксикарбонил-2-(5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидина (III)

К раствору 1,34 г (0,011 моль, 1.2 экв.) бензойной кислоты в 50 мл хлористого метилена добавили 1,51 г (0,012 моль, 1.3 экв.) N,N'-диизопропилкарбодиимида. Смесь перемешивали 20 мин при комнатной температуре и добавили 2,1 г (0,0092 моль, 1 экв.) полученного на предыдущей стадии (S)-1-N-трет-бутоксикарбонил-2-(N-гидроксикарбамимидоил)-пирролидина (продукт II). Реакционную массу перемешивали 5 ч при комнатной температуре. Далее растворитель упаривали на роторном испарителе и к остатку добавляли 50 мл пиридина. Реакционную массу кипятили в течение ночи. Пиридин удаляли на роторном испарителе и остаток хроматографировали на силикагеле (элюент: н-гексан-этилацетат 1:1). Получен продукт III (0,51 г, 6%).
Пример 4
Получение продукта IV в виде гидрохлорида
(S)-2-(5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидина гидрохлорид (IV)
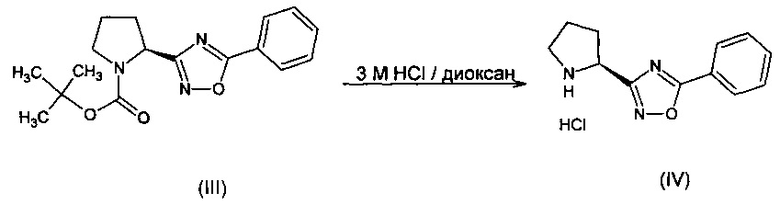
К раствору 0.51 г (0,0015 моль, 1 экв.) (S)-1-N-трет-бутоксикарбонил-2-(5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидина (III) добавили 2 мл 3 М HCl в диоксане, перемешивали при комнатной температуре в течение ночи. Реакционную массу упарили досуха на роторном испарителе и остаток промыли 10 мл диэтилового эфира. Эфир декантировали и осадок сушили в вакууме масляного насоса. Получен продукт IV в виде гидрохлорида (0,29 г, 71%).
Пример 5
Получение продукта V в виде гидрохлорида
3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-она гидрохлорида (V)
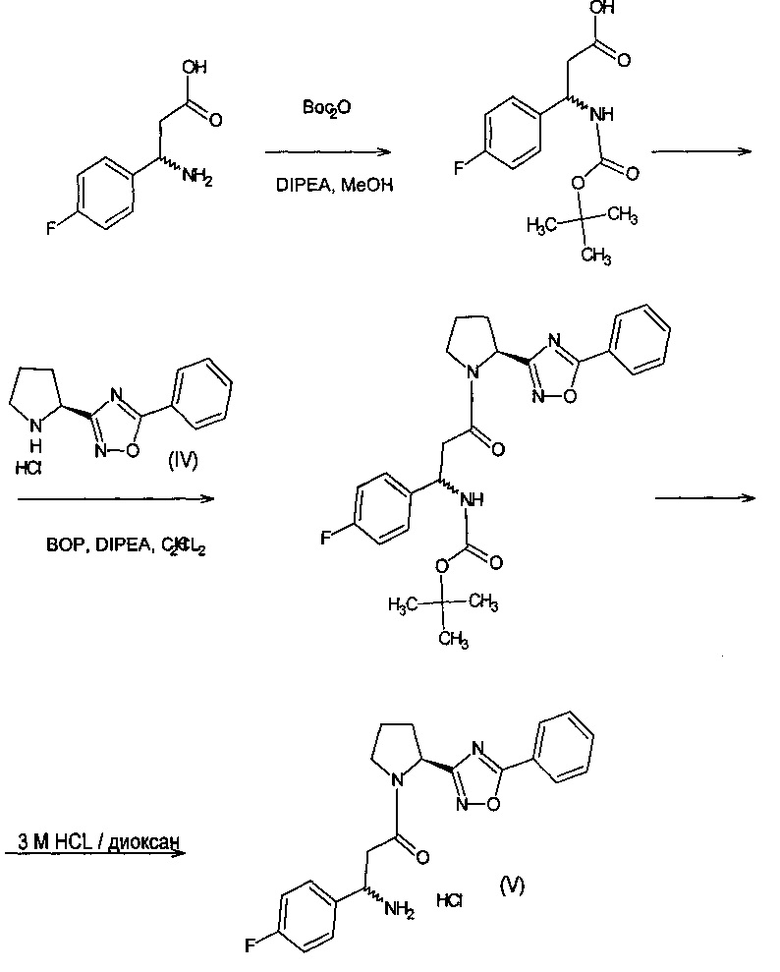
К суспензии 0,031 г (0,17 ммоль, 1 экв.) (R/S)-3-амино-3-(4-фторфенил)пропановой кислоты в 4 мл метанола добавили 0,038 г - ди-трет-бутилдикарбоната (Boc2O) (0,18 ммоль, 1,05 экв.) и 0,068 мл (0,39 ммоль, 2,3 экв.) диизопропилэтиламина. Реакционную массу перемешивали при комнатной температуре в течение 3 часов. Затем растворитель упаривали досуха, и остаток растворяли в 5 мл хлористого метилена. К раствору добавили 0,075 г (бензотриазол-1-илокси)трис(диметиламино)фосфоний гексафторфосфата (ВОР-реагент) (0,17 ммоль) и 0,071 г (0,17 ммоль, 1 экв.) соединения IV. Реакционную смесь перемешивали при комнатной температуре в течение ночи, затем разбавили 5 мл хлористого метилена, промыли 10 мл 5% лимонной кислоты, водой и раствором 5% NaHCO3. Органический слой высушили над безводным Na2SO4, отфильтровали и упарили досуха. К остатку добавили 2 мл 3 М HCl в диоксане; перемешивали в течение ночи. Растворитель упаривали досуха.
Остаток высушивали в вакууме масляного насоса. Получено 0,042 г (60% выход, 100% чистоты по LC/MS) продукта V в виде гидрохлорида (Mr = 380; 381-протонированная форма [380+Н+]).
В результате произведенных действий получено вещество:
(R/S)-3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-он (с молекулярной массой Mr = 380) в виде гидрохлорида, соответствующее структурной формуле:

Пример 6
Анализ образцов
Согласно описанному выше регламенту получено вещество:
(R/S)-3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-он (с молекулярной массой Mr = 380) в виде гидрохлорида, соответствующее структурной формуле:
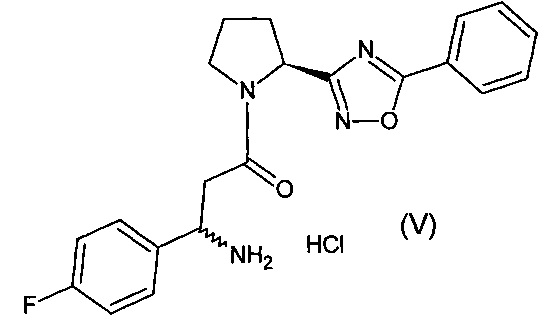
Пример 6.
Анализ ОФ ВЭЖХ синтезированного вещества (V)
Условия проведения ВЭЖХ:
Колонка - Onyx С18 50×4,6 мм;
Рабочий раствор С - 0,1% FA в воде;
Рабочий раствор D - 0,1% FA в ACN;
Давление на старте - 71,1 бар;
Давление при окончании - 45,3 бар;
Скорость потока - 3,75 мл в мин;
Градиент - "С" -> 2,9 мин -> "D" -> 0,2 мин -> "С" -> промывка;
Детекция - УФ и масс-спектрометрия.
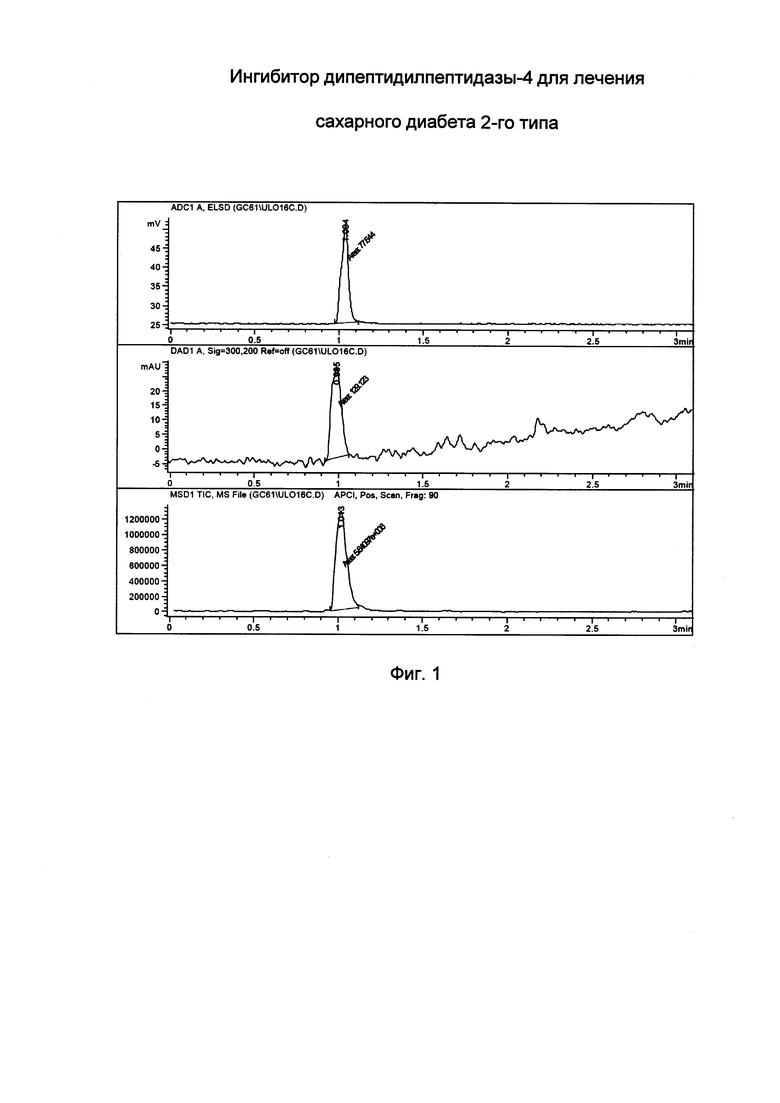
Получены результаты ВЭЖХ синтезированного продукта, представленные на Фиг. 1.
ВЭЖХ синтезированного вещества продемонстрировала отсутствие примесей в анализируемом образце - наличие единичного пика на каждом из трех датчиков детекции - ELSD, УФ-датчика (DAD1) и масс-детектора (MSD1).
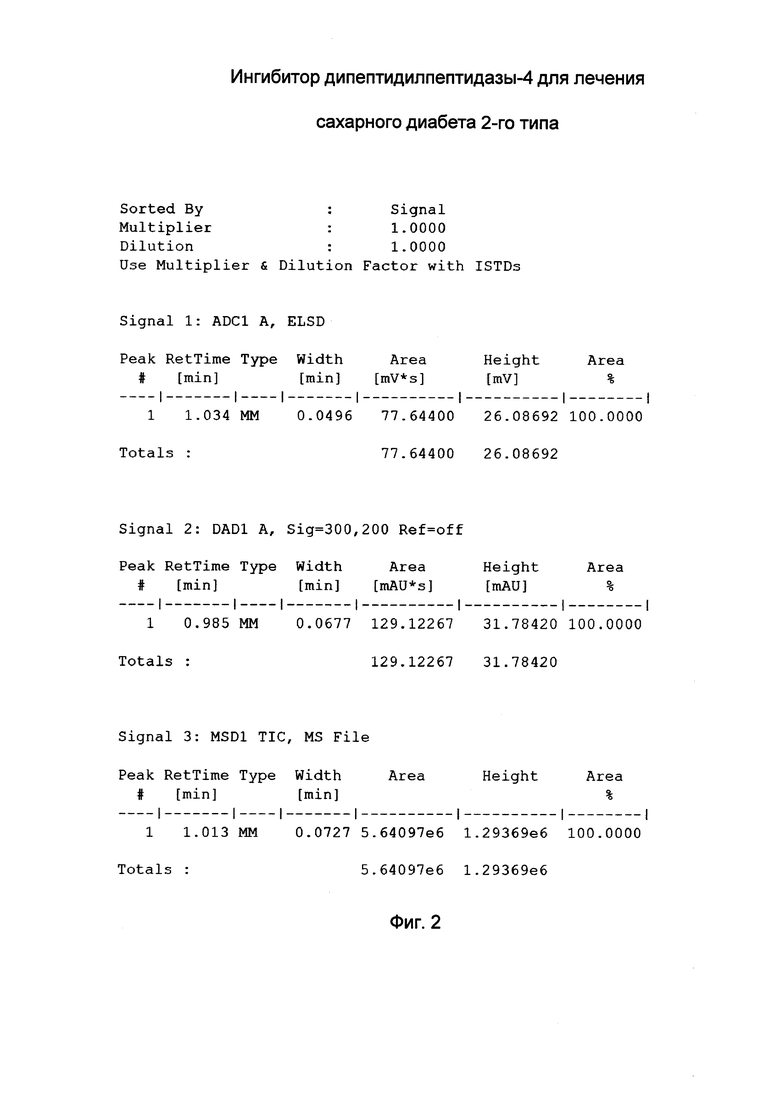
Проведен анализ пика вещества, выявленного при ВЭЖХ. Результаты анализа представлены на Фиг. 2.
На фиг. 2 представлены результаты анализа площадей пиков синтезированного продукта, полученных при ВЭЖХ.
При анализе площадей пиков, полученных на трех датчиках детекции, выявлена 100%-ная чистота синтезированного продукта.
Масс-спектрометрия полученного продукта
Результаты масс-спектрометрии представлены на Фиг 3.
Молекулярная масса вещества, выявленного при LC/MS анализе (Mr~380,7), соответствует заявленной (Mr=381).
Характеристика готового продукта
Наименование продукции: лекарственное вещество - ингибитор дипептидилпептидазы-4 из группы N-ацильных производных аминоацил-2-цианопирролидина.
Основное назначение продукции: ингибитор дипептидилпептидазы-4 из группы N-ацильных производных аминоацил-2-цианопирролидина для терапии сахарного диабета 2-го типа. Эмпирическая (химическая) формула: C21H21FN4O2 (×HCl), c учетом солевой формы гидрохлорида: C21H22Cl FN4O2
Молекулярная масса: 380; [380+(36,5 - гидрохлорид)=416,5]
Описание: Субстанция представляет собой аморфный порошок желтоватого цвета.
Растворимость: легко растворим в ДМСО, растворим в 70% этиловом спирте (10 мг субстанции в 10 мл 70% этилового спирта).
Условия хранения: В сухом, защищенном от света месте, при температуре не выше 30°С.
В таблице приведена концентрация расщепленного субстрата (специфичного для дипептидилпептидазы-4) в отсутствие ингибитора (колонка Ctrl) и в присутствии ингибитора - полученного вещества в концентрации 2 mM.
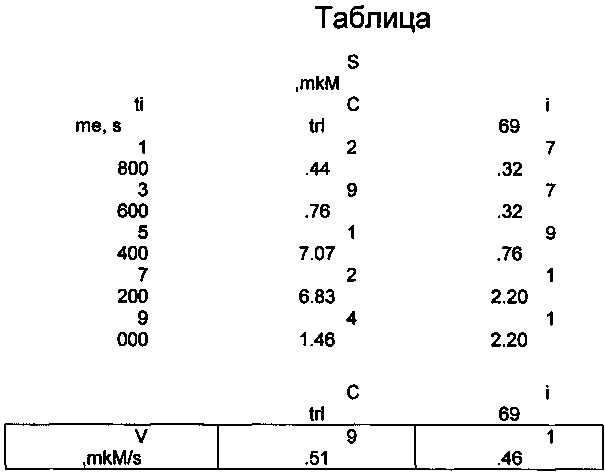
В соответствии с таблицей построен график, см. фиг. 4:
по оси X - время в секундах, по оси Y - концентрация расщепленного субстрата в мкМ.
Скорость реакции - это угол наклона графика. Для контрольного графика - это 9.51 мкМ/с, для i69 - 1.46 мкМ/с.
Из графика следует, что в присутствии ингибитора, то есть полученного вещества, в концентрации, сопоставимой с концентрацией субстрата, скорость реакции расщепления субстрата снизилась в 6.5 раз, что свидетельствует об эффективном конкурентном ингибировании и эффективности полученного ингибитора дипептилпептидазы-4 для лечения сахарного диабета 2-го типа.
В соответствии с полученными результатами можно сделать вывод, что поставленная задача решена и очевидна промышленная применимость полученного вещества для лечения сахарного диабета 2-го типа в связи с доказанной активностью полученного ингибитора дипептилпептидазы-4.
СОКРАЩЕНИЯ И ОБОЗНАЧЕНИЯ
АЛТ - аланинаминотрансфераза
АПФ - ангиотензин-превращающий фермент
ACT - аспартатаминотрансфераза
ВГН - верхняя граница нормы
ВОЗ - Всемирная организация здравоохранения
ВЭЖХ - высокоэффективная жидкостная хроматография
ГИП - глюкозозависимый инсулинотропный полипептид
ГПП-1 - глюкагоноподобный пептид-1
ГПП-2 - глюкагоноподобный пептид-2
ГППП - глицентин производный панкреатический протеин
ГЭРБ - гастроэзофагеальная рефлюксная болезнь
ДМСО - диметилсульфоксид
ДНК - дезоксирибонуклеиновая кислота
ДПП-4 - дипептидилпептидаза-4
ЖКТ - желудочно-кишечный тракт
КСТ - краткосрочный скрининговый тест
ЛП - лекарственный препарат
Про-ГИП - предшественник глюкозозависимого
инсулинотропного полипептида
Про-ГПП - предшественник глюкагоноподобного пептида-1
ПП-1 - промежуточный пептид-1
ПП-2 - промежуточный пептид-2
СД 2-го типа - сахарный диабет 2-го типа
УФ - ультрафиолетовое излучение
хч - химически чистый
чда - чистый для анализа
ACN - ацетонитрил
AUC - площадь под кинетической кривой
Cmax - средняя максимальная концентрация
dNTP - дезоксинуклеозид трифосфат
[Е] - коэффициент молярной экстинкции
EtOH - этанол
FA - муравьиная кислота
Glu250 - расположение остатка глютаминовой кислоты в 250
положении аминокислотной цепи
полипептида
Glu-Pro-pNA - глутамин-пролин-паранитроанилин
in vitro - «в пробирке»
LC/MS - анализ вещества комбинацией методов ВЭЖХ и масс-спектрометрии
МеОН - метанол
Mr - молекулярная масса
Ser630 - расположение остатка серина в 630 положении
аминокислотной цепи полипептида
Val25Met - замена валина на метионин в 25 положении
полипептидной цепи
Vd - кажущийся объем распределения
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР ДИПЕПТИДИЛПЕПТИДАЗЫ-4 ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА 2-ГО ТИПА, СОЕДИНЕНИЯ (ВАРИАНТЫ) | 2018 |
|
RU2712097C1 |
| ГИПОГЛИКЕМИЧЕСКОЕ СРЕДСТВО ПЕПТИДНОЙ СТРУКТУРЫ, ИНГИБИРУЮЩЕЕ ДИПЕПТИДИЛПЕПТИДАЗУ-4 | 2015 |
|
RU2600810C1 |
| СРЕДСТВО ПЕПТИДНОЙ СТРУКТУРЫ, ИНГИБИРУЮЩЕЕ ДИПЕПТИДИЛПЕПТИДАЗУ-4, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2015 |
|
RU2589258C1 |
| ИНГИБИРУЮЩЕЕ ДИПЕПТИДИЛПЕПТИДАЗУ IV СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2011 |
|
RU2485952C2 |
| СОЛИ МЕТИЛ(R)-7-[3-АМИНО-4-(2,4,5-ТРИФТОРФЕНИЛ)-БУТИРИЛ]-3-ТРИФТОРМЕТИЛ-5,6,7,8-ТЕТРАГИДРО-ИМИДАЗО[1,5-a]ПИРАЗИН-1-КАРБОКСИЛАТА | 2010 |
|
RU2528233C2 |
| СПОСОБ УЛУЧШЕНИЯ ПЕРЕДАЧИ СИГНАЛА В ОСТРОВКАХ ЛАНГЕРГАНСА ПРИ САХАРНОМ ДИАБЕТЕ И ЕГО ПРОФИЛАКТИКЕ | 2001 |
|
RU2261096C2 |
| НОВЫЕ ИНГИБИТОРЫ ДИПЕПТИДИЛПЕПТИДАЗЫ IV И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОНИЖЕНИЯ КРОВЯНОГО ДАВЛЕНИЯ | 2002 |
|
RU2305553C2 |
| КОМБИНАЦИЯ ДЛЯ РЕГЕНЕРАТИВНОЙ ТЕРАПИИ БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 1 ТИПА | 2018 |
|
RU2694527C1 |
| N-ЗАМЕЩЕННЫЕ 2-ЦИАНПИРРОЛИДИНЫ | 1999 |
|
RU2251544C2 |
| N-ЗАМЕЩЕННЫЕ 2-ЦИАНОПИРРОЛИДИНЫ | 1997 |
|
RU2180901C2 |
Изобретение относится к медицине, а именно к веществам, являющимся ингибиторами дипептидилпептидазы-4. Предложено применение (R/S)-3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-она (с молекулярной массой Mr=380) в виде гидрохлорида (в пересчете на солевую форму Mr=380+36.5 (HCl)=416.5), соответствующее структурной формуле (I) в качестве ингибитора дипептидилпептидазы-4 для лечения сахарного диабета 2-го типа. Технический результат: химическая структура соединения препятствует его внутримолекулярной циклизации, что сохраняет химическую и пространственную структуру в естественных условиях человеческого организма. 4 ил., 1 табл., 6 пр.
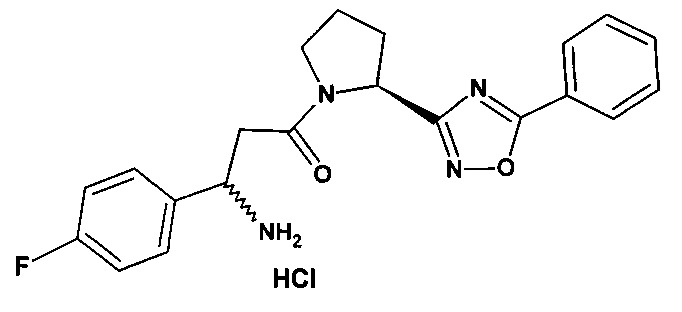 (I)
(I)
Применение (R/S)-3-амино-1-[(S)-5-фенил-[1,2,4]оксадиазол-3-ил)-пирролидин-1-ил]-3-(4-фторфенил)-пропан-1-она гидрохлорида, обладающего молекулярной массой Mr 381, в качестве ингибитора дипептидилпептидазы-4 для лечения сахарного диабета 2-го типа.
| NORDHOFF S | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Bioorg.Med.Chem | |||
| Lett | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| N-ЗАМЕЩЕННЫЕ 2-ЦИАНПИРРОЛИДИНЫ | 1999 |
|
RU2251544C2 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2017-08-21—Публикация
2015-11-27—Подача