Гетерогенная униполярная и биполярная депрессия является обычным психиатрическим расстройством, которое наиболее вероятно обусловлено нейрохимическими изменениями в центральной нервной системе. В течение нескольких последних десятилетий широкое распространение в медицине для лечения униполярной депрессии получило применение антидепрессивных лекарств. Настоящее изобретение относится к новым пептидам и их применению в качестве терапевтических агентов для лечения пациентов, страдающих депрессией.
Полагают, что эндогенная депрессия генетически обусловлена биохимическим нарушением, приводящим к неспособности противостоять стрессу. Эту форму депрессии часто классифицируют как униполярную депрессию, которую подразделяют на депрессивную фазу маниакально-депрессивного психоза и на ажитированную депрессию. Депрессивная фаза маниакально-депрессивного психоза характеризуется замедлением психомоторных реакций, когда субъект в определенной степени неадекватно взаимодействует с окружающей средой. С другой стороны, ажитированная депрессия характеризуется повышенной нецелесообразной активностью, такой как повышенное сердцебиение, навязчивое движение рук и т.п.
Наиболее вероятно, что униполярная депрессия представляет собой нарушение, обусловленное многочисленными гетерогенными изменениями в головном мозге. Специалисты одной из научных школ придерживаются катехоламинной теории, согласно которой эндогенная депрессия вызывается снижением концентрации норэпинефрина в области сайтов адренергического рецептора в головном мозге. Также возможно, что эндогенная депрессия вызывается абсолютным или относительным дефицитом индоламина, а именно 5-гидрокситриптамина, в сайтах рецептора в головном мозге.
Курс лечения эндогенной депрессии состоит в электрошоковой терапии или лечении лекарственными средствами. Лекарства, вводимые с целью терапевтического лечения депрессии, включают (1) трициклические антидепрессанты, (2) ингибиторы моноаминоксидазы (МАО) и (3) антидепрессанты второго поколения.
Первыми лекарствами, выбранными для лечения эндогенной депрессии более тридцати лет назад, были трициклические препараты. Однако эти лекарства обладали ограниченной эффективностью, поэтому у двух третей пациентов, получавших трициклические препараты, не было благоприятной реакции. Трициклические препараты обладают многочисленными побочными эффектами, включающими холинергическую блокаду, осложнения на сердце, аллергические реакции, сухость во рту, запоры, "пелену перед глазами" и тахикардию. Строение трициклических лекарств характеризуется наличием трициклического ядра. Трициклические антидепрессанты включают имипрамин, дезилрамин, амитриптилин, нортриптилин, протриптилин, доксепин и тримипрамин. Метаболизм этих трициклических структур происходит через систему оксидаз со смешанными функциями. Образовавшиеся метаболиты являются фармакологически активными соединениями.
С 50-х годов для лечения депрессии применяли ингибиторы МАО. Эти соединения подразделяют на гидразиды, например, с С-N-N-фрагментом (например, фенелзин и изокарбоксазид), и негидразиды (например, транилципромин). Эти лекарства не получили широкого распространения вследствие серьезных побочных эффектов.
Лекарства так называемого второго поколения представляют группу новых лекарств, включающую амоксапин, мапротилин, флуокситин, тразодон и бупропион. Большинство этих лекарств, вероятно, действуют таким же образом, как и трициклические препараты.
Антидепрессивные лекарства должны преодолевать гематоэнцефалический барьер в фармакологически эффективных концентрациях. Капилляры центральной нервной системы, в отличие от капиллярного ложа, снабжающего другие органы, обладают тесными связями с эндотелиальными клетками коры головного мозга. Известно, что гематоэнцефалический барьер у человека представляет собой липидный барьер без пор. Любое потенциальное антидепрессивное лекарство должно быть создано так, чтобы соединение было способно преодолеть гематоэнцефалический барьер. Соединения с низкой растворимостью в липидах, так же как и высокоионизированные соединения, не способны выйти из кровотока для проникновения во внеклеточную жидкость головного мозга. Водорастворимые соединения могут преодолеть гематоэнцефалический барьер только при наличии специальной мембранной транспортной системы. И наоборот, для жирорастворимых лекарств гематоэнцефалический барьер по существу не является препятствием.
Было установлено, что трипептид MIF, называемый иначе фактором ингибирования меланоцитстимулирующего гормона и имеющий следующую химическую формулу: пролил-лейцил-глицинамид или Pro-Leu-Gly-NH2, оказывает многочисленные неэндокринные воздействия на головной мозг. На многочисленных животных-моделях было также показано, что трипептид MIF является активным в отношении лечения депрессии.
Первоначально MIF был выделен из экстрактов гипоталамуса быка (Nair и др. , 1971, Biochem. Biophys. Res. Comm. 43(6): 1376-1381) и экстрактов гипоталамуса крысы (Celis и др. , 1971, Proc. Natl. Acad. Sci. USA 68(7): 1428-1433) и охарактеризован. Активность MIF связана с подавлением высвобождения меланоцитстимулирующего гормона, гипофизного гормона, который, как известно, стимулирует производство меланина. Ни в одной из вышеуказанных публикаций не предполагается и не описывается какая-либо антидепрессивная активность MIF.
В патенте США 3708593 (выданном на имя N.Р. Plotnikoff 2 января 1973) описано, что MIF проявляет антидепрессивную активность в отношении мышей, что было установлено с помощью модифицированного допа-теста (Everett и др., 1966, Рrос. 1st. Int. Sym. Anti-depressant Drugs, стр. 164).
В патенте США 3795738 (выданном на имя N.Р. Plotnikoff 5 марта 1974) описано, что MIF индивидуально или в комбинации с другими известными лекарствами проявляет повышенную активность в отношении болезни Паркинсона.
В патенте США 3931184 (выданном на имя С.G. Lex 6 января 1976) представлен способ выделения фармацевтически чистого MIF. Полугидрат MIF растворяют в метаноле с последующим добавлением диэтилового эфира, получая белый кристаллический осадок MIF. Этот чистый MIF собирают, промывают эфиром и сушат под вакуумом перед применением.
В патенте США 4278595 (выданном на имя J.H. Cort 14 июля 1981) описано, что практическому применению MIF препятствует то, что MIF быстро метаболизируется после введения. Вследствие этого относительно короткого времени полужизни MIF для получения эффективных концентраций оказывается необходимым внутривенное введение больших количеств MIF в течение продолжительных периодов времени. Cort описывает аналог MIF, характеризующийся замещением Leu на его D-изомер, для получения аналога MIF необязательно замещают Pro на пиро-Glu и необязательно алкилируют концевую амидную группу Gly-NH2. Такой аналог может обладать такой же антидепрессивной активностью, как и MIF, и повышенной стабильностью. Cort описывает трипептид, имеющий формулу X-D-Leu-NH2-CH2-CONR1R2, где Х обозначает Pro или пиро-Glu и каждый из R1 и R2 независимо друг от друга обозначает Н или низший алкил, предпочтительно метил или этил.
Было установлено, что Tyr-MIF-1 (Tyr-Pro-Leu-Gly-NH2), представляющий собой пептид, имеющий происхождение из головного мозга, оказывает действие на пассивное избегание у крыс (Hayashi и др., 1983, Brain Res. Bull. 11: 659-662). Различные аналоги Tyr-MIF-1 (т.е. пептиды с различными заместителями остатка Туг, что приводит к получению Ala-MIF-1, Leu-MIF-1 или Phe-MIF-1) были изучены с точки зрения возможности оказывать влияние на поведение и двигательную активность (Hayashi и др., 1984, Pharmacology Biochemistry & Behavior 21: 809-812). Ala-MIF-1 и Phe-MIF-1, но не Leu-MIF-1, оказывали воздействие на реакцию пассивного избегания у крыс. Было установлено, что ни один из этих пептидов не оказывает воздействия на двигательную реакцию.
Kastin и др., (1984, Pharmacology Biochemistry & Behavior 21: 767-777) показали, что MIF-1 и Tyr-MIF-1 являются активными антидепрессантами. Уровень активности определяли с помощью теста водяного колеса, представляющего собой модификацию плавательного теста Порсольта.
Kastin и др., (1985, Pharmacology Biochemistry & Behavior 23: 1045-1049) установили, что Tyr-MIF-1 и некоторые аналоги Tyr-MIF-1 обладают антиопиумным действием. Наряду с Tyr-MIF-1, Phe-MIF-1 проявил активность в качестве ингибитора обезболивающего воздействия морфина у крыс.
Banks и др. , (1986, Am. J. Physiol. 251 [Endocrine Metabolism 14]: E477-E482) выявили медиируемую носителем транспортную систему, ответственную за доставку Tyr-MIF-1 из системы кровотока во внеклеточную мозговую жидкость.
Таким образом, существует необходимость в разработке и создании модифицированных малых пептидов для лечения страдающих депрессией пациентов, которые обладали бы фармакологической активностью после преодоления гематоэнцефалического барьера, не приводя к побочным эффектам, присущим большинству доступных, применяемых в настоящее время антидепрессивных лекарств.
Настоящее изобретение относится к модифицированным малым пептидам для применения в качестве антидепрессивных соединений. В соответствии с изобретением эти новые пептиды применяют для лечения пациентов, страдающих депрессией. Эти преобразования затрагивают остатки с концевой аминогруппой, остатки с концевой карбоксильной группой и остатки внутренних аминокислот и включают присоединение и замещение аминокислотных остатков и преобразование пептидных связей и функциональных боковых групп соответствующих аминокислотных остатков, как это более подробно описано ниже.
Предметом изобретения являются пептиды, обладающие фармакологической активностью.
Другим предметом изобретения являются пептиды, пригодные для лечения пациентов, проявляющих симптомы депрессии.
Отличительным признаком изобретения является синтез и получение малых пептидов, характеризующихся новыми преобразованиями, замещениями, присоединениями и/или делениями в структуре ядра MIF, которые обладают антидепрессивной активностью.
Преимущество изобретения состоит в получении малых пептидов, которые могут быть введены в более низких дозах, чем известные антидепрессанты, для снижения потенциальных вредных побочных эффектов.
В одном из примеров осуществления изобретения малые пептиды по изобретению являются трипептидами, представленными формулой (1)
R1-Pro1-АА1-NR2-СН2-R, (1)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы, включающей Trp, Orn, Lys, Leu, D-Leu, Arg, D-Arg или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и R2 обозначает атом водорода или группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, при условии, что если Рrо1 обозначает Pro и АА1 обозначает Leu, то оба R1 и R2 не могут обозначать водород, когда R обозначает карбамильную группу, поскольку MIF является известным соединением.
Примером трипептидов формулы (1), заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (1а)
Pro1-АА1-Gly-NH2, (1a)
где Pro1 и АА1 имеют значения, описанные выше для формулы (1).
Предпочтительные композиции трипептидов формулы (1а) включают: Рrо-Тrр-Gly-NH2, Pro-Arg-Gly-NH2, Pro-D-Arg-Gly-NH2, Pro-Lys-Gly-NH2, Pro-Orn-Gly-NH2 и Pro-Ile-Gly-NH2, но не обязательно ограничены ими.
Другим примером трипептидов формулы (1), заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (1b)
R1-Pro1-АА1-Gly-NH2, (1b)
где Pro1, АА1 и R1 имеют значения, описанные выше для формулы (1).
Предпочтительные композиции трипептидов формулы (1b) включают: цис- или тpaнс-4-OH-Pro-D-Arg-Gly-NH2, цис- или тpaнс-4-OH-Pro-Ile-Gly-NH2, цис- или тpaнс-4-OH-Pro-Arg-Gly-NH2, цис- или транс-4-OH-Pro-Trp-Gly-NH2 и цис- или тpaнс-4-тиo-Pro-Leu-Gly-NH2, но не обязательно ограничены ими.
Еще одним примером трипептидов формулы (1), заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (1с)
Prol-AAl-NR2-CH2-R, (1с)
где Pro1, AA1, R и R2 имеют значения, описанные выше для формулы (1), при условии, что, когда Pro1 обозначает Pro и АА1 обозначает Leu, R2 не может обозначать атом водорода, если R обозначает либо карбоксильную группу, либо гидроксиалкильную группу, поскольку эти соединения, т.е. Pro-Leu-NHCH2-СO2Н (или Pro-Leu-Gly) и Pro-Leu-NHCH2-CH2OH, не подпадают под объем данного изобретения, а также еще при одном условии, что, когда Pro обозначает Pro и АА1 обозначает Тrр, R2 не может обозначать атом водорода, если R обозначает гидроксиалкильную группу, так как Pro-Trp-NHCH2-CH2OH является известным соединением. Предпочтительные композиции трипептидов формулы (1с) включают: Pro-Leu-N(CH3)CH2-CONH2 (или Pro-Leu-Sar-NH2) и Pro-Trp-NHCH2-CO2H (или Pro-Trp-Gly), но не обязательно ограничены ими.
Еще одним примером трипептидов по настоящему изобретению, заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (2)
R1-Pro1-АА1-Ala-R, (2)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы Arg или D-Arg; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонил; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером трипептидов формулы (2), заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (2а)
Pro1-АА1-Ala-NH2, (2a)
где Pro1 и АА1 имеют значения, описанные выше для формулы (2).
Предпочтительные композиции трипептидов формулы (2a) включают: Pro-Arg-Ala-NH2 и Pro-D-Arg-Ala-NH2, но не обязательно ограничены ими.
Еще одним примером трипептидов по настоящему изобретению, заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (3)
R1-Pro1-АА1-Tyr-R, (3)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту Orn; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером трипептидов формулы (3), заявленных для применения при лечении депрессии у пациентов, являются трипептиды формулы (3а)
R1-Рrо1-АА1-Туr-NН2, (3а)
где Pro1, АА1 и R1 имеют значения, описанные выше для формулы (3).
Предпочтительные композиции трипептидов формулы (3а) включают: Рrо-Оrn-Tyr-NH2 и цис- или тpaнс-4-OH-Pro-Orn-Tyr-NH2, но не обязательно ограничены ими.
Настоящее изобретение также относится к тетрапептидам и их применению для лечения депрессии. Один вариант выполнения изобретения относится к композициям тетрапептидов с увеличенным С-концом, представленным формулой (4)
R1-Pro1-АА1-Gly-АА2-R, (4)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает Ile, Leu, Arg, D-Arg или Trp; AA2 обозначает аминокислоту, выбранную из группы Trp или Туг; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером тетрапептидов формулы (4), заявленных для применения при лечении депрессии у пациентов, являются тетрапептиды формулы (4а)
R1-Pro1-АА1-Gly-АА2-NН2, (4a)
где Pro1, AA1, АА2 и R1 имеют значения, описанные выше для формулы (4).
Предпочтительные композиции тетрапептидов формулы (4a) включают: цис- или тpaнс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 1), цис- или транс-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 2), цис- или транс-4-OH-Pro-D-Arg-Gly-Trp-NH2, 3,4-дeгидpo-Pro-D-Arg-Gly-Trp-NH2 и 3,4-дeгидpo-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 62), но не обязательно ограничены ими.
Еще одним примером тетрапептидов формулы (4), заявленных для применения при лечении депрессии у пациентов, являются тетрапептиды формулы (4b)
Pro1-АА1-Gly-АА2-NН2, (4b)
где Pro1, АА1 и АА2 имеют значения, описанные выше для формулы (4).
Предпочтительные композиции тетрапептидов формулы (4b) включают: Pro-Ilе-Gly-Trp-NH2 (SEQ ID NO: 3), 3,4-дeгидpo-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 4), Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 5), Pro-Leu-Gly-Tyr-NH2 (SEQ ID NO: 6), Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 7), Pro-Trp-Gly-Trp-NH2 (SEQ ID NO: 8), Pro-D-Arg-Gly-Trp-NH2 и Pro-Ile-Gly-Tyr-NH2 (SEQ ID NO: 9), но не обязательно ограничены ими.
Еще одним примером тетрапептидов по изобретению являются композиции тетрапептидов с увеличенным N-концом, представленные формулой (5)
R1-АА1-R2-Pro1-АА2-Gly-R, (5)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы Тrр, Туr или Phe; АА2 обозначает аминокислоту, выбранную из группы Leu, Ilе или Тrр; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и каждый R1 и R2 независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером тетрапептидов формулы (5), заявленных для применения при лечении депрессии у пациентов, являются тетрапептиды формулы (5а):
Rl-AAl-R2-Prol-AA2-Gly-NH2, (5а)
где Pro1, AA1, АА2, R1 и R2 имеют значения, описанные выше для формулы (5), при условии, что, если Pro1 обозначает Pro, оба R1 и R2 не могут обозначать атом водорода, когда AA1 обозначает Туr и АА2 обозначает Тrр, поскольку это соединение, т.е. Tyr-Pro-Trp-Gly-NH2 (SEQ ID NO: 54), является известным соединением, а также еще при одном условии, что, если Pro1 обозначает Pro и АА2 обозначает Leu, оба R1 и R2 не могут обозначать атом водорода, когда АА1 обозначает Phe или Туr, поскольку Phe-MIF-1 и Tyr-MIF-1 являются известными соединениями. Предпочтительные композиции тетрапептидов формулы (5а) включают: Trp-Pro-Leu-Gly-NH2 (SEQ ID NO: 10), Phe-Pro-Leu-Gly-NH2 (SEQ ID NO: 11), 4-F-Phe-Pro-Leu-Gly-NH2 (SEQ ID NO: 12), 4-Cl-Phe-Pro-Leu-Gly-NH2 (SEQ ID NO: 13), 4-F-Phe-Pro-Ile-Gly-NH2 (SEQ ID NO: 14), 4-F-Phe-циc- или -тpaнс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 15), 4-F-Рhе-цис- или -тpaнс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 16), Trp-Pro-Leu-Gly-NH2 (SEQ ID NO: 17), Trp-Pro-Ile-Gly-NH2 (SEQ ID NO: 18), Тrр-цис- или -тpaнс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 19), Тrр-цис- или -тpaнс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 20) и 4-Сl-Рhе-цис- или -транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 60), но не обязательно ограничены ими.
Настоящее изобретение также относится к пентапептидам и их применению для лечения депрессии. В одном из вариантов пентапептиды по изобретению представляют собой композиции пентапептидов с увеличенным N-концом, представленные формулой (6)
R1-АА1-AA2-R2-Pro1-АА3-Gly-R, (6)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 и АА2 каждый независимо друг от друга обозначает аминокислоту, выбранную из группы Phe или Туr; АА3 обозначает аминокислоту, выбранную из группы Leu или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером пентапептидов формулы (6), заявленных для применения при лечении депрессии у пациентов, являются пентапептиды формулы (6а)
R1-AA1-AA2-R2-Pro1-AA3-Gly-NH2, (6a)
где Pro1, AA1, AA2, R1 и R2 имеют значения, описанные выше для формулы (6).
Предпочтительные композиции пентапептидов формулы (6а) включают: 4-F-Phe-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 21), 4-Cl-Phe-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 22), Phe-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 23), Phe-Tyr-Pro-Ile-Gly-NH2 (SEQ ID NO: 24), Phe-Tyr-цис- или -транс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 25), Phe-Tyr-цис- или -тpaнс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 26), Tyr-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 27), Tyr-Tyr-Pro-Ile-Gly-NH2 (SEQ ID NO: 28), Туr-Туr-цис- или -тpaнс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 29) и Туr-Туr-цис- или -тpaнс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 30), но не обязательно ограничены ими.
Другим примером пентапептидов по изобретению являются композиции пентапептидов с одновременно увеличенными N-концом и С-концом, представленные формулой (7)
R1-АА1-R2-Pro1-АА2-Gly-АА3-R, (7)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; AA1 обозначает аминокислоту, выбранную из группы Phe или Туr; AA2 обозначает аминокислоту, выбранную из группы Leu, Ile, Arg, D-Arg или Тrр; AA3 обозначает аминокислоту Trp; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером пентапептидов формулы (7), заявленных для применения при лечении депрессии у пациентов, являются пентапептиды формулы (7а)
Rl-AAl-R2-Prol-AA2-Gly-Trp-NH2, (7а)
где Pro1, AA1, AA2, R1 и R2 имеют значения, описанные выше для формулы (7).
Предпочтительные композиции пентапептидов формулы (7а) включают: Phe-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 31), Tyr-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 32), Phe-цис- или -тpaнс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 33), Phe-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 34), Phe-цис- или -транс-4-ОН-Рrо-Ile-Gly-Trp-NH2 (SEQ ID NO: 35), Туr-цис- или -транс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 36), Tyr-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 37), Туr-цис- или -тpaнс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 38), Tyr-Pro-Trp-Gly-Trp-NH2 (SEQ ID NO: 39), Туг-цис- или -транс-4-OH-Pro-Trp-Gly-Trp-NH2 (SEQ ID NO: 40), 4-F-Рhе-цис- или -тpaнс-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 41), Phe-цис- или -тpaнс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 42), 4-F-Phe-циc- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 43), 4-F-Рhе-цис- или -тpaнс-4-OH-Pro-D-Arg-Gly-Trp-NH2, 3-F-Рhе-цис- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 66); 2-F-Рhе-цис- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 68); и 4-Сl-Рhе-цис- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 61), но не обязательно ограничены ими.
Еще одна группа предпочтительных композиций пентапептидов формулы (7а) характеризуется необязательным преобразованием Pro1 в дегидро-Рrо, предпочтительно в 3,4-дегидро-Рrо. Дополнительные предпочтительные пептиды формулы (7а) включают: 4-F-Рhе-3,4-дегидро-Рrо-Ilе-Glу-Тrр-NН2 (SEQ ID NO: 72) и 4-F-Phe-3,4-дегидро-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 55), но не ограничены ими.
Другая группа примеров, подпадающих под объем формулы (7а), включает, но не ограничена ими, дополнительные необязательные преобразования АА2, предпочтительно в Arg, His, гомо-Arg, L-алло-Ilе или канаванин; дополнительные необязательные преобразования R1 и/или R2 (предпочтительно R1), предпочтительно в аминогруппу, карбоксильную группу, нитрогруппу или фосфоновую группу (предпочтительно в виде фосфон-Тrу); дополнительные необязательные преобразования гетероциклического азотсодержащего кольца Pro1, предпочтительно с помощью цис- или транс-4-ОН или гомо-Рrо. Также предпочтительными пептидами формулы (7а) являются 4-NH2-Phe-цис- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 63); 4-F-Рhе-цис- или -тpaнс-4-OH-Pro-His-Gly-Trp-NH2 (SEQ ID NO: 64); 4-NO2-Phe-цис- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 65); 4-СН3О-Рhе-цис- или -тpaнс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 59); 4-F-Phe-цис- или -тpaнс-4-OH-Pro-гoмо-Arg-Gly-Trp-NH2 (SEQ ID NO: 71); 4-F-Phe-гoмо-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 69); 4-F-Phe-гoмо-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 57); и 4-F-Рhе-цис- или -транс-4-OH-Pro-L-aлло-Ile-Gly-Trp-NH2 (SEQ ID NO: 73).
Другим примером пентапептидов по изобретению являются композиции пентапептидов с увеличенными внутренней областью и С-концом, представленные формулой (8)
R1-Pro1-АА1-АА2-Gly-АА3-R, (8)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 и АА2 каждый независимо друг от друга обозначает аминокислоту из группы Leu или Ilе; АА3 обозначает аминокислоту Trp; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Примером пентапептидов формулы (8), заявленных для применения при лечении депрессии у пациентов, являются пентапептиды формулы (8а)
Rl-Prol-AAl-AA2-Gly-Trp-NH2, (8а)
где Рrо1, АА1, АА2 и R1 имеют значения, описанные выше для формулы (8).
Предпочтительные композиции пентапептидов формулы (8а) включают: Pro-Ilе-Leu-Gly-Trp-NH2 (SEQ ID NO: 44) и цис- или транс-4-OH-Pro-Ile-Leu-Gly-Trp-NH2 (SEQ ID NO: 45), но не обязательно ограничены ими.
В другом примере выполнения изобретения, включающем добавление как N-концевой аминокислоты, так и С-концевой аминокислоты, композиции пентапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (9):
R1-АА1-R2-Pro1-АА2-Gly-АА3-R, (9)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту Ala; AA2 обозначает аминокислоту, выбранную из группы, включающей Leu, Ile, Arg, D-Arg, Trp или канаванин; АА3 обозначает аминокислоту Trp; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает пиридильное кольцо, предпочтительно в виде такого фрагмента, как 3-(3-пиридил); R2 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Предпочтительной композицией формулы (9), которую не следует рассматривать как ограничивающую, является 3-(3-пиридил)-Аlа-4-ОН-Рrо-Arg-Gly-Trp-NH2 (SEQ ID NO: 70).
В другом примере выполнения изобретения, включающем добавление как N-концевой аминокислоты, так и С-концевой аминокислоты, композиции гексапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (10):
R1-АА1-R2-Pro1-АА2-АА4-Gly-АА3-R, (10)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы Phe или Туr; АА2 обозначает аминокислоту, выбранную из группы, включающей Leu, Ile, Arg, D-Arg, Trp или канаванин; АА3 обозначает аминокислоту Trp; АА4 обозначает аминокислоту Gly или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Группа предпочтительных композиций гексапептидов формулы (10), которые могут применяться по отдельности или в комбинации с другими пептидами, приведенными в описании настоящего изобретения, для лечения пациентов, страдающих депрессией, характеризуется добавлением С-концевой аминокислоты Тrр, необязательным преобразованием гетероциклического азотсодержащего кольца Pro1, предпочтительно с помощью цис- или транс-4-ОН-группы, наличием атома фтора в положении 4 в Phe; предпочтительно Arg в качестве АА2; Тrр в качестве АА3; и Ilе или Gly в качестве АА4; и тем, что С-концевой амид остается непреобразованным. Формулу (10а) изображают в виде
R1-Phe-R2-Pro1-AA2-AA4-Gly-Trp-NH2, (10а)
причем предпочтительные пептиды формулы (10а) включают, но не ограничены ими, 4F-Phe-4-OH-Pro-Arg-Gly-Gly-Trp-NH2 (SEQ ID NO: 58) и 4F-Phe-4-OH-Pro-Arg-Ile-Gly-Trp-NH2 (SEQ ID NO: 67).
В другом примере выполнения изобретения, включающем добавление как N-концевой аминокислоты, так и С-концевой аминокислоты, композиции гептапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (11):
Rl-AAl-R2-Prol-AA2-AA4-AA5-Gly-AA3-R, (11)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, АА1 обозначает аминокислоту, выбранную из группы Phe или Туr; АА2 обозначает аминокислоту, выбранную из группы, включающей Leu, Ile, Arg, D-Arg, Тrр или канаванин; АА3 обозначает аминокислоту Тrр; АА4 и АА5 обозначают аминокислоту Gly или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу, или фосфоновую группу (предпочтительно фосфонтирозин).
Предпочтительная композиция формулы (11) включает 4-F-Phe-4-OH-Pro-Arg-Gly-Ile-Gly-Trp-NH2 (SEQ ID NO: 56), но не ограничена им.
В объеме настоящего изобретения также предполагается, что Gly в формулах с (7) по (11) необязательно может быть замещен на Val или Аlа.
Наиболее предпочтительные композиции по настоящему изобретению содержат малые пептиды, которые проявляют более высокую активность в плавательном тесте Порсольта, представленном в данном описании. Эти малые пептиды могут иметь различную длину, причем предпочтительными пептидами являются тетрапептиды, пентапептиды, гексапептиды и гептапептиды. Формула этих наиболее предпочтительных пептидов, приведенных в данном описании, может быть представлена в виде
R1-Phe-Pro1-AA2-AA3-NH2
для тетрапептида, в котором R1 предпочтительно обозначает атом галогена, наиболее предпочтительно атом фтора или хлора, карбоксильную группу, аминогруппу или нитрогруппу, причем все преобразования предпочтительно касаются атома С4 в Phe; Pro1 обозначает расположенные в порядке уменьшения предпочтительности 3,4-дегидро-Рrо, гомо-Рrо, цис- или транс-4-ОН-Рrо или Pro; АА2 предпочтительно обозначает Ilе, Leu или Arg; и АА3 предпочтительно обозначает Gly или Тrр.
Другим предпочтительным тетрапептидом по настоящему изобретению является Pro-Ile-Gly-Trp (SEQ ID NO: 3).
Формула наиболее предпочтительных пентапептидов, гексапептидов и гептапептидов, также приведенных в данном описании, может быть представлена в виде
R1-Phe-Pro1-AA2-Gly-AA(n)-AA3-NH2
где R1 предпочтительно обозначает атом галогена, предпочтительно атом фтора или хлора, карбоксильную группу, аминогруппу или нитрогруппу, причем все преобразования предпочтительно касаются атома С4 в Phe; Pro1 обозначает расположенные в порядке уменьшения предпочтительности 3,4-дегидро-Рrо, гомо-Рrо, цис- или транс-4-ОН-Рrо или Pro; АА2 предпочтительно обозначает Arg, Ile, Leu или His, причем Arg является наиболее предпочтительным; AA(n) обозначает 0-2 аминокислотных остатка, если n=1, то предпочтительным аминокислотным остатком является Gly, а если n=2, то предпочтительны Ilе-Gly, Ile-Ile или Gly-Gly; и АА3 предпочтительно обозначает Тrр или Gly, причем Тrр является наиболее предпочтительным.
Настоящее изобретение, кроме того, относится к химическим комбинациям полипептидов и/или частично совпадающим химическим комбинациям любых пептидов, представленных формулами от (1) до (11), предназначенных для применения при лечении депрессии у пациентов. Эти химически объединенные полипептиды предпочтительно имеют по крайней мере от приблизительно трех до по крайней мере приблизительно десяти модифицированных и/или немодифицированных аминокислот.
Настоящее изобретение также относится к смесям пептидов, представленных формулами от (1) до (11), с известными антидепрессивными соединениями, такими как амитриптилин, флуоксетин (Prozac) и сертралин (Zoloft). Для специалиста в данной области техники очевидно, каким образом создать различные смеси с малыми пептидами по настоящему изобретению дополнительно к таковым, приведенным в примерах в настоящем описании.
Малые пептиды по настоящему изобретению могут быть представлены в виде композиций с пригодным фармацевтическим носителем для введения in vivo пациенту с помощью стандартного метода, известного в данной области техники так, чтобы фармакологически эффективная концентрация достигала места действия. Пригодные пути введения включают оральный (введение через рот или перорально), подъязычный, парентеральный (например, внутривенный, интраспинальный, интратекальный, интравентрикулярный, эпидермальный, интрацистернальный, внутрикожный или интрадермальный, подкожный или внутримышечный), надкожный или трансдермальный, интраназальный или ректальный, а также ингаляционный (с использованием поли- или микродисперсного аэрозоля), но неограничены ими.
Перечисленные ниже термины, используемые в настоящем описании, имеют следующие значения.
Pro - L-пролин; Leu - L-лейцин; Gly - L-глицин; Туr - L-тирозин; Ala - L-аланин; Arg - L-аргинин; Lys - L-лизин; Phe - L-фенилаланин; Trp - L-триптофан; Ile - L-изолейцин; Orn - L-орнитин; D-Arg - D-аргинин; D-Leu - D-лейцин; 3,4-дегидро-Рrо - 3,4-дегидро-L-пролин; пиро-Glu - пироглутаминовая кислота; Sar - L-саркозин (N-метилглицин); 4-ОН-Pro - 4-гидроксипролин; 4-тио-Рrо - 4-тиопролин; 2-F-Phe - 2-фторфенилаланин; 3-F-Phe - 3-фторфенилаланин; 4-F-Phe - 4-фторфенилаланин; 4-Cl-Phe - 4-хлорфенилаланин; 4-NH2-Phe - 4-аминофенилаланин; 3-(3-пиридил)-Аlа - 3-(3-пиридил)аланин; гомо-Arg - гомо-аргинин; гомо-Рrо - гомо-пролин; ФМОК - 9-флуоренилметоксикарбонил; ТФУ - трифторуксусная кислота; карбоксил - группа карбоновой кислоты или -СО2Н; гидроксиалкил - спиртовая группа или -ROH, где R обозначает группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; карбамил - 1o амидная группа или -CONH2; алкилкарбамил - 2o или 3o алкилированная амидная группа или -CONR1R2, где каждый R1 и R2 независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; алкоксикарбонил - сложноэфирная группа или -CO2R, где R обозначает группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; дегидро - ангидрогруппа, в которой удалены один или несколько атомов водорода; гидроксил - спиртовая группа или -ОН или -ROH, где R обозначает группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; сульфгидрил - тиольная группа -SH или -RSH, где R обозначает группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; алкиламино - -NHR, где R обозначает группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; диалкиламино - -NR2, где R обозначает группу низшего алкила, предпочтительно имеющего 1-3 атома углерода; пациент - включает любого представителя царства животных, определение включает людей, но не ограничено ими; и КНГ - контрольная неактивная группа.
На чертежах представлены некоторые примеры предпочтительных композиций малых пептидов по изобретению и их фармакологическая активность в качестве антидепрессантов. Очевидно, что изобретение не ограничено представленными в качестве примеров, показанных на чертежах, и представленными в таблице 1 вариантами выполнения настоящего изобретения, и возможны вариации в объеме нижеприведенной формулы изобретения.
На фиг. 1 показано усредненное количество животных, реагирующих соответствующим образом в плавательном тесте Порсольта на обработку отобранными соединениями, перечисленными под следующими номерами 1-15:
1) 4-F-Phe-3,4-дегидро-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 55);
2) 4-F-Phe-4-OH-Pro-Arg-Gly-Ile-Gly-Trp-NH2 (SEQ ID NO: 56);
3) 4-F-Phe-4-гомо-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 57);
4) Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 3);
5) 4-F-Phe-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 16);
6) Амитриптилин;
7) 4-F-Phe-4-OH-Pro-Arg-Gly-Gly-Trp-NH2 (SEQ ID NO: 58);
8) 4-CH3O-Phe-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 59);
9) 4-Cl-Phe-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 60);
10) 4-F-Phe-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 41);
11) 4-F-Phe-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 43);
12) 4-OH-Pro-Ile-Gly-NH2;
13) Zoloft;
14) Prozac; и
15) Pro-Leu-Gly-NH2.
В указанных примерах пептиды вводили в концентрации 0,1 мг/мл.
На фиг. 2 показана разница между средним временем движения в КНГ и в группах животных, обработанных отобранными соединениями, перечисленными под номерами 1-15, которые указаны выше для фиг.1.
На фиг. 3 показаны средние Z-баллы, вычисленные для времени движения в группах животных, обработанных отобранными соединениями, перечисленными под номерами 1-15, которые указаны выше для фиг.1.
Фрагмент трипептидного гормона, имеющий общую формулу Pro-Leu-Gly-NH2, иначе называемый L-пролил-L-лейцил-глицином, фактором ингибирования меланоцитстимулирующего гормона, фактором, угнетающим высвобождение меланотрофа или MIF, как известно, обладает антидепрессивной активностью. Обычно в литературе MIF описывают как трипептид, имеющий строение Pro-Leu-Gly-NH2 или Pro-Leu-Gly-амид. В настоящем описании MIF, который имеет следующее химическое строение, обозначают как Pro-Leu-Gly-NH2:
Pro-Leu-NHCH2CONH2 или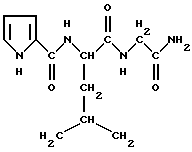
В соответствии с изобретением преобразования трипептидной структуры MIF приводят к получению новых малых пептидов, применяемых для лечения пациентов, страдающих депрессией. Эти преобразования затрагивают остатки с концевой аминогруппой, остатки с концевой карбоксильной группой и остатки внутренних аминокислот и включают присоединение и замещение аминокислотных остатков и преобразование пептидных связей и функциональных боковых групп соответствующих аминокислотных остатков, что более подробно описано ниже.
В целом аминокислота(ы), которую(ые) добавляют или замещают на конце со свободной аминогруппой (на N-конце), на конце со свободной карбоксильной группой (на С-конце) или на внутренних аминокислотных остатках последовательности ядра MIF, для синтеза малых пептидов по изобретению может(гут) быть выбрана(ы) из группы, включающей Ala, Arg, D-Arg, Gly, Ile, Leu, D-Leu, Lys, Orn, Phe, Pro, дегидро-Pro, Sar, Trp и Туr или любую из оставшихся аминокислот. Преобразования карбоксильного конца малых пептидов по изобретению могут включать необязательное замещение карбамильной (амидной) группы на карбоксильном конце последовательности ядра MIF на карбоксильную (кислотную) группу, на гидроксиалкильную (спиртовую) группу, на алкоксикарбонильную (сложноэфирную) группу или на алкилкарбамильную (алкилированную амидную) группу и т. п. Преобразования концевой аминогруппы и внутренние преобразования малых пептидов по изобретению могут включать необязательные добавления или удаления на гетероциклических, ароматических и других углеродных остатках аминокислот алкильной группы, предпочтительно алкильной группы, имеющей 1-3 атома углерода, дегидрогруппы (ангидрогруппы), галоидгруппы, гидроксильной группы, сульфгидрильной группы, алкиламиногруппы или диалкиламиногруппы и т.п. Кроме того, аминогруппы малых пептидов по изобретению могут быть алкилированы, предпочтительно с помощью алкильной группы, имеющей 1-3 атома углерода. Для специалиста в данной области техники очевидно, что эти дополнения, замещения, удаления и/или преобразования могут быть осуществлены обычными методами синтеза полипептидов и органического синтеза.
В настоящем описании подробно изложены данные обширных биологических экспериментов, подкрепляющие следующее положение: заявленные в настоящем описании малые пептиды проявляют выраженную антидепрессивную активность, измеренную на основе плавательного теста Порсольта. Раздел "Пример" содержит сравнительные данные для выбранных в качестве примеров пептидов по настоящему изобретению и известных антидепрессантов амитриптилина, флуоксетина (Prozac) и сертралина (Zoloft), полученные в сериях плавательных тестов Порсольта. Группировка малых пептидов по изобретению в виде приведенных ниже формул сделана только для удобства и не должна рассматриваться как ограничивающая каким-либо образом объем изобретения.
В одном из примеров выполнения изобретения малые пептиды представляют собой трипептиды, характеризующиеся необязательным замещением остатка Leu в последовательности ядра MIF на аминокислоту, выбранную из группы, включающей Trp, Orn, Lys, Arg, D-Arg или Ilе; необязательным замещением остатка Pro на дегидро-Рrо, предпочтительно на 3,4-дегидро-Рrо; необязательным преобразованием амидной группы карбоксильного конца с помощью заместителя, выбранного из карбоксильной группы, гидроксиалкильной группы, предпочтительно гидроксиметильной группы, алкоксикарбонильной группы или алкилированной карбамильной группы; необязательным преобразованием гетероциклической группы или дегидрогетероциклической группы концевой аминогруппы с помощью заместителя, выбранного из группы, включающей группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу; или алкиаминогруппу или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и/или необязательным преобразованием атомов водорода у атомов азота аминокислотных пептидных связей с помощью группы низшего алкила, предпочтительно имеющего 1-3 атома углерода.
Указанная композиция трипептида или его фармацевтически приемлемая соль могут быть представлены следующей формулой (1):
R1-Pro1-АА1-NR2-СН2-R, (1)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту из группы Trp, Orn, Lys, Leu, Arg, D-Arg или Ile; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и R2 обозначает атом водорода или группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, при условии, что если Pro1 обозначает Pro и АА1 обозначает Leu, то оба R1 и R2 не могут обозначать водород, когда R обозначает карбамильную (амидную) группу, поскольку MIF является известным соединением.
В следующих абзацах описаны композиции трипепетидов формулы (1), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Первая группа предпочтительных композиций трипептидов формулы (1), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся замещением Leu и, кроме того, характеризующаяся тем, что N-концевой остаток Pro1 и С-концевая амидная группа остаются непреобразованными, может быть представлена формулой (la). Формулу (1а) изображают в виде
Pro1-AA1-Gly-NH2, (1а)
где Pro1 и АА1 имеют значения, описанные выше для формулы (1). Трипептиды формулы (1а) могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией. Предпочтительными композициями трипептидов формулы (1а) являются Pro-Trp-Gly-NH2; Pro-Arg-Gly-NH2; Pro-D-Arg-Gly-NH2; Pro-Lys-Gly-NH2; Pro-Orn-Gly-NH2 и Pro-Ile-Gly-NH2.
Вторая группа предпочтительных композиций трипептидов формулы (1), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся необязательным замещением Leu и, кроме того, характеризующаяся необязательным преобразованием N-концевого гетероциклического азотсодержащего кольца Pro1, предпочтительно в положении С4 гетероциклического азотсодержащего кольца, предпочтительно путем добавления цис- или транс-гидроксильной группы или цис- или транс-сульфгидрильной группы, и тем, что С-концевая амидная группа остается непреобразованной, может быть представлена формулой (1b). Формулу (1b) изображают в виде
R1-Pro1-AA1-Gly-NH2 (1b)
где Pro1, АА1 и R1 имеют значения, описанные выше для формулы (1).
Предпочтительными композициями трипептидов формулы (1b) являются: цис- или транс-4-OH-Pro-D-Arg-Gly-NH2; цис- или транс-4-OH-Pro-Ile-Gly-NH2; цис- или транс-4-OH-Pro-Arg-Gly-NH2; цис- или транс-4-ОН-Рrо-Тrр-Glу-NН2 и цис- или транс-4-тио-Pro-Leu-Gly-NH2.
Третья группа предпочтительных композиций трипептидов формулы (1), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся необязательным замещением Leu, необязательным преобразованием С-концевой амидной группы, необязательным преобразованием С-концевого атома водорода у азота, входящего в пептидную связь между Leu и Gly, и тем, что N-концевое гетероциклическое азотсодержащее кольцо Pro1 остается непреобразованным, может быть представлена формулой (1с). Формулу (1с) изображают в виде
Prol-AAl-NR2-CH2-R, (1с)
где Pro1, AA1, R и R2 имеют значения, описанные выше для формулы (1), при условии, что, когда Pro1 обозначает Pro и AA1 обозначает Leu, R2 не может обозначать атом водорода, если R обозначает либо карбоксильную группу, либо гидроксиалкильную группу, поскольку эти соединения, т.е. Pro-Leu-NHCH2-СО2Н (или Pro-Leu-Gly) и Pro-Leu-NHCH2-CH2OH, не подпадают под объем настоящего изобретения, а также еще при одном условии, что, когда Pro1 обозначает Pro и AA1 обозначает Trp, R2 не может обозначать атом водорода, если R обозначает гидроксиалкильную группу, так как Pro-Trp-NHCH2-CH2OH является известным соединением. Предпочтительными композициями трипептидов формулы (1с) являются Pro-Leu-N(CH3)CH2-CONH2; и Pro-Trp-NHCH2-CO2H.
В другом примере осуществления изобретения дополнительные трипептиды характеризуются замещением Leu на Arg или на D-Arg; замещением Gly на Аlа; необязательным замещением Pro на дегидро-Рrо, предпочтительно на 3,4-дегидро-Рrо; необязательным преобразованием С-концевой амидной группы с помощью функциональной группы, выбранной из группы, включающей карбоксильную группу, гидроксиалкильную группу, предпочтительно гидроксиметильную группу, алкоксикарбонильную группу, или алкилированную карбамильную группу; необязательным преобразованием N-концевого гетероциклического азотсодержащего кольца Pro1 с помощью заместителя, выбранного из группы, включающей группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу; или алкиламиногруппу или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и/или необязательным преобразованием атомов водорода у атомов азота аминокислотных пептидных связей с помощью группы низшего алкила, предпочтительно имеющего 1-3 атома углерода.
Указанная композиция трипептида или его фармацевтически приемлемая соль могут быть представлены следующей формулой (2):
R1-Pro1-АА1-Ala-R (2)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы Arg или D-Arg; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонил; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции трипептидов формулы (2), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций трипептидов формулы (2), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся замещением Leu и Gly и тем, что N-концевой остаток Pro1 и С-концевой амид остаются непреобразованными, может быть представлена формулой (2а). Формулу (2а) изображают в виде:
Рrо1-АА1-Alа-NН2, (2а)
где Pro1 и АА1 имеют значения, описанные выше для формулы (2).
Предпочтительными композициями трипептидов формулы (2а) являются Pro-Arg-Ala-NH2 и Pro-D-Arg-Ala-NH2.
Еще в одном примере осуществления по изобретению малые трипептиды характеризуются замещением Leu на Оrn; замещением Gly на Туr; необязательным замещением Pro на дегидро-Рrо, предпочтительно на 3,4-дегидро-Рrо; необязательным преобразованием С-концевой амидной группы с помощью заместителя, выбранного из группы, включающей карбоксильную группу, гидроксиалкильную группу, предпочтительно гидроксиметильную группу, алкоксикарбонильную группу, или алкилированную карбамильную группу; необязательным преобразованием N-концевого гетероциклического азотсодержащего кольца Рrо1 с помощью заместителя, выбранного из группы, включающей группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу; или алкиламиногруппу или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и/или необязательным преобразованием атомов водорода у атомов азота аминокислотных пептидных связей с помощью группы низшего алкила, предпочтительно имеющего 1-3 атома углерода.
Указанная композиция трипептида или его фармацевтически приемлемая соль могут быть представлены следующей формулой (3):
R1-Pro1-AA1-Tyr-R, (3)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту Orn; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции трипептидов формулы (3), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций трипептидов формулы (3), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся замещением Leu и Gly, необязательным преобразованием N-концевого гетероциклического азотсодержащего кольца Pro1, и тем, что С-концевой амид остается непреобразованным, может быть представлена формулой (3а). Формулу (3а) изображают в виде
R1-Рrо1-АА1-Туr-NН2, (3а)
где Pro1, АА1 и R1 имеют значения, описанные выше для формулы (3).
Предпочтительными композициями трипептидов формулы (3а) являются Pro-Orn-Tyr-NH2 и цис- или транс-4-OH-Pro-Orn-Tyr-NH2.
Еще в одном примере осуществления изобретения малые пептиды представляют собой трипептиды, которые характеризуются либо добавлением С-концевой аминокислоты Тrр или Туr к Gly или добавлением N-концевой аминокислоты Тrр или Phe к Pro в трипептидах, имеющих последовательность ядра MIF; необязательным замещением Leu на Ilе, Arg, D-Arg или Тrр; необязательным замещением Pro на дегидро-Рrо, предпочтительно на 3,4-дегидро-Рrо; необязательным преобразованием С-концевого амида с помощью заместителя, выбранного из группы, включающей карбоксильную группу, гидроксиалкильную группу, предпочтительно гидроксиметильную группу, алкоксикарбонильную группу, или алкилированную карбамильную группу; необязательным преобразованием гетероциклических азотсодержащих колец Pro1 и Тrр и необязательным преобразованием ароматического кольца Phe с помощью заместителя, выбранного из группы, включающей группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламиногруппу или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и/или необязательным преобразованием атомов водорода у атомов азота аминокислотных пептидных связей с помощью группы низшего алкила, предпочтительно имеющего 1-3 атома углерода.
В одном из примеров осуществления, включающем добавление С-концевой аминокислоты, композиции тетрапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (4):
R1-Pro1-АА1-Gly-АА2-R, (4)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает Ilе, Leu, Arg, D-Arg или Тrр; АА2 обозначает Тrр или Туr; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, дегидрогруппу, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции тетрапептидов формулы (4), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций тетрапептидов формулы (4), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением Тrр или Туr к С-концевому Gly, необязательным замещением Leu, необязательным преобразованием N-концевого гетероциклического азотсодержащего кольца Pro1 и тем, что С-концевой амид остается непреобразованным, может быть представлена формулой (4а). Формулу (4а) изображают в виде
R1-Pro1-АА1-Gly-АА2-NН2 (4a)
где Pro1, АА1, АА2 и R1 имеют значения, описанные выше для формулы (4).
Предпочтительными композициями тетрапептидов формулы (4a) являются
цис- или транс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 1);
цис- или транс-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 2);
цис- или транс-4-OH-Pro-D-Arg-Gly-Trp-NH2 и
3,4-дегидрo-Pro-D-Arg-Gly-Trp-NH2.
Другой предпочтительной композицией тетрапептида формулы (4a) является 3,4-дегидрo-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 62).
Вторая группа предпочтительных композиций тетрапептидов формулы (4), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением Тrр или Туr к С-концевому Gly, необязательным замещением Leu и тем, что N-концевое гетероциклическое азотсодержащее кольцо Pro1 остается непреобразованным, может быть представлена формулой (4b). Формулу (4b) изображают в виде
Pro1-АА1-Gly-АА2-NН2 (4b)
где Pro1, АA1 и АА2 имеют значения, описанные выше для формулы (4).
Предпочтительными композициями тетрапептидов формулы (4b) являются:
Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 3);
3,4-дегидрo-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 4);
Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 5);
Pro-Leu-Gly-Tyr-NH2 (SEQ ID NO: 6);
Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 7);
Pro-Trp-Gly-Trp-NH2 (SEQ ID NO: 8);
Pro-D-Arg-Gly-Trp-NH2 и
Pro-Ile-Gly-Tyr-NH2 (SEQ ID NO: 9).
В другом примере осуществления, включающем добавление N-концевой аминокислоты, композиции тетрапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (5):
R1-АА1-R2-Pro1-АА2-Gly-R, (5)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы Тrр, Туr или Phe; АА2 обозначает аминокислоту, выбранную из группы Leu, Ilе или Тrр; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, сульфгидрильную группу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции тетрапептидов формулы (5), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций тетрапептидов формулы (5), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением Тrр, Туr или Phe к N-концевому Pro1, необязательным замещением Leu, необязательным преобразованием гетероциклических азотсодержащих колец Pro1 и Тrр, и необязательным преобразованием ароматического кольца Phe и Туr и тем, что С-концевой амид остается непреобразованным, может быть представлена формулой (5а). Формулу (5а) изображают в виде
Rl-AAl-R2-Prol-AA2-Gly-NH2, (5а)
где Pro1, АА1, АА2, R1 и R2 имеют значения, описанные выше для формулы (5), при условии, что, если Pro1 обозначает Pro, оба R1 и R2 не могут обозначать атом водорода, когда АА1 обозначает Туr и АА2 обозначает Тrр, поскольку Туr-Pro-Trp-Gly-NH2 является известным соединением, а также еще при одном условии, что, если Pro1 обозначает Pro и АА2 обозначает Leu, оба R1 и R2 не могут обозначать атом водорода, когда АА1 обозначает Phe или Туr, поскольку Phe-MIF-1 и Tyr-MIF-1 являются известными соединениями. Предпочтительными композициями тетрапептидов формулы (5а) являются:
Trp-Pro-Leu-Gly-NH2 (SEQ ID NO: 10);
Phe-Pro-Leu-Gly-NH2 (SEQ ID NO: 11);
4-F-Phe-Pro-Leu-Gly-NH2 (SEQ ID NO: 12);
4-Cl-Phe-Pro-Leu-Gly-NH2 (SEQ ID NO: 13);
4-F-Phe-Pro-Ile-Gly-NH2 (SEQ ID NO: 14);
4-F-Phе-цис- или -транс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 15);
4-F-Рhе-цис- или -транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 16);
Trp-Pro-Leu-Gly-NH2 (SEQ ID NO: 17);
Trp-Pro-Ile-Gly-NH2 (SEQ ID NO: 18);
Тrр-цис- или -транс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 19); и
Тrр-цис- или -транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 20).
Дополнительной предпочтительной композицией тетрапептида формулы (5а) является 4-Сl-Рhе-цис- или -транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 60).
Еще в одном примере осуществления изобретения пептиды представляют собой пентапептиды, для которых характерно либо добавление двух N-концевых аминокислот Phe, Туr, Leu или Ilе к Pro1, добавление N-концевой аминокислоты Phe или Туr к Pro1 и добавление С-концевой аминокислоты Тrр к Gly, либо добавление С-концевой аминокислоты Тrр к Gly и внутренней аминокислоты между Pro и Gly, в трипептидах, имеющих последовательность ядра MIF; необязательное замещение Leu на Ilе или Тrр; необязательное замещение Pro на дегидро-Рrо, предпочтительно на 3,4-дегидро-Рrо; необязательное преобразование С-концевого амида с помощью заместителя, выбранного из группы, включающей карбоксильную группу, гидроксиалкильную группу, предпочтительно гидроксиметильную группу, алкоксикарбонильную группу, или алкилированную карбамильную группу; необязательное преобразование гетероциклического азотсодержащего кольца Pro1 и необязательное преобразование ароматических колец Туr или Phe с помощью заместителя, выбранного из группы, включающей группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу или алкиламиногруплу или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу; и/или необязательное преобразование атомов водорода у атомов азота аминокислотных пептидных связей с помощью группы низшего алкила, предпочтительно имеющего 1-3 атома углерода.
В одном из примеров осуществления, включающем добавление двух N-концевых аминокислот, композиции пентапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (6):
R1-АА1-AA2-R2-Pro1-АА3-Gly-R, (6)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; каждый АА1 и АА2 независимо друг от друга обозначает аминокислоту, выбранную из группы Phe или Туr; АА3 обозначает аминокислоту, выбранную из группы Leu или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции пентапептидов формулы (6), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций пентапептидов формулы (6), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением двух N-концевых аминокислот Phe и Туr к Pro1, необязательным преобразованием гетероциклического азотсодержащего кольца Pro1 и необязательным преобразованием ароматических колец Phe или Туr, необязательным замещением Leu и тем, что С-концевой амид Gly остается непреобразованным, может быть представлена формулой (6а). Формулу (6а) изображают в виде
R1-AA1-AA2-R2-Pro1-AA3-Gly-NH2, (6а)
где Pro1, AA1, АА2, R1 и R2 имеют значения, описанные выше для формулы (6).
Предпочтительными пентапептидами формулы (6а) являются:
4-F-Phe-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 21);
4-Cl-Phe-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 22);
Phe-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 23);
Phe-Tyr-Pro-Ile-Gly-NH2 (SEQ ID NO: 24);
Phe-Tyr-цис- или -транс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 25);
Phe-Tyr-цис- или -транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 26);
Tyr-Tyr-Pro-Leu-Gly-NH2 (SEQ ID NO: 27);
Tyr-Tyr-Pro-Ile-Gly-NH2 (SEQ ID NO: 28);
Tyr-Tyr-цис- или -транс-4-OH-Pro-Leu-Gly-NH2 (SEQ ID NO: 29); и
Туr-Туг-цис- или -транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 30).
В другом примере осуществления изобретения, включающем добавление как N-концевой аминокислоты, так и С-концевой аминокислоты, композиции пентапептидов или их фармацевтически приемлемые соли могут быть представлены формулой (7)
R1-АА1-R2-Pro1-АА2-Gly-АА3-R, (7)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту, выбранную из группы Phe или Туr; АА2 обозначает аминокислоту, выбранную из группы Leu, Ile, Arg, D-Arg или Trp; AA3 обозначает аминокислоту Trp; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции пентапептидов формулы (7), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций пентапептидов формулы (7), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением N-концевой аминокислоты Рhе или Туr к Pro1, добавлением С-концевой аминокислоты Trp к Gly, необязательным преобразованием гетероциклического азотсодержащего кольца Pro и необязательным преобразованием ароматических колец Рhе или Туr, необязательным замещением Leu на Ilе, Arg, D-Arg или Trp и тем, что С-концевой амид остается непреобразованным, может быть представлена формулой 7(а). Формулу 7(а) изображают в виде
Rl-AAl-R2-Prol-AA2-Gly-Trp-NH2, (7a)
где Pro1, AA1, AA2, R1 и R2 имеют значения, описанные выше для формулы (7).
Предпочтительными пентапептидами формулы (7a) являются:
Phe-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 31);
Tyr-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 32);
Phe-цис- или -транс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 33);
Phe-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 34);
Phe-цис- или -транс-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 35);
Туr-цис- или -транс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 36);
Tyr-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 37);
Туr-цис- или -транс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 38);
Tyr-Pro-Trp-Gly-Trp-NH2 (SEQ ID NO: 39);
Туr-цис- или -транс-4-OH-Pro-Trp-Gly-Trp-NH2 (SEQ ID NO: 40);
4-F-Рhе-цис- или -транс-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 41);
4-F-Phe-цис- или -транс-4-OH-Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 42);
4-F-Рhе-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 43) и
4-F-Рhе-цис- или -транс-4-OH-Pro-D-Arg-Gly-Trp-NH2.
Дополнительный пример осуществления включает предпочтительные пентапептиды формулы (7а):
3-F-Рhе-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 66);
2-F-Рhе-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 68);
4-Сl-Рhе-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 61), но не ограничен только ими.
Дополнительная группа предпочтительных композиций пентпапептидов формулы (7а) характеризуется необязательным преобразованием Pro1 в дегидро-Рrо, предпочтительно в 3,4-дегидро-Рrо. Дополнительные предпочтительные пептиды формулы (7а) включают: 4-F-Рhе-3,4-дегидро-Рrо-Ile-Gly-Trp-NH2 (SEQ ID NO: 72); и 4-F-Phe-3,4-дегидро-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 55), но не ограничены ими.
Другая группа примеров осуществления, подпадающих под объем формулы (7а), включает, но не ограничена только ими, другие дополнительные необязательные преобразования АА2 предпочтительно в Arg, His, гомо-Arg, L-алло-Ile или канаванин; другие дополнительные необязательные преобразования R1 и/или R2 (предпочтительно R1) и предпочтительно в аминогруппу, карбоксильную группу, нитрогруппу или фосфоновую группу (предпочтительно в фосфон-Туr); дополнительные необязательные преобразования гетероциклического азотсодержащего кольца Pro1 предпочтительно с помощью цис- или транс-4-ОН или гомо-Рrо. Дополнительными предпочтительными пептидами формулы (7а) являются:
4-NН2-Рhе-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 63);
4-F-Рhе-цис- или -транс-4-ОН-Pro-His-Gly-Trp-NH2 (SEQ ID NO: 64);
4-NO2-Phe-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 65);
4-СН3О-Рhе-цис- или -транс-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 59);
4-F-Рhе-цис- или -транс-4-OH-Pro-гомо-Arg-Gly-Trp-NH2 (SEQ ID NO: 71);
4-F-Phe-гомо-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 69);
4-F-Phe-гомо-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 57); и
4-F-Рhе-цис- или -транс-4-OH-Pro-L-aллo-Ile-Gly-Trp-NH2 (SEQ ID NO: 73).
В еще одном примере осуществления изобретения, включающем добавление С-концевой аминокислоты и внутренней аминокислоты, композиции пентапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (8):
R1-Pro1-АА1-АА2-Gly-АА3-R, (8)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 и АА2 каждый независимо друг от друга обозначает аминокислоту из группы Leu или Ilе; АА3 обозначает Trp; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
В следующем абзаце описаны композиции пентапептидов формулы (8), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией.
Группа предпочтительных композиций пентапептидов формулы (8), которые могут применяться по отдельности или в сочетании с другими пептидами, приведенными в данном описании, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением С-концевой аминокислоты Тrр к Gly, добавлением внутренней аминоксилоты Leu или Ilе между Pro1 и Gly, необязательным преобразованием гетероциклического азотсодержащего кольца Pro1, необязательным замещением Leu на Ilе и тем, что С-концевой амид остается непреобразованным, может быть представлена формулой (8а). Формулу (8а) изображают в виде
Rl-Prol-AAl-AA2-Gly-Trp-NH2, (8a)
где Pro1, АА1, АА2 и R1 имеют значения, описанные выше для формулы (8).
Предпочтительными пентапептидами формулы (8a) являются Pro-Ile-Leu-Gly-Trp-NH2 (SEQ ID NO: 44) и цис- или транс-4-OH-Pro-Ile-Leu-Gly-Trp-NH2 (SEQ ID NO: 45).
В другом примере осуществления изобретения, включающем добавление как N-концевой аминокислоты, так и С-концевой аминокислоты, композиции пентапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (9):
R1-АА1-R2-Pro1-АА2-Gly-АА3-R, (9)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, предпочтительно 3,4-дегидро-Рrо; АА1 обозначает аминокислоту Аlа; АА2 обозначает аминокислоту, выбранную из группы, содержащей Leu, Ile, Arg, D-Arg, Trp или канаванин; АА3 обозначает аминокислоту Тrр; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 обозначает пиридильное кольцо, предпочтительно в виде такого фрагмента, как 3-(3-пиридил); R2 обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Предпочтительная композиция формулы (9), включает 3-(3-пиридил)-Аlа-4-ОН-Рrо-Arg-Glу-Тrр-NН2 (SEQ ID NO: 70), но не ограничена им.
В другом примере осуществления изобретения, включающем добавление как N-концевой аминоксилоты, так и С-концевой аминокислоты, композиции гексапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (10):
R1-АА1-R2-Pro1-АА2-АА4-Gly-АА3-R, (10)
где Pro1 обозначает аминокислоту Pro или дегидро-Рго, АА1 обозначает аминокислоту, выбранную из группы, включающей Рhе или Туr; АА2 обозначает аминокислоту, выбранную из группы, включающей Leu, Ile, Arg, D-Arg, Тrр или канаванин; АА3 обозначает аминокислоту Тrр; АА4 обозначает аминокислоту Gly или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу.
Группа предпочтительных композиций гексапептидов формулы (10), которые могут применяться по отдельности или в комбинации с другими пептидами, приведенными в данном описании изобретения, для лечения пациентов, страдающих депрессией, характеризующаяся добавлением С-концевой аминокислоты Тrр, необязательным преобразованием гетероциклического азотсодержащего кольца Pro1, предпочтительно с помощью цис- или транс-4-ОН-группы, наличием атома фтора в положении 4 в Phe; предпочтительно Arg в качестве АА2; Тrр в качестве АА3; и Ilе или Gly в качестве АА4; и тем, что С-концевой амид остается непреобразованным, может быть представлена формулой (10а). Формулу (10а) изображают в виде:
R1-Phe-R2-Pro1-AA2-AA4-Gly-Trp-NH2, (10a)
причем предпочтительными пептидами формулы (10a) являются 4F-Phe-4-OH-Pro-Arg-Gly-Gly-Trp-NH2 (SEQ ID NO: 58) и 4F-Phe-4-OH-Pro-Arg-ILe-Gly-Trp-NH2 (SEQ ID NO: 67).
В другом примере осуществления изобретения, включающем добавление как N-концевой аминокислоты, так и С-концевой аминокислоты, композиции гептапептидов или их фармацевтически приемлемые соли могут быть представлены следующей формулой (11):
R1-AA1-R2-Pro1-AA2-AA4-AA5-Gly-AA3-R, (11)
где Pro1 обозначает аминокислоту Pro или дегидро-Рrо, AA1 обозначает аминокислоту, выбранную из группы, включающей Phe или Туr; AA2 обозначает аминокислоту, выбранную из группы, включающей Leu, Ile, Arg, D-Arg, Trp или канаванин; AA3 обозначает аминокислоту Тrр; AA4 и AA5 обозначают аминокислоту Gly или Ilе; R обозначает карбоксильную группу, гидроксиалкильную группу, карбамильную группу, алкилкарбамильную группу или алкоксикарбонильную группу; и R1 и R2 каждый независимо друг от друга обозначает атом водорода, группу низшего алкила, предпочтительно имеющего 1-3 атома углерода, атом галогена, предпочтительно атом фтора или хлора, гидроксильную группу, предпочтительно цис- или транс-4-ОН-группу, сульфгидрильную группу, предпочтительно цис- или транс-4-тиогруппу, или алкиламино- или диалкиламиногруппу, предпочтительно метил- или этиламиногруппу, или диметил- или диэтиламиногруппу, или фосфоновую группу (предпочтительно фосфон-Туr).
Предпочтительной композицией формулы (11) является 4-F-Phe-4-OH-Pro-Arg-Gly-Ile-Gly-Trp-NH2 (SEQ ID NO: 56).
В соответствии с изобретением также предполагается, что Gly в формулах с (7) по (11) необязательно может быть замещен на Val или Аlа.
В еще одном примере осуществления изобретения пептиды представляют собой полипептиды, включающие химические комбинации и/или частично совпадающие химические комбинации любого из малых пептидов любой из описанных выше формул с (1) по (11), которые могут применяться по отдельности или в комбинации с другими пептидами, приведенными в данном описании изобретения, для лечения пациентов, страдающих депрессией. Заявленные химические комбинации и/или частично совпадающие химические комбинации пептидов предпочтительно содержат от по крайней мере приблизительно трех до по крайней мере приблизительно десяти аминокислот. Примеры таких комбинаций включают, но не обязательно ограничены ими, следующие композиции: 4-F-Phе-цис или -транс-4-ОН-Рrо-Ilе-Glу-Тrр-Glу-NН2 (SEQ ID NO: 46); 4-F-Phe-цис или -транс-4-ОН-Рrо-Ilе-Glу-Тrр-Glу-Тrр-NН2 (SEQ ID NO: 47); 4-F-Рhе-цис или -транс-4-OH-Pro-Leu-Gly-Trp-Gly-NH2 (SEQ ID NO: 48); 4-F-Phe-цис или -транс-4-OH-Pro-Leu-Gly-Trp-Gly-Trp-NH2 (SEQ ID NO: 49); Pro-Ile-Gly-Trp-Pro-Ile-Gly-NH2 (SEQ ID NO: 50); 4-F-Рhе-цис или -транс-4-OH-Pro-Arg-Gly-Trp-Gly-NH2 (SEQ ID NO: 51); 4-F-Рhе-цис или -транс-4-OH-Pro-Arg-Gly-Trp-Gly-Trp-NH2 (SEQ ID NO: 52); цис- или транс-4-ОН-Рrо-Ilе-Glу-цис или транс-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 53); 3,4-дeгидpo-Pro-D-Arg-Gly-3,4-дeгидpo-Pro-D-Arg-Gly-NH2; 3,4-дeгидpo-Pro-D-Arg-Gly-Trp-Gly-NH2; и 3,4-дeгидpo-Pro-D-Arg-Gly-Trp-Gly-Trp-NH2.
Наиболее предпочтительные композиции по настоящему изобретению содержат малые пептиды, которые проявляют более высокую активность в плавательном тесте Порсольта, представленном в данном описании. Эти малые пептиды могут иметь различную длину, причем предпочтительными пептидами являются тетрапептиды, пентапептиды, гексапептиды и гептапептиды. Формула этих наиболее предпочтительных пептидов, приведенных в данном описании, может быть представлена в виде
R1-Phe-Pro1-AA2-AA3-NH2,
для тетрапептида, в котором R1 предпочтительно обозначает атом галогена, наиболее предпочтительно атом фтора или хлора, карбоксильную группу, аминогруппу или нитрогруппу, причем все преобразования предпочтительно касаются атома С4 Phe; Pro обозначает расположенные в порядке уменьшения предпочтительности 3,4-дегидро-Рrо, гомо-Рrо, цис- или транс-4-OH-Pro или Pro; AA2 предпочтительно обозначает Ilе, Leu или Arg; и АА3 предпочтительно обозначает Gly или Тrр.
Другим предпочтительным тетрапептидом по настоящему изобретению является Pro-Ile-Gly-Trp (SEQ ID NO: 3).
Формула наиболее предпочтительных пентапептидов, гексапептидов и гептапептидов, также приведенных в данном описании, может быть представлена в виде
R1-Phe-Pro1-AA2-Gly-AA(n)-AA3-NH2
где R1 предпочтительно обозначает атом галогена, предпочтительно атом фтора или хлора, карбоксильную группу, аминогруппу или нитрогруппу, причем все преобразования предпочтительно касаются атома С4 Phe; Pro обозначает расположенные в порядке уменьшения предпочтительности 3,4-дегидро-Рrо, гомо-Рrо, цис- или транс-4-OH-Pro или Pro; AA2 предпочтительно обозначает Arg, Ile, Leu или His, причем Arg является наиболее предпочтительным; АА(n) обозначает 0-2 аминокислотных остатка, если n=1, то предпочтительным аминокислотным остатком является Gly, а если n=2, то предпочтительны Ilе-Gly, Ile-Ile или Gly-Gly; и АА3 предпочтительно обозначает Тrр или Gly, причем Тrр является наиболее предпочтительным.
Настоящее изобретение также относится к смесям пептидов, представленных формулами от (1) до (11), с известными антидепрессивными соединениями, такими как амитриптилин, флуоксетин (Prozac) и сертралин (Zoloft). Для специалиста в данной области техники очевидно, каким образом создать различные смеси с малыми пептидами по настоящему изобретению дополнительно к таковым, приведенным в примерах в настоящем описании.
Малые пептиды, к которым относится настоящее изобретение, легко получают обычными методами многоступенчатого синтеза полипептидов (т.е. карбодиимидным методом, смешанным ангидридным методом, N,N-карбонилдиимидазольным методом), а также с помощью твердофазного синтеза пептидов. Замещающие группы также легко добавляют к полипептидным остаткам обычными способами.
Малые пептиды по изобретнию обладают антидепрессивной активностью, что установлено с помощью плавательного теста Порсольта, описанного в разделе "Пример." Плавательный тест Порсольта основан на наблюдении, что, когда крысу заставляют плавать в ситуации, из которой нет выхода, крыса полностью прекращает двигаться и делает только движения, необходимые для того, чтобы держать голову над водой. Неподвижность свидетельствует о состоянии депрессии. Следовательно, соединение, проявляющее антидепрессивную активность, должно задерживать начало вышеуказанной стадии неподвижности.
Действующее вещество, которое может содержать один или несколько пептидов, описанных в настоящем изобретении, может быть представлена в виде композиции с пригодным фармацевтическим носителем для введения in vivo пациенту с помощью любого стандартного метода, известного в данной области техники. Пригодные пути введения включают оральный (введение через рот или перорально), подъязычный, парентеральный (например, внутривенный, интраспинальный, интратекальный, интравентрикулярный, эпидермальный, интрацистернальный, внутрикожный или интрадермальный, подкожный или внутримышечный), надкожный или трансдермальный, интраназальный или ректальный, а также ингаляционный (с использованием поли- или микродисперсного аэрозоля), но неограничены ими.
С позиции других фармацевтических стратегий доставки действующего вещества первичная дозируемая форма зависит от способа введения. Оральное введение включает применение таблеток, капсул, растворов, суспензий, гелей, порошков, эликсиров или сиропов, но не ограничено ими. Подъязычное введение включает применение таблеток или лепешек, но не ограничено ими. Парентеральное введение включает применение растворов или суспензий, но не ограничено ими. Надкожные или трансдермальные аппликации включают применение мазей, кремов, паст, пластырей, порошков, аэрозолей, лосьонов, трансдермальных бляшек, дисков и растворов, но не ограничено ими. Интраназальное введение пептида или пептидов по настоящему изобретению включает применение растворов, распыляемых растворов, ингалянтов или мазей, но не ограничено ими. Ректальное введение может включать применение растворов, мазей или суппозиториев, но не обязательно ограничено ими. Действующее вещество также может быть представлено в форме для включения в липосомы, микрокапсулы, полимерную или восковую основу и в препараты с контролируемым высвобождением. Для получения дополнительных сведений, касающихся способов введения и достижения норм фармацевтически эффективных доз, см. главу 3 в "Dosage Form Design: Biopharmaceutical Considerations" в Pharmaceutical Dosage Forms and Drug Delivery Systems, 1990, Ansel, H.C. и Popovich, N.G. пятое издание; ред. Lea и Febiger, Филадельфия.
Концентрации пептида(ов), применяемые в любой из вышеперечисленных композиций, будут зависеть от эффективной дозы и способа введения, использованного для усиления соответствующего биологического действия. Доза должна быть достаточной для достижения таких концентраций действующего вещества в плазме кровеносной системы, чтобы эффективные количества, преодолевшие гематоэнцефалический барьер, оказались действенными. Например, когда действующим веществом является тетрапептид Рrо-Leu-Gly-Trp-NH2, его содержание в плазме кровеносной системы для среднего взрослого человека должно составлять от приблизительно 30 мг до приблизительно 90 мг; для среднего взрослого человека предпочтительно содержание приблизительно 60 мг. Эффективные дозы при различных путях введения могут быть выведены на основе кривых доза - эффект, полученных in vitro или с использованием животных в качестве модельных тест-систем.
Ниже изобретение дополнительно поясняется на примерах, представляющих собой только пример синтеза и применения малых пептидов по изобретнию.
ПРИМЕР: Три-, тетра- или пентапептид в качестве антидепрессанта
Материалы и методы
Синтез пептидов
Малые пептиды по настоящему изобретнию синтезировали с использованием методов, известных специалисту в данной области техники. Коротко говоря, 5 мМ амидную смолу Ринка помещают в реакционный сосуд пептидного синтезатора модели Applied Biosystem 431A. Применяли циклы двойного связывания, поскольку количество исходной смолы в два раза превышало таковое для стандартного режима. Осуществляли следующие стадии: (1) сначала при помощи промывания 20%-ным пиперидином удаляли группу, блокирующую ФМОК на смоле; (2) затем смолу промывали N-метилпирролидиноном; (3) в реакционнй сосуд добавляли 2 мМ ФМОК-пролин вместе с 0,45 мМ гексафторфосфатом 2-(1Н-бензтриазол-1-ил)-1,1,3,3-тетраметилурония в растворе 1-гидроксибензтриазола и 1 мМ диизопропилэтиламином; (4) смолу промывали N-метилпирролидиноном; (5) повторяли цикл с ФМОК-лейцином, затем с ФМОК-глицином и в завершение с ФМОК-триптофаном; (6) пептидную связь смолы расщепляли следующим раствором: 0,25 мл этандитиола, 0,25 мл Н2О и 9,5 мл ТФУ, время расщепления составляло 3-4 часа; (7) затем пептид очищали с использованием двух процедур жидкостной хроматографии высокого разрешения (ЖХВР) с обращенной фазой, в первой из которых в качестве элюирующего раствора использовали 0,1%-ную ТФУ в воде, а во второй в качестве элюирующего раствора использовали 0,1%-ную ТФУ в ацетонитриле.
Чистоту синтезированных пептидов анализировали с помощью аналитической ЖХВР с использованием хроматографа типа HP1090L, снабженного диодным лучом. Получали график, показывающий на основе хода УФ-луча адсорбцию пептида в диапазоне от 220 нм до 310 нм. Молекулярные массы определяли с помощью масс-спектрометрии.
Синтез Pro-Are-Glv-NH2
Pro-Arg-Gly-NH2 синтезировали вручную с использованием фриттованной воронки и с последовательностью стадий, указанной для синтеза Pro-Leu-Gly-Trp-NH2 (SEQ ID NO: 5), и с применением соответствующих ФМОК-аминокислот. При синтезе Pro-Arg-Gly-NH2 вместо N-метилпирролидинона использовали диметилформамид и на стадии (6) пептидную связь смолы расщепляли с помощью следующей смеси растворителей: 0,75 г фенола в 0,25 мл тиоанизола, 0,5 мл Н2О и 10 мл ТФУ.
Другие пептиды, представленные в данном описании, кроме трипептида Pro-Arg-Gly-NH2, получали как описано выше.
Специалистам в данной области техники известны любые разнообразные методы, которые можно применять для синтеза пептидов по настоящему изобретению.
Каждый очищенный пептид хранили в замороженном состоянии в виде белого кристаллического порошка. MIF также синтезировали с использованием методов, известных специалистам в данной области техники. Этот трипептид хранили в замороженном состоянии в виде белого кристаллического порошка.
Модификация плавательного теста Порсольта для выявления пептидов с антидепрессивной активностью
Самцов крыс линии Sprague Dawley получали из лаборатории Charles River, Уилмингтон, Миннесота. Крыс размещали по отдельности в клетках из проволоки из нержавеющей стали с размером ячеек в полдюйма, изготовленных в соответствии с "Руководством по содержанию и использованию лабораторных животных" Institute of Laboratory Animals Resources National Research and Counsel. Световой режим в помещениях для животных составлял 12 часов световой фазы/ 12 часов темновой фазы, температуру поддерживали на уровне 18-26oС и относительную влажность на уровне 40-70%. Подопытных животных подвергали акклиматизации в течение минимум 7 дней до начала исследования. Суточные дозы малых пептидов по настоящему изобретению получали путем растворения 1 мг q.s. до 10,0 мл следующего состава: 0,01 М уксусная кислота в 0,9%-ном физиологическом растворе. Затем путем внутрибрюшинной инъекции один раз в день в течение пяти дней подряд вводили соответствующий пептид из расчета 1 мг/кг.
Антидепрессивную активность пептидов по настоящему изобретению определяли путем модифицированного плавательного теста Порсольта (Porsolt и др., 1977, Nature 266: 730-732). Метод основан на том наблюдении, что, когда крысу заставляют плавать в ситуации, из которой нет выхода, она после начального периода интенсивной активности полностью прекращает двигаться и делает только движения, необходимые для того, чтобы держать голову над водой. Неподвижность свидетельствует о состоянии отчаяния, в котором стандартная крыса не может найти выход и подчиняется экспериментальным условиям. В первый день эксперимента животных окунали по отдельности в вертикальный плексиглазовый цилиндр (высотой 40 см и диаметром 18 см), наполненный до отметки в 24 см водой, температуру которой поддерживали на уровне 25-26oС. Цилиндр был окрашен в белый цвет. Воду меняли после опыта с каждой крысой. После 15 минут пребывания в цилиндре крыс вынимали и возвращали в их индивидуальные клетки, не высушивая. Через час после этого крысам вводили тетрапептид, MIF или контроль (0,01 М уксусную кислоту в 0,9%-ном физиологическом растворе) в количестве, определенном на основе веса каждого животного. На 2-й, 3-й и 4-й день в момент времени, соответствующий среднему времени обработки всей группы подопытных животных, крысам вводили либо пептид с 1 по 39, либо контрольный раствор. На 5-й день после взвешивания каждую крысу обрабатывали дозой, определенной на основе ее собственного веса. Порядок дозирования регулировали таким образом, чтобы обеспечить достаточный промежуток времени между опытами над каждым отдельным животным для оценки результатов теста. Через пятнадцать минут после инъекции каждую крысу помещали на 300 секунд в воду. Для каждой крысы определяли период интенсивной активности (время движения).
Результаты
В таблице 1 и на фиг.1-3 представлены результаты, полученные на основе многочисленных плавательных тестов Порсольта, при введении пептидов по настоящему изобретению, известных соединений-антидепрессантов (например, амитриптилина, флуоксетина [Prozac] и сертралина [Zoloft]), известных соединений (например, Pro-Leu-Gly-NH2, Pro-D-Leu-Gly-NH2) и плацебо (КНГ: обработка 0,1 М уксусной кислотой в 0,9%-ном физиологическом растворе, доза 1 мл/кг).
Количество реагирующих соответствующим образом животных из общего количества 12 животных в каждой тест-группе приведено в колонке 4 таблицы 1 для всех изученных соединений, доз и комбинаций. На фиг.1 представлен графический анализ среднего количества реагирующих соответствующим образом животных из общего количества 12 животных в одной или нескольких экспериментальных группах при изучении выбранных соединений по настоящему изобретению, а также для тест-соединений. В частности на фиг.1 представлены данные для следующих соединений:
1) 4-F-Рhе-3,4-дегидро-Рrо-Аrg-Glу-Тrр-NН2 (SEQ ID NO: 55), соответствует 2 в таблице 1;
2) 4-F-Phe-4-OH-Pro-Arg-Gly-Ile-Gly-Trp-NH2 (SEQ ID NO: 56), соответствует 3 в таблице 1;
3) 4-F-Phe-4-гомо-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 57), соответствует 4 в таблице 1;
4) Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 3), соответствует 5 в таблице 1;
5) 4-F-Phe-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 16), соответствует 8 в таблице 1;
6) Амитриптилин, соответствует 9 в таблице 1;
7) 4-F-Phe-4-OH-Pro-Arg-Gly-Gly-Trp-NH2 (SEQ ID NO: 58), соответствует 11 в таблице 1;
8) 4-CH3O-Phe-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 59). соответствует 12 в таблице 1;
9) 4-Cl-Phe-4-OH-Pro-Ile-Gly-NH2 (SEQ ID NO: 60), соответствует 13 в таблице 1;
10) 4-F-Phe-4-OH-Pro-Ile-Gly-Trp-NH2 (SEQ ID NO: 41), соответствует 14 в таблице 1;
11) 4-F-Phe-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 43), соответствует 17 в таблице 1;
12) 4-OH-Pro-Ile-Gly-NH2, соответствует 20 в таблице 1;
13) Zoloft, соответствует 41 в таблице 1;
14) Prozac, соответствует 48 в таблице 1; и
15) Pro-Leu-Gly-NH2, соответствует 55 в таблице 1.
Перечисленные выше соединения 1-15 соответствуют таким же номерам на графиках, представленных на фиг.2 и 3.
Обозначения соединений сделаны только для облегчения ссылок. Использованная в таблице 1 нумерация не соответствует обозначениям соединений 1-15 на фиг. 1, 2 и 3. Данные, представленные на фиг.1-3, соответствуют тестам, проведенным с использованием стандартной дозы 0,1 мг/мл. Данные, приведенные в таблице 1, представляют собой эти результаты, а также результаты многочисленных дополнительных тестов с другими пептидами по настоящему изобретению, с различными комбинациями соединений и при различных дозировках.
Под реагирующим соответствующим образом животным понимают животное, время движения которого при выдерживании в сосуде с водой в течение 300 секунд не превышает среднего времени движения контрольной неактивной группы (КНГ) плюс одно стандартное отклонение. Например, если среднее время движения КНГ, состоящей из 12 подопытных крыс, составляет 35 секунд плюс или минус одно стандартное отклонение в 15 секунд, то под реагирующим соответствующим образом животным понимают животное, время движения которого превышает пятьдесят секунд. Таким образом, значение для контрольной группы плюс одно стандартное отклонение принимали в качестве порога отклика; количество крыс, время движения которых превышало этот уровень, приведено в таблице как количество реагирующих соответствующим образом животных.
В таблице 1 (колонка 5) приведена разница между временами движения при исследовании различных изученных соединений, комбинаций соединений и доз и временем движения в контрольной неактивной группе. Представлено среднее время движения при исследовании каждого пептида. Среднее средних значений времени движения по экспериментальным группам, обработанным каждым из перечисленных выше соединений 1-15, помеченных двумя звездочками, также представлена на фиг.2. На фиг.2 показано среднее время движения для животных, обработанных пептидами, обозначенными, как соединения 1-15. Усредненные результаты для обработанных животных сравнивали с усредненными результатами, полученными для контрольной группы (КНГ), с использованием одновыборочного t-критерия Стьюдента. Полученные таким образом оценки достоверности различий для всех исследованных соединений приведены в таблице 1 (колонка 8).
Z-баллы среднего времени движения при исследовании уже перечисленных выше соединений 1-15 приведены на фиг.3 и в таблице 1 (колонка 9). Z-балл представляет собой безразмерный коэффициент эффективности, который усредняли по данным многих экспериментов. Средний Z-балл определяют как разницу между средним временем движения в обработанной группе и средним временем движения в контрольной группе, деленную на стандартное отклонение среднего времени движения в контрольной группе. Таким образом, для неэффективного соединения значение Z-балла близко к нулю, а более высокие Z-баллы соответствуют более высокой эффективности.
Данные, представленные в таблице 1, и графическое изображение данных для перечисленных выше соединений 1-15 на фиг.1-3 показывают, что многие пептиды по настоящему изобретению проявляют более высокую антидепрессивную активность при сравнении с известными соединениями-антидепрессантами, такими как амитриптилин, Prozac и Zoloft. Кроме того, подавляющее большинство приведенных в качестве примеров пептидов по настоящему изобретению проявляют более высокую активность, чем MIF. Полученные результаты также свидетельствуют о том, что между пептидами по настоящему изобретению и известными соединениями-антидепрессантами, такими как Prozac, может наблюдаться синергистическое действие. Например, данные, представленные в таблице 1 под No. 1, показывают, что смесь, состоящая из 4-F-Phe-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 43) в концентрации 0,1 мг/мл и Prozac в концентрации 0,8 мг/мл, приводит к соответствующей реакции у 12 животных из 12 изученных. Кроме того, данные, представленные в таблице 1 под No. 6, показывают, что смесь, состоящая из 4-F-Phe-4-OH-Pro-Arg-Gly-Trp-NH2 (SEQ ID NO: 43) в концентрации 0,1 мг/мл и амитриптилина, приводит к соответствующей реакции у 10 животных из 12 изученных.
Таким образом, заявители описывают многочисленные малые пептиды для применения в качестве антидепрессивных соединений, подкрепляя возможность такого применения результатами биологических экспериментов.
Для специалистов в данной области техники на основе изучения данного описания или приведенного в данном описании практического применения изобретения должны быть очевидны другие примеры осуществления изобретения. Предполагается, что описание и примеры должны рассматриваться только в качестве иллюстрации, а истинный объем и сущность изобретения, на которые заявляются исключительные права, даются в пунктах формулы изобретения.
Перечень последовательностей приведен в конце описания.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ КОМПОЗИЦИИ АГОНИСТОВ ЭКСЕНДИНА И СПОСОБЫ ИХ ВВЕДЕНИЯ | 2000 |
|
RU2242244C2 |
| СПОСОБ ВВЕДЕНИЯ МОЛЕКУЛ GLP-1 | 2003 |
|
RU2332229C2 |
| СПОСОБЫ ПОДАВЛЕНИЯ ГЛЮКАГОНА | 2000 |
|
RU2247575C9 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ОСНОВЕ α-ЦИКЛОДЕКСТРИНА ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ АНАЛОГОВ РИЛИЗИНГ-ГОРМОНА ЛЮТЕИНИЗИРУЮЩЕГО ГОРМОНА (LH-RH) | 1999 |
|
RU2214270C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2004 |
|
RU2353383C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2004 |
|
RU2543350C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА | 2018 |
|
RU2783258C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ КОНТРОЛЯ ЗАБОЛЕВАНИЙ, ПЕРЕДАВАЕМЫХ ПЕРЕНОСЧИКАМИ | 2018 |
|
RU2804136C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2014 |
|
RU2763796C2 |
| НЕОАНТИГЕНЫ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2813924C2 |














































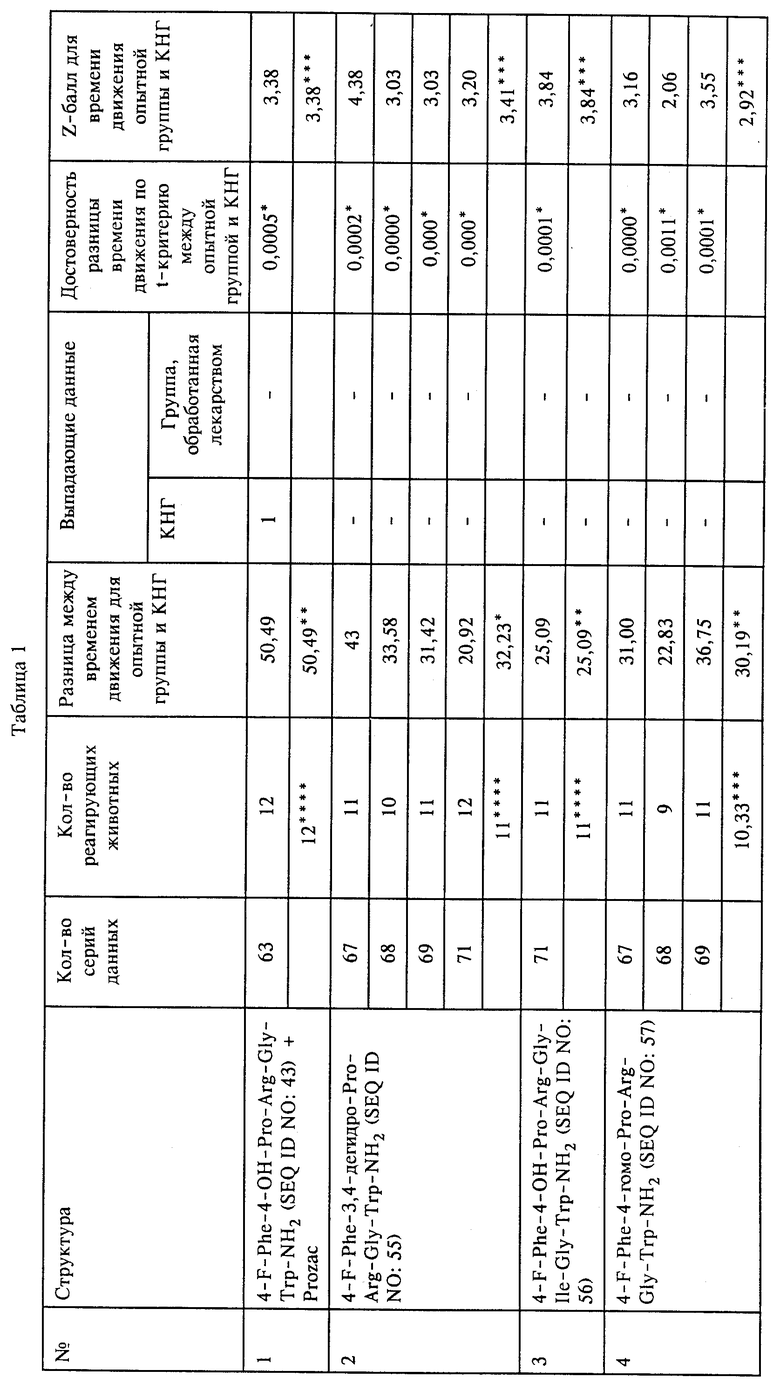
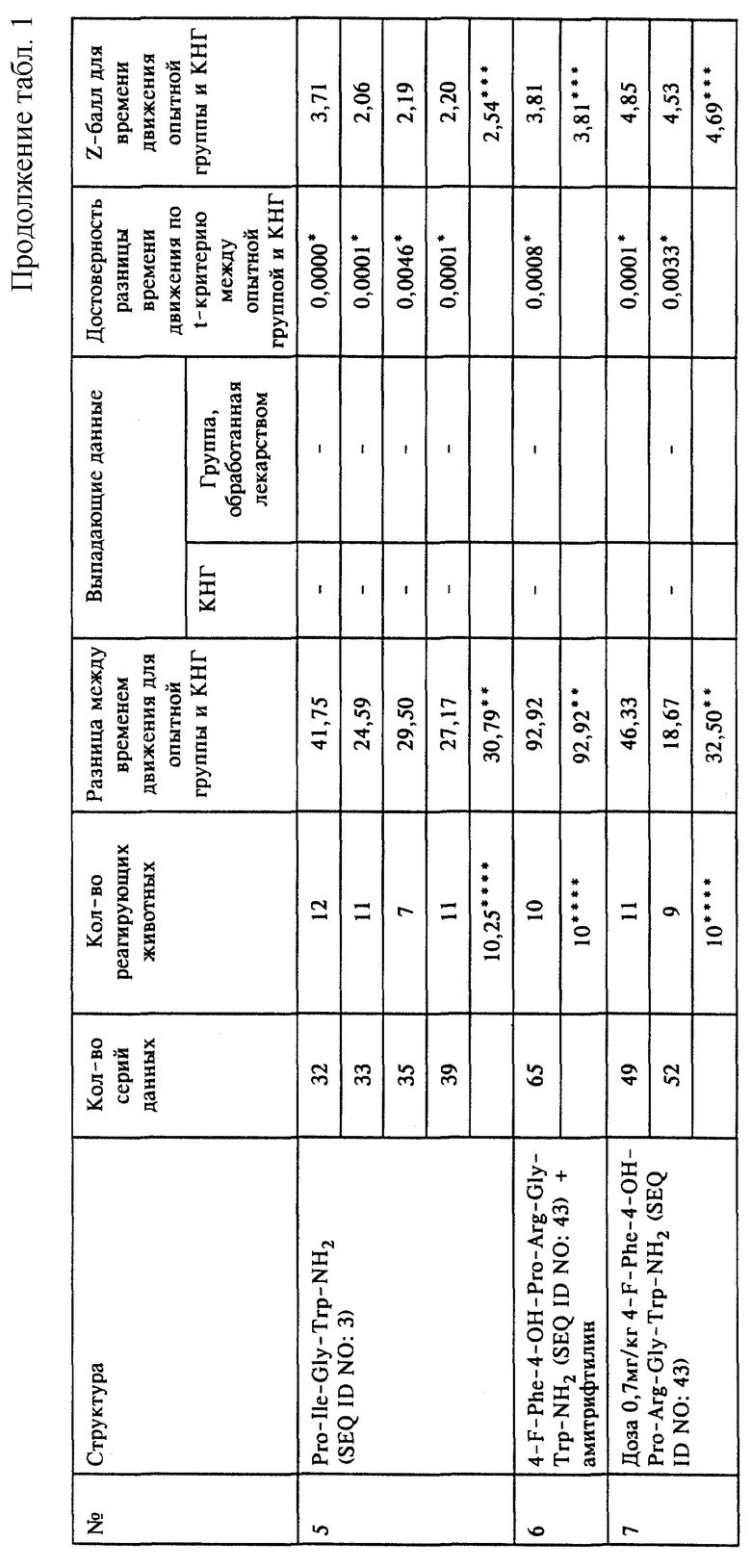

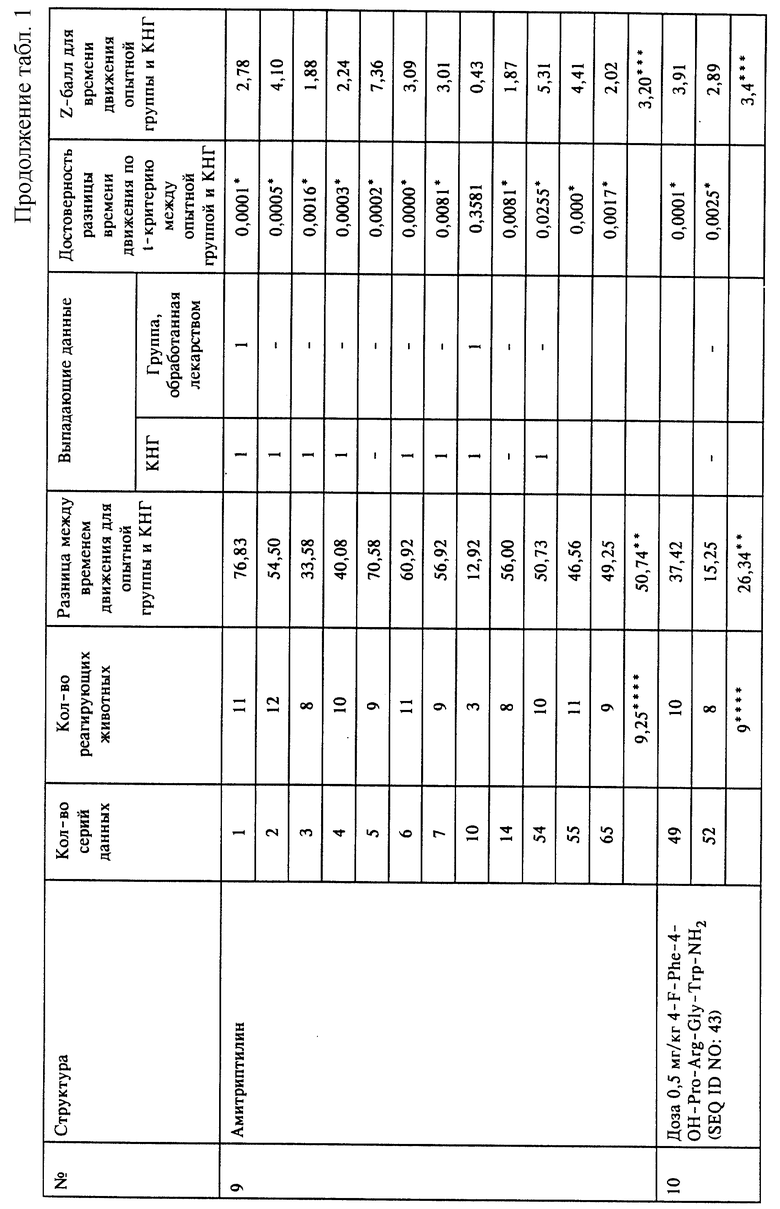
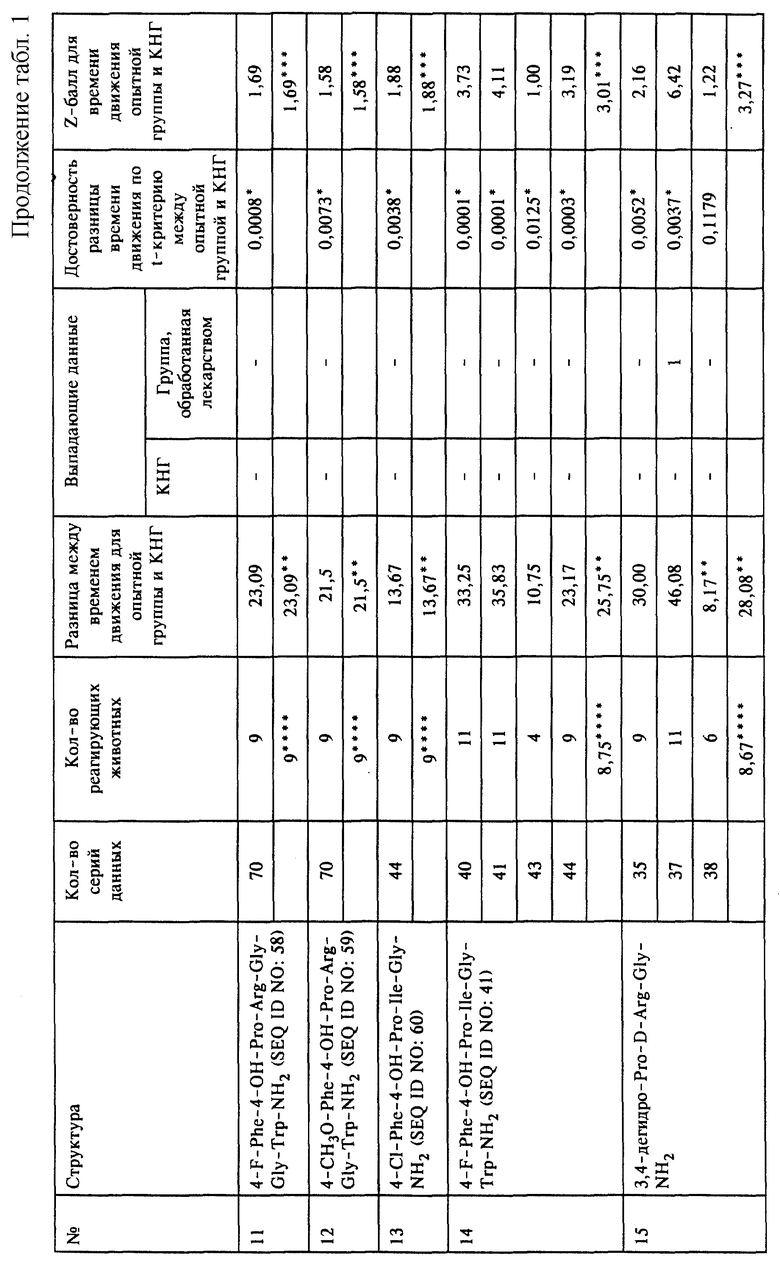
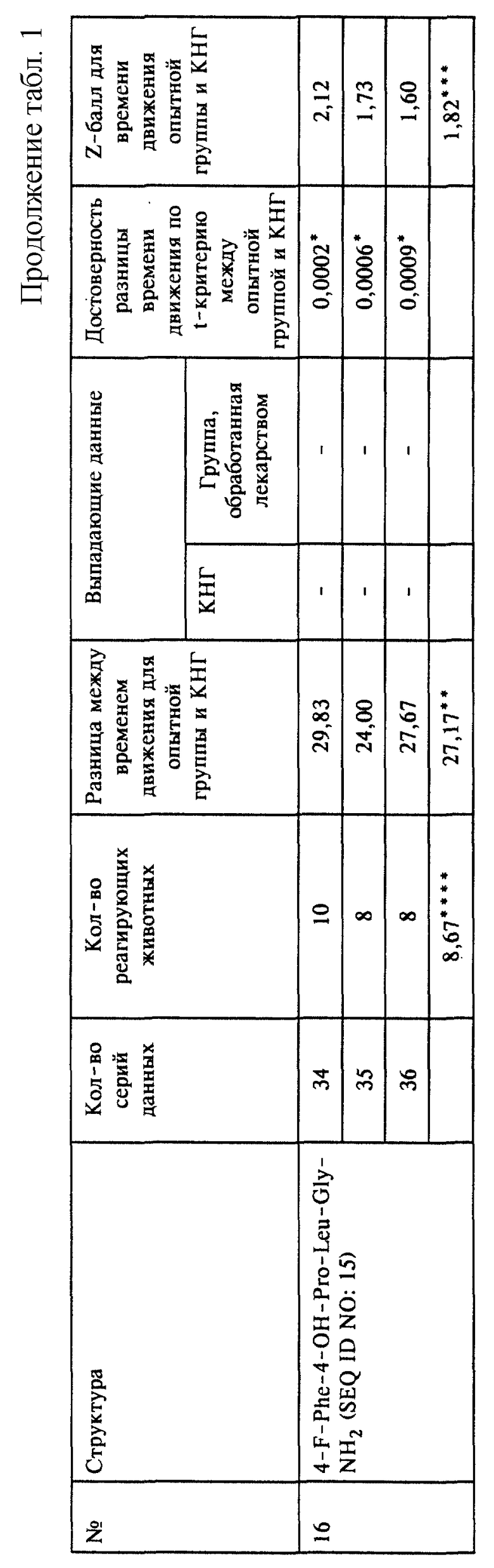
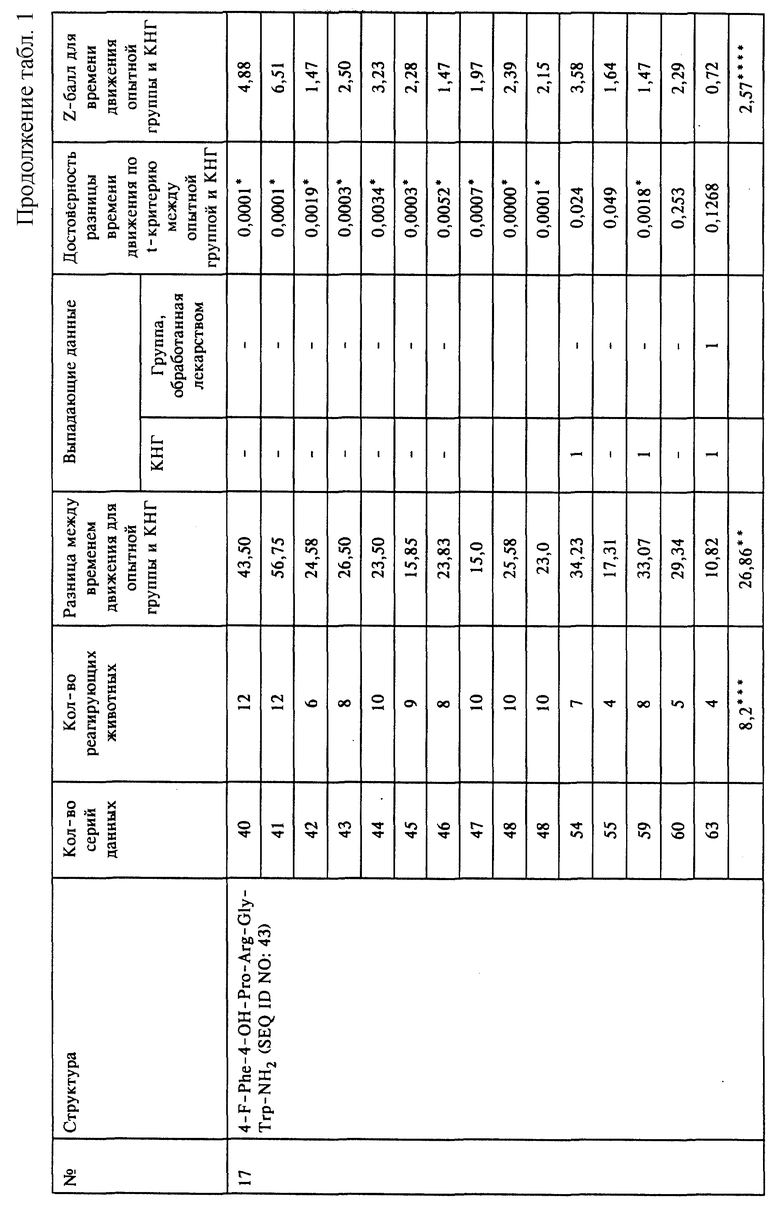

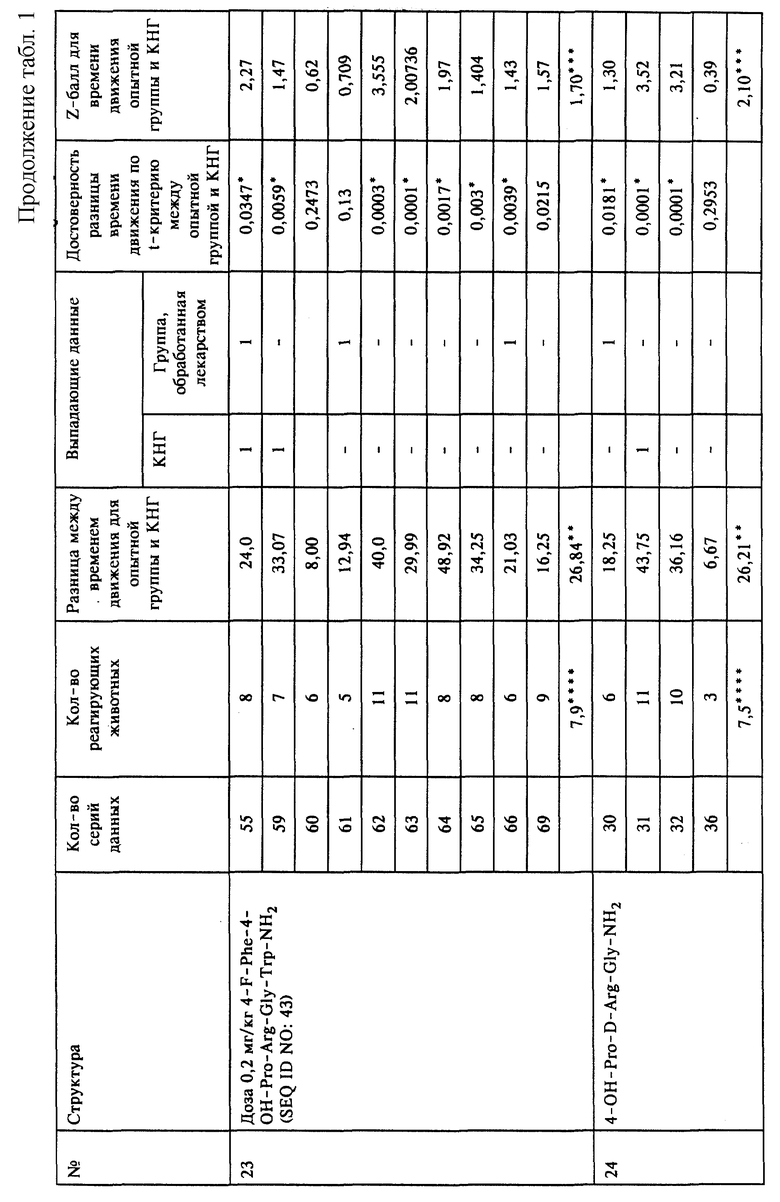


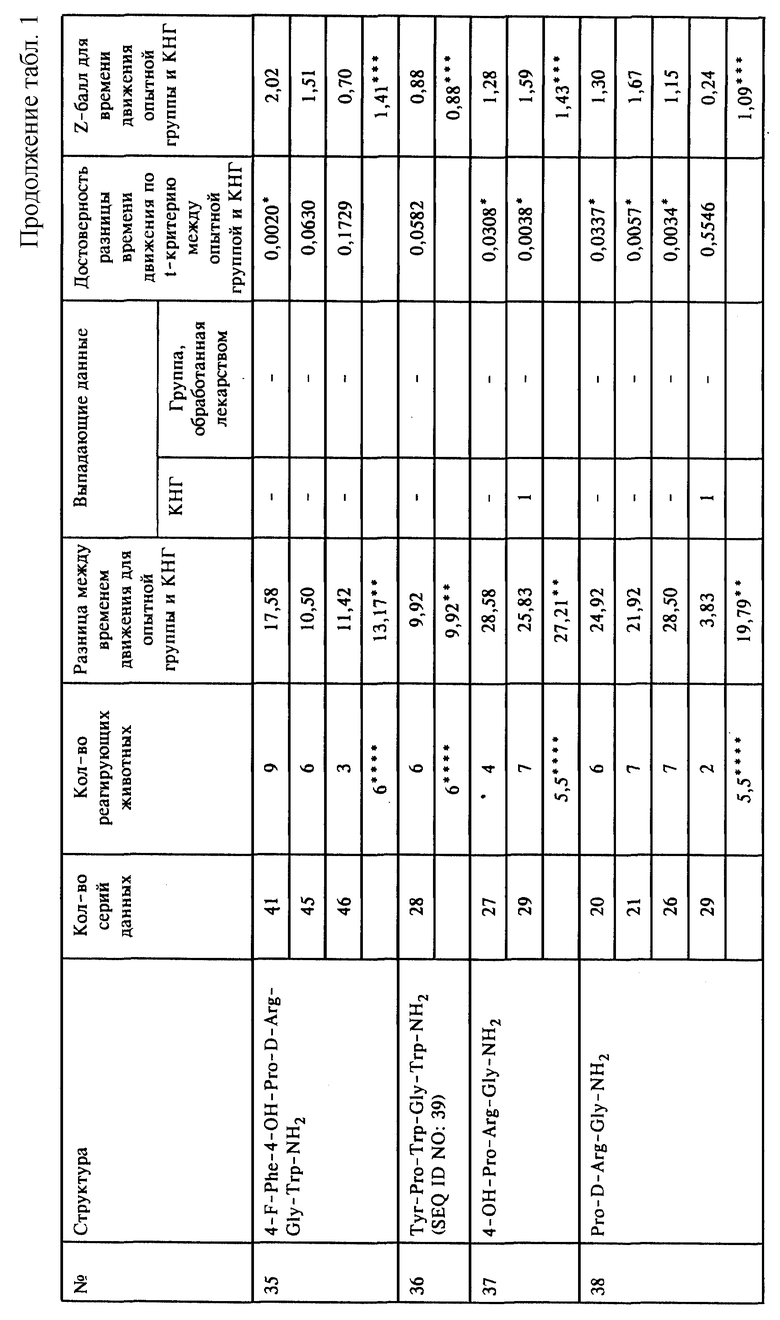


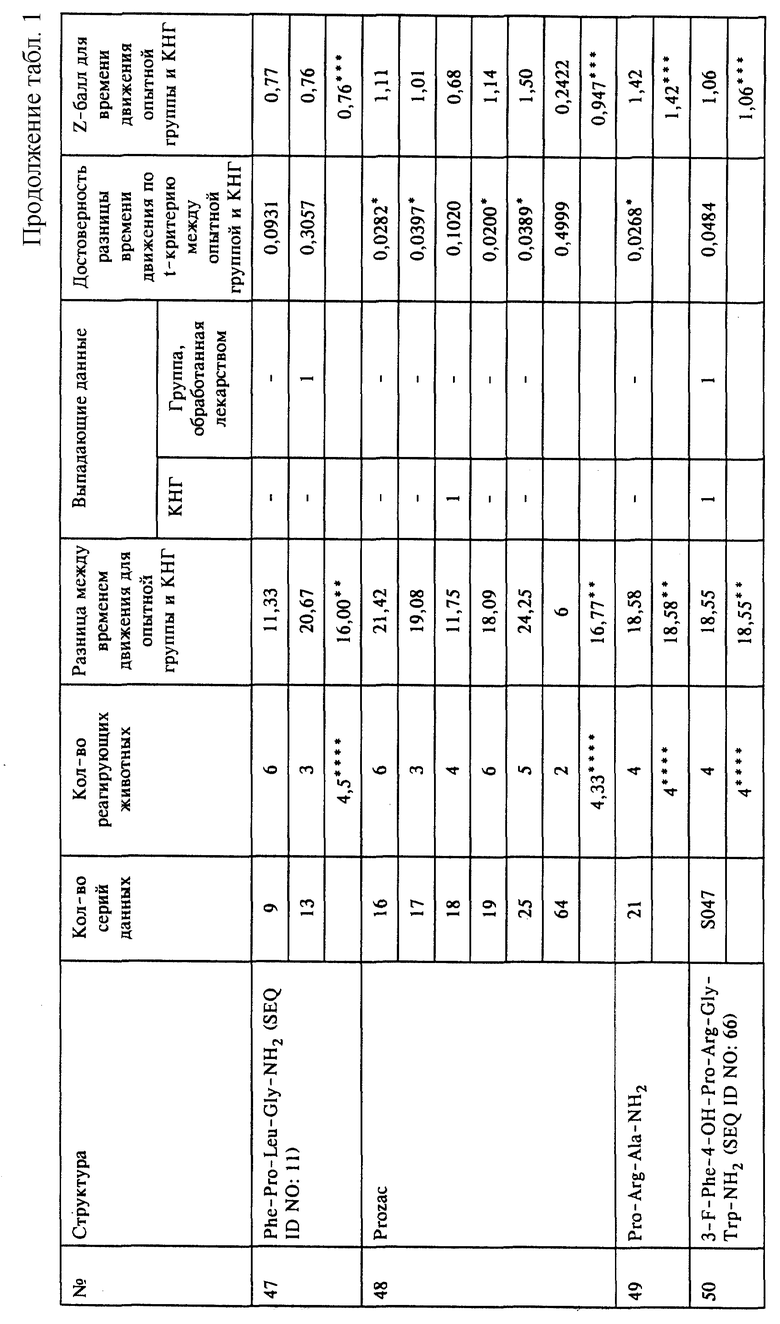
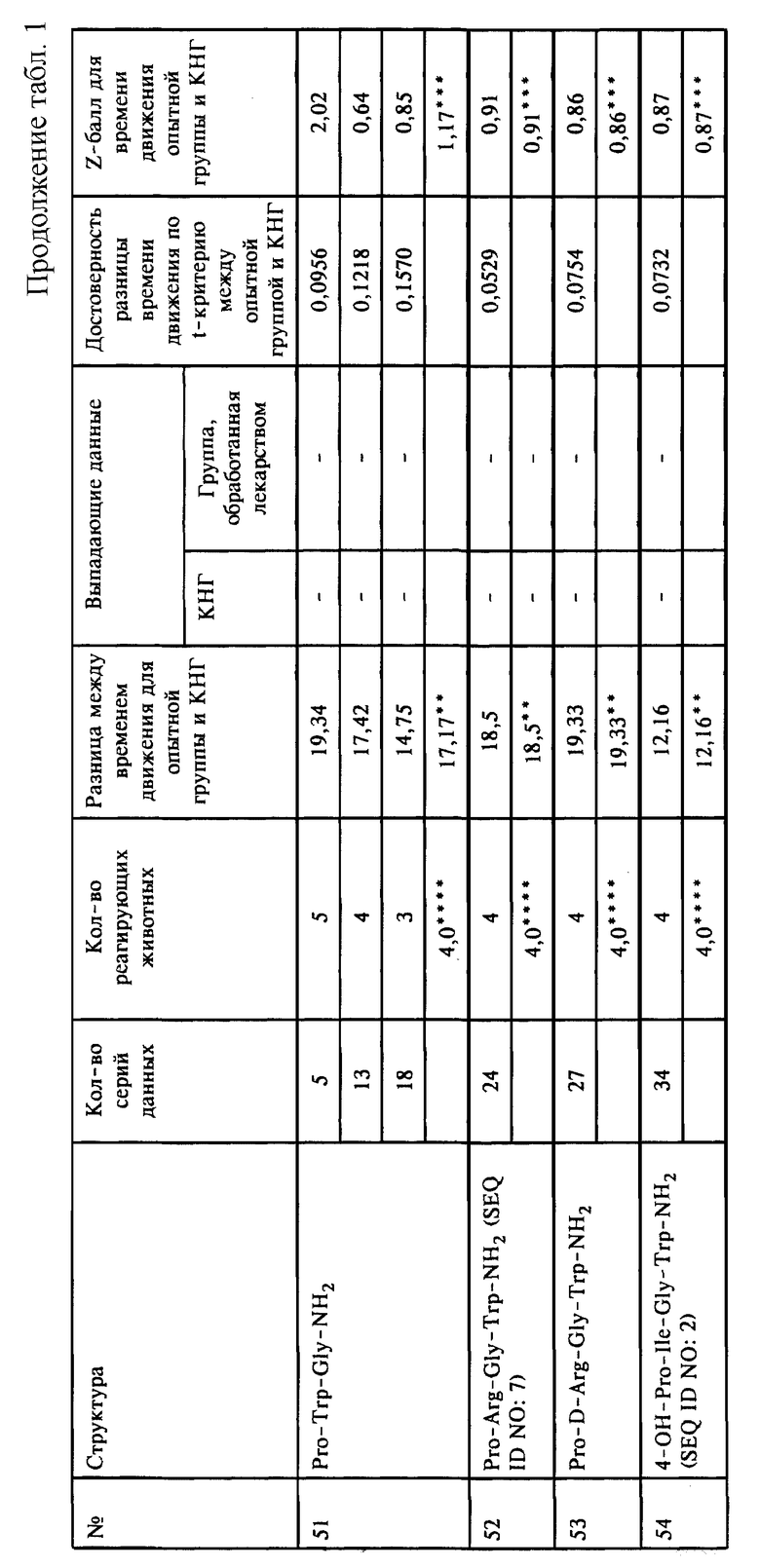
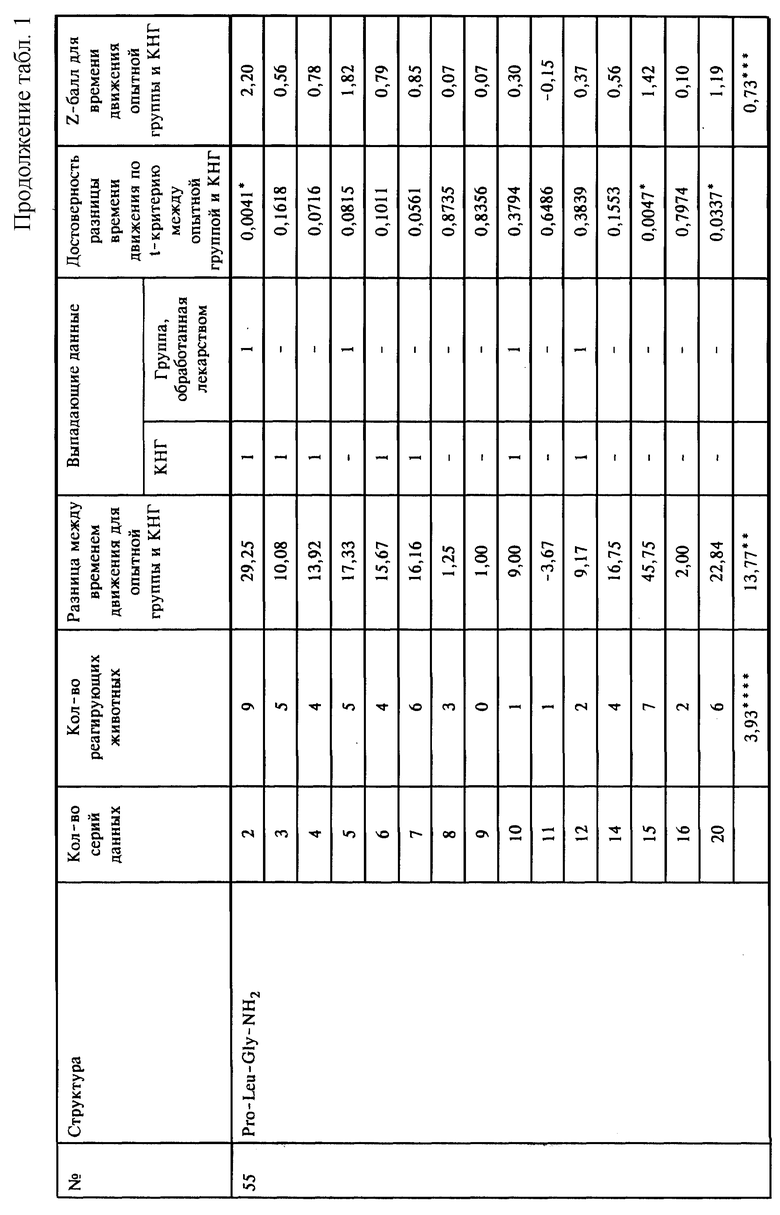
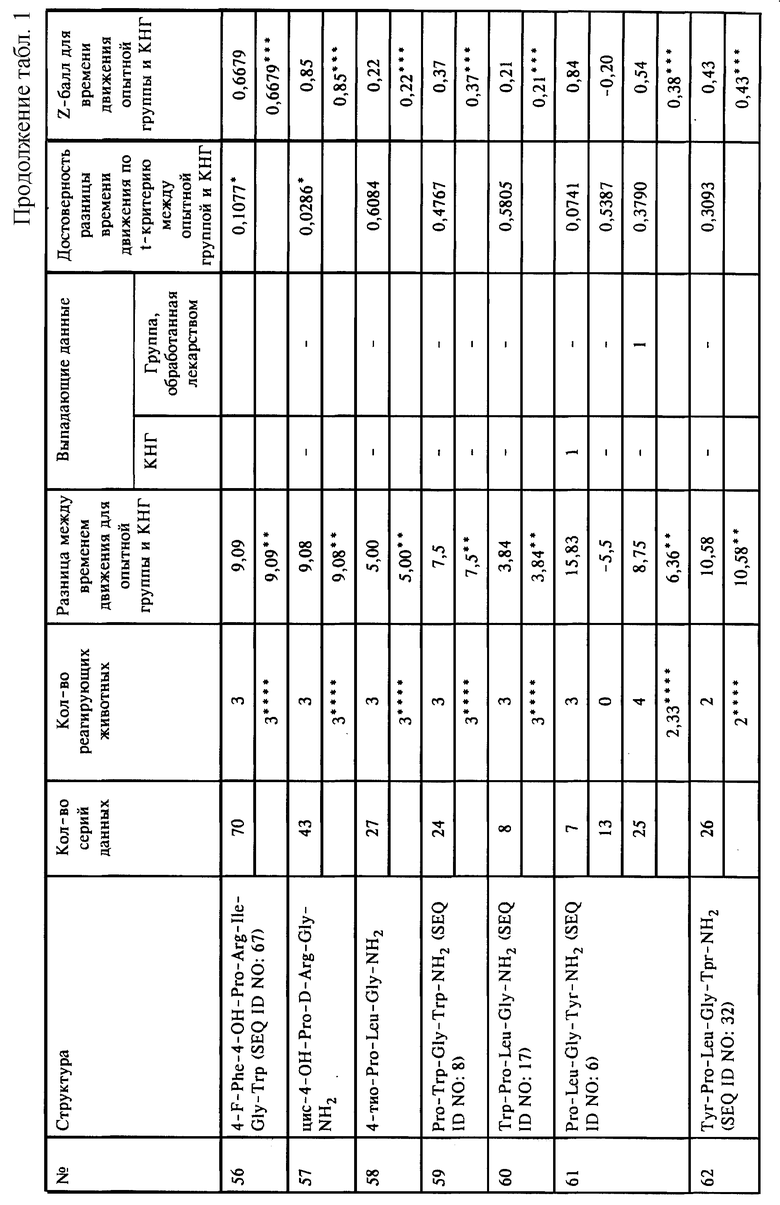
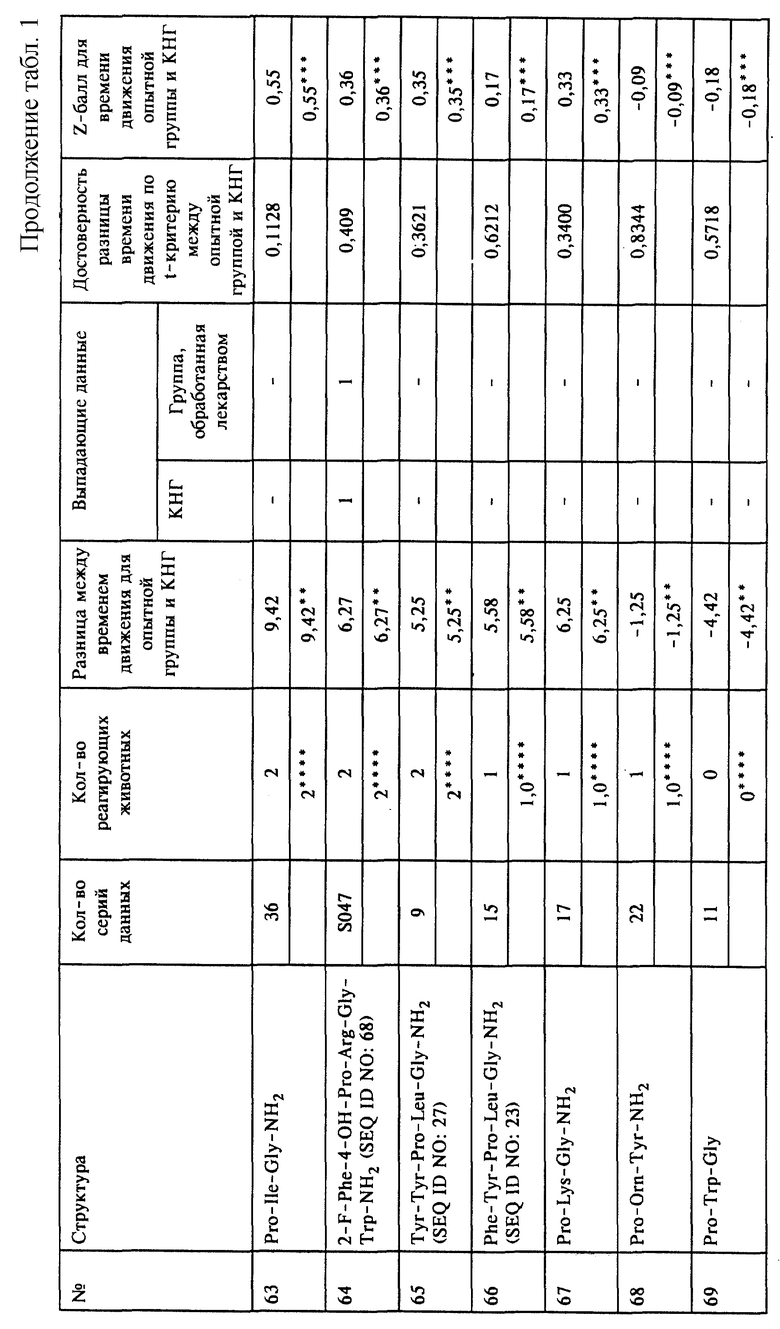
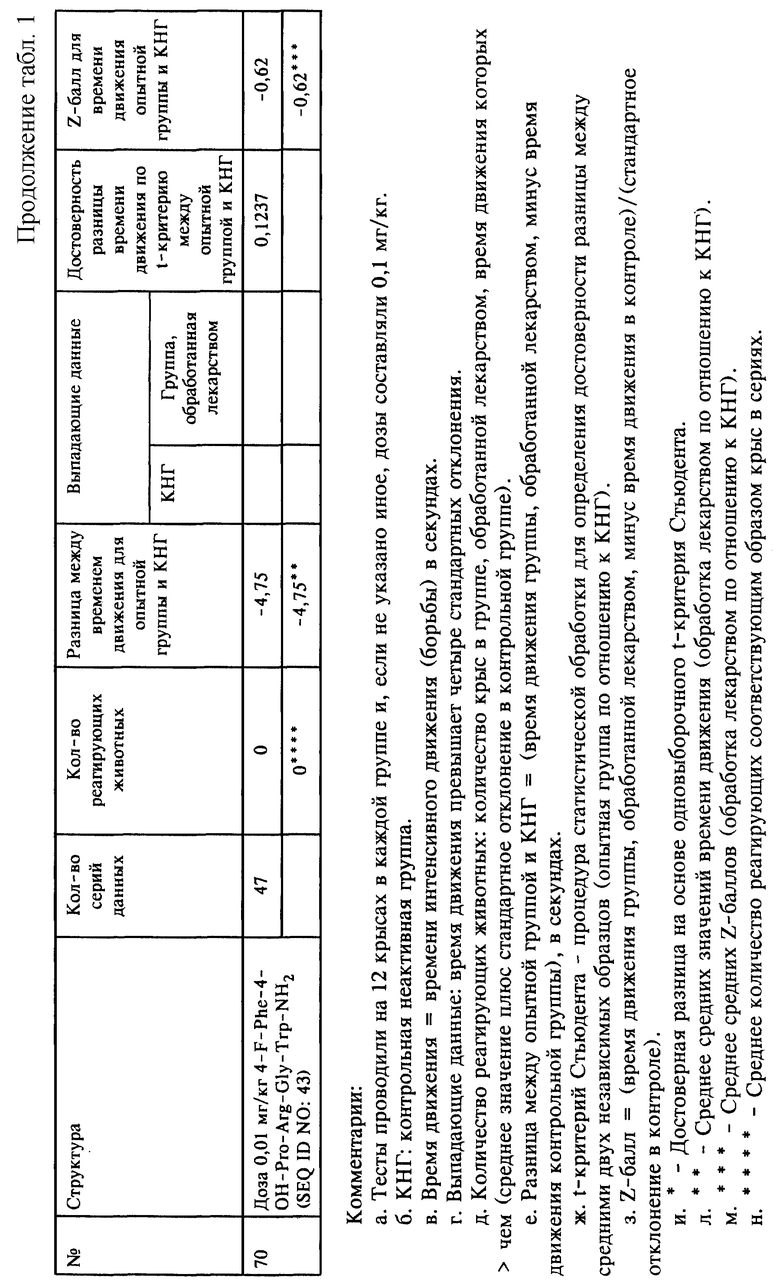
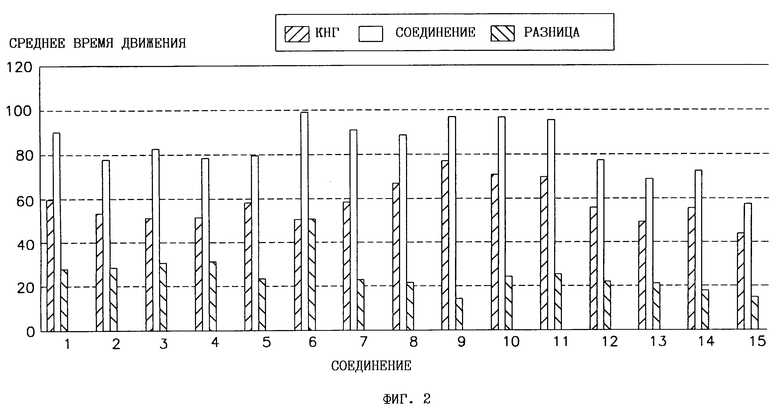

В заявке описаны новые пептиды, применяемые для лечения пациентов, страдающих депрессией. Указанные новые пептиды представляют собой модификации трипептидного гормона МIF, полученные, в том числе, в результате преобразования остатков с концевой аминогруппой, остатков с концевой карбоксильной группой и внутренних аминокислотных остатков, включающего добавление или замещение аминокислотных остатков и преобразование пептидных связей и функциональных боковых групп соответствующих аминокислотных остатков. Для лечения пациентов, страдающих депрессией, три-, тетра-, пента- и полипептиды по настоящему изобретению могут применяться по отдельности или в композиции. 5 с. и 104 з.п.ф-лы, 3 ил., 1 табл.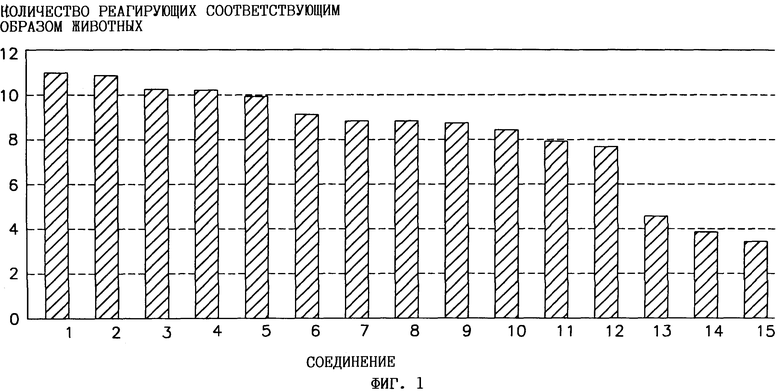
R1-Pro1-АА1-NR2-СН2-R, (1)
где Pro1 обозначает аминокислоту, выбранную из группы, состоящей из Pro и дегидро-Pro;
АА1 - аминокислоту, выбранную из группы, состоящей из Тrр, Оrn, Lys, Leu, Arg, D-Arg и Ile;
R - группу, выбранную из карбамильной группы, карбоксильной группы и гидроксиалкильной группы;
R1 выбирают из группы, состоящей из атома водорода, атома галогена, гидроксильной группы;
R2 - из группы, состоящей из атома водорода и группы низшего алкила, имеющего 1-3 атома углерода, при условии, что если Pro1 обозначает Pro и АА1 - Leu, Ile, Lys, Arg или Оrn, то R1 и R2 оба не могут обозначать атом водорода, когда R обозначает карбамильную группу; если Pro1 обозначает Pro и АА1 - Leu, то R1 и R2 оба не могут обозначать атом водорода, когда R обозначают карбоксильную группу, и если Pro1 обозначает Pro и АА1 - Тrp, то R1 и R2 оба не могут обозначать атом водорода, когда R обозначают гидроксиалкильную группу;
или (б) трипептид общей формулы (2)
R1-Pro1-АА1-Ala-R, (2)
где АА1 обозначает аминокислоту, выбранную из группы, состоящей из Arg и D-Arg;
R - карбамильную группу;
R1 - атом водорода,
или (в) трипептид общей формулы (3)
R1-Pro1-АА1-Gly-АА2-R, (3)
где Pro1 обозначает аминокислоту, выбранную из группы, состоящей из Pro и дегидро-Pro;
АА1 - аминокислоту, выбранную из группы, состоящей Ile, Leu, Arg и D-Arg;
АА2 - аминокислоту, выбранную из группы, состоящей из Тrp и Tyr;
R - карбамильную группу;
R1 выбирают из группы, состоящей из атома водорода и гидроксильной группы;
или (г) тетрапептид общей формулы (4)
R1-АА1-R2-Pro1-АА2-Gly-R, (4)
где АА1 обозначает аминокислоту, выбранную из группы, состоящей из Тrp, Tyr и Phe;
АА2 - аминокислоту, выбранную из группы, состоящей из Leu и Ile;
R - карбамильную группу;
R1 и R2 каждый независимо друг от друга выбирают из группы, состоящей из атома водорода, атома галогена и гидроксильной группы, при условии, что если Pro1 обозначает Pro, АА2 - Leu и R - карбамильную группу, то R1 и R2 оба не могут обозначать атом водорода, когда АА1 - Phe или Tyr; и если Pro1 обозначает Pro и R - карбамильную группу, то R1 и R2 не могут обозначать атом водорода, когда АА1 - Trp и AA2 - Leu;
или (д) тетрапепид общей формулы (5)
R1-АА1-R2-Pro1-АА2-Gly-АА3-R (5)
где Pro1 обозначает аминокислоту, выбранную из группы, состоящей из Pro и дегидро-Pro;
АА1 - аминокислоту, выбранную из группы, состоящей из Tyr и Phe;
АА2 - аминокислоту, выбранную из группы, состоящей из Leu, Ile, Arg и D-Arg;
АА3 - аминокислоту Тrp;
R - карбамильную группу;
R1 и R2 каждый независимо друг от друга выбирают из группы, состоящей из атома водорода, атома галогена и гидроксильной группы;
или (е) пентапептид общей формулы (6)
R1-АА1-R2-Pro-АА2-Gly-АА3-R, (6)
где АА1 обозначает аминокислоту Аla;
АА2 - аминокислоту, выбранную из группы, состоящей из Arg или D-Arg;
АА3 - аминокислоту Тrp;
R - карбамильную группу;
R1 выбирают из группы, состоящей из фрагмента 3-(3-пиридила);
R2 - из цис- или транс-4-ОН-группы;
или (ж) пептид общей формулы (7)
R1-АА1-R2-Pro-АА2-АА4-Gly-АА3-R, (7)
где АА1 обозначает аминокислоту Рhe или Tyr;
АА2 - аминокислоту, выбранную из группы, состоящей из Arg или D-Arg;
АА3 - аминокислоту Тrp;
АА4 - аминокислоту Gly или Ile;
R - карбамильную группу;
R1 и R2 каждый независимо друг от друга выбирают из группы, состоящей из атома фтора, атома хлора, цис- или транс-4-ОН-группы;
или (з) пептид общей формулы (8)
R1-АА1-R2-Pro-АА2-АА4-АА5-Gly-АА3-R, (8)
где АА1 обозначают аминокислоту Phe или Tyr;
АА2 выбирают из группы, состоящей из Аrg или D-Arg;
АА3 обозначают аминокислоту Тrp;
АА4 и АА5 - аминокислоту Gly или Ile;
R - карбамильную группу;
R1 и R2 каждый независимо выбирают из группы, состоящей из атома водорода, атома фтора, атома хлора, цис-, или транс-4-ОН-групп,
или их соли.
R1-Phe-Pro1-АА2-АА3-NH2,
где R1 - атом галогена, предпочтительно атом фтора или хлора, или нитрогруппа, причем все преобразования предпочтительно касаются атома С4 в Phe;
Pro1 - 3,4-дегидро-Pro, гомо-Pro, цис- или транс-4-ОН-Pro или Pro;
АА2 - Ile, Leu или Arg;
АА3 - Gly или Тrp,
или его соль.
R1-Phe-Pro1-АА2-Gly-АА(n)-АА3-NH2,
где R1 - атом галогена, предпочтительно атом фтора или хлора, или нитрогруппа, причем все преобразования предпочтительно касаются атома С4 в Phe;
Pro1 - 3,4-дегидро-Pro, гомо-Pro, цис- или транс-4-ОН-Pro или Pro;
АА2 - Arg, Ile, Leu или His;
АА(n) - 0-2 аминокислотных остатка, причем, если n= 1, то предпочтительным аминокислотным остатком является Gly, а если n= 2, то предпочтительны Ile-Gly, Ile-Ile или Gly-Gly;
АА3 - Тrp или Gly, или его соль.
| FR 9407078 А1, 09.06.1994 | |||
| WO 9219253 А1, 12.11.1992 | |||
| МАРКОВ Д.А., ЛЕОНОВИЧ А.Л | |||
| Рассеянный склероз | |||
| - М.: Медицина, 1976, с | |||
| Котел | 1921 |
|
SU246A1 |
Авторы
Даты
2002-05-27—Публикация
1995-05-02—Подача