ПЕРЕКРЕСТНАЯ ССЫЛКА
По настоящей заявке испрашивается приоритет временной заявки США № 62/687,191, поданной 19 июня 2018, временной заявки США № 62/702,567, поданной 24 июля 2018, временной заявки США № 62/726,804, поданной 4 сентября 2018, временной заявки США № 62/789,162, поданной 7 января 2019, временной заявки США № 62/801,981, поданной 6 февраля 2019, временной заявки США № 62/800,700, поданной 4 февраля 2019, и временной заявки США № 62/800,792, поданной 4 февраля 2019, каждая из которых полностью включена в настоящее описание в качестве ссылки.
УРОВЕНЬ ТЕХНИКИ
Иммунотерапия рака представляет собой использование иммунной системы для лечения рака. В иммунотерапии используют тот факт, что раковые клетки часто имеют на своей поверхности молекулы, которые могут быть обнаружены иммунной системой, известные как опухолевые антигены, которые часто являются белками или другими макромолекулами (например, углеводами). Активная иммунотерапия направляет иммунную систему атаковать опухолевые клетки путем нацеливания на опухолевые антигены. Пассивная иммунотерапия усиливает существующие противоопухолевые ответы и включает использование моноклональных антител, лимфоцитов и цитокинов. Опухолевые вакцины обычно состоят из опухолевых антигенов и иммуностимулирующих молекул (например, адъювантов, цитокинов или лигандов TLR), которые работают вместе, чтобы индуцировать антиген-специфические цитотоксические Т-клетки (CTL), которые распознают и лизируют опухолевые клетки. Одним из критических барьеров для разработки лечебной и опухолеспецифическая иммунотерапии является идентификация и выбор высокоспецифичных и ограниченных опухолевых антигенов для избегания аутоиммунитета.
Неоантигены опухоли, которые возникают в результате генетических изменений (например, инверсий, транслокаций, делеций, миссенс-мутаций, мутаций сайтов сплайсинга и т. д.) в злокачественных клетках, представляют собой наиболее опухолеспецифический класс антигенов и могут быть пациент-специфичными или перекрестнореагирующими. Неоантигены опухоли уникальны для опухолевой клетки, поскольку мутация и соответствующий ей белок присутствуют только в опухоли. Они также избегают центральной толерантности и, следовательно, с большей вероятностью являются иммуногенными. Таким образом, опухолевые неоантигены являются отличной мишенью для иммунного распознавания, в том числе с помощью как гуморального, так и клеточного иммунитета. Однако опухолевые неоантигены редко используют в противораковых вакцинах или иммуногенных композициях из-за технических трудностей их идентификации, выбора оптимизированных антигенов и производства неоантигенов для использования в вакцине или иммуногенной композиции. Соответственно, все еще существует потребность в разработке дополнительных противораковых терапевтических средств.
ВКЛЮЧЕНИЕ В КАЧЕСТВЕССЫЛКИ
Все публикации, патенты и заявки на патенты, упомянутые в этом описании, включены в него в качестве ссылки в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент были специально и индивидуально указаны как подлежащие включению в качестве ссылки.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте изобретение относится к фармацевтической композиции, содержащей (a) по меньшей мере один полипептид или его фармацевтически приемлемую соль, содержащий первую мутантную GATA3 пептидную последовательность и вторую мутантную GATA3 пептидную последовательность, где (i) каждая из первой мутантной GATA3 пептидной последовательности и второй мутантной GATA3 пептидной последовательности содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1, и (ii) C-концевую последовательность первой мутантной GATA3 пептидной последовательности, перекрывающиеся с N-концевой последовательностью второй мутантной GATA3 пептидной последовательности; где по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1 содержат по меньшей мере одну аминокислоту с последовательностью: PGRPLQTHVLPEPHLALQPLQPHADHAHADAPAIQPVLWTTPPLQHGHRHGLEPCSMLTGPPARVPAVPFDLHFCRSSIMKPKRDGYMFLKAESKIMFAT LQRSSLWCLCSNH (SEQ ID NO: 2), или (b) по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид.
В некоторых вариантах осуществления, первая мутантная GATA3 пептидная последовательность или вторая мутантная GATA3 пептидная последовательность содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2. В некоторых вариантах осуществления, первая мутантная GATA3 пептидная последовательность и вторая мутантная пептидная последовательность содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2.
В некоторых вариантах осуществления по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2 содержат по меньшей мере 8 непрерывных аминокислотных последовательностей: PGRPLQTHVLPEPHLALQPLQPHADHAHADAPAIQPVLWTTPPLQHGHRHGL (SEQ ID NO: 3).
В некоторых вариантах осуществления по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2 содержат по меньшей мере одну аминокислоту последовательности: EPCSMLTGPPARVPAVPFDLHFCRSSIMKPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 4).
В некоторых вариантах осуществления по меньшей мере одна из первой мутантной GATA3 пептидной последовательности и второй мутантной GATA3 пептидной последовательности содержит по меньшей мере 14 мутантных аминокислот. В некоторых вариантах осуществления по меньшей мере один полипептид содержит по меньшей мере 3 мутантных GATA3 пептидных последовательностей. В некоторых вариантах осуществления по меньшей мере один полипептид содержит по меньшей мере два полипептида. В некоторых вариантах осуществления по меньшей мере один полипептид дополнительно содержит третью мутантную GATA3 пептидную последовательность, где третья мутантная GATA3 пептидная последовательность содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1, где по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1 содержит по меньшей мере одну аминокислоту последовательности SEQ ID NO: 2. В некоторых вариантах осуществления третий GATA3 мутантный пептид содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2.
В некоторых вариантах осуществления по меньшей мере один полипептид содержит по меньшей мере одну мутантную GATA3 пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную GATA3 пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым: (a) HLA-A02:01 аллелем и HLA-A24:02 аллелем, (b) HLA-A02:01 аллелем и HLA-B08:01 аллелем, (c) HLA-A24:02 аллелем и HLA-B08:01 аллелем, или (d) HLA-A02:01 аллелем, HLA-A24:02 аллелем и HLA-B08:01 аллелем. В некоторых вариантах осуществления, (a) первая мутантная GATA3 пептидная последовательность связывается с или предположительно связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем или HLA-B08:01 аллелем; и (b) вторая GATA3 пептидная последовательность связывается с или предположительно связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем или HLA-B08:01 аллелем; где первая мутантная GATA3 пептидная последовательность связывается с или предположительно связывается с белком, кодируемым HLA аллелем, отличающейся от таковой для второй мутантной GATA3 пептидной последовательности.
В некоторых вариантах осуществления, по меньшей мере одна из первой мутантной GATA3 пептидной последовательности и второй мутантной GATA 3 пептидной последовательности связывается с белком, кодируемым HLA аллелем с аффинностью менее чем 500 нМ.
В некоторых вариантах осуществления, по меньшей мере одна из первой мутантной GATA3 пептидной последовательности и второй мутантной пептидной последовательности связывается с белком, кодируемым HLA аллелем, со стабильностью более 1 часа.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну из следующих последовательностей: (a) TLQRSSLWCL (SEQ ID NO: 5), VLPEPHLAL (SEQ ID NO: 6), HVLPEPHLAL (SEQ ID NO: 7), ALQPLQPHA (SEQ ID NO: 8), AIQPVLWTT (SEQ ID NO: 9), APAIQPVLWTT (SEQ ID NO: 10), SMLTGPPARV (SEQ ID NO: 11), MLTGPPARV (SEQ ID NO: 12), и/или YMFLKAESKI (SEQ ID NO: 13), и/или (b) MFLKAESKI (SEQ ID NO: 14) и/или YMFLKAESKI (SEQ ID NO: 15), и/или (c) VLWTTPPLQH (SEQ ID NO: 16), YMFLKAESK (SEQ ID NO: 17) и/или KIMFATLQR (SEQ ID NO: 18), и/или (d) FATLQRSSL (SEQ ID NO: 19), EPHLALQPL (SEQ ID NO: 20), QPVLWTTPPL (SEQ ID NO: 21), GPPARVPAV (SEQ ID NO: 22), MFATLQRSSL (SEQ ID NO: 23), KPKRDGYMF (SEQ ID NO: 24) и/или KPKRDGYMFL (SEQ ID NO: 25), и/или (e) IMKPKRDGYM (SEQ ID NO: 26), MFATLQRSSL (SEQ ID NO: 27), FLKAESKIMF (SEQ ID NO: 28), LHFCRSSIM (SEQ ID NO: 29), EPHLALQPL (SEQ ID NO: 30), FATLQRSSL (SEQ ID NO: 31), ESKIMFATL (SEQ ID NO: 32), FLKAESKIM (SEQ ID NO: 33) и/или YMFLKAESKI (SEQ ID NO: 34).
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере две из следующих последовательностей: (a) TLQRSSLWCL (SEQ ID NO: 35), VLPEPHLAL (SEQ ID NO: 36), HVLPEPHLAL (SEQ ID NO: 37), ALQPLQPHA (SEQ ID NO: 38), AIQPVLWTT (SEQ ID NO: 39), APAIQPVLWTT (SEQ ID NO: 40), SMLTGPPARV (SEQ ID NO: 41), MLTGPPARV (SEQ ID NO: 42), и/или YMFLKAESKI (SEQ ID NO: 43), и/или (b) MFLKAESKI (SEQ ID NO: 44) и/или YMFLKAESKI (SEQ ID NO: 45), и/или (c) VLWTTPPLQH (SEQ ID NO: 46), YMFLKAESK (SEQ ID NO: 47) и/или KIMFATLQR (SEQ ID NO: 48), и/или (d) FATLQRSSL (SEQ ID NO: 49), EPHLALQPL (SEQ ID NO: 50), QPVLWTTPPL (SEQ ID NO: 51), GPPARVPAV (SEQ ID NO: 52), MFATLQRSSL (SEQ ID NO: 53), KPKRDGYMF (SEQ ID NO: 54) и/или KPKRDGYMFL (SEQ ID NO: 55), и/или (e) IMKPKRDGYM (SEQ ID NO: 56), MFATLQRSSL (SEQ ID NO: 57), FLKAESKIMF (SEQ ID NO: 58), LHFCRSSIM (SEQ ID NO: 59), EPHLALQPL (SEQ ID NO: 60), FATLQRSSL (SEQ ID NO: 61), ESKIMFATL (SEQ ID NO: 62), FLKAESKIM (SEQ ID NO: 63) и/или YMFLKAESKI (SEQ ID NO: 64).
В некоторых вариантах осуществления мутантные GATA3 пептидные последовательности содержат (a) первую мутантную GATA3 пептидную последовательность из (a) и вторую мутантную GATA3 пептидную последовательность из (b), (b) первую мутантную GATA3 пептидную последовательность из (a) и вторую мутантную GATA3 пептидную последовательность из (c), (c) первую мутантную GATA3 пептидную последовательность из (a) и вторую мутантную GATA3 пептидную последовательность из (d), (d) первую мутантную GATA3 пептидную последовательность из (a) и вторую мутантную GATA3 пептидную последовательность из (e), (e) первую мутантную GATA3 пептидную последовательность из (b) и вторую мутантную GATA3 пептидную последовательность из (c), (f) первую мутантную GATA3 пептидную последовательность из (b) и вторую мутантную GATA3 пептидную последовательность из (d), (g) первую мутантную GATA3 пептидную последовательность из (b) и вторую мутантную GATA3 пептидную последовательность из (e), (h) первую мутантную GATA3 пептидную последовательность из (c) и вторую мутантную GATA3 пептидную последовательность из (d), (i) первую мутантную GATA3 пептидную последовательность из (c) и вторую мутантную GATA3 пептидную последовательность из (e), или (j) первую мутантную GATA3 пептидную последовательность из (d) и вторую мутантную GATA3 пептидную последовательность из (e).
В некоторых вариантах осуществления первые мутантные GATA3 пептидные последовательности и вторая мутантная GATA 3 пептидная последовательность содержит пептид из таблицы 5 и/или таблицы 6. В некоторых вариантах осуществления, первая мутантная GATA3 пептидная последовательность содержит первый неоэпитоп белка GATA3 и вторая пептидная мутантная GATA3 пептидная последовательность содержит второй неоэпитоп мутантного белка GATA, где первая мутантная GATA3 пептидная последовательность отличается от второй мутантной GATA3 пептидной последовательности, и где первый неоэпитоп содержит по меньшей мере одну мутантную аминокислоту, и второй неоэпитоп содержит ту же мутантную аминокислоту.
В некоторых вариантах осуществления каждая из первой мутантной GATA3 пептидной последовательности и второй мутантной GATA3 пептидной последовательности, содержащих по меньшей мере восемь непрерывных аминокислот, представленных формулой: [Xaa]F-[Xaa]N-[Xaa]C или [Xaa]N-[Xaa]C-[Xaa]F, где каждый Xaa является аминокислотой, где каждая из [Xaa]N и [Xaa]C содержит аминокислотную последовательность, кодированную разными частями гена GATA3, где [Xaa]F является любой аминокислотной последовательностью, где [Xaa]N кодируется в рамке считывания не дикого типа гена GATA3, где [Xaa]C содержит по меньшей мере одну мутантную аминокислоту и кодируется в рамке считывания не дикого типа гена GATA3, где N является целым числом от 0-100, где C является целым числом от 1-100, где F является целым числом от 0-100, где сумма N и M составляет по меньшей мере 8.
В некоторых вариантах осуществления, каждый Xaa из [Xaa]F является лизиновым остатком, и F является целым числом от 1-100, 1-10, 9, 8, 7, 6, 5, 4, 3, 2 или 1. В некоторых вариантах осуществления, F равно 3, 4 или 5.
В некоторых вариантах осуществления, каждая из мутантных GATA3 пептидных последовательностей присутствует в концентрации по меньшей мере 50 мкг/мл - 400 мкг/мл. В некоторых вариантах осуществления, первые мутантные GATA3 пептидные последовательности и вторая мутантная GATA3 пептидная последовательность содержит последовательность из таблицы 1 или 2. В некоторых вариантах осуществления, композиция дополнительно содержит иммуномодулирующий агент или адьювант. В некоторых вариантах осуществления, адьювантом является полиICLC.
В одном аспекте изобретение относится к фармацевтической композиции, содержащей: одну или более мутантных GATA3 пептидных последовательностей, где одна или более мутантных GATA3 пептидных последовательностей содержит последовательность, выбранную из группы, состоящей из ESKIMFATLQRSSL (SEQ ID NO: 65), KPKRDGYMFLKAESKI (SEQ ID NO: 66), SMLTGPPARVPAVPFDLH (SEQ ID NO: 67), EPCSMLTGPPARVPAVPFDLH (SEQ ID NO: 68), LHFCRSSIMKPKRDGYMFLKAESKI (SEQ ID NO: 69), GPPARVPAVPFDLHFCRSSIMKPKRD (SEQ ID NO: 70), и KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 71).
В некоторых вариантах осуществления одной или более мутантными GATA3 пептидными последовательностями является ESKIMFATLQRSSL (SEQ ID NO: 72). В некоторых вариантах осуществления, одной или более мутантными GATA3 пептидными последовательностями является KPKRDGYMFLKAESKI (SEQ ID NO: 73). В некоторых вариантах осуществления, одной или более мутантными GATA3 пептидными последовательностями является SMLTGPPARVPAVPFDLH (SEQ ID NO: 74). В некоторых вариантах осуществления, одной или более мутантными GATA3 пептидными последовательностями является EPCSMLTGPPARVPAVPFDLH (SEQ ID NO: 75). В некоторых вариантах осуществления, одной или более мутантными GATA3 пептидными последовательностями является LHFCRSSIMKPKRDGYMFLKAESKI (SEQ ID NO: 76). В некоторых вариантах осуществления, одной или более мутантными GATA3 пептидными последовательностями является GPPARVPAVPFDLHFCRSSIMKPKRD (SEQ ID NO: 77). В некоторых вариантах осуществления, одной или более мутантными GATA3 пептидными последовательностями является KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 78).
В некоторых вариантах осуществления, фармацевтическая композиция содержит pH модификатор, присутствующий в концентрации от 0,1 мМ - 1 мМ. В некоторых вариантах осуществления, фармацевтическая композиция содержит pH модификатор, присутствующий в концентрации от 1 мМ - 10 мМ.
В одном аспекте изобретение относится к способу синтеза GATA3 пептида, где пептид содержит последовательность из, по меньшей мере двух непрерывных аминокислот, выбранных из группы, состоящей из Xaa-Cys, Xaa-Ser и Xaa-Thr, где Xaa является любой аминокислотой, где способ включает: (a) сочетание по меньшей мере одного ди-пептида или его производного с аминокислотой или ее производным GATA3 пептида или его производного с получением псевдо-пролина, содержащего GATA3 пептид или его производное, где дипептид или его производное содержит псевдо-пролиновую группу, (b) сочетание одной или более выбранных аминокислот, малых пептидов или их производных с псевдо-пролином, содержащим GATA3 пептид или его производное, и (c) отщепление псевдо-пролина, содержащего GATA3 пептид или его производное от смолы. В некоторых вариантах осуществления, способ включает снятие защиты с псевдо-пролина, содержащего GATA3 пептид, или его производного.
В некоторых вариантах осуществления, аминокислоту или ее производное, с которой сочетается по меньшей мере один дипептид или его производное, выбирают из группы, состоящей из Ala, Cys, Asp, Glu, Phe, Gly, Ile, Lys, Leu, Met, Asn, Pro, Gln, Arg, Ser, Thr, Trp, Tyr, His и Val. В некоторых вариантах осуществления, одна или более выбранных аминокислот, малых пептидов или их производных, необязательно сопряженных с псевдо-пролином, содержащим GATA3 пептид или его производное, содержат Fmoc-Ala-OH∙H2O, Fmoc-Cys(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asp(OMpe)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Phe-OH, Fmoc-Gly-OH, Fmoc-Ile-OH, Fmoc-Lys(Boc)-OH, Fmoc-Leu-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Pro-OH, Fmoc-Gln(Trt)-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Trp(Boc)-OH, Fmoc-Tyr(tBu)-OH, Fmoc-Val-OH, Fmoc-His(Trt)-OH и Fmoc-His(Boc)-OH.
В некоторых вариантах осуществления, N-концевая аминокислота или ее производное GATA3 пептида или его производного выбрана из группы, состоящей из Fmoc-Ala-OH∙H2O, Fmoc-Cys(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asp(OMpe)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Phe-OH, Fmoc-Gly-OH, Fmoc-Ile-OH, Fmoc-Lys(Boc)-OH, Fmoc-Leu-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Pro-OH, Fmoc-Gln(Trt)-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Trp(Boc)-OH, Fmoc-Tyr(tBu)-OH, Fmoc-Val-OH, Fmoc-His(Trt)-OH и Fmoc-His(Boc)-OH.
В некоторых вариантах осуществления, псевдо-пролиновой группой является (a) Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH, (b) Fmoc-Ala-Thr(psi(Me,Me)pro)-OH, (c) Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH, (d) Fmoc-Leu-Thr(psi(Me,Me)pro)-OH, (e) Fmoc-Leu-Cys(psi(Dmp,H)pro)-OH. В некоторых вариантах осуществления, (a) Xaa-Ser является Ser-Ser, (b) Xaa-Ser является Glu-Ser, (c) Xaa-Thr является Ala-Thr, (d) Xaa-Thr является Leu-Thr или (e) Xaa-Cys является Leu-Cys.
В одном аспекте изобретение относится к способу лечения онкологического субъекта, включающему введение субъекту заявленной фармацевтической композиции по любому из аспектов, описанных выше.
В одном аспекте изобретение относится к способу идентификации онкологического субъекта как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодируемый HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем, где терапевтическое средство содержит (a) по меньшей мере один полипептид, содержащий одну или более мутантных GATA3 пептидных последовательностей, где каждая из одной или более мутантных GATA3 пептидных последовательностей содержит по меньшей мере одну мутантную аминокислоту и является фрагментом, по меньшей мере 8 непрерывных аминокислот мутантного GATA3 белка, возникающего при мутации в гене GATA3 раковой клетки; или (b) по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид, где каждая из одной или более мутантных GATA3 пептидных последовательностей или их частей связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем. В некоторых вариантах осуществления, способ дополнительно включает введение терапевтического агента субъекту.
В одном аспекте изобретение относится к способу лечения онкологического субъекта, включающему введение субъекту фармацевтической композиции, содержащей: (a) по меньшей мере один полипептид, содержащий первую мутантную GATA3 пептидную последовательность и вторую мутантную GATA3 пептидную последовательность, где (i) первая мутантная GATA3 пептидная последовательность и вторая мутантная GATA3 пептидная последовательность каждая содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1, и (ii) C-концевая последовательность первой мутантной GATA3 пептидной последовательности перекрывается с N-концевой последовательностью второй мутантной GATA3 пептидной последовательности; где по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1 содержат по меньшей мере одну аминокислоту с последовательностью PGRPLQTHVLPEPHLALQPLQPHADHAHADAPAIQPVLWTTPPLQHGHRHGLEPCSMLTGPPARVPAVPFDLHFCRSSIMKPKRDGYMFLKAESKIMFAT LQRSSLWCLCSNH (SEQ ID NO: 2), или (b) по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид, где HLA аллели, экспрессированные субъектом, являются неизвестными во время введения.
В некоторых вариантах осуществления, по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1 содержат по меньшей мере одну аминокислоту с последовательностью: PGRPLQTHVLPEPHLALQPLQPHADHAHADAPAIQPVLWTTPPLQHGHRHGLEPCSMLTGPPARVPAVPFDLHFCRSSIMKPKRDGYMFLKAESKIMFAT LQRSSLWCLCSNH (SEQ ID NO: 2).
В некоторых вариантах осуществления, рак выбран из группы, состоящей из меланомы, рака яичников, рака легких, рака предстательной железы, рака молочной железы, рака прямой кишки, рака эндометрия и хронического лимфолейкоза (ХЛЛ). В некоторых вариантах осуществления, субъект имеет рак молочной железы, устойчивый к антиэстрогеновой терапии, рак молочной железы MSI, метастатический рак молочной железы, Her2 отрицательный рак молочной железы, Her2 положительный рак молочной железы, ER отрицательный рак молочной железы, ER положительный рак молочной железы, PR положительный рак молочной железы, PR отрицательный рак молочной железы или любую их комбинацию.
В некоторых вариантах осуществления, рак молочной железы экспрессирует рецептор эстрогена с мутацией. В некоторых вариантах осуществления, способ аспектов, описанных выше, дополнительно включает введение по меньшей мере одного дополнительного терапевтического агента или способа воздействия. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом или способом воздействия является хирургическое вмешательство, ингибитор контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т-клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент, анти-CD40 агент, летрозол, фулвестрант, ингибитор PI3 киназы и/или ингибитор CDK 4/6. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является палбоциклиб, рибоциклиб, абемациклиб, селициклиб, динациклиб, милциклиб, ронициклиб, атувециклиб, брициклиб, ривициклиб, селициклиб, трилациклиб, воруциклиб или любая их комбинация.
В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является палбоциклиб (PD0332991); абемациклиб (LY2835219); рибоциклиб (LEE 011); варуциклиб (P1446A-05); фаскаплисин; арцириафлавин; 2-бром-12,13-дигидро-5H-индоло[2,3-a]пирроло[3,4-c]карбазол-5,7(6H)-дион; 3-аминотиоакридон (3-ATA), транс-4-((6-(этиламино)-2-((1-(фенилметил)-1H-индол-5-ил)амино)-4-пиримидинил)амино)циклогексано (CINK4); 1,4-диметоксиакридин-9(10H)-тион (NSC 625987); 2-метил-5-(p-толиламино)бензо[d] тиазол-4,7-дион (риувидин); флавопиридол (альвоцидиб); селициклиб; динациклиб; милциклиб; ронициклиб; атувециклиб; брициклиб; ривициклиб; трилациклиб (G1T28); или любая их комбинация.
В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, BDPX-696, воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136.
В некоторых вариантах осуществления, раком является рецидивирующий или метастатический рак молочной железы. В некоторых вариантах осуществления субъектом является субъект, у которого наблюдалось прогрессирование заболевания после эндокринной терапии в сочетании с ингибитором CDK 4/6; или где субъект ранее не получал системную терапию. В некоторых вариантах осуществления способ включает определение статуса мутации гена рецептора эстрогена в клетке субъекта. В некоторых вариантах осуществления клетками являются выделенные клетки или клетки, обогащенные для экспрессии рецептора эстрогена.
В некоторых аспектах изобретение относится к композиции, содержащей по меньшей мере один полипептид, содержащий одну или более мутантных GATA3 пептидных последовательностей, каждая из одной или более мутантных GATA3 пептидных последовательностей содержит по меньшей мере одну мутантную аминокислоту, и является фрагментом, по меньшей мере 8 непрерывных аминокислот мутантного GATA3 белка, возникающего при мутации в гене GATA3 раковой клетки; по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид; одну или более APC, содержащих по меньшей мере один полипептид; или T-клеточный рецептор (TCR), специфический для неоэпитопа по меньшей мере одного полипептида в комплексе с HLA белком.
В некоторых вариантах осуществления, одна или более мутантных GATA3 пептидных последовательностей содержит две или более мутантных GATA3 пептидных последовательностей. В некоторых вариантах осуществления, каждая из одной или более мутантных GATA3 пептидных последовательностей содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1 или 2.
В некоторых аспектах изобретение относится к композиции, содержащей по меньшей мере один полипептид, содержащий две или более мутантных GATA3 пептидных последовательностей, где каждая из двух или нескольких мутантных GATA3 пептидных последовательностей содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1, и C-концевая последовательность первой GATA3 пептидной последовательности перекрывается с N-концевой последовательностью второй GATA3 пептидной последовательности; по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид одной или более APC, содержащих по меньшей мере один полипептид; или T-клеточный рецептор (TCR), специфический для неоэпитопа, по меньшей мере одного полипептида в комплексе с HLA белком.
В некоторых вариантах осуществления, мутантная GATA3 пептидная последовательность содержит фрагмент мутантного GATA3 белка, возникающего при мутации «сдвига рамки» в гене GATA3 раковой клетки. В некоторых вариантах осуществления, по меньшей мере 8 непрерывных аминокислот содержит по меньшей мере одну аминокислоту, кодированную GATA3 neoORF последовательностью. В некоторых вариантах осуществления, мутацией в GATA3 гене раковой клетки является мутация «сдвига рамки». В некоторых вариантах осуществления, мутацией в GATA3 гене раковой клетки является миссенс-мутация, мутация сайта сплайсинга или мутация слияния генов. В некоторых вариантах осуществления, каждая из мутантных GATA3 пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 мутантных аминокислот.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере 3, 4, 5, 6, 7, 8, 9, или 10 мутантных GATA3 пептидных последовательностей. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере два полипептида, или по меньшей мере один полинуклеотид содержит по меньшей мере два полинуклеотида. В некоторых вариантах осуществления, по меньшей мере одна из одной или более GATA3 пептидных последовательностей или, по меньшей мере одна из двух или нескольких GATA3 пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, или 40 непрерывных аминокислот белка GATA3. В некоторых вариантах осуществления, по меньшей мере две из GATA3 пептидных последовательностей содержат по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот белка GATA3.
В некоторых вариантах осуществления, каждая из GATA3 пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот GATA3 белка. В некоторых вариантах осуществления, по меньшей мере одна из двух или нескольких мутантных GATA3 пептидных последовательностей содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2. В некоторых вариантах осуществления, по меньшей мере 3, 4, 5, 6, 7, 8, 9, или 10 из двух или нескольких мутантных GATA3 пептидных последовательностей содержат по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2. В некоторых вариантах осуществления, каждая из одной из двух или нескольких мутантных GATA3 пептидных последовательностей содержат по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 2. В некоторых вариантах осуществления, по меньшей мере одна из двух или нескольких мутантных GATA3 пептидных последовательностей содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 3.
В некоторых вариантах осуществления, по меньшей мере одна из по меньшей мере 8 непрерывных аминокислот является аминокислотой SEQ ID NO: 4. В некоторых вариантах осуществления, непрерывная аминокислота из по меньшей мере 8 непрерывных аминокислот, не является аминокислотой SEQ ID NO: 4. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную GATA3 пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную GATA3 пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым: HLA-A02:01 аллелем и HLA-A24:02 аллелем; HLA-A02:01 аллелем и HLA-B08:01 аллелем; HLA-A24:02 аллелем и HLA-B08:01 аллелем; или HLA-A02:01 аллелем, HLA-A24:02 аллелем и HLA-B08:01 аллелем.
В некоторых вариантах осуществления, две или более мутантных GATA3 пептидных последовательностей содержат первую мутантную GATA3 пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем или HLA-B08:01 аллелем; и вторую GATA3 пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем или HLA-B08:01 аллелем; где первая мутантная GATA3 пептидная последовательность связывается или предположительно связывается с белком, кодируемым HLA аллелем, отличающейся от таковой для второй мутантной GATA3 пептидной последовательности.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную GATA3 пептидную последовательность, которая связывается с белком, кодируемым HLA аллелем с аффинностью менее чем 10 мкМ, менее чем 1 мкМ, менее чем 500 нМ, менее чем 400 нМ, менее чем 300 нМ, менее чем 250 нМ, менее чем 200 нМ, менее чем 150 нМ, менее чем 100 нМ, или менее чем 50 нМ. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную GATA3 пептидную последовательность, которая связывается с белком, кодируемым HLA аллелем со стабильностью более 24 часов, более 12 часов, более 9 часов, более 6 часов, более 5 часов, более 4 часа, более 3 часа, более 2 часов, более 1 часа, более 45 минут, более 30 минут, более 15 минут или более 10 минут. В некоторых вариантах осуществления, HLA аллель выбрана из группы, состоящей из HLA-A02:01, HLA-A24:02, HLA-A03:01, HLA-B07:02, HLA-B08:01 и любой их комбинации.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну из следующих последовательностей: TLQRSSLWCL (SEQ ID NO: 79), VLPEPHLAL (SEQ ID NO: 80), HVLPEPHLAL (SEQ ID NO: 81), ALQPLQPHA (SEQ ID NO: 82), AIQPVLWTT (SEQ ID NO: 83), APAIQPVLWTT (SEQ ID NO: 84), SMLTGPPARV (SEQ ID NO: 85), MLTGPPARV (SEQ ID NO: 86), и/или YMFLKAESKI (SEQ ID NO: 87); и/или MFLKAESKI (SEQ ID NO: 88) и/или YMFLKAESKI (SEQ ID NO: 89), VLWTTPPLQH (SEQ ID NO: 90), YMFLKAESK (SEQ ID NO: 91) и/или KIMFATLQR (SEQ ID NO: 92); и/или FATLQRSSL (SEQ ID NO: 93), EPHLALQPL (SEQ ID NO: 94), QPVLWTTPPL (SEQ ID NO: 95), GPPARVPAV (SEQ ID NO: 96), MFATLQRSSL (SEQ ID NO: 97), KPKRDGYMF (SEQ ID NO: 98) и/или KPKRDGYMFL(SEQ ID NO: 99) и/или IMKPKRDGYM (SEQ ID NO: 100), MFATLQRSSL (SEQ ID NO: 101), FLKAESKIMF (SEQ ID NO: 102), LHFCRSSIM (SEQ ID NO: 103), EPHLALQPL (SEQ ID NO: 104), FATLQRSSL (SEQ ID NO: 105), ESKIMFATL (SEQ ID NO: 106), FLKAESKIM (SEQ ID NO: 107) и/или YMFLKAESKI (SEQ ID NO: 108).
В некоторых вариантах осуществления, две или более мутантных GATA3 пептидных последовательностей содержат по меньшей мере две из следующих последовательностей: TLQRSSLWCL (SEQ ID NO: 109), VLPEPHLAL (SEQ ID NO: 110), HVLPEPHLAL (SEQ ID NO: 111), ALQPLQPHA (SEQ ID NO: 112), AIQPVLWTT (SEQ ID NO: 113), APAIQPVLWTT (SEQ ID NO: 114), SMLTGPPARV (SEQ ID NO: 115), MLTGPPARV (SEQ ID NO: 116), и/или YMFLKAESKI (SEQ ID NO: 117); и/или MFLKAESKI (SEQ ID NO: 118) и/или YMFLKAESKI (SEQ ID NO: 119), VLWTTPPLQH (SEQ ID NO: 120), YMFLKAESK (SEQ ID NO: 121) и/или KIMFATLQR (SEQ ID NO: 122); и/или FATLQRSSL (SEQ ID NO: 123), EPHLALQPL (SEQ ID NO: 124), QPVLWTTPPL (SEQ ID NO: 125), GPPARVPAV (SEQ ID NO: 126), MFATLQRSSL (SEQ ID NO: 127), KPKRDGYMF (SEQ ID NO: 128) и/или KPKRDGYMFL (SEQ ID NO: 129) и/или IMKPKRDGYM (SEQ ID NO: 130), MFATLQRSSL (SEQ ID NO: 131), FLKAESKIMF (SEQ ID NO: 132), LHFCRSSIM (SEQ ID NO: 133), EPHLALQPL (SEQ ID NO: 134), FATLQRSSL (SEQ ID NO: 135), ESKIMFATL (SEQ ID NO: 136), FLKAESKIM (SEQ ID NO: 137) и/или YMFLKAESKI (SEQ ID NO: 138).
В некоторых вариантах осуществления, мутантные GATA3 пептидные последовательности содержат по меньшей мере две из следующих последовательностей: EPCSMLTGPPARVPAVPFDLH (SEQ ID NO: 139), SMLTGPPARVPAVPFDLH (SEQ ID NO: 140), GPPARVPAVPFDLHFCRSSIMKPKRD (SEQ ID NO: 141), DLHFCRSSIMKPKRDGYMFLKAESKI (SEQ ID NO: 142), KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 143), FLKAESKIMFATLQRS (SEQ ID NO: 144) и KPKRDGYMFLKAESKI (SEQ ID NO: 145).
В некоторых вариантах осуществления, мутантные GATA3 пептидные последовательности содержат по меньшей мере две последовательности их таблицы 5 и/или таблицы 6. В некоторых вариантах осуществления, первая мутантная GATA3 пептидная последовательность из двух или нескольких мутантных GATA3 пептидных последовательностей содержит первый неоэпитоп GATA3 белка, и вторая пептидная мутантная GATA3 пептидная последовательность содержит второй неоэпитоп мутантного GATA3 белка, где первая мутантная GATA3 пептидная последовательность отличается от мутантной GATA3 пептидной последовательности, и где первый неоэпитоп содержит по меньшей мере одну мутантную аминокислоту, и второй неоэпитоп содержит ту же мутантную аминокислоту.
В некоторых аспектах изобретение относится к композиции, содержащей, по меньшей мере один полипептид, содержащий одну или более мутантных GATA3 пептидных последовательностей, где по меньшей мере один полипептид представлен формулой [Xaa]F-[Xaa]N-[Xaa]C, где каждая Xaa независимо является любой аминокислотой, где [Xaa]N-[Xaa]C представляет одну или более мутантных GATA3 пептидных последовательностей, где каждая из [Xaa]N и [Xaa]C содержит непрерывную аминокислотную последовательность, кодированную разными частями гена GATA3, где [Xaa]N кодируется рамкой считывания не дикого типа, где [Xaa]C содержит по меньшей мере одну мутантную аминокислоту и кодируется рамкой считывания не дикого типа, где N является целым числом от 0-100, где C является целым числом от 1-100, где F является целым числом от 0-100, где сумма N и M составляет по меньшей мере 8.
В некоторых вариантах осуществления, каждая из мутантных GATA3 пептидных последовательностей, по меньшей мере восемь непрерывных аминокислот, представлены формулой [Xaa]F-[Xaa]N-[Xaa]C или [Xaa]N-[Xaa]C-[Xaa]F, где каждая Xaa является аминокислотой, где каждая из [Xaa]N и [Xaa]C содержат аминокислотную последовательность, кодированную разными частями гена GATA3, где [Xaa]F является любой аминокислотной последовательностью, где [Xaa]N кодируется в рамке считывания не дикого типа гена GATA3, где [Xaa]C содержит по меньшей мере одну мутантную аминокислоту и кодируется в рамке считывания не дикого типа гена GATA3, где N является целым числом от 0-100, где C является целым числом от 1-100, где F является целым числом от 0-100, где сумма N и M составляет по меньшей мере 8. В некоторых вариантах осуществления, каждая Xaa из [Xaa]F является лизиновым остатком, и F является целым числом от 1-100, 1-10, 9, 8, 7, 6, 5, 4, 3, 2 или 1. В некоторых вариантах осуществления, F равно 3, 4 или 5.
В некоторых вариантах осуществления, по меньшей мере одна мутантная аминокислота содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных мутантных аминокислот. В некоторых вариантах осуществления, каждая из мутантных GATA3 пептидных последовательностей присутствует в концентрации, по меньшей мере 1 мкг/мл, по меньшей мере 10 мкг/мл, по меньшей мере 25 мкг/мл, по меньшей мере 50 мкг/мл, по меньшей мере 100 мкг/мл, по меньшей мере 200 мкг/мл, по меньшей мере 250 мкг/мл, по меньшей мере 300 мкг/мл или по меньшей мере 400 мкг/мл. В некоторых вариантах осуществления, каждая из мутантных GATA3 пептидных последовательностей присутствует в концентрации самое большее 5000 мкг/мл, самое большее 2500 мкг/мл, самое большее 1000 мкг/мл, самое большее 750 мкг/мл, самое большее 500 мкг/мл, самое большее 400 мкг/мл, или самое большее 300 мкг/мл. В некоторых вариантах осуществления, каждая из мутантных GATA3 пептидных последовательностей присутствует в концентрации от 10 мкг/мл до 5000 мкг/мл, 10 мкг/мл до 4000 мкг/мл, 10 мкг/мл до 3000 мкг/мл, 10 мкг/мл до 2000 мкг/мл, 10 мкг/мл до 1000 мкг/мл, 25 мкг/мл до 500 мкг/мл, 50 мкг/мл до 500 мкг/мл, 100 мкг/мл до 500 мкг/мл, 200 мкг/мл до 500 мкг/мл, 200 мкг/мл до 400 мкг/мл или 3000 мкг/мл до 400 мкг/мл.
В некоторых вариантах осуществления, композиция дополнительно включает иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, адъювантом является полиICLC. В некоторых аспектах изобретение относится к фармацевтической композиции, содержащей описанную здесь композицию и фармацевтически приемлемый эксципиент. В некоторых вариантах осуществления, фармацевтическая композиция содержит pH модификатор, присутствующий в концентрации менее чем 1 мМ или более 1 мМ. В некоторых вариантах осуществления, фармацевтическая композиция является вакцинной композицией. В некоторых вариантах осуществления, фармацевтическая композиция является водной.
В некоторых вариантах осуществления, один или более из по меньшей мере одного полипептида связан pI>5 и HYDRO >-6, pI>8 и HYDRO >-8, pI<5 и HYDRO >-5, pI>9 и HYDRO <-8, pI >7 и HYDRO значение >-5,5, pI < 4,3 и -4≥HYDRO≥-8, pI>0 и HYDRO<-8, pI>0 и HYDRO >-4, или pI>4,3 и -4≥HYDRO≥-8, pI>0 и HYDRO>-4, или pI>4,3 и HYDRO≤-4, pI>0 и HYDRO>-4, или pI>4,3 и -4≥HYDRO≥-9, 5≥pI ≥12 и -4≥HYDRO≥-9.
В некоторых вариантах осуществления, pH модификатором является основание. В некоторых вариантах осуществления модификатором pH является конъюгат основания слабой кислоты. В некоторых вариантах осуществления, модификатором pH является фармацевтически приемлемая соль. В некоторых вариантах осуществления, модификатором pH является дикарбоксилат или трикарбоксилат. В некоторых вариантах осуществления, модификатором pH является лимонная кислота и/или цитрат. В некоторых вариантах осуществления, цитратом является цитрат динатрия и/или цитрат тринатрия. В некоторых вариантах осуществления, модификатором pH является янтарная кислота и/или сукцинат. В некоторых вариантах осуществления, сукцинатом является сукцинат динатрия и/или сукцинат мононатрия. В некоторых вариантах осуществления, сукцинатом является гексагидрат сукцината. В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 0,1 мМ - 10 мМ. В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 0,1 мМ - 5 мМ. В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 0,1 мМ - 1 мМ. В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 1 мМ - 10 мМ. В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 1 мМ - 5 мМ.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит жидкость. В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит воду. В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит сахар. В некоторых вариантах осуществления, сахар содержит декстрозу или маннит. В некоторых вариантах осуществления, декстроза или маннит присутствует в концентрации от 1-10% масс./об.. В некоторых вариантах осуществления, сахар содержит трегалозу. В некоторых вариантах осуществления, сахар содержит сахарозу. В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит диметилсульфоксид (ДМСО).
В некоторых вариантах осуществления, ДМСО присутствует в концентрации от 0,1% - 10%, 0,5% - 5%, 1% - 5%, 2% - 5%, 2% - 4% или 2% - 4%. В некоторых вариантах осуществления, фармацевтически приемлемый носитель не содержит диметилсульфоксид (ДМСО). В некоторых вариантах осуществления, фармацевтическая композиция является лиофилизируемой. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулятор или адъювант. В некоторых вариантах осуществления, иммуномодулятор или адъювант выбран из группы, состоящей из поли-ICLC, 1018 ISS, солей алюминия, Ампливакса, AS15, BCG, CP-870,893, CpG7909, CyaA, ARNAX, агонистов STING, dSLIM, GM-CSF, IC30, IC31, Имиквимода, ImuFact IMP321, IS Patch, ISS, ISCOMATRIX, Juvlmmune, LipoVac, MF59, монофосфориллипида A, Монтанида IMS 1312, Монтанида ISA 206, Монтанида ISA 50V, Монтанида ISA-51, OK-432, OM-174, OM-197-MP-EC, ONTAK, PepTel®, системы векторов, PLGA микрочастиц, резиквимода, SRL172, Виросом и других вирусоподобных частиц, YF-17D, VEGF ловушки, R848, бета-глюкана, Pam3Cys, и Aquila’s QS21 стимулона.
В некоторых вариантах осуществления, иммуномодулятор или адъювант содержит поли-ICLC. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет от 2:1 до 1:10 об.:об. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет примерно 1:1, 1:1,5, 1:2, 1:3, 1:4 или 1:5 об.:об. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет примерно 1:3 об.:об.
В некоторых аспектах изобретение относится к способу синтеза GATA3 пептида, где пептид содержит последовательность, по меньшей мере двух непрерывных аминокислот, выбранных из группы, состоящей из Xaa-Cys, Xaa-Ser и Xaa-Thr, где Xaa является любой аминокислотой, где способ включает: сочетание по меньшей мере одного ди-пептида или его производного с аминокислотой или ее производным GATA3 пептида или его производного с получением псевдо-пролина, содержащего GATA3 пептид или его производные, где дипептид или его производное содержит псевдо-пролиновую группу; сочетание одной или более выбранных аминокислот, малых пептидов или их производных с псевдо-пролином, содержащим GATA3 пептид или его производное; и отщепление псевдо-пролина, содержащего GATA3 пептид или его производное, от смолы.
В некоторых вариантах осуществления, способ включает снятие защиты с псевдо-пролина, содержащего GATA3 пептид или его производное. В некоторых вариантах осуществления, GATA3 пептидом является пептид из по меньшей мере одного полипептида композиции, описанной в настоящем документе, или фармацевтической композиции. В некоторых вариантах осуществления, N-концевая аминокислота или ее производное GATA3 пептида или его производного, присоединена к смоле. В некоторых вариантах осуществления, смолой является смола Ванга или 2-хлортритиловая смола (2-Cl-Trt смола). В некоторых вариантах осуществления, исходным материалом для сочетания является Fmoc-His(Trt)-Wang смола, H-His(Trt)-2Cl-Trt смола, Fmoc-Asp(OtBu)-Wang смола, Fmoc-Ile-Wang смола, Fmoc-Ser(tBu)-Wang смола или Fmoc-Leu-Wang смола. В некоторых вариантах осуществления, аминокислота или ее производное, в которой сопряжен, по меньшей мере один дипептид или его производное, выбрана из группы, состоящей из Ala, Cys, Asp, Glu, Phe, Gly, Ile, Lys, Leu, Met, Asn, Pro, Gln, Arg, Ser, Thr, Trp, Tyr, His и Val.
В некоторых вариантах осуществления, одна или более выбранных аминокислот, малых пептидов или их производных, необязательно сопряженных с псевдо-пролином, содержащим GATA3 пептид или его производное, содержит Fmoc-Ala-OH∙H2O, Fmoc-Cys(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asp(OMpe)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Phe-OH, Fmoc-Gly-OH, Fmoc-Ile-OH, Fmoc-Lys(Boc)-OH, Fmoc-Leu-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Pro-OH, Fmoc-Gln(Trt)-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Trp(Boc)-OH, Fmoc-Tyr(tBu)-OH, Fmoc-Val-OH, Fmoc-His(Trt)-OH и Fmoc-His(Boc)-OH.
В некоторых вариантах осуществления, N-концевая аминокислота или ее производное GATA3 пептида или его производного выбрана из группы, состоящей из Fmoc-Ala-OH∙H2O, Fmoc-Cys(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asp(OMpe)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Phe-OH, Fmoc-Gly-OH, Fmoc-Ile-OH, Fmoc-Lys(Boc)-OH, Fmoc-Leu-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Pro-OH, Fmoc-Gln(Trt)-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Trp(Boc)-OH, Fmoc-Tyr(tBu)-OH, Fmoc-Val-OH, Fmoc-His(Trt)-OH и Fmoc-His(Boc)-OH.
В некоторых вариантах осуществления, псевдо-пролиновой группой является Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH. В некоторых вариантах осуществления, псевдо-пролиновой группой является Fmoc-Ala-Thr(psi(Me,Me)pro)-OH. В некоторых вариантах осуществления, псевдо-пролиновой группой является Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH. В некоторых вариантах осуществления, псевдо-пролиновой группой является Fmoc-Leu- Thr(psi(Me,Me)pro)-OH. В некоторых вариантах осуществления, псевдо-пролиновой группой является Fmoc-Leu-Cys(psi(Dmp,H)pro)-OH.
В некоторых вариантах осуществления, Xaa-Ser является Ser-Ser. В некоторых вариантах осуществления, Xaa-Ser является Glu-Ser. В некоторых вариантах осуществления, Xaa-Thr является Ala-Thr. В некоторых вариантах осуществления, Xaa-Thr является Leu-Thr. В некоторых вариантах осуществления, Xaa-Cys является Leu-Cys.
В некоторых аспектах изобретение относится к способу лечения онкологического субъекта, включающему введение субъекту фармацевтической композиции, описанной в настоящем изобретении.
В некоторых аспектах изобретение относится к способу идентификации онкологического субъекта как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодируемый HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем, где терапевтический агент содержит по меньшей мере один полипептид содержащий одну или более мутантных GATA3 пептидных последовательностей, где каждая из одной или более мутантных GATA3 пептидных последовательностей содержит по меньшей мере одну мутантную аминокислоту и является фрагментом, по меньшей мере 8 непрерывных аминокислот мутантного GATA3 белка, возникающего при мутации в гене GATA3 раковой клетки; по меньшей мере одни полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид; одну или более APC, содержащую, по меньшей мере один полипептид; или Т-клеточный рецептор (TCR), специфический к, по меньшей мере одному полипептиду в комплексе с HLA белком; где каждая из одной или более мутантных GATA3 пептидных последовательностей или их часть связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем. В некоторых вариантах осуществления, способ дополнительно включает введение терапевтического агента субъекту.
В некоторых аспектах изобретение относится к способу лечения онкологического субъекта, включающему введение субъекту композиции, содержащей: по меньшей мере один полипептид, содержащий одну или более мутантных GATA3 пептидных последовательностей, где каждая из одной или более мутантных GATA3 пептидных последовательностей содержит по меньшей мере одну мутантную аминокислоту и является фрагментом, по меньшей мере 8 непрерывных аминокислот мутантного GATA3 белка, возникающего при мутации в гене GATA3 раковой клетки; по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид; одну или более APC, содержащую, по меньшей мере один полипептид; или Т-клеточный рецептор (TCR), специфический к неоэпитопу, по меньшей мере одного полипептида в комплексе с HLA белком; где мутантный GATA3 пептид или его часть связывается с белком, кодируемым HLA-A02:01 аллелем, HLA-A24:02 аллелем, HLA-A03:01 аллелем, HLA-B07:02 аллелем и/или HLA-B08:01 аллелем; где субъект идентифицирован как экспрессирующий HLA-A02:01 аллель, HLA-A24:02 аллель, HLA-A03:01 аллель, HLA-B07:02 аллель и/или HLA-B08:01 аллель.
В некоторых аспектах изобретение относится к способу лечения онкологического субъекта, включающему введение субъекту композиции, содержащей, по меньшей мере один полипептид, содержащий две или более мутантных GATA3 пептидных последовательностей, где каждая из двух нескольких мутантных GATA3 пептидных последовательностей содержит по меньшей мере 8 непрерывных аминокислот SEQ ID NO: 1, и C-концевая последовательность первой GATA3 пептидной последовательности перекрывается с N-концевой последовательностью второй GATA3 пептидной последовательности; по меньшей мере один полинуклеотид, содержащий последовательность, кодирующую по меньшей мере один полипептид; одну или более APC, содержащую, по меньшей мере один полипептид; или Т-клеточный рецептор (TCR), специфический к, неоэпитопу, по меньшей мере одного полипептида в комплексе с HLA белком; где HLA аллели, экспрессированные субъектом, являются неизвестными в момент введения.
В некоторых вариантах осуществления, иммунный ответ вызывается у субъекта. В некоторых вариантах осуществления, иммунным ответом является гуморальный ответ. В некоторых вариантах осуществления, мутантные GATA3 пептидные последовательности вводят одновременно, отдельно или последовательно. В некоторых вариантах осуществления, первый пептид вводят последовательно после периода времени, достаточного для второго пептида для активации вторых Т-клеток. В некоторых вариантах осуществления, рак выбран из группы, состоящей из меланомы, рака яичников, рака легких, рака предстательной железы, рака молочной железы, рака прямой кишки, рака эндометрия и хронического лимфолейкоза (ХЛЛ). В некоторых вариантах осуществления, субъект имеет рак молочной железы, устойчивый к антиэстрогеновой терапии, рак молочной железы MSI, метастатический рак молочной железы, Her2 отрицательный рак молочной железы, Her2 положительный рак молочной железы, ER отрицательный рак молочной железы, ER положительный рак молочной железы, PR положительный рак молочной железы, PR отрицательный рак молочной железы или любую их комбинацию. В некоторых вариантах осуществления, рак молочной железы экспрессирует рецептор эстрогена с мутацией. В некоторых вариантах осуществления, способ дополнительно включает введение по меньшей мере одного дополнительно терапевтического агента или способа воздействия.
В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом или способом воздействия является хирургическое вмешательство, ингибитор контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т-клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент, анти-CD40 агент, летрозол, фулвестрант, ингибитор PI3 киназы и/или ингибитор CDK 4/6. В некоторых вариантах осуществления, по меньшей мере один дополнительный терапевтический агент выбран из группы, состоящей из палбоциклиба (PD0332991); абемациклиба (LY2835219); рибоциклиба (LEE 011); воруциклиба (P1446A-05); фаскаплисина; арцириафлавина; 2-бром-12,13-дигидро-5H-индоло[2,3-a]пирроло[3,4-c]карбазол-5,7(6H)-диона; 3-аминотиоакридона (3-ATA), транс-4-((6-(этиламино)-2-((1-(фенилметил)-1H-индол-5-ил)амино)-4-пиримидинил)амино)циклогексано (CINK4); 1,4-диметоксиакридин-9(10H)-тиона (NSC 625987); 2-метил-5-(p-толиламино)бензо[d]тиазол-4,7-диона (риувидина); и флавопиридола (альвоцидиба); селициклиба; динациклиба; милциклиба; ронициклиба; атувециклиба; брициклиба; ривициклиба; трилациклиба (G1T28); или любой их комбинации.
В некоторых вариантах осуществления, дополнительный терапевтический агент вводя до, одновременно с или после введения мутантных GATA3 пептидных последовательностей. В некоторых вариантах осуществления, введение включает введение подкожно или внутривенно. В некоторых вариантах осуществления, раком является рецидивирующий или метастатический рак молочной железы. В некоторых вариантах осуществления, субъектом является субъект, у которого наблюдалось прогрессирование заболевания после эндокринной терапии в комбинации с ингибитором CDK 4/6.
Мутацией, общей для ХЛЛ и некоторых лимфом, является изменение цистеина на серин в положении (C481S) в гене BTK (тирозинкиназы Брутона). Мутация расположена в области, имеющей аминокислотную последовательность: IFIITEYMANGSLLNYLREMRHR (SEQ ID NO: 146), мутированный серин подчеркнут. Это изменение дает множество связывающих пептидов, которые связываются и диапазоном HLA молекул.
В одном аспекте изобретение относится к композиции, содержащей полипептид, содержащий одну или более мутантных BTK пептидных последовательностей от C481S мутантного BTK белка, одну или нескольких мутантных BTK пептидных последовательностей, содержащих по меньшей мере 8 непрерывных аминокислот мутантного BTK белка, где аминокислотными последовательностями пептидов являются: ANGSLLNY (SEQ ID NO: 147); ANGSLLNYL (SEQ ID NO: 148); ANGSLLNYLR (SEQ ID NO: 149); EYMANGSL (SEQ ID NO: 150); EYMANGSLLN (SEQ ID NO: 151); EYMANGSLLNY (SEQ ID NO: 152); GSLLNYLR (SEQ ID NO: 153); GSLLNYLREM (SEQ ID NO: 154); ITEYMANGS (SEQ ID NO: 155); ITEYMANGSL (SEQ ID NO: 156); ITEYMANGSLL (SEQ ID NO: 157); MANGSLLNYL (SEQ ID NO: 158); MANGSLLNYLR (SEQ ID NO: 159); NGSLLNYL (SEQ ID NO: 160); NGSLLNYL (SEQ ID NO: 161); SLLNYLREMR (SEQ ID NO: 162); TEYMANGSLL (SEQ ID NO: 163); TEYMANGSLLNY (SEQ ID NO: 164); YMANGSLL (SEQ ID NO: 165); или YMANGSLLN (SEQ ID NO: 166), перечисленные в таблице 34.
В некоторых вариантах осуществления, одна или более мутантных BTK пептидных последовательностей содержат: (a) ANGSLLNY (SEQ ID NO: 167) и связывается с или предположительно связывается с белком, кодируемым HLA-A36:01 аллелем, (b) ANGSLLNYL (SEQ ID NO: 168) и связывается с или предположительно связывается с белком, кодируемым HLA аллелем, выбранной из группы, состоящей из HLA-C15:02, HLA-C08:01, HLA-C06:02, HLA-A02:04, HLA-C12:02, HLA-B44:02, HLA-C17:01 и HLA-B38:01, (c) ANGSLLNYLR (SEQ ID NO: 169) и связывается с или предположительно связывается с белком, кодируемым HLA-A74:01 аллелем, или HLA-A31:01 аллелем, (d) EYMANGSL (SEQ ID NO: 170) и связывается с или предположительно связывается с белком, кодируемым HLA аллелем, выбранной из группы, состоящей из HLA-C14:02, HLA-C14:03 и HLA-A24:02, (e) EYMANGSLLN (SEQ ID NO: 171) и связывается с или предположительно связывается с белком, кодируемым HLA-A24:02 аллелем или HLA-A23:01 аллелем, (f) EYMANGSLLNY (SEQ ID NO: 172) и связывается с или предположительно связывается с белком, кодируемым HLA-A29:02 аллелем, (g) GSLLNYLR (SEQ ID NO: 173) и связывается с или предположительно связывается с белком, кодируемым HLA-A31:01аллелем или HLA-A74:01 аллелем, (h) GSLLNYLREM (SEQ ID NO: 174) и связывается с или предположительно связывается с белком, кодируемым HLA-B58:02 аллелем или HLA-B57:01 аллелем, (i) ITEYMANGS (SEQ ID NO: 175) и связывается с или предположительно связывается с белком, кодируемым HLA-A01:01 аллелем, (j) ITEYMANGSL (SEQ ID NO: 176) и связывается с или предположительно связывается с белком, кодируемым HLA-A01:01 аллелем, (k) ITEYMANGSLL (SEQ ID NO: 177) и связывается с или предположительно связывается с белком, кодируемым HLA-A01:01аллелем, (l) MANGSLLNYL (SEQ ID NO: 178) и связывается с или предположительно связывается с белком, кодируемым HLA аллелем, выбранной из группы, состоящей из HLA-C17:01, HLA-C02:02, HLA-B35:01, HLA-C03:03, HLA-C08:01, HLA-B35:03, HLA-C12:02, HLA-C01:02, HLA-C03:04 и HLA-C08:02, (m) MANGSLLNYLR (SEQ ID NO: 179) и связывается с или предположительно связывается с белком, кодируемым HLA-A33:03 аллелем или HLA-A74:01 аллелем, (n) NGSLLNYL (SEQ ID NO: 180) и связывается с или предположительно связывается с белком, кодируемым HLA-B14:02 аллелем, (o) NGSLLNYL (SEQ ID NO: 181) и связывается с или предположительно связывается с белком, кодируемым HLA аллелем, выбранной из группы, состоящей из: HLA-A68:01, HLA-A33:03, HLA-A31:01 и HLA-A74:01, (p) SLLNYLREMR (SEQ ID NO: 182) и связывается с или предположительно связывается с белком, кодируемым HLA-A74:01 аллелем или HLA-A31:01 аллелем, (q) TEYMANGSLL (SEQ ID NO: 183) и связывается с или предположительно связывается с белком, кодируемым HLA аллелем, выбранной из группы, состоящей из : HLA-B40:01, HLA-B44:03, HLA-B49:01, HLA-B44:02 и HLA-B40:02, (r) TEYMANGSLLNY (SEQ ID NO: 184) и связывается с или предположительно связывается с белком, кодируемым HLA-B44:03 аллелем, (s) YMANGSLL (SEQ ID NO: 185) и связывается с или предположительно связывается с белком, кодируемым HLA аллелем, выбранной из группы, состоящей из HLA-B15:09, HLA-C03:04, HLA-C03:03, HLA-C17:01, HLA-C03:02, HLA-C14:03, HLA-C14:02, HLA-C04:01, HLA-C02:02, HLA-A01:01, или (t) YMANGSLLN (SEQ ID NO: 186) и связывается с или предположительно связывается с белком, кодируемым HLA-A29:02 аллелем или HLA-A01:01 аллелем.
В некоторых вариантах осуществления, одна или более мутантных BTK пептидных последовательностей является специфической к распознанному Т-клеточному рецептору в комплексе с HLA белком. В некоторых вариантах осуществления, композиция содержит две или более мутантных BTK пептидных последовательностей.
В одном аспекте изобретение относится к композиции, содержащей: по меньшей мере один полипептид, содержащий одну или более мутантных BTK пептидных последовательностей, где каждая имеет по меньшей мере 8 непрерывных аминокислот из C481S мутантного BTK белка, одну или более мутантных BTK пептидных последовательностей, выбранных из таблицы 34, дополнительно содержащих три или несколько аминокислотных остатков, которые являются гетерологическими к мутантному BTK белку, связанному с N-концом или C-концом мутантной BTK пептидной последовательности, где три или несколько аминокислотных остатков улучшают процессирование мутантных BTK пептидных последовательностей внутри клетки и/или улучшают презентацию эпитопа мутантных BTK пептидных последовательностей. В некоторых вариантах осуществления, три или несколько аминокислотных остатков, которые являются гетерологическими к мутантному BTK белку, содержат аминокислотную последовательность из CMV-pp65, HIV, MART-1 или не вирусного, не-BTK эндогенного пептида.
В некоторых вариантах осуществления, три или более аминокислотных остатков, которые являются гетерологическими к мутантному BTK белку, содержат по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 аминокислот.
В некоторых вариантах осуществления, три или более аминокислотных остатков, которые являются гетерологическими к мутантному BTK белку, содержат самое большее 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 50, 60, 70, 80, 90 или 100 аминокислот.
В одном аспекте изобретение относится к композиции, содержащей: по меньшей мере один полипептид формулы (N-конец Xaa)N-(XaaBTK)P-(Xaa-C-конец)C, где P является целым числом более 7; (XaaBTK)P является мутантной BTK пептидной последовательностью, содержащей, по меньшей мере 8 непрерывных аминокислот, выбранных из последовательности IFIITEYMANGSLLNYLREMRHR (SEQ ID NO: 187) мутантного BTK белка, содержащего C481S мутантную аминокислоту; N равно (i) 0 или (ii) целому числу более 2; (N-конец Xaa)N является любой аминокислотной последовательностью, гетерологической к мутантному BTK белку; C равно (i) 0 или (ii) целому числу более 2; (Xaa-C-конец)C является любой аминокислотной последовательностью, гетерологической к мутантному BTK белку; и оба N и C равны 0.
В некоторых вариантах осуществления, (N-конец Xaa)N и/или (Xaa-C-конец)C содержит аминокислотную последовательность CMV-pp65, HIV, MART-1 или не вирусного, не-BTK эндогенного белка или пептида.
В некоторых вариантах осуществления, N и/или C является целым числом более 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40.
В некоторых вариантах осуществления, N и/или C является целым числом менее чем 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 50, 60, 70, 80, 90 или 100. В некоторых вариантах осуществления, композицией является любая из пунктов 8-10, где N равно 0. В некоторых вариантах осуществления, 8-10, где C равно 0.
В одном аспекте изобретение относится к композиции, содержащей полинуклеотидную последовательность, кодирующую полипептид по пункту 1. В одном аспекте, композиция содержит полинуклеотидную последовательность, кодирующую одну или более пептидных последовательностей любого из мутантных BTK пептидов, описанных выше, и в таблицах 34 и таблице 36. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере 3, 4, 5, 6, 7, 8, 9, или 10 мутантных BTK пептидных последовательностей. В некоторых вариантах осуществления, по меньшей мере одна из мутантных BTK пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного BTK белка. В некоторых вариантах осуществления, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, или 10 мутантных ВТК пептидных последовательностей содержат по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного BTK белка. В некоторых вариантах осуществления, каждая из мутантных ВТК пептидных последовательностей или каждая из двух или нескольких BTK пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного BTK белка. В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную BTK пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым HLA аллелями, перечисленными в таблице 35 с аффинностью 150 нМ или менее и/или периодом полужизни 2 часа или более. В некоторых вариантах осуществления, мутантные ВТК пептидные последовательности содержат (a) первую мутантную BTK пептидную последовательность, выбранную из таблицы 34 и которая связывается с или предположительно связывается с белком, кодируемым HLA аллелем; и (b) второй BTK пептид, имеющий C481S мутацию, где первая мутантная BTK пептидная последовательность и вторая мутантная BTK пептидная последовательность не являются идентичными.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную BTK пептидную последовательность, которая связывается с белком, кодируемым HLA аллелем, с аффинностью менее чем 10 мкМ, менее чем 1 мкМ, менее чем 500 нМ, менее чем 400 нМ, менее чем 300 нМ, менее чем 250 нМ, менее чем 200 нМ, менее чем 150 нМ, менее чем 100 нМ или менее чем 50 нМ.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную BTK пептидную последовательность, которая связывается с белком, кодируемым HLA аллелем, со стабильностью более 24 часов, более 12 часов, более 9 часов, более 6 часов, более 5 часов, более 4 часа, более 3 часа, более 2 часов, более 1 часа, более 45 минут, более 30 минут, более 15 минут или более 10 минут.
В некоторых вариантах осуществления, (N-конец Xaa)N содержит аминокислотную последовательность IDIIMKIRNA (SEQ ID NO: 188), FFFFFFFFFFFFFFFFFFFFIIFFIFFWMC (SEQ ID NO: 189), FFFFFFFFFFFFFFFFFFFFFFFFAAFWFW (SEQ ID NO: 190), IFFIFFIIFFFFFFFFFFFFIIIIIIIWEC (SEQ ID NO: 191), FIFFFIIFFFFFIFFFFFIFIIIIIIFWEC (SEQ ID NO: 192), TEY, WQAGILAR (SEQ ID NO: 193), HSYTTAE (SEQ ID NO: 194), PLTEEKIK (SEQ ID NO: 195), GALHFKPGSR (SEQ ID NO: 196), RRANKDATAE (SEQ ID NO: 197), KAFISHEEKR (SEQ ID NO: 198), TDLSSRFSKS (SEQ ID NO: 199), FDLGGGTFDV (SEQ ID NO: 200), CLLLHYSVSK (SEQ ID NO: 201) или MTEYKLVVV (SEQ ID NO: 202). В некоторых вариантах осуществления, (C-конец Xaa)C содержит аминокислотную последовательность KKNKKDDIKD (SEQ ID NO: 203), AGNDDDDDDDDDDDDDDDDDKKDKDDDDDD (SEQ ID NO: 204), AGNKKKKKKKNNNNNNNNNNNNNNNNNNNN (SEQ ID NO: 205), AGRDDDDDDDDDDDDDDDDDDDDDDDDDDD (SEQ ID NO: 206), GKSALTIQL (SEQ ID NO: 207), GKSALTI (SEQ ID NO: 208), QGQNLKYQ (SEQ ID NO: 209), ILGVLLLI (SEQ ID NO: 210), EKEGKISK (SEQ ID NO: 211), AASDFIFLVT (SEQ ID NO: 212), KELKQVASPF (SEQ ID NO: 213), KKKLINEKKE (SEQ ID NO: 214), KKCDISLQFF (SEQ ID NO: 215), KSTAGDTHLG (SEQ ID NO: 216), ATFYVAVTVP(SEQ ID NO: 217), LTIQLIQNHFVDEYDPTIEDSYRKQVVIDG (SEQ ID NO: 218) или TIQLIQNHFVDEYDPTIEDSYRKQVVIDGE (SEQ ID NO: 219).
В некоторых вариантах осуществления, по меньшей мере одна из мутантных ВТК пептидных последовательностей содержит мутантную аминокислоту, не кодированную геномом раковой клетки субъекта.
В некоторых вариантах осуществления, каждая из мутантных ВТК пептидных последовательностей присутствует в концентрации по меньшей мере 1 мкг/мл, по меньшей мере 10 мкг/мл, по меньшей мере 25 мкг/мл, по меньшей мере 50 мкг/мл, или по меньшей мере 100 мкг/мл. В некоторых вариантах осуществления, каждая из мутантных ВТК пептидных последовательностей присутствует в концентрации самое большее 5000 мкг/мл, самое большее 2500 мкг/мл, самое большее 1000 мкг/мл, самое большее 750 мкг/мл, самое большее 500 мкг/мл, самое большее 400 мкг/мл или самое большее 300 мкг/мл. В некоторых вариантах осуществления, каждая из мутантных ВТК пептидных последовательностей присутствует в концентрации от 10 мкг/мл до 5000 мкг/мл, 10 мкг/мл до 4000 мкг/мл, 10 мкг/мл до 3000 мкг/мл, 10 мкг/мл до 2000 мкг/мл, 10 мкг/мл до 1000 мкг/мл, 25 мкг/мл до 500 мкг/мл или 50 мкг/мл до 300 мкг/мл. В некоторых вариантах осуществления, композиция дополнительно содержит иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, адъювантом является полиICLC.
В одном аспекте изобретение относится к фармацевтической композиции содержащей: (a) композицию, описанную выше, и (b) фармацевтически приемлемый эксципиент. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит pH модификатор. В некоторых вариантах осуществления, фармацевтической композицией является вакцинная композиция. В некоторых вариантах осуществления, фармацевтическая композиция является водной. В некоторых вариантах осуществления, фармацевтическая композиция, содержащая один или более из по меньшей мере одного полипептида, связана через (a) pI>5 и HYDRO >-6, (b) pI>8 и HYDRO >-8, (c) pI<5 и HYDRO >-5, (d) pI>9 и HYDRO <-8, (e) pI >7 и HYDRO значение >-5,5, (f) pI < 4,3 и -4≥HYDRO≥-8, (g) pI>0 и HYDRO<-8, pI>0 и HYDRO >-4, или pI>4,3 и -4≥HYDRO≥-8, (h) pI>0 и HYDRO>-4, или pI>4,3 и HYDRO≤-4, (i) pI>0 и HYDRO>-4, или pI>4,3 и -4≥HYDRO≥-9, (j) 5≥pI ≥12 и -4≥HYDRO≥-9.
В некоторых вариантах осуществления, pH модификатором является основание. В некоторых вариантах осуществления, pH модификатором является конъюгат основания слабой кислоты. В некоторых вариантах осуществления, pH модификатором является фармацевтически приемлемая соль. В некоторых вариантах осуществления, pH модификатором является дикарбоксилат или трикарбоксилат. В некоторых вариантах осуществления, pH модификатором является лимонная кислота и/или цитрат. В некоторых вариантах осуществления, цитратом является цитрат динатрия и/или цитрат тринатрия. В некоторых вариантах осуществления, pH модификатором является янтарная кислота и/или сукцинат. В некоторых вариантах осуществления, сукцинатом является сукцинат динатрия и/или сукцинат мононатрия. В некоторых вариантах осуществления, сукцинатом является гексагидрат сукцината динатрия. В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 0,1 мМ - 1 мМ. В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит жидкость. В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит воду.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит сахар. В некоторых вариантах осуществления, сахар содержит декстрозу. В некоторых вариантах осуществления, декстроза присутствует в концентрации от 1-10% масс./об. В некоторых вариантах осуществления, сахар содержит трегалозу. В некоторых вариантах осуществления, сахар содержит сахарозу.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит диметилсульфоксид (ДМСО). В некоторых вариантах осуществления, ДМСО присутствует в концентрации от 0,1% до 10%, 0,5% до 5%, или 1% до 3%. В некоторых вариантах осуществления, фармацевтически приемлемый носитель не содержит диметилсульфоксид (ДМСО). В некоторых вариантах осуществления, фармацевтическая композиция является лиофилизируемой. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулятор или адъювант. В некоторых вариантах осуществления, иммуномодулятор или адъювант выбран из группы, состоящей из поли-ICLC, 1018 ISS, солей алюминия, Ампливакса, AS15, BCG, CP-870,893, CpG7909, CyaA, ARNAX, агонистов STING, dSLIM, GM-CSF, IC30, IC31, Имиквимода, ImuFact IMP321, IS Patch, ISS, ISCOMATRIX, Juvlmmune, LipoVac, MF59, монофосфориллипида A, Монтанида IMS 1312, Монтанида ISA 206, Монтанида ISA 50V, Монтанида ISA-51, OK-432, OM-174, OM-197-MP-EC, ONTAK, PepTel®, системы векторов, PLGA микрочастиц, резиквимода, SRL172, Виросом и других вирусоподобных частиц, YF-17D, VEGF ловушки, R848, бета-глюкана, Pam3Cys, и Aquila’s QS21 стимулона.
В некоторых вариантах осуществления, иммуномодулятор или адъювант содержит поли-ICLC. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет от 2:1 до 1:10 об.:об. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет примерно 1:1, 1:2, 1:3, 1:4 или 1:5 об.:об. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет примерно 1:3 об.:об.
В одном аспекте изобретение относится к способу лечения рака у субъекта, включающему введение субъекту фармацевтической композиции, описанной выше.
В одном аспекте изобретение относится к способу лечения рака у субъекта, где способ включает: введение субъекту, нуждающемуся в этом, композиции, содержащей пептид, имеющей последовательность, выбранную из таблицы 34, 36 или 37, левой колонки; где субъект экспрессирует белок, кодируемый любой из HLA аллелей, перечисленных в правой колонке, соответствующей пептиду в таблице. В некоторых вариантах осуществления, изобретение относится к способу лечения рака у субъекта, включающему: введение субъекту, нуждающемуся в этом, композиции, содержащей один или более мутантных BTK пептидов, или одну или более нуклеиновых кислот, кодирующих один или более мутантных BTK пептидов, где каждый мутантный BTK пептид содержит по меньшей мере 8 непрерывных аминокислот мутантного BTK белка, содержащего мутацию C481S, где по меньшей мере один из одного или нескольких пептидов связывается с белком, кодируемым HLA аллелем, перечисленной в таблице 34, 36 или 37, которая экспрессирована субъектом. В некоторых вариантах осуществления, пептид связывается с HLA белком с аффинностью 150 нМ или менее и/или периодом полужизни 2 часа или более.
В одном аспекте изобретение относится к способу лечения рака у субъекта, включающему введение субъекту, нуждающемуся в этом, первого и второго пептида или нуклеиновой кислоты, кодирующей первый и второй пептид, где первый пептид имеет аминокислотную последовательность, выбранную из: таблиц 34, 36 или 37; и второй пептид имеет аминокислотную последовательность, выбранную из любой из таблиц 34, 36 или 37.
В некоторых вариантах осуществления, иммунный ответ вызывается у субъекта. В некоторых вариантах осуществления, иммунным ответом является гуморальный ответ.
В некоторых вариантах осуществления, один или более мутантных BTK пептидов вводят одновременно, отдельно или последовательно.
В некоторых вариантах осуществления, второй пептид вводят последовательно после периода времени, достаточного для первого пептида, чтобы активировать вторую T-клетку.
В некоторых вариантах осуществления, рак выбран из группы, состоящей из определенных типов лимфомы и определенных типов лейкоза. В некоторых вариантах осуществления раком является острый лимфобластный лейкоз (ОЛЛ), мантийноклеточная лимфома (МКЛ), хроническая лимфоцитарная лимфома или B-клеточная неходжкинская лимфома.
В некоторых вариантах осуществления, способ дополнительно включает введение по меньшей мере одного дополнительного терапевтического агента или способа воздействия.
В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом или способом воздействия является хирургическое вмешательство, ингибитор контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т-клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация.
В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент или анти-CD40 агент. В некоторых вариантах осуществления, дополнительный терапевтический агент вводят до, одновременно или после введения мутантных ВТК пептидных последовательностей.
В одном аспекте изобретение относится к способу лечения рака у субъекта, включающему стадии: (a) идентификации первого белка, экспрессированного субъектом, где первый белок кодируется первой HLA аллелем субъекта, и где первой HLA аллелем является HLA аллель, представленная в одной из таблиц 34, 37 или 38, (b) введение субъекту (i) первого мутантного BTK пептида, где первым мутантным BTK пептидом является пептид к первой HLA аллели, представленной в любой из таблиц 34, 36 или 37; или (ii) полинуклеиновой кислоты, кодирующей первый мутантный BTK пептид.
В одном аспекте изобретение относится к способу идентификации онкологического субъекта как кандидата для терапии, где способ включает идентификацию субъекта как экспрессирующего белок, кодируемый HLA из одной из таблиц 34, 36 или 37, где терапевтическим агентом является мутантный BTK пептид или нуклеиновая кислота, кодирующая мутантный BTK пептид, где мутантный BTK пептид содержит по меньшей мере 8 непрерывных аминокислот мутантного BTK белка, содержащего мутацию на C481, где пептид (i) содержит мутацию C481S, (ii) содержит последовательность пептида из любой из таблиц 34, 36 или 37 и (iii) связывается с соответствующим белком, кодируемым HLA из любой из таблиц 34, 36 или 37.
В некоторых аспектах изобретение относится к композиции, содержащей полипептид, содержащий одну или более мутантных EGFR пептидных последовательностей от T790M мутантного EGFR белка, одну или более мутантных EGFR пептидных последовательностей, содержащих по меньшей мере 8 непрерывных аминокислот, выбранных из группы, состоящей из: LIMQLMPF (SEQ ID NO: 220), TVQLIMQL (SEQ ID NO: 221), TSTVQLIMQL (SEQ ID NO: 222), TVQLIMQLM (SEQ ID NO: 223), VQLIMQLM (SEQ ID NO: 224), STVQLIMQL (SEQ ID NO: 225) и LTSTVQLIM (SEQ ID NO: 226).
В некоторых вариантах осуществления, одна или более мутантных EGFR пептидных последовательностей являются специфическими для распознанного Т-клеточного рецептора в комплексе с HLA белком.
В некоторых вариантах осуществления, композиция содержит смесь двух или трех или нескольких мутантных EGFR пептидных последовательностей. В некоторых вариантах осуществления, композиция содержит по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, или 10 мутантных EGFR пептидных последовательностей. В некоторых вариантах осуществления, по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного EGFR белка.
В некоторых аспектах изобретение относится к композиции, содержащей по меньшей мере один полипептид, содержащий одну или более мутантных EGFR пептидных последовательностей из T790M мутантного EGFR белка, одну или более мутантных EGFR пептидных последовательностей, содержащих по меньшей мере 8 непрерывных аминокислот, выбранных из группы, состоящей из: LIMQLMPF (SEQ ID NO: 227), TVQLIMQL (SEQ ID NO: 228), TSTVQLIMQL (SEQ ID NO: 229), TVQLIMQLM (SEQ ID NO: 230), VQLIMQLM (SEQ ID NO: 231), STVQLIMQL (SEQ ID NO: 232) и LTSTVQLIM (SEQ ID NO: 233), дополнительно содержащих три или более аминокислотных остатков, которые являются гетерологическими к мутантному EGFR белку, соединенных с N-концом или C-концом мутантной EGFR пептидной последовательности, где три или более аминокислотных остатков улучшают процессирование мутантных EGFR пептидных последовательностей внутри клетки и/или улучшают презентацию эпитопа мутантных EGFR пептидных последовательностей.
В некоторых вариантах осуществления, три или более аминокислотных остатков, которые являются гетерологическими к мутантному EGFR белку, содержат аминокислотную последовательность из CMV-pp65, HIV, MART-1 или не вирусного, не-EGFR эндогенного пептида.
В некоторых вариантах осуществления, три или более аминокислотных остатков, которые являются гетерологическими к мутантному EGFR белку, содержат по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 аминокислот.
В некоторых вариантах осуществления, три или более аминокислотных остатков, которые являются гетерологическими к мутантному EGFR белку, связаны с N-концом или C-концом двух или нескольких мутантных EGFR пептидных последовательностей содержит самое большее 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 50, 60, 70, 80, 90 или 100 аминокислот.
В некоторых вариантах осуществления, (Xaa-C-конец)C является любой аминокислотной последовательностью, гетерологической к мутантному EGFR белку; и оба, N и C, не равны 0.
В некоторых вариантах осуществления, (N-конец Xaa)N и/или (Xaa-C-конец)C содержит аминокислотную последовательность CMV-pp65, HIV, MART-1 или не вирусного, не-EGFR эндогенного белка или пептида.
В некоторых вариантах осуществления, N и/или C является целым числом более 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40.
В некоторых вариантах осуществления, N и/или C является целым числом менее чем 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 50, 60, 70, 80, 90 или 100. В некоторых вариантах осуществления, N равно 0. В некоторых вариантах осуществления, C равно 0.
В одном аспекте изобретение относится к композиции, содержащей полинуклеотидную последовательность, кодирующую полипептид, описанный выше. В одном варианте осуществления, композиция содержит полинуклеотидную последовательность, кодирующую один или более мутантных EGFR пептидных последовательностей, раскрытых в настоящем изобретении.
В некоторых вариантах осуществления, композиция, содержащая одну или более мутантных EGFR пептидных последовательностей, дополнительно содержит один или более мутантных EGFR пептидов, выбранных из таблицы 40A-40D.
В некоторых вариантах осуществления, по меньшей мере один полипептид, содержащий, по меньшей мере 3, 4, 5, 6, 7, 8, 9, или 10 мутантных EGFR пептидных последовательностей.
В некоторых вариантах осуществления, по меньшей мере одна из мутантных EGFR пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного EGFR белка. В некоторых вариантах осуществления, по меньшей мере 2, 3, 4, 5, 6, 7, 8 9, или 10 мутантных EGFR пептидных последовательностей содержат по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного EGFR белка. В некоторых вариантах осуществления, каждая из мутантных EGFR пептидных последовательностей или каждая из двух или нескольких EGFR пептидных последовательностей содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 непрерывных аминокислот мутантного EGFR белка.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную EGFR пептидную последовательность, которая связывается с или предположительно связывается с белком, кодируемым HLA аллелем, перечисленной в таблице 41 с аффинностью 150 нМ или менее и/или периодом полужизни 2 часа или более.
В некоторых вариантах осуществления, мутантные EGFR пептидные последовательности содержат первую мутантную EGFR пептидную последовательность, которая выбрана из группы, состоящей из STVQLIMQL (SEQ ID NO: 234), LIMQLMPF (SEQ ID NO: 235), LTSTVQLIM (SEQ ID NO: 236), TVQLIMQL (SEQ ID NO: 237), TSTVQLIMQL (SEQ ID NO: 238), TVQLIMQLM (SEQ ID NO: 239) и VQLIMQLM (SEQ ID NO: 240) и вторую мутантную EGFR пептидную последовательность, имеющую T790M мутацию.
В некоторых вариантах осуществления, мутантные EGFR пептидные последовательности содержат: (a) первую мутантную EGFR пептидную последовательность, которая выбрана из группы, состоящей из STVQLIMQL (SEQ ID NO: 241), LIMQLMPF (SEQ ID NO: 242), LTSTVQLIM (SEQ ID NO: 243), TVQLIMQL (SEQ ID NO: 244), TSTVQLIMQL (SEQ ID NO: 245), TVQLIMQLM (SEQ ID NO: 246) и VQLIMQLM (SEQ ID NO: 247), где первая мутантная EGFR пептидная последовательность связывается с или предположительно связывается с белком, кодируемым HLA-A68:02, HLA-C15:02, HLA-A25:01, HLA-B57:03, HLA-C12:02, HLA-C03:02, HLA-A26:01, HLA-C12:03, HLA-C06:02, HLA-C03:03, HLA-B52:01, HLA-A30:01, HLA-C02:02, HLA-C12:03, HLA-A11:01, HLA-A32:01, HLA-A02:04, HLA-A68:01, HLA-B15:09, HLA-C17:01, HLA-C03:04, HLA-B08:01, HLA-A01:01, HLA-B42:01, HLA-B57:01, HLA-B15:01, HLA-B14:02, HLA-B37:01, HLA-A36:01, HLA-C15:02, HLA-B15:09, HLA-C12:02, HLA-B38:01, HLA-C03:03, HLA-A02:03, HLA-B58:02, HLA-C08:01, HLA-B35:01, HLA-B40:01 и/или HLA-B35:03 аллелем; и (b) вторую EGFR пептидную последовательность, содержащую T790M мутацию, где первый и второй пептиды не являются идентичными.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную EGFR пептидную последовательность, которая связывается с белком, кодируемым HLA аллелем, с аффинностью менее чем 10 мкМ, менее чем 1 мкМ, менее чем 500 нМ, менее чем 400 нМ, менее чем 300 нМ, менее чем 250 нМ, менее чем 200 нМ, менее чем 150 нМ, менее чем 100 нМ, или менее чем 50 нМ.
В некоторых вариантах осуществления, по меньшей мере один полипептид содержит по меньшей мере одну мутантную EGFR пептидную последовательность, которая связывается с белком, кодируемым HLA аллелем, со стабильностью более 24 часов, более 12 часов, более 9 часов, более 6 часов, более 5 часов, более 4 часа, более 3 часа, более 2 часов, более 1 часа, более 45 минут, более 30 минут, более 15 минут или более 10 минут.
В некоторых вариантах осуществления, (N-конец Xaa)N содержит аминокислотную последовательность IDIIMKIRNA (SEQ ID NO: 248), FFFFFFFFFFFFFFFFFFFFIIFFIFFWMC (SEQ ID NO: 249), FFFFFFFFFFFFFFFFFFFFFFFFAAFWFW (SEQ ID NO: 250), IFFIFFIIFFFFFFFFFFFFIIIIIIIWEC (SEQ ID NO: 251), FIFFFIIFFFFFIFFFFFIFIIIIIIFWEC (SEQ ID NO: 252), TEY, WQAGILAR (SEQ ID NO: 253), HSYTTAE (SEQ ID NO: 254), PLTEEKIK (SEQ ID NO: 255), GALHFKPGSR (SEQ ID NO: 256), RRANKDATAE (SEQ ID NO: 257), KAFISHEEKR (SEQ ID NO: 258), TDLSSRFSKS (SEQ ID NO: 259), FDLGGGTFDV (SEQ ID NO: 260), CLLLHYSVSK (SEQ ID NO: 261) или MTEYKLVVV (SEQ ID NO: 262).
В некоторых вариантах осуществления, (C-конец Xaa)C содержит аминокислотную последовательность KKNKKDDIKD (SEQ ID NO: 263), AGNDDDDDDDDDDDDDDDDDKKDKDDDDDD (SEQ ID NO: 264), AGNKKKKKKKNNNNNNNNNNNNNNNNNNNN (SEQ ID NO: 265), AGRDDDDDDDDDDDDDDDDDDDDDDDDDDD (SEQ ID NO: 266), GKSALTIQL (SEQ ID NO: 267), GKSALTI (SEQ ID NO: 268), QGQNLKYQ (SEQ ID NO: 269), ILGVLLLI (SEQ ID NO: 270), EKEGKISK (SEQ ID NO: 271), AASDFIFLVT (SEQ ID NO: 272), KELKQVASPF (SEQ ID NO: 273), KKKLINEKKE (SEQ ID NO: 274), KKCDISLQFF (SEQ ID NO: 275), KSTAGDTHLG (SEQ ID NO: 276), ATFYVAVTVP (SEQ ID NO: 277), LTIQLIQNHFVDEYDPTIEDSYRKQVVIDG (SEQ ID NO: 278) или TIQLIQNHFVDEYDPTIEDSYRKQVVIDGE (SEQ ID NO: 279).
В некоторых вариантах осуществления, по меньшей мере одна из мутантных EGFR пептидных последовательностей содержит мутантную аминокислоту, не кодированную геномом раковой клетки субъекта.
В некоторых вариантах осуществления, мутантные EGFR пептидные последовательности присутствуют в концентрации по меньшей мере 1 мкг/мл, по меньшей мере 10 мкг/мл, по меньшей мере 25 мкг/мл, по меньшей мере 50 мкг/мл или, по меньшей мере 100 мкг/мл.
В некоторых вариантах осуществления, каждая из мутантных EGFR пептидных последовательностей присутствует в концентрации самое большее 5000 мкг/мл, самое большее 2500 мкг/мл, самое большее 1000 мкг/мл, самое большее 750 мкг/мл, самое большее 500 мкг/мл, самое большее 400 мкг/мл или самое большее 300 мкг/мл.
В некоторых вариантах осуществления, каждая из мутантных EGFR пептидных последовательностей присутствует в концентрации от 10 мкг/мл до 5000 мкг/мл, 10 мкг/мл до 4000 мкг/мл, 10 мкг/мл до 3000 мкг/мл, 10 мкг/мл до 2000 мкг/мл, 10 мкг/мл до 1000 мкг/мл, 25 мкг/мл до 500 мкг/мл или 50 мкг/мл до 300 мкг/мл.
В некоторых вариантах осуществления, композиция дополнительно содержит иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, адъювантом является полиICLC.
В одном аспекте изобретение относится к фармацевтической композиции, содержащей:
(a) композицию, содержащую, по меньшей мере один полипептид, содержащий, по меньшей мере одну мутантную EGFR пептидную последовательность, как описано выше, и (b) фармацевтически приемлемый эксципиент.
В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит pH модификатор.
В некоторых вариантах осуществления, фармацевтической композицией является вакцинная композиция.
В некоторых вариантах осуществления, фармацевтическая композиция является водной.
В некоторых вариантах осуществления, один или более из по меньшей мере одного полипептида связан через pI>5 и HYDRO >-6, pI>8 и HYDRO >-8,pI<5 и HYDRO >-5, pI>9 и HYDRO <-8, pI >7 и HYDRO значение >-5,5, pI <4,3 и -4≥HYDRO≥-8, pI>0 и HYDRO<-8, pI>0 и HYDRO >-4, или pI>4,3 и -4≥HYDRO≥-8, pI>0 и HYDRO>-4 или pI>4,3 и HYDRO≤-4, pI>0 и HYDRO>-4, или pI>4,3 и -4≥HYDRO≥-9, 5≥pI≥12 и -4≥HYDRO≥-9.
В некоторых вариантах осуществления, фармацевтическая композиция содержит pH модификатор, который является основанием.
В некоторых вариантах осуществления, pH модификатором является конъюгированное основание слабой кислоты.
В некоторых вариантах осуществления, pH модификатором является фармацевтически приемлемая соль.
В некоторых вариантах осуществления, pH модификатором является дикарбоксилат или трикарбоксилат.
В некоторых вариантах осуществления, pH модификатором является лимонная кислота и/или цитрат.
В некоторых вариантах осуществления, цитратом является цитрат динатрия и/или цитрат тринатрия.
В некоторых вариантах осуществления, pH модификатором является янтарная кислота и/или сукцинат.
В некоторых вариантах осуществления, сукцинатом является сукцинат динатрия и/или сукцинат мононатрия.
В некоторых вариантах осуществления, сукцинатом является гексагидрат сукцината динатрия.
В некоторых вариантах осуществления, pH модификатор присутствует в концентрации от 0,1 мМ - 1 мМ.
В некоторых вариантах осуществления, фармацевтическая композиция содержит фармацевтически приемлемый носитель, содержащий жидкость.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит воду.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит сахар.
В некоторых вариантах осуществления, сахар содержит декстрозу.
В некоторых вариантах осуществления, декстроза присутствует в концентрации от 1-10% масс./об.
В некоторых вариантах осуществления, сахар содержит трегалозу.
В некоторых вариантах осуществления, сахар содержит сахарозу.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель содержит диметилсульфоксид (ДМСО).
В некоторых вариантах осуществления, ДМСО присутствует в концентрации от 0,1% до 10%, 0,5% до 5% или 1% до 3%.
В некоторых вариантах осуществления, фармацевтически приемлемый носитель не содержит диметилсульфоксид (ДМСО).
В некоторых вариантах осуществления, фармацевтическая композиция является лиофилизируемой.
В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулятор или адъювант.
В некоторых вариантах осуществления, иммуномодулятор или адъювант выбран из группы, состоящей из поли-ICLC, 1018 ISS, солей алюминия, Ампливакса, AS15, BCG, CP-870,893, CpG7909, CyaA, ARNAX, агонистов STING, dSLIM, GM-CSF, IC30, IC31, Имиквимода, ImuFact IMP321, IS Patch, ISS, ISCOMATRIX, Juvlmmune, LipoVac, MF59, монофосфориллипида A, Монтанида IMS 1312, Монтанида ISA 206, Монтанида ISA 50V, Монтанида ISA-51, OK-432, OM-174, OM-197-MP-EC, ONTAK, PepTel®, системы векторов, PLGA микрочастиц, резиквимода, SRL172, Виросом и другие вирусоподобных частиц, YF-17D, VEGF ловушки, R848, бета-глюкана, Pam3Cys и Aquila’s QS21 стимулона.
В некоторых вариантах осуществления, иммуномодулятор или адъювант содержит поли-ICLC. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет от 2:1 до 1:10 об.:об. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет примерно 1:1, 1:2, 1:3, 1:4 или 1:5 об.:об. В некоторых вариантах осуществления, отношение поли-ICLC к пептидам в фармацевтической композиции составляет примерно 1:3 об.:об.
В одном аспекте изобретение относится к способу лечения рака у субъекта, включающему введение субъекту фармацевтической композиции, описанной выше.
В одном аспекте изобретение относится к способу лечения рака у субъекта, включающему введение субъекту нуждающемуся в этом, композиции, содержащей один или более мутантных EGFR пептидов, или одну или более нуклеиновых кислот, кодирующих один или более мутантных EGFR пептидов, где каждый мутантный EGFR пептид содержит по меньшей мере 8 непрерывных аминокислот мутантного EGFR белка, содержащего мутацию T790M, где один или более мутантных EGFR пептидов имеет аминокислотную последовательность, указанную в таблице 40A-40D; где по меньшей мере один из одного или нескольких пептидов связывается с аффинностью 150 нМ или менее и/или периодом полужизни 2 часа или более, с белком, кодируемым, связывается с или предположительно связывается с белком, кодируемым HLA-A68:02, HLA-C15:02, HLA-A25:01, HLA-B57:03, HLA-C12:02, HLA-C03:02, HLA-A26:01, HLA-C12:03, HLA-C06:02, HLA-C03:03, HLA-B52:01, HLA-A30:01, HLA-C02:02, HLA-C12:03, HLA-A11:01, HLA-A32:01, HLA-A02:04, HLA-A68:01, HLA-B15:09, HLA-C17:01, HLA-C03:04, HLA-B08:01, HLA-A01:01, HLA-B42:01, HLA-B57:01, HLA-B15:01, HLA-B14:02, HLA-B37:01, HLA-A36:01, HLA-C15:02, HLA-B15:09, HLA-C12:02, HLA-B38:01, HLA-C03:03, HLA-A02:03, HLA-B58:02, HLA-C08:01, HLA-B35:01, HLA-B40:01 и/или HLA-B35:03 аллелем; и где указанная аллель экспрессирована субъектом.
В одном аспекте изобретение относится к способу лечения онкологического субъекта, где способ включает: введение субъекту, нуждающемуся в этом, полипептида, содержащего мутантную EGFR пептидную последовательность, или полинуклеотида, кодирующего мутантный EGFR пептид, где (a) мутантный EGFR пептид имеет последовательность LIMQLMPF (SEQ ID NO: 280) и субъект экспрессирует белок, кодируемый HLA-C03:02 аллелем, (b) мутантный EGFR пептид имеет последовательность LTSTVQLIM (SEQ ID NO: 281) и субъект экспрессирует белок, кодируемый HLA аллелем, выбранной из группы, состоящей из: HLA-C12:03, HLA-C15:02, HLA-B57:01, HLA-B57:01, HLA-A36:01, HLA-C12:02, HLA-C03:03 и HLA-B58:02, (c) мутантный EGFR пептид имеет последовательность QLIMQLMPF (SEQ ID NO: 282) и субъект экспрессирует белок, кодируемый HLA-A26:01 аллелем, (d) мутантный EGFR пептид имеет последовательность STVQLIMQL (SEQ ID NO: 283) и субъект экспрессирует белок, кодируемый HLA аллелем, выбранной из группы, состоящей из: HLA-A68:02, HLA-C15:02, HLA-A25:01, HLA-B57:03, HLA-C12:02, HLA-A26:01, HLA-C12:03, HLA-C06:02, HLA-C03:03, HLA-A30:01, HLA-C02:02, HLA-A11:01, HLA-A32:01, HLA-A02:04, HLA-A68:01, HLA-B15:09, HLA-C03:04, HLA-B38:01, HLA-B57:01, HLA-A02:03, HLA-C08:01, HLA-B35:01 и HLA-B40:01, (e) мутантный EGFR пептид имеет последовательность STVQLIMQLM (SEQ ID NO: 284) и субъект экспрессирует белок, кодируемый HLA-B57:01 аллелем, (f) мутантный EGFR пептид имеет последовательность TSTVQLIMQL (SEQ ID NO: 285) и субъект экспрессирует белок, кодируемый HLA-C15:02 аллелем, (g) мутантный EGFR пептид имеет последовательность TVQLIMQL (SEQ ID NO: 286) и субъект экспрессирует белок, кодируемый HLA аллелем, выбранной из группы, состоящей из: HLA-C17:01, HLA-B08:01, HLA-B42:01, HLA-B14:02, HLA-B37:01, HLA-B15:09, (h) мутантный EGFR пептид имеет последовательность TVQLIMQLM (SEQ ID NO: 287) и субъект экспрессирует белок, кодируемый HLA-B35:03 аллелем, или (i) мутантный EGFR пептид имеет последовательность VQLIMQLM (SEQ ID NO: 288) и субъект экспрессирует белок, кодируемый HLA аллелем, выбранной из группы, состоящей из HLA-B52:01, HLA-B14:02 и HLA-B37:01.
В некоторых вариантах осуществления, способ дополнительно включает введение второй полипептидной композиции, содержащей по меньшей мере один мутантный EGFR пептид, где второй мутантный EGFR пептид выбран из таблицы 40A-40D.
В одном аспекте изобретение относится к способу лечения рака у субъекта, где способ включает стадии (a) идентификации первого белка, экспрессированного субъектом, где первый белок кодируется первой HLA аллелем субъекта, и где первой HLA аллелем является HLA аллель, представленная в любой из таблиц 41-43; и (b) введения субъекту (i) первого мутантного EGFR пептида, где первым мутантным EGFR пептидом является пептид к первой HLA аллели, представленной в любой из таблиц 42Ai и ii, 42B или 43, или (ii) полинуклеиновой кислоты, кодирующей первый мутантный EGFR пептид. В некоторых вариантах осуществления, способ лечения рака у субъекта включает стадии: идентификации одного или нескольких специфических HLA подтипов, экспрессированных у субъекта; введения субъекту композиции, содержащей один или нескольких мутантных EGFR пептидов, описанных в настоящем изобретении, таких как одна или более пептидных связей с, по меньшей мере одни подтипом HLA, экспрессированным субъектом с аффинностью 150 нМ или менее и/или периодом полужизни 2 часа или более.
В одном аспекте изобретение относится к способу лечения рака у субъекта, где способ включает стадии (a) идентификации субъекта как экспрессирующего белок, кодируемый HLA-B57:01 аллелем генома субъекта; (b) введения субъекту композиции, содержащей пептид, имеющий последовательность STVQLIMQLM (SEQ ID NO: 289). В одном варианте осуществления, способ включает стадии (a) идентификации того, экспрессирует ли субъект белок, кодируемый HLA-A26:01 аллелем генома субъекта; (b) введения субъекту композиции, содержащей пептид, имеющий последовательность QLIMQLMPF (SEQ ID NO: 290).
В некоторых вариантах осуществления, иммунный ответ вызывается у субъекта. В одном варианте осуществления, иммунным ответом является гуморальный ответ.
В некоторых вариантах осуществления, одну или более мутантных EGFR пептидных последовательностей вводят одновременно, отдельно или последовательно. В некоторых вариантах осуществления, второй пептид последовательно вводят после периода времени, достаточного для первого пептида для активации вторых Т-клеток.
В некоторых вариантах осуществления, рак выбран из группы, состоящей из, выбран из группы, состоящей из глиобластомы, аденокарциномы легкого, немелкоклеточного рака легкого, плоскоклеточного рака легкого, рака почки, рака головы и шеи, рака яичников, рака шейки матки, рака мочевого пузыря, рака желудка, рака молочной железы, рака толстой кишки, рака эндометрия и рака пищевода.
В некоторых вариантах осуществления, способ дополнительно включает введение по меньшей мере одного дополнительного терапевтического агента или способа воздействия.
В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом или способом воздействия является хирургическое вмешательство, ингибитор контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т-клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент, или анти-CD40 агент. В некоторых вариантах осуществления, дополнительный терапевтический агент вводят до, одновременно или после введения мутантных EGFR пептидных последовательностей.
В одном аспекте изобретение относится к способу идентификации онкологического субъекта как кандидата для терапии, где способ включает идентификацию субъекта как субъекта, экспрессирующего блок, кодируемый HLA из одной из таблиц 41, 42Ai, 42Aii, 42B, или 43, где терапевтическим агентом является мутантный EGFR пептид или нуклеиновая кислота, кодирующая мутантный EGFR пептид, где мутантный EGFR пептид содержит по меньшей мере 8 непрерывных аминокислот мутантного EGFR белка, содержащего мутацию на T790, где пептид (i) содержит мутацию T790M, (ii) содержит последовательность пептида из любой из таблиц 42Ai, 42Aii, 42B, 43, и 44 и (iii) связывается с соответствующим белком, кодируемым HLA из одной из таблиц 42Ai, 42Aii, 42B, 43 и 44.
В одном аспекте изобретение относится к способу идентификации субъекта как кандидата для терапии, где способ включает определение того, что субъект экспрессирует белок, кодируемый HLA-B57:01 аллелем, где терапевтический агент содержит мутантный EGFR пептид, имеющий аминокислотную последовательность STVQLIMQLM (SEQ ID NO: 291).
В одном аспекте изобретение относится к способу идентификации субъекта как кандидата для терапии, где способ включает определение того, что субъект экспрессирует белок, кодируемый HLA-A26:01 аллелем, где терапевтический агент содержит мутантный EGFR пептид, имеющий аминокислотную последовательность QLIMQLMPF (SEQ ID NO: 292).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Особенности настоящего раскрытия подробно изложены в прилагаемой формуле изобретения. Лучшее понимание характеристик и преимуществ настоящего описания будет получено со ссылкой на следующее подробное описание, в котором представлены иллюстративные варианты осуществления, в которых используются принципы раскрытия, и прилагаемые чертежи, на которых:
На ФИГ. 1 показан типовой технологический процесс для определения GATA3 эпитопов, которые могут индуцировать CD8+ и/или CD4+ T-клетки.
На ФИГ. 2 показан типовой технологический процесс для определения того, процессированы и презентированы ли эпитопы (верх) и распознаны ли эпитопы Т-клетками (низ). Этот технологический процесс подтверждает, что GATA3 неоантигены были процессированы и презентированы (определяется масс-спектрометрией), и GATA3 неоантигены, связанные с HLA мультимером, могут быть распознаны рекомбинантным Т-клеточным рецептором (TCR), экспрессированным в клеточной линии Jurkat.
На ФИГ. 3 показана типовая схема технологического процесса для определения GATA3 neoORF эпитопов масс-спектрометрией. Для выделения пептида проводят периодический лизис, и HLA пан-антитело I класса (W6/32) используют для иммунопреципитации.
На ФИГ. 4 показана типовая схема технологического процесса для GATA3 антиген-специфического размножения CD8+ T-клеток.
На ФИГ. 5 показана сводка экспериментов, показывающий, что спрогнозированные GATA3 эпитопы к HLA-A02 (слева), HLA-B07 (середина) и HLA-B08 (справа) могут быть определены масс-спектрометрией. На ФИГ. 5 раскрыты "HLA-A*02:01" определенные пептидные последовательности как SEQ ID NOS 3824-3826, "HLA-B*07:02" определенные пептидные последовательности как SEQ ID NOS 3827-3828, "HLA-B*08:01" определенные пептидные последовательности как SEQ ID NO: 3829 и последовательность конструктов как 3830-3832, все, соответственно, в порядке появления.
На ФИГ. 6 показаны GATA3 neoORF. Затененная область представляет часть GATA3 neoORF последовательности, общую для всех пациентов (общая область) и общую для некоторых пациентов (вариабельная область).
На ФИГ. 7A показана GATA3 neoORF последовательность (SEQ ID NO: 2) с последовательностью переменной области (SEQ ID NO: 3) и последовательностями общей области (SEQ ID NO: 4).
На ФИГ. 7B изображена схема, показывающая GATA3 последовательность (SEQ ID NO: 1) с neoORF последовательностью (SEQ ID NO: 2) и что 3 спрогнозированные HLA-02:01 эпитопы, 2 спрогнозированные HLA-B07:02 эпитопы и 1 спрогнозированные HLA-B08:01 эпитопы определяют масс-спектрометрией. Эти данные показывают, что эпитопы являются нацеливаемыми.
На ФИГ. 7C показан пример схемы дизайна пептида перекрывающихся пептидов (OLP) по всей GATA3 neoORF области. На ФИГ. 7C раскрыта SEQ ID NO: 3853.
На ФИГ. 7D представлена типовая аминокислотная последовательность переменной области GATA3 neo ORF (SEQ ID NO: 3)
На ФИГ. 7E представлена типовая аминокислотная последовательность общей области GATA3 neo ORF (SEQ ID NO: 4)
На ФИГ.8 представлен график, изображающий количество GATA3 neoORF эпитопов терапевтического класса I в сравнении с долей пациентов, содержащих эти эпитопы. Большинство пациентов имеют 4-5 эпитопов.
На ФИГ. 9A изображены типовые результаты, показывающие антигенспецифические ответы CD8+ T-клетки на указанный пептид (SEQ ID NO: 3834) с применением образца PBMC от донора-человека.
На ФИГ. 9B изображены типовые результаты, показывающие антигенспецифические ответы CD8+ T-клетки на указанный пептид (SEQ ID NO: 3835) с применением образца PBMC от доноров-людей.
На ФИГ. 9C изображены типовые результаты, показывающие антигенспецифические ответы CD8+ T-клетки на указанные пептиды с применением образца PBMC от доноров-людей. На ФИГ. 9C раскрыты "A02:01" последовательности как SEQ ID NOS 3836-3837, "A03:01" последовательность как SEQ ID NO: 3838, "A11:01" последовательность как SEQ ID NO: 3839, "B07:02" последовательности как SEQ ID NOS 3840-3841 и "B08:01" последовательность как SEQ ID NO: 3842, все, соответственно, в порядке появления.
На ФИГ. 10A изображены типовые результаты, показывающие антигенспецифические ответы CD8+ T-клетки на указанные пептиды (SEQ ID NOS 3843-3845, соответственно, в порядке появления) с применением образца PBMC от доноров-людей.
На ФИГ. 10B изображены типовые результаты, показывающие антигенспецифические ответы CD8+ T-клетки на указанные пептиды (SEQ ID NOS 3846-3848, соответственно, в порядке появления) с применением образца PBMC от доноров-людей.
На ФИГ. 11 изображен FACS анализ антигенспецифической индукции уровней IFNγ и TNFα CD4+ клеток от здорового HLA-A02:01 донора, стимулированной APC, загруженными с или без GATA3 neoORF пептида.
На ФИГ. 12A показано, что указанные пептиды были растворимы в указанных концентрациях пептида в фармацевтических композициях с 5 мМ или 0,25 мМ сукцината, без ДМСО, 5% декстрозой в воде (5DW) и без полиICLC.
На ФИГ. 12B показано, что указанные пептиды были растворимы в указанных концентрациях пептида в фармацевтических композициях с 5 мМ или 0,25 мМ сукцината, без ДМСО, 5% декстрозой в воде (5DW) и с полиICLC.
На ФИГ. 12C показано, что указанные пептиды были растворимы в указанных концентрациях пептида в фармацевтических композициях с 5 мМ или 0,25 мМ сукцината, без ДМСО, 5% декстрозой в воде (5DW) и с полиICLC с указанным соотношением пептид:полиICLC.
На ФИГ. 13 показана аминокислотная последовательность общей области GATA3 мутаций со сдвигом рамки (SEQ ID NO: 4).
На ФИГ. 14 показана кривая выживания Каплана-Мейера для пациентов в массиве данных MSK-IMPACT рака молочной железы.
На ФИГ. 15 показан имитированный анализ презентированных эпитопов на пациента.
На ФИГ. 16 показан участок выравнивания дикого типа GATA3 (SEQ ID NO: 3849) и мутация (SEQ ID NO: 3850) нуклеотидных последовательностей.
На ФИГ. 17 показан участок выравнивания дикого типа GATA3 и мутация аминокислотных последовательностей. На ФИГ. 17 описаны SEQ ID NOS 3851-3853, соответственно, в порядке появления.
На ФИГ. 18 показана кодированная мутацией GATA3 карта плазмид.
На ФИГ. 19 показан участок мультивыравнивания мутированного гена GATA3 и данные секвенирования ДНК конструкта плазмиды мутированного GATA3. На ФИГ. 19 раскрыты SEQ ID NOS 3854-3856, соответственно, в порядке появления.
На ФИГ. 20 показано расщепление рестрикционным ферментом плазмиды мутации GATA3 с AflII.
На ФИГ. 21 показана MHC класса I и MHC класса II экспрессия GATA3 трансдуцированных HEK 293T клеток.
На ФИГ. 22A-22D показан HLA-A02 и MHC-ABC профиль экспрессии HLA-A02.01, HLA-B07.02 и HLA-B08.01 трансфицированных GATA3 HEK293T клеток.
На ФИГ. 22A показаны не трансфицированные GATA3 HEK293T клетки.
На ФИГ. 22B показаны HLA-A02.01 трансфицированные GATA3 HEK293T клетки.
На ФИГ. 22C показаны HLA-B07.02 трансфицированные GATA3 HEK293T клетки.
На ФИГ. 22D показаны HLA-B08.01 трансфицированные GATA3 HEK293T клетки.
На ФИГ. 23 показано определение спрогнозированных пептидных эпитопов, полученных из общей области GATA3 neoORF, стабильно экспрессированных в HEK293T клетках. Светло-серая и черная последовательность означает переменную и общую области GATA3 neoORF, соответственно. На ФИГ. 23 раскрыта SEQ ID NO: 3857.
На ФИГ. 24A показан МС/МС спектр для эндогенно процессированного пептидного эпитопа SMLTGPPARV (SEQ ID NO: 293) (низ) и его соответствующего синтетического пептида (верх).
На ФИГ. 24B показан сплошной график МС/МС спектральной совместимости. На ФИГ. 24B раскрыта "SMLTGPPARV" как SEQ ID NO: 3858.
На ФИГ. 25A показан МС/МС спектр для эндогенно процессированного пептидного эпитопа MLTGPPARV (SEQ ID NO: 294) (низ) и его соответствующего синтетического пептида (верх).
На ФИГ. 25B показан сплошной график спектральной совместимости. На ФИГ. 25B раскрыта "MLTGPPARV" как SEQ ID NO: 3859.
На ФИГ. 26A показан МС/МС спектр для эндогенно процессированного пептидного эпитопа KPKRDGYMF (SEQ ID NO: 295) (низ) и его соответствующего синтетического пептида (верх).
На ФИГ. 26B показан сплошной график спектральной совместимости. На ФИГ. 26B раскрыта "KPKRDGYMF" как SEQ ID NO: 3860.
На ФИГ. 27A показан МС/МС спектр для эндогенно процессированного пептидного эпитопа KPKRDGYMFL (SEQ ID NO: 296) (низ) и его соответствующего синтетического пептида (верх).
На ФИГ. 27B показан сплошной график спектральной совместимости. На ФИГ. 27B раскрыта "KPKRDGYMFL" как SEQ ID NO: 3861.
На ФИГ. 28A показан МС/МС спектр для эндогенно процессированного пептидного эпитопа ESKImFATL (SEQ ID NO: 297) (низ) и его соответствующего синтетического пептида (верх).
На ФИГ. 28B показан сплошной график спектральной совместимости. На ФИГ. 28B раскрыта "ESKImFATL" как SEQ ID NO: 3862.
На ФИГ. 29A показана типовая индукция CD8+ ответов с GATA3 neoORF специфическим пептидом (FLT-mDC GATA3 Stim2 мультимер). На ФИГ. 29A раскрыта "MLTGPPARV" как SEQ ID NO: 3863.
На ФИГ. 29 B показан отрицательный контроль без индукции CD8+ ответов в PBMC и дендритных клетках. На ФИГ. 29B раскрыты "MLTGPPARV" как SEQ ID NO: 3864.
На ФИГ. 30A показана индукция антигенспецифических CD4 T-клеток при отсутствии пептида.
На ФИГ. 30B показана индукция антигенспецифических CD4 T-клеток с GATA3 neoORF специфическим пептидом.
На ФИГ. 31A-31D показаны GATA3 специфические CD8+ T-клетки через окрашивание мультимера.
На ФИГ. 31A показаны GATA3 специфические CD8+ T-клетки, наблюдаемые при среднем 1,16% положительных после долговременного стимулирования для здорового донора HD47.
На ФИГ. 31B показаны GATA3 специфические CD8+ T-клетки, наблюдаемые при среднем 1,29% положительных после долговременного стимулирования для здорового донора HD50.
На ФИГ. 31C показаны GATA3 специфические CD8+ T-клетки, наблюдаемые при среднем 1,9% положительных после долговременного стимулирования для здорового донора HD51.
На ФИГ. 31D показаны GATA3 специфические CD8+ T-клетки, наблюдаемые при среднем 4,5% положительных после долговременного стимулирования для здорового донора HD51 при концентрации пептида, отличной от ФИГ. 31C.
На ФИГ. 32 показано сравнение Caspase-3 положительной доли живых клеток-мишеней. 4 разных GATA3-индуцированных PBMC от здоровых доноров 1-4 совместно культивируют с трансдуцированными GATA3 мутацией HEK 293T клетками (GATA3Trd) или не трансдуцированными HEK 293T клетками (NoTRd293T) в качестве группы отрицательного контроля.
На ФИГ. 33 показана значительная разница между GATA3 трансдуцированными HEK293T клетками и не трансдуцированными HEK293T клетками.
На ФИГ. 34 показана разница экспрессии CD107a CD8+ T-клеток, совместно культивированных с GATA3 трансдуцированными HEK293T клетками и не трансдуцированными HEK293T клетками.
На ФИГ. 35 показана разница в концентрации IFN-γ в условиях совместного культивирования между GATA3 трансдуцированными HEK293T клетками и не трансдуцированными HEK293T клетками с GATA3 индуцированными Т-клетками.
На ФИГ. 36 показан обзор GATA3 специфического клонирования TCR. Подробности описаны в примере 26.
На ФИГ. 37 показаны типовые способы создания GATA3 специфических TCR трансдуцированных Jurkat и PBMC. Подробности описаны в примере 26.
На ФИГ. 38 показан обзор функционального анализа с TCR трансдуцированными Jurkat.
На ФИГ. 39 показаны GATA3 специфические CD8+ T клетки через окрашивание мультимера для сортировки.
На ФИГ. 40 показан GATA3 специфический TCR конструкт для лентивируса.
На ФИГ. 41A показано мульти-выравнивание GATA3 TCR альфа последовательности и дикого типа ДНК последовательности. На ФИГ. 41A описаны SEQ ID NOS 3865-3868, соответственно, в порядке появления.
На ФИГ. 41B показано мульти-выравнивание GATA3 TCR бета последовательности и дикого типа ДНК последовательности. На ФИГ. 41B описаны SEQ ID NOS 3869-3872, соответственно, в порядке появления.
На ФИГ. 42 показано расщепление рестрикционным ферментом GATA3 TCR плазмида с AflII.
На ФИГ. 43 показаны GATA3 специфические TCR трансдуцированные Jurkat, окрашенные GATA3 мультимером PE и GATA3 мультимером BV650.
На ФИГ. 44 показан анализ титрования GATA3 специфического TCR пептида.
На ФИГ. 45 показан анализ выделения IL-2 GATA3 специфических TCR трансдуцированных Jurkat клеток и GATA3 мутацией трансдуцированных клеток-мишеней.
На ФИГ. 46 показана стереохимия типового GATA3 neo ORF пептида. Пептид состоит из 14 аминокислот и последовательности ESKIMFATLQRSSL (SEQ ID NO: 298). Пептид имеет молекулярную формулу C70H119N19O22S и молекулярную массу 1610,89 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 47 показана стереохимия типового GATA3 neo ORF пептида. Пептид состоит из 16 аминокислот и последовательности KPKRDGYMFLKAESKI (SEQ ID NO: 299). Пептид имеет молекулярную формулу C87H143N23O23S и молекулярную массу 1911,30 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 48 показана стереохимия типового GATA3 neo ORF пептида. Пептид состоит из 18 аминокислот и последовательности SMLTGPPARVPAVPFDLH (SEQ ID NO: 300). Пептид имеет молекулярную формулу C87H137N23O23S и молекулярную массу 1905,25 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 49 показана стереохимия типового GATA3 neo ORF пептид. Пептид состоит из 21 аминокислот и последовательности EPCSMLTGPPARVPAVPFDLH (SEQ ID NO: 301). Пептид имеет молекулярную формулу C100H156N26O28S2 и молекулярную массу 2234,62 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 50 показана стереохимия типового GATA3 neo ORF пептида. Пептид состоит из 25 аминокислот и последовательности LHFCRSSIMKPKRDGYMFLKAESKI (SEQ ID NO: 302). Пептид имеет молекулярную формулу C134H217N37O34S3 и молекулярную массу 2986,62 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 51 показана стереохимия типового GATA3 neo ORF пептида. Пептид состоит из 26 аминокислот последовательности GPPARVPAVPFDLHFCRSSIMKPKRD (SEQ ID NO: 303). Пептид имеет молекулярную формулу C131H209N39O33S2 и молекулярную массу 2922,47 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 52 показана стереохимия типового GATA3 neo ORF пептида. Пептид состоит из 33 аминокислот и последовательности KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 304). Пептид имеет молекулярную формулу C173H274N48O46S4 и молекулярную массу 3890,63 г/моль. Пептид имеет форму соли трифторуксусной кислоты (ТФК).
На ФИГ. 53 показаны ответы специфических к BTK антигенному пептиду CD8+ T-клеток с применением образцов PBMC от доноров-людей.
На ФИГ. 54 показаны ответы специфических к EGFR антигенному пептиду CD8+ T-клеток с применением образцов PBMC от доноров-людей.
ПОДРОБНОЕ ОПИСАНИЕ
GATA3 является геном, сверхэкспрессируемым при раке молочной железы, и одним из наиболее часто мутированных генов при таких раках. Наиболее часто встречающимися классами мутаций в этом гене являются вставки или делеции между нуклеотидами, кодирующими аминокислоты 393 и 445 (природный стоп-кодон). Когда они сдвигают открытую рамку считывания на +1 рамку, они дают расширенную новую рамку считывания (“neoORF”), что дает, по меньшей мере 61 и не более 113 аминокислот, которые обычно не экспрессируются в здоровых клетках. 61 аминокислота является общей для всех пациентов (консервативная область), в то время как каждый пациент имеет 0-52 дополнительных аминокислот (вариабельная область). Поэтому эпитопы, которые процессируются и презентируются из этой neoORF, являются неоантигенами, которые являются общими для всех пациентов, которые содержат этот одинаковый класс мутаций. GATA3 neoORF, по видимому, являются побочным прогностическим фактором при раке молочной железы. GATA3 дикого типа является сверхэкспрессирующимся геном, и GATA3 neoORF сохраняет эту экспрессию. GATA3 neoORF транслирован и ассоциирован с повышенным риском рака молочной железы.
В некоторых вариантах осуществления, перекрывающиеся длинные пептиды (OLP), которые покрывают всю neoORF, могут использоваться для лечения рака. В некоторых аспектах, OLP, описанные в настоящем изобретении, были сконструированы так, чтобы включать эпитопы на концах пептидов, которые упрощают процесс процессинга и презентирования (так как необходим только один расщепляющий агент). В некоторых аспектах, короткие пептиды (например, 9-11 аминокислоты) могут вводиться субъекту для лечения рака, которые связываются с белком MHC I класса. Подходы, описанные в настоящем изобретении, могут использоваться для направления многих антигенов без необходимости выбирать пациентов на основе их HLA композиции.
В некоторых вариантах осуществления, пептиды, описанные в настоящем изобретении, могут содержать модификацию, которая может повышать иммуногенность (например, липидизацию). В некоторых вариантах осуществления, представлен полинуклеотид, кодирующий полипептид, кодируемый всей GATA3 neoORF (например, политела). В некоторых вариантах осуществления, клеточная терапия, такая как сконструированные T-клетки, экспрессирующие TCR-направленные специфические эпитопы, может использоваться для лечения онкологических субъектов.
Синтетические длинные пептиды (SLP), которые покрывают общую область GATA3 белка, раскрыты здесь. Эти пептиды растворимы в составах, описанных в настоящем изобретении, и совместимы с полиICLC для п.к. инъекций. Высокие чистоты и синтетические выходы одного или нескольких таких пептидов могут быть достигнуты принятием псевдо-пролиновых строительных блоков во время твердофазного пептидного синтеза (SPPS). Условия очистки каждого из этих пептидов также были разработаны.
В настоящем изобретении описаны новые иммунотерапевтические агенты и их применение, основанное на открытии неоантигенов, происходящих после событий мутации, уникальных для опухоли индивидуума. Следовательно, настоящее раскрытие, описанное в настоящем изобретении, представляет пептиды, полинуклеотиды, кодирующие пептиды, и агенты, связывающие пептиды, которые могут использоваться, например, для стимулирования иммунного ответа у опухольассоциированного антигена или неоэпитопа, для создания иммуногенной композиции или противораковой вакцины для применения в лечении заболевания.
Следующее ниже описание и примеры подробно иллюстрируют варианты осуществления настоящего описания. Следует понимать, что это настоящее описание не ограничивается конкретными вариантами осуществления, описанными в настоящем изобретении, и само по себе может варьировать. Специалисты в данной области техники поймут, что существуют многочисленные варианты и модификации этого настоящего описания, которые входят в его объем.
Все термины предназначены для понимания так, как они будут поняты специалистом в данной области. Если не определено иное, все технические и научные термины, используемые в настоящем изобретении, имеют то же значение, которое обычно понимается одним из специалистов в области, к которой относится описание.
Заголовки разделов, используемые в настоящем изобретении, предназначены только для организационных целей и не должны рассматриваться как ограничивающие заявленный предмет.
Хотя различные признаки настоящего описания могут быть описаны в контексте одного варианта осуществления, признаки также могут быть предоставлены отдельно или в любой подходящей комбинации. И наоборот, хотя настоящее описание может быть описано в настоящем изобретении в контексте отдельных вариантов осуществления для ясности, настоящее описание может также быть реализованным в единственном варианте.
Следующие ниже определения дополняют определения в данной области техники и относятся к текущей заявке и не должны относиться к какому-либо связанному или не относящемуся к делу случаю, например, к любому патенту или заявке, находящимся в совместном владении. Хотя любые способы и материалы, аналогичные и эквивалентные, описанные в настоящем изобретении, могут использоваться на практике для тестирования настоящего описания, предпочтительные материалы и способы описаны в настоящем изобретении. Соответственно, терминология, используемая в данном документе, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения.
Определения
Терминология, используемая здесь, предназначена только для описания конкретных случаев и не предназначена для ограничения. В этой заявке использование единственного числа включает множественное, если специально не указано иное. Используемые здесь формы единственного числа также включают множественное число, если контекст ясно не указывает на иное.
В этой заявке использование «или» означает «и/или», если не указано иное. Термины «и/или» и «любые их комбинации» и их грамматические эквиваленты, используемые в данном документе, могут использоваться взаимозаменяемо. Эти термины могут передавать то, что специально рассматривается любая комбинация. Исключительно в иллюстративных целях следующие фразы «A, B и/или C» или «A, B, C или любая их комбинация» могут означать «A индивидуально; B индивидуально; C индивидуально; и B; B и C; и C; и A, B и C». Термин «или» может использоваться совместно или отдельно, если контекст специально не относится к отдельному использованию.
Термин «примерно» или «приблизительно» может означать в пределах допустимого диапазона ошибок для конкретного значения, определенного одним из специалистов в данной области техники, что частично будет зависеть от того, как значение измеряется или определяется, то есть от ограничений системы измерения. Например, «примерно» может означать в пределах 1 или более чем 1 стандартного отклонения, на практику в данной области техники. Альтернативно, «примерно» может означать диапазон до 20%, до 10%, до 5% или до 1% от данного значения. Альтернативно, особенно в отношении биологических систем или процессов, термин может означать в пределах порядка величины, в пределах 5-кратного, и более предпочтительно, в пределах 2-кратного значения. Там, где конкретные значения описаны в заявке и формуле изобретения, если не указано иное, термин «примерно» означает в пределах допустимого диапазона ошибок для конкретного значения.
В этом описании и формуле изобретения, слова «содержащий» (и любая форма слова «содержащий», например, «содержать» и «содержит»), «имеющий» (и любая форма слова «имеющий», например «иметь» и «имеет»), «включающий» (и любая форма слова «включающий», такая как «включать» и «включает») или «содержащий» (и любая форма слова «содержащий», такая как «содержит» и «содержать») являются включающими или открытыми и не исключают дополнительных, не перечисленных элементов или стадий способа. Предполагается, что любой вариант осуществления, обсуждаемый в этом описании, может быть реализован в отношении любого способа или композиции настоящего описания, и наоборот. Кроме того, композиции настоящего описания могут использоваться для достижения способов настоящего описания.
Ссылка в описании на «некоторые варианты осуществления», «вариант осуществления», «один вариант осуществления» или «другие варианты осуществления» означает, что конкретный признак, структура или характеристика, описанные в связи с вариантами осуществления, включены по меньшей мере в некоторые варианты осуществления, но не обязательно все варианты осуществления настоящего описания. Для облегчения понимания настоящего описания ниже даны определения некоторых терминов и фраз.
“Главный комплекс гистосовместимости” или “MHC” является кластером генов, которые играют роль в контроле клеточных взаимодействий, отвечающих за физиологические иммунные ответы. У человека, MHC комплекс также известен как комплекс человеческих лейкоцитарных антигенов (HLA). Подробное описание комплексов MHC и HLA дано в Paul, Fundamental Immunology, 3rd Ed., Raven Press, New York (1993). “Белки или молекулы главного комплекса гистосовместимости (MHC)”, “молекулы MHC”, “белки MHC” или “белки HLA” следует понимать как белки, способные связывать пептиды, возникающие при протеолитическом расщеплении антигенов белков и представлении потенциальных лимфоцитарных эпитопов (например, T-клеточного эпитопа и B-клеточного эпитопа), транспортирующих их на поверхность клетки и презентирующих их там специфическим клеткам, в частности, цитотоксическим T-лимфоцитам, T-хелперным клеткам или B-клеткам. Главный комплекс гистосовместимости в геноме содержит генетическую область, генные продукты которой, экспрессированные на поверхности клетки, являются важными для связывания и презентирования эндогенных и/или чужеродных антигенов и, следовательно, для регулирования иммунологических процессов. Главный комплекс гистосовместимости классифицирован на две группы генов, кодирующих для разных белков, в именно молекул MHC I класса и молекул MHC II класса. Клеточная биология и профили экспрессии двух классов MHC адаптированы для этих разных ролей.
“Человеческий лейкоцитарный антиген” или “HLA” является белком главного комплекса гистосовместимости (MHC) I класса или II класса (см., например, Stites, et al., Immunology, 8thEd., Lange Publishing, Los Altos, Calif. (1994).
“Полипептид”, “пептид” и их грамматические эквиваленты в настоящем изобретении относятся к полимеру аминокислотного остатка, обычно, L-аминокислотам, соединенным друг с другом, обычно пептидными связями между α-амино и карбоксильной группами соседних аминокислот. Полипептиды и пептиды включают, но не ограничены ими, “мутантные пептиды”, “пептиды неоантигена” и “неоантигенные пептиды”. Полипептиды или пептиды могут быть разной длины, либо в их нейтральных (незаряженных) формах, которые являются солями, либо свободными от модификаций, таких как гликозилирование, окисление боковые цепей или фосфорилирование, либо содержать эти модификации, при условии, что модификация не разрушает биологическую активность полипептидов, описанных в настоящем изобретении. “Зрелым белком” является белок, который имеет полную длину и который, необязательно, включает гликозилирование или другие модификации, типовые для белка в данной клеточной среде. Полипептиды и белки, описанные в настоящем изобретении (включая их функциональные части и функциональные варианты) могут содержать синтетические аминокислоты вместо одной или более существующих в природе аминокислот. Такие синтетические аминокислоты известны в данной области техники и включают, например, аминоциклогексанкарбоновую кислоту, норлейцин, α-амино н-декановую кислоту, гомосерин, S-ацетиламинометилцистеин, транс-3- и транс-4-гидроксипролин, 4-аминофенилаланин, 4-нитрофенилаланин, 4-хлорфенилаланин, 4-карбоксифенилаланин, β-фенилсерин β-гидроксифенилаланин, фенилглицин, α-нафтилаланин, циклогексилаланин, циклогексилглицин, индолин-2-карбоновую кислоту, 1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту, аминомалоновую кислоту, моноамид аминомалоновой кислоты, N’-бензил-N’-метиллизин, N’,N’-дибензиллизин, 6-гидроксилизин, орнитин, α-аминоциклопентанкарбоновой кислоты, α-аминоциклогексанкарбоновой кислоты, α-аминоциклогептанкарбоновой кислоты, α-(2-амино-2-норборнан)карбоновой кислоты, α,γ-диаминомасляной кислоты, α,β-диаминопропионовой кислоты, гомофенилаланина и α-трет-бутилглицина. Настоящее описание дополнительно рассматривает, что экспрессия полипептидов, описанная в настоящем изобретении, в сконструированной клетке может быть связана с пост-трансляционными модификациями одной или более аминокислот полипептидных конструктов. Не ограничивающие примеры пост-трансляционных модификаций включают фосфорилирование, ацилирование, включая ацетилирование и формилирование, гликозилирование (включая N-связанное и O-связанное), амидирование, гидроксилирование, алкилирование, включая метилирование и этилирование, убиквитинирование, добавление пирролидонкарбоновой кислоты, образование дисульфидных мостиков, сульфирование, миристоилирование, пальмитоилирование, изопренилирование, фарнезилирование, геранилирование, глипиацию, липоилирование и йодирование.
Пептид или полипептид может содержать по меньшей мере одну фланкирующую последовательность. Термин “фланкирующая последовательность” в настоящем изобретении относится к фрагменту или области пептида, которая не является частью эпитопа.
“Иммуногенный” пептид или “иммуногенный” эпитоп или “пептидный эпитоп” является пептидом, который содержит аллель-специфический мотив так, что пептид будет связывать HLA молекулу и вызывать клеточно-опосредованный или гуморальный ответ, например, ответ цитотоксического T лимфоцита (CTL (например, CD8+)), хелперного T лимфоцита (Th (например, CD4+)) и/или B лимфоцита. Таким образом, иммуногенные пептиды, описанные в настоящем изобретении, способны связывать подходящую молекулу HLA и затем вызывать CTL (цитотоксический) ответ, или HTL (и гуморальный) ответ, на пептид.
“Неоантиген” означает опухолевые антигены, которые возникают при опухольспецифических изменения в белках. Неоантигены охватывают, но не ограничены ими, опухолевые антигены, которые возникают при, например, замещении в последовательности белка, мутации со сдвигом рамки, слиянии полипептида, делеции внутри рамки считывания, вставки, экспрессии эндогенных ретровирусных полипептидов и опухолеспецифической сверхэкспрессии полипептидов.
Термин “остаток” относится к аминокислотному остатку или аминокислотному миметику остатка, введенному в пептид или белок через амидную связь или миметик амидной связи, и нуклеиновой кислоте (ДНК или РНК), которая кодирует аминокислоту или миметик аминокислоты.
“Неоэпитоп”, “опухолеспецифический неоэпитоп” или “опухолевый антиген” относится к эпитопу или области антигенной детерминанты, которая не присутствует в ссылке, такой как не болезненная клетка, например, не раковая клетка или первичная клетка, но найдена в болезненной клетке, например, раковой клетке. Это включает ситуации, где соответствующий эпитоп найден в нормальной не болезненной клетке или первичной клетке, но, из-за одной или более мутаций в болезненной клетке, например, раковой клетке, последовательность эпитопа изменена так, чтобы получить неоэпитоп. Термин “неоэпитоп” в настоящем изобретении относится к области антигенной детерминанты в пептиде или неоантигенном пептиде. Неоэпитоп может содержать по меньшей мере один “якорный остаток” и, по меньшей мере одну “фланкирующую область якорного остатка”. Неоэпитоп может дополнительно содержать “область разделения”. Термин “якорный остаток” относится к аминокислотному остатку, который связывается со специфическими карманами на HLA, что вызывает специфичность взаимодействие с HLA. В некоторых случаях, якорный остаток может быть в каноническом якорном положении. В других случаях, якорный остаток может быть в не каноническом якорном положении. Неоэпитопы могут связываться с молекулами HLA через первичные и вторичные якорные остатки, выступающие в карманах в пептидных полостях связывания. В пептидных полостях связывания, определенные аминокислоты составляют карманы, в которых размещены соответствующие боковые цепи якорных остатков представленных неоэпитопов. Предпочтения пептидного связывания существуют среди различных аллелей обеих HLA I и HLA II молекул. Молекулы HLA I класса связывают короткие неоэпитопы, N- и C-концы которых закреплены в карманах, расположенных на концах полостей связывания неоэпитопа. Хотя большинство связывающих неоэпитопов HLA I класса имеют примерно 9 аминокислот, более длинные неоэпитопы могут быть могут быть размещены за счет выпуклости их центральной части, что вызывает связывание неоэпитопов из примерно 8-12 аминокислот. Неоэпитопы, связывающиеся с белками HLA II класса, не ограничены в размере и могут варьировать от приблизительно 16-25 аминокислот. Полость связывания неоэпитопов в молекуле HLA II класса открыта на обоих концах, что позволяет связывание пептидов с относительно большой длиной. Этот коровый сегмент длиной 9 аминокислотных остатков больше всего способствует распознаванию неоэпитопа, фланкирующие области якорного остатка также являются важными для специфичности пептида к аллели HLA II класса. В некоторых случаях, фланкирующей областью якорного остатка являются N-концевые остатки. В другом случае, фланкирующей областью якорного остатка являются C-концевые остатки. В еще одном случае, фланкирующей областью якорного остатка являются и N-концевые остатки, и C-концевые остатки. В некоторых случаях, фланкирующая область якорного остатка фланкирована, по меньшей мере двумя якорными остатками. Фланкирующая область якорного остатка, фланкированная якорными остатками, является “областью разделения.”
«Ссылка» может быть использована для корреляции и сравнения результатов, полученных в способах согласно настоящему описанию на образце опухоли. Обычно «ссылка» может быть получена на основе одного или нескольких нормальных образцов, в частности образцов, которые не поражены раком, либо полученных от пациента или одного или нескольких разных индивидуумов, например, здоровых индивидуумов, в частности, индивидуумов одного и того же вида. «Ссылка» может быть определена эмпирически, путем тестирования достаточно большого количества нормальных образцов.
“Эпитоп” является коллективной характеристикой молекулы, такой как первичная, вторичная и третичная пептидная структура, и заряда, которые вместе формируют сайт, распознаваемый, например, иммуноглобулином, Т-клеточным рецептором, HLA молекулой или химерным антигенным рецептором. Альтернативно, эпитоп может быть определен как совокупность аминокислотных остатков, которые вовлечены в распознавание конкретным иммуноглобулином, или, в контексте T-клеток, остатков, которые необходимы для распознавания белками Т-клеточного рецептора, химерными антигенными рецепторами и/или рецепторами главного комплекса гистосовместимости (MHC). “T-клеточный эпитоп” должен пониматься как означающий пептидную последовательность, которая может быть связана молекулами MHC I или II класса в форме пептид-презентирующих молекул MHC или комплекса MHC, и затем, в этой форме, быть распознана и связана T-клетками, такими как T-лимфоциты или T-хелперные клетки. Эпитопы могут быть получены выделением из природного источника, или они могут быть синтезированы согласно стандартным протоколам в данной области техники. Синтетические эпитопы могут содержать искусственные аминокислотные остатки, “аминокислотные миметики”, такие как D изомеры существующих в природе L аминокислотных остатков или не существующих в природе аминокислотных остатков, таких как циклогексилаланин. В настоящем описании, эпитопы могут быть обозначены в некоторых случаях как пептиды или пептидные эпитопы. Должно быть понятно, что белки или пептиды, которые содержат эпитоп или аналог, описанный в настоящем изобретении, а также дополнительную аминокислоту(ы) все еще включены в рамки настоящего описания. В определенных вариантах осуществления, пептид содержит фрагмент антигена. В определенных вариантах осуществления, существует ограничение по длине пептида настоящего описания. Вариант осуществления с ограничением по длине существует, когда белок или пептид, содержащий эпитоп, описанный в настоящем изобретении, содержит область (т.е., непрерывный ряд аминокислотных остатков), имеющую 100% идентичность с исходной последовательностью. Чтобы избежать определения эпитопа из считывания, например, на полных природных молекулах, существует ограничение по длине любой области, которая имеет 100% идентичность с исходной пептидной последовательностью. Таким образом, для пептида, содержащего эпитоп, описанный в настоящем изобретении, и область с 100% идентичностью с исходной пептидной последовательностью, область с 100% идентичностью с исходной пептидной последовательностью обычно имеет длину: менее чем или равную 600 аминокислотным остаткам, менее чем или равную 500 аминокислотным остаткам, менее чем или равную 400 аминокислотным остаткам, менее чем или равную 250 аминокислотным остаткам, менее чем или равную 100 аминокислотным остаткам, менее чем или равную 85 аминокислотным остаткам, менее чем или равную 75 аминокислотным остаткам, менее чем или равную 65 аминокислотным остаткам, и менее чем или равную 50 аминокислотным остаткам. В определенных вариантах осуществления, “эпитоп”, описанный в настоящем изобретении, состоит из пептида, имеющего область с менее чем 51 аминокислотными остатками, которая имеет 100% идентичностью с исходной пептидной последовательностью, с любым шагом до 5 аминокислотных остатков; например 50, 49, 48, 47, 46, 45, 44, 43, 42, 41, 40, 39, 38, 37, 36, 35, 34, 33, 32, 31, 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 аминокислотных остатков.
Номенклатура, использованная для описания пептидов или белков, следует обычно практике, где аминогруппа представлена слева (амино- или N-конец) и карбоксильная группа справа (карбокси- или C-конец) каждого аминокислотного остатка. Если положения аминокислот упоминаются в пептидном эпитопе, они пронумерованы в направлении от амино к карбоксилу, где положение один расположено на амино конце эпитопа, или пептиде или белке, в состав которого он может входить. В формуле, представляющей выбранные конкретные варианты осуществления настоящего описания, амино- и карбоксил-концевые группы, хотя не показаны специально, имеют форму, которую они могли бы принять при физиологических значениях pH, если не указано иначе. В формуле аминокислотной структуры, каждый остаток обычно представлен стандартными трехбуквенными или однобуквенными обозначениями. L-форма аминокислотного остатка представлены заглавной буквой или заглавной буквой трехбуквенного символа, и D-форма для тех аминокислотных остатков, которые имеют D-формы, представлена одной строчной буквой или строчным трехбуквенным символом. Однако, если трехбуквенные символы или полные наименования используют без заглавных букв, они могут относиться к L аминокислотным остаткам. Глицин не имеет асимметрического атома углерода и просто обозначен как “Gly” или “G”. Аминокислотные последовательности пептидов, представленных в настоящем изобретении, обычно обозначены с применением стандартных буквенных символов. (A, Аланин; C, Цистеин; D, Аспарагиновая кислота; E, Глутаминовая кислота; F, Фенилаланин; G, Глицин; H, Гистидин; I, Изолейцин; K, Лизин; L, Лейцин; M, Метионин; N, Аспарагин; P, Пролин; Q, Глутамин; R, Аргинин; S, Серин; T, Треонин; V, Валин; W, Триптофан; и Y, Тирозин.)
Термин “мутация” относится к изменению или разнице в последовательности нуклеиновой кислоты (нуклеотидному замещению, добавлению или делеции) по сравнению со ссылкой. “Соматическая мутация” может происходить в любой из клеток тела, за исключением зародышевых клеток (спермы и яйцеклеток), и поэтому передается детям. Эти изменения (но не всегда) вызывают рак или другие заболевания. В некоторых вариантах осуществления, мутацией является не-несмысловая мутация. Термин “не-несмысловая мутация” относится к мутации, например, нуклеотидному замещению, которые не вызывает изменение аминокислоты, такое как замещение аминокислоты в продукте трансляции. “Сдвиг рамки” происходит, когда мутация прерывает нормальную фазу периодичности кодона гена (также известного как “рамка считывания”), вызывая трансляцию не природной последовательности белков. Для разных мутаций в гене возможно достижение одной и той же измененной рамки считывания.
“Консервативной” аминокислотной заменой является такая, при которой один аминокислотный остаток заменяется на другой аминокислотный остаток, имеющий аналогичную боковую цепь. Семейства аминокислотных остатков, имеющих аналогичные боковые цепи, определены в данной области техники, включая основные боковые цепи (например, лизин, аргинин, гистидин), кислые боковые цепи (например, аспарагиновая кислота, глутаминовая кислота), не измененные полярные боковые цепи (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), не полярные боковые цепи (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленные боковые цепи (например, треонин, валин, изолейцин) и ароматические боковые цепи (например, тирозин, фенилаланин, триптофан, гистидин). Например, замена фенилаланина на тирозин является консервативной заменой. Способы идентификации нуклеотида и аминокислотных консервативных замещений, которые не ликвидируют пептидную функцию, хорошо известны в данной области техники.
В настоящем изобретении, термин “аффинность” относится к мере силы связывания между двумя членами связывающейся пары, например, HLA-связывающего пептида и HLA I или II класса. KD является константой диссоциации и измеряется в единицах молярности. Аффинная константа является величиной, обратной константе диссоциации. Аффинную константу иногда используют как общий термин для описания этого химической структурной единицы. Она является прямой мерой энергии связывания. Аффинность может быть определена экспериментально, например, поверхностным плазмонным резонансом (SPR) с применением коммерчески доступных Biacore SPR единиц. Аффинность также может быть выражена как ингибирующая концентрация 50 (IC50), то есть концентрация, при которой 50% пептида замещается, ln(IC50) относится к естественному логарифму IC50. Koff относится к константе скорости диссоциации, например, для диссоциации HLA-связывающего пептида и HLA I или II класса. В этом описании, результаты “данных связывания” могут быть выражены как “IC50. ”IC50 является концентрацией тестированного пептида в анализе связывания, при которой наблюдается 50% ингибирование связывания меченного ссылочного пептида. В данных условиях, в которых проводят анализы (т.е., ограничение концентраций HLA белка и меченного ссылочного пептида), эти значения имитируют значения KD. Анализы для определения связывания известны в данной области техники и описаны подробно, например, в публикациях PCT WO 94/20127 и WO 94/03205, и других публикациях, таких как Sidney et al., Current Protocols in Immunology 18,3,1 (1998); Sidney, et al., J. Immunol. 154:247 (1995); и Sette, et al., Mol. Immunol. 31:813 (1994). Альтернативно, связывание может выражаться относительно связывания ссылочным стандартным пептидом. Например, могут быть основаны на их IC50, в сравнении с IC50 ссылочного стандартного пептида. Связывание также может быть определено с применением других аналитических систем, включающих такие, которые используют: живые клетки (например, Ceppellini et al., Nature 339:392 (1989); Christnick et al., Nature 352:67 (1991); Busch et al., Int. Immunol. 2:443 (1990); Hill et al., J. Immunol. 147:189 (1991); del Guercio et al., J. Immunol. 154:685 (1995)), не содержащие клетки системы с применением моющих лизатов (например, Cerundolo et al., J. Immunol. 21:2069 (1991)), иммобилизованных очищенных MHC (например, Hill et al., J. Immunol. 152, 2890 (1994); Marshall et al., J. Immunol. 152:4946 (1994)), систем ELISA (например, Reay et al., EMBO J. 11:2829 (1992)), поверхностного плазмонного резонанса (например, Khilko et al., J. Biol. Chem. 268:15425 (1993)); анализов в растворимой фазе с большой плотностью потока (Hammer et al., J. Exp. Med. 180:2353 (1994)) и измерения стабилизации или сборки MHC I класса (например, Ljunggren et al., Nature 346:476 (1990); Schumacher et al., Cell 62:563 (1990); Townsend et al., Cell 62:285 (1990); Parker et al., J. Immunol. 149:1896 (1992)).“Перекрестно-реактивное связывание” означает, что пептид связан более чем одной HLA молекулой; синонимом является вырожденное связывание.
Термин “производный” и его грамматические эквиваленты, при применении в обсуждении эпитопа, является синонимом для “полученный” и его грамматическим эквивалентам. Производный эпитоп может быть выделен из природного источника, или он может быть синтезирован согласно стандартным протоколам в данной области техники. Синтетические эпитопы могут содержать искусственные аминокислотные остатки “аминокислотные миметики”, такие как D изомеры существующих в природе L аминокислотных остатков или не существующих в природе аминокислотных остатков, таких как циклогексилаланин. Производный или полученный эпитоп может быть аналогом природного эпитопа.
“Природная” или “дикого типа” последовательность относится к последовательности, найденной в природе. Такая последовательность может содержать более длинные последовательности в природе.
“Рецептор” следует понимать как означающий биологическую молекулу или группу молекул, способных связывать лиганд. Рецептор может служить для передачи информации в клетке, клеточном образовании или организме. Рецептор содержит по меньшей мере одну рецепторную единицу, например, где каждая рецепторная единица может состоять из молекулы белка. Рецептор имеет структуру, которая комплементарна структуре лиганда и может образовывать комплекс с лигандом в качестве связывающего партнера. Информация передается, в частности, конформационными изменениями рецептора после комплексообразования лиганда на поверхности клетки. В некоторых вариантах осуществления, рецептор понимается как обозначение, в частности, белков MHC I и II классов, способных образовывать комплекс рецептор/лиганд с лигандом, в частности, пептидом или пептидным фрагментом подходящей длины.
“Лиганд” понимается как означающий молекулу, которая имеет структуру, комплементарную структуре рецептора, и способна образовывать комплекс с этим рецептором. В некоторых вариантах осуществления, лиганд понимается как означающий пептид или пептидный фрагмент, который имеет подходящую длину и подходящие связывающие мотивы в его аминокислотной последовательности, так, что пептид или пептидный фрагмент способен образовывать комплекс с белками MHC I класса или MHC II класса.
В некоторых вариантах осуществления, “комплекс рецептор/лиганд ” также понимается как означающий “комплекс рецептор/пептид” или “комплекс рецептор/пептидный фрагмент”, включая пептид- или пептидный фрагмент-презентирующую молекулу MHC I класса или II класса.
“Синтетический пептид” относится к пептиду, который получают из не природного источника, например, созданный человеком. Такие пептиды могут быть получены с применением таких способов, как химический синтез или технология рекомбинантной ДНК. “Синтетические пептиды” включают “слитые белки”.
Термин “мотив” относится к шаблону остатков в аминокислотной последовательности определенной длины, например, пептиду длиной менее чем примерно 15 аминокислотных остатков, или длиной менее чем примерно 13 аминокислотных остатков, например, от приблизительно 8 до приблизительно 13 аминокислотных остатков (например, 8, 9, 10, 11, 12 или 13) для HLA мотива I класса и от приблизительно 6 до приблизительно 25 аминокислотных остатков (например, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25) для HLA мотива II класса, который распознается конкретной молекулой HLA. Мотивы обычно отличаются для каждого белка HLA, кодированного данной HLA аллелем человека. Эти мотивы отличаются их шаблоном первичных и вторичных якорных остатков. В некоторых вариантах осуществления, MHC мотив I класса определяет пептид длиной 9, 10 или 11 аминокислотных остатков.
Термин “существующий в природе” и его грамматические эквиваленты в настоящем изобретении относится к тому факту, что объект может быть найден в природе. Например, пептид или нуклеиновая кислота, которые присутствуют в организме (включая вирусы) и могут быть выделены из источника в природе, и которые не модифицированы преднамеренно человеком, являются существующими в природе.
Согласно настоящему описанию, термин “вакцина” относится к фармацевтическому препарату (фармацевтической композиции) или продукту, который при введении вызывает иммунный ответ, например, клеточный или гуморальный иммунный ответ, который распознает и атакует патоген или болезненную клетку, такую как раковая клетка. Вакцина может использоваться для профилактики или лечения заболевания. Термин “индивидуализированная противораковая вакцина” или “персонализированная противораковая вакцина” относится к конкретному онкологическому пациенту и означает, что противораковая вакцина адаптирована к нуждам или особым обстоятельствам отдельного онкологического пациента.
“Антигенный процессинг” или “процессинг” и его грамматические эквиваленты относится к разложению полипептида или антигена на продукты процессинга, которые являются фрагментами указанного полипептида или антигена (например, разложения полипептида на пептиды) и ассоциации одного или нескольких таких фрагментов (например, через связывание) с MHC молекулами для презентирования клетками, например, антиген-презентирующими клетками, для специфических T-клеток.
“Антигенпрезентирующие клетки” (APC) являются клетками, которые презентируют пептидные фрагменты белковых антигенов в ассоциации с MHC молекулами на их клеточной поверхности. Некоторые APC могут активировать антигенспецифические T-клетки. Профессиональные антигенпрезентирующие клетки являются очень эффективными при поглощении антигена, либо фагоцитозом, либо рецептор-опосредованным эндоцитозом, и затем визуализации фрагмента антигена, связанного с MHC молекулой II класса, на их мембране. T-клетка распознает и взаимодействует с комплексом антиген - MHC молекула II класса на мембране антигенпрезентирующей клетки. Дополнительный костимулирующий сигнал затем вырабатывается антигенпрезентирующей клеткой, что приводит к активации Т-клетки. Экспрессия костиулирующих молекул является определяющим признаком профессиональных антигенпрезентирующих клеток. Основные типы профессиональных антигенпрезентирующих клеток включают дендритные клетки, которые имеют широчайший диапазон презентирования антигенов и являются, вероятно, наиболее важными антигенпрезентирующими клетками, макрофаги, B-клетки и определенные активированные эпителиальные клетки. Дендритные клетки (DC) являются популяциями лейкоцитов, которые презентируют антигены, захваченные периферическими тканями в Т-клетки через антигенпрезентирующие пути MHC I и II класса. Хорошо известно, что дендритные клетки являются мощными эвокаторами иммунных ответов, и активация этих клеток является критической стадией для индукции противоопухолевого иммунитета. Дендритные клетки для удобства разделены на категории “незрелых” и “зрелых” клеток, которые могут использоваться в качестве простого пути различения двух хорошо охарактеризованных фенотипов. Однако эта номенклатура не должна считаться как исключающая все возможные промежуточные стадии дифференциации. Незрелые дендритные клетки характеризуются как антигенпрезентирующие клетки с высокой способностью поглощения и процессинга антигена, что коррелирует с высокой экспрессией Fc рецептора (FcR) и рецептора маннозы. Зрелый фенотип обычно характеризуется более низкой экспрессией этих маркеров, но высокой экспрессией поверхностноклеточных молекул, отвечающих за активацию Т-клетки, такой как MHC I класса и II класса, адгезивных молекул (например, CD54 и CD11) и костимулирующих молекул (например, CD40, CD80, CD86 и 4-1 BB).
Термины “идентичный” и его грамматические эквиваленты в настоящем изобретении, или “идентичность последовательности” в контексте двух последовательностей нуклеиновых кислот или аминокислотных последовательностей полипептидов, относится к остаткам в двух последовательностях, которые являются одинаковыми при выравнивании для максимального соответствия в определенном окне сравнения. “Окно сравнения” в настоящем изобретении относится к сегменту по меньшей мере приблизительно 20 непрерывных положений, обычно от приблизительно 50 до приблизительно 200, более обычно, от приблизительно 100 до приблизительно 150, где последовательность может сравниваться со ссылочной последовательностью с тем же количеством непрерывных положений поле оптимального выравнивания двух последовательностей. Способы выравнивания последовательностей для сравнения хорошо известны в данной области техники. Оптимальное выравнивание последовательностей для сравнения может быть проведено с применением алгоритма локальной гомологии из Smith and Waterman, Adv. Appl. Math., 2:482 (1981); алгоритмом выравнивания из Needleman and Wunsch, J. Mol. Biol., 48:443 (1970); поиском методом подобия из Pearson and Lipman, Proc. Nat. Acad. Sci. U.S.A., 85:2444 (1988); компьютеризованными реализациями этих алгоритмов (включая, но не ограничиваясь ими, CLUSTAL в программе PC/Gene от Intelligentics, Mountain View Calif., GAP, BESTFIT, BLAST, FASTA и TFASTA в Wisconsin Genetics Software Package, Genetics Computer Group (GCG), 575 Science Dr., Madison, Wis., U.S.A.); программа CLUSTAL хорошо описана в Higgins and Sharp, Gene, 73:237-244 (1988) и Higgins and Sharp, CABIOS, 5:151-153 (1989); Corpet et al., Nucleic Acids Res., 16:10881-10890 (1988); Huang et al., Computer Applications in Biosciences, 8:155-165 (1992); и Pearson et al., Methods in Molecular Biology, 24:307-331 (1994). Выравнивание часто проводят через проверку и ручное выравнивание. В одном классе вариантов осуществления, полипептиды в настоящем изобретении имеют по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности со ссылочным полипептидом или его фрагментом, например, по данным BLASTP (или CLUSTAL, или любой другой доступной программы для выравнивания), с применением параметров по умолчанию. Также, нуклеиновые кислоты также могут быть описаны со ссылкой на исходную нуклеиновую кислоту, например, они могут иметь 50%, 60%, 70%, 75%, 80%, 85%, 90%, 98%, 99% или 100% идентичность последовательности со ссылочной нуклеиновой кислотой или ее фрагментом, например, по данным BLASTN (или CLUSTAL, или любой другой доступной программы для выравнивания) с применением параметров по умолчанию. Если говорят, что одна молекула имеет определенный процент идентичности последовательности с большей молекулой, это означает, что когда две молекулы оптимально выровнены, указанный процент остатков в меньшей молекуле совпадает с остатками в большей молекуле в соответствии с порядком, в котором две молекулы оптимально выровнены.
Термин “по существу идентичная” и его грамматические эквиваленты, используемый к последовательностям нуклеиновых кислот или аминокислот, означает, что последовательность нуклеиновой кислоты или аминокислоты содержит последовательность, которая имеет по меньшей мере 90% идентичность последовательности или более, по меньшей мере 95%, по меньшей мере 98% и по меньшей мере 99%, по сравнению со ссылочной последовательностью с применением программ, описанных выше, например, BLAST, с применением стандартных параметров. Например, программа BLASTN (для нуклеотидных последовательностей) применяет в качестве параметров по умолчанию длину слова (W) 11, ожидание (E) 10, M=5, N=-4, и сравнение обоих цепей. Для аминокислотных последовательностей, программа BLASTP применяет в качестве параметров по умолчанию длину слова (W) 3, ожидание (E) 10, и матрицу замен BLOSUM62 (см. Henikoff & Henikoff, Proc. Natl. Acad. Sci. USA 89:10915 (1992)). Долю идентичности последовательности определяют сравнением двух оптимально выровненных последовательностей в окне сравнения, где часть полинуклеотидной последовательности в окне сравнения может содержать добавления или делеции (т.е., гэпы) по сравнению со ссылочной последовательностью (которая не содержит добавления или делеции) для оптимального выравнивания двух последовательностей. Долю рассчитывают через определение количества положений, в которых идентичное основание нуклеиновой кислоты или аминокислотный остаток существуют в обеих последовательностях с получением количества совпадающих положений, деление количества совпадающих положений на общее количество положений в окне сравнения и умножение результата на 100 с получением процентной доли идентичности последовательности. В вариантах осуществления, идентичность по существу существует в области последовательностей, которая имеет длину, по меньшей мере приблизительно 50 остатков, в области, по меньшей мере приблизительно 100 остатков, и в вариантах осуществления, последовательности по существу идентичных в, по меньшей мере приблизительно 150 остатков. В вариантах осуществления, последовательности по существу идентичны по всей длине кодирующих областей.
Термин “вектор” в настоящем изобретении означает конструкцию, которая способна доставлять и обычно экспрессировать один или более генов или последовательностей, представляющих интерес, в клетках-хозяевах. Примеры векторов включают, но не ограничены ими, вирусные векторы, векторы экспрессии голой ДНК или РНК, плазмиду, космиду или фаговые векторы, векторы экспрессии ДНК или РНК, ассоциированные с катионными конденсирующими агентами, и векторы экспрессии ДНК или РНК, инкапсулированные в липосомы.
Полипептидом, антителом, полинуклеотидом, вектором, клеткой или композицией, которые “выделены”, является полипептид, антитело, полинуклеотид, вектор, клетка или композиция, которые имеют форму, не имеющеюся в природе. Выделенные полипептиды, антитела, полинуклеотиды, векторы, клетки или композиции включают такие, которые были очищены до степени, в которой они больше не имеют форму, в которой они находятся в природе. В некоторых вариантах осуществления, полипептид, антитело, полинуклеотид, вектор, клетка или композиция, которая выделена, является по существу чистой. В некоторых вариантах осуществления, “выделенный полинуклеотид” охватывает ПЦР или количественную ПЦР реакцию, содержащую полинуклеотид, амплифицированный в ПЦР или количественной ПЦР реакции.
Термин “выделенный”, “биологически чистый” или их грамматические эквиваленты относится к материалу, который по существу или преимущественно не содержит компоненты, которые обычно сопровождают материал в его исходном состоянии. Таким образом, выделенные пептиды, описанные в настоящем изобретении, не содержат некоторые или все материалы, обычно ассоциированные с пептидами в их in situ среде. “Выделенный” эпитоп относится к эпитопу, который не включает полную последовательность антигена, из которого произведен эпитоп. Обычно “выделенный” эпитоп не имеет присоединенные к нему дополнительные аминокислотные остатки, которые дают последовательность, которая имеет 100% идентичность по всей длине исходной последовательности. Исходной последовательностью может быть последовательность, такая как опухолеассоциированный антиген, из которого получен эпитоп. Таким образом, термин “выделенный” означает, что материал удаляют из его исходной среды (например, природной среды, если он существует в природе). “Выделенной” нуклеиновой кислотой является нуклеиновая кислота, удаленная из ее природной среды. Например, существующий в природе полинуклеотид или пептид, присутствующий в живом животном, не является выделенным, но тот же полинуклеотид или пептид, отделенный от некоторых или всех сосуществующих с ним материалов в природной системе, является выделенным. Такой полинуклеотид может быть частью вектора, и/или такой полинуклеотид или пептид может быть частью композиции, и все еще быть “выделенным” в том смысле, что такой вектор или композиция не является частью его природной среды. Выделенные РНК молекулы включают in vivo или in vitro РНК транскрипты ДНК молекул, описанных в настоящем изобретении, и дополнительно включают такие молекулы, полученные синтетически.
Термин “по существу очищенный” и его грамматические эквиваленты в настоящем изобретении относится к последовательности нуклеиновых кислот, полипептиду, белку или другому соединению, которое по существу не содержит, т.е., не содержит более чем приблизительно 50%, не содержит более чем приблизительно 70%, не содержит более чем приблизительно 90% полинуклеотидов, белков, полипептидов и других молекул, с которыми он ассоциирован в природе.
Термин “по существу чистый” в настоящем изобретении относится к материалу, который на, по меньшей мере 50% чистый (т.е., не содержит примеси), по меньшей мере 90% чистый, по меньшей мере 95% чистый, по меньшей мере 98% чистый, или, по меньшей мере 99% чистый.
Термины “полинуклеотид”, “нуклеотид”, “нуклеиновая кислота”, “полинуклеиновая кислота” или “олигонуклеотид” и их грамматические эквиваленты используются взаимозаменяемо в настоящем изобретении и относятся к полимерам нуклеотидов любой длины, и включают ДНК и РНК, например, мРНК. Таким образом, эти термины включают двухцепочечные и одноцепочечные ДНК, трехцепочечные ДНК, а также двухцепочечные и одноцепочечные РНК. Они также включают модифицированные, например, метилированием и/или кэпированием, и не модифицированные формы полинуклеотида. Термин также включает молекулы, которые включают не существующие в природе или синтетические нуклеотиды, а также аналоги нуклеотида. Последовательности нуклеиновых кислот и векторы, раскрытые или рассматриваемые в настоящем изобретении, могут быть введены в клетку, например, трансфекцией, трансформацией или трансдукцией. Нуклеотидами могут быть деоксирибонуклеотиды, рибонуклеотиды, модифицированные нуклеотиды или основания и/или их аналоги, или любой субстрат, который может быть введен в полимер ДНК или РНК полимеразами. В некоторых вариантах осуществления, полинуклеотид и нуклеиновая кислота могут быть in vitro транскрибированной мРНК. В некоторых вариантах осуществления, полинуклеотидом, который вводят с применением способов настоящего описания, является мРНК.
“Трансфекция”, “трансформация” или “трансдукция” в настоящем изобретении относятся к введению одного или нескольких экзогенных полинуклеотидов в клетку-хозяина с применением физических или химических способов. Многие методики трансфекции известны в данной области техники и включают, например, совместное осаждение фосфата кальция и ДНК (см., например, Murray E. J. (ed.), Methods in Molecular Biology, Vol. 7, Gene Transfer and Expression Protocols, Humana Press (1991)); DEAE-декстран; электропорацию; катионную липосома-опосредованную трансфекцию; усиленную частицами вольфрама бомбардировку микрочастицами (Johnston, Nature, 346: 776-777 (1990)); и совместное осаждение фосфата стронция и ДНК (Brash et al., Mol. Cell Biol., 7: 2031-2034 (1987)). Фаговые или вирусные векторы могут быть введены в клетки-хозяева после роста инфекционных частиц в подходящих упаковывающих клетках, многие из которых коммерчески доступны.
Нуклеиновые кислоты и/или последовательности нуклеиновых кислот являются “гомологичными”, когда их получают, естественно или искусственно, из известных предковых нуклеиновых кислот или последовательностей нуклеиновых кислот. Белки и/или белковые последовательности являются “гомологичными”, когда кодирующие их ДНК получают, естественно или искусственно, из известных предковых нуклеиновых кислот или последовательностей нуклеиновых кислот. Гомологичные молекулы могут называться гомологами. Например, любые существующие в природе белки, такие как описаны в настоящем изобретении, могут быть модифицированы любым доступным способом мутагенеза. При экспрессии, такие мутагенизированные нуклеиновые кислоты кодируют полипептид, который является гомологичным к белку, кодированному исходной нуклеиновой кислотой. Гомология обычно выводится из идентичности последовательности между двумя или несколькими нуклеиновыми кислотами или белками (или их последовательностями). Точная процентная доля идентичности между последовательностями, которые используют для установления гомологии, зависит от нуклеиновой кислоты и белка, о которых идет речь, но не менее 25% идентичность последовательности обычно используют для установления гомологии. Более высокие уровни идентичности последовательности, например, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 99% или более, также могут использоваться для установления гомологии. Способы определения долей идентичности последовательности (например, BLASTP и BLASTN с применением параметров по умолчанию) описаны в настоящем изобретении и обычно доступны.
Термин «субъект» относится к любому животному (например, млекопитающему), включая, но не ограничиваясь ими, людей, приматов, отличных от человека, собак, кошек, грызунов и подобных, которые подлежат особому лечению. Обычно термины «субъект» и «пациент» используются здесь взаимозаменяемо по отношению к человеку.
Термин «эффективное количество», «терапевтически эффективное количество» или «терапевтический эффект» относится к количеству терапевтического агента, эффективному для «лечения» заболевания или расстройства у субъекта или млекопитающего. Терапевтически эффективное количество лекарственного средства имеет терапевтический эффект и как таковое может предотвращать развитие заболевания или расстройства; замедлять развитие заболевания или расстройства; замедлять прогрессирование заболевания или расстройства; облегчать до некоторой степени один или более симптомов, связанных с заболеванием или расстройством; снижать заболеваемость и смертность; улучшать качество жизни; или комбинация таких эффектов.
Термин «лечащий» или «лечение» или «лечить» или «облегчение» или «облегчать» относятся к обеим (1) терапевтическим мерам, которые излечивают, замедляют, ослабляют симптомы и/или останавливают прогрессирование диагностированного патологического состояния или расстройства; и (2) профилактическим или превентивным мерам, которые предотвращают или замедляют развитие целевого патологического состояния или расстройства. Таким образом, те, кто нуждается в лечении, включают тех, кто уже имеет расстройство; склонных к расстройству; и тех, у которых нужно предотвратить расстройство.
«Фармацевтически приемлемая» относится к обычно нетоксичной, инертной и/или физиологически совместимой композиции или компоненту композиции.
«Фармацевтический эксципиент» или «эксципиент» содержит материал, такой как адъювант, носитель, регуляторы pH и буферные агенты, агенты, регулирующие тоничность, смачивающие агенты, консерванты и подобные. «Фармацевтический эксципиент» является эксципиентом, который фармацевтически приемлем.
Неоантигены и их применение
Одним из критических барьеров для разработки лечебной и опухолеспецифической иммунотерапии является идентификация и выбор высокоспецифических и ограниченных опухолевых антигенов для того, чтобы избежать аутоиммунитета. Опухолевые неоантигены, которые возникают в результате генетического изменения (например, вставок, транслокаций, делеций, миссенс-мутаций, мутаций сайта сплайсинга и т.д.) в злокачественных Т-клетках, представляют наиболее опухолеспецифический класс антигенов. Неоантигены редко используют в противораковых вакцинах или иммуногенных композиций из-за технических трудностей при их идентификации, выборе оптимизированных антигенов и продуцировании неоантигенов для применения в вакцине или иммуногенной композиции. Эти проблемы могут быть решены: идентификацией мутаций в новообразованиях/опухолях, которые присутствуют на уровне ДНК в опухоли, но не в сопоставленных образцах исходных клеток от значительной доли онкологических субъектов; анализом идентифицированных мутаций с применением одного или нескольких алгоритмов прогнозирования связывания пептид-MHC для создания множества неоантигенов Т-клеточных эпитопов, которые экспрессированы в новообразовании/опухоли, и которые связаны со значительной долей HLA аллелей пациента; и синтезом множества неоантигенных пептидов, выбранных из множеств всех неоантигенных пептидов и спрогнозированных связывающих пептидов для применения в противораковой вакцине или иммуногенной композиции, подходящей для лечения значительной доли онкологических субъектов.
Например, трансляция информации о секвенировании пептида в терапевтическую вакцину может включать прогнозирование мутированных пептидов, которые могут связываться в HLA молекулами значительной доли индивидуумов. Эффективный выбор того, какие конкретные мутации применять в качестве иммуногена, требует возможности прогнозировать, какие мутированые пептиды будут эффективно связываться с HLA аллелями значительной доли пациентов. В последнее время подходы к обучению на основе нейронных сетей с проверенными связывающими и не связывающими пептидами повысили точность алгоритмов прогнозирования для основных HLA-A и -B аллелей. Однако даже с использованием передовых алгоритмов на основе нейронных сетей для кодирования правил связывания HLA-пептидов несколько факторов ограничивают способность прогнозировать пептиды, презентированные на HLA-аллелях.
Другой пример трансляции информации о секвенировании пептидов в терапевтическую вакцину может включать создание лекарственного препарата в виде мультиэпитопной вакцины с длинными пептидами. Таргетирование как можно большего количества мутировавших эпитопов максимально эффективно использует огромные возможности иммунной системы, предотвращает возможность ускользания от иммунологического ответа за счет понижающей модуляции иммунного таргетированного генного продукта, и компенсирует известную неточность подходов к прогнозированию эпитопов. Синтетические пептиды представляют полезные средства для эффективного получения множества иммуногенов и для быстрого транслирования идентификации мутантных эпитопов в эффективную вакцину. Пептиды могут быть легко синтезированы химически и легко очищены с применением реагентов, не содержащих загрязняющие бактерии или вещества животного происхождения. Маленький размер позволяет четко сфокусироваться на мутированной области белка, и также снижает нерелевантную антигенную конкуренцию других компонентов (антигенов не мутированного белка или вирусного вектора).
Еще один пример трансляции информации о секвенировании пептидов в терапевтическую вакцину может включать комбинацию с сильным вакцинным адъювантом. Эффективные вакцины могут потребовать сильный адъювант для запуска иммунного ответа. Например, поли-ICLC, агонист TLR3 и РНК геликазы-доменов MDA5 и RIG3, показали некоторые желаемые свойства для вакцинного адъюванта. Эти свойства включают индукцию местной и системной активации иммунных клеток in vivo, продуцирование стимулирующих хемокинов и цитокинов, и стимулирование презентирования антигенов DC. Более того, поли-ICLC может вызывать устойчивые CD4+ и CD8+ ответы у людей. Важно, что поразительное сходство в активации путей транскрипции и трансдукции сигнала наблюдалось у субъектов, вакцинированных поли-ICLC, и у добровольцев, получивших высокоэффективную репликационно-способную вакцину против желтой лихорадки. Более того, >90% пациентов с карциномой яичников, иммунизированных поли-ICLC в комбинации с NYESO-1 пептидной вакциной (в дополнение к Монтаниду) показали индукцию CD4+ и CD8+ Т-клеток, в также ответы антитела на пептид в недавней 1 фазе исследования. В то же время, поли-ICLC обширно тестировали в более чем 25 клинических исследованиях на данный момент, и он показал относительно доброкачественный профиль токсичности.
В некоторых аспектах изобретение относится к композиции, содержащей: первый пептид, содержащий первый неоэпитоп белка и второй пептид, содержащий второй неоэпитоп того же белка, полинуклеотид, кодирующий первый пептид и второй пептид, одну или более APC, содержащих первый пептид и второй пептид, или первый Т-клеточный рецептор (TCR), специфический к первому неоэпитопу, в комплексе с HLA белком, и второй TCR специфический ко второму неоэпитопу в комплексе с HLA белком; где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию.
В некоторых аспектах изобретение относится к композиции, содержащей: первый пептид, содержащий первый неоэпитоп области белка, и второй пептид, содержащий второй неоэпитоп области того же белка, где первый неоэпитоп и второй неоэпитоп содержит по меньшей мере одну аминокислоту области, которая является одинаковой, полинуклеотид, кодирующий первый пептид и второй пептид, или несколько APC, содержащих первый пептид и второй пептид, или первый Т-клеточный рецептор (TCR), специфический к первому неоэпитопу, в комплексе с HLA белком, и второй TCR, специфический к второму неоэпитопу, в комплексе с HLA белком; где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию.
В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми. В некоторых вариантах осуществления, первый пептид и второй пептид являются разными молекулами. В некоторых вариантах осуществления, первый неоэпитоп содержит первый неоэпитоп области того же белка, где второй неоэпитоп содержит второй неоэпитоп области того же белка. В некоторых вариантах осуществления, первый неоэпитоп и второй неоэпитоп содержат по меньшей мере одну аминокислоту области, которая является такой же. В некоторых вариантах осуществления, область белка содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 40, 50, 60,70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 600, 700, 800, 900 или 1000 непрерывных аминокислот белка. В некоторых вариантах осуществления, область белка содержит самое большее 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 40, 50, 60,70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 600, 700, 800, 900 или 1000 непрерывных аминокислот белка. В некоторых вариантах осуществления, первый неоэпитоп связывается с HLA белком I класса с образованием комплекса HLA-пептид I класса. В некоторых вариантах осуществления, второй неоэпитоп связывается с HLA белком II класса с образованием комплекса HLA-пептид II класса. В некоторых вариантах осуществления, второй неоэпитоп связывается с HLA белком I класса с образованием комплекса HLA-пептид I класса. В некоторых вариантах осуществления, первый неоэпитоп связывается с HLA белком II класса с образованием комплекса HLA-пептид II класса. В некоторых вариантах осуществления, первым неоэпитопом является первый неоэпитопный пептид, процессированный из первого пептида, и/или вторым неоэпитопом является второй неоэпитопный пептид, процессированный из второго пептида. В некоторых вариантах осуществления, первый неоэпитоп короче по длине, чем первый пептид и/или второй неоэпитоп короче по длине, чем второй пептид. В некоторых вариантах осуществления, первый неоэпитопный пептид процессирован антигенпрезентирующей клеткой (APC), содержащей первый пептид, и/или второй неоэпитопный пептид процессирован APC, содержащей второй пептид. В некоторых вариантах осуществления, первый неоэпитоп активирует CD8+ Т-клетки. В некоторых вариантах осуществления, второй неоэпитоп активирует CD4+ Т-клетки. В некоторых вариантах осуществления, второй неоэпитоп активирует CD8+ Т-клетки. В некоторых вариантах осуществления, первый неоэпитоп активирует CD4+ Т-клетки. В некоторых вариантах осуществления, TCR CD4+ Т-клетки связывается с комплексом HLA-пептид II класса, содержащим первый или второй пептид. В некоторых вариантах осуществления, TCR CD8+ Т-клетки связывается с комплексом HLA-пептид I класса, содержащим первый или второй пептид. В некоторых вариантах осуществления, TCR CD4+ Т-клетки связывается с комплексом HLA-пептид I класса, содержащим первый или второй пептид. В некоторых вариантах осуществления, TCR CD8+ Т-клетки связывается с комплексом HLA-пептид II класса, содержащим первый или второй пептид. В некоторых вариантах осуществления, одна или более APC содержат первую APC, содержащую первый пептид, и вторую APC, содержащую второй пептид. В некоторых вариантах осуществления, мутация выбрана из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутации «сдвига рамки», мутации сквозного прочитывания, мутации слияния генов и любой их комбинации. В некоторых вариантах осуществления, первый неоэпитоп и второй неоэпитоп содержит последовательность, кодированную геном из таблицы 1 или 2. В некоторых вариантах осуществления, белок кодируется геном из таблицы 1 или 2. В некоторых вариантах осуществления, мутацией является мутация из столбца 2 таблицы 1 или 2. В некоторых вариантах осуществления, белком является GATA3. В некоторых вариантах осуществления, первый неоэпитоп и второй неоэпитоп содержит последовательность, кодированную геном из таблицы 34 или таблицы 36. В некоторых вариантах осуществления, белок кодируется геном из таблицы 34 или таблицы 36. В некоторых вариантах осуществления, мутацией является мутация из столбца 2 таблицы 34 или таблицы 36. В некоторых вариантах осуществления, белком является BTK. В некоторых вариантах осуществления, первый неоэпитоп и второй неоэпитоп содержит последовательность, кодированную геном из таблицы 40A-40D. В некоторых вариантах осуществления, белок кодируется геном из таблицы 3 или 35. В некоторых вариантах осуществления, мутацией является мутация из столбца 2 таблицы 3 или 35. В некоторых вариантах осуществления, белком является EGFR. В некоторых вариантах осуществления, единственный полипептид содержит первый пептид и второй пептид, или единственный полинуклеотид кодирует первый пептид и второй пептид. В некоторых вариантах осуществления, первый пептид и второй пептид кодированы последовательностью, транскрибированной из одного и того же сайта начала транскрипции. В некоторых вариантах осуществления, первый пептид кодируется последовательностью, транскрибированной из первого сайта начала транскрипции, и второй пептид кодируется последовательностью, транскрибированной из второго сайта начала транскрипции. В некоторых вариантах осуществления, один полипептид имеет длину по меньшей мере 18; 19; 20; 21; 22; 23; 24; 25; 26; 27; 28; 29; 30; 40; 50; 60;70; 80; 90; 100; 150; 200; 250; 300; 350; 400; 450; 500; 600; 700; 800; 900; 1000; 1500; 2000; 2500; 3000; 4000; 5000; 7500; или 10000 аминокислот. В некоторых вариантах осуществления, полипептид содержит первую последовательность с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с первой соответствующей последовательностью дикого типа; и вторую последовательность с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей второй последовательностью дикого типа. В некоторых вариантах осуществления, полипептид содержит первую последовательность из по меньшей мере 8 или 9 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с первой соответствующей последовательностью дикого типа; и вторую последовательность из по меньшей мере 16 или 17 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей второй последовательностью дикого типа. В некоторых вариантах осуществления, второй пептид длиннее, чем первый пептид. В некоторых вариантах осуществления, первый пептид длиннее, чем второй пептид. В некоторых вариантах осуществления, первый пептид имеет длину по меньшей мере 9; 10; 11; 12; 13; 14; 15; 16; 17;; 18; 19; 20; 21; 22; 23; 24; 25; 26; 27; 28; 29; 30; 40; 50; 60;70; 80; 90; 100; 150; 200; 250; 300; 350; 400; 450; 500; 600; 700; 800; 900; 1000; 1500; 2000; 2500; 3000; 4000; 5000; 7500; или 10000аминокислот. В некоторых вариантах осуществления, второй пептид имеет длину по меньшей мере 17; 18; 19; 20; 21; 22; 23; 24; 25; 26; 27; 28; 29; 30; 40; 50; 60;70; 80; 90; 100; 150; 200; 250; 300; 350; 400; 450; 500; 600; 700; 800; 900; 1000; 1500; 2000; 2500; 3000; 4000; 5000; 7500; или 10000аминокислот. В некоторых вариантах осуществления, первый пептид содержит последовательность из по меньшей мере 9 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления, второй пептид содержит последовательность из по меньшей мере 17 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления, второй неоэпитоп длиннее, чем первый неоэпитоп. В некоторых вариантах осуществления, первый неоэпитоп имеет длину по меньшей мере 8 аминокислот. В некоторых вариантах осуществления, первый неоэпитоп имеет длину от 8 до 12 аминокислот. В некоторых вариантах осуществления, первый неоэпитоп содержит последовательность из по меньшей мере 8 непрерывных аминокислот, где по меньшей мере 2 из 8 непрерывных аминокислот отличаются в соответствующих положениях последовательности дикого типа. В некоторых вариантах осуществления, второй неоэпитоп имеет длину по меньшей мере 16 аминокислот. В некоторых вариантах осуществления, второй неоэпитоп имеет длину от 16 до 25 аминокислот. В некоторых вариантах осуществления, второй неоэпитоп содержит последовательность из по меньшей мере 16 непрерывных аминокислот, где по меньшей мере 2 из 16 непрерывных аминокислот отличаются в соответствующих положениях последовательности дикого типа.
В некоторых вариантах осуществления, первый пептид содержит по меньшей мере одну дополнительную мутацию. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации не является мутацией в первом неоэпитопе. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации является мутацией в первом неоэпитопе. В некоторых вариантах осуществления, второй пептид содержит по меньшей мере одну дополнительную мутацию. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации не является мутацией во втором неоэпитопе. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации является мутацией во втором неоэпитопе. В некоторых вариантах осуществления, первый пептид, второй пептид или оба содержат по меньшей мере одну фланкирующую последовательность, где по меньшей мере одна фланкирующая последовательность расположены выше или ниже неоэпитопа. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая последовательность имеет по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая последовательность содержит последовательность не дикого типа. В некоторых вариантах осуществления, по меньшей мере одной фланкирующей последовательностью является N-концевая фланкирующая последовательность. В некоторых вариантах осуществления, по меньшей мере одной фланкирующей последовательностью является C-концевая фланкирующая последовательность. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая последовательность первого пептида имеет по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности к, по меньшей мере одной фланкирующей последовательности второго пептида. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая область первого пептида отличается от, по меньшей мере одной фланкирующей области второго пептида. В некоторых вариантах осуществления, по меньшей мере один фланкирующий остаток содержит мутацию. В некоторых вариантах осуществления, первый неоэпитоп, второй неоэпитоп или оба содержат по меньшей мере один якорный остаток. В некоторых вариантах осуществления, по меньшей мере один якорный остаток первого неоэпитопа находится в каноническом якорном положении. В некоторых вариантах осуществления, по меньшей мере один якорный остаток первого неоэпитопа находится в не каноническом якорном положении. В некоторых вариантах осуществления, по меньшей мере один якорный остаток второго неоэпитопа находится в каноническом якорном положении. В некоторых вариантах осуществления, по меньшей мере один якорный остаток второго неоэпитопа находится не в каноническом якорном положении. В некоторых вариантах осуществления, по меньшей мере один якорный остаток первого неоэпитопа отличается от, по меньшей мере одного якорного остатка второго неоэпитопа. В некоторых вариантах осуществления, по меньшей мере один якорный остаток является остатком дикого типа. В некоторых вариантах осуществления, по меньшей мере один якорный остаток является замещением. В некоторых вариантах осуществления, первый неоэпитоп и/или второй неоэпитоп связывается с HLA белком с большей аффинностью, чем соответствующий неоэпитоп без замещения. В некоторых вариантах осуществления, первый неоэпитоп и/или второй неоэпитоп связывается с HLA белком с большей аффинностью, чем соответствующая последовательность дикого типа без замещения. В некоторых вариантах осуществления, по меньшей мере один якорный остаток не содержит мутацию. В некоторых вариантах осуществления, первый неоэпитоп, второй неоэпитоп или оба содержат по меньшей мере одну фланкирующую область якорного остатка. В некоторых вариантах осуществления, неоэпитоп содержит по меньшей мере один якорный остаток. В некоторых вариантах осуществления, по меньшей мере один якорный остаток содержит по меньшей мере два якорных остатка. В некоторых вариантах осуществления, по меньшей мере два якорных остатка разделены областью разделения, содержащей по меньшей мере 1 аминокислоту. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая область якорного остатка не находится в внутри области разделения. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая область якорного остатка находится выше N-концевого якорного остатка, по меньшей мере двух якорных остатков ниже C-концевого якорного остатка из по меньшей мере двух якорных остатков обоих (a) и (b).
В некоторых вариантах осуществления, композиция содержит адъювант. В некоторых вариантах осуществления, композиция содержит один или более дополнительных пептидов, где один или более дополнительных пептидов содержат третий неоэпитоп. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком с большей аффинностью, чем соответствующая последовательность дикого типа. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком I класса с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком II класса с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с белком, кодируемым HLA аллелем, экспрессируемым субъектом. В некоторых вариантах осуществления, мутация не присутствует в не раковых клетках субъекта. В некоторых вариантах осуществления, первый и/или второй неоэпитоп кодируется геном или экспрессированным геном раковых клеток субъекта. В некоторых вариантах осуществления, композиция содержит первую Т-клетку, содержащую первый TCR. В некоторых вариантах осуществления, композиция содержит вторую Т-клетку, содержащую второй TCR. В некоторых вариантах осуществления, первый TCR содержит ненативный внутриклеточный домен и/или второй TCR содержит ненативный внутриклеточный домен. В некоторых вариантах осуществления, первым TCR является растворимый TCR и/или вторым TCR является растворимый TCR. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является цитотоксическая Т-клетка. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является гамма дельта Т-клетка. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является хелперная Т-клетка. В некоторых вариантах осуществления, первой Т-клеткой является Т-клетка, стимулированная, размноженная или индуцированная первым неоэпитопом, и/или второй Т-клеткой является Т-клетка, стимулированная, размноженная или индуцированная вторым неоэпитопом. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является аутологическая Т-клетка. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является аллогенная Т-клетка. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является сконструированная Т-клетка. В некоторых вариантах осуществления, первой и/или второй Т-клеткой является Т-клетка клеточной линии. В некоторых вариантах осуществления, первый и/или второй TCR связывается с комплексом HLA-пептид с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых аспектах, в настоящем изобретении представлен вектор, содержащий полинуклеотид, кодирующий первый и второй пептид, описанный в настоящем изобретении. В некоторых вариантах осуществления, полинуклеотид функционально связан с промотором. В некоторых вариантах осуществления, вектором является самоамплифицирующийся РНК репликон, плазмида, фаг, транспозон, космида, вирус или вирион. В некоторых вариантах осуществления, вектором является вирусный вектор. В некоторых вариантах осуществления, вектор получен из ретровируса, лентивируса, аденовируса, аденоассоциированного вируса, вируса герпеса, вируса оспы, альфа-вируса, вируса коровьей оспы, вируса гепатита В, вируса папилломы человека или их псевдотипа. В некоторых вариантах осуществления, вектором является не вирусный вектором. В некоторых вариантах осуществления, не вирусным вектором является наночастица, катионный липид, катионный полимер, металлический нанополимер, наностержень, липосома, мицелла, микропузырьки, проникающий в клетки пептид или липосфера.
В некоторых аспектах изобретение относится к фармацевтической композиции, содержащей: композицию, описанную в настоящем изобретении, или вектор, описанный в настоящем изобретении; и фармацевтически приемлемый эксципиент.
В некоторых вариантах осуществления, множеством клеток являются аутологические клетки. В некоторых вариантах осуществления, множеством APC клеток являются аутологические клетки. В некоторых вариантах осуществления, множеством Т-клеток являются аутологические клетки. В некоторых вариантах осуществления, фармацевтическая композиция дополнительно содержит иммуномодулирующий агент или адъювант. В некоторых вариантах осуществления, иммуномодулирующим агентом является цитокин. В некоторых вариантах осуществления, адъювантом является полиICLC. В некоторых вариантах осуществления, адъювантом является Хилтонол.
В некоторых аспектах изобретение относится к способу лечения рака, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, описанной в настоящем изобретении.
В некоторых аспектах изобретение относится к способу профилактики резистентности к противораковой терапии, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, описанной в настоящем изобретении.
В некоторых аспектах изобретение относится к способу вызова иммунного ответа, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции, описанной в настоящем изобретении.
В некоторых вариантах осуществления, иммунным ответом является гуморальный ответ. В некоторых вариантах осуществления, первый пептид и второй пептид вводят одновременно, отдельно или последовательно. В некоторых вариантах осуществления, первый пептид вводят последовательно после второго пептида. В некоторых вариантах осуществления, второй пептид вводят последовательно после первого пептида. В некоторых вариантах осуществления, первый пептид вводят последовательно после периода времени, достаточного для активации Т-клеток вторым пептидом. В некоторых вариантах осуществления, второй пептид вводят последовательно после периода времени, достаточного для активации Т-клеток первым пептидом. В некоторых вариантах осуществления, первый пептид последовательно вводят после второго пептида для рестимуляции Т-клеток. В некоторых вариантах осуществления, второй пептид последовательно вводят после первого пептида для рестимуляции Т-клеток. В некоторых вариантах осуществления, первый пептид вводят для стимуляции Т-клеток и второй пептид вводят после первого пептида для рестимуляции Т-клеток. В некоторых вариантах осуществления, второй пептид вводят для стимуляции Т-клеток и первый пептид вводят после второго пептида для рестимуляции Т-клеток.
В некоторых вариантах осуществления, субъект имеет рак, где рак выбран из группы, состоящей из меланомы, рака яичников, рака легких, рака предстательной железы, рака молочной железы, колоректального рака, эндометриального рака и хронического лимфоцитарного лейкоза (ХЛЛ). В некоторых вариантах осуществления, раком является рак молочной железы, устойчивый к антиэстрогеновой терапии, рак молочной железы MSI, метастатический рак молочной железы, Her2 отрицательный рак молочной железы, Her2 положительный рак молочной железы, ER отрицательный рак молочной железы, ER положительный рак молочной железы, PR положительный рак молочной железы, PR отрицательный рак молочной железы или любая их комбинация. В некоторых вариантах осуществления, рак молочной железы экспрессирует рецептор эстрогена с мутацией. В некоторых вариантах осуществления, субъект имеет рак молочной железы, устойчивый к антиэстрогенной терапии. В некоторых вариантах осуществления, рак молочной железы экспрессирует рецептор эстрогена с мутацией. В некоторых вариантах осуществления, субъект имеет ХЛЛ, устойчивый к терапии ибрутинибом. В некоторых вариантах осуществления, ХЛЛ экспрессирует тирозинкиназу Брутона с мутацией, такой как C481S мутация. В некоторых вариантах осуществления, субъект имеет рак легких, устойчивый к тирозин ингибитору тирозинкиназы. В некоторых вариантах осуществления, рак легких экспрессирует рецептор эпидермального фактора роста (EGFR) с мутацией, такой как T790M мутация. В некоторых вариантах осуществления, множество APC клеток, содержащих первый пептид, и множество APC клеток, содержащих второй пептид, вводят одновременно, отдельно или последовательно. В некоторых вариантах осуществления, множество Т-клеток, содержащих первый TCR, и множество Т-клеток, содержащих второй TCR вводят одновременно, отдельно или последовательно. В некоторых вариантах осуществления, способ дополнительно включает введение по меньшей мере одного дополнительного терапевтического агента или способа воздействия. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом или способом воздействия является хирургическое вмешательство, ингибитор контрольной точки, антитело или его фрагмент, химиотерапевтический агент, облучение, вакцина, малая молекула, Т-клетка, вектор и APC, полинуклеотид, онколитический вирус или любая их комбинация. В некоторых вариантах осуществления, по меньшей мере одним дополнительным терапевтическим агентом является анти-PD-1 агент и анти-PD-L1 агент, анти-CTLA-4 агент или анти-CD40 агент. В некоторых вариантах осуществления, дополнительный терапевтический агент вводят до, одновременно или после введения фармацевтической композиции, описанной в настоящем изобретении.
Пептиды
В некоторых аспектах настоящее описание относится к выделенным пептидам, которые содержат опухолеспецифическую мутацию из таблицы 1 или 2. В некоторых аспектах настоящее описание относится к выделенным пептидам, которые содержат опухолеспецифическую мутацию из таблицы 34. В некоторых аспектах настоящее описание относится к выделенным пептидам, которые содержат опухолеспецифическую мутацию из таблицы 40A-40D. Эти пептиды и полипептиды называют здесь “неоантигенные пептиды” или “неоантигенные полипептиды”. “Полипептид”, “пептид” и их грамматические эквиваленты в настоящем изобретении относятся к полимеру аминокислотных остатков, обычно L-аминокислот, соединенных друг с другом, обычно, пептидными связями между α-амино и карбоксильными группами соседних аминокислот. Полипептиды и пептиды включают, но не ограничены ими, “мутантные пептиды”, “пептиды неоантигена” и “неоантигенные пептиды”. Полипептиды или пептиды могут иметь разную длину, быть в их нейтральных (не заряженных) формах или формах, которые являются солями, и либо не содержать модификации, такие как гликозилирование, окисление боковых цепей или фосфорилирование, либо содержать эти модификации, при условии, что модификация не разрушает биологическую активность полипептидов, как описано здесь. Пептид или полипептид может содержать по меньшей мере одну фланкирующую последовательность. Термин “фланкирующая последовательность” в настоящем изобретении относится к фрагменту или области пептида, которая не является частью эпитопа.
Таблица 1. Список GATA3 neoORF пептидов
В таблице 2 ниже перечислены типовые выбранные пептиды
N334fs
CQWGPCLQCL (A02.01) (SEQ ID NO: 1562)
QWGPCLQCL (A24.02) (SEQ ID NO: 1563)
QWGPCLQCLW (A24.02) (SEQ ID NO: 1564)
S408fs
S408fs
S430fs
H434fs
H435fs
ALQPLQPHA (A02.01) (SEQ ID NO: 1566)
DLHFCRSSIM (B08.01) (SEQ ID NO: 1567)
EPHLALQPL (B07.02, B08.01) (SEQ ID NO: 1568)
ESKIMFATL (B08.01) (SEQ ID NO: 1569)
FATLQRSSL (B07.02, B08.01) (SEQ ID NO: 1570)
FLKAESKIM (B08.01) (SEQ ID NO: 1571)
FLKAESKIMF (B08.01) (SEQ ID NO: 1572)
GPPARVPAV (B07.02) (SEQ ID NO: 1573)
IMKPKRDGYM (B08.01) (SEQ ID NO: 1574)
KIMFATLQR (A03.01) (SEQ ID NO: 1575)
KPKRDGYMF (B07.02) (SEQ ID NO: 1576)
KPKRDGYMFL (B07.02) (SEQ ID NO: 1577)
LHFCRSSIM (B08.01) (SEQ ID NO: 1578)
LQHGHRHGL (B08.01) (SEQ ID NO: 1579)
MFATLQRSSL (B07.02, B08.01) (SEQ ID NO: 1580)
MFLKAESKI (A24.02) (SEQ ID NO: 1581)
MLTGPPARV (A02.01) (SEQ ID NO: 1582)
QPVLWTTPPL (B07.02) (SEQ ID NO: 1583)
SMLTGPPARV (A02.01) (SEQ ID NO: 1584)
TLQRSSLWCL (A02.01) (SEQ ID NO: 1585)
VLPEPHLAL (A02.01) (SEQ ID NO: 1586)
VPAVPFDLHF (B07.02) (SEQ ID NO: 1587)
YMFLKAESK (A03.01) (SEQ ID NO: 1588)
YMFLKAESKI (A02.01, A03.01, A24.02, B08.01) (SEQ ID NO: 1589)
1 Подчеркнутые AA представляют ненативные AA
Таблица 3
WLHKRGKYI (A02.01, B07.02, B08.01) (SEQ ID NO: 1633)
WLHKRGKYIK (A03.01) (SEQ ID NO: 1634)
GVSAPKPLSK (A03.01) (SEQ ID NO: 1636)
VSAPKPLSK (A03.01) (SEQ ID NO: 1637)
KLSDSRTALK (A03.01) (SEQ ID NO: 1640)
LSDSRTALK (A01.01, A03.01) (SEQ ID NO: 1641)
RTALKSGYGK (A03.01) (SEQ ID NO: 1642)
TALKSGYGK (A03.01) (SEQ ID NO: 1643)
ALSASNSCFI (A02.01) (SEQ ID NO: 1645)
FQNGKMALSA (A02.01, B08.01) (SEQ ID NO: 1646)
(Резистентность)
LVVVGACGV (A02.01) (SEQ ID NO: 1650)
VVGACGVGK (A03.01, A11.01) (SEQ ID NO: 1651)
VVVGACGVGK (A03.01) (SEQ ID NO: 1652)
VVVGADGVGK (A11.01) (SEQ ID NO: 1654)
KLVVVGADGV (A02.01) (SEQ ID NO: 1655)
LVVVGADGV (A02.01) (SEQ ID NO: 1656)
LVVVGAVGV (A02.01) (SEQ ID NO: 1658)
VVGAVGVGK (A03.01, A11.01) (SEQ ID NO: 1659)
VVVGAVGVGK (A03.01, A11.01) (SEQ ID NO: 1660)
LLDILDTAGL (A02.01) (SEQ ID NO: 1663)
CLLISYTTNAFSGEYIP
TVFDNYSANVMVDGKPV
NLGLWDTAGQEDYDRLR
PLSYPQTVGET
(SEQ ID NO: 1606)
TTNAFSGEY (A01.01) (SEQ ID NO: 1669)
YTTNAFSGEY (A01.01) (SEQ ID NO: 1670)
GSMNRRPIL (B08.01) (SEQ ID NO: 1675)
MGSMNRRPI (B08.01) (SEQ ID NO: 1676)
MGSMNRRPIL (B08.01) (SEQ ID NO: 1677)
SMNRRPILTI (A02.01, A24.02, B08.01) (SEQ ID NO: 1678)
GMNQRPILTI (A02.01, B08.01) (SEQ ID NO: 1680)
NQRPILTII (A02.01, B08.01) (SEQ ID NO: 1681)
GMNWRPILTI (A02.01, B08.01) (SEQ ID NO: 1683)
MNWRPILTI (A02.01, A24.02, B08.01) (SEQ ID NO: 1684)
MNWRPILTII (A02.01, A24.02) (SEQ ID NO: 1685)
VVVPCEPPEV (A02.01) (SEQ ID NO: 1689)
LLPEDTPPL (A02.01) (SEQ ID NO: 1691)
CLADVLLSV (A02.01) (SEQ ID NO: 1693)
FLQERNLPPK (A03.01) (SEQ ID NO: 1694)
HLIVLRVVRL (A02.01, B08.01) (SEQ ID NO: 1695)
HPKVHLNTM (B07.02, B08.01) (SEQ ID NO: 1696)
HPKVHLNTMF (B07.02, B08.01) (SEQ ID NO: 1697)
KVHLNTMFR (A03.01) (SEQ ID NO: 1698)
KVHLNTMFRR (A03.01) (SEQ ID NO: 1699)
LPAPFRVNHA (B07.02) (SEQ ID NO: 1700)
MFRRPHSCL (B07.02, B08.01) (SEQ ID NO: 1701)
MFRRPHSCLA (B08.01) (SEQ ID NO: 1702)
NTMFRRPHSC (B08.01) (SEQ ID NO: 1703)
RPHSCLADV (B07.02) (SEQ ID NO: 1704)
RPHSCLADVL (B07.02) (SEQ ID NO: 1705)
RVVRLPAPFR (A03.01) (SEQ ID NO: 1706)
SVHLIVLRV (A02.01) (SEQ ID NO: 1707)
TMFRRPHSC (B08.01) (SEQ ID NO: 1708)
TMFRRPHSCL (A02.01, B08.01) (SEQ ID NO: 1709)
VLLSVHLIV (A02.01) (SEQ ID NO: 1710)
VLLSVHLIVL (A02.01) (SEQ ID NO: 1711)
VLRVVRLPA (B08.01) (SEQ ID NO: 1712)
VVRLPAPFR (A03.01) (SEQ ID NO: 1713)
APLLAAPSPA (B07.02) (SEQ ID NO: 1715)
APRTNFHSS (B07.02) (SEQ ID NO: 1716)
APRTNFHSSL (B07.02, B08.01) (SEQ ID NO: 1717)
CPQPSPSLPA (B07.02) (SEQ ID NO: 1718)
GQWMAHMAL (A02.01) (SEQ ID NO: 1719)
GQWMAHMALL (A02.01) (SEQ ID NO: 1720)
HMALLPSGTK (A03.01) (SEQ ID NO: 1721)
HTALGRGSL (B07.02) (SEQ ID NO: 1722)
IPMAISSPP (B07.02) (SEQ ID NO: 1723)
IPMAISSPPK (B07.02) (SEQ ID NO: 1724)
KLPSLPLSK (A03.01) (SEQ ID NO: 1725)
KLPSLPLSKM (A02.01) (SEQ ID NO: 1726)
KMYTTSMAM (A02.01, A03.01) (SEQ ID NO: 1727)
LLAAPSPASR (A03.01) (SEQ ID NO: 1728)
LLLSADQQAA (A02.01) (SEQ ID NO: 1729)
LLSADQQAA (A02.01) (SEQ ID NO: 1730)
LPASNKLPS (B07.02) (SEQ ID NO: 1731)
LPASNKLPSL (B07.02, B08.01) (SEQ ID NO: 1732)
LPLPQLLLSA (B07.02) (SEQ ID NO: 1733)
LPSLPLSKM (B07.02) (SEQ ID NO: 1734)
LSKMYTTSM (B08.01) (SEQ ID NO: 1735)
MALLPSGTK (A03.01) (SEQ ID NO: 1736)
MPILPLPQL (B07.02) (SEQ ID NO: 1737)
MPILPLPQLL (B07.02) (SEQ ID NO: 1738)
MYTTSMAMPI (A24.02) (SEQ ID NO: 1739)
PMAISSPPK (A03.01) (SEQ ID NO: 1740)
QWMAHMALL (A24.02) (SEQ ID NO: 1741)
SKMYTTSMAM (B07.02) (SEQ ID NO: 1742)
SMAMPILPL (A02.01, B07.02, B08.01) (SEQ ID NO: 1743)
SNKLPSLPL (B08.01) (SEQ ID NO: 1744)
SPASRLQCI (B07.02, B08.01) (SEQ ID NO: 1745)
SPPKAPLLAA (B07.02) (SEQ ID NO: 1746)
SPSLPASNKL (B07.02) (SEQ ID NO: 1747)
YTTSMAMPI (A02.01) (SEQ ID NO: 1748)
YTTSMAMPIL (A02.01) (SEQ ID NO: 1749)
GLTHPAHQPL (A02.01) (SEQ ID NO: 1751)
HPAHQPLGSM (B07.02) (SEQ ID NO: 1752)
LTHPAHQPL (B07.02) (SEQ ID NO: 1753)
RPTSRARQSC (B07.02) (SEQ ID NO: 1754)
RQSCCLPGL (A02.01) (SEQ ID NO: 1755)
TSRARQSCCL (B08.01) (SEQ ID NO: 1756)
EWKVKFPEL (B08.01) (SEQ ID NO: 1758)
KFPELLCVW (A24.02) (SEQ ID NO: 1759)
LLCVWVSSI (A02.01) (SEQ ID NO: 1760)
LLTSSSREWK (A03.01) (SEQ ID NO: 1761)
LTSSSREWK (A03.01) (SEQ ID NO: 1762)
YPAYSKDSGL (B07.02) (SEQ ID NO: 1763)
N334fs
CQWGPCLQCL (A02.01) (SEQ ID NO: 1765)
QWGPCLQCL (A24.02) (SEQ ID NO: 1766)
QWGPCLQCLW (A24.02) (SEQ ID NO: 1767)
S408fs
S408fs
S430fs
H434fs
H435fs
ALQPLQPHA (A02.01) (SEQ ID NO: 1769)
DLHFCRSSIM (B08.01) (SEQ ID NO: 1770)
EPHLALQPL (B07.02, B08.01) (SEQ ID NO: 1771)
ESKIMFATL (B08.01) (SEQ ID NO: 1772)
FATLQRSSL (B07.02, B08.01) (SEQ ID NO: 1773)
FLKAESKIM (B08.01) (SEQ ID NO: 1774)
FLKAESKIMF (B08.01) (SEQ ID NO: 1775)
GPPARVPAV (B07.02) (SEQ ID NO: 1776)
IMKPKRDGYM (B08.01) (SEQ ID NO: 1777)
KIMFATLQR (A03.01) (SEQ ID NO: 1778)
KPKRDGYMF (B07.02) (SEQ ID NO: 1779)
KPKRDGYMFL (B07.02) (SEQ ID NO: 1780)
LHFCRSSIM (B08.01) (SEQ ID NO: 1781)
LQHGHRHGL (B08.01) (SEQ ID NO: 1782)
MFATLQRSSL (B07.02, B08.01) (SEQ ID NO: 1783)
MFLKAESKI (A24.02) (SEQ ID NO: 1784)
MLTGPPARV (A02.01) (SEQ ID NO: 1785)
QPVLWTTPPL (B07.02) (SEQ ID NO: 1786)
SMLTGPPARV (A02.01) (SEQ ID NO: 1787)
TLQRSSLWCL (A02.01) (SEQ ID NO: 1788)
VLPEPHLAL (A02.01) (SEQ ID NO: 1789)
VPAVPFDLHF (B07.02) (SEQ ID NO: 1790)
YMFLKAESK (A03.01) (SEQ ID NO: 1791)
YMFLKAESKI (A02.01, A03.01, A24.02, B08.01) (SEQ ID NO: 1792)
L656fs
CLRSHTCPPR (A03.01) (SEQ ID NO: 1794)
CLWCHACLHR (A03.01) (SEQ ID NO: 1795)
CPHLGSHPC (B07.02) (SEQ ID NO: 1796)
CPLGLKSPL (B07.02) (SEQ ID NO: 1797)
CPRSCRCPH (B07.02) (SEQ ID NO: 1798)
CPRSCRCPHL (B07.02, B08.01) (SEQ ID NO: 1799)
CSLPLGNHPY (A01.01) (SEQ ID NO: 1800)
GLRNRICPL (A02.01, B07.02, B08.01) (SEQ ID NO: 1801)
GLRSHTYLR (A03.01) (SEQ ID NO: 1802)
GLRSHTYLRR (A03.01) (SEQ ID NO: 1803)
GPRGRTCHPG (B07.02) (SEQ ID NO: 1804)
HLGSHPCRL (B08.01) (SEQ ID NO: 1805)
HLRLHASPH (A03.01) (SEQ ID NO: 1806)
HLRSCPCSL (B07.02, B08.01) (SEQ ID NO: 1807)
HLRTHLLPH (A03.01) (SEQ ID NO: 1808)
HLRTHLLPHH (A03.01) (SEQ ID NO: 1809)
HLRYRAYPP (B08.01) (SEQ ID NO: 1810)
HLRYRAYPPC (B08.01) (SEQ ID NO: 1811)
HPHHLRTHL (B07.02) (SEQ ID NO: 1812)
HPHHLRTHLL (B07.02, B08.01) (SEQ ID NO: 1813)
HTYLRRLRSH (A03.01) (SEQ ID NO: 1814)
LPCPHRLRSL (B07.02, B08.01) (SEQ ID NO: 1815)
LPHHRRTRSC (B07.02, B08.01) (SEQ ID NO: 1816)
LPLGNHPYL (B07.02) (SEQ ID NO: 1817)
LPRPLHLRL (B07.02, B08.01) (SEQ ID NO: 1818)
NLRNHTCPP (B08.01) (SEQ ID NO: 1819)
PPRLRSRTCL (B07.02, B08.01) (SEQ ID NO: 1820)
RLHASPHHL (A02.01) (SEQ ID NO: 1821)
RLHASPHHLR (A03.01) (SEQ ID NO: 1822)
RLRDHICPL (A02.01, B07.02, B08.01) (SEQ ID NO: 1823)
RLRNLPCPH (A03.01) (SEQ ID NO: 1824)
RLRNLPCPHR (A03.01) (SEQ ID NO: 1825)
RLRSHTCPP (B08.01) (SEQ ID NO: 1826)
RLRSLPRPL (B07.02, B08.01) (SEQ ID NO: 1827)
RLRSLPRPLH (A03.01) (SEQ ID NO: 1828)
RLRSRTCLL (B07.02, B08.01) (SEQ ID NO: 1829)
RNRICPLSL (B07.02, B08.01) (SEQ ID NO: 1830)
RPLHLRLHA (B07.02) (SEQ ID NO: 1831)
RPLHLRLHAS (B07.02) (SEQ ID NO: 1832)
RSHACPPGLR (A03.01) (SEQ ID NO: 1833)
RSHACPPNLR (A03.01) (SEQ ID NO: 1834)
RSHAYALCLR (A03.01) (SEQ ID NO: 1835)
RSHPCCHYLR (A03.01) (SEQ ID NO: 1836)
RSHPCPLGLK (A03.01) (SEQ ID NO: 1837)
RSHTCPPSLR (A03.01) (SEQ ID NO: 1838)
RSLPRPLHLR (A03.01) (SEQ ID NO: 1839)
RSRTCLLCL (B07.02) (SEQ ID NO: 1840)
RSRTCLLCLR (A03.01) (SEQ ID NO: 1841)
RSRTCPPGL (B07.02) (SEQ ID NO: 1842)
RSRTCPPGLR (A03.01) (SEQ ID NO: 1843)
RTHLLPHHRR (A03.01) (SEQ ID NO: 1844)
RTRSCPCRWR (A03.01) (SEQ ID NO: 1845)
RYRAYPPCL (A24.02) (SEQ ID NO: 1846)
RYRAYPPCLW (A24.02) (SEQ ID NO: 1847)
SLGNHLCPL (A02.01, B07.02, B08.01) (SEQ ID NO: 1848)
SLPLGNHPYL (A02.01) (SEQ ID NO: 1849)
SLPRPLHLRL (A02.01) (SEQ ID NO: 1850)
SLRNCTCPPR (A03.01) (SEQ ID NO: 1851)
SLRSHAYAL (A02.01, B07.02, B08.01) (SEQ ID NO: 1852)
SLRSHPCPL (A02.01, B07.02, B08.01) (SEQ ID NO: 1853)
SPHHLRTPP (B07.02) (SEQ ID NO: 1854)
SPHHLRTPPH (B07.02) (SEQ ID NO: 1855)
SPLRSQANAL (B07.02, B08.01) (SEQ ID NO: 1856)
YLRRLRSHTC (B08.01) (SEQ ID NO: 1857)
YLRSRNSAP (B08.01) (SEQ ID NO: 1858)
YLRSRNSAPG (B08.01) (SEQ ID NO: 1859)
ALAPTLTHML (A02.01) (SEQ ID NO: 1861)
LLQVTQTSFA (A02.01) (SEQ ID NO: 1862)
LQVTQTSFAL (A02.01) (SEQ ID NO: 1863)
RLWHLLLQV (A02.01) (SEQ ID NO: 1864)
RLWHLLLQVT (A02.01) (SEQ ID NO: 1865)
FFPITPPVW (A24.02) (SEQ ID NO: 1867)
FPITPPVWHI (B07.02) (SEQ ID NO: 1868)
GPRMQLCTQL (B07.02, B08.01) (SEQ ID NO: 1869)
ITPPVWHIL (A24.02) (SEQ ID NO: 1870)
LALGPRMQL (B07.02) (SEQ ID NO: 1871)
MQLCTQLARF (A24.02) (SEQ ID NO: 1872)
RFFPITPPV (A02.01, A24.02) (SEQ ID NO: 1873)
RFFPITPPVW (A24.02) (SEQ ID NO: 1874)
RMQLCTQLA (A02.01) (SEQ ID NO: 1875)
RMQLCTQLAR (A03.01) (SEQ ID NO: 1876)
SPPLALGPRM (B07.02) (SEQ ID NO: 1877)
TQLARFFPI (A02.01, A24.02, B08.01) (SEQ ID NO: 1878)
ALKKLRSPL (B08.01, B07.02) (SEQ ID NO: 1880)
HLQLKSCRRK (A03.01) (SEQ ID NO: 1881)
KISNWSLKK (A03.01, A11.01) (SEQ ID NO: 1882)
KISNWSLKKV (A03.01) (SEQ ID NO: 1883)
KLRSPLWIF (A24.02) (SEQ ID NO: 1884)
KSRQNHLQLK (A03.01) (SEQ ID NO: 1885)
NWSLKKVPAL (B08.01) (SEQ ID NO: 1886)
SLKKVPALK (A03.01, A11.01) (SEQ ID NO: 1887)
SLKKVPALKK (A03.01) (SEQ ID NO: 1888)
SQKSRQNHL (B08.01) (SEQ ID NO: 1889)
WSLKKVPAL (B08.01) (SEQ ID NO: 1890)
WSLKKVPALK (A03.01) (SEQ ID NO: 1891)
P72fs
G108fs
R110fs
KPTRAATVSV (B07.02) (SEQ ID NO: 1893)
LPPWPLHQQL (B07.02) (SEQ ID NO: 1894)
LPRKPTRAA (B07.02, B08.01) (SEQ ID NO: 1895)
LPRKPTRAAT (B07.02) (SEQ ID NO: 1896)
QQLLHRRPL (B08.01) (SEQ ID NO: 1897)
RLLPPWPLH (A03.01) (SEQ ID NO: 1898)
APWPSTSSH (B07.02) (SEQ ID NO: 1900)
RPAPASAPW (B07.02) (SEQ ID NO: 1901)
WPSTSSHST (B07.02) (SEQ ID NO: 1902)
PTKMSYAANLKNVMNMQNRQ
KKKGKNSPCCQKKLRVQ
NQGHLLMILLHN* (SEQ ID NO: 1629)
G123fs
FWLTKLNYL (A24.02, B08.01) (SEQ ID NO: 1905)
HLSMLTDSL (A02.01) (SEQ ID NO: 1906)
HTMGFWLTK (A03.01) (SEQ ID NO: 1907)
HTMGFWLTKL (A02.01) (SEQ ID NO: 1908)
KLNYLCHLSM (A02.01) (SEQ ID NO: 1909)
LPISHCQCI (B07.02, B08.01) (SEQ ID NO: 1910)
LPISHCQCIL (B07.02, B08.01) (SEQ ID NO: 1911)
LTDSLFLPI (A01.01, A02.01) (SEQ ID NO: 1912)
LTKLNYLCHL (B08.01) (SEQ ID NO: 1913)
MLTDSLFLPI (A01.01, A02.01, B08.01) (SEQ ID NO: 1914)
MQGHTMGFWL (A02.01) (SEQ ID NO: 1915)
NYLCHLSML (A24.02) (SEQ ID NO: 1916)
SMLTDSLFL (A02.01) (SEQ ID NO: 1917)
TMGFWLTKL (A02.01) (SEQ ID NO: 1918)
YLCHLSMLT (A02.01) (SEQ ID NO: 1919)
VMAYVMAGV (A02.01) (SEQ ID NO: 1921)
YVMAYVMAG (A02.01, B07.02, B08.01) (SEQ ID NO: 1922)
YVMAYVMAGV (A02.01, B07.02, B08.01) (SEQ ID NO: 1923)
1Подчеркнутые AA представляют ненативные AA
2Выделенные жирным AA представляют нативные AA аминокислотной последовательности, кодированной вторым из двух слитых генов
3Выделенные жирным и подчеркнутые AA представляют ненативные AA аминокислотной последовательности, кодированной вторым из двух конденсированных генов из-за сдвига рамки.
Самой частой мутацией ибрутиниба, молекулы, направленной на тирозинкиназу Брутона (BTK) и применяемой для ХЛЛ и определенных лимфом, является замена цистеина на серин в положении 481 (C481S). Это изменение дает множество пептидов, которые связываются для ранжирования HLA молекул. Мутация содержится в области, имеющей аминокислотную последовательность: IFIITEYMANGSLLNYLREMRHR (SEQ ID NO: 1924), мутированный серин подчеркнут.
Типовые неоантигенные пептиды, соответствующие C481S мутации, представлены в таблице 34. В таблице также представлен список HLA аллелей, кодированных белковыми продуктами, которые могут связываться с пептидами. В некоторых вариантах осуществления, описание представляет C481S неоэпитопы для противораковой терапии, такие как ANGSLLNY (SEQ ID NO: 1925); ANGSLLNYL (SEQ ID NO: 1926); ANGSLLNYLR (SEQ ID NO: 1927); EYMANGSL (SEQ ID NO: 1928); EYMANGSLLN (SEQ ID NO: 1929); EYMANGSLLNY (SEQ ID NO: 1930); GSLLNYLR (SEQ ID NO: 1931); GSLLNYLREM (SEQ ID NO: 1932); ITEYMANGS (SEQ ID NO: 1933); ITEYMANGSL (SEQ ID NO: 1934); ITEYMANGSLL (SEQ ID NO: 1935); MANGSLLNYL (SEQ ID NO: 1936); MANGSLLNYLR (SEQ ID NO: 1937); NGSLLNYL (SEQ ID NO: 1938); NGSLLNYL (SEQ ID NO: 1939); SLLNYLREMR (SEQ ID NO: 1940); TEYMANGSLL (SEQ ID NO: 1941); TEYMANGSLLNY (SEQ ID NO: 1942); YMANGSLL (SEQ ID NO: 1943); и YMANGSLLN (SEQ ID NO: 1944). В таблицах 35 и 3 представлены типовые кандидатные неоантигены, соответствующие другим опухолеассоциированным генным мутациям. В таблице 36 представлен список выбранных HLA-ограниченных BTK пептидов для целей этой заявки и соответствующего белка, кодированного HLA аллелем, с которым связывается BTK пептид или предположительно связывается. В таблице 37 представлен список выбранных BTK пептидов и соответствующий предпочтительный белок, кодируемый HLA аллелем, с которым связывается BTK пептид или предположительно связывается, применяемых в контексте этой заявки.
В таблице 34 ниже перечислены типовые неоантигенные пептиды, соответствующие C481S мутации
В таблице 35 представлены типовые кандидатные неоантигены, соответствующие другим рак-ассоциированным генным мутациям
GQYGKVYEGV (A02.01) (SEQ ID NO: 2106)
KLGGGQYGK (A03.01) (SEQ ID NO: 2107)
KLGGGQYGKV (A02.01) (SEQ ID NO: 2108)
KVYEGVWKK (A02.01, A03.01) (SEQ ID NO: 2109)
KVYEGVWKKY (A03.01) (SEQ ID NO: 2110)
QYGKVYEGV (A24.02) (SEQ ID NO: 2111)
QYGKVYEGVW (A24.02) (SEQ ID NO: 2112)
GQYGVVYEGV (A02.01) (SEQ ID NO: 2114)
KLGGGQYGV (A02.01) (SEQ ID NO: 2115)
KLGGGQYGVV (A02.01) (SEQ ID NO: 2116)
QYGVVYEGV (A24.02) (SEQ ID NO: 2117)
QYGVVYEGVW (A24.02) (SEQ ID NO: 2118)
VVYEGVWKK (A02.01, A03.01) (SEQ ID NO: 2119)
VVYEGVWKKY (A03.01) (SEQ ID NO: 2120)
ISSATEYLEK (A03.01) (SEQ ID NO: 2122)
SSATEYLEK (A03.01) (SEQ ID NO: 2123)
TQISSATEYL (A02.01) (SEQ ID NO: 2124)
YMATQISSAT (A02.01) (SEQ ID NO: 2125)
IIEFMTYGNL (A02.01) (SEQ ID NO: 2127)
IIIEFMTYG (A02.01) (SEQ ID NO: 2128)
IIIEFMTYGN (A02.01) (SEQ ID NO: 2129)
YIIIEFMTYG (A02.01) (SEQ ID NO: 2130)
KLGGGQHGEV (A02.01) (SEQ ID NO: 2132)
RVAKIADFGM (A02.01, B07.02) (SEQ ID NO: 2134)
ILMELMAGG (A02.01) (SEQ ID NO: 2136)
ILMELMAGGD (A02.01) (SEQ ID NO: 2137)
LMELMAGGDL (A02.01) (SEQ ID NO: 2138)
LPRFILMEL (B07.02, B08.01) (SEQ ID NO: 2139)
LPRFILMELM (B07.02) (SEQ ID NO: 2140)
LQSLPRFILM (A02.01, B08.01) (SEQ ID NO: 2141)
SLPRFILMEL (A02.01, A24.02, B07.02, B08.01) (SEQ ID NO: 2142)
LATEKSRWSG (A02.01, B08.01) (SEQ ID NO: 2144)
LYGLLLEML (A24.02) (SEQ ID NO: 2148)
NVVPLYGLL (A02.01) (SEQ ID NO: 2149)
PLYGLLLEM (A02.01) (SEQ ID NO: 2150)
PLYGLLLEML (A02.01, A24.02) (SEQ ID NO: 2151)
VPLYGLLLEM (B07.02) (SEQ ID NO: 2152)
VVPLYGLLL (A02.01, A24.02) (SEQ ID NO: 2153)
GVYTFLPST (A02.01) (SEQ ID NO: 2155)
GVYTFLPSTL (A02.01, A24.02) (SEQ ID NO: 2156)
TFLPSTLKSL (A24.02) (SEQ ID NO: 2157)
VYTFLPSTL (A24.02) (SEQ ID NO: 2158)
YTFLPSTLK (A03.01) (SEQ ID NO: 2159)
NVVPLCDLLL (A02.01) (SEQ ID NO: 2161)
PLCDLLLEM (A02.01) (SEQ ID NO: 2162)
PLCDLLLEML (A02.01) (SEQ ID NO: 2163)
VPLCDLLLEM (B07.02) (SEQ ID NO: 2164)
VVPLCDLLL (A02.01, A24.02) (SEQ ID NO: 2165)
NVVPLNDLLL (A02.01) (SEQ ID NO: 2167)
PLNDLLLEM (A02.01) (SEQ ID NO: 2168)
PLNDLLLEML (A02.01) (SEQ ID NO: 2169)
VPLNDLLLEM (B07.02) (SEQ ID NO: 2170)
NVVPLSDLLL (A02.01) (SEQ ID NO: 2172)
PLSDLLLEM (A02.01) (SEQ ID NO: 2173)
PLSDLLLEML (A02.01) (SEQ ID NO: 2174)
VPLSDLLLEM (B07.02) (SEQ ID NO: 2175)
VVPLSDLLL (A02.01, A24.02) (SEQ ID NO: 2176)
YTLDVLERC (A02.01) (SEQ ID NO: 2178)
(Резистентность)
TIGGPTLVII (A02.01) (SEQ ID NO: 2186)
VIIEYCCYG (A02.01) (SEQ ID NO: 2187)
IANLLGACTI (A02.01) (SEQ ID NO: 2189)
MNIANLLGA (A02.01) (SEQ ID NO: 2190)
YLGNHMNIA (A02.01, B08.01) (SEQ ID NO: 2191)
YLGNHMNIAN (A02.01) (SEQ ID NO: 2192)
VLHESNSPYI (A02.01) (SEQ ID NO: 2194)
LYIVGFYGAF (A24.02) (SEQ ID NO: 2196)
NSLYIVGFY (A01.01) (SEQ ID NO: 2197)
QVLHECNSL (A02.01, B08.01) (SEQ ID NO: 2198)
SLYIVGFYG (A02.01) (SEQ ID NO: 2199)
SLYIVGFYGA (A02.01) (SEQ ID NO: 2200)
VLHECNSLY (A03.01) (SEQ ID NO: 2201)
VLHECNSLYI (A02.01, A03.01) (SEQ ID NO: 2202)
QQQSDLQPPA (A02.01) (SEQ ID NO: 2204)
QQSDLQPPA (A02.01) (SEQ ID NO: 2205)
YQQQQQSDL (A02.01, B08.01) (SEQ ID NO: 2206)
LLSTPPLSPS (A02.01) (SEQ ID NO: 2208)
IWKKFELLPI (A24.02) (SEQ ID NO: 2210)
LLPIPPLSPS (A02.01, B07.02) (SEQ ID NO: 2211)
LPIPPLSPS (B07.02) (SEQ ID NO: 2212)
IIIEYCFYG (A02.01) (SEQ ID NO: 2214)
IYIIIEYCF (A24.02) (SEQ ID NO: 2215)
IYIIIEYCFY (A24.02) (SEQ ID NO: 2216)
YIIIEYCFYG (A02.01) (SEQ ID NO: 2217)
DPLSEITK (A03.01) (SEQ ID NO: 2220)
KTCLLISYTTNAFSG
EYIPTVFDNYSANVM
VDGKPVNLGLWDTAG
QEDYDRLRPLSYPQT
VGET (SEQ ID NO: 2006)
YMCNSSCMGS (A02.01) (SEQ ID NO: 2225)
ALKYIFVAVR (A03.01) (SEQ ID NO: 2230)
AVRAICVMK (A03.01) (SEQ ID NO: 2231)
AVRAICVMKS (A03.01) (SEQ ID NO: 2232)
CVEKKTALK (A03.01) (SEQ ID NO: 2233)
CVEKKTALKY (A01.01) (SEQ ID NO: 2234)
CVMKSFLIF (A24.02, B08.01) (SEQ ID NO: 2235)
CVMKSFLIFR (A03.01) (SEQ ID NO: 2236)
FLIFRRWKS (A02.01, B08.01) (SEQ ID NO: 2237)
FRRWKSHSPL (B08.01) (SEQ ID NO: 2238)
FVAVRAICV (A02.01, B08.01) (SEQ ID NO: 2239)
FVAVRAICVM (B08.01) (SEQ ID NO: 2240)
IQLHLSHPI (A02.01) (SEQ ID NO: 2241)
KSFLIFRRWK (A03.01) (SEQ ID NO: 2242)
KTALKYIFV (A02.01) (SEQ ID NO: 2243)
KYIFVAVRAI (A24.02) (SEQ ID NO: 2244)
RWKSHSPLQI (A24.02) (SEQ ID NO: 2245)
TALKYIFVAV (A02.01, B08.01) (SEQ ID NO: 2246)
VAVRAICVMK (A03.01) (SEQ ID NO: 2247)
VMKSFLIFR (A03.01) (SEQ ID NO: 2248)
VMKSFLIFRR (A03.01) (SEQ ID NO: 2249)
YIFVAVRAI (A02.01) (SEQ ID NO: 2250)
ALFFFFFETK (A03.01) (SEQ ID NO: 2252)
AQAGVQWRSL (A02.01) (SEQ ID NO: 2253)
CLANFCIFNR (A03.01) (SEQ ID NO: 2254)
CLSFLSSWDY (A01.01, A03.01) (SEQ ID NO: 2255)
FFETKSCSV (B08.01) (SEQ ID NO: 2256)
FFFETKSCSV (A02.01) (SEQ ID NO: 2257)
FKLFSCLSFL (A02.01) (SEQ ID NO: 2258)
FLSSWDYRRM (A02.01) (SEQ ID NO: 2259)
GFKLFSCLSF (A24.02) (SEQ ID NO: 2260)
KLFSCLSFL (A02.01, A03.01) (SEQ ID NO: 2261)
KLFSCLSFLS (A02.01, A03.01) (SEQ ID NO: 2262)
LALFFFFFET (A02.01) (SEQ ID NO: 2263)
LFFFFFETK (A03.01) (SEQ ID NO: 2264)
LSFLSSWDY (A01.01) (SEQ ID NO: 2265)
LSFLSSWDYR (A03.01) (SEQ ID NO: 2266)
RMPPCLANF (A24.02) (SEQ ID NO: 2267)
RRMPPCLANF (A24.02) (SEQ ID NO: 2268)
SLQPPPPGFK (A03.01) (SEQ ID NO: 2269)
VQWRSLGSL (A02.01) (SEQ ID NO: 2270)
MSVCFFFFSV (A02.01) (SEQ ID NO: 2272)
SVCFFFFSV (A02.01, B08.01) (SEQ ID NO: 2273)
SVCFFFFSVI (A02.01) (SEQ ID NO: 2274)
MSVCFFFFCY (A01.01) (SEQ ID NO: 2276)
SVCFFFFCYI (A02.01) (SEQ ID NO: 2277)
VLWMPTSTV (A02.01) (SEQ ID NO: 2279)
FEWKLKEGHKKIYGK
QSMVDEVSGKVLEMD
ISKKKHYNRKISIKK
LNRMKVPLMKLITRV*
(SEQ ID NO: 2021)
QLKWTPHILK (A03.01) (SEQ ID NO: 2285)
IVSEKNQQLK (A03.01) (SEQ ID NO: 2286)
QLKWTPHILK (A03.01) (SEQ ID NO: 2287)
QQLKWTPHI (A24.02) (SEQ ID NO: 2288)
NQQLKWTPHIL (B08.01) (SEQ ID NO: 2289)
NQQLKWTPHI (B08.01) (SEQ ID NO: 2290)
QLKWTPHIL (B08.01) (SEQ ID NO: 2291)
PPRPPRAAC (B07.02) (SEQ ID NO: 2293)
CLIVSRTLL (B08.01) (SEQ ID NO: 2297)
CLIVSRTLLL (A02.01, B08.01) (SEQ ID NO: 2298)
FLLALWECS (A02.01) (SEQ ID NO: 2299)
FLLALWECSL (A02.01, B08.01) (SEQ ID NO: 2300)
IVSRTLLLV (A02.01) (SEQ ID NO: 2301)
LIVSRTLLL (A02.01, B08.01) (SEQ ID NO: 2302)
LIVSRTLLLV (A02.01) (SEQ ID NO: 2303)
LLALWECSL (A02.01, B08.01) (SEQ ID NO: 2304)
LPQARLCLI (B08.01, B07.02) (SEQ ID NO: 2305)
LPQARLCLIV (B08.01) (SEQ ID NO: 2306)
NVRDKKRATF (B08.01) (SEQ ID NO: 2307)
SLPQARLCLI (A02.01, B08.01) (SEQ ID NO: 2308)
FFFCWILSCK (A03.01) (SEQ ID NO: 2310)
ITAFFFCWI (A02.01) (SEQ ID NO: 2311)
LYITAFFFCW (A24.02) (SEQ ID NO: 2312)
YITAFFFCWI (A02.01) (SEQ ID NO: 2313)
LLYITAFFL (A02.01, B08.01) (SEQ ID NO: 2315)
LLYITAFFLL (A02.01, A24.02) (SEQ ID NO: 2316)
LYITAFFLL (A24.02) (SEQ ID NO: 2317)
LYITAFFLLD (A24.02) (SEQ ID NO: 2318)
YITAFFLLDI (A02.01) (SEQ ID NO: 2319)
MPKDVNIQV (B07.02) (SEQ ID NO: 2321)
TGSNEVTTRY (A01.01) (SEQ ID NO: 2322)
KLMLLRLNL (A02.01, A03.01, B07.02, B08.01) (SEQ ID NO: 2324)
KLMLLRLNLR (A03.01) (SEQ ID NO: 2325)
LLRLNLRKM (B08.01) (SEQ ID NO: 2326)
LMLLRLNL (B08.01) (SEQ ID NO: 2327)
LMLLRLNLRK (A03.01) (SEQ ID NO: 2328)
LNLRKMCGPF (B08.01) (SEQ ID NO: 2329)
MLLRLNLRK (A03.01) (SEQ ID NO: 2330)
MLLRLNLRKM (A02.01, A03.01, B08.01) (SEQ ID NO: 2331)
NLRKMCGPF (B08.01) (SEQ ID NO: 2332)
NYCQKKLMLL (A24.02) (SEQ ID NO: 2333)
YCQKKLMLL (B08.01) (SEQ ID NO: 2334)
QPAEDGQGETNKNRT
KGGWQQKSKGPKKTA
KSKKKETFKKKTYTC
AITTVKATETKAGKW
SRWE* (SEQ ID NO: 2036)
ITTVKATETK (A03.01) (SEQ ID NO: 2336)
KSKKKETFK (A03.01) (SEQ ID NO: 2337)
KSKKKETFKK (A03.01) (SEQ ID NO: 2338)
KTYTCAITTV (A02.01, A24.02) (SEQ ID NO: 2339)
TFKKKTYTC (B08.01) (SEQ ID NO: 2340)
TYTCAITTV (A24.02) (SEQ ID NO: 2341)
TYTCAITTVK (A03.01) (SEQ ID NO: 2342)
YTCAITTVK (A03.01) (SEQ ID NO: 2343)
SLKKVPAL (B08.01) (SEQ ID NO: 2347)
RKISNWSLKK (A03.01) (SEQ ID NO: 2348)
VPALKKLRSPL (B07.02) (SEQ ID NO: 2349)
MTKKKRVNTA (B08.01) (SEQ ID NO: 2351)
RVNTAWKTK (A03.01) (SEQ ID NO: 2352)
RVNTAWKTKK (A03.01) (SEQ ID NO: 2353)
TKKKRVNTA (B08.01) (SEQ ID NO: 2354)
WKTKKTSFSL (B08.01) (SEQ ID NO: 2355)
AMTTSSSQK (A03.01, A11.01) (SEQ ID NO: 2357)
AMTTSSSQKN (A03.01) (SEQ ID NO: 2358)
CIMKEKKSL (B08.01) (SEQ ID NO: 2359)
CIMKEKKSLV (B08.01) (SEQ ID NO: 2360)
IMKEKKSL (B08.01) (SEQ ID NO: 2361)
IMKEKKSLV (B08.01) (SEQ ID NO: 2362)
KSLVRLSSCV (A02.01) (SEQ ID NO: 2363)
LVRLSSCVPV (A02.01) (SEQ ID NO: 2364)
RLSSCVPVA (A02.01, A03.01) (SEQ ID NO: 2365)
RLSSCVPVAL (A02.01) (SEQ ID NO: 2366)
SAMTTSSSQK (A03.01, A11.01) (SEQ ID NO: 2367)
SLVRLSSCV (A02.01) (SEQ ID NO: 2368)
VPVALMSAM (B07.02) (SEQ ID NO: 2369)
VRLSSCVPVA (A02.01) (SEQ ID NO: 2370)
DSLDIRWGIRYLKQT
AVPTIFSLPEDNQGK
DPSKKNPRRKTWKMR
KKYAQKPSQKNHLY*
(SEQ ID NO: 2045)
FVMSDTTYKI (A02.01) (SEQ ID NO: 2373)
KTFEKKGEK (A03.01) (SEQ ID NO: 2374)
LFVMSDTTYK (A03.01) (SEQ ID NO: 2375)
MSDTTYKIY (A01.01) (SEQ ID NO: 2376)
VMSDTTYKI (A02.01) (SEQ ID NO: 2377)
VMSDTTYKIY (A01.01) (SEQ ID NO: 2378)
F1354fs
Q1378fs
S1398fs
FRRPHSCLA (B08.01) (SEQ ID NO: 2381)
LIVLRVVRL (B08.01) (SEQ ID NO: 2382)
LLSVHLIVL (A02.01, B08.01) (SEQ ID NO: 2383)
R1435fs
T1438fs
P1442fs
P1443fs
V1452fs
P1453fs
K1462fs
E1464fs
HLHHLLKQLK (A03.01) (SEQ ID NO: 2385)
HLLLKRERV (B08.01) (SEQ ID NO: 2386)
KIKHLLLKR (A03.01) (SEQ ID NO: 2387)
KPSEKYLKI (B07.02) (SEQ ID NO: 2388)
KYLKIKHLL (A24.02) (SEQ ID NO: 2389)
KYLKIKHLLL (A24.02) (SEQ ID NO: 2390)
LLKQLKPSEK (A03.01) (SEQ ID NO: 2391)
LLKRERVDL (B08.01) (SEQ ID NO: 2392)
LLLKRERVDL (B08.01) (SEQ ID NO: 2393)
QLKPSEKYLK (A03.01) (SEQ ID NO: 2394)
YLKIKHLLL (A02.01, B08.01) (SEQ ID NO: 2395)
YLKIKHLLLK (A03.01) (SEQ ID NO: 2396)
H1490fs
L1488fs
KVLQMDFLV (A02.01, A24.02) (SEQ ID NO: 2398)
LPRKVLQMDF (B07.02, B08.01) (SEQ ID NO: 2399)
LQMDFLVHPA (A02.01) (SEQ ID NO: 2400)
QMDFLVHPA (A02.01) (SEQ ID NO: 2401)
YILPRKVLQM (A02.01, B08.01) (SEQ ID NO: 2402)
S1316fs
Y1324fs
T1348fs
G1351fs
G1378fs
P1467fs
HPLAPMPSKT (B07.02) (SEQ ID NO: 2404)
ILPLPQLLL (A02.01) (SEQ ID NO: 2405)
LLLSADQQA (A02.01) (SEQ ID NO: 2406)
LPTQTRGCI (B07.02) (SEQ ID NO: 2407)
LPTQTRGCIL (B07.02) (SEQ ID NO: 2408)
RISCLPTQTR (A03.01) (SEQ ID NO: 2409)
SLAETVSLH (A03.01) (SEQ ID NO: 2410)
TPRSSSSSS (B07.02) (SEQ ID NO: 2411)
TPRSSSSSSS (B07.02) (SEQ ID NO: 2412)
P725fs
R727fs
I736fs
ALPPVLLSLA (A02.01) (SEQ ID NO: 2414)
ALPRPLLAL (A02.01) (SEQ ID NO: 2415)
ASRTASCIL (B07.02) (SEQ ID NO: 2416)
EALPRPLLAL (B08.01) (SEQ ID NO: 2417)
HLGHPVASR (A03.01) (SEQ ID NO: 2418)
HPVASRTAS (B07.02) (SEQ ID NO: 2419)
HPVASRTASC (B07.02) (SEQ ID NO: 2420)
IIQLSLLSLL (A02.01) (SEQ ID NO: 2421)
IQLSLLSLL (A02.01) (SEQ ID NO: 2422)
IQLSLLSLLI (A02.01, A24.02) (SEQ ID NO: 2423)
LLALPPVLL (A02.01) (SEQ ID NO: 2424)
LLIPPLTCL (A02.01) (SEQ ID NO: 2425)
LLIPPLTCLA (A02.01) (SEQ ID NO: 2426)
LLSLLIPPL (A02.01) (SEQ ID NO: 2427)
LLSLLIPPLT (A02.01) (SEQ ID NO: 2428)
LPRPLLALPP (B07.02) (SEQ ID NO: 2429)
QLSLLSLLI (A02.01) (SEQ ID NO: 2430)
RLLQCQATR (A03.01) (SEQ ID NO: 2431)
RPLLALPPV (B07.02) (SEQ ID NO: 2432)
RPLLALPPVL (B07.02) (SEQ ID NO: 2433)
SLAQDHSRL (A02.01) (SEQ ID NO: 2434)
SLAQDHSRLL (A02.01) (SEQ ID NO: 2435)
SLLIPPLTCL (A02.01) (SEQ ID NO: 2436)
SLLSLLIPP (A02.01) (SEQ ID NO: 2437)
SLLSLLIPPL (A02.01, B08.01) (SEQ ID NO: 2438)
Q473fs
H477fs
S499fs
P504fs
Q548fs
P549fs
AAIPASTSAV (B07.02) (SEQ ID NO: 2440)
AIPASTSAV (A02.01) (SEQ ID NO: 2441)
ALPAGCVSSA (A02.01) (SEQ ID NO: 2442)
APLLTATGSV (B07.02) (SEQ ID NO: 2443)
APVLSASIL (B07.02) (SEQ ID NO: 2444)
ATLLPATTV (A02.01) (SEQ ID NO: 2445)
ATVSTTTAPV (A02.01) (SEQ ID NO: 2446)
AVPANCLFPA (A02.01) (SEQ ID NO: 2447)
CLFPAALPST (A02.01) (SEQ ID NO: 2448)
CPTFVSAAA (B07.02) (SEQ ID NO: 2449)
FPAALPSTA (B07.02) (SEQ ID NO: 2450)
FPAALPSTAG (B07.02) (SEQ ID NO: 2451)
GAECHGRPL (B07.02) (SEQ ID NO: 2452)
GAISRFIWV (A02.01) (SEQ ID NO: 2453)
ILPAAIPAST (A02.01) (SEQ ID NO: 2454)
IWVSGILSPL (A24.02) (SEQ ID NO: 2455)
LLTATGSVSL (A02.01) (SEQ ID NO: 2456)
LLYTADSSL (A02.01) (SEQ ID NO: 2457)
LPAAATSAA (B07.02) (SEQ ID NO: 2458)
LPAAATSAAS (B07.02) (SEQ ID NO: 2459)
LPAAIPAST (B07.02) (SEQ ID NO: 2460)
LPAGCVSSA (B07.02) (SEQ ID NO: 2461)
LPAGCVSSAP (B07.02) (SEQ ID NO: 2462)
LYTADSSLW (A24.02) (SEQ ID NO: 2463)
QPAKSSPSA (B07.02) (SEQ ID NO: 2464)
QPAKSSPSAA (B07.02) (SEQ ID NO: 2465)
RFIWVSGIL (A24.02) (SEQ ID NO: 2466)
RPQRVWSTG (B07.02) (SEQ ID NO: 2467)
RVWSTGPDSI (A02.01) (SEQ ID NO: 2468)
SAVPGSIPL (B07.02) (SEQ ID NO: 2469)
SILPAAIPA (A02.01) (SEQ ID NO: 2470)
SLPAAATSA (A02.01) (SEQ ID NO: 2471)
SLPAAATSAA (A02.01) (SEQ ID NO: 2472)
SLWTTRPQR (A03.01) (SEQ ID NO: 2473)
SLWTTRPQRV (A02.01) (SEQ ID NO: 2474)
SPSAAAATL (B07.02) (SEQ ID NO: 2475)
SPSAAAATLL (B07.02) (SEQ ID NO: 2476)
TLDALPAGCV (A02.01) (SEQ ID NO: 2477)
TVSTTTAPV (A02.01) (SEQ ID NO: 2478)
VLSASILPA (A02.01) (SEQ ID NO: 2479)
VLSASILPAA (A02.01) (SEQ ID NO: 2480)
VPANCLFPA (B07.02) (SEQ ID NO: 2481)
VPANCLFPAA (B07.02) (SEQ ID NO: 2482)
VPDPSCPTF (B07.02) (SEQ ID NO: 2483)
VPGSIPLPA (B07.02) (SEQ ID NO: 2484)
VPGSIPLPAV (B07.02) (SEQ ID NO: 2485)
WVSGILSPL (A02.01) (SEQ ID NO: 2486)
YTADSSLWTT (A02.01) (SEQ ID NO: 2487)
A441fs
Y447fs
P483fs
P484fs
P504fs
S519fs
H544fs
P549fs
P554fs
Q563fs
ASLHRRSYL (B08.01) (SEQ ID NO: 2489)
ASLHRRSYLK (A03.01) (SEQ ID NO: 2490)
FLLMDNKAPA (A02.01) (SEQ ID NO: 2491)
HPRRSPSRL (B07.02, B08.01) (SEQ ID NO: 2492)
HPSLHISSP (B07.02) (SEQ ID NO: 2493)
HRRSYLKIHL (B08.01) (SEQ ID NO: 2494)
HSRFLLMDNK (A03.01) (SEQ ID NO: 2495)
KLPIPSSASL (A02.01) (SEQ ID NO: 2496)
KVLTLSSSSH (A03.01) (SEQ ID NO: 2497)
LIHSRFLLM (B08.01) (SEQ ID NO: 2498)
LLMDNKAPA (A02.01) (SEQ ID NO: 2499)
LMDNKAPAGM (A02.01) (SEQ ID NO: 2500)
LPIPSSASL (B07.02) (SEQ ID NO: 2501)
MPNLRISSS (B07.02, B08.01) (SEQ ID NO: 2502)
MPNLRISSSH (B07.02) (SEQ ID NO: 2503)
NLRISSSHSL (B07.02, B08.01) (SEQ ID NO: 2504)
PPTHSHRLSL (B07.02) (SEQ ID NO: 2505)
RAGRRVPWAA (B08.01) (SEQ ID NO: 2506)
RARLHITTSK (A03.01) (SEQ ID NO: 2507)
RISSSHSLNH (A03.01) (SEQ ID NO: 2508)
RLHTPPSSR (A03.01) (SEQ ID NO: 2509)
RLHTPPSSRR (A03.01) (SEQ ID NO: 2510)
RLRILSPSL (A02.01, B07.02, B08.01) (SEQ ID NO: 2511)
RPLMPNLRI (B07.02) (SEQ ID NO: 2512)
RPRPLMPNL (B07.02) (SEQ ID NO: 2513)
SASLHRRSYL (B07.02, B08.01) (SEQ ID NO: 2514)
SLHISSPRL (A02.01) (SEQ ID NO: 2515)
SLHRRSYLK (A03.01) (SEQ ID NO: 2516)
SLHRRSYLKI (B08.01) (SEQ ID NO: 2517)
SLIHSRFLL (A02.01) (SEQ ID NO: 2518)
SLIHSRFLLM (A02.01, B08.01) (SEQ ID NO: 2519)
SLLTSSSNL (A02.01) (SEQ ID NO: 2520)
SLNHHSSSPL (A02.01, B07.02, B08.01) (SEQ ID NO: 2521)
SLSSPSKLPI (A02.01) (SEQ ID NO: 2522)
SPLSLHTPS (B07.02) (SEQ ID NO: 2523)
SPLSLHTPSS (B07.02) (SEQ ID NO: 2524)
SPPTHSHRL (B07.02) (SEQ ID NO: 2525)
SPRLHTPPS (B07.02) (SEQ ID NO: 2526)
SPRLHTPPSS (B07.02) (SEQ ID NO: 2527)
SPSLSSPSKL (B07.02) (SEQ ID NO: 2528)
SYLKIHLGL (A24.02) (SEQ ID NO: 2529)
TPSNHRPRPL (B07.02, B08.01) (SEQ ID NO: 2530)
TPSSHPSLHI (B07.02) (SEQ ID NO: 2531)
P2139fs
L1970fs
V1994fs
HCVPFWTGRIL (B07.02) (SEQ ID NO: 2533)
ILLPSAASV (A02.01) (SEQ ID NO: 2534)
ILLPSAASVC (A02.01) (SEQ ID NO: 2535)
LLPSAASVCPI (A02.01) (SEQ ID NO: 2536)
LPSAASVCPI (B07.02) (SEQ ID NO: 2537)
MRPHCVPF (B08.01) (SEQ ID NO: 2538)
RILLPSAASV (A02.01) (SEQ ID NO: 2539)
RMRPHCVPF (A24.02, B07.02, B08.01) (SEQ ID NO: 2540)
RMRPHCVPFW (A24.02) (SEQ ID NO: 2541)
RTNPTVRMR (A03.01) (SEQ ID NO: 2542)
SVCPIPFEA (A02.01) (SEQ ID NO: 2543)
TVRMRPHCV (B08.01) (SEQ ID NO: 2544)
TVRMRPHCVPF (B08.01) (SEQ ID NO: 2545)
VPFWTGRIL (B07.02) (SEQ ID NO: 2546)
VPFWTGRILL (B07.02) (SEQ ID NO: 2547)
VRMRPHCVPF (B08.01) (SEQ ID NO: 2548)
S764fs
T783fs
Q799fs
A817fs
AMVPRGVSMA (A02.01) (SEQ ID NO: 2550)
AWAPTSRTPW (A24.02) (SEQ ID NO: 2551)
CPMPTTPVQA (B07.02) (SEQ ID NO: 2552)
CPSTVPPSPA (B07.02) (SEQ ID NO: 2553)
GAMVPRGVSM (B07.02, B08.01) (SEQ ID NO: 2554)
MPCPMPTTPV (B07.02) (SEQ ID NO: 2555)
MPTTPVQAW (B07.02) (SEQ ID NO: 2556)
MPTTPVQAWL (B07.02) (SEQ ID NO: 2557)
SLPEDRYTQA (A02.01) (SEQ ID NO: 2558)
SPAQPYLRV (B07.02) (SEQ ID NO: 2559)
SPAQPYLRVS (B07.02) (SEQ ID NO: 2560)
TIMPCPMPT (A02.01) (SEQ ID NO: 2561)
TPVQAWLEA (B07.02) (SEQ ID NO: 2562)
TSRTPWGAM (B07.02) (SEQ ID NO: 2563)
VPPSPAQPYL (B07.02) (SEQ ID NO: 2564)
VPRGVSMAH (B07.02) (SEQ ID NO: 2565)
E67fs
L74fs
F82fs
T91fs
E94fs
CTTLNSPPLK (A03.01) (SEQ ID NO: 2567)
GLSISCTTL (A02.01) (SEQ ID NO: 2568)
SPPLKKMSM (B07.02, B08.01) (SEQ ID NO: 2569)
TLNSPPLKK (A03.01) (SEQ ID NO: 2570)
TTLNSPPLK (A03.01) (SEQ ID NO: 2571)
TTLNSPPLKK (A03.01) (SEQ ID NO: 2572)
S14fs
LQRFRFTHVI (B08.01) (SEQ ID NO: 2574)
RLSSVLQRF (A24.02) (SEQ ID NO: 2575)
RLSSVLQRFR (A03.01) (SEQ ID NO: 2576)
VLQRFRFTHV (A02.01, B08.01) (SEQ ID NO: 2577)
P708fs
L711fs
KFLPFWGFL (A24.02) (SEQ ID NO: 2579)
LASVGRHSL (B07.02) (SEQ ID NO: 2580)
LPFWGFLEEF (B07.02) (SEQ ID NO: 2581)
PFWGFLEEF (A24.02) (SEQ ID NO: 2582)
SVGRHSLSK (A03.01) (SEQ ID NO: 2583)
P126fs
H128fs
N144fs
V157fs
P159fs
N166fs
N181fs
F189fs
P201fs
F205fs
APRPIRPPFL (B07.02) (SEQ ID NO: 2585)
AQKMKKAHFL (B08.01) (SEQ ID NO: 2586)
FLPSAAQKM (A02.01) (SEQ ID NO: 2587)
GLFLPSAAQK (A03.01) (SEQ ID NO: 2588)
HPLLVSLLL (B07.02) (SEQ ID NO: 2589)
KAHFLKTWFR (A03.01) (SEQ ID NO: 2590)
KARFSTASL (B07.02) (SEQ ID NO: 2591)
KMKKAHFLK (A03.01) (SEQ ID NO: 2592)
KTWFRSNPTK (A03.01) (SEQ ID NO: 2593)
LAKELTHPL (B07.02, B08.01) (SEQ ID NO: 2594)
LAKELTHPLL (B08.01) (SEQ ID NO: 2595)
NPTKTKKARF (B07.02) (SEQ ID NO: 2596)
QKMKKAHFL (B08.01) (SEQ ID NO: 2597)
RFSTASLAK (A03.01) (SEQ ID NO: 2598)
RPIRPPFLES (B07.02) (SEQ ID NO: 2599)
RSNPTKTKK (A03.01) (SEQ ID NO: 2600)
SLAKELTHPL (A02.01, B08.01) (SEQ ID NO: 2601)
TKKARFSTA (B08.01) (SEQ ID NO: 2602)
P127fs
V132fs
P160fs
ISQLLSWPQK (A03.01) (SEQ ID NO: 2604)
RIAHISQLL (A02.01) (SEQ ID NO: 2605)
RLGYSSHQL (A02.01) (SEQ ID NO: 2606)
SQLLSWPQK (A03.01) (SEQ ID NO: 2607)
SRIAHISQL (B08.01) (SEQ ID NO: 2608)
WPQKTEERL (B07.02) (SEQ ID NO: 2609)
YSSHQLPRK (A03.01) (SEQ ID NO: 2610)
R749fs
E757fs
G759fs
EAEKRTRTL (B08.01) (SEQ ID NO: 2612)
GTTFITMMK (A03.01) (SEQ ID NO: 2613)
GTTFITMMKK (A03.01) (SEQ ID NO: 2614)
ITMMKKEAEK (A03.01) (SEQ ID NO: 2615)
RMTPGTTFI (A02.01) (SEQ ID NO: 2616)
SPYCPQRMT (B07.02) (SEQ ID NO: 2617)
TMMKKEAEK (A03.01) (SEQ ID NO: 2618)
TPGTTFITM (B07.02) (SEQ ID NO: 2619)
TPGTTFITMM (B07.02) (SEQ ID NO: 2620)
TTFITMMKK (A03.01) (SEQ ID NO: 2621)
E24fs
S36fs
CPGATWREAA (B07.02) (SEQ ID NO: 2623)
RSRCPGATWR (A03.01) (SEQ ID NO: 2624)
TPRATRSRC (B07.02) (SEQ ID NO: 2625)
P387fs
S398fs
H400fs
M401fs
S408fs
P409fs
S408fs
P409fs
T419fs
H424fs
P425fs
S427fs
F431fs
S430fs
H434fs
H435fs
S438fs
M443fs
G444fs
*445fs
RPLQTHVLPE (B07.02) (SEQ ID NO: 2627)
VLWTTPPLQH (A03.01) (SEQ ID NO: 2628)
H434fs
P433fs
T441fs
CPLDHTTPPA (B07.02) (SEQ ID NO: 2630)
FLQEQYHEA (A02.01, B08.01) (SEQ ID NO: 2631)
RLAFLQEQYH (A03.01) (SEQ ID NO: 2632)
SPCSPFRLAF (B07.02) (SEQ ID NO: 2633)
SPPWVRALL (B07.02) (SEQ ID NO: 2634)
YPACPLDHTT (B07.02) (SEQ ID NO: 2635)
E524fs
P647fs
S654fs
L656fs
R755fs
L761fs
Q773fs
CLHHRRHLV (B08.01) (SEQ ID NO: 2637)
CLHHRRHLVC (B08.01) (SEQ ID NO: 2638)
CLHRKSHPHL (B08.01) (SEQ ID NO: 2639)
CLRSHACPP (B08.01) (SEQ ID NO: 2640)
CLRSHTCPP (B08.01) (SEQ ID NO: 2641)
CLWCHACLH (A03.01) (SEQ ID NO: 2642)
CPHHLKNHL (B07.02) (SEQ ID NO: 2643)
CPHHLKNLL (B07.02) (SEQ ID NO: 2644)
CPHHLRTRL (B07.02, B08.01) (SEQ ID NO: 2645)
CPLHLRSLPF (B07.02, B08.01) (SEQ ID NO: 2646)
CPLPRHLKHL (B07.02, B08.01) (SEQ ID NO: 2647)
CPLSLRSHPC (B07.02) (SEQ ID NO: 2648)
CPRHLRNCPL (B07.02, B08.01) (SEQ ID NO: 2649)
FPHHLRHHA (B07.02, B08.01) (SEQ ID NO: 2650)
FPHHLRHHAC (B07.02, B08.01) (SEQ ID NO: 2651)
GLRSRTCPP (B08.01) (SEQ ID NO: 2652)
HACLHRLRNL (B08.01) (SEQ ID NO: 2653)
HLACLHHLR (A03.01) (SEQ ID NO: 2654)
HLCPPHLRY (A03.01) (SEQ ID NO: 2655)
HLCPPHLRYR (A03.01) (SEQ ID NO: 2656)
HLKHLACLH (A03.01) (SEQ ID NO: 2657)
HLKHRPCPH (B08.01) (SEQ ID NO: 2658)
HLKNHLCPP (B08.01) (SEQ ID NO: 2659)
HLKSHPCLH (A03.01) (SEQ ID NO: 2660)
HLKSLLCPL (A02.01, B08.01) (SEQ ID NO: 2661)
HLLHLRRLY (A03.01) (SEQ ID NO: 2662)
HLRNCPLPR (A03.01) (SEQ ID NO: 2663)
HLRNCPLPRH (A03.01) (SEQ ID NO: 2664)
HLRRLYPHHL (B08.01) (SEQ ID NO: 2665)
HLRSHPCPL (B07.02, B08.01) (SEQ ID NO: 2666)
HLRSHPCPLH (A03.01) (SEQ ID NO: 2667)
HLRSLPFPH (A03.01) (SEQ ID NO: 2668)
HLRTRLCPH (A03.01, B08.01) (SEQ ID NO: 2669)
HLVCSHHLK (A03.01) (SEQ ID NO: 2670)
HPCLHHRRHL (B07.02, B08.01) (SEQ ID NO: 2671)
HPGLRSRTC (B07.02) (SEQ ID NO: 2672)
HPHLLHLRRL (B07.02, B08.01) (SEQ ID NO: 2673)
HRKSHPHLL (B08.01) (SEQ ID NO: 2674)
HRRTRSCPC (B08.01) (SEQ ID NO: 2675)
KSHPHLLHLR (A03.01) (SEQ ID NO: 2676)
KSLLCPLHLR (A03.01) (SEQ ID NO: 2677)
LLCPLHLRSL (A02.01, B08.01) (SEQ ID NO: 2678)
LLHLRRLYPH (B08.01) (SEQ ID NO: 2679)
LPRHLKHLA (B07.02) (SEQ ID NO: 2680)
LPRHLKHLAC (B07.02, B08.01) (SEQ ID NO: 2681)
LRRLRSHTC (B08.01) (SEQ ID NO: 2682)
LRRLYPHHL (B08.01) (SEQ ID NO: 2683)
LVCSHHLKSL (B08.01) (SEQ ID NO: 2684)
NLRNHTCPPS (B08.01) (SEQ ID NO: 2685)
PLHLRSLPF (B08.01) (SEQ ID NO: 2686)
RLCPHHLKNH (A03.01) (SEQ ID NO: 2687)
RLYPHHLKH (A03.01) (SEQ ID NO: 2688)
RLYPHHLKHR (A03.01) (SEQ ID NO: 2689)
RPCPHHLKNL (B07.02) (SEQ ID NO: 2690)
RSHPCPLHLK (A03.01) (SEQ ID NO: 2691)
RSLPFPHHLR (A03.01) (SEQ ID NO: 2692)
RTRLCPHHL (B07.02) (SEQ ID NO: 2693)
RTRLCPHHLK (A03.01) (SEQ ID NO: 2694)
SLLCPLHLR (A03.01) (SEQ ID NO: 2695)
SLRSHACPP (B08.01) (SEQ ID NO: 2696)
SPLRSQANA (B07.02) (SEQ ID NO: 2697)
YLRRLRSHT (B08.01) (SEQ ID NO: 2698)
YPHHLKHRPC (B07.02, B08.01) (SEQ ID NO: 2699)
I135fs
A148fs
L152fs
D162fs
I168fs
IFITSGQIF (A24.02) (SEQ ID NO: 2701)
SQSEALCVL (A02.01) (SEQ ID NO: 2702)
SQSEALCVLL (A02.01) (SEQ ID NO: 2703)
K266fs
E40fs
V45fs
R47fs
N48fs
DLKAYTGTILMM*
(SEQ ID NO: 2069)
DLKAYTGTIL (B08.01) (SEQ ID NO: 2705)
T321fs
K327fs
A328fs
A333fs
KMILTKQIK (A03.01) (SEQ ID NO: 2707)
KPTDTFLQI (B07.02) (SEQ ID NO: 2708)
KPTDTFLQIL (B07.02) (SEQ ID NO: 2709)
MILTKQIKTK (A03.01) (SEQ ID NO: 2710)
E73fs
A86fs
N94fs
LIAELHNIL (A02.01) (SEQ ID NO: 2712)
LIAELHNILL (A02.01) (SEQ ID NO: 2713)
MTPPNLIAEL (A02.01) (SEQ ID NO: 2714)
NLIAELHNI (A02.01) (SEQ ID NO: 2715)
NLIAELHNIL (A02.01) (SEQ ID NO: 2716)
RYTIFVLKDI (A24.02) (SEQ ID NO: 2717)
TITRYTIFVL (A02.01) (SEQ ID NO: 2718)
TPPNLIAEL (B07.02) (SEQ ID NO: 2719)
G209fs
C211fs
I224fs
G230fs
P231fs
R233fs
D236fs
LPAKGEDIFL (B07.02) (SEQ ID NO: 2721)
LQFRTHTTGR (A03.01) (SEQ ID NO: 2722)
NLQSSVCGL (A02.01) (SEQ ID NO: 2723)
SSVCGLPAK (A03.01) (SEQ ID NO: 2724)
VQWRNLQSSV (A02.01) (SEQ ID NO: 2725)
E256fs
K260fs
Q261fs
L265fs
M270fs
H272fs
T286fs
E288fs
HTRTRGNLRK (A03.01) (SEQ ID NO: 2727)
ILHTRTRGNL (B08.01) (SEQ ID NO: 2728)
KGQNVSLLGK (A03.01) (SEQ ID NO: 2729)
LLGKYILHT (A02.01) (SEQ ID NO: 2730)
LRKSRKWKSM (B08.01) (SEQ ID NO: 2731)
SLLGKYILH (A03.01) (SEQ ID NO: 2732)
SLLGKYILHT (A02.01) (SEQ ID NO: 2733)
P72fs
A76fs
A79fs
P89fs
W91fs
S96fs
V97fs
V97fs
G108fs
G117fs
S121fs
V122fs
C124fs
K139fs
V143fs
FPENLPGQL (B07.02) (SEQ ID NO: 2735)
GLLAFWDSQV (A02.01) (SEQ ID NO: 2736)
IFCPFPENL (A24.02) (SEQ ID NO: 2737)
LLAFWDSQV (A02.01) (SEQ ID NO: 2738)
LLAPVIFCP (A02.01) (SEQ ID NO: 2739)
LLAPVIFCPF (A02.01, A24.02) (SEQ ID NO: 2740)
LPCPQQDVL (B07.02) (SEQ ID NO: 2741)
RFPSGLLAF (A24.02) (SEQ ID NO: 2742)
RFPSGLLAFW (A24.02) (SEQ ID NO: 2743)
SPLLAPVIF (B07.02) (SEQ ID NO: 2744)
SPRGPCTSS (B07.02) (SEQ ID NO: 2745)
SPRGPCTSSS (B07.02) (SEQ ID NO: 2746)
SQVCDLHVL (A02.01) (SEQ ID NO: 2747)
VIFCPFPENL (A02.01) (SEQ ID NO: 2748)
H178fs
D186fs
H193fs
L194fs
E198fs
V203fs
E204fs
L206fs
D207fs
N210fs
T211fs
F212fs
V225fs
S241fs
AMVWPLLSIL (A02.01) (SEQ ID NO: 2750)
AQIAMVWPL (A02.01, A24.02) (SEQ ID NO: 2751)
AQIAMVWPLL (A02.01) (SEQ ID NO: 2752)
CPMSRLRLA (B07.02, B08.01) (SEQ ID NO: 2753)
CPMSRLRLAL (B07.02, B08.01) (SEQ ID NO: 2754)
IAMVWPLLSI (A02.01, A24.02, B08.01) (SEQ ID NO: 2755)
ILSEWKEICV (A02.01) (SEQ ID NO: 2756)
IVWWCPMSR (A03.01) (SEQ ID NO: 2757)
IVWWCPMSRL (A02.01) (SEQ ID NO: 2758)
IWMTETLFDI (A24.02) (SEQ ID NO: 2759)
LLSILSEWK (A03.01) (SEQ ID NO: 2760)
MSAAQIAMV (A02.01) (SEQ ID NO: 2761)
MSRLRLALT (B08.01) (SEQ ID NO: 2762)
MSRLRLALTV (B08.01) (SEQ ID NO: 2763)
MVWPLLSIL (A02.01) (SEQ ID NO: 2764)
RLALTVPPST (A02.01) (SEQ ID NO: 2765)
TLFDIVWWC (A02.01) (SEQ ID NO: 2766)
TLFDIVWWCP (A02.01) (SEQ ID NO: 2767)
TMSAAQIAMV (A02.01) (SEQ ID NO: 2768)
VWSIWMTETL (A24.02) (SEQ ID NO: 2769)
WMTETLFDI (A02.01, A24.02) (SEQ ID NO: 2770)
WMTETLFDIV (A01.01, A02.01) (SEQ ID NO: 2771)
P250fs
S260fs
N263fs
G266fs
N268fs
V272fs
V274fs
P278fs
D281fs
R282fs
T284fs
E285fs
L289fs
K292fs
P301fs
S303fs
T312fs
S314fs
K319fs
K320fs
P322fs
Y327fs
F328fs
L330fs
R333fs
R335fs
R337fs
E339fs
ALRCVFVPVL (A02.01, B08.01) (SEQ ID NO: 2773)
ALSEHCPTT (A02.01) (SEQ ID NO: 2774)
AQRKRISARK (A03.01) (SEQ ID NO: 2775)
GAQRKRISA (B08.01) (SEQ ID NO: 2776)
HWMENISPF (A24.02) (SEQ ID NO: 2777)
LPSQRRNHW (B07.02) (SEQ ID NO: 2778)
LPSQRRNHWM (B07.02, B08.01) (SEQ ID NO: 2779)
NISPFRSVGV (A02.01) (SEQ ID NO: 2780)
RISARKGSL (B07.02, B08.01) (SEQ ID NO: 2781)
SPFRSVGVSA (B07.02) (SEQ ID NO: 2782)
SPSSHWKTPV (B07.02, B08.01) (SEQ ID NO: 2783)
TALRCVFVPV (A02.01) (SEQ ID NO: 2784)
VIYWDGTAL (A02.01) (SEQ ID NO: 2785)
VIYWDGTALR (A03.01) (SEQ ID NO: 2786)
VLGETGAQRK (A03.01) (SEQ ID NO: 2787)
P151fs
P152fs
V157fs
Q165fs
S166fs
H168fs
V173fs
HPRPRHGHLQ (B07.02) (SEQ ID NO: 2789)
RPRHGHLQA (B07.02) (SEQ ID NO: 2790)
RPRHGHLQAV (B07.02, B08.01) (SEQ ID NO: 2791)
D48fs
D49fs
Q52fs
F54fs
E56fs
P58fs
P60fs
E62fs
M66fs
P72fs
V73fs
P75fs
A78fs
P82fs
P85fs
S96fs
P98fs
T102fs
Y103fs
G108fs
F109fs
R110fs
G117fs
PPGPCHLLSL (B07.02) (SEQ ID NO: 2793)
RTILNNGSLK (A03.01) (SEQ ID NO: 2794)
SLKTQVQMK (A03.01) (SEQ ID NO: 2795)
SLKTQVQMKL (B08.01) (SEQ ID NO: 2796)
TILNNGSLK (A03.01) (SEQ ID NO: 2797)
P27fs
P34fs
P36fs
A39fs
Q38fs
TFCPPCRPKQWMI*
(SEQ ID NO: 2079)
TTFCPPCRPK (A03.01) (SEQ ID NO: 2799)
L130fs
N131fs
C135fs
K139fs
A138fs
T140fs
V143fs
Q144fs
V147fs
T150fs
P151fs
P152fs
G154fs
R156fs
R158fs
A161fs
FANWPRPAL (B07.02, B08.01) (SEQ ID NO: 2801)
GLIPHPRPA (A02.01) (SEQ ID NO: 2802)
HPRPAPASA (B07.02, B08.01) (SEQ ID NO: 2803)
HPRPAPASAP (B07.02) (SEQ ID NO: 2804)
IPHPRPAPA (B07.02, B08.01) (SEQ ID NO: 2805)
IPHPRPAPAS (B07.02) (SEQ ID NO: 2806)
RPALCSCGL (B07.02) (SEQ ID NO: 2807)
RPALCSCGLI (B07.02) (SEQ ID NO: 2808)
TPLPSTRCF (B07.02) (SEQ ID NO: 2809)
WPRPALCSC (B07.02) (SEQ ID NO: 2810)
WPRPALCSCG (B07.02) (SEQ ID NO: 2811)
D179fs
L184fs
T202fs
R205fs
D213fs
G212fs
GLVPSLVSK (A03.01) (SEQ ID NO: 2813)
KISVETYTV (A02.01) (SEQ ID NO: 2814)
LLMVLMSLDL (A02.01, B08.01) (SEQ ID NO: 2815)
LMSLDLDTGL (A02.01) (SEQ ID NO: 2816)
LMVLMSLDL (A02.01) (SEQ ID NO: 2817)
LVSKCLILRV (A02.01) (SEQ ID NO: 2818)
QLLMVLMSL (A02.01, B08.01) (SEQ ID NO: 2819)
RPGAADTGA (B07.02) (SEQ ID NO: 2820)
RPGAADTGAH (B07.02) (SEQ ID NO: 2821)
SLDLDTGLV (A02.01) (SEQ ID NO: 2822)
SLVSKCLIL (A02.01, B08.01) (SEQ ID NO: 2823)
SQLLMVLMSL (A02.01) (SEQ ID NO: 2824)
TVSSQLLMV (A02.01) (SEQ ID NO: 2825)
TYTVSSQLL (A24.02) (SEQ ID NO: 2826)
TYTVSSQLLM (A24.02) (SEQ ID NO: 2827)
VLMSLDLDT (A02.01) (SEQ ID NO: 2828)
VPSLVSKCL (B07.02) (SEQ ID NO: 2829)
VSKCLILRVK (A03.01) (SEQ ID NO: 2830)
YTVSSQLLM (A01.01) (SEQ ID NO: 2831)
YTVSSQLLMV (A02.01) (SEQ ID NO: 2832)
K159fs
R161fs
Q164fs
I147fs
F148fs
L158fs
ERAMPPGCPEPSQA*
(SEQ ID NO: 2083)
S72fs
I75fs
S80fs
P86fs
P97fs
I109fs
H115fs
L116fs
G123fs
T124fs
N131fs
L135fs
V137fs
G144fs
D143fs
I147fs
CPYGSTSTAS (B07.02) (SEQ ID NO: 2835)
LARAAASTAT (B07.02) (SEQ ID NO: 2836)
MLTDSLFLP (A02.01) (SEQ ID NO: 2837)
PPRSSSAIAV (B07.02) (SEQ ID NO: 2838)
RAAASTATEV (B07.02) (SEQ ID NO: 2839)
SPPRSSSAI (B07.02) (SEQ ID NO: 2840)
SPPRSSSAIA (B07.02) (SEQ ID NO: 2841)
SPTQRCRLA (B07.02) (SEQ ID NO: 2842)
TQRCRLARA (B08.01) (SEQ ID NO: 2843)
TQRCRLARAA (B08.01) (SEQ ID NO: 2844)
P172fs
N174fs
L178fs
D179fs
L188fs
WTSSGRSTK (A03.01) (SEQ ID NO: 2846)
V66fs
Q73fs
V84fs
F91fs
T100fs
P103fs
S111fs
L116fs
H115fs
D126fs
AQLRRRAAA (B08.01) (SEQ ID NO: 2848)
AQLRRRAAAL (B08.01) (SEQ ID NO: 2849)
ARRAARMAQL (B08.01) (SEQ ID NO: 2850)
HPQLPRSPL (B07.02, B08.01) (SEQ ID NO: 2851)
HPQLPRSPLA (B07.02) (SEQ ID NO: 2852)
LARALPGHL (B07.02) (SEQ ID NO: 2853)
LARALPGHLL (B07.02) (SEQ ID NO: 2854)
MAQLRRRAA (B07.02, B08.01) (SEQ ID NO: 2855)
MAQLRRRAAA (B07.02, B08.01) (SEQ ID NO: 2856)
QLRRRAAAL (B07.02, B08.01) (SEQ ID NO: 2857)
RAAALPNAAA (B07.02) (SEQ ID NO: 2858)
RMAQLRRRAA (B07.02, B08.01) (SEQ ID NO: 2859)
SQSARRAARM (B08.01) (SEQ ID NO: 2860)
RVGNCKHLK (A03.01) (SEQ ID NO: 2862)
*вне рамки считыва ния
KICNESASRK (A03.01) (SEQ ID NO: 2864)
NRRLDVTVANGR:S:
WKYGWSLLRVPQVNG
IQVLNVSLKSSSNVI
SYE* (SEQ ID NO: 2089)
IQVLNVSLK (A03.01) (SEQ ID NO: 2866)
KSSSNVISY (A01.01, A03.01) (SEQ ID NO: 2867)
KYGWSLLRV (A24.02) (SEQ ID NO: 2868)
RSWKYGWSL (A02.01) (SEQ ID NO: 2869)
SLKSSSNVI (B08.01) (SEQ ID NO: 2870)
SWKYGWSLL (A24.02) (SEQ ID NO: 2871)
TVANGRSWK (A03.01) (SEQ ID NO: 2872)
VPQVNGIQV (B07.02) (SEQ ID NO: 2873)
VPQVNGIQVL (B07.02) (SEQ ID NO: 2874)
VTVANGRSWK (A03.01) (SEQ ID NO: 2875)
WSLLRVPQV (B08.01) (SEQ ID NO: 2876)
KLRVPGSSV (B07.02) (SEQ ID NO: 2878)
KLRVPGSSVL (B07.02) (SEQ ID NO: 2879)
RVPGSSVLV (A02.01) (SEQ ID NO: 2880)
SVLVTVPGL (A02.01) (SEQ ID NO: 2881)
VPGSSVLVTV (B07.02) (SEQ ID NO: 2882)
ALSALLLRPR (A03.01) (SEQ ID NO: 2884)
ATGFKQSSK (A03.01) (SEQ ID NO: 2887)
KGPELFPLI (A02.01, A24.02) (SEQ ID NO: 2889)
KGPELFPLIF (A24.02) (SEQ ID NO: 2890)
STREKNSQV (B08.01) (SEQ ID NO: 2893)
VYRRKHQEL (A24.02, B08.01) (SEQ ID NO: 2894)
VLTVTSTDVK (A03.01) (SEQ ID NO: 2896)
IMSLWGLVSK (A03.01) (SEQ ID NO: 2898)
KLKQEATSK (A03.01) (SEQ ID NO: 2899)
QIMSLWGLV (A02.01) (SEQ ID NO: 2900)
SQIMSLWGL (A02.01, A24.02, B08.01) (SEQ ID NO: 2901)
SQIMSLWGLV (A02.01) (SEQ ID NO: 2902)
TSKSQIMSL (B08.01) (SEQ ID NO: 2903)
LQEFDVQEAL (A02.01) (SEQ ID NO: 2905)
RNRTEKHSTM (B08.01) (SEQ ID NO: 2907)
ALNSEALSVV (A02.01) (SEQ ID NO: 2909)
MALNSEALSV (A02.01, B08.01) (SEQ ID NO: 2910)
1Подчеркнутые AA представляют ненативные AA
2Выделенные жирным AA представляют нативные AA аминокислотной последовательности, кодированной вторым из двух слитых генов
3Выделенные жирным и подчеркнутые AA представляют ненативные AA аминокислотной последовательности, кодированной вторым из двух конденсированных генов из-за сдвига рамки.
В таблице 36 ниже представлен список выбранных HLA-ограниченных BTK пептидов для цели этой заявки, и соответствующий белок, кодируемый HLA аллелем, с которыммутантный BTK пептид связывается или предположительно связывается.
Таблица 36
В таблице 37 представлен список выбранных BTK пептидов и соответствующего предпочтительного белка, кодированного HLA аллелем, с которым пептид связывается или предположительно связывается, как применимо в контексте этой заявки.
Таблица 37
Типовые мутации EGFR гена, которые преобладают в разных типах рака, представлены в таблице 40A-40D. В таблице также представлены EGFR неоантигенные пептиды. Мутации, включающие отдельные аминокислотные замещения, преобладающие при раке, перечислены в таблицах 40A-40C. Типовые мутации, включающие делецию и вставку, представлены в таблице 40D.
Таблица 40A. Типовые EGFR точечные мутации при раке и мутантные пептиды
GAGAAGC
(SEQ ID NO: 3820)
TSPKANKEILDEAYVMAS
VDNPHVCRLLGICLTSTV
QLIT
(SEQ ID NO: 2948)
("ELREA" раскрыта как SEQ ID NO: 3822)
Таблица 40B. Типовые EGFR точечные мутации при раке и мутантные пептиды
HLA.A11.01
HLA.A30.01
Таблица 40C. Типовые EGFR точечные мутации при раке и мутантные пептиды
Таблица 40D. Типовые EGFR мутации делеции, мутации слияния при раке
В таблицах выше, для одного или нескольких типовых слияний, последовательность, указанная до первого “:” принадлежит экзону последовательности полипептида, кодированного первым геном, последовательность, указанная после второго “:” принадлежит экзону последовательности полипептида, кодированного вторым геном, и аминокислота, которая появляется между символами “:” кодируется кодоном, который разделяется между экзоном последовательности полипептида, кодированного первым геном и экзоном последовательности полипептида, кодированного вторым геном.
Однако в некоторых вариантах осуществления, например, NAB:STAT6, NAB экзон связан с 5’ UTR STAT6, и первая аминокислота, которая появляется после точки соединения, является нормальным старт-кодоном STAT6 (никакая рамка в этой сайте не присутствует (поскольку он не транслирован нормально).
AR-V7 в таблицах выше также можно рассматривать, в некоторых вариантах осуществления, как вариант сплайсинга AR гена, который кодирует белок, который не имеет лиганд-связывающего домена, найденного в полноразмерном AR.
В некоторых вариантах осуществления, способы секвенирования используют для идентификации опухолеспецифических мутаций. Любой подходящий способ секвенирования может быть использован в соответствии с настоящим описанием, например, технологии секвенирования следующего поколения (NGS). Способы секвенирования третьего поколения могут быть заменой технологии NGS в будущем для ускорения стадии секвенирования способа. В целях пояснения: термины “секвенирование следующего поколения” или “NGS” в контексте настоящего описания означает все новые высокоэффективные технологии секвенирования, которые, в отличие от “обычной” методики секвенирования, известной как химия Сэнгера, считывают шаблоны нуклеиновой кислоты случайным образом, параллельно по всему геному, разбивая весь геном на мелкие части (также известные как технологии массового параллельного секвенирования) и способны доставлять информацию о последовательности нуклеиновых кислот всего генома, экзома, транскриптома (всех транскрибированных последовательностей генома) или метилома (всех метилированных последовательностей генома) в очень короткие периоды времени, например, в течение 1-2 недель, например, в течение 1-7 дней или в течение менее чем 24 часов, и позволяют, в принципе, подходы к секвенированию отдельных клеток. Множество NGS платформ, которые коммерчески доступны или которые упомянуты в литературе, могут использоваться в контексте настоящего описания, например, такие, которые описаны подробно в WO 2012/159643.
В некоторых вариантах осуществления пептид, описанный в настоящем изобретении, может содержать, но не ограничен ими, приблизительно 5, приблизительно 6, приблизительно 7, приблизительно 8, приблизительно 9, приблизительно 10, приблизительно 11, приблизительно 12, приблизительно 13, приблизительно 14, приблизительно 15, приблизительно 16, приблизительно 17, приблизительно 18, приблизительно 19, приблизительно 20, приблизительно 21, приблизительно 22, приблизительно 23, приблизительно 24, приблизительно 25, приблизительно 26, приблизительно 27, приблизительно 28, приблизительно 29, приблизительно 30, приблизительно 31, приблизительно 32, приблизительно 33, приблизительно 34, приблизительно 35, приблизительно 36, приблизительно 37, приблизительно 38, приблизительно 39, приблизительно 40, приблизительно 41, приблизительно 42, приблизительно 43, приблизительно 44, приблизительно 45, приблизительно 46, приблизительно 47, приблизительно 48, приблизительно 49, приблизительно 50, приблизительно 60, приблизительно 70, приблизительно 80, приблизительно 90, приблизительно 100, приблизительно 110, приблизительно 120, приблизительно 150, приблизительно 200, приблизительно 300, приблизительно 350, приблизительно 400, приблизительно 450, приблизительно 500, приблизительно 600, приблизительно 700, приблизительно 800, приблизительно 900, приблизительно 1000, приблизительно 1500, приблизительно 2000, приблизительно 2500, приблизительно 3000, приблизительно 4000, приблизительно 5000, приблизительно 7500, приблизительно 10000 аминокислот или более аминокислотный остаток, и любой диапазон, производный в нем. В конкретных вариантах осуществления, неоантигенная пептидная молекула равна или менее чем 100 аминокислот.
В некоторых вариантах осуществления пептиды могут быть длиной от приблизительно 8 и до приблизительно 50 аминокислотных остатков, или от приблизительно 8 и до приблизительно 30, от приблизительно 8 и до приблизительно 20, от приблизительно 8 и до приблизительно 18, от приблизительно 8 и до приблизительно 15, или от приблизительно 8 и до приблизительно 12 аминокислотных остатков в длину. В некоторых вариантах осуществления, пептиды могут быть от приблизительно 8 и до приблизительно 500 аминокислотных остатков в длину, или от приблизительно 8 и до приблизительно 450, от приблизительно 8 и до приблизительно 400, от приблизительно 8 и до приблизительно 350, от приблизительно 8 и до приблизительно 300, от приблизительно 8 и до приблизительно 250, от приблизительно 8 и до приблизительно 200, от приблизительно 8 и до приблизительно 150, от приблизительно 8 и до приблизительно 100, от приблизительно 8 и до приблизительно 50, или от приблизительно 8 и до приблизительно 30 аминокислотных остатков в длину.
В некоторых вариантах осуществления, пептиды могут быть по меньшей мере 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50 или более аминокислотных остатков в длину. В некоторых вариантах осуществления, пептиды могут быть по меньшей мере 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 55, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500 или более аминокислотных остатков в длину. В некоторых вариантах осуществления, пептиды могут быть самое большее 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50 или менее аминокислотных остатков в длину. В некоторых вариантах осуществления, пептиды могут быть самое большее 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 55, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500 или менее аминокислотных остатков в длину.
В некоторых вариантах осуществления, пептиды имеют общую длину по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24, по меньшей мере 25, по меньшей мере 26, по меньшей мере 27, по меньшей мере 28, по меньшей мере 29, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90, по меньшей мере 100, по меньшей мере 150, по меньшей мере 200, по меньшей мере 250, по меньшей мере 300, по меньшей мере 350, по меньшей мере 400, по меньшей мере 450, или, по меньшей мере 500 аминокислот.
В некоторых вариантах осуществления, пептиды имеют общую длину самое большее 8, самое большее 9, самое большее 10, самое большее 11, самое большее 12, самое большее 13, самое большее 14, самое большее 15, самое большее 16, самое большее 17, самое большее 18, самое большее 19, самое большее 20, самое большее 21, самое большее 22, самое большее 23, самое большее 24, самое большее 25, самое большее 26, самое большее 27, самое большее 28, самое большее 29, самое большее 30, самое большее 40, самое большее 50, самое большее 60, самое большее 70, самое большее 80, самое большее 90, самое большее 100, самое большее 150, самое большее 200, самое большее 250, самое большее 300, самое большее 350, самое большее 400, самое большее 450, или самое большее 500 аминокислот.
Более длинный пептид может быть сконструирован несколькими путями. В некоторых вариантах осуществления, когда HLA-связывающие пептиды спрогнозированы или известны, более длинный пептид содержит (1) отдельные связывающие пептиды с удлинениями 2-5 аминокислот в направлении N- и C-конца каждого соответствующего генного продукта; или (2) конкатенацию некоторых или всех связывающих пептидов с удлиненными последовательностями для каждого. В других вариантах осуществления, когда секвенирование показывает длинную (>10 остатков) неоэпитопную последовательность, присутствующую в опухоли (например, из-за сдвига рамки, сквозного прохождения или включения интрона, которые дают новую пептидную последовательность), более длинный пептид может состоять из целых участков новых опухолеспецифических аминокислот в виде либо одного более длинного пептида, либо нескольких перекрывающихся более длинных пептидов. В некоторых вариантах осуществления, применение более длинного пептида предположительно позволяет эндогенный процессинг клетками пациента, и может привести к более эффективному презентированию антигена и вызову ответов Т-клетки. В некоторых вариантах осуществления, могут использоваться два или несколько пептидов, где пептиды перекрываются и обложены длинными неоантигенными пептидами.
В некоторых вариантах осуществления, пептиды могут иметь значение pI от приблизительно 0,5 до приблизительно 12, от приблизительно 2 до приблизительно 10, или от приблизительно 4 до приблизительно 8. В некоторых вариантах осуществления, пептиды могут иметь значение pI, по меньшей мере 4,5, 5, 5,5, 6, 6,5, 7, 7,5 или более. В некоторых вариантах осуществления, пептиды могут иметь значение pI самое большее 4,5, 5, 5,5, 6, 6,5, 7, 7,5 или менее.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может быть в растворе, лиофилизиованным или может иметь кристаллическую форму. В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может быть получен синтетически, методом рекомбинантной ДНК или химическим синтезом, или может быть выделен из природных источников, таких как нативные опухоли или патогенные организмы. Неоэпитопы могут быть синтезированы по отдельности или объединены прямо или косвенно в пептид. Хотя пептид, описанный в настоящем изобретении, может по существу не содержать другие существующие в природе белки клеток-хозяев и их фрагменты, в некоторых вариантах осуществления, пептид может быть синтетически конъюгирован для соединения с нативными фрагментами или частицами.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может быть получены множеством путей. В некоторых вариантах осуществления, пептиды могут быть синтезированы в растворе или на твердой подложке согласно обычным методикам. Разные автоматические синтезаторы коммерчески доступны и могут использоваться согласно известным протоколам. См., например, Stewart & Young, Solid Phase Peptide Synthesis, 2d. Ed., Pierce Chemical Co., 1984. Кроме того, отдельные пептиды могут быть объединены с применением химического лигирования с получением больших пептидов, которые все еще входят в объем настоящего описания.
Альтернативно, технология рекомбинантной ДНК может использоваться, где нуклеотидная последовательность, которая кодирует пептид, вставленный в вектор экспрессии, трансформирована или трансфицирована в подходящие клетки-хозяева и культивирована в условиях, подходящих для экспрессии. Эти методики обычно известны в данной области техники, как описано, в общем, у Sambrook et al., Molecular Cloning, Laboratory Manual, Cold Spring Harbor Press, Cold Spring Harbor, N.Y. (1989). Таким образом, рекомбинантные пептиды, которые содержат один или более неоантигенных пептидов, описанных в настоящем изобретении, могут использоваться для презентирования подходящего эпитопа Т-клетки.
В некоторых вариантах осуществления, пептид кодируется геном с точечной мутацией, возникающей при аминокислотном замещении нативного пептида. В некоторых вариантах осуществления, пептид кодируется геном с точечной мутацией, возникающей при мутации со сдвигом рамки. Сдвиг рамки происходит, когда мутация разрывает нормальную фазу периодичности кодона гена (также известную как “рамка считывания”), что вызывает трансляцию ненативной белковой последовательности. Разные мутации в гене могут достигать одинаковых измененных рамок считывания. В некоторых вариантах осуществления, пептид кодируется геном с мутацией, дающей слитый полипептид, делецию внутри рамки считывания, вставку, экспрессию эндогенных ретровирусных полипептидов и опухолеспецифическую сверхэкспрессию полипептидов. В некоторых вариантах осуществления, пептид кодируется слиянием первого гена со вторым геном. В некоторых вариантах осуществления, пептид кодируется слиянием внутри рамки считывания первого гена со вторым геном. В некоторых вариантах осуществления, пептид кодируется слияние первого гена с экзоном сплайс-варианта первого гена. В некоторых вариантах осуществления, пептид кодируется слиянием первого гена с криптическим экзоном первого гена. В некоторых вариантах осуществления, пептид кодируется слиянием первого гена со вторым геном, где пептид содержит аминокислотную последовательность, кодированную последовательностью вне рамки считывания, полученную при слиянии.
В некоторых аспектах, настоящее описание относится к композиции, содержащей по меньшей мере два или более двух пептидов. В некоторых вариантах осуществления, композиция, описанная в настоящем изобретении, содержит по меньшей мере два отдельных пептида. В некоторых вариантах осуществления, композиция, описанная в настоящем изобретении, содержит первый пептид, содержащий первый неоэпитоп, и второй пептид, содержащий второй неоэпитоп. В некоторых вариантах осуществления, первый и второй пептиды получают из одного и того же белка. По меньшей мере два отдельных пептида могут варьировать по длине, аминокислотной последовательности или обоих. Пептиды могут быть получены из любого белка, у которого известна или найдена опухолеспецифическая мутация. В некоторых вариантах осуществления, композиция, описанная в настоящем изобретении, содержит первый пептид, содержащий первый неоэпитоп белка, и второй пептид, содержащий второй неоэпитоп того же белка, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию. В некоторых вариантах осуществления, композиция, описанная в настоящем изобретении, содержит первый пептид, содержащий первый неоэпитоп первой области белка, и второй пептид, содержащий второй неоэпитоп второй области того же белка, где первая область содержит по меньшей мере одну аминокислоту второй области, где первый пептид отличается от второго пептида и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию. В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми. В некоторых вариантах осуществления, мутация выбрана из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутация «сдвига рамки», мутация сквозного прочитывания, мутация слияния генов и любой их комбинации.
В некоторых вариантах осуществления, пептид может быть получен из белка замечающей мутацией, например, KRAS G12C, G12D, G12V, Q61H или Q61L мутацией, или NRAS Q61K или Q61R мутацией, или BTK C481S мутацией, или EGFR S492R или EGFR T490M мутацией. Замещение может быть расположено в любом месте по длине пептида. Например, оно может быть расположено в N-концевой трети пептид, центральной трети пептида или C-концевой трети пептида. В другом варианте осуществления, замещенный остаток расположен в 2-5 остатках от N-конца или 2-5 остатках от C-конца. Пептиды так же могут быть получены из опухолеспецифических инсерционных мутаций, где пептид содержит один или более, или все вставленные остатки.
В некоторых вариантах осуществления, первый пептид содержит по меньшей мере одну дополнительную мутацию. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации не является мутацией в первом неоэпитопе. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации является мутацией в первом неоэпитопе. В некоторых вариантах осуществления, второй пептид содержит по меньшей мере одну дополнительную мутацию. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации не является мутацией во втором неоэпитопе. В некоторых вариантах осуществления, одна или более из по меньшей мере одной дополнительной мутации является мутацией во втором неоэпитопе.
В некоторых аспектах, настоящее описание относится к композиции, содержащей один полипептид, содержащий первый пептид и второй пептид, или один полинуклеотид, кодирующий первый пептид и второй пептид. В некоторых вариантах осуществления, представленная в настоящем изобретении композиция содержит один или более дополнительных пептидов, где один или более дополнительных пептидов содержат третий неоэпитоп. В некоторых вариантах осуществления, первый пептид и второй пептид кодированы последовательностью, транскрибированной из одного и того же сайта начала транскрипции. В некоторых вариантах осуществления, первый пептид кодируется последовательностью, транскрибированной из первого сайта начала транскрипции, и второй пептид кодируется последовательностью, транскрибированной из второго сайта начала транскрипции. В некоторых вариантах осуществления, полипептид имеет длину по меньшей мере 26; 27; 28; 29; 30; 40; 50; 60; 70; 80; 90; 100; 150; 200; 250; 300; 350; 400; 450; 500; 600; 700; 800; 900; 1000; 1500; 2000; 2500; 3000; 4000; 5000; 7500; или 10000 аминокислот. В некоторых вариантах осуществления, полипептид содержит первую последовательность с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей последовательностью дикого типа; и вторую последовательность с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления, полипептид содержит первую последовательность из по меньшей мере 8 или 9 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей последовательностью дикого типа; и вторую последовательность из по меньшей мере 16 или 17 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей последовательностью дикого типа.
В некоторых вариантах осуществления, второй пептид длиннее, чем первый пептид. В некоторых вариантах осуществления, первый пептид длиннее, чем второй пептид. В некоторых вариантах осуществления, первый пептид имеет длину по меньшей мере 9; 10; 11; 12; 13; 14; 15; 16; 17; 18; 19; 20; 21; 22; 23; 24; 25; 26; 27; 28; 29; 30; 40; 50; 60; 70; 80; 90; 100; 150; 200; 250; 300; 350; 400; 450; 500; 600; 700; 800; 900; 1000; 1500; 2000; 2500; 3000; 4000; 5000; 7500; или 10000 аминокислот. В некоторых вариантах осуществления, второй пептид имеет длину по меньшей мере 17; 18; 19; 20; 21; 22; 23; 24; 25; 26; 27; 28; 29; 30; 40; 50; 60; 70; 80; 90; 100; 150; 200; 250; 300; 350; 400; 450; 500; 600; 700; 800; 900; 1000; 1500; 2000; 2500; 3000; 4000; 5000; 7500; или 10000 аминокислот. В некоторых вариантах осуществления, первый пептид содержит последовательность из по меньшей мере 9 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления, второй пептид содержит последовательность из по меньшей мере 17 непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности с соответствующей последовательностью дикого типа.
В некоторых вариантах осуществления, первый пептид, второй пептид или оба содержат по меньшей мере одну фланкирующую последовательность, где по меньшей мере одна фланкирующая последовательность расположена выше или ниже неоэпитопа. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая последовательность имеет по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая последовательность содержит последовательность не дикого типа. В некоторых вариантах осуществления, по меньшей мере одой фланкирующей последовательностью является N-концевая фланкирующая последовательность. В некоторых вариантах осуществления, по меньшей мере одной фланкирующей последовательностью является C-концевая фланкирующая последовательность. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая последовательность первого пептида имеет по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичность последовательности с по меньшей мере одной фланкирующей последовательностью второго пептида. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая область первого пептида отличается от, по меньшей мере одной фланкирующей области второго пептида. В некоторых вариантах осуществления, по меньшей мере один фланкирующий остаток содержит мутацию.
В некоторых вариантах осуществления, неоантигенный пептид с фланкирующими последовательностями содержит полипептид, который может быть представлен формулой (N-конец Xaa)N-(XaaBTK)P-(Xaa-С-конец)C, где (XaaBTK)P является мутантной BTK пептидной последовательностью, содержащей по меньшей мере 8 непрерывных аминокислот мутантного BTK белка, P является целым числом более 7; N равен (i) 0 или (ii) целому числу более 2; (N-конец Xaa)N является любой аминокислотной последовательностью, гетерологической к мутантному белку; C равно (i) 0 или (ii) целому числу более 2; (Xaa-С-конец)C является любой аминокислотной последовательностью, гетерологической к мутантному BTK белку; и оба N и C не равны 0.
В некоторых вариантах осуществления, неоантигенный пептид с фланкирующими последовательностями содержит полипептид, который может быть представлен формулой (N-конец Xaa)N-(XaaEGFR)P-(Xaa-С-конец)C, где (XaaEGFR)P является мутантной EGFR пептидной последовательностью, содержащей по меньшей мере 8 непрерывных аминокислот мутантного EGFR белка, P является целым числом более 7; N равно (i) 0 или (ii) целому числу более 2; (N-конец Xaa)N является любой аминокислотной последовательностью, гетерологической к мутантному EGFR белку; C равно (i) 0 или (ii) целому числу более 2; (Xaa-С-конец)C является любой аминокислотной последовательностью гетерологической к мутантному EGFR белку; и оба N и C не равны 0.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере одну мутантную аминокислоту. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или несколько мутантных аминокислот. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше по меньшей мере одной мутантной аминокислоты. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже по меньшей мере одной мутантной аминокислоты. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту; по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше по меньшей мере одной мутантной аминокислоты; и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже по меньшей мере одной мутантной аминокислоты.
В некоторых вариантах осуществления, пептид содержит неоантигенную пептидную последовательность, изображенную в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, изображенную в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере одну мутантную аминокислоту (подчеркнутые аминокислоты), изображенную в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более мутантных аминокислот (подчеркнутых аминокислот), изображенных в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоантигенную пептидную последовательность, изображенную в таблицах 34 или 36. В некоторых вариантах осуществления, пептид содержит неоэпитопную BTK последовательность, изображенную в таблицах 34 или 36. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере одну мутантную аминокислоту, изображенную в таблицах 34 или 36. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более мутантных амино. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) и по меньшей мере одну выделенную жирным шрифтом аминокислоту, изображенную в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот, изображенных в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше, по меньшей мере одной мутантной аминокислоты, изображенной в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот, ниже, по меньшей мере одной мутантной аминокислоты, изображенной в таблицах 1 или 2. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше, по меньшей мере одной мутантной аминокислоты, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже, по меньшей мере одной мутантной аминокислоты, изображенных в таблицах 1 или 2.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже, по меньшей мере одной мутантной аминокислоты, изображенной в таблицах 34 или 36. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше, по меньшей мере одной мутантной аминокислоты, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже, по меньшей мере одной мутантной аминокислоты, изображенных в таблицах 34 или 36.
В некоторых вариантах осуществления, пептид содержит неоантигенную пептидную последовательность, изображенную в таблицах 40A-40D, 32 или 3A-3D. В некоторых вариантах осуществления, пептид содержит неоэпитопную EGFR последовательность, изображенную в таблицах 40A-40D. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере одну мутантную аминокислоту, изображенную в таблицах 40A-40D. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более мутантных аминокислот (например, подчеркнутых аминокислот в любой из таблиц 40A-40D). В некоторых вариантах осуществления, EGFR пептид содержит неоэпитопную последовательность, содержащую по меньшей мере одну мутантную аминокислоту, изображенную жирным шрифтом в таблице 40D. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот, изображенных в таблицах 40A-40D. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (например, подчеркнутую аминокислоту в таблице 40C) и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше, по меньшей мере одной мутантной аминокислоты, изображенной в таблицах 40A-40D. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже, по меньшей мере одной мутантной аминокислоты, изображенной в таблицах 40A-40D. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот выше, по меньшей мере одной мутантной аминокислоты, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более не-мутантных аминокислот ниже, по меньшей мере одной мутантной аминокислоты, изображенных в таблицах 40A-40D.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) изображенную в таблицах 1 или 2 и последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту) изображенную в таблицах 1 или 2 и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 1 или 2, последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 1 или 2 и последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 1 или 2 и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 1 или 2, последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, BTK пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 34 или 36 и последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, изображенную в таблицах 34 или 36, и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, изображенную в таблицах 34 или 36, последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 34 или 36, и последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, изображенную в таблицах 34 или 36 и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 34 или 36, последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
Типовые неоантигенные пептиды, соответствующие C481S мутации, представлены в таблице 34. В таблице также представлен список HLA аллелей, кодированных белками, продукты которых могут связываться с пептидами. В некоторых вариантах осуществления, пептидом содержащим C481S мутацию, является: MIKEGSMSEDEFIEEAKVMMNLSHEKLVQLYGVCTKQRPIFIITEYMANGSLLNYLREMRHRFQTQQLLEMCKDVCEAMEYLESKQFLHRDLAARNCLVND (SEQ ID NO: 3089). В некоторых вариантах осуществления, пептид, содержащий BTK мутацию, содержит неоэпитопную последовательность ANGSLLNY (SEQ ID NO: 3090). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность ANGSLLNYL (SEQ ID NO: 3091). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность ANGSLLNYLR (SEQ ID NO: 3092). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность EYMANGSL (SEQ ID NO: 3093). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность EYMANGSLLN (SEQ ID NO: 3094). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность EYMANGSLLNY (SEQ ID NO: 3095). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность GSLLNYLR (SEQ ID NO: 3096). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность GSLLNYLREM (SEQ ID NO: 3097). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность ITEYMANGS (SEQ ID NO: 3098). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность ITEYMANGSL (SEQ ID NO: 3099). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность ITEYMANGSLL (SEQ ID NO: 3100). MANGSLLNYL (SEQ ID NO: 3101). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность MANGSLLNYLR (SEQ ID NO: 3102). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность NGSLLNYL (SEQ ID NO: 3103). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность NGSLLNYL (SEQ ID NO: 3104). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность SLLNYLREMR (SEQ ID NO: 3105). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность TEYMANGSLL (SEQ ID NO: 3106); TEYMANGSLLNY (SEQ ID NO: 3107). В некоторых вариантах осуществления, пептид, содержащий C481S BTK мутацию, содержит неоэпитопную последовательность YMANGSLL (SEQ ID NO: 3108).
В некоторых вариантах осуществления, EGFR пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 40A-40D и последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 40A -40D и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту, изображенную в таблицах 40A-40D, последовательность выше, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже, по меньшей мере одной мутантной аминокислоты с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 40A-40D и последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 40A-40D и последовательность ниже, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа. В некоторых вариантах осуществления, пептид содержит неоэпитопную последовательность, полученную из белка, содержащего по меньшей мере одну мутантную аминокислоту (подчеркнутую аминокислоту), изображенную в таблицах 40A-40D, последовательность выше, по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа, и последовательность ниже по меньшей мере одной мутантной аминокислоты содержащей по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более непрерывных аминокислот с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к соответствующей последовательности дикого типа.
В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит последовательность GICLTSTVQLIMQLMPFGCLLDY (SEQ ID NO: 3109). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность VQLIMQLMPF (SEQ ID NO: 3110). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность STVQLIMQLM (SEQ ID NO: 3111). В некоторых вариантах осуществления, мутантный EGFR пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность QLIMQLMPF (SEQ ID NO: 3112). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность MQLMPFGCLL (SEQ ID NO: 3113). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность LIMQLMPF (SEQ ID NO: 3114). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность LTSTVQLIM (SEQ ID NO: 3115). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность STVQLIMQL (SEQ ID NO: 3116). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность TSTVQLIMQL (SEQ ID NO: 3117). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность TVQLIMQL (SEQ ID NO: 3118). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность TVQLIMQLM (SEQ ID NO: 3119). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность VQLIMQLM (SEQ ID NO: 3120). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность CLTSTVQLIM (SEQ ID NO: 3121). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность IMQLMPFGC (SEQ ID NO: 3122). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность IMQLMPFGC (SEQ ID NO: 3123). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность IMQLMPFGCL (SEQ ID NO: 3124). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность LIMQLMPFG (SEQ ID NO: 3125). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность LIMQLMPFGC (SEQ ID NO: 3126). В некоторых вариантах осуществления, пептид, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность QLIMQLMPFG (SEQ ID NO: 3127).
В некоторых вариантах осуществления, пептид, содержащий EGFR, S492R мутацию, содержит последовательность SLNITSLGLRSLKEISDGDVIISGNKNLCYANTINWKKLFGTSGQKTKIIRNRGENSCKATGQVCHALCSPEGCWGPEPRDCVSCRNVSRGRECVDKCNLL (SEQ ID NO: 3128). В некоторых вариантах осуществления, пептид, содержащий EGFR S492R мутацию, содержит неоэпитопную последовательность IIRNRGENSCK (SEQ ID NO: 3129).
В некоторых вариантах осуществления, EGFR неопептид выбран из таблиц 40A-40D.
В некоторых вариантах осуществления, пептид, содержащий делеционную мутацию в EGFR, такую как делеция G в EGFRvIII (внутренняя делеция), MRPSGTAGAALLALLAALCPASRALEEKK:G:NYVVTDHGSCVRACGADSYEMEEDGVRKCKKCEGPCRKVCNGIGIGEFKD (SEQ ID NO: 3130), содержит неоэпитопную последовательность ALEEKKGNYV (SEQ ID NO: 3131).
В некоторых вариантах осуществления, пептид, содержащий мутацию, изображенную в последовательности: LPQPPICTIDVYMIMVKCWMIDADSRPKFRELIIEFSKMARDPQRYLVIQ::LQDKFEHLKMIQQEEIRKLEEEKKQLEGEIIDFYKMKAASEALQTQLSTD (SEQ ID NO: 3132), содержит неоэпитопную последовательность IQLQDKFEHL (SEQ ID NO: 3133). В некоторых вариантах осуществления, пептид, содержащий мутацию, изображенную в последовательности: LPQPPICTIDVYMIMVKCWMIDADSRPKFRELIIEFSKMARDPQRYLVIQ::LQDKFEHLKMIQQEEIRKLEEEKKQLEGEIIDFYKMKAASEALQTQLSTD (SEQ ID NO: 3134), содержит неоэпитопную последовательность QLQDKFEHL (SEQ ID NO: 3135). В некоторых вариантах осуществления, пептид содержащий мутацию, изображенную в последовательности: LPQPPICTIDVYMIMVKCWMIDADSRPKFRELIIEFSKMARDPQRYLVIQ::LQDKFEHLKMIQQEEIRKLEEEKKQLEGEIIDFYKMKAASEALQTQLSTD (SEQ ID NO: 3136), содержит неоэпитопную последовательность QLQDKFEHLK (SEQ ID NO: 3137). В некоторых вариантах осуществления, пептид содержащий мутацию, изображенную в последовательности: LPQPPICTIDVYMIMVKCWMIDADSRPKFRELIIEFSKMARDPQRYLVIQ::LQDKFEHLKMIQQEEIRKLEEEKKQLEGEIIDFYKMKAASEALQTQLSTD (SEQ ID NO: 3138), содержит неоэпитопную последовательность
Модификация пептида
В некоторых вариантах осуществления, настоящее описание включает модифицированные пептиды. Модификация может включать ковалентную химическую модификацию, которая не изменяет первичную аминокислотную последовательность самого антигенного пептида. Модификации могут давать пептиды с желаемыми свойствами, например, продленный период полужизни in vivo, повышенную стабильность, пониженный клиренс, измененную иммуногенность или аллергичность, возможность индуцирования определенных антител, клеточное направление, поглощение антигена, процессинг антигена, HLA аффинность, HLA стабильность или презентирование антигена. В некоторых вариантах осуществления, пептид может содержать одну или более последовательностей, которые улучшают процессинг и презентирование эпитопов APC, например, для создания иммунного ответа.
В некоторых вариантах осуществления, пептид может быть модифицирован с получением желаемых параметров. Например, способность пептидов вызывать активность CTL может быть улучшена связыванием с последовательностью, которая содержит по меньшей мере один эпитоп, который способен вызывать ответ T-хелперной клетки. В некоторых вариантах осуществления, иммуногенные пептиды/T-хелперные конъюгаты связаны молекулой спейсера. В некоторых вариантах осуществления, спейсер содержит относительно маленькие нейтральные молекулы, такие как аминокислоты или миметики аминокислот, которые по существу не заряжены в физиологических условиях. Спейсеры могут быть выбраны из, например, Ala, Gly или других нейтральных спейсеров неполярных аминокислот или нейтральных полярных аминокислот. Должно быть понятно, что необязательно присутствующий спейсер не обязательно состоит из одинаковых остатков и, поэтому, может быть гетеро- или гомо-олигомером. Неоантигенный пептид может быть связан с T-хелперным пептидом прямо или через спейсер, либо на амино, либо на карбокси конце пептида. Амино конец либо неоантигенного пептида, либо T-хелперного пептида может быть ацилирован. Примеры T-хелперных пептидов включают остатки столбнячного токсина 830-843, остатки гриппа 307-319 и остатки циркумспорозоита малярии 382-398 и остатки 378-389.
Пептидные последовательности настоящего описания необязательно могут быть изменены через изменения на уровне ДНК, в частности, мутацией ДНК, кодирующей пептид на заранее выбранных основаниях, так, что создаются кодоны, которые будут транслировать в желаемые аминокислоты.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может сдержать замещения для модификации физического свойства (например, стабильности или растворимости) полученного пептида. Например, пептиды могут быть модифицированы замещением цистеина (C) на α-аминомасляную кислоту (“B”). Благодаря его химической природе, цистеин имеет склонность к образованию дисульфидных мостиков и в достаточной степени изменяет структуру пептида так, чтобы снизить связывающую способность. Замещение C α-аминоаминомасляной кислотой не только облегчает эту проблему, но действительно улучшает связывание и способность к поперечному сшиванию в определенных случаях. Замещение цистеина α-аминомасляной кислотой может происходить на любом остатке неоантигенного пептида, например, в любом якорном или не якорном положениях эпитопа или аналога в пептиде, или на других положениях пептида.
Пептид также может быть модифицирован увеличением или уменьшением аминокислотной последовательности соединения, например, добавлением или делецией аминокислот. Пептиды или аналоги также могут быть модифицированы изменением порядка или композиции определенных остатков. Должно быть понятно специалисту в данной области техники, что определенные аминокислотные остатки, жизненно необходимые для биологической активности, например, находящиеся на критических контактных сайтах, или консервативные остатки, обычно не могут быть изменены без неблагоприятного действия на биологическую активность. Не критические аминокислоты не обязательно ограничены существующими в природе остатками в белках, такими как L-α-аминокислоты, но также могут включать не существующие в природе аминокислоты, такие как D-изомер, β-γ-δ-аминокислоты, а также многие производные L-α-аминокислот.
В некоторых вариантах осуществления, пептид может быть модифицирован с применением ряда пептидов с отдельными аминокислотными замещениями для определения действия электростатического заряда, гидрофобности и т.д. на связывание HLA. Например, ряд положительно заряженных (например, Lys или Arg) или отрицательно заряженных (например, Glu) аминокислотных замещений может быть сделан по длине пептида, раскрывая разные шаблоны чувствительности в отношении разных молекул HLA и Т-клеточных рецепторов. Кроме того, могут использоваться множественные замещения с применением малых, относительной нейтральных групп, таких как Ala, Gly, Pro, или подобных остатков. Замещения могут быть гомо-олигомерами или гетеро-олигомерами. Количество и типы остатков, которые замещены или добавлены, зависят от расстояния, необходимого между существенными точками контакта и определенными искомыми функциональными признаками (например, гидрофобностью и гидрофильностью). Повышенная аффинность связывания для HLA молекул или Т-клеточного рецептора также может быть достигнута такими замещениями, по сравнению с аффинностью исходного пептида. В любом случае, такие замещения должны применять аминокислотные остатки или другие молекулярные фрагменты, выбранные для того, чтобы избежать, например, пространственного и зарядового вмешательства, которые могут разорвать связь. Аминокислотные замещения обычно являются отдельными остатками. Замещения, делеции, вставки или любые их комбинации могут быть объединены с получением конечного пептида.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может содержать аминокислотные миметики или не существующие в природе аминокислотные остатки, например D- или L-нафтилаланин; D- или L-фенилглицин; D- или L-2-тиенеилаланин; D- или L-1, -2, 3-, или 4-пиренеилаланин; D- или L-3 тиенеилаланин; D- или L-(2-пиридинил)аланин; D- или L-(3-пиридинил)аланин; D- или L-(2-пиразинил)аланин; D- или L-(4-изопропил)фенилглицин; D-(трифторметил)фенилглицин; D-(трифторметил)фенилаланин; D-ρ-фторфенилаланин; D- или L-ρ-бифенилфенилаланин; D- или L-ρ-метоксиифенилфенилаланин; D- или L-2-индол(аллил)аланины; и, D- или L-алкилаланины, где алкильная группа может быть замещенным или не замещенным метилом, этилом, пропилом, гексилом, бутилом, пентилом, изопропилом, изобутилом, втор-изотилом, изопентилом; или не кислотные остатки аминокислоты. Ароматические кольца не существующих в природе аминокислот включают, например, тиазолильные, тиофенильные, пиразолильные, бензимидазолильные, нафтильные, фуранильные, пирролильные, пиридильные ароматические кольца. Модифицированные пептиды, которые содержат различные аминокислотные миметики или не существующие в природе аминокислотные остатки, могут иметь повышенную стабильность in vivo. Такие пептиды также могут иметь улучшенный срок годности или производственные свойства.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может быть модифицирован концевым-NH2 ацилированием, например, алканоилом (C1-C20), или тиогликолильным цетилированием, концевым-карбоксильным амидированием, например, аммиаком, метиламином и т.д. В некоторых вариантах осуществления, эти модификации могут обеспечить сайты для связывания с подложкой или другой молекулой. В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может содержать модификации, такие как, но не ограниченные ими, гликозилирование, окисление боковой цепи, биотинилирование, фосфорилирование, добавление поверхностно-активного вещества, например, жира, или могут быть химически модифицированы, например, ацетилированием и т.д. Более того, связи в пептиде могут отличаться от пептидных связей, например, являются ковалентными связями, сложными или простыми эфирными связями, дисульфидными связями, водородными связями, ионными связями и ит.д.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может содержать носители, которые хорошо известны в данной области техники, например, тиреоглобулин, альбумины, такие как сывороточный альбумин человека, столбнячный анатоксин, полиаминокислотные остатки, такие как поли L-лизин и поли L-глутаминовая кислота, белки вируса гриппа, коровый белок вируса гепатита В и подобные.
Пептиды могут быть дополнительно модифицированы так, чтобы содержать дополнительные химические группы, обычно не являющиеся частью белка. Такие производные группы могут улучшать растворимость, биологическую полужизнь, абсорбцию белка или аффинность связывания. Группы также могут снижать или исключать любые желаемые побочные эффекты пептидов и подобных. Обзор таких групп может быть найден в Remington’s Pharmaceutical Sciences, 20th ed., Mack Publishing Co., Easton, PA (2000). Например, неоантигенные пептиды, имеющие желаемую активность, могут быть модифицированы при необходимости с получением определенных желаемых признаков, например улучшенных фармакологических характеристик, при повышении или по меньшей мере сохранении по существу всей биологической активности не модифицированного пептида для связывания желаемой молекулы HLA и активации соответствующей Т-клетки. Например, пептид может быть объектом для различных изменений, таких как замещения, консервативные или не консервативные, где такие изменения могут давать определенные преимущества в их применении, такие как улучшенное связывание с HLA. Такие консервативные замещения могут охватывать замещение аминокислотного остатка другим аминокислотным остатком, который биологические и/или химически аналогичный, например, одного гидрофобного остатка на другой, или одного полярного остатка на другой. Действие отдельных аминокислотных замещений также может быть опробовано с применением D-аминокислот. Такие модификации могут быть проведены с применением хорошо известных методов пептидного синтеза, как описано в, например, Merrifield, Science 232:341-347 (1986), Barany & Merrifield, Peptides, Gross & Meienhofer, eds. (N.Y., Academic Press), pp. 1-284 (1979); и Stewart & Young, Solid Phase Peptide Synthesis, (Rockford, III., Pierce), 2d Ed. (1984).
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может быть конъюгирован с большими, медленно метаболизируемыми макромолекулами, такими как белки; полисахариды, такие как сефароза, агароза, целлюлоза, целлюлозные сферы; полимерные аминокислоты, такие как полиглутаминовая кислота, полилизин; coполимер аминокислоты; частицы инактивированного вируса; инактивированные бактериальные токсины, такие как токсоидные препараты дифтерии, столбняка, холеры, молекулы лейкотоксина; инактивированные бактерии; и дендритные клетки.
Изменения пептида могут включать, но не ограничены ими, конъюгацию с белком-носителем, конъюгацию с лигандом, конъюгацию с антителом, PEGилирование, полисиалилирование, HESилирование, рекомбинантные PEG миметики, Fc слияние, слияние с альбумином, присоединением наночастицы, инкапсулирование наночастиц, слияние с холестерином, слияние с железом, ацилирование, амидирование, окисление боковых цепей, фосфорилирование, биотинилирование, добавление поверхностно-активного вещества, добавление аминокислотных миметиков или добавление не существующих в природе аминокислот.
Гликозилирование может влиять на физические свойства белков и также может быть важным для стабильности белка, секреции и субклеточной локализации. Подходящее гликозилирование может быть важным для биологической активностью. Фактически, некоторые гены их эукариотических организмов, при экспрессировании в бактерии (например, E. coli), которая не имеет клеточных процессов для гликозилирования белков, дают белки, которые восстанавливаются с незначительной или отсутствием активности благодаря отсутствию у них гликозилирования. Добавление сайтов гликозилирования может сопровождаться изменением аминокислотной последовательности. Изменение пептида или белка может быть проведено, например, добавлением или замещением одним или несколькими сериновыми или треониновыми остатками (для O-связанных сайтов гликозилирования) или аспарагиновыми остатками (для N-связанных сайтов гликозилирования). Структура N-связанных и O-связанных олигосахаридов и сахарных остатков, найденных в каждом типе, может отличаться. Одним типом сахара, к4оторый обычно находят на обоих, является N-ацетилнейраминовой кислотой (далее названной сиаловая кислота). Сиаловая кислота обычно является концевым остатком обоих, N-связанных и O-связанных олигосахаридов и, благодаря ее отрицательному заряду, может придавать кислотные свойства гликопротеину. Варианты осуществления настоящего описания содержат создание и применение N-гликозилированных вариантов. Удаление углеводов может быть проведено химически или ферментативно, или замещением кодонов, кодирующих аминокислотные остатки, которые гликозилированы. Методики химического дегликозилирования известны, и ферментативное расщепление углеводных групп на полипептидах может быть достигнуто с применением множества эндо- и экзогликозидаз.
Дополнительные подходящие компоненты и молекулы для конъюгирования включают, например, молекулы для направления на лимфатическую систему, тироглобулин; альбумины, такие как сывороточный альбумин человека (HAS); токсоидный препарат столбняка; токсоидный препарат дифтерии; полиаминокислоты, такие как поли(D-лизин:D-глутаминовая кислота); VP6 полипептиды ротавирусов; гемагглютинин вируса гриппа, нуклеопротеин вируса гриппа; гемоцианин лимфы улитки (KLH); и коровый белок вируса гепатита B и поверхностный антиген; или любая комбинация вышеперечисленных.
Другим типом модификации является конъюгирование (например, связывание) одного или нескольких дополнительных компонентов или молекул на N- и/или C-концах полипептидной последовательности, такой как другой белок (например, белок, имеющий аминокислотную последовательность, гетерологичную белку субъекта) или молекула носителя. Таким образом, типовые полипептидные последовательности могут быть представлены в виде конъюгатов с другим компонентом или молекулой. В некоторых вариантах осуществления, слияние альбумина с пептидом или белка настоящего описания может, например, быть достигнуто генетической манипуляцией, такой как ДНК кодирование для HSA, или его фрагмента, соединенного с ДНК, кодирующей один или более полипептидных последовательностей. Затем подходящий хозяин может быть трансформирован или трансфицирован слитыми нуклеотидными последовательностями в форме, например, подходящей плазмиды так, чтобы экспрессировать полипептид. Экспрессия может быть проведена in vitro из, например, прокариотических или эукариотических клеток, или in vivo из, например, трансгенного организма. В некоторых вариантах осуществления настоящего описания, экспрессию слитого белка проводят в клеточной линии млекопитающих, клеточных линиях CHO. Более того, сам альбумин может быть модифицирован для продления его периода полужизни в кровотоке. Слияние модифицированного альбумина с одним или несколькими полипептидами может быть достигнуто методами генетической манипуляции, описанными выше, или химическим конъюгированием; полученные слитые молекулы имеют период полужизни, превышающий таковой для слияний не модифицированного альбумина (см., например, WO2011/051489). Несколько стратегия связывания альбумина было разработано в качестве альтернатив прямого слияния, включая связывание альбумин через конъюгированную цепь жирной кислоты (ацилирование). Так как сывороточный альбумин является транспортным белком для жирных кислот, эти природные лиганды с активностью связывания альбумина используют для продления периода полужизни терапевтических агентов на основе малых белков.
Дополнительные кандидатные компоненты и молекулы для конъюгации включают такие, которые подходят для выделения или очистки. Не ограничивающие примеры включают связывающие молекулы, такие как биотин (биотин-авидиновые специфические связывающие пары), антитело, рецептор, лиганд, лектин или молекулы, которые содержат твердую подложку, включая, например, пластиковые или полистирольные сферы, пластины или шарики, магнитные шарики, тестовые полоски и мембраны. Способы очистки, такие как катионообменная хроматография, могут использоваться для разделения конъюгатов через разницу зарядов, которая эффективно разделяет конъюгаты на их разные молекулярные массы. Содержимое фракций, полученных катионообменной хроматографией, может быть идентифицировано молекулярной массой с применением обычных способов, например, масс спектроскопии, SDS-PAGE или других известных способов разделения молекулярных веществ через молекулярную массу.
В некоторых вариантах осуществления, амино- или карбоксильный конец пептидной или белковой последовательности настоящего описания может быть конденсирован с Fc областью иммуноглобулина (например, Fc человека) с получением слитого конъюгата (или слитой молекулы). Было показано, что Fc слитые конъюгаты повышают системный период полужизни биофармацевтических агентов, и поэтому биофармацевтический агент может потребовать менее частого введения. Fc связывается с неонатальным Fc рецептором (FcRn) в эндотелиальных клетках, которые выстилают кровеносные сосуды, и, при связывании, Fc слитые молекулы защищены от разрушения и повторно выделяются в кровоток, дольше сохраняя молекулу в кровотоке. Полагают, что такое Fc связывание является механизмом, посредством которого эндогенный IgG сохраняет свой долгий период полужизни в плазме. Более современная технология Fc-слияния связывает одну копию биофармацевтического агента с Fc областью антитела для оптимизации фармакокинетических и фармакодинамических свойств биофармацевтического агента по сравнению с традиционными Fc-слитыми конъюгатами.
В настоящем описании рассматривается использование других модификаций, известных в настоящее время или тех, которые будут разработаны в будущем, пептидов для улучшения одного или нескольких свойств. Один из таких способов пролонгирования периода полужизни в кровотоке, повышения стабильности, снижения клиренса или изменения иммуногенности пептида настоящего описания включает модификацию пептидных последовательностей хезилированием, в котором используют производные гидроксиэтилового крахмала, связанные с другими молекулами для модификации характеристик молекулы. Разные аспекты хезилирования описаны в, например, заявках на патент США №№ 2007/0134197 и 2006/0258607.
Пептидная стабильность может быть оценена множеством путей. Например, пептидазы и разные биологические среды, такие как плазма и сыворотка человека, используют для тестирования стабильности. См., например, Verhoef, et al., Eur. J. Drug Metab. Pharmacokinetics 11:291 (1986). Период полужизни пептидов, описанных в настоящем изобретении, для удобства определяют с применением анализа 25% сыворотки человека (об./об.). Протокол следующий: объединенную сыворотку человека (тип AB, не инактивированная теплом) разрушают центрифугированием до применения. Затем сыворотку разводят до 25% RPMI-1640 или другой подходящей средой для культивирования тканей. В определенные заранее интервалы времени, небольшое количество реакционного раствора удаляют и добавляют либо в 6% водную трихлоруксусную кислоту (TCA), либо этанол. Мутный реакционный образец охлаждают (4°C) в течение 15 минут и затем центрифугируют до получения лепешки осажденных сывороточных белков. Присутствие пептидов затем определяют ВЭЖХ с обращенной фазой с применением специфических к стабильности условий хроматографии.
Проблемы, связанные с коротким периодом полужизни в плазме или подверженностью протеазному разложению, могут быть преодолены разными модификациями, включая конъюгирование или связывание пептидной или белковой последовательности с любым из множества не белковых полимеров, например, полиэтиленгликолем (ПЭГ), полипропиленгликолем или полиоксиалкиленами (см., например, обычно через связывание группы, ковалентно связанной с обеими белками и не белковым полимером, например, ПЭГ). Было показано, что такие ПЭГ конъюгированные биомолекулы обладают клинически полезными свойствами, включая лучшую физическую и термическую стабильность, защиту от предрасположенности к ферментативному разложению, повышенную растворимость, более долгий in vivo период полужизни в кровотоке и пониженный клиренс, пониженную иммуногенность и антигенность, и пониженную токсичность.
PEG, подходящие для конъюгирования с полипептидной или белковой последовательностью, обычно растворимы в воде при комнатной температуре, и имеют общую формулу R-(O-CH2-CH2)n-O-R, где R является водородом или защитной группой, такой как алкильная или алканоильная группа, и где n является целым числом от 1 до 1000. Если R является защитной группой, он обычно имеет от 1 до 8 атомов углерода. ПЭГ, конъюгированный с полипептидной последовательностью, может быть линейным или разветвленным. Разветвленные ПЭГ производные, “звездобразные-ПЭГ” и многоплечие ПЭГ рассматриваются настоящим описанием. Настоящее описание также рассматривает композиции конъюгатов, где ПЭГ имеет различные значения n, и такие разные ПЭГ присутствуют в определенных долях. Например, некоторые композиции включают смесь конъюгатов, где n=1, 2, 3 и 4. В некоторых композициях, доля конъюгатов, где n=1, составляет 18-25%, доля конъюгатов, где n=2, составляет 50-66%, доля конъюгатов, где n=3 составляет 12-16%, и доля конъюгатов, где n=4 составляет вплоть до 5%. Такие композиции могут быть получены в условиях реакции и способами очистки, известными в данной области техники. Например, катионообменная хроматография может использоваться для разделения конъюгатов, и затем идентифицируют долю, которая содержит конъюгат имеющий, например, желаемое количество присоединенных ПЭГ, очищают от немодифицированных белковых последовательностей и от конъюгатов, имеющих другое количество присоединенных ПЭГ.
PEG может быть связан с пептидом или белком настоящего описания через концевую реакционноспособную группу (“спейсер”). Спейсером является, например, концевая реакционноспособная группа, которая опосредует связь между свободными амино или карбоксильными группами одной или более полипептидных последовательностей и ПЭГ. ПЭГ, имеющий спейсер, который может быть связан со свободной аминогруппой, включает N-гидроксисукцинилимид ПЭГ, который может быть получен активацией сложного эфира янтарной кислоты ПЭГ с N-гидроксисукцинилмимдом. Другим активированным ПЭГ, который может быть связан со свободной аминогруппой, является 2,4-бис(O-метоксиполиэтиленгликоль)-6-хлор-s-триащзин, который может быть получен взаимодействием ПЭГ PEG монометилового эфира с циануровым хлоридом. Активированный ПЭГ, который связан сл свободной карбоксильной группой, включает полиоксиэтилендиамин.
Конъюгирование одной или более пептидных или белковых последовательностей настоящего описания с ПЭГ, имеющим спейсер, может проводиться разными обычными способами. Например, реакция конъюгирования может проводиться в растворе при pH от 5 до 10, при температуре от 4°C до комнатной температуры, в течение от 30 минут до 20 часов, с применением солярного отношения реагента к пептиду/белку от 4:1 до 30:1. Условия реакции могут быть выбраны для направления реакции в сторону производства преимущественно желаемой степени замещения. В общем, низкая температура, низкий pH (например, pH=5) и короткое время реакции имеет тенденцию к снижению количества присоединенных ПЭГ, в то время как высокая температура, pH от нейтрального до высокого (например, pH>7) и более длительное время реакции имеют тенденцию к повышению количества присоединенных ПЭГ. Разные средства, известные в данной области техники, могут использоваться для остановки реакции. В некоторых вариантах осуществления, реакцию останавливают подкислением реакционной смеси и ее замораживанием при, например, -20°C.
Настоящее описание также рассматривает применение ПЭГ миметиков. Были разработаны рекомбинантные ПЭГ миметики, которые сохраняют признаки ПЭГ (например, улучшенный период полужизни в сыворотке), при этом приобретая некоторые дополнительные благоприятные свойства. В качестве примера, простые полипептидные цепи (содержащие, например, Ala, Glu, Gly, Pro, Ser и Thr), способные образовывать расширенную конформацию, аналогичную ПЭГ, могут быть получены рекомбинантно уже слитыми с пептидным или белковым лекарственным средством, представляющим интерес (например, технология AmunixXTEN; Mountain View, CA). Это устраняет необходимость в дополнительной стадии конъюгации во время производственного процесса. Более того, установленные методы молекулярной биологии позволяют контролировать композицию боковых цепей полипептидных цепей, позволяя оптимизировать иммуногенность и производственные свойства.
Неоэпитопы
Неоэпитоп содержит неоантигенную определяющую часть неоантигенного пептида или неоантигенного полипептида, которая распознается иммунной системой. Неоэпитоп относится к эпитопу, который не присутствует в ссылке, такой как не болезненная клетка, например, не раковая клетка или исходная клетка, но находится в болезненной клетке, например, раковой клетке. Это включает ситуации, когда соответствующий эпитоп находят в нормальной не болезненной клетке или исходной клетке, но, из-за одной или более мутаций в болезненной клетке, например, раковой клетке, последовательность эпитопа изменяется так, что дает неоэпитоп. Термин “неоэпитоп” используют взаимозаменяемо с “опухолеспецифический неоэпитоп” в настоящем описании для обозначения рядов остатков, обычно L-аминокислот, соединенных друг с другом, обычно через пептидные связи между α-амино и карбоксильными группами соседних аминокислот. Неоэпитоп может иметь разную длину, быть либо в нейтральных (неизмененных) формах, либо в форах, которые являются солями, и либо не имеют модификации, такие как гликозилирование, окисление боковых цепей или фосфорилирование, либо содержат эти модификации, при условии что модификации не разрушают биологическую активность полипептидов, как описано в настоящем изобретении. В настоящем описании представлены выделенные неоэпитопы, которые содержат опухолеспецифические мутации из таблиц 1 или 2. Настоящее описание также представляет типовые выделенные неоэпитопы, которые содержат опухолеспецифические мутации из таблицы 34. Это описание также представляет типовые выделенные неоэпитопы, которые содержат опухолеспецифические мутации из таблиц 40A-40D и таблиц 3A-3D.
В некоторых вариантах осуществления, неоэпитопы, описанные в настоящем изобретении для HLA I класса, имеют 13 остатков или менее в длину и обычно состоят из от приблизительно 8 и до приблизительно 12 остатков, в частности, 9 или 10 остатков. В некоторых вариантах осуществления, неоэпитопы, описанные в настоящем изобретении для HLA II класса, имеют 25 остатков или менее в длину и обычно состоят из от приблизительно 16 и до приблизительно 25 остатков.
В некоторых вариантах осуществления, композиция, описанная в настоящем изобретении, содержит первый пептид, содержащий первый неоэпитоп белка, и второй пептид, содержащий второй неоэпитоп того же белка, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию. В некоторых вариантах осуществления, композиция, описанная в настоящем изобретении, содержит первый пептид, содержащий первый неоэпитоп первой области белка, и второй пептид, содержащий второй неоэпитоп второй области того же белка, где первая область содержит по меньшей мере одну аминокислоту второй области, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию. В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми. В некоторых вариантах осуществления, мутация выбрана из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутации «сдвига рамки», мутации сквозного прочитывания, мутации слияния генов и любой их комбинации.
В некоторых вариантах осуществления, первый неоэпитоп связывается с HLA белком I класса с образованием комплекса HLA-пептид I класса. В некоторых вариантах осуществления, второй неоэпитоп связывается с HLA белком II класса с образованием комплекса HLA-пептид II класса. В некоторых вариантах осуществления, второй неоэпитоп связывается с HLA белком I класса с образованием комплекса HLA-пептид I класса. В некоторых вариантах осуществления, первый неоэпитоп связывается с HLA белком II класса с образованием комплекса HLA-пептид II класса. В некоторых вариантах осуществления, первый неоэпитоп активирует CD8+ Т-клетки. В некоторых вариантах осуществления, первый неоэпитоп активирует CD4+ Т-клетки. В некоторых вариантах осуществления, второй неоэпитоп активирует CD4+ Т-клетки. В некоторых вариантах осуществления, второй неоэпитоп активирует CD8+ Т-клетки. В некоторых вариантах осуществления, TCR CD4+ Т-клетки связывается с комплексом HLA-пептид II класса. В некоторых вариантах осуществления, TCR CD8+ Т-клетки связывается с комплексом HLA-пептид II класса. В некоторых вариантах осуществления, TCR CD8+ Т-клетки связывается с комплексом HLA-пептид I класса. В некоторых вариантах осуществления, TCR CD4+ Т-клетки связывается с комплексом HLA-пептид I класса. В некоторых вариантах осуществления, композиция, содержащая неоантигенные C481S BTK пептиды, содержит первый BTK неоэпитоп и второй BTK неоэпитоп. В некоторых вариантах осуществления, первый BTK неоэпитоп содержит неоэпитоп, выбранный из таблицы 34. В некоторых вариантах осуществления, второй BTK неоэпитоп содержит неоэпитоп, выбранный из таблицы 34.
В некоторых вариантах осуществления, первая мутантная BTK пептидная последовательность, которая выбрана из таблицы 34, связывается с или предположительно связывается с белком, кодируемым HLA аллелем, перечисленной в таблице 34, соответствующим соответствующему пептиду (левый столбец и правый).
В некоторых вариантах осуществления, композиция, содержащая неоантигенные EGFR пептиды, содержит первый EGFR неоэпитоп и второй EGFR неоэпитоп. В некоторых вариантах осуществления, первый EGFR неоэпитоп содержит неоэпитоп, выбранный из таблиц 40A-40D. В некоторых вариантах осуществления, второй EGFR неоэпитоп содержит неоэпитоп, выбранный из таблиц 40A-40D.
В некоторых вариантах осуществления, первый мутантный EGFR неоэпитоп выбран из группы, состоящей из STVQLIMQL (SEQ ID NO: 3139), LIMQLMPF (SEQ ID NO: 3140), LTSTVQLIM (SEQ ID NO: 3141), TVQLIMQL (SEQ ID NO: 3142), TSTVQLIMQL (SEQ ID NO: 3143), TVQLIMQLM (SEQ ID NO: 3144) и VQLIMQLM (SEQ ID NO: 3145).
В некоторых вариантах осуществления, первая мутантная EGFR пептидная последовательность, которая выбрана из группы, состоящей из STVQLIMQL (SEQ ID NO: 3146), LIMQLMPF (SEQ ID NO: 3147), LTSTVQLIM (SEQ ID NO: 3148), TVQLIMQL (SEQ ID NO: 3149), TSTVQLIMQL (SEQ ID NO: 3150), TVQLIMQLM (SEQ ID NO: 3151) и VQLIMQLM (SEQ ID NO: 3152), связывается с или предположительно связывается с белком, кодируемым HLA-A68:01 аллелем, HLA-B15:02 аллелем, HLA-A25:01 аллелем, HLA-B57:03 аллелем, HLA-C12:02 аллелем, HLA-C03:02 аллелем и HLA-A26:01 аллелем, HLA-C12:03 аллелем, HLA-C06:02 аллелем, HLA-C03:03, HLA-B52:01 аллелем, HLA-A30:01 аллелем, HLA-C02:02 аллелем, HLA-C12:03 аллелем, HLA-A11:01 аллелем, HLA-A32:01 аллелем, HLA-A02:04 аллелем, HLA-B15:09 аллелем, HLA-C17:01 аллелем, HLA-C03:04 аллелем, HLA-B08:01 аллелем, HLA-A01:01 аллелем, HLA-B42:01 аллелем, HLA-B57:01 аллелем, HLA-B14:02 аллелем, HLA-B37:01 аллелем, HLA-B36:01 аллелем, HLA-B38:01 аллелем, HLA-C03:03 аллелем, HLA-B14:02 аллелем, HLA-B37:01 аллелем, HLA-A02:03 аллелем, HLA-B58:02 аллелем, HLA-C08:01 аллелем, HLA-B35:01 аллелем, HLA-B40:01 аллелем и/или HLA-B35:03 аллелем.
В таблице 41 представлен список типовых HLA аллелей, кодирующих HLA белок, который может связываться или предположительно связываться с EGFR неоантигенным пептидом.
В таблицах 42Ai, 42Aii и 42B показаны EGFR неоэпитопы с спрогнозированной специфичностью HLA подтипа.
В таблицах 5Ai, 5Aii и 5B показаны EGFR неоэпитопы с спрогнозированной специфичностью HLA подтипа.
Таблица 42Ai
Таблица 42Aii
Таблица 42B
В некоторых вариантах осуществления, первый и второй неоэпитопы являются разными эпитопами. В некоторых вариантах осуществления, второй неоэпитоп длиннее, чем первый неоэпитоп. В некоторых вариантах осуществления, первый неоэпитоп имеет длину по меньшей мере 8 аминокислот. В некоторых вариантах осуществления, первый неоэпитоп имеет длину от 8 до 12 аминокислот. В некоторых вариантах осуществления, первый неоэпитоп содержит последовательность из по меньшей мере 8 непрерывных аминокислот, где по меньшей мере 1 из 8 непрерывных аминокислот отличаются в соответствующих положениях от последовательности дикого типа. В некоторых вариантах осуществления, первый неоэпитоп содержит последовательность из по меньшей мере 8 непрерывных аминокислот, где по меньшей мере 2 из 8 непрерывных аминокислот отличаются в соответствующих положениях от последовательности дикого типа. В некоторых вариантах осуществления, второй неоэпитоп имеет длину по меньшей мере 16 аминокислот. В некоторых вариантах осуществления, второй неоэпитоп имеет длину от 16 до 25 аминокислот. В некоторых вариантах осуществления, второй неоэпитоп содержит последовательность из по меньшей мере 16 непрерывных аминокислот, где по меньшей мере 1 из 16 непрерывных аминокислот отличаются в соответствующих положениях от последовательности дикого типа. В некоторых вариантах осуществления, второй неоэпитоп содержит последовательность из по меньшей мере 16 непрерывных аминокислот, где по меньшей мере 2 из 16 непрерывных аминокислот отличаются в соответствующих положениях от последовательности дикого типа.
В некоторых вариантах осуществления, неоэпитоп содержит по меньшей мере один якорный остаток. В некоторых вариантах осуществления, первый неоэпитоп, второй неоэпитоп или оба содержит по меньшей мере один якорный остаток. В одном варианте осуществления, по меньшей мере один якорный остаток первого неоэпитопа находится в каноническом якорном положении или не каноническом якорном положении. В другом варианте осуществления, по меньшей мере один якорный остаток второго неоэпитопа находится в каноническом якорном положении или не каноническом якорном положении. В еще одном варианте осуществления, по меньшей мере один якорный остаток первого неоэпитопа отличается от по меньшей мере одного якорного остатка второго неоэпитопа.
В некоторых вариантах осуществления, по меньшей мере один якорный остаток является остатком дикого типа. В некоторых вариантах осуществления, по меньшей мере один якорный остаток является замещением. В некоторых вариантах осуществления, по меньшей мере один якорный остаток не содержит мутацию.
В некоторых вариантах осуществления, первый или второй неоэпитоп или оба содержат по меньшей мере одну фланкирующую область якорного остатка. В некоторых вариантах осуществления, неоэпитоп содержит по меньшей мере один якорный остаток. В некоторых вариантах осуществления, по меньшей мере один якорный остаток содержит по меньшей мере два якорных остатка. В некоторых вариантах осуществления, по меньшей мере два якорных остатка разделены областью разделения, содержащей по меньшей мере 1 аминокислоту. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая область якорного остатка не находится внутри области разделения. В некоторых вариантах осуществления, по меньшей мере одна фланкирующая область якорного остатка находится (a) выше N-конца якорного остатка из по меньшей мере двух якорных остатков; (b) ниже C-конца якорного остатка из по меньшей мере двух якорных остатков; или оба (a) и (b). В некоторых вариантах осуществления, второй неопептид выбран из таблицы 34.
В некоторых вариантах осуществления, второй неоэпитоп содержит мутацию T790M. В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность VQLIMQLMPF (SEQ ID NO: 3181). В некоторых вариантах осуществления второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность STVQLIMQLM (SEQ ID NO: 3182). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность QLIMQLMPF (SEQ ID NO: 3183). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность MQLMPFGCLL (SEQ ID NO: 3184). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность LIMQLMPF (SEQ ID NO: 3185). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность LTSTVQLIM (SEQ ID NO: 3186). В некоторых вариантах осуществления, второй неопептид, содержащий EGFR T790M мутацию, содержит последовательность STVQLIMQL (SEQ ID NO: 3187). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность TSTVQLIMQL (SEQ ID NO: 3188). В некоторых вариантах осуществления второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность TVQLIMQL (SEQ ID NO: 3189). В некоторых вариантах осуществления второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность TVQLIMQLM (SEQ ID NO: 3190). В некоторых вариантах осуществления второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность VQLIMQLM (SEQ ID NO: 3191). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность CLTSTVQLIM (SEQ ID NO: 3192). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность IMQLMPFGC (SEQ ID NO: 3193). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность IMQLMPFGC (SEQ ID NO: 3194). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность IMQLMPFGCL (SEQ ID NO: 3195). В некоторых вариантах осуществления второй неоэпитоп, содержащий EGFR T790M мутацию, содержит неоэпитопную последовательность LIMQLMPFG (SEQ ID NO: 3196). В некоторых вариантах осуществления второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность LIMQLMPFGC (SEQ ID NO: 3197). В некоторых вариантах осуществления, второй неоэпитоп, содержащий EGFR T790M мутацию, содержит последовательность QLIMQLMPFG (SEQ ID NO: 3198).
В некоторых вариантах осуществления, второй неоэпитоп содержит EGFR S492R мутацию. В некоторых вариантах осуществления, пептид, содержащий EGFR S492R мутацию, содержит неоэпитопную последовательность IIRNRGENSCK (SEQ ID NO: 3199).
В некоторых вариантах осуществления, второй EGFR неоэпитоп содержит делеционную мутацию в EGFR, такую как делеция G в EGFRvIII (внутреннюю делецию), где неоэпитопной последовательностью является ALEEKKGNYV (SEQ ID NO: 3200).
В некоторых вариантах осуществления, второй неоэпитоп содержит мутацию, изображенную в последовательности: LPQPPICTIDVYMIMVKCWMIDADSRPKFRELIIEFSKMARDPQRYLVIQ::LQDKFEHLKMIQQEEIRKLEEEKKQLEGEIIDFYKMKAASEALQTQLSTD (SEQ ID NO: 3201), где неоэпитопной последовательностью является IQLQDKFEHL (SEQ ID NO: 3202). В некоторых вариантах осуществления, второй неоэпитопной последовательностью является QLQDKFEHL (SEQ ID NO: 3203). В некоторых вариантах осуществления, второй неоэпитопной последовательностью является QLQDKFEHLK (SEQ ID NO: 3204). В некоторых вариантах осуществления, второй неоэпитопной последовательностью является YLVIQLQDKF (SEQ ID NO: 3205).
В некоторых вариантах осуществления, второй неопептид выбран из таблицы 35 или таблицы 3A-таблицы 3D.
В некоторых вариантах осуществления, неоэпитопы связывают HLA белок (например, HLA I класса или HLA II класса). В некоторых вариантах осуществления, неоэпитопы связывают HLA белок с большей аффинностью, чем соответствующий пептид дикого типа. В некоторых вариантах осуществления, неоэпитоп имеет IC50 менее чем 5000 нМ, менее чем1000 нМ, менее чем 500 нМ, менее чем 100 нМ, менее чем 50 нМ или менее.
В некоторых вариантах осуществления, неоэпитоп может иметь аффинность связывания HLA от приблизительно 1 пM и до приблизительно 1 мМ, от приблизительно 100 пM и до приблизительно 500 мкМ, от приблизительно 500 пM и до приблизительно 10 мкМ, от приблизительно 1 нМ и до приблизительно 1 мкМ, или до приблизительно 10 нМ и до приблизительно 1 мкМ. В некоторых вариантах осуществления, неоэпитоп может иметь аффинность связывания HLA, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 700, 800, 900 или 1000 нМ или более. В некоторых вариантах осуществления, неоэпитоп может иметь аффинность связывания HLA самое большее 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 700, 800, 900 или 1000 нМ.
В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком с большей аффинностью, чем соответствующий неоэпитоп дикого типа. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком I класса с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй неоэпитоп связывается с HLA белком II класса с KD или IC50 менее чем 2000 нМ, 1500 нМ, 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
В одном аспекте первый и/или второй неоэпитоп связывается с белком, кодируемым HLA аллелем, экспрессированной субъектом. В другом аспекте, мутация не присутствует в не раковых клетках субъекта. В еще одном аспекте, первый и/или второй неоэпитоп кодируется геном или экспрессированным геном раковых клеток субъекта.
В некоторых вариантах осуществления, первый неоэпитоп содержит мутацию, изображенную в столбце 2 таблицы 1 или 2. В некоторых вариантах осуществления, второй неоэпитоп содержит мутацию, изображенную в столбце 2 таблицы 1 или 2. В некоторых вариантах осуществления, определенные антигенные пептиды спарены с определенными аллелями.
Замещение может быть расположено в любом положении по сей длине неоэпитопа. Например, оно может быть расположено в N-концевой трети пептида, центральной трети пептида или С-концевой трети пептида. В другом варианте осуществления, замещенный остаток расположен в 2-5 остатках от N-конца или 2-5 остатках от С-конца. Пептиды могут быть аналогично получены из опухолеспецифических вставочных мутаций, где пептид содержит один или более, или все вставленные остатки.
В некоторых вариантах осуществления, пептид, описанный в настоящем изобретении, может быть легко синтезирован химически с применением реагентов, которые не содержат загрязняющие бактериальные или животные вещества (Merrifield RB: Solid phase peptide synthesis. I. synthesis of tetrapeptide. J. Am. Chem. Soc.85:2149-54, 1963). В некоторых вариантах осуществления, пептиды получают (1) параллельным твердофазным синтезом многоканальных инструментов с применением однородных условий синтеза и расщепления; (2) очисткой на колонке ОФ-ВЭЖХ с десорбционной колонкой; и повторным промыванием, но не замещением, между пептидами; с последующим (3) анализом с ограниченным набором наиболее информативных анализов. След правил производства и контроля качестве лекарственных средств (GMP) может быть определен вокруг ряда пептидов для отдельного пациента, тем самым требуя методик смены ряда только между синтезом пептидов для разных пациентов.
Полинуклеотиды
Альтернативно, нуклеиновая кислота (например, полинуклеотид), кодирующая пептид согласно настоящему описанию, может использоваться для получения неоантигенного пептида in vitro. Полинуклеотидом может быть, например, ДНК, кДНК, ПНК, CNA, РНК, одно- и/или двухцепочечная, или нативные или стабилизированные формы полинуклеотидов, такие как, например полинуклеотиды с фосфоротиатным скелетом, или из комбинации, и они могут содержать или не содержать интроны, пока они кодируют пептид. В некоторых вариантах осуществления in vitro трансляцию используют для получения пептида.
Настоящее изобретение относится к неоантигенным полинуклеотидам, кодирующим каждый неоантигенный пептид, описанный в настоящем описании. Термин “полинуклеотид”, “нуклеотиды” или “нуклеиновая кислота” используются взаимозаменяемо с “мутантный полинуклеотид”, “мутантный нуклеотид”, “мутантная нуклеиновая кислота”, “неоантигенный полинуклеотид”, “неоантигенный нуклеотид” или “неоантигенная мутантная нуклеиновая кислота” в настоящем описании. Разные последовательности нуклеиновых кислот могут кодировать один и тот же пептид из-за избыточности генетического кода. Каждая из этих нуклеиновых кислот попадает в объем настоящего описания. Нуклеиновые кислоты, кодирующие пептиды, могут быть ДНК или РНК, например, мРНК, или сочетанием ДНК и РНК. В некоторых вариантах осуществления, последовательность нуклеиновых кислот, кодирующая пептид, является самоамплифицирующейся мРНК (Brito et al., Adv. Genet. 2015; 89:179-233). Любой подходящий полинуклеотид, который кодирует пептид, описанный в настоящем изобретении, попадает в объем настоящего описания.
Термин “РНК” включает, и в некоторых вариантах осуществления, относится к “мРНК.” Термин “мРНК” означает “мессенджер-РНК” и относится к “транскрипту”, который создан с применением шаблона ДНК и кодирует пептид или полипептид. Обычно, мРНК содержит 5’-UTR, область, кодирующую белок и 3’-UTR. мРНК обладает только ограниченным периодом полужизни в клетках и in vitro. В некоторых вариантах осуществления, мРНК является самоамплифицирующейся мРНК. В контексте настоящего описания, мРНК может быть сконструирована in vitro транскрипцией из шаблона ДНК. Методика транскрипции in vitro известна специалистам в данной области техники. Например, существует множество коммерчески доступных наборов для транскрипции in vitro.
Стабильность и эффективность трансляции РНК может быть модифицирована как требуется. Например, РНК может быть стабилизирована, и ее трансляция повышена одной или более модификациями, оказывающими стабилизирующее действие и/или повышающими эффективность трансляции РНК. Такие модификации описаны, например, в PCT/EP2006/009448, включенной сюда в качестве ссылки. Для повышения экспрессии РНК, применяемой согласно данному описанию, она может быть модифицирована в кодирующей области, т.е. последовательности, кодирующей экспрессированный пептид или белок, без изменения последовательности экспрессированного пептида или белка, так, чтобы повысить содержание GC для повышения стабильности мРНК и для проведения оптимизации кодона и, следовательно, улучшения трансляции в клетках.
Термин “модификация” в контексте РНК, используемый в настоящем описании, включает любую модификацию РНК, которая не присутствует в природе в указанной РНК. В некоторых вариантах осуществления, РНК не имеет некэпированные 5’-трифосфаты. Удаление таких некэпированных 5’-трифосфатов может быть достигнуто обработкой РНК фосфатазой. В других вариантах осуществления, РНК может иметь модифицированные рибонуклеотиды для повышения ее стабильности и/или снижения цитотоксичности. В некоторых вариантах осуществления, 5-метилцитидином может быть замещен частично или полностью в РНК, например, цитидин. Альтернативно, псевдоуридином замещен частично или полностью, например, уридин.
В некоторых вариантах осуществления, термин “модификация” относится к получению РНК с 5’-кжпом или аналогом 5’-кэпа. Термин “5’-кэп” относится к кэповой структуре, найденной на 5’-конце молекулы мРНК и обычно состоит из гуанозинового нуклеотида, соединенного с мРНК через необычную 5’ - 5’ трифосфатную связь. В некоторых вариантах осуществления, этот гуанозин метилирован в положении 7. Термин “обычный 5’-кэп” относится к существующему в природе 5’-кэпу РНК, к 7-метилгуанозиновому кэпу (m G). В контексте настоящего описания, термин “5’-кэп” включает аналог 5’-кэпа, который похож на структуру РНК кэпа и модифицирован для придания способности стабилизировать РНК и/или улучшать трансляцию присоединенной к нему РНК in vivo и/или в клетке.
В некоторых вариантах осуществления, мРНК, кодирующую неоантигенный пептид согласно настоящему описанию, вводят субъекту, нуждающемуся в этом. В некоторых вариантах осуществления, настоящее описание относится к РНК, олигорибонуклеотид и молекулы полирибонуклеотида, содержащие модифицированный нуклеозид, содержащие их векторы генной терапии, способы генной терапии и способы выключения транскрипции генов, содержащих их. В некоторых вариантах осуществления, вводимая мРНК содержит по меньшей мере один модифицированный нуклеозид.
Полинуклеотиды, кодирующие пептиды, описанные в настоящем изобретении, могут быть синтезированы химическими методами, например, фосфотриэфирным способом из Matteucci, et al., J. Am. Chem. Soc. 103:3185 (1981). Полинуклеотиды, кодирующие пептиды, содержащие или составляющие аналога, могут быть получены просто замещением подходящими и желаемыми основаниями нуклеиновых кислот тех, которые кодируют нативный эпитоп.
Полинуклеотиды, описанные в настоящем изобретении, могут содержать один или более синтетических или существующих в природе интронов в транскрибированной области. Включение последовательностей стабилизации мРНК и последовательностей для репликации в клетках млекопитающих также может считаться повышающим экспрессию полинуклеотида. Кроме того, полинуклеотид, описанный в настоящем изобретении, может содержать иммуностимулирующие последовательности (ISS или CpG). Эти последовательности могут быть включены в вектор вне полинуклеотида, кодирующего последовательность для улучшения иммуногенности.
В некоторых вариантах осуществления, полинуклеотиды могут содержать кодирующую последовательность для пептида или белка, слитого в одной и той же рамке считывания, с полинуклеотидом, который помогает, например, при экспрессии и/или секреции пептида или белка из клетки-хозяина (например, лидерной последовательности, которая действует как секреторная последовательность для регулирования транспорта полипептида из клетки). Полипептид, имеющий лидерную последовательность, является пре-белком и может иметь лидерную последовательность, расщепленную клеткой-хозяином с образованием зрелой формы полипептида.
В некоторых вариантах осуществления, полинуклеотиды могут содержать кодирующую последовательность для пептида или белка, слитого в одной и той же рамке считывания, с маркерной последовательностью, которая позволяет, например, очистку кодированного пептида, который потом может быть вставлен в персонализированную вакцину от заболевания или иммуногенную композицию. Например, маркерной последовательностью может быть гексагистидиновая метка (SEQ ID NO: 3206), поставляемая pQE-9 вектором для осуществления очистки зрелого полипептида, конденсированного с маркером в случае бактериального хозяина, или маркерной последовательностью может быть гемагглютининовая (HA) метка, полученная из белка гемагглютинина гриппа при млекопитающем хозяине (например, COS-7 клетки). Дополнительные метки включают, но не ограничены ими, кальмодулиновые метки, FLAG метки, Myc метки, S метки, SBP метки, Softag 1, Softag 3, V5 метку, Xpress метку, Isopeptag, SpyTag, метки белка-носителя биотинкарбоксила (BCCP), GST метки, метки флуоресцентного белка (например, метки зеленого флуоресцентного белка), метки белка, связывающего мальтозу, Nus метки, Strep-метка, тиоредоксиновая метка, TC метка, Ty метка, и подобные.
В некоторых вариантах осуществления, полинуклеотиды могут содержать кодирующую последовательность для одного или нескольких описанных в настоящем изобретении пептидов или белков, слитых в одной и той же рамке считывания для создания одного конкатамеризованного неоантигенного пептидного конструкта, способного продуцировать множество неоантигенных пептидов.
В некоторых вариантах осуществления, ДНК последовательность сконструирована с применением рекомбинантной технологии через выделение или синтез ДНК последовательности, кодирующей белок дикого типа, представляющий интерес. Необязательно, последовательность может быть мутагенизирована сайт-специфическим мутагенезом с получением его функциональных аналогов. См., например, Zoeller et al., Proc. Nat’l. Acad. Sci. USA 81:5662-5066 (1984) и патент США № 4,588,585. В другом варианте осуществления, ДНК последовательность, кодирующая пептид или белок, представляющий интерес, может быть сконструирована химическим синтезом с применением олигонуклеотидного синтезатора. Такие олигонуклеотиды могут быть созданы на основе аминокислотной последовательности желаемого пептида и выбора таких кодонов, которые одобрены в клетке-хозяине, в которой рекомбинантный полипептид, представляющий интерес, продуцируется. Стандартные способы могут использоваться для синтеза выделенной полинуклеотидной последовательности, кодирующей выделенный полипептид, представляющий интерес. Например, полная аминокислотная последовательность может использоваться для конструирования гена с возможной последовательностью, восстановленной по полипептиду. Затем может быть синтезирован ДНК олигомер, содержащий нуклеотидную последовательность, кодирующую конкретный выделенный полипептид. Например, несколько малых олигонуклеотидов, кодирующих части желаемого полипептида, могут быть синтезированы и затем лигированы. Отдельные олигонуклеотиды обычно содержат 5’ или 3’ липкие концы для комплементарной сборки.
После сборки (например, синтезом, сайт-направленным мутагенезом или другим способом), полинуклеотидные последовательности, кодирующие конкретный выделенный полипептид, представляющий интерес, вставляют в вектор экспрессии и необязательно функционально связывают с регуляторной последовательностью экспрессии для экспрессии белка у желаемого хозяина. Подходящая сборка может быть подтверждена нуклеотидным секвенированием, рестрикционным картированием и экспрессией биологически активного полипептида у подходящего хозяина. Как хорошо известно в данной области техники, для получения высоких уровней экспрессии трансфицированного гена у хозяина, ген может быть функционально связан с транскрипционной и трансляционной последовательностями регулирования экспрессии, которые являются функциональными в выбранном для экспрессии хозяине.
Таким образом, настоящее описание также направлено на векторы и векторы экспрессии, используемые для продуцирования и введения неоантигенных пептидов и неоэпитопов, описанных в настоящем изобретении, и на клетки-хозяева, содержащие такие векторы.
Векторы
В некоторых вариантах осуществления также может быть получен вектор экспрессии, способный экспрессировать пептид или белок, описанный в настоящем изобретении. Векторы экспрессии для разных типов клеток хорошо известны в данной области техники и могут быть выбраны без излишнего экспериментирования. Обычно, ДНК вставляют в вектор экспрессии, Такой как плазмида, в подходящей ориентации и правильной рамке считывания для экспрессии. При необходимости, ДНК может быть связана с подходящими транскрипционными и трансляционными регулирующими регуляторными нуклеотидными последовательностями, распознаваемыми желаемым хозяином (например, бактерией), хотя такие контроли обычно находятся в векторе экспрессии. Затем вектор вводят в бактерию-хозяина для клонирования с применением стандартных методов (см., например, Sambrook et al. (1989) Molecular Cloning, Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.).
Большое количество векторов и систем-хозяев, подходящих для производства и введения неоантигенного пептида, описанного в настоящем изобретении, известны специалисту в данной области техники, и коммерчески доступны. Следующие векторы представлены в качестве примера. Бактериальные: pQE70, pQE60, pQE-9 (Qiagen), pBS, pD10, phagescript, psiX174, pBluescript SK, pbsks, pNH8A, pNH16a, pNH18A, pNH46A (Stratagene); ptrc99a, pKK223-3, pKK233-3, pDR540, pRIT5 (Pharmacia); pCR (Invitrogen). Эукариотические: pWLNEO, pSV2CAT, pOG44, pXT1, pSG (Stratagene) pSVK3, pBPV, pMSG, pSVL (Pharmacia); p75,6 (Valentis); pCEP (Invitrogen); pCEI (Epimmune). Однако, любая другая плазмида или вектор могут использоваться, пока они являются реплицируемыми и жизнеспособными в хозяине.
Для экспрессии неоантигенных пептидов, описанных в настоящем изобретении, кодирующая последовательность должна быть представлена с функционально связанными старт- и стоп-кодонами, промотором и терминаторными областями, и в некоторых вариантах осуществления, и системой репликации для того, чтобы дать вектор экспрессии для экспрессии в желаемом клеточном хозяине. Например, последовательности промотора, совместимые с бактериальными хозяевами, представлены в плазмидах, содержащих удобные сайты рестрикции для вставки желаемых кодирующих последовательностей. Полученные векторы экспрессии трансформируют в подходящие бактериальные хозяева.
Векторы экспрессии млекопитающих будут содержать точку начала репликации, подходящий промотор и энхансер, а также любые необходимые сайты связывания рибосомы, сайт полиаденилирования, донор сплайсинга и сайты акцептора, транскрипционные стоп-кодоны и 5’ фланкирующие не транскрибированные последовательности. Такие промоторы также могут быть получены из вирусных источников, таких как, например, цитомегаловирус человека (CMV-IE промотор) или вирус простого герпеса типа-1 (HSV TK промотор). Нуклеиновые кислотные последовательности, полученные из SV40 сплайсинга, и сайты полиаденилирования могут использоваться для получения требуемых не транскрибированных генетических элементов.
Рекомбинантные векторы экспрессии могут использоваться для амплификации и экспрессирования ДНК, кодирующей пептид или белок, описанный в настоящем изобретении. Рекомбинантные векторы экспрессии являются реплицируемыми ДНК конструктами, которые имеют синтетические или кДНК-полученные ДНК фрагменты, кодирующие пептид или биоэквивалентный аналог, связанный с подходящими транскрипционными или трансляционными регулирующими элементами, полученными из генов млекопитающих, микробов, вирусов или насекомых. Транскрипционная единица обычно содержит сборку из (1) генетического элемента или элементов, имеющих регулирующую роль в экспрессии гена, например, транскрипционных промоторов или энхансеров, (2) структурной или кодирующей последовательности, которая транскрибирована в мРНК и транслирована в белок, и (3) подходящих последовательностей инициации и окончания транскрипции и трансляции, подробно описанных в настоящем изобретении. Такие регулирующие элементы могут включать последовательность оператора для контроля транскрипции. Может быть дополнительно включена способность реплицироваться в хозяине, обычно предоставляемая точкой начала репликации, и ген селекции для усиления распознавания трансформантов. Области ДНК функционально связаны, когда они являются функционально родственными друг другу. Например, ДНК для сигнального пептида (секреторного лидера) функционально связана с ДНК для полипептид, если она экспрессируется как предшественник, который участвует в секреции полипептида; промотор функционально связан с кодирующей последовательностью, если он контролирует транскрипцию последовательности; или сайт связывания рибосомы функционально связан с кодирующей последовательностью, если он расположен так, чтобы позволить трансляцию. В общем, функционально связанные означает непрерывные, и в случае секреторных лидеров, означает непрерывные и в пределах рамки считывания. Структурные элементы, предназначенные для применения в дрожжевых системах экспрессии, включают лидерную последовательность, позволяющую внеклеточную секрецию транслированного белка клеткой-хозяином. Альтернативно, если рекомбинантный белок экспрессирован без лидерной или транспортной последовательности, он может включать N-концевой метиониновый остаток. Этот остаток необязательно может быть далее отщеплен от экспрессированного рекомбинантного белка с получением конечного продукта.
Обычно рекомбинантные векторы экспрессии будут включать точки начала репликации и выбираемые маркеры, позволяющие трансформацию клетки-хозяина, например, гена резистентности ампициллина E. coli и гена S. cerevisiaeTRP1, и промотор, полученный из экспрессированного на высоком уровне гена для направления транскрипции ниже структурной последовательности. Такие промоторы могут быть получены из оперонов, кодирующих гликолитические ферменты, такие как 3-фосфоглицераткиназа (PGK), кислая фосфатаза или белки теплового шока, среди прочих. Гетерологическая структурная последовательность собрана в подходящей фазе с последовательностями начала и терминации трансляции, и в некоторых вариантах осуществления, лидерной последовательностью, способной направлять секрецию транслированного белка в периплазматическое пространство или внеклеточную среду. Необязательно, гетерологическая последовательность может кодировать слитый белок, включающий N-концевой идентификационный пептид, придающий желаемые характеристики, например, стабилизацию или упрощенную очистку экспрессированного рекомбинантного продукта.
Полинуклеотиды, кодирующие неоантигенные пептиды, описанные в настоящем изобретении, также могут содержать последовательность сигнала убиквитинирования и/или направляющую последовательность, такие как последовательность сигнала эндоплазматического ретикулюма (ER) для облегчения движения полученного пептида в эндоплазматический ретикулюм.
В некоторых вариантах осуществления, неоантигенный пептид, описанный в настоящем изобретении, также может вводиться и/или экспрессироваться вирусными или бактериальными векторами. Примеры векторов экспрессии включают ослабленных вирусных хозяев, таких как осповакцина или оспа кур. В качестве примера этого подхода, вирус осповакцины используют в качестве вектора для экспрессии нуклеотидных последовательностей, которые кодируют неоантигенные пептиды, описанные в настоящем изобретении. Векторы осповакцины и способы, используемые в протоколах иммунизации описаны в, например, патенте США № 4,722,848. Другим вектором является BCG (бацилла Кальмета-Герена). BCG векторы описаны у Stover et al., Nature 351:456-460 (1991).
Широкий спектр других векторов, полезных для терапевтического введения или иммунизации неоантигенных полипептидов, описанных в настоящем изобретении, например векторов адено- и аденоассоциированных вирусов, векторов ретровирусов, векторов Salmonella Typhimurium, векторов детоксифицированного токсина сибирской язвы, векторов вируса Сендай, векторов поксвируса, векторов оспы канареек и векторов оспы кур, и подобных, будет очевиден специалистам в данной области из описания настоящего документа. В некоторых вариантах осуществления, вектором является модифицированный вирус осповакцины Анкара (VA) (например, Bavarian Noridic (MVA-BN)).
Среди векторов, которые могут использоваться на практике настоящего описания, интеграция в геном хозяина клетки возможна с применением способов ретровирусного генного переноса, часто дающих долговременную экспрессию вставленного трансгена. В некоторых вариантах осуществления, ретровирусом является лентивирус. Дополнительно, высокая эффективность трансдукции наблюдалась во многих разных типах клеток и целевых тканей. Тропизм ретровируса может быть изменен введением чужеродных оболочечных белков, размножая потенциальную целевую популяцию клеток-мишеней. Также ретровирус может быть сконструирован так, чтобы позволять условную экспрессию вставленного трансгена так, что только определенные клеточные типы будут заражены лентивирусом. Промоторы, специфические к клеточным типам, могут использоваться для направленной экспрессии в определенных клеточных типах. Лентивирусные векторы являются ретровирусными векторами (и, следовательно, и лентивирусные, и ретровирусные векторы могут использоваться на практике настоящего описания). Более того, лентивирусные векторы способны трансдуцировать или заражать не делящиеся клетки и обычно дают высокие вирусные титры. Выбор системы переноса ретровирусного гена поэтому может зависеть от целевой ткани. Ретровирусные векторы состоят из цис-действующих длинных концевых повторов с упаковочной способностью вплоть до 6-10 т.н. чужеродной последовательности. Минимум цис-действующих LTR является достаточным для репликации и упаковки векторов, которые затем используют для интеграции желаемой нуклеиновой кислоты в клетку-мишень для получения постоянной экспрессии. Широко используемые ретровирусные векторы, которые могут использоваться на практике настоящего описания, включают такие, которые основаны на вирусе лейкоза мыши (MuLV), вирусе лейкоза гиббонов (GaLV), вирусе иммунодефицита обезьян (SIV), вируса иммунодефицита человека (HIV) и их комбинаций (см., например, Buchscher et al., (1992) J. Virol. 66:2731-2739; Johann et al., (1992) J. Virol,66:1635-1640; Sommnerfelt et al., (1990) Virol,176:58-59; Wilson et al., (1998) J. Virol,63:2374-2378; Miller et al., (1991) J. Virol,65:2220-2224; PCT/US94/05700).
в практике настоящего описания также может быть использован минимальный лентивирусный вектор не приматов, такой как лентивирусный вектор на основе вируса инфекционной анемии лошадей (EIAV). Векторы могут иметь промотор цитомегаловируса (CMV), управляющий экспрессией гена-мишени. Соответственно, настоящее описание рассматривает среди вектора(ов), применимых в практике настоящего описания: вирусные векторы, включая ретровирусные векторы и лентивирусные векторы.
в практике настоящего описания также может быть использован аденовирусный вектор. Одним из преимуществ является способность рекомбинантных аденовирусов эффективно переносить и экспрессировать рекомбинантные гены во множестве клеток и тканей млекопитающих in vitro и in vivo, с получением высокой экспрессии перенесенных нуклеиновых кислот. Также, способность продуктивно заражать покоящиеся клетки расширяет применимость рекомбинантных аденовирусных векторов. Кроме того, высокие уровни экспрессии обеспечивают то, что продукты нуклеиновых кислот будут экспрессироваться до достаточных уровней для создания иммунного ответа (см., например, патент США № 7,029,848, включенный сюда в качестве ссылки).
Что касается аденовирусных векторов, которые могут быть использованы в практике настоящего описания, может быть упомянут патент США № 6,955,808. Используемый аденовирусный вектор может быть выбран из группы, состоящей из Ad5, Ad35, Ad11, C6, и C7 векторов. Последовательность генома Аденовируса 5 (“Ad5”) опубликована. (Chroboczek, J., Bieber, F., и Jacrot, B. (1992) Sequence Genome of Adenovirus Type 5 and Its Comparison with Genome of Adenovirus Type 2, Virology 186, 280-285; содержание которой включено сюда в качестве ссылки). Ad35 векторы описаны в патентах США №№ 6,974,695, 6,913,922 и 6,869,794. Ad11 векторы описаны в патенте США № 6,913,922. C6 аденовирусные векторы описаны в патентах США №№ 6,780,407; 6,537,594; 6,309,647; 6,265,189; 6,156,567; 6,090,393; 5,942,235 и 5,833,975. C7 векторы описаны в патенте США № 6,277,558. Аденовирусные векторы, которые являются E1-дефектными или удаленными, E3-дефектными или удаленными и/или E4-дефектными или удаленными, также могут использоваться. Определенные аденовирусы, имеющие мутации в E1 области, имеют улучшенный резерв безопасности, так как E1-дефектные аденовирусные мутанты являются репликация-дефектными в непермиссивных клетках, или по меньшей мере являются сильно ослабленными. Аденовирусы, имеющие мутации в E3 области, могут иметь улучшенную иммуногенность посредством механизма разрыва, которым аденовирус подавляет молекулы MHC I класса. Аденовирусы, имеющие E4 мутации, могут иметь пониженную иммуногенность аденовирусного вектора из-за подавления поздней экспрессии гена. Такие векторы могут быть особенно полезны, когда желательна повторная ревакцинация с применением того же вектора. Аденовирусные векторы, которые удалены или мутированы в E1, E3, E4; E1 и E3; и E1 и E4, могут использоваться в соответствии с настоящим описанием.
Более того, “выпотрошенные” аденовирусные векторы, в которых удалены все вирусные векторы, также могут использоваться в соответствии с настоящим описанием. Такие векторы требуют вирус-помощник для их репликации и требуют специальной колонии 293 клеток человека, экспрессирующей и E1a, и Cre, условия, которое не существует в природе. Такие “выпотрошенные” вектор являются не иммуногенными, и поэтому векторы могут быть инокулированы множество раз для ревакцинации. “Выпотрошенные” аденовирусные векторы могут использоваться для вставки гетерологических вставок/генов, таких как трансгены настоящего описания, и могут даже использоваться для совместной доставки большого количества гетерологических вставок/генов.
В некоторых вариантах осуществления, доставка происходит через аденовирус, который может быть в одной ревакцинирующей дозе. В некоторых вариантах осуществления, аденовирус доставляют множеством доз. Что касается in vivo доставки, AAV имеет преимущество над другими вирусными векторами благодаря низкой токсичности и низкой вероятности вызова инсерционного мутагенеза, так как он не s интегрируется в геном хозяина. AAV имеет упаковочный лимит 4,5 или 4,75 т.н. Конструкты более 4,5 или 4,75 т.н. дает значительное снижение продуцирования вируса. Существует множество промоторов, которые могут использоваться для управления экспрессией молекул нуклеиновой кислоты. AAV ITR может служить в качестве промотора и является предпочтительным для устранения необходимости в дополнительном промоторном элементе.
Для повсеместной экспрессии могут использоваться следующие промоторы: CMV, CAG, CBh, PGK, SV40, тяжелые и легкие цепи Ферритина и т.д. Для экспрессии в мозге могут использоваться следующие промоторы: SynapsinI для всех нейронов, CaMKIIalpha для возбуждающих нейронов, GAD67 или GAD65 или VGAT для GABAэргических нейронов и т.д. Промоторы, используемые для управления синтезом РНК, могут включать: Pol III промоторы, такие как U6 или H1. Применение Pol II промотора и интронных кассет может использоваться для экспрессии направляющей РНК (нРНК). Что касается AAV векторов, применяемых в практике настоящего описания, можно упомянуть патенты США №№ 5658785, 7115391, 7172893, 6953690, 6936466, 6924128, 6893865, 6793926, 6537540, 6475769 и 6258595, и цитированные там документы. Что касается AAV, AAV может быть AAV1, AAV2, AAV5 или любой их комбинацией. Можно выбрать AAV, принимая во внимание клетки, являющиеся мишенями; например, можно выбрать AAV серотипы 1, 2, 5 или гибридный капсидный AAV1, AAV2, AAV5 или любую их комбинацию для таргетирования мозга или нейронов; и можно выбрать AAV4 для таргетирования сердечной ткани. AAV8 используют для доставки в печень. В некоторых вариантах осуществления, доставка происходит через AAV. Доза может быть скорректирована так, чтобы уравновесить терапевтическую пользу и любые побочные эффекты.
В некоторых вариантах осуществления в описанной здесь композиции используют поксвирус . Они включают ортопоксвирус, авипоксвирус, осповакцину, MVA, NYVAC, канарипокс, ALVAC, вирус оспы кур, TROVAC и т.д. (см., например, Verardiet al., Hum. Vaccin. Immunother. 2012 Jul;8(7):961-70; и Moss, Vaccine. 2013; 31(39): 4220–4222). Поксвирусные векторы экспрессии были описаны в 1982 и быстро стали широко использоваться для развития вакцин, а также для исследований во множестве областей. Преимущества векторов включают простую конструкцию, способность размещать большие количества чужеродных ДНК и высокие уровни экспрессии. Информация относительно поксвирусов, которые могут использоваться в практике настоящего описания, таких как поксвирусы субсемейства Chordopoxvirinae (поксвирусы позвоночных), например, ортопоксвирусы и авипоксвирусы, например, вирус осповакцины (например, Wyeth Штамм, WR Штамм (например, ATCC® VR-1354), Copenhagen Штамм, NYVAC, NYVAC,1, NYVAC,2, MVA, MVA-BN), канарипоксвирус (например, Wheatley C93 Штамм, ALVAC), вирус оспы кур (например, FP9 Штамм, Webster Штамм, TROVAC), вирус оспы голубей, вирус оспы голубей, вирус оспы перепелов, вирус оспы енотов, кроме прочего, их синтетические и не существующие в природе рекомбинанты, их применение и способы получения и применения таких рекомбинантов могут быть найдены в научной и патентной литературе.
В некоторых вариантах осуществления, вирус осповакцины используют в вакцине против заболевания или иммуногенной композиции для экспрессии антигена. (Rolph et al., Recombinant viruses as vaccines and immunological tools. Curr. Opin. Immunol. 9:517-524, 1997). Рекомбинантный вирус осповакцины способен реплицироваться в цитоплазме зараженной клетки-хозяина и, следовательно, полипептид представляющий интерес, может вызвать иммунный. Более того, поксвирусы широко используют в качестве векторов вакцины или иммуногенной композиции из-за их способности таргетировать кодированные антигены для процессинга путем главного комплекса гистосовместимости I класса через прямое заражение иммунных клеток, в частности, антигенпрезентирующих клеток, а также из-за их способности быть само-адъювантом.
В некоторых вариантах осуществления, ALVAC используют в качестве вектора в вакцине против заболевания или иммуногенной композиции. ALVAC является канарипоксвирусом, который может быть модифицирован для экспрессии чужеродных трансгенов и применяется в качестве способа вакцинации против и прокариотических и эукариотических антигенов (Horig H, Lee DS, Conkright W, et al. Phase I clinical trial of recombinant canarypoxvirus (ALVAC) vaccine expressing human carcinoembryonic antigen и B7.1 co-stimulatory molecule. Cancer Immunol. Immunother,2000;49:504–14; von Mehren M, Arlen P, Tsang KY, et al. Pilot study of dual gene recombinant avipox vaccine containing both carcinoembryonic antigen (CEA) and B7.1 transgenes in patients with recurrent CEA-expressing adenocarcinomas. Clin. Cancer. Res. 2000;6:2219–28; Musey L, Ding Y, Elizaga M, et al. HIV-1 vaccination administered intramuscularly can induce both systemic и mucosal Т-cell immunity in HIV-1-uninfected individuals. J. Immunol. 2003;171:1094–101; Paoletti E. Applications of pox virus vectors to vaccination: update. Proc. Natl. Acad. Sci. U S 1996;93:11349–53; патент США №7,255,862). В клиническом испытании I фазы, ALVAC вирус, экспрессирующий опухолевый антиген CEA, показал превосходный профиль безопасности и вызвал повышение CEA-специфических ответов Т-клетки у выбранных пациентов; объективные клинические ответы, однако, не наблюдались (Marshall JL, Hawkins MJ, Tsang KY, et al. Phase I study in cancer patients of replication-defective avipox recombinant vaccine that expresses human carcinoembryonic antigen. J. Clin. Oncol. 1999;17:332–7).
В некоторых вариантах осуществления, модифицированный вирус осповакцины Анкара (MVA) может использоваться в качестве вирусного вектора для антигенной вакцины или иммуногенной композиции. MVA является членом семейства Ортопоксвирусов и был создан через, приблизительно 570 серийных пассажей на фибробластах эмбриона курицы штамма Анкара вируса осповакцины (CVA) (см., например, Mayr, A., et al., Infection 3, 6-14, 1975). В результате этих пассажей, полученный MVA вирус содержит на 31 тысячу нуклеотидов меньше геномной информации по сравнению с CVA, и является осень ограниченным клеткой-хозяином (Meyer, H. et al., J. Gen. Virol. 72, 1031-1038, 1991). MVA характеризуется экстремальным ослаблением, а именно, уменьшенной вирулентностью или способностью заражать, но все еще имеет превосходную иммуногенность. При тестировании на множестве животных моделей было доказано, что MVA является авирулентным даже у индивидуумов в подавленным иммунитетом. Более того MVA-BN®-HER2 является кандидатной иммунотерапией, созданной для лечения HER-2-положительного рака молочной железы и в настоящее время проходит клинические испытания. (Mandl et al., Cancer Immunol. Immunother. Jan 2012; 61(1): 19–29). Способы получения и применением рекомбинантного MVA были описаны (например, см. патенты США №№ 8,309,098 и 5,185,146 включенные сюда в качестве ссылки полностью).
Подходяще клетки-хозяева для экспрессии полипептида включают прокариоты, дрожжи, эукариотические клетки насекомых или высших животных, под контролем подходящих промоторов. Прокариоты включают грамотрицательные или грамположительные микроорганизмы, например E. coli, или бациллы. Высшие эукариотические клетки включают устойчивые клеточные линии млекопитающего происхождения. Бесклеточные системы трансляции также могут использоваться. Подходящие клонирующие и векторы экспрессии для применения с бактериальными, грибковыми, дрожжевыми и млекопитающими клетками-хозяевами хорошо известны в данной области техники (см. Pouwels et al., Cloning Vectors: Laboratory Manual, Elsevier, N.Y., 1985).
Различные системы культивирования клеток млекопитающих или насекомых также преимущественно используют для экспрессии рекомбинантного белка. Экспрессия рекомбинантных белков в клетках млекопитающих может выполняться, так как такие белки обычно правильно свернуты, подходящим образом модифицированы и полностью функциональны. Примеры подходящих колоний клеток-хозяев млекопитающих включают COS-7 колонии клеток почек обезьян, описанные у Gluzman (Cell 23:175, 1981), и другие колонии клеток, способные экспрессировать подходящий вектор, включающие, например, L клетки, C127, 3T3, клетки яичников китайского хомяка (CHO), 293, колонии клеток HeLa и BHK. Векторы экспрессии млекопитающих содержат нетранскрибируемые элементы, такие как точка начала репликации, подходящий промотор и энхансер, связанный с экспрессируемым геном, и другие 5’ или 3’ фланкирующие нетранскрибируемые последовательности, и 5’ или 3’ нетранслируемые последовательности, такие как необходимые сайты связывания рибосомы, сайт полиаденилирования, сайты доноров и акцепторов сплайсинга и последовательности терминации транскрипции. Бакуловирусные системы для продуцирования гетерологических белков в клетках насекомых описаны в Luckow и Summer, Bio/Technology 6:47 (1988).
Клетки-хозяева генетически сконструированы (трансдуцированы или трансформированы или трансфицированы) векторами, которые могут быть, например, клонирующим вектором или вектором экспрессии. Вектор может быть, например, в форме плазмиды, вирусной частицы, фага и т.д. Сконструированные клетки-хозяева могут быть культивированы в обычной питательной среде, модифицированной соответствующим образом для активации промоторов, выбора трансформантов или амплификации полинуклеотидов. Условия культивирования, такие как температура, pH и подобные, такие же, как используемые ранее для клеток-хозяев, выбранных для экспрессии, и будут очевидны для специалиста в данной области техники.
В качестве типовых примеров подходящих хозяев могут быть указаны: бактериальные клетки, такие как E. coli, Bacillus subtilis, Salmonella typhimurium и разные виды родов Pseudomonas, Streptomyces и Staphylococcus; грибковые клетки, такие как дрожжи; клетки насекомых, такие как Drosophila и Sf9; клетки животных, такие как колонии COS-7 фибробластов почек обезьян, описанные у Gluzman, Cell 23:175 (1981), и другие колонии клеток, способные экспрессировать совместимый вектор, например, колонии клеток C127, 3T3, CHO, HeLa и BHK или меланомы Боуэса; клетки растений и т.д. Выбор подходящего хозяина считается находящимся в компетенции специалиста в данной области техники, исходя из изложенных здесь идей.
Также могут использоваться клетки-хозяева дрожжей, насекомых или млекопитающих, использующие подходящие векторы и регуляторные последовательности. Примеры систем экспрессии млекопитающих включают колонии COS-7 фибробластов почек обезьян, описанные у Gluzman, Cell 23:175 (1981), и другие колонии клеток, способные экспрессировать совместимый вектор, например, колонии клеток C127, 3T3, CHO, HeLa и BHK.
Полинуклеотиды, описанные в настоящем изобретении, могут вводиться и экспрессироваться в клетках человека (например, иммунных клетках, включая дендритные клетки). Таблица применения кодонов человека может использоваться в качестве руководства для выбора кодона для каждой аминокислоты. Такие полинуклеотиды содержат спейсерный аминокислотный остаток между эпитопами и/или аналогами, такими как описаны выше, или могут содержать существующие в природе фланкирующие последовательности, соседние к эпитопам и/или аналогам (и/или CTL (например, CD8+), Th (например, CD4+) и B-клеточными эпитопами).
Стандартные регуляторные последовательности, хорошо известные специалистам в данной области техники, могут быть включены в вектор для обеспечивания экспрессии в клетках-мишенях человека. Желательные несколько элементов вектора: промотор с нижележащим сайтом клонирования для полинуклеотида, например, вставкой минигена; сигнал полиаденилирования для эффективной терминации транскрипции; точка начала репликации E. coli; и селектируемый маркер E. coli (например, резистентность к ампициллину или канамицину). Множество промоторов могут использоваться для этой цели, например, промотор цитомегаловируса человека (hCMV). См., например, патенты США №№ 5,580,859 и 5,589,466 для других подходящих промоторных последовательностей. В некоторых вариантах осуществления, промотором является CMV-IE промотор.
Полезные векторы экспрессии эукариотических хозяев, особенно млекопитающих или человека, включают, например, векторы, содержащие последовательности контроля экспрессии из SV40, папилломавирус коровы, аденовирус и цитомегаловирус. Полезные векторы экспрессии для бактериальных хозяев включают известные бактериальные плазмиды, такие как плазмиды от Escherichia coli, включая pCR1, pBR322, pMB9 и их производные, плазмиды с более широким кругом хозяев, такие как M13 и фаги нитевидных одноцепочечных ДНК.
Векторы могут быть введены в ткани животных множеством разных способов. Два наиболее популярных подхода включают инъекцию ДНК в солевом растворе с применением стандартной гиподермальной иглы, доставку генной пушкой. Схематическое изображение конструкции плазмиды ДНК вакцины и ее последующая доставка этими двумя способами хозяину иллюстрирована в Scientific American (Weiner et al., (1999) Scientific American 281 (1): 34–41). Инъекцию в солевом растворе обычно проводят внутримышечно (ВМ) в скелетную мышцу, или внутрикожно (ВК) где ДНК доставляется во внеклеточные пространства. Этому может способствовать электропорация через временное повреждение мышечных волокон миотоксинами, такими как бупивакаин; или с применением гипертонических растворов солевого раствора или сахарозы (Alarcon et al., (1999). Adv. Parasitol. Advances in Parasitology 42: 343–410). На иммунные ответы на этот способ доставки могут влиять многие факторы, включая тип иглы, расположение иглы, скорость инъекции, объем инъекции, тип мышцы и возраст, под и физиологическое состояние животному, которому делают инъекцию (Alarcon et al., (1999). Adv. Parasitol. Advances in Parasitology 42: 343–410).
Доставка генной пушкой, другой широко используемый способ доставки, баллистически усиливает плазмидную ДНК (пДНК), которая адсорбирована на микрочастицы золота или вольфрама в клетках-мишенях, с применением сжатого гелия в качестве усилителя (Alarcon et al., (1999). Adv. Parasitol. Advances in Parasitology 42: 343–410; Lewis et al., (1999). Advances in Virus Research (Academic Press) 54: 129–88).
Альтернативные способы доставки могут включать аэрозольную инстилляцию голой ДНК на слизистые поверхности, такие как слизистая носа и легких (Lewis et al., (1999). Advances in Virus Research (Academic Press) 54: 129–88) и местное введение пДНК в глаз и на слизистую вагины (Lewis et al., (1999) Advances in Virus Research (Academic Press) 54: 129–88). Доставка на слизистую поверхность также достигается с применением катионных препаратов липосома-ДНК, биоразлагаемых микросфер, ослабленных векторов Shigella или Listeria для перорального введения на слизистую кишечника и рекомбинантные аденовирусные векторы. ДНК или РНК также могут доставляться в клетки после умеренного механического разрыва клеточной мембраны, временно пермеабилизируя клетки. Такой умеренный механический разрыв мембраны может проводиться осторожным проталкиванием клеток через мелкие отверстия (Sharei et al., Ex Vivo Cytosolic Delivery of Functional Macromolecules to Immune Cells, PLOS ONE (2015)).
Химические средства введения полинуклеотида в клетку-хозяина включают коллоидные дисперсионные системы, такие как макромолекулярные комплексы, наночастицы, сферы и системы на основе жиров, включая эмульсии масло-в-воде, мицеллы, смешанные мицеллы и липосомы. Типовой коллоидной системой для применения в качестве средства доставки in vitro и in vivo является липосома (например, искусственный мембранный пузырек). При применении не вирусной системы доставки, типовым средством доставки является липосома. “Липосома” является общим термином, охватывающим множество одно- и многослойных жировых носителей, образованных через создание замкнутых жировых бислоев или агрегатов. Липосомы могут характеризоваться как имеющие пузырчатые структуры с фосфолипидной двухслойной мембраной и внутренней водной средой. Многослойная липосома имеет множество жировых слоев, разделенных водной средой. Они образуются спонтанно при суспендировании фосфолипидов в избытке водного раствора. Жировые компоненты претерпевают само-реаранжировку до образования закрытых структур и улавливают воду и растворенные в ней вещества между жировыми бислоями (Ghosh et al., Glycobiology 5: 505-10 (1991)). Однако композиции, которые имеют структуры в растворе, отличные от нормальной пузырчатой структуры, также охватываются. Например, жиры могут принимать мицеллярную структуру или просто существовать в виде неоднородных агрегатов жировых молекул. Также рассматриваются комплексы липофектамин-нуклеиновая кислота.
Применение жировых составов рассматривается для введения нуклеиновых кислот в клетки-хозяева (in vitro, ex vivo или in vivo). В другом аспекте, нуклеиновая кислота может быть связана с жиром. Нуклеиновая кислота, связанная с жиром, может быть инкапсулирована в водную внутреннюю часть липосомы, диспергирована в жировом бислое липосомы, присоединены к липосоме через связующую молекулу, которая связана и с липосомой, и с олигонуклеотидом, уловлена в липосому, образовывать комплекс с липосомой, диспергирована в раствор, содержащий жир, смешана с жиром, объединена с жиром, содержаться в виде суспензии в жире, содержаться в или образовывать комплекс с мицеллой, или другим образом быть связанной с жиром. Композиции, связанные с жиром, жиром/ДНК или жиром/вектором экспрессии не ограничены какой-либо конкретной структурой в растворе. Например, они могут присутствовать в двухслойной структуре, в виде мицелл и с “разрушенной” структурой. Они также могут быть просто диспергированы в растворе, с возможным образованием агрегатов, которые неоднородны по размеру или форме. Жирами являются жирные вещества, которые могут существовать в природе, или синтетические жиры. Например, жиры включают жирные капли, которые в природе существуют в цитоплазме, а также класс соединений, который содержит длинноцепные алифатические углеводороды и их производные, такие как жирные кислоты, спирты, амины, аминоспирты и альдегиды.
Жиры, подходящие для применения, могут быть получены из коммерческих источников. Например, димиристилфосфатидилхолин (“DMPC”) может быть получен от Sigma, St. Louis, Mo.; дицетилфосфат (“DCP”) может быть получен от K & K Laboratories (Plainview, N.Y.); холестерин (“Choi”) может быть получен от Calbiochem-Behring; димиристилфосфатидилглицерин (“DMPG”) и другие жиры могут быть получены от Avanti Polar Lipids, Inc. (Birmingham, Ala.). Базовые растворы жиров в хлороформе или хлороформе/метаноле могут храниться при приблизительно -20°C. Хлороформ используют в качестве единственного растворителя, так как он более легко испаряется, чем метанол.
В некоторых вариантах осуществления, вектор содержит полинуклеотид, кодирующий первый пептид, содержащий первый неоэпитоп, и второй пептид, содержащий второй неоэпитоп. В некоторых вариантах осуществления, первый и второй пептиды получают из одного и того же белка. По меньшей мере два отдельных пептида могут варьировать по длине, аминокислотной последовательности или обоих. Пептиды получают из любого белка, про который известно или было обнаружено, что он содержит опухолеспецифическую мутацию. В некоторых вариантах осуществления, вектор содержит первый пептид, содержащий первый неоэпитоп белка, и второй пептид, содержащий второй неоэпитоп того же белка, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию. В некоторых вариантах осуществления, вектор содержит первый пептид, содержащий первый неоэпитоп первой области белка, и второй пептид, содержащий второй неоэпитоп второй области того же белка, где первая область содержит по меньшей мере одну аминокислоту второй области, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию. В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми. В некоторых вариантах осуществления, мутация выбрана из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутации «сдвига рамки», мутации сквозного прочитывания, мутации слияния генов и любой их комбинации.
В некоторых вариантах осуществления, вектор содержит полинуклеотид, функционально связанный с промотором. В некоторых вариантах осуществления, вектором является самоамплифицирующийся РНК репликон, плазмида, фаг, транспозон, космида, вирус или вирион. В некоторых вариантах осуществления, вектор получают из ретровируса, лентивируса, аденовируса, адено-ассоциированного вируса, герпесвируса, поксвируса, альфавируса, вируса осповакцины, вируса гепатита B, папилломавируса человека или его псевдотипа. В некоторых вариантах осуществления, вектором является не вирусный вектор. В некоторых вариантах осуществления, не вирусным вектором является наночастица, катионный жир, катионный полимер, металлический нанополимер, ноностержень, липосома, мицелла, микропузырек, пептид, способствующий проникновению в клетку, или липосфера.
Т-клеточные рецепторы
В одном аспекте, настоящее описание относится к клеткам, экспрессирующим неоантиген-распознающий рецептор, который активирует иммунореактивную клетку (например, Т-клеточный рецептор (TCR) или химерный антигенный рецептор (CAR)), и способы применения таких клеток для лечения заболевания, которое требует улучшенного иммунного ответа. Такие клетки включают генетически модифицированные иммунореактивные клетки (например, Т-клетки, естественные киллеры (NK), цитотоксические T лимфоциты (CTL (например, CD8+)), хелперные T лимфоциты (Th (например, CD4+))), экспрессирующие антиген-распознающий рецептор (например, TCR или CAR), который связывает один из неоантигенных пептидов, описанных в настоящем изобретении, и способы их применения для лечения новообразований и других патологий, при которых желательно повышение антиген-специфического иммунного ответа. Активация Т-клеток опосредована TCR или CAR направленных на антиген.
Настоящее описание относится к клеткам, экспрессирующим комбинацию антиген-распознающего рецептора, который активирует иммунореактивную клетку (например, TCR, CAR) и химерного костимулирующего рецептора (CCR), и способы применения таких клеток для лечения заболевания, которое требует усиленного иммунного ответа. В некоторых вариантах осуществления, специфические к опухолевому антигену Т-клетки, NK клетки, CTL клетки или другие иммунореактивные клетки используют в качестве челноков для селективного обогащения одного или нескольких костимулирующих лигандов для лечения или профилактики новообразований. Такие клетки вводят человеку, нуждающемуся в этом, для лечения или профилактики конкретного рака.
В некоторых вариантах осуществления, специфические к опухолевому антигену лимфоциты человека, которые могут использоваться в способах согласно настоящему описанию, включают, без ограничений, периферические донорные лимфоциты, генетически модифицированные для экспрессии химерных антигенных рецепторов (CAR) (Sadelain, M., et al. 2003 Nat Rev Cancer 3:35-45), периферические донорные лимфоциты, генетически модифицированные для экспрессии полноразмерного, распознающего опухолевый антиген комплекса Т-клеточного рецептора, содержащего a и p гетеродимер (Morgan, R. A., et al. 2006 Science 314:126-129), лимфоцитарные культуры, полученные из опухолей, инфильтрующих лимфоциты (TIL) в биопсиях опухоли (Panelli, M. C., et al. 2000 J Immunol 164:495-504; Panelli, M. C., et al. 2000 J Immunol 164:4382-4392) и селективно in vitro-размноженные антигенспецифические периферические лейкоциты крови, применяющие искусственные антигенпрезентирующие клетки (AAPC) или активированные дендритные клетки (Dupont, J., et al. 2005 Cancer Res 65:5417-5427; Papanicolaou, G. A., et al. 2003 Blood 102:2498-2505). Т-клетки могут быть аутологичными, аллогенными или полученными in vitro из сконструированного предшественника или стволовых клеток.
В некоторых вариантах осуществления, иммунотерапевтическим агентом является сконструированный рецептор. В некоторых вариантах осуществления, сконструированным рецептором является химерный антигенный рецептор (CAR), Т-клеточный рецептор (TCR), или B-клеточный рецептор (BCR), адоптивная Т-клеточная терапия (ACT) или их производное. В других аспектах, сконструированным рецептором является химерный антигенный рецептор (CAR). В некоторых аспектах, CAR является CAR первого поколения. В других аспектах, CAR является CAR второго поколения. В дополнительных других аспектах, CAR является CAR третьего поколения. В некоторых аспектах, CAR содержит внеклеточную часть, трансмембранную часть и внутриклеточную часть. В некоторых аспектах, внутриклеточная часть содержит по меньшей мере один Т-клеточный костимулирующий домен. В некоторых аспектах, Т-клеточный костимулирующий домен выбран из группы, состоящей из CD27, CD28, TNFRS9 (4-1BB), TNFRSF4 (OX40), TNFRSF8 (CD30), CD40LG (CD40L), ICOS, ITGB2 (LFA-1), CD2, CD7, KLRC2 (NKG2C), TNFRS18 (GITR), TNFRSF14 (HVEM) или любой их комбинации.
В некоторых аспектах, сконструированный рецептор связывает мишень. В некоторых аспектах, связывание является специфическим к пептиду, специфическому к одному или нескольким субъектам, страдающим заболеванием или состоянием.
В некоторых аспектах, иммунотерапевтическим агентом является клетка, подробно описанная здесь. В некоторых аспектах, иммунотерапевтическим агентом является клетка, содержащая рецептор, который специфически связывает пептид или неоэпитоп, описанный в настоящем изобретении. В некоторых аспектах, иммунотерапевтическим агентом является клетка, применяемая в комбинации с пептидами/нуклеиновыми кислотами настоящего описания. В некоторых вариантах осуществления, клеткой является клетка пациента. В некоторых вариантах осуществления, клеткой является Т-клетка. В некоторых вариантах осуществления, клеткой является лимфоцит, инфильтрирующий клетку.
В некоторых аспектах, субъекта с состоянием или заболеванием лечат на основе репертуара Т-клеточного рецептора субъекта. В некоторых вариантах осуществления, пептид или неоэпитоп выбирают на основе репертуара Т-клеточного рецептора субъекта. В некоторых вариантах осуществления, субъекта лечат Т-клетками, экспрессирующими TCR, специфические к пептиду или неоэпитопу, описанному в настоящем изобретении. В некоторых вариантах осуществления, субъекта лечат пептидом или неоэпитопом, специфическим к TCR, например, субъект-специфическим TCR. В некоторых вариантах осуществления, субъекта лечат пептидом или неоэпитопом, специфическим к Т-клеткам, экспрессирующим TCR, например, субъект-специфические TCR. В некоторых вариантах осуществления, субъекта лечат пептидом или неоэпитопом, специфическим к субъект-специфическим TCR.
В некоторых вариантах осуществления, композиции, описанные в настоящем изобретении, выбирают на основе TCR, идентифицированных у одного или нескольких субъектов. В некоторых вариантах осуществления, идентификацию репертуара Т-клетки и тестирование в функциональных анализах используют для определения композиции для введения одному или нескольким субъектам с состоянием или заболеванием. В некоторых вариантах осуществления, композицией является антигенная вакцина, содержащая один или более пептидов или белков, как описано в настоящем изобретении. В некоторых вариантах осуществления, вакцина содержит субъект-специфические неоантигенные пептиды. В некоторых вариантах осуществления, пептиды, включаемые в вакцину, выбирают на основе количественной оценки субъект-специфических TCR, которые связываются с неоэпитопами. В некоторых вариантах осуществления, пептиды выбирают на основе аффинности связывания пептида с TCR. В некоторых вариантах осуществления, выбор основан на комбинации и количества и аффинности связывания. Например, TCR, который сильно связывается с неоэпитопом в функциональном анализе, но который не представлены в высоких количествах в репертуаре TCR, может быть хорошим кандидатом для антигенной вакцины, так как Т-клетки, экспрессирующие TCR, будут преимущественно амплифицированы.
В некоторых вариантах осуществления, пептид или белок выбирают для введения одному или нескольким субъектам на основе связывания с TCR. В некоторых вариантах осуществления, Т-клетки, такие как Т-клетки от субъекта с заболеванием или состоянием, могут быть размножены. Размноженные Т-клетки, которые экспрессируют TCR, специфические к неоантигенному пептиду или неоэпитопу, могут вводиться обратно субъекту. В некоторых вариантах осуществления, подходящие клетки, например, PBMC, трансдуцируют или трансфицируют полинуклеотидами для экспрессии TCR, специфических к неоантигенному пептиду или неоэпитопу, и вводят субъекту. Т-клетки, экспрессирующие TCR, специфические к неоантигенному пептиду или неоэпитопу, могут быть размножены и введены обратно субъекту. В некоторых вариантах осуществления, Т-клетки, экспрессирующие TCR, специфические к неоантигенному пептиду или неоэпитопу, которые вызывают цитолитическую активность при инкубировании с аутологичными болезненными тканями, могут быть размножены и введены субъекту. В некоторых вариантах осуществления, Т-клетки, используемые в функциональных анализах, приводящих к связыванию с неоантигенным пептидом или неоэпитопом, могут быть размножены и введены субъекту. В некоторых вариантах осуществления, TCR, которые определены как связывающиеся со специфическими неоантигеными пептидами или неоэпитопами субъекта, могут быть экспрессированы в Т-клетках и введены субъекту.
В варианте осуществления, настоящее описание относится к композиция, содержащая первый пептид, содержащий первый неоэпитоп, и второй пептид, содержащий второй неоэпитоп, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию. В некоторых вариантах осуществления, композиция, представленная здесь, содержит первую Т-клетку содержащую первый Т-клеточный рецептор (TCR), специфический к первому неоэпитопу, и вторую Т-клетку, содержащую второй TCR, специфический к второму неоэпитопу. В некоторых вариантах осуществления, первый и второй пептиды получены из одного и того же белка.
В другом варианте осуществления, настоящее описание относится к композиции, содержащей первый пептид, содержащий первый неоэпитоп первой области белка, и второй пептид, содержащий второй неоэпитоп второй области того же белка, где первая область содержит по меньшей мере одну аминокислоту второй области, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию. В некоторых вариантах осуществления, композиция, представленная в настоящем изобретении, содержит первую Т-клетку, содержащую первый Т-клеточный рецептор (TCR), специфический к первому неоэпитопу, и вторую Т-клетку, содержащую второй TCR, специфический к второму неоэпитопу. В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми.
В некоторых вариантах осуществления, первый неоэпитоп связывается с HLA белком I класса с образованием комплекса HLA-пептид I класса. В некоторых вариантах осуществления, первый неоэпитоп связывается с HLA белком II класса с образованием комплекса HLA-пептид II класса. В некоторых вариантах осуществления, второй неоэпитоп связывается с HLA белком II класса с образованием комплекса HLA-пептид II класса. В некоторых вариантах осуществления, второй неоэпитоп связывается с HLA белком I класса с образованием комплекса HLA-пептид I класса. В некоторых вариантах осуществления, первый неоэпитоп активирует CD8+ Т-клетки. В некоторых вариантах осуществления, первый неоэпитоп активирует CD4+ Т-клетки. В некоторых вариантах осуществления, второй неоэпитоп активирует CD4+ Т-клетки. В некоторых вариантах осуществления, второй неоэпитоп активирует CD8+ Т-клетки. В некоторых вариантах осуществления, TCR CD4+ Т-клетки связывается с комплексом HLA-пептид II класса. В некоторых вариантах осуществления, TCR CD8+ Т-клетки связывается с комплексом HLA-пептид II класса. В некоторых вариантах осуществления, TCR CD8+ Т-клетки связывается комплексом HLA-пептид I класса. В некоторых вариантах осуществления, TCR CD4+ Т-клетки связывается комплексом HLA-пептид I класса.
В некоторых вариантах осуществления, первым TCR является первый химерный антигенный рецептор, специфический к первому неоэпитопу, и вторым TCR является второй химерный антигенный рецептор, специфический к второму неоэпитопу. В некоторых вариантах осуществления, первой Т-клеткой является цитотоксическая Т-клетка. В некоторых вариантах осуществления, первой Т-клеткой является гамма дельта Т-клетка. В некоторых вариантах осуществления, второй Т-клеткой является хелперная Т-клетка. В некоторых вариантах осуществления, первый и/или второй TCR связывается с комплексом HLA-пептид с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй TCR связывается с комплексом HLA I класса-пептид с KD или IC50 менее чем 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ. В некоторых вариантах осуществления, первый и/или второй TCR связывается с комплексом HLA II класса-пептид с KD или IC50 менее чем 2000, 1500, 1000 нМ, 900 нМ, 800 нМ, 700 нМ, 600 нМ, 500 нМ, 250 нМ, 150 нМ, 100 нМ, 50 нМ, 25 нМ или 10 нМ.
Антигенпрезентирующие клетки
Неоантигенный пептид или белок может быть представлен в виде антигенпрезентирующих клеток (например, дендритных клеток), содержащих такие пептиды, белки или полинуклеотиды, как описано в настоящем изобретении. В других вариантах осуществления, такие антигенпрезентирующие клетки используют для стимулирования Т-клеток для применения у пациентов. Таким образом, одним из вариантов осуществления настоящего описания является композиция, содержащая, по меньшей мере одну антигенпрезентирующую клетку (например, дендритную клетку), которая активирована или загружена с одним или несколькими неоантигенными пептидами или полинуклеотидами, описанными в настоящем изобретении. В некоторых вариантах осуществления, такие APC является аутологическими (например, аутологическими дендритными клетками). Альтернативно, мононуклеарные клетки периферической крови (PBMC), выделенные у пациента, могут быть загружены неоантигенными пептидами или полинуклеотидами ex vivo. В близких вариантах осуществления, такие APC или PBMC вводят инъекцией обратно пациенту. В некоторых вариантах осуществления, антигенпрезентирующими клетками являются дендритные клетки. В близких вариантах осуществления, дендритными клетками являются аутологические дендритные клетки, которые активированы неоантигенным пептидом или нуклеиновой кислотой. Неоантигенным пептидом может быть любой подходящий пептид, который вызывает подходящий Т-клеточный ответ. Т-клеточная терапия с применением аутологических дендритных клетках, активированных пептидами из опухольассоциированного антигена, описана у Murphy et al. (1996) Prostate 29, 371-380 и Tjua et al. (1997) Prostate 32, 272-278. В некоторых вариантах осуществления, Т-клеткой является CTL (например, CD8+).В некоторых вариантах осуществления, Т-клеткой является хелперный T лимфоцит (Th (например, CD4+)).
В некоторых вариантах осуществления, настоящее описание относится к композиции, содержащей иммуногенную фармацевтическую композицию на основе клеток, которая также может вводиться субъекту. Например, иммуногенная фармацевтическая композиция на основе антигенпрезентирующей клетки (APC) может быть составлена с применением любых хорошо известных методов, носителей и эксципиентов, как подходит и как понимается в данной области техники. APC включают моноциты, клетки, полученные из моноцитов, макрофаги и дендритные клетки. Иногда, иммуногенной фармацевтической композицией на основе APC может быть иммуногенная фармацевтическая композиция на основе дендритной клетки.
Иммуногенная фармацевтическая композиция на основе дендритной клетки может быть получена любыми способами, известными в данной области техники. В некоторых случаях, иммуногенные фармацевтические композиции на основе дендритной клетки могут быть получены ex vivo или in vivo способом. Ex vivo способ может включать применение аутологических DC, активированных ex vivo полипептидами, описанными в настоящем изобретении, для активации иди загрузки DC до введения пациенту. In vivo способ может включать направленные специфические DC рецепторы, применяющие антитела, сопряженные с полипептидами, описанными в настоящем изобретении. Иммуногенная фармацевтическая композиция на основе DC может дополнительно содержать активаторы DC, такие как TLR3, TLR-7-8 и CD40 агонисты. Иммуногенная фармацевтическая композиция на основе DC может дополнительно содержать адъюванты и фармацевтически приемлемый носитель.
Антигенпрезентирующие клетки (APC) могут быть получены из множества источников, включая человека и приматов, отличных от человека, других млекопитающих и позвоночных. В некоторых вариантах осуществления, APC могут быть получены из крови человека или позвоночного, отличного от человека. APC также могут быть выделены из обогащенной популяции лейкоцитов. Популяции лейкоцитов могут быть получены способами, известными специалистам в данной области техники. Такие способы обычно включают сбор гепаринизированной крови, аферез или лейкоферез, получение лейкоцитарной пленки, розеткообразование, центрифугирование, центрифугирование с градиентом плотности (например, с применением Фиколла, частиц коллоидного диоксида кремния и сахарозы), дифференциальный лизис клеток, отличных от лейкоцитов, и фильтрацию. Популяция лейкоцитов также может быть получена сбором крови у субъекта, дефибриллированием для удаления тромбоцитов и лизированием красных клеток крови. Популяция лейкоцитов необязательно может быть обогащена предшественниками моноцитарных дендритнных клеток.
Популяции клеток крови могут быть получены от множества субъектов, согласно желаемому применению обогащенной популяции лейкоцитов. Субъектом может быть здоровый субъект. Альтернативно, клетки крови могут быть получены у субъекта, нуждающегося в иммуностимулировании, такого как, например, онкологический пациент или другой пациент, для которого иммуностимулирование будет полезным. Также, клетки крови могут быть получены у субъекта, нуждающегося в подавлении иммунитета, такого как, например, пациент, имеющий аутоиммунное расстройство (например, ревматоидный артрит, диабет, волчанку, рассеянный склероз и подобные). Популяция лейкоцитов также может быть получена от HLA-подходящего здорового индивидуума.
Когда кровь используют в качестве источника APC, лейкоциты крови могут быть получены с применением обычных способов, которые сохраняют их жизнеспособность. Согласно одному аспекту настоящего описания, кровь может быть разведена в среде, которая может содержать или не содержать гепарин или другой подходящий антикоагулянт. Объем крови к среде может быть приблизительно 1 к 1. Клетки могут быть концентрированы центрифугированием крови в среде при приблизительно 1000 об./мин. (150 g) при 4°C. Тромбоциты и красные клетки крови могут быть обеднены ресуспендированием клеток в любом количестве растворов, известных в данной области техники, которые будут лизировать эритроциты, например, хлориде аммония. Например, смесью может быть среда и хлорид аммония в соотношении приблизительно 1:1 по объему. Клетки могут быть концентрированы центрифугированием и промыты в желаемом растворе до получения популяции лейкоцитов, по существу не содержащей тромбоциты и красные клетки крови. Любой изотонический раствор, обычно используемый при культивировании ткани, может использоваться в качестве среды для отделения лейкоцитов крови от тромбоцитов и красных клеток крови. Примерами таких изотонических растворов могут быть физиологический раствор с фосфатным буфером, сбалансированный солевой раствор Хэнка и полная среда роста. APC и/или предшественники также могут быть очищены элютриацией.
В одном варианте осуществления, APC могут быть не номинальные APC в воспалительных или другим образом активированных условиях. Например, не номинальные APC могут включать эпителиальные клетки, стимулированные интерфероном-гамма, Т-клетки, B клетки и/или моноциты, активированные факторами или условиями, которые вызывают активность APC. Такие не номинальные APC могут быть получены способами, известными в данной области техники.
APC могут быть культивированными, размноженными, дифференцированными и/или созревшими, при желании, согласно типу APC. APC могут быть культивированы в любом подходящем сосуде для культивирования, таком как, например, культуральные планшеты, колбы, культуральные мешки и биореакторы.
В некоторых вариантах осуществления, APC могут быть культивированы в подходящей среде для культивирования или выращивания для сохранения и/или увеличения количества APC в препарате. Культуральная среда может быть выбрана согласно типу выделенных APC. Например, зрелые APC, такие как зрелые дендритные клетки, могут быть культивированы в среде для выращивания, подходящей для их сохранения и размножения. В культуральную среду могут быть добавлены аминокислоты, витамины, антибиотики, двухвалентные катионы и подобные. Кроме того, цитокины, факторы роста и/или гормоны могут быть включены в среду для выращивания. Например, для сохранения и/или размножения зрелых дендритных клеток, могут быть добавлены цитокины, такие как гранулоцитарный/макрофаговый колониестимулирующий фактор (GM-CSF) и/или интерлейкин 4 (IL-4). В других вариантах осуществления, незрелые APC могут быть культивированы и/или размножены. Незрелые дендритные клетки могут сохранять способность поглощать мРНК-мишень и процессировать новый антиген. В некоторых вариантах осуществления, незрелые дендритные клетки могут быть культивированы в среде, подходящей для их сохранения и культивирования. В культуральную среду могут быть добавлены аминокислоты, витамины, антибиотики, двухвалентные катионы и подобные. Кроме того, цитокины, факторы роста и/или гормоны могут быть включены в среду для выращивания.
Другие незрелые APC также могут быть культивированы или размножены. Препараты незрелых APC могут быть оставлены дозревать для получения зрелых APC. Созревание APC может происходить во время или после обработки неоантигенными пептидами. В некоторых вариантах осуществления, препараты незрелых дендритных клеток могут быть оставлены для созревания. Подходящие факторы созревания включают, например, цитокины TNF-α, бактериальные продукты (например, BCG) и подобные. В другом аспекте, выделенные предшественники APC могут использоваться для получения препаратов незрелых APC. Предшественники APC могут быть культивированы, дифференцированы и/или оставлены созревать. В некоторых вариантах осуществления, предшественники моноцитарных дендритных клеток могут быть культивированы в присутствии подходящей культуральной среды с добавлением аминокислот, витаминов, цитокинов и/или двухвалентных катионов для того, чтобы способствовать дифференциации предшественников моноцитарных дендритных клеток в незрелые дендритные клетки. В некоторых вариантах осуществления, предшественники APC выделяют из PBMC. PBMC могут быть получены от донора, например, донора-человека, и могут использоваться свежими или замораживаться для будущего применения. В некоторых вариантах осуществления, APC получают из одного или нескольких препаратов APC. В некоторых вариантах осуществления, APC содержит APC, загруженную первым и вторым неоантигенными пептидами, содержащими первый и второй неоэпитопы, или полинуклеотидами, кодирующими первый и второй неоантигенные пептиды, содержащие первый и второй неоэпитопы. В некоторых вариантах осуществления, APC является аутологическая APC, аллогенная APC или искусственная APC.
В варианте осуществления, настоящее описание относится к композиции, содержащей APC, содержащую первый пептид, содержащий первый неоэпитоп, и второй пептид, содержащий второй неоэпитоп, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию. В некоторых вариантах осуществления, первый и второй пептиды получают из одного и того же белка. В другом варианте осуществления, настоящее описание относится к композиции, содержащей APC, содержащую первый пептид, содержащий первый неоэпитоп первой области белка, и второй пептид, содержащий второй неоэпитоп второй области того же белка, где первая область содержит по меньшей мере одну аминокислоту второй области, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию. В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми.
Адъюванты
Адъювант может использоваться для улучшения иммунного ответа (гуморального и/или клеточного), вызываемого у пациента, получающего композицию, представленную здесь. Иногда адъюванты могут вызвать ответ Th1-типа. В другое время, адъюванты могут вызвать ответ Th2-типа. Ответ Th1-типа может быть охарактеризован продуцированием цитокинов, таких как IFN-γ, в отличие от ответа Th2-типа, который может быть охарактеризован продуцированием цитокинов, таких как IL-4, IL-5 и IL-10.
В некоторых аспектах, адъюванты на основе жира, такие как MPLA и MDP, могут использоваться с иммуногенными фармацевтическими композициями, описанными в настоящем изобретении. Монофосфорил-липид (MPLA), например, является адъювантом, который вызывает повышенное презентирование липосомального антигена к специфическим T лимфоцитам. Кроме того, мурамилдипептид (MDP) также может использоваться в качестве подходящего адъюванта в сочетании с иммуногенными фармацевтическими составами, описанными в настоящем изобретении.
Подходящие адъюванты известны в данной области техники (см., WO 2015/095811) и включают, но не ограничены ими, поли(I:C), поли-ICLC, Хиотонол, агонист STING, 1018 ISS, соли алюминия, Ампливакс, AS15, BCG, CP-870,893, CpG7909, CyaA, dSLIM, GM-CSF, IC30, IC31, Имиквимод, ImuFact IMP321, IS Patch, ISS, ISCOMATRIX, JuvImmune, LipoVac, MF59, монофосфорил-липид A, Монтанид IMS 1312, Монтанид ISA 206, Монтанид ISA 50V, Монтанид ISA-51, OK-432, OM-174, OM-197-MP-EC, ONTAK, PepTel®, системы векторов, PLG микрочастицы, резиквимод, SRL172, виросомы и другие вирусоподобные частицы, YF-17D, VEGF ловушку, R848, бета-глюкан, Pam3Cys, Pam3CSK4, Aquila’s QS21 стимулон (Aquila Biotech, Worcester, Mass., USA), который получают из сапонина, микобактериальные экстракты и синтетические миметики стенки бактериальной клетки, и другие подходящие адъюванты, такие как Ribi’s Detox, Quil или Superfos. Адъюванты также включают неполный адьювант Фрейнда или GM-CSF. Несколько иммунологических адъювантов (например, MF59), специфических к дендритным клеткам, и их получение было описано ранее (Dupuis M, et al., Cell Immunol. 1998; 186(1):18-27; Allison C; Dev. Biol. Stand. 1998; 92:3-11) (Mosca et al. Frontiers in Bioscience, 2007; 12:4050-4060) (Gamvrellis et al. Immunol & Cell Biol. 2004; 82: 506-516). Также могут использоваться цитокины. Несколько цитокинов были непосредственно связаны для влияния на миграцию дендритных клеток в лимфоидные ткани (например, TNF-альфа), усиливая созревание дендритных клеток в эффективные антигенпрезентирующие клетки для T-лимфоцитов (например, GM-CSF, PGE1, PGE2, IL-1, IL-1b, IL-4, IL-6 и CD40L) (патент США № 5,849,589, включенный сюда в качестве ссылки полностью) и действуя как иммуноадъюванты (например, IL-12) (Gabrilovich D I, et al., J. Immunother. Emphasis Tumor Immunol. 1996 (6):414-418).
Адъювант также может содержать стимулирующие молекулы, такие как цитокины. Не ограничивающие примеры цитокинов включают: CCL20, a-интерферон (IFN-a), β-интерферон (IFN-β), γ-интерферон, фактор роста тромбоцитов (PDGF), TNFα, TNFβ (лимфотоксин альфа (LTα)), GM-CSF, эпидермальный фактор роста (EGF), привлекающий кожные Т-клетки хемокин (CTACK), эпителиальный хемокин, экспрессированный в вилочковой железе (TECK), ассоциированный со слизистыми эпителиальный хемокин (MEC), IL-12, IL-15, IL-28, MHC, CD80, CD86, IL-1, IL-2, IL-4, IL-5, IL-6, IL-10, IL-18, MCP-1, MIP-la, MIP-1-, IL-8, L- селектин, P-селектин, E-селектин, CD34, GlyCAM-1, MadCAM-1, LFA-1, VLA-1, Mac-1, pl50,95, PECAM, ICAM-1, ICAM-2, ICAM-3, CD2, LFA-3, M-CSF, G-CSF, мутантные формы IL-18, CD40, CD40L, фактор роста сосудов, фактор роста фибробластов, IL-7, фактор роста нервов, фактор роста сосудов эндотелия, Fas, TNF рецептор, Fit, Apo-1, p55, WSL-1, DR3, TRAMP, Apo-3, AIR, LARD, NGRF, DR4, DRS, KILLER, TRAIL-R2, TRICK2, DR6, Каспазу ICE, Fos, c-jun, Sp-1, Ap-1, Ap-2, p38, p65Rel, MyD88, IRAK, TRAF6, IκB, неактивный NIK, SAP K, SAP-I, JNK, гены ответа интерферона, NFκB, Bax, TRAIL, TRAILrec, TRAILrecDRC5, TRAIL-R3, TRAIL-R4, RANK, RANK ЛИГАНД, Ox40, Ox40 ЛИГАНД, NKG2D, MICA, MICB, NKG2A, NKG2B, NKG2C, NKG2E, NKG2F, TAPI, и TAP2.
Дополнительные адъюванты включают: MCP-1, MIP-la, MIP-lp, IL-8, RANTES, L-селектин, P-селектин, E-селектин, CD34, GlyCAM-1, MadCAM-1, LFA-1, VLA-1, Mac-1, pl50,95, PECAM, ICAM-1, ICAM-2, ICAM-3, CD2, LFA-3, M-CSF, G-CSF, IL-4, мутантные формы IL-18, CD40, CD40L, фактор роста сосудов, фактор роста фибробластов, IL-7, IL-22, фактор роста нервов, фактор роста сосудов эндотелия, Fas, TNF рецептор, Fit, Apo-1, p55, WSL-1, DR3, TRAMP, Apo-3, AIR, LARD, NGRF, DR4, DR5, KILLER, TRAIL-R2, TRICK2, DR6, Caspase ICE, Fos, c-jun, Sp-1, Ap-1, Ap-2, p38, p65Rel, MyD88, IRAK, TRAF6, IκB, неактивный NIK, SAP K, SAP-1, JNK, гены ответа интерферона, NFκB, Bax, TRAIL, TRAILrec, TRAILrecDRC5, TRAIL-R3, TRAIL-R4, RANK, RANK ЛИГАНД, Ox40, Ox40 ЛИГАНД, NKG2D, MICA, MICB, NKG2A, NKG2B, NKG2C, NKG2E, NKG2F, TAP1, TAP2 и их функциональные фрагменты.
В некоторых аспектах, адъювантом может быть модулятор толл-подобного рецептора. Примеры модуляторов толл-подобных рецепторов включают TLR-9 агонисты и не ограничены низкомолекулярными модуляторами толл-подобных рецепторов, таких как Имиквимод. Другие примеры адъювантов, которые используются в комбинации с иммуногенными фармацевтическими композициями, описанными в настоящем изобретении, могут включать и не ограничены ими, сапонин, CpG ODN и подобные. Иногда адъювант выбран из бактериальных токсоидов, полиоксипропиленового-полиоксиэтиленового блокполимера, солей алюминия, липосом, CpG полимера, эмульсий масло-в-воде или их сочетания. Иногда адъювантом является эмульсия масло-в-воде. Эмульсия масло-в-воде может включать, по меньшей мере одно масло и по меньшей мере одно поверхностно-активное вещество, где масло(а) и поверхностно-активное вещество(а) являются биоразлагаемыми (метаболизируемыми) и биосовместимыми. Капли масла в эмульсии могут быть менее чем 5 мкм в диаметре, и даже могут иметь субмикронный диаметр, где такие маленькие размеры достигаются с применением микрофлюидизатора с получением стабильных эмульсий. Капли с размером менее 220 нм могут быть подвергнуты стерилизации фильтрацией.
Способы лечения и фармацевтические композиции
Неоантигенные терапевтические агенты (например, пептиды, полинуклеотиды, TCR, CAR, клетки, содержащие TCR или CAR, APC или дендритные клетки, содержащие полипептид, дендритные клетки, содержащие полинуклеотид, антитело, и т.д.), описанные в настоящем изобретении, используют во множестве областей, включая, но не ограничиваясь ими, терапевтические способы лечения, такие как лечение рака. В некоторых вариантах осуществления, терапевтические способы лечения включают иммунотерапию. В некоторых вариантах осуществления, неоантигенный пептид используют для активации, стимуляции, повышения и/или усиления иммунного ответа, перенаправления существующего иммунного ответа на новую мишень, повышения иммуногенности опухоли, ингибирования роста опухоли, снижения объема опухоли, повышения апоптоза опухолевых клеток и/или снижения онкогенности опухоли. Способами применения могут быть in vitro, ex vivo или in vivo способы.
В некоторых аспектах, настоящее описание относится к способам активации иммунного ответа у субъекта с использованием неоантигенного пептида или белка, описанного в настоящем изобретении. В некоторых вариантах осуществления, настоящее описание относится к способам стимуляции иммунного ответа у субъекта с использованием неоантигеного пептида, описанного в настоящем изобретении. В некоторых вариантах осуществления, настоящее описание относится к способам повышения иммунного ответа у субъекта с использованием неоантигеного пептида, описанного в настоящем изобретении. В некоторых вариантах осуществления, настоящее описание относится к способам усиления иммунного ответа с использованием неоантигенного пептида. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает повышение опосредованного клеткой иммунитета. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает повышение активности Т-клетки или гуморального иммунитета. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает повышение активности CTL или Th. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает повышение активности NK клетки. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает повышение активности Т-клетки и повышение активности NK клетки. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает повышение активности CTL и повышение активности NK клетки. В некоторых вариантах осуществления, активация, стимуляция, повышение и/или улучшение иммунного ответа включает ингибирование или снижение подавляющей активности T регуляторных (Treg) клеток. В некоторых вариантах осуществления, иммунный ответ является результатом антигенной стимуляции. В некоторых вариантах осуществления, антигенной стимуляцией является опухолевая клетка. В некоторых вариантах осуществления, антигенной стимуляцией является рак.
В некоторых вариантах осуществления, настоящее описание относится к способам активации, стимуляции, повышения и/или улучшения иммунного ответа с использованием неоантигенного пептида, описанного в настоящем изобретении. В некоторых вариантах осуществления, способ включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного пептида, который доставляет неоантигенный пептид или полинуклеотид в опухолевую клетку. В некоторых вариантах осуществления, способ содержит введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного пептида, поглощенного опухолевой клеткой. В некоторых вариантах осуществления, способ содержит введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного пептида, который поглощается опухолевой клеткой, и неоантигеный пептид процессируется клеткой. В некоторых вариантах осуществления, способ содержит введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного полипептида, который поглощается опухолевой клеткой, и неоэпитоп присутствует на поверхности опухолевой клетки. В некоторых вариантах осуществления, способ содержит введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного полипептида, который поглощается опухолевой клеткой, процессированного клеткой, и антигенный пептид присутствует на поверхности опухолевой клетки.
В некоторых вариантах осуществления, способ включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного пептида или полинуклеотида, описанного в настоящем изобретении, который доставляет экзогенный полипептид, содержащий, по меньшей мере один неоантигенный пептид, в опухолевую клетку, где по меньшей мере один неоэпитоп, полученный из неоантигеного пептида, присутствует на поверхности опухолевой клетки. В некоторых вариантах осуществления, антигенный пептид присутствует на поверхности опухолевой клетки в комплексе с молекулой MHC I класса. В некоторых вариантах осуществления, неоэпитоп присутствует на поверхности опухолевой клетки в комплексе с молекулой MHC II класса.
В некоторых вариантах осуществления, способ включает контактирование опухолевой клетки с неоантигенным полипептидом или полинуклеотидом, описанным в настоящем изобретении, который доставляет экзогенный полипептид, содержащий, по меньшей мере один неоантигенный пептид, в опухолевую клетку, где по меньшей мере один неоэпитоп, полученный из по меньшей мере одного неоантигенного пептида, присутствует на поверхности опухолевой клетки. В некоторых вариантах осуществления, неоэпитоп присутствует на поверхности опухолевой клетки в комплексе с молекулой MHC I класса. В некоторых вариантах осуществления, неоэпитоп присутствует на поверхности опухолевой клетки в комплексе с молекулой MHC II класса.
В некоторых вариантах осуществления, способ включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного полипептида или полинуклеотида, описанного в настоящем изобретении, который доставляет экзогенный полипептид, содержащий, по меньшей мере один антигенный пептид в опухолевую клетку, где неоэпитоп присутствует на поверхности опухолевой клетки и вызывает иммунный ответ против опухолевой клетки. В некоторых вариантах осуществления, иммунный ответ против опухолевой клетки повышается. В некоторых вариантах осуществления, неоантигенный полипептид или полинуклеотид доставляет экзогенный полипептид, содержащий, по меньшей мере один неоантигенный пептид в опухолевую клетку, где неоэпитоп присутствует на поверхности опухолевой клетки и ингибирует рост опухоли.
В некоторых вариантах осуществления, способ включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества неоантигенного полипептида или полинуклеотида, описанного в настоящем изобретении, который доставляет экзогенный полипептид, содержащий, по меньшей мере один неоантигенный пептид в опухолевую клетку, где неоэпитоп, полученный из по меньшей мере одного неоантигенного пептида, присутствует на поверхности опухолевой клетки и вызывает цитолиз Т-клетки, направленный против опухолевой клетки. В некоторых вариантах осуществления, цитолиз Т-клетки, направленный против опухолевой клетки, усиливается. В некоторых вариантах осуществления, цитолиз Т-клетки, направленный против опухолевой клетки, повышается.
В некоторых вариантах осуществления, способ повышения иммунного ответа у субъекта включает введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, описанного в настоящем изобретении, где агентом является антитело, которое специфически связывает неоантиген, описанный в настоящем изобретении. В некоторых вариантах осуществления, способ повышения иммунного ответа у субъекта включает введение субъекту терапевтически эффективного количества антитела.
Настоящее описание относится к способам перенаправления существующего иммунного ответа на опухоль. В некоторых вариантах осуществления, способ перенаправления существующего иммунного ответа на опухоль включает введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, описанного в настоящем изобретении. В некоторых вариантах осуществления, существующий иммунный ответ направлен против вируса. В некоторых вариантах осуществления, вирус выбран из группы, состоящей из: вируса кори, вируса варицелла-зостер (VZV; вируса ветряной оспы), вируса гриппа, вируса паротита, полиовируса, вируса краснухи, ротавируса, вируса гепатита (HAV), вируса гепатита B (HBV), вируса Эпштейна-Барра (EBV) и цитомегаловируса (CMV). В некоторых вариантах осуществления, вирусом является вирус варицелла-зостер. В некоторых вариантах осуществления, вирусом является цитомегаловирус. В некоторых вариантах осуществления, вирусом является вирус кори. В некоторых вариантах осуществления, существующий иммунный ответ был приобретен после природной вирусной инфекции. В некоторых вариантах осуществления, существующий иммунный ответ был приобретен после вакцинации против вируса. В некоторых вариантах осуществления, существующий иммунный ответ является клеточно-опосредованным ответом. В некоторых вариантах осуществления, существующий иммунный ответ содержит цитотоксические Т-клетки (CTLs) или Th клетки.
В некоторых вариантах осуществления, способ перенаправления существующего иммунного ответа на опухоль включает введение слитого белка, содержащего (i) антитело, которое специфически связывает неоантиген, и (ii) по меньшей мере один неоантигенный пептид, описанный в настоящем изобретении, где (a) слитый белок поглощен опухолевой клеткой после связывания с опухолеассоциированным антигеном или неоэпитопом; (b) неоантигенный пептид процессирован и презентирован на поверхности опухолевой клетки связанным молекулой MHC I класса; и (c) комплекс неоантигенный пептид/MHC I класса распознается цитотоксической Т-клеткой. В некоторых вариантах осуществления, цитотоксическими Т-клетками являются Т-клетки памяти. В некоторых вариантах осуществления, Т-клетки памяти являются результатом вакцинации неоантигенным пептидом.
Настоящее описание относится к способам повышения иммуногенности опухоли. В некоторых вариантах осуществления, способ повышения иммуногенности опухоли включает контакт опухоли или опухолевых клеток с эффективным количеством неоантигенного терапевтического агента, описанного в настоящем изобретении. В некоторых вариантах осуществления, способ повышения иммуногенности опухоли включает введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, описанного в настоящем изобретении.
Настоящее описание также относится к способам ингибирования роста опухоли с использованием неоантигенного терапевтического агента, описанного в настоящем изобретении. В некоторых вариантах осуществления, способ ингибирования роста опухоли включает контакт смеси клеток с неоантигенным терапевтическим агентом in vitro. Например, линию иммортализованных клеток или линию раковых клеток, смешанную с иммунными клетками (например, Т-клетками) культивируют в среде, в которую добавлен неоантигенный пептид. В некоторых вариантах осуществления, опухолевые клетки выделяют из образца пациента, например, биопсии ткани, плеврального выпота или образца крови, смешанного с иммунными клетками (например, Т-клетками), и культивируют в среде, к которой добавлен неоантигенный терапевтический агент. В некоторых вариантах осуществления, неоантигенный терапевтический агент повышает, стимулирует и/или улучшает активность иммунных клеток. В некоторых вариантах осуществления, неоантигенный терапевтический агент ингибирует рост опухолевой клетки. В некоторых вариантах осуществления, неоантигенный терапевтический агент активирует уничтожение опухолевых клеток.
В некоторых вариантах осуществления, субъектом является человек. В некоторых вариантах осуществления, субъект имеет опухоль или субъект имеет опухоль, которая была, по меньшей мере частично удалена.
В некоторых вариантах осуществления, способ ингибирования роста опухоли включает перенаправление существующего иммунного ответа на новую мишень, включающее введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, где существующий иммунный ответ направлен против антигенного пептида, доставленного в опухолевую клетку неоантигенным пептидом. В некоторых вариантах осуществления, способ лечения включает стадию идентификации одного или нескольких подтипов HLA, экспрессированных у субъекта до введения пептида так, что пептид связывается с по меньшей мере одним или несколькими подтипами HLA, специфически экспрессированными субъектом. В некоторых вариантах осуществления, если один несколько мутантных BTK пептидов, выбранных из таблицы 34, вводят субъекту, перед этим у субъекта определяют экспрессию подтипа HLA, соответствующего пептиду из таблицы 34, так, что введенный пептид связывается с по меньшей мере одним или несколькими подтипами HLA, специфически экспрессированными субъектом. В некоторых вариантах осуществления, способ включает определение того, что субъект экспрессирует белок, кодируемый HLA-C14:02 аллелем, HLA-C14:03 аллелем, HLA-A33:03 аллелем, HLA-C04:01 аллелем, HLA-B15:09 аллелем или HLA-B38:02 аллелем, где терапевтический агент содержит мутантный BTK пептид, имеющий аминокислотную последовательность EYMANGSLL (SEQ ID NO: 3207). В некоторых вариантах осуществления, если способ содержит определение того, что субъект экспрессирует белок, кодируемый любой из HLA-C02:02 аллели, HLA-C03:02 аллели, HLA-B53:01 аллели, HLA-C12:02 аллели, HLA-C12:03 аллели, HLA-A36:01 аллели, HLA-A26:01 аллели, HLA-A25:01 аллели, HLA-B57:01 аллели, HLA-A03:01 аллели, HLA-B46:01 аллели, HLA-B15:03 аллели, HLA-A33:03 аллели, HLA-B35:03 аллели или HLA-A11:01 аллели, где терапевтический агент содержит мутантный BTK пептид, имеющий аминокислотную последовательность MANGSLLNY (SEQ ID NO: 3208). В некоторых вариантах осуществления, способ содержит определение того, что субъект экспрессирует белок, кодируемый любой из HLA-A02:04 аллели, HLA-A02:03 аллели, HLA-C03:02 аллели, HLA-A03:01 аллели, HLA-A32:01 аллели, HLA-A02:07 аллели, HLA-C14:03 аллели, HLA-C14:02 аллели, HLA-A31:01 аллели, HLA-A30:02 аллели, HLA-A74:01 аллели, HLA-C06:02 аллели, HLA-B15:03 аллели, HLA-B46:01 аллели, HLA-B13:02 аллели, HLA-A25:01 аллели, HLA-A29:02 аллели или HLA-C01:02 аллели, где терапевтический агент содержит мутантный BTK пептид, имеющий аминокислотную последовательность SLLNYLREM (SEQ ID NO: 3209).
В некоторых вариантах осуществления, способ включает определение того, что субъект экспрессирует белок, кодируемый любой из HLA-B14:02 аллели, HLA-B49:01 аллели, HLA-B44:03 аллели, HLA-B44:02 аллели, HLA-B37:01 аллели, HLA-B15:09 аллели, HLA-B41:01 или HLA-B50:01 аллели, где терапевтический агент содержит мутантный BTK пептид, имеющий аминокислотную последовательность TEYMANGSL (SEQ ID NO: 3210).
В некоторых вариантах осуществления, опухоль содержит раковые стволовые клетки. В некоторых вариантах осуществления, частота раковых стволовых клеток в опухоли снижается введением неоантигенного терапевтического агента. В некоторых вариантах осуществления, представлен способ снижения частоты раковых стволовых клеток в опухоли у субъекта, включающий введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента.
Кроме того, в некоторых аспектах настоящее описание относится к способу снижения онкогенности опухоли у субъекта, включающему введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, описанного в настоящем изобретении. В некоторых вариантах осуществления, опухоль содержит раковые стволовые клетки. В некоторых вариантах осуществления, онкогенность опухоли снижается через снижение частоты раковых стволовых клеток в опухоли. В некоторых вариантах осуществления, способы включают применение неоантигенного терапевтического агента, описанного в настоящем изобретении. В некоторых вариантах осуществления, частота раковых стволовых клеток в опухоли снижается введением неоантигенного терапевтического агента, описанного в настоящем изобретении.
В некоторых вариантах осуществления, опухолью является солидная опухоль. В некоторых вариантах осуществления, опухолью является опухоль, выбранная из группы, состоящей из: колоректальной опухоли, опухоли поджелудочной железы, опухоли легкого, опухоли яичников, опухоли печени, опухоли молочной железы, опухоли почки, опухоли предстательной железы, нейроэндокринной опухоли, опухоли желудочно-кишечного тракта, меланомы, опухоли шейки матки, опухоли мочевого пузыря, глиобластомы и опухоли головы и шеи. В некоторых вариантах осуществления, опухолью является колоректальная опухоль. В некоторых вариантах осуществления, опухолью является опухоль яичников. В некоторых вариантах осуществления, опухолью является опухоль молочной железы. В некоторых вариантах осуществления, опухолью является опухоль легкого. В некоторых вариантах осуществления, опухолью является опухоль поджелудочной железы. В некоторых вариантах осуществления, опухолью является меланома. В некоторых вариантах осуществления, опухолью является солидная опухоль.
Настоящее описание также относится к способам лечения рака у субъекта, включающим введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, описанного в настоящем изобретении.
В некоторых вариантах осуществления, способ лечения рака включает перенаправление иммунного ответа на новую мишень, где способ включает введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, где существующий иммунный ответ направлен против антигенного пептида, доставленного в раковую клетку неоантигенным пептидом.
Настоящее описание относится к способам лечения рака, включающим введение субъекту терапевтически эффективного количества неоантигенного терапевтического агента, описанного в настоящем изобретении (например, субъекту, нуждающемуся в лечении). В некоторых вариантах осуществления, субъектом является человек. В некоторых вариантах осуществления, субъект имеет злокачественную опухоль. В некоторых вариантах осуществления, субъект имел опухоль, по меньшей мере частично удаленную.
Субъектами могут быть, например, млекопитающие, люди, беременные женщины, пожилые люди, взрослые, подростки, люди детско-юношеского возраста, дети, малыши, младенцы, новорожденные или новорожденные в возрасте до одного месяца. Субъектом может быть пациент. В некоторых случаях, субъектом может быть человек. В некоторых случаях, субъектом может быть ребенок (т.е. молодой человек до достижения половой зрелости). В некоторых случаях, субъектом может быть младенец. В некоторых случаях субъектом может быть младенец на искусственном вскармливании. В некоторых случаях, субъект может быть индивидуальный участник клинического исследования. В некоторых случаях, субъектом может быть лабораторное животное, например, млекопитающее или грызун. В некоторых случаях, субъектом может быть мышь. В некоторых случаях, субъект может иметь ожирение или лишний вес.
В некоторых вариантах осуществления, субъекта ранее лечили одним или несколькими различными способами лечения рака. В некоторых вариантах осуществления, субъекта ранее лечили одной или более из лучевой терапии, химиотерапии или иммунотерапии. В некоторых вариантах осуществления, субъекта лечили одним, двумя, три, четырьмя или пятью линиями предшествующей терапии. В некоторых вариантах осуществления, предшествующей терапией является цитотоксическая терапия.
В некоторых вариантах осуществления, раком является рак, выбранный из группы, состоящий из колоректального рака, рака поджелудочной железы, рака легких, рака яичников, рака печени, рака молочной железы, рака почки, рака предстательной железы, рака желудочно-кишечного тракта, меланомы, рака шейки матки, нейроэндокринного рака, рака мочевого пузыря, глиобластомы и рака головы и шеи. В некоторых вариантах осуществления, раком является рак поджелудочной железы. В некоторых вариантах осуществления, раком является рак яичников. В некоторых вариантах осуществления, раком является колоректальный рак. В некоторых вариантах осуществления, раком является рак молочной железы. В некоторых вариантах осуществления, раком является рак предстательной железы. В некоторых вариантах осуществления, раком является рак легких. В некоторых вариантах осуществления, раком является меланома. В некоторых вариантах осуществления, раком является солидный рак. В некоторых вариантах осуществления, рак содержит солидную опухоль.
В некоторых вариантах осуществления, раком является гематологический рак. В некоторых вариантах осуществления, рак выбран из группы, состоящей из: острого миелогенного лейкоза (AML), лимфомы Ходжкина, множественной миеломы, Т-клеточного острого лимфобластного лейкоза (Т-ALL), хронического лимфоцитарного лейкоза (CLL), волосатоклеточного лейкоза, хронического миелогенного лейкоза (CML), неходжкинской лимфомы, диффузной В-крупноклеточной лимфомы (DLBCL), мантийноклеточной лимфомы (MCL) и кожной Т-клеточной лимфомы (CTCL).
В некоторых вариантах осуществления, неоантигенный терапевтический агент вводят в виде комбинированной терапии. Комбинированная терапия двумя или несколькими терапевтическими агентами применяет агенты, которые работают через разные механизмы действия, хотя это не требуется. Комбинированная терапия с использованием агентов с разными механизмами действия может быть аддитивный или синергетический эффекты. Комбинированная терапия может позволить снизить дозу каждого агента, который используют в монотерапии, тем самым снижая токсические побочные эффекты и/или повышая терапевтический индекс агента(ов). Комбинированная терапия может снизить вероятность того, что разовьется резистетный рак. В некоторых вариантах осуществления, комбинированная терапия включает терапевтический агент, который влияет на иммунный ответ (например, улучшает или активирует ответ) и терапевтический агент, который влияет (например, ингибирует или уничтожает) на опухолевые/раковые клетки.
В некоторых случаях, иммуногенная фармацевтическая композиция может вводиться с дополнительным агентом. В некоторых вариантах осуществления, неоантигенный терапевтический агент может вводиться с иммунотерапией. Иммунотерапией может быть, например, антитело, направленное на иммунную контрольную точку. В некоторых вариантах осуществления, антителом является биспецифическое антитело. Выбор дополнительного агента может зависеть, по меньшей мере частично, от лечимого состояния. Дополнительный агент может включать, например, ингибитор иммунной контрольной точки, такой как анти-PD1, анти-CTLA4, анти-PD-L1, анти-CD40, или анти-TIM3 агент (например, анти-PD1, анти-CTLA4, анти-PD-L1, анти-CD40 или анти-TIM3 антитело); или любые агенты, оказывающие терапевтическое действие на патогенную инфекцию (например, вирусную инфекцию), включающие, например, лекарственные средства, используемые для лечения воспалительного состояния, такие как NSAID, например, ибупрофен, напроксен, ацетаминофен, кетопрофен или аспирин. Например, ингибитором иммунной контрольной точки может быть PD-1/PD-L1 антагонист, выбранный из группы, состоящей из: ниволумаба (ONO-4538/BMS-936558, MDX1 106, OPDIVO), пембролизумаба (MK-3475, KEYTRUDA), пидилизумаба (CT-011), и MPDL328OA (ROCHE). В качестве другого примера, составы могут дополнительно содержать одну или более добавок, таких как витамин C, E или другие антиоксиданты.
Способы описания могут использоваться для лечения любого вида рака, известного в данной области техники. Не ограничивающие примеры рака, подлежащего лечению способами настоящего описания, могут включать меланому (например, метастатическую злокачественную меланому), рак почек (например, светлоклеточную карциному), рак предстательной железы (например, гормонально-рефрактерную аденокарциному предстательной железы), аденокарциному поджелудочной железы, рак молочной железы, рак толстой кишки, рак легких (например, немелкоклеточный рак легких), рак пищевода, плоскоклеточную карциному головы и шеи, рак печени, рак яичников, рак шейки матки, рак щитовидной железы, глиобластому, глиому, лейкоз, лимфому и другие злокачественные новообразования.
Дополнительно, представленное здесь заболевание или состояние включает рефрактерные или рецидивирующие злокачественные образования, рост которых может быть ингибирован с использованием способов лечения настоящего описания. В некоторых вариантах осуществления, рак, лечимый способами лечения настоящего описания, выбран из группы, состоящей из карциномы, плоскоклеточной карциномы, аденокарциномы, саркомы, рака эндометрия, рака молочной железы, рака яичников, рака шейки матки, рака маточной трубы, первичного рака брюшины, рака толстой кишки, колоректального рака, плоскоклеточной карциномы аногенитальной области, меланомы, почечно-клеточной карциномы, рака легких, немелкоклеточного рака легких, плоскоклеточного рак легких, рака желудка, рака мочевого пузыря, рака желчного пузыря, рака печени, рака щитовидной железы, рака гортани, рака слюнных желез, рака пищевода, рака головы и шеи, глиобластомы, глиомы, плоскоклеточной карциномы головы и шеи, рака предстательной железы, рака поджелудочной железы, мезотелиомы, саркомы, гематологического рака, лейкоза, лимфомы, невромы и их комбинаций. В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, включает, например, карциному, плоскоклеточную карциному (например, цервикального канала, века, соединительной оболочки, влагалища, легкого, полости рта, кожи, мочевого пузыря, языка, гортани и пищевода) и аденокарциному (например, предстательной железы, тонкого кишечника, эндометрия, цервикального канала, толстой кишки, легкого, поджелудочной железа, глотки, прямой кишки, матки, желудка, молочной железы и яичника). В некоторых вариантах осуществления, рак, подлежащий лечению способами настоящего описания, дополнительно включает саркому (например, миогенную саркому), лейкоз, неврому, меланому и лимфому. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является рак молочной железы. В некоторых вариантах осуществления раком, подлежащим лечению способами лечения настоящего раскрытия, является трижды негативный рак молочной железы (TNBC). В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является рак яичника. В некоторых вариантах осуществления, раком, подлежащим лечению способами настоящего описания, является колоректальный рак.
В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащая лечению фармацевтической композицией настоящего описания, имеет солидную опухоль. В некоторых вариантах осуществления, солидной опухолью является меланома, почечно-клеточная карцинома, рак легких, рак мочевого пузыря, рак молочной железы, рак шейки матки, рак толстой кишки, рак желчного пузыря, рак гортани, рак печени, рак щитовидной железы, рак желудка, рак слюнной железы, рак предстательной железы, рак поджелудочной железы или карцинома из клеток Меркеля. В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащая лечению фармацевтической композицией настоящего описания, имеет гематологический рак. В некоторых вариантах осуществления, пациент имеет гематологический рак, такой как диффузная В-крупноклеточная лимфома (“DLBCL”), лимфома Ходжкина (“HL”), неходжкинская лимфома (“NHL”), фолликулярная лимфома (“FL”), острый миелоидный лейкоз (“AML”) или множественная миелома (“MM”). В некоторых вариантах осуществления, пациент или популяция пациентов, подлежащая лечению, имеет рак, выбранный из группы, состоящей из рака яичников, рака легких и меланомы.
Конкретные примеры рака, который можно предотвратить и/или лечить в соответствии с настоящим описанием, включают, но не ограничиваются ими, следующие: рак почек, рак почки, мультиформную глиобластому, метастатический рак молочной железы; карциному молочной железы; саркому молочной железы; нейрофиброму; нейрофиброматоз; детские опухоли; нейробластому; злокачественную меланому; карциномы эпидермиса; лейкозы, такие как, но не ограничиваясь ими, острый лейкоз, острый лимфоцитарный лейкоз, острый миелоцитарный лейкоз, такой как миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный, эритролейкозный лейкоз и миелодиспластический синдром, хронические лейкозы, такие как, но не ограниченные ими, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический лимфолейкоз, волосатоклеточный лейкоз; истинную полицитемию; лимфомы, такие как, но не ограниченные ими, болезнь Ходжкина, неходжкинскую болезнь; множественные миеломы, такие как, но не ограниченные ими, «тлеющая» множественная миелома, несекреторная миелома, остеосклеротическая миелома, плазмоклеточный лейкоз, одиночная плазмоцитома и экстрамедуллярная плазмоцитома; макроглобулинемию Вальденстрема; моноклональную гаммопатия неустановленного значения; доброкачественную моноклональную гаммопатию; болезнь тяжелых цепей; рак костей и саркомы соединительной ткани, такие как, но не ограниченные ими, саркома костей, миеломная болезнь костей, множественная миелома, остеосаркома костей, вызванная холестеатомой, костная болезнь Педжета, остеосаркома, хондросаркома, саркома Юинга, злокачественная гигантоклеточная опухоль, фибросаркома кости, хордома, паростальная саркома, саркома мягких тканей, ангиосаркома (гемангиосаркома), фибросаркома, саркома Капоши, лейомиосаркома, липосаркома, лимфангиосаркома, невринома, рабдомиосаркома и синовиальная саркома; опухоли головного мозга, такие как, но не ограниченные ими, глиома, астроцитома, глиома ствола головного мозга, эпендимома, олигодендроглиома, неглиальная опухоль, акустическая невринома, краниофарингиома, медуллобластома, менингиома, пинеоцитома, пинеобластома и первичная лимфома головного мозга; рак молочной железы, включающий, но не ограниченный ими, аденокарциному, лобулярную (мелкоклеточную) карциному, внутрипротоковую карциному, медуллярный рак молочной железы, муцинозный рак молочной железы, тубулярный рак молочной железы, папиллярный рак молочной железы, болезнь Педжета (включая ювенильную болезнь Педжета) и воспалительный рак молочной железы; рак надпочечников, такой как, но не ограниченный ими, феохромоцитома и адренокортикальная карцинома; рак щитовидной железы, такой как, но не ограниченный ими, папиллярный или фолликулярный рак щитовидной железы, медуллярный рак щитовидной железы и анапластический рак щитовидной железы; рак поджелудочной железы, такой как, но не ограниченный ими, инсулинома, гастринома, глюкагонома, випома, опухоль, секретирующая соматостатин и карциноидная опухоль или опухоль островковых клеток; рак гипофиза, такой как, но не ограниченный ими, болезнь Кушинга, опухоль, секретирующая пролактин, акромегалия и несахарный диабет; раки глаза, такие как, но не ограниченные ими, глазная меланома, такая как меланома радужной оболочки, меланома хориоидеи, и меланома ресничного тела, и ретинобластома; рак влагалища, такой как плоскоклеточный рак, аденокарцинома и меланома; рак вульвы, такой как плоскоклеточная карцинома, меланома, аденокарцинома, базальноклеточная карцинома, саркома и болезнь Педжета; рак шейки матки, такой как, но не ограниченный ими, плоскоклеточная карцинома и аденокарцинома; рак матки, такой как, но не ограниченный ими, карцинома эндометрия и саркома матки; рак яичников, такой как, но не ограниченный ими, эпителиальная карцинома, пограничная опухоль, опухоль зародышевых клеток и стромальная опухоль; карциному шейки матки; рак пищевода, такой как, но не ограниченный ими, плоскоклеточный рак, аденокарцинома, аденокистозная карцинома, мукоэпидермоидная карцинома, аденосквамозная карцинома, саркома, меланома, плазмоцитома, веррукозная карцинома и овсяноклеточная (мелкоклеточная) карцинома; рак желудка, такой как, но не ограниченный ими, аденокарцинома, грибовидная (полипоидная), язвенная, поверхностная распространяющаяся, диффузно распространяющаяся, злокачественная лимфома, липосаркома, фибросаркома и карциносаркома; рак толстой кишки; колоректальный рак, колоректальный рак с мутацией KRAS; карциному толстой кишки; рак прямой кишки; рак печени, такой как, но не ограниченный ими, печеночно-клеточная карцинома и гепатобластома, рак желчного пузыря, такой как аденокарцинома; холангиокарциномы, такие как, но не ограниченные ими, папиллярные, узловые и диффузные; рак легких, такой как немелкоклеточный рак легких с мутацией KRAS, немелкоклеточный рак легких, плоскоклеточный рак (эпидермоидная карцинома), аденокарцинома, крупноклеточная карцинома и мелкоклеточный рак легких; карциному легких; рак яичка, такой как, но не ограниченный ими, зародышевые опухоли, семинома, анапластическая, классическая (типичная), сперматоцитарная, несеминома, эмбриональная карцинома, карцинома тератомы, хориокарцинома (опухоль желточного мешка), рак предстательной железы, такой как, но не ограниченный ими, андроген-независимый рак предстательной железы, андроген-зависимый рак предстательной железы, аденокарцинома, лейомиосаркома и рабдомиосаркома; рак пениса; рак ротовой полости, такой как, но не ограниченный ими, плоскоклеточная карцинома; базальный рак; рак слюнных желез, такой как, но не ограниченный ими, аденокарцинома, мукоэпидермоидная карцинома и аденоидно-кистозная карцинома; рак глотки, такой как, но не ограниченный ими, плоскоклеточный рак и веррикозный; рак кожи, такой как, но не ограниченны ими, базальноклеточная карцинома, плоскоклеточная карцинома и меланома, поверхностно распространяющаяся меланома, узелковая меланома, злокачественная меланома лентиго, лентигиноз конечностей; рак почек, такой как, но не ограниченный ими, почечно-клеточный рак, аденокарцинома, гипернефрома, фибросаркома, переходно-клеточный рак (почечной лоханки и/или мочеточника); карцинома почек; опухоль Вильмса; рак мочевого пузыря, такой как, но не ограниченный ими, переходно-клеточная карцинома, плоскоклеточный рак, аденокарцинома, карциносаркома. Кроме того, рак включает миксосаркому, остеогенную саркому, эндотелиосаркому, лимфангиоэндотелиосаркому, мезотелиому, синовиому, гемангиобластому, эпителиальную карциному, цистаденокарциному, бронхогенную карциному, карциному потовых желез, карциному сальной железы, папиллярную карциному и папиллярную аденокарциному.
Раки включают, но не ограничены ими, В-клеточный рак, например, множественную миелому, макроглобулинемию Вальденстрема, заболевания тяжелых цепей, такие как, например, болезнь альфа-цепи, болезнь гамма-цепи, болезнь мю-цепи, доброкачественную моноклональную гаммопатию и иммуноцитарный амилоидоз, меланомы, рак молочной железы, рак легких, рак бронхов, колоректальный рак, рак предстательной железы (например, метастатический, гормоно-рефрактерный рак предстательной железы), рак поджелудочной железы, рак желудка, рак яичников, рак мочевого пузыря, рак мозга или центральной нервной системы, рак периферической нервной системы, рак пищевода, рак шейки матки, рак матки или эндометрия, рак полости рта или глотки, рак печени, рак почки, рак яичек, рак желчевыводящих путей, рак тонкой кишки или аппендикса, рак слюнной железы, рак щитовидной железы, рак надпочечников, остеосаркому, хондросаркому, рак гематологических тканей и подобные. Другие не ограничивающие примеры типов рака, применимые к способам, охватываемым настоящим описанием, включают саркомы и карциномы человека, например, фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, карциному толстой кишки, колоректальный рак, рак поджелудочной железы, рак молочной железы, рак яичников, плоскоклеточную карциному, базальноклеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярные аденокарциномы, цистаденокарциному, медуллярную карциному, бронхогенную карциному, почечно-клеточную карциному, гепатому, карциному желчных протоков, рак печени, хориокарциному, семиному, эмбриональную карциному, опухоль Вильмса, рак шейки матки, рак костей, опухоль головного мозга, рак яичек, карциному легких, мелкоклеточную карциному легких, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, акустическую шванному, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому; лейкозы, например, острый лимфолейкоз и острый миелоцитарный лейкоз (миелобластный, промиелоцитарный, миеломоноцитарный, моноцитарный и эритролейкоз); хронический лейкоз (хронический миелоцитарный (гранулоцитарный) лейкоз и хронический лимфолейкоз); и истинную полицитемию, лимфому (болезнь Ходжкина и неходжкинскую болезнь), множественную миелому, макроглобулинемию Вальденстрема и болезнь тяжелых цепей. В некоторых вариантах осуществления, раком, фенотип которого определяется способом настоящего описания, является эпителиальный рак, такой как, но не ограниченный ими, рак мочевого пузыря, рак молочной железы, рак шейки матки, рак толстой кишки, гинекологические раки, рак почек, рак гортани, рак легких, рак полости рта, рак головы и шеи, рак яичников, рак поджелудочной железы, рак предстательной железы или рак кожи. В других вариантах осуществления, раком является рак молочной железы, рак предстательной железы, рак легких или рак толстой кишки. В других вариантах осуществления, эпителиальным раком является немелкоклеточный рак легких, непапиллярная почечно-клеточная карцинома, карцинома шейки матки, карцинома яичников (например, серозная карцинома яичников) или карцинома молочной железы. Эпителиальные раки могут быть охарактеризованы различными другими путями, включая, но не ограничиваясь ими, серозный, эндометриоидный, слизеобразующий, светлоклеточный, бреннеровский или недифференцированный. В некоторых вариантах осуществления, настоящее описание используется для лечения, диагностики и/или прогнозирования лимфомы или ее подтипов, включая, но не ограничиваясь ими, мантийноклеточную лимфому. Лимфопролиферативные расстройства также считаются пролиферативными заболеваниями.
В некоторых вариантах осуществления, комбинация агента, описанного в настоящем изобретении, и по меньшей мере одного дополнительного терапевтического агента дает аддитивные или синергетические результаты. В некоторых вариантах осуществления, комбинированная терапия дает повышение терапевтического индекса агента. В некоторых вариантах осуществления, комбинированная терапия дает повышение терапевтического индекса дополнительного терапевтического агента(ов). В некоторых вариантах осуществления, комбинированная терапия дает снижение токсичности и/или побочных эффектов агента. В некоторых вариантах осуществления, комбинированная терапия дает снижение токсичности и/или побочных эффектов дополнительного терапевтического агента(ов).
В некоторых вариантах осуществления, в дополнение к введению неоантигенного терапевтического агента, описанного в настоящем изобретении, способ или лечение дополнительно включает введение по меньшей мере одного дополнительного терапевтического агента. Дополнительный терапевтический агент может вводиться до, одновременно и/или после введения агента. В некоторых вариантах осуществления, по меньшей мере один дополнительный терапевтический агент содержит 1, 2, 3 или несколько дополнительных терапевтических агентов.
Терапевтические агенты, которые могут быть введены в комбинации с неоантигенным терапевтическим агентом, описанным в настоящем изобретении, включают химиотерапевтические агенты. Таким образом, в некоторых вариантах осуществления, способ или лечение включают введение агента, описанного в настоящем изобретении в комбинации с химиотерапевтическим агентом, или в комбинации с коктейлем из химиотерапевтическими агентами. Лечение агентом может проходить до, одновременно с или после введения химиотерапии. Объединенное введение может включать совместное введение, либо в одном фармацевтическом составе, либо с использованием отдельных составов, или последовательное введение в любом порядке, но обычно в течение такого периода времени, чтобы все активные агенты могли оказать свое биологическое действие одновременно. Препараты и схемы дозирования для таких химиотерапевтических агентов могут использоваться согласно инструкциям производителя или как определено эмпирически практикующим специалистом. Препараты и схемы дозирования для такой химиотерапии также описаны в Chemotherapy Source Book, 4th Edition, 2008, M. C. Perry, Editor, Lippincott, Williams & Wilkins, Philadelphia, PA.
Полезные классы химиотерапевтических агентов включают, например, анти-тубулиновые агенты, ауристатины, связывающие малые бороздки ДНК агенты, ингибиторы репликации ДНК, алкилирующие агенты (например, комплексы платины, такие как цисплатин, комплексы моно(платины), бис(платины) и трехъядерной платины и карбоплатина), антрациклины, антибиотики, анти-фолаты, антиметаболиты, химиотерапевтические сенсибилизаторы, дуокармицины, этопозиды, фторированные пиримидины, ионофоры, лекситропсины, нитрозомочевины, платинолы, пуриновые антиметаболиты, пуромицины, радиационные сенсибилизаторы, стероиды, таксаны, ингибиторы топоизомеразы, алкалоиды барвинка или подобные. В некоторых вариантах осуществления, вторым терапевтическим агентом является алкилирующий агент, антиметаболит, антимитотик, ингибитор топоизомеразы или ингибитор ангиогенеза.
Химиотерапевтические агенты, используемые в настоящем описании, включают, но не ограничиваются ими, алкилирующие агенты, такие как тиотепа и циклофосфамид (ЦИТОКСАН); алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбохон, метуредопа и уредопа; этиленимины и метиламеламины, включая альтретамин, триэтилнемеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилоломеламин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, мехлорэтамин оксид гидрохлорид, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урамустин; нитрозомочевины, такие как кармустин, хлорзотоцин, фотемустин, ломустин, нимустин, ранимустин; антибиотики, такие как аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, калихеамицин, карабицин, каминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин, эпирубицин, эсорубицин, идарубицин, марцелломицин, митомицины микофенольная кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, келамицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; анти-метаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитозин арабинозид, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин, 5-FU; андрогены, такие как калустерон, дромостанолона пропионат, эпитиостанол, мепитиостан, тестолактон; средства, угнетающие функции надпочечников, такие как аминоглютетимид, митотан, трилостан; восполнители фолиевой кислоты, такие как фолиниевая кислота; ацеглатон; гликозид альдофосфамида; аминолевулиновая кислота; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; элформитин; эллиптиния ацетат; этоглюцид; нитрат галлия; гидроксимочевина; лентинан; лонидамин; митогуазон; митоксантрон; мопидамол; нитракрин; пентостатин; фенамет; пирарубицин; подофиллиновая кислота; 2-этилгидразид; прокарбазин; PSK; разоксан; сизофуран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2’,2’’-трихлортриэтиламин; уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид (Ara-C); таксоиды, например, паклитаксел (TAXOL) и доцетаксел (TAXOTERE); хлорамбуцил; гемцитабин; 6-тиогуанин; меркаптопурин; аналоги платины, такие как цисплатин и карбоплатин; винбластин; платина; этопозид (VP-16); ифосфамид; митомицин C; митоксантрон; винкристин; винорелбин; навелбин; новантрон; тенипозид; дауномицин; аминоптерин; ибандронат; CPT11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноевая кислота; эсперамицины; капецитабин (XELODA); и фармацевтически приемлемые соли, кислоты или производные любого из вышеперечисленных. Химиотерапевтические агенты также включают антигормональные агенты, которые регулируют или ингибируют действие гормонов на опухоли, такие как антиэстрогены, включая, например, тамоксифен, ралоксифен, ингибирующие ароматазу 4(5)-имидазолы, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и торемифен (FARESTON); и анти-андрогены, такие как флутамид, нилутамид, бикалутамид, лейпролид и гозерелин; и фармацевтически приемлемые соли, кислоты или производные любого из вышеперечисленных. В некоторых вариантах осуществления дополнительным терапевтическим агентом является цисплатин. В некоторых вариантах осуществления дополнительным терапевтическим агентом является карбоплатин.
В некоторых вариантах осуществления, химиотерапевтическим агентом является ингибитор топоизомеразы. Ингибиторы топоизомеразы являются химиотерапевтическими агентами, которые вмешиваются в действие фермента топоизомеразы (например, топоизомеразы I или II). Ингибиторы топоизомеразы включают, но не ограничены ими, доксорубицин HCl, даунорубицин цитрат, митоксантрон HCl, актиномицин D, этопозид, топотекан HCl, тенипозид (VM-26) и иринотекан, а также фармацевтически приемлемые соли, кислоты или производные любого из них. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является иринотекан.
В некоторых вариантах осуществления, химиотерапевтическим агентом является антиметаболит. Антиметаболитом является химическое вещество со структурой, которая похожа на метаболит, требуемый для нормальных биохимических реакций, но достаточно отличается для того, чтобы препятствовать одной или нескольким нормальным функциям клеток, таким как деление клеток. Антиметаболиты включают, но не ограничены ими, гемцитабин, фторурацил, капецитабин, метотрексат натрия, ралитрексед, пеметрексед, тегафур, цитозинарабинозид, тиогуанин, 5-азацитидин, 6-меркаптопурин, азатиоприн, 6-тиогуанин, пентостатин, флударабина фосфат и кладрибин, а также фармацевтически приемлемые соли, кислоты или производные любого из них. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является гемцитабин.
В некоторых вариантах осуществления, химиотерапевтическим агентом является антимитотический агент, включающий, но не ограниченный ими, агенты, которые связывают тубулин. В некоторых вариантах осуществления, агентом является таксан. В некоторых вариантах осуществления, агентом является паклитаксел или доцетаксел или фармацевтически приемлемая соль, кислота или производное паклитаксела или доцетаксела. В некоторых вариантах осуществления, агентом является паклитаксел (TAXOL), доцетаксел (TAXOTERE), альбумин-связанный паклитаксел (ABRAXANE), DHA-паклитаксел или PG-паклитаксел. В определенных альтернативных вариантах осуществления, антимитотический агент содержит алкалоид барвинка, такой как винкристин, винбластин, винорелбин или виндезин, или их фармацевтически приемлемые соли, кислоты или производные. В некоторых вариантах осуществления, антимитотическим агентом является ингибитор кинезина Eg5 или ингибитор митотической киназы, такой как Aurora или Plk1. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является паклитаксел. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является альбумин-связанный паклитаксел.
В некоторых вариантах осуществления, дополнительный терапевтический агент содержит агент, такой как малая молекула. Например, лечение может включать объединенное введение агента настоящего описания с малой молекулой, которая действует как ингибитор против опухолеассоциированных антигенов, включающих, но не ограниченных ими, EGFR, HER2 (ErbB2) и/или VEGF. В некоторых вариантах осуществления, агент настоящего описания вводят в комбинации с ингибитором протеинкиназы, выбранным из группы, состоящей из: гефитиниба (IRESSA), эрлотиниба (TARCEVA), сунитиниба (SUTENT), лапатиниба, вандетаниба (ZACTIMA), AEE788, CI-1033, цедираниба (RECENTIN), сорафениба (NEXAVAR) и пазопаниба (GW786034B). В некоторых вариантах осуществления, дополнительный терапевтический агент содержит ингибитор mTOR. В другом варианте осуществления, дополнительным терапевтическим агентом является химиотерапия или другие ингибиторы, которые снижают количество Treg клеток. В некоторых вариантах осуществления, терапевтическим агентом является циклофосфамид или анти-CTLA4 антитело. В другом варианте осуществления, дополнительный терапевтический агент снижает присутствие полученных из миелоида супрессорных клеток. В дополнительном варианте осуществления, дополнительным терапевтическим агентом является карботаксол. В другом варианте осуществления, дополнительный терапевтический агент сдвигает клетки к T хелмерному 1 ответу. В дополнительном варианте осуществления, дополнительным терапевтическим агентом является ибрутиниб.
В некоторых вариантах осуществления, дополнительный терапевтический агент содержит биологическую молекулу, такую как антитело. Например, лечение может включать комбинированное введение агента настоящего описания с антителами против опухолеассоциированных антигенов, включающими, но не ограниченными ими, антитела, которые связывают EGFR, HER2/ErbB2 и/или VEGF. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является антитело, специфическое к маркеру раковой стволовой клетки. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является антитело, которое является ингибитором ангиогенеза (например, антитело к анти-VEGF или VEGF рецептору). В некоторых вариантах осуществления, дополнительным терапевтическим агентом является бевацизумаб (AVASTIN), рамуцирумаб, трастузумаб (HERCEPTIN), пертузумаб (OMNITARG), панитумумаб (VECTIBIX), нимотузумаб, залутумумаб или цетуксимаб (ERBITUX).
Агенты и композиции, представленные здесь, могут использоваться индивидуально или в комбинации с обычными терапевтическими схемами, такими как хирургическое вмешательство, облучение, химиотерапия и/или трансплантация костного мозга (аутологическая, сингенная, аллогенная или неродственная). Множество опухолевых антигенов может быть полезно, например, у значительной доли онкологических пациентов.
В некоторых вариантах осуществления, по меньшей мере один или более химиотерапевтических агентов могут вводиться в дополнение к композиции, содержащей иммуногенную вакцину. В некоторых вариантах осуществления, один или более химиотерапевтических агентов могут принадлежать к разным классам химиотерапевтических агентов.
Примеры химиотерапевтических агентов включают, но не ограничены ими, алкилирующие агенты, такие как азотистые иприты (например, мехлоретамин (азотистый иприт), хлорамбуцил, циклофосфамид (Cytoxan®), ифосфамид и мелфалан); нитрозомочевины (например N-нитрозо-N-метилмочевина, стрептозоцин, кармустин (BCNU), ломустин и семустин); алкилсульфонаты (например, бусульфан); тетразины (например, дакарбазин (DTIC), митозоломид и темозоломид (Temodar®)); азиридины (например, тиотепа, митомицин и диазиквон); и лекарственные средства на основе платины (например, цисплатин, карбоплатин и оксалиплатин); не классические алкилирующие агенты, такие как прокарбазин и алтретамин (гексаметилмеламин); анти-метаболиты, такие как 5-фторурацил (5-FU), 6-меркаптопурин (6-MP), капецитабин (Xeloda®), кладрибин, клофарабин, цитарабин (Ara-C®), децитабин, флоксуридин, флударабин, неларабин, гемцитабин (Gemzar®), гидроксимочевина, метотрексат, пеметрексед (Alimta®), пентостатин, тиогуанин, Видаза; ингибиторы полимеризации тубулина, такие как алкалоиды барвинка (например, винкристин, винбластин, винорелбин, виндезин и винфлунин); таксаны (например, паклитаксел (Taxol®), доцетаксел (Taxotere®)); подофиллотоксин (например, этопозид и тенипозид); эпотилоны (например, иксабепилон (Ixempra®)); эстрамустин (Emcyt®); противоопухолевые антибиотики, такие как антрациклины (например, даунорубицин, доксорубицин (Adriamycin®, эпирубицин, идарубицин); актиномицин-D; и блеомицин; ингибиторы топоизомеразы I, такие как топотекан и иринотекан (CPT-11); ингибиторы топоизомеразы II, такие как этопозид (VP-16), тенипозид, митоксантрон, новобиоцин, мербарон и акларубицин; кортикостероиды, такие как преднизон, метилпреднизолон (Solumedrol®) и дексаметазон (Decadron®); L-аспарагиназу; бортезомиб (Velcade®); иммунотерапевтические агенты, такие как ритуксимаб (Rituxan®), алемтузумаб (Campath®), талидомид, леналидомид (Revlimid®), BCG, интерлейкин-2, интерферон-альфа и раковые вакцины, такие как Provenge®; гормональные терапевтические агенты, такие как фульвестрант (Faslodex®), тамоксифен, торемифен (Fareston®), анастрозол (Arimidex®), экземестан (Aromasin®), летрозол (Femara®), мегестрол ацетат (Megace®), эстрогены, бикалутамид (Casodex®), флутамид (Eulexin®), нилутамид (Nilandron®), лейпролид (Lupron®) и госерелин (Zoladex®); дифференцирующие агенты, такие как ретиноиды, третиноин (ATRA или Atralin®), бексаротен (Targretin®) и окись мышьяка (Arsenox®); и таргетные терапевтические агенты, такие как иматиниб (Gleevec®), гефитиниб (Iressa®) и сунитиниб (Sutent®). В некоторых вариантах осуществления, химиотерапией является коктейльная терапия. Примеры коктейльной терапии включают, но не ограничены ими, CHOP/R-CHOP (ритуксан, циклофосфамид, гидроксидоксорубицин, винкристин и преднизон), EPOCH (этопозид, преднизон, винкристин, циклофосфамид, гидроксидоксорубицин), Hyper-CVAD (циклофосфамид, винкристин, гидроксидоксорубицин, дексаметазон), FOLFOX (фторурацил (5-FU), лейковорин, оксалиплатин), ICE (ифосфамид, карбоплатин, этопозид), DHAP (высокая доза цитарабина [ara-C], дексаметазон, цисплатин), ESHAP (этопозид, метилпреднизолон, цитарабин [ara-C], цисплатин) и CMF (циклофосфамид, метотрексат, фторурацил).
В некоторых вариантах осуществления, иммуногенная вакцина может использоваться в комбинации с ингибитором фосфоинозитид 3-киназы (PI3 киназы, PI3K). Например, иммуногенная вакцина может использоваться в комбинации с Вортманнином, Деметоксивиридином, LY294002, гибисконом C, Иделалисибом, Копанлисибом, Дувелисибом, Тазелисибом, Перифозином, Бупарлисибом, Дувелисибом, Альпелисибом (BYL719), Умбралисибом, (TGR 1202), Копанлисибом (BAY 80-6946), PX-866, Дактолисибом, CUDC-907, Воксталисибом (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисибом (GDC-0941), XL147 (SAR245408), Паломидом 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477, AEZS-136 или любой их комбинацией.
В некоторых вариантах осуществления, доза ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136, применяемая для лечения человека, может быть в диапазоне от приблизительно 0,01 мг/кг до приблизительно 100 мг/кг в сутки (например, от приблизительно 0,1 мг/кг до приблизительно 100 мг/кг в сутки, от приблизительно 0,1 мг/кг до приблизительно 50 мг/кг в сутки, от приблизительно 10 мг/кг в сутки или до приблизительно 30 мг/кг в сутки). Желаемая доза для удобства может вводиться одной дозой или несколькими дозами с подходящими интервалами, например в виде двух, трех, четырех или более субдоз в сутки.
В некоторых вариантах осуществления, доза ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 может быть от приблизительно 1 нг/кг до приблизительно 100 мг/кг. Дозой ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 может быть любая доза, включающая, но не ограниченная ими, приблизительно 1 мкг/кг, 25 мкг/кг, 50 мкг/кг, 75 мкг/кг, 100 µ мкг/кг, 125 мкг/кг, 150 мкг/кг, 175 мкг/кг, 200 мкг/кг, 225 мкг/кг, 250 мкг/кг, 275 мкг/кг, 300 мкг/кг, 325 мкг/кг, 350 мкг/кг, 375 мкг/кг, 400 мкг/кг, 425 мкг/кг, 450 мкг/кг, 475 мкг/кг, 500 мкг/кг, 525 мкг/кг, 550 мкг/кг, 575 мкг/кг, 600 мкг/кг, 625 мкг/кг, 650 мкг/кг, 675 мкг/кг, 700 мкг/кг, 725 мкг/кг, 750 мкг/кг, 775 мкг/кг, 800 мкг/кг, 825 мкг/кг, 850 мкг/кг, 875 мкг/кг, 900 мкг/кг, 925 мкг/кг, 950 мкг/кг, 975 мкг/кг, 1 мг/кг, 2,5 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 60 мг/кг, 70 мг/кг, 80 мг/кг, 90 мг/кг или 100 мг/кг.
Способ введения иммуногеннной вакцины и ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 может быть одновременным или последовательным, где иммуногенную вакцину и по меньшей мере один дополнительные фармацевтически активный агент вводят последовательно (или отдельно). Например, иммуногенная вакцина и ингибитор PI3 киназы, например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 могут быть представлены в стандартной дозированной форме для принятия вместе или в виде отдельных веществ (например, в раздельных контейнерах) для введения одновременно или с некоторой разницей во времени. Эта разница во времени может составлять от 1 часа до 1 месяца, например, от 1 дня до1 недели, например, от 48 часов до 3 дня. Кроме того, возможно вводить иммуногенную вакцину путем введения, отличным от пути введения ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136. Например, может быть предпочтительно вводить либо иммуногенную вакцину, либо ингибитор PI3 киназы, например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136, внутривенно, а другой вводить системно или перорально. Например, иммуногенную вакцину вводят внутривенно или подкожно, и ингибитор PI3 киназы, например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136, перорально.
В некоторых вариантах осуществления, иммуногенную вакцину вводят хронологически до ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136. В некоторых вариантах осуществления, иммуногенную вакцину вводят за 1-24 часа, 2-24 часа, 3-24 часа, 4-24 часа, 5-24 часа, 6-24 часа, 7-24 часа, 8-24 часа, 9-24 часа, 10-24 часа, 11-24 часа, 12-24 часа, 1-30 дней, 2-30 дней, 3-30 дней, 4-30 дней, 5-30 дней, 6-30 дней, 7-30 дней, 8-30 дней, 9-30 дней, 10-30 дней, 11-30 дней, 12-30 дней, 13-30 дней, 14-30 дней, 15-30 дней, 16-30 дней, 17-30 дней, 18-30 дней, 19-30 дней, 20-30 дней, 21-30 дней, 22-30 дней, 23-30 дней, 24-30 дней, 25-30 дней, 26-30 дней, 27-30 дней, 28-30 дней, 29-30 дней, 1-4 недели, 2-4 недели, 3-4 недели, 1-12 месяцев, 2-12 месяцев, 3-12 месяцев, 4-12 месяцев, 5-12 месяцев, 6-12 месяцев, 7-12 месяцев, 8-12 месяцев, 9-12 месяцев, 10-12 месяцев, 11-12 месяцев, или любая их комбинация, до введения ингибитора PI3 киназы. В некоторых вариантах осуществления, иммуногенную вакцину вводят за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения ингибитора PI3 киназы. Например, иммуногенная вакцина может вводиться по меньшей мере за 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136.
В некоторых вариантах осуществления, иммуногенную вакцину вводят за, самое большее, 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения ингибитора PI3 киназы. Например, иммуногенная вакцина может быть введена за, самое большее 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136.
В некоторых вариантах осуществления, иммуногенную вакцину вводят за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения ингибитора PI3 киназы. Например, иммуногенная вакцина может быть введена за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136.
В некоторых вариантах осуществления, иммуногенную вакцину вводят хронологически в то же время, как и по меньшей мере один дополнительный фармацевтически активный агент.
В некоторых вариантах осуществления, иммуногенную вакцину вводят хронологически после введения ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136. В некоторых вариантах осуществления, Ингибитор PI3 киназы вводят за 1-24 часа, 2-24 часа, 3-24 часа, 4-24 часа, 5-24 часа, 6-24 часа, 7-24 часа, 8-24 часа, 9-24 часа, 10-24 часа, 11-24 часа, 12-24 часа, 1-30 дней, 2-30 дней, 3-30 дней, 4-30 дней, 5-30 дней, 6-30 дней, 7-30 дней, 8-30 дней, 9-30 дней, 10-30 дней, 11-30 дней, 12-30 дней, 13-30 дней, 14-30 дней, 15-30 дней, 16-30 дней, 17-30 дней, 18-30 дней, 19-30 дней, 20-30 дней, 21-30 дней, 22-30 дней, 23-30 дней, 24-30 дней, 25-30 дней, 26-30 дней, 27-30 дней, 28-30 дней, 29-30 дней, 1-4 недели, 2-4 недели, 3-4 недели, 1-12 месяцев, 2-12 месяцев, 3-12 месяцев, 4-12 месяцев, 5-12 месяцев, 6-12 месяцев, 7-12 месяцев, 8-12 месяцев, 9-12 месяцев, 10-12 месяцев, 11-12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. В некоторых вариантах осуществления, ингибитор PI3 киназы вводят за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. Например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 может быть введен за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины.
В некоторых вариантах осуществления, ингибитор PI3 киназы вводят за, самое большее 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. Например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 может быть введен за, самое большее 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины.
В некоторых вариантах осуществления ингибитор PI3 киназы вводят за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. Например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136 может быть введен за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины.
В некоторых вариантах осуществления изобретение относится к способу лечения состояния или заболевания, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества иммуногенной вакцины в сочетании с терапевтически эффективным количеством ингибитора PI3 киназы. Например, изобретение относится к способу лечения состояния или заболевания, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества иммуногенной вакцины, в комбинации с терапевтически эффективным количеством Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136.
В некоторых вариантах осуществления, иммуногенную вакцину вводят один, два или три раза в сутки в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 последовательных дней с последующими 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 днями отдыха (например, без введения иммуногенной вакцины/приостановления лечения) в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28-дневном курсе; и ингибитор PI3 киназы (например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136) вводят до, одновременно с или после введения иммуногенной вакцины в одни или несколько дней (например, на 1 день 1 курса). В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, или 13 циклов из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 дней. В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1-12 или 13 курсов по 28 дней (например, приблизительно 12 месяцев).
В некоторых вариантах осуществления изобретение относится к способу лечения состояния или заболевания, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества иммуногенной вакцины в комбинации с терапевтически эффективным количеством ингибитора PI3 киназы, например, Вортманнина, Деметоксивиридина, LY294002, гибискона C, Иделалисиба, Копанлисиба, Дувелисиба, Тазелисиба, Перифозина, Бупарлисиба, Дувелисиба, Альпелисиба (BYL719), Умбралисиба, (TGR 1202), Копанлисиба (BAY 80-6946), PX-866, Дактолисиба, CUDC-907, Воксталисиба (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиба (GDC-0941), XL147 (SAR245408), Паломида 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136, и вторичного активного агента, такого как ингибитор иммунной контрольной точки. В некоторых вариантах осуществления, иммуногенную вакцину вводит один, два или три раза в сутки в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 последовательных дней, с последующими 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 днями отдыха (например, без введения иммуногенной вакцины/приостановления лечения) в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28-дневном курсе; ингибитор PI3 киназы (например, Вортманнин, Деметоксивиридин, LY294002, гибискон C, Иделалисиб, Копанлисиб, Дувелисиб, Тазелисиб, Перифозин, Бупарлисиб, Дувелисиб, Альпелисиб (BYL719), Умбралисиб, (TGR 1202), Копанлисиб (BAY 80-6946), PX-866, Дактолисиб, CUDC-907, Воксталисиб (SAR245409, XL765), CUDC-907, ME-401, IPI-549, SF1126, RP6530, INK1117, пиктилисиб (GDC-0941), XL147 (SAR245408), Паломид 529, GSK1059615, ZSTK474, PWT33597, IC87114, TG100–115, CAL263, RP6503, PI-103, GNE-477 или AEZS-136) вводят до, одновременно с или после введения иммуногенной вакцины в один или более дней (например, на 1 день 1 курса), и вторичный агент вводят ежедневно, еженедельно или ежемесячно. В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12 или 13 курсов из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 дней. В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1-12 или 13 курсов из 28 дней (например, приблизительно 12 месяцев).
В некоторых вариантах осуществления, иммуногенная вакцина может использоваться в комбинации с ингибиторами циклин-зависимых киназ, например, с ингибитором CDK4 и/или CDK6. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является палбоциклиб (IBRANCE) (см., например, Clin. Cancer Res.; 2015, 21(13); 2905–10). Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является рибоциклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является абемациклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является селициклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является динациклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является милциклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является ронициклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является атувециклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является брициклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является ривициклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является селициклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является трилациклиб. Примером такого ингибитора, который может использоваться в комбинации с настоящей иммуногенной вакциной, является воруциклиб. В некоторых примерах, иммуногенные вакцины настоящего описания могут использоваться в комбинации с ингибитором CDK4 и/или CDK6 и с агентом, который усиливает цитостатическую активность ингибиторов CDK4/6 и/или с агентом, который превращает обратимый цитостаз в необратимую остановку роста или смерть клетки. Типовые подтипы рака включают NSCLC, меланому, нейробластому, глиобластому, липосаркому и мантийноклеточную лимфому.
В некоторых вариантах осуществления, дозы циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба, применяемого для лечения человека, может быть в диапазоне от приблизительно 0,01 мг/кг до приблизительно 100 мг/кг в сутки (например, от приблизительно 0,1 мг/кг до приблизительно 100 мг/кг в сутки, от приблизительно 0,1 мг/кг до приблизительно 50 мг/кг в сутки, от приблизительно 10 мг/кг в сутки или до приблизительно 30 мг/кг в сутки). Желаемая доза для удобства может вводиться одной дозой или несколькими дозами с подходящими интервалами, например в виде двух, трех, четырех или более субдоз в сутки.
В некоторых вариантах осуществления, доза циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба, может быть от приблизительно 1 нг/кг до приблизительно 100 мг/кг. Доза циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба, может быть любой дозой, включающей, но не ограниченной ими, приблизительно 1 мкг/кг, 25 мкг/кг, 50 мкг/кг, 75 мкг/кг, 100 µ мкг/кг, 125 мкг/кг, 150 мкг/кг, 175 мкг/кг, 200 мкг/кг, 225 мкг/кг, 250 мкг/кг, 275 мкг/кг, 300 мкг/кг, 325 мкг/кг, 350 мкг/кг, 375 мкг/кг, 400 мкг/кг, 425 мкг/кг, 450 мкг/кг, 475 мкг/кг, 500 мкг/кг, 525 мкг/кг, 550 мкг/кг, 575 мкг/кг, 600 мкг/кг, 625 мкг/кг, 650 мкг/кг, 675 мкг/кг, 700 мкг/кг, 725 мкг/кг, 750 мкг/кг, 775 мкг/кг, 800 мкг/кг, 825 мкг/кг, 850 мкг/кг, 875 мкг/кг, 900 мкг/кг, 925 мкг/кг, 950 мкг/кг, 975 мкг/кг, 1 мг/кг, 2,5 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 60 мг/кг, 70 мг/кг, 80 мг/кг, 90 мг/кг или 100 мг/кг.
Способ введения иммуногеннной вакцины и циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба может быть одновременным или последовательным, где иммуногенную вакцину и по меньшей мере один дополнительные фармацевтически активный агент вводят последовательно (или отдельно). Например, иммуногенная вакцина и циклин-зависимый ингибитор киназы, например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб могут быть представлены в стандартной дозированной форме для принятия вместе или в виде отдельных веществ (например, в раздельных контейнерах) для введения одновременно или с некоторой разницей во времени. Эта разница во времени может составлять от 1 часа до 1 месяца, например, от 1 дня до1 недели, например, от 48 часов до 3 дня. Кроме того, возможно вводить иммуногенную вакцину путем введения, отличным от пути введения циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба. Например, может быть предпочтительно вводить либо иммуногенную вакцину, либо циклин-зависимый ингибитор киназы, например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб, внутривенно, а другой вводить системно или перорально. Например, иммуногенную вакцину вводят внутривенно или подкожно, и циклин-зависимый ингибитор киназы, например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб, перорально.
В некоторых вариантах осуществления, иммуногенную вакцин вводят хронологически до циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба. В некоторых вариантах осуществления, иммуногенную вакцину вводят за 1-24 часа, 2-24 часа, 3-24 часа, 4-24 часа, 5-24 часа, 6-24 часа, 7-24 часа, 8-24 часа, 9-24 часа, 10-24 часа, 11-24 часа, 12-24 часа, 1-30 дней, 2-30 дней, 3-30 дней, 4-30 дней, 5-30 дней, 6-30 дней, 7-30 дней, 8-30 дней, 9-30 дней, 10-30 дней, 11-30 дней, 12-30 дней, 13-30 дней, 14-30 дней, 15-30 дней, 16-30 дней, 17-30 дней, 18-30 дней, 19-30 дней, 20-30 дней, 21-30 дней, 22-30 дней, 23-30 дней, 24-30 дней, 25-30 дней, 26-30 дней, 27-30 дней, 28-30 дней, 29-30 дней, 1-4 недели, 2-4 недели, 3-4 недели, 1-12 месяцев, 2-12 месяцев, 3-12 месяцев, 4-12 месяцев, 5-12 месяцев, 6-12 месяцев, 7-12 месяцев, 8-12 месяцев, 9-12 месяцев, 10-12 месяцев, 11-12 месяцев, или любая их комбинация, до введения циклин-зависимого ингибитора киназы. В некоторых вариантах осуществления, иммуногенную вакцину вводят за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения циклин-зависимого ингибитора киназы. Например, иммуногенная вакцина может быть введена за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения селициклиба, рибоциклиба, абемациклиба или палбоциклиба.
В некоторых вариантах осуществления, иммуногенную вакцину вводят, самое большее, за 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения циклин-зависимого ингибитора киназы. Например, иммуногенная вакцина может быть введена за, самое большее 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения селициклиба, рибоциклиба, абемациклиба или палбоциклиба.
В некоторых вариантах осуществления, иммуногенную вакцину вводят за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до ведения циклин-зависимого ингибитора киназы. Например, иммуногенная вакцина может быть введена за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения селициклиба, рибоциклиба, абемациклиба или палбоциклиба.
В некоторых вариантах осуществления, иммуногенную вакцину вводят хронологически в то же время, как и по меньшей мере один дополнительный фармацевтически активный агент.
В некоторых вариантах осуществления, иммуногенную вакцину вводят хронологически после циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба. В некоторых вариантах осуществления, циклин-зависимый ингибитор киназы вводят за 1-24 часа, 2-24 часа, 3-24 часа, 4-24 часа, 5-24 часа, 6-24 часа, 7-24 часа, 8-24 часа, 9-24 часа, 10-24 часа, 11-24 часа, 12-24 часа, 1-30 дней, 2-30 дней, 3-30 дней, 4-30 дней, 5-30 дней, 6-30 дней, 7-30 дней, 8-30 дней, 9-30 дней, 10-30 дней, 11-30 дней, 12-30 дней, 13-30 дней, 14-30 дней, 15-30 дней, 16-30 дней, 17-30 дней, 18-30 дней, 19-30 дней, 20-30 дней, 21-30 дней, 22-30 дней, 23-30 дней, 24-30 дней, 25-30 дней, 26-30 дней, 27-30 дней, 28-30 дней, 29-30 дней, 1-4 недели, 2-4 недели, 3-4 недели, 1-12 месяцев, 2-12 месяцев, 3-12 месяцев, 4-12 месяцев, 5-12 месяцев, 6-12 месяцев, 7-12 месяцев, 8-12 месяцев, 9-12 месяцев, 10-12 месяцев, 11-12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. В некоторых вариантах осуществления, циклин-зависимый ингибитор киназы вводят за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. Например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб может быть введен за по меньшей мере 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины.
В некоторых вариантах осуществления циклин-зависимый ингибитор киназы вводят за самое большее 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. Например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб могут быть введены за, самое большее 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины.
В некоторых вариантах осуществления циклин-зависимый ингибитор киназы вводят за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, три недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины. Например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб может быть введен за приблизительно 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9, дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней, 21 день, 22 дня, 23 дня, 24 дня, 25 дней, 26 дней, 27 дней, 28 дней, 29 дней, 30 дней, 1 неделю, 2 недели, 3 недели, 4 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, или любая их комбинация, до введения иммуногенной вакцины.
В некоторых вариантах осуществления изобретение относится к способу лечения состояния или заболевания, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества иммуногенной вакцины в комбинации с терапевтически эффективным количеством циклин-зависимого ингибитора киназы. Например, представлен способ лечения состояния или заболевания, включающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества иммуногенной вакцины в комбинации с терапевтически эффективным количеством селициклиба, рибоциклиба, абемациклиба или палбоциклиба.
В некоторых вариантах осуществления, иммуногенную вакцину вводят один, два или три раза в сутки в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30, последовательных дней с последующими 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 днями отдыха (например, без введения иммуногенной вакцины/приостановления лечения) в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28-дневном курсе; и циклин-зависимый ингибитор киназы (например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб) вводят до, одновременно с или после введения иммуногенной вакцины в один или более дней (например, на 1 день 1 курса). В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, или 13 циклов из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 дней. В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1-12 или 13 курсов по 28 дней (например, приблизительно 12 месяцев).
В некоторых вариантах осуществления изобретение относится к способу лечения состояния или заболевания, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества иммуногенной вакцины в комбинации с терапевтически эффективным количеством циклин-зависимого ингибитора киназы, например, селициклиба, рибоциклиба, абемациклиба или палбоциклиба, и вторичного активного агента, такого как ингибитор иммунной контрольной точки. В некоторых вариантах осуществления, иммуногенную вакцину вводят один, два или три раза в сутки в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 последовательных дней с последующими 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 днями отдыха (например, без введения иммуногенной вакцины/приостановления лечения) в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28-дневном цикле; циклин-зависимый ингибитор киназы (например, селициклиб, рибоциклиб, абемациклиб или палбоциклиб) вводят до, одновременно с или после введения иммуногенной вакцины в один или более дней (например, на 1 день 1 курса), и вторичный агент вводят ежедневно, еженедельно или ежемесячно. В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, или 13 циклов из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 дней. В некоторых вариантах осуществления, комбинированную терапию вводят в течение 1-12 или 13 циклов по 28 дней (например, приблизительно 12 месяцев).
В некоторых вариантах осуществления, дополнительный терапевтический агент содержит второй иммунотерапевтический агент. В некоторых вариантах осуществления, дополнительный иммунотерапевтический агент включает, но не ограничен ими, колониестиулирующий фактор, интерлейкин, антитело, которое блокирует иммунодепрессивные функции (например, анти-CTLA-4 антитело, анти-CD28 антитело, анти-CD3 антитело, анти-PD-1 антитело, анти-PD-L1 антитело, анти-TIGIT антитело), антитело, которое усиливает функции иммунной клетки (например, анти-GITR антитело, анти-OX-40 антитело, анти-CD40 антитело или анти-4-1BB антитело), толл-подобный рецептор (например, TLR4, TLR7, TLR9), растворимый лиганд (например, GITRL, GITRL-Fc, OX-40L, OX-40L-Fc, CD40L, CD40L-Fc, 4-1BB лиганд или 4-1BB лиганд-Fc) или член семейства B7 (например, CD80, CD86). В некоторых вариантах осуществления, дополнительный иммунотерапевтический агент направлен на CTLA-4, CD28, CD3, PD-1, PD-L1, TIGIT, GITR, OX-40, CD-40 или 4-1BB.
В некоторых вариантах осуществления, дополнительным терапевтическим агентом является ингибитор иммунной контрольной точки. В некоторых вариантах осуществления, ингибитором иммунной контрольной точки является анти-PD-1 антитело, анти-PD-L1 антитело, анти-CTLA-4 антитело, анти-CD28 антитело, анти-TIGIT антитело, анти-LAG3 антитело, анти-TIM3 антитело, анти-GITR антитело, анти-4-1BB антитело или анти-OX-40 антитело. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-TIGIT антитело. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-PD-1 антитело, выбранное из группы, состоящей из: ниволумаба (OPDIVO), пембролизумаба (KEYTRUDA), пидилзумаба, MEDI0680, REGN2810, BGB-A317 и PDR001. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-PD-L1 антитело, выбранное из группы, состоящей из: BMS935559 (MDX-1105), атексолизумаба (MPDL3280A), дурвалумаба (MEDI4736) и авелумаба (MSB0010718C). В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-CTLA-4 антитело, выбранное из группы, состоящей из: ипилимумаба (YERVOY) и тремелимумаба. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-LAG-3 антитело, выбранное из группы, состоящей из: BMS-986016 и LAG525. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-OX-40 антитело, выбранное из группы, состоящей из: MEDI6469, MEDI0562 и MOXR0916. В некоторых вариантах осуществления, дополнительным терапевтическим агентом является анти-4-1BB антитело, выбранное из группы, состоящей из: PF-05082566.
В некоторых вариантах осуществления, неоантигенный терапевтический агент может быть введен в комбинации с биологической молекулой, выбранной из группы, состоящей из: адреномедуллина (AM), ангиопоэтина (Ang), BMP, BDNF, EGF, эритропоэтина (EPO), FGF, GDNF, гранулоцитарного колониестимулирующего фактора (G-CSF), гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF), макрофагального колониестимулирующего фактора (M-CSF), фактора стволовых клеток (SCF), GDF9, HGF, HDGF, IGF, фактора, стимулирующего миграцию, миостатина (GDF-8), NGF, нейротрофинов, PDGF, тромбопоэтина, TGF-α, TGF-β, TNF-α, VEGF, PlGF, гамма-IFN, IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-12, IL-15 и IL-18.
В некоторых вариантах осуществления, лечение неоантигенным терапевтическим агентом, описанным в настоящем изобретении, может сопровождаться хирургическим удалением опухолей, удалением раковых клеток или любой другой хирургической терапией, которую считает необходимой лечащий врач.
В некоторых вариантах осуществления, лечение включает введение неоантигенного терапевтического агента, описанного в настоящем изобретении, в комбинации с радиационной терапией. Лечение агентом может происходить до, одновременно или после проведения радиационной терапии. Схемы дозирования для такой радиационной терапии могут быть определены практикующим врачом.
Объединенное введение может включать совместное введение, либо в одном фармацевтическом составе, либо с использованием отдельных составов, или последовательное введение в любом порядке, но обычно в течение такого количества времени, чтобы все активные агенты могли оказать их биологическую активность одновременно.
Следует принимать во внимание, что комбинация неоантигенного терапевтического агента, описанного в настоящем изобретении и по меньшей мере одного дополнительного терапевтического агента может вводиться в любом порядке или одновременно. В некоторых вариантах осуществления агент будет вводиться пациентам, которые ранее проходили лечение вторым терапевтическим агентом. В некоторых других вариантах осуществления, неоантигенный терапевтический агент и второй терапевтический агент будут вводиться по существу одновременно или одновременно. Например, субъекту можно давать агент во время прохождения курса лечения вторым терапевтическим агентом (например, химиотерапии). В некоторых вариантах осуществления, неоантигенный терапевтический агент будет вводиться в течение 1 года после лечения вторым терапевтическим агентом. Кроме того, будет принято во внимание, что два (или более) агента или методов лечения могут быть назначены субъекту в течение нескольких часов или минут (т.е. по существу одновременно).
Для лечения заболевания, подходящая дозировка неоантигенного терапевтического агента, описанного в настоящем изобретении, зависит от типа заболевания, которое подлежит лечению, тяжести и течения заболевания, чувствительности заболевания, от того, вводят ли агент для терапевтических или профилактических целей, предыдущей терапии, истории болезни пациента и так далее, все на усмотрение лечащего врача. Неоантигенный терапевтический агент может быть введен один раз или в течение серии курсов лечения продолжительностью от нескольких дней до нескольких месяцев, или до тех пор, пока не будет достигнуто излечение или уменьшение болезненного состояния (например, уменьшение размера опухоли). Оптимальные схемы дозирования могут быть рассчитаны на основе измерений накопления лекарства в теле пациента, и будут варьировать в зависимости от относительной активности отдельного агента. Лечащий врач может определить оптимальные дозировки, методики дозирования и частоту повторения.
В некоторых вариантах осуществления, неоантигенный терапевтический агент может вводиться в исходной более высокой “загрузочной” дозе с последующей одной или более более низкими дозами. В некоторых вариантах осуществления, частота введения также может изменяться. В некоторых вариантах осуществления, схема дозирования может включать введение исходной дозы с последующими дополнительными дозами (или “поддерживающими” дозами) один раз в неделю, один раз каждые две недели, один раз каждые три недели или один раз в месяц. Например, схема дозирования может включать введение исходной загрузочной дозы с последующим еженедельным поддержанием дозы, например, в половину исходной дозы. Или схема дозирования может включать введение исходной загрузочной дозы с последующим поддержанием доз, например, в половину исходной дозы через неделю. Или схема дозирования может включать введение трех исходных доз в течение 3 недель с последующим поддержанием доз, например, в том же количестве через неделю.
Как известно специалистам в данной области, введение любого терапевтического агента может приводить к побочным эффектам и/или токсичности. В некоторых случаях побочные эффекты и/или токсичность настолько серьезны, что препятствуют введению конкретного агента в терапевтически эффективной дозе. В некоторых случаях терапия должна быть прекращена, и могут быть попробованы другие агенты. Однако многие агенты одного терапевтического класса проявляют схожие побочные эффекты и/или токсичность, что означает, что пациент либо должен прекратить терапию, либо, если возможно, страдать от неприятных побочных эффектов, связанных с терапевтическим агентом.
В некоторых вариантах осуществления, схема дозирования может быть ограничены определенным количеством введений или “курсов”. В некоторых вариантах осуществления, агент вводят в течение 3, 4, 5, 6, 7, 8 или более курсов. Например, агент вводят каждые 2 недели в течение 6 курсов, агент вводят каждые 3 недели в течение 6 курсов, агент вводят каждые 2 недели в течение 4 курсов, агент вводят каждые 3 недели в течение 4 курсов и т.д. Схемы дозирования могут выбираться и замет модифицироваться специалистам в данной области техники.
Настоящее описание относится к способам введения субъекту неоантигенного терапевтического агента, описанного в настоящем изобретении, включающим использование стратегии прерывистого введения одного или нескольких агентов, что может снижать побочные эффекты и/или токсичность, связанные с введением агента, химиотерапевтического агента и т.д. В некоторых вариантах осуществления, способ лечения рака у человека включает введение субъекту терапевтически эффективной дозы неоантигенного терапевтического агента в комбинации с терапевтически эффективной дозой химиотерапевтического агента, где один или оба агента вводят согласно стратегии прерывистого введения. В некоторых вариантах осуществления, способ лечения рака у человека включает введение субъекту терапевтически эффективной дозы неоантигенного терапевтического агента в комбинации с терапевтически эффективной дозой второго иммунотерапевтического агента, где один или оба агента вводят согласно стратегии прерывистого введения. В некоторых вариантах осуществления, стратегия прерывистого введения включает введение исходной дозы неоантигенного терапевтического агента субъекту, и введение последующих доз агента приблизительно один раз каждые 2 недели. В некоторых вариантах осуществления, стратегия прерывистого введения включает введение исходной дозы неоантигенного терапевтического агента субъекту, и введение последующих доз агента приблизительно один раз каждые 3 недели. В некоторых вариантах осуществления, стратегия прерывистого введения включает введение исходной дозы неоантигенного терапевтического агента субъекту, и введение последующих доз агента приблизительно один раз каждые 4 недели. В некоторых вариантах осуществления, агент вводят с использованием стратегии прерывистого введения, и дополнительный терапевтический агент вводят еженедельно.
Настоящее описание относится к композициям, содержащим неоантигенный терапевтический агент, описанный в настоящем изобретении. Настоящее описание также относится к фармацевтическим композициям, содержащим неоантигенный терапевтический агент, описанный в настоящем изобретении, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления, фармацевтические композиции используют в иммунотерапии. В некоторых вариантах осуществления, композиции используют для ингибирования роста опухоли. В некоторых вариантах осуществления, фармацевтические композиции используют для ингибирования роста опухоли у субъекта (например, человека). В некоторых вариантах осуществления, композиции используют при лечении рака. В некоторых вариантах осуществления, фармацевтические композиции используют для лечения рака у субъекта (например, человека).
Составы готовят для хранения и использования путем комбинирования неоантигенного терапевтического агента настоящего описания с фармацевтически приемлемым носителем (например, носителем или эксципиентом). Специалисты в данной области обычно считают фармацевтически приемлемые носители, эксципиенты и/или стабилизаторы неактивными ингредиентами состава или фармацевтической композиции. Примеры составов перечислены в WO 2015/095811.
Подходящие фармацевтически приемлемые носители включают, но не ограничены ими, нетоксичные буферы, такие как фосфат, цитрат и другие органические кислоты; соли, такие как хлорид натрия; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты, такие как октадецилдиметилбензилхлорид аммония, хлорид гексаметония, хлорид бензалкония, хлорид бензетония, фенол, бутиловый или бензиловый спирт, алкилпарабены, такие как метил или пропилпарабен, катехол, резорцин, циклогексанол, 3-пентанол, и м-крезол; низкомолекулярные полипептиды (например, менее чем приблизительно 10 аминокислотных остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильный полимер, такой как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; углеводы, такие как моносахариды, дисахариды, глюкоза, манноза или декстрины; хелатирующие агенты, такие как ЭДТК; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы металлов, такие как комплексы Zn-белок; и неионные поверхностно-активные вещества, такие как TWEEN или полиэтиленгликоль (PEG). (Remington: Science и Practice of Pharmacy, 22st Edition, 2012, Pharmaceutical Press, London). В некоторых вариантах осуществления, носителем является 5% раствор декстрозы в воде.
Фармацевтические композиции, описанные в настоящем изобретении, можно вводить любым количеством способов как для местного, так и для системного лечения. Введение может быть местным, с помощью эпидермальных или трансдермальных пластырей, мазей, лосьонов, кремов, гелей, капель, суппозиториев, спреев, жидкостей и порошков; легочным, путем ингаляции или инсуффляции порошков или аэрозолей, в том числе с помощью небулайзера, интратрахеальным и интраназальным; пероральным; или парентеральным, включая внутривенное, внутриартериальное, внутриопухолевое, подкожное, внутрибрюшинное, внутримышечное (например, инъекцией или инфузией) или внутричерепное (например, интратекальное или внутрижелудочковое).
Терапевтический состав может быть в стандартной дозированной форме. Такие составы включают таблетки, пилюли, капсулы, порошки, гранулы, растворы или суспензии в воде или неводной среде, или суппозитории.
Неоантигенные пептиды, описанные в настоящем изобретении, также могут быть заключены в микрокапсулы. Такие микрокапсулы готовят, например, методами коацервации или межфазной полимеризацией, например, гидроксиметилцеллюлозных или желатиновых микрокапсул и поли-(метилметацилата), соответственно, в коллоидных системах доставки лекарств (например, липосомах, микросферах альбумина, микроэмульсиях, наночастиц) или в макроэмульсиях, как описано в Remington: Science and Practice of Pharmacy, 22st Edition, 2012, Pharmaceutical Press, London.
В некоторых вариантах осуществления фармацевтические составы включают неоантигенный терапевтический агент, описанный в настоящем изобретении, в комплексе с липосомами. Способы получения липосом известны специалистам в данной области. Например, некоторые липосомы могут быть созданы путем выпаривания с обращенной фазой с жировыми композициями, содержащими фосфатидилхолин, холестерин и PEG-дериватизированный фосфатидилэтаноламин (PEG-PE). Липосомы могут быть экструдированы через фильтры с определенным размером пор с получением липосом желаемого диаметра.
В некоторых вариантах осуществления могут быть получены препараты с замедленным высвобождением, содержащие неоантигенные пептиды, описанные в настоящем изобретении. Подходящие примеры препаратов с замедленным высвобождением включают полупроницаемые матрицы твердых гидрофобных полимеров, содержащих агент, где матрицы находятся в виде формованных изделий (например, пленок или микрокапсул). Примеры матриц с замедленным высвобождением включают сложные полиэфиры, гидрогели, такие как поли(2-гидроксиэтилметакрилат) или поли(виниловый спирт), полилактиды, сополимер L-глутаминовой кислоты и 7-этил-L-глутамата, неразлагаемый этиленвинилацетат, разлагаемый сополимер молочной и гликолевой кислот, такой как LUPRON DEPOT™ (микросферы для инъекций, состоящие из сополимера молочной и гликолевой кислоты и ацетата лейпролида), изобутират ацетата сахарозы и поли-D-(-)-3-гидроксимасляную кислоту.
Настоящее описание относится к способам лечения, включающим иммуногенную вакцину. Изобретение относится к способам лечения заболевания (такого как рак или вирусная инфекция). Способ может включать введение субъекту эффективного количества композиции, содержащей иммуногенный антиген. В некоторых вариантах осуществления, антиген содержит вирусный антиген. В некоторых вариантах осуществления, антиген содержит опухолевый антиген.
Неограничивающие примеры вакцин, которые могут быть получены, включают вакцину на основе пептида, вакцину на основе нуклеиновой кислоты, вакцину на основе антитела, вакцину на основе Т-клетки и вакцину на основе антигенпрезентирующей клетки.
Вакцинные композиции могут быть составлены с использованием одного или нескольких физиологически приемлемых носителей, включая эксципиенты и вспомогательные вещества, которые облегчают переработку активных агентов в препараты, которые можно использовать фармацевтически. Правильный состав может зависеть от выбранного пути введения. Любые хорошо известные методики, носители и эксципиенты могут использоваться как подходящие и как это понимается в данной области техники.
В некоторых случаях, вакцинная композиция составлена в виде вакцины на основе пептида, вакцины на основе нуклеиновой кислоты, вакцины на основе антитела или вакцины на клеточной основе. Например, вакцинная композиция может включать голую кДНК в катионных жировых составах; липопептиды (например, Vitiello, A. et al., J. Clin. Invest. 95:341, 1995), голую кДНК или пептиды, инкапсулированные, например, в поли(DL-лактид-ко-гликолидные) (“PLG”) микросферы (см., например, Eldridge, et al., Molec. Immunol. 28:287-294, 1991: Alonso et al, Vaccine 12:299-306, 1994; Jones et al, Vaccine 13:675-681, 1995); пептидные композиции, содержащиеся в иммуностимулирующих комплексах (ISCOMS) (например, Takahashi et al, Nature 344:873-875, 1990; Hu et al, Clin. Exp.Immunol. 113:235-243, 1998); или множество антигенных пептидных систем (MAP) (см., например, Tam, J. P., Proc. Natl Acad. Sci. U.S.A. 85:5409-5413, 1988; Tarn, J.P., J. Immunol. Methods 196:17-32, 1996). Иногда, вакцина составлена как вакцина на основе пептида или вакцина на основе нуклеиновой кислоты, в которой нуклеиновая кислота кодирует полипептиды. Иногда, вакцина составлена как вакцина на основе антитела. Иногда, вакцина составлена как вакцина на клеточной основе.
Идентифицированный аминокислотной последовательностью специфический с заболеванию иммуногенный неоантигенный пептид может быть использован для разработки фармацевтически приемлемой композиции. Источником антигена могут быть, но не ограничен ими, природные или синтетические белки, включая гликопротеины, пептиды и суперантигены; комплексы антитело/антиген; липопротеины; РНК или продукт ее трансляции; и ДНК или полипептид, кодируемый ДНК. Источник антигена также может содержать не трансформированные, трансформированные, трансфицированные или трансдуцированные клетки или клеточные линии. Клетки могут быть трансформированы, трансфицированы или трансдуцированы с использованием любого из множества векторов экспрессии или ретровирусных векторов, известных специалистам в данной области, которые можно использовать для экспрессии рекомбинантных антигенов. Экспрессия также может быть достигнута в любое подходящей клетке-хозяине, которая трансформирована, трансфицирована или трансдуцирована вектором экспрессии или ретровирусным вектором, содержащим молекулы, кодирующие рекомбинантный антиген(ы). Может использоваться любое количество протоколов трансфекции, трансформации и трансдукции, известных специалистам в данной области. Рекомбинантные векторы осповакцины и клетки, зараженные вектором осповакцины, можно использовать в качестве источника антигена.
Композиция может содержать синтетический специфический к заболеванию иммуногенный неоантигеный пептид. Композиция может содержать два или несколько специфических к заболеванию иммуногенных неоантигенных пептидов. Композиция может содержать предшественник специфического к заболеванию иммуногенного пептида (например, белок, пептид, ДНК и РНК). Предшественник специфического к заболеванию иммуногенного пептида может создавать или быть созданным для идентифицированного специфического к заболеванию иммуногенного неоантигеного пептида. В некоторых вариантах осуществления, терапевтическая композиция содержит предшественник иммуногенного пептида. Предшественником специфического к заболеванию иммуногенного пептида может быть пролекарство. В некоторых вариантах осуществления, композиция, содержащая специфический к заболеванию иммуногенный неоантигенный пептида может дополнительно включать адъювант. Например, неоантигенный пептид может использоваться в качестве вакцины. В некоторых вариантах осуществления, иммуногенная вакцина может содержать фармацевтически приемлемый иммуногенный неоантигеный пептид. В некоторых вариантах осуществления, иммуногенная вакцина может содержать фармацевтически приемлемый предшественник иммуногенного неоантигеного пептида (такой как белок, пептид, ДНК и РНК). В некоторых вариантах осуществления, способ лечения включает введение субъекту эффективного количества антитела, специфически распознающего иммуногенный неоантигеный пептид. В некоторых вариантах осуществления, способ лечения включает введение субъекту эффективного количества растворимого TCR или аналога TCR, специфически распознающего иммуногенный неоантигеный пептид.
Способы, описанные в настоящем изобретении, особенно полезны в контексте персонализированной медицины, где иммуногенные неоантигенные пептиды используют для разработки терапевтических агентов (таких как вакцины или терапевтические антитела) для того же индивидуума. Таким образом, способ лечения заболевания у субъекта может содержать идентификацию иммуногенного неоантигенного пептида у субъекта согласно способам, описанным в настоящем изобретении; и синтез пептида (или его предшественника); и введение пептида или антитела, специфически распознающего пептид, субъекту. В некоторых вариантах осуществления, шаблон экспрессии иммуногенного неоантигена может служить в качестве существенной основы для создания специфических вакцин для пациента. В некоторых вариантах осуществления, шаблон экспрессии иммуногенного неоантигена может служить в качестве существенной основы для создания вакцины для группы пациентов с конкретным заболеванием. Таким образом, конкретные заболевания, например, конкретные типы опухолей, могут селективно лечиться у группы пациентов.
В некоторых вариантах осуществления, пептиды, описанные в настоящем изобретении, являются структурно нормальными антигенами, которые могут быть распознаны аутологическими анти-болезненными Т-клетками в больших группах пациентов. В некоторых вариантах осуществления, шаблон экспрессии антигена группы субъектов с заболеванием, у которые определено заболевание, экспрессирующее структурно нормальные неоантигены.
В некоторых вариантах осуществления, пептиды, описанные в настоящем изобретении, содержат первый пептид, содержащий первый неоэпитоп белка, и второй пептид, содержащий второй неоэпитоп того же белка, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит мутацию и второй неоэпитоп содержит ту же мутацию. В некоторых вариантах осуществления, пептиды, описанные в настоящем изобретении, содержат первый пептид, содержащий первый неоэпитоп первой области белка, и второй пептид, содержащий второй неоэпитоп второй области того же белка, где первая область содержит по меньшей мере одну аминокислоту второй области, где первый пептид отличается от второго пептида, и где первый неоэпитоп содержит первую мутацию и второй неоэпитоп содержит вторую мутацию. В некоторых вариантах осуществления, первая мутация и вторая мутация являются одинаковыми. В некоторых вариантах осуществления, мутация выбрана из группы, состоящей из точечной мутации, мутации сайта сплайсинга, мутации «сдвига рамки», мутации сквозного прочитывания, мутации слияния генов и любой их комбинации.
Существует множество способов получения иммуногенных неоантигенов. Белки или пептиды могут быть получены любым методом, известным специалистам в данной области, включая экспрессию белков, полипептидов или пептидов с помощью стандартных молекулярно-биологических методов, выделение белков или пептидов из природных источников, in vitro трансляцию или химический синтез белков или пептидов. Как правило, такие специфические к заболеванию неоантигены можно получать in vitro или in vivo. Иммуногенные неоантигены можно получать in vitro в виде пептидов или полипептидов, которые затем могут быть составлены в персонализированную вакцину или иммуногенную композицию и введены субъекту. In vitro получение иммуногенных неоантигенов может содержать пептидный синтез или экспрессию пептида/полипептида из ДНК или РНК молекулы в любой из множества бактериальных, эукариотических или вирусных рекомбинантных систем экспрессии, с последующей очисткой экспрессированного пептида/полипептида. Альтернативно, иммуногенные неоантигены могут быть получены in vivo введением молекул (например, ДНК, РНК и вирусных систем экспрессии), которые кодируют иммуногенный неоантиген, в субъекта, при этом экспрессируются кодированные иммуногенные неоантигены. В некоторых вариантах осуществления, полинуклеотид, кодирующий иммуногенный неоантигеный пептид, может использоваться для получения неоантигеного пептида in vitro.
В некоторых вариантах осуществления, полинуклеотид содержит последовательность с по меньшей мере 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности к полинуклеотиду, кодирующему иммуногенный неоантиген.
Полинуклеотидом может быть, например, ДНК, кДНК, ПНК, CNA, РНК, одно- и/или двухцепочечные, нативные или стабилизированные формы полинуклеотидов или их комбинации. Последовательности нуклеиновых кислот, кодирующих иммуногенный неоантиген пептид, может содержать или не содержать интроны до тех пор, пока последовательности нуклеиновых кислот кодируют пептид. В некоторых вариантах осуществления in vitro трансляцию используют для получения пептида.
Также рассматриваются векторы экспрессии, содержащие последовательности, кодирующие неоантиген, а также клетки-хозяева, содержащие вектор экспрессии. Векторы экспрессии, подходящие для использования в настоящем описании, могут содержать по меньшей мере один элемент контроля экспрессии, функционально связанный с последовательностью нуклеиновых кислот. Элементы контроля экспрессии вставлены в вектор для контроля и регулирования экспрессии последовательности нуклеиновых кислот. Примеры элементов контроля экспрессии хорошо известны в данной области и включают, например, систему lac, операторные и промоторные области фага лямбда, дрожжевые промоторы и промоторы, полученные из полиомы, аденовируса, ретровируса или SV40. Дополнительные функциональные элементы включают, но не ограничены ими, лидерные последовательности, стоп-кодоны, сигналы полиаденилирования и любые другие последовательности, необходимые или предпочтительные для соответствующей транскрипции и последующей трансляции последовательностей нуклеиновых кислот в системе хозяина. Специалисту будет понятно, что правильная комбинация элементов контроля экспрессии будет зависеть от выбранной системы хозяина. Далее будет понятно, что вектор экспрессии должен содержать дополнительные элементы, необходимые для переноса и последующей репликации вектора экспрессии, содержащего последовательность нуклеиновых кислот, в системе хозяина. Примеры таких элементов включают, но не ограничены ими, точки начала репликации и селектируемый маркер.
Неоантигенные пептиды могут быть представлены в форме РНК или кДНК молекул, кодирующих желаемые неоантигенные пептиды. Один или более неоантигенных пептидов согласно настоящему описанию могут кодироваться одним вектором экспрессии. Обычно, ДНК вставляют в вектор экспрессии, такой как плазмида, в нужном направлении и в корректной рамке считывания для экспрессии, при необходимости, ДНК может быть связана с подходящим транскрипционными и трансляционными регуляторными контрольными нуклеотидными последовательностями, распознанными желаемым хозяином (например, бактерией), хотя такие контроли обычно доступны в векторе экспрессии. Вектор затем вводят в бактерию-хозяина для клонирования с использованием стандартной методики. Полезные векторы экспрессии для эукариотических хозяев, особенно млекопитающего или человека, включают, например, векторы, содержащие последовательности контроля экспрессии из SV40, вируса папилломы крупного рогатого скота, аденовируса и цитомегаловируса. Полезные векторы экспрессии для бактериальных хозяев включают известные бактериальные плазмиды, такие как плазмиды из E. coli, включая pCR 1, pBR322, pMB9 и их производные, плазмиды с более широким диапазоном хозяев, такие как M13 и нитевидные фаги одноцепочечной ДНК.
В вариантах осуществления, ДНК последовательность, кодирующая полипептид, представляющий интерес, может быть сконструирована химическим синтезом с использованием олигонуклеотидного синтезатора. Такие олигонуклеотиды могут быть сконструированы на основе аминокислотной последовательности желаемого полипептида и выбором таких кодонов, которые благоприятны в клетке-хозяине, в которой продуцируется полипептид, представляющий интерес. Стандартные способы могут использоваться для синтеза выделенных полинуклеотидных последовательностей, кодирующих выделенный полипептид, представляющий интерес.
Подходящие клетки-хозяева для экспрессии полипептида включают прокариоты, дрожжи, клетки насекомых или высшие эукариотические клетки под контролем подходящих промоторов. Прокариоты включают грамотрицательные или грамположительные организмы, например E. coli или бациллы. Высшие эукариотические клетки включают устойчивые клеточные линии, происходящие от млекопитающих. Также могут использоваться бесклеточные системы трансляции. Подходящие векторы клонирования и экспрессии для применения с бактериальными, грибковыми, дрожжевыми и млекопитающими клеточными хозяевами хорошо известны в данной области техники. Разные системы культивирования клеток млекопитающих или насекомых могут использоваться для экспрессирования рекомбинантного белка. Типовые клеточные линии клеток-хозяев млекопитающих включают, но не ограничены ими, клеточные линии COS-7, L клеток, C127, 3T3, яичников китайского хомяка (CHO), 293, HeLa и BHK. Векторы экспрессии млекопитающих могут содержать не транскрибированные элементы, такие как точка начала репликации, подходящий промотор и усиленный линкер для экспрессируемого гена, и другие 5’ или 3’ фланкирующие не транскрибированные последовательности, и 5’ или 3’ не транслированные последовательности, такие как необходимые сайты связывания рибосомы, сайт полиаденилирования, сайты донора и акцептора сплайсинга и последовательности терминации транскрипции.
Белки, продуцированные трансформированным хозяином, могут быть очищены любым подходящим способом. Такие стандартные способы включают хроматографию (например, ионообменную, аффинную и колоночную хроматографию с распределением по размерам, и подобные), центрифугирование, дифференциальную растворимость или любую другую стандартную методику очистки белков. Аффинные метки, такие как гексагистидин (SEQ ID NO: 3211), домен связывания мальтозы, последовательность вируса гриппа, глутатион-S-трансфераза и подобные могут быть присоединены к белку для простоты очистки пропусканием через колонку с подходящей аффинностью. Выделенные белки также могут быть физически охарактеризованы с использованием таких методик, как протеолиз, ядерный магнитный резонанс и рентгеновская кристаллография.
Вакцина может содержать вещество, которое связывает полипептидную последовательность, описанную в настоящем изобретении. Веществом может быть антитело. Вакцина на основе антитела может быть составлены с использованием любых хорошо известных методик, носителей и эксципиентов, как подходит и как понимается в данной области техники. В некоторых вариантах осуществления, пептиды, описанные в настоящем изобретении, могут использоваться для получения неоантиген-специфических терапевтических агентов, таких как терапевтическое антитело. Например, неоантигены могут использоваться для повышения и/или идентификации антитела, специфически распознающего неоантигены. Эти антитела могут использоваться в качестве терапевтических агентов. Антителом может быть природное антитело, химерное антитело, гуманизированное антитело или может быть фрагмент антитела. Антитело может распознавать один или более полипептидов, описанных в настоящем изобретении. В некоторых вариантах осуществления, антитело может распознавать полипептид, имеющий последовательность с, самое большее 40%, 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности к полипептиду, описанному в настоящем изобретении. В некоторых вариантах осуществления, антитело может распознавать полипептид, имеющий последовательность с по меньшей мере 40%, 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью последовательности с полипептидом, описанным в настоящем изобретении. В некоторых вариантах осуществления, антитело может распознавать полипептидную последовательность, которая составляет по меньшей мере 30%, 40%, 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% длины полипептида, описанного в настоящем изобретении. В некоторых вариантах осуществления, антитело может распознавать полипептидную последовательность, которая составляет, самое большее 30%, 40%, 50%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% длины полипептида, описанного в настоящем изобретении.
В настоящем описании также рассматривается использование молекул нуклеиновых кислот в качестве носителей для доставки неоантигенных пептидов/полипептидов субъекту, нуждающемуся в этом, in vivo, в форме, например, ДНК/РНК вакцин.
В некоторых вариантах осуществления вакциной является вакцина нуклеиновой кислоты. В некоторых вариантах осуществления неоантигены можно вводить субъекту с использованием плазмиды. Плазмиды можно вводить в ткани животных различными способами, например, инъекцией или аэрозольной инстилляцией голой ДНК на поверхности слизистых оболочек, таких как слизистая оболочка носа и легких. В некоторых вариантах осуществления может использоваться физическая доставка, такая как «генная пушка». Точный выбор вектора экспрессии может зависеть от того, какие пептиды/полипептиды будут экспрессированы, и находится в компетенции специалистов в данной области техники.
В некоторых вариантах осуществления, нуклеиновая кислота кодирует иммуногенный пептид или предшественник пептида. В некоторых вариантах осуществления, вакцина нуклеиновой кислоты содержит последовательности фланкирующих последовательностей, кодирующих иммуногенный пептид или предшественник пептида. В некоторых вариантах осуществления, вакцина нуклеиновой кислоты содержит более чем один иммуногенный эпитоп. В некоторых вариантах осуществления, вакциной нуклеинов кислот является вакцина на основе ДНК. В некоторых вариантах осуществления, вакциной нуклеиновой кислоты является вакцина на основе РНК. В некоторых вариантах осуществления, вакцина на основе РНК содержит мРНК. В некоторых вариантах осуществления, вакцина на основе РНК содержит голую мРНК. В некоторых вариантах осуществления, вакцина на основе РНК содержит модифицированную мРНК (например, мРНК, защищенную от разложения с использованием протамина, мРНК, содержащую 5’ CAP структуру или мРНК, содержащую модифицированные нуклеотиды). В некоторых вариантах осуществления, вакцина на основе РНК содержит одноцепочечную мРНК.
Полинуклеотид может быть по существу чистым или содержаться в подходящем векторе или системе доставки. Подходящие векторы и системы доставки включают вирус, такой как системы на основе аденовируса, вируса осповакцины, ретровирусов, герпесвируса, адено-ассоциированного вируса или гибридов, содержащих элементы более одного вируса. Не вирусные системы доставки включают катионные жиры и катионный полимер (например, катионные липосомы.
Один или более неоантигенных пептидов могут кодироваться и экспрессированы in vivo с использованием системы на основе вируса. Вирусные векторы могут использоваться в качестве рекомбинантных векторов в настоящем описании, где часть вирусного генома удалена для введения новых генов, без разрушения инфекционности вируса. Вирусным вектором настоящего описания является не патогенный вирус. В некоторых вариантах осуществления, вирусный вектор имеет тропизм для конкретного типа клеток у млекопитающего. В другом варианте осуществления, вирусный вектор настоящего описания способен заражать профессиональные антигенпрезентирующие клетки, такие как дендритные клетки и макрофаги. В еще одном варианте осуществления настоящего описания, вирусный вектор способен заражать любую клетку млекопитающего. Вирусный вектор также может заражать опухолевые клетки. Вирусные векторы, используемые в настоящем описании, включают, но не ограничиваются ими, поксвирус, такой как вирус осповакцины, авипокс вирус, вирус оспы кур и сильно ослабленный вирус осповакцины (Анкара или MVA), ретровирус, аденовирус, бакуловирус и подобные.
Вакцина может быть доставлена разными путями. Пути доставки могут включать пероральное (включая буккальное и сублингвальное), ректальное, назальное, местное, трансдермальный пластырь, легочное, вагинальное, суппозиторием или парентеральное (включая внутримышечное, внутриартериальное, интратекальное, внутрикожное, внутрибрюшинное, подкожное и внутривенное) введение, или в форме, подходящей для введения путем аэрозолизации, ингаляции или инсуффляции. Общую информацию о системах доставки лекарств можно найти в Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems (Lippencott Williams & Wilkins, Baltimore Md. (1999). Вакцина, описанная в настоящем изобретении, может быть введена в мышцу или может быть введена с помощью внутрикожных или подкожных инъекций или трансдермально, например, с помощью ионтофореза. Может использоваться эпидермальное введение вакцины.
В некоторых случаях вакцина также может быть составлена для введения через носовые ходы. Составы, подходящие для назального введения, где носитель является твердым, могут включать крупный порошок, имеющий размер частиц, например, в диапазоне от приблизительно 10 до приблизительно 500 микрон, который вводится таким же образом, как принимается нюхательный табак, т. е. путем быстрого вдыхания через носовой проход из контейнера с порошком, поднесенного близко к носу. Состав может быть назальным спреем, назальными каплями или аэрозолем, вводимым с помощью небулайзера. Состав может включать водные или масляные растворы вакцины.
Вакцина может быть жидким препаратом, таким как суспензия, сироп или эликсир. Вакцина также быть препаратом для парентерального, подкожного, внутрикожного, внутримышечного или внутривенного введения (например, введения инъекцией), таким как стерильная суспензия или эмульсия.
Вакцина может включать материал для однократной иммунизации или может включать материал для множественной иммунизации (то есть набор «многократных доз»). Включение консерванта предпочтительно в схемах приема нескольких доз. В качестве альтернативы (или в дополнение) к включению консерванта в многодозовые композиции, композиции могут содержаться в контейнере, имеющем асептический адаптер для удаления материала.
Вакцина может быть введена в дозе приблизительно 0,5 мл, хотя детям можно вводить половинную дозу (т.е. приблизительно 0,25 мл). Иногда вакцину можно вводить в более высокой дозе, например, приблизительно 1 мл.
Вакцина может быть введена в виде 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более курсовых схем. Иногда вакцину вводят как 1, 2, 3 или 4-курсовую схему. Иногда вакцину вводят как 1-курсовую схему. Иногда вакцину вводят как 2-х курсовую схему.
Введение первой дозы и второй дозы может быть разделено, приблизительно 0 днем, 1 днем, 2 днями, 5 днями, 7 днями, 14 днями, 21 днем, 30 днями, 2 месяцами, 4 месяцами, 6 месяцами, 9 месяцами, 1 годом, 1,5 годами, 2 годами, 3 годами, 4 годами или более.
Вакцина, описанная в настоящем изобретении, может вводиться каждые 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более лет. Иногда, вакцину, описанную в настоящем изобретении, вводят каждые 2, 3, 4, 5, 6, 7 или более лет. Иногда, вакцину, описанную в настоящем изобретении, вводят каждые 4, 5, 6, 7 или более лет. Иногда, вакцину, описанную в настоящем изобретении, вводят один раз.
Примеры дозировок не являются ограничивающими и используются только для иллюстрации конкретных схем дозирования для введения вакцины, описанной в настоящем изобретении. эффективное количество для применения у человека можно определить на животных моделях. Например, доза для людей может быть составлена для достижения концентраций в крови, печени, местном и/или желудочно-кишечном тракте, которые, как было обнаружено, эффективны для животных. На основе данных о животных и других типов подобных данных, специалисты в данной области могут определить эффективные количества вакцинной композиции, подходящие для людей.
Эффективное количество относительно агента или комбинации агентов обычно будет означать диапазоны доз, способы введения, составы и т. д., которые были рекомендованы или одобрены любой из различных регулирующих или консультативных организаций в области медицины или фармацевтики (например, FDA, AMA) или производителем или поставщиком.
В некоторых аспектах, вакцина и набор, описанные в настоящем изобретении, могут храниться при от 2°C до 8°C. В некоторых случаях, вакцину не хранят замороженной. В некоторых случаях, вакцину хранят при температурах -20°C или -80°C. В некоторых случаях, вакцину хранят в месте, защищенном от солнечного света.
Наборы
Неоантигенный терапевтический агент, описанный в настоящем изобретении, может быть представлен в форме набора вместе с инструкциями по применению. Обычно набор должен включать желаемый неоантигеный терапевтический агент в контейнере, в стандартной дозированной форме, и инструкции по применению. В набор также могут быть включены дополнительные терапевтические агенты, например, цитокины, лимфокины, ингибиторы иммунных контрольных точек, антитела. Другие компоненты набора, которые также могут быть желательными, включают, например, стерильный шприц, дозы активатора и другие желаемые эксципиенты.
Настоящее изобретение также относится к наборам и готовым изделиям для использования с одним или несколькими способами, описанными в настоящем изобретении. Наборы могут содержать один или более неоантигенных полипептидов, содержащих один или более неоэпитопов. Наборы также могут содержать нуклеиновые кислоты, которые кодируют один или более пептидов или белков, описанных в настоящем изобретении, антитела, которые распознают один или более пептидов, описанных в настоящем изобретении, или клетки на основе APC, активированные одним или несколькими пептидами, описанными в настоящем изобретении. Наборы могут дополнительно содержать адъюванты, реагенты и буферы, необходимые для производства и доставки вакцин.
Наборы могут также включать носитель, упаковку или контейнер, который разделен на отсеки для приема одного или нескольких контейнеров, таких как флаконы, ампулы и подобные, где каждый из контейнеров содержит один из отдельных элементов, таких как пептиды и адъюванты, которые будут использоваться в способе, описанном в настоящем изобретении. Подходящие контейнеры включают, например, бутылки, флаконы, шприцы и пробирки. Контейнеры могут быть изготовлены из различных материалов, таких как стекло или пластик.
Представленные здесь готовые изделия содержат упаковочные материалы. Примеры фармацевтических упаковочных материалов включают, но не ограничены ими, блистерные упаковки, бутылки, пробирки, пакеты, контейнеры, флаконы и любой упаковочный материал, подходящий для выбранной композиции и предполагаемого способа введения и лечения. Набор обычно включает этикетки с указанием содержимого и/или инструкции по применению, и вкладыши в упаковку с инструкциями по применению. Также обычно включен набор инструкций.
Настоящее описание будет описано более подробно на конкретных примерах. Следующие примеры предлагаются в иллюстративных целях и никоим образом не предназначены для ограничения настоящего описания. Специалисты в данной области легко распознают множество не критических параметров, которые могут быть изменены или модифицированы для получения альтернативных вариантов осуществления в соответствии с настоящим описанием. Все патенты, заявки на патенты и печатные публикации, перечисленные здесь, полностью включены в настоящий документ в качестве ссылки.
ПРИМЕРЫ
Эти примеры представлены только для иллюстративных целей и не ограничивают объем формулы изобретения, представленной здесь.
Пример 1 – Вызов ответов CD4+ и CD8+ Т-клеток
In vitro индукцию Т-клетки используют для размножения неоантиген-специфических Т-клеток. Зрелые профессиональные APC получают для этих анализов следующим образом. Моноциты обогащают из PBMC здорового донора-человека с использованием набора на основе сфер (Miltenyi). Обогащенные клетки высевают в GM-CSF и IL-4 для индуцирования незрелых DC. Через 5 дней, незрелые DC инкубируют при 37°C с пулами пептидов в течение 1 часа, затем добавляют коктейль для созревания цитокинов (GM-CSF, IL-1β, IL-4, IL-6, TNFα, PGE1β). Пулы пептидов могут включать множество мутаций, и с шортмерами и с лонгмерами, для размножения CD8+ и CD4+ Т-клеток, соответственно. Клетки инкубируют при 37°C до созревания DC.
После созревания DC, PBMC (либо объединенные, либо обогащенные для Т-клеток) добавляют к зрелым дендритным клеткам с цитокинами пролиферации. Культуры отслеживают на пептид-специфические Т-клетки с использованием комбинации функциональных анализов и/или окрашивания тетрамера. Параллельные анализы иммуногенности с модифицированными и исходными пептидами позволяют сравнить относительную эффективность, с которой пептиды размножают пептид-специфические Т-клетки.
Пример 2- Анализ окрашивания тетрамера
MHC тетрамер покупают или производят на месте и используют для измерения пептид-специфического размножения Т-клеток в анализах иммуногенности. Для оценки, тетрамер добавляют к 1x105 клеткам в ФРФБ, содержащем 1% ФТС и 0,1% азида натрия (буфере FACS) согласно инструкциям производителя. Клетки инкубируют в темноте в течение 20 минут при комнатной температуре. Антитела, специфические к маркерам Т-клетки, таким как CD8, затем добавляют в конечной концентрации, предложенной производителем, и клетки инкубируют в темноте при 4°C в течение 20 минут. Клетки промывают холодным буфером FACS и ресуспендируют в буфере, содержащем 1% формальдегида. Информацию по клеткам получают на инструменте FACS Calibur (Becton Dickinson) и анализируют с использованием программы Cellquest (Becton Dickinson). Для анализа положительных к тетрамеру клеток, лимфоцитарные «ворота» берут из графиков прямого и бокового рассеяния. Данные представлены как доля клеток, которые были CD8+/тетрамер+.
Пример 3 – Анализ внутриклеточного окрашивания цитокина
В отсутствие хорошо налаженного окрашивания тетрамером для идентификации антиген-специфических популяций Т-клеток, специфичность к антигену может быть оценена с использованием оценки продуцирования цитокина с использованием хорошо налаженных анализов проточной цитометрии. Коротко, Т-клетки стимулируют пептидом, представляющим интерес, и сравнивают с контролем. После стимулирования продуцирование цитокинов CD4+ Т-клетками (например, IFNγ и TNFα) оценивают внутриклеточным окрашиванием. Эти цитокины, особенно IFNγ, могут использоваться для идентификации стимулированных клеток. На ФИГ. 11 изображен анализ FACS антиген-специфической индукции IFNγ и TNFα уровней в CD4+ клетках от здорового HLA-A02:01 донора, стимулированных APC, загруженными с или без GATA3 neoORF пептида.
Пример 4 – Анализ ELISPOT
Пептид-специфические Т-клетки функционально высчитывают с использованием анализа ELISPOT (BD Biosciences), который измеряет выделение IFNγ из Т-клеток на одноклеточной основе. В клетки-мишени (T2 или HLA-A0201 трансфицированные C1R) вводят 10 мкМ пептида в течение 1 часа при 37°C и промывают три раза. 1x105 мишеней с добавленным пептидом совместно культивируют в лунках планшета ELISPOT с разными концентрациями Т-клеток (5x102 до 2x103), взятых из иммуногенной культуры. Планшеты обрабатывают согласно протоколу производителя и анализируют на ридере ELISPOT (Cellular Technology Ltd.) с использованием прилагаемой программы. Споты, соответствующие количеству IFNγ-продуцирующих Т-клеток, указывают как абсолютное количество спотов на количество высеянных Т-клеток. Т-клетки, размноженные на модифицированных пептидах, тестируют не только на их способность распознавать мишени, в которые введен модифицированный пептид, но также на их способность распознавать мишени, в которые добавлен исходный пептид. На ФИГ. 35 представлен график, показывающий антиген-специфическую индукцию IFNγ. Показаны уровни IFNγ двух образцов с имитацией трансдукции или трансдуцированных лентивирусным вектором экспрессии, кодирующим GATA3 neoORF пептид.
Пример 5 – Анализ окрашивания CD107
CD107a и b экспрессируют на клеточной поверхности CD8+ Т-клеток с последующей активацией распознанным пептидом. Протеазосодержащие вакуоли Т-клеток имеют жировой бислой, который содержит ассоциированные с лизосомами мембранные гликопротеины (“LAMPs”), которые включают молекулы CD107a и b. Когда цитотоксические Т-клетки активируют через Т-клеточный рецептор, мембраны этих протеазосодержащих вакуолей мобилизуют и сливают с плазматической мембраной Т-клетки. Содержание гранул выделяется, и это приводит к смерти клетки-мишени. Поскольку мембрана вакуолей сливается с плазматической мембраной, C107a и b появляются на поверхности клетки и поэтому являются маркерами дегрануляции. Так как дегрануляция по данным CD107a и b окрашивания указывается на одноклеточной основе, анализ используют для функционального подсчета пептид-специфических Т-клеток. Для проведения анализа, пептид добавляют к HLA-A02:01-трансфицированным клеткам C1R до конечной концентрации 20 мкМ, клетки инкубируют в течение 1 часа при 37°C и промывают три раза. 1x105 C1R клеток с добавлением пептида аликвотируют в пробирки, и антитела, специфические к CD107a и b добавляют до конечной концентрации, предложенной производителем (Becton Dickinson). Антитела добавляют до добавления Т-клеток для «улавливания» CD107 молекул, когда они временно появляются на поверхности во время анализа. Затем добавляют 1x105 Т-клеток из иммуногенной культуры, и образцы инкубируют в течение 4 часов при 37°C. Т-клетки затем дополнительно окрашивают для дополнительных поверхностноклеточных молекул, таких как CD8, и информацию получают на инструменте FACS Calibur (Becton Dickinson). Данные анализируют с использованием прилагаемой программы Cellquest, и показывают как долю CD8+/CD107a и b+ клеток. На ФИГ. 34 представлен график, показывающий антиген-специфическую индукцию цитотоксического маркера CD107a. Показана доля CD107a+ клеток от общего количества CD8+ клеток из двух образцов с имитацией трансдукции или трансдуцированных лентивирусным вектором экспрессии, кодирующим GATA3 neoORF пептид.
Пример 6 – Цитотоксические анализы
Цитотоксическую активность измеряют с использованием способа 1 или способа 2. Способ 1 подразумевает анализ выделения хрома. T2 клетки-мишени метят Na51Cr в течение 1 часа при 37°C и промывают, 5x1035 x 103 T2 клеток-мишеней затем добавляют к разным количествам Т-клеток из иммуногенной культуры. Выделение хрома измеряют в супернатанте, собранном через 4 часа инкубации при 37°C. Долю специфического лизиса рассчитывают как:
Уравнение 10. Экспериментальное выделение-спонтанное выделение/Общее выделение-спонтанное выделение x 100.
В способе 2 цитотоксическую активность измеряют определением расщепленной каспазы 3 в клетках-мишенях через проточную цитометрию. Раковые клетки-мишени конструируют для экспрессии мутантного пептида вместе с подходящей MHC-I аллелем. Клетки-мишени с имитированной трансдукцией (т.е. не экспрессирующие мутантный пептид) используют в качестве отрицательного контроля. Клетки метят CFSE для того, чтобы отличить их от стимулированных PBMC, применяемых в качестве клеток-эффекторов. Мишени и клетки-эффекторы совместно культивируют в течение 6 часов до сбора. Внутриклеточное окрашивание проводят для определения расщепленной формы каспазы 3 в CFSE-положительных раковых клетках-мишенях. Долю специфического лизиса рассчитывают как:
Уравнение 11. Экспериментальное расщепление каспазы 3/спонтанное расщепление каспазы 3 (измеренное в отсутствие экспрессии мутантного пептида) x 100.
Анализ цитотоксичности способом 2 представлен в разделе «Материалы и способы» в примере 25 в настоящем изобретении.
Пример 7 – Улучшенные ответы CD8+ Т-клетки in vivo с использованием лонгмеров и шортмеров последовательно
Вакцинация лонгмерными пептидами может вызвать ответы и CD4+ и CD8+ Т-клеток, в зависимости от процессинга и презентирования пептидов. Вакцинация минимальными шортмерными эпитопами сфокусирована на создании ответов CD8+ Т-клетки, но не требует процессинга пептида до антигенного презентирования. Как таковая, любая клетка может легко презентировать эпитоп, а не только профессиональные антигенпрезентирующие клетки (APC). Это может привести к толерантности Т-клеток, которые контактируют со здоровыми клетками, презентирующими антигены как часть периферической толерантности. Чтобы обойти это, исходная иммунизация лонгмером позволяет примировать CD8+ Т-клетки только APC, которые могут процессировать и презентировать пептиды. Последующие иммунизации усиливают ответы CD8+ Т-клетки.
Анализы иммуногенности in vivo
Девятнадцать самок мышей C57BL/6 в возрасте 8-12 недель (Taconic Biosciences) произвольно и планово распределяют на группы обработки при поступлении. Животных акклиматизируют в течение трех (3) дней до начала исследования. Животных кормят стерильным кормом для грызунов LabDiet™ 5053, и стерильную воду дают ad libitum. Животные в группе 1 служат в качестве контроля с только адъювантом, и им вводят только полиинозиновую:полицитидиловую кислоту (полиI:C) в дозе 100 мкг в объеме 0,1 мл подкожной инъекцией (п.к.) в дни 0, 7 и 14. Животным в группе 2 вводят по 50 мкг каждого из шести лонгмерных пептидов (описанных ниже) вместе с полиI:C в дозе 100 мкг п.к. в объеме 0,1 мл в дни 0, 7 и 14. Животным в группе 3 вводят по 50 мкг каждого из шести лонгмерных пептидов (описанных ниже) вместе с полиI:C в дозе 100 мкг п.к. в объеме 0,1 мл в день 0 и молярные эквиваленты соответствующих шортмерных пептидов (описаны ниже) вместе с полиI:C в дозе 100 мкг п.к. в объеме 0,1 мл в дни 7 и 14. Животных взвешивают и ежедневно отслеживают общее состояние здоровья. Животных умерщвляют сверхдозой CO2 в день 21 завершения исследования, если животное теряет >30% массы тела по сравнению с массой в день 0; или если животное обнаружено агонирующим. При умерщвлении, селезенки собирают и обрабатывают в одноклеточные суспензии с использованием стандартных протоколов. Коротко, селезенки механически разрушают через 70 мкМ фильтр, пеллетируют и лизируют с ACK лизисным буфером (Sigma) перед ресуспендированием в среде для культивирования клеток.
Пептиды
Шесть ранее идентифицированных неоантигенов мыши используют на основе продемонстрированной ими способности вызывать ответы CD8+ Т-клетки. Для каждого неоантигена, был определен шортмер (8-11 аминокислот), соответствующий минимальному эпитопу. Используют лонгмер, соответствующий 20-27 аминокислотам, окружающим мутацию.
ELISPOT
Анализ ELISPOT (Mouse IFNγ ELISPOT Reasy-SET-Go; EBioscience) проводят согласно протоколу набора. Коротко, за день до анализа, 96-луночные фильтровальные планшеты (гидрофобная PVDF мембрана с размером пор 0,45 мкМ; EMD Millipore) активируют (35% EtOH), промывают (ФРФБ) и покрывают иммобилизованным антителом (1:250; 4°C O/N). В день анализа, лунки промывают и блокируют (среда; 2 часа при 37°C). Приблизительно 2x105 клеток в 100 мкл добавляют в лунки вместе с 100 мкл 10 мМ тестируемого пептидного пула (шортмер) или PMA/иономицин положительным контрольным антигеном или носителем. Клетки инкубируют с антигеном в течение ночи (16-18 часов) при 37°C. На следующий день суспензию клеток вынимают и лунки промывают один раз ФРФБ и два раза деионизированной водой. Для всех стадий промывки в оставшейся части анализа, лунки замачивают на 3 минуты на каждой стадии промывки. Затем лунки промывают три раза промывочным буфером (ФРФБ+0,05% Tween-20), и идентифицирующее антитело (1:250) добавляют во все лунки. Планшеты инкубируют в течение двух часов при комнатной температуре. Раствор идентифицирующего антитела удаляют, и лунки промывают три раза буфером. Авидин-HRP (1:250) добавляют во все лунки, и планшеты инкубируют в течение одного часа при комнатной температуре. Раствор конъюгата удаляют, и лунки три раза промывают промывочным буфером, затем один раз ФРФБ. Субстрат (3-амино-9-этилкарбазол, 0,1 M в ацетатном буфере, H2O2) добавляют во все лунки, и отслеживают развитие спота (приблизительно 10 минут). Субстратную реакцию останавливают промыванием лунок водой, и планшеты сушат на воздухе в течение ночи. Планшеты анализируют на ридере ELISPOT (Cellular Technology Ltd.) с использованием прилагаемой программы. Споты, соответствующие количеству IFNγ-продуцирующих Т-клеток, показывают как абсолютное количество спотов на количество высеянных Т-клеток.
Пример 8 – Определение GATA3 neoORF пептидов масс спектрометрией
Клетки 293Т трансдуцируют лентивирусным вектором, кодирующим разные области пептидов, кодированных GATA3 neoORF. 50-700 миллионов трансдуцированных клеток, экспрессирующих пептиды, кодированные GATA3 neoORF последовательностью, культивируют, и пептиды элюируют из комплексов HLA-пептид с использованием кислой промывки. Элюированные пептиды затем анализируют МС/МС. Для клеток 293Т, экспрессирующих HLA-A02:01 белок, пептиды VLPEPHLAL (SEQ ID NO: 3212), SMLTGPPARV (SEQ ID NO: 3213) и MLTGPPARV (SEQ ID NO: 3214) определяют масс спектрометрией (ФИГ. 5). Для клеток 293Т, экспрессирующих HLA-B07:02 белок, пептиды KPKRDGYMF (SEQ ID NO: 3215) и KPKRDGYMFL (SEQ ID NO: 3216) определяют масс спектрометрией (ФИГ. 5). Для клеток 293Т, экспрессирующих HLA-B08:01 белок, пептид ESKIMFATL (SEQ ID NO: 3217) определяют масс спектрометрией (ФИГ. 5).
Пример 9 - GATA3 neoORF продуцирует сильные эпитопы на множестве аллелей.
Множество пептидов, содержащих неоэпитопы в таблице 4 ниже, экспрессируют или загружают в антигенпрезентирующие клетки (APC). Затем проводят масс спектрометрию и определяют аффинность неоэпитопов с указанными HLA аллелями и стабильность неоэпитопов с HLA аллелями.
В таблице 4 перечислены типовые GATA3 neoORF продуцированные эпитопы на множестве аллелей
Пример 10 – Множество неоэпитопов вызывает ответы CD8+ Т-клетки
Образцы PBMC от донора-человека используют для проведения антиген специфической индукции Т-клетки. Индукции CD8+ Т-клетки анализируют после производства Т-клеток. Образцы клеток могут быть взяты в разные моменты времени для анализа. pMHC мультимер используют для отслеживания доли антиген-специфических CD8+ Т-клеток в индукционных культурах. На FIG. 9A-9C и 10A-10B изображены типовые результаты, показывающие долю антиген-специфических CD8+ Т-клеток памяти, индуцированных и с SMLTGPPARV (SEQ ID NO: 3249) и с MLTGPPARV (SEQ ID NO: 3250), соответственно. На ФИГ. 9A изображен типовой результат анализа ответа Т-клетки с использованием PBMC от 6 разных здоровых доноров, показывающий долю антиген-специфических CD8+Т-клеток, которые отвечают на MLTGPPARV (SEQ ID NO: 3251) пептид, анализированных проточной цитометрией после стимуляции или индукции. Наблюдается повышение доли антиген-специфических Т-клеток. На ФИГ. 9B изображен типовой результат анализа ответа Т-клетки с использованием PBMC от здорового донора, показывающий долю антиген-специфических CD8+Т-клеток, которые отвечают на SMLTGPPARV (SEQ ID NO: 3252) пептид, анализированных проточной цитометрией после стимуляции или индукции. Наблюдается повышение доли антиген-специфических Т-клеток. Из пяти тестированных здоровых доноров, 4 показали повышение доли антиген специфических CD8+Т-клеток, которые отвечают на MLTGPPARV (SEQ ID NO: 3253) пептид. Анализ ответа Т-клетки с использованием PBMC от 3 разных здоровых доноров показал повышение доли антиген-специфических CD8+Т-клеток, которые отвечают на VLPEPHLAL (SEQ ID NO: 3254) пептид, анализированных проточной цитометрией после стимуляции или индукции у одного из трех доноров. На ФИГ. 9C изображен типовой результат ответа Т-клетки с использованием PBMC от HLA-A02:01, HLA-A03:01 HLA-A11:01, HLA-B07:02 и HLA-B08:01 здоровых доноров, показывающий долю антиген-специфических CD8+Т-клеток, которые отвечают на SMLTGPPARV (SEQ ID NO: 3255), MLTGPPARV (SEQ ID NO: 3256), KIMFATLQR (SEQ ID NO: 3257), KPKRDGYMFL (SEQ ID NO: 3258),KPKRDGYMF (SEQ ID NO: 3259) или ESKIMFATL (SEQ ID NO: 3260) пептид, анализированных проточной цитометрией после стимуляции или индукции. На ФИГ. 10A изображен типовой результат ответа Т-клетки с использованием PBMC от HLA-B07:02 здорового донора, показывающий долю антиген-специфических CD8+Т-клеток, которые отвечают на стимулирующий пептид KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 3261) (анализированы минимальные эпитопы KPKRDGYMF (SEQ ID NO: 3262) и KPKRDGYMFL (SEQ ID NO: 3263)). На ФИГ. 10B изображен типовой результат ответа Т-клетки с использованием PBMC от HLA-A02:01 здорового донора, показывающий долю антиген-специфических CD8+Т-клеток, которые отвечают на стимулирующий пептид SMLTGPPARVPAVPFDLH (SEQ ID NO: 3264) (анализированы минимальные эпитопы SMLTGPPARV (SEQ ID NO: 3265) и MLTGPPARV (SEQ ID NO: 3266)).
Пример 11 – Анализ цитотоксичности индуцированных Т-клеток
Анализ цитотоксичности используют для оценки того, могут ли индуцированные Т-клеточные культуры убивать антигенэкспрессирующие опухолевые колонии. В этом примере, экспрессию активной каспазы 3 на живых и мертвых опухолевых клетках измеряют для количественной оценки ранней смерти клетки и мертвых опухолевых клеток. На ФИГ. 33, индуцированные CD8+ ответы способны убивать антигенэкспрессирующие опухолевые мишени. Показана доля живых каспаза-A положительных клеток-мишеней в двух образцах, с имитацией трансдукции или трансдуцированных лентивирусным вектором экспрессии, кодирующим GATA3 neoORF пептид.
Пример 12 – Синтез пептида
Пептиды в таблице 5 ниже синтезируют и очищают. Показаны прогнозированные и определенные молекулярные массы. Также показаны неочищенные примеси и конечные примеси для указанных пептидов.
Таблица 5
Пример 13 – Тесты растворимости синтетического GATA3 neoORF пептида
Растворимость каждого пептида в таблице 6 ниже тестируют в разных указанных растворах. SS=сукцинат натрия. Тестированный состав А включает 4% ДМСО, 5 мМ сукцината натрия (SS) в D5W. Тестированный состав B включает отсутствие ДМСО, 5 мМ SS в D5W. Тестированный состав C включает отсутствие ДМСО, 0,25 мМ SS в D5W. Синтез 33мера L15, который содержит два цистеина, проводят с использованием создания псевдопролиновых структурных блоков через конъюгацию боковых цепей ES, AT и SS в последовательности. Это позволяет очищать L15 до 95% чистоты и предотвратить агрегацию во время твердофазного синтеза пептида.
В таблице 6 ниже перечислены растворимости пептида
ICLC
+ 0,5 мМ SS в D5W масс./ 4% ДМСО
ICLC
+ 0,75 мМ SS в D5W масс./ 4% ДМСО
ICLC
+ 0,25 мМ SS в D5W масс./ 4% ДМСО
ICLC
+5 мМ SS в D5W масс./ 4% ДМСО
ICLC
+ 0,25 мМ SS в D5W масс./0 ДМСО
ICLC
+ 5 мМ SS в D5W масс./0 ДМСО
ARVPAVPFDLH
(SEQ ID NO: 3295)
VPAVPFDLH
(SEQ ID NO: 3296)
HFCRSSIMKPKRD
(SEQ ID NO: 3297)
DGYMFLKAESKI
(SEQ ID NO: 3298)
ESKIMFATLQR
(SEQ ID NO: 3299)
TLQRSSLWCL
(SEQ ID NO: 3300)
SLWCLCSNH
(SEQ ID NO: 3301)
KAESKIMFAT
(SEQ ID NO: 3302)
ATLQRSSLWCL
(SEQ ID NO: 3303)
MFATLQRSS
(SEQ ID NO: 3304)
TLQRSSLWCL
(SEQ ID NO: 3305)
LWCLCSNH
(SEQ ID NO: 3306)
FLKAESKIMFAT
(SEQ ID NO: 3307)
KIMFATLQRSS
(SEQ ID NO: 3308)
ATLQRSSLWCL
(SEQ ID NO: 3309)
SSLWCLCSNH
(SEQ ID NO: 3310)
RSSLWCLCSNH
(SEQ ID NO: 3311)
LKAESKI
(SEQ ID NO: 3312)
SKIMFAT
(SEQ ID NO: 3313)
FATLQRS
(SEQ ID NO: 3314)
QRSSLWC
(SEQ ID NO: 3315)
FATLQR
(SEQ ID NO: 3316)
QRSSL
(SEQ ID NO: 3317)
SSLWCLC
(SEQ ID NO: 3318)
CLCSNH
(SEQ ID NO: 3319)
SKIMFATLQRSSL
WCLCSNH
(SEQ ID NO: 3320)
AESKIMFATL
QRSSLWCL
(SEQ ID NO: 3321)
RDGYMFLKAESKI
MFATLQRSSLWCL
(SEQ ID NO: 3322)
FLKAESKIMFAT
(SEQ ID NO: 3323)
KIMFATLQRSS
(SEQ ID NO: 3324)
ATLQRSSLWCL
(SEQ ID NO: 3325)
SSLWCLCSNH
(SEQ ID NO: 3326)
RSSLWCLCSNH
(SEQ ID NO: 3327)
Пример 14 – Дизайн пулов синтетического GATA3 neoORF пептида для введения субъектам
Разные пулы указанных GATA3 пептидов создают согласно таблице 7 ниже. Например, “Дизайн 1” содержит три пептидных пула, где пул 1 содержит три пептида (т.е., L7, L8 и L14), пул 2 содержит два пептида (т.е., L9 и L10c) и пул 3 содержит два пептида (т.е., L15 и L11f). Например, “Дизайн 6” содержит два пептидных пула, где пул 1 содержит четыре пептида (т.е., L7, L8, L9 и L14) и пул 2 содержит два пептида (т.е., L15 и L11f). Например, “Дизайн 10” содержит четыре пептидных пула, где пул 1 содержит пять пептидов (т.е., L7, L8, L9, L10c и L14), пул 2 содержит один пептид (т.е., L15), пул 3 содержит один пептид (т.е., L11f) и пул 4 содержит один пептид (т.е., L11i). Концентрация каждого пептида в пулах может быть изменения специалистом в области получения пептидных составов. В таблице 7 ниже перечислено описание дизайнов GATA3 пула.
Таблица 7
Пример 15 – Синтез GATA3 neoORF пептида
Обычный синтез проводят с целью 700 мг неочищенного продукта. Следующие Fmoc-аминокислоты с подходящей защитой боковой цепи используют для конструирования L7 пептида (EPCSMLTGPPARVPAVPFDLH (SEQ ID NO: 3328)): Fmoc-Ala-OH∙H2O, Fmoc-Cys(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Gly-OH, Fmoc-Leu-OH, Fmoc-Met-OH, Fmoc-Pro-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH и Fmoc-Val-OH. C-концевой гистидин вводят в последовательность путем предварительной загрузки в смолу с использованием либо H-His(Trt)-2Cl-Trt смолы, либо Fmoc-His(Trt)-Wang смолы. Fmoc-Asp(OMpe)-OH может использоваться вместо Fmoc-Asp(OtBu)-OH для улучшения синтеза, например, чтобы минимизировать образование аспартамида для комбинаций последовательности “DG”.
Пептидные последовательности раздувают диметилформамидом (ДМФ) и дважды дренируют. Синтез начинают со снятия защиты N-α-FMOC защитной группы с использованием 20% пиперидина в ДМФ с азотом, диспергированным в смеси. После дренирования, смолу промывают ДМФ. Затем добавляют 0,4 M раствор аминокислоты вместе с 0,4 M HCTU и 0,8 M DIEA. Реакцию сочетания проводят с азотом, диспергированным в смеси, с последующим дренированием реакционного сосуда (RV). Добавление аминокислоты, HCTU и DIEA повторяют для двух циклов сочетания при тех же параметрах смешивания и дренирования, как в первом цикле сочетания. Затем смолу снова промывают ДМФ. Этот цикл повторяют для каждого аминокислотного остатка. Конечный способ снятия защиты удаляет N-концевую Fmoc через 20% пиперидин в ДМФ, и смолу промывают ДМФ с последующими промывками MeOH. Смола находится в инструменте под азотом до удаления.
Для микроволнового синтеза используют ту же исходную Fmoc-аминокислоту, при этом применяя только Fmoc-His(Trt)-Wang смолу (но не H-His(Trt)-2Cl Trt смолу) для введения C-концевого гистидина.
На микроволновом синтезаторе, смолу раздувают в ДМФ дока она не перенесется через HT линии в микроволновый реакционный сосуд (RV). При нахождении в RV, Fmoc-His(Trt)-OH загруженную смолу обрабатывают 25% пирролидином в ДМФ для удаления N-α-FMOC под 85°C/90W, затем 100°C/20W. Затем RV дренируют и промывают ДМФ и снова дренируют. Запрограммированные Fmoc-аминокислоты добавляют (0,5 M в ДМФ) в RV вместе с 4M DIC и 0,25 M Oxymapure. Эту реакцию сочетания продолжают при 105°C/288W нагревании, затем при 105°C/73W нагревании. Это первое снятие защиты изначально разбавляют ДМФ, однако эта стадия не требуется для каких-либо последующих снятий защиты, так как RV уж содержит ДМФ из реакции сочетания, промывают, и циклы сочетания повторяют для каждого остатка до тех пор, пока не будет синтезирован пептид. Для аргининовых остатков проводят двойную стадию сочетания, где после проведения одного сочетания раствор дренируют, и стадию сочетания повторяют перед снятием защиты. Конечное снятие защиты N-концевой Fmoc группы проводят как описано выше, за исключением дренирования и промывки ДМФ дважды перед переносом через ДМФ обратно в исходное положение HT смолы.
После синтеза, смолу переносят на фриттовый шприц с использованием ДМФ, промывают MeOH и сушат с использованием вакуумного коллектора. Затем смолу отщепляют с использованием реагента K (82,5% трифторуксусной кислоты (ТФК), 5% воды, 5% тиоанизола, 5% фенола и 2,5% этандитиола) с использованием вертикального держателя на осциллирующем шейкере в течение трех часов при комнатной температуре.
Расщепляющий коктейль затем пропускают через фильтрованную шприцевую фритту в холодный диэтиловый эфир или холодный метил-трет-бутиловый эфир (МТБЭ). Каждый шприц затем промывают 95:5 раствором трифторуксусной кислоты:воды при перемешивании. Промывку затем добавляют к остатку смеси коктейль/простой эфир. Затем смесь центрифугируют. После отгонки простого эфира, добавляют другую промывку на основе холодного простого эфира. Контейнер встряхивают и центрифугируют снова. Это повторяют для тщательного промывания лепешки. Конечную промывку отгоняют, и лепешку сушат в вакуумном осушителе. Образец лепешки растворяют в растворителе (например, ДМСО, ДМФ, воде или ацетонитриле) и анализируют СЭЖХ-МС для идентификации, определения чистоты и времени удержания. Другие пептиды, например L14 (SMLTGPPARVPAVPFDLH (SEQ ID NO: 3329)), L8 (GPPARVPAVPFDLHFCRSSIMKPKRD (SEQ ID NO: 3330)), L10c (KPKRDGYMFLKAESKI (SEQ ID NO: 3331)), L11h (FLKAESKIMFATLQR (SEQ ID NO: 3332)) и L11i (ESKIMFATLQRSSL (SEQ ID NO: 3333)) получают подобным образом, с использованием аминокислот и заранее загруженных смол, специфических к этим последовательностям.
Пример 16 – Синтез GATA3 neoORF пептида
Следующие Fmoc-аминокислоты используют в синтезе пептида L15 (KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 3334)): Fmoc-Ala-OH∙H2O, Fmoc-Cys(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Phe-OH, Fmoc-Gly-OH, Fmoc-Ile-OH, Fmoc-Lys(Boc)-OH, Fmoc-Leu-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Pro-OH, Fmoc-Gln(Trt)-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Trp(Boc)-OH, и Fmoc-Tyr(tBu)-OH. C-концевой гистидин вводят в последовательность путем предварительной загрузки в смолу с использованием либо H-His(Trt)-2Cl-Trt смолы, либо Fmoc-His(Trt)-Wang смолы. Fmoc-Asp(OMpe)-OH может использоваться вместо Fmoc-Asp(OtBu)-OH для улучшения синтеза, например, чтобы минимизировать образование аспартамида для комбинаций последовательности “DG”. Если присутствуют сериновый (Ser, S) и треониновый (Thr, T) остатки, аминокислотные дипептиды (псвдопролины) вводят для улучшения выхода, такие как Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH вместо “SS”, Fmoc-Ala-Thr(psi(Me,Me)pro)-OH вместо “AT”, и Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH вместо “ES”. Для некоторых синтезов L15, используют сочетание всех трех псевдопролинов (т.е., Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH вместо “SS”, Fmoc-Ala-Thr(psi(Me,Me)pro)-OH вместо “AT”, и Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH)вместо “ES”). Для других синтезов L15, используют следующий псевдопролин и комбинации псевдопролина, соответственно: Fmoc-Ala-Thr(psi(Me,Me)pro)-OH вместо “AT” и Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH вместо “ES”; Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH вместо “SS” и Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH вместо “ES”; Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH вместо “SS” и Fmoc-Ala-Thr(psi(Me,Me)pro)-OH вместо “AT”; Fmoc-Ala-Thr(psi(Me,Me)pro)-OH вместо “AT”; Fmoc-Glu(OtBu)-Ser(psi(Me,Me)pro)-OH) вместо “ES”; и Fmoc-Ser(tBu)-Ser(psi(Me,Me)pro)-OH вместо “SS”.
Пептидные последовательности раздувают ДМФ и дважды дренируют. Синтез начинают со снятия защиты N-α-FMOC группы с использованием 20% пиперидина в ДМФ с азотом, диспергированным в смеси. После дренирования, смолу промывают ДМФ. Затем добавляют 0,4 M раствор аминокислоты вместе с 0,4 M HCTU и 0,8 M DIEA. Реакцию сочетания проводят с азотом, диспергированным в смеси, с последующим дренированием реакционного сосуда (RV). Добавление аминокислоты, HCTU и DIEA повторяют для двух циклов сочетания при тех же параметрах смешивания и дренирования, как в первом цикле сочетания. Затем смолу снова промывают ДМФ. Этот цикл повторяют для каждого аминокислотного остатка. Конечный способ снятия защиты удаляет N-концевую Fmoc через 20% пиперидин в ДМФ, и смолу промывают ДМФ с последующими промывками MeOH. Смола находится в инструменте под азотом до удаления.
Для микроволнового синтеза используют те же исходные материалы, при этом применяя только Fmoc-His(Trt)-Wang смолу (но не H-His(Trt)-2Cl-Trt смолу) для введения C-концевого гистидина.
На микроволновом синтезаторе, смолу раздувают в ДМФ дока она не перенесется через HT линии в микроволновый реакционный сосуд (RV). При нахождении в RV, Fmoc-His(Trt) загруженную смолу обрабатывают 25% пирролидином в ДМФ для удаления N-α-FMOC под 85°C/90W, затем 100°C/20W. Это первое снятие защиты изначально разбавляют ДМФ, однако эта стадия не требуется для каких-либо последующих снятий защиты, так как RV уже содержит ДМФ из реакции сочетания. Затем RV дренируют и промывают ДМФ и снова дренируют. Запрограммированные Fmoc-аминокислоты добавляют (0,5 M в ДМФ) в RV вместе с 4M DIC и 0,25 M Oxymapure. Эту реакцию сочетания продолжают при 105°C/288W нагревании, затем при 105°C/73W нагревании. Снятие защиты, промывку и циклы сочетания повторяют для каждого остатка до тех пор, пока не будет синтезирован пептид. Для аргининовых остатков проводят двойную стадию сочетания, где после проведения одного сочетания раствор дренируют, и стадию сочетания повторяют перед снятием защиты. Конечное снятие защиты N-концевой Fmoc группы проводят так же, как все другие стадии снятия защиты, за исключением дренирования и промывки ДМФ дважды перед переносом через ДМФ обратно в исходное положение HT смолы.
После синтеза, смолу переносят на фриттовый шприц с использованием ДМФ, промывают MeOH и сушат с использованием вакуумного коллектора. Затем смолу отщепляют с использованием Reагента K (82,5% трифторуксусной кислоты (ТФК), 5% воды, 5% тиоанизола, 5% фенола и 2,5% этандитиола) с использованием вертикального держателя на осциллирующем шейкере в течение трех часов при комнатной температуре.
Расщепляющий коктейль затем пропускают через фильтрованную шприцевую фритту в холодный диэтиловый эфир (или холодный МТБЭ). Каждый шприц затем промывают 95:5 раствором трифторуксусной кислоты:воды при перемешивании. Промывку затем добавляют к остатку смеси коктейль/простой эфир. Затем смесь центрифугируют. После отгонки простого эфира, добавляют другую промывку на основе холодного простого эфира. Контейнер встряхивают и центрифугируют снова. Это повторяют для тщательного промывания лепешки. Конечную промывку отгоняют, и лепешку сушат в вакуумном осушителе. Образец лепешки растворяют в растворителе (например, ДМСО, ДМФ, воде или ацетонитриле) и анализируют СЭЖХ-МС для идентификации, определения чисто ты и времени удержания.
Другие пептиды, например L9 (LHFCRSSIMKPKRDGYMFLKAESKI (SEQ ID NO: 3335)), получают подобным образом, с использованием аминокислот и заранее загруженных смол, специфических к этим последовательностям, а также производных псевдопролина, где присутствуют сериновый (Ser, S) или треониновый (Thr, T) остатки и Fmoc-Asp(OMpe)-OH, как описано выше.
Пример 17 – Исследования растворимости
Множество GATA3 пептидов с неоэпитопами сначала тестировали на растворимость с использованием 5 мМ сукцината натрия (SS) в D5W с 4% ДМСО. На основе начальных результатов, стратегию получения составов улучшают корректировкой концентрации сукцината натрия (SS) и количества ДМСО, что привело к выбору 7 пептидов. Стратегии пулинга этих пептидов определяли для определения растворимости и совместимости с полиICLC. На основе этих результатов, были выбраны три пула. Каждый из двух пулов с только одним пептидом в 0,25мМ SS в D5W и третий пул с 5 пептидами в 5мМ SS в D5W. pH пула после объединения с полиICLC во всех случаях составлял рН 5,0-6,0 и были минимальные потери во время фильтрации.
Пептиды подвергают для скриннинга для следующих исследований, все которые перечислены в таблице 8.
Таблица 8
Все буферы получают ежедневно. D5W получают взвешиванием декстрозы и добавлением воды milliQ в декстрозе до достижения подходящего объема. Например, воду добавляют до 12,5 г декстрозы до достижения общего объема 250 мл. Для получения 50 мл 5 мМ SS в D5W взвешиванием 67,54 мг SS взвешивают и добавляют к D5W до достижения общего объема 50 мл. Для получения 0,25 мМ SS в D5W, 2,5 мл 5 мМ SS в D5W разбавляют 47,5 мл D5W.
% содержания пептида для каждого пептида определяют следующим образом: общая теоретическая ТФК равна сумме количества положительных зарядов (N-конец, Arg, Lys и His). Это количество вводят в следующее уравнение, где ММ является молекулярной массой пептида:
Уравнение 1. % ТФК=100*((%ТФК*114,02)/((%ТФК*114,02)+ММ))
Это значение затем используют для расчета процентной доли содержания пептида с использованием 6,45% в качестве теоретического содержания воды:
Уравнение 2. %Пептида=100-%ТФК-6,45%
Целевую полную массу для этих экспериментов рассчитывают с использованием уравнения ниже.
Уравнение 3. Целевая полная масса = (13,2*10000)/(% содержания пептида*% чистоты)
Пептиды взвешивают в 15-мл или 50-мл конических пробирках с использованием аналитических весов Mettler Toledo XP105 Delta Mass, и действительную общую массу записывают и используют для определения количества ДМСО, необходимого для получения 50 мг/мл. Расчет показан ниже:
Уравнение 4. ДМСО (мкл) = (Действительная общая масса (мг)*264 мкл)/(Целевая общая масса (мг))
Затем исходный раствор разводят до 2 мг/мл (1 часть исходного ДМСО, 24 части буфера) в подходящем буфере для состава.
Массы пептидов и процентное содержание рассчитывают, как описано выше, и подходящий буфер добавляют непосредственно к пептидам. Целевую общую массу, рассчитанную с использованием уравнения 3 и объема буфера, использованного для получения 2 мг/мл пептида, рассчитывают с использованием Уравнения 5.
Уравнение 5. Буфер (мл) = (Действительная общая масса (мг) *6,6 (мл)/(Целевая общая масса (мг))
Затем пептиды далее разводят 1:4 буфером с получением 0,4 мг/мл или, только где указано, буфер добавляют непосредственно к сухому пептиду с получением 0,4 мг/мл. В последнем случае, Уравнение 6 используют для определения подходящего объема добавляемого буфера.
Уравнение 6. Буфер (мл) = (Действительная общая масса (мг) *33 (мл)/(Целевая общая масса (мг))
Пептиды растворяют переворачиванием конических пробирок, но не ультразвуковой обработкой или встряхиванием.
Для объединения 5 пептидов, равный объем из каждого 2 мг/мл исходного раствора, объединяют с получением 0,4 мг/мл каждого пептида. В случае объединения менее чем 5 пептидов, равные объемы пептидов объединяют, затем раствор разводят подходящим буфером с получением 0,4 мг/мл каждого пептида. Пул переворачивают 3-5 раз для смешивания. Составленные пептиды переносят в стеклянные флаконы для визуализации растворимости. Фотографии делают каждые два часа для того, чтобы отметить какие-либо изменения во внешнем виде.
ПолиICLC получают коммерчески. Пулы объединяют в соотношении 3:1 пептида к полиICLC с использованием 150 мкл полиICLC с 450 мкл пептидного пула в 2 мл стеклянном флаконе. Раствор переворачивают 3-5 раз для смешивания и фотографии делают каждые два часа в течение 6 часов для того, чтобы отметить какие-либо изменения во внешнем виде. Все измерения pH проводят с использованием рН-метра Mettler Toledo inLab Micro pH meter, который калибруют каждый день перед применением, 100 мкл анализируемого образца удаляют и добавляют в микроцентрифужную пробирку для измерения pH. Затем образец выбрасывают. Образцы по СЭЖХ-МС (Waters Acquity H-Class м масс спектрометром Acquity QDa). 2 мкг инъекции каждого образца анализируют дважды с использованием 8-минутного градиента от 10:90 растворитель A:B до 50:50 растворитель A:B (A: 0,1% ТФК/вода, B: 0,1% ТФК:ацетонитрил). Исходную растворимость пептидов в стандартном составе определяют для каждого пептида при 0,4 мг/мл и 2 мг/мл. Хотя фотографии делают, они не всегда четко показывают растворимость, так как гели часто были прозрачными или пептиды давали мелкие стекловидные частицы при растворении. Растворимость пептидов в 5 мМ SS/D5W с 4% ДМСО показана в таблице 9.
В таблице 9 ниже перечислена растворимость пептида и внешний вид в 5 мМ SS/D5W с 4% ДМСО
Пептиды, которые были нерастворимы в 5 мМ SS, тестировали с использованием 0,25 мМ SS в D5W с 4% ДМСО. Результаты суммированы в таблице 10. Многие из этих пептидов, которые были нерастворимы в 5 мМ SS, были растворимы при концентрации 0,4 мг/мл в 0,25 мМ SS/D5W с 4% ДМСО через 6 часов, и были тестированы в последующих исследованиях с использованием этой низкой концентрации SS.
В таблице 10 перечислена растворимость пептида и внешний вид в 0,25 мМ SS/D5W с 4% ДМСО
На основе этих результатов, пептиды L7, L8, L9, L14, L10c, L11d, L11f и L15 были выбраны для исследований составов. Составы без ДМСО тестировали как средство улучшения стабильности составленных пептидов и для замедления димеризации цистеин-содержащих пептидов. Все пептиды тестировали (L7, L8, L9, L14, L10c, L11d, L11f и L15) в концентрации 0,4 мг/мл в 0,25 мМ SS, и они были растворимы без ДМСО через 6 часов. Пептиды L7, L8, L9, L10c, L12d и L14 тестировали в дозе 5 мМ SS и они также были растворимы без ДМСО через 6 часов. Значения pH пептидных составов в 0,25 мМ SS/D5W и 5 мМ SS/D5W перечислены в таблице 11.
В таблице 11 ниже показаны pH 0,4 мг/мл пептидных составов в 0,25 мМ SS/D5W и 5 мМ SS/D5W
Так как все пептиды, указанные в таблице 11, были растворимы в 0,25 мМ SS, исходные дизайны пулов исследовали с использованием более низкой концентрации SS. Пулы также были сконструированы с индивидуальной растворимостью в уме. Так как L15 и L11f были растворимы в низком SS, эти два пептиды были объединены. Первые три дизайна пулов показаны в таблице 12.
В таблице 12 ниже показаны исходные пептидные пулы в 0,25 мМ SS/D5W
Все пептиды оставались растворимыми после объединения. Значения pH пептидных пулов с или без добавления полиICLC даны в таблице 13.
В таблице 13 ниже перечислены pH пептидных пулов из таблицы 12 с или без добавления полиICLC
Пулы из каждого дизайна затем смешивают с полиICLC для тестирования их совместимости с адъювантом. Пул 3 и каждый пул, содержащий пептид L10c, выпадали в осадок при объединении с полиICLC. Дополнительно, пулы с 3 пептидами имеют pH ниже 5,0 при объединении с полиICLC, что позволяет предположить, что буферность должны быть выше, если пул содержит более чем два пептида.
Так как все из L7, L8, L9, L10c и L14 были растворимы в воде в 5мМ SS, их тестируют в пулах с высокой концентрацией SS. Три пула тестируют с этими пятью пептидами. Один пул был без L10c, один включал только L10c и третий включал все пять пептидов. Так как L11f и L15 не были растворимы при такой высокой концентрации, их составляют в 0,25 мМ SS. Однако, из-за наблюдаемого осадок, они были составлены при 0,4 мг/мл по отдельности, а не в одном пуле. Каждый из пептидов был растворим в их соответствующих составах. Эти пулы также были совместимы с полиICLC по данным визуализации, и все значения pH после объединения пула с полиICLC составляли между 5,0 и 6,3 (таблица 14), которые подходят для подкожного введения.
В таблице 14 перечислены pH пептидных пулов без полиICLC в сравнении с pH пептидных пулов с полиICLC
Пептид L11i тестировали в D5W с разными концентрациями сукцината без ДМСО. Пептид оказался растворимым во всех концентрациях SS при 0,4 мг/мл. Некоторый осадок наблюдали при 2 мг/мл в более высокой концентрации SS. Все образцы выглядели одинаковыми при объединении с полиICLC. Значения pH составов 2 мг/мл или 0,4 мг/мл пептида L11i в 0,25 мМ SS, 0,5 мМ SS или 5 мМ SS без полиICLC и 0,4 мг/мл пептида L11i в 0,25 мМ SS, 0,5 мМ SS или 5 мМ SS с полиICLC показаны в таблице 15.
В таблице 15 перечислены pH 2 мг/мл или 0,4 мг/мл L11i пептида в 0,25 мМ SS, 0,5 мМ SS и 5 мМ SS без полиICLC и 0,4 мг/мл в 0,25 мМ SS, 0,5 мМ SS и 5 мМ SS с полиICLC
Конечные пулы по результатам включают Пул 1 (L7, L8, L9, L10c и L14 в 5 мМ SS/D5W), пул 2 (либо L11i, либо L11f в 0,25 мМ SS/D5W) и пул 3 (L15 в 0,25 мМ SS/D5W). Каждый из этих пулов тестируют на удержание на 0,2 мкМ фильтре от Pall (HP1002). Образец перед фильтрацией, а также образец после каждой из 2 фильтраций анализируют СЭЖХ-МС. Менее чем 3% L11f и L11i теряется после первой стадии фильтрации, и никакой дополнительный пептид не теряется после второй стадии фильтрации. Только 4,9% L15 теряется после первой фильтрации и затем 1,3% теряется после второй фильтрации. Менее чем 3% в общем каждого пептида в Пуле 1 теряется после двух стадий фильтрации.
Заключения
Ряд потенциальных GATA3 пептидов тестируют на растворимость в буфере для состава, содержащем 5 мМ SS/D5W с 4% ДМСО. Пептиды, которые были нерастворимы в 5 мМ SS также тестировали при более низких концентрациях SS. На основе этих результатов, семь пептидов были выбраны, где пять из них были растворимы в 5 мМ SS (L7, L8, L9, L10c, и L14) и другие были растворимы в более низких концентрациях (L11f, L11i, и L15). Удаление ДМСО также тестировали, и оно может улучшать растворимость и замедлять образование дисульфида, который может затруднить анализ СЭЖХ. Каждый из выбранных пептидов был растворим без ДМСО.
На основе результатов растворимости, дизайны 3 пула создают с использованием 0,25 мМ SS/D5W. Хотя пулы были растворимыми, некоторые из них были несовместимыми с полиICLC. В некоторых случаях, осадок наблюдали при смешивании пулов, содержащих L10c, с полиICLC. То же наблюдение было сделано при объединении пула, содержащего и L11f и L15, с полиICLC. На основании этих результатов, был создан четвертый набор пулов. Первый пул содержал L7, L8, L9, L10c и L14 в 5 мМ SS/D5W и был совместим с полиICLC. Пептиды L15 и L11f или L11i оставляют в качестве отдельных пептидов для приготовления растворением непосредственно в 0,4 мг/мл с 0,25 мМ SS/D5W. Все эти пулы имели pH выше 5,0 при смешивании с полиICLC, что приемлемо для подкожного введения.
Пример 18. Распространенность GATA3 neoORF мутации
Этот пример характеризует распространенность и трансляционное доказательство GATA3 neoORF мутации. Вакцина состоит из пула длинных пептидов, которые охватывают новую открытую рамку считывания в GATA3 (GATA связывающем белке 3), который присутствует только в клетках, имеющих определенные мутации со сдвигом рамки в этом гене. В зависимости от исходного положения мутации со сдвигом рамки, полученные открытые рамки считывания могут варьировать в длину, но все они имеют общую транслированную область “GATA3 neoORF”. На ФИГ. 13 представлена типовая аминокислотная последовательность общей транслированной области. Любая генетическая мутация со сдвигом рамки, которая дает GATA3 neoORF транслированную последовательность, является “GATA3 neoORF мутацией”. Общедоступные геномные и протеомные наборы данных исследуют на распространенность GATA3 neoORF мутации и доказательство трансляции для GATA3 neoORF
Материалы и способы
Наборы данных
Набор данных MSK-IMPACT рака молочной железы: набор данных MSK-IMPACT рака молочной железы (Razavi et al., 2018) является публичным набором данных, доступным на cBioPortal for Cancer Genomics (http://www.cbioportal.org/study?id=breast_msk_2018). Этот набор данных содержит данные секвенирования с использованием MSK-IMPACT, анализа секвенирования нового поколения на основе захвата гибридизации, в котором анализируют все кодирующие белок экзоны между 341 и 468 опухолеассоциированных генов, для суммарно 1918 образцов рака молочной железы и сопоставимых нормальных образцов от 1756 пациентов. Общедоступные данные мутации и клинические данные, которые включают ER статус, HER2 статус и общую выживаемость, загружают для этого исследования.
Набор данных протеом TCGA рак молочной железы: набор данных протеом TCGA рак молочной железы (NCI CPTAC et al., 2016) является публичным набором данных, доступным на портале данных CPTAC (https://cptac-data-portal.georgetown.edu/cptac/s/S015). Этот набор данных содержит данные тандемной масс-спектрометрии из глобальной протеомы 105 пациентов с TCGA раком молочной железы, полученные с использованием способов количественной оценки белка iTRAQ. Общедоступные исходные данные были загружены для этого исследования.
Анализ распространенности мутации
Идентификация GATA3 neoORF: Каждое событие мутации GATA3 гена из набора данных MSK-IMPACT рака молочной железы сопоставляют с GATA3 транскриптом ENST00000346208.3 из генома человека (hg19, GRCh37 Genome Reference Consortium Human Reference 37) и затем транслируют in silico в полноразмерный белок. Если полноразмерный белок содержит GATA3 neoORF последовательность, образец, который содержит это событие мутации метят как GATA3 neoORF положительный.
Распространенность GATA3 neoORF: Для всех субъектов в когорте, если субъект имеет по меньшей мере один секвенированный образец опухоли, который был идентифицирован как GATA3 neoORF положительный, субъект считается GATA3 neoORF положительным. Распространенность GATA3 neoORF определяют как долю GATA3 neoORF положительных субъектов в когорте.
Идентификация пептида из данных протеомики
База данных белковых последовательностей: база данных белковых последовательностей содержит 63691 белковых последовательностей из UCSC базы данных белковых последовательностей (Feb. 2009 ссылочная последовательность человека, GRCh37/hg19) и одного полноразмерного белка, который содержит GATA3 neoORF последовательность.
Идентификация пептида: исходные данные набора данных протеомы TCGA рака молочной железы анализируют с использованием поисковой системы Comet (http://comet-ms.sourceforge.net), программного пакета с открытым исходным кодом для интерпретации тандемных масс-спектров. Comet (версия 2017.01 rev.2) используют для поиска всех МС/МС спектров из набора данных протеомы TCGA рака молочной железы против базы данных UCSC белковых последовательностей. В поиск разрешены спектры МС/МС с ионами-предшественниками до +6. Допуск погрешности массы для ионов-предшественников составлял ±10 частей на миллион (ч./млн.), и m/z ширину бина 0,02 используют для фрагментирования ионов. Все поиски были ограничены трипсином, так что каждый пептид, соответствующий экспериментальному спектру, должен был соответствовать специфичности расщепления фермента, т.е. C-коневой стороне лизинов или аргининов. Позволяется максимум 2 недоразрезов. Фиксированную модификацию +144.1021 Да используют к N-концу пептида и каждого лизинового остатка, как ожидается для iTRAQ мечения. Переменные модификации включали вплоть до двух окисленных метиониновых остатков на пептид. Фиксированную модификацию +57.021464 Да используют для всех цистеинов для карбамидометилированных цистеинов. Во время поиска, пептиды-ловушки автоматически создаются как часть поисковой системы Comet для оценки вероятности ложного обнаружения мишени-ловушки. Результаты поиска обрабатывают Percolator (версия 3.02.0) для расчета q-значений пептидного уровня, обычно меры для оценки вероятности ложной идентификации пептида с использованием данных тандемной масс спектрометриию. Стандартный порог (q-значение <0,01) используют для принятия пептидов, идентифицированных из набора данных так, что менее чем 1% принятых пептидов были, вероятно, ложными обнаружениями.
Доказательство трансляции GATA3 neoORF: Пептиды, специфически полученные из белковой последовательности, содержащей GATA3 neoORF, и не из другого белка в базе данных UCSC белковой последовательности, называют GATA3 neoORF специфическими пептидами. Идентификация GATA3 neoORF специфических пептидов считается доказательством трансляции GATA3 neoORF.
Результаты
Распространенность GATA3 neoORF мутации в раке молочной железы
Из набора данных MSK-IMPACT рака молочной железы от 1756 пациентов проводят анализ распространенности мутации (Материалы и способы из раздела 1 выше) и идентифицируют 91 пациента, которые были GATA3 neoORF положительными. Из этих 91 пациентов, 77 пациентов были описаны как HR+Her2(-), и 62 пациента были описаны как метастатические при диагностике. Распространенность GATA3 neoORF положительных пациентов в каждой подгруппе представлена в таблице 16 ниже. Среди HR+Her2(-) пациентов, GATA3 neoORF положительные пациенты не имеют статистической разницы в общем выживании по сравнению со всеми HR+Her2(-) пациентами (независимо от из GATA3 neoORF статуса) (p-значение=0,246) (ФИГ. 14).
В таблице 16 ниже показана распространенность GATA3 neoORF
В таблице 17 ниже показаны GATA3 neoORF специфические пептиды и другие пептиды, сопоставленные с каноническим GATA3, идентифицированным из набора данных протеомы TCGA рака молочной железы
Исследование геномного набора данных рака молочной железы показало, что GATA3 neoORF распространена у 6-7% пациентов с HR+Her2(-) раком молочной железы в зависимости от их метастатического статуса. Множество GATA3 neoORF специфических пептидов вместе с другими пептидами, которые сопоставлены с каноническим GATA3, было идентифицировано, что указывает на трансляцию GATA3 neoORF. Вместе, эти результаты демонстрируют, что GATA3 neoORF мутация распространена при HR+Her2(-) раке молочной железы, и, если присутствует, GATA3 neoORF может быть транслирована с получением белковых продуктов.
Пример 19 Подсчет GATA3 neoORF эпитопа среди HLA типов
В этом примере представлена оценка типового количества эпитопов, которое может ожидаться из GATA3 neoORF в популяции пациентов и разными типами HLA.
Материалы и способы
Все пептиды (длины 8-11) с общей областью GATA3 neoORF (как определена в Примере EXAMPLE 18) оценивают на вероятность презентирования с использованием in silico алгоритма прогнозирования, который совместно рассматривает экспрессию гена, потенциал связывания HLA и потенциал процессинга протесом. Алгоритм объединяет три переменные в общий прогноз презентирования через подгонку логистической регрессии на данных профилирования моноаллельной масс спектрометрии HLA-I. Следующие предположения и инструменты использовались для определения трех входных переменных:
Экспрессия
На основе RNA-Seq данных Cancer Genome Atlas (TCGA), образцы рака молочной железы имеют среднюю экспрессию GATA3 ~700 транскриптов на миллион (TPM). Предполагая, что мутантная аллель и аллель дикого типа вносят равный вклад в общую экспрессию GATA3, мы подсчитали, что трансскрипт neoORF будет экспрессироваться при 350 TPM.
Потенциал связывания HLA
Частоту аллелей в США вводят на основе этнически-специфических частот и оценки, что население США составляет 62,3% европейцев, 13,3% афроамериканцев, 6,8% уроженцев азиатско-тихоокеанского региона и 17,6% испанцев (таблица 18). Для 21 наиболее частых HLA-A аллелей и 49 наиболее частых HLA-B аллелей, прогнозы связывания пептида делают с использованием инструмента NetMHCpan-3,0 (21 и 49 аллелей обеспечивают покрытие 95% популяции для HLA-A и HLA-B, соответственно).
Потенциал процессинга
Предсказатель потенциала процессинга был обучен с использованием общедоступных данных профилирования HLA-I на основе масс-спектрометрии, например, как описано в Abelin. J. et al. Immunity, 2017, Bassani-Sternberg, M. et al Molecular & Cellular Proteomics 2015, конфигурации нейронной сети, которая определяет потенциал процессинга на основе контекста восходящей и нисходящей последовательности каждого пептида.
Чтобы смоделировать количество эпитопов на пациента, имитирующие генотипы HLA были созданы путем случайного рисования двух HLA-A и двух HLA-B аллелей (с заменой, чтобы учесть гомозиготность) в соответствии с их общими частотами в США (таблица 18). У большинства имитирующих пациентов было 4 различных аллели, но, поскольку была разрешена гомозиготность, у некоторых имитирующих пациентов было только 2 или 3 различных аллели. Для каждой пары пептид-аллель у имитирующего пациента, было проведено «подбрасывание монеты» Бернулли, параметризованное расчетной вероятностью презентирования (полученной из вышеописанной модели); положительный результат принимают как указание на то, что данный пептид будет презентирован на данной аллели. Для каждого имитирующего пациента, общее количество уникальных положительных пептидов суммировали для определения общего количества реакционноспособных эпитопов (что означает, что пептид, презентированный на множестве аллелей при имитации, быт посчитан только один раз). Результаты далее отбраковывают подсчетом вложенных эпитопов (например, положительный 9мер полностью содержится в положительном 10мере) в качестве единственного эпитопа. Десять тысяч пациентов стимулировали таким образом с использованием статистического языка программирования R.
В таблице 18 ниже перечислена частота аллелей, применяемых в стимулировании
Результаты
Анализ, описанный в разделе «способы» показали, что 95% пациентов может презентировать ≥2 HLA-I эпитопов из GATA3 neoORF (ФИГ. 15). GATA3 neoORF имеет множество презентируемых HLA-I эпитопов независимо от генотипа HLA пациента на основе подробностей, представленных выше. Это показывает эффективность терапии, вызывающей ответы Т-клетки против этих спрогнозированных неоантигенов. Подмножество спрогнозированных эпитопов выбирают для валидации следующих исследований, подробно описанных в примерах 20, 21, 22, 23 ниже.
Пример 20. Биохимические измерения эпитопа
В примере ниже представлена биохимическая валидация аффинности эпитопов из GATA3neoORF. Большое количество эпитопов может связываться со многими HLA аллелями (как описано в Примере 19). В этом примере, эпитопы оценивают на их способность связываться с несколькими общими HLA аллелями, а именно HLA-A02:01, HLA-B07:02 и HLA-B08:01. Оценивают и аффинность, и стабильность связывания между эпитопами и их спрогнозированными HLA.
Аффинность является мерой силы связывания эпитопа с HLA. Сильное связывание (обычно определенное как <500 нМ) является важной характеристикой для неоантигена, который может быть таргетирован Т-клеткой. Это происходит потому что неоантиген должен быть презентирован на поверхности опухолевых клеток, и поэтому должен обойти в конкурентной борьбе другие антигены, продуцированные опухолевой клеткой для связывающего кармана одной из HLA молекул, так как только один пептид может связываться с отдельной HLA молекулой в момент времени. Кроме того, было показано, что иммуногенные эпитопы имеют тенденцию к наличию сильной аффинности к их специфической HLA.
Стабильность является мерой того, как долго данный эпитоп остается связанным с распознанной HLA. Стабильное связывание (обычно определенное как >1 часа) также является важной характеристикой для неоантигена, который может быть таргетирован Т-клетками. Эпитопы должны оставаться связанными с опухолевыми клетками на поверхности клетки для того, чтобы быть распознанными Т-клетками. Кроме того, как и аффинность, ранее было показано, что иммуногенные эпитопы имеют тенденцию к стабильному связыванию с их специфической HLA.
Для оценки стабильности и аффинности эпитопов для их распознанных HLA молекул, пептиды синтезируют с чистотой >70% (по УФ анализу % площади) и разводят до 20 мМ или менее, и измеряют их аффинность и стабильность.
В этом примере представлена аффинность и стабильность связывания между 14 эпитопами и распознанными HLA молекулами. Четыре эпитопа изучают на HLA-A02:01, пять эпитопов изучают на HLA-B07:02 и восемь эпитопов изучают на HLA-B08:01 (три эпитопа изучают на обеих HLA-B07:02 и HLA-B08:01). Все пептиды продемонстрировали сильное связывание через аффинность, варьирующееся от 9,5 нМ до 242,8 нМ. Стабильность варьирует от 0 часов до 21,7 часов, с по меньшей мере одним эпитопом на каждой аллели, превышающим 1 час. Эти результаты показывают, что существует, по меньшей мере один сильный эпитоп, полученный из GATA3 neoORF, на аллель.
Материалы и методы
Выбор эпитопов для биохимических измерений
Множество эпитопов, полученных из GATA3 neoORF, было выбрано для подтверждения их способности связываться со специфической общей HLA аллелем, а именно HLA-A02:01, HLA-B07:02 или HLA-B08:01. Эти эпитопы предположительно варьируются от слабых до сильных связующих агентов.
Твердофазный синтез пептида
Пептиды получают в масштабе 5 мкМоль с использованием твердофазного пептидного синтеза на Intavis Peptide Synthesizer. Снятие защиты Fmoc проводят с использованием 20% пиперидина в ДМФ и промывают чистым ДМФ. Все аминокислоты дважды сочетают в течение 15 минут при комнатной температуре с использованием 60 мкл 0,5 M аминокислот (6 экв.), 55 мкл 0,5 M HCTU (5,5 экв.), 5 мкл NMP (0,5 экв.) и 14 мкл 4 M NMM (11,2 экв.). После каждого цикла двойного сочетания, кэпирование ацетила проводят добавлением 100 мкл раствора DIEA (сначала в виде 2M раствора в NMP и затем разбавленного до 12,5% с использованием ДМФ) и 6,25% уксусного ангидрида в ДМФ в течение 15 минут с последующим вакуумным дренированием и промыванием ДМФ. Снятие защиты, промывание, двойное сочетание, кэпирование ацетила, цикл промывки повторяют для каждой аминокислоты в последовательности. Конечное снятие защиты проводят с 20% пиперидином в ДМФ, и конечные промывки с ДМФ, EtOH и ДХМ. Конечное дренирование завершают в течение 5 минут на инструменте, после чего дно планшета промывают ДХМ.
Расщепление пептидов
Пептиды расщепляют с использованием раствора 92,5% ТФК, 2,5% TIPS, 2,5% H2O, 2,5% EDT. Через 1 час планшеты дренируют в вакууме в 1,2 мл подставки для пробирок Micronic. Через 3 часа в общем, пептиды осаждают холодным диэтиловым эфиром через центрифугирование.
СЭЖХ-УФ-МС анализ пептидов
Неочищенные пептиды сушат и ресуспендируют в 1:1 ACN:H2O, содержащем 0,1% ТФК и хранят при -80°С до полного замораживания. Пептиды затем лиофилизируют для выделения пептида в форме порошка. Пептидные порошки растворяют сначала в чистом ДМСО и затем разводят 3:1 в ДМСО:H2O для СЭЖХ-УФ-МС анализа. УФ отслеживание проводят при длине волны 214 нм с интервалом масс-детектора 200-1250 Да. СЭЖХ-УФ-МС способ, используемый для пептидов менее чем 9 аминокислот в длину, включает градиент 0-100% подвижной фазы B (0,085% ТФК в ацетонитриле, с соответствующей подвижной фазой 0,1% ТФК в воде) в течение 5 минут на СЭЖХ колонке 2,1x50 мм 1,7 мкМ BEH Acquity UPLC, а способ для пептидов более 9 аминокислот включает градиент 10-80% подвижной фазы B в течение 8 минут на СЭЖХ колонке 2,1x100 мм 1,7 мкМ BEH Acquity UPLC.
Определение концентрации пептида способом A214
Неочищенные пептиды растворяют в чистом ДМСО с концентрациями 2-5 мг/мл для оценки способом A214. Площадь пика пептида на СЭЖХ-УФ хроматограмме была пропорциональна количеству пептида, введенного для анализа и коэффициенту экстинкции пептида при длине волны определения. Поэтому концентрация пептида может быть определена сравнением его УФ площади пика с УФ площадью пика ссылочного пептида с известной концентрацией, с учетом соответствующих коэффициентов экстинкции. Следующее уравнение используют для расчета концентрации пептида:
Уравнение 7. 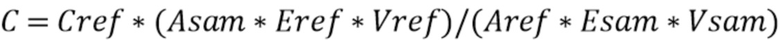
где C является концентрацией образца пептида в мМ, Cref является концентрацией ссылочного пептида в мМ, Asam является УФ площадью пика образца пептида, Aref является УФ площадью пика ссылочного пептида, Eref является коэффициентом экстинкции ссылочного пептида в M-1 см-1, Esam является коэффициентом экстинкции образца пептида в M-1 см-1, Vsam является объемом впрыска образца, и Vref является объемом впрыска ссылочного пептида.
Коэффициент экстинкции пептида при 214 нм прогнозируют объединением коэффициентов экстинкции отдельных аминокислот и пептидных связей. Ссылочный пептид с последовательностью RAKFKQLL (SEQ ID NO: 3376) (пептид ID LS-18) при 0,2 мг/мл пропускают последовательно с образцами неочищенного пептида на СЭЖХ-УФ-МС. УФ площади пика и рассчитанные коэффициенты экстинкции затем используют для расчета концентрации пептида в мМ.
Измерения аффинности
Аффинность связывания пептида с HLA молекулами измеряют через оценку его способности конкурировать с определенным радиомеченным пептидом для связывающего кармана на HLA молекуле. Это было проведено очисткой HLA молекул и инкубирования их со множеством концентраций пептида, представляющего интерес, и высокоаффинного связывающего пептида, который является радиомеченным. Через 2 дня инкубации, несвязанный радиомеченный пептид отделяют гельфильтрационной хроматографией с разделением по размерам, и определяют долю HLA молекул, которые имеют радиомеченный пептид. Пептиды, которые имеют низкую долю радиомеченного пептида в конце анализа, имеют сильную аффинность к HLA. Количественно, концентрация пептида, представляющего интерес, требуемая для ингибирования связывания радиомеченного пептида на 50%, может быть определена регрессионным анализом ингибирования для множества концентраций. Это измерение IC50 используют как приближение к истинной аффинности связывания.
В первой волне проанализированных пептидов, акутальные концентрации пептидов были известны на основе измерений A214, и были проведены любые необходимые коррекции на основе концентрации. Во второй волне анализированных пептидов, предполагалось, что концентрация всех пептидов была 20 мМ, и исходные IC50 были рассчитаны на основе этого предположения, с проведенными позже корректировками на действительную концентрацию. Для пептидов с действительной концентрацией ниже 20 мМ, измеренные IC50 были скорректированы умножением действительной концентрации, определенной способом A214, и делением на 20 мМ.
Измерения стабильности
Для измерения стабильности связывания пептидов с MHC I класса, синтетические гены, кодирующие тяжелые и легкие цепи биотинилированной MHC-I, экспрессируют в E. coli и очищают от телец включения стандартными способами. Легкая цепь (β2m) была радиомечена йодом (125I) и объединена с тяжелой цепью очищенной MHC-I и пептидом, представляющим интерес, при 18°C для начала образования комплекса pMHC-I. Эти реакции проводят в планшетах, покрытых стрептавидином, для связывания тяжелых цепей биотинилированной MHC-I с поверхностью, и измеряют радиомеченную легкую цепь для отслеживания образования комплекса. Диссоциацию инициируют добавлением более высоких концентраций немеченной легкой цепи и инкубацией при 37°C. Стабильность определяют как длительность периода времени в часах, требуемого для диссоциации половины комплексов, по данным сцинтилляционного счетчика. Проводят двойные измерения. Среднее для двух измерений берут как стабильность.
Результаты
Измерения аффинности
В таблице 19 ниже показаны измерения аффинности эпитопа.
*Примечание: действительная концентрация пептида и измеренная IC50, представленные здесь, округлены из исходных данных, но скорректированные значения IC50 были рассчитаны с использованием не округленных исходных данных.
Измерения стабильности
В таблице 20 ниже представлены измерения стабильности
В Примере 20, оценивают спрогнозированные эпитопы из GATA3 neoORF на множестве общих HLA молекул (HLA-A02:01, HLA-B07:02, HLA-B08:01). Было определено, что все эпитопы имеют сильную аффинность (<500 нМ). Подмножество этих эпитопов также является стабильными связующими агентами (>1 часа) с по меньшей мере одним сильным связующим агентом на каждой из оцениваемых HLA аллелей. Эти данные показывают, что GATA3 neoORF эпитопы присутствуют во множестве HLA аллелей.
Пример 21: Создание клеточной линии с GATA3 мутацией и HLA аллелем
В этом примере описано получение клеточной линии с мутацией GATA связывающего белка 3 (GATA3) новой открытой рамкой считывания (neoORF) и значительным преобладанием HLA аллелей, HLA-A02:01 и HLA-B07:02. Эта клеточная линия может использоваться в качестве in vitro суррогата опухолевых клеток, которые содержат GATA3 neoORF мутации. Клеточные линии, которые в природе имеют специфическую GATA3 neoORF в фокусе не являются легко доступными, их получают стабильной лентивирусной трансдукцией обычно применяемой клеточной линии, HEK293T. Эту клеточную линию выбирают, так как она в природе экспрессирует две из известных HLA аллелей, HLA-A02:01 и HLA-B07:02. Эту модифицированную клеточную линию используют для функциональных анализов с Т-клетками (пример 25 и пример 26). Дополнительно, эту клеточную линию используют для валидации неоантигенов процессирующих/презентирующих из GATA3 neoORF на множестве HLA аллелей (пример 22). Для этих исследований, HLA аллеля временно трансфицируют в модифицированную клеточную линию.
Материалы и методы
Обзор создания клеточной линии с GATA3 мутацией
Создание GATA3 мутации трансдуцированных HEK 293Т клеток включает (a) дизайн плазмиды, кодированной GATA3 мутацией, получение лентивируса, трансдукцию GATA3 мутации в колонию HEK 293Т клеток и выбор трансдуцированных клеток. Эти стадии создания клеточной линии с GATA3 мутацией описаны ниже.
Клеточные линии и культуры
Колонии HEK 293Т клеток покупают у American Type Culture Collection (Rockford, MD, USA) и сохраняют в среде DMEM 10% ФТС и Pen/Strep.
Дизайн плазмиды, кодированной GATA3 мутацией
Ген GATA3 мутации
Для эффективной экспрессии конструкта плазмиды гена GATA3 мутации, 600 п.н. последовательности GATA связывающего белка 3 (GATA3) дикого типа от 1473 до 2074 (которая содержит кодирующую ДНК последовательность (CDS) последовательность от 558 до 1892) получают из NCBI ссылочной последовательности: NM_001002295.01. Последовательность GATA3 мутации затем создают делецией 2 нуклеотидов на 1734 и 1735 из ссылочной последовательности (ФИГ. 16). Последовательность GATA3 мутации затем транслирует сдвиг рамки в положении 87 аминокислотной последовательности из последовательности дикого типа (ФИГ. 17). Этот ДНК конструкт может покрывать 87 остатков дикого типа GATA3 аминокислотной последовательности и 114 GATA3 neoORF аминокислотной последовательности со сдвигом рамки считывания, который вызван делецией.
Дизайн плазмиды с GATA3 мутацией
Последовательности GATA3 мутации кодон-оптимизируют, синтезируют и клонируют в pCDH-CMV-Puro вектор (Genescript) (ФИГ. 18).
Получение лентивируса
Lenti-X 293Т клетки (ClonTech) культивируют в полной культуральной среде (DMEM, содержащей 10% ФТС, Pen/Strep) и трансфицируют кодированной GATA3 мутацией лентивирусной плазмидой с получением лентивируса для гена GATA3 мутации. За день до трансфекции, 8x105 клеток высевают на лунку 6-луночного планшета. Культуральную среду меняют в день трансфекции. 4 мкг лентивирусной сконструированной плазмиды и 4,6 мкл смеси лентивирусной упаковывающей плазмиды (Sigma-Aldrich) смешивают в Opti-MEM (Thermo Fisher). Смесь смешивают с 10 мкл FuGENE HD (Promega) и добавляют непосредственно к клеткам. Через 24 часа среду заменяют свежей полной культуральной средой. Супернатант, содержащий лентивирус, собирают через 72 часа после трансфекции.
Трансдукция GATA3 мутации
5x105 HEK 293Т клеток (ATCC) высевают в 2 мл среды DMEM, содержащей 6 мкг/мл полибрена и 10% ФТС на 12-луночном планшете. 130 мкл супернатанта, содержащего GATA3 лентивирус, добавляют непосредственно к клеткам. Клетки инкубируют в 5% CO2 инкубаторе. Среду заменяют на среду DMEM с 10% ФТС и Pen/Strep через 24 часа.
Выбор пиромицина
Обработку 1 мкг/мл концентрацией пиромицина начинают на 2 день после трансдукции лентивируса с GATA3 мутацией. Клетки культивируют и размножают с использованием среды DMEM с 10% ФТС, Pen/Strep и 1 мкг/мл Пиромицина до сбора.
Трансфекция HLA-кодирующих конструктов
1,5x107 трансдуцрованных GATA3 мутацией HEK 293Т клеток высевают в колбу T175. 15 мкг HLA-A02:01, HLA-B07:02 или HLA-B08.01 кодированных плазмид (Genewiz) смешивают с 70 мкл Fugene HD (Promega) и инкубируют при комнатной температуре в течение 15 минут. Смеси плазмида каждого HLA типа и Fugene HD добавляют к трансдуцированным GATA3 мутацией HEK 293Т клеткам в колбе T175 для трансфекции. Трансфицированные 3 разными HLA и трансдуцированные GATA3 мутацией HEK 293Т клетки культивируют в течение 48 часов, затем собирают.
Сбор трансдуцированных GATA3 мутацией и трансфицировнных HLA клеток
Клетки промывают 1 x ФРФБ и добавляют 0,25% Трипсин-ЭДТК (Thermo-Fisher scientific). Через 3 минуты инкубации при 37°C, клетки ресуспендируют и собирают со средой DMEM с 10% ФТС и Pen/Strep. Стадии промывания проводят 3 раза, они включают центрифугирование при 1500 об./мин. в течение 5 мин, затем суспендирование с ФРФБ буфером. Дебрис мгновенно замораживают на сухом льду в 70% этанола. Замороженные дебрисы хранят при -80°С в морозильнике для анализа протеомики.
Результаты
Трансдуцированные GATA3 мутацией HEK 293T используют в качестве клеток-мишеней для оценки GATA3 специфического TCR функционального анализа, и в качестве материала для оценки презентирования GATA мутации на HLA-A02.01 масс спектрометрией (пример 22). Ниже приведены результаты, демонстрирующие создание экспрессирующих GATA3 мутацию HEK 293Т клеток.
Конструкт плазмиды с GATA3 мутацией
Кодируемый GATA3 мутацией конструкт плазмиды создают и оценивают через ДНК секвенирование на GENEWIZ. Данные ДНК секвенирования на конечной плазмиде, кодированной GATA3 мутацией, на 100% совпадают со сконструированной последовательностью гена с GATA3 мутацией (ФИГ. 19). После переваривания рестрикционной эндонуклеазы AflII, два ДНК диска наблюдают между 5000 п.н. и 3000 п.н. на треке 2 анализа методом гель-элктрофореза. Эти диски коррелируют с ожидаемыми размерами 4243 п.н. и 3424 п.н., соответственно (ФИГ. 20).
Трансдукция и сбор GATA3 мутации
HEK 293Т клетки используют для трансдукции GATA3 мутации. Трансдуцированные клетки культивируют до достижения общего количества клеток 200х106 клеток. В день сбора, 1x106 клеток используют для экспрессии HLA-Класса I и HLA-Класса II на проточном цитометре (ФИГ. 21). 99,5% клеток были HLA-Класс I положительными. 193х106 клеток замораживают для анализа протеомики.
HLA трансфекция
Трансдуцированные GATA3 мутацией HEK 293Т клетки временно трансфицируют кодируемыми BAP меченной HLA-A02.01, BAP меченной HLA-B07.02 и BAP меченной HLA-B08.01 плазмидами экспрессии. Трансфицированные клетки культивируют в течение 48 часов и собирают. В день сбора, 1x106 клеток используют для экспрессии HLA-A02.01 и HLA-I класса с использованием проточной цитометрии (ФИГ. 22). Не трансфицированные (ФИГ. 22A), HLA-A02.01 трансфицированные (ФИГ. 22B), HLA-B07.02 трансфицированные (ФИГ. 22C) и HLA-B08.01 трансфицированные (ФИГ. 22C) GATA3 HEK293Т клетки. Все трансфицированные клетки сверхэкспрессируют HLA-A02.01 и HLA-I класса.
Создают модифицированную клеточную линию, которая экспрессирует GATA3 neoORF при стабильной трансдукции лентивируса, содержащего мутированный ген GATA3 в HEK293Т клетках. Трансдуцированные GATA3 мутацией HEK 293Т клетки экспрессируют HLA-I класса. Эту клеточную линию затем используют в качестве мишени для функциональных анализов с Т-клетками, специфическими к GATA3 неоантигена (пример 25 и пример 26). Затем, после трансфекции несколькими обычными HLA аллелями, эти клеточные линии показали более широкое распределение уровня экспрессии HLA-I класса и HLA-A:02, и их используют для оценки процессинга и презентирования множества неоантигенов на этих аллелях (пример 22).
Пример 22 Оценка GATA3 neoORF пептидных эпитопов масс спектрометрией
В этом примере представлена валидация эндогенного процессинга и презентирования спрогнозированных пептидных эпитопов, полученных из общей области GATA связывающего белка 3 (GATA3) новой открытой рамки считывания (neoORF), для связывания с HLA-A*02:01, HLA-B*07:02 и HLA-B*08:01 гетеродимера, масс спектрометрией. HEK293Т клетки конструируют для стабильной экспрессии GATA3 neoORF и временно трансфицируют для экспрессии меченных биотиновым акцепторным пептидом (BAP) HLA аллелей, представляющих интерес. Прогнозирование аллель-специфических пептидных эпитопов и создание HEK293Т клеток описано в примере 19 и примере 21, соответственно. Комплексы HLA-пептид выделяют из клеточных лизатов аффинной адсорбцией биотинилированной BAP-метки, экспрессированной на альфа цепи каждого гетеродимера HLA I класса. Пептидные лиганды выделяют из комплексов HLA-пептид обработкой кислотой и обессоливают жидкостной хроматографией с обращенной фазой. HLA-пептидные лиганды затем отделяют наножидкостной хроматографией в сочетании с тандемной масс спектрометрией высокого разрешения (нЖХ-МС/МС). Спрогнозированные пептидные эпитопы, полученные из GATA3 neoORF, подвергают направленной нЖХ-МС/МС, посредством чего a priori знание массы предшественника каждого пептидного эпитопа используют для выбора теоретической моноизотопной массы каждого пептидного эпитопа для фрагментации путем высокоактивной столкновительной диссоциации (HCD) и последующего секвенирования пептидов. GATA3 neoORF пептидные эпитопы сопоставляют с полученных тандемных масс-спектров (МС/МС) с помощью алгоритма сопоставления базы данных с базой данных, содержащей GATA3 neoORF, и с помощью спектрального сравнения массы предшественника (МС) и МС/МС спектров, соответствующих их синтетическим пептидным аналогам.
В общем, пять пептидных эпитопов из общей области GATA3 neoORF, которые связываются с тремя разными HLA гетеродимерами, определяют нЖХ-МС/МС в сконструированных HEK293Т клетках. Для HLA-A*02:01, были определены следующие два из четырех таргетированных пептидных эпитопов: SMLTGPPARV (SEQ ID NO: 3411) и MLTGPPARV (SEQ ID NO: 3412). Для HLA-B*07:02, были определены следующие два из пяти таргетированных пептидных эпитопов: KPKRDGYMF (SEQ ID NO: 3413) и KPKRDGYMFL (SEQ ID NO: 3414). Для HLA-B*08:01, был определен следующий один из восьми таргетированных пептидных эпитопов: ESKIMFATL (SEQ ID NO: 3415). Определение и идентификация этих пептидных эпитопов с использованием нЖХ-МС/МС из клеток, экспрессирующих GATA3 neoORF, продемонстрировали, что они эндогенно процессированы и затем связаны HLA гетеродимером.
Материалы и методы
Пептиды: Синтезируют 12C14N синтетические пептиды, соответствующие GATA3 neoORF пептидным эпитопам.
В таблице 21 ниже представлен список синтетических пептидов, соответствующих GATA3 neoORF спрогнозированным пептидным эпитопам.
Клеточная культура
Создание сконструированных HEK293Т клеток, который стабильно экспрессируют GATA3 neoORF и временная трансфекция каждой аффинно-меченной (BAP-меченной) аллели описаны в примере 21. В таблице 22 перечислены образцы и количество клеток, которые используют для направленной нЖХ-МС/МС.
В таблице 22 ниже представлены образцы для таргетированной нЖХ-МС/МС
Аффинная адсорбция аффинно-меченных (BAP-меченных) комплексов HLA-пептид
Замороженные дебрисы, содержащие BAP-меченные HLA молекулы, оттаивают на льду в течение 20 мин, затем осторожно лизируют ручным пипетированием в холодном лизисном буфере [20 мМ Tris-Cl pH 8, 100 мМ NaCl, 6 мМ MgCl2, 1,5% (об./об.) Triton X-100, 60 мМ октил B-D-глюкопитанозида, 0,2 мМ 2-йодацетамида, 1 мМ ЭДТК pH 8, 1 мМ PMSF, 1X полный коктейль ингибитора протеазы, не содержащий ЭДТК] в соотношении 1,2 мл лизисного буфер на 50x106 клеток. Лизаты инкубируют при переворачивании при 4°С в течение 15 мин и добавляют нуклеазу бензоназу в соотношении ≥250 единиц бензоназы на 50x106 клеток для разложения ДНК/РНК, затем центрифугируют при 15000 x g при 4°С в течение 20 мин для удаления клеточного дебриса и нерастворимых материалов. Очищенные надосадочные жидкости переносят в новые пробирки, и BAP-меченные HLA молекулы биотинилируют инкубированием с переворачиванием при комнатной температуре в течение 10 мин в 1,5 мл пробирке с 0,56 мкМ биотина, 1 мМ АТФ/1 мМ ацетата магния и 3 мкМ BirA. Супернатанты инкубируют при переворачивании при 4°С в течение 30 мин в объеме, соответствующем 200 мкл суспензии высокоэффективной смолы на основе гранулированной агарозы Pierce NeutrAvidin, на 50x106 клеток для обогащенных аффинностью комплексов биотинилированный-HLA-пептид. Наконец, HLA-связанную смолу промывают четыре раза 1 мл холодного промывочного буфера (20 мМ Tris-Cl pH 8, 100 мМ NaCl, 60 мМ октил B-D-глюкопиранозида, 0,2 мМ 2-йодацетамида, 1 мМ ЭДТК, pH 8), затем промывают четыре раза 1 мл холодного промывочного 10 мМ Tris-Cl pH 8. Между промывками, HLA-связанную смолу осторожно перемешивают вручную, затем пеллетируют центрифугированием при 1500 x g при 4°С в течение 1 мин. Смолу на основе гранулированной агарозы NeutrAvidin промывают три раза 1 мл холодного ФРФБ перед применением. Промытую HLA-связанную смолу хранят при -80°C в течение менее одной недели, затем элюируют HLA-пептидом.
Обессоливание, восстановление и алкилирование HLA-пептида
HLA-пептиды элюируют из аффинно-меченных (BAP-меченных) комплексов HLA и одновременно обессоливают с использованием системы твердофазной экстракции Sep-Pak. Коротко, картриджи Sep-Pak присоединяют к 24-позиционному коллектору для твердофазной экстракции, активируют два раза 200 мкл метанола, затем 100 мкл 50% (об./об.) ацетонитрила/0,1% (об./об.) муравьиной кислоты, затем промывают четыре раза 500 мкл 1% (об./об.) муравьиной кислоты. Для диссоциации HLA-пептидов из аффинно-меченных (BAP-меченных) HLA молекул и улучшения связывания пептидов с твердой фазой tC18, 400 мкл 3% (об./об.) ацетонитрила/5% (об./об.) муравьиной кислоты добавляют в пробирки, содержащие HLA-связанную смолу на основе гранулированной агарозы. Суспензию смешивают пипетированием, затем переносят в картриджи Sep-Pak. Пробирки и пипетку промывают 1% (об./об.) муравьиной кислоты (2x200 мкл) и промывку переносят в картриджи. 100 фемтомолей смеси для калибровки времени удержания пептида Пирса добавляют в картриджи в качестве контроля нагрузки. Смолу на основе гранулированной агарозы инкубируют два раза в течение 5 мин с 200 мкл 10% (об./об.) уксусной кислоты для дальнейшей диссоциации HLA-пептидов от аффинно-меченных (BAP-меченных) HLA молекул, затем промывают четыре раза 500 мкл 1% (об./об.) муравьиной кислоты. HLA-пептиды элюируют tC18 в новые 1,5 мл микропробирки постадийным фракционированием с 250 мкл 15% (об./об.) ацетонитрила/1% (об./об.) муравьиной кислоты, затем 250 мкл 30% (об./об.) ацетонитрила/1% (об./об.) муравьиной кислоты. Растворы используют для активации, загрузки образца, промывания и элюирования через гравитацию, и вакуум (≥-2,5 ф/д2) используют для удаления оставшегося элюата из картриджей. Элюаты, содержащие HLA-пептиды, замораживают, сушат вакуумным центрифугированием и хранят при -80°С, затем подвергают восстановлению, алкилированию и второму обессоливанию.
Восстановление и алкилирование цистеинсодержащих HLA-пептидов проводят в 1,5 мл микропробирках следующим образом. Высушенные пептиды солюбилизируют в 200 мкл 10 мМ Tris-Cl pH 8, затем восстанавливают инкубированием с 5 мМ дитиотреитола при 60°С в течение 30 мин при встряхивании при 1000 об./мин. в ThermoMixer. Восстановленные тиолы алкилируют инкубированием с 15 мМ 2-йодацетамидом при комнатной температуре в течение 30 мин в темноте. Любой непрореагировавший 2-йодацетамид гасят инкубированием с 5 мМ дитиотреитола в течение 15 мин при комнатной температуре в темноте. Образцы обессоливают сразу же после восстановления и алкилирования.
Вторичное обессоливание образцов HLA-пептида проводят с использованием внутренних встроенных StageTips, упакованных с использованием двух пуансонов 16 калибра Empore C18 диска твердофазной экстракции. StageTips активируют два раза 100 мкл метанола, затем 50 мкл 99,9% (об./об.) ацетонитрила/0,1% (об./об.) муравьиной кислоты, затем промывают три раза 100 мкл 1% (об./об.) муравьиной кислоты. Пептидный раствор подкисляют добавлением 200 мкл 3% (об./об.) ацетонитрила/5% (об./об.) и загружают на StageTips. Пробирки и кончики пипеток промывают 200 мкл 3% (об./об.) ацетонитрила/5% (об./об.), затем 1% (об./об.) муравьиной кислоты (2x100 мкл) и промывки переносят на StageTips. StageTips промывают пять раз 100 мкл 1% (об./об.) муравьиной кислоты. Пептиды элюируют в 1,5 мл микропробирки с использованием постадийного градиента 20 мкл 15% (об./об.) ацетонитрила/1% (об./об.) муравьиной кислоты, затем двумя 20 мкл порциями 30% (об./об.) ацетонитрила/1% (об./об.) муравьиной кислоты. Загрузку образца, промывку и элюирование проводят на настолько центрифуге с максимальной скоростью 1800-3500 x g при комнатной температуре. Элюаты замораживают, сушат вакуумным центрифугированием и хранят при -80°С.
Секвенирование HLA-пептида через нЖХ-МС/МС
Во всех нЖХ-МС/МС анализах используются одни и те же условия разделения жидкостной хроматографией, описанные ниже. Пептиды хроматографически разделяют с использованием EASY-nLC 1200 System, оборудованной нанораспылительной колонкой PicoFrit с внутренним диаметром 75 мкМ и 10 мкМ испускателем, упакованной при давлении ~1000 ф/д2 гелия до ~35 см с использованием упаковочного материала ReproSil-Pur 120Ǻ C18-AQ 1,9 мкМ, и нагревают при 60°C во время разделения. Колонку уравновешивают 10X объемом слоя растворителя А [3% (об./об.) ацетонитрила/0,1% (об./об.) муравьиной кислоты], образцы загружают в 4 мкл 3% (об./об.) ацетонитрила/5% (об./об.) муравьиной кислоты, и пептиды элюируют линейным градиентом 6-40% растворителя B [80% (об./об.) ацетонитрила/0,1% (об./об.) муравьиной кислоты] в течение 84 мин, 40-60% растворителя B в течение 9 мин, затем выдерживают в 90% растворителя B в течение 5 мин и 50% растворителя B в течение 9 мин для промывания колонки. Линейные градиенты пропускают со скоростью 200 нл/мин.
Пептиды элюируют в Orbitrap Fusion Lumos Tribrid Mass Spectrometer, оборудованный Nanospray Flex Ion источником при 2,5 кВ. Полнодиапазонный МС получают при разрешении 15000 от 300-1800 m/z с целью автоматизированного контроля заполнения ловушки ионами (AGC) 4x105 и максимальным временем впрыска 50 миллисекунд. После каждого скана МС затем проводят сканирование МС/МС согласно списка включенной массы (таблица 23), содержащего расчетные массы ионов (m/z) таргетированных GATA3 neoORF пептидных эпитопов и их спрогнозированные зарядовые состояния (z). Дополнительные расчетные массы ионов были включены для пептидов, которые отвечают следующим критериям: i) ожидается множество зарядовых состояний из-за присутствия одного или нескольких основных остатков в последовательности и/или ii) пептидов, содержащих аминокислоты, которые предположительно будут модифицированы во время процессинга образца, такие как цистеин, метионин и N-концевой глутамин. Максимальное время впрыска варьирует от 100 миллисекунд до 120 миллисекунд для сохранения времени цикла 2-2,8 сек в хроматографическом пике. Сканы МС/МС получают при разрешении 15000 от 110 до 1300-1500 m/z, с использованием ширины изоляции 1 m/z, нормализованной HCD энергии соударений 34, и AGC мишени 1x 105.
В таблице 23 представлен список массы включения GATA3 neoORF пептидных эпитопов для каждого HLA аллеля
Поиск в базе данных
Масс спектры интерпретируют с помощью программного пакета Spectrum Mill. Спектры МС/МС исключают из поиска, если они не имели предшественника MH+ в диапазоне 600-2000 Да, имели заряд предшественника >5 или имели <4 обнаруженных пика. Объединение аналогичных спектров с одним и тем же m/z предшественника, полученное в одном хроматографическом пике, отключают. Спектры МС/МС были анализируют в базе данных, которая содержала все гены UCSC Genome Browser с аннотацией генома hg19 и его кодирующих белки транскриптов (63691 запись) в сочетании с полноразмерной последовательностью GATA3 neoORF и 150 распространенными примесями. Перед поиском в базе данных все МС/МС должны были пройти фильтр спектрального качества с длиной тега последовательности >2 (т.е. минимум 3 массы, разделенные массой аминокислоты в цепи). Минимальную оценку расщепления позвоночника устанавливают как 5 и используют схема оценки «ESI QExactive HLA v2». Все спектры исследуют с использованием не ферментной специфичности, фиксированной модификации карбамидометилирования цистеина (Camc) и следующих переменных модификаций: окисленного метионина (m), пироглутаминовой кислоты и цистеинилирования (Ccys). Допуски по массе предшественника и продукта устанавливают как 0,1 Да и 10 ч./млн., соответственно, а минимальную согласованную интенсивность пика устанавливают на уровне 30%. Пептидные совпадения спектра (PSM) для отдельных спектров были автоматически разработаны как уверенно назначенные с использованием модуля автовалидации Spectrum Mill для применения оценки FDR на основе мишени-ловушки в ранге PSM для установки критериев порога оценки. Стратегия автоматических порогов с использованием минимальной длины последовательности, равной 7, автоматическая фильтрация по массе предшественника с переменным диапазоном, и оценка и дельта порогов оценки Rank1-Rank2 были оптимизированы для всех прогонов нЖХ-МС/МС для HLA аллеля, что дало оценку PSM FDR <1% для каждого состояния заряда предшественника.
Уравнение
Экспериментальную моноизотопную молекулярную массу (ММ) каждого пептидного эпитопа рассчитывают в соответствии со следующим уравнением, где m/z является отношением массы к заряду пептидного эпитопа, обнаруженного масс-спектрометром, z является зарядом пептидного эпитопа, и 1,007276 является моноизотопной молекулярной массой протона.
Уравнение 8. Экспериментальная ММ = ((m/z) × (z)) – ((z) × (1,007276))
РЕЗУЛЬТАТЫ
Направленную нЖХ-МС/МС используют для валидации эндогенного процессинга пептидных эпитопов, полученных из GATA3 neoORF, которые были спрогнозированы для связывания с HLA-A*02:01, HLA-B*07:02 и HLA-B*08:01. Пять пептидных эпитопов, полученных из общей области GATA3 neoORF, определяют в HEK293Т клетках для трех аллелей (ФИГ. 23).
Для HLA-A*02:01 гетеродимера, пять пептидов, полученных из общей области GATA3 neoORF, таргетируют нЖХ-МС/МС. Два пептида из общей области, SMLTGPPARV (SEQ ID NO: 3474) и MLTGPPARV (SEQ ID NO: 3475), были успешно идентифицированы поиском по базе данных и спектральной совместимостью с их синтетическими пептидными партнерами. Теоретические и экспериментальные моноизотопные молекулярные массы для каждого пептидного эпитопа с ассоциированной ошибкой по массе показаны в таблице 24. Оценка расщепления скелета и оцененная интенсивность пика по данным механизма поиска в базе данных Spectrum Mill, приведены в таблице 25. Оценка расщепления скелета указывает на количество фрагмент-специфических ионов, генерируемых HCD, тогда как оцененная интенсивность пика показывает процент ионного тока в спектре МС/МС, что объясняется поисковой интерпретацией.
В таблице 24 ниже перечислены теоретические и экспериментальные молекулярные массы с ошибкой по массе
В таблице 25 показаны критерии интерпретации из поиска по базе данных
Ключ: / y-ион, \ b-ион, | b- и y-ионы
Каждый МС/МС спектр, полученный на эндогенно процессированном пептидном эпитопе, соответствовал МС/МС спектру, созданному с использованием соответствующего синтетического пептида. На ФИГ. 24 показано спектральное сравнение МС/МС спектра для эндогенно процессированного пептидного эпитопа SMLTGPPARV (SEQ ID NO: 3486) (ФИГ. 24A низ) и МС/МС спектра его соответствующего синтетического пептида (ФИГ. 24A верх). На ФИГ. 24B показано альтернативное изображение идентичного спектрального соответствия. Эти графики сверху-вниз были созданы с использованием верхних 45 или 50 наиболее распространенных ионов для 9мерных и 10мерных пептидных эпитопов, соответственно (http://orgmassspec.github.io/).
На ФИГ. 25 показано сравнение МС/МС спектров для HLA-A*02:01 эндогенно процессированного пептида MLTGPPARV (SEQ ID NO: 3487).
Для HLA-B*07:02, пять пептидных эпитопов, полученных из общей области GATA3 neoORF, таргетируют нЖХ-МС/МС. Два пептидных эпитопа из общей области, KPKRDGYMF (SEQ ID NO: 3488) и KPKRDGYMFL (SEQ ID NO: 3489), были успешно идентифицированы поиском по базе данных и спектральной совместимостью с их синтетическими пептидами. Теоретические и экспериментальные молекулярные массы для каждого пептидного эпитопа с ассоциированной ошибкой по массе показаны в таблице 24. Оценка расщепления скелета и оцененная интенсивность пика по данным механизма поиска приведены в таблице 25.
На ФИГ. 26 и ФИГ. 27 показано сравнение спектров для HLA-B*07:02 пептидных эпитопов KPKRDGYMF (SEQ ID NO: 3490) и KPKRDGYMFL (SEQ ID NO: 3491), соответственно.
Для HLA-B*08:01, восемь пептидных эпитопов, полученных из общей области GATA3 neoORF, таргетируют нЖХ-МС/МС. Один пептидный эпитоп из общей области, ESKIMFATL (SEQ ID NO: 3492), были успешно идентифицированы поиском по базе данных и спектральной совместимостью с соответствующим синтетическим пептидом. Этот пептид определяют с сульфоксидной формой метионина, что дает сдвиг массы 15999 Да, указывающих на добавление кислорода с боковой цепи. Окисление метионина (показанное прописной m) до сульфоксидной формы является обычным результатом процессинга образца. Теоретическая и экспериментальная молекулярная масса для ESKImFATL (SEQ ID NO: 3493) с ассоциированной ошибкой по массе показана в таблице 24. Оценка расщепления скелета и оцененная интенсивность пика по данным механизма поиска приведены в таблице 25.
На ФИГ. 28 показано сравнение спектров для HLA-B*08:01 пептидного эпитопа ESKImFATL (SEQ ID NO: 3494).
Направленную нЖХ-МС/МС был использован для валидации процессинга и презентирования пяти пептидных эпитопов, полученных из общей области GATA3 neoORF, которые были спрогнозированы для связывания с HLA-A*02:01, HLA-B*07:02 и HLA-B*08:01 гетеродимером. Гетеродимер HLA I класса очищают из HEK293Т клеток, стабильно экспрессирующих GATA3 neoORF, с использованием аффинной метки, которая генетически экспрессирована на альфа цепи каждого гетеродимера HLA I класса. Каждый аффинно-меченный гетеродимер (BAP-меченную HLA аллель) временно трансфицируют в HEK293Т клетки, экспрессирующие GATA3 neoORF, как описано в RP19-005. Правильную линейную последовательность для каждого целевого пептидного эпитопа подтверждают нЖХ-МС/МС пептидным секвенированием. Все спектры МС/МС интерпретируют с помощью механизма поиска в базе данных Spectrum Mill, который сопоставляем экспериментальные спектры МС/МС с пептидами из базы данных, содержащей >63000 записей, включая полноразмерный GATA3 neoORF. Молекулярную массу для каждого наблюдаемого пептидного эпитопа рассчитывают в пределах ±0,01 Да от его теоретической молекулярной массы. Интерпретация экспериментальных спектров МС/МС показала, что ≥72% ионного тока в спектрах МС/МС можно объяснить ионами специфического к последовательности фрагмента. Дополнительное подтверждение последовательности эндогенно процессированного пептидного эпитопа проводят путем спектрального сопоставления со спектром МС/МС соответствующего синтетического пептида, который показал идентичные массы ионов фрагмента и шаблоны расщепления скелета. Вместе, направленная нЖХ-МС/МС подтверждает, что HLA-A*02:01 пептидные эпитопы SMLTGPPARV (SEQ ID NO: 3495) и MLTGPPARV (SEQ ID NO: 3496), HLA-B*07:02 пептидные эпитопы KPKRDGYMF (SEQ ID NO: 3497) и KPKRDGYMFL (SEQ ID NO: 3498) и HLA-B*08:01 пептидный эпитоп ESKIMFATL (SEQ ID NO: 3499) эндогенно процессированы в HEK293Т клетках и затем связаны HLA гетеродимером.
Пример 23. Иммуногенность на MHC I
В этом примере оценивают иммуногенность GATA3 neoORF на разных, наиболее распространенных HLA аллелях. GATA3 neoORF является мутацией со сдвигом рамки, возникающей до природного стоп-кодона, вызывающий удлинение белка на, по меньшей мере 61 новую аминокислоту. Иммуногенность оценивают in vitro индукцией PBMC от здорового донора (HD) против спрогнозированных минимальных эпитопов, специфических к HLA-A02:01, A03:01, A24:02, B07:02 или B08:01.
Материалы и методы
В таблице 26 перечислены пептидные пулы, полученные на основе ограничения аллели
В таблице 27 перечислена информация о здоровом доноре
Н/Д=донор является гомозиготным для конкретной аллели. Таргетированные эпитопом аллели выделены жирным.
Индукция с использованием лиганда FMS-подобной тирозинкиназы 3 (FLT3L) для стимулирования DC
FLT3L стимулирование проводят следующим способом. PBMC оттаивают и ресуспендируют в количестве 5x107 клеток/мл в среде AIM-V. Бензоназу (Sigma-Aldrich 70746) добавляют в количестве 25-29 Ед/мкл и инкубируют при 37°C в течение 30 мин – 1 ч. CD14/CD25 истощение проводят для удаления моноцитов (CD14) и T регуляторных клеток (CD25) согласно протоколу производителя (Miltenyi Biotec, Inc 130-050-201, 130-092-983). Клетки в количестве 2x106 клеток/мл ресуспендируют в среде AIM-V с FLT3L (CellGenix 1415-050) при 50 нг/мл и высевают по 2 мл на лунку в 24-луночный планшет в течение ночи. Пептид, разведенный в AIM-V, добавляют в конечной концентрации 2 мкМ, и лунки осторожно смешивают. Клетки инкубируют с пептидом в течение 1 часа при 37°C.
Добавляют коктейль для созревания с фактором некроза опухоли (TNF-a) (1000 Ед/мл) (CellGenix1406-050), IL-1b (10 нг/мл) (CellGenix1411-050), простагландином-E 1 (PGE-1) (0,5 мкг/мл) и IL-7 (0,5 нг/мл) и инкубируют при 37°C в течение ночи. После ночи инкубирования коктейля для созревания, ФТС добавляют в каждую лунку в конечной концентрации 10% по объему и смешивают. Совместную культуру вводят каждые 2-3 дня, начиная на 5 день, осторожной заменой 75% среды на свежую Roswell Park Memorial Institute 1640 (RPMI) + 10% ФТС с достаточным количеством IL-7 и IL-15 для конечной концентрации 5 нг/мл в лунку. Для введений после первого, среду меняют на свежую 20/80+10% ФТС с достаточным количеством IL-7 и IL-15 для конечной концентрации 5 нг/мл в лунку. Начало образования mDC началось на 4 день.
Образование зрелых дендритных клеток (mDC)
PBMC оттаивают и ресуспендируют в количестве 5x107 клеток/мл в среде с дендритными клетками (DC) (Cellgenix 20801-0500). Бензоназу добавляют (sigma-aldrich 70746) в количестве 25-29 Ед/мл и инкубируют при 37°C в течение 30 мин – 1 ч.
Выделение моноцитов сортировкой проводят согласно протоколу производителя (Miltenyi biotec, Inc 130-096-537). Клетки высевают в 6-луночные планшеты 3x106 клеток/лунку в 2 мл DC среды с гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF) (800 Ед/мл) (CellGenix 1412-050) и IL-4 (400 Ед/мл) (CellGenix 1403-050) и инкубируют при 37°C в течение 5 дней.
Загрузку и созревание пептида проводят следующим образом. immDC из лунок собирают пипетированием и пеллетируют центрифугированием при 1200 об./мин. в течение 5 минут. Клетки ресуспендируют в 1 мл в DC среде. Клетки отделяют в пулы с 0,2x106 (или 0,5x106) клетками на лунку для каждого пула и инкубируют в течение 1 ч при 37°C с 1,6 мкМ пептида (0,4 мкМ конечной концентрации). 800 мкл (или 2 мл) DC среды добавляют на лунку к immDC с загруженными пептидом и высевают в 6-луночный планшет со следующими цитокинами и инкубируют при 37°C в течение 2 дней: IL-4 (400 Ед/мл) (CellGenix 1403-050), GM-CSF (800 Ед/мл) (CellGenix 1412-050), TNF-a (10 нг/мл) (CellGenix1406-050), IL-1b (10 нг/мл) (CellGenix1411-050), PGE-1 (0,5 мкг/мл) (Cayman из Czech republic), IL-6 (10 нг/мл) (CellGenix 1004-50).
Зрелые дендритные клетки, опосредованные долговременной стимуляцией (mDC LTS)
На 12 день добавляют стимулированные FLT3L Т-клетки. DC ресуспендируют в 1 мл 20/80. Лунки совместного культивирования собирают и считают, и клетки ресуспендируют в количестве 5x106/мл в 20/80. 1 мл наивных Т-клеток добавляют к mDC в соотношении 10:1 (Т-клетки:mDC) с цитокинами IL-7 (5 нг/мл) IL-15 (5 нг/мл). Добавляют среду до конечного объема 5 мл на лунку. Сокультуры инкубируют при 37°C. Сокультуру загружают каждые 2-3 дня, начиная с 15 дня. Клетки размножают в колбах большего объема при необходимости.
Уравнение 9. Среда для добавления (мл) = (текущий объем (мл)×(180-глюкоза))/60
Культуры рестимулируют на 23 день на новых mDC. DC ресуспендируют в 1 мл 20/80. Лунки с сокультурой собирают, и клетки ресуспендируют при 2e6/мл (или 5e6/мл) в 20/80. 1 мл наивных Т-клеток добавляют к mDC в соотношении 10:1 (Т-клетки:mDC) с цитокинами IL-7 (5 нг/мл) IL-15 (5 нг/мл). Среду добавляют до конечного объема 5 мл на лунку. Сокультуру инкубируют при 37°C. Сокультуру загружают каждые 2-3 дня. Клетки размножают в колбах большего объема при необходимости.
Уравнение 9: Среда для добавления (мл) = (текущий объем (мл)×(180-глюкоза))/60
На 31 день клетки замораживают в 1 мл среды для замораживания (90% ФТС, 10% ДМСО). Клетки хранят в течение ночи при -80°C в CoolCell Freeze Container (VWR 75779-816), затем переносят их в жидкий азот для долговременного хранения.
Создание и анализ мультимера
Мономер для пептидного обмена
Мономер HLA MHC I класса, загруженный УФ отщепляемым пептидом, создают внутри. Мономер ресуспендируют при 100 мкг/мл в фильтрованном ФРФБ, и аналитические пептиды ресуспендируют при 10 мг/мл в ДМСО, и УФ отщепляемый пептид меняют на отдельные аналитические пептиды в соотношении 1 мкл пептида:50 мкл мономера под УФ облучением в течение 1 ч при 4°C. Обмененный мономер центрифугируют при 3600 об./мин. и собирают супернатант.
Конъюгирование флуорохрома
50 мкл pMHC объединяют с меченным стрептавидином флуорохромом на льду в течение 30 мин в темноте согласно соотношению конъюгирования каждого из следующих флуорохромов (CR): PE (BioLegend 405203) (CR: 2); APC (BioLegend 405207) (CR: 3); BV421 (BioLegend 405226) (CR: 2); QD605 (Life Technologies Q10101 MP) (CR: 2); QD705 (Life Technologies Q10161 MP) (CR: 2); BUV395 (BD 564176) (CR: 2); BV650 (BD 563855) (CR: 2). Каждый pMHC расщепляют и конъюгируют с двумя отдельными флуорохромами. Добавляют биотин (Avidity BIO200) + 0,5% азида при соотношении 1:20, и мультимер хранят при 4°C в темноте в течение от 1 до 3 дней. Данные проточной цитометрии получают в 11 и 22 день и после замораживания. ~2x106 клеток собирают в пропиленовый 96-луночный планшет с V-образным дном в среде с бензоназой (sigma-aldrich 70746) при 25-29 Ед/мкл и инкубируют при 37°C в течение 30 мин – 1 ч.
Клетки окрашивают всеми следующими мультимерами, конъюгированными с флуорохромом, загруженными индуцированными пептидами в 50 мкл фильтрованного физиологического раствора с фосфатным буфером (ФРФБ) в течение 15 мин при 37°C в темноте. PE (BioLegend 405203) 1 мкл; APC (BioLegend 405207) 3 мкл; BV421 (BioLegend 405226) 1 мкл; QD605 (Life Technologies Q10101 MP) 4,5 мкл; QD705 (Life Technologies Q10161 MP) 4,5 мкл; BUV395 (BD 564176) 3,5 мкл; BV650 (BD 563855) 2,5 мкл. Образцы окрашивают следующими поверхностными антителами в течение 30 мин на льду в темноте. Анализируют на LSR-Fortessa для дифференцировочного кластера (CD)8(+) / CD4(-) / CD14(-) / CD16(-) / CD19(-)/ мертвый(-) / мультимер_1(+) / мультимер_2 (+) / нерелевантный мультимер(-): CD8-FITC (Biolegend 344704) 2 мкл, CD4-AF700 (BD 557922) 1 мкл, CD14-AF700 (BD 557923) 1 мкл, CD19-AFF700 (BD 557921) 1 мкл, CD16-AF700 (BD 557920) 1 мкл, Live dead stain (Molecular probes L-23101) 0,1 мкл.
Результаты
Каждый образец окрашивают двумя мультимерами для каждого пептидного донора, индуцированного против уникальной комбинации флуорохрома. Положительные индукции определяли по меньшей мере 10 событиями, положительными для, по меньшей мере 1 комбинации специфического флуорохрома, и отрицательными для нерелевантных комбинаций флуорохрома. Данные собирают после каждой стимуляции, и положительный результат для двух стимуляций считают положительной индукцией. На ФИГ. 29А и ФИГ. 29B показана типовая индукция ответов GATA3 неоантигена CD8+.
В таблице 28 показана доля положительных ответов GATA3 неоантигена CD8+
В таблице 28 представлена доля репликатов, которые вызывают индукцию наивных CD8+ Т-клеток, подтвержденную для двух независимых стимуляций.
Эти результаты показывают, что существует, по меньшей мере один минимальный эпитоп в GATA3 neoORF, который может создавать CD8+ специфическую индукцию in vitro для 4 из 5 проанализированных HLA. Результаты указывают на широкую иммуногенность GATA3 neoORF по всем HLA и определяют иммуногенные минимальные неоантигенные эпитопы, специфические к значительно распространенным HLA.
Пример 24. Иммуногенность на MHC II
В этом примере оценивают CD4 иммуногенность лонгмерных пептидов (>15 аминокислот), специфических к GATA3 neoORF. Для прогнозирования in vivo CD4 иммуногенности используют анализ in vitro индукции против пяти разных здоровых доноров с минимальным перекрытием HLA-II класса.
Материалы и методы
В таблице 29 ниже перечислены индуцирующие пептиды
В таблице 30 ниже представлена информация для здоровых доноров
Создание зрелых дендритных клеток (mDC)
Выделение моноцита
PBMC оттаивают и ресуспендируют при 5x107 клеток/мл в среде с дендритными клетками (DC) (Cellgenix 20801-0500). Добавляют бензоназу (sigma-aldrich 70746) при 25-29 Ед/мкл и инкубируют при 37°C в течение 30 мин - 1 ч. Выделение моноцитов сортировкой проводят согласно протоколу производителя (Miltenyi biotec, Inc 130-096-537). Клетки высевают в 6-луночные планшеты при 3x106 клеток/лунку в 2 мл DC среды с GM-CSF (800 Ед/мл) и IL-4 (400 Ед/мл) и инкубируют при 37°C в течение 5 дней.
Загрузка и созревание пептида
immDCs собирают из лунок пипетированием и пеллетируют центрифугированием при 1200 об./мин. в течение 5 минут. Клетки ресуспендируют при 1 в DC среде. Клетки отделяют в пулы с 0,2x106 (или 0,5x106) клеток на лунку для каждого пула и инкубируют в течение 1 ч при 37°C с 1,6 мкМ пептида (0,4 мкМ конечной концентрации). 800 мкл (или 2 мл) DC среды добавляют на лунку для загруженных пептидом immDCs и высевают в 24- (или 6-) луночный планшет со следующими цитокинами и инкубируют при 37°C в течение 2 дней; IL-4 (400 Ед/мл) (CellGenix 1403-050), GM-CSF (800 Ед/мл) (CellGenix 1412-050), TNF-a (10 нг/мл) (CellGenix1406-050), IL-1b (10 нг/мл) (CellGenix1411-050), PGE-1 (0,5 мкг/мл) (Cayman от Czech republic), IL-6 (10 нг/мл) (CellGenix 1004-50)
Долговременная стимуляция (LTS)
Добавляют наивные Т-клетки. PBMC оттаивают и ресуспендируют при 5x107 клеток/мл в DC среде (Cellgenix 20801-0500). Добавляют бензоназу (sigma-aldrich 70746) при 25-29 Ед/мкл и инкубируют при 37°C в течение 30 мин - 1 ч.
CD14/CD25 обеднение проводят для удаления моноцитов (CD14) и T регуляторных клеток (CD25) согласно протоколу производителя (Miltenyi Biotec, Inc 130-050-201, 130-092-983). 1 мл наивных Т-клеток добавляют к mDC в соотношении 10:1 (Т-клетки:mDC) с цитокинами IL-7 (5 нг/мл; CellGenix) IL-15 (5 нг/мл; CellGenix). Сокультуру инкубируют при 37°C. mDC либо ресуспендируют в 20/80, либо хранят в DC среде с цитокинами.
Сокультуру загружают каждые 2-3 дней, начиная с 5 дня, затем используют либо способ 1, либо способ 2 ниже (2.3.2.1.1 или 2.3.2.1.2). Клетки размножают в колбах большего объема при необходимости. Для способа 1, среду для добавления рассчитывают как (мл) = (текущий объем (мл)×(180-глюкоза))/60. Для способа 2, глюкометр используют для проверки, если среды является желтой. Если глюкоза остается высокой (>90 мг/дл), 100 мкл 20x IL-7 и IL-15 добавляют в лунку. Если глюкоза является низкой (<90 мг/дл), клетки размножают до 6-луночного планшета (4 мл/лунку) и добавляют 1x IL-15 и IL-7. Если глюкоза является очень низкой (<60 мг/дл), размножают до 6 мл/лунку в 6-дуночном планшете. В 6 и 13 или 14 дни создают новые mDC.
На 13 и 21 или 22 дни культуры на новых mDC рестимулируют. Лунки с сокультурой собирают и считают, и ресуспендируют клетки при 2x106/мл (или 5x106/мл) в 20/80. 1 мл наивных Т-клеток добавляют к mDC в соотношении 10:1 (Т-клетки:mDC) с цитокинами IL-7 (5 нг/мл) IL-15 (5 нг/мл). Сокультуру инкубируют при 37°C. mDC либо ресуспендируют в 20/80, либо хранят в DC среде с цитокинами. В 28 или 29 день клетки замораживают в 1 мл среды для замораживания (90% ФТС, 10% ДМСО). Клетки хранят в течение ночи при -80°C в CoolCell Freeze Container (VWR 75779-816), затем переносят их в жидкий азот для долговременного хранения.
Анализ вторичного иммунного ответа CD4
Либо создают новые mDC, либо оттаивают свежие PBMC от того же донора индукции. Высевают клетки при 0,26/лунку PBMC и 0,02x106/лунку mDC в 96-луночный планшет с u-образным дном с пептидом или ДМСО при 0,8 мкМ конечной концентрации. Индукционный образец добавляют в лунки при соотношении 1:1 индуции:PBMC или 10:1 индукции:mDC и инкубируют при 32°C в течение 20-24 часа.
Данные проточной цитометрии
Golgy stop (BD 554724) и Golgy plug (BD 555029) добавляют к культурам согласно протоколу производителя и инкубируют в течение 4 часов. Клетки окрашивают CD4-BV786 (BD 563877), CD8-AF700 (BD 561453), CD14-FITC (BD 340682), CD16-FITC (BD 340704), CD19-FITC (BD 340864), Live dead stain (Molecular probes L-23101) в течение 20 минут. Образцы фиксируют с использованием набора Fixation/Permeabilization kit (BD 554714) согласно протоколу производителя. Клетки окрашивают IFN-y-PE (Biolegend 502508) в течение 20 минут. Анализ проводят на LSR-Fortessa для CD4 (+) / CD8 (-) / CD14 (-) / CD16 (-) / CD19 (-), Dead (-) / IFNy (+).
Результаты
С использованием проточной цитометрии идентифицируют антигенспецифические CD4 Т-клетки (ФИГ. 30A и ФИГ. 30B). По меньшей мере идентифицируют одну индукцию GATA3 neoORF специфического пептида у каждого здорового донора.
Специфические реакционноспособные пептиды идентифицируют через вторичный иммунный ответ индуцированных клеток против отдельных пептидов и сравнения с вторичным иммунным ответом без пептида. Каждый индукционный образец сначала анализируют против индуцирования пула, и у положительных образцов затем вызывают вторичный иммунный ответ против отдельных пептидов. Все образцы обрабатывают на двойных планшетах, и если средняя доля CD4+/IFNy+ индукционных образцов с пептидом составляет более 2% по сравнению с тем же образцом без пептида, образец считается пораженным.
В таблице 31 показана доля ответов GATA3 неоантигена CD4
Последовательности, выделенные жирным, находятся в области GATA3 NeoOrf, общей для всех пациентов
По меньшей мере один CD4 специфический ответ наблюдают для общей области GATA3 neoORF у всех тестированных здоровых доноров. Эти доноры имеют широкий диапазон HLA аллелей MHC II класса, показывая, что способность создавать CD4 GATA3 ответ не зависит от аллели.
Пример 25. Функциональные анализы с индуцированными CD8+ Т-клетками
В этом примере показана способность CD8+ Т-клеток, специфических к неоантигенам, полученным из GATA связывающего белка 3 (GATA3) новой открытой рамки считывания (neoORF), убивать клетки, имеющие подходящую GATA3 neoORF мутацию. Индукция неоантиген-специфических CD8+ Т-клеток описана ранее в примере 23, и создание клеточной линии, имеющей GATA3 neoORF мутацию, описано в примере 21.
В этом примере, CD8+ Т-клетки, специфические к одному эпитопу из GATA3 neoORF, презентированном на HLA-A02:01 (покрытой пептидной последовательностью MLTGPPARV (SEQ ID NO: 3547)) выбирают для этого подробного анализа. Коротко, индуцированные CD8+ Т-клетки сокультивируют с клетками-мишенями, либо трансдуцированными с GATA3 neoORF, либо с не обработанными в качестве отрицательного контроля. После сокультивирования, клетки-мишени оценивают на экспрессию каспазы 3, маркера смерти клетки, как меру цитотоксичности, вызванной CD8+ Т-клеткой. Повышенная каспаза 3 на клетках-мишенях, экспрессирующих GATA3 neoORF, в сравнении с необработанными клетками, представляет специфическое уничтожение из-за того, что распознанный эпитоп был презентирован на поверхности клетки-мишени. Кроме того, CD8+ Т-клетки оценивают на экспрессию CD107a, маркера активации Т-клетки, для измерения активации антигенспецифической Т-клетки. Для дальнейшей оценки антигенспецифического распознавания индуцированных GATA3 PBMC, IFN-γ, цитокин, продуцированный CD8+ цитотоксической Т-клеткой при распознавании антигена, также измеряют в супернатанте.
В общем, четыре разных популяции CD8+ Т-клеток, специфических к GATA3 neoORF эпитопу на HLA-A02:01, тестируют на способность уничтожать клетки-мишени, имеющие мутацию. Во всех четырех случаях, повышенную каспазу 3 наблюдают на клетках-мишенях, имеющих GATA3 neoORF, по сравнению с клетками-мишенями без мутации. Повышение каспазы 3 демонстрирует способность CD8+ Т-клеток, специфических к эпитопам из GATA3 neoORF, уничтожать клетки, имеющие GATA3 neoORF мутацию.
Материалы и методы
Анализ цитотоксичности
Колонии HEK 293Т клеток покупают у American Type Culture Collection (Rockford, MD, USA) и выдерживают в среде DMEM, 10% ФТС и Pen/Strep. Создают GATA3 ген, кодируемый лентивирусом, и трансдуцируют его в HEK 293Т клетки. Трансдуцированные GATA3 HEK 293Т клети выдерживают под 1 мкг/мл пуромицина в полной среде в течение более 2 недель. Дополнительные подробности описаны в примере 21.
1х107 клеток-мишеней в 1 мл добавляют к 1 мкл Tag-it Violet (Biolegend) с последующей инкубацией в 5% CO2 инкубаторе в течение 20 минут, дважды промывая 5 мл культуральной среды с 10% ФТС, и ресуспендируя клетки при 1х106 клеток в культуральной среде.
Индуцированные PBMC флаконы оттаивают помещением в 37°C водяную баню. Затем 1 мл ФТС добавляют в каждый флакон. Клетки переносят в 50 мл коническую пробирку, содержащую 15 мл культуральной среды AIM-V, 10% ФТС и Pen/Strep. Клетки центрифугируют при 1500 об./мин. в течение 5 мин и ресуспендируют в 5 мл культуральной среды. Клетки выдерживают в течение 1 часа и 30 мин при 37°C, в 5% CO2 инкубаторе, затем добавляют 5 мкл бензоназы (Millipore Sigma) и далее инкубируют в течение 30 мин при 37°C в 5% CO2 инкубаторе. Инкубированные клетки снова центрифугируют, и после удаления супернатанта ресуспендируют в 5 мл среды AIM-V. Количество клеток считают с использованием счетчика Vi-CELL (Beckman coulter).
Клетки центрифугируют и ресуспендируют в 40 мкл MACS буфера на 1х107 клеток-мишеней. CD8+ положительные клетки отрицательно обогащают согласно набору для выделения CD8+ Т-клеток человека (Miltenyi Biotec). CD8+ клетки ресуспендируют при 2,5х106 клеток в 1 мл среды AIM-V. 5х104 клеток-мишеней на лунку высевают в 50 мкл культуральной среды на 96-луночный плоскодонный планшет и культивируют в течение ночи при 37°C в 5% CO2 инкубаторе. GATA3 индуцированные и CD8+ обогащенные клетки высевают над клетками-мишенями при 2,5х105 клеток на лунку в 100 мкл среды AIM-V. Сокультивированные клетки инкубируют в течение 6 часов при 37°C в 5% CO2 инкубаторе.
Культуральные супернатанты сокультуры собирают и оценивают IFN-γ концентрацию с помощью анализов V-PLEX Human IFN-γ согласно протоколу производителя (Meso Scale Discovery).
Клетки суспензии переносят в новый планшет для окрашивания, и адгезивные клетки переносят после добавления 50 мкл трипсина на лунку, инкубируют при 37°C и ресуспендируют со средой AIM V. Клетки объединяют, центрифугируют и промывают FACS буфером. 50 мкл смеси антител (анти-CD3-BUV8052, анти-CD4-BV711, анти-CD107a-BV786, анти-CD8+-PE-cy5 и ИК красителя Live/Dead; BD) добавляют к каждому образцу, затем инкубируют в течение 30 мин на льду. Клетки промывают 100 мкл FACS буфера. Внутриклеточной окрашивание каспазы-3 проводят согласно инструкции производителя набора Cytofix/Cytoperm (BD) с 2 мкл каспаза-3 антитела. Окрашенные клетки анализируют на Fortessa II (BD).
Результаты
Анализ цитотоксичности GATA3 индуцированных PBMC
PBMC от трех разных здоровых доноров (HD47, HD50 и HD51) индуцируют GATA3 HLA-A:02 неоантигенным пептидом MLTGPPARV (SEQ ID NO: 3548) способом долговременной стимуляции. Эту комбинацию эпитоп:аллель определяют как оптимальную для тестирования в анализе цитотоксичности по сравнению с другими эпитопами:аллелями, родственными GATA3 neoORF, учитывая частоту аллели и количество клеток. На ФИГ. 31A-31D показаны GATA3 специфические CD8+ Т-клетки через окрашивание мультимера. Эти Т-клетки выбирают в качестве эффекторных клеток для анализа цитоткосичности.
GATA3 трансдуцированные HEK293Т клетки используют в качестве клеток-мишеней (пример 21). Также, не трансдуцированные HEK 293Т клетки используют для отрицательного контроля. Через 6 часов сокультивирования эффекторных клеток и клеток-мишеней, среднее из 3,3%, 3,7%, 2,5% и 2,8% каспаза-3положительных клеток было найдено в 4 экспериментах в не трансдуцированных клетках-мишенях, и среднее из 4,4%, 5,2%, 6,3% и 6,9% каспаза-3 положительных клеток было найдено в GATA3 трансдуцированных клетках, соответственно (ФИГ. 32). Значительное большее количество каспаза-3 положительных клеток-мишеней было найдено в сокультуре с GATA3 индуцированными PBMC из HD51 (ФИГ. 33). Более высокая частота CD107a экспрессированных CD8+ Т-клеток наблюдалась в условиях сокультивирования GATA3 трансдуцированных HEK293Т клетках с 2 из GATA индуцированных PBMC здорового донора (образец 1 и образец 2) (ФИГ. 34). Более высокий уровень IFN-γ определили в тех же условиях сокультиврования с 2 из GATA индуцированных PBMC здорового донора (образец 1 и образец 2) (ФИГ. 35).
Анализ цитотоксичности in vitro используют для оценки способности CD8+ Т клеток, специфических к GATA3 neoORF, распознавать и уничтожать клетки, имеющие GATA3 мутацию «сдвига рамки». PBMC, включающие Т-клетки, специфические к неоантигенам GATA3 со сдвигом рамки на HLA-A02:01, полученные у здоровых доноров, стимулированные пептидом GATA3 со сдвигом рамки MLTGPPARV (SEQ ID NO: 3549), тестируют как типовые для типов Т-клеток, которые могут быть индуцированы из вакцин GATA3 со сдвигом рамки. Эти Т-клетки приводят к смерти опухолевой клетки, что подтверждено анализом наличия маркера смерти клетки-мишени, каспазы-3. Результаты анализов маркера активации CD8+ Т-клетки D107a и цитокина IFN-γ также позволяют предположить, что эти индуцированные пептидом Т-клетки могут распознавать и убивать клетки, которые в природе процессируют и презентируют неоантигены GATA3 со сдвигом рамки.
Пример 26 Клонирование TCR и функциональные анализы
В примере ниже показано клонирование Т-клеточного рецептора (TCR) из CD8+ Т-клеток, специфических к неоантигену, из GATA3 neoORF на HLA-A02:01, и функциональные анализы. Индукция неоантиген-специфических CD8+ Т-клеток описана в примере 23. Специфические CD8+ Т-клетки выделяют с использованием сортировки флуоресцентно-активированных клеток (FACS), и TCR последовательность идентифицируют с использованием платформ 10x Genomics и MiSeq. Выбранные TCR затем рекомбинантно экспрессируют в колонии Т-клеток для функциональной характеризации TCR и оценки процессинга и презентирования неоантигена на поверхности клетки, имеющей GATA3 neoORF мутацию, создание которые описано в примере 21.
TCR характеризуется авидностью ниже 40 нМ. Это демонстрирует, что возможно создавать CD8+ Т-клетки с TCR к неоантигенам GATA3. Кроме того, TCR способен распознавать процессированный и презентированный неоантиген на поверхности HEK293Т клеток, несущих мутацию GATA3 neoORF, что подтверждается результатами в Примере 22, демонстрируя процессинг и презентирование GATA3неоантигенов на поверхности клеток, несущих мутацию.
Материалы и методы
На ФИГ. 36-38 показан обзор TCR клонирования и функционального анализа. GATA3 CD8+ Т-клетки сортируют мультимером.
GATA3 neoORF специфические Т-клетки индуцируют и размножают (Пример 23). Индуцированные клетки окрашивают GATA3 9мером пептидного мультимера и поверхностными антителами (CD8, CD4, CD14, CD16, CD19 и ближним-ИК флуоресцентным реакционноспособным красителем). GATA3 специфические Т-клетки, которые были положительные к GATA3 мультимеру и CD8, сортируют с использованием FACS ARIA fusion (BD) и собирают в 1,5 мл пробирку, содержащую 2% ФТС в ФРФБ.
Секвенирование TCR отдельной Т-клетки с использованием 10x Genomics и MiSeq
После сортировки, собранные клетки сразу же обрабатывают баркодированием отдельной клетки и созданием кДНК с использованием наборов Chromium Single Cell V(D)J Reagent Kits (10x Genomics). Обогащение TCR последовательности и конструирование библиотеки проводят согласно протоколу производителя. Секвенирование проводят в 10 пМ масштабе с набором реагентов MiSeq 300 cycles reagent kit и MiSeq (Illumina). Анализ TCR последовательности и клональных свойств проводят с использованием программы Cell ranger и браузера Loupe VDJ (10x Genomics).
Синтез и клонирование TCR гена
Выбранные TCR последовательности кодон-оптимизируют для системы млекопитающих. TCR ДНК последовательности синтезируют и клонируют в лентивирусный вектор (pCDH-EF1ɑ-Puro, System Biosciences) от GENEWIZ (NJ, USA). Лентивирусный вектор содержит EF1ɑ промотор, за которым следует TCR бета, сайт расщепления фурина, F2A, TCR альфа, T2A и сайт резистентности к пиромицину (ФИГ. 40)
Получение лентивируса
Для получения лентивируса, кодирующего GATA3 neoORF TCR ген, лентивирусный вектор, упаковочные плазмиды и свежие HEK 293Т клетки (ATCC) используют способом трансфекции. Подробности трансфекции и сбора описаны в примере 21.
Трансдукция в клетки Jurkat или PBMC
Модифицированные клетки Jurkat (J.RT3-T3.5, ATCC), которые не имеют TCR бета, модифицируют для экспрессирования CD8+ альфа цепи лнтивирусом, кодирующим CD8+ альфа ген. Модифицированные клетки Jurkat используют для трансдукции GATA3 TCR лентивирус. 1,8х106 клеток Jurkat высевают в 1,2 мл среды RPMI-1640 с 10% ФТС и 6 мкг/мл полибрена в 24-луночный планшет. Затем 0,6 мл GATA3 специфического TCR лентивируса добавляют к клеткам, планшет центрифугируют при 2400 об./мин. в течение 45 минут при 32°C. Клетки инкубируют в 5% CO2 инкубаторе в течение 24 часов. Трансдуцированные клетки Jurkat выдерживают в среде RPMI-1640 с 10% ФТС с 1 мкг/мл пуромицина в течение 10 дней.
Анализ выделения IL-2 с пептидным титрованием
Для оценки чувствительности TCR, который клонировали в клетки Jurkat, проводят анализ пептидного титрования. Клетки Jurkat специфически секретируют IL-2 в ответ на подачу сигнала TCR. Так как клетки Jurkat, используемые в это анализе, не имеют эндогенный TCR бета, TCR на поверхности этих клеток является специфически клонированным TCR. Пептиды добавляют в широком диапазоне концентраций в клетки-мишени HEK293T с релевантной HLA (HLA-A02:01), но не с GATA3 мутацией, для оценки максимальной секреции IL-2, и для оценки концентрации пептида, требуемой для выделения 50% от этой максимальной секреции (EC50). Эту EC50 берут как авидность TCR. 20000 немодифицированных HEK 293Т клеток, которые эндогенно экспрессируют HLA:A02.01, высевают на 96-луночный планшет с добавлением 100 мкл GATA3 пептида или иррелевантного пептида в концентрации от 20 мкМ до 2 пМ в DMEM с 10% ФТС. После инкубации в течение ночи при 37°С, 200000 GATA3 neoORF специфических TCR трансдуцированных клеток Jurkat добавляют в каждую лунку в соотношении 10:1 TCR трансдуцированных клеток Jurkat к HEK 293Т клеткам с загруженным пептидом. Сокультуру инкубируют в 5% CO2 инкубаторе при 37°С в течение 24 часов. 50 мкл супернатанта из каждой лунки собирают, и концентрацию IL-2 человека измеряют набором Meso scale discovery kit согласно протоколу производителя.
Анализ выделения IL-2 с клетками-мишенями, трансдуцированными GATA3 мутацией
Для оценки способности TCR распознавать действительно процессированный и презентированный неоантиген, сокультивируют TCR-трансдуцированные клетки Jurkat и клетки-мишени HEK 293T. В этой системе, однако, никакие пептиды не добавляют экзогенно. Вместо этого, клеточные линии, трансдуцированные либо GATA3 neoORF, либо иррелевантным геном, используют в качестве мишеней. Таким образом, для того, чтобы TCR-трансдуцированные клетки Jurkat распознавали их мишени, GATA3 неоантиген должен быть процессирован и презентирован на поверхности клетки-мишени.
20000 HEK 293Т клеток, трансдуцированных GATA3 мутацией или иррелевантным геном, высевают на 96-луночный планшет. После инкубации в течение ночи, 200000 GATA3 специфических TCR трансдуцированных клеток Jurkat добавляют в каждую лунку. Сокультуру инкубируют в 5% CO2 инкубаторе при 37°С в течение 24 часов. 50 мкл супернатанта из каждой лунки собирают, и концентрацию IL-2 человека измеряют набором Meso scale discovery kit согласно протоколу производителя (Meso Scale Discovery).
Результаты
GATA3 специфические TCR клетки Jurkat
Сортировка GATA3 специфических CD8+ Т-клеток
2,1% GATA3 специфических CD8+ Т-клеток определяют в лунке № 5 здорового донора 42 с использованием GATA3 HLA-A02 мультимера после долговременного стимулирования GATA3 neoORF пептидом MLTGPPARV (SEQ ID NO: 3550). 5402 дважды положительных к мультимеру клеток сортируют с использованием FACSARIA (ФИГ. 39). Сортированные клетки обрабатывают баркодированием отдельной клетки с использованием набора 10X Genomics V(D)J. Спаренные TCR альфа и бета последовательности анализируют с использованием браузера Loupe V(D)J. Доминирующий клонотип (клонотип1) имеет последовательности CALDIYGNNRLAF (SEQ ID NO: 3551) и CASSLDFVLAGSYSYEQFF (SEQ ID NO: 3552) CDR3 TCR альфа и бета аминокислотных последовательностей, соответственно. Клонотип 2 имеет ту же TCR бета последовательность, что и клонотип1, без последовательности TCR альфа. Клонотип 4 имеет ту же TCR альфа последовательность, что и клонотип1, без последовательности TCR бета. Суммарная доля клонотипа 1, 2 и 4 составляет 82,5% от всех TCR клонотипов, и другие клонотипы составляют менее чем 1% (таблица 32).
В таблице 32 ниже показан типовой анализ клонотипа GATA3 специфического TCR
Синтез и клонирование ДНК GATA3 специфического TCR
Клонотип 1 TCR альфа и бета последовательностей кодон-оптимизируют согласно частоте применения кодона человека для максимальной экспрессии в клеточной линии и PBMC человека (таблица 32). Кодированную TCR геном лентивирусную плазмиду (ФИГ. 40) оценивают ДНК секвенированием и расщеплением рестрикционной эндонуклеазы. Данные ДНК последовательности конечной GATA3 neoORF специфической TCR кодированной плазмиды на 100% совпадают с TCR альфа и бета кодон-оптимизированной последовательности (жирный шрифт на ФИГ. 41). После расщепления рестрикционной эндонуклеазы AflII, наблюдают два диска ДНК; один диск между 6000 п.о. и 5000 п.о., и другой диск между 4000 п.о. и 3000 п.о. Эти диски коррелируют с ожидаемым размером 5590 п.о. и 3424 п.о., соответственно (ФИГ. 42).
В таблице 33 ниже показаны GATA3 специфические TCR альфа и бета ДНК последовательности и кодон-оптимизированные последовательности.
Экспрессия GATA3 специфического TCR
Для клеток Jurkat, экспрессирующих GATA3 специфический TCR, лентивирусную систему используют после трансфекции колонии HEK 293Т клеток GATA3 специфическим TCR конструктом, и лентивирус трансдуцируют в клетки Jurkat. Трансдуцированные и пиромицин-выбранные клетки Jurkat окрашивают GATA3 мультимером-PE и GATA3 мультимером-BV650 и сравнивают с не трансдуцированными клетками Jurkat для верификации экспрессии GATA3 специфического TCR. 73,1% клеток были положительные для обоих, GATA3 мультимера-PE и GATA3 мультимера-BV650, что указывает на экспрессию GATA3 neoORF специфического TCR (ФИГ. 43)
Тест титрования пептида
Для верификации того, что рекомбинантный TCR является функциональным, концентрации пептида от 20 мкМ до 0,2 пМ тестируют с GATA3 специфическими TCR трансдуцированными клетками Jurkat. Уровни секреции IL-2 из клеток Jurkat показали нелинейную корреляцию с концентрацией GATA3 пептида с наблюдаемой EC50=37,85 нМ (ФИГ. 44).
Анализ выделения IL-2 для GATA3 специфических TCR трансдуцированных Jurkat
Для верификации распознавания эндогенного антигена с GATA3 мутацией с использованием GATA3 мутация-специфических TCR Jurkat, HEK 293Т клетки с трансдуцированной мутацией используют в качестве клеток-мишеней и сокультивируют с GATA3 TCR трансдуцированными клетками Jurkat. Уровень IL-2 был выше в группе HEK 293Т клеток с загруженным пептидом с GATA3 мутацией (круги) по сравнению с группой клеток с загруженным иррелевантным пептидом (треугольники) на ФИГ. 45. Уровень IL-2 был также выше в группе клеток-мишеней с трансдуцированной GATA3 мутацией (квадраты) по сравнению с группой клеток-мишеней с трансдуцированным иррелевантным геном (перевернутые треугольники) на ФИГ. 45.
В этом исследовании, TCR клонируют из CD8+ Т-клеток, специфических к GATA3 неоантигену, презентированному на HLA-A02:01. Авидность TCR определяют как менее чем 40 нМ пептидным титрованием (EC50), и TCR способен распознавать клеточную линию, экспрессирующую GATA3 neoORF. Эти данные подтверждают создание CD8+ Т-клеток, которые имеют эффективные TCR, которые могут распознавать клетки с GATA3 neoORF мутацией.
Примеры 27 - Пример 41 описанные ниже относятся к мутантным BTK и мутантным EGFR пептидам
Пример 27 Анализ внутриклеточного окрашивания цитокином
Индукцию ответов BTK неоантиген-специфических CD4+ и CD8+ Т-клеток и анализ тетрамерного окрашивания проводят как описано в Примере 1 и Примере 2. Индукцию ответов EGFR неоантиген-специфических CD4+ и CD8+ Т-клеток и анализ тетрамерного окрашивания проводят как описано в Примере 1 и Примере 2. В отсутствие установившегося тетрамерного окрашивания для идентификации антиген-специфических популяций Т-клеток, специфичность к антигену может быть оценена с использованием оценки продуцирования цитокина с использованием установившихся анализов проточной цитометрией. Коротко, Т-клетки стимулируют пептидом, представляющим интерес, и сравнивают с контролем. После стимуляции, продуцирование цитокинов CD4+ Т-клетками (например, IFNγ и TNFα) оценивают внутриклеточным окрашиванием. Эти цитокины, особенно IFNγ, могут использоваться для идентификации стимулированных клеток. Проводят FACS анализ антиген-специфической индукции уровней IFNγ и TNFα CD4+ клеток от здорового донора, стимулированных APC, загруженными с или без мутантной BTK. Проводят FACS анализ антиген-специфической индукции уровней IFNγ и TNFα CD4+ клеток от здорового донора, стимулированных APC, загруженными с или без мутантного пептида EGFR.
Пример 28 – Анализ ELISPOT
Пептид-специфические Т-клетки функционально пересчитывают с использованием анализа ELISPOT (BD Biosciences), который измеряет выделение IFNγ из Т-клеток на одноклеточной основе. Клетки-мишени (T2 или HLA-A0201 трансфицированные C1R) активируют с 10 мкМ пептида в течение 1 часа при 37°C и промывают три раза. 1x105 активированных пептидом мишеней костимулируют в лунках планшета ELISPOT с разными концентрациями Т-клеток (5x102-2x103), взятых из иммуногенной культуры. Планшеты обрабатывают согласно протоколу производителя и анализируют на ридере ELISPOT (Cellular Technology Ltd.) с использованием прилагаемой программы. Споты, соответствующие количеству IFNγ-продуцирующих Т-клеток, описаны как абсолютное количество спотов на количество высеянных Т-клеток. Т-клетки, размноженные на модифицированных пептидах, тестируют не только на их способность распознавать мишени, активированные модифицированным пептидом, но также на их способность распознавать мишени, активированные исходным пептидом. Определяют уровни IFNγ в образцах с имитацией трансдукции или трансдуцированных лентивирусным вектором экспрессии, кодирующим мутантный BTK пептид или мутантный EGFR пептид.
Пример 29 – Анализ окрашивания CD107
CD107a и b экспрессируют на клеточной поверхности CD8+ Т-клеток после активации распознанным пептидом. Протеазосодержащие вакуоли Т-клеток имеют жировой бислой, который содержит лизосомально-ассоциированные мембранные гликопротеины (“LAMP”), которые включают молекулы CD107a и b. Когда цитотоксические Т-клетки активируют через Т-клеточный рецептор, мембраны этих протеазосодержащих вакуолей мобилизуются и сливаются с мембраной плазмы Т-клетки. Выделяется гранулированное содержимое, и это приводит к смерти клетки-мишени. При слиянии мембраны гранул с мембраной плазмы, C107a и b обнажаются на поверхности клетки и поэтому становятся маркерами дегрануляции. Так как дегрануляция по данным CD107a и b окрашивания описана на одноклеточной основе, анализ используют для функционального подсчета пептид-специфических Т-клеток. Для проведения анализа, пептид добавляют к HLA-A02:01-трансфицированным клеткам C1R до конечной концентрации 20 мкМ, клетки инкубируют в течение 1 часа при 37°C и промывают три раза. 1x105 активированных пептидом C1R клеток аликвотируют в пробирки, и антитела, специфические к CD107a и b, добавляют до конечной концентрации, предложенной производителем (Becton Dickinson). Антитела добавляют до добавления Т-клеток для “улавливания” CD107 молекул, как только они временно появляются на поверхности во время проведения анализа. Затем добавляют 1x105 Т-клеток из иммуногенной культуры, и образцы инкубируют в течение 4 часа при 37°C. Т-клетки затем окрашивают для дополнительных поверхностноклеточных молекул, таких как CD8, и данные получают на инструменте FACS Calibur (Becton Dickinson). Данные анализируют с использованием прилагаемой программы Cellquest, и результаты показаны как доля CD8+/CD107a и b+ клеток.
Пример 30 – Анализы цитотоксичности
Цитотоксическую активность измеряют с использованием способа 1 или способа 2. Способ 1 включает анализ выделения хрома. T2 клетки-мишени метят Na51Cr в течение 1 часа при 37°C и промывают, 5x103 T2 клеток-мишеней затем добавляют к разным количествам Т-клеток из иммуногенной культуры. Выделение хрома измеряют в супернатанте, собранном через 4 часа инкубации при 37°C. Долю специфического лизиса рассчитывают как:
Уравнение 10. Экспериментальное выделение – спонтанное выделение/Общее выделение – спонтанное выделение x 100.
В способе 2 цитотоксическую активность измеряют с определением расщепленной каспазы 3 в клетках-мишенях проточной цитометрией. Раковые клетки-мишени конструируют для экспрессии мутантного пептида вместе с подходящей MHC-I аллелем. Клетки-мишени с имитацией трансдукции (т.е. не экспрессирующие мутантный пептид) используют в качестве отрицательного контроля. Клетки метят CFSE для отделения их от стимулированных PBMC, применяемых в качестве эффекторных клеток. Мишени и эффекторные клетки сокультивируют в течение 6 часов, затем собирают. Внутриклеточное окрашивание проводят для определения расщепленной формы каспазы 3 в CFSE-положительных раковых клетках-мишенях. Долю специфического лизиса рассчитывают как:
Уравнение 11. Экспериментальное расщепление каспазы 3/спонтанное расщепление каспазы 3 (измеренное в отсутствие экспрессии мутантного пептида) x 100.
Способ 2 анализа цитотоксичности представлен в разделе «Материалы и способы» Примера 25 настоящего описания.
Пример 31 – Усиленные ответы CD8+ Т-клетки in vivo с последовательным применением лонгмера и шортмера
Вакцинация лонгмерными пептидами может вызывать ответы и CD4+ и CD8+ Т-клеток, в зависимости от процессинга и презентирования пептидов. Вакцинация минимальными шортмерными эпитопами сфокусирована на создании ответов CD8+ Т-клеток, но не требует процессинга пептида до презентирования антигена. Как таковая, любая клетка может легко презентировать эпитоп, а не только профессиональные антигенпрезентирующие клетки (APC). Это может привести к толерантности Т-клеток, которые контактируют со здоровыми клетками, презентирующими антигены как часть периферической толерантности. Чтобы обойти это, исходная иммунизация лонгмером позволяет примирование CD8+ Т-клеток только APC, которые могут процессировать и презентировать пептиды. Последующие иммунизации усиливают исходные ответы CD8+ Т-клетки.
Анализы иммуногенности in vivo
Девятнадцать самок мышей C57BL/6 в возрасте 8-12 недель (Taconic Biosciences) произвольно и планово распределяют на группы обработки при поступлении. Животных акклиматизируют в течение трех (3) дней до начала исследования. Животных кормят стерильным кормом для грызунов LabDiet™ 5053, и стерильную воду дают ad libitum. Животные в группе 1 служат в качестве контроля с только адъювантом, и им вводят только полиинозиновую:полицитидиловую кислоту (полиI:C) в дозе 100 мкг в объеме 0,1 мл подкожной инъекцией (п.к.) в дни 0, 7 и 14. Животным в группе 2 вводят по 50 мкг каждого из шести лонгмерных пептидов (описанных ниже) вместе с полиI:C в дозе 100 мкг п.к. в объеме 0,1 мл в дни 0, 7 и 14. Животным в группе 3 вводят по 50 мкг каждого из шести лонгмерных пептидов (описанных ниже) вместе с полиI:C в дозе 100 мкг п.к. в объеме 0,1 мл в день 0 и молярные эквиваленты соответствующих шортмерных пептидов (описаны ниже) вместе с полиI:C в дозе 100 мкг п.к. в объеме 0,1 мл в дни 7 и 14. Животных взвешивают и ежедневно отслеживают общее состояние здоровья. Животных умерщвляют сверхдозой CO2 в день 21 завершения исследования, если животное теряет >30% массы тела по сравнению с массой в день 0; или если животное обнаружено агонирующим. При умерщвлении, селезенки собирают и обрабатывают в одноклеточные суспензии с использованием стандартных протоколов. Коротко, селезенки механически разрушают через 70 мкМ фильтр, пеллетируют и лизируют с ACK лизисным буфером (Sigma) перед ресуспендированием в среде для культивирования клеток.
Пептиды
Шесть ранее идентифицированных неоантигенов мыши используют на основе продемонстрированной ими способности вызывать ответы CD8+ Т-клетки. Для каждого неоантигена, был определен шортмер (8-11 аминокислот), соответствующий минимальному эпитопу. Используют лонгмер, соответствующий 20-27 аминокислотам, окружающим мутацию.
ELISPOT
Анализ ELISPOT (Mouse IFNγ ELISPOT Reasy-SET-Go; EBioscience) проводят согласно протоколу набора. Коротко, за день до анализа, 96-луночные фильтровальные планшеты (гидрофобная PVDF мембрана с размером пор 0,45 мкМ; EMD Millipore) активируют (35% EtOH), промывают (ФРФБ) и покрывают иммобилизованным антителом (1:250; 4°C O/N). В день анализа, лунки промывают и блокируют (среда; 2 часа при 37°C). Приблизительно 2x105 клеток в 100 мкл добавляют в лунки вместе с 100 мкл 10 мМ тестируемого пептидного пула (шортмер) или PMA/иономицин положительным контрольным антигеном или носителем. Клетки инкубируют с антигеном в течение ночи (16-18 часов) при 37°C. На следующий день суспензию клеток вынимают и лунки промывают один раз ФРФБ и два раза деионизированной водой. Для всех стадий промывки в оставшейся части анализа, лунки замачивают на 3 минуты на каждой стадии промывки. Затем лунки промывают три раза промывочным буфером (ФРФБ+0,05% Tween-20), и идентифицирующее антитело (1:250) добавляют во все лунки. Планшеты инкубируют в течение двух часов при комнатной температуре. Раствор идентифицирующего антитела удаляют, и лунки промывают три раза буфером. Авидин-HRP (1:250) добавляют во все лунки, и планшеты инкубируют в течение одного часа при комнатной температуре. Раствор конъюгата удаляют, и лунки три раза промывают промывочным буфером, затем один раз ФРФБ. Субстрат (3-амино-9-этилкарбазол, 0,1 M в ацетатном буфере, H2O2) добавляют во все лунки, и отслеживают развитие спота (приблизительно 10 минут). Субстратную реакцию останавливают промыванием лунок водой, и планшеты сушат на воздухе в течение ночи. Планшеты анализируют на ридере ELISPOT (Cellular Technology Ltd.) с использованием прилагаемой программы. Споты, соответствующие количеству IFNγ-продуцирующих Т-клеток, показывают как абсолютное количество спотов на количество высеянных Т-клеток.
Пример 32 – Определение мутантных BTK пептидов масс спектрометрией
293Т клетки трансдуцируют лентивирусным вектором, кодирующим разные области мутантного BTK пептида. 50-100 миллионов трансдуцированных клеток, экспрессирующих пептиды, кодированные мутантным BTK пептидом, культивируют и пептиды элюируют из комплексов HLA-пептид с использованием кислой промывки. Элюированные пептиды затем анализируют МС/МС.
Пример 33 Мутантные BTK пептиды продуцируют сильные эпитопы на множестве аллелей.
Множественные пептиды, содержащие неоэпитопы, экспрессируют или загружают в антигенпрезентирующие клетки (APC). Затем проводят масс спектрометрию, и определяют аффинность неоэпитопов для указанных HLA аллелей и стабильность неоэпитопов с HLA аллелями.
Пример 34 Множество BTK неоэпитопов вызывают ответ CD8+ Т-клетки
Образцы PBMC от донора-человека могут использоваться для проведения антиген-специфической индукции Т-клетки. Индукции CD8+ Т-клеток анализируют после производства Т-клеток. Образцы клеток могут быть взяты в разные моменты времени для анализа. pMHC мультимер используют для отслеживания доли антиген-специфических CD8+ Т-клеток в индукционных культурах.
Пример 35 Спрогнозированная HLA специфичность мутантных BTK неопептидов
Специфические неопептиды BTK прогоняют по запатентованному алгоритму RECON для прогнозирования специфичности HLA. Неопептиды ранжируют на основе спрогнозированной аффинности связывания. В таблице 38 показана специфичность к аллелям, которые далее ранжируют по аффинности от высокой до низкой. Более низкое ранговое значение указывает на более сильную аффинность. В таблице 38 также показано, что мутантные BTK неопептиды, идентифицированные и охарактеризованные в настоящем изобретении, имеют сильные эпитопы с множеством аллелей.
В таблице 38 изображена аллельная специфичность, которая далее ранжируется по аффинности от высокой до низкой
Пример 36. Аффинность и стабильность мутантных BTK неопептидов
Множество пептидов, содержащих неоэпитопы, в таблице ниже либо экспрессируют, либо загружают в антигенпрезентирующие клетки. Затем проводят масс спектрометрией и определяют аффинность неоэпитопов для указанных HLA аллелей, и определяют стабильность неоэпитопов с HLA аллелями.
В таблице 39 показана соответствующая аффинность и стабильность мутантных BTK пептидов.
Пример 37 – Определение мутантных EGFR пептидов масс спектрометрией
293Т клетки трансдуцируют лентивирусным вектором, кодирующим разные области мутантного EGFR пептида. 50-100 миллионов трансдуцированных клеток, экспрессирующих пептиды, кодированные мутантным EGFR пептидом, культивируют и пептиды элюируют из комплексов HLA-пептид с использованием кислой промывки. Элюированные пептиды затем анализируют МС/МС.
Пример 38 – Мутантные EGFR пептиды продуцируют сильные эпитопы на множестве аллелей.
Множественные пептиды, содержащие неоэпитопы, экспрессируют или загружают в антигенпрезентирующие клетки (APC). Затем проводят масс спектрометрию, и определяют аффинность неоэпитопов для указанных HLA аллелей и стабильность неоэпитопов с HLA аллелями.
Пример 39 - Множество EGFR неоэпитопов вызывают ответ CD8+ Т-клетки
Образцы PBMC от донора-человека могут использоваться для проведения антиген-специфической индукции Т-клетки. Индукции CD8+ Т-клеток анализируют после производства Т-клеток. Образцы клеток могут быть взяты в разные моменты времени для анализа. pMHC мультимер используют для отслеживания доли антиген-специфических CD8+ Т-клеток в индукционных культурах.
Пример 40 – Спрогнозированная HLA специфичность мутантных EGFR неопептидов
Специфические неопептиды прогоняют по запатентованному алгоритму RECON для прогнозирования специфичности HLA. Неопептиды ранжируют на основе спрогнозированной аффинности связывания. В таблице 43 показана специфичность к аллелям, которые далее ранжируют по аффинности от высокой до низкой. Более низкое ранговое значение указывает на более сильную аффинность. В таблице 43 также показано, что мутантные EGFR неопептиды, идентифицированные и охарактеризованные в настоящем изобретении, имеют сильные эпитопы с множеством аллелей.
Таблица 43
Пример 41 Аффинность и стабильность мутантных EGFR неопептидов
Множество пептидов, содержащих неоэпитопы, в таблице ниже либо экспрессируют, либо загружают в антигенпрезентирующие клетки. Затем проводят масс спектрометрией и определяют аффинность неоэпитопов для указанных HLA аллелей, и определяют стабильность неоэпитопов с HLA аллелями. В таблице 44 показана соответствующая аффинность и стабильность мутантных EGFR пептидов.
Таблица 44
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NEON THERAPEUTICS, INC.
<120> НЕОАНТИГЕНЫ И ИХ ПРИМЕНЕНИЕ
<130> 50401-731.601
<140>PCT/US2019/038061
<141>2019-06-19
<150> 62/801,981
<151> 2019-02-06
<150> 62/800,700
<151> 2019-02-04
<150> 62/800,792
<151> 2019-02-04
<150> 62/789,162
<151> 2019-01-07
<150> 62/726,804
<151> 2018-09-04
<150> 62/702,567
<151> 2018-07-24
<150> 62/687,191
<151> 2018-06-19
<160> 3872
<170> PatentIn version 3.5
<210> 1
<211> 201
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn
1 5 10 15
Cys Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp
20 25 30
Pro Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn
35 40 45
Arg Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys
50 55 60
Met Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu
65 70 75 80
Asp Phe Pro Lys Asn Ser Ser Phe Pro Gly Arg Pro Leu Gln Thr His
85 90 95
Val Leu Pro Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala
100 105 110
Asp His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu Trp Thr
115 120 125
Thr Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser
130 135 140
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
145 150 155 160
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
165 170 175
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
180 185 190
Ser Leu Trp Cys Leu Cys Ser Asn His
195 200
<210> 2
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
50 55 60
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
65 70 75 80
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
85 90 95
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
100 105 110
His
<210> 3
<211> 52
<212> БЕЛОК
<213> Homo sapiens
<400> 3
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu
50
<210> 4
<211> 61
<212> БЕЛОК
<213> Homo sapiens
<400> 4
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
35 40 45
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
50 55 60
<210> 5
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 5
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 6
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 6
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 7
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 7
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 8
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 8
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 9
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 9
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 10
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 10
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5 10
<210> 11
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 11
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 12
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 12
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 13
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 13
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 14
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 14
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 15
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 16
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 16
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 17
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 17
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 18
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 18
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 19
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 19
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 20
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 20
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 21
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 21
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 22
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 22
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 23
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 23
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 24
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 24
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 25
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 25
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 26
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 26
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 27
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 27
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 28
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 28
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 29
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 29
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 30
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 30
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 31
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 31
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 32
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 32
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 33
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 33
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 34
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 34
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 35
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 35
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 36
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 36
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 37
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 37
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 38
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 38
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 39
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 39
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 40
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 40
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5 10
<210> 41
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 41
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 42
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 42
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 43
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 43
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 44
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 44
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 45
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 45
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 46
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 46
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 47
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 47
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 48
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 48
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 49
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 49
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 50
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 50
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 51
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 51
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 52
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 52
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 53
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 53
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 54
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 54
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 55
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 55
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 56
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 56
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 57
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 57
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 58
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 58
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 59
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 59
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 60
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 60
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 61
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 61
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 62
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 62
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 63
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 63
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 64
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 64
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 65
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 65
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 66
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 66
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 67
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 67
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 68
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 68
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 69
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 69
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 70
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 70
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 71
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 71
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 72
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 72
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 73
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 73
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 74
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 74
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 75
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 75
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 76
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 76
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 77
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 77
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 78
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 78
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 79
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 79
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 80
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 80
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 81
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 81
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 82
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 82
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 83
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 83
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 84
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 84
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5 10
<210> 85
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 85
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 86
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 86
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 87
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 87
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 88
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 88
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 89
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 89
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 90
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 90
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 91
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 91
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 92
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 92
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 93
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 93
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 94
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 94
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 95
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 95
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 96
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 96
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 97
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 97
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 98
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 98
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 99
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 99
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 100
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 100
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 101
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 101
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 102
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 102
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 103
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 103
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 104
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 104
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 105
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 105
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 106
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 106
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 107
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 107
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 108
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 108
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 109
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 109
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 110
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 110
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 111
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 111
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 112
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 112
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 113
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 113
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 114
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 114
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5 10
<210> 115
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 115
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 116
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 116
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 117
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 117
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 118
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 118
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 119
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 119
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 120
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 120
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 121
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 121
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 122
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 122
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 123
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 123
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 124
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 124
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 125
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 125
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 126
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 126
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 127
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 127
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 128
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 128
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 129
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 129
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 130
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 130
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 131
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 131
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 132
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 132
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 133
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 133
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 134
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 134
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 135
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 135
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 136
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 136
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 137
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 137
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 138
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 138
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 139
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 139
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 140
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 140
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 141
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 141
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 142
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 142
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 143
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 143
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 144
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 144
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
<210> 145
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 145
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 146
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 146
Ile Phe Ile Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10 15
Leu Arg Glu Met Arg His Arg
20
<210> 147
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 147
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 148
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 148
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 149
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 149
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 150
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 150
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 151
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 151
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 152
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 152
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 153
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 153
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 154
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 154
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 155
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 155
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 156
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 156
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 157
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 157
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 158
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 158
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 159
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 159
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 160
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 160
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 161
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 161
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 162
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 162
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 163
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 163
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 164
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 164
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 165
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 165
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 166
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 166
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 167
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 167
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 168
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 168
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 169
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 169
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 170
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 170
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 171
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 171
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 172
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 172
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 173
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 173
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 174
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 174
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 175
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 175
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 176
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 176
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 177
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 177
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 178
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 178
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 179
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 179
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 180
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 180
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 181
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 181
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 182
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 182
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 183
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 183
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 184
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 184
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 185
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 185
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 186
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 186
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 187
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 187
Ile Phe Ile Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10 15
Leu Arg Glu Met Arg His Arg
20
<210> 188
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 188
Ile Asp Ile Ile Met Lys Ile Arg Asn Ala
1 5 10
<210> 189
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 189
Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe
1 5 10 15
Phe Phe Phe Phe Ile Ile Phe Phe Ile Phe Phe Trp Met Cys
20 25 30
<210> 190
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 190
Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe
1 5 10 15
Phe Phe Phe Phe Phe Phe Phe Phe Ala Ala Phe Trp Phe Trp
20 25 30
<210> 191
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 191
Ile Phe Phe Ile Phe Phe Ile Ile Phe Phe Phe Phe Phe Phe Phe Phe
1 5 10 15
Phe Phe Phe Phe Ile Ile Ile Ile Ile Ile Ile Trp Glu Cys
20 25 30
<210> 192
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 192
Phe Ile Phe Phe Phe Ile Ile Phe Phe Phe Phe Phe Ile Phe Phe Phe
1 5 10 15
Phe Phe Ile Phe Ile Ile Ile Ile Ile Ile Phe Trp Glu Cys
20 25 30
<210> 193
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 193
Trp Gln Ala Gly Ile Leu Ala Arg
1 5
<210> 194
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 194
His Ser Tyr Thr Thr Ala Glu
1 5
<210> 195
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 195
Pro Leu Thr Glu Glu Lys Ile Lys
1 5
<210> 196
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 196
Gly Ala Leu His Phe Lys Pro Gly Ser Arg
1 5 10
<210> 197
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 197
Arg Arg Ala Asn Lys Asp Ala Thr Ala Glu
1 5 10
<210> 198
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 198
Lys Ala Phe Ile Ser His Glu Glu Lys Arg
1 5 10
<210> 199
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 199
Thr Asp Leu Ser Ser Arg Phe Ser Lys Ser
1 5 10
<210> 200
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 200
Phe Asp Leu Gly Gly Gly Thr Phe Asp Val
1 5 10
<210> 201
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 201
Cys Leu Leu Leu His Tyr Ser Val Ser Lys
1 5 10
<210> 202
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 202
Met Thr Glu Tyr Lys Leu Val Val Val
1 5
<210> 203
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 203
Lys Lys Asn Lys Lys Asp Asp Ile Lys Asp
1 5 10
<210> 204
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 204
Ala Gly Asn Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp
1 5 10 15
Asp Asp Asp Asp Lys Lys Asp Lys Asp Asp Asp Asp Asp Asp
20 25 30
<210> 205
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 205
Ala Gly Asn Lys Lys Lys Lys Lys Lys Lys Asn Asn Asn Asn Asn Asn
1 5 10 15
Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn
20 25 30
<210> 206
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 206
Ala Gly Arg Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp
1 5 10 15
Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp
20 25 30
<210> 207
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 207
Gly Lys Ser Ala Leu Thr Ile Gln Leu
1 5
<210> 208
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 208
Gly Lys Ser Ala Leu Thr Ile
1 5
<210> 209
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 209
Gln Gly Gln Asn Leu Lys Tyr Gln
1 5
<210> 210
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 210
Ile Leu Gly Val Leu Leu Leu Ile
1 5
<210> 211
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 211
Glu Lys Glu Gly Lys Ile Ser Lys
1 5
<210> 212
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 212
Ala Ala Ser Asp Phe Ile Phe Leu Val Thr
1 5 10
<210> 213
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 213
Lys Glu Leu Lys Gln Val Ala Ser Pro Phe
1 5 10
<210> 214
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 214
Lys Lys Lys Leu Ile Asn Glu Lys Lys Glu
1 5 10
<210> 215
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 215
Lys Lys Cys Asp Ile Ser Leu Gln Phe Phe
1 5 10
<210> 216
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 216
Lys Ser Thr Ala Gly Asp Thr His Leu Gly
1 5 10
<210> 217
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 217
Ala Thr Phe Tyr Val Ala Val Thr Val Pro
1 5 10
<210> 218
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 218
Leu Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr Asp Pro
1 5 10 15
Thr Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly
20 25 30
<210> 219
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 219
Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr Asp Pro Thr
1 5 10 15
Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly Glu
20 25 30
<210> 220
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 220
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 221
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 221
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 222
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 222
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 223
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 223
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 224
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 224
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 225
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 225
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 226
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 226
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 227
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 227
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 228
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 228
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 229
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 229
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 230
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 230
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 231
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 231
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 232
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 232
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 233
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 233
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 234
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 234
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 235
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 235
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 236
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 236
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 237
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 237
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 238
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 238
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 239
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 239
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 240
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 240
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 241
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 241
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 242
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 242
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 243
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 243
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 244
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 244
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 245
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 245
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 246
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 246
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 247
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 247
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 248
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 248
Ile Asp Ile Ile Met Lys Ile Arg Asn Ala
1 5 10
<210> 249
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 249
Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe
1 5 10 15
Phe Phe Phe Phe Ile Ile Phe Phe Ile Phe Phe Trp Met Cys
20 25 30
<210> 250
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 250
Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe Phe
1 5 10 15
Phe Phe Phe Phe Phe Phe Phe Phe Ala Ala Phe Trp Phe Trp
20 25 30
<210> 251
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 251
Ile Phe Phe Ile Phe Phe Ile Ile Phe Phe Phe Phe Phe Phe Phe Phe
1 5 10 15
Phe Phe Phe Phe Ile Ile Ile Ile Ile Ile Ile Trp Glu Cys
20 25 30
<210> 252
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 252
Phe Ile Phe Phe Phe Ile Ile Phe Phe Phe Phe Phe Ile Phe Phe Phe
1 5 10 15
Phe Phe Ile Phe Ile Ile Ile Ile Ile Ile Phe Trp Glu Cys
20 25 30
<210> 253
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 253
Trp Gln Ala Gly Ile Leu Ala Arg
1 5
<210> 254
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 254
His Ser Tyr Thr Thr Ala Glu
1 5
<210> 255
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 255
Pro Leu Thr Glu Glu Lys Ile Lys
1 5
<210> 256
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 256
Gly Ala Leu His Phe Lys Pro Gly Ser Arg
1 5 10
<210> 257
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 257
Arg Arg Ala Asn Lys Asp Ala Thr Ala Glu
1 5 10
<210> 258
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 258
Lys Ala Phe Ile Ser His Glu Glu Lys Arg
1 5 10
<210> 259
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 259
Thr Asp Leu Ser Ser Arg Phe Ser Lys Ser
1 5 10
<210> 260
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 260
Phe Asp Leu Gly Gly Gly Thr Phe Asp Val
1 5 10
<210> 261
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 261
Cys Leu Leu Leu His Tyr Ser Val Ser Lys
1 5 10
<210> 262
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 262
Met Thr Glu Tyr Lys Leu Val Val Val
1 5
<210> 263
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 263
Lys Lys Asn Lys Lys Asp Asp Ile Lys Asp
1 5 10
<210> 264
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 264
Ala Gly Asn Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp
1 5 10 15
Asp Asp Asp Asp Lys Lys Asp Lys Asp Asp Asp Asp Asp Asp
20 25 30
<210> 265
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 265
Ala Gly Asn Lys Lys Lys Lys Lys Lys Lys Asn Asn Asn Asn Asn Asn
1 5 10 15
Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn Asn
20 25 30
<210> 266
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 266
Ala Gly Arg Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp
1 5 10 15
Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp Asp
20 25 30
<210> 267
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 267
Gly Lys Ser Ala Leu Thr Ile Gln Leu
1 5
<210> 268
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 268
Gly Lys Ser Ala Leu Thr Ile
1 5
<210> 269
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 269
Gln Gly Gln Asn Leu Lys Tyr Gln
1 5
<210> 270
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 270
Ile Leu Gly Val Leu Leu Leu Ile
1 5
<210> 271
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 271
Glu Lys Glu Gly Lys Ile Ser Lys
1 5
<210> 272
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 272
Ala Ala Ser Asp Phe Ile Phe Leu Val Thr
1 5 10
<210> 273
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 273
Lys Glu Leu Lys Gln Val Ala Ser Pro Phe
1 5 10
<210> 274
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 274
Lys Lys Lys Leu Ile Asn Glu Lys Lys Glu
1 5 10
<210> 275
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 275
Lys Lys Cys Asp Ile Ser Leu Gln Phe Phe
1 5 10
<210> 276
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 276
Lys Ser Thr Ala Gly Asp Thr His Leu Gly
1 5 10
<210> 277
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 277
Ala Thr Phe Tyr Val Ala Val Thr Val Pro
1 5 10
<210> 278
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 278
Leu Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr Asp Pro
1 5 10 15
Thr Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly
20 25 30
<210> 279
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 279
Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr Asp Pro Thr
1 5 10 15
Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly Glu
20 25 30
<210> 280
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 280
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 281
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 281
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 282
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 282
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 283
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 283
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 284
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 284
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 285
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 285
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 286
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 286
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 287
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 287
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 288
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 288
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 289
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 289
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 290
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 290
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 291
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 291
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 292
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 292
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 293
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 293
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 294
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 294
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 295
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 295
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 296
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 296
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 297
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 297
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 298
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 298
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 299
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 299
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 300
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 300
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 301
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 301
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 302
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 302
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 303
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 303
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 304
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 304
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 305
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 305
Glu Pro Cys Ser Met Leu Thr Gly
1 5
<210> 306
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 306
Pro Cys Ser Met Leu Thr Gly Pro
1 5
<210> 307
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 307
Cys Ser Met Leu Thr Gly Pro Pro
1 5
<210> 308
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 308
Ser Met Leu Thr Gly Pro Pro Ala
1 5
<210> 309
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 309
Met Leu Thr Gly Pro Pro Ala Arg
1 5
<210> 310
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 310
Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 311
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 311
Thr Gly Pro Pro Ala Arg Val Pro
1 5
<210> 312
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 312
Gly Pro Pro Ala Arg Val Pro Ala
1 5
<210> 313
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 313
Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 314
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 314
Pro Ala Arg Val Pro Ala Val Pro
1 5
<210> 315
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 315
Ala Arg Val Pro Ala Val Pro Phe
1 5
<210> 316
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 316
Arg Val Pro Ala Val Pro Phe Asp
1 5
<210> 317
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 317
Val Pro Ala Val Pro Phe Asp Leu
1 5
<210> 318
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 318
Pro Ala Val Pro Phe Asp Leu His
1 5
<210> 319
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 319
Ala Val Pro Phe Asp Leu His Phe
1 5
<210> 320
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 320
Val Pro Phe Asp Leu His Phe Cys
1 5
<210> 321
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 321
Pro Phe Asp Leu His Phe Cys Arg
1 5
<210> 322
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 322
Phe Asp Leu His Phe Cys Arg Ser
1 5
<210> 323
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 323
Asp Leu His Phe Cys Arg Ser Ser
1 5
<210> 324
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 324
Leu His Phe Cys Arg Ser Ser Ile
1 5
<210> 325
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 325
His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 326
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 326
Phe Cys Arg Ser Ser Ile Met Lys
1 5
<210> 327
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 327
Cys Arg Ser Ser Ile Met Lys Pro
1 5
<210> 328
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 328
Arg Ser Ser Ile Met Lys Pro Lys
1 5
<210> 329
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 329
Ser Ser Ile Met Lys Pro Lys Arg
1 5
<210> 330
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 330
Ser Ile Met Lys Pro Lys Arg Asp
1 5
<210> 331
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 331
Ile Met Lys Pro Lys Arg Asp Gly
1 5
<210> 332
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 332
Met Lys Pro Lys Arg Asp Gly Tyr
1 5
<210> 333
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 333
Lys Pro Lys Arg Asp Gly Tyr Met
1 5
<210> 334
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 334
Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 335
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 335
Lys Arg Asp Gly Tyr Met Phe Leu
1 5
<210> 336
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 336
Arg Asp Gly Tyr Met Phe Leu Lys
1 5
<210> 337
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 337
Asp Gly Tyr Met Phe Leu Lys Ala
1 5
<210> 338
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 338
Gly Tyr Met Phe Leu Lys Ala Glu
1 5
<210> 339
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 339
Tyr Met Phe Leu Lys Ala Glu Ser
1 5
<210> 340
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 340
Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 341
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 341
Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 342
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 342
Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 343
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 343
Lys Ala Glu Ser Lys Ile Met Phe
1 5
<210> 344
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 344
Ala Glu Ser Lys Ile Met Phe Ala
1 5
<210> 345
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 345
Glu Ser Lys Ile Met Phe Ala Thr
1 5
<210> 346
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 346
Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 347
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 347
Lys Ile Met Phe Ala Thr Leu Gln
1 5
<210> 348
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 348
Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 349
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 349
Met Phe Ala Thr Leu Gln Arg Ser
1 5
<210> 350
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 350
Phe Ala Thr Leu Gln Arg Ser Ser
1 5
<210> 351
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 351
Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 352
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 352
Thr Leu Gln Arg Ser Ser Leu Trp
1 5
<210> 353
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 353
Leu Gln Arg Ser Ser Leu Trp Cys
1 5
<210> 354
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 354
Gln Arg Ser Ser Leu Trp Cys Leu
1 5
<210> 355
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 355
Arg Ser Ser Leu Trp Cys Leu Cys
1 5
<210> 356
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 356
Ser Ser Leu Trp Cys Leu Cys Ser
1 5
<210> 357
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 357
Ser Leu Trp Cys Leu Cys Ser Asn
1 5
<210> 358
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 358
Glu Pro Cys Ser Met Leu Thr Gly Pro
1 5
<210> 359
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 359
Pro Cys Ser Met Leu Thr Gly Pro Pro
1 5
<210> 360
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 360
Cys Ser Met Leu Thr Gly Pro Pro Ala
1 5
<210> 361
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 361
Ser Met Leu Thr Gly Pro Pro Ala Arg
1 5
<210> 362
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 362
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 363
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 363
Leu Thr Gly Pro Pro Ala Arg Val Pro
1 5
<210> 364
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 364
Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5
<210> 365
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 365
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 366
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 366
Pro Pro Ala Arg Val Pro Ala Val Pro
1 5
<210> 367
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 367
Pro Ala Arg Val Pro Ala Val Pro Phe
1 5
<210> 368
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 368
Ala Arg Val Pro Ala Val Pro Phe Asp
1 5
<210> 369
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 369
Arg Val Pro Ala Val Pro Phe Asp Leu
1 5
<210> 370
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 370
Val Pro Ala Val Pro Phe Asp Leu His
1 5
<210> 371
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 371
Pro Ala Val Pro Phe Asp Leu His Phe
1 5
<210> 372
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 372
Ala Val Pro Phe Asp Leu His Phe Cys
1 5
<210> 373
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 373
Val Pro Phe Asp Leu His Phe Cys Arg
1 5
<210> 374
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 374
Pro Phe Asp Leu His Phe Cys Arg Ser
1 5
<210> 375
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 375
Phe Asp Leu His Phe Cys Arg Ser Ser
1 5
<210> 376
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 376
Asp Leu His Phe Cys Arg Ser Ser Ile
1 5
<210> 377
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 377
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 378
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 378
His Phe Cys Arg Ser Ser Ile Met Lys
1 5
<210> 379
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 379
Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5
<210> 380
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 380
Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5
<210> 381
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 381
Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5
<210> 382
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 382
Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5
<210> 383
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 383
Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5
<210> 384
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 384
Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5
<210> 385
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 385
Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5
<210> 386
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 386
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 387
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 387
Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5
<210> 388
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 388
Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5
<210> 389
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 389
Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5
<210> 390
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 390
Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5
<210> 391
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 391
Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5
<210> 392
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 392
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 393
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 393
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 394
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 394
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 395
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 395
Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5
<210> 396
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 396
Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5
<210> 397
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 397
Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5
<210> 398
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 398
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 399
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 399
Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5
<210> 400
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 400
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 401
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 401
Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5
<210> 402
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 402
Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5
<210> 403
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 403
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 404
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 404
Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5
<210> 405
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 405
Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5
<210> 406
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 406
Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5
<210> 407
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 407
Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5
<210> 408
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 408
Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5
<210> 409
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 409
Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5
<210> 410
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 410
Ser Leu Trp Cys Leu Cys Ser Asn His
1 5
<210> 411
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 411
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro
1 5 10
<210> 412
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 412
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala
1 5 10
<210> 413
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 413
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
1 5 10
<210> 414
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 414
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 415
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 415
Met Leu Thr Gly Pro Pro Ala Arg Val Pro
1 5 10
<210> 416
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 416
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5 10
<210> 417
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 417
Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10
<210> 418
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 418
Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10
<210> 419
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 419
Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10
<210> 420
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 420
Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10
<210> 421
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 421
Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10
<210> 422
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 422
Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10
<210> 423
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 423
Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 424
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 424
Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10
<210> 425
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 425
Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10
<210> 426
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 426
Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10
<210> 427
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 427
Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10
<210> 428
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 428
Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10
<210> 429
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 429
Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 430
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 430
Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10
<210> 431
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 431
His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10
<210> 432
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 432
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10
<210> 433
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 433
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10
<210> 434
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 434
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10
<210> 435
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 435
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10
<210> 436
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 436
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10
<210> 437
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 437
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 438
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 438
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10
<210> 439
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 439
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 440
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 440
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10
<210> 441
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 441
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10
<210> 442
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 442
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10
<210> 443
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 443
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10
<210> 444
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 444
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10
<210> 445
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 445
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 446
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 446
Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10
<210> 447
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 447
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 448
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 448
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10
<210> 449
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 449
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10
<210> 450
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 450
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10
<210> 451
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 451
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10
<210> 452
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 452
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10
<210> 453
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 453
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10
<210> 454
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 454
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10
<210> 455
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 455
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 456
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 456
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10
<210> 457
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 457
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10
<210> 458
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 458
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 459
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 459
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 460
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 460
Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10
<210> 461
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 461
Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10
<210> 462
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 462
Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 463
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 463
Ser Leu Trp Cys Leu Cys Ser Asn His
1 5
<210> 464
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 464
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala
1 5 10
<210> 465
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 465
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
1 5 10
<210> 466
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 466
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 467
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 467
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro
1 5 10
<210> 468
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 468
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5 10
<210> 469
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 469
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10
<210> 470
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 470
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10
<210> 471
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 471
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10
<210> 472
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 472
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10
<210> 473
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 473
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10
<210> 474
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 474
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10
<210> 475
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 475
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 476
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 476
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10
<210> 477
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 477
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10
<210> 478
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 478
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10
<210> 479
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 479
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10
<210> 480
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 480
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10
<210> 481
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 481
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 482
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 482
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10
<210> 483
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 483
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10
<210> 484
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 484
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10
<210> 485
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 485
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10
<210> 486
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 486
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10
<210> 487
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 487
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10
<210> 488
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 488
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10
<210> 489
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 489
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 490
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 490
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10
<210> 491
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 491
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 492
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 492
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10
<210> 493
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 493
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10
<210> 494
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 494
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10
<210> 495
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 495
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10
<210> 496
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 496
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10
<210> 497
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 497
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 498
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 498
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10
<210> 499
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 499
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 500
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 500
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10
<210> 501
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 501
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10
<210> 502
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 502
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10
<210> 503
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 503
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10
<210> 504
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 504
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10
<210> 505
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 505
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10
<210> 506
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 506
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10
<210> 507
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 507
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 508
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 508
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10
<210> 509
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 509
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10
<210> 510
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 510
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 511
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 511
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 512
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 512
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10
<210> 513
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 513
Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10
<210> 514
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 514
Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 515
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 515
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
1 5 10
<210> 516
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 516
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 517
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 517
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro
1 5 10
<210> 518
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 518
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5 10
<210> 519
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 519
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10
<210> 520
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 520
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10
<210> 521
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 521
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10
<210> 522
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 522
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10
<210> 523
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 523
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10
<210> 524
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 524
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10
<210> 525
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 525
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 526
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 526
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10
<210> 527
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 527
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10
<210> 528
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 528
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10
<210> 529
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 529
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10
<210> 530
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 530
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10
<210> 531
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 531
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 532
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 532
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10
<210> 533
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 533
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10
<210> 534
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 534
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10
<210> 535
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 535
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10
<210> 536
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 536
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10
<210> 537
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 537
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10
<210> 538
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 538
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10
<210> 539
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 539
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 540
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 540
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10
<210> 541
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 541
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 542
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 542
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10
<210> 543
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 543
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10
<210> 544
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 544
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10
<210> 545
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 545
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10
<210> 546
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 546
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10
<210> 547
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 547
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 548
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 548
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10
<210> 549
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 549
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 550
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 550
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10
<210> 551
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 551
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10
<210> 552
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 552
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10
<210> 553
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 553
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10
<210> 554
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 554
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10
<210> 555
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 555
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10
<210> 556
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 556
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10
<210> 557
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 557
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 558
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 558
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10
<210> 559
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 559
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10
<210> 560
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 560
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 561
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 561
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 562
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 562
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10
<210> 563
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 563
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10
<210> 564
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 564
Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 565
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 565
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 566
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 566
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro
1 5 10
<210> 567
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 567
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5 10
<210> 568
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 568
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10
<210> 569
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 569
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10
<210> 570
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 570
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10
<210> 571
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 571
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10
<210> 572
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 572
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10
<210> 573
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 573
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10
<210> 574
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 574
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 575
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 575
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10
<210> 576
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 576
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10
<210> 577
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 577
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10
<210> 578
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 578
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10
<210> 579
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 579
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10
<210> 580
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 580
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 581
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 581
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10
<210> 582
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 582
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10
<210> 583
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 583
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10
<210> 584
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 584
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10
<210> 585
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 585
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10
<210> 586
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 586
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10
<210> 587
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 587
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10
<210> 588
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 588
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 589
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 589
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10
<210> 590
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 590
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 591
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 591
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10
<210> 592
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 592
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10
<210> 593
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 593
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10
<210> 594
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 594
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10
<210> 595
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 595
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10
<210> 596
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 596
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 597
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 597
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10
<210> 598
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 598
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 599
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 599
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10
<210> 600
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 600
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10
<210> 601
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 601
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10
<210> 602
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 602
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10
<210> 603
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 603
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10
<210> 604
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 604
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10
<210> 605
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 605
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10
<210> 606
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 606
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 607
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 607
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10
<210> 608
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 608
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10
<210> 609
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 609
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 610
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 610
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 611
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 611
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10
<210> 612
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 612
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10
<210> 613
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 613
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 614
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 614
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro
1 5 10
<210> 615
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 615
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5 10
<210> 616
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 616
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10
<210> 617
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 617
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10
<210> 618
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 618
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10
<210> 619
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 619
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10
<210> 620
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 620
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10
<210> 621
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 621
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10
<210> 622
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 622
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 623
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 623
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10
<210> 624
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 624
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10
<210> 625
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 625
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10
<210> 626
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 626
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10
<210> 627
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 627
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10
<210> 628
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 628
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 629
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 629
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10
<210> 630
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 630
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10
<210> 631
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 631
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10
<210> 632
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 632
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10
<210> 633
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 633
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10
<210> 634
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 634
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10
<210> 635
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 635
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10
<210> 636
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 636
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 637
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 637
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10
<210> 638
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 638
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 639
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 639
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10
<210> 640
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 640
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10
<210> 641
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 641
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10
<210> 642
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 642
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10
<210> 643
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 643
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10
<210> 644
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 644
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 645
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 645
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10
<210> 646
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 646
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 647
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 647
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10
<210> 648
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 648
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10
<210> 649
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 649
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10
<210> 650
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 650
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10
<210> 651
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 651
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10
<210> 652
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 652
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10
<210> 653
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 653
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10
<210> 654
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 654
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 655
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 655
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10
<210> 656
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 656
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10
<210> 657
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 657
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 658
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 658
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 659
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 659
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10
<210> 660
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 660
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10
<210> 661
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 661
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 662
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 662
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
1 5 10 15
<210> 663
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 663
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
<210> 664
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 664
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
<210> 665
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 665
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
<210> 666
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 666
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
<210> 667
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 667
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
<210> 668
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 668
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
<210> 669
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 669
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
<210> 670
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 670
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
<210> 671
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 671
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
<210> 672
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 672
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
<210> 673
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 673
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
<210> 674
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 674
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
<210> 675
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 675
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
<210> 676
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 676
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
<210> 677
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 677
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
<210> 678
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 678
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
<210> 679
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 679
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
<210> 680
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 680
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
<210> 681
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 681
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
<210> 682
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 682
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
<210> 683
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 683
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
<210> 684
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 684
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
<210> 685
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 685
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
<210> 686
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 686
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
<210> 687
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 687
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
<210> 688
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 688
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
<210> 689
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 689
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
<210> 690
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 690
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
<210> 691
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 691
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 692
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 692
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
<210> 693
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 693
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
<210> 694
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 694
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
<210> 695
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 695
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
<210> 696
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 696
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
<210> 697
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 697
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
<210> 698
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 698
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
<210> 699
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 699
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
<210> 700
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 700
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
<210> 701
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 701
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
<210> 702
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 702
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
<210> 703
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 703
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
<210> 704
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 704
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10 15
<210> 705
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 705
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
<210> 706
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 706
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10 15
<210> 707
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 707
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10 15
<210> 708
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 708
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10 15
<210> 709
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 709
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
<210> 710
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 710
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
<210> 711
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 711
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
<210> 712
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 712
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
<210> 713
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 713
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
<210> 714
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 714
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
<210> 715
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 715
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
<210> 716
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 716
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
<210> 717
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 717
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
<210> 718
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 718
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
<210> 719
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 719
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
<210> 720
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 720
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
<210> 721
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 721
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
<210> 722
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 722
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
<210> 723
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 723
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
<210> 724
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 724
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
<210> 725
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 725
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
<210> 726
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 726
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
<210> 727
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 727
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
<210> 728
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 728
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
<210> 729
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 729
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
<210> 730
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 730
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
<210> 731
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 731
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
<210> 732
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 732
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
<210> 733
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 733
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
<210> 734
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 734
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
<210> 735
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 735
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
<210> 736
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 736
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
<210> 737
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 737
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 738
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 738
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
<210> 739
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 739
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
<210> 740
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 740
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
<210> 741
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 741
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
<210> 742
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 742
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
<210> 743
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 743
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
<210> 744
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 744
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
<210> 745
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 745
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
<210> 746
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 746
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
<210> 747
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 747
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
<210> 748
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 748
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
<210> 749
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 749
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
<210> 750
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 750
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10 15
<210> 751
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 751
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
<210> 752
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 752
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10 15
<210> 753
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 753
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10 15
<210> 754
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 754
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10 15
<210> 755
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 755
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro
<210> 756
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 756
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe
<210> 757
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 757
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp
<210> 758
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 758
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu
<210> 759
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 759
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His
<210> 760
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 760
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe
<210> 761
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 761
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys
<210> 762
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 762
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg
<210> 763
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 763
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser
<210> 764
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 764
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser
<210> 765
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 765
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile
<210> 766
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 766
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met
<210> 767
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 767
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys
<210> 768
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 768
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro
<210> 769
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 769
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys
<210> 770
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 770
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg
<210> 771
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 771
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp
<210> 772
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 772
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly
<210> 773
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 773
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr
<210> 774
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 774
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met
<210> 775
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 775
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe
<210> 776
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 776
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu
<210> 777
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 777
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys
<210> 778
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 778
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala
<210> 779
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 779
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu
<210> 780
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 780
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser
<210> 781
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 781
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys
<210> 782
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 782
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile
<210> 783
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 783
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met
<210> 784
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 784
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe
<210> 785
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 785
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala
<210> 786
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 786
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr
<210> 787
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 787
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu
<210> 788
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 788
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln
<210> 789
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 789
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg
<210> 790
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 790
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser
<210> 791
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 791
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser
<210> 792
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 792
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu
<210> 793
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 793
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp
<210> 794
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 794
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
Cys
<210> 795
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 795
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu
<210> 796
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 796
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10 15
Cys
<210> 797
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 797
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
Ser
<210> 798
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 798
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10 15
Asn
<210> 799
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 799
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10 15
His
<210> 800
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 800
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe
<210> 801
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 801
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp
<210> 802
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 802
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu
<210> 803
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 803
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 804
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 804
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe
<210> 805
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 805
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys
<210> 806
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 806
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg
<210> 807
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 807
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser
<210> 808
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 808
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser
<210> 809
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 809
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile
<210> 810
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 810
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met
<210> 811
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 811
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys
<210> 812
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 812
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro
<210> 813
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 813
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys
<210> 814
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 814
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg
<210> 815
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 815
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp
<210> 816
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 816
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly
<210> 817
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 817
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr
<210> 818
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 818
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met
<210> 819
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 819
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe
<210> 820
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 820
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu
<210> 821
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 821
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys
<210> 822
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 822
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala
<210> 823
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 823
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu
<210> 824
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 824
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser
<210> 825
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 825
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys
<210> 826
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 826
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile
<210> 827
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 827
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met
<210> 828
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 828
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe
<210> 829
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 829
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala
<210> 830
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 830
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr
<210> 831
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 831
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu
<210> 832
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 832
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln
<210> 833
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 833
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg
<210> 834
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 834
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser
<210> 835
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 835
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser
<210> 836
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 836
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu
<210> 837
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 837
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp
<210> 838
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 838
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys
<210> 839
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 839
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
Cys Leu
<210> 840
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 840
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys
<210> 841
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 841
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10 15
Cys Ser
<210> 842
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 842
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
Ser Asn
<210> 843
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 843
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
1 5 10 15
Asn His
<210> 844
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 844
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp
<210> 845
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 845
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu
<210> 846
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 846
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His
<210> 847
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 847
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe
<210> 848
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 848
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys
<210> 849
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 849
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg
<210> 850
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 850
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser
<210> 851
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 851
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser
<210> 852
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 852
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile
<210> 853
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 853
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met
<210> 854
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 854
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys
<210> 855
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 855
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro
<210> 856
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 856
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys
<210> 857
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 857
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg
<210> 858
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 858
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp
<210> 859
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 859
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly
<210> 860
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 860
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr
<210> 861
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 861
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met
<210> 862
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 862
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe
<210> 863
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 863
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu
<210> 864
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 864
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys
<210> 865
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 865
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala
<210> 866
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 866
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu
<210> 867
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 867
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser
<210> 868
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 868
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys
<210> 869
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 869
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile
<210> 870
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 870
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met
<210> 871
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 871
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe
<210> 872
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 872
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala
<210> 873
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 873
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr
<210> 874
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 874
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu
<210> 875
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 875
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln
<210> 876
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 876
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg
<210> 877
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 877
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser
<210> 878
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 878
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser
<210> 879
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 879
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu
<210> 880
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 880
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp
<210> 881
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 881
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys
<210> 882
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 882
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu
<210> 883
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 883
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
Cys Leu Cys
<210> 884
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 884
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys Ser
<210> 885
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 885
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10 15
Cys Ser Asn
<210> 886
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 886
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
Ser Asn His
<210> 887
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 887
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu
20
<210> 888
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 888
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His
20
<210> 889
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 889
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe
20
<210> 890
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 890
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys
20
<210> 891
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 891
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg
20
<210> 892
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 892
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser
20
<210> 893
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 893
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser
20
<210> 894
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 894
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile
20
<210> 895
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 895
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met
20
<210> 896
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 896
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys
20
<210> 897
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 897
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro
20
<210> 898
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 898
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys
20
<210> 899
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 899
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg
20
<210> 900
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 900
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp
20
<210> 901
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 901
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly
20
<210> 902
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 902
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr
20
<210> 903
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 903
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met
20
<210> 904
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 904
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe
20
<210> 905
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 905
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu
20
<210> 906
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 906
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys
20
<210> 907
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 907
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala
20
<210> 908
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 908
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu
20
<210> 909
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 909
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser
20
<210> 910
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 910
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys
20
<210> 911
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 911
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile
20
<210> 912
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 912
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met
20
<210> 913
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 913
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe
20
<210> 914
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 914
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala
20
<210> 915
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 915
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr
20
<210> 916
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 916
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu
20
<210> 917
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 917
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln
20
<210> 918
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 918
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg
20
<210> 919
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 919
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser
20
<210> 920
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 920
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser
20
<210> 921
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 921
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu
20
<210> 922
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 922
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp
20
<210> 923
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 923
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys
20
<210> 924
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 924
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys Leu
20
<210> 925
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 925
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys
20
<210> 926
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 926
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
Cys Leu Cys Ser
20
<210> 927
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 927
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys Ser Asn
20
<210> 928
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 928
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10 15
Cys Ser Asn His
20
<210> 929
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 929
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 930
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 930
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe
20
<210> 931
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 931
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys
20
<210> 932
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 932
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg
20
<210> 933
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 933
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser
20
<210> 934
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 934
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser
20
<210> 935
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 935
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile
20
<210> 936
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 936
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met
20
<210> 937
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 937
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys
20
<210> 938
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 938
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro
20
<210> 939
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 939
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys
20
<210> 940
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 940
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg
20
<210> 941
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 941
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp
20
<210> 942
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 942
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly
20
<210> 943
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 943
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr
20
<210> 944
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 944
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met
20
<210> 945
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 945
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe
20
<210> 946
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 946
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu
20
<210> 947
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 947
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys
20
<210> 948
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 948
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala
20
<210> 949
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 949
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu
20
<210> 950
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 950
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser
20
<210> 951
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 951
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys
20
<210> 952
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 952
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile
20
<210> 953
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 953
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met
20
<210> 954
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 954
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe
20
<210> 955
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 955
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala
20
<210> 956
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 956
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr
20
<210> 957
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 957
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu
20
<210> 958
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 958
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln
20
<210> 959
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 959
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg
20
<210> 960
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 960
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser
20
<210> 961
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 961
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser
20
<210> 962
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 962
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu
20
<210> 963
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 963
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp
20
<210> 964
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 964
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp Cys
20
<210> 965
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 965
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu
20
<210> 966
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 966
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys Leu Cys
20
<210> 967
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 967
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser
20
<210> 968
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 968
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
Cys Leu Cys Ser Asn
20
<210> 969
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 969
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys Ser Asn His
20
<210> 970
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 970
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe
20
<210> 971
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 971
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys
20
<210> 972
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 972
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg
20
<210> 973
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 973
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser
20
<210> 974
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 974
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser
20
<210> 975
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 975
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile
20
<210> 976
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 976
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met
20
<210> 977
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 977
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys
20
<210> 978
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 978
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro
20
<210> 979
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 979
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys
20
<210> 980
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 980
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg
20
<210> 981
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 981
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp
20
<210> 982
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 982
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly
20
<210> 983
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 983
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr
20
<210> 984
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 984
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met
20
<210> 985
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 985
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe
20
<210> 986
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 986
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu
20
<210> 987
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 987
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys
20
<210> 988
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 988
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala
20
<210> 989
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 989
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu
20
<210> 990
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 990
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser
20
<210> 991
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 991
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys
20
<210> 992
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 992
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile
20
<210> 993
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 993
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met
20
<210> 994
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 994
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe
20
<210> 995
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 995
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala
20
<210> 996
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 996
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr
20
<210> 997
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 997
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu
20
<210> 998
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 998
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln
20
<210> 999
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 999
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg
20
<210> 1000
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1000
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser
20
<210> 1001
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1001
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser
20
<210> 1002
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1002
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu
20
<210> 1003
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1003
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp
20
<210> 1004
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1004
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys
20
<210> 1005
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1005
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp Cys Leu
20
<210> 1006
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1006
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu Cys
20
<210> 1007
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1007
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys Leu Cys Ser
20
<210> 1008
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1008
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser Asn
20
<210> 1009
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 1009
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
1 5 10 15
Cys Leu Cys Ser Asn His
20
<210> 1010
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1010
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys
20
<210> 1011
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1011
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg
20
<210> 1012
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1012
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser
20
<210> 1013
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1013
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser
20
<210> 1014
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1014
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile
20
<210> 1015
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1015
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met
20
<210> 1016
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1016
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys
20
<210> 1017
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1017
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro
20
<210> 1018
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1018
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys
20
<210> 1019
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1019
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg
20
<210> 1020
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1020
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp
20
<210> 1021
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1021
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly
20
<210> 1022
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1022
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr
20
<210> 1023
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1023
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met
20
<210> 1024
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1024
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe
20
<210> 1025
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1025
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu
20
<210> 1026
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1026
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys
20
<210> 1027
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1027
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala
20
<210> 1028
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1028
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu
20
<210> 1029
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1029
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser
20
<210> 1030
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1030
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys
20
<210> 1031
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1031
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile
20
<210> 1032
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1032
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met
20
<210> 1033
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1033
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe
20
<210> 1034
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1034
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala
20
<210> 1035
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1035
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr
20
<210> 1036
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1036
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu
20
<210> 1037
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1037
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln
20
<210> 1038
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1038
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg
20
<210> 1039
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1039
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser
20
<210> 1040
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1040
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser
20
<210> 1041
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1041
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu
20
<210> 1042
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1042
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp
20
<210> 1043
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1043
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp Cys
20
<210> 1044
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1044
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu
20
<210> 1045
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1045
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp Cys Leu Cys
20
<210> 1046
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1046
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu Cys Ser
20
<210> 1047
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1047
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys Leu Cys Ser Asn
20
<210> 1048
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 1048
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser Asn His
20
<210> 1049
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1049
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg
20
<210> 1050
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1050
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser
20
<210> 1051
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1051
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser
20
<210> 1052
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1052
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile
20
<210> 1053
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1053
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met
20
<210> 1054
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1054
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys
20
<210> 1055
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1055
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro
20
<210> 1056
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1056
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys
20
<210> 1057
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1057
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg
20
<210> 1058
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1058
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp
20
<210> 1059
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1059
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly
20
<210> 1060
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1060
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr
20
<210> 1061
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1061
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met
20
<210> 1062
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1062
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe
20
<210> 1063
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1063
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu
20
<210> 1064
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1064
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys
20
<210> 1065
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1065
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala
20
<210> 1066
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1066
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu
20
<210> 1067
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1067
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser
20
<210> 1068
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1068
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys
20
<210> 1069
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1069
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile
20
<210> 1070
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1070
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met
20
<210> 1071
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1071
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe
20
<210> 1072
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1072
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala
20
<210> 1073
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1073
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr
20
<210> 1074
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1074
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu
20
<210> 1075
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1075
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln
20
<210> 1076
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1076
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg
20
<210> 1077
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1077
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser
20
<210> 1078
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1078
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser
20
<210> 1079
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1079
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu
20
<210> 1080
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1080
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp
20
<210> 1081
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1081
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp Cys
20
<210> 1082
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1082
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp Cys Leu
20
<210> 1083
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1083
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu Cys
20
<210> 1084
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1084
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp Cys Leu Cys Ser
20
<210> 1085
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1085
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu Cys Ser Asn
20
<210> 1086
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 1086
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys Leu Cys Ser Asn His
20
<210> 1087
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1087
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser
20 25
<210> 1088
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1088
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser
20 25
<210> 1089
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1089
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile
20 25
<210> 1090
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1090
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met
20 25
<210> 1091
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1091
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys
20 25
<210> 1092
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1092
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro
20 25
<210> 1093
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1093
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25
<210> 1094
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1094
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25
<210> 1095
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1095
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 1096
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1096
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25
<210> 1097
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1097
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25
<210> 1098
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1098
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25
<210> 1099
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1099
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25
<210> 1100
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1100
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25
<210> 1101
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1101
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25
<210> 1102
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1102
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25
<210> 1103
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1103
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25
<210> 1104
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1104
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25
<210> 1105
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1105
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 1106
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1106
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 1107
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1107
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25
<210> 1108
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1108
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25
<210> 1109
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1109
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25
<210> 1110
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1110
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25
<210> 1111
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1111
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25
<210> 1112
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1112
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25
<210> 1113
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1113
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25
<210> 1114
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1114
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25
<210> 1115
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1115
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25
<210> 1116
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1116
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25
<210> 1117
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1117
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25
<210> 1118
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1118
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25
<210> 1119
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1119
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 1120
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1120
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25
<210> 1121
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1121
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25
<210> 1122
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1122
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25
<210> 1123
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 1123
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu Cys Ser Asn His
20 25
<210> 1124
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1124
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser
20 25
<210> 1125
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1125
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile
20 25
<210> 1126
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1126
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met
20 25
<210> 1127
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1127
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys
20 25
<210> 1128
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1128
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro
20 25
<210> 1129
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1129
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25
<210> 1130
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1130
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25
<210> 1131
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1131
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 1132
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1132
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25
<210> 1133
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1133
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25
<210> 1134
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1134
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25
<210> 1135
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1135
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25
<210> 1136
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1136
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25
<210> 1137
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1137
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25
<210> 1138
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1138
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25
<210> 1139
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1139
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25
<210> 1140
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1140
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25
<210> 1141
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1141
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 1142
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1142
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 1143
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1143
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25
<210> 1144
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1144
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25
<210> 1145
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1145
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25
<210> 1146
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1146
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25
<210> 1147
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1147
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25
<210> 1148
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1148
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25
<210> 1149
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1149
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25
<210> 1150
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1150
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25
<210> 1151
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1151
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25
<210> 1152
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1152
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25
<210> 1153
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1153
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25
<210> 1154
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1154
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25
<210> 1155
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1155
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 1156
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1156
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25
<210> 1157
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1157
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25
<210> 1158
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1158
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25
<210> 1159
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 1159
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25
<210> 1160
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1160
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
20 25
<210> 1161
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1161
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
20 25
<210> 1162
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1162
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
20 25
<210> 1163
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1163
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
20 25
<210> 1164
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1164
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25
<210> 1165
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1165
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25
<210> 1166
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1166
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 1167
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1167
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25
<210> 1168
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1168
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25
<210> 1169
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1169
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25
<210> 1170
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1170
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25
<210> 1171
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1171
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25
<210> 1172
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1172
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25
<210> 1173
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1173
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25
<210> 1174
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1174
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25
<210> 1175
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1175
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25
<210> 1176
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1176
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 1177
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1177
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 1178
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1178
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25
<210> 1179
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1179
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25
<210> 1180
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1180
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25
<210> 1181
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1181
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25
<210> 1182
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1182
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25
<210> 1183
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1183
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25
<210> 1184
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1184
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25
<210> 1185
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1185
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25
<210> 1186
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1186
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25
<210> 1187
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1187
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25
<210> 1188
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1188
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25
<210> 1189
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1189
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25
<210> 1190
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1190
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 1191
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1191
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25
<210> 1192
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1192
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25
<210> 1193
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1193
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25
<210> 1194
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 1194
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25
<210> 1195
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1195
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
20 25
<210> 1196
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1196
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
20 25
<210> 1197
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1197
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
20 25
<210> 1198
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1198
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25
<210> 1199
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1199
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25
<210> 1200
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1200
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 1201
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1201
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25
<210> 1202
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1202
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25
<210> 1203
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1203
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25
<210> 1204
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1204
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25
<210> 1205
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1205
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25
<210> 1206
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1206
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25
<210> 1207
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1207
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25
<210> 1208
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1208
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25
<210> 1209
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1209
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25
<210> 1210
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1210
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 1211
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1211
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 1212
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1212
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25
<210> 1213
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1213
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25
<210> 1214
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1214
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25
<210> 1215
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1215
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25
<210> 1216
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1216
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25
<210> 1217
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1217
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25
<210> 1218
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1218
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25
<210> 1219
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1219
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25
<210> 1220
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1220
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25
<210> 1221
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1221
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25
<210> 1222
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1222
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25
<210> 1223
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1223
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25
<210> 1224
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1224
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 1225
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1225
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25
<210> 1226
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1226
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25
<210> 1227
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1227
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25
<210> 1228
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 1228
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5 10 15
Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25
<210> 1229
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1229
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
20 25
<210> 1230
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1230
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
20 25
<210> 1231
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1231
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25
<210> 1232
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1232
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25
<210> 1233
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1233
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 1234
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1234
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25
<210> 1235
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1235
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25
<210> 1236
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1236
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25
<210> 1237
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1237
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25
<210> 1238
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1238
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25
<210> 1239
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1239
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25
<210> 1240
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1240
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25
<210> 1241
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1241
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25
<210> 1242
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1242
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25
<210> 1243
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1243
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 1244
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1244
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 1245
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1245
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25
<210> 1246
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1246
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25
<210> 1247
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1247
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25
<210> 1248
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1248
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25
<210> 1249
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1249
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25
<210> 1250
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1250
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25
<210> 1251
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1251
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25
<210> 1252
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1252
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25
<210> 1253
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1253
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25
<210> 1254
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1254
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25
<210> 1255
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1255
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25
<210> 1256
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1256
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25
<210> 1257
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1257
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 1258
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1258
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25
<210> 1259
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1259
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25
<210> 1260
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1260
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25
<210> 1261
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 1261
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25
<210> 1262
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1262
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
20 25 30
<210> 1263
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1263
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25 30
<210> 1264
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1264
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
<210> 1265
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1265
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
<210> 1266
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1266
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
<210> 1267
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1267
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
<210> 1268
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1268
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
<210> 1269
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1269
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
<210> 1270
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1270
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
<210> 1271
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1271
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
<210> 1272
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1272
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
<210> 1273
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1273
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
<210> 1274
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1274
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
<210> 1275
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1275
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
<210> 1276
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1276
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
<210> 1277
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1277
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
<210> 1278
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1278
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
<210> 1279
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1279
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
<210> 1280
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1280
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
<210> 1281
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1281
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
<210> 1282
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1282
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
<210> 1283
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1283
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
<210> 1284
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1284
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
<210> 1285
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1285
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
<210> 1286
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1286
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
<210> 1287
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1287
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
<210> 1288
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1288
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
<210> 1289
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1289
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
<210> 1290
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1290
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25 30
<210> 1291
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1291
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25 30
<210> 1292
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1292
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
<210> 1293
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 1293
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
1 5 10 15
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25 30
<210> 1294
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1294
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
20 25 30
<210> 1295
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1295
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
<210> 1296
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1296
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
<210> 1297
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1297
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
<210> 1298
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1298
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
<210> 1299
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1299
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
<210> 1300
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1300
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
<210> 1301
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1301
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
<210> 1302
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1302
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
<210> 1303
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1303
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
<210> 1304
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1304
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
<210> 1305
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1305
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
<210> 1306
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1306
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
<210> 1307
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1307
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
<210> 1308
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1308
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
<210> 1309
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1309
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
<210> 1310
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1310
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
<210> 1311
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1311
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
<210> 1312
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1312
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
<210> 1313
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1313
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
<210> 1314
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1314
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
<210> 1315
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1315
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
<210> 1316
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1316
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
<210> 1317
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1317
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
<210> 1318
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1318
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
<210> 1319
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1319
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
<210> 1320
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1320
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
<210> 1321
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1321
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25 30
<210> 1322
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1322
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25 30
<210> 1323
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1323
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
<210> 1324
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 1324
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25 30
<210> 1325
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1325
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
<210> 1326
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1326
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
<210> 1327
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1327
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
<210> 1328
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1328
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
<210> 1329
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1329
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
<210> 1330
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1330
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
<210> 1331
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1331
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
<210> 1332
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1332
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
<210> 1333
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1333
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
<210> 1334
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1334
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
<210> 1335
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1335
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
<210> 1336
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1336
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
<210> 1337
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1337
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
<210> 1338
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1338
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
<210> 1339
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1339
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
<210> 1340
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1340
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
<210> 1341
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1341
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
<210> 1342
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1342
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
<210> 1343
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1343
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
<210> 1344
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1344
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
<210> 1345
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1345
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
<210> 1346
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1346
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
<210> 1347
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1347
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
<210> 1348
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1348
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
<210> 1349
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1349
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
<210> 1350
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1350
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
<210> 1351
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1351
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25 30
<210> 1352
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1352
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25 30
<210> 1353
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1353
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
<210> 1354
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 1354
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5 10 15
Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
20 25 30
<210> 1355
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1355
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp
<210> 1356
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1356
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly
<210> 1357
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1357
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr
<210> 1358
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1358
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met
<210> 1359
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1359
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe
<210> 1360
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1360
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu
<210> 1361
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1361
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys
<210> 1362
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1362
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala
<210> 1363
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1363
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu
<210> 1364
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1364
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser
<210> 1365
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1365
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys
<210> 1366
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1366
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile
<210> 1367
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1367
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met
<210> 1368
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1368
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe
<210> 1369
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1369
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala
<210> 1370
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1370
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr
<210> 1371
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1371
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu
<210> 1372
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1372
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln
<210> 1373
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1373
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg
<210> 1374
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1374
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser
<210> 1375
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1375
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser
<210> 1376
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1376
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu
<210> 1377
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1377
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp
<210> 1378
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1378
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
Cys
<210> 1379
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1379
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
Leu
<210> 1380
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1380
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
Cys
<210> 1381
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1381
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25 30
Ser
<210> 1382
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1382
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25 30
Asn
<210> 1383
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 1383
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 1384
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1384
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly
<210> 1385
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1385
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr
<210> 1386
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1386
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met
<210> 1387
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1387
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe
<210> 1388
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1388
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu
<210> 1389
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1389
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys
<210> 1390
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1390
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala
<210> 1391
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1391
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu
<210> 1392
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1392
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser
<210> 1393
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1393
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys
<210> 1394
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1394
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile
<210> 1395
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1395
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met
<210> 1396
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1396
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe
<210> 1397
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1397
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala
<210> 1398
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1398
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr
<210> 1399
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1399
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu
<210> 1400
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1400
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln
<210> 1401
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1401
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg
<210> 1402
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1402
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser
<210> 1403
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1403
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser
<210> 1404
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1404
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu
<210> 1405
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1405
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp
<210> 1406
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1406
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp Cys
<210> 1407
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1407
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
Cys Leu
<210> 1408
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1408
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
Leu Cys
<210> 1409
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1409
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
Cys Ser
<210> 1410
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1410
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25 30
Ser Asn
<210> 1411
<211> 34
<212> БЕЛОК
<213> Homo sapiens
<400> 1411
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5 10 15
Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser
20 25 30
Asn His
<210> 1412
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1412
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr
35
<210> 1413
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1413
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr Met
35
<210> 1414
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1414
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met Phe
35
<210> 1415
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1415
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe Leu
35
<210> 1416
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1416
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu Lys
35
<210> 1417
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1417
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys Ala
35
<210> 1418
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1418
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala Glu
35
<210> 1419
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1419
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu Ser
35
<210> 1420
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1420
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser Lys
35
<210> 1421
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1421
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys Ile
35
<210> 1422
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1422
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile Met
35
<210> 1423
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1423
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met Phe
35
<210> 1424
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1424
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe Ala
35
<210> 1425
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1425
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala Thr
35
<210> 1426
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1426
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr Leu
35
<210> 1427
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1427
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu Gln
35
<210> 1428
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1428
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln Arg
35
<210> 1429
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1429
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg Ser
35
<210> 1430
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1430
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser
35
<210> 1431
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1431
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser Leu
35
<210> 1432
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1432
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu Trp
35
<210> 1433
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1433
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp Cys
35
<210> 1434
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1434
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp Cys Leu
35
<210> 1435
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1435
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
Cys Leu Cys
35
<210> 1436
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1436
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
Leu Cys Ser
35
<210> 1437
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1437
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
Cys Ser Asn
35
<210> 1438
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1438
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
1 5 10 15
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
20 25 30
Ser Asn His
35
<210> 1439
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1439
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr Met
35
<210> 1440
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1440
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr Met Phe
35
<210> 1441
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1441
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met Phe Leu
35
<210> 1442
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1442
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe Leu Lys
35
<210> 1443
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1443
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu Lys Ala
35
<210> 1444
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1444
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys Ala Glu
35
<210> 1445
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1445
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala Glu Ser
35
<210> 1446
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1446
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu Ser Lys
35
<210> 1447
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1447
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser Lys Ile
35
<210> 1448
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1448
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys Ile Met
35
<210> 1449
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1449
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile Met Phe
35
<210> 1450
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1450
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met Phe Ala
35
<210> 1451
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1451
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe Ala Thr
35
<210> 1452
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1452
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala Thr Leu
35
<210> 1453
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1453
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr Leu Gln
35
<210> 1454
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1454
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu Gln Arg
35
<210> 1455
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1455
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln Arg Ser
35
<210> 1456
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1456
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg Ser Ser
35
<210> 1457
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1457
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu
35
<210> 1458
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1458
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser Leu Trp
35
<210> 1459
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1459
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu Trp Cys
35
<210> 1460
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1460
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp Cys Leu
35
<210> 1461
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1461
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp Cys Leu Cys
35
<210> 1462
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1462
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
Cys Leu Cys Ser
35
<210> 1463
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1463
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
Leu Cys Ser Asn
35
<210> 1464
<211> 36
<212> БЕЛОК
<213> Homo sapiens
<400> 1464
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
1 5 10 15
Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25 30
Cys Ser Asn His
35
<210> 1465
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1465
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr Met Phe
35
<210> 1466
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1466
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr Met Phe Leu
35
<210> 1467
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1467
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met Phe Leu Lys
35
<210> 1468
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1468
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe Leu Lys Ala
35
<210> 1469
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1469
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu Lys Ala Glu
35
<210> 1470
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1470
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys Ala Glu Ser
35
<210> 1471
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1471
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala Glu Ser Lys
35
<210> 1472
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1472
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu Ser Lys Ile
35
<210> 1473
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1473
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser Lys Ile Met
35
<210> 1474
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1474
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys Ile Met Phe
35
<210> 1475
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1475
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile Met Phe Ala
35
<210> 1476
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1476
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met Phe Ala Thr
35
<210> 1477
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1477
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe Ala Thr Leu
35
<210> 1478
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1478
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala Thr Leu Gln
35
<210> 1479
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1479
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr Leu Gln Arg
35
<210> 1480
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1480
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu Gln Arg Ser
35
<210> 1481
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1481
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln Arg Ser Ser
35
<210> 1482
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1482
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg Ser Ser Leu
35
<210> 1483
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1483
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu Trp
35
<210> 1484
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1484
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser Leu Trp Cys
35
<210> 1485
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1485
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu Trp Cys Leu
35
<210> 1486
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1486
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp Cys Leu Cys
35
<210> 1487
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1487
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp Cys Leu Cys Ser
35
<210> 1488
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1488
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
Cys Leu Cys Ser Asn
35
<210> 1489
<211> 37
<212> БЕЛОК
<213> Homo sapiens
<400> 1489
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
20 25 30
Leu Cys Ser Asn His
35
<210> 1490
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1490
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr Met Phe Leu
35
<210> 1491
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1491
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr Met Phe Leu Lys
35
<210> 1492
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1492
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met Phe Leu Lys Ala
35
<210> 1493
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1493
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe Leu Lys Ala Glu
35
<210> 1494
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1494
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu Lys Ala Glu Ser
35
<210> 1495
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1495
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys Ala Glu Ser Lys
35
<210> 1496
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1496
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala Glu Ser Lys Ile
35
<210> 1497
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1497
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu Ser Lys Ile Met
35
<210> 1498
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1498
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser Lys Ile Met Phe
35
<210> 1499
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1499
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys Ile Met Phe Ala
35
<210> 1500
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1500
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile Met Phe Ala Thr
35
<210> 1501
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1501
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met Phe Ala Thr Leu
35
<210> 1502
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1502
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe Ala Thr Leu Gln
35
<210> 1503
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1503
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala Thr Leu Gln Arg
35
<210> 1504
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1504
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr Leu Gln Arg Ser
35
<210> 1505
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1505
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu Gln Arg Ser Ser
35
<210> 1506
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1506
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln Arg Ser Ser Leu
35
<210> 1507
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1507
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg Ser Ser Leu Trp
35
<210> 1508
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1508
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu Trp Cys
35
<210> 1509
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1509
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser Leu Trp Cys Leu
35
<210> 1510
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1510
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu Trp Cys Leu Cys
35
<210> 1511
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1511
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp Cys Leu Cys Ser
35
<210> 1512
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1512
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp Cys Leu Cys Ser Asn
35
<210> 1513
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 1513
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
1 5 10 15
Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp
20 25 30
Cys Leu Cys Ser Asn His
35
<210> 1514
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1514
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr Met Phe Leu Lys
35
<210> 1515
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1515
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr Met Phe Leu Lys Ala
35
<210> 1516
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1516
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met Phe Leu Lys Ala Glu
35
<210> 1517
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1517
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe Leu Lys Ala Glu Ser
35
<210> 1518
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1518
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu Lys Ala Glu Ser Lys
35
<210> 1519
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1519
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys Ala Glu Ser Lys Ile
35
<210> 1520
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1520
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala Glu Ser Lys Ile Met
35
<210> 1521
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1521
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu Ser Lys Ile Met Phe
35
<210> 1522
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1522
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser Lys Ile Met Phe Ala
35
<210> 1523
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1523
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys Ile Met Phe Ala Thr
35
<210> 1524
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1524
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile Met Phe Ala Thr Leu
35
<210> 1525
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1525
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met Phe Ala Thr Leu Gln
35
<210> 1526
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1526
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe Ala Thr Leu Gln Arg
35
<210> 1527
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1527
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala Thr Leu Gln Arg Ser
35
<210> 1528
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1528
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr Leu Gln Arg Ser Ser
35
<210> 1529
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1529
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu Gln Arg Ser Ser Leu
35
<210> 1530
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1530
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln Arg Ser Ser Leu Trp
35
<210> 1531
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1531
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg Ser Ser Leu Trp Cys
35
<210> 1532
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1532
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu Trp Cys Leu
35
<210> 1533
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1533
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser Leu Trp Cys Leu Cys
35
<210> 1534
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1534
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu Trp Cys Leu Cys Ser
35
<210> 1535
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1535
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp Cys Leu Cys Ser Asn
35
<210> 1536
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 1536
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10 15
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
20 25 30
Trp Cys Leu Cys Ser Asn His
35
<210> 1537
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1537
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
20 25 30
Asp Gly Tyr Met Phe Leu Lys Ala
35 40
<210> 1538
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1538
Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro
1 5 10 15
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25 30
Gly Tyr Met Phe Leu Lys Ala Glu
35 40
<210> 1539
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1539
Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe
1 5 10 15
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
20 25 30
Tyr Met Phe Leu Lys Ala Glu Ser
35 40
<210> 1540
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1540
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
20 25 30
Met Phe Leu Lys Ala Glu Ser Lys
35 40
<210> 1541
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1541
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
1 5 10 15
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
20 25 30
Phe Leu Lys Ala Glu Ser Lys Ile
35 40
<210> 1542
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1542
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
1 5 10 15
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
20 25 30
Leu Lys Ala Glu Ser Lys Ile Met
35 40
<210> 1543
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1543
Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10 15
Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
20 25 30
Lys Ala Glu Ser Lys Ile Met Phe
35 40
<210> 1544
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1544
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys
20 25 30
Ala Glu Ser Lys Ile Met Phe Ala
35 40
<210> 1545
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1545
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
20 25 30
Glu Ser Lys Ile Met Phe Ala Thr
35 40
<210> 1546
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1546
Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser
1 5 10 15
Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu
20 25 30
Ser Lys Ile Met Phe Ala Thr Leu
35 40
<210> 1547
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1547
Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser
1 5 10 15
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser
20 25 30
Lys Ile Met Phe Ala Thr Leu Gln
35 40
<210> 1548
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1548
Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile
1 5 10 15
Met Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25 30
Ile Met Phe Ala Thr Leu Gln Arg
35 40
<210> 1549
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1549
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10 15
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25 30
Met Phe Ala Thr Leu Gln Arg Ser
35 40
<210> 1550
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1550
Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys
1 5 10 15
Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met
20 25 30
Phe Ala Thr Leu Gln Arg Ser Ser
35 40
<210> 1551
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1551
Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro
1 5 10 15
Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
20 25 30
Ala Thr Leu Gln Arg Ser Ser Leu
35 40
<210> 1552
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1552
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
1 5 10 15
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
20 25 30
Thr Leu Gln Arg Ser Ser Leu Trp
35 40
<210> 1553
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1553
Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg
1 5 10 15
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
20 25 30
Leu Gln Arg Ser Ser Leu Trp Cys
35 40
<210> 1554
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1554
Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
1 5 10 15
Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu
20 25 30
Gln Arg Ser Ser Leu Trp Cys Leu
35 40
<210> 1555
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1555
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu Trp Cys Leu Cys
35 40
<210> 1556
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1556
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
20 25 30
Ser Ser Leu Trp Cys Leu Cys Ser
35 40
<210> 1557
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1557
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10 15
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
20 25 30
Ser Leu Trp Cys Leu Cys Ser Asn
35 40
<210> 1558
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 1558
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5 10 15
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
20 25 30
Leu Trp Cys Leu Cys Ser Asn His
35 40
<210> 1559
<211> 48
<212> БЕЛОК
<213> Homo sapiens
<400> 1559
Ala Gln Ala Lys Ala Val Cys Ser Gln Glu Ser Arg Asp Val Leu Cys
1 5 10 15
Glu Leu Ser Asp His His Asn His Thr Leu Glu Glu Glu Cys Gln Trp
20 25 30
Gly Pro Cys Leu Gln Cys Leu Trp Ala Leu Leu Gln Ala Ser Gln Tyr
35 40 45
<210> 1560
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 1560
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
50 55 60
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
65 70 75 80
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
85 90 95
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
100 105 110
His
<210> 1561
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1561
Cys Leu Gln Cys Leu Trp Ala Leu Leu
1 5
<210> 1562
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1562
Cys Gln Trp Gly Pro Cys Leu Gln Cys Leu
1 5 10
<210> 1563
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1563
Gln Trp Gly Pro Cys Leu Gln Cys Leu
1 5
<210> 1564
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1564
Gln Trp Gly Pro Cys Leu Gln Cys Leu Trp
1 5 10
<210> 1565
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1565
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 1566
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1566
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 1567
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1567
Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 1568
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1568
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 1569
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1569
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 1570
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1570
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 1571
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1571
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 1572
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1572
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 1573
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1573
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 1574
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1574
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 1575
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1575
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 1576
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1576
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 1577
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1577
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 1578
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1578
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 1579
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1579
Leu Gln His Gly His Arg His Gly Leu
1 5
<210> 1580
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1580
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 1581
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1581
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 1582
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1582
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 1583
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1583
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 1584
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1584
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 1585
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1585
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 1586
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1586
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 1587
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1587
Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 1588
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1588
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 1589
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1589
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 1590
<211> 67
<212> БЕЛОК
<213> Homo sapiens
<400> 1590
Met Ser Asp Val Ala Ile Val Lys Glu Gly Trp Leu His Lys Arg Gly
1 5 10 15
Lys Tyr Ile Lys Thr Trp Arg Pro Arg Tyr Phe Leu Leu Lys Asn Asp
20 25 30
Gly Thr Phe Ile Gly Tyr Lys Glu Arg Pro Gln Asp Val Asp Gln Arg
35 40 45
Glu Ala Pro Leu Asn Asn Phe Ser Val Ala Gln Cys Gln Leu Met Lys
50 55 60
Thr Glu Arg
65
<210> 1591
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1591
Thr Met Leu Val Leu Glu Gly Ser Gly Asn Leu Val Leu Tyr Thr Gly
1 5 10 15
Val Val Arg Val Gly Lys Val Phe Ile Pro Gly Leu Pro Ala Pro Ser
20 25 30
Leu Thr Met Ser Asn Thr Met Pro Arg Pro Ser Thr Pro Leu Asp Gly
35 40 45
Val Ser Ala Pro Lys Pro Leu Ser Lys Leu Leu Gly Ser Leu Asp Glu
50 55 60
Val Val Leu Leu Ser Pro Val Pro Glu Leu Arg Asp Ser Ser Lys Leu
65 70 75 80
His Asp Ser Leu Tyr Asn Glu Asp Cys Thr Phe Gln Gln Leu Gly Thr
85 90 95
Tyr Ile His Ser Ile
100
<210> 1592
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1592
His Arg Ile Gly Gly Ile Lys Leu Arg His Gln Gln Trp Ser Leu Val
1 5 10 15
Met Glu Ser Val Val Pro Ser Asp Arg Gly Asn Tyr Thr Cys Val Val
20 25 30
Glu Asn Lys Phe Gly Ser Ile Arg Gln Thr Tyr Thr Leu Asp Val Leu
35 40 45
Glu Arg Cys Pro His Arg Pro Ile Leu Gln Ala Gly Leu Pro Ala Asn
50 55 60
Gln Thr Ala Val Leu Gly Ser Asp Val Glu Phe His Cys Lys Val Tyr
65 70 75 80
Ser Asp Ala Gln Pro His Ile Gln Trp Leu Lys His Val Glu Val Asn
85 90 95
Gly Ser Lys Val Gly
100
<210> 1593
<211> 90
<212> БЕЛОК
<213> Homo sapiens
<400> 1593
Met Arg Glu Pro Ile Tyr Met His Ser Thr Met Val Phe Leu Pro Trp
1 5 10 15
Glu Leu His Thr Lys Lys Gly Pro Ser Pro Pro Glu Gln Phe Met Ala
20 25 30
Val Lys Leu Ser Asp Ser Arg Thr Ala Leu Lys Ser Gly Tyr Gly Lys
35 40 45
Tyr Leu Gly Ile Asn Ser Asp Glu Leu Val Gly His Ser Asp Ala Ile
50 55 60
Gly Pro Arg Glu Gln Trp Glu Pro Val Phe Gln Asn Gly Lys Met Ala
65 70 75 80
Leu Leu Ala Ser Asn Ser Cys Phe Ile Arg
85 90
<210> 1594
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1594
Ala Val Lys Leu Ser Asp Ser Arg Ile Ala Leu Lys Ser Gly Tyr Gly
1 5 10 15
Lys Tyr Leu Gly Ile Asn Ser Asp Glu Leu Val Gly His Ser Asp Ala
20 25 30
Ile Gly Pro Arg Glu Gln Trp Glu Pro Val Phe Gln Asn Gly Lys Met
35 40 45
Ala Leu Ser Ala Ser Asn Ser Cys Phe Ile Arg Cys Asn Glu Ala Gly
50 55 60
Asp Ile Glu Ala Lys Ser Lys Thr Ala Gly Glu Glu Glu Met Ile Lys
65 70 75 80
Ile Arg Ser Cys Ala Glu Lys Glu Thr Lys Lys Lys Asp Asp Ile Pro
85 90 95
Glu Glu Asp Lys Gly
100
<210> 1595
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1595
Ala Met Pro Asn Gln Ala Gln Met Arg Ile Leu Lys Glu Thr Glu Leu
1 5 10 15
Arg Lys Val Lys Val Leu Gly Ser Gly Ala Phe Gly Thr Val Tyr Lys
20 25 30
Gly Ile Trp Ile Pro Asp Gly Glu Asn Val Lys Ile Pro Val Ala Ile
35 40 45
Lys Val Ser Arg Glu Asn Thr Ser Pro Lys Ala Asn Lys Glu Ile Leu
50 55 60
Asp Glu Ala Tyr Val Met Ala Gly Val Gly Ser Pro Tyr Val Ser Arg
65 70 75 80
Leu Leu Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Val Thr Gln Leu
85 90 95
Met Pro Tyr Gly Cys
100
<210> 1596
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1596
Arg Val Glu Glu Phe Lys Leu Lys Gln Met Trp Lys Ser Pro Asn Gly
1 5 10 15
Thr Ile Arg Asn Ile Leu Gly Gly Thr Val Phe Arg Glu Ala Ile Ile
20 25 30
Cys Lys Asn Ile Pro Arg Leu Val Ser Gly Trp Val Lys Pro Ile Ile
35 40 45
Ile Gly Gly His Ala Tyr Gly Asp Gln Tyr Arg Ala Thr Asp Phe Val
50 55 60
Val Pro Gly Pro Gly Lys Val Glu Ile Thr Tyr Thr Pro Ser Asp Gly
65 70 75 80
Thr Gln Lys Val Thr Tyr Leu Val His Asn Phe Glu Glu Gly Gly Gly
85 90 95
Val Ala Met Gly Met
100
<210> 1597
<211> 62
<212> БЕЛОК
<213> Homo sapiens
<400> 1597
Met Thr Glu Tyr Lys Leu Val Val Val Gly Ala Cys Gly Val Gly Lys
1 5 10 15
Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr
20 25 30
Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly
35 40 45
Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr Ala Gly Gln Glu
50 55 60
<210> 1598
<211> 62
<212> БЕЛОК
<213> Homo sapiens
<400> 1598
Met Thr Glu Tyr Lys Leu Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10 15
Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr
20 25 30
Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly
35 40 45
Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr Ala Gly Gln Glu
50 55 60
<210> 1599
<211> 62
<212> БЕЛОК
<213> Homo sapiens
<400> 1599
Met Thr Glu Tyr Lys Leu Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10 15
Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr
20 25 30
Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly
35 40 45
Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr Ala Gly Gln Glu
50 55 60
<210> 1600
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1600
Ala Gly Gly Val Gly Lys Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn
1 5 10 15
His Phe Val Asp Glu Tyr Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys
20 25 30
Gln Val Val Ile Asp Gly Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr
35 40 45
Ala Gly His Glu Glu Tyr Ser Ala Met Arg Asp Gln Tyr Met Arg Thr
50 55 60
Gly Glu Gly Phe Leu Cys Val Phe Ala Ile Asn Asn Thr Lys Ser Phe
65 70 75 80
Glu Asp Ile His His Tyr Arg Glu Gln Ile Lys Arg Val Lys Asp Ser
85 90 95
Glu Asp Val Pro Met
100
<210> 1601
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1601
Ala Gly Gly Val Gly Lys Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn
1 5 10 15
His Phe Val Asp Glu Tyr Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys
20 25 30
Gln Val Val Ile Asp Gly Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr
35 40 45
Ala Gly Leu Glu Glu Tyr Ser Ala Met Arg Asp Gln Tyr Met Arg Thr
50 55 60
Gly Glu Gly Phe Leu Cys Val Phe Ala Ile Asn Asn Thr Lys Ser Phe
65 70 75 80
Glu Asp Ile His His Tyr Arg Glu Gln Ile Lys Arg Val Lys Asp Ser
85 90 95
Glu Asp Val Pro Met
100
<210> 1602
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1602
Ala Gly Gly Val Gly Lys Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn
1 5 10 15
His Phe Val Asp Glu Tyr Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys
20 25 30
Gln Val Val Ile Asp Gly Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr
35 40 45
Ala Gly Lys Glu Glu Tyr Ser Ala Met Arg Asp Gln Tyr Met Arg Thr
50 55 60
Gly Glu Gly Phe Leu Cys Val Phe Ala Ile Asn Asn Ser Lys Ser Phe
65 70 75 80
Ala Asp Ile Asn Leu Tyr Arg Glu Gln Ile Lys Arg Val Lys Asp Ser
85 90 95
Asp Asp Val Pro Met
100
<210> 1603
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1603
Ala Gly Gly Val Gly Lys Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn
1 5 10 15
His Phe Val Asp Glu Tyr Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys
20 25 30
Gln Val Val Ile Asp Gly Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr
35 40 45
Ala Gly Arg Glu Glu Tyr Ser Ala Met Arg Asp Gln Tyr Met Arg Thr
50 55 60
Gly Glu Gly Phe Leu Cys Val Phe Ala Ile Asn Asn Ser Lys Ser Phe
65 70 75 80
Ala Asp Ile Asn Leu Tyr Arg Glu Gln Ile Lys Arg Val Lys Asp Ser
85 90 95
Asp Asp Val Pro Met
100
<210> 1604
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1604
Ile Glu Glu His Ala Asn Trp Ser Val Ser Arg Glu Ala Gly Phe Ser
1 5 10 15
Tyr Ser His Ala Gly Leu Ser Asn Arg Leu Ala Arg Asp Asn Glu Leu
20 25 30
Arg Glu Asn Asp Lys Glu Gln Leu Lys Ala Ile Ser Thr Arg Asp Pro
35 40 45
Leu Ser Lys Ile Thr Glu Gln Glu Lys Asp Phe Leu Trp Ser His Arg
50 55 60
His Tyr Cys Val Thr Ile Pro Glu Ile Leu Pro Lys Leu Leu Leu Ser
65 70 75 80
Val Lys Trp Asn Ser Arg Asp Glu Val Ala Gln Met Tyr Cys Leu Val
85 90 95
Lys Asp Trp Pro Pro
100
<210> 1605
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1605
Lys Phe Asn Cys Arg Val Ala Gln Tyr Pro Phe Glu Asp His Asn Pro
1 5 10 15
Pro Gln Leu Glu Leu Ile Lys Pro Phe Cys Glu Asp Leu Asp Gln Trp
20 25 30
Leu Ser Glu Asp Asp Asn His Val Ala Ala Ile His Cys Lys Ala Gly
35 40 45
Lys Gly Gln Thr Gly Val Met Ile Cys Ala Tyr Leu Leu His Arg Gly
50 55 60
Lys Phe Leu Lys Ala Gln Glu Ala Leu Asp Phe Tyr Gly Glu Val Arg
65 70 75 80
Thr Arg Asp Lys Lys Gly Val Thr Ile Pro Ser Gln Arg Arg Tyr Val
85 90 95
Tyr Tyr Tyr Ser Tyr
100
<210> 1606
<211> 79
<212> БЕЛОК
<213> Homo sapiens
<400> 1606
Met Gln Ala Ile Lys Cys Val Val Val Gly Asp Gly Ala Val Gly Lys
1 5 10 15
Thr Cys Leu Leu Ile Ser Tyr Thr Thr Asn Ala Phe Ser Gly Glu Tyr
20 25 30
Ile Pro Thr Val Phe Asp Asn Tyr Ser Ala Asn Val Met Val Asp Gly
35 40 45
Lys Pro Val Asn Leu Gly Leu Trp Asp Thr Ala Gly Gln Glu Asp Tyr
50 55 60
Asp Arg Leu Arg Pro Leu Ser Tyr Pro Gln Thr Val Gly Glu Thr
65 70 75
<210> 1607
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1607
Ala Val Cys Lys Ser Lys Lys Ser Trp Gln Ala Arg His Thr Gly Ile
1 5 10 15
Lys Ile Val Gln Gln Ile Ala Ile Leu Met Gly Cys Ala Ile Leu Pro
20 25 30
His Leu Arg Ser Leu Val Glu Ile Ile Glu His Gly Leu Val Asp Glu
35 40 45
Gln Gln Glu Val Arg Thr Ile Ser Ala Leu Ala Ile Ala Ala Leu Ala
50 55 60
Glu Ala Ala Thr Pro Tyr Gly Ile Glu Ser Phe Asp Ser Val Leu Lys
65 70 75 80
Pro Leu Trp Lys Gly Ile Arg Gln His Arg Gly Lys Gly Leu Ala Ala
85 90 95
Phe Leu Lys Ala Ile
100
<210> 1608
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1608
Tyr Leu Ser Leu Tyr Leu Leu Leu Val Ser Cys Pro Lys Ser Glu Val
1 5 10 15
Arg Ala Lys Phe Lys Phe Ser Ile Leu Asn Ala Lys Gly Glu Glu Thr
20 25 30
Lys Ala Met Glu Ser Gln Arg Ala Tyr Arg Phe Val Gln Gly Lys Asp
35 40 45
Trp Gly Leu Lys Lys Phe Ile Arg Arg Asp Phe Leu Leu Asp Glu Ala
50 55 60
Asn Gly Leu Leu Pro Asp Asp Lys Leu Thr Leu Phe Cys Glu Val Ser
65 70 75 80
Val Val Gln Asp Ser Val Asn Ile Ser Gly Gln Asn Thr Met Asn Met
85 90 95
Val Lys Val Pro Glu
100
<210> 1609
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1609
Tyr Leu Ser Leu Tyr Leu Leu Leu Val Ser Cys Pro Lys Ser Glu Val
1 5 10 15
Arg Ala Lys Phe Lys Phe Ser Ile Leu Asn Ala Lys Gly Glu Glu Thr
20 25 30
Lys Ala Met Glu Ser Gln Arg Ala Tyr Arg Phe Val Gln Gly Lys Asp
35 40 45
Trp Gly Val Lys Lys Phe Ile Arg Arg Asp Phe Leu Leu Asp Glu Ala
50 55 60
Asn Gly Leu Leu Pro Asp Asp Lys Leu Thr Leu Phe Cys Glu Val Ser
65 70 75 80
Val Val Gln Asp Ser Val Asn Ile Ser Gly Gln Asn Thr Met Asn Met
85 90 95
Val Lys Val Pro Glu
100
<210> 1610
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1610
Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn
1 5 10 15
Thr Phe Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly
20 25 30
Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys
35 40 45
Met Gly Ser Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu
50 55 60
Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val
65 70 75 80
Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg
85 90 95
Lys Lys Gly Glu Pro
100
<210> 1611
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1611
Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg
1 5 10 15
His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys
20 25 30
Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly
35 40 45
Met Asn Gln Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser
50 55 60
Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys
65 70 75 80
Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly
85 90 95
Glu Pro His His Glu
100
<210> 1612
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1612
Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg
1 5 10 15
His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys
20 25 30
Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly
35 40 45
Met Asn Trp Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser
50 55 60
Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys
65 70 75 80
Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly
85 90 95
Glu Pro His His Glu
100
<210> 1613
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1613
Pro Glu Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys
1 5 10 15
Asn Ser Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile
20 25 30
Ile Thr Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe
35 40 45
Glu Val Cys Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu
50 55 60
Glu Asn Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly
65 70 75 80
Ser Thr Lys Arg Ala Leu Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro
85 90 95
Lys Lys Lys Pro Leu
100
<210> 1614
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1614
Pro Glu Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys
1 5 10 15
Asn Ser Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile
20 25 30
Ile Thr Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe
35 40 45
Glu Val His Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu
50 55 60
Glu Asn Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly
65 70 75 80
Ser Thr Lys Arg Ala Leu Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro
85 90 95
Lys Lys Lys Pro Leu
100
<210> 1615
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1615
Thr Glu Val Val Arg Arg Cys Pro His His Glu Arg Cys Ser Asp Ser
1 5 10 15
Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg Val Glu Gly Asn Leu
20 25 30
Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg His Ser Val Val
35 40 45
Val Pro Cys Glu Pro Pro Glu Val Gly Ser Asp Cys Thr Thr Ile His
50 55 60
Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly Met Asn Arg Arg
65 70 75 80
Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser Gly Asn Leu Leu
85 90 95
Gly Arg Asn Ser Phe
100
<210> 1616
<211> 54
<212> БЕЛОК
<213> Homo sapiens
<400> 1616
Tyr Asn Phe Asp Lys Asn Tyr Lys Asp Trp Gln Ser Ala Val Glu Cys
1 5 10 15
Ile Ala Val Leu Asp Val Leu Leu Cys Leu Ala Asn Tyr Ser Arg Gly
20 25 30
Gly Asp Gly Pro Met Cys Arg Pro Val Ile Leu Leu Pro Glu Asp Thr
35 40 45
Pro Pro Leu Leu Arg Ala
50
<210> 1617
<211> 93
<212> БЕЛОК
<213> Homo sapiens
<400> 1617
Ala Lys Phe Gln Gln Cys His Ser Thr Leu Glu Pro Asn Pro Ala Asp
1 5 10 15
Cys Arg Val Leu Val Tyr Leu Gln Asn Gln Pro Gly Thr Lys Leu Leu
20 25 30
Asn Phe Leu Gln Glu Arg Asn Leu Pro Pro Lys Val Val Leu Arg His
35 40 45
Pro Lys Val His Leu Asn Thr Met Phe Arg Arg Pro His Ser Cys Leu
50 55 60
Ala Asp Val Leu Leu Ser Val His Leu Ile Val Leu Arg Val Val Arg
65 70 75 80
Leu Pro Ala Pro Phe Arg Val Asn His Ala Val Glu Trp
85 90
<210> 1618
<211> 179
<212> БЕЛОК
<213> Homo sapiens
<400> 1618
Ala Leu Gly Pro His Ser Arg Ile Ser Cys Leu Pro Thr Gln Thr Arg
1 5 10 15
Gly Cys Ile Leu Leu Ala Ala Thr Pro Arg Ser Ser Ser Ser Ser Ser
20 25 30
Ser Asn Asp Met Ile Pro Met Ala Ile Ser Ser Pro Pro Lys Ala Pro
35 40 45
Leu Leu Ala Ala Pro Ser Pro Ala Ser Arg Leu Gln Cys Ile Asn Ser
50 55 60
Asn Ser Arg Ile Thr Ser Gly Gln Trp Met Ala His Met Ala Leu Leu
65 70 75 80
Pro Ser Gly Thr Lys Gly Arg Cys Thr Ala Cys His Thr Ala Leu Gly
85 90 95
Arg Gly Ser Leu Ser Ser Ser Ser Cys Pro Gln Pro Ser Pro Ser Leu
100 105 110
Pro Ala Ser Asn Lys Leu Pro Ser Leu Pro Leu Ser Lys Met Tyr Thr
115 120 125
Thr Ser Met Ala Met Pro Ile Leu Pro Leu Pro Gln Leu Leu Leu Ser
130 135 140
Ala Asp Gln Gln Ala Ala Pro Arg Thr Asn Phe His Ser Ser Leu Ala
145 150 155 160
Glu Thr Val Ser Leu His Pro Leu Ala Pro Met Pro Ser Lys Thr Cys
165 170 175
His His Lys
<210> 1619
<211> 67
<212> БЕЛОК
<213> Homo sapiens
<400> 1619
Arg Ser Tyr Arg Arg Met Ile His Leu Trp Trp Thr Ala Gln Ile Ser
1 5 10 15
Leu Gly Val Cys Arg Ser Leu Thr Val Ala Cys Cys Thr Gly Gly Leu
20 25 30
Val Gly Gly Thr Pro Leu Ser Ile Ser Arg Pro Thr Ser Arg Ala Arg
35 40 45
Gln Ser Cys Cys Leu Pro Gly Leu Thr His Pro Ala His Gln Pro Leu
50 55 60
Gly Ser Met
65
<210> 1620
<211> 60
<212> БЕЛОК
<213> Homo sapiens
<400> 1620
Gln His Ser Gly Arg Asp Val Ser Leu Arg Gly Leu Ser Cys Ala Arg
1 5 10 15
Ala Thr Leu Ser Phe Trp Pro Gly Gly Tyr Pro Ala Tyr Ser Lys Asp
20 25 30
Ser Gly Leu Leu Thr Ser Ser Ser Arg Glu Trp Lys Val Lys Phe Pro
35 40 45
Glu Leu Leu Cys Val Trp Val Ser Ser Ile Arg His
50 55 60
<210> 1621
<211> 48
<212> БЕЛОК
<213> Homo sapiens
<400> 1621
Ala Gln Ala Lys Ala Val Cys Ser Gln Glu Ser Arg Asp Val Leu Cys
1 5 10 15
Glu Leu Ser Asp His His Asn His Thr Leu Glu Glu Glu Cys Gln Trp
20 25 30
Gly Pro Cys Leu Gln Cys Leu Trp Ala Leu Leu Gln Ala Ser Gln Tyr
35 40 45
<210> 1622
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 1622
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
50 55 60
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
65 70 75 80
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
85 90 95
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
100 105 110
His
<210> 1623
<211> 494
<212> БЕЛОК
<213> Homo sapiens
<400> 1623
Thr Arg Arg Cys His Cys Cys Pro His Leu Arg Ser His Pro Cys Pro
1 5 10 15
His His Leu Arg Asn His Pro Arg Pro His His Leu Arg His His Ala
20 25 30
Cys His His His Leu Arg Asn Cys Pro His Pro His Phe Leu Arg His
35 40 45
Cys Thr Cys Pro Gly Arg Trp Arg Asn Arg Pro Ser Leu Arg Arg Leu
50 55 60
Arg Ser Leu Leu Cys Leu Pro His Leu Asn His His Leu Phe Leu His
65 70 75 80
Trp Arg Ser Arg Pro Cys Leu His Arg Lys Ser His Pro His Leu Leu
85 90 95
His Leu Arg Arg Leu Tyr Pro His His Leu Lys His Arg Pro Cys Pro
100 105 110
His His Leu Lys Asn Leu Leu Cys Pro Arg His Leu Arg Asn Cys Pro
115 120 125
Leu Pro Arg His Leu Lys His Leu Ala Cys Leu His His Leu Arg Ser
130 135 140
His Pro Cys Pro Leu His Leu Lys Ser His Pro Cys Leu His His Arg
145 150 155 160
Arg His Leu Val Cys Ser His His Leu Lys Ser Leu Leu Cys Pro Leu
165 170 175
His Leu Arg Ser Leu Pro Phe Pro His His Leu Arg His His Ala Cys
180 185 190
Pro His His Leu Arg Thr Arg Leu Cys Pro His His Leu Lys Asn His
195 200 205
Leu Cys Pro Pro His Leu Arg Tyr Arg Ala Tyr Pro Pro Cys Leu Trp
210 215 220
Cys His Ala Cys Leu His Arg Leu Arg Asn Leu Pro Cys Pro His Arg
225 230 235 240
Leu Arg Ser Leu Pro Arg Pro Leu His Leu Arg Leu His Ala Ser Pro
245 250 255
His His Leu Arg Thr Pro Pro His Pro His His Leu Arg Thr His Leu
260 265 270
Leu Pro His His Arg Arg Thr Arg Ser Cys Pro Cys Arg Trp Arg Ser
275 280 285
His Pro Cys Cys His Tyr Leu Arg Ser Arg Asn Ser Ala Pro Gly Pro
290 295 300
Arg Gly Arg Thr Cys His Pro Gly Leu Arg Ser Arg Thr Cys Pro Pro
305 310 315 320
Gly Leu Arg Ser His Thr Tyr Leu Arg Arg Leu Arg Ser His Thr Cys
325 330 335
Pro Pro Ser Leu Arg Ser His Ala Tyr Ala Leu Cys Leu Arg Ser His
340 345 350
Thr Cys Pro Pro Arg Leu Arg Asp His Ile Cys Pro Leu Ser Leu Arg
355 360 365
Asn Cys Thr Cys Pro Pro Arg Leu Arg Ser Arg Thr Cys Leu Leu Cys
370 375 380
Leu Arg Ser His Ala Cys Pro Pro Asn Leu Arg Asn His Thr Cys Pro
385 390 395 400
Pro Ser Leu Arg Ser His Ala Cys Pro Pro Gly Leu Arg Asn Arg Ile
405 410 415
Cys Pro Leu Ser Leu Arg Ser His Pro Cys Pro Leu Gly Leu Lys Ser
420 425 430
Pro Leu Arg Ser Gln Ala Asn Ala Leu His Leu Arg Ser Cys Pro Cys
435 440 445
Ser Leu Pro Leu Gly Asn His Pro Tyr Leu Pro Cys Leu Glu Ser Gln
450 455 460
Pro Cys Leu Ser Leu Gly Asn His Leu Cys Pro Leu Cys Pro Arg Ser
465 470 475 480
Cys Arg Cys Pro His Leu Gly Ser His Pro Cys Arg Leu Ser
485 490
<210> 1624
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 1624
Gly Pro Arg Ser His Pro Leu Pro Arg Leu Trp His Leu Leu Leu Gln
1 5 10 15
Val Thr Gln Thr Ser Phe Ala Leu Ala Pro Thr Leu Thr His Met Leu
20 25 30
Ser Pro His
35
<210> 1625
<211> 172
<212> БЕЛОК
<213> Homo sapiens
<400> 1625
Pro Leu Gly Leu Val Pro Trp Thr Arg Trp Cys Pro Gln Gly Lys Pro
1 5 10 15
Arg Phe Pro Ala Met Ser Thr Thr Thr Ala Thr Gly Thr Thr Thr Thr
20 25 30
Lys Ser Gly Ser Ser Gly Met Ala Gly Ser Leu Ala Gln Lys Pro Glu
35 40 45
Ser Pro Ser Pro Gly Leu Leu Phe Leu Gly His Ser Pro Ser Gln Ser
50 55 60
His Leu Leu Leu Ile Ser Lys Ser Pro Asp Pro Thr Gln Gln Pro Leu
65 70 75 80
Arg Gly Gly Ser Leu Thr His Ser Ala Pro Gly Pro Ser Leu Ser Gln
85 90 95
Pro Leu Ala Gln Leu Thr Pro Pro Ala Ser Ala Pro Val Pro Ala Val
100 105 110
Cys Ser Thr Cys Lys Asn Pro Ala Ser Leu Pro Asp Thr His Arg Gly
115 120 125
Lys Gly Gly Gly Val Pro Pro Ser Pro Pro Leu Ala Leu Gly Pro Arg
130 135 140
Met Gln Leu Cys Thr Gln Leu Ala Arg Phe Phe Pro Ile Thr Pro Pro
145 150 155 160
Val Trp His Ile Leu Gly Pro Gln Arg His Thr Pro
165 170
<210> 1626
<211> 97
<212> БЕЛОК
<213> Homo sapiens
<400> 1626
Lys Tyr Glu Lys Lys Lys Tyr Tyr Asp Lys Asn Ala Ile Ala Ile Thr
1 5 10 15
Asn Ile Ser Ser Ser Asp Ala Pro Leu Gln Pro Leu Val Ser Ser Pro
20 25 30
Ser Leu Gln Ala Ala Val Asp Lys Asn Lys Leu Glu Lys Glu Lys Glu
35 40 45
Lys Lys Arg Lys Arg Lys Arg Glu Lys Arg Ser Gln Lys Ser Arg Gln
50 55 60
Asn His Leu Gln Leu Lys Ser Cys Arg Arg Lys Ile Ser Asn Trp Ser
65 70 75 80
Leu Lys Lys Val Pro Ala Leu Lys Lys Leu Arg Ser Pro Leu Trp Ile
85 90 95
Phe
<210> 1627
<211> 78
<212> БЕЛОК
<213> Homo sapiens
<400> 1627
Cys Cys Pro Arg Thr Ile Leu Asn Asn Gly Ser Leu Lys Thr Gln Val
1 5 10 15
Gln Met Lys Leu Pro Glu Cys Gln Arg Leu Leu Pro Pro Trp Pro Leu
20 25 30
His Gln Gln Leu Leu His Arg Arg Pro Leu His Gln Pro Pro Pro Gly
35 40 45
Pro Cys His Leu Leu Ser Leu Pro Arg Lys Pro Thr Arg Ala Ala Thr
50 55 60
Val Ser Val Trp Ala Ser Cys Ile Leu Gly Gln Pro Ser Leu
65 70 75
<210> 1628
<211> 46
<212> БЕЛОК
<213> Homo sapiens
<400> 1628
Leu Ala Arg Thr Pro Leu Pro Ser Thr Arg Cys Phe Ala Asn Trp Pro
1 5 10 15
Arg Pro Ala Leu Cys Ser Cys Gly Leu Ile Pro His Pro Arg Pro Ala
20 25 30
Pro Ala Ser Ala Pro Trp Pro Ser Thr Ser Ser His Ser Thr
35 40 45
<210> 1629
<211> 77
<212> БЕЛОК
<213> Homo sapiens
<400> 1629
Ser Gln Gly Leu Tyr Ser Ser Ser Ala Ser Ser Gly Lys Cys Leu Met
1 5 10 15
Glu Val Thr Val Asp Arg Asn Cys Leu Glu Val Leu Pro Thr Lys Met
20 25 30
Ser Tyr Ala Ala Asn Leu Lys Asn Val Met Asn Met Gln Asn Arg Gln
35 40 45
Lys Lys Lys Gly Lys Asn Ser Pro Cys Cys Gln Lys Lys Leu Arg Val
50 55 60
Gln Asn Gln Gly His Leu Leu Met Ile Leu Leu His Asn
65 70 75
<210> 1630
<211> 91
<212> БЕЛОК
<213> Homo sapiens
<400> 1630
Thr Arg Ala Ser Pro Pro Arg Ser Ser Ser Ala Ile Ala Val Arg Ala
1 5 10 15
Ser Cys Cys Pro Tyr Gly Ser Thr Ser Thr Ala Ser Arg Ser Pro Thr
20 25 30
Gln Arg Cys Arg Leu Ala Arg Ala Ala Ala Ser Thr Ala Thr Glu Val
35 40 45
Thr Phe Gly Ser Ser Glu Met Gln Gly His Thr Met Gly Phe Trp Leu
50 55 60
Thr Lys Leu Asn Tyr Leu Cys His Leu Ser Met Leu Thr Asp Ser Leu
65 70 75 80
Phe Leu Pro Ile Ser His Cys Gln Cys Ile Leu
85 90
<210> 1631
<211> 104
<212> БЕЛОК
<213> Homo sapiens
<400> 1631
Leu Gly Ser Gly Ala Phe Gly Thr Val Tyr Lys Gly Ile Trp Ile Pro
1 5 10 15
Asp Gly Glu Asn Val Lys Ile Pro Val Ala Ile Lys Val Leu Arg Glu
20 25 30
Asn Thr Ser Pro Lys Ala Asn Lys Glu Ile Leu Asp Glu Ala Tyr Val
35 40 45
Met Ala Tyr Val Met Ala Gly Val Gly Ser Pro Tyr Val Ser Arg Leu
50 55 60
Leu Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Val Thr Gln Leu Met
65 70 75 80
Pro Tyr Gly Cys Leu Leu Asp His Val Arg Glu Asn Arg Gly Arg Leu
85 90 95
Gly Ser Gln Asp Leu Leu Asn Trp
100
<210> 1632
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1632
Lys Tyr Ile Lys Thr Trp Arg Pro Arg Tyr
1 5 10
<210> 1633
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1633
Trp Leu His Lys Arg Gly Lys Tyr Ile
1 5
<210> 1634
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1634
Trp Leu His Lys Arg Gly Lys Tyr Ile Lys
1 5 10
<210> 1635
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1635
Ala Pro Lys Pro Leu Ser Lys Leu Leu
1 5
<210> 1636
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1636
Gly Val Ser Ala Pro Lys Pro Leu Ser Lys
1 5 10
<210> 1637
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1637
Val Ser Ala Pro Lys Pro Leu Ser Lys
1 5
<210> 1638
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1638
Cys Pro His Arg Pro Ile Leu Gln Ala
1 5
<210> 1639
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1639
Lys Leu Ser Asp Ser Arg Thr Ala Leu
1 5
<210> 1640
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1640
Lys Leu Ser Asp Ser Arg Thr Ala Leu Lys
1 5 10
<210> 1641
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1641
Leu Ser Asp Ser Arg Thr Ala Leu Lys
1 5
<210> 1642
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1642
Arg Thr Ala Leu Lys Ser Gly Tyr Gly Lys
1 5 10
<210> 1643
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1643
Thr Ala Leu Lys Ser Gly Tyr Gly Lys
1 5
<210> 1644
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1644
Ala Leu Ser Ala Ser Asn Ser Cys Phe
1 5
<210> 1645
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1645
Ala Leu Ser Ala Ser Asn Ser Cys Phe Ile
1 5 10
<210> 1646
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1646
Phe Gln Asn Gly Lys Met Ala Leu Ser Ala
1 5 10
<210> 1647
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1647
Lys Val Ser Arg Glu Asn Thr Ser Pro Lys
1 5 10
<210> 1648
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1648
Lys Pro Ile Ile Ile Gly Gly His Ala Tyr
1 5 10
<210> 1649
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1649
Lys Leu Val Val Val Gly Ala Cys Gly Val
1 5 10
<210> 1650
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1650
Leu Val Val Val Gly Ala Cys Gly Val
1 5
<210> 1651
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1651
Val Val Gly Ala Cys Gly Val Gly Lys
1 5
<210> 1652
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1652
Val Val Val Gly Ala Cys Gly Val Gly Lys
1 5 10
<210> 1653
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1653
Val Val Gly Ala Asp Gly Val Gly Lys
1 5
<210> 1654
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1654
Val Val Val Gly Ala Asp Gly Val Gly Lys
1 5 10
<210> 1655
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1655
Lys Leu Val Val Val Gly Ala Asp Gly Val
1 5 10
<210> 1656
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1656
Leu Val Val Val Gly Ala Asp Gly Val
1 5
<210> 1657
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1657
Lys Leu Val Val Val Gly Ala Val Gly Val
1 5 10
<210> 1658
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1658
Leu Val Val Val Gly Ala Val Gly Val
1 5
<210> 1659
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1659
Val Val Gly Ala Val Gly Val Gly Lys
1 5
<210> 1660
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1660
Val Val Val Gly Ala Val Gly Val Gly Lys
1 5 10
<210> 1661
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1661
Ile Leu Asp Thr Ala Gly His Glu Glu Tyr
1 5 10
<210> 1662
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1662
Ile Leu Asp Thr Ala Gly Leu Glu Glu Tyr
1 5 10
<210> 1663
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1663
Leu Leu Asp Ile Leu Asp Thr Ala Gly Leu
1 5 10
<210> 1664
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1664
Ile Leu Asp Thr Ala Gly Lys Glu Glu Tyr
1 5 10
<210> 1665
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1665
Ile Leu Asp Thr Ala Gly Arg Glu Glu Tyr
1 5 10
<210> 1666
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1666
Ala Ile Ser Thr Arg Asp Pro Leu Ser Lys
1 5 10
<210> 1667
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1667
Gln Thr Gly Val Met Ile Cys Ala Tyr
1 5
<210> 1668
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1668
Phe Ser Gly Glu Tyr Ile Pro Thr Val
1 5
<210> 1669
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1669
Thr Thr Asn Ala Phe Ser Gly Glu Tyr
1 5
<210> 1670
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1670
Tyr Thr Thr Asn Ala Phe Ser Gly Glu Tyr
1 5 10
<210> 1671
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1671
Gly Leu Val Asp Glu Gln Gln Glu Val
1 5
<210> 1672
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1672
Phe Val Gln Gly Lys Asp Trp Gly Leu
1 5
<210> 1673
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1673
Phe Val Gln Gly Lys Asp Trp Gly Val
1 5
<210> 1674
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1674
Cys Met Gly Ser Met Asn Arg Arg Pro Ile
1 5 10
<210> 1675
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1675
Gly Ser Met Asn Arg Arg Pro Ile Leu
1 5
<210> 1676
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1676
Met Gly Ser Met Asn Arg Arg Pro Ile
1 5
<210> 1677
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1677
Met Gly Ser Met Asn Arg Arg Pro Ile Leu
1 5 10
<210> 1678
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1678
Ser Met Asn Arg Arg Pro Ile Leu Thr Ile
1 5 10
<210> 1679
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1679
Cys Met Gly Gly Met Asn Gln Arg Pro Ile
1 5 10
<210> 1680
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1680
Gly Met Asn Gln Arg Pro Ile Leu Thr Ile
1 5 10
<210> 1681
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1681
Asn Gln Arg Pro Ile Leu Thr Ile Ile
1 5
<210> 1682
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1682
Cys Met Gly Gly Met Asn Trp Arg Pro Ile
1 5 10
<210> 1683
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1683
Gly Met Asn Trp Arg Pro Ile Leu Thr Ile
1 5 10
<210> 1684
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1684
Met Asn Trp Arg Pro Ile Leu Thr Ile
1 5
<210> 1685
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1685
Met Asn Trp Arg Pro Ile Leu Thr Ile Ile
1 5 10
<210> 1686
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1686
Asn Ser Phe Glu Val Cys Val Cys Ala
1 5
<210> 1687
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1687
Asn Ser Phe Glu Val His Val Cys Ala
1 5
<210> 1688
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1688
Val Val Pro Cys Glu Pro Pro Glu Val
1 5
<210> 1689
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1689
Val Val Val Pro Cys Glu Pro Pro Glu Val
1 5 10
<210> 1690
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1690
Ile Leu Leu Pro Glu Asp Thr Pro Pro Leu
1 5 10
<210> 1691
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1691
Leu Leu Pro Glu Asp Thr Pro Pro Leu
1 5
<210> 1692
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1692
Ala Pro Phe Arg Val Asn His Ala Val
1 5
<210> 1693
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1693
Cys Leu Ala Asp Val Leu Leu Ser Val
1 5
<210> 1694
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1694
Phe Leu Gln Glu Arg Asn Leu Pro Pro Lys
1 5 10
<210> 1695
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1695
His Leu Ile Val Leu Arg Val Val Arg Leu
1 5 10
<210> 1696
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1696
His Pro Lys Val His Leu Asn Thr Met
1 5
<210> 1697
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1697
His Pro Lys Val His Leu Asn Thr Met Phe
1 5 10
<210> 1698
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1698
Lys Val His Leu Asn Thr Met Phe Arg
1 5
<210> 1699
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1699
Lys Val His Leu Asn Thr Met Phe Arg Arg
1 5 10
<210> 1700
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1700
Leu Pro Ala Pro Phe Arg Val Asn His Ala
1 5 10
<210> 1701
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1701
Met Phe Arg Arg Pro His Ser Cys Leu
1 5
<210> 1702
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1702
Met Phe Arg Arg Pro His Ser Cys Leu Ala
1 5 10
<210> 1703
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1703
Asn Thr Met Phe Arg Arg Pro His Ser Cys
1 5 10
<210> 1704
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1704
Arg Pro His Ser Cys Leu Ala Asp Val
1 5
<210> 1705
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1705
Arg Pro His Ser Cys Leu Ala Asp Val Leu
1 5 10
<210> 1706
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1706
Arg Val Val Arg Leu Pro Ala Pro Phe Arg
1 5 10
<210> 1707
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1707
Ser Val His Leu Ile Val Leu Arg Val
1 5
<210> 1708
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1708
Thr Met Phe Arg Arg Pro His Ser Cys
1 5
<210> 1709
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1709
Thr Met Phe Arg Arg Pro His Ser Cys Leu
1 5 10
<210> 1710
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1710
Val Leu Leu Ser Val His Leu Ile Val
1 5
<210> 1711
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1711
Val Leu Leu Ser Val His Leu Ile Val Leu
1 5 10
<210> 1712
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1712
Val Leu Arg Val Val Arg Leu Pro Ala
1 5
<210> 1713
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1713
Val Val Arg Leu Pro Ala Pro Phe Arg
1 5
<210> 1714
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1714
Ala Met Pro Ile Leu Pro Leu Pro Gln Leu
1 5 10
<210> 1715
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1715
Ala Pro Leu Leu Ala Ala Pro Ser Pro Ala
1 5 10
<210> 1716
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1716
Ala Pro Arg Thr Asn Phe His Ser Ser
1 5
<210> 1717
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1717
Ala Pro Arg Thr Asn Phe His Ser Ser Leu
1 5 10
<210> 1718
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1718
Cys Pro Gln Pro Ser Pro Ser Leu Pro Ala
1 5 10
<210> 1719
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1719
Gly Gln Trp Met Ala His Met Ala Leu
1 5
<210> 1720
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1720
Gly Gln Trp Met Ala His Met Ala Leu Leu
1 5 10
<210> 1721
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1721
His Met Ala Leu Leu Pro Ser Gly Thr Lys
1 5 10
<210> 1722
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1722
His Thr Ala Leu Gly Arg Gly Ser Leu
1 5
<210> 1723
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1723
Ile Pro Met Ala Ile Ser Ser Pro Pro
1 5
<210> 1724
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1724
Ile Pro Met Ala Ile Ser Ser Pro Pro Lys
1 5 10
<210> 1725
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1725
Lys Leu Pro Ser Leu Pro Leu Ser Lys
1 5
<210> 1726
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1726
Lys Leu Pro Ser Leu Pro Leu Ser Lys Met
1 5 10
<210> 1727
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1727
Lys Met Tyr Thr Thr Ser Met Ala Met
1 5
<210> 1728
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1728
Leu Leu Ala Ala Pro Ser Pro Ala Ser Arg
1 5 10
<210> 1729
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1729
Leu Leu Leu Ser Ala Asp Gln Gln Ala Ala
1 5 10
<210> 1730
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1730
Leu Leu Ser Ala Asp Gln Gln Ala Ala
1 5
<210> 1731
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1731
Leu Pro Ala Ser Asn Lys Leu Pro Ser
1 5
<210> 1732
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1732
Leu Pro Ala Ser Asn Lys Leu Pro Ser Leu
1 5 10
<210> 1733
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1733
Leu Pro Leu Pro Gln Leu Leu Leu Ser Ala
1 5 10
<210> 1734
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1734
Leu Pro Ser Leu Pro Leu Ser Lys Met
1 5
<210> 1735
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1735
Leu Ser Lys Met Tyr Thr Thr Ser Met
1 5
<210> 1736
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1736
Met Ala Leu Leu Pro Ser Gly Thr Lys
1 5
<210> 1737
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1737
Met Pro Ile Leu Pro Leu Pro Gln Leu
1 5
<210> 1738
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1738
Met Pro Ile Leu Pro Leu Pro Gln Leu Leu
1 5 10
<210> 1739
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1739
Met Tyr Thr Thr Ser Met Ala Met Pro Ile
1 5 10
<210> 1740
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1740
Pro Met Ala Ile Ser Ser Pro Pro Lys
1 5
<210> 1741
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1741
Gln Trp Met Ala His Met Ala Leu Leu
1 5
<210> 1742
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1742
Ser Lys Met Tyr Thr Thr Ser Met Ala Met
1 5 10
<210> 1743
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1743
Ser Met Ala Met Pro Ile Leu Pro Leu
1 5
<210> 1744
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1744
Ser Asn Lys Leu Pro Ser Leu Pro Leu
1 5
<210> 1745
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1745
Ser Pro Ala Ser Arg Leu Gln Cys Ile
1 5
<210> 1746
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1746
Ser Pro Pro Lys Ala Pro Leu Leu Ala Ala
1 5 10
<210> 1747
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1747
Ser Pro Ser Leu Pro Ala Ser Asn Lys Leu
1 5 10
<210> 1748
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1748
Tyr Thr Thr Ser Met Ala Met Pro Ile
1 5
<210> 1749
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1749
Tyr Thr Thr Ser Met Ala Met Pro Ile Leu
1 5 10
<210> 1750
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1750
Cys Leu Pro Gly Leu Thr His Pro Ala
1 5
<210> 1751
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1751
Gly Leu Thr His Pro Ala His Gln Pro Leu
1 5 10
<210> 1752
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1752
His Pro Ala His Gln Pro Leu Gly Ser Met
1 5 10
<210> 1753
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1753
Leu Thr His Pro Ala His Gln Pro Leu
1 5
<210> 1754
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1754
Arg Pro Thr Ser Arg Ala Arg Gln Ser Cys
1 5 10
<210> 1755
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1755
Arg Gln Ser Cys Cys Leu Pro Gly Leu
1 5
<210> 1756
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1756
Thr Ser Arg Ala Arg Gln Ser Cys Cys Leu
1 5 10
<210> 1757
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1757
Glu Leu Leu Cys Val Trp Val Ser Ser Ile
1 5 10
<210> 1758
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1758
Glu Trp Lys Val Lys Phe Pro Glu Leu
1 5
<210> 1759
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1759
Lys Phe Pro Glu Leu Leu Cys Val Trp
1 5
<210> 1760
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1760
Leu Leu Cys Val Trp Val Ser Ser Ile
1 5
<210> 1761
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1761
Leu Leu Thr Ser Ser Ser Arg Glu Trp Lys
1 5 10
<210> 1762
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1762
Leu Thr Ser Ser Ser Arg Glu Trp Lys
1 5
<210> 1763
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1763
Tyr Pro Ala Tyr Ser Lys Asp Ser Gly Leu
1 5 10
<210> 1764
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1764
Cys Leu Gln Cys Leu Trp Ala Leu Leu
1 5
<210> 1765
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1765
Cys Gln Trp Gly Pro Cys Leu Gln Cys Leu
1 5 10
<210> 1766
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1766
Gln Trp Gly Pro Cys Leu Gln Cys Leu
1 5
<210> 1767
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1767
Gln Trp Gly Pro Cys Leu Gln Cys Leu Trp
1 5 10
<210> 1768
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1768
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 1769
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1769
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 1770
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1770
Asp Leu His Phe Cys Arg Ser Ser Ile Met
1 5 10
<210> 1771
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1771
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 1772
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1772
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 1773
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1773
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 1774
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1774
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 1775
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1775
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 1776
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1776
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 1777
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1777
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 1778
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1778
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 1779
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1779
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 1780
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1780
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 1781
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1781
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 1782
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1782
Leu Gln His Gly His Arg His Gly Leu
1 5
<210> 1783
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1783
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 1784
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1784
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 1785
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1785
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 1786
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1786
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 1787
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1787
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 1788
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1788
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 1789
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1789
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 1790
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1790
Val Pro Ala Val Pro Phe Asp Leu His Phe
1 5 10
<210> 1791
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1791
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 1792
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1792
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 1793
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1793
Ala Pro Gly Pro Arg Gly Arg Thr Cys
1 5
<210> 1794
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1794
Cys Leu Arg Ser His Thr Cys Pro Pro Arg
1 5 10
<210> 1795
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1795
Cys Leu Trp Cys His Ala Cys Leu His Arg
1 5 10
<210> 1796
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1796
Cys Pro His Leu Gly Ser His Pro Cys
1 5
<210> 1797
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1797
Cys Pro Leu Gly Leu Lys Ser Pro Leu
1 5
<210> 1798
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1798
Cys Pro Arg Ser Cys Arg Cys Pro His
1 5
<210> 1799
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1799
Cys Pro Arg Ser Cys Arg Cys Pro His Leu
1 5 10
<210> 1800
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1800
Cys Ser Leu Pro Leu Gly Asn His Pro Tyr
1 5 10
<210> 1801
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1801
Gly Leu Arg Asn Arg Ile Cys Pro Leu
1 5
<210> 1802
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1802
Gly Leu Arg Ser His Thr Tyr Leu Arg
1 5
<210> 1803
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1803
Gly Leu Arg Ser His Thr Tyr Leu Arg Arg
1 5 10
<210> 1804
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1804
Gly Pro Arg Gly Arg Thr Cys His Pro Gly
1 5 10
<210> 1805
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1805
His Leu Gly Ser His Pro Cys Arg Leu
1 5
<210> 1806
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1806
His Leu Arg Leu His Ala Ser Pro His
1 5
<210> 1807
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1807
His Leu Arg Ser Cys Pro Cys Ser Leu
1 5
<210> 1808
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1808
His Leu Arg Thr His Leu Leu Pro His
1 5
<210> 1809
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1809
His Leu Arg Thr His Leu Leu Pro His His
1 5 10
<210> 1810
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1810
His Leu Arg Tyr Arg Ala Tyr Pro Pro
1 5
<210> 1811
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1811
His Leu Arg Tyr Arg Ala Tyr Pro Pro Cys
1 5 10
<210> 1812
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1812
His Pro His His Leu Arg Thr His Leu
1 5
<210> 1813
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1813
His Pro His His Leu Arg Thr His Leu Leu
1 5 10
<210> 1814
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1814
His Thr Tyr Leu Arg Arg Leu Arg Ser His
1 5 10
<210> 1815
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1815
Leu Pro Cys Pro His Arg Leu Arg Ser Leu
1 5 10
<210> 1816
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1816
Leu Pro His His Arg Arg Thr Arg Ser Cys
1 5 10
<210> 1817
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1817
Leu Pro Leu Gly Asn His Pro Tyr Leu
1 5
<210> 1818
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1818
Leu Pro Arg Pro Leu His Leu Arg Leu
1 5
<210> 1819
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1819
Asn Leu Arg Asn His Thr Cys Pro Pro
1 5
<210> 1820
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1820
Pro Pro Arg Leu Arg Ser Arg Thr Cys Leu
1 5 10
<210> 1821
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1821
Arg Leu His Ala Ser Pro His His Leu
1 5
<210> 1822
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1822
Arg Leu His Ala Ser Pro His His Leu Arg
1 5 10
<210> 1823
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1823
Arg Leu Arg Asp His Ile Cys Pro Leu
1 5
<210> 1824
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1824
Arg Leu Arg Asn Leu Pro Cys Pro His
1 5
<210> 1825
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1825
Arg Leu Arg Asn Leu Pro Cys Pro His Arg
1 5 10
<210> 1826
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1826
Arg Leu Arg Ser His Thr Cys Pro Pro
1 5
<210> 1827
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1827
Arg Leu Arg Ser Leu Pro Arg Pro Leu
1 5
<210> 1828
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1828
Arg Leu Arg Ser Leu Pro Arg Pro Leu His
1 5 10
<210> 1829
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1829
Arg Leu Arg Ser Arg Thr Cys Leu Leu
1 5
<210> 1830
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1830
Arg Asn Arg Ile Cys Pro Leu Ser Leu
1 5
<210> 1831
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1831
Arg Pro Leu His Leu Arg Leu His Ala
1 5
<210> 1832
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1832
Arg Pro Leu His Leu Arg Leu His Ala Ser
1 5 10
<210> 1833
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1833
Arg Ser His Ala Cys Pro Pro Gly Leu Arg
1 5 10
<210> 1834
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1834
Arg Ser His Ala Cys Pro Pro Asn Leu Arg
1 5 10
<210> 1835
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1835
Arg Ser His Ala Tyr Ala Leu Cys Leu Arg
1 5 10
<210> 1836
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1836
Arg Ser His Pro Cys Cys His Tyr Leu Arg
1 5 10
<210> 1837
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1837
Arg Ser His Pro Cys Pro Leu Gly Leu Lys
1 5 10
<210> 1838
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1838
Arg Ser His Thr Cys Pro Pro Ser Leu Arg
1 5 10
<210> 1839
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1839
Arg Ser Leu Pro Arg Pro Leu His Leu Arg
1 5 10
<210> 1840
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1840
Arg Ser Arg Thr Cys Leu Leu Cys Leu
1 5
<210> 1841
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1841
Arg Ser Arg Thr Cys Leu Leu Cys Leu Arg
1 5 10
<210> 1842
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1842
Arg Ser Arg Thr Cys Pro Pro Gly Leu
1 5
<210> 1843
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1843
Arg Ser Arg Thr Cys Pro Pro Gly Leu Arg
1 5 10
<210> 1844
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1844
Arg Thr His Leu Leu Pro His His Arg Arg
1 5 10
<210> 1845
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1845
Arg Thr Arg Ser Cys Pro Cys Arg Trp Arg
1 5 10
<210> 1846
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1846
Arg Tyr Arg Ala Tyr Pro Pro Cys Leu
1 5
<210> 1847
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1847
Arg Tyr Arg Ala Tyr Pro Pro Cys Leu Trp
1 5 10
<210> 1848
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1848
Ser Leu Gly Asn His Leu Cys Pro Leu
1 5
<210> 1849
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1849
Ser Leu Pro Leu Gly Asn His Pro Tyr Leu
1 5 10
<210> 1850
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1850
Ser Leu Pro Arg Pro Leu His Leu Arg Leu
1 5 10
<210> 1851
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1851
Ser Leu Arg Asn Cys Thr Cys Pro Pro Arg
1 5 10
<210> 1852
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1852
Ser Leu Arg Ser His Ala Tyr Ala Leu
1 5
<210> 1853
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1853
Ser Leu Arg Ser His Pro Cys Pro Leu
1 5
<210> 1854
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1854
Ser Pro His His Leu Arg Thr Pro Pro
1 5
<210> 1855
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1855
Ser Pro His His Leu Arg Thr Pro Pro His
1 5 10
<210> 1856
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1856
Ser Pro Leu Arg Ser Gln Ala Asn Ala Leu
1 5 10
<210> 1857
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1857
Tyr Leu Arg Arg Leu Arg Ser His Thr Cys
1 5 10
<210> 1858
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1858
Tyr Leu Arg Ser Arg Asn Ser Ala Pro
1 5
<210> 1859
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1859
Tyr Leu Arg Ser Arg Asn Ser Ala Pro Gly
1 5 10
<210> 1860
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1860
Ala Leu Ala Pro Thr Leu Thr His Met
1 5
<210> 1861
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1861
Ala Leu Ala Pro Thr Leu Thr His Met Leu
1 5 10
<210> 1862
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1862
Leu Leu Gln Val Thr Gln Thr Ser Phe Ala
1 5 10
<210> 1863
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1863
Leu Gln Val Thr Gln Thr Ser Phe Ala Leu
1 5 10
<210> 1864
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1864
Arg Leu Trp His Leu Leu Leu Gln Val
1 5
<210> 1865
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1865
Arg Leu Trp His Leu Leu Leu Gln Val Thr
1 5 10
<210> 1866
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1866
Cys Thr Gln Leu Ala Arg Phe Phe Pro Ile
1 5 10
<210> 1867
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1867
Phe Phe Pro Ile Thr Pro Pro Val Trp
1 5
<210> 1868
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1868
Phe Pro Ile Thr Pro Pro Val Trp His Ile
1 5 10
<210> 1869
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1869
Gly Pro Arg Met Gln Leu Cys Thr Gln Leu
1 5 10
<210> 1870
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1870
Ile Thr Pro Pro Val Trp His Ile Leu
1 5
<210> 1871
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1871
Leu Ala Leu Gly Pro Arg Met Gln Leu
1 5
<210> 1872
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1872
Met Gln Leu Cys Thr Gln Leu Ala Arg Phe
1 5 10
<210> 1873
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1873
Arg Phe Phe Pro Ile Thr Pro Pro Val
1 5
<210> 1874
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1874
Arg Phe Phe Pro Ile Thr Pro Pro Val Trp
1 5 10
<210> 1875
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1875
Arg Met Gln Leu Cys Thr Gln Leu Ala
1 5
<210> 1876
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1876
Arg Met Gln Leu Cys Thr Gln Leu Ala Arg
1 5 10
<210> 1877
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1877
Ser Pro Pro Leu Ala Leu Gly Pro Arg Met
1 5 10
<210> 1878
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1878
Thr Gln Leu Ala Arg Phe Phe Pro Ile
1 5
<210> 1879
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1879
Lys Ser Arg Gln Asn His Leu Gln Leu
1 5
<210> 1880
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1880
Ala Leu Lys Lys Leu Arg Ser Pro Leu
1 5
<210> 1881
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1881
His Leu Gln Leu Lys Ser Cys Arg Arg Lys
1 5 10
<210> 1882
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1882
Lys Ile Ser Asn Trp Ser Leu Lys Lys
1 5
<210> 1883
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1883
Lys Ile Ser Asn Trp Ser Leu Lys Lys Val
1 5 10
<210> 1884
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1884
Lys Leu Arg Ser Pro Leu Trp Ile Phe
1 5
<210> 1885
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1885
Lys Ser Arg Gln Asn His Leu Gln Leu Lys
1 5 10
<210> 1886
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1886
Asn Trp Ser Leu Lys Lys Val Pro Ala Leu
1 5 10
<210> 1887
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1887
Ser Leu Lys Lys Val Pro Ala Leu Lys
1 5
<210> 1888
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1888
Ser Leu Lys Lys Val Pro Ala Leu Lys Lys
1 5 10
<210> 1889
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1889
Ser Gln Lys Ser Arg Gln Asn His Leu
1 5
<210> 1890
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1890
Trp Ser Leu Lys Lys Val Pro Ala Leu
1 5
<210> 1891
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1891
Trp Ser Leu Lys Lys Val Pro Ala Leu Lys
1 5 10
<210> 1892
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1892
Lys Leu Pro Glu Cys Gln Arg Leu Leu
1 5
<210> 1893
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1893
Lys Pro Thr Arg Ala Ala Thr Val Ser Val
1 5 10
<210> 1894
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1894
Leu Pro Pro Trp Pro Leu His Gln Gln Leu
1 5 10
<210> 1895
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1895
Leu Pro Arg Lys Pro Thr Arg Ala Ala
1 5
<210> 1896
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1896
Leu Pro Arg Lys Pro Thr Arg Ala Ala Thr
1 5 10
<210> 1897
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1897
Gln Gln Leu Leu His Arg Arg Pro Leu
1 5
<210> 1898
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1898
Arg Leu Leu Pro Pro Trp Pro Leu His
1 5
<210> 1899
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1899
Ala Pro Ala Ser Ala Pro Trp Pro Ser Thr
1 5 10
<210> 1900
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1900
Ala Pro Trp Pro Ser Thr Ser Ser His
1 5
<210> 1901
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1901
Arg Pro Ala Pro Ala Ser Ala Pro Trp
1 5
<210> 1902
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1902
Trp Pro Ser Thr Ser Ser His Ser Thr
1 5
<210> 1903
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1903
Arg Val Gln Asn Gln Gly His Leu Leu
1 5
<210> 1904
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1904
Phe Leu Pro Ile Ser His Cys Gln Cys Ile
1 5 10
<210> 1905
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1905
Phe Trp Leu Thr Lys Leu Asn Tyr Leu
1 5
<210> 1906
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1906
His Leu Ser Met Leu Thr Asp Ser Leu
1 5
<210> 1907
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1907
His Thr Met Gly Phe Trp Leu Thr Lys
1 5
<210> 1908
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1908
His Thr Met Gly Phe Trp Leu Thr Lys Leu
1 5 10
<210> 1909
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1909
Lys Leu Asn Tyr Leu Cys His Leu Ser Met
1 5 10
<210> 1910
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1910
Leu Pro Ile Ser His Cys Gln Cys Ile
1 5
<210> 1911
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1911
Leu Pro Ile Ser His Cys Gln Cys Ile Leu
1 5 10
<210> 1912
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1912
Leu Thr Asp Ser Leu Phe Leu Pro Ile
1 5
<210> 1913
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1913
Leu Thr Lys Leu Asn Tyr Leu Cys His Leu
1 5 10
<210> 1914
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1914
Met Leu Thr Asp Ser Leu Phe Leu Pro Ile
1 5 10
<210> 1915
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1915
Met Gln Gly His Thr Met Gly Phe Trp Leu
1 5 10
<210> 1916
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1916
Asn Tyr Leu Cys His Leu Ser Met Leu
1 5
<210> 1917
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1917
Ser Met Leu Thr Asp Ser Leu Phe Leu
1 5
<210> 1918
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1918
Thr Met Gly Phe Trp Leu Thr Lys Leu
1 5
<210> 1919
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1919
Tyr Leu Cys His Leu Ser Met Leu Thr
1 5
<210> 1920
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1920
Ile Leu Asp Glu Ala Tyr Val Met Ala Tyr
1 5 10
<210> 1921
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1921
Val Met Ala Tyr Val Met Ala Gly Val
1 5
<210> 1922
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1922
Tyr Val Met Ala Tyr Val Met Ala Gly
1 5
<210> 1923
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1923
Tyr Val Met Ala Tyr Val Met Ala Gly Val
1 5 10
<210> 1924
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 1924
Ile Phe Ile Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10 15
Leu Arg Glu Met Arg His Arg
20
<210> 1925
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1925
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 1926
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1926
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 1927
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1927
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 1928
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1928
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 1929
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1929
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 1930
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1930
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 1931
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1931
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 1932
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1932
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 1933
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1933
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 1934
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1934
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 1935
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1935
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 1936
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1936
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 1937
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1937
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 1938
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1938
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 1939
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1939
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 1940
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1940
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 1941
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1941
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 1942
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 1942
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 1943
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1943
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 1944
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1944
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 1945
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1945
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 1946
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1946
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 1947
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1947
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 1948
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1948
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 1949
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1949
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 1950
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1950
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 1951
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1951
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 1952
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1952
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 1953
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1953
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 1954
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1954
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 1955
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1955
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 1956
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1956
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 1957
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1957
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 1958
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1958
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 1959
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 1959
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 1960
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1960
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 1961
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1961
Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 1962
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1962
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 1963
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1963
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 1964
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1964
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 1965
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1965
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 1966
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 1966
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 1967
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 1967
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 1968
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 1968
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 1969
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 1969
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 1970
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1970
Val Ala Asp Gly Leu Ile Thr Thr Leu His Tyr Pro Ala Pro Lys Arg
1 5 10 15
Asn Lys Pro Thr Val Tyr Gly Val Ser Pro Asn Tyr Asp Lys Trp Glu
20 25 30
Met Glu Arg Thr Asp Ile Thr Met Lys His Lys Leu Gly Gly Gly Gln
35 40 45
Tyr Gly Lys Val Tyr Glu Gly Val Trp Lys Lys Tyr Ser Leu Thr Val
50 55 60
Ala Val Lys Thr Leu Lys Glu Asp Thr Met Glu Val Glu Glu Phe Leu
65 70 75 80
Lys Glu Ala Ala Val Met Lys Glu Ile Lys His Pro Asn Leu Val Gln
85 90 95
Leu Leu Gly Val Cys
100
<210> 1971
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1971
Val Ala Asp Gly Leu Ile Thr Thr Leu His Tyr Pro Ala Pro Lys Arg
1 5 10 15
Asn Lys Pro Thr Val Tyr Gly Val Ser Pro Asn Tyr Asp Lys Trp Glu
20 25 30
Met Glu Arg Thr Asp Ile Thr Met Lys His Lys Leu Gly Gly Gly Gln
35 40 45
Tyr Gly Val Val Tyr Glu Gly Val Trp Lys Lys Tyr Ser Leu Thr Val
50 55 60
Ala Val Lys Thr Leu Lys Glu Asp Thr Met Glu Val Glu Glu Phe Leu
65 70 75 80
Lys Glu Ala Ala Val Met Lys Glu Ile Lys His Pro Asn Leu Val Gln
85 90 95
Leu Leu Gly Val Cys
100
<210> 1972
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1972
Leu Leu Gly Val Cys Thr Arg Glu Pro Pro Phe Tyr Ile Ile Thr Glu
1 5 10 15
Phe Met Thr Tyr Gly Asn Leu Leu Asp Tyr Leu Arg Glu Cys Asn Arg
20 25 30
Gln Glu Val Asn Ala Val Val Leu Leu Tyr Met Ala Thr Gln Ile Ser
35 40 45
Ser Ala Thr Glu Tyr Leu Glu Lys Lys Asn Phe Ile His Arg Asp Leu
50 55 60
Ala Ala Arg Asn Cys Leu Val Gly Glu Asn His Leu Val Lys Val Ala
65 70 75 80
Asp Phe Gly Leu Ser Arg Leu Met Thr Gly Asp Thr Tyr Thr Ala His
85 90 95
Ala Gly Ala Lys Phe
100
<210> 1973
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1973
Ser Leu Thr Val Ala Val Lys Thr Leu Lys Glu Asp Thr Met Glu Val
1 5 10 15
Glu Glu Phe Leu Lys Glu Ala Ala Val Met Lys Glu Ile Lys His Pro
20 25 30
Asn Leu Val Gln Leu Leu Gly Val Cys Thr Arg Glu Pro Pro Phe Tyr
35 40 45
Ile Ile Ile Glu Phe Met Thr Tyr Gly Asn Leu Leu Asp Tyr Leu Arg
50 55 60
Glu Cys Asn Arg Gln Glu Val Asn Ala Val Val Leu Leu Tyr Met Ala
65 70 75 80
Thr Gln Ile Ser Ser Ala Met Glu Tyr Leu Glu Lys Lys Asn Phe Ile
85 90 95
His Arg Asp Leu Ala
100
<210> 1974
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1974
Ser Thr Val Ala Asp Gly Leu Ile Thr Thr Leu His Tyr Pro Ala Pro
1 5 10 15
Lys Arg Asn Lys Pro Thr Val Tyr Gly Val Ser Pro Asn Tyr Asp Lys
20 25 30
Trp Glu Met Glu Arg Thr Asp Ile Thr Met Lys His Lys Leu Gly Gly
35 40 45
Gly Gln His Gly Glu Val Tyr Glu Gly Val Trp Lys Lys Tyr Ser Leu
50 55 60
Thr Val Ala Val Lys Thr Leu Lys Glu Asp Thr Met Glu Val Glu Glu
65 70 75 80
Phe Leu Lys Glu Ala Ala Val Met Lys Glu Ile Lys His Pro Asn Leu
85 90 95
Val Gln Leu Leu Gly
100
<210> 1975
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1975
Ser Ser Leu Ala Met Leu Asp Leu Leu His Val Ala Arg Asp Ile Ala
1 5 10 15
Cys Gly Cys Gln Tyr Leu Glu Glu Asn His Phe Ile His Arg Asp Ile
20 25 30
Ala Ala Arg Asn Cys Leu Leu Thr Cys Pro Gly Pro Gly Arg Val Ala
35 40 45
Lys Ile Ala Asp Phe Gly Met Ala Arg Asp Ile Tyr Arg Ala Ser Tyr
50 55 60
Tyr Arg Lys Gly Gly Cys Ala Met Leu Pro Val Lys Trp Met Pro Pro
65 70 75 80
Glu Ala Phe Met Glu Gly Ile Phe Thr Ser Lys Thr Asp Thr Trp Ser
85 90 95
Phe Gly Val Leu Leu
100
<210> 1976
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1976
Gln Val Ala Val Lys Thr Leu Pro Glu Val Cys Ser Glu Gln Asp Glu
1 5 10 15
Leu Asp Phe Leu Met Glu Ala Leu Ile Ile Ser Lys Phe Asn His Gln
20 25 30
Asn Ile Val Arg Cys Ile Gly Val Ser Leu Gln Ser Leu Pro Arg Phe
35 40 45
Ile Leu Met Glu Leu Met Ala Gly Gly Asp Leu Lys Ser Phe Leu Arg
50 55 60
Glu Thr Arg Pro Arg Pro Ser Gln Pro Ser Ser Leu Ala Met Leu Asp
65 70 75 80
Leu Leu His Val Ala Arg Asp Ile Ala Cys Gly Cys Gln Tyr Leu Glu
85 90 95
Glu Asn His Phe Ile
100
<210> 1977
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1977
Met Ile Lys Leu Ile Asp Ile Ala Arg Gln Thr Ala Gln Gly Met Asp
1 5 10 15
Tyr Leu His Ala Lys Ser Ile Ile His Arg Asp Leu Lys Ser Asn Asn
20 25 30
Ile Phe Leu His Glu Asp Leu Thr Val Lys Ile Gly Asp Phe Gly Leu
35 40 45
Ala Thr Glu Lys Ser Arg Trp Ser Gly Ser His Gln Phe Glu Gln Leu
50 55 60
Ser Gly Ser Ile Leu Trp Met Ala Pro Glu Val Ile Arg Met Gln Asp
65 70 75 80
Lys Asn Pro Tyr Ser Phe Gln Ser Asp Val Tyr Ala Phe Gly Ile Val
85 90 95
Leu Tyr Glu Leu Met
100
<210> 1978
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1978
Met Ile Lys Glu Gly Ser Met Ser Glu Asp Glu Phe Ile Glu Glu Ala
1 5 10 15
Lys Val Met Met Asn Leu Ser His Glu Lys Leu Val Gln Leu Tyr Gly
20 25 30
Val Cys Thr Lys Gln Arg Pro Ile Phe Ile Ile Thr Glu Tyr Met Ala
35 40 45
Asn Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg His Arg Phe Gln
50 55 60
Thr Gln Gln Leu Leu Glu Met Cys Lys Asp Val Cys Glu Ala Met Glu
65 70 75 80
Tyr Leu Glu Ser Lys Gln Phe Leu His Arg Asp Leu Ala Ala Arg Asn
85 90 95
Cys Leu Val Asn Asp
100
<210> 1979
<211> 93
<212> БЕЛОК
<213> Homo sapiens
<400> 1979
Met Gly Phe Gly Asp Leu Lys Ser Pro Ala Gly Leu Gln Val Leu Asn
1 5 10 15
Asp Tyr Leu Ala Asp Lys Ser Tyr Ile Glu Gly Tyr Val Pro Ser Gln
20 25 30
Ala Asp Val Ala Val Phe Glu Ala Val Ser Gly Pro Pro Pro Ala Asp
35 40 45
Leu Cys His Ala Leu Arg Trp Tyr Asn His Ile Lys Ser Tyr Glu Lys
50 55 60
Glu Lys Ala Ser Leu Pro Gly Val Lys Lys Ala Leu Gly Lys Tyr Gly
65 70 75 80
Pro Ala Asp Val Glu Asp Thr Thr Gly Ser Gly Ala Thr
85 90
<210> 1980
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1980
Glu Arg Cys Glu Val Val Met Gly Asn Leu Glu Ile Val Leu Thr Gly
1 5 10 15
His Asn Ala Asp Leu Ser Phe Leu Gln Trp Ile Arg Glu Val Thr Gly
20 25 30
Tyr Val Leu Val Ala Met Asn Glu Phe Ser Thr Leu Pro Leu Pro Asn
35 40 45
Leu Arg Met Val Arg Gly Thr Gln Val Tyr Asp Gly Lys Phe Ala Ile
50 55 60
Phe Val Met Leu Asn Tyr Asn Thr Asn Ser Ser His Ala Leu Arg Gln
65 70 75 80
Leu Arg Leu Thr Gln Leu Thr Glu Ile Leu Ser Gly Gly Val Tyr Ile
85 90 95
Glu Lys Asn Asp Lys
100
<210> 1981
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1981
His Leu Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg
1 5 10 15
Leu Ala Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn
20 25 30
Lys Gly Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro
35 40 45
Leu Tyr Gly Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu His Ala
50 55 60
Pro Thr Ser Arg Gly Gly Ala Ser Val Glu Glu Thr Asp Gln Ser His
65 70 75 80
Leu Ala Thr Ala Gly Ser Thr Ser Ser His Ser Leu Gln Lys Tyr Tyr
85 90 95
Ile Thr Gly Glu Ala
100
<210> 1982
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1982
Asn Gln Gly Lys Cys Val Glu Gly Met Val Glu Ile Phe Asp Met Leu
1 5 10 15
Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu
20 25 30
Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr
35 40 45
Phe Leu Pro Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His
50 55 60
Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys
65 70 75 80
Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu
85 90 95
Leu Ile Leu Ser His
100
<210> 1983
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1983
Ile His Leu Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln
1 5 10 15
Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser
20 25 30
Asn Lys Gly Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val
35 40 45
Pro Leu Cys Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu His
50 55 60
Ala Pro Thr Ser Arg Gly Gly Ala Ser Val Glu Glu Thr Asp Gln Ser
65 70 75 80
His Leu Ala Thr Ala Gly Ser Thr Ser Ser His Ser Leu Gln Lys Tyr
85 90 95
Tyr Ile Thr Gly Glu
100
<210> 1984
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1984
Ile His Leu Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln
1 5 10 15
Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser
20 25 30
Asn Lys Gly Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val
35 40 45
Pro Leu Asn Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu His
50 55 60
Ala Pro Thr Ser Arg Gly Gly Ala Ser Val Glu Glu Thr Asp Gln Ser
65 70 75 80
His Leu Ala Thr Ala Gly Ser Thr Ser Ser His Ser Leu Gln Lys Tyr
85 90 95
Tyr Ile Thr Gly Glu
100
<210> 1985
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1985
Ile His Leu Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln
1 5 10 15
Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser
20 25 30
Asn Lys Gly Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val
35 40 45
Pro Leu Ser Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu His
50 55 60
Ala Pro Thr Ser Arg Gly Gly Ala Ser Val Glu Glu Thr Asp Gln Ser
65 70 75 80
His Leu Ala Thr Ala Gly Ser Thr Ser Ser His Ser Leu Gln Lys Tyr
85 90 95
Tyr Ile Thr Gly Glu
100
<210> 1986
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1986
His Arg Ile Gly Gly Ile Lys Leu Arg His Gln Gln Trp Ser Leu Val
1 5 10 15
Met Glu Ser Val Val Pro Ser Asp Arg Gly Asn Tyr Thr Cys Val Val
20 25 30
Glu Asn Lys Phe Gly Ser Ile Arg Gln Thr Tyr Thr Leu Asp Val Leu
35 40 45
Glu Arg Cys Pro His Arg Pro Ile Leu Gln Ala Gly Leu Pro Ala Asn
50 55 60
Gln Thr Ala Val Leu Gly Ser Asp Val Glu Phe His Cys Lys Val Tyr
65 70 75 80
Ser Asp Ala Gln Pro His Ile Gln Trp Leu Lys His Val Glu Val Asn
85 90 95
Gly Ser Lys Val Gly
100
<210> 1987
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1987
Ala Val Lys Leu Ser Asp Ser Arg Ile Ala Leu Lys Ser Gly Tyr Gly
1 5 10 15
Lys Tyr Leu Gly Ile Asn Ser Asp Glu Leu Val Gly His Ser Asp Ala
20 25 30
Ile Gly Pro Arg Glu Gln Trp Glu Pro Val Phe Gln Asn Gly Lys Met
35 40 45
Ala Leu Ser Ala Ser Asn Ser Cys Phe Ile Arg Cys Asn Glu Ala Gly
50 55 60
Asp Ile Glu Ala Lys Ser Lys Thr Ala Gly Glu Glu Glu Met Ile Lys
65 70 75 80
Ile Arg Ser Cys Ala Glu Lys Glu Thr Lys Lys Lys Asp Asp Ile Pro
85 90 95
Glu Glu Asp Lys Gly
100
<210> 1988
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1988
Gly Ser Gly Ala Phe Gly Thr Val Tyr Lys Gly Ile Trp Ile Pro Asp
1 5 10 15
Gly Glu Asn Val Lys Ile Pro Val Ala Ile Lys Val Leu Arg Glu Asn
20 25 30
Thr Ser Pro Lys Ala Asn Lys Glu Ile Leu Asp Glu Ala Tyr Val Met
35 40 45
Ala Gly Leu Gly Ser Pro Tyr Val Ser Arg Leu Leu Gly Ile Cys Leu
50 55 60
Thr Ser Thr Val Gln Leu Val Thr Gln Leu Met Pro Tyr Gly Cys Leu
65 70 75 80
Leu Asp His Val Arg Glu Asn Arg Gly Arg Leu Gly Ser Gln Asp Leu
85 90 95
Leu Asn Trp Cys Met
100
<210> 1989
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1989
Arg Val Glu Glu Phe Lys Leu Lys Gln Met Trp Lys Ser Pro Asn Gly
1 5 10 15
Thr Ile Arg Asn Ile Leu Gly Gly Thr Val Phe Arg Glu Ala Ile Ile
20 25 30
Cys Lys Asn Ile Pro Arg Leu Val Ser Gly Trp Val Lys Pro Ile Ile
35 40 45
Ile Gly His His Ala Tyr Gly Asp Gln Tyr Arg Ala Thr Asp Phe Val
50 55 60
Val Pro Gly Pro Gly Lys Val Glu Ile Thr Tyr Thr Pro Ser Asp Gly
65 70 75 80
Thr Gln Lys Val Thr Tyr Leu Val His Asn Phe Glu Glu Gly Gly Gly
85 90 95
Val Ala Met Gly Met
100
<210> 1990
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1990
Arg Val Glu Glu Phe Lys Leu Lys Gln Met Trp Lys Ser Pro Asn Gly
1 5 10 15
Thr Ile Arg Asn Ile Leu Gly Gly Thr Val Phe Arg Glu Ala Ile Ile
20 25 30
Cys Lys Asn Ile Pro Arg Leu Val Ser Gly Trp Val Lys Pro Ile Ile
35 40 45
Ile Gly Cys His Ala Tyr Gly Asp Gln Tyr Arg Ala Thr Asp Phe Val
50 55 60
Val Pro Gly Pro Gly Lys Val Glu Ile Thr Tyr Thr Pro Ser Asp Gly
65 70 75 80
Thr Gln Lys Val Thr Tyr Leu Val His Asn Phe Glu Glu Gly Gly Gly
85 90 95
Val Ala Met Gly Met
100
<210> 1991
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1991
Arg Val Glu Glu Phe Lys Leu Lys Gln Met Trp Lys Ser Pro Asn Gly
1 5 10 15
Thr Ile Arg Asn Ile Leu Gly Gly Thr Val Phe Arg Glu Ala Ile Ile
20 25 30
Cys Lys Asn Ile Pro Arg Leu Val Ser Gly Trp Val Lys Pro Ile Ile
35 40 45
Ile Gly Gly His Ala Tyr Gly Asp Gln Tyr Arg Ala Thr Asp Phe Val
50 55 60
Val Pro Gly Pro Gly Lys Val Glu Ile Thr Tyr Thr Pro Ser Asp Gly
65 70 75 80
Thr Gln Lys Val Thr Tyr Leu Val His Asn Phe Glu Glu Gly Gly Gly
85 90 95
Val Ala Met Gly Met
100
<210> 1992
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1992
Arg Val Glu Glu Phe Lys Leu Lys Gln Met Trp Lys Ser Pro Asn Gly
1 5 10 15
Thr Ile Arg Asn Ile Leu Gly Gly Thr Val Phe Arg Glu Ala Ile Ile
20 25 30
Cys Lys Asn Ile Pro Arg Leu Val Ser Gly Trp Val Lys Pro Ile Ile
35 40 45
Ile Gly Ser His Ala Tyr Gly Asp Gln Tyr Arg Ala Thr Asp Phe Val
50 55 60
Val Pro Gly Pro Gly Lys Val Glu Ile Thr Tyr Thr Pro Ser Asp Gly
65 70 75 80
Thr Gln Lys Val Thr Tyr Leu Val His Asn Phe Glu Glu Gly Gly Gly
85 90 95
Val Ala Met Gly Met
100
<210> 1993
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1993
Val Ala Val Lys Met Leu Lys Pro Ser Ala His Leu Thr Glu Arg Glu
1 5 10 15
Ala Leu Met Ser Glu Leu Lys Val Leu Ser Tyr Leu Gly Asn His Met
20 25 30
Asn Ile Val Asn Leu Leu Gly Ala Cys Thr Ile Gly Gly Pro Thr Leu
35 40 45
Val Ile Ile Glu Tyr Cys Cys Tyr Gly Asp Leu Leu Asn Phe Leu Arg
50 55 60
Arg Lys Arg Asp Ser Phe Ile Cys Ser Lys Gln Glu Asp His Ala Glu
65 70 75 80
Ala Ala Leu Tyr Lys Asn Leu Leu His Ser Lys Glu Ser Ser Cys Ser
85 90 95
Asp Ser Thr Asn Glu
100
<210> 1994
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1994
Val Glu Ala Thr Ala Tyr Gly Leu Ile Lys Ser Asp Ala Ala Met Thr
1 5 10 15
Val Ala Val Lys Met Leu Lys Pro Ser Ala His Leu Thr Glu Arg Glu
20 25 30
Ala Leu Met Ser Glu Leu Lys Val Leu Ser Tyr Leu Gly Asn His Met
35 40 45
Asn Ile Ala Asn Leu Leu Gly Ala Cys Thr Ile Gly Gly Pro Thr Leu
50 55 60
Val Ile Thr Glu Tyr Cys Cys Tyr Gly Asp Leu Leu Asn Phe Leu Arg
65 70 75 80
Arg Lys Arg Asp Ser Phe Ile Cys Ser Lys Gln Glu Asp His Ala Glu
85 90 95
Ala Ala Leu Tyr Lys
100
<210> 1995
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1995
Ile Ser Glu Leu Gly Ala Gly Asn Gly Gly Val Val Phe Lys Val Ser
1 5 10 15
His Lys Pro Ser Gly Leu Val Met Ala Arg Lys Leu Ile His Leu Glu
20 25 30
Ile Lys Pro Ala Ile Arg Asn Gln Ile Ile Arg Glu Leu Gln Val Leu
35 40 45
His Glu Ser Asn Ser Pro Tyr Ile Val Gly Phe Tyr Gly Ala Phe Tyr
50 55 60
Ser Asp Gly Glu Ile Ser Ile Cys Met Glu His Met Asp Gly Gly Ser
65 70 75 80
Leu Asp Gln Val Leu Lys Lys Ala Gly Arg Ile Pro Glu Gln Ile Leu
85 90 95
Gly Lys Val Ser Ile
100
<210> 1996
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1996
Leu Gly Ala Gly Asn Gly Gly Val Val Phe Lys Val Ser His Lys Pro
1 5 10 15
Ser Gly Leu Val Met Ala Arg Lys Leu Ile His Leu Glu Ile Lys Pro
20 25 30
Ala Ile Arg Asn Gln Ile Ile Arg Glu Leu Gln Val Leu His Glu Cys
35 40 45
Asn Ser Leu Tyr Ile Val Gly Phe Tyr Gly Ala Phe Tyr Ser Asp Gly
50 55 60
Glu Ile Ser Ile Cys Met Glu His Met Asp Gly Gly Ser Leu Asp Gln
65 70 75 80
Val Leu Lys Lys Ala Gly Arg Ile Pro Glu Gln Ile Leu Gly Lys Val
85 90 95
Ser Ile Ala Val Ile
100
<210> 1997
<211> 89
<212> БЕЛОК
<213> Homo sapiens
<400> 1997
Met Pro Leu Asn Val Ser Phe Thr Asn Arg Asn Tyr Asp Leu Asp Tyr
1 5 10 15
Asp Ser Val Gln Pro Tyr Phe Tyr Cys Asp Glu Glu Glu Asn Phe Tyr
20 25 30
Gln Gln Gln Gln Gln Ser Asp Leu Gln Pro Pro Ala Pro Ser Glu Asp
35 40 45
Ile Trp Lys Lys Phe Glu Leu Leu Pro Thr Pro Pro Leu Ser Pro Ser
50 55 60
Arg Arg Ser Gly Leu Cys Ser Pro Ser Tyr Val Ala Val Thr Pro Phe
65 70 75 80
Ser Leu Arg Gly Asp Asn Asp Gly Gly
85
<210> 1998
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1998
Phe Thr Asn Arg Asn Tyr Asp Leu Asp Tyr Asp Ser Val Gln Pro Tyr
1 5 10 15
Phe Tyr Cys Asp Glu Glu Glu Asn Phe Tyr Gln Gln Gln Gln Gln Ser
20 25 30
Glu Leu Gln Pro Pro Ala Pro Ser Glu Asp Ile Trp Lys Lys Phe Glu
35 40 45
Leu Leu Ser Thr Pro Pro Leu Ser Pro Ser Arg Arg Ser Gly Leu Cys
50 55 60
Ser Pro Ser Tyr Val Ala Val Thr Pro Phe Ser Leu Arg Gly Asp Asn
65 70 75 80
Asp Gly Gly Gly Gly Ser Phe Ser Thr Ala Asp Gln Leu Glu Met Val
85 90 95
Thr Glu Leu Leu Gly
100
<210> 1999
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 1999
Thr Asn Arg Asn Tyr Asp Leu Asp Tyr Asp Ser Val Gln Pro Tyr Phe
1 5 10 15
Tyr Cys Asp Glu Glu Glu Asn Phe Tyr Gln Gln Gln Gln Gln Ser Glu
20 25 30
Leu Gln Pro Pro Ala Pro Ser Glu Asp Ile Trp Lys Lys Phe Glu Leu
35 40 45
Leu Pro Ile Pro Pro Leu Ser Pro Ser Arg Arg Ser Gly Leu Cys Ser
50 55 60
Pro Ser Tyr Val Ala Val Thr Pro Phe Ser Leu Arg Gly Asp Asn Asp
65 70 75 80
Gly Gly Gly Gly Ser Phe Ser Thr Ala Asp Gln Leu Glu Met Val Thr
85 90 95
Glu Leu Leu Gly Gly
100
<210> 2000
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2000
Val Ala Val Lys Met Leu Lys Pro Thr Ala Arg Ser Ser Glu Lys Gln
1 5 10 15
Ala Leu Met Ser Glu Leu Lys Ile Met Thr His Leu Gly Pro His Leu
20 25 30
Asn Ile Val Asn Leu Leu Gly Ala Cys Thr Lys Ser Gly Pro Ile Tyr
35 40 45
Ile Ile Ile Glu Tyr Cys Phe Tyr Gly Asp Leu Val Asn Tyr Leu His
50 55 60
Lys Asn Arg Asp Ser Phe Leu Ser His His Pro Glu Lys Pro Lys Lys
65 70 75 80
Glu Leu Asp Ile Phe Gly Leu Asn Pro Ala Asp Glu Ser Thr Arg Ser
85 90 95
Tyr Val Ile Leu Ser
100
<210> 2001
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2001
Ile Glu Glu His Ala Asn Trp Ser Val Ser Arg Glu Ala Gly Phe Ser
1 5 10 15
Tyr Ser His Ala Gly Leu Ser Asn Arg Leu Ala Arg Asp Asn Glu Leu
20 25 30
Arg Glu Asn Asp Lys Glu Gln Leu Lys Ala Ile Ser Thr Arg Asp Pro
35 40 45
Leu Ser Lys Ile Thr Glu Gln Glu Lys Asp Phe Leu Trp Ser His Arg
50 55 60
His Tyr Cys Val Thr Ile Pro Glu Ile Leu Pro Lys Leu Leu Leu Ser
65 70 75 80
Val Lys Trp Asn Ser Arg Asp Glu Val Ala Gln Met Tyr Cys Leu Val
85 90 95
Lys Asp Trp Pro Pro
100
<210> 2002
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2002
His Ala Asn Trp Ser Val Ser Arg Glu Ala Gly Phe Ser Tyr Ser His
1 5 10 15
Ala Gly Leu Ser Asn Arg Leu Ala Arg Asp Asn Glu Leu Arg Glu Asn
20 25 30
Asp Lys Glu Gln Leu Lys Ala Ile Ser Thr Arg Asp Pro Leu Ser Glu
35 40 45
Ile Thr Lys Gln Glu Lys Asp Phe Leu Trp Ser His Arg His Tyr Cys
50 55 60
Val Thr Ile Pro Glu Ile Leu Pro Lys Leu Leu Leu Ser Val Lys Trp
65 70 75 80
Asn Ser Arg Asp Glu Val Ala Gln Met Tyr Cys Leu Val Lys Asp Trp
85 90 95
Pro Pro Ile Lys Pro
100
<210> 2003
<211> 72
<212> БЕЛОК
<213> Homo sapiens
<400> 2003
Leu Phe Ile Asn Leu Phe Ser Met Met Leu Gly Ser Gly Met Pro Glu
1 5 10 15
Leu Gln Ser Phe Asp Asp Ile Ala Tyr Ile Arg Lys Thr Leu Ala Leu
20 25 30
Asp Lys Thr Glu Gln Glu Ala Leu Glu Tyr Phe Met Lys Gln Met Asn
35 40 45
Asp Ala Arg His Gly Gly Trp Thr Thr Lys Met Asp Trp Ile Phe His
50 55 60
Thr Ile Lys Gln His Ala Leu Asn
65 70
<210> 2004
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2004
Gln Arg Gly Gly Val Ile Thr Asp Glu Glu Glu Thr Ser Lys Lys Ile
1 5 10 15
Ala Asp Gln Leu Asp Asn Ile Val Asp Met Arg Glu Tyr Asp Val Pro
20 25 30
Tyr His Ile Arg Leu Ser Ile Asp Ile Glu Thr Thr Lys Leu Pro Leu
35 40 45
Lys Phe Arg Asp Ala Glu Thr Asp Gln Ile Met Met Ile Ser Tyr Met
50 55 60
Ile Asp Gly Gln Gly Tyr Leu Ile Thr Asn Arg Glu Ile Val Ser Glu
65 70 75 80
Asp Ile Glu Asp Phe Glu Phe Thr Pro Lys Pro Glu Tyr Glu Gly Pro
85 90 95
Phe Cys Val Phe Asn
100
<210> 2005
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2005
Lys Phe Asn Cys Arg Val Ala Gln Tyr Pro Phe Glu Asp His Asn Pro
1 5 10 15
Pro Gln Leu Glu Leu Ile Lys Pro Phe Cys Glu Asp Leu Asp Gln Trp
20 25 30
Leu Ser Glu Asp Asp Asn His Val Ala Ala Ile His Cys Lys Ala Gly
35 40 45
Lys Gly Gln Thr Gly Val Met Ile Cys Ala Tyr Leu Leu His Arg Gly
50 55 60
Lys Phe Leu Lys Ala Gln Glu Ala Leu Asp Phe Tyr Gly Glu Val Arg
65 70 75 80
Thr Arg Asp Lys Lys Gly Val Thr Ile Pro Ser Gln Arg Arg Tyr Val
85 90 95
Tyr Tyr Tyr Ser Tyr
100
<210> 2006
<211> 79
<212> БЕЛОК
<213> Homo sapiens
<400> 2006
Met Gln Ala Ile Lys Cys Val Val Val Gly Asp Gly Ala Val Gly Lys
1 5 10 15
Thr Cys Leu Leu Ile Ser Tyr Thr Thr Asn Ala Phe Ser Gly Glu Tyr
20 25 30
Ile Pro Thr Val Phe Asp Asn Tyr Ser Ala Asn Val Met Val Asp Gly
35 40 45
Lys Pro Val Asn Leu Gly Leu Trp Asp Thr Ala Gly Gln Glu Asp Tyr
50 55 60
Asp Arg Leu Arg Pro Leu Ser Tyr Pro Gln Thr Val Gly Glu Thr
65 70 75
<210> 2007
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2007
Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn
1 5 10 15
Thr Phe Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly
20 25 30
Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys
35 40 45
Met Gly Ser Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu
50 55 60
Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val
65 70 75 80
Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg
85 90 95
Lys Lys Gly Glu Pro
100
<210> 2008
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2008
Thr Tyr Ser Pro Ala Leu Asn Lys Met Phe Cys Gln Leu Ala Lys Thr
1 5 10 15
Cys Pro Val Gln Leu Trp Val Asp Ser Thr Pro Pro Pro Gly Thr Arg
20 25 30
Val Arg Ala Met Ala Ile Tyr Lys Gln Ser Gln His Met Thr Glu Val
35 40 45
Val Arg His Cys Pro His His Glu Arg Cys Ser Asp Ser Asp Gly Leu
50 55 60
Ala Pro Pro Gln His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu
65 70 75 80
Tyr Leu Asp Asp Arg Asn Thr Phe Arg His Ser Val Val Val Pro Tyr
85 90 95
Glu Pro Pro Glu Val
100
<210> 2009
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2009
Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg
1 5 10 15
His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys
20 25 30
Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly
35 40 45
Met Asn Gln Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser
50 55 60
Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys
65 70 75 80
Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly
85 90 95
Glu Pro His His Glu
100
<210> 2010
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2010
Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg
1 5 10 15
His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys
20 25 30
Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly
35 40 45
Met Asn Trp Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser
50 55 60
Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys
65 70 75 80
Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly
85 90 95
Glu Pro His His Glu
100
<210> 2011
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2011
Pro Glu Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys
1 5 10 15
Asn Ser Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile
20 25 30
Ile Thr Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe
35 40 45
Glu Val Cys Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu
50 55 60
Glu Asn Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly
65 70 75 80
Ser Thr Lys Arg Ala Leu Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro
85 90 95
Lys Lys Lys Pro Leu
100
<210> 2012
<211> 53
<212> БЕЛОК
<213> Homo sapiens
<400> 2012
Gly Val Glu Pro Cys Tyr Gly Asp Lys Asp Lys Arg Arg His Cys Phe
1 5 10 15
Ala Thr Trp Lys Asn Ile Ser Gly Ser Ile Glu Ile Val Lys Gln Gly
20 25 30
Cys Trp Leu Asp Asp Ile Asn Cys Tyr Asp Arg Thr Asp Cys Val Glu
35 40 45
Lys Lys Arg Gln Pro
50
<210> 2013
<211> 103
<212> БЕЛОК
<213> Homo sapiens
<400> 2013
Gly Val Glu Pro Cys Tyr Gly Asp Lys Asp Lys Arg Arg His Cys Phe
1 5 10 15
Ala Thr Trp Lys Asn Ile Ser Gly Ser Ile Glu Ile Val Lys Gln Gly
20 25 30
Cys Trp Leu Asp Asp Ile Asn Cys Tyr Asp Arg Thr Asp Cys Val Glu
35 40 45
Lys Lys Thr Ala Leu Lys Tyr Ile Phe Val Ala Val Arg Ala Ile Cys
50 55 60
Val Met Lys Ser Phe Leu Ile Phe Arg Arg Trp Lys Ser His Ser Pro
65 70 75 80
Leu Gln Ile Gln Leu His Leu Ser His Pro Ile Thr Thr Ser Cys Ser
85 90 95
Ile Pro Trp Cys His Leu Cys
100
<210> 2014
<211> 118
<212> БЕЛОК
<213> Homo sapiens
<400> 2014
Thr Ala Glu Ala Val Asn Val Ala Ile Ala Ala Pro Pro Ser Glu Gly
1 5 10 15
Glu Ala Asn Ala Glu Leu Cys Arg Tyr Leu Ser Lys Val Leu Glu Leu
20 25 30
Arg Lys Ser Asp Val Val Leu Asp Lys Val Gly Leu Ala Leu Phe Phe
35 40 45
Phe Phe Phe Glu Thr Lys Ser Cys Ser Val Ala Gln Ala Gly Val Gln
50 55 60
Trp Arg Ser Leu Gly Ser Leu Gln Pro Pro Pro Pro Gly Phe Lys Leu
65 70 75 80
Phe Ser Cys Leu Ser Phe Leu Ser Ser Trp Asp Tyr Arg Arg Met Pro
85 90 95
Pro Cys Leu Ala Asn Phe Cys Ile Phe Asn Arg Asp Gly Val Ser Pro
100 105 110
Cys Trp Ser Gly Trp Ser
115
<210> 2015
<211> 71
<212> БЕЛОК
<213> Homo sapiens
<400> 2015
Leu Ser Val Ile Ile Phe Phe Phe Val Tyr Ile Trp His Trp Ala Leu
1 5 10 15
Pro Leu Ile Leu Asn Asn His His Ile Cys Leu Met Ser Ser Ile Ile
20 25 30
Leu Asp Cys Asn Ser Val Arg Gln Ser Ile Met Ser Val Cys Phe Phe
35 40 45
Phe Phe Ser Val Ile Phe Ser Thr Arg Cys Leu Thr Asp Ser Arg Tyr
50 55 60
Pro Asn Ile Cys Trp Phe Lys
65 70
<210> 2016
<211> 60
<212> БЕЛОК
<213> Homo sapiens
<400> 2016
Leu Ser Val Ile Ile Phe Phe Phe Val Tyr Ile Trp His Trp Ala Leu
1 5 10 15
Pro Leu Ile Leu Asn Asn His His Ile Cys Leu Met Ser Ser Ile Ile
20 25 30
Leu Asp Cys Asn Ser Val Arg Gln Ser Ile Met Ser Val Cys Phe Phe
35 40 45
Phe Phe Cys Tyr Ile Leu Asn Thr Met Phe Asp Arg
50 55 60
<210> 2017
<211> 106
<212> БЕЛОК
<213> Homo sapiens
<400> 2017
Val Leu Val Leu Ser Cys Asp Leu Ile Thr Asp Val Ala Leu His Glu
1 5 10 15
Val Val Asp Leu Phe Arg Ala Tyr Asp Ala Ser Leu Ala Met Leu Met
20 25 30
Arg Lys Gly Gln Asp Ser Ile Glu Pro Val Pro Gly Gln Lys Gly Lys
35 40 45
Lys Lys Gln Trp Ser Ser Val Thr Ser Leu Glu Trp Thr Ala Gln Glu
50 55 60
Arg Gly Cys Ser Ser Trp Leu Met Lys Gln Thr Trp Met Lys Ser Trp
65 70 75 80
Ser Leu Arg Asp Pro Ser Tyr Arg Ser Ile Leu Glu Tyr Val Ser Thr
85 90 95
Arg Val Leu Trp Met Pro Thr Ser Thr Val
100 105
<210> 2018
<211> 112
<212> БЕЛОК
<213> Homo sapiens
<400> 2018
Ser Ile Gln Val Met Arg Ala Gln Met Asn Gln Ile Gln Ser Val Glu
1 5 10 15
Gly Gln Pro Leu Ala Arg Arg Pro Arg Ala Thr Gly Arg Thr Lys Arg
20 25 30
Cys Gln Pro Arg Asp Val Thr Lys Lys Thr Cys Asn Ser Asn Asp Gly
35 40 45
Lys Lys Arg Glu Trp Glu Lys Arg Lys Gln Ile Leu Gly Gly Gly Gly
50 55 60
Lys Tyr Lys Glu Tyr Phe Leu Lys Arg Ile Leu Ile Arg Lys Ala Met
65 70 75 80
Thr Val Leu Ala Gly Asp Lys Lys Gly Leu Gly Arg Phe Met Arg Cys
85 90 95
Val Gln Ser Glu Thr Lys Ala Val Ser Leu Gln Leu Pro Leu Gly Arg
100 105 110
<210> 2019
<211> 57
<212> БЕЛОК
<213> Homo sapiens
<400> 2019
Leu Asp Phe Leu Gly Glu Phe Ala Thr Asp Ile Arg Thr His Gly Val
1 5 10 15
His Met Val Leu Asn His Gln Gly Arg Pro Ser Gly Asp Ala Phe Ile
20 25 30
Gln Met Lys Ser Ala Asp Arg Ala Phe Met Ala Ala Gln Lys Cys His
35 40 45
Lys Lys Lys His Glu Gly Gln Ile Cys
50 55
<210> 2020
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2020
Leu Asp Phe Leu Gly Glu Phe Ala Thr Asp Ile Arg Thr His Gly Val
1 5 10 15
His Met Val Leu Asn His Gln Gly Arg Pro Ser Gly Asp Ala Phe Ile
20 25 30
Gln Met Lys Ser Ala Asp Arg Ala Phe Met Ala Ala Gln Lys Cys His
35 40 45
Lys Lys Thr
50
<210> 2021
<211> 75
<212> БЕЛОК
<213> Homo sapiens
<400> 2021
Gly Ala Leu Cys Lys Asp Gly Arg Phe Arg Ser Asp Ile Gly Glu Phe
1 5 10 15
Glu Trp Lys Leu Lys Glu Gly His Lys Lys Ile Tyr Gly Lys Gln Ser
20 25 30
Met Val Asp Glu Val Ser Gly Lys Val Leu Glu Met Asp Ile Ser Lys
35 40 45
Lys Lys His Tyr Asn Arg Lys Ile Ser Ile Lys Lys Leu Asn Arg Met
50 55 60
Lys Val Pro Leu Met Lys Leu Ile Thr Arg Val
65 70 75
<210> 2022
<211> 58
<212> БЕЛОК
<213> Homo sapiens
<400> 2022
Arg Glu Arg Ala Gln Leu Leu Glu Glu Gln Glu Lys Thr Leu Thr Ser
1 5 10 15
Lys Leu Gln Glu Gln Ala Arg Val Leu Lys Glu Arg Cys Gln Gly Glu
20 25 30
Ser Thr Gln Leu Gln Asn Glu Ile Gln Lys Leu Gln Lys Thr Leu Lys
35 40 45
Lys Lys Pro Arg Asp Ile Cys Arg Ile Ser
50 55
<210> 2023
<211> 53
<212> БЕЛОК
<213> Homo sapiens
<400> 2023
Val Asn Thr Leu Lys Glu Gly Lys Arg Leu Pro Cys Pro Pro Asn Cys
1 5 10 15
Pro Asp Glu Val Tyr Gln Leu Met Arg Lys Cys Trp Glu Phe Gln Pro
20 25 30
Ser Asn Arg Thr Ser Phe Gln Asn Leu Ile Glu Gly Phe Glu Ala Leu
35 40 45
Leu Lys Thr Ser Asn
50
<210> 2024
<211> 65
<212> БЕЛОК
<213> Homo sapiens
<400> 2024
Cys Arg Pro Val Thr Pro Ser Cys Lys Glu Leu Ala Asp Leu Met Thr
1 5 10 15
Arg Cys Met Asn Tyr Asp Pro Asn Gln Arg Pro Phe Phe Arg Ala Ile
20 25 30
Met Arg Asp Ile Asn Lys Leu Glu Glu Gln Asn Pro Asp Ile Val Ser
35 40 45
Glu Lys Asn Gln Gln Leu Lys Trp Thr Pro His Ile Leu Lys Ser Ala
50 55 60
Ser
65
<210> 2025
<211> 69
<212> БЕЛОК
<213> Homo sapiens
<400> 2025
Asp Asp His Asp Val Leu Ser Phe Leu Thr Phe Gln Leu Thr Glu Pro
1 5 10 15
Gly Lys Glu Pro Pro Thr Pro Asp Lys Glu Ile Ser Glu Lys Glu Lys
20 25 30
Glu Lys Tyr Gln Glu Glu Phe Glu His Phe Gln Gln Glu Leu Asp Lys
35 40 45
Lys Lys Arg Gly Ile Pro Glu Gly Pro Pro Arg Pro Pro Arg Ala Ala
50 55 60
Cys Gly Gly Asn Ile
65
<210> 2026
<211> 71
<212> БЕЛОК
<213> Homo sapiens
<400> 2026
Asp Asp His Asp Val Leu Ser Phe Leu Thr Phe Gln Leu Thr Glu Pro
1 5 10 15
Gly Lys Glu Pro Pro Thr Pro Asp Lys Glu Ile Ser Glu Lys Glu Lys
20 25 30
Glu Lys Tyr Gln Glu Glu Phe Glu His Phe Gln Gln Glu Leu Asp Lys
35 40 45
Lys Lys Arg Asn Ser Arg Arg Ala Thr Pro Thr Ser Lys Gly Ser Leu
50 55 60
Arg Arg Lys Tyr Leu Arg Val
65 70
<210> 2027
<211> 68
<212> БЕЛОК
<213> Homo sapiens
<400> 2027
Thr Lys Ser Thr Leu Ile Gly Glu Asp Val Asn Pro Leu Ile Lys Leu
1 5 10 15
Asp Asp Ala Val Asn Val Asp Glu Ile Met Thr Asp Thr Ser Thr Ser
20 25 30
Tyr Leu Leu Cys Ile Ser Glu Asn Lys Glu Asn Val Arg Asp Lys Lys
35 40 45
Lys Gly Gln His Phe Tyr Trp His Cys Gly Ser Ala Ala Cys His Arg
50 55 60
Arg Gly Cys Val
65
<210> 2028
<211> 81
<212> БЕЛОК
<213> Homo sapiens
<400> 2028
Leu Tyr Thr Lys Ser Thr Leu Ile Gly Glu Asp Val Asn Pro Leu Ile
1 5 10 15
Lys Leu Asp Asp Ala Val Asn Val Asp Glu Ile Met Thr Asp Thr Ser
20 25 30
Thr Ser Tyr Leu Leu Cys Ile Ser Glu Asn Lys Glu Asn Val Arg Asp
35 40 45
Lys Lys Arg Ala Thr Phe Leu Leu Ala Leu Trp Glu Cys Ser Leu Pro
50 55 60
Gln Ala Arg Leu Cys Leu Ile Val Ser Arg Thr Leu Leu Leu Val Gln
65 70 75 80
Ser
<210> 2029
<211> 58
<212> БЕЛОК
<213> Homo sapiens
<400> 2029
Leu Pro Pro Pro Lys Leu Thr Asp Pro Arg Leu Leu Tyr Ile Gly Phe
1 5 10 15
Leu Gly Tyr Cys Ser Gly Leu Ile Asp Asn Leu Ile Arg Arg Arg Pro
20 25 30
Ile Ala Thr Ala Gly Leu His Arg Gln Leu Leu Tyr Ile Thr Ala Phe
35 40 45
Phe Phe Cys Trp Ile Leu Ser Cys Lys Thr
50 55
<210> 2030
<211> 56
<212> БЕЛОК
<213> Homo sapiens
<400> 2030
Ser Leu Pro Pro Pro Lys Leu Thr Asp Pro Arg Leu Leu Tyr Ile Gly
1 5 10 15
Phe Leu Gly Tyr Cys Ser Gly Leu Ile Asp Asn Leu Ile Arg Arg Arg
20 25 30
Pro Ile Ala Thr Ala Gly Leu His Arg Gln Leu Leu Tyr Ile Thr Ala
35 40 45
Phe Phe Leu Leu Asp Ile Ile Leu
50 55
<210> 2031
<211> 112
<212> БЕЛОК
<213> Homo sapiens
<400> 2031
Asn Gln Ser Gly Gly Ala Gly Glu Asp Cys Gln Ile Phe Ser Thr Pro
1 5 10 15
Gly His Pro Lys Met Ile Tyr Ser Ser Ser Asn Leu Lys Thr Pro Ser
20 25 30
Lys Leu Cys Ser Gly Ser Lys Ser His Asp Val Gln Glu Val Leu Lys
35 40 45
Lys Lys Thr Gly Ser Asn Glu Val Thr Thr Arg Tyr Glu Glu Lys Lys
50 55 60
Thr Gly Ser Val Arg Lys Ala Asn Arg Met Pro Lys Asp Val Asn Ile
65 70 75 80
Gln Val Arg Lys Lys Gln Lys His Glu Thr Arg Arg Lys Ser Lys Tyr
85 90 95
Asn Glu Asp Phe Glu Arg Ala Trp Arg Glu Asp Leu Thr Ile Lys Arg
100 105 110
<210> 2032
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 2032
Met Ala Pro Val Lys Lys Leu Val Val Lys Gly Gly Lys Lys Lys Glu
1 5 10 15
Ala Ser Ser Glu Val His Ser
20
<210> 2033
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 2033
Met Ala Pro Val Lys Lys Leu Val Val Lys Gly Gly Lys Lys Arg Ser
1 5 10 15
Lys Phe
<210> 2034
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2034
Met Pro Ser His Gln Gly Ala Glu Gln Gln Gln Gln Gln His His Val
1 5 10 15
Phe Ile Ser Gln Val Val Thr Glu Lys Glu Phe Leu Ser Arg Ser Asp
20 25 30
Gln Leu Gln Gln Ala Val Gln Ser Gln Gly Phe Ile Asn Tyr Cys Gln
35 40 45
Lys Lys Asn
50
<210> 2035
<211> 65
<212> БЕЛОК
<213> Homo sapiens
<400> 2035
Met Pro Ser His Gln Gly Ala Glu Gln Gln Gln Gln Gln His His Val
1 5 10 15
Phe Ile Ser Gln Val Val Thr Glu Lys Glu Phe Leu Ser Arg Ser Asp
20 25 30
Gln Leu Gln Gln Ala Val Gln Ser Gln Gly Phe Ile Asn Tyr Cys Gln
35 40 45
Lys Lys Leu Met Leu Leu Arg Leu Asn Leu Arg Lys Met Cys Gly Pro
50 55 60
Phe
65
<210> 2036
<211> 79
<212> БЕЛОК
<213> Homo sapiens
<400> 2036
Ala Glu Val Phe Glu Lys Glu Gln Ser Ile Cys Ala Ala Glu Glu Gln
1 5 10 15
Pro Ala Glu Asp Gly Gln Gly Glu Thr Asn Lys Asn Arg Thr Lys Gly
20 25 30
Gly Trp Gln Gln Lys Ser Lys Gly Pro Lys Lys Thr Ala Lys Ser Lys
35 40 45
Lys Lys Glu Thr Phe Lys Lys Lys Thr Tyr Thr Cys Ala Ile Thr Thr
50 55 60
Val Lys Ala Thr Glu Thr Lys Ala Gly Lys Trp Ser Arg Trp Glu
65 70 75
<210> 2037
<211> 53
<212> БЕЛОК
<213> Homo sapiens
<400> 2037
Met Ala Glu Val Phe Glu Lys Glu Gln Ser Ile Cys Ala Ala Glu Glu
1 5 10 15
Gln Pro Ala Glu Asp Gly Gln Gly Glu Thr Asn Lys Asn Arg Thr Lys
20 25 30
Gly Gly Trp Gln Gln Lys Ser Lys Gly Pro Lys Lys Thr Ala Lys Ser
35 40 45
Lys Lys Arg Asn Leu
50
<210> 2038
<211> 71
<212> БЕЛОК
<213> Homo sapiens
<400> 2038
Asn Ile Met Glu Ile Arg Gln Leu Pro Ser Ser His Ala Leu Glu Ala
1 5 10 15
Lys Leu Ser Arg Met Ser Tyr Pro Val Lys Glu Gln Glu Ser Ile Leu
20 25 30
Lys Thr Val Gly Lys Leu Thr Ala Thr Gln Val Ala Lys Ile Ser Phe
35 40 45
Phe Phe Ala Leu Cys Gly Phe Trp Gln Ile Cys His Ile Lys Lys His
50 55 60
Phe Gln Thr His Lys Leu Leu
65 70
<210> 2039
<211> 68
<212> БЕЛОК
<213> Homo sapiens
<400> 2039
Tyr Glu Lys Lys Lys Tyr Tyr Asp Lys Asn Ala Ile Ala Ile Thr Asn
1 5 10 15
Ile Ser Ser Ser Asp Ala Pro Leu Gln Pro Leu Val Ser Ser Pro Ser
20 25 30
Leu Gln Ala Ala Val Asp Lys Asn Lys Leu Glu Lys Glu Lys Glu Lys
35 40 45
Lys Lys Gly Arg Glu Lys Glu Arg Lys Gly Ala Arg Lys Ala Gly Lys
50 55 60
Thr Thr Tyr Ser
65
<210> 2040
<211> 97
<212> БЕЛОК
<213> Homo sapiens
<400> 2040
Lys Tyr Glu Lys Lys Lys Tyr Tyr Asp Lys Asn Ala Ile Ala Ile Thr
1 5 10 15
Asn Ile Ser Ser Ser Asp Ala Pro Leu Gln Pro Leu Val Ser Ser Pro
20 25 30
Ser Leu Gln Ala Ala Val Asp Lys Asn Lys Leu Glu Lys Glu Lys Glu
35 40 45
Lys Lys Arg Lys Arg Lys Arg Glu Lys Arg Ser Gln Lys Ser Arg Gln
50 55 60
Asn His Leu Gln Leu Lys Ser Cys Arg Arg Lys Ile Ser Asn Trp Ser
65 70 75 80
Leu Lys Lys Val Pro Ala Leu Lys Lys Leu Arg Ser Pro Leu Trp Ile
85 90 95
Phe
<210> 2041
<211> 65
<212> БЕЛОК
<213> Homo sapiens
<400> 2041
Ile Tyr Gln Asp Ala Tyr Arg Ala Glu Trp Gln Val Tyr Lys Glu Glu
1 5 10 15
Ile Ser Arg Phe Lys Glu Gln Leu Thr Pro Ser Gln Ile Met Ser Leu
20 25 30
Glu Lys Glu Ile Met Asp Lys His Leu Lys Arg Lys Ala Met Thr Lys
35 40 45
Lys Lys Arg Val Asn Thr Ala Trp Lys Thr Lys Lys Thr Ser Phe Ser
50 55 60
Leu
65
<210> 2042
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2042
Ile Tyr Gln Asp Ala Tyr Arg Ala Glu Trp Gln Val Tyr Lys Glu Glu
1 5 10 15
Ile Ser Arg Phe Lys Glu Gln Leu Thr Pro Ser Gln Ile Met Ser Leu
20 25 30
Glu Lys Glu Ile Met Asp Lys His Leu Lys Arg Lys Ala Met Thr Lys
35 40 45
Lys Lys Ser
50
<210> 2043
<211> 52
<212> БЕЛОК
<213> Homo sapiens
<400> 2043
Lys Pro Gln Glu Val Cys Val Ala Val Trp Arg Lys Asn Asp Glu Asn
1 5 10 15
Ile Thr Leu Glu Thr Val Cys His Asp Pro Lys Leu Pro Tyr His Asp
20 25 30
Phe Ile Leu Glu Asp Ala Ala Ser Pro Lys Cys Ile Met Lys Glu Lys
35 40 45
Lys Lys Ala Trp
50
<210> 2044
<211> 84
<212> БЕЛОК
<213> Homo sapiens
<400> 2044
Glu Lys Pro Gln Glu Val Cys Val Ala Val Trp Arg Lys Asn Asp Glu
1 5 10 15
Asn Ile Thr Leu Glu Thr Val Cys His Asp Pro Lys Leu Pro Tyr His
20 25 30
Asp Phe Ile Leu Glu Asp Ala Ala Ser Pro Lys Cys Ile Met Lys Glu
35 40 45
Lys Lys Ser Leu Val Arg Leu Ser Ser Cys Val Pro Val Ala Leu Met
50 55 60
Ser Ala Met Thr Thr Ser Ser Ser Gln Lys Asn Ile Thr Pro Ala Ile
65 70 75 80
Leu Thr Cys Cys
<210> 2045
<211> 74
<212> БЕЛОК
<213> Homo sapiens
<400> 2045
Val Pro Ser Lys Tyr Gln Phe Leu Cys Ser Asp His Phe Thr Pro Asp
1 5 10 15
Ser Leu Asp Ile Arg Trp Gly Ile Arg Tyr Leu Lys Gln Thr Ala Val
20 25 30
Pro Thr Ile Phe Ser Leu Pro Glu Asp Asn Gln Gly Lys Asp Pro Ser
35 40 45
Lys Lys Asn Pro Arg Arg Lys Thr Trp Lys Met Arg Lys Lys Tyr Ala
50 55 60
Gln Lys Pro Ser Gln Lys Asn His Leu Tyr
65 70
<210> 2046
<211> 88
<212> БЕЛОК
<213> Homo sapiens
<400> 2046
Gly Thr Thr Glu Glu Met Lys Tyr Val Leu Gly Gln Leu Val Gly Leu
1 5 10 15
Asn Ser Pro Asn Ser Ile Leu Lys Ala Ala Lys Thr Leu Tyr Glu His
20 25 30
Tyr Ser Gly Gly Glu Ser His Asn Ser Ser Ser Ser Lys Thr Phe Glu
35 40 45
Lys Lys Gly Glu Lys Asn Asp Leu Gln Leu Phe Val Met Ser Asp Thr
50 55 60
Thr Tyr Lys Ile Tyr Trp Thr Val Ile Leu Leu Asn Pro Cys Gly Asn
65 70 75 80
Leu His Leu Lys Thr Thr Ser Leu
85
<210> 2047
<211> 55
<212> БЕЛОК
<213> Homo sapiens
<400> 2047
Gln Gln Leu Ile Arg Glu Thr Leu Ile Ser Trp Leu Gln Ala Gln Met
1 5 10 15
Leu Asn Pro Gln Pro Glu Lys Thr Phe Ile Arg Asn Lys Ala Ala Gln
20 25 30
Val Phe Ala Leu Leu Phe Val Thr Glu Tyr Leu Thr Lys Trp Pro Lys
35 40 45
Phe Phe Leu Thr Phe Ser Gln
50 55
<210> 2048
<211> 93
<212> БЕЛОК
<213> Homo sapiens
<400> 2048
Ala Lys Phe Gln Gln Cys His Ser Thr Leu Glu Pro Asn Pro Ala Asp
1 5 10 15
Cys Arg Val Leu Val Tyr Leu Gln Asn Gln Pro Gly Thr Lys Leu Leu
20 25 30
Asn Phe Leu Gln Glu Arg Asn Leu Pro Pro Lys Val Val Leu Arg His
35 40 45
Pro Lys Val His Leu Asn Thr Met Phe Arg Arg Pro His Ser Cys Leu
50 55 60
Ala Asp Val Leu Leu Ser Val His Leu Ile Val Leu Arg Val Val Arg
65 70 75 80
Leu Pro Ala Pro Phe Arg Val Asn His Ala Val Glu Trp
85 90
<210> 2049
<211> 53
<212> БЕЛОК
<213> Homo sapiens
<400> 2049
Ala Pro Val Ile Phe Gln Ile Ala Leu Asp Lys Pro Cys His Gln Ala
1 5 10 15
Glu Val Lys His Leu His His Leu Leu Lys Gln Leu Lys Pro Ser Glu
20 25 30
Lys Tyr Leu Lys Ile Lys His Leu Leu Leu Lys Arg Glu Arg Val Asp
35 40 45
Leu Ser Lys Leu Gln
50
<210> 2050
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 2050
Met Leu Gln Phe Arg Gly Ser Arg Phe Phe Gln Met Leu Ile Leu Tyr
1 5 10 15
Tyr Ile Leu Pro Arg Lys Val Leu Gln Met Asp Phe Leu Val His Pro
20 25 30
Ala
<210> 2051
<211> 179
<212> БЕЛОК
<213> Homo sapiens
<400> 2051
Ala Leu Gly Pro His Ser Arg Ile Ser Cys Leu Pro Thr Gln Thr Arg
1 5 10 15
Gly Cys Ile Leu Leu Ala Ala Thr Pro Arg Ser Ser Ser Ser Ser Ser
20 25 30
Ser Asn Asp Met Ile Pro Met Ala Ile Ser Ser Pro Pro Lys Ala Pro
35 40 45
Leu Leu Ala Ala Pro Ser Pro Ala Ser Arg Leu Gln Cys Ile Asn Ser
50 55 60
Asn Ser Arg Ile Thr Ser Gly Gln Trp Met Ala His Met Ala Leu Leu
65 70 75 80
Pro Ser Gly Thr Lys Gly Arg Cys Thr Ala Cys His Thr Ala Leu Gly
85 90 95
Arg Gly Ser Leu Ser Ser Ser Ser Cys Pro Gln Pro Ser Pro Ser Leu
100 105 110
Pro Ala Ser Asn Lys Leu Pro Ser Leu Pro Leu Ser Lys Met Tyr Thr
115 120 125
Thr Ser Met Ala Met Pro Ile Leu Pro Leu Pro Gln Leu Leu Leu Ser
130 135 140
Ala Asp Gln Gln Ala Ala Pro Arg Thr Asn Phe His Ser Ser Leu Ala
145 150 155 160
Glu Thr Val Ser Leu His Pro Leu Ala Pro Met Pro Ser Lys Thr Cys
165 170 175
His His Lys
<210> 2052
<211> 79
<212> БЕЛОК
<213> Homo sapiens
<400> 2052
Ala His Gln Gly Phe Pro Ala Ala Lys Glu Ser Arg Val Ile Gln Leu
1 5 10 15
Ser Leu Leu Ser Leu Leu Ile Pro Pro Leu Thr Cys Leu Ala Ser Glu
20 25 30
Ala Leu Pro Arg Pro Leu Leu Ala Leu Pro Pro Val Leu Leu Ser Leu
35 40 45
Ala Gln Asp His Ser Arg Leu Leu Gln Cys Gln Ala Thr Arg Cys His
50 55 60
Leu Gly His Pro Val Ala Ser Arg Thr Ala Ser Cys Ile Leu Pro
65 70 75
<210> 2053
<211> 222
<212> БЕЛОК
<213> Homo sapiens
<400> 2053
Pro Ile Leu Ala Ala Thr Gly Thr Ser Val Arg Thr Ala Ala Arg Thr
1 5 10 15
Trp Val Pro Arg Ala Ala Ile Arg Val Pro Asp Pro Ala Ala Val Pro
20 25 30
Asp Asp His Ala Gly Pro Gly Ala Glu Cys His Gly Arg Pro Leu Leu
35 40 45
Tyr Thr Ala Asp Ser Ser Leu Trp Thr Thr Arg Pro Gln Arg Val Trp
50 55 60
Ser Thr Gly Pro Asp Ser Ile Leu Gln Pro Ala Lys Ser Ser Pro Ser
65 70 75 80
Ala Ala Ala Ala Thr Leu Leu Pro Ala Thr Thr Val Pro Asp Pro Ser
85 90 95
Cys Pro Thr Phe Val Ser Ala Ala Ala Thr Val Ser Thr Thr Thr Ala
100 105 110
Pro Val Leu Ser Ala Ser Ile Leu Pro Ala Ala Ile Pro Ala Ser Thr
115 120 125
Ser Ala Val Pro Gly Ser Ile Pro Leu Pro Ala Val Asp Asp Thr Ala
130 135 140
Ala Pro Pro Glu Pro Ala Pro Leu Leu Thr Ala Thr Gly Ser Val Ser
145 150 155 160
Leu Pro Ala Ala Ala Thr Ser Ala Ala Ser Thr Leu Asp Ala Leu Pro
165 170 175
Ala Gly Cys Val Ser Ser Ala Pro Val Ser Ala Val Pro Ala Asn Cys
180 185 190
Leu Phe Pro Ala Ala Leu Pro Ser Thr Ala Gly Ala Ile Ser Arg Phe
195 200 205
Ile Trp Val Ser Gly Ile Leu Ser Pro Leu Asn Asp Leu Gln
210 215 220
<210> 2054
<211> 185
<212> БЕЛОК
<213> Homo sapiens
<400> 2054
Pro Cys Arg Ala Gly Arg Arg Val Pro Trp Ala Ala Ser Leu Ile His
1 5 10 15
Ser Arg Phe Leu Leu Met Asp Asn Lys Ala Pro Ala Gly Met Val Asn
20 25 30
Arg Ala Arg Leu His Ile Thr Thr Ser Lys Val Leu Thr Leu Ser Ser
35 40 45
Ser Ser His Pro Thr Pro Ser Asn His Arg Pro Arg Pro Leu Met Pro
50 55 60
Asn Leu Arg Ile Ser Ser Ser His Ser Leu Asn His His Ser Ser Ser
65 70 75 80
Pro Leu Ser Leu His Thr Pro Ser Ser His Pro Ser Leu His Ile Ser
85 90 95
Ser Pro Arg Leu His Thr Pro Pro Ser Ser Arg Arg His Ser Ser Thr
100 105 110
Pro Arg Ala Ser Pro Pro Thr His Ser His Arg Leu Ser Leu Leu Thr
115 120 125
Ser Ser Ser Asn Leu Ser Ser Gln His Pro Arg Arg Ser Pro Ser Arg
130 135 140
Leu Arg Ile Leu Ser Pro Ser Leu Ser Ser Pro Ser Lys Leu Pro Ile
145 150 155 160
Pro Ser Ser Ala Ser Leu His Arg Arg Ser Tyr Leu Lys Ile His Leu
165 170 175
Gly Leu Arg His Pro Gln Pro Pro Gln
180 185
<210> 2055
<211> 58
<212> БЕЛОК
<213> Homo sapiens
<400> 2055
Arg Thr Asn Pro Thr Val Arg Met Arg Pro His Cys Val Pro Phe Trp
1 5 10 15
Thr Gly Arg Ile Leu Leu Pro Ser Ala Ala Ser Val Cys Pro Ile Pro
20 25 30
Phe Glu Ala Cys His Leu Cys Gln Ala Met Thr Leu Arg Cys Pro Asn
35 40 45
Thr Gln Gly Cys Cys Ser Ser Trp Ala Ser
50 55
<210> 2056
<211> 90
<212> БЕЛОК
<213> Homo sapiens
<400> 2056
Thr Asn Gln Ala Leu Pro Lys Ile Glu Val Ile Cys Arg Gly Thr Pro
1 5 10 15
Arg Cys Pro Ser Thr Val Pro Pro Ser Pro Ala Gln Pro Tyr Leu Arg
20 25 30
Val Ser Leu Pro Glu Asp Arg Tyr Thr Gln Ala Trp Ala Pro Thr Ser
35 40 45
Arg Thr Pro Trp Gly Ala Met Val Pro Arg Gly Val Ser Met Ala His
50 55 60
Lys Val Ala Thr Pro Gly Ser Gln Thr Ile Met Pro Cys Pro Met Pro
65 70 75 80
Thr Thr Pro Val Gln Ala Trp Leu Glu Ala
85 90
<210> 2057
<211> 41
<212> БЕЛОК
<213> Homo sapiens
<400> 2057
Arg Met Glu Arg Glu Leu Lys Lys Trp Ser Ile Gln Thr Cys Leu Ser
1 5 10 15
Ala Arg Thr Gly Leu Ser Ile Ser Cys Thr Thr Leu Asn Ser Pro Pro
20 25 30
Leu Lys Lys Met Ser Met Pro Ala Val
35 40
<210> 2058
<211> 35
<212> БЕЛОК
<213> Homo sapiens
<400> 2058
Leu Cys Ser Arg Tyr Ser Leu Phe Leu Ala Trp Arg Leu Ser Ser Val
1 5 10 15
Leu Gln Arg Phe Arg Phe Thr His Val Ile Gln Gln Arg Met Glu Ser
20 25 30
Gln Ile Ser
35
<210> 2059
<211> 39
<212> БЕЛОК
<213> Homo sapiens
<400> 2059
Arg Ser Ala Cys Val Thr Val Lys Gly Pro Leu Ala Ser Val Gly Arg
1 5 10 15
His Ser Leu Ser Lys Gln Asp Cys Lys Phe Leu Pro Phe Trp Gly Phe
20 25 30
Leu Glu Glu Phe Leu Leu Cys
35
<210> 2060
<211> 97
<212> БЕЛОК
<213> Homo sapiens
<400> 2060
Ile Gln Trp Gly Thr Thr Thr Ala Pro Arg Pro Ile Arg Pro Pro Phe
1 5 10 15
Leu Glu Ser Lys Gln Asn Cys Ser His Phe Pro Thr Pro Leu Leu Ala
20 25 30
Ser Glu Asp Arg Arg Glu Thr Gly Leu Phe Leu Pro Ser Ala Ala Gln
35 40 45
Lys Met Lys Lys Ala His Phe Leu Lys Thr Trp Phe Arg Ser Asn Pro
50 55 60
Thr Lys Thr Lys Lys Ala Arg Phe Ser Thr Ala Ser Leu Ala Lys Glu
65 70 75 80
Leu Thr His Pro Leu Leu Val Ser Leu Leu Leu Lys Glu Lys Gln Asp
85 90 95
Gly
<210> 2061
<211> 73
<212> БЕЛОК
<213> Homo sapiens
<400> 2061
Pro Thr Asp Pro Phe Leu Gly Leu Arg Leu Gly Leu His Leu Gln Lys
1 5 10 15
Val Phe His Gln Ser His Ala Glu Tyr Ser Gly Ala Pro Pro Pro Pro
20 25 30
Pro Ala Pro Ser Gly Leu Arg Phe Trp Asn Pro Ser Arg Ile Ala His
35 40 45
Ile Ser Gln Leu Leu Ser Trp Pro Gln Lys Thr Glu Glu Arg Leu Gly
50 55 60
Tyr Ser Ser His Gln Leu Pro Arg Lys
65 70
<210> 2062
<211> 45
<212> БЕЛОК
<213> Homo sapiens
<400> 2062
Phe Cys Cys Ser Cys Cys Phe Phe Gly Gly Glu Arg Trp Ser Lys Ser
1 5 10 15
Pro Tyr Cys Pro Gln Arg Met Thr Pro Gly Thr Thr Phe Ile Thr Met
20 25 30
Met Lys Lys Glu Ala Glu Lys Arg Thr Arg Thr Leu Thr
35 40 45
<210> 2063
<211> 95
<212> БЕЛОК
<213> Homo sapiens
<400> 2063
Trp Arg Arg Asn Cys Lys Ala Pro Val Ser Leu Arg Lys Ser Val Gln
1 5 10 15
Thr Pro Ala Arg Ser Ser Pro Ala Arg Pro Asp Arg Thr Arg Arg Leu
20 25 30
Pro Ser Leu Gly Val Pro Gly Gln Pro Trp Ala Leu Gly Ala Ala Ala
35 40 45
Ser Arg Arg Cys Cys Cys Cys Cys Arg Ser Pro Leu Gly Ser Ala Arg
50 55 60
Ser Arg Ser Pro Ala Thr Leu Ala Leu Thr Pro Arg Ala Thr Arg Ser
65 70 75 80
Arg Cys Pro Gly Ala Thr Trp Arg Glu Ala Ala Ser Trp Ala Glu
85 90 95
<210> 2064
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 2064
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
50 55 60
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
65 70 75 80
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
85 90 95
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
100 105 110
His
<210> 2065
<211> 57
<212> БЕЛОК
<213> Homo sapiens
<400> 2065
Pro Arg Pro Arg Arg Cys Thr Arg His Pro Ala Cys Pro Leu Asp His
1 5 10 15
Thr Thr Pro Pro Ala Trp Ser Pro Pro Trp Val Arg Ala Leu Leu Asp
20 25 30
Ala His Arg Ala Pro Ser Glu Ser Pro Cys Ser Pro Phe Arg Leu Ala
35 40 45
Phe Leu Gln Glu Gln Tyr His Glu Ala
50 55
<210> 2066
<211> 494
<212> БЕЛОК
<213> Homo sapiens
<400> 2066
Thr Arg Arg Cys His Cys Cys Pro His Leu Arg Ser His Pro Cys Pro
1 5 10 15
His His Leu Arg Asn His Pro Arg Pro His His Leu Arg His His Ala
20 25 30
Cys His His His Leu Arg Asn Cys Pro His Pro His Phe Leu Arg His
35 40 45
Cys Thr Cys Pro Gly Arg Trp Arg Asn Arg Pro Ser Leu Arg Arg Leu
50 55 60
Arg Ser Leu Leu Cys Leu Pro His Leu Asn His His Leu Phe Leu His
65 70 75 80
Trp Arg Ser Arg Pro Cys Leu His Arg Lys Ser His Pro His Leu Leu
85 90 95
His Leu Arg Arg Leu Tyr Pro His His Leu Lys His Arg Pro Cys Pro
100 105 110
His His Leu Lys Asn Leu Leu Cys Pro Arg His Leu Arg Asn Cys Pro
115 120 125
Leu Pro Arg His Leu Lys His Leu Ala Cys Leu His His Leu Arg Ser
130 135 140
His Pro Cys Pro Leu His Leu Lys Ser His Pro Cys Leu His His Arg
145 150 155 160
Arg His Leu Val Cys Ser His His Leu Lys Ser Leu Leu Cys Pro Leu
165 170 175
His Leu Arg Ser Leu Pro Phe Pro His His Leu Arg His His Ala Cys
180 185 190
Pro His His Leu Arg Thr Arg Leu Cys Pro His His Leu Lys Asn His
195 200 205
Leu Cys Pro Pro His Leu Arg Tyr Arg Ala Tyr Pro Pro Cys Leu Trp
210 215 220
Cys His Ala Cys Leu His Arg Leu Arg Asn Leu Pro Cys Pro His Arg
225 230 235 240
Leu Arg Ser Leu Pro Arg Pro Leu His Leu Arg Leu His Ala Ser Pro
245 250 255
His His Leu Arg Thr Pro Pro His Pro His His Leu Arg Thr His Leu
260 265 270
Leu Pro His His Arg Arg Thr Arg Ser Cys Pro Cys Arg Trp Arg Ser
275 280 285
His Pro Cys Cys His Tyr Leu Arg Ser Arg Asn Ser Ala Pro Gly Pro
290 295 300
Arg Gly Arg Thr Cys His Pro Gly Leu Arg Ser Arg Thr Cys Pro Pro
305 310 315 320
Gly Leu Arg Ser His Thr Tyr Leu Arg Arg Leu Arg Ser His Thr Cys
325 330 335
Pro Pro Ser Leu Arg Ser His Ala Tyr Ala Leu Cys Leu Arg Ser His
340 345 350
Thr Cys Pro Pro Arg Leu Arg Asp His Ile Cys Pro Leu Ser Leu Arg
355 360 365
Asn Cys Thr Cys Pro Pro Arg Leu Arg Ser Arg Thr Cys Leu Leu Cys
370 375 380
Leu Arg Ser His Ala Cys Pro Pro Asn Leu Arg Asn His Thr Cys Pro
385 390 395 400
Pro Ser Leu Arg Ser His Ala Cys Pro Pro Gly Leu Arg Asn Arg Ile
405 410 415
Cys Pro Leu Ser Leu Arg Ser His Pro Cys Pro Leu Gly Leu Lys Ser
420 425 430
Pro Leu Arg Ser Gln Ala Asn Ala Leu His Leu Arg Ser Cys Pro Cys
435 440 445
Ser Leu Pro Leu Gly Asn His Pro Tyr Leu Pro Cys Leu Glu Ser Gln
450 455 460
Pro Cys Leu Ser Leu Gly Asn His Leu Cys Pro Leu Cys Pro Arg Ser
465 470 475 480
Cys Arg Cys Pro His Leu Gly Ser His Pro Cys Arg Leu Ser
485 490
<210> 2067
<211> 53
<212> БЕЛОК
<213> Homo sapiens
<400> 2067
Ser Trp Lys Gly Thr Asn Trp Cys Asn Asp Met Cys Ile Phe Ile Thr
1 5 10 15
Ser Gly Gln Ile Phe Lys Gly Thr Arg Gly Pro Arg Phe Leu Trp Gly
20 25 30
Ser Lys Asp Gln Arg Gln Lys Gly Ser Asn Tyr Ser Gln Ser Glu Ala
35 40 45
Leu Cys Val Leu Leu
50
<210> 2068
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2068
Lys Arg Thr Lys Cys Phe Thr Phe Gly
1 5
<210> 2069
<211> 27
<212> БЕЛОК
<213> Homo sapiens
<400> 2069
Pro Ile Phe Ile Gln Thr Leu Leu Leu Trp Asp Phe Leu Gln Lys Asp
1 5 10 15
Leu Lys Ala Tyr Thr Gly Thr Ile Leu Met Met
20 25
<210> 2070
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 2070
Gln Lys Met Ile Leu Thr Lys Gln Ile Lys Thr Lys Pro Thr Asp Thr
1 5 10 15
Phe Leu Gln Ile Leu Arg
20
<210> 2071
<211> 43
<212> БЕЛОК
<213> Homo sapiens
<400> 2071
Gly Phe Trp Ile Gln Ser Ile Lys Thr Ile Thr Arg Tyr Thr Ile Phe
1 5 10 15
Val Leu Lys Asp Ile Met Thr Pro Pro Asn Leu Ile Ala Glu Leu His
20 25 30
Asn Ile Leu Leu Lys Thr Ile Thr His His Ser
35 40
<210> 2072
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 2072
Asn Tyr Ser Asn Val Gln Trp Arg Asn Leu Gln Ser Ser Val Cys Gly
1 5 10 15
Leu Pro Ala Lys Gly Glu Asp Ile Phe Leu Gln Phe Arg Thr His Thr
20 25 30
Thr Gly Arg Gln Val His Val Leu
35 40
<210> 2073
<211> 44
<212> БЕЛОК
<213> Homo sapiens
<400> 2073
Tyr Gln Ser Arg Val Leu Pro Gln Thr Glu Gln Asp Ala Lys Lys Gly
1 5 10 15
Gln Asn Val Ser Leu Leu Gly Lys Tyr Ile Leu His Thr Arg Thr Arg
20 25 30
Gly Asn Leu Arg Lys Ser Arg Lys Trp Lys Ser Met
35 40
<210> 2074
<211> 85
<212> БЕЛОК
<213> Homo sapiens
<400> 2074
Ser Ser Gln Asn Ala Arg Gly Cys Ser Pro Arg Gly Pro Cys Thr Ser
1 5 10 15
Ser Ser Tyr Thr Gly Gly Pro Cys Thr Ser Pro Leu Leu Ala Pro Val
20 25 30
Ile Phe Cys Pro Phe Pro Glu Asn Leu Pro Gly Gln Leu Arg Phe Pro
35 40 45
Ser Gly Leu Leu Ala Phe Trp Asp Ser Gln Val Cys Asp Leu His Val
50 55 60
Leu Pro Cys Pro Gln Gln Asp Val Leu Pro Thr Gly Gln Asp Leu Pro
65 70 75 80
Cys Ala Ala Val Gly
85
<210> 2075
<211> 72
<212> БЕЛОК
<213> Homo sapiens
<400> 2075
Gly Ala Ala Pro Thr Met Ser Ala Ala Gln Ile Ala Met Val Trp Pro
1 5 10 15
Leu Leu Ser Ile Leu Ser Glu Trp Lys Glu Ile Cys Val Trp Ser Ile
20 25 30
Trp Met Thr Glu Thr Leu Phe Asp Ile Val Trp Trp Cys Pro Met Ser
35 40 45
Arg Leu Arg Leu Ala Leu Thr Val Pro Pro Ser Thr Thr Thr Thr Cys
50 55 60
Val Thr Val Pro Ala Trp Ala Ala
65 70
<210> 2076
<211> 97
<212> БЕЛОК
<213> Homo sapiens
<400> 2076
Thr Gly Gly Pro Ser Ser Pro Ser Ser His Trp Lys Thr Pro Val Val
1 5 10 15
Ile Tyr Trp Asp Gly Thr Ala Leu Arg Cys Val Phe Val Pro Val Leu
20 25 30
Gly Glu Thr Gly Ala Gln Arg Lys Arg Ile Ser Ala Arg Lys Gly Ser
35 40 45
Leu Thr Thr Ser Cys Pro Gln Gly Ala Leu Ser Glu His Cys Pro Thr
50 55 60
Thr Pro Ala Pro Leu Pro Ser Gln Arg Arg Asn His Trp Met Glu Asn
65 70 75 80
Ile Ser Pro Phe Arg Ser Val Gly Val Ser Ala Ser Arg Cys Ser Glu
85 90 95
Ser
<210> 2077
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 2077
Phe His Thr Pro Ala Arg His Pro Arg Pro Arg His Gly His Leu Gln
1 5 10 15
Ala Val Thr Ala His Asp Gly Gly Cys Glu Ala Leu Pro Pro Pro
20 25 30
<210> 2078
<211> 78
<212> БЕЛОК
<213> Homo sapiens
<400> 2078
Cys Cys Pro Arg Thr Ile Leu Asn Asn Gly Ser Leu Lys Thr Gln Val
1 5 10 15
Gln Met Lys Leu Pro Glu Cys Gln Arg Leu Leu Pro Pro Trp Pro Leu
20 25 30
His Gln Gln Leu Leu His Arg Arg Pro Leu His Gln Pro Pro Pro Gly
35 40 45
Pro Cys His Leu Leu Ser Leu Pro Arg Lys Pro Thr Arg Ala Ala Thr
50 55 60
Val Ser Val Trp Ala Ser Cys Ile Leu Gly Gln Pro Ser Leu
65 70 75
<210> 2079
<211> 28
<212> БЕЛОК
<213> Homo sapiens
<400> 2079
Val Arg Lys His Phe Gln Thr Tyr Gly Asn Tyr Phe Leu Lys Thr Thr
1 5 10 15
Phe Cys Pro Pro Cys Arg Pro Lys Gln Trp Met Ile
20 25
<210> 2080
<211> 46
<212> БЕЛОК
<213> Homo sapiens
<400> 2080
Leu Ala Arg Thr Pro Leu Pro Ser Thr Arg Cys Phe Ala Asn Trp Pro
1 5 10 15
Arg Pro Ala Leu Cys Ser Cys Gly Leu Ile Pro His Pro Arg Pro Ala
20 25 30
Pro Ala Ser Ala Pro Trp Pro Ser Thr Ser Ser His Ser Thr
35 40 45
<210> 2081
<211> 81
<212> БЕЛОК
<213> Homo sapiens
<400> 2081
Glu Leu Gln Glu Thr Gly His Arg Gln Val Ala Leu Arg Arg Ser Gly
1 5 10 15
Arg Pro Pro Lys Cys Ala Glu Arg Pro Gly Ala Ala Asp Thr Gly Ala
20 25 30
His Cys Thr Ser Thr Asp Gly Arg Leu Lys Ile Ser Val Glu Thr Tyr
35 40 45
Thr Val Ser Ser Gln Leu Leu Met Val Leu Met Ser Leu Asp Leu Asp
50 55 60
Thr Gly Leu Val Pro Ser Leu Val Ser Lys Cys Leu Ile Leu Arg Val
65 70 75 80
Lys
<210> 2082
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2082
Lys Ser Asp Ala Ser Arg Leu Ser Gly Ala
1 5 10
<210> 2083
<211> 29
<212> БЕЛОК
<213> Homo sapiens
<400> 2083
Arg Thr Ala Tyr Phe Cys Gln Tyr His Thr Ala Ser Val Tyr Ser Glu
1 5 10 15
Arg Ala Met Pro Pro Gly Cys Pro Glu Pro Ser Gln Ala
20 25
<210> 2084
<211> 91
<212> БЕЛОК
<213> Homo sapiens
<400> 2084
Thr Arg Ala Ser Pro Pro Arg Ser Ser Ser Ala Ile Ala Val Arg Ala
1 5 10 15
Ser Cys Cys Pro Tyr Gly Ser Thr Ser Thr Ala Ser Arg Ser Pro Thr
20 25 30
Gln Arg Cys Arg Leu Ala Arg Ala Ala Ala Ser Thr Ala Thr Glu Val
35 40 45
Thr Phe Gly Ser Ser Glu Met Gln Gly His Thr Met Gly Phe Trp Leu
50 55 60
Thr Lys Leu Asn Tyr Leu Cys His Leu Ser Met Leu Thr Asp Ser Leu
65 70 75 80
Phe Leu Pro Ile Ser His Cys Gln Cys Ile Leu
85 90
<210> 2085
<211> 31
<212> БЕЛОК
<213> Homo sapiens
<400> 2085
Ser Ser Leu Arg Ile Thr Gly Asp Trp Thr Ser Ser Gly Arg Ser Thr
1 5 10 15
Lys Ile Trp Lys Thr Thr Gln Met Cys Arg Lys Thr Trp Ser Gly
20 25 30
<210> 2086
<211> 104
<212> БЕЛОК
<213> Homo sapiens
<400> 2086
Arg Arg Arg Arg Gly Gly Val Gly Arg Arg Gly Val Arg Pro Gly Arg
1 5 10 15
Val Arg Pro Gly Gly Thr Gly Arg Arg Gly Gly Asp Gly Gly Arg Ala
20 25 30
Ala Ala Ala Arg Ala Ala Leu Gly Glu Leu Ala Arg Ala Leu Pro Gly
35 40 45
His Leu Leu Gln Ser Gln Ser Ala Arg Arg Ala Ala Arg Met Ala Gln
50 55 60
Leu Arg Arg Arg Ala Ala Ala Leu Pro Asn Ala Ala Ala Trp His Gly
65 70 75 80
Pro Pro His Pro Gln Leu Pro Arg Ser Pro Leu Ala Leu Gln Arg Cys
85 90 95
Arg Asp Thr Arg Trp Ala Ser Gly
100
<210> 2087
<211> 66
<212> БЕЛОК
<213> Homo sapiens
<400> 2087
Ser Cys Lys Val Phe Phe Lys Arg Ala Ala Glu Gly Lys Gln Lys Tyr
1 5 10 15
Leu Cys Ala Ser Arg Asn Asp Cys Thr Ile Asp Lys Phe Arg Arg Lys
20 25 30
Asn Cys Pro Ser Cys Arg Leu Arg Lys Cys Tyr Glu Ala Gly Met Thr
35 40 45
Leu Gly Glu Lys Phe Arg Val Gly Asn Cys Lys His Leu Lys Met Thr
50 55 60
Arg Pro
65
<210> 2088
<211> 49
<212> БЕЛОК
<213> Homo sapiens
<400> 2088
Met Ala Gly Ala Pro Pro Pro Ala Ser Leu Pro Pro Cys Ser Leu Ile
1 5 10 15
Ser Asp Cys Cys Ala Ser Asn Gln Arg Asp Ser Val Gly Val Gly Pro
20 25 30
Ser Glu Pro Gly Asn Asn Ile Lys Ile Cys Asn Glu Ser Ala Ser Arg
35 40 45
Lys
<210> 2089
<211> 61
<212> БЕЛОК
<213> Homo sapiens
<400> 2089
His Gly Trp Arg Pro Phe Leu Pro Val Arg Ala Arg Ser Arg Trp Asn
1 5 10 15
Arg Arg Leu Asp Val Thr Val Ala Asn Gly Arg Ser Trp Lys Tyr Gly
20 25 30
Trp Ser Leu Leu Arg Val Pro Gln Val Asn Gly Ile Gln Val Leu Asn
35 40 45
Val Ser Leu Lys Ser Ser Ser Asn Val Ile Ser Tyr Glu
50 55 60
<210> 2090
<211> 65
<212> БЕЛОК
<213> Homo sapiens
<400> 2090
Arg Leu Lys Glu Val Phe Gln Thr Lys Ile Gln Glu Phe Arg Lys Ala
1 5 10 15
Cys Tyr Thr Leu Thr Gly Tyr Gln Ile Asp Ile Thr Thr Glu Asn Gln
20 25 30
Tyr Arg Leu Thr Ser Leu Tyr Ala Glu His Pro Gly Asp Cys Leu Ile
35 40 45
Phe Lys Leu Arg Val Pro Gly Ser Ser Val Leu Val Thr Val Pro Gly
50 55 60
Leu
65
<210> 2091
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 2091
Ala Glu Val Leu Lys Val Ile Arg Gln Ser Ala Gly Gln Lys Thr Thr
1 5 10 15
Cys Gly Gln Gly Leu Glu Gly Pro Trp Glu Arg Pro Pro Pro Leu Asp
20 25 30
Glu Ser Glu Arg Asp Gly Gly Ser Glu Asp Gln Val Glu Asp Pro Ala
35 40 45
Leu Ser Ala Leu Leu Leu Arg Pro Arg Pro Pro Arg Pro Glu Val Gly
50 55 60
Ala His Gln Asp Glu Gln Ala Ala Gln Gly Ala Asp Pro Arg Leu Gly
65 70 75 80
Ala Gln Pro Ala Cys Arg Gly Leu Pro Gly Leu Leu Thr Val Pro Gln
85 90 95
Pro Glu Pro Leu Leu Ala Pro Pro Ser Ala Ala
100 105
<210> 2092
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 2092
Glu Arg Ala Glu Trp Arg Glu Asn Ile Arg Glu Gln Gln Lys Lys Cys
1 5 10 15
Phe Arg Ser Phe Ser Leu Thr Ser Val Glu Leu Gln Met Leu Thr Asn
20 25 30
Ser Cys Val Lys Leu Gln Thr Val His Ser Ile Pro Leu Thr Ile Asn
35 40 45
Lys Glu Glu Ala Leu Gln Arg Pro Val Ala Ser Asp Phe Glu Pro Gln
50 55 60
Gly Leu Ser Glu Ala Ala Arg Trp Asn Ser Lys Glu Asn Leu Leu Ala
65 70 75 80
Gly Pro Ser Glu Asn Asp Pro Asn Leu Phe Val Ala Leu Tyr Asp Phe
85 90 95
Val Ala Ser Gly
100
<210> 2093
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2093
Glu Leu Gln Met Leu Thr Asn Ser Cys Val Lys Leu Gln Thr Val His
1 5 10 15
Ser Ile Pro Leu Thr Ile Asn Lys Glu Asp Asp Glu Ser Pro Gly Leu
20 25 30
Tyr Gly Phe Leu Asn Val Ile Val His Ser Ala Thr Gly Phe Lys Gln
35 40 45
Ser Ser Lys Ala Leu Gln Arg Pro Val Ala Ser Asp Phe Glu Pro Gln
50 55 60
Gly Leu Ser Glu Ala Ala Arg Trp Asn Ser Lys Glu Asn Leu Leu Ala
65 70 75 80
Gly Pro Ser Glu Asn Asp Pro Asn Leu Phe Val Ala Leu Tyr Asp Phe
85 90 95
Val Ala Ser Gly Asp
100
<210> 2094
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2094
Ile Ser Asn Ser Trp Asp Ala His Leu Gly Leu Gly Ala Cys Gly Glu
1 5 10 15
Ala Glu Gly Leu Gly Val Gln Gly Ala Glu Glu Glu Glu Glu Glu Glu
20 25 30
Glu Glu Glu Glu Glu Glu Gly Ala Gly Val Pro Ala Cys Pro Pro Lys
35 40 45
Gly Pro Glu Leu Phe Pro Leu Ile Phe Pro Ala Glu Pro Ala Gln Ala
50 55 60
Ser Gly Pro Tyr Val Glu Ile Ile Glu Gln Pro Lys Gln Arg Gly Met
65 70 75 80
Arg Phe Arg Tyr Lys Cys Glu Gly Arg Ser Ala Gly Ser Ile Pro Gly
85 90 95
Glu Arg Ser Thr Asp
100
<210> 2095
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 2095
Leu Gln Arg Leu Asp Gly Met Gly Cys Leu Glu Phe Asp Glu Glu Arg
1 5 10 15
Ala Gln Gln Glu Asp Ala Leu Ala Gln Gln Ala Phe Glu Glu Ala Arg
20 25 30
Arg Arg Thr Arg Glu Phe Glu Asp Arg Asp Arg Ser His Arg Glu Glu
35 40 45
Met Glu Val His Glu Leu Glu Lys Ser Lys Arg Ala Leu Glu Thr Gln
50 55 60
Met Glu Glu Met Lys Thr Gln Leu Glu Glu Leu Glu Asp Glu Leu Gln
65 70 75 80
Ala Thr Glu Asp Ala Lys Leu Arg Leu Glu Val Asn Met Gln Ala Leu
85 90 95
Lys Gly Gln Phe
100
<210> 2096
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 2096
Lys Gly Ser Phe Pro Glu Asn Leu Arg His Leu Lys Asn Thr Met Glu
1 5 10 15
Thr Ile Asp Trp Lys Val Phe Glu Ser Trp Met His His Trp Leu Leu
20 25 30
Phe Glu Met Ser Arg His Ser Leu Glu Gln Lys Pro Thr Asp Ala Pro
35 40 45
Pro Lys Ala Gly Val Pro Asn Lys Pro Gly Ile Pro Lys Leu Leu Glu
50 55 60
Gly Ser Lys Asn Ser Ile Gln Trp Glu Lys Ala Glu Asp Asn Gly Cys
65 70 75 80
Arg Ile Thr Tyr Tyr Ile Leu Glu Ile Arg Lys Ser Thr Ser Asn Asn
85 90 95
Leu Gln Asn Gln
100
<210> 2097
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2097
Ser Trp Glu Asn Ser Asp Asp Ser Arg Asn Lys Leu Ser Lys Ile Pro
1 5 10 15
Ser Thr Pro Lys Leu Ile Pro Lys Val Thr Lys Thr Ala Asp Lys His
20 25 30
Lys Asp Val Ile Ile Asn Gln Ala Lys Met Ser Thr Arg Glu Lys Asn
35 40 45
Ser Gln Val Tyr Arg Arg Lys His Gln Glu Leu Gln Ala Met Gln Met
50 55 60
Glu Leu Gln Ser Pro Glu Tyr Lys Leu Ser Lys Leu Arg Thr Ser Thr
65 70 75 80
Ile Met Thr Asp Tyr Asn Pro Asn Tyr Cys Phe Ala Gly Lys Thr Ser
85 90 95
Ser Ile Ser Asp Leu
100
<210> 2098
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 2098
Glu Gly His Arg Met Asp Lys Pro Ala Asn Cys Thr His Asp Leu Tyr
1 5 10 15
Met Ile Met Arg Glu Cys Trp His Ala Ala Pro Ser Gln Arg Pro Thr
20 25 30
Phe Lys Gln Leu Val Glu Asp Leu Asp Arg Val Leu Thr Val Thr Ser
35 40 45
Thr Asp Val Lys Ala Thr Gln Glu Glu Asn Arg Glu Leu Arg Ser Arg
50 55 60
Cys Glu Glu Leu His Gly Lys Asn Leu Glu Leu Gly Lys Ile Met Asp
65 70 75 80
Arg Phe Glu Glu Val Val Tyr Gln Ala Met Glu Glu Val Gln Lys Gln
85 90 95
Lys Glu Leu Ser
100
<210> 2099
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 2099
Arg Asp Asn Thr Leu Leu Leu Arg Arg Val Glu Leu Phe Ser Leu Ser
1 5 10 15
Arg Gln Val Ala Arg Glu Ser Thr Tyr Leu Ser Ser Leu Lys Gly Ser
20 25 30
Arg Leu His Pro Glu Glu Leu Gly Gly Pro Pro Leu Lys Lys Leu Lys
35 40 45
Gln Glu Ala Thr Ser Lys Ser Gln Ile Met Ser Leu Trp Gly Leu Val
50 55 60
Ser Lys Met Pro Pro Glu Lys Val Gln Arg Leu Tyr Val Asp Phe Pro
65 70 75 80
Gln His Leu Arg His Leu Leu Gly Asp Trp Leu Glu Ser Gln Pro Trp
85 90 95
Glu Phe Leu Val Gly Ser Asp Ala Phe Cys Cys
100 105
<210> 2100
<211> 83
<212> БЕЛОК
<213> Homo sapiens
<400> 2100
Met Ser Arg Glu Met Gln Asp Val Asp Leu Ala Glu Val Lys Pro Leu
1 5 10 15
Val Glu Lys Gly Glu Thr Ile Thr Gly Leu Leu Gln Glu Phe Asp Val
20 25 30
Gln Glu Ala Leu Ser Val Val Ser Glu Asp Gln Ser Leu Phe Glu Cys
35 40 45
Ala Tyr Gly Thr Pro His Leu Ala Lys Thr Glu Met Thr Ala Ser Ser
50 55 60
Ser Ser Asp Tyr Gly Gln Thr Ser Lys Met Ser Pro Arg Val Pro Gln
65 70 75 80
Gln Asp Trp
<210> 2101
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2101
Val Leu Asp Met His Gly Phe Leu Arg Gln Ala Leu Cys Arg Leu Arg
1 5 10 15
Gln Glu Glu Pro Gln Ser Leu Gln Ala Ala Val Arg Thr Asp Gly Phe
20 25 30
Asp Glu Phe Lys Val Arg Leu Gln Asp Leu Ser Ser Cys Ile Thr Gln
35 40 45
Gly Lys Ala Ile Glu Thr Gln Ser Ser Ser Ser Glu Glu Ile Val Pro
50 55 60
Ser Pro Pro Ser Pro Pro Pro Leu Pro Arg Ile Tyr Lys Pro Cys Phe
65 70 75 80
Val Cys Gln Asp Lys Ser Ser Gly Tyr His Tyr Gly Val Ser Ala Cys
85 90 95
Glu Gly Cys Lys Gly
100
<210> 2102
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2102
Arg Ser Ser Pro Glu Gln Pro Arg Pro Ser Thr Ser Lys Ala Val Ser
1 5 10 15
Pro Pro His Leu Asp Gly Pro Pro Ser Pro Arg Ser Pro Val Ile Gly
20 25 30
Ser Glu Val Phe Leu Pro Asn Ser Asn His Val Ala Ser Gly Ala Gly
35 40 45
Glu Ala Ala Ile Glu Thr Gln Ser Ser Ser Ser Glu Glu Ile Val Pro
50 55 60
Ser Pro Pro Ser Pro Pro Pro Leu Pro Arg Ile Tyr Lys Pro Cys Phe
65 70 75 80
Val Cys Gln Asp Lys Ser Ser Gly Tyr His Tyr Gly Val Ser Ala Cys
85 90 95
Glu Gly Cys Lys Gly
100
<210> 2103
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 2103
Val Ala Arg Phe Asn Asp Leu Arg Phe Val Gly Arg Ser Gly Arg Gly
1 5 10 15
Lys Ser Phe Thr Leu Thr Ile Thr Val Phe Thr Asn Pro Pro Gln Val
20 25 30
Ala Thr Tyr His Arg Ala Ile Lys Ile Thr Val Asp Gly Pro Arg Glu
35 40 45
Pro Arg Asn Arg Thr Glu Lys His Ser Thr Met Pro Asp Ser Pro Val
50 55 60
Asp Val Lys Thr Gln Ser Arg Leu Thr Pro Pro Thr Met Pro Pro Pro
65 70 75 80
Pro Thr Thr Gln Gly Ala Pro Arg Thr Ser Ser Phe Thr Pro Thr Thr
85 90 95
Leu Thr Asn Gly Thr
100
<210> 2104
<211> 55
<212> БЕЛОК
<213> Homo sapiens
<400> 2104
Met Ala Leu Asn Ser Glu Ala Leu Ser Val Val Ser Glu Asp Gln Ser
1 5 10 15
Leu Phe Glu Cys Ala Tyr Gly Thr Pro His Leu Ala Lys Thr Glu Met
20 25 30
Thr Ala Ser Ser Ser Ser Asp Tyr Gly Gln Thr Ser Lys Met Ser Pro
35 40 45
Arg Val Pro Gln Gln Asp Trp
50 55
<210> 2105
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2105
Gly Gln Tyr Gly Lys Val Tyr Glu Gly
1 5
<210> 2106
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2106
Gly Gln Tyr Gly Lys Val Tyr Glu Gly Val
1 5 10
<210> 2107
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2107
Lys Leu Gly Gly Gly Gln Tyr Gly Lys
1 5
<210> 2108
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2108
Lys Leu Gly Gly Gly Gln Tyr Gly Lys Val
1 5 10
<210> 2109
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2109
Lys Val Tyr Glu Gly Val Trp Lys Lys
1 5
<210> 2110
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2110
Lys Val Tyr Glu Gly Val Trp Lys Lys Tyr
1 5 10
<210> 2111
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2111
Gln Tyr Gly Lys Val Tyr Glu Gly Val
1 5
<210> 2112
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2112
Gln Tyr Gly Lys Val Tyr Glu Gly Val Trp
1 5 10
<210> 2113
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2113
Gly Gln Tyr Gly Val Val Tyr Glu Gly
1 5
<210> 2114
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2114
Gly Gln Tyr Gly Val Val Tyr Glu Gly Val
1 5 10
<210> 2115
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2115
Lys Leu Gly Gly Gly Gln Tyr Gly Val
1 5
<210> 2116
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2116
Lys Leu Gly Gly Gly Gln Tyr Gly Val Val
1 5 10
<210> 2117
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2117
Gln Tyr Gly Val Val Tyr Glu Gly Val
1 5
<210> 2118
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2118
Gln Tyr Gly Val Val Tyr Glu Gly Val Trp
1 5 10
<210> 2119
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2119
Val Val Tyr Glu Gly Val Trp Lys Lys
1 5
<210> 2120
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2120
Val Val Tyr Glu Gly Val Trp Lys Lys Tyr
1 5 10
<210> 2121
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2121
Ala Thr Gln Ile Ser Ser Ala Thr Glu Tyr
1 5 10
<210> 2122
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2122
Ile Ser Ser Ala Thr Glu Tyr Leu Glu Lys
1 5 10
<210> 2123
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2123
Ser Ser Ala Thr Glu Tyr Leu Glu Lys
1 5
<210> 2124
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2124
Thr Gln Ile Ser Ser Ala Thr Glu Tyr Leu
1 5 10
<210> 2125
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2125
Tyr Met Ala Thr Gln Ile Ser Ser Ala Thr
1 5 10
<210> 2126
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2126
Phe Tyr Ile Ile Ile Glu Phe Met Thr Tyr
1 5 10
<210> 2127
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2127
Ile Ile Glu Phe Met Thr Tyr Gly Asn Leu
1 5 10
<210> 2128
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2128
Ile Ile Ile Glu Phe Met Thr Tyr Gly
1 5
<210> 2129
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2129
Ile Ile Ile Glu Phe Met Thr Tyr Gly Asn
1 5 10
<210> 2130
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2130
Tyr Ile Ile Ile Glu Phe Met Thr Tyr Gly
1 5 10
<210> 2131
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2131
Gly Gln His Gly Glu Val Tyr Glu Gly Val
1 5 10
<210> 2132
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2132
Lys Leu Gly Gly Gly Gln His Gly Glu Val
1 5 10
<210> 2133
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2133
Lys Ile Ala Asp Phe Gly Met Ala Arg
1 5
<210> 2134
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2134
Arg Val Ala Lys Ile Ala Asp Phe Gly Met
1 5 10
<210> 2135
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2135
Phe Ile Leu Met Glu Leu Met Ala Gly Gly
1 5 10
<210> 2136
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2136
Ile Leu Met Glu Leu Met Ala Gly Gly
1 5
<210> 2137
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2137
Ile Leu Met Glu Leu Met Ala Gly Gly Asp
1 5 10
<210> 2138
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2138
Leu Met Glu Leu Met Ala Gly Gly Asp Leu
1 5 10
<210> 2139
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2139
Leu Pro Arg Phe Ile Leu Met Glu Leu
1 5
<210> 2140
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2140
Leu Pro Arg Phe Ile Leu Met Glu Leu Met
1 5 10
<210> 2141
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2141
Leu Gln Ser Leu Pro Arg Phe Ile Leu Met
1 5 10
<210> 2142
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2142
Ser Leu Pro Arg Phe Ile Leu Met Glu Leu
1 5 10
<210> 2143
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2143
Leu Ala Thr Glu Lys Ser Arg Trp Ser
1 5
<210> 2144
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2144
Leu Ala Thr Glu Lys Ser Arg Trp Ser Gly
1 5 10
<210> 2145
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2145
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 2146
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2146
Gly Pro Pro Pro Ala Asp Leu Cys His Ala Leu
1 5 10
<210> 2147
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2147
Gly Leu Leu Leu Glu Met Leu Asp Ala
1 5
<210> 2148
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2148
Leu Tyr Gly Leu Leu Leu Glu Met Leu
1 5
<210> 2149
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2149
Asn Val Val Pro Leu Tyr Gly Leu Leu
1 5
<210> 2150
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2150
Pro Leu Tyr Gly Leu Leu Leu Glu Met
1 5
<210> 2151
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2151
Pro Leu Tyr Gly Leu Leu Leu Glu Met Leu
1 5 10
<210> 2152
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2152
Val Pro Leu Tyr Gly Leu Leu Leu Glu Met
1 5 10
<210> 2153
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2153
Val Val Pro Leu Tyr Gly Leu Leu Leu
1 5
<210> 2154
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2154
Phe Leu Pro Ser Thr Leu Lys Ser Leu
1 5
<210> 2155
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2155
Gly Val Tyr Thr Phe Leu Pro Ser Thr
1 5
<210> 2156
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2156
Gly Val Tyr Thr Phe Leu Pro Ser Thr Leu
1 5 10
<210> 2157
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2157
Thr Phe Leu Pro Ser Thr Leu Lys Ser Leu
1 5 10
<210> 2158
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2158
Val Tyr Thr Phe Leu Pro Ser Thr Leu
1 5
<210> 2159
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2159
Tyr Thr Phe Leu Pro Ser Thr Leu Lys
1 5
<210> 2160
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2160
Asn Val Val Pro Leu Cys Asp Leu Leu
1 5
<210> 2161
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2161
Asn Val Val Pro Leu Cys Asp Leu Leu Leu
1 5 10
<210> 2162
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2162
Pro Leu Cys Asp Leu Leu Leu Glu Met
1 5
<210> 2163
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2163
Pro Leu Cys Asp Leu Leu Leu Glu Met Leu
1 5 10
<210> 2164
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2164
Val Pro Leu Cys Asp Leu Leu Leu Glu Met
1 5 10
<210> 2165
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2165
Val Val Pro Leu Cys Asp Leu Leu Leu
1 5
<210> 2166
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2166
Asn Val Val Pro Leu Asn Asp Leu Leu
1 5
<210> 2167
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2167
Asn Val Val Pro Leu Asn Asp Leu Leu Leu
1 5 10
<210> 2168
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2168
Pro Leu Asn Asp Leu Leu Leu Glu Met
1 5
<210> 2169
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2169
Pro Leu Asn Asp Leu Leu Leu Glu Met Leu
1 5 10
<210> 2170
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2170
Val Pro Leu Asn Asp Leu Leu Leu Glu Met
1 5 10
<210> 2171
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2171
Asn Val Val Pro Leu Ser Asp Leu Leu
1 5
<210> 2172
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2172
Asn Val Val Pro Leu Ser Asp Leu Leu Leu
1 5 10
<210> 2173
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2173
Pro Leu Ser Asp Leu Leu Leu Glu Met
1 5
<210> 2174
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2174
Pro Leu Ser Asp Leu Leu Leu Glu Met Leu
1 5 10
<210> 2175
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2175
Val Pro Leu Ser Asp Leu Leu Leu Glu Met
1 5 10
<210> 2176
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2176
Val Val Pro Leu Ser Asp Leu Leu Leu
1 5
<210> 2177
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2177
Val Leu Glu Arg Cys Pro His Arg Pro Ile
1 5 10
<210> 2178
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2178
Tyr Thr Leu Asp Val Leu Glu Arg Cys
1 5
<210> 2179
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2179
Phe Gln Asn Gly Lys Met Ala Leu Ser
1 5
<210> 2180
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2180
Val Met Ala Gly Leu Gly Ser Pro Tyr Val
1 5 10
<210> 2181
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2181
Lys Pro Ile Ile Ile Gly His His Ala
1 5
<210> 2182
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2182
Lys Pro Ile Ile Ile Gly Cys His Ala
1 5
<210> 2183
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2183
Lys Pro Ile Ile Ile Gly Gly His Ala
1 5
<210> 2184
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2184
Lys Pro Ile Ile Ile Gly Ser His Ala
1 5
<210> 2185
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2185
Ile Ile Glu Tyr Cys Cys Tyr Gly Asp Leu
1 5 10
<210> 2186
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2186
Thr Ile Gly Gly Pro Thr Leu Val Ile Ile
1 5 10
<210> 2187
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2187
Val Ile Ile Glu Tyr Cys Cys Tyr Gly
1 5
<210> 2188
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2188
His Met Asn Ile Ala Asn Leu Leu Gly Ala
1 5 10
<210> 2189
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2189
Ile Ala Asn Leu Leu Gly Ala Cys Thr Ile
1 5 10
<210> 2190
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2190
Met Asn Ile Ala Asn Leu Leu Gly Ala
1 5
<210> 2191
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2191
Tyr Leu Gly Asn His Met Asn Ile Ala
1 5
<210> 2192
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2192
Tyr Leu Gly Asn His Met Asn Ile Ala Asn
1 5 10
<210> 2193
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2193
Val Leu His Glu Ser Asn Ser Pro Tyr
1 5
<210> 2194
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2194
Val Leu His Glu Ser Asn Ser Pro Tyr Ile
1 5 10
<210> 2195
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2195
Leu Gln Val Leu His Glu Cys Asn Ser Leu
1 5 10
<210> 2196
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2196
Leu Tyr Ile Val Gly Phe Tyr Gly Ala Phe
1 5 10
<210> 2197
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2197
Asn Ser Leu Tyr Ile Val Gly Phe Tyr
1 5
<210> 2198
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2198
Gln Val Leu His Glu Cys Asn Ser Leu
1 5
<210> 2199
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2199
Ser Leu Tyr Ile Val Gly Phe Tyr Gly
1 5
<210> 2200
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2200
Ser Leu Tyr Ile Val Gly Phe Tyr Gly Ala
1 5 10
<210> 2201
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2201
Val Leu His Glu Cys Asn Ser Leu Tyr
1 5
<210> 2202
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2202
Val Leu His Glu Cys Asn Ser Leu Tyr Ile
1 5 10
<210> 2203
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2203
Phe Tyr Gln Gln Gln Gln Gln Ser Asp Leu
1 5 10
<210> 2204
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2204
Gln Gln Gln Ser Asp Leu Gln Pro Pro Ala
1 5 10
<210> 2205
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2205
Gln Gln Ser Asp Leu Gln Pro Pro Ala
1 5
<210> 2206
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2206
Tyr Gln Gln Gln Gln Gln Ser Asp Leu
1 5
<210> 2207
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2207
Phe Glu Leu Leu Ser Thr Pro Pro Leu
1 5
<210> 2208
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2208
Leu Leu Ser Thr Pro Pro Leu Ser Pro Ser
1 5 10
<210> 2209
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2209
Phe Glu Leu Leu Pro Ile Pro Pro Leu
1 5
<210> 2210
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2210
Ile Trp Lys Lys Phe Glu Leu Leu Pro Ile
1 5 10
<210> 2211
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2211
Leu Leu Pro Ile Pro Pro Leu Ser Pro Ser
1 5 10
<210> 2212
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2212
Leu Pro Ile Pro Pro Leu Ser Pro Ser
1 5
<210> 2213
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2213
Ile Ile Glu Tyr Cys Phe Tyr Gly Asp Leu
1 5 10
<210> 2214
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2214
Ile Ile Ile Glu Tyr Cys Phe Tyr Gly
1 5
<210> 2215
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2215
Ile Tyr Ile Ile Ile Glu Tyr Cys Phe
1 5
<210> 2216
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2216
Ile Tyr Ile Ile Ile Glu Tyr Cys Phe Tyr
1 5 10
<210> 2217
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2217
Tyr Ile Ile Ile Glu Tyr Cys Phe Tyr Gly
1 5 10
<210> 2218
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2218
Lys Ile Thr Glu Gln Glu Lys Asp Phe Leu
1 5 10
<210> 2219
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2219
Ser Thr Arg Asp Pro Leu Ser Glu Ile Thr Lys
1 5 10
<210> 2220
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2220
Asp Pro Leu Ser Glu Ile Thr Lys
1 5
<210> 2221
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2221
Leu Pro Leu Lys Phe Arg Asp Ala Glu Thr
1 5 10
<210> 2222
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2222
Gln Thr Gly Val Met Ile Cys Ala Tyr Leu
1 5 10
<210> 2223
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2223
Ala Phe Ser Gly Glu Tyr Ile Pro Thr Val
1 5 10
<210> 2224
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2224
Ser Met Asn Arg Arg Pro Ile Leu Thr
1 5
<210> 2225
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2225
Tyr Met Cys Asn Ser Ser Cys Met Gly Ser
1 5 10
<210> 2226
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2226
Gly Met Asn Gln Arg Pro Ile Leu Thr
1 5
<210> 2227
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2227
Gly Met Asn Trp Arg Pro Ile Leu Thr
1 5
<210> 2228
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2228
Leu Leu Gly Arg Asn Ser Phe Glu Val Cys
1 5 10
<210> 2229
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2229
Ala Leu Lys Tyr Ile Phe Val Ala Val
1 5
<210> 2230
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2230
Ala Leu Lys Tyr Ile Phe Val Ala Val Arg
1 5 10
<210> 2231
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2231
Ala Val Arg Ala Ile Cys Val Met Lys
1 5
<210> 2232
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2232
Ala Val Arg Ala Ile Cys Val Met Lys Ser
1 5 10
<210> 2233
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2233
Cys Val Glu Lys Lys Thr Ala Leu Lys
1 5
<210> 2234
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2234
Cys Val Glu Lys Lys Thr Ala Leu Lys Tyr
1 5 10
<210> 2235
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2235
Cys Val Met Lys Ser Phe Leu Ile Phe
1 5
<210> 2236
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2236
Cys Val Met Lys Ser Phe Leu Ile Phe Arg
1 5 10
<210> 2237
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2237
Phe Leu Ile Phe Arg Arg Trp Lys Ser
1 5
<210> 2238
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2238
Phe Arg Arg Trp Lys Ser His Ser Pro Leu
1 5 10
<210> 2239
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2239
Phe Val Ala Val Arg Ala Ile Cys Val
1 5
<210> 2240
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2240
Phe Val Ala Val Arg Ala Ile Cys Val Met
1 5 10
<210> 2241
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2241
Ile Gln Leu His Leu Ser His Pro Ile
1 5
<210> 2242
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2242
Lys Ser Phe Leu Ile Phe Arg Arg Trp Lys
1 5 10
<210> 2243
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2243
Lys Thr Ala Leu Lys Tyr Ile Phe Val
1 5
<210> 2244
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2244
Lys Tyr Ile Phe Val Ala Val Arg Ala Ile
1 5 10
<210> 2245
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2245
Arg Trp Lys Ser His Ser Pro Leu Gln Ile
1 5 10
<210> 2246
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2246
Thr Ala Leu Lys Tyr Ile Phe Val Ala Val
1 5 10
<210> 2247
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2247
Val Ala Val Arg Ala Ile Cys Val Met Lys
1 5 10
<210> 2248
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2248
Val Met Lys Ser Phe Leu Ile Phe Arg
1 5
<210> 2249
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2249
Val Met Lys Ser Phe Leu Ile Phe Arg Arg
1 5 10
<210> 2250
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2250
Tyr Ile Phe Val Ala Val Arg Ala Ile
1 5
<210> 2251
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2251
Ala Leu Phe Phe Phe Phe Phe Glu Thr
1 5
<210> 2252
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2252
Ala Leu Phe Phe Phe Phe Phe Glu Thr Lys
1 5 10
<210> 2253
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2253
Ala Gln Ala Gly Val Gln Trp Arg Ser Leu
1 5 10
<210> 2254
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2254
Cys Leu Ala Asn Phe Cys Ile Phe Asn Arg
1 5 10
<210> 2255
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2255
Cys Leu Ser Phe Leu Ser Ser Trp Asp Tyr
1 5 10
<210> 2256
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2256
Phe Phe Glu Thr Lys Ser Cys Ser Val
1 5
<210> 2257
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2257
Phe Phe Phe Glu Thr Lys Ser Cys Ser Val
1 5 10
<210> 2258
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2258
Phe Lys Leu Phe Ser Cys Leu Ser Phe Leu
1 5 10
<210> 2259
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2259
Phe Leu Ser Ser Trp Asp Tyr Arg Arg Met
1 5 10
<210> 2260
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2260
Gly Phe Lys Leu Phe Ser Cys Leu Ser Phe
1 5 10
<210> 2261
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2261
Lys Leu Phe Ser Cys Leu Ser Phe Leu
1 5
<210> 2262
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2262
Lys Leu Phe Ser Cys Leu Ser Phe Leu Ser
1 5 10
<210> 2263
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2263
Leu Ala Leu Phe Phe Phe Phe Phe Glu Thr
1 5 10
<210> 2264
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2264
Leu Phe Phe Phe Phe Phe Glu Thr Lys
1 5
<210> 2265
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2265
Leu Ser Phe Leu Ser Ser Trp Asp Tyr
1 5
<210> 2266
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2266
Leu Ser Phe Leu Ser Ser Trp Asp Tyr Arg
1 5 10
<210> 2267
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2267
Arg Met Pro Pro Cys Leu Ala Asn Phe
1 5
<210> 2268
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2268
Arg Arg Met Pro Pro Cys Leu Ala Asn Phe
1 5 10
<210> 2269
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2269
Ser Leu Gln Pro Pro Pro Pro Gly Phe Lys
1 5 10
<210> 2270
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2270
Val Gln Trp Arg Ser Leu Gly Ser Leu
1 5
<210> 2271
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2271
Phe Phe Phe Ser Val Ile Phe Ser Thr
1 5
<210> 2272
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2272
Met Ser Val Cys Phe Phe Phe Phe Ser Val
1 5 10
<210> 2273
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2273
Ser Val Cys Phe Phe Phe Phe Ser Val
1 5
<210> 2274
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2274
Ser Val Cys Phe Phe Phe Phe Ser Val Ile
1 5 10
<210> 2275
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2275
Phe Phe Cys Tyr Ile Leu Asn Thr Met Phe
1 5 10
<210> 2276
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2276
Met Ser Val Cys Phe Phe Phe Phe Cys Tyr
1 5 10
<210> 2277
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2277
Ser Val Cys Phe Phe Phe Phe Cys Tyr Ile
1 5 10
<210> 2278
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2278
Lys Gln Trp Ser Ser Val Thr Ser Leu
1 5
<210> 2279
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2279
Val Leu Trp Met Pro Thr Ser Thr Val
1 5
<210> 2280
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2280
Ile Leu Ile Arg Lys Ala Met Thr Val
1 5
<210> 2281
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2281
Arg Met Lys Val Pro Leu Met Lys
1 5
<210> 2282
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2282
Thr Leu Lys Lys Lys Pro Arg Asp Ile
1 5
<210> 2283
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2283
Leu Ile Glu Gly Phe Glu Ala Leu Leu Lys
1 5 10
<210> 2284
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2284
Gln Gln Leu Lys Trp Thr Pro His Ile
1 5
<210> 2285
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2285
Gln Leu Lys Trp Thr Pro His Ile Leu Lys
1 5 10
<210> 2286
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2286
Ile Val Ser Glu Lys Asn Gln Gln Leu Lys
1 5 10
<210> 2287
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2287
Gln Leu Lys Trp Thr Pro His Ile Leu Lys
1 5 10
<210> 2288
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2288
Gln Gln Leu Lys Trp Thr Pro His Ile
1 5
<210> 2289
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2289
Asn Gln Gln Leu Lys Trp Thr Pro His Ile Leu
1 5 10
<210> 2290
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2290
Asn Gln Gln Leu Lys Trp Thr Pro His Ile
1 5 10
<210> 2291
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2291
Gln Leu Lys Trp Thr Pro His Ile Leu
1 5
<210> 2292
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2292
Gly Pro Pro Arg Pro Pro Arg Ala Ala Cys
1 5 10
<210> 2293
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2293
Pro Pro Arg Pro Pro Arg Ala Ala Cys
1 5
<210> 2294
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2294
Ser Leu Arg Arg Lys Tyr Leu Arg Val
1 5
<210> 2295
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2295
Ser Ala Ala Cys His Arg Arg Gly Cys Val
1 5 10
<210> 2296
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2296
Ala Leu Trp Glu Cys Ser Leu Pro Gln Ala
1 5 10
<210> 2297
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2297
Cys Leu Ile Val Ser Arg Thr Leu Leu
1 5
<210> 2298
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2298
Cys Leu Ile Val Ser Arg Thr Leu Leu Leu
1 5 10
<210> 2299
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2299
Phe Leu Leu Ala Leu Trp Glu Cys Ser
1 5
<210> 2300
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2300
Phe Leu Leu Ala Leu Trp Glu Cys Ser Leu
1 5 10
<210> 2301
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2301
Ile Val Ser Arg Thr Leu Leu Leu Val
1 5
<210> 2302
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2302
Leu Ile Val Ser Arg Thr Leu Leu Leu
1 5
<210> 2303
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2303
Leu Ile Val Ser Arg Thr Leu Leu Leu Val
1 5 10
<210> 2304
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2304
Leu Leu Ala Leu Trp Glu Cys Ser Leu
1 5
<210> 2305
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2305
Leu Pro Gln Ala Arg Leu Cys Leu Ile
1 5
<210> 2306
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2306
Leu Pro Gln Ala Arg Leu Cys Leu Ile Val
1 5 10
<210> 2307
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2307
Asn Val Arg Asp Lys Lys Arg Ala Thr Phe
1 5 10
<210> 2308
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2308
Ser Leu Pro Gln Ala Arg Leu Cys Leu Ile
1 5 10
<210> 2309
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2309
Phe Phe Cys Trp Ile Leu Ser Cys Lys
1 5
<210> 2310
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2310
Phe Phe Phe Cys Trp Ile Leu Ser Cys Lys
1 5 10
<210> 2311
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2311
Ile Thr Ala Phe Phe Phe Cys Trp Ile
1 5
<210> 2312
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2312
Leu Tyr Ile Thr Ala Phe Phe Phe Cys Trp
1 5 10
<210> 2313
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2313
Tyr Ile Thr Ala Phe Phe Phe Cys Trp Ile
1 5 10
<210> 2314
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2314
Ile Thr Ala Phe Phe Leu Leu Asp Ile
1 5
<210> 2315
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2315
Leu Leu Tyr Ile Thr Ala Phe Phe Leu
1 5
<210> 2316
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2316
Leu Leu Tyr Ile Thr Ala Phe Phe Leu Leu
1 5 10
<210> 2317
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2317
Leu Tyr Ile Thr Ala Phe Phe Leu Leu
1 5
<210> 2318
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2318
Leu Tyr Ile Thr Ala Phe Phe Leu Leu Asp
1 5 10
<210> 2319
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2319
Tyr Ile Thr Ala Phe Phe Leu Leu Asp Ile
1 5 10
<210> 2320
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2320
Gly Ser Asn Glu Val Thr Thr Arg Tyr
1 5
<210> 2321
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2321
Met Pro Lys Asp Val Asn Ile Gln Val
1 5
<210> 2322
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2322
Thr Gly Ser Asn Glu Val Thr Thr Arg Tyr
1 5 10
<210> 2323
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2323
Lys Lys Leu Met Leu Leu Arg Leu Asn Leu
1 5 10
<210> 2324
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2324
Lys Leu Met Leu Leu Arg Leu Asn Leu
1 5
<210> 2325
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2325
Lys Leu Met Leu Leu Arg Leu Asn Leu Arg
1 5 10
<210> 2326
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2326
Leu Leu Arg Leu Asn Leu Arg Lys Met
1 5
<210> 2327
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2327
Leu Met Leu Leu Arg Leu Asn Leu
1 5
<210> 2328
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2328
Leu Met Leu Leu Arg Leu Asn Leu Arg Lys
1 5 10
<210> 2329
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2329
Leu Asn Leu Arg Lys Met Cys Gly Pro Phe
1 5 10
<210> 2330
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2330
Met Leu Leu Arg Leu Asn Leu Arg Lys
1 5
<210> 2331
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2331
Met Leu Leu Arg Leu Asn Leu Arg Lys Met
1 5 10
<210> 2332
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2332
Asn Leu Arg Lys Met Cys Gly Pro Phe
1 5
<210> 2333
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2333
Asn Tyr Cys Gln Lys Lys Leu Met Leu Leu
1 5 10
<210> 2334
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2334
Tyr Cys Gln Lys Lys Leu Met Leu Leu
1 5
<210> 2335
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2335
Phe Lys Lys Lys Thr Tyr Thr Cys Ala Ile
1 5 10
<210> 2336
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2336
Ile Thr Thr Val Lys Ala Thr Glu Thr Lys
1 5 10
<210> 2337
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2337
Lys Ser Lys Lys Lys Glu Thr Phe Lys
1 5
<210> 2338
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2338
Lys Ser Lys Lys Lys Glu Thr Phe Lys Lys
1 5 10
<210> 2339
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2339
Lys Thr Tyr Thr Cys Ala Ile Thr Thr Val
1 5 10
<210> 2340
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2340
Thr Phe Lys Lys Lys Thr Tyr Thr Cys
1 5
<210> 2341
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2341
Thr Tyr Thr Cys Ala Ile Thr Thr Val
1 5
<210> 2342
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2342
Thr Tyr Thr Cys Ala Ile Thr Thr Val Lys
1 5 10
<210> 2343
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2343
Tyr Thr Cys Ala Ile Thr Thr Val Lys
1 5
<210> 2344
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2344
Thr Ala Lys Ser Lys Lys Arg Asn Leu
1 5
<210> 2345
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2345
Phe Ala Leu Cys Gly Phe Trp Gln Ile
1 5
<210> 2346
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2346
Leu Lys Lys Leu Arg Ser Pro Leu
1 5
<210> 2347
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2347
Ser Leu Lys Lys Val Pro Ala Leu
1 5
<210> 2348
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2348
Arg Lys Ile Ser Asn Trp Ser Leu Lys Lys
1 5 10
<210> 2349
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2349
Val Pro Ala Leu Lys Lys Leu Arg Ser Pro Leu
1 5 10
<210> 2350
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2350
Lys Arg Val Asn Thr Ala Trp Lys Thr Lys
1 5 10
<210> 2351
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2351
Met Thr Lys Lys Lys Arg Val Asn Thr Ala
1 5 10
<210> 2352
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2352
Arg Val Asn Thr Ala Trp Lys Thr Lys
1 5
<210> 2353
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2353
Arg Val Asn Thr Ala Trp Lys Thr Lys Lys
1 5 10
<210> 2354
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2354
Thr Lys Lys Lys Arg Val Asn Thr Ala
1 5
<210> 2355
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2355
Trp Lys Thr Lys Lys Thr Ser Phe Ser Leu
1 5 10
<210> 2356
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2356
Ala Leu Met Ser Ala Met Thr Thr Ser
1 5
<210> 2357
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2357
Ala Met Thr Thr Ser Ser Ser Gln Lys
1 5
<210> 2358
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2358
Ala Met Thr Thr Ser Ser Ser Gln Lys Asn
1 5 10
<210> 2359
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2359
Cys Ile Met Lys Glu Lys Lys Ser Leu
1 5
<210> 2360
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2360
Cys Ile Met Lys Glu Lys Lys Ser Leu Val
1 5 10
<210> 2361
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2361
Ile Met Lys Glu Lys Lys Ser Leu
1 5
<210> 2362
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2362
Ile Met Lys Glu Lys Lys Ser Leu Val
1 5
<210> 2363
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2363
Lys Ser Leu Val Arg Leu Ser Ser Cys Val
1 5 10
<210> 2364
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2364
Leu Val Arg Leu Ser Ser Cys Val Pro Val
1 5 10
<210> 2365
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2365
Arg Leu Ser Ser Cys Val Pro Val Ala
1 5
<210> 2366
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2366
Arg Leu Ser Ser Cys Val Pro Val Ala Leu
1 5 10
<210> 2367
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2367
Ser Ala Met Thr Thr Ser Ser Ser Gln Lys
1 5 10
<210> 2368
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2368
Ser Leu Val Arg Leu Ser Ser Cys Val
1 5
<210> 2369
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2369
Val Pro Val Ala Leu Met Ser Ala Met
1 5
<210> 2370
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2370
Val Arg Leu Ser Ser Cys Val Pro Val Ala
1 5 10
<210> 2371
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2371
Lys Met Arg Lys Lys Tyr Ala Gln Lys
1 5
<210> 2372
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2372
Phe Val Met Ser Asp Thr Thr Tyr Lys
1 5
<210> 2373
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2373
Phe Val Met Ser Asp Thr Thr Tyr Lys Ile
1 5 10
<210> 2374
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2374
Lys Thr Phe Glu Lys Lys Gly Glu Lys
1 5
<210> 2375
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2375
Leu Phe Val Met Ser Asp Thr Thr Tyr Lys
1 5 10
<210> 2376
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2376
Met Ser Asp Thr Thr Tyr Lys Ile Tyr
1 5
<210> 2377
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2377
Val Met Ser Asp Thr Thr Tyr Lys Ile
1 5
<210> 2378
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2378
Val Met Ser Asp Thr Thr Tyr Lys Ile Tyr
1 5 10
<210> 2379
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2379
Tyr Leu Thr Lys Trp Pro Lys Phe Phe Leu
1 5 10
<210> 2380
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2380
Phe Leu Gln Glu Arg Asn Leu Pro Pro
1 5
<210> 2381
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2381
Phe Arg Arg Pro His Ser Cys Leu Ala
1 5
<210> 2382
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2382
Leu Ile Val Leu Arg Val Val Arg Leu
1 5
<210> 2383
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2383
Leu Leu Ser Val His Leu Ile Val Leu
1 5
<210> 2384
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2384
Glu Val Lys His Leu His His Leu Leu
1 5
<210> 2385
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2385
His Leu His His Leu Leu Lys Gln Leu Lys
1 5 10
<210> 2386
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2386
His Leu Leu Leu Lys Arg Glu Arg Val
1 5
<210> 2387
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2387
Lys Ile Lys His Leu Leu Leu Lys Arg
1 5
<210> 2388
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2388
Lys Pro Ser Glu Lys Tyr Leu Lys Ile
1 5
<210> 2389
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2389
Lys Tyr Leu Lys Ile Lys His Leu Leu
1 5
<210> 2390
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2390
Lys Tyr Leu Lys Ile Lys His Leu Leu Leu
1 5 10
<210> 2391
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2391
Leu Leu Lys Gln Leu Lys Pro Ser Glu Lys
1 5 10
<210> 2392
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2392
Leu Leu Lys Arg Glu Arg Val Asp Leu
1 5
<210> 2393
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2393
Leu Leu Leu Lys Arg Glu Arg Val Asp Leu
1 5 10
<210> 2394
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2394
Gln Leu Lys Pro Ser Glu Lys Tyr Leu Lys
1 5 10
<210> 2395
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2395
Tyr Leu Lys Ile Lys His Leu Leu Leu
1 5
<210> 2396
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2396
Tyr Leu Lys Ile Lys His Leu Leu Leu Lys
1 5 10
<210> 2397
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2397
Ile Leu Pro Arg Lys Val Leu Gln Met
1 5
<210> 2398
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2398
Lys Val Leu Gln Met Asp Phe Leu Val
1 5
<210> 2399
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2399
Leu Pro Arg Lys Val Leu Gln Met Asp Phe
1 5 10
<210> 2400
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2400
Leu Gln Met Asp Phe Leu Val His Pro Ala
1 5 10
<210> 2401
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2401
Gln Met Asp Phe Leu Val His Pro Ala
1 5
<210> 2402
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2402
Tyr Ile Leu Pro Arg Lys Val Leu Gln Met
1 5 10
<210> 2403
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2403
Ala Pro Ser Pro Ala Ser Arg Leu Gln Cys
1 5 10
<210> 2404
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2404
His Pro Leu Ala Pro Met Pro Ser Lys Thr
1 5 10
<210> 2405
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2405
Ile Leu Pro Leu Pro Gln Leu Leu Leu
1 5
<210> 2406
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2406
Leu Leu Leu Ser Ala Asp Gln Gln Ala
1 5
<210> 2407
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2407
Leu Pro Thr Gln Thr Arg Gly Cys Ile
1 5
<210> 2408
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2408
Leu Pro Thr Gln Thr Arg Gly Cys Ile Leu
1 5 10
<210> 2409
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2409
Arg Ile Ser Cys Leu Pro Thr Gln Thr Arg
1 5 10
<210> 2410
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2410
Ser Leu Ala Glu Thr Val Ser Leu His
1 5
<210> 2411
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2411
Thr Pro Arg Ser Ser Ser Ser Ser Ser
1 5
<210> 2412
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2412
Thr Pro Arg Ser Ser Ser Ser Ser Ser Ser
1 5 10
<210> 2413
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2413
Ala Leu Pro Pro Val Leu Leu Ser Leu
1 5
<210> 2414
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2414
Ala Leu Pro Pro Val Leu Leu Ser Leu Ala
1 5 10
<210> 2415
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2415
Ala Leu Pro Arg Pro Leu Leu Ala Leu
1 5
<210> 2416
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2416
Ala Ser Arg Thr Ala Ser Cys Ile Leu
1 5
<210> 2417
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2417
Glu Ala Leu Pro Arg Pro Leu Leu Ala Leu
1 5 10
<210> 2418
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2418
His Leu Gly His Pro Val Ala Ser Arg
1 5
<210> 2419
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2419
His Pro Val Ala Ser Arg Thr Ala Ser
1 5
<210> 2420
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2420
His Pro Val Ala Ser Arg Thr Ala Ser Cys
1 5 10
<210> 2421
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2421
Ile Ile Gln Leu Ser Leu Leu Ser Leu Leu
1 5 10
<210> 2422
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2422
Ile Gln Leu Ser Leu Leu Ser Leu Leu
1 5
<210> 2423
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2423
Ile Gln Leu Ser Leu Leu Ser Leu Leu Ile
1 5 10
<210> 2424
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2424
Leu Leu Ala Leu Pro Pro Val Leu Leu
1 5
<210> 2425
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2425
Leu Leu Ile Pro Pro Leu Thr Cys Leu
1 5
<210> 2426
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2426
Leu Leu Ile Pro Pro Leu Thr Cys Leu Ala
1 5 10
<210> 2427
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2427
Leu Leu Ser Leu Leu Ile Pro Pro Leu
1 5
<210> 2428
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2428
Leu Leu Ser Leu Leu Ile Pro Pro Leu Thr
1 5 10
<210> 2429
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2429
Leu Pro Arg Pro Leu Leu Ala Leu Pro Pro
1 5 10
<210> 2430
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2430
Gln Leu Ser Leu Leu Ser Leu Leu Ile
1 5
<210> 2431
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2431
Arg Leu Leu Gln Cys Gln Ala Thr Arg
1 5
<210> 2432
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2432
Arg Pro Leu Leu Ala Leu Pro Pro Val
1 5
<210> 2433
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2433
Arg Pro Leu Leu Ala Leu Pro Pro Val Leu
1 5 10
<210> 2434
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2434
Ser Leu Ala Gln Asp His Ser Arg Leu
1 5
<210> 2435
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2435
Ser Leu Ala Gln Asp His Ser Arg Leu Leu
1 5 10
<210> 2436
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2436
Ser Leu Leu Ile Pro Pro Leu Thr Cys Leu
1 5 10
<210> 2437
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2437
Ser Leu Leu Ser Leu Leu Ile Pro Pro
1 5
<210> 2438
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2438
Ser Leu Leu Ser Leu Leu Ile Pro Pro Leu
1 5 10
<210> 2439
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2439
Ala Ala Ala Thr Ser Ala Ala Ser Thr Leu
1 5 10
<210> 2440
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2440
Ala Ala Ile Pro Ala Ser Thr Ser Ala Val
1 5 10
<210> 2441
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2441
Ala Ile Pro Ala Ser Thr Ser Ala Val
1 5
<210> 2442
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2442
Ala Leu Pro Ala Gly Cys Val Ser Ser Ala
1 5 10
<210> 2443
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2443
Ala Pro Leu Leu Thr Ala Thr Gly Ser Val
1 5 10
<210> 2444
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2444
Ala Pro Val Leu Ser Ala Ser Ile Leu
1 5
<210> 2445
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2445
Ala Thr Leu Leu Pro Ala Thr Thr Val
1 5
<210> 2446
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2446
Ala Thr Val Ser Thr Thr Thr Ala Pro Val
1 5 10
<210> 2447
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2447
Ala Val Pro Ala Asn Cys Leu Phe Pro Ala
1 5 10
<210> 2448
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2448
Cys Leu Phe Pro Ala Ala Leu Pro Ser Thr
1 5 10
<210> 2449
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2449
Cys Pro Thr Phe Val Ser Ala Ala Ala
1 5
<210> 2450
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2450
Phe Pro Ala Ala Leu Pro Ser Thr Ala
1 5
<210> 2451
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2451
Phe Pro Ala Ala Leu Pro Ser Thr Ala Gly
1 5 10
<210> 2452
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2452
Gly Ala Glu Cys His Gly Arg Pro Leu
1 5
<210> 2453
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2453
Gly Ala Ile Ser Arg Phe Ile Trp Val
1 5
<210> 2454
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2454
Ile Leu Pro Ala Ala Ile Pro Ala Ser Thr
1 5 10
<210> 2455
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2455
Ile Trp Val Ser Gly Ile Leu Ser Pro Leu
1 5 10
<210> 2456
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2456
Leu Leu Thr Ala Thr Gly Ser Val Ser Leu
1 5 10
<210> 2457
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2457
Leu Leu Tyr Thr Ala Asp Ser Ser Leu
1 5
<210> 2458
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2458
Leu Pro Ala Ala Ala Thr Ser Ala Ala
1 5
<210> 2459
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2459
Leu Pro Ala Ala Ala Thr Ser Ala Ala Ser
1 5 10
<210> 2460
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2460
Leu Pro Ala Ala Ile Pro Ala Ser Thr
1 5
<210> 2461
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2461
Leu Pro Ala Gly Cys Val Ser Ser Ala
1 5
<210> 2462
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2462
Leu Pro Ala Gly Cys Val Ser Ser Ala Pro
1 5 10
<210> 2463
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2463
Leu Tyr Thr Ala Asp Ser Ser Leu Trp
1 5
<210> 2464
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2464
Gln Pro Ala Lys Ser Ser Pro Ser Ala
1 5
<210> 2465
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2465
Gln Pro Ala Lys Ser Ser Pro Ser Ala Ala
1 5 10
<210> 2466
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2466
Arg Phe Ile Trp Val Ser Gly Ile Leu
1 5
<210> 2467
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2467
Arg Pro Gln Arg Val Trp Ser Thr Gly
1 5
<210> 2468
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2468
Arg Val Trp Ser Thr Gly Pro Asp Ser Ile
1 5 10
<210> 2469
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2469
Ser Ala Val Pro Gly Ser Ile Pro Leu
1 5
<210> 2470
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2470
Ser Ile Leu Pro Ala Ala Ile Pro Ala
1 5
<210> 2471
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2471
Ser Leu Pro Ala Ala Ala Thr Ser Ala
1 5
<210> 2472
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2472
Ser Leu Pro Ala Ala Ala Thr Ser Ala Ala
1 5 10
<210> 2473
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2473
Ser Leu Trp Thr Thr Arg Pro Gln Arg
1 5
<210> 2474
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2474
Ser Leu Trp Thr Thr Arg Pro Gln Arg Val
1 5 10
<210> 2475
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2475
Ser Pro Ser Ala Ala Ala Ala Thr Leu
1 5
<210> 2476
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2476
Ser Pro Ser Ala Ala Ala Ala Thr Leu Leu
1 5 10
<210> 2477
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2477
Thr Leu Asp Ala Leu Pro Ala Gly Cys Val
1 5 10
<210> 2478
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2478
Thr Val Ser Thr Thr Thr Ala Pro Val
1 5
<210> 2479
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2479
Val Leu Ser Ala Ser Ile Leu Pro Ala
1 5
<210> 2480
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2480
Val Leu Ser Ala Ser Ile Leu Pro Ala Ala
1 5 10
<210> 2481
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2481
Val Pro Ala Asn Cys Leu Phe Pro Ala
1 5
<210> 2482
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2482
Val Pro Ala Asn Cys Leu Phe Pro Ala Ala
1 5 10
<210> 2483
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2483
Val Pro Asp Pro Ser Cys Pro Thr Phe
1 5
<210> 2484
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2484
Val Pro Gly Ser Ile Pro Leu Pro Ala
1 5
<210> 2485
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2485
Val Pro Gly Ser Ile Pro Leu Pro Ala Val
1 5 10
<210> 2486
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2486
Trp Val Ser Gly Ile Leu Ser Pro Leu
1 5
<210> 2487
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2487
Tyr Thr Ala Asp Ser Ser Leu Trp Thr Thr
1 5 10
<210> 2488
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2488
Ala Pro Ala Gly Met Val Asn Arg Ala
1 5
<210> 2489
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2489
Ala Ser Leu His Arg Arg Ser Tyr Leu
1 5
<210> 2490
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2490
Ala Ser Leu His Arg Arg Ser Tyr Leu Lys
1 5 10
<210> 2491
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2491
Phe Leu Leu Met Asp Asn Lys Ala Pro Ala
1 5 10
<210> 2492
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2492
His Pro Arg Arg Ser Pro Ser Arg Leu
1 5
<210> 2493
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2493
His Pro Ser Leu His Ile Ser Ser Pro
1 5
<210> 2494
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2494
His Arg Arg Ser Tyr Leu Lys Ile His Leu
1 5 10
<210> 2495
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2495
His Ser Arg Phe Leu Leu Met Asp Asn Lys
1 5 10
<210> 2496
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2496
Lys Leu Pro Ile Pro Ser Ser Ala Ser Leu
1 5 10
<210> 2497
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2497
Lys Val Leu Thr Leu Ser Ser Ser Ser His
1 5 10
<210> 2498
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2498
Leu Ile His Ser Arg Phe Leu Leu Met
1 5
<210> 2499
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2499
Leu Leu Met Asp Asn Lys Ala Pro Ala
1 5
<210> 2500
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2500
Leu Met Asp Asn Lys Ala Pro Ala Gly Met
1 5 10
<210> 2501
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2501
Leu Pro Ile Pro Ser Ser Ala Ser Leu
1 5
<210> 2502
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2502
Met Pro Asn Leu Arg Ile Ser Ser Ser
1 5
<210> 2503
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2503
Met Pro Asn Leu Arg Ile Ser Ser Ser His
1 5 10
<210> 2504
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2504
Asn Leu Arg Ile Ser Ser Ser His Ser Leu
1 5 10
<210> 2505
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2505
Pro Pro Thr His Ser His Arg Leu Ser Leu
1 5 10
<210> 2506
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2506
Arg Ala Gly Arg Arg Val Pro Trp Ala Ala
1 5 10
<210> 2507
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2507
Arg Ala Arg Leu His Ile Thr Thr Ser Lys
1 5 10
<210> 2508
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2508
Arg Ile Ser Ser Ser His Ser Leu Asn His
1 5 10
<210> 2509
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2509
Arg Leu His Thr Pro Pro Ser Ser Arg
1 5
<210> 2510
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2510
Arg Leu His Thr Pro Pro Ser Ser Arg Arg
1 5 10
<210> 2511
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2511
Arg Leu Arg Ile Leu Ser Pro Ser Leu
1 5
<210> 2512
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2512
Arg Pro Leu Met Pro Asn Leu Arg Ile
1 5
<210> 2513
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2513
Arg Pro Arg Pro Leu Met Pro Asn Leu
1 5
<210> 2514
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2514
Ser Ala Ser Leu His Arg Arg Ser Tyr Leu
1 5 10
<210> 2515
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2515
Ser Leu His Ile Ser Ser Pro Arg Leu
1 5
<210> 2516
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2516
Ser Leu His Arg Arg Ser Tyr Leu Lys
1 5
<210> 2517
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2517
Ser Leu His Arg Arg Ser Tyr Leu Lys Ile
1 5 10
<210> 2518
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2518
Ser Leu Ile His Ser Arg Phe Leu Leu
1 5
<210> 2519
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2519
Ser Leu Ile His Ser Arg Phe Leu Leu Met
1 5 10
<210> 2520
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2520
Ser Leu Leu Thr Ser Ser Ser Asn Leu
1 5
<210> 2521
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2521
Ser Leu Asn His His Ser Ser Ser Pro Leu
1 5 10
<210> 2522
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2522
Ser Leu Ser Ser Pro Ser Lys Leu Pro Ile
1 5 10
<210> 2523
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2523
Ser Pro Leu Ser Leu His Thr Pro Ser
1 5
<210> 2524
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2524
Ser Pro Leu Ser Leu His Thr Pro Ser Ser
1 5 10
<210> 2525
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2525
Ser Pro Pro Thr His Ser His Arg Leu
1 5
<210> 2526
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2526
Ser Pro Arg Leu His Thr Pro Pro Ser
1 5
<210> 2527
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2527
Ser Pro Arg Leu His Thr Pro Pro Ser Ser
1 5 10
<210> 2528
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2528
Ser Pro Ser Leu Ser Ser Pro Ser Lys Leu
1 5 10
<210> 2529
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2529
Ser Tyr Leu Lys Ile His Leu Gly Leu
1 5
<210> 2530
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2530
Thr Pro Ser Asn His Arg Pro Arg Pro Leu
1 5 10
<210> 2531
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2531
Thr Pro Ser Ser His Pro Ser Leu His Ile
1 5 10
<210> 2532
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2532
Cys Val Pro Phe Trp Thr Gly Arg Ile Leu
1 5 10
<210> 2533
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2533
His Cys Val Pro Phe Trp Thr Gly Arg Ile Leu
1 5 10
<210> 2534
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2534
Ile Leu Leu Pro Ser Ala Ala Ser Val
1 5
<210> 2535
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2535
Ile Leu Leu Pro Ser Ala Ala Ser Val Cys
1 5 10
<210> 2536
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2536
Leu Leu Pro Ser Ala Ala Ser Val Cys Pro Ile
1 5 10
<210> 2537
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2537
Leu Pro Ser Ala Ala Ser Val Cys Pro Ile
1 5 10
<210> 2538
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2538
Met Arg Pro His Cys Val Pro Phe
1 5
<210> 2539
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2539
Arg Ile Leu Leu Pro Ser Ala Ala Ser Val
1 5 10
<210> 2540
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2540
Arg Met Arg Pro His Cys Val Pro Phe
1 5
<210> 2541
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2541
Arg Met Arg Pro His Cys Val Pro Phe Trp
1 5 10
<210> 2542
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2542
Arg Thr Asn Pro Thr Val Arg Met Arg
1 5
<210> 2543
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2543
Ser Val Cys Pro Ile Pro Phe Glu Ala
1 5
<210> 2544
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2544
Thr Val Arg Met Arg Pro His Cys Val
1 5
<210> 2545
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2545
Thr Val Arg Met Arg Pro His Cys Val Pro Phe
1 5 10
<210> 2546
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2546
Val Pro Phe Trp Thr Gly Arg Ile Leu
1 5
<210> 2547
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2547
Val Pro Phe Trp Thr Gly Arg Ile Leu Leu
1 5 10
<210> 2548
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2548
Val Arg Met Arg Pro His Cys Val Pro Phe
1 5 10
<210> 2549
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2549
Ala Met Val Pro Arg Gly Val Ser Met
1 5
<210> 2550
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2550
Ala Met Val Pro Arg Gly Val Ser Met Ala
1 5 10
<210> 2551
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2551
Ala Trp Ala Pro Thr Ser Arg Thr Pro Trp
1 5 10
<210> 2552
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2552
Cys Pro Met Pro Thr Thr Pro Val Gln Ala
1 5 10
<210> 2553
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2553
Cys Pro Ser Thr Val Pro Pro Ser Pro Ala
1 5 10
<210> 2554
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2554
Gly Ala Met Val Pro Arg Gly Val Ser Met
1 5 10
<210> 2555
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2555
Met Pro Cys Pro Met Pro Thr Thr Pro Val
1 5 10
<210> 2556
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2556
Met Pro Thr Thr Pro Val Gln Ala Trp
1 5
<210> 2557
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2557
Met Pro Thr Thr Pro Val Gln Ala Trp Leu
1 5 10
<210> 2558
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2558
Ser Leu Pro Glu Asp Arg Tyr Thr Gln Ala
1 5 10
<210> 2559
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2559
Ser Pro Ala Gln Pro Tyr Leu Arg Val
1 5
<210> 2560
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2560
Ser Pro Ala Gln Pro Tyr Leu Arg Val Ser
1 5 10
<210> 2561
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2561
Thr Ile Met Pro Cys Pro Met Pro Thr
1 5
<210> 2562
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2562
Thr Pro Val Gln Ala Trp Leu Glu Ala
1 5
<210> 2563
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2563
Thr Ser Arg Thr Pro Trp Gly Ala Met
1 5
<210> 2564
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2564
Val Pro Pro Ser Pro Ala Gln Pro Tyr Leu
1 5 10
<210> 2565
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2565
Val Pro Arg Gly Val Ser Met Ala His
1 5
<210> 2566
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2566
Cys Leu Ser Ala Arg Thr Gly Leu Ser Ile
1 5 10
<210> 2567
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2567
Cys Thr Thr Leu Asn Ser Pro Pro Leu Lys
1 5 10
<210> 2568
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2568
Gly Leu Ser Ile Ser Cys Thr Thr Leu
1 5
<210> 2569
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2569
Ser Pro Pro Leu Lys Lys Met Ser Met
1 5
<210> 2570
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2570
Thr Leu Asn Ser Pro Pro Leu Lys Lys
1 5
<210> 2571
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2571
Thr Thr Leu Asn Ser Pro Pro Leu Lys
1 5
<210> 2572
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2572
Thr Thr Leu Asn Ser Pro Pro Leu Lys Lys
1 5 10
<210> 2573
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2573
Leu Gln Arg Phe Arg Phe Thr His Val
1 5
<210> 2574
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2574
Leu Gln Arg Phe Arg Phe Thr His Val Ile
1 5 10
<210> 2575
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2575
Arg Leu Ser Ser Val Leu Gln Arg Phe
1 5
<210> 2576
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2576
Arg Leu Ser Ser Val Leu Gln Arg Phe Arg
1 5 10
<210> 2577
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2577
Val Leu Gln Arg Phe Arg Phe Thr His Val
1 5 10
<210> 2578
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2578
Ala Ser Val Gly Arg His Ser Leu Ser Lys
1 5 10
<210> 2579
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2579
Lys Phe Leu Pro Phe Trp Gly Phe Leu
1 5
<210> 2580
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2580
Leu Ala Ser Val Gly Arg His Ser Leu
1 5
<210> 2581
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2581
Leu Pro Phe Trp Gly Phe Leu Glu Glu Phe
1 5 10
<210> 2582
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2582
Pro Phe Trp Gly Phe Leu Glu Glu Phe
1 5
<210> 2583
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2583
Ser Val Gly Arg His Ser Leu Ser Lys
1 5
<210> 2584
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2584
Ala Pro Arg Pro Ile Arg Pro Pro Phe
1 5
<210> 2585
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2585
Ala Pro Arg Pro Ile Arg Pro Pro Phe Leu
1 5 10
<210> 2586
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2586
Ala Gln Lys Met Lys Lys Ala His Phe Leu
1 5 10
<210> 2587
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2587
Phe Leu Pro Ser Ala Ala Gln Lys Met
1 5
<210> 2588
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2588
Gly Leu Phe Leu Pro Ser Ala Ala Gln Lys
1 5 10
<210> 2589
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2589
His Pro Leu Leu Val Ser Leu Leu Leu
1 5
<210> 2590
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2590
Lys Ala His Phe Leu Lys Thr Trp Phe Arg
1 5 10
<210> 2591
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2591
Lys Ala Arg Phe Ser Thr Ala Ser Leu
1 5
<210> 2592
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2592
Lys Met Lys Lys Ala His Phe Leu Lys
1 5
<210> 2593
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2593
Lys Thr Trp Phe Arg Ser Asn Pro Thr Lys
1 5 10
<210> 2594
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2594
Leu Ala Lys Glu Leu Thr His Pro Leu
1 5
<210> 2595
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2595
Leu Ala Lys Glu Leu Thr His Pro Leu Leu
1 5 10
<210> 2596
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2596
Asn Pro Thr Lys Thr Lys Lys Ala Arg Phe
1 5 10
<210> 2597
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2597
Gln Lys Met Lys Lys Ala His Phe Leu
1 5
<210> 2598
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2598
Arg Phe Ser Thr Ala Ser Leu Ala Lys
1 5
<210> 2599
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2599
Arg Pro Ile Arg Pro Pro Phe Leu Glu Ser
1 5 10
<210> 2600
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2600
Arg Ser Asn Pro Thr Lys Thr Lys Lys
1 5
<210> 2601
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2601
Ser Leu Ala Lys Glu Leu Thr His Pro Leu
1 5 10
<210> 2602
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2602
Thr Lys Lys Ala Arg Phe Ser Thr Ala
1 5
<210> 2603
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2603
Gly Leu Arg Phe Trp Asn Pro Ser Arg
1 5
<210> 2604
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2604
Ile Ser Gln Leu Leu Ser Trp Pro Gln Lys
1 5 10
<210> 2605
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2605
Arg Ile Ala His Ile Ser Gln Leu Leu
1 5
<210> 2606
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2606
Arg Leu Gly Tyr Ser Ser His Gln Leu
1 5
<210> 2607
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2607
Ser Gln Leu Leu Ser Trp Pro Gln Lys
1 5
<210> 2608
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2608
Ser Arg Ile Ala His Ile Ser Gln Leu
1 5
<210> 2609
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2609
Trp Pro Gln Lys Thr Glu Glu Arg Leu
1 5
<210> 2610
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2610
Tyr Ser Ser His Gln Leu Pro Arg Lys
1 5
<210> 2611
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2611
Cys Pro Gln Arg Met Thr Pro Gly Thr Thr
1 5 10
<210> 2612
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2612
Glu Ala Glu Lys Arg Thr Arg Thr Leu
1 5
<210> 2613
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2613
Gly Thr Thr Phe Ile Thr Met Met Lys
1 5
<210> 2614
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2614
Gly Thr Thr Phe Ile Thr Met Met Lys Lys
1 5 10
<210> 2615
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2615
Ile Thr Met Met Lys Lys Glu Ala Glu Lys
1 5 10
<210> 2616
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2616
Arg Met Thr Pro Gly Thr Thr Phe Ile
1 5
<210> 2617
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2617
Ser Pro Tyr Cys Pro Gln Arg Met Thr
1 5
<210> 2618
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2618
Thr Met Met Lys Lys Glu Ala Glu Lys
1 5
<210> 2619
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2619
Thr Pro Gly Thr Thr Phe Ile Thr Met
1 5
<210> 2620
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2620
Thr Pro Gly Thr Thr Phe Ile Thr Met Met
1 5 10
<210> 2621
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2621
Thr Thr Phe Ile Thr Met Met Lys Lys
1 5
<210> 2622
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2622
Cys Pro Gly Ala Thr Trp Arg Glu Ala
1 5
<210> 2623
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2623
Cys Pro Gly Ala Thr Trp Arg Glu Ala Ala
1 5 10
<210> 2624
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2624
Arg Ser Arg Cys Pro Gly Ala Thr Trp Arg
1 5 10
<210> 2625
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2625
Thr Pro Arg Ala Thr Arg Ser Arg Cys
1 5
<210> 2626
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2626
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 2627
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2627
Arg Pro Leu Gln Thr His Val Leu Pro Glu
1 5 10
<210> 2628
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2628
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 2629
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2629
Ala Pro Ser Glu Ser Pro Cys Ser Pro Phe
1 5 10
<210> 2630
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2630
Cys Pro Leu Asp His Thr Thr Pro Pro Ala
1 5 10
<210> 2631
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2631
Phe Leu Gln Glu Gln Tyr His Glu Ala
1 5
<210> 2632
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2632
Arg Leu Ala Phe Leu Gln Glu Gln Tyr His
1 5 10
<210> 2633
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2633
Ser Pro Cys Ser Pro Phe Arg Leu Ala Phe
1 5 10
<210> 2634
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2634
Ser Pro Pro Trp Val Arg Ala Leu Leu
1 5
<210> 2635
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2635
Tyr Pro Ala Cys Pro Leu Asp His Thr Thr
1 5 10
<210> 2636
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2636
Ala Leu His Leu Arg Ser Cys Pro Cys
1 5
<210> 2637
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2637
Cys Leu His His Arg Arg His Leu Val
1 5
<210> 2638
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2638
Cys Leu His His Arg Arg His Leu Val Cys
1 5 10
<210> 2639
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2639
Cys Leu His Arg Lys Ser His Pro His Leu
1 5 10
<210> 2640
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2640
Cys Leu Arg Ser His Ala Cys Pro Pro
1 5
<210> 2641
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2641
Cys Leu Arg Ser His Thr Cys Pro Pro
1 5
<210> 2642
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2642
Cys Leu Trp Cys His Ala Cys Leu His
1 5
<210> 2643
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2643
Cys Pro His His Leu Lys Asn His Leu
1 5
<210> 2644
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2644
Cys Pro His His Leu Lys Asn Leu Leu
1 5
<210> 2645
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2645
Cys Pro His His Leu Arg Thr Arg Leu
1 5
<210> 2646
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2646
Cys Pro Leu His Leu Arg Ser Leu Pro Phe
1 5 10
<210> 2647
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2647
Cys Pro Leu Pro Arg His Leu Lys His Leu
1 5 10
<210> 2648
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2648
Cys Pro Leu Ser Leu Arg Ser His Pro Cys
1 5 10
<210> 2649
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2649
Cys Pro Arg His Leu Arg Asn Cys Pro Leu
1 5 10
<210> 2650
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2650
Phe Pro His His Leu Arg His His Ala
1 5
<210> 2651
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2651
Phe Pro His His Leu Arg His His Ala Cys
1 5 10
<210> 2652
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2652
Gly Leu Arg Ser Arg Thr Cys Pro Pro
1 5
<210> 2653
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2653
His Ala Cys Leu His Arg Leu Arg Asn Leu
1 5 10
<210> 2654
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2654
His Leu Ala Cys Leu His His Leu Arg
1 5
<210> 2655
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2655
His Leu Cys Pro Pro His Leu Arg Tyr
1 5
<210> 2656
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2656
His Leu Cys Pro Pro His Leu Arg Tyr Arg
1 5 10
<210> 2657
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2657
His Leu Lys His Leu Ala Cys Leu His
1 5
<210> 2658
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2658
His Leu Lys His Arg Pro Cys Pro His
1 5
<210> 2659
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2659
His Leu Lys Asn His Leu Cys Pro Pro
1 5
<210> 2660
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2660
His Leu Lys Ser His Pro Cys Leu His
1 5
<210> 2661
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2661
His Leu Lys Ser Leu Leu Cys Pro Leu
1 5
<210> 2662
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2662
His Leu Leu His Leu Arg Arg Leu Tyr
1 5
<210> 2663
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2663
His Leu Arg Asn Cys Pro Leu Pro Arg
1 5
<210> 2664
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2664
His Leu Arg Asn Cys Pro Leu Pro Arg His
1 5 10
<210> 2665
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2665
His Leu Arg Arg Leu Tyr Pro His His Leu
1 5 10
<210> 2666
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2666
His Leu Arg Ser His Pro Cys Pro Leu
1 5
<210> 2667
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2667
His Leu Arg Ser His Pro Cys Pro Leu His
1 5 10
<210> 2668
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2668
His Leu Arg Ser Leu Pro Phe Pro His
1 5
<210> 2669
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2669
His Leu Arg Thr Arg Leu Cys Pro His
1 5
<210> 2670
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2670
His Leu Val Cys Ser His His Leu Lys
1 5
<210> 2671
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2671
His Pro Cys Leu His His Arg Arg His Leu
1 5 10
<210> 2672
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2672
His Pro Gly Leu Arg Ser Arg Thr Cys
1 5
<210> 2673
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2673
His Pro His Leu Leu His Leu Arg Arg Leu
1 5 10
<210> 2674
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2674
His Arg Lys Ser His Pro His Leu Leu
1 5
<210> 2675
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2675
His Arg Arg Thr Arg Ser Cys Pro Cys
1 5
<210> 2676
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2676
Lys Ser His Pro His Leu Leu His Leu Arg
1 5 10
<210> 2677
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2677
Lys Ser Leu Leu Cys Pro Leu His Leu Arg
1 5 10
<210> 2678
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2678
Leu Leu Cys Pro Leu His Leu Arg Ser Leu
1 5 10
<210> 2679
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2679
Leu Leu His Leu Arg Arg Leu Tyr Pro His
1 5 10
<210> 2680
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2680
Leu Pro Arg His Leu Lys His Leu Ala
1 5
<210> 2681
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2681
Leu Pro Arg His Leu Lys His Leu Ala Cys
1 5 10
<210> 2682
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2682
Leu Arg Arg Leu Arg Ser His Thr Cys
1 5
<210> 2683
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2683
Leu Arg Arg Leu Tyr Pro His His Leu
1 5
<210> 2684
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2684
Leu Val Cys Ser His His Leu Lys Ser Leu
1 5 10
<210> 2685
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2685
Asn Leu Arg Asn His Thr Cys Pro Pro Ser
1 5 10
<210> 2686
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2686
Pro Leu His Leu Arg Ser Leu Pro Phe
1 5
<210> 2687
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2687
Arg Leu Cys Pro His His Leu Lys Asn His
1 5 10
<210> 2688
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2688
Arg Leu Tyr Pro His His Leu Lys His
1 5
<210> 2689
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2689
Arg Leu Tyr Pro His His Leu Lys His Arg
1 5 10
<210> 2690
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2690
Arg Pro Cys Pro His His Leu Lys Asn Leu
1 5 10
<210> 2691
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2691
Arg Ser His Pro Cys Pro Leu His Leu Lys
1 5 10
<210> 2692
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2692
Arg Ser Leu Pro Phe Pro His His Leu Arg
1 5 10
<210> 2693
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2693
Arg Thr Arg Leu Cys Pro His His Leu
1 5
<210> 2694
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2694
Arg Thr Arg Leu Cys Pro His His Leu Lys
1 5 10
<210> 2695
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2695
Ser Leu Leu Cys Pro Leu His Leu Arg
1 5
<210> 2696
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2696
Ser Leu Arg Ser His Ala Cys Pro Pro
1 5
<210> 2697
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2697
Ser Pro Leu Arg Ser Gln Ala Asn Ala
1 5
<210> 2698
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2698
Tyr Leu Arg Arg Leu Arg Ser His Thr
1 5
<210> 2699
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2699
Tyr Pro His His Leu Lys His Arg Pro Cys
1 5 10
<210> 2700
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2700
Phe Ile Thr Ser Gly Gln Ile Phe Lys
1 5
<210> 2701
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2701
Ile Phe Ile Thr Ser Gly Gln Ile Phe
1 5
<210> 2702
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2702
Ser Gln Ser Glu Ala Leu Cys Val Leu
1 5
<210> 2703
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2703
Ser Gln Ser Glu Ala Leu Cys Val Leu Leu
1 5 10
<210> 2704
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2704
Ala Tyr Thr Gly Thr Ile Leu Met Met
1 5
<210> 2705
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2705
Asp Leu Lys Ala Tyr Thr Gly Thr Ile Leu
1 5 10
<210> 2706
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2706
Ile Leu Thr Lys Gln Ile Lys Thr Lys
1 5
<210> 2707
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2707
Lys Met Ile Leu Thr Lys Gln Ile Lys
1 5
<210> 2708
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2708
Lys Pro Thr Asp Thr Phe Leu Gln Ile
1 5
<210> 2709
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2709
Lys Pro Thr Asp Thr Phe Leu Gln Ile Leu
1 5 10
<210> 2710
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2710
Met Ile Leu Thr Lys Gln Ile Lys Thr Lys
1 5 10
<210> 2711
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2711
Ile Thr Arg Tyr Thr Ile Phe Val Leu Lys
1 5 10
<210> 2712
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2712
Leu Ile Ala Glu Leu His Asn Ile Leu
1 5
<210> 2713
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2713
Leu Ile Ala Glu Leu His Asn Ile Leu Leu
1 5 10
<210> 2714
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2714
Met Thr Pro Pro Asn Leu Ile Ala Glu Leu
1 5 10
<210> 2715
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2715
Asn Leu Ile Ala Glu Leu His Asn Ile
1 5
<210> 2716
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2716
Asn Leu Ile Ala Glu Leu His Asn Ile Leu
1 5 10
<210> 2717
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2717
Arg Tyr Thr Ile Phe Val Leu Lys Asp Ile
1 5 10
<210> 2718
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2718
Thr Ile Thr Arg Tyr Thr Ile Phe Val Leu
1 5 10
<210> 2719
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2719
Thr Pro Pro Asn Leu Ile Ala Glu Leu
1 5
<210> 2720
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2720
Phe Leu Gln Phe Arg Thr His Thr Thr
1 5
<210> 2721
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2721
Leu Pro Ala Lys Gly Glu Asp Ile Phe Leu
1 5 10
<210> 2722
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2722
Leu Gln Phe Arg Thr His Thr Thr Gly Arg
1 5 10
<210> 2723
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2723
Asn Leu Gln Ser Ser Val Cys Gly Leu
1 5
<210> 2724
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2724
Ser Ser Val Cys Gly Leu Pro Ala Lys
1 5
<210> 2725
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2725
Val Gln Trp Arg Asn Leu Gln Ser Ser Val
1 5 10
<210> 2726
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2726
Gly Gln Asn Val Ser Leu Leu Gly Lys
1 5
<210> 2727
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2727
His Thr Arg Thr Arg Gly Asn Leu Arg Lys
1 5 10
<210> 2728
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2728
Ile Leu His Thr Arg Thr Arg Gly Asn Leu
1 5 10
<210> 2729
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2729
Lys Gly Gln Asn Val Ser Leu Leu Gly Lys
1 5 10
<210> 2730
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2730
Leu Leu Gly Lys Tyr Ile Leu His Thr
1 5
<210> 2731
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2731
Leu Arg Lys Ser Arg Lys Trp Lys Ser Met
1 5 10
<210> 2732
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2732
Ser Leu Leu Gly Lys Tyr Ile Leu His
1 5
<210> 2733
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2733
Ser Leu Leu Gly Lys Tyr Ile Leu His Thr
1 5 10
<210> 2734
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2734
Cys Thr Ser Pro Leu Leu Ala Pro Val
1 5
<210> 2735
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2735
Phe Pro Glu Asn Leu Pro Gly Gln Leu
1 5
<210> 2736
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2736
Gly Leu Leu Ala Phe Trp Asp Ser Gln Val
1 5 10
<210> 2737
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2737
Ile Phe Cys Pro Phe Pro Glu Asn Leu
1 5
<210> 2738
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2738
Leu Leu Ala Phe Trp Asp Ser Gln Val
1 5
<210> 2739
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2739
Leu Leu Ala Pro Val Ile Phe Cys Pro
1 5
<210> 2740
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2740
Leu Leu Ala Pro Val Ile Phe Cys Pro Phe
1 5 10
<210> 2741
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2741
Leu Pro Cys Pro Gln Gln Asp Val Leu
1 5
<210> 2742
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2742
Arg Phe Pro Ser Gly Leu Leu Ala Phe
1 5
<210> 2743
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2743
Arg Phe Pro Ser Gly Leu Leu Ala Phe Trp
1 5 10
<210> 2744
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2744
Ser Pro Leu Leu Ala Pro Val Ile Phe
1 5
<210> 2745
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2745
Ser Pro Arg Gly Pro Cys Thr Ser Ser
1 5
<210> 2746
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2746
Ser Pro Arg Gly Pro Cys Thr Ser Ser Ser
1 5 10
<210> 2747
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2747
Ser Gln Val Cys Asp Leu His Val Leu
1 5
<210> 2748
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2748
Val Ile Phe Cys Pro Phe Pro Glu Asn Leu
1 5 10
<210> 2749
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2749
Ala Met Val Trp Pro Leu Leu Ser Ile
1 5
<210> 2750
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2750
Ala Met Val Trp Pro Leu Leu Ser Ile Leu
1 5 10
<210> 2751
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2751
Ala Gln Ile Ala Met Val Trp Pro Leu
1 5
<210> 2752
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2752
Ala Gln Ile Ala Met Val Trp Pro Leu Leu
1 5 10
<210> 2753
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2753
Cys Pro Met Ser Arg Leu Arg Leu Ala
1 5
<210> 2754
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2754
Cys Pro Met Ser Arg Leu Arg Leu Ala Leu
1 5 10
<210> 2755
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2755
Ile Ala Met Val Trp Pro Leu Leu Ser Ile
1 5 10
<210> 2756
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2756
Ile Leu Ser Glu Trp Lys Glu Ile Cys Val
1 5 10
<210> 2757
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2757
Ile Val Trp Trp Cys Pro Met Ser Arg
1 5
<210> 2758
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2758
Ile Val Trp Trp Cys Pro Met Ser Arg Leu
1 5 10
<210> 2759
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2759
Ile Trp Met Thr Glu Thr Leu Phe Asp Ile
1 5 10
<210> 2760
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2760
Leu Leu Ser Ile Leu Ser Glu Trp Lys
1 5
<210> 2761
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2761
Met Ser Ala Ala Gln Ile Ala Met Val
1 5
<210> 2762
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2762
Met Ser Arg Leu Arg Leu Ala Leu Thr
1 5
<210> 2763
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2763
Met Ser Arg Leu Arg Leu Ala Leu Thr Val
1 5 10
<210> 2764
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2764
Met Val Trp Pro Leu Leu Ser Ile Leu
1 5
<210> 2765
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2765
Arg Leu Ala Leu Thr Val Pro Pro Ser Thr
1 5 10
<210> 2766
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2766
Thr Leu Phe Asp Ile Val Trp Trp Cys
1 5
<210> 2767
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2767
Thr Leu Phe Asp Ile Val Trp Trp Cys Pro
1 5 10
<210> 2768
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2768
Thr Met Ser Ala Ala Gln Ile Ala Met Val
1 5 10
<210> 2769
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2769
Val Trp Ser Ile Trp Met Thr Glu Thr Leu
1 5 10
<210> 2770
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2770
Trp Met Thr Glu Thr Leu Phe Asp Ile
1 5
<210> 2771
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2771
Trp Met Thr Glu Thr Leu Phe Asp Ile Val
1 5 10
<210> 2772
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2772
Ala Leu Arg Cys Val Phe Val Pro Val
1 5
<210> 2773
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2773
Ala Leu Arg Cys Val Phe Val Pro Val Leu
1 5 10
<210> 2774
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2774
Ala Leu Ser Glu His Cys Pro Thr Thr
1 5
<210> 2775
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2775
Ala Gln Arg Lys Arg Ile Ser Ala Arg Lys
1 5 10
<210> 2776
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2776
Gly Ala Gln Arg Lys Arg Ile Ser Ala
1 5
<210> 2777
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2777
His Trp Met Glu Asn Ile Ser Pro Phe
1 5
<210> 2778
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2778
Leu Pro Ser Gln Arg Arg Asn His Trp
1 5
<210> 2779
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2779
Leu Pro Ser Gln Arg Arg Asn His Trp Met
1 5 10
<210> 2780
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2780
Asn Ile Ser Pro Phe Arg Ser Val Gly Val
1 5 10
<210> 2781
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2781
Arg Ile Ser Ala Arg Lys Gly Ser Leu
1 5
<210> 2782
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2782
Ser Pro Phe Arg Ser Val Gly Val Ser Ala
1 5 10
<210> 2783
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2783
Ser Pro Ser Ser His Trp Lys Thr Pro Val
1 5 10
<210> 2784
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2784
Thr Ala Leu Arg Cys Val Phe Val Pro Val
1 5 10
<210> 2785
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2785
Val Ile Tyr Trp Asp Gly Thr Ala Leu
1 5
<210> 2786
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2786
Val Ile Tyr Trp Asp Gly Thr Ala Leu Arg
1 5 10
<210> 2787
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2787
Val Leu Gly Glu Thr Gly Ala Gln Arg Lys
1 5 10
<210> 2788
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2788
His Pro Arg Pro Arg His Gly His Leu
1 5
<210> 2789
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2789
His Pro Arg Pro Arg His Gly His Leu Gln
1 5 10
<210> 2790
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2790
Arg Pro Arg His Gly His Leu Gln Ala
1 5
<210> 2791
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2791
Arg Pro Arg His Gly His Leu Gln Ala Val
1 5 10
<210> 2792
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2792
Gly Ser Leu Lys Thr Gln Val Gln Met Lys
1 5 10
<210> 2793
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2793
Pro Pro Gly Pro Cys His Leu Leu Ser Leu
1 5 10
<210> 2794
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2794
Arg Thr Ile Leu Asn Asn Gly Ser Leu Lys
1 5 10
<210> 2795
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2795
Ser Leu Lys Thr Gln Val Gln Met Lys
1 5
<210> 2796
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2796
Ser Leu Lys Thr Gln Val Gln Met Lys Leu
1 5 10
<210> 2797
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2797
Thr Ile Leu Asn Asn Gly Ser Leu Lys
1 5
<210> 2798
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2798
Cys Pro Pro Cys Arg Pro Lys Gln Trp Met
1 5 10
<210> 2799
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2799
Thr Thr Phe Cys Pro Pro Cys Arg Pro Lys
1 5 10
<210> 2800
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2800
Cys Phe Ala Asn Trp Pro Arg Pro Ala Leu
1 5 10
<210> 2801
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2801
Phe Ala Asn Trp Pro Arg Pro Ala Leu
1 5
<210> 2802
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2802
Gly Leu Ile Pro His Pro Arg Pro Ala
1 5
<210> 2803
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2803
His Pro Arg Pro Ala Pro Ala Ser Ala
1 5
<210> 2804
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2804
His Pro Arg Pro Ala Pro Ala Ser Ala Pro
1 5 10
<210> 2805
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2805
Ile Pro His Pro Arg Pro Ala Pro Ala
1 5
<210> 2806
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2806
Ile Pro His Pro Arg Pro Ala Pro Ala Ser
1 5 10
<210> 2807
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2807
Arg Pro Ala Leu Cys Ser Cys Gly Leu
1 5
<210> 2808
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2808
Arg Pro Ala Leu Cys Ser Cys Gly Leu Ile
1 5 10
<210> 2809
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2809
Thr Pro Leu Pro Ser Thr Arg Cys Phe
1 5
<210> 2810
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2810
Trp Pro Arg Pro Ala Leu Cys Ser Cys
1 5
<210> 2811
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2811
Trp Pro Arg Pro Ala Leu Cys Ser Cys Gly
1 5 10
<210> 2812
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2812
Ala Leu Arg Arg Ser Gly Arg Pro Pro Lys
1 5 10
<210> 2813
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2813
Gly Leu Val Pro Ser Leu Val Ser Lys
1 5
<210> 2814
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2814
Lys Ile Ser Val Glu Thr Tyr Thr Val
1 5
<210> 2815
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2815
Leu Leu Met Val Leu Met Ser Leu Asp Leu
1 5 10
<210> 2816
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2816
Leu Met Ser Leu Asp Leu Asp Thr Gly Leu
1 5 10
<210> 2817
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2817
Leu Met Val Leu Met Ser Leu Asp Leu
1 5
<210> 2818
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2818
Leu Val Ser Lys Cys Leu Ile Leu Arg Val
1 5 10
<210> 2819
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2819
Gln Leu Leu Met Val Leu Met Ser Leu
1 5
<210> 2820
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2820
Arg Pro Gly Ala Ala Asp Thr Gly Ala
1 5
<210> 2821
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2821
Arg Pro Gly Ala Ala Asp Thr Gly Ala His
1 5 10
<210> 2822
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2822
Ser Leu Asp Leu Asp Thr Gly Leu Val
1 5
<210> 2823
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2823
Ser Leu Val Ser Lys Cys Leu Ile Leu
1 5
<210> 2824
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2824
Ser Gln Leu Leu Met Val Leu Met Ser Leu
1 5 10
<210> 2825
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2825
Thr Val Ser Ser Gln Leu Leu Met Val
1 5
<210> 2826
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2826
Thr Tyr Thr Val Ser Ser Gln Leu Leu
1 5
<210> 2827
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2827
Thr Tyr Thr Val Ser Ser Gln Leu Leu Met
1 5 10
<210> 2828
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2828
Val Leu Met Ser Leu Asp Leu Asp Thr
1 5
<210> 2829
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2829
Val Pro Ser Leu Val Ser Lys Cys Leu
1 5
<210> 2830
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2830
Val Ser Lys Cys Leu Ile Leu Arg Val Lys
1 5 10
<210> 2831
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2831
Tyr Thr Val Ser Ser Gln Leu Leu Met
1 5
<210> 2832
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2832
Tyr Thr Val Ser Ser Gln Leu Leu Met Val
1 5 10
<210> 2833
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2833
Phe Cys Gln Tyr His Thr Ala Ser Val
1 5
<210> 2834
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2834
Cys Pro Tyr Gly Ser Thr Ser Thr Ala
1 5
<210> 2835
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2835
Cys Pro Tyr Gly Ser Thr Ser Thr Ala Ser
1 5 10
<210> 2836
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2836
Leu Ala Arg Ala Ala Ala Ser Thr Ala Thr
1 5 10
<210> 2837
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2837
Met Leu Thr Asp Ser Leu Phe Leu Pro
1 5
<210> 2838
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2838
Pro Pro Arg Ser Ser Ser Ala Ile Ala Val
1 5 10
<210> 2839
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2839
Arg Ala Ala Ala Ser Thr Ala Thr Glu Val
1 5 10
<210> 2840
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2840
Ser Pro Pro Arg Ser Ser Ser Ala Ile
1 5
<210> 2841
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2841
Ser Pro Pro Arg Ser Ser Ser Ala Ile Ala
1 5 10
<210> 2842
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2842
Ser Pro Thr Gln Arg Cys Arg Leu Ala
1 5
<210> 2843
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2843
Thr Gln Arg Cys Arg Leu Ala Arg Ala
1 5
<210> 2844
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2844
Thr Gln Arg Cys Arg Leu Ala Arg Ala Ala
1 5 10
<210> 2845
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2845
Lys Ile Trp Lys Thr Thr Gln Met Cys Arg
1 5 10
<210> 2846
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2846
Trp Thr Ser Ser Gly Arg Ser Thr Lys
1 5
<210> 2847
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2847
Ala Leu Gly Glu Leu Ala Arg Ala Leu
1 5
<210> 2848
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2848
Ala Gln Leu Arg Arg Arg Ala Ala Ala
1 5
<210> 2849
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2849
Ala Gln Leu Arg Arg Arg Ala Ala Ala Leu
1 5 10
<210> 2850
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2850
Ala Arg Arg Ala Ala Arg Met Ala Gln Leu
1 5 10
<210> 2851
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2851
His Pro Gln Leu Pro Arg Ser Pro Leu
1 5
<210> 2852
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2852
His Pro Gln Leu Pro Arg Ser Pro Leu Ala
1 5 10
<210> 2853
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2853
Leu Ala Arg Ala Leu Pro Gly His Leu
1 5
<210> 2854
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2854
Leu Ala Arg Ala Leu Pro Gly His Leu Leu
1 5 10
<210> 2855
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2855
Met Ala Gln Leu Arg Arg Arg Ala Ala
1 5
<210> 2856
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2856
Met Ala Gln Leu Arg Arg Arg Ala Ala Ala
1 5 10
<210> 2857
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2857
Gln Leu Arg Arg Arg Ala Ala Ala Leu
1 5
<210> 2858
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2858
Arg Ala Ala Ala Leu Pro Asn Ala Ala Ala
1 5 10
<210> 2859
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2859
Arg Met Ala Gln Leu Arg Arg Arg Ala Ala
1 5 10
<210> 2860
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2860
Ser Gln Ser Ala Arg Arg Ala Ala Arg Met
1 5 10
<210> 2861
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2861
Gly Met Thr Leu Gly Glu Lys Phe Arg Val
1 5 10
<210> 2862
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2862
Arg Val Gly Asn Cys Lys His Leu Lys
1 5
<210> 2863
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2863
Gly Pro Ser Glu Pro Gly Asn Asn Ile
1 5
<210> 2864
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2864
Lys Ile Cys Asn Glu Ser Ala Ser Arg Lys
1 5 10
<210> 2865
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2865
Gly Ile Gln Val Leu Asn Val Ser Leu Lys
1 5 10
<210> 2866
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2866
Ile Gln Val Leu Asn Val Ser Leu Lys
1 5
<210> 2867
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2867
Lys Ser Ser Ser Asn Val Ile Ser Tyr
1 5
<210> 2868
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2868
Lys Tyr Gly Trp Ser Leu Leu Arg Val
1 5
<210> 2869
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2869
Arg Ser Trp Lys Tyr Gly Trp Ser Leu
1 5
<210> 2870
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2870
Ser Leu Lys Ser Ser Ser Asn Val Ile
1 5
<210> 2871
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2871
Ser Trp Lys Tyr Gly Trp Ser Leu Leu
1 5
<210> 2872
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2872
Thr Val Ala Asn Gly Arg Ser Trp Lys
1 5
<210> 2873
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2873
Val Pro Gln Val Asn Gly Ile Gln Val
1 5
<210> 2874
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2874
Val Pro Gln Val Asn Gly Ile Gln Val Leu
1 5 10
<210> 2875
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2875
Val Thr Val Ala Asn Gly Arg Ser Trp Lys
1 5 10
<210> 2876
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2876
Trp Ser Leu Leu Arg Val Pro Gln Val
1 5
<210> 2877
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2877
His Pro Gly Asp Cys Leu Ile Phe Lys Leu
1 5 10
<210> 2878
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2878
Lys Leu Arg Val Pro Gly Ser Ser Val
1 5
<210> 2879
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2879
Lys Leu Arg Val Pro Gly Ser Ser Val Leu
1 5 10
<210> 2880
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2880
Arg Val Pro Gly Ser Ser Val Leu Val
1 5
<210> 2881
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2881
Ser Val Leu Val Thr Val Pro Gly Leu
1 5
<210> 2882
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2882
Val Pro Gly Ser Ser Val Leu Val Thr Val
1 5 10
<210> 2883
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2883
Ala Leu Leu Leu Arg Pro Arg Pro Pro Arg
1 5 10
<210> 2884
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2884
Ala Leu Ser Ala Leu Leu Leu Arg Pro Arg
1 5 10
<210> 2885
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2885
Leu Thr Ile Asn Lys Glu Glu Ala Leu
1 5
<210> 2886
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2886
Ile Val His Ser Ala Thr Gly Phe Lys
1 5
<210> 2887
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2887
Ala Thr Gly Phe Lys Gln Ser Ser Lys
1 5
<210> 2888
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2888
Glu Leu Phe Pro Leu Ile Phe Pro Ala
1 5
<210> 2889
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2889
Lys Gly Pro Glu Leu Phe Pro Leu Ile
1 5
<210> 2890
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2890
Lys Gly Pro Glu Leu Phe Pro Leu Ile Phe
1 5 10
<210> 2891
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2891
Lys Pro Thr Asp Ala Pro Pro Lys Ala Gly Val
1 5 10
<210> 2892
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2892
Gln Val Tyr Arg Arg Lys His Gln Glu Leu
1 5 10
<210> 2893
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2893
Ser Thr Arg Glu Lys Asn Ser Gln Val
1 5
<210> 2894
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2894
Val Tyr Arg Arg Lys His Gln Glu Leu
1 5
<210> 2895
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2895
Val Leu Thr Val Thr Ser Thr Asp Val
1 5
<210> 2896
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2896
Val Leu Thr Val Thr Ser Thr Asp Val Lys
1 5 10
<210> 2897
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2897
Ile Met Ser Leu Trp Gly Leu Val Ser
1 5
<210> 2898
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2898
Ile Met Ser Leu Trp Gly Leu Val Ser Lys
1 5 10
<210> 2899
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2899
Lys Leu Lys Gln Glu Ala Thr Ser Lys
1 5
<210> 2900
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2900
Gln Ile Met Ser Leu Trp Gly Leu Val
1 5
<210> 2901
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2901
Ser Gln Ile Met Ser Leu Trp Gly Leu
1 5
<210> 2902
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2902
Ser Gln Ile Met Ser Leu Trp Gly Leu Val
1 5 10
<210> 2903
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2903
Thr Ser Lys Ser Gln Ile Met Ser Leu
1 5
<210> 2904
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2904
Leu Leu Gln Glu Phe Asp Val Gln Glu Ala
1 5 10
<210> 2905
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2905
Leu Gln Glu Phe Asp Val Gln Glu Ala Leu
1 5 10
<210> 2906
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2906
Gly Pro Arg Glu Pro Arg Asn Arg Thr
1 5
<210> 2907
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2907
Arg Asn Arg Thr Glu Lys His Ser Thr Met
1 5 10
<210> 2908
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2908
Ala Leu Asn Ser Glu Ala Leu Ser Val
1 5
<210> 2909
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2909
Ala Leu Asn Ser Glu Ala Leu Ser Val Val
1 5 10
<210> 2910
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2910
Met Ala Leu Asn Ser Glu Ala Leu Ser Val
1 5 10
<210> 2911
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2911
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 2912
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2912
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 2913
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2913
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 2914
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2914
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 2915
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2915
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 2916
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2916
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 2917
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2917
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 2918
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2918
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 2919
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2919
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 2920
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2920
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 2921
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2921
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 2922
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2922
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 2923
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2923
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 2924
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2924
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 2925
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2925
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 2926
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2926
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 2927
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2927
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 2928
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2928
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 2929
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2929
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 2930
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 2930
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 2931
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2931
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 2932
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2932
Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 2933
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2933
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 2934
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2934
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 2935
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2935
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 2936
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2936
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 2937
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 2937
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 2938
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2938
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 2939
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2939
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 2940
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2940
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 2941
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2941
Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile
1 5 10 15
Asp Gly Pro Arg Cys Val Arg Thr Cys Ser Ala Gly Val Met Gly Glu
20 25 30
Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His
35 40 45
Leu Cys His
50
<210> 2942
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2942
Cys Thr Gly Arg Cys Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile
1 5 10 15
Asp Gly Pro His Cys Val Lys Thr Cys Leu Ala Gly Val Met Gly Glu
20 25 30
Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His
35 40 45
Leu Cys His
50
<210> 2943
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2943
Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly
1 5 10 15
Pro His Cys Val Lys Thr Cys Pro Ala Ala Val Met Gly Glu Asn Asn
20 25 30
Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys
35 40 45
His Pro Asn
50
<210> 2944
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2944
Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly
1 5 10 15
Pro His Cys Val Lys Thr Cys Pro Ala Val Val Met Gly Glu Asn Asn
20 25 30
Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys
35 40 45
His Pro Asn
50
<210> 2945
<211> 50
<212> БЕЛОК
<213> Homo sapiens
<400> 2945
Lys Leu Thr Gln Leu Gly Thr Phe Glu Asp His Phe Leu Ser Leu Gln
1 5 10 15
Arg Met Phe Asn Asn Cys Leu Val Val Arg Gly Asn Leu Glu Ile Thr
20 25 30
Tyr Val Gln Arg Asn Tyr Asp Leu Ser Phe Leu Lys Thr Gln Glu Val
35 40 45
Ala Gly
50
<210> 2946
<211> 50
<212> БЕЛОК
<213> Homo sapiens
<400> 2946
Gln Glu Arg Glu Leu Val Glu Pro Leu Thr Pro Ser Gly Glu Ala Pro
1 5 10 15
Asn Gln Ala Leu Leu Arg Ile Leu Lys Lys Thr Glu Phe Lys Lys Ile
20 25 30
Lys Val Leu Gly Ser Gly Ala Phe Gly Thr Val Tyr Lys Gly Leu Trp
35 40 45
Ile Pro
50
<210> 2947
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2947
Pro Ser Gly Glu Ala Pro Asn Gln Ala Leu Leu Arg Ile Leu Lys Glu
1 5 10 15
Thr Glu Phe Lys Lys Ile Lys Val Leu Ala Ser Gly Ala Phe Gly Thr
20 25 30
Val Tyr Lys Gly Leu Trp Ile Pro Glu Gly Glu Lys Val Lys Ile Pro
35 40 45
Val Ala Ile
50
<210> 2948
<211> 65
<212> БЕЛОК
<213> Homo sapiens
<400> 2948
Gly Ala Phe Gly Thr Val Tyr Lys Gly Leu Trp Ile Pro Glu Gly Glu
1 5 10 15
Lys Val Lys Ile Pro Val Ala Ile Lys Thr Ser Pro Lys Ala Asn Lys
20 25 30
Glu Ile Leu Asp Glu Ala Tyr Val Met Ala Ser Val Asp Asn Pro His
35 40 45
Val Cys Arg Leu Leu Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Ile
50 55 60
Thr
65
<210> 2949
<211> 52
<212> БЕЛОК
<213> Homo sapiens
<400> 2949
Ala Ile Lys Glu Leu Arg Glu Gln Ala Thr Ser Pro Lys Ala Asn Lys
1 5 10 15
Glu Ile Leu Asp Glu Ala Tyr Val Met Ala Ile Val Asp Asn Pro His
20 25 30
Val Cys Arg Leu Leu Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Ile
35 40 45
Thr Gln Leu Met
50
<210> 2950
<211> 52
<212> БЕЛОК
<213> Homo sapiens
<400> 2950
Tyr Leu Leu Asn Val Val Cys Val Gln Leu Ala Lys Gly Met Asn Tyr
1 5 10 15
Leu Glu Asp Arg Arg Leu Val His Arg Asp Met Ala Ala Arg Asn Val
20 25 30
Leu Val Lys Thr Pro Gln His Val Lys Ile Thr Asp Phe Gly Leu Ala
35 40 45
Lys Leu Leu Gly
50
<210> 2951
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2951
Leu Val His Arg Asp Leu Ala Ala Arg Asn Val Leu Val Lys Thr Pro
1 5 10 15
Gln His Ile Val Lys Ile Thr Asp Glu Gly Arg Ala Lys Leu Gly Ala
20 25 30
Glu Glu Lys Glu Tyr His Ala Phe Gly Gly Arg Val Pro Ile Lys Trp
35 40 45
Met Ala Leu
50
<210> 2952
<211> 50
<212> БЕЛОК
<213> Homo sapiens
<400> 2952
Arg Asp Leu Ala Ala Arg Asn Val Leu Val Lys Thr Pro Gln His Val
1 5 10 15
Arg Ile Thr Asp Phe Gly Leu Ala Lys Gln Leu Gly Ala Glu Glu Lys
20 25 30
Glu Tyr His Ala Glu Gly Gly Lys Val Pro Ile Lys Trp Met Ala Leu
35 40 45
Glu Ser
50
<210> 2953
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2953
Gln Glu Val Ala Gly Tyr Val Leu Ile Ala Leu Asn Thr Val Glu Arg
1 5 10 15
Ile Pro Leu Glu Asn Leu Gln Ala Ile Glu Lys Gly Asn Met Tyr Tyr
20 25 30
Glu Asn Ser Tyr Ala Leu Val Leu Ser Asn Tyr Asp Ala Asn Lys Thr
35 40 45
Gly Leu Lys
50
<210> 2954
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2954
Ser Pro Ser Asp Glu Cys Leu Met Asn Gln Cys Ala Ala Gly Glu Ile
1 5 10 15
Gly Pro Asn Glu Ser Asp Leu Val Cys Cys Lys Phe Arg Asp Glu Ala
20 25 30
Thr Cys Lys Asp Thr Cys Pro Pro Leu Met Leu Tyr Asn Pro Thr Thr
35 40 45
Tyr Gln Met
50
<210> 2955
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2955
Cys Pro Pro Leu Met Leu Tyr Asn Pro Thr Thr Tyr Gln Met Asp Val
1 5 10 15
Asn Pro Glu Gly Lys Tyr Ser Phe Gly Thr Thr Cys Val Lys Lys Cys
20 25 30
Pro Arg Asn Tyr Val Val Thr Asp His Gly Ser Cys Val Arg Ala Cys
35 40 45
Gly Ala Asp
50
<210> 2956
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2956
Cys Pro Pro Leu Met Leu Tyr Asn Pro Thr Thr Tyr Gln Met Asp Val
1 5 10 15
Asn Pro Glu Gly Lys Tyr Ser Phe Gly Asp Thr Cys Val Lys Lys Cys
20 25 30
Pro Arg Asn Tyr Val Val Thr Asp His Gly Ser Cys Val Arg Ala Cys
35 40 45
Gly Ala Asp
50
<210> 2957
<211> 51
<212> БЕЛОК
<213> Homo sapiens
<400> 2957
Cys Pro Pro Leu Met Leu Tyr Asn Pro Thr Thr Tyr Gln Met Asp Val
1 5 10 15
Asn Pro Glu Gly Lys Tyr Ser Phe Gly Val Thr Cys Val Lys Lys Cys
20 25 30
Pro Arg Asn Tyr Val Val Thr Asp His Gly Ser Cys Val Arg Ala Cys
35 40 45
Gly Ala Asp
50
<210> 2958
<211> 52
<212> БЕЛОК
<213> Homo sapiens
<400> 2958
Val Asn Pro Glu Gly Lys Tyr Ser Phe Gly Ala Thr Cys Val Lys Lys
1 5 10 15
Ile Cys Pro Arg Asn Tyr Val Val Thr Asp Tyr Gly Ser Cys Val Arg
20 25 30
Ala Cys Gly Ala Asp Ser Tyr Glu Met Glu Glu Asp Gly Val Arg Lys
35 40 45
Cys Lys Lys Cys
50
<210> 2959
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2959
Cys Val Lys Thr Cys Ser Ala Gly Val
1 5
<210> 2960
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2960
Val Lys Thr Cys Ser Ala Gly Val Met
1 5
<210> 2961
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2961
Cys Val Lys Thr Cys Ser Ala Gly Val Met
1 5 10
<210> 2962
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2962
Cys Val Lys Thr Cys Leu Ala Gly Val
1 5
<210> 2963
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2963
Gly Pro His Cys Val Lys Thr Cys Leu
1 5
<210> 2964
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2964
Val Lys Thr Cys Leu Ala Gly Val Met
1 5
<210> 2965
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2965
Cys Val Lys Thr Cys Pro Ala Ala Val
1 5
<210> 2966
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2966
Val Lys Thr Cys Pro Ala Ala Val Met
1 5
<210> 2967
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2967
Ala Val Met Gly Glu Asn Asn Thr Leu
1 5
<210> 2968
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2968
Ala Val Met Gly Glu Asn Asn Thr Leu Val
1 5 10
<210> 2969
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2969
Cys Val Lys Thr Cys Pro Ala Ala Val Met
1 5 10
<210> 2970
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2970
Ala Ala Val Met Gly Glu Asn Asn Thr Leu
1 5 10
<210> 2971
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2971
Cys Val Lys Cys Pro Ala Val Val
1 5
<210> 2972
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2972
Val Lys Thr Cys Pro Ala Val Val Met
1 5
<210> 2973
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2973
Val Val Met Gly Glu Asn Asn Thr Leu Val
1 5 10
<210> 2974
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2974
Cys Val Lys Thr Cys Pro Ala Val Val Met
1 5 10
<210> 2975
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2975
Met Phe Asn Asn Cys Glu Val Val Arg
1 5
<210> 2976
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2976
Glu Val Val Arg Gly Asn Leu Glu Ile
1 5
<210> 2977
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2977
Val Arg Gly Asn Leu Glu Thr Thr Tyr
1 5
<210> 2978
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2978
Arg Met Phe Asn Asn Cys Glu Val Val Arg
1 5 10
<210> 2979
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2979
Val Val Arg Gly Asn Leu Glu Ile Thr Tyr
1 5 10
<210> 2980
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2980
Cys Glu Val Val Arg Gly Asn Ile Glu
1 5
<210> 2981
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2981
Arg Ile Leu Lys Lys Thr Glu Phe Lys
1 5
<210> 2982
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2982
Ile Leu Lys Lys Thr Glu Phe Lys Lys
1 5
<210> 2983
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2983
Gln Ala Leu Leu Arg Ile Leu Lys Lys
1 5
<210> 2984
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2984
Leu Arg Ile Leu Lys Thr Glu Phe
1 5
<210> 2985
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2985
Arg Ile Leu Lys Lys Thr Glu Phe Lys Lys
1 5 10
<210> 2986
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2986
Asn Gln Ala Leu Leu Arg Ile Leu Lys Lys
1 5 10
<210> 2987
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2987
Leu Leu Arg Leu Lys Lys Thr Glu Phe
1 5
<210> 2988
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2988
Ala Ser Gly Ala Phe Gly Thr Val Tyr
1 5
<210> 2989
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2989
Val Leu Ala Ser Gly Ala Phe Gly Thr
1 5
<210> 2990
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 2990
Leu Ala Ser Ala Phe Gly Thr Tyr
1 5
<210> 2991
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2991
Lys Ile Lys Val Leu Ala Ser Gly Ala
1 5
<210> 2992
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2992
Lys Val Leu Ala Ser Gly Ala Phe Gly
1 5
<210> 2993
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2993
Ile Lys Val Leu Ala Ser Gly Ala Phe
1 5
<210> 2994
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 2994
Lys Lys Ile Lys Val Leu Ala Ser Gly
1 5
<210> 2995
<211> 5
<212> БЕЛОК
<213> Homo sapiens
<400> 2995
Val Leu Ala Ser Gly
1 5
<210> 2996
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2996
Val Leu Ala Ser Gly Ala Phe Gly Thr Val
1 5 10
<210> 2997
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2997
Ala Ser Gly Ala Phe Gly Thr Val Tyr Lys
1 5 10
<210> 2998
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2998
Lys Ile Lys Val Leu Ala Ser Gly Ala Phe
1 5 10
<210> 2999
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 2999
Leu Ala Ser Gly Ala Phe Gly Thr Val Tyr
1 5 10
<210> 3000
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3000
Lys Lys Ile Lys Val Leu Ala Ser Gly Ala
1 5 10
<210> 3001
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3001
Thr Glu Phe Lys Lys Ile Lys Val Ile Ala
1 5 10
<210> 3002
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3002
Ala Ile Lys Thr Ser Pro Lys Ala Asn Lys
1 5 10
<210> 3003
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3003
Lys Val Lys Ile Pro Val Ala Ile Lys Thr
1 5 10
<210> 3004
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3004
Lys Thr Ser Pro Lys Ala Asn Lys Glu Ile
1 5 10
<210> 3005
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3005
Met Ala Ile Val Asp Asn Pro His Val
1 5
<210> 3006
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3006
Val Met Ala Ile Val Asp Asn Pro His
1 5
<210> 3007
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3007
Asp Glu Ala Tyr Val Met Ala Ile Val
1 5
<210> 3008
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3008
Leu Asp Glu Ala Tyr Tyr Met Ala Ile
1 5
<210> 3009
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3009
Arg Asp Glu Ala Tyr Val Met Ala Ile
1 5
<210> 3010
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3010
Val Met Ala Ile Val Asp Asn Pro His Val
1 5 10
<210> 3011
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3011
Ala Ile Val Asp Asn Pro His Val Cys Arg
1 5 10
<210> 3012
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3012
Tyr Val Met Ala Ile Val Asp Asn Pro His
1 5 10
<210> 3013
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3013
Asp Glu Ala Tyr Val Met Ala Ile Val Asp
1 5 10
<210> 3014
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3014
Arg Leu Val His Arg Asp Met Ala Ala
1 5
<210> 3015
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3015
Asp Met Ala Ala Arg Asn Val Leu Val
1 5
<210> 3016
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3016
Met Ala Ala Arg Asn Val Leu Val Lys
1 5
<210> 3017
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3017
Leu Val His Arg Asp Met Ala Arg Arg
1 5
<210> 3018
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3018
Arg Asp Met Ala Ala Arg Asn Val Leu
1 5
<210> 3019
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3019
Arg Leu Val His Arg Asp Met Ala Ala Arg
1 5 10
<210> 3020
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3020
Asp Met Ala Ala Arg Asn Val Leu Val Lys
1 5 10
<210> 3021
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3021
His Arg Asp Met Ala Ala Arg Asn Val Leu
1 5 10
<210> 3022
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3022
Arg Asp Met Ala Ala Arg Asn Val Leu Val
1 5 10
<210> 3023
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3023
Lys Ile Thr Asp Gly Arg Ala Lys
1 5
<210> 3024
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3024
His Val Lys Ile Thr Asp Phe Gly Arg
1 5
<210> 3025
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3025
Phe Gly Arg Ala Lys Leu Leu Gly Ala
1 5
<210> 3026
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3026
His Val Lys Ile Thr Asp Phe Gly Arg Ala
1 5 10
<210> 3027
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3027
Arg Ala Lys Leu Ile Gly Ala Glu Glu Lys
1 5 10
<210> 3028
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3028
Leu Ala Lys Gln Leu Gly Ala Glu Glu Lys
1 5 10
<210> 3029
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3029
Lys Gln Leu Gly Ala Glu Glu Lys Glu Tyr
1 5 10
<210> 3030
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3030
Gln His Lys Gly Asn Met Tyr Tyr
1 5
<210> 3031
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3031
Leu Gln His Lys Gly Asn Met Tyr
1 5
<210> 3032
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3032
Leu Gln His Lys Gly Asn Met Tyr Tyr
1 5
<210> 3033
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3033
Lys Gly Asn Met Tyr Tyr Glu Asn Ser Tyr
1 5 10
<210> 3034
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3034
Arg Glu Ser Asp Cys Leu Val Cys Cys
1 5
<210> 3035
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3035
Tyr Ser Phe Gly Thr Thr Cys Val Lys
1 5
<210> 3036
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3036
Thr Thr Cys Val Lys Lys Cys Pro Arg
1 5
<210> 3037
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3037
Gly Lys Tyr Ser Phe Gly Thr Thr Cys
1 5
<210> 3038
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3038
Tyr Ser Phe Gly Thr Thr Cys Val Lys Lys
1 5 10
<210> 3039
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3039
Lys Tyr Ser Phe Gly Thr Thr Cys Val Lys
1 5 10
<210> 3040
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3040
Gly Thr Thr Cys Val Lys Lys Cys Pro Arg
1 5 10
<210> 3041
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3041
Gly Lys Tyr Ser Phe Gly Thr Thr Cys Val
1 5 10
<210> 3042
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3042
Tyr Ser Phe Gly Asp Thr Cys Val Lys
1 5
<210> 3043
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3043
Asp Thr Cys Val Lys Lys Cys Pro Arg
1 5
<210> 3044
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3044
Gly Lys Tyr Ser Phe Gly Asp Thr Cys
1 5
<210> 3045
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3045
Tyr Ser Phe Gly Asp Thr Cys Val Lys Lys
1 5 10
<210> 3046
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3046
Lys Tyr Ser Phe Gly Thr Cys Val Lys
1 5
<210> 3047
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3047
Gly Lys Tyr Ser Phe Gly Asp Thr Cys Val
1 5 10
<210> 3048
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3048
Tyr Ser Phe Gly Val Thr Cys Val Lys
1 5
<210> 3049
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3049
Lys Tyr Ser Phe Gly Val Thr Cys Val
1 5
<210> 3050
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3050
Val Thr Cys Val Lys Lys Cys Pro Arg
1 5
<210> 3051
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3051
Gly Lys Tyr Ser Phe Gly Val Thr Cys
1 5
<210> 3052
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3052
Tyr Ser Phe Gly Val Thr Cys Val Lys Lys
1 5 10
<210> 3053
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3053
Lys Tyr Ser Phe Gly Val Thr Cys Val Lys
1 5 10
<210> 3054
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3054
Gly Val Thr Cys Val Lys Lys Cys Pro Arg
1 5 10
<210> 3055
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3055
Gly Lys Tyr Ser Phe Gly Val Thr Cys Val
1 5 10
<210> 3056
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3056
Val Val Thr Asp Tyr Gly Ser Cys Val
1 5
<210> 3057
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3057
Tyr Val Val Thr Asp Tyr Gly Ser Cys Val
1 5 10
<210> 3058
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3058
Val Val Thr Asp Tyr Gly Ser Cys Val Arg
1 5 10
<210> 3059
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3059
Cys Pro Arg Asn Tyr Val Val Thr Asp Tyr
1 5 10
<210> 3060
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3060
Phe Gly Arg Ala Lys Leu Leu Gly Ala
1 5
<210> 3061
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3061
Lys Ile Thr Asp Phe Gly Arg Ala Lys
1 5
<210> 3062
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 3062
Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Ile Met Gln Leu Met Pro
1 5 10 15
Phe Gly Cys Leu Leu Asp Tyr
20
<210> 3063
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 3063
Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser
1 5 10 15
Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn
20 25 30
Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys
35 40 45
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val
50 55 60
Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg
65 70 75 80
Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp
85 90 95
Lys Cys Asn Leu Leu
100
<210> 3064
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3064
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3065
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3065
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 3066
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3066
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3067
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3067
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3068
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3068
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3069
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3069
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3070
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3070
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3071
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3071
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3072
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3072
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3073
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3073
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3074
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3074
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3075
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3075
Cys Leu Thr Ser Thr Val Gln Leu Ile Met
1 5 10
<210> 3076
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3076
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3077
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3077
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3078
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3078
Leu Ile Met Gln Leu Met Pro Phe Gly
1 5
<210> 3079
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3079
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 3080
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3080
Gln Leu Ile Met Gln Leu Met Pro Phe Gly
1 5 10
<210> 3081
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3081
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys
1 5 10
<210> 3082
<211> 80
<212> БЕЛОК
<213> Homo sapiens
<400> 3082
Met Arg Pro Ser Gly Thr Ala Gly Ala Ala Leu Leu Ala Leu Leu Ala
1 5 10 15
Ala Leu Cys Pro Ala Ser Arg Ala Leu Glu Glu Lys Lys Gly Asn Tyr
20 25 30
Val Val Thr Asp His Gly Ser Cys Val Arg Ala Cys Gly Ala Asp Ser
35 40 45
Tyr Glu Met Glu Glu Asp Gly Val Arg Lys Cys Lys Lys Cys Glu Gly
50 55 60
Pro Cys Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp
65 70 75 80
<210> 3083
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3083
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3084
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3084
Ala Leu Glu Glu Lys Lys Gly Asn Tyr Val
1 5 10
<210> 3085
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3085
Ile Gln Leu Gln Asp Lys Phe Glu His Leu
1 5 10
<210> 3086
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3086
Gln Leu Gln Asp Lys Phe Glu His Leu
1 5
<210> 3087
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3087
Gln Leu Gln Asp Lys Phe Glu His Leu Lys
1 5 10
<210> 3088
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3088
Tyr Leu Val Ile Gln Leu Gln Asp Lys Phe
1 5 10
<210> 3089
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 3089
Met Ile Lys Glu Gly Ser Met Ser Glu Asp Glu Phe Ile Glu Glu Ala
1 5 10 15
Lys Val Met Met Asn Leu Ser His Glu Lys Leu Val Gln Leu Tyr Gly
20 25 30
Val Cys Thr Lys Gln Arg Pro Ile Phe Ile Ile Thr Glu Tyr Met Ala
35 40 45
Asn Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg His Arg Phe Gln
50 55 60
Thr Gln Gln Leu Leu Glu Met Cys Lys Asp Val Cys Glu Ala Met Glu
65 70 75 80
Tyr Leu Glu Ser Lys Gln Phe Leu His Arg Asp Leu Ala Ala Arg Asn
85 90 95
Cys Leu Val Asn Asp
100
<210> 3090
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3090
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3091
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3091
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3092
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3092
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 3093
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3093
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3094
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3094
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 3095
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3095
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3096
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3096
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3097
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3097
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 3098
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3098
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 3099
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3099
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 3100
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3100
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3101
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3101
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3102
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3102
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 3103
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3103
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3104
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3104
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3105
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3105
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 3106
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3106
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3107
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 3107
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3108
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3108
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3109
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 3109
Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Ile Met Gln Leu Met Pro
1 5 10 15
Phe Gly Cys Leu Leu Asp Tyr
20
<210> 3110
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3110
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3111
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3111
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 3112
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3112
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3113
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3113
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3114
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3114
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3115
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3115
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3116
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3116
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3117
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3117
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3118
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3118
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3119
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3119
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3120
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3120
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3121
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3121
Cys Leu Thr Ser Thr Val Gln Leu Ile Met
1 5 10
<210> 3122
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3122
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3123
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3123
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3124
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3124
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3125
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3125
Leu Ile Met Gln Leu Met Pro Phe Gly
1 5
<210> 3126
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3126
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 3127
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3127
Gln Leu Ile Met Gln Leu Met Pro Phe Gly
1 5 10
<210> 3128
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 3128
Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser
1 5 10 15
Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn
20 25 30
Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys
35 40 45
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val
50 55 60
Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg
65 70 75 80
Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp
85 90 95
Lys Cys Asn Leu Leu
100
<210> 3129
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3129
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys
1 5 10
<210> 3130
<211> 80
<212> БЕЛОК
<213> Homo sapiens
<400> 3130
Met Arg Pro Ser Gly Thr Ala Gly Ala Ala Leu Leu Ala Leu Leu Ala
1 5 10 15
Ala Leu Cys Pro Ala Ser Arg Ala Leu Glu Glu Lys Lys Gly Asn Tyr
20 25 30
Val Val Thr Asp His Gly Ser Cys Val Arg Ala Cys Gly Ala Asp Ser
35 40 45
Tyr Glu Met Glu Glu Asp Gly Val Arg Lys Cys Lys Lys Cys Glu Gly
50 55 60
Pro Cys Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp
65 70 75 80
<210> 3131
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3131
Ala Leu Glu Glu Lys Lys Gly Asn Tyr Val
1 5 10
<210> 3132
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3132
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3133
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3133
Ile Gln Leu Gln Asp Lys Phe Glu His Leu
1 5 10
<210> 3134
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3134
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3135
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3135
Gln Leu Gln Asp Lys Phe Glu His Leu
1 5
<210> 3136
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3136
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3137
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3137
Gln Leu Gln Asp Lys Phe Glu His Leu Lys
1 5 10
<210> 3138
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3138
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3139
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3139
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3140
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3140
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3141
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3141
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3142
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3142
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3143
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3143
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3144
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3144
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3145
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3145
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3146
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3146
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3147
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3147
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3148
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3148
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3149
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3149
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3150
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3150
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3151
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3151
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3152
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3152
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3153
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 3153
Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser
1 5 10 15
Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn
20 25 30
Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys
35 40 45
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val
50 55 60
Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg
65 70 75 80
Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp
85 90 95
Lys Cys Asn Leu Leu
100
<210> 3154
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3154
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys
1 5 10
<210> 3155
<211> 101
<212> БЕЛОК
<213> Homo sapiens
<400> 3155
Ile Pro Val Ala Ile Lys Glu Leu Arg Glu Ala Thr Ser Pro Lys Ala
1 5 10 15
Asn Lys Glu Ile Leu Asp Glu Ala Tyr Val Met Ala Ser Val Asp Asn
20 25 30
Pro His Val Cys Arg Leu Leu Gly Ile Cys Leu Thr Ser Thr Val Gln
35 40 45
Leu Ile Met Gln Leu Met Pro Phe Gly Cys Leu Leu Asp Tyr Val Arg
50 55 60
Glu His Lys Asp Asn Ile Gly Ser Gln Tyr Leu Leu Asn Trp Cys Val
65 70 75 80
Gln Ile Ala Lys Gly Met Asn Tyr Leu Glu Asp Arg Arg Leu Val His
85 90 95
Arg Asp Leu Ala Ala
100
<210> 3156
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3156
Cys Leu Thr Ser Thr Val Gln Leu Ile Met
1 5 10
<210> 3157
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3157
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3158
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3158
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3159
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3159
Leu Ile Met Gln Leu Met Pro Phe Gly
1 5
<210> 3160
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3160
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 3161
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3161
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3162
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3162
Met Gln Leu Met Pro Phe Gly Cys Leu
1 5
<210> 3163
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3163
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3164
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3164
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3165
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3165
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3166
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3166
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3167
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3167
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3168
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3168
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3169
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3169
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 3170
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3170
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3171
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3171
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3172
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3172
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3173
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3173
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3174
<211> 80
<212> БЕЛОК
<213> Homo sapiens
<400> 3174
Met Arg Pro Ser Gly Thr Ala Gly Ala Ala Leu Leu Ala Leu Leu Ala
1 5 10 15
Ala Leu Cys Pro Ala Ser Arg Ala Leu Glu Glu Lys Lys Gly Asn Tyr
20 25 30
Val Val Thr Asp His Gly Ser Cys Val Arg Ala Cys Gly Ala Asp Ser
35 40 45
Tyr Glu Met Glu Glu Asp Gly Val Arg Lys Cys Lys Lys Cys Glu Gly
50 55 60
Pro Cys Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp
65 70 75 80
<210> 3175
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3175
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3176
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3176
Ala Leu Glu Glu Lys Lys Gly Asn Tyr Val
1 5 10
<210> 3177
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3177
Ile Gln Leu Gln Asp Lys Phe Glu His Leu
1 5 10
<210> 3178
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3178
Gln Leu Gln Asp Lys Phe Glu His Leu
1 5
<210> 3179
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3179
Gln Leu Gln Asp Lys Phe Glu His Leu Lys
1 5 10
<210> 3180
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3180
Tyr Leu Val Ile Gln Leu Gln Asp Lys Phe
1 5 10
<210> 3181
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3181
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3182
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3182
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 3183
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3183
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3184
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3184
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3185
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3185
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3186
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3186
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3187
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3187
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3188
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3188
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3189
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3189
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3190
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3190
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3191
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3191
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3192
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3192
Cys Leu Thr Ser Thr Val Gln Leu Ile Met
1 5 10
<210> 3193
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3193
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3194
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3194
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3195
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3195
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3196
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3196
Leu Ile Met Gln Leu Met Pro Phe Gly
1 5
<210> 3197
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3197
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 3198
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3198
Gln Leu Ile Met Gln Leu Met Pro Phe Gly
1 5 10
<210> 3199
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3199
Ile Ile Arg Asn Arg Gly Glu Asn Ser Cys Lys
1 5 10
<210> 3200
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3200
Ala Leu Glu Glu Lys Lys Gly Asn Tyr Val
1 5 10
<210> 3201
<211> 100
<212> БЕЛОК
<213> Homo sapiens
<400> 3201
Leu Pro Gln Pro Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val
1 5 10 15
Lys Cys Trp Met Ile Asp Ala Asp Ser Arg Pro Lys Phe Arg Glu Leu
20 25 30
Ile Ile Glu Phe Ser Lys Met Ala Arg Asp Pro Gln Arg Tyr Leu Val
35 40 45
Ile Gln Leu Gln Asp Lys Phe Glu His Leu Lys Met Ile Gln Gln Glu
50 55 60
Glu Ile Arg Lys Leu Glu Glu Glu Lys Lys Gln Leu Glu Gly Glu Ile
65 70 75 80
Ile Asp Phe Tyr Lys Met Lys Ala Ala Ser Glu Ala Leu Gln Thr Gln
85 90 95
Leu Ser Thr Asp
100
<210> 3202
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3202
Ile Gln Leu Gln Asp Lys Phe Glu His Leu
1 5 10
<210> 3203
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3203
Gln Leu Gln Asp Lys Phe Glu His Leu
1 5
<210> 3204
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3204
Gln Leu Gln Asp Lys Phe Glu His Leu Lys
1 5 10
<210> 3205
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3205
Tyr Leu Val Ile Gln Leu Gln Asp Lys Phe
1 5 10
<210> 3206
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
6xHis tag
<400> 3206
His His His His His His
1 5
<210> 3207
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3207
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3208
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3208
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3209
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3209
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3210
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3210
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3211
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
6xHis метка
<400> 3211
His His His His His His
1 5
<210> 3212
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3212
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3213
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3213
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3214
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3214
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3215
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3215
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3216
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3216
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3217
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3217
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3218
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3218
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 3219
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3219
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3220
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3220
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3221
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3221
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3222
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3222
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3223
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3223
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3224
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3224
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 3225
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3225
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3226
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3226
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 3227
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3227
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 3228
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3228
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3229
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3229
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 3230
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3230
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 3231
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3231
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 3232
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3232
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3233
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3233
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3234
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3234
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3235
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3235
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3236
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3236
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3237
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3237
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 3238
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3238
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3239
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3239
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3240
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3240
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3241
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3241
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3242
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3242
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3243
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3243
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3244
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3244
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3245
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3245
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3246
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3246
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3247
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3247
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3248
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3248
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3249
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3249
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3250
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3250
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3251
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3251
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3252
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3252
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3253
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3253
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3254
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3254
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3255
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3255
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3256
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3256
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3257
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3257
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3258
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3258
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3259
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3259
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3260
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3260
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3261
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 3261
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3262
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3262
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3263
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3263
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3264
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3264
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3265
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3265
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3266
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3266
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3267
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3267
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 3268
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3268
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3269
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3269
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 3270
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3270
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg
20
<210> 3271
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3271
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr
20
<210> 3272
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3272
Lys Lys Lys Lys Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr
20
<210> 3273
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3273
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 3274
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3274
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu
20
<210> 3275
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3275
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu
20
<210> 3276
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3276
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser
<210> 3277
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3277
Lys Lys Lys Lys Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser
20
<210> 3278
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3278
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu
<210> 3279
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3279
Lys Lys Lys Lys Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu
20
<210> 3280
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3280
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
<210> 3281
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3281
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
<210> 3282
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3282
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
<210> 3283
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3283
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
<210> 3284
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3284
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3285
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3285
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
Ser Asn His
<210> 3286
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3286
Lys Lys Lys Lys Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser Asn His
20
<210> 3287
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3287
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10 15
His
<210> 3288
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3288
Lys Lys Lys Lys Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys Ser Asn His
20
<210> 3289
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3289
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 3290
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3290
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 3291
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3291
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3292
<211> 33
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3292
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3293
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3293
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 3294
<211> 39
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3294
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu Trp Cys Leu
35
<210> 3295
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3295
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 3296
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3296
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3297
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3297
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3298
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3298
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 3299
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3299
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg
20
<210> 3300
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3300
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu
20
<210> 3301
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3301
Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10 15
Ser Asn His
<210> 3302
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3302
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr
20
<210> 3303
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3303
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu
20
<210> 3304
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3304
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser
<210> 3305
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3305
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu
<210> 3306
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3306
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10 15
His
<210> 3307
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3307
Lys Lys Lys Lys Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr
20
<210> 3308
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3308
Lys Lys Lys Lys Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser
20
<210> 3309
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3309
Lys Lys Lys Lys Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu
20
<210> 3310
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3310
Lys Lys Lys Lys Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys Ser Asn His
20
<210> 3311
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3311
Lys Lys Lys Lys Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser Asn His
20
<210> 3312
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3312
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 3313
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3313
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
<210> 3314
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3314
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
<210> 3315
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3315
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
<210> 3316
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3316
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
<210> 3317
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3317
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3318
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3318
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 3319
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3319
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 3320
<211> 33
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3320
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3321
<211> 29
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3321
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
20 25
<210> 3322
<211> 39
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3322
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
20 25 30
Arg Ser Ser Leu Trp Cys Leu
35
<210> 3323
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3323
Lys Lys Lys Lys Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala
1 5 10 15
Glu Ser Lys Ile Met Phe Ala Thr
20
<210> 3324
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3324
Lys Lys Lys Lys Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10 15
Ala Thr Leu Gln Arg Ser Ser
20
<210> 3325
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3325
Lys Lys Lys Lys Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser Leu Trp Cys Leu
20
<210> 3326
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3326
Lys Lys Lys Lys Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
Leu Cys Ser Asn His
20
<210> 3327
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3327
Lys Lys Lys Lys Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser Asn His
20
<210> 3328
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3328
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 3329
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3329
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3330
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3330
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3331
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3331
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 3332
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3332
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5 10 15
<210> 3333
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3333
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3334
<211> 33
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3334
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3335
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3335
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 3336
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3336
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 3337
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3337
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3338
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3338
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 3339
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3339
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr
20
<210> 3340
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3340
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln
1 5 10 15
Arg Ser Ser
<210> 3341
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3341
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu
<210> 3342
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3342
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
1 5 10 15
His
<210> 3343
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3343
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg
20
<210> 3344
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3344
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 3345
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3345
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
Ser Leu Trp Cys Leu
20
<210> 3346
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3346
Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr
1 5 10 15
<210> 3347
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3347
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
1 5 10 15
<210> 3348
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3348
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys
1 5 10 15
<210> 3349
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3349
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys
1 5 10
<210> 3350
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3350
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
1 5 10
<210> 3351
<211> 33
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3351
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3352
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3352
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3353
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3353
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3354
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 3354
His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
1 5 10 15
<210> 3355
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3355
Arg Asp Gly Tyr Met Phe Leu Lys
1 5
<210> 3356
<211> 7
<212> БЕЛОК
<213> Homo sapiens
<400> 3356
Ser Ser Ile Met Lys Pro Lys
1 5
<210> 3357
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 3357
Ala Gly Thr Ser Cys Ala Asn Cys Gln Thr Thr Thr Thr Thr Leu Trp
1 5 10 15
Arg
<210> 3358
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3358
Ala Leu Gly Ser His His Thr Ala Ser Pro Trp Asn Leu Ser Pro Phe
1 5 10 15
Ser Lys
<210> 3359
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 3359
Asp Gly Thr Gly His Tyr Leu Cys Asn Ala Cys Gly Leu Tyr His Lys
1 5 10 15
<210> 3360
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3360
Asp Val Ser Pro Asp Pro Ser Leu Ser Thr Pro Gly Ser Ala Gly Ser
1 5 10 15
Ala Arg
<210> 3361
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 3361
Glu Cys Val Asn Cys Gly Ala Thr Ser Thr Pro Leu Trp Arg
1 5 10
<210> 3362
<211> 6
<212> БЕЛОК
<213> Homo sapiens
<400> 3362
Glu Gly Ile Gln Thr Arg
1 5
<210> 3363
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3363
Glu Gly Ile Gln Thr Arg Asn Arg
1 5
<210> 3364
<211> 7
<212> БЕЛОК
<213> Homo sapiens
<400> 3364
Lys Glu Gly Ile Gln Thr Arg
1 5
<210> 3365
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3365
Lys Val His Asp Ser Leu Glu Asp Phe Pro Lys
1 5 10
<210> 3366
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3366
Leu His Asn Ile Asn Arg Pro Leu Thr Met Lys
1 5 10
<210> 3367
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 3367
Leu His Asn Ile Asn Arg Pro Leu Thr Met Lys Lys
1 5 10
<210> 3368
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 3368
Met Asn Gly Gln Asn Arg Pro Leu Ile Lys Pro Lys
1 5 10
<210> 3369
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 3369
Asn Ala Asn Gly Asp Pro Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys
1 5 10 15
<210> 3370
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3370
Asn Ser Ser Phe Asn Pro Ala Ala Leu Ser Arg
1 5 10
<210> 3371
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3371
Arg Ala Gly Thr Ser Cys Ala Asn Cys Gln Thr Thr Thr Thr Thr Leu
1 5 10 15
Trp Arg
<210> 3372
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 3372
Arg Asp Gly Thr Gly His Tyr Leu Cys Asn Ala Cys Gly Leu Tyr His
1 5 10 15
Lys
<210> 3373
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 3373
Ser Ser Thr Glu Gly Arg Glu Cys Val Asn Cys Gly Ala Thr Ser Thr
1 5 10 15
Pro Leu Trp Arg
20
<210> 3374
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3374
Val His Asp Ser Leu Glu Asp Phe Pro Lys
1 5 10
<210> 3375
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3375
Tyr Gln Val Pro Leu Pro Asp Ser Met Lys
1 5 10
<210> 3376
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3376
Arg Ala Lys Phe Lys Gln Leu Leu
1 5
<210> 3377
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3377
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3378
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3378
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3379
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3379
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3380
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3380
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3381
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3381
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3382
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3382
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3383
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3383
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3384
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3384
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3385
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3385
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3386
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3386
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3387
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3387
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3388
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3388
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3389
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3389
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3390
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3390
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3391
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3391
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3392
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3392
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3393
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3393
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3394
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3394
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3395
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3395
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3396
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3396
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3397
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3397
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3398
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3398
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3399
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3399
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3400
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3400
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3401
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3401
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3402
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3402
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3403
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3403
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3404
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3404
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3405
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3405
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3406
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3406
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3407
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3407
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3408
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3408
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3409
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3409
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3410
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3410
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3411
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3411
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3412
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3412
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3413
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3413
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3414
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3414
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3415
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3415
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3416
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3416
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3417
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3417
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3418
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3418
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3419
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3419
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3420
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3420
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3421
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3421
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3422
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3422
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3423
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3423
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3424
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3424
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3425
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3425
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3426
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3426
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3427
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3427
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3428
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3428
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3429
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3429
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3430
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3430
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3431
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3431
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3432
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3432
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3433
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3433
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3434
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3434
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3435
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3435
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3436
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3436
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3437
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3437
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3438
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3438
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3439
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3439
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3440
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3440
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3441
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3441
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3442
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3442
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3443
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3443
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3444
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3444
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3445
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3445
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3446
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3446
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3447
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3447
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3448
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3448
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3449
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3449
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3450
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3450
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3451
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3451
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3452
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3452
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3453
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3453
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3454
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3454
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3455
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3455
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3456
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3456
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3457
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3457
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3458
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3458
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3459
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3459
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3460
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3460
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3461
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3461
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3462
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3462
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3463
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3463
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3464
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3464
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3465
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3465
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3466
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3466
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3467
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3467
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3468
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3468
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3469
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3469
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3470
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3470
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3471
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3471
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3472
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3472
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3473
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3473
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3474
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3474
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3475
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3475
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3476
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3476
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3477
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3477
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3478
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3478
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3479
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3479
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3480
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3480
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3481
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3481
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3482
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3482
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3483
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3483
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3484
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3484
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3485
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3485
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3486
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3486
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3487
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3487
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3488
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3488
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3489
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3489
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3490
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3490
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3491
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3491
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3492
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3492
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3493
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3493
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3494
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3494
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3495
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3495
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3496
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3496
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3497
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3497
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3498
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3498
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3499
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3499
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3500
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3500
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3501
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3501
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3502
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3502
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3503
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3503
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3504
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3504
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3505
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3505
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 3506
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3506
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3507
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3507
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 3508
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3508
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3509
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3509
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 3510
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3510
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 3511
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3511
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3512
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3512
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 3513
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3513
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3514
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3514
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3515
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3515
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3516
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3516
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3517
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3517
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3518
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3518
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3519
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3519
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3520
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3520
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3521
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3521
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3522
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3522
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3523
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3523
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3524
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3524
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3525
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3525
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3526
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3526
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3527
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3527
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3528
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3528
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3529
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3529
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3530
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3530
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3531
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3531
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala
20 25
<210> 3532
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3532
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10 15
Gly His Arg His Gly Leu Glu Pro Cys Ser
20 25
<210> 3533
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3533
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3534
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3534
Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala Asp His Ala
1 5 10 15
His Ala Asp Ala Pro Ala Ile Gln Pro Val
20 25
<210> 3535
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3535
Thr Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser
1 5 10 15
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
20 25
<210> 3536
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3536
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 3537
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3537
Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10 15
Trp Cys Leu Cys Ser Asn His
20
<210> 3538
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3538
His Ala Asp His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu
1 5 10 15
Trp Thr Thr Pro Pro Leu Gln His
20
<210> 3539
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3539
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His Phe Cys Arg
20
<210> 3540
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3540
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser
20
<210> 3541
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3541
Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala Asp His Ala
1 5 10 15
His Ala Asp Ala Pro Ala Ile Gln Pro Val
20 25
<210> 3542
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3542
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10 15
Gly His Arg His Gly Leu Glu Pro Cys Ser
20 25
<210> 3543
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3543
Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg
1 5 10 15
Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3544
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3544
Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly
1 5 10 15
Tyr Met Phe Leu Lys Ala Glu Ser Lys
20 25
<210> 3545
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3545
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser
20
<210> 3546
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3546
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
1 5 10 15
Leu Trp Cys Leu Cys Ser Asn His
20
<210> 3547
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3547
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3548
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3548
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3549
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3549
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3550
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3550
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3551
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3551
Cys Ala Leu Asp Ile Tyr Gly Asn Asn Arg Leu Ala Phe
1 5 10
<210> 3552
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 3552
Cys Ala Ser Ser Leu Asp Phe Val Leu Ala Gly Ser Tyr Ser Tyr Glu
1 5 10 15
Gln Phe Phe
<210> 3553
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3553
Cys Ala Leu Asp Ile Tyr Gly Asn Asn Arg Leu Ala Phe
1 5 10
<210> 3554
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 3554
Cys Ala Ser Ser Leu Asp Phe Val Leu Ala Gly Ser Tyr Ser Tyr Asn
1 5 10 15
Glu Gln Phe Phe
20
<210> 3555
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 3555
Cys Ala Ser Ser Leu Asp Phe Val Leu Ala Gly Ser Tyr Ser Tyr Asn
1 5 10 15
Glu Gln Phe Phe
20
<210> 3556
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3556
Cys Ala Leu Asp Ile Tyr Gly Asn Asn Arg Leu Ala Phe
1 5 10
<210> 3557
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 3557
Cys Ala Glu Lys Val Pro Asn Thr Gly Asn Gln Phe Tyr Phe
1 5 10
<210> 3558
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 3558
Cys Ala Ser Ser Ser Leu Gly Thr Val Arg Thr Glu Ala Phe Phe
1 5 10 15
<210> 3559
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3559
Cys Ala Val Glu Ala Tyr Asn Phe Asn Lys Phe Tyr Phe
1 5 10
<210> 3560
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3560
Cys Ala Ser Arg Ser Glu Asn Thr Ile Tyr Phe
1 5 10
<210> 3561
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3561
Cys Ile Leu Ser Asp Ser Gly Asn Thr Pro Leu Val Phe
1 5 10
<210> 3562
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 3562
Cys Ala Ser Ser Asp Trp Ala Val Ser Gly Asn Thr Ile Tyr Phe
1 5 10 15
<210> 3563
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 3563
Cys Ala Gly Ala Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr
1 5 10 15
Phe
<210> 3564
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 3564
Cys Ala Ser Ser Gln Ala Gln Gly Ala Asn Tyr Gly Tyr Thr Phe
1 5 10 15
<210> 3565
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 3565
Cys Ala Glu Ile Pro Thr Phe Ser Gly Gly Tyr Asn Lys Leu Ile Phe
1 5 10 15
<210> 3566
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3566
Cys Ala Ser Ser Leu Ala Gly Gln Glu Thr Gln Tyr Phe
1 5 10
<210> 3567
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3567
Cys Leu Arg Gly Gly Ser Thr Leu Gly Arg Leu Tyr Phe
1 5 10
<210> 3568
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3568
Cys Ala Ser Ser Leu Tyr Pro Thr Gly Gly Ser Gly Met Asp Glu Gln
1 5 10 15
Tyr Phe
<210> 3569
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 3569
Cys Ala Val Arg Asp Gly Asn Thr Gly Gly Phe Lys Thr Ile Phe
1 5 10 15
<210> 3570
<211> 13
<212> БЕЛОК
<213> Homo sapiens
<400> 3570
Cys Ala Ser Ser Glu Leu Lys Thr Gly Gly Ala Phe Phe
1 5 10
<210> 3571
<211> 453
<212> ДНК
<213> Homo sapiens
<400> 3571
atggcttttt ggctgagaag gctgggtcta catttcaggc cacatttggg gagacgaatg
60
gagtcattcc tgggaggtgt tttgctgatt ttgtggcttc aagtggactg ggtgaagagc
120
caaaagatag aacagaattc cgaggccctg aacattcagg agggtaaaac ggccaccctg
180
acctgcaact atacaaacta ttctccagca tacttacagt ggtaccgaca agatccagga
240
agaggccctg ttttcttgct actcatacgt gaaaatgaga aagaaaaaag gaaagaaaga
300
ctgaaggtca cctttgatac cacccttaaa cagagtttgt ttcatatcac agcctcccag
360
cctgcagact cagctaccta cctctgtgct ctagacattt atgggaacaa cagactcgct
420
tttgggaagg ggaaccaagt ggtggtcata cca
453
<210> 3572
<211> 415
<212> ДНК
<213> Homo sapiens
<400> 3572
atgggaatca ggctcctctg tcgtgtggcc ttttgtttcc tggctgtagg cctcgtagat
60
gtgaaagtaa cccagagctc gagatatcta gtcaaaagga cgggagagaa agtttttctg
120
gaatgtgtcc aggatatgga ccatgaaaat atgttctggt atcgacaaga cccaggtctg
180
gggctacggc tgatctattt ctcatatgat gttaaaatga aagaaaaagg agatattcct
240
gaggggtaca gtgtctctag agagaagaag gagcgcttct ccctgattct ggagtccgcc
300
agcaccaacc agacatctat gtacctctgt gccagcagtt tagattttgt gctagcgggg
360
tcctactcct acaatgagca gttcttcggg ccagggacac ggctcaccgt gctag
415
<210> 3573
<211> 453
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3573
atggccttct ggctgaggag actgggttta cacttcagac cccatttagg cagaagaatg
60
gagagctttt taggcggcgt gctgctgatt ttatggctgc aagttgactg ggtgaagagc
120
cagaagatcg agcagaacag cgaggcttta aacattcaag aaggcaagac agccacttta
180
acttgtaact ataccaacta ctcccccgct tatttacagt ggtacagaca agatcccggc
240
agaggccccg tgtttttact gctgattcgt gagaacgaga aggagaagag gaaggagaga
300
ctgaaggtga ccttcgacac cactttaaag cagtctttat tccacatcac cgccagccag
360
cccgctgata gcgccaccta tttatgcgct ttagacatct acggcaacaa tcgtctggcc
420
ttcggcaagg gcaaccaagt tgtggtgatc ccc
453
<210> 3574
<211> 414
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3574
atgggcattc gtctgctgtg tcgtgtggcc ttctgctttt tagccgtggg tttagtggac
60
gtgaaggtga cccagtcctc tcgttattta gtgaagagga ccggcgagaa ggtgttttta
120
gaatgcgtgc aagatatgga ccacgagaac atgttctggt acagacaaga tcccggactg
180
ggtttaaggc tgatctactt cagctacgac gtgaagatga aggagaaggg cgacatcccc
240
gagggctact ccgtgtctcg tgagaagaag gagaggttct ctttaatttt agagtccgcc
300
agcaccaacc agaccagcat gtatttatgc gccagctctt tagactttgt gctggccggc
360
agctacagct acaacgagca gttcttcggc cccggcacca gactgaccgt gctg
414
<210> 3575
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 3575
Ile Phe Ile Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10 15
Leu Arg Glu Met Arg His Arg
20
<210> 3576
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3576
Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3577
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3577
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3578
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3578
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3579
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3579
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3580
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3580
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3581
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3581
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3582
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3582
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3583
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3583
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3584
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3584
Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3585
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3585
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 3586
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3586
Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 3587
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3587
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3588
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3588
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3589
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3589
Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3590
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3590
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3591
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3591
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3592
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3592
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3593
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3593
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3594
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3594
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3595
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3595
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3596
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3596
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3597
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3597
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3598
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3598
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 3599
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3599
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5 10
<210> 3600
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3600
Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3601
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3601
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3602
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3602
Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3603
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3603
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 3604
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3604
Gly Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5 10
<210> 3605
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3605
Ile Thr Glu Tyr Met Ala Asn Gly Ser
1 5
<210> 3606
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3606
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5 10
<210> 3607
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3607
Ile Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3608
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3608
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3609
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3609
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3610
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3610
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3611
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3611
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3612
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3612
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3613
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3613
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3614
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3614
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3615
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3615
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3616
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3616
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3617
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3617
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3618
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3618
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3619
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3619
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3620
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3620
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3621
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3621
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3622
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3622
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3623
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3623
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3624
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3624
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3625
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3625
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3626
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3626
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3627
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3627
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3628
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3628
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3629
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3629
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3630
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3630
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3631
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3631
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3632
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3632
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3633
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3633
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3634
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3634
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3635
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3635
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3636
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3636
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3637
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3637
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3638
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3638
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3639
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3639
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 3640
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3640
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5 10
<210> 3641
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3641
Asn Gly Ser Leu Leu Asn Tyr Leu
1 5
<210> 3642
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3642
Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3643
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3643
Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3644
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3644
Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3645
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3645
Asn Gly Ser Leu Leu Asn Tyr Leu Arg
1 5
<210> 3646
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3646
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3647
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3647
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3648
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3648
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3649
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3649
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3650
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3650
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3651
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3651
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3652
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3652
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3653
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3653
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3654
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3654
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3655
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3655
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3656
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3656
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3657
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3657
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3658
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3658
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3659
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3659
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3660
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3660
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3661
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3661
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3662
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3662
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3663
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3663
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3664
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3664
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3665
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3665
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 3666
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3666
Ser Leu Leu Asn Tyr Leu Arg Glu Met Arg
1 5 10
<210> 3667
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3667
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3668
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3668
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3669
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3669
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3670
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3670
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3671
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3671
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3672
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3672
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3673
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3673
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3674
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3674
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3675
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3675
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3676
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3676
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3677
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3677
Thr Glu Tyr Met Ala Asn Gly Ser Leu
1 5
<210> 3678
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3678
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3679
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3679
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3680
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3680
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3681
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3681
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3682
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3682
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5 10
<210> 3683
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 3683
Thr Glu Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3684
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3684
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3685
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3685
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3686
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3686
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3687
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3687
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3688
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3688
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3689
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3689
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3690
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3690
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3691
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3691
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3692
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3692
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3693
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3693
Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3694
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3694
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 3695
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3695
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 3696
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3696
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3697
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3697
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3698
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3698
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3699
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3699
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3700
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3700
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3701
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3701
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3702
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3702
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3703
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3703
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3704
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3704
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3705
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3705
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3706
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3706
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3707
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3707
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3708
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3708
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3709
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3709
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3710
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3710
Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5
<210> 3711
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3711
Tyr Met Ala Asn Gly Ser Leu Leu Asn Tyr
1 5 10
<210> 3712
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3712
Glu Tyr Met Ala Asn Gly Ser Leu Leu
1 5
<210> 3713
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3713
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3714
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3714
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3715
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3715
Tyr Met Ala Asn Gly Ser Leu Leu Asn
1 5
<210> 3716
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3716
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3717
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3717
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3718
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3718
Ser Leu Leu Asn Tyr Leu Arg Glu Met
1 5
<210> 3719
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3719
Met Ala Asn Gly Ser Leu Leu Asn Tyr Leu
1 5 10
<210> 3720
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3720
Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3721
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3721
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3722
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3722
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3723
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3723
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3724
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3724
Ser Thr Val Gln Leu Ile Met Gln Leu Met
1 5 10
<210> 3725
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3725
Thr Ser Thr Val Gln Leu Ile Met Gln Leu
1 5 10
<210> 3726
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3726
Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3727
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3727
Thr Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3728
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 3728
Val Gln Leu Ile Met Gln Leu Met
1 5
<210> 3729
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3729
Leu Thr Ser Thr Val Gln Leu Ile Met
1 5
<210> 3730
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3730
Cys Leu Thr Ser Thr Val Gln Leu Ile Met
1 5 10
<210> 3731
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3731
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3732
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3732
Met Gln Leu Met Pro Phe Gly Cys Leu
1 5
<210> 3733
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3733
Leu Ile Met Gln Leu Met Pro Phe Gly Cys
1 5 10
<210> 3734
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3734
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3735
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3735
Cys Leu Thr Ser Thr Val Gln Leu Ile Met
1 5 10
<210> 3736
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3736
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3737
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3737
Ile Met Gln Leu Met Pro Phe Gly Cys
1 5
<210> 3738
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3738
Leu Ile Met Gln Leu Met Pro Phe Gly
1 5
<210> 3739
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3739
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3740
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3740
Gln Leu Ile Met Gln Leu Met Pro Phe Gly
1 5 10
<210> 3741
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3741
Ser Thr Val Gln Leu Ile Met Gln Leu
1 5
<210> 3742
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3742
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3743
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3743
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3744
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3744
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3745
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3745
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3746
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3746
Met Gln Leu Met Pro Phe Gly Cys Leu
1 5
<210> 3747
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3747
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3748
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3748
Ile Met Gln Leu Met Pro Phe Gly Cys Leu
1 5 10
<210> 3749
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3749
Met Gln Leu Met Pro Phe Gly Cys Leu
1 5
<210> 3750
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3750
Met Gln Leu Met Pro Phe Gly Cys Leu Leu
1 5 10
<210> 3751
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3751
Val Gln Leu Ile Met Gln Leu Met Pro Phe
1 5 10
<210> 3752
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3752
Gln Leu Ile Met Gln Leu Met Pro Phe
1 5
<210> 3753
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3753
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3754
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3754
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3755
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3755
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 3756
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3756
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 3757
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3757
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 3758
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3758
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5 10
<210> 3759
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3759
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3760
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3760
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3761
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3761
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3762
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3762
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 3763
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3763
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3764
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3764
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 3765
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3765
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 3766
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3766
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3767
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3767
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3768
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3768
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3769
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3769
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 3770
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3770
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3771
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3771
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3772
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3772
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3773
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3773
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3774
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3774
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3775
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3775
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3776
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3776
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3777
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3777
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3778
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3778
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3779
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3779
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3780
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3780
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3781
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3781
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3782
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3782
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3783
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3783
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu
1 5 10
<210> 3784
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3784
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3785
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3785
His Val Leu Pro Glu Pro His Leu Ala Leu
1 5 10
<210> 3786
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3786
Ala Leu Gln Pro Leu Gln Pro His Ala
1 5
<210> 3787
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3787
Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5
<210> 3788
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 3788
Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
1 5 10
<210> 3789
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3789
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3790
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3790
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3791
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3791
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3792
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3792
Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5
<210> 3793
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3793
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3794
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3794
Val Leu Trp Thr Thr Pro Pro Leu Gln His
1 5 10
<210> 3795
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3795
Tyr Met Phe Leu Lys Ala Glu Ser Lys
1 5
<210> 3796
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3796
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3797
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3797
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3798
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3798
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3799
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3799
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu
1 5 10
<210> 3800
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3800
Gly Pro Pro Ala Arg Val Pro Ala Val
1 5
<210> 3801
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3801
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3802
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3802
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3803
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3803
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3804
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3804
Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
1 5 10
<210> 3805
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3805
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3806
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3806
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe
1 5 10
<210> 3807
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3807
Leu His Phe Cys Arg Ser Ser Ile Met
1 5
<210> 3808
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3808
Glu Pro His Leu Ala Leu Gln Pro Leu
1 5
<210> 3809
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3809
Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5
<210> 3810
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3810
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3811
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3811
Phe Leu Lys Ala Glu Ser Lys Ile Met
1 5
<210> 3812
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3812
Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10
<210> 3813
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 3813
Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser Leu
1 5 10
<210> 3814
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 3814
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
<210> 3815
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3815
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3816
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 3816
Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val
1 5 10 15
Pro Phe Asp Leu His
20
<210> 3817
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 3817
Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr
1 5 10 15
Met Phe Leu Lys Ala Glu Ser Lys Ile
20 25
<210> 3818
<211> 26
<212> БЕЛОК
<213> Homo sapiens
<400> 3818
Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His Phe Cys
1 5 10 15
Arg Ser Ser Ile Met Lys Pro Lys Arg Asp
20 25
<210> 3819
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 3819
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3820
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 3820
Gly Gly Ala Ala Thr Thr Ala Ala Gly Ala Gly Ala Ala Gly Cys
1 5 10 15
<210> 3821
<211> 5
<212> БЕЛОК
<213> Homo sapiens
<400> 3821
Glu Leu Arg Glu Ala
1 5
<210> 3822
<211> 5
<212> БЕЛОК
<213> Homo sapiens
<400> 3822
Glu Leu Arg Glu Ala
1 5
<210> 3823
<211> 4
<212> БЕЛОК
<213> Homo sapiens
<400> 3823
Tyr Val Met Ala
1
<210> 3824
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3824
Val Leu Pro Glu Pro His Leu Ala Leu
1 5
<210> 3825
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3825
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3826
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3826
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3827
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3827
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3828
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3828
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3829
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3829
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3830
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3830
Met Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn
1 5 10 15
Cys Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp
20 25 30
Pro Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn
35 40 45
Arg Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys
50 55 60
Met Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu
65 70 75 80
Asp Phe Pro Lys Asn Ser Ser Phe Pro Gly Arg Pro Leu Gln Thr His
85 90 95
Val Leu Pro Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala
100 105 110
Asp His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu Trp Thr
115 120 125
Thr Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser
130 135 140
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
145 150 155 160
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
165 170 175
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
180 185 190
Ser Leu Trp Cys Leu Cys Ser Asn His
195 200
<210> 3831
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3831
Met Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn
1 5 10 15
Cys Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp
20 25 30
Pro Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn
35 40 45
Arg Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys
50 55 60
Met Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu
65 70 75 80
Asp Phe Pro Lys Asn Ser Ser Phe Pro Gly Arg Pro Leu Gln Thr His
85 90 95
Val Leu Pro Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala
100 105 110
Asp His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu Trp Thr
115 120 125
Thr Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser
130 135 140
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
145 150 155 160
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
165 170 175
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
180 185 190
Ser Leu Trp Cys Leu Cys Ser Asn His
195 200
<210> 3832
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 3832
Met Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn
1 5 10 15
Cys Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp
20 25 30
Pro Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn
35 40 45
Arg Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys
50 55 60
Met Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu
65 70 75 80
Asp Phe Pro Lys Asn Ser Ser Phe Pro Gly Arg Pro Leu Gln Thr His
85 90 95
Val Leu Pro Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala
100 105 110
Asp His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu Trp Thr
115 120 125
Thr Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser
130 135 140
Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu
145 150 155 160
His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met
165 170 175
Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser
180 185 190
Ser Leu Trp Cys Leu Cys Ser Asn His
195 200
<210> 3833
<211> 110
<212> БЕЛОК
<213> Homo sapiens
<400> 3833
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala Asp Ala Pro Ala Ile
20 25 30
Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His His Arg His Gly
35 40 45
Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala
50 55 60
Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met Lys Pro Lys
65 70 75 80
Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile Met Phe Ala
85 90 95
Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn His
100 105 110
<210> 3834
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3834
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3835
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3835
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3836
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3836
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3837
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3837
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3838
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3838
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3839
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3839
Lys Ile Met Phe Ala Thr Leu Gln Arg
1 5
<210> 3840
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3840
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3841
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3841
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3842
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3842
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3843
<211> 33
<212> БЕЛОК
<213> Homo sapiens
<400> 3843
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
1 5 10 15
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
20 25 30
His
<210> 3844
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3844
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3845
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3845
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3846
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 3846
Ser Met Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp
1 5 10 15
Leu His
<210> 3847
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3847
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3848
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3848
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3849
<211> 600
<212> ДНК
<213> Homo sapiens
<400> 3849
cgaaggctgt ctgcagccag gagagcaggg acgtcctgtg cgaactgtca gaccaccaca
60
accacactct ggaggaggaa tgccaatggg gaccctgtct gcaatgcctg tgggctctac
120
tacaagcttc acaatattaa cagacccctg actatgaaga aggaaggcat ccagaccaga
180
aaccgaaaaa tgtctagcaa atccaaaaag tgcaaaaaag tgcatgactc actggaggac
240
ttccccaaga acagctcgtt tcccggccgc cctctccaga cacatgtcct ccctgagcca
300
catctcgccc ttcagccact ccagccacat gctgaccacg cccacgccga tgcacccgcc
360
atccagcctg tcctttggac cacaccaccc ctccagcatg gtcaccgcca tgggttagag
420
ccctgctcga tgctcacagg gcccccagcg agagtccctg cagtcccttt cgacttgcat
480
ttttgcagga gcagtatcat gaagcctaaa cgcgatggat atatgttttt gaaggcagaa
540
agcaaaatta tgtttgccac tttgcaaagg agctcactgt ggtgtctgtg ttccaaccac
600
<210> 3850
<211> 602
<212> ДНК
<213> Homo sapiens
<400> 3850
cgaaggctgt ctgcagccag gagagcaggg acgtcctgtg cgaactgtca gaccaccaca
60
accacactct ggaggaggaa tgccaatggg gaccctgtct gcaatgcctg tgggctctac
120
tacaagcttc acaatattaa cagacccctg actatgaaga aggaaggcat ccagaccaga
180
aaccgaaaaa tgtctagcaa atccaaaaag tgcaaaaaag tgcatgactc actggaggac
240
ttccccaaga acagctcgtt taacccggcc gccctctcca gacacatgtc ctccctgagc
300
cacatctcgc ccttcagcca ctccagccac atgctgacca cgcccacgcc gatgcacccg
360
ccatccagcc tgtcctttgg accacaccac ccctccagca tggtcaccgc catgggttag
420
agccctgctc gatgctcaca gggcccccag cgagagtccc tgcagtccct ttcgacttgc
480
atttttgcag gagcagtatc atgaagccta aacgcgatgg atatatgttt ttgaaggcag
540
aaagcaaaat tatgtttgcc actttgcaaa ggagctcact gtggtgtctg tgttccaacc
600
ac
602
<210> 3851
<211> 197
<212> БЕЛОК
<213> Homo sapiens
<400> 3851
Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn Cys
1 5 10 15
Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp Pro
20 25 30
Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn Arg
35 40 45
Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys Met
50 55 60
Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu Asp
65 70 75 80
Phe Pro Lys Asn Ser Ser Phe Asn Pro Ala Ala Leu Ser Arg His Met
85 90 95
Ser Ser Leu Ser His Ile Ser Pro Phe Ser His Ser Ser His Met Leu
100 105 110
Thr Thr Pro Thr Pro Met His Pro Pro Ser Ser Leu Ser Phe Gly Pro
115 120 125
His His Pro Ser Ser Met Val Thr Ala Met Gly Ser Pro Ala Arg Cys
130 135 140
Ser Gln Gly Pro Gln Arg Glu Ser Leu Gln Ser Leu Ser Thr Cys Ile
145 150 155 160
Phe Ala Gly Ala Val Ser Ser Leu Asn Ala Met Asp Ile Cys Phe Arg
165 170 175
Gln Lys Ala Lys Leu Cys Leu Pro Leu Cys Lys Gly Ala His Cys Gly
180 185 190
Val Cys Val Pro Thr
195
<210> 3852
<211> 200
<212> БЕЛОК
<213> Homo sapiens
<400> 3852
Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn Cys
1 5 10 15
Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp Pro
20 25 30
Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn Arg
35 40 45
Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys Met
50 55 60
Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu Asp
65 70 75 80
Phe Pro Lys Asn Ser Ser Phe Pro Gly Arg Pro Leu Gln Thr His Val
85 90 95
Leu Pro Glu Pro His Leu Ala Leu Gln Pro Leu Gln Pro His Ala Asp
100 105 110
His Ala His Ala Asp Ala Pro Ala Ile Gln Pro Val Leu Trp Thr Thr
115 120 125
Pro Pro Leu Gln His Gly His Arg His Gly Leu Glu Pro Cys Ser Met
130 135 140
Leu Thr Gly Pro Pro Ala Arg Val Pro Ala Val Pro Phe Asp Leu His
145 150 155 160
Phe Cys Arg Ser Ser Ile Met Lys Pro Lys Arg Asp Gly Tyr Met Phe
165 170 175
Leu Lys Ala Glu Ser Lys Ile Met Phe Ala Thr Leu Gln Arg Ser Ser
180 185 190
Leu Trp Cys Leu Cys Ser Asn His
195 200
<210> 3853
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (104)..(105)
<223> Может присутствовать или не присутствовать
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (137)..(137)
<223> Может присутствовать или не присутствовать
<220>
<221> MOD_RES
<222> (140)..(140)
<223> Met или Leu
<220>
<221> MOD_RES
<222> (167)..(167)
<223> Val или Ile
<220>
<221> MOD_RES
<222> (185)..(185)
<223> Leu или Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (200)..(201)
<223> Может присутствовать или не присутствовать
<400> 3853
Arg Arg Leu Ser Ala Ala Arg Arg Ala Gly Thr Ser Cys Ala Asn Cys
1 5 10 15
Gln Thr Thr Thr Thr Thr Leu Trp Arg Arg Asn Ala Asn Gly Asp Pro
20 25 30
Val Cys Asn Ala Cys Gly Leu Tyr Tyr Lys Leu His Asn Ile Asn Arg
35 40 45
Pro Leu Thr Met Lys Lys Glu Gly Ile Gln Thr Arg Asn Arg Lys Met
50 55 60
Ser Ser Lys Ser Lys Lys Cys Lys Lys Val His Asp Ser Leu Glu Asp
65 70 75 80
Phe Pro Lys Asn Ser Ser Phe Asn Gly Ala Ala Leu Gln Arg His Met
85 90 95
Leu Pro Glu Pro His Ile Ala Leu Gln Pro Leu Gln His His Ala Asp
100 105 110
His Ala His Ala Asp Ala Pro Ala His Gln Pro Ser Leu Leu Ser Phe
115 120 125
Gly Pro His Gln His Gly His Arg Val His Ala Xaa Glu Pro Cys Ala
130 135 140
Arg Cys Ser Gln Gly Pro Ala Arg Glu Pro Ala Gln Pro Leu Asp Leu
145 150 155 160
Cys Ile Cys Ala Gly Ala Xaa Met Lys Leu Asn Ala Asp Asp Ile Cys
165 170 175
Phe Arg Gln Ala Ala Lys Leu Cys Xaa Phe Ala Cys Leu Gln Ala His
180 185 190
Cys Gly Trp Cys Leu Cys Ser Asn His
195 200
<210> 3854
<211> 624
<212> ДНК
<213> Homo sapiens
<400> 3854
gaattcgacg ccaccatgag aaggctgagc gccgctagaa gagccggcac cagctgcgcc
60
aactgccaga ccaccaccac caccctgtgg agaaggaacg ccaacggcga tcccgtgtgt
120
aacgcctgcg gcctgtacta caagctgcac aacatcaaca ggcccctgac catgaagaag
180
gagggcatcc agaccaggaa caggaagatg tccagcaaga gcaagaagtg caagaaggtg
240
cacgacagcc tggaggactt ccccaagaac agcagcttcc ccggaagacc cctgcagaca
300
cacgtgctgc ccgagcctca tctggccctg cagcctctcc agccccatgc cgatcatgcc
360
cacgccgatg cccctgccat ccaacccgtg ctgtggacca cccctcctct gcagcacgga
420
cacagacacg gcctggagcc ctgtagcatg ctgacaggac ctcccgccag agtgcctgcc
480
gtgcctttcg acctgcactt ctgcagaagc agcatcatga agcccaagag ggacggctat
540
atgttcctga aggccgagtc caagatcatg ttcgccaccc tgcagagaag ctccctgtgg
600
tgcctgtgca gcaaccacgg atcc
624
<210> 3855
<211> 759
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3855
tgacgcaaat gggcggtagg cgtgtacggt gggaggtcta tataagcaga gcttctagag
60
ctagcgaatt cgacgccacc atgagaaggc tgagcgccgc tagaagagcc ggcaccagct
120
gcgccaactg ccagaccacc accaccaccc tgtggagaag gaacgccaac ggcgatcccg
180
tgtgtaacgc ctgcggcctg tactacaagc tgcacaacat caacaggccc ctgaccatga
240
agaaggaggg catccagacc aggaacagga agatgtccag caagagcaag aagtgcaaga
300
aggtgcacga cagcctggag gacttcccca agaacagcag cttccccgga agacccctgc
360
agacacacgt gctgcccgag cctcatctgg ccctgcagcc tctccagccc catgccgatc
420
atgcccacgc cgatgcccct gccatccaac ccgtgctgtg gaccacccct cctctgcagc
480
acggacacag acacggcctg gagccctgta gcatgctgac aggacctccc gccagagtgc
540
ctgccgtgcc tttcgacctg cacttctgca gaagcagcat catgaagccc aagagggacg
600
gctatatgtt cctgaaggcc gagtccaaga tcatgttcgc caccctgcag agaagctccc
660
tgtggtgcct gtgcagcaac cacggatccg cggccgctga gggcagagga agtcttctaa
720
catgcggtga cgtggaggag aatcccggcc cttccggga
759
<210> 3856
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3856
gaattcgacg ccaccatgag aaggctgagc gccgctagaa gagccggcac cagctgcgcc
60
aactgccaga ccaccaccac caccctgtgg agaaggaacg ccaacggcga tcccgtgtgt
120
aacgcctgcg gcctgtacta caagctgcac aacatcaaca ggcccctgac catgaagaag
180
gagggcatcc agaccaggaa caggaagatg tccagcaaga gcaagaagtg caagaaggtg
240
cacgacagcc tggaggactt ccccaagaac agcagcttcc ccggaagacc cctgcagaca
300
cacgtgctgc ccgagcctca tctggccctg cagcctctcc agccccatgc cgatcatgcc
360
cacgccgatg cccctgccat ccaacccgtg ctgtggacca cccctcctct gcagcacgga
420
cacagacacg gcctggagcc ctgtagcatg ctgacaggac ctcccgccag agtgcctgcc
480
gtgcctttcg acctgcactt ctgcagaagc agcatcatga agcccaagag ggacggctat
540
atgttcctga aggccgagtc caagatcatg ttcgccaccc tgcagagaag ctccctgtgg
600
tgcctgtgca gcaaccacgg atcc
624
<210> 3857
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 3857
Pro Gly Arg Pro Leu Gln Thr His Val Leu Pro Glu Pro His Leu Ala
1 5 10 15
Leu Gln Pro Leu Gln Pro His Ala Asp His Ala His Ala Asp Ala Pro
20 25 30
Ala Ile Gln Pro Val Leu Trp Thr Thr Pro Pro Leu Gln His Gly His
35 40 45
Arg His Gly Leu Glu Pro Cys Ser Met Leu Thr Gly Pro Pro Ala Arg
50 55 60
Val Pro Ala Val Pro Phe Asp Leu His Phe Cys Arg Ser Ser Ile Met
65 70 75 80
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu Lys Ala Glu Ser Lys Ile
85 90 95
Met Phe Ala Thr Leu Gln Arg Ser Ser Leu Trp Cys Leu Cys Ser Asn
100 105 110
His
<210> 3858
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3858
Ser Met Leu Thr Gly Pro Pro Ala Arg Val
1 5 10
<210> 3859
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3859
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3860
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3860
Lys Pro Lys Arg Asp Gly Tyr Met Phe
1 5
<210> 3861
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 3861
Lys Pro Lys Arg Asp Gly Tyr Met Phe Leu
1 5 10
<210> 3862
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3862
Glu Ser Lys Ile Met Phe Ala Thr Leu
1 5
<210> 3863
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3863
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3864
<211> 9
<212> БЕЛОК
<213> Homo sapiens
<400> 3864
Met Leu Thr Gly Pro Pro Ala Arg Val
1 5
<210> 3865
<211> 840
<212> ДНК
<213> Homo sapiens
<400> 3865
acagatccaa gctgtgaccg gcgcctactc tagagctagc gaattcgacg ccaccatggg
60
cattcgtctg ctgtgtcgtg tggccttctg ctttttagcc gtgggtttag tggacgtgaa
120
ggtgacccag tcctctcgtt atttagtgaa gaggaccggc gagaaggtgt ttttagaatg
180
cgtgcaagat atggaccacg agaacatgtt ctggtacaga caagatcccg gactgggttt
240
aaggctgatc tacttcagct acgacgtgaa gatgaaggag aagggcgaca tccccgaggg
300
ctactccgtg tctcgtgaga agaaggagag gttctcttta attttagagt ccgccagcac
360
caaccagacc agcatgtatt tatgcgccag ctctttagac tttgtgctgg ccggcagcta
420
cagctacaac gagcagttct tcggccccgg caccagactg accgtgctgg aggacctgaa
480
caaggtcttt cctcccgaag tggccgtgtt tgagcccagc gaggccgaga tcagccatac
540
ccagaaggcc acactcgtgt gcctggccac cggcttcttt cccgaccatg tggagctgag
600
ctggtgggtg aacggcaagg aggtccactc cggagtcagc accgatcccc agcctctcaa
660
agagcagccc gctctcaacg actccaggta ttgcctgtcc agcaggctga gagtcagcgc
720
caccttttgg cagaatccca ggaaccactt caggtgccag gtccagttct atggcctgag
780
cgagaacgac gagtgacaca ggatagagct aagcccgtga cccagattgt cagcgccgag
840
<210> 3866
<211> 1035
<212> ДНК
<213> Homo sapiens
<400> 3866
atgggcattc gtctgctgtg tcgtgtggcc ttctgctttt tagccgtggg tttagtggac
60
gtgaaggtga cccagtcctc tcgttattta gtgaagagga ccggcgagaa ggtgttttta
120
gaatgcgtgc aagatatgga ccacgagaac atgttctggt acagacaaga tcccggactg
180
ggtttaaggc tgatctactt cagctacgac gtgaagatga aggagaaggg cgacatcccc
240
gagggctact ccgtgtctcg tgagaagaag gagaggttct ctttaatttt agagtccgcc
300
agcaccaacc agaccagcat gtatttatgc gccagctctt tagactttgt gctggccggc
360
agctacagct acaacgagca gttcttcggc cccggcacca gactgaccgt gctggaggac
420
ctgaacaagg tctttcctcc cgaagtggcc gtgtttgagc ccagcgaggc cgagatcagc
480
catacccaga aggccacact cgtgtgcctg gccaccggct tctttcccga ccatgtggag
540
ctgagctggt gggtgaacgg caaggaggtc cactccggag tcagcaccga tccccagcct
600
ctcaaagagc agcccgctct caacgactcc aggtattgcc tgtccagcag gctgagagtc
660
agcgccacct tttggcagaa tcccaggaac cacttcaggt gccaggtcca gttctatggc
720
ctgagcgaga acgacgagtg gacacaggat agagctaagc ccgtgaccca gattgtcagc
780
gccgaggcct ggggcagagc cgactgtgga ttcacaagcg tgtcctatca gcaaggcgtg
840
ctcagcgcca ccattctgta cgagatcctg ctgggcaaag ccaccctgta cgctgtgctg
900
gtgtccgctc tggtgctgat ggctatggtc aagaggaagg actttcggat caggcgcagc
960
ggaagcggag tgaagcaaac cctcaacttc gacctgctca agctggccgg agatgtggaa
1020
agcaatcccg gaccc
1035
<210> 3867
<211> 267
<212> ДНК
<213> Homo sapiens
<400> 3867
cagattgtca gcgccgaggc ctggggcaga gccgactgtg gattcacaag cgtgtcctat
60
cagcaaggcg tgctcagcgc caccattctg tacgagatcc tgctgggcaa agccaccctg
120
tacgctgtgc tggtgtccgc tctggtgctg atggctatgg tcaagaggaa ggactttcgg
180
atcaggcgca gcggaagcgg agtgaagcaa accctcaact tcgacctgct caagctggcc
240
ggagatgtgg aaagcaatcc cggaccc
267
<210> 3868
<211> 1034
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3868
atgggcattc gtctgctgtg tcgtgtggcc ttctgctttt tagccgtggg tttagtggac
60
gtgaaggtga cccagtcctc tcgttattta gtgaagagga ccggcgagaa ggtgttttta
120
gaatgcgtgc aagatatgga ccacgagaac atgttctggt acagacaaga tcccggactg
180
ggtttaaggc tgatctactt cagctacgac gtgaagatga aggagaaggg cgacatcccc
240
gagggctact ccgtgtctcg tgagaagaag gagaggttct ctttaatttt agagtccgcc
300
agcaccaacc agaccagcat gtatttatgc gccagctctt tagactttgt gctggccggc
360
agctacagct acaacgagca gttcttcggc cccggcacca gactgaccgt gctggaggac
420
ctgaacaagg tctttcctcc cgaagtggcc gtgtttgagc ccagcgaggc cgagatcagc
480
catacccaga aggccacact cgtgtgcctg gccaccggct tctttcccga ccatgtggag
540
ctgagctggt gggtgaacgg caaggaggtc cactccggag tcagcaccga tccccagcct
600
ctcaaagagc agcccgctct caacgactcc aggtattgcc tgtccagcag gctgagagtc
660
agcgccacct tttggcagaa tcccaggaac cacttcaggt gccaggtcca gttctatggc
720
ctgagcgaga acgacgagtg acacaggata gagctaagcc cgtgacccag attgtcagcg
780
ccgaggcctg gggcagagcc gactgtggat tcacaagcgt gtcctatcag caaggcgtgc
840
tcagcgccac cattctgtac gagatcctgc tgggcaaagc caccctgtac gctgtgctgg
900
tgtccgctct ggtgctgatg gctatggtca agaggaagga ctttcggatc aggcgcagcg
960
gaagcggagt gaagcaaacc ctcaacttcg acctgctcaa gctggccgga gatgtggaaa
1020
gcaatcccgg accc
1034
<210> 3869
<211> 878
<212> ДНК
<213> Homo sapiens
<400> 3869
tttaggcggc gtgctgctga ttttatggct gcaagttgac tgggtgaaga gccagaagat
60
cgagcagaac agcgaggctt taaacattca agaaggcaag acagccactt taacttgtaa
120
ctataccaac tactcccccg cttatttaca gtggtacaga caagatcccg gcagaggccc
180
cgtgttttta ctgctgattc gtgagaacga gaaggagaag aggaaggaga gactgaaggt
240
gaccttcgac accactttaa agcagtcttt attccacatc accgccagcc agcccgctga
300
tagcgccacc tatttatgcg ctttagacat ctacggcaac aatcgtctgg ccttcggcaa
360
gggcaaccaa gttgtggtga tccccgatat tcagaatccc gatcccgctg tgtaccagct
420
gagggattcc aagtcctccg ataagtccgt ctgtctgttc accgacttcg atagccagac
480
caacgtgagc caaagcaagg actccgacgt gtatatcaca gacaagaccg tgctggacat
540
gaggagcatg gacttcaaga gcaatagcgc cgtggcctgg tccaataaga gcgatttcgc
600
ctgcgccaac gccttcaaca atagcatcat tcccgaggac accttcttcc ccagccccga
660
aagcagctgc gatgtgaaac tggtggagaa gtcctttgag accgacacca acctcaactt
720
ccagaacctc tccgtgatcg gattcaggat tctgctgctg aaggtggctg gctttaacct
780
gctgatgacc ctcaggctgt ggtccagcta aggatccgtc gacaatcaac ctctggatta
840
caaaatttgt gaaagattga ctggtattct taactatg
878
<210> 3870
<211> 876
<212> ДНК
<213> Homo sapiens
<400> 3870
atggccttct ggctgaggag actgggttta cacttcagac cccatttagg cagaagaatg
60
gagagctttt taggcggcgt gctgctgatt ttatggctgc aagttgactg ggtgaagagc
120
cagaagatcg agcagaacag cgaggcttta aacattcaag aaggcaagac agccacttta
180
acttgtaact ataccaacta ctcccccgct tatttacagt ggtacagaca agatcccggc
240
agaggccccg tgtttttact gctgattcgt gagaacgaga aggagaagag gaaggagaga
300
ctgaaggtga ccttcgacac cactttaaag cagtctttat tccacatcac cgccagccag
360
cccgctgata gcgccaccta tttatgcgct ttagacatct acggcaacaa tcgtctggcc
420
ttcggcaagg gcaaccaagt tgtggtgatc cccgatattc agaatcccga tcccgctgtg
480
taccagctga gggattccaa gtcctccgat aagtccgtct gtctgttcac cgacttcgat
540
agccagacca acgtgagcca aagcaaggac tccgacgtgt atatcacaga caagaccgtg
600
ctggacatga ggagcatgga cttcaagagc aatagcgccg tggcctggtc caataagagc
660
gatttcgcct gcgccaacgc cttcaacaat agcatcattc ccgaggacac cttcttcccc
720
agccccgaaa gcagctgcga tgtgaaactg gtggagaagt cctttgagac cgacaccaac
780
ctcaacttcc agaacctctc cgtgatcgga ttcaggattc tgctgctgaa ggtggctggc
840
tttaacctgc tgatgaccct caggctgtgg tccagc
876
<210> 3871
<211> 613
<212> ДНК
<213> Homo sapiens
<400> 3871
tgtggaaagc aatcccggac ccatggcctt ctggctgagg agactgggtt tacacttcag
60
accccattta ggcagaagaa tggagagctt tttaggcggc gtgctgctga ttttatggct
120
gcaagttgac tgggtgaaga gccagaagat cgagcagaac agcgaggctt taaacattca
180
agaaggcaag acagccactt taacttgtaa ctataccaac tactcccccg cttatttaca
240
gtggtacaga caagatcccg gcagaggccc cgtgttttta ctgctgattc gtgagaacga
300
gaaggagaag aggaaggaga gactgaaggt gaccttcgac accactttaa agcagtcttt
360
attccacatc accgccagcc agcccgctga tagcgccacc tatttatgcg ctttagacat
420
ctacggcaac aatcgtctgg ccttcggcaa gggcaaccaa gttgtggtga tccccgatat
480
tcagaatccc gatcccgctg tgtaccagct gagggattcc aagtcctccg ataagtccgt
540
ctgtctgttc accgacttcg atagccagac caacgtgagc caaagcaagg actccgacgt
600
gtatatcaca gac
613
<210> 3872
<211> 876
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3872
atggccttct ggctgaggag actgggttta cacttcagac cccatttagg cagaagaatg
60
gagagctttt taggcggcgt gctgctgatt ttatggctgc aagttgactg ggtgaagagc
120
cagaagatcg agcagaacag cgaggcttta aacattcaag aaggcaagac agccacttta
180
acttgtaact ataccaacta ctcccccgct tatttacagt ggtacagaca agatcccggc
240
agaggccccg tgtttttact gctgattcgt gagaacgaga aggagaagag gaaggagaga
300
ctgaaggtga ccttcgacac cactttaaag cagtctttat tccacatcac cgccagccag
360
cccgctgata gcgccaccta tttatgcgct ttagacatct acggcaacaa tcgtctggcc
420
ttcggcaagg gcaaccaagt tgtggtgatc cccgatattc agaatcccga tcccgctgtg
480
taccagctga gggattccaa gtcctccgat aagtccgtct gtctgttcac cgacttcgat
540
agccagacca acgtgagcca aagcaaggac tccgacgtgt atatcacaga caagaccgtg
600
ctggacatga ggagcatgga cttcaagagc aatagcgccg tggcctggtc caataagagc
660
gatttcgcct gcgccaacgc cttcaacaat agcatcattc ccgaggacac cttcttcccc
720
agccccgaaa gcagctgcga tgtgaaactg gtggagaagt cctttgagac cgacaccaac
780
ctcaacttcc agaacctctc cgtgatcgga ttcaggattc tgctgctgaa ggtggctggc
840
tttaacctgc tgatgaccct caggctgtgg tccagc
876
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОДОМИНАНТНЫЕ БЕЛКИ И ФРАГМЕНТЫ ПРИ РАССЕЯННОМ СКЛЕРОЗЕ | 2019 |
|
RU2828590C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ T-КЛЕТОК И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2835034C2 |
| АНТИТЕЛА К PD-1 И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2761640C2 |
| Композиции и способы лечения и предупреждения инфекций, вызванных Staphylococcus aureus | 2015 |
|
RU2764981C1 |
| ПРИМЕНЕНИЕ АНТИТЕЛ К СКЛЕРОСТИНУ ДЛЯ ЛЕЧЕНИЯ НЕСОВЕРШЕННОГО ОСТЕОГЕНЕЗА | 2017 |
|
RU2789033C2 |
| HPV-СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2018 |
|
RU2804664C2 |
| ПРОКОАГУЛЯНТНЫЕ АНТИТЕЛА | 2018 |
|
RU2810094C2 |
| ИСКУССТВЕННЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2763798C1 |
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
| МОДИФИЦИРОВАННЫЕ АНТИТЕЛА IGG, КОТОРЫЕ СВЯЗЫВАЮТСЯ С ТРАНСФОРМИРУЮЩИМ ФАКТОРОМ РОСТА БЕТА-1 С ВЫСОКОЙ АФФИННОСТЬЮ, АВИДНОСТЬЮ И СПЕЦИФИЧНОСТЬЮ | 2016 |
|
RU2728858C2 |
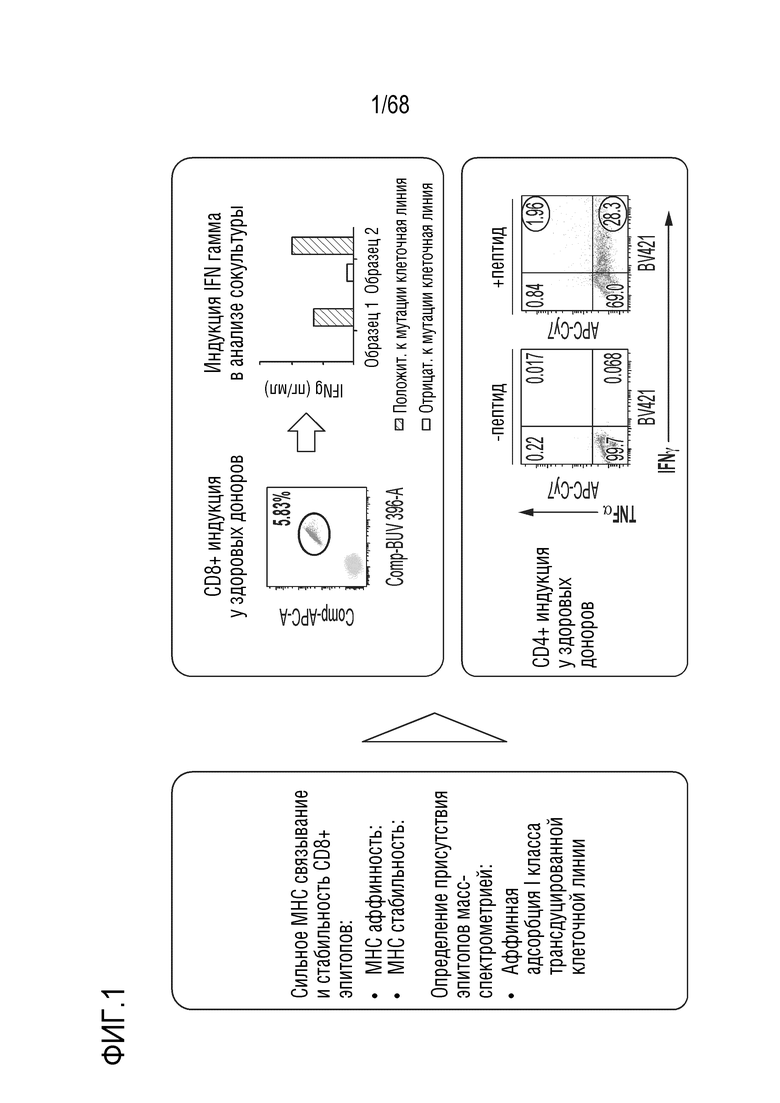

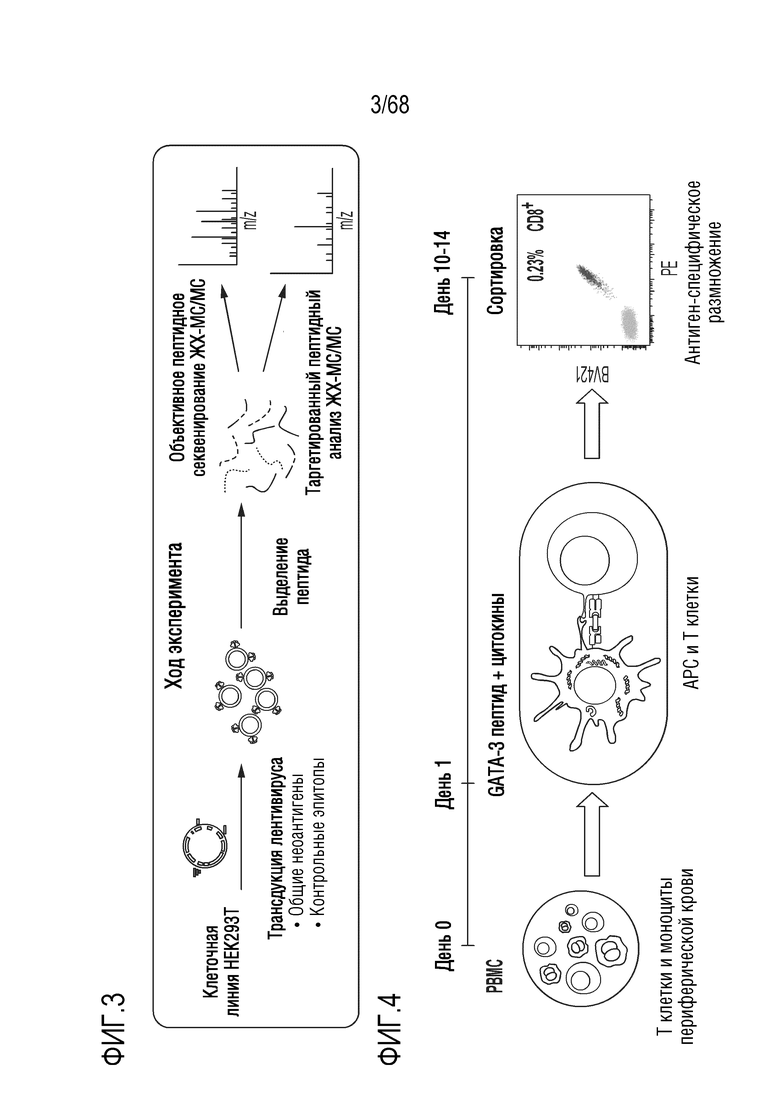

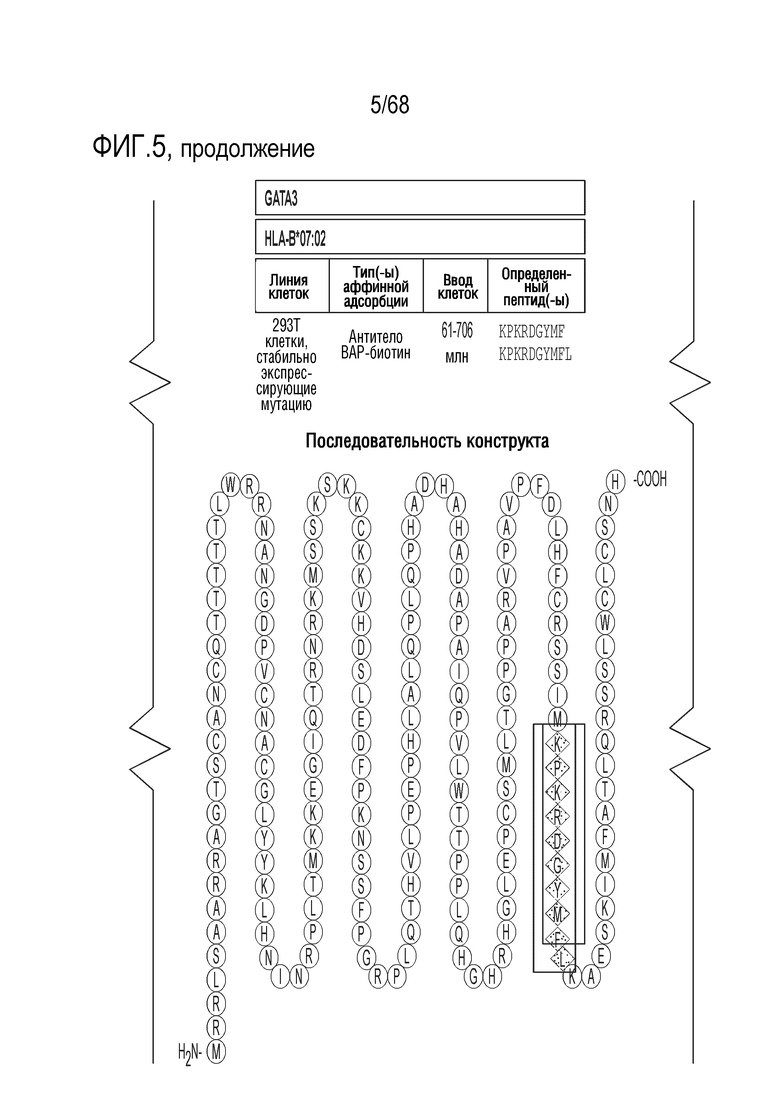
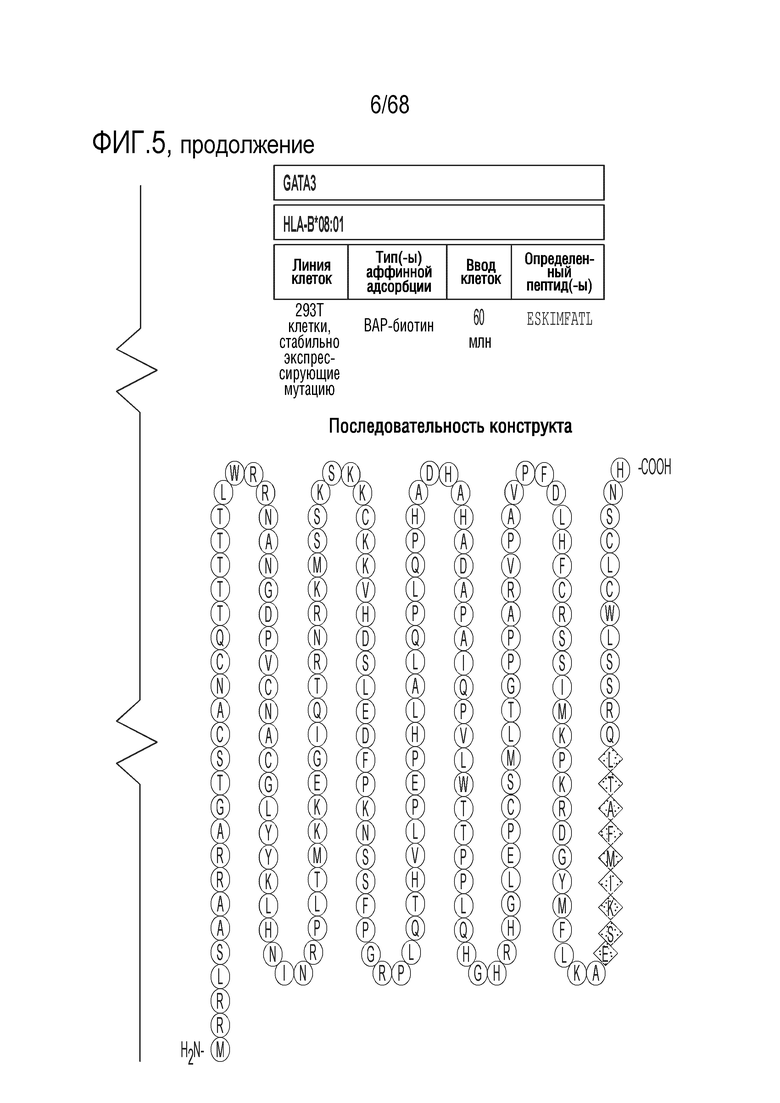
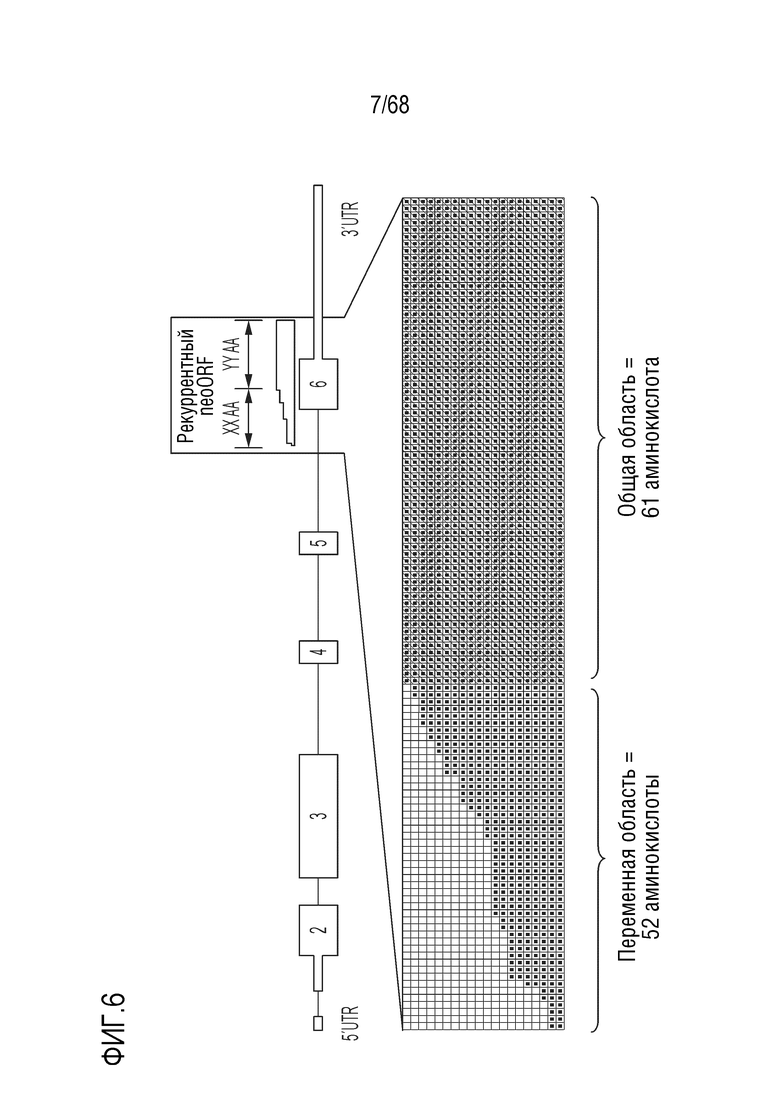


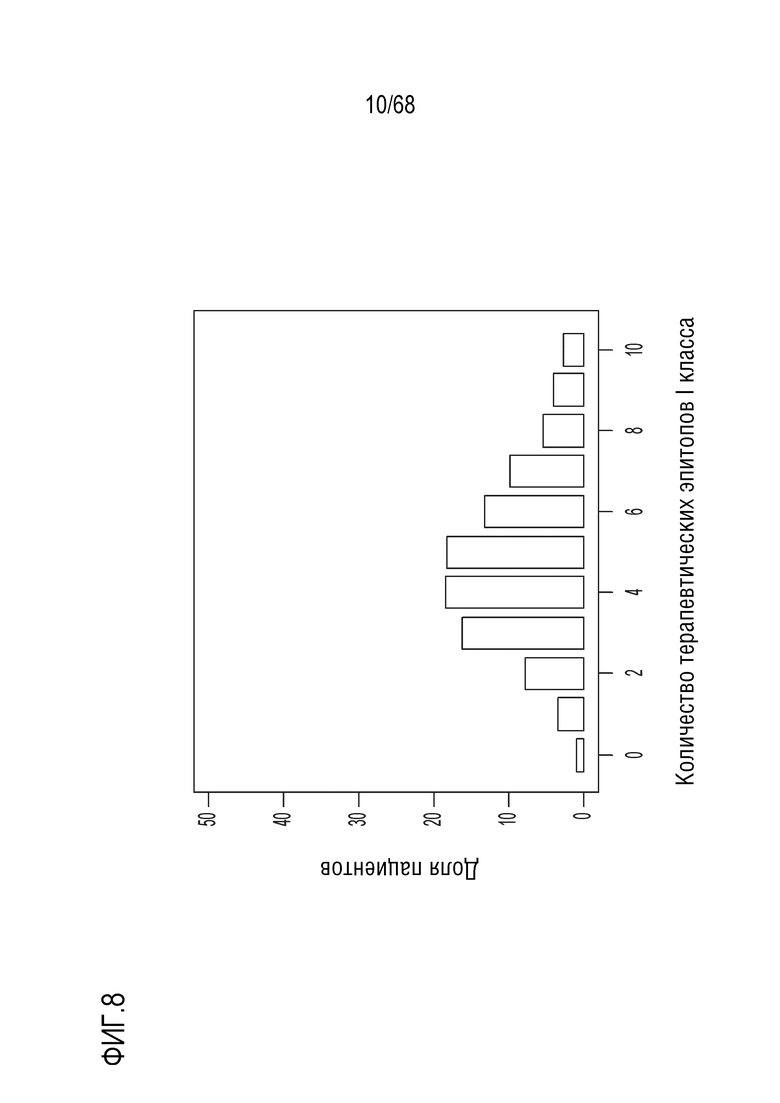
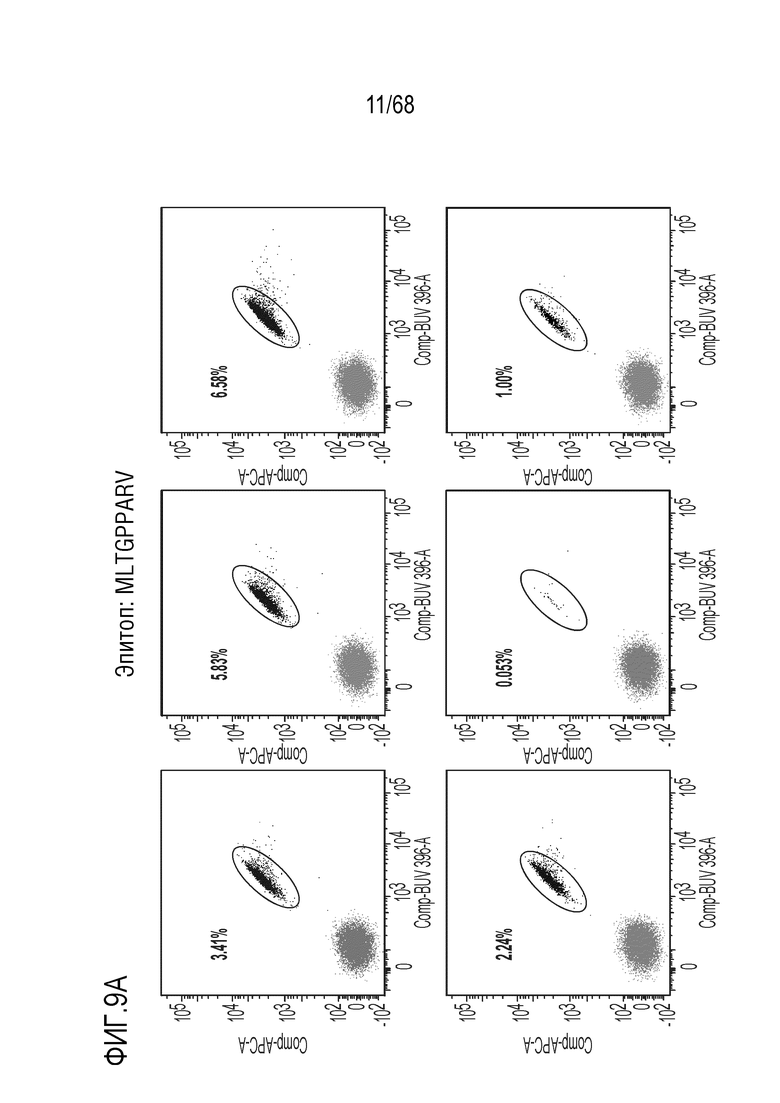
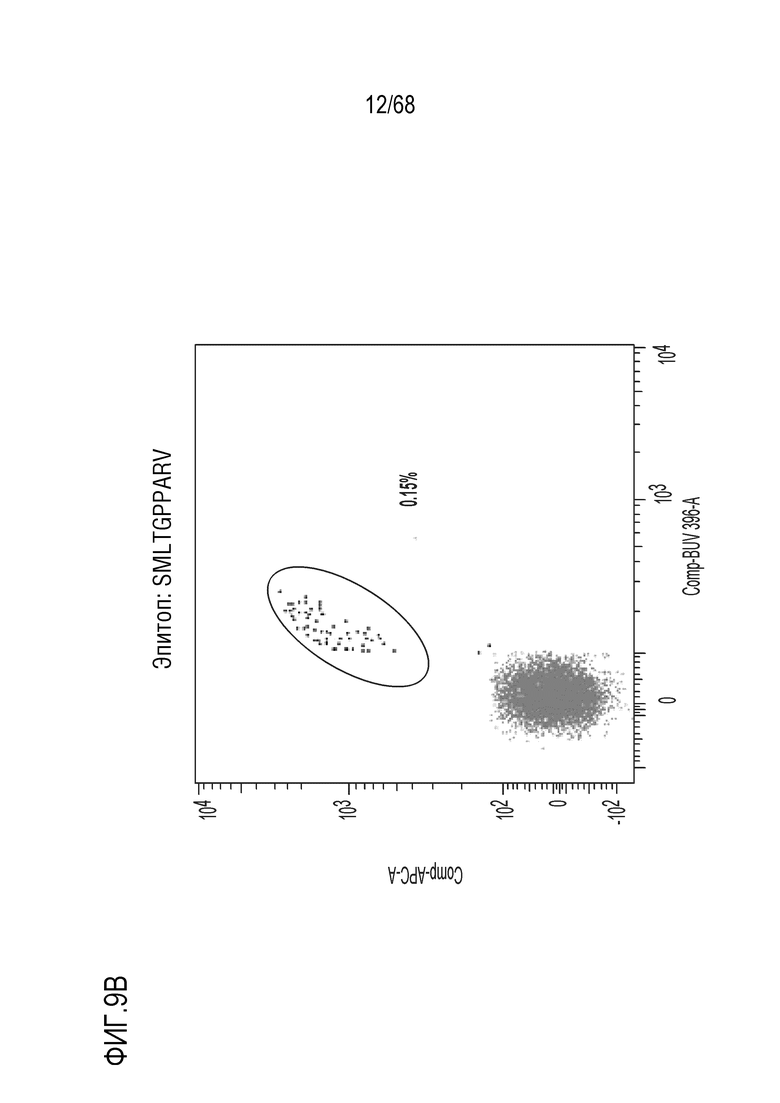
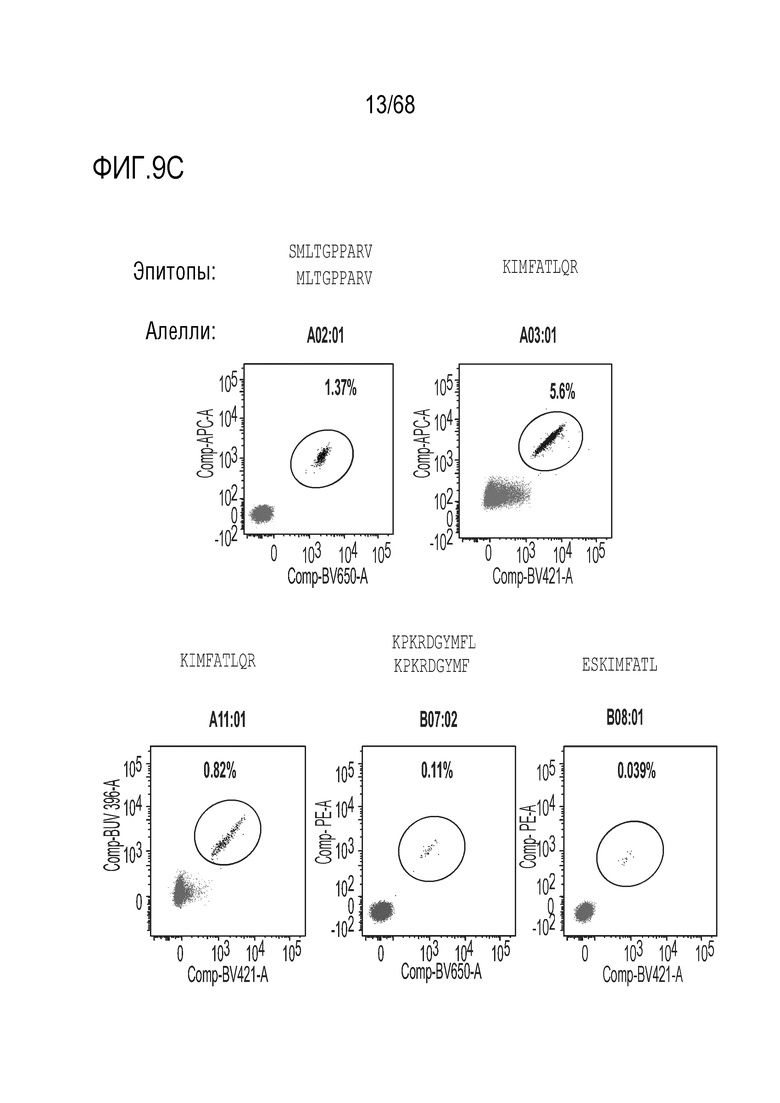
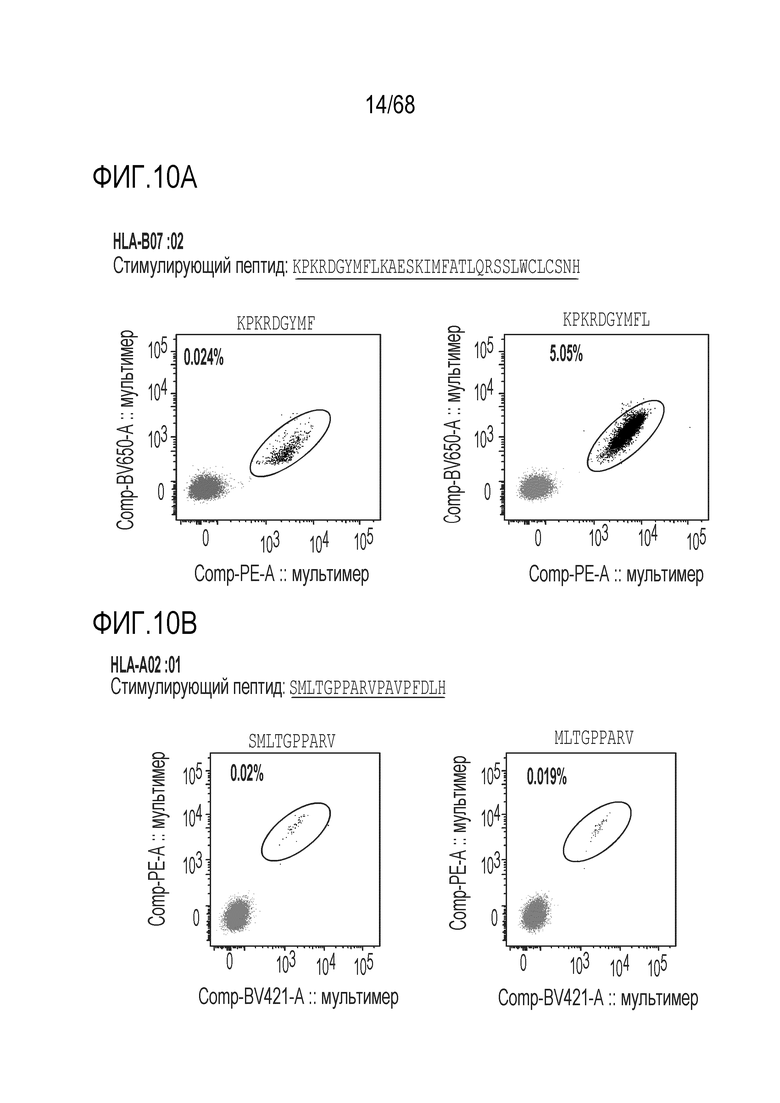
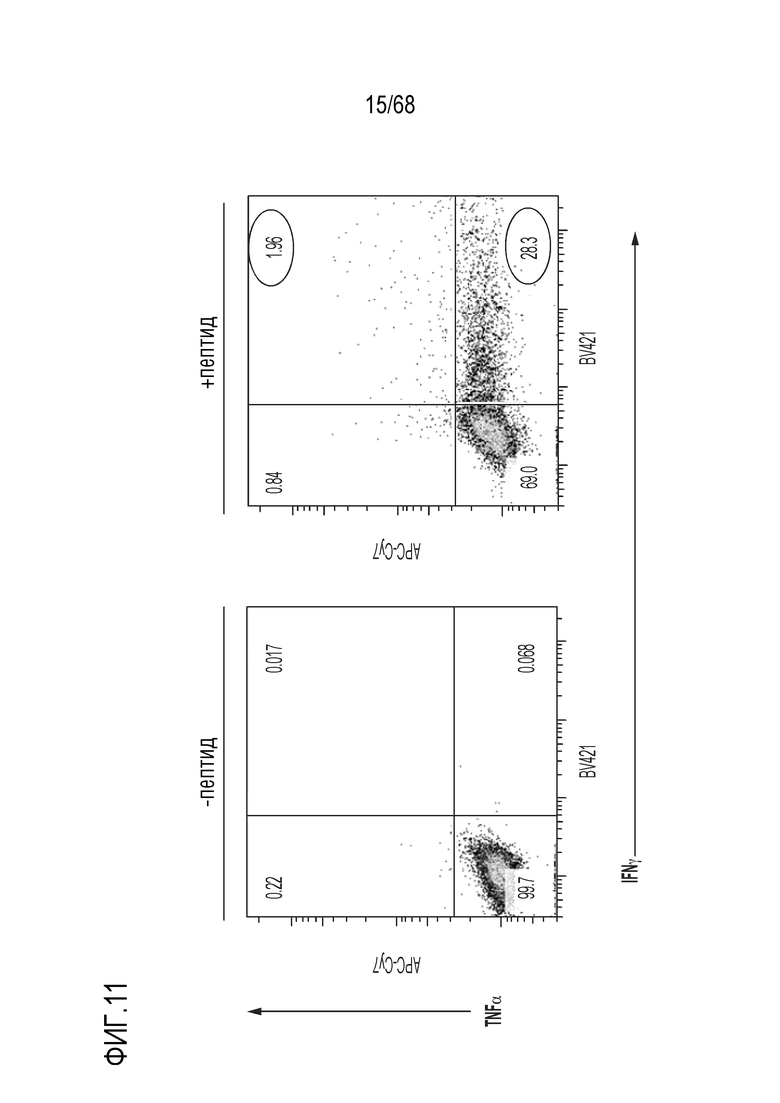

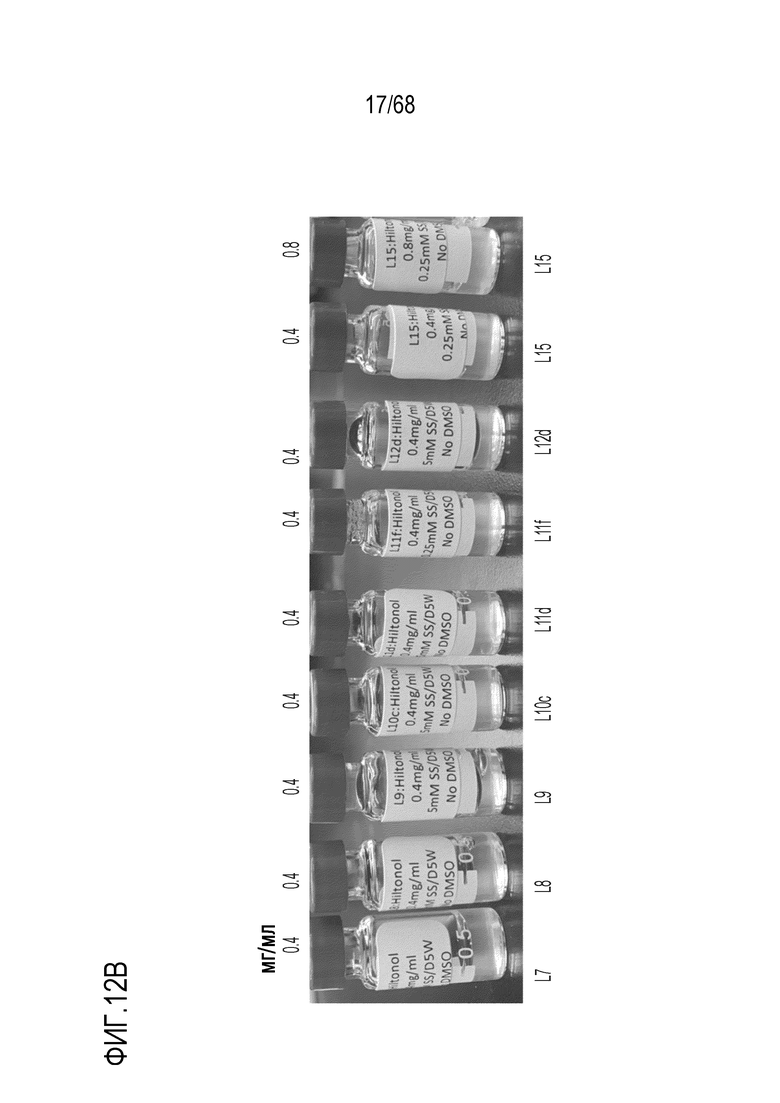
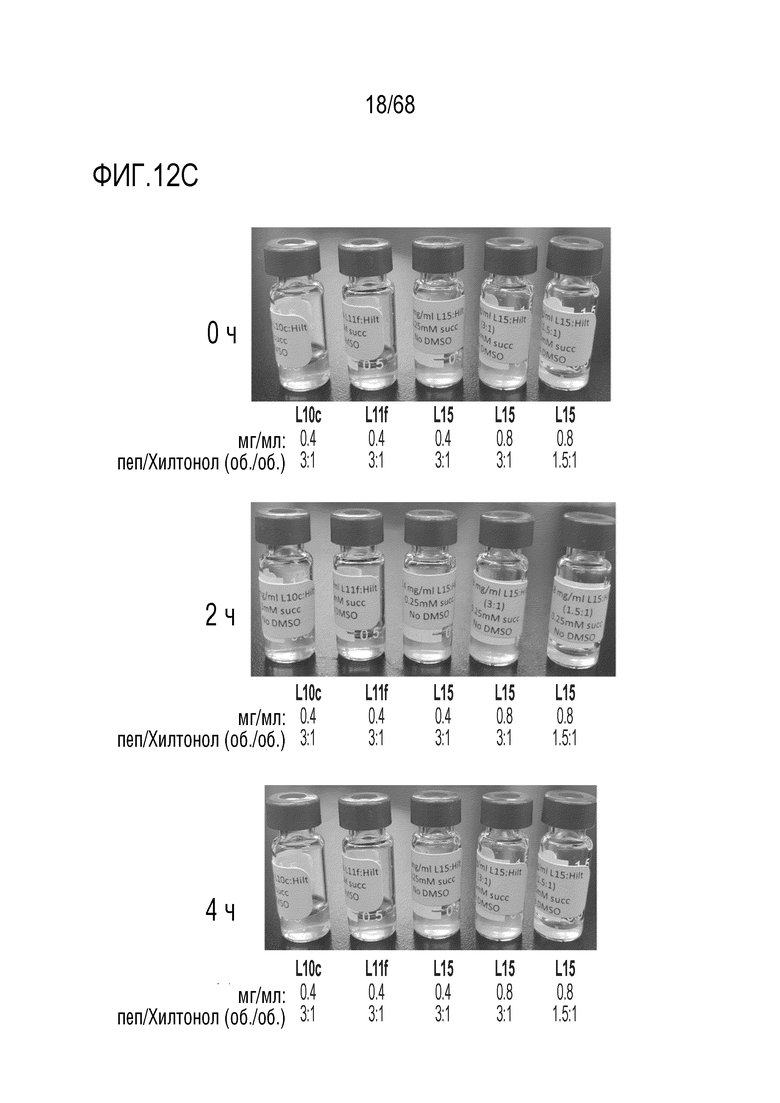

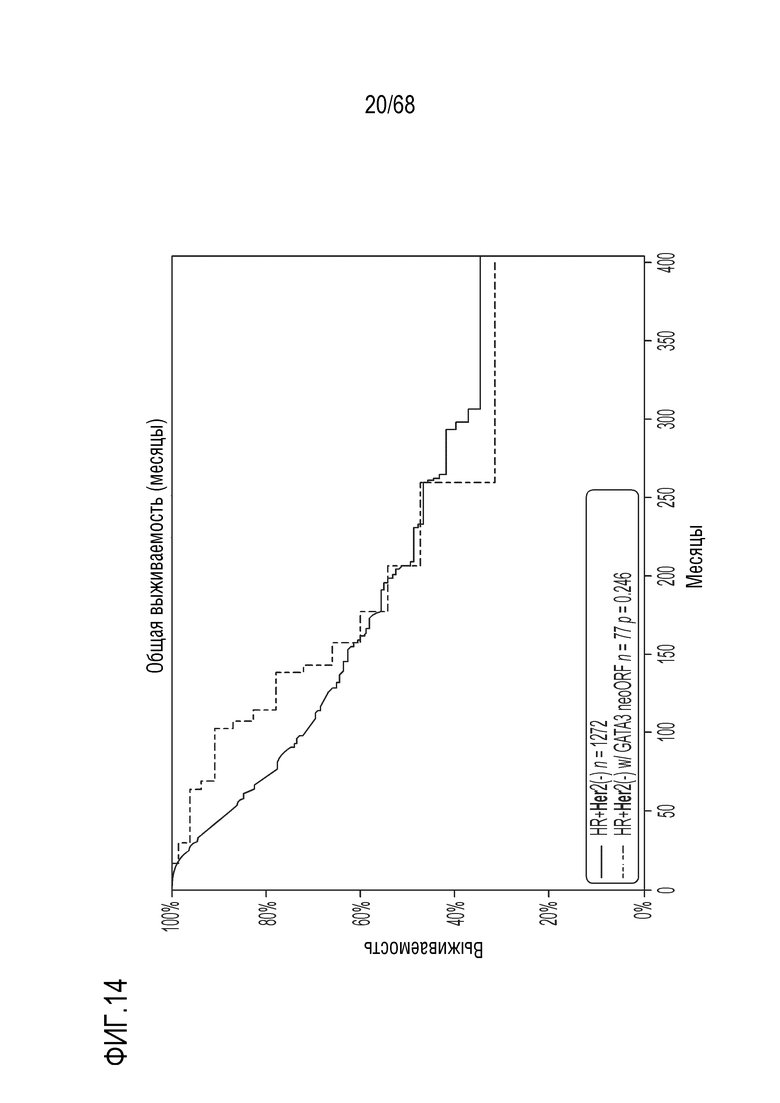
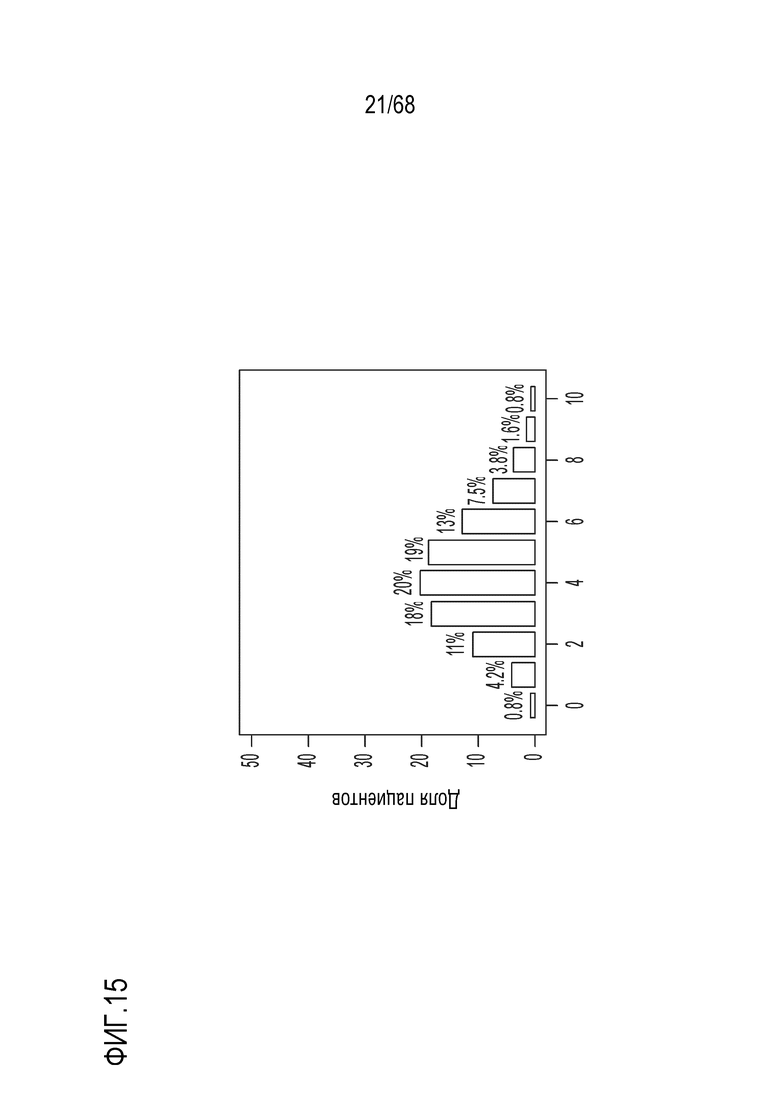


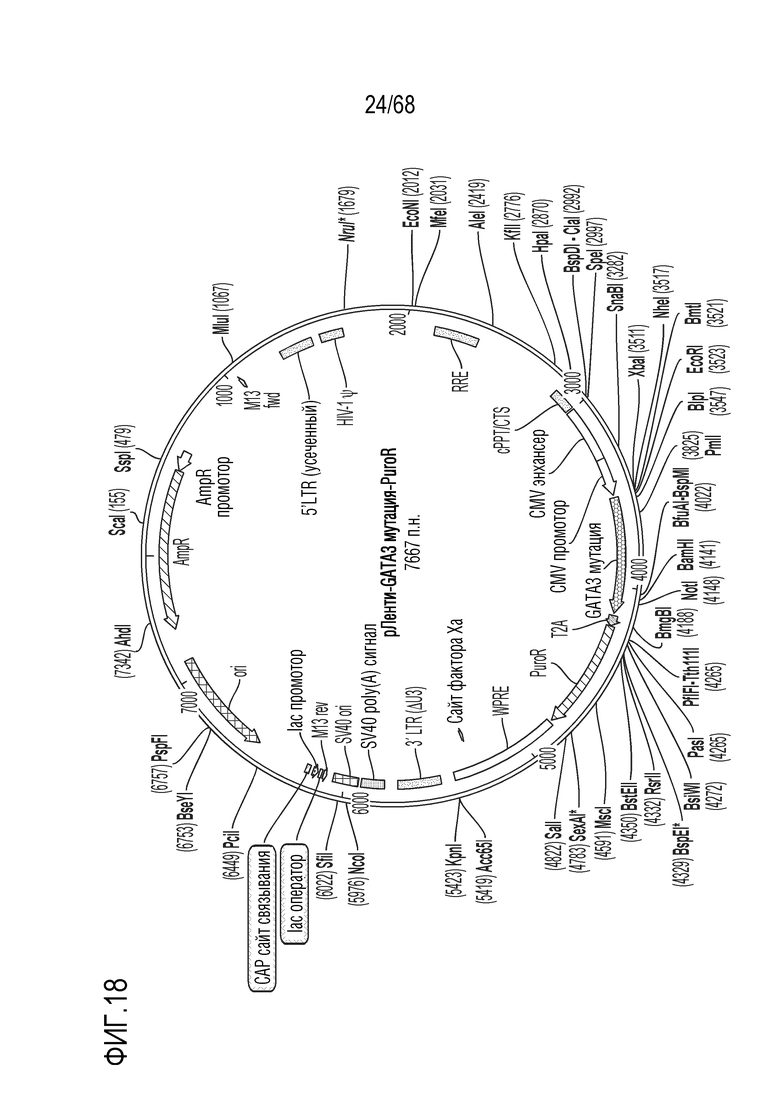
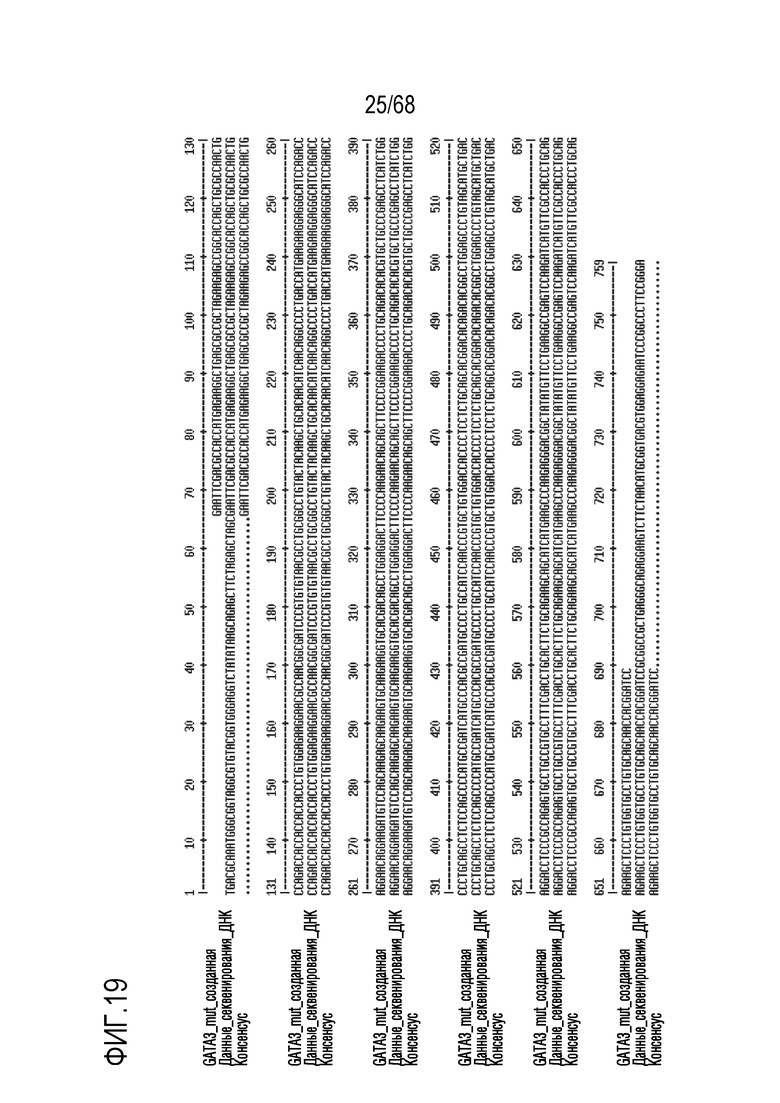
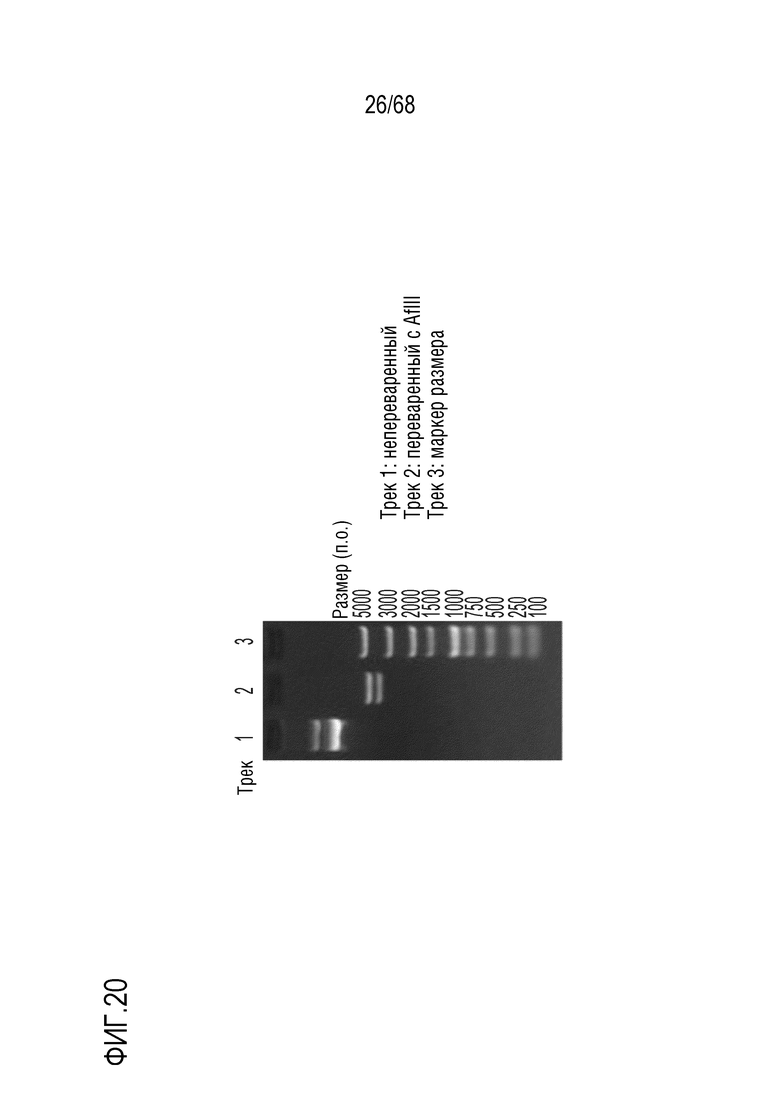
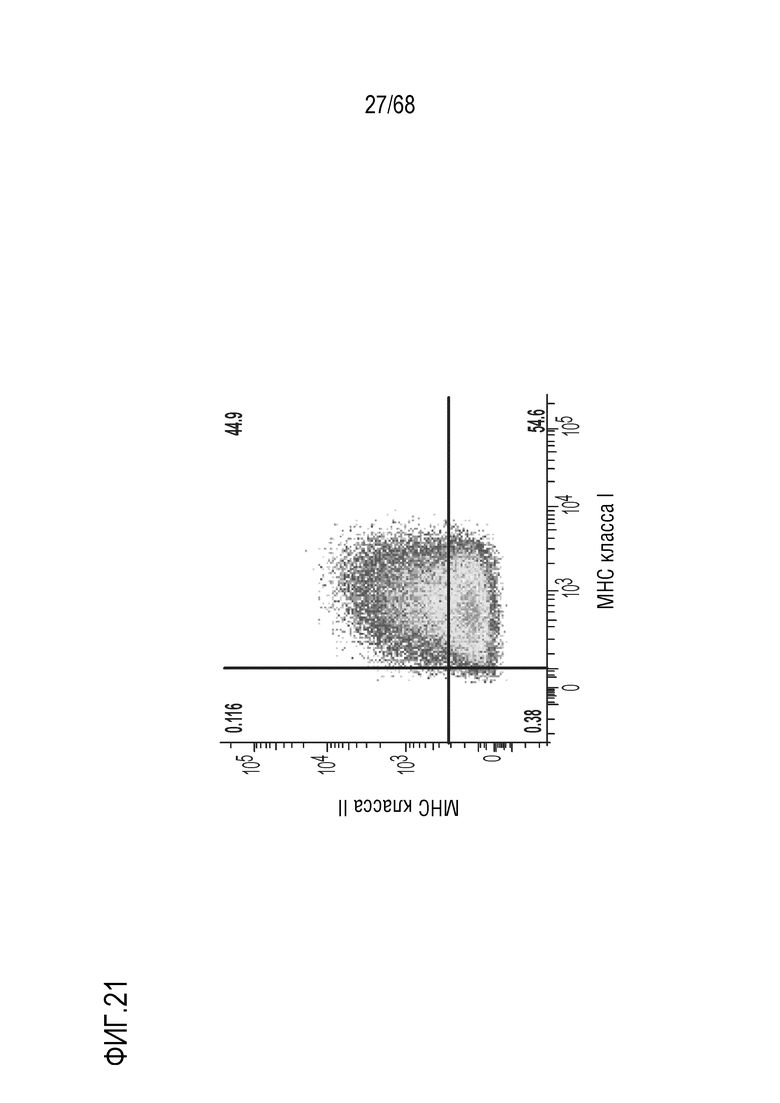

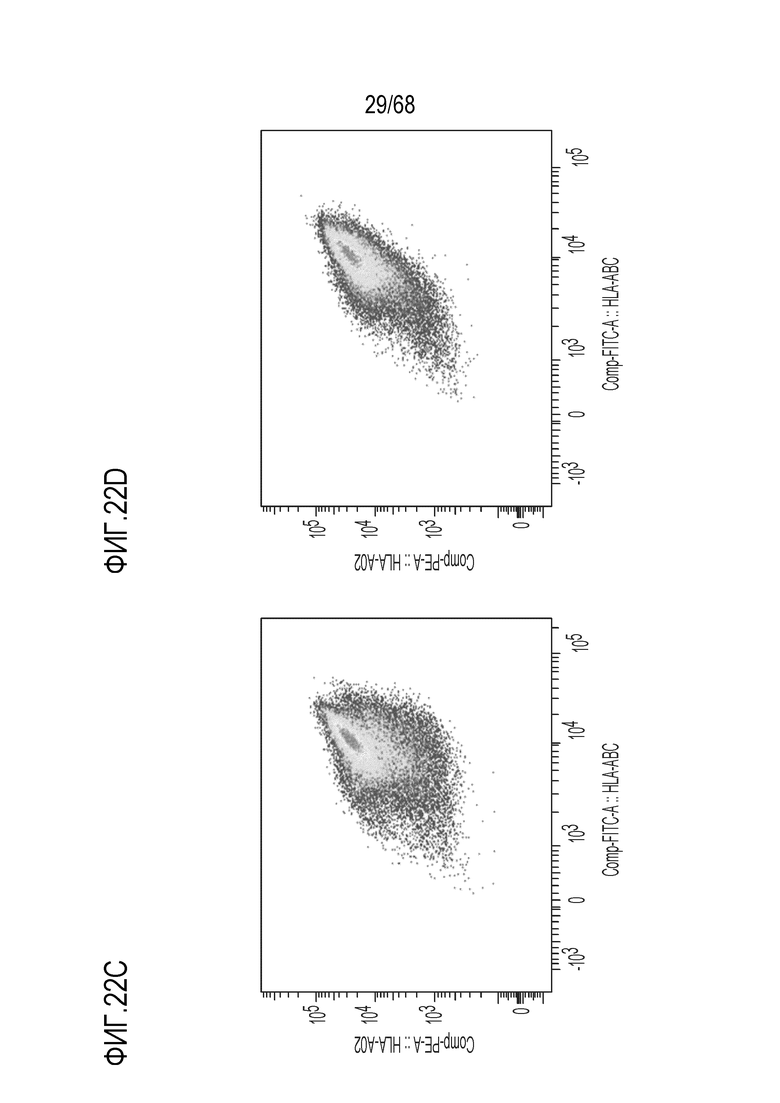
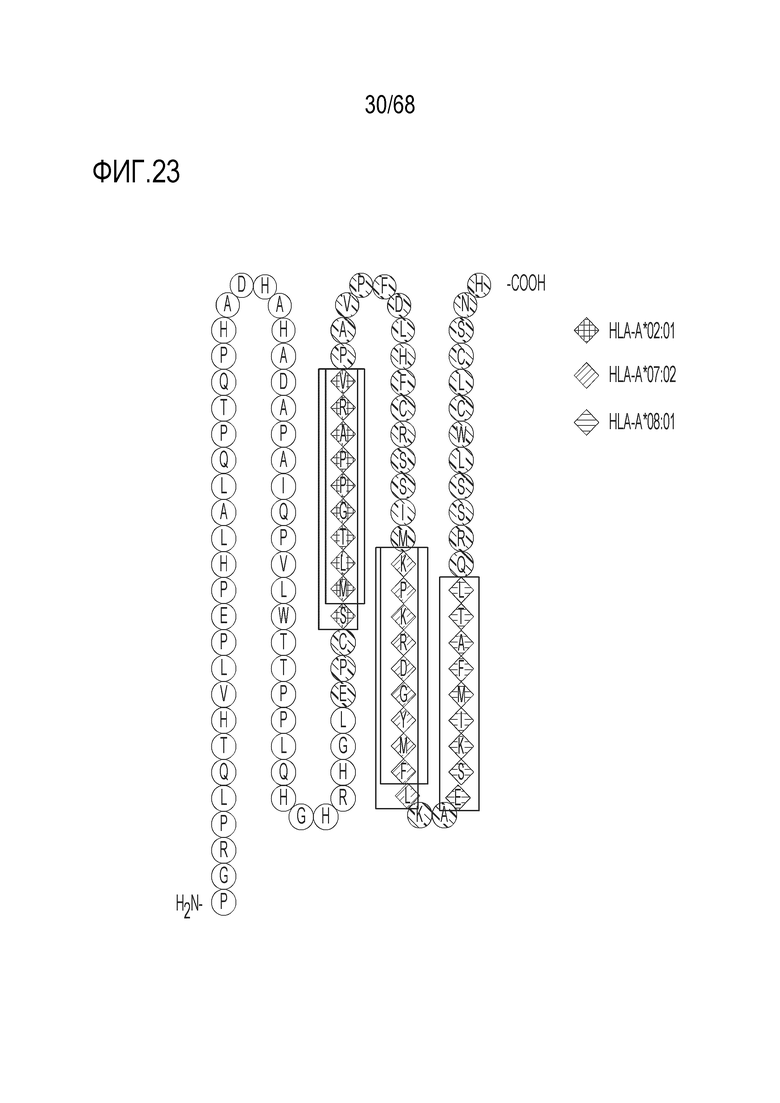
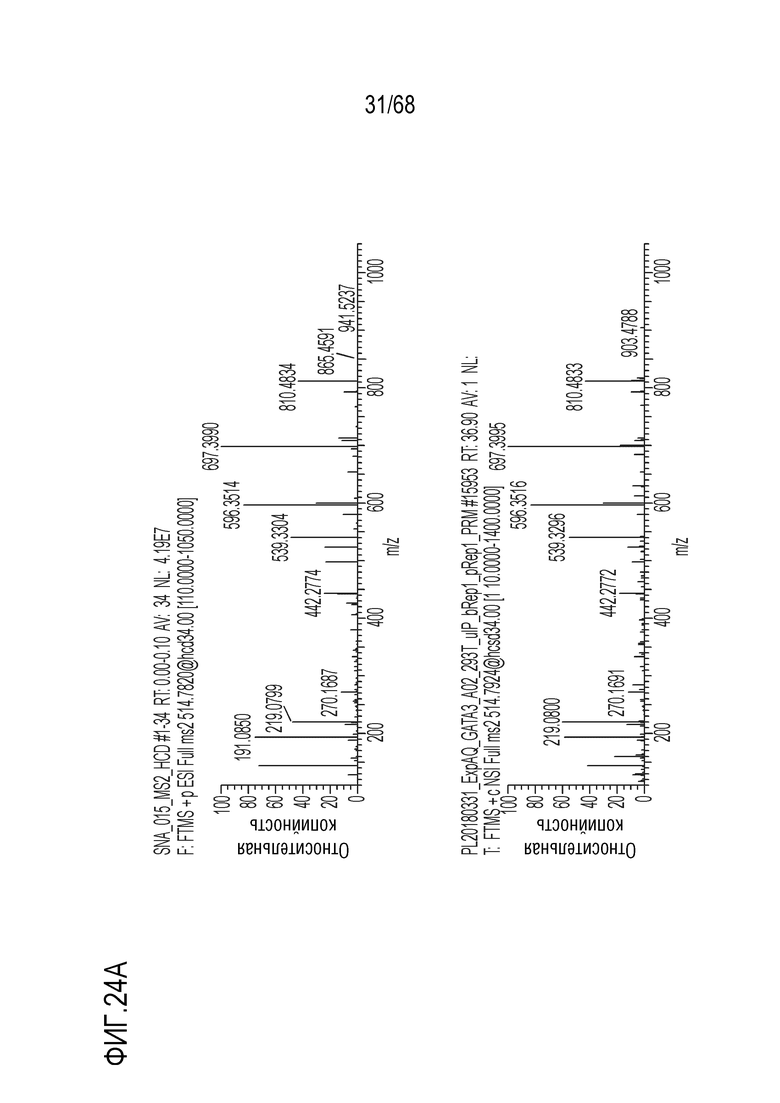
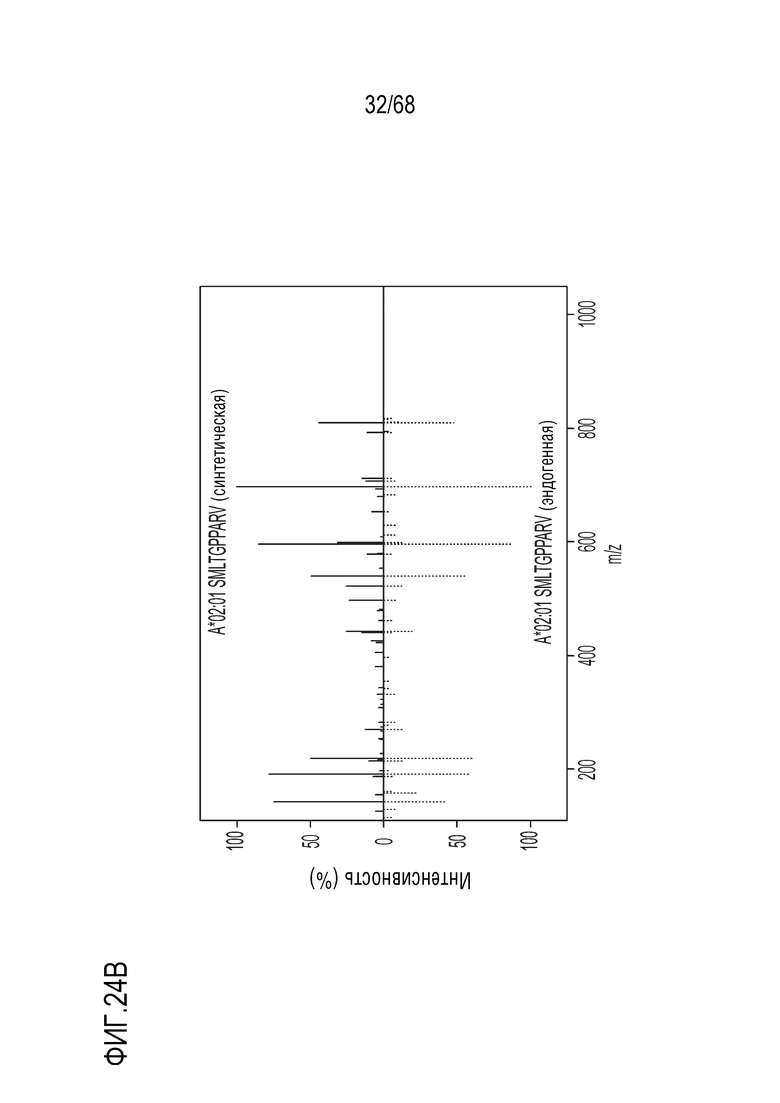
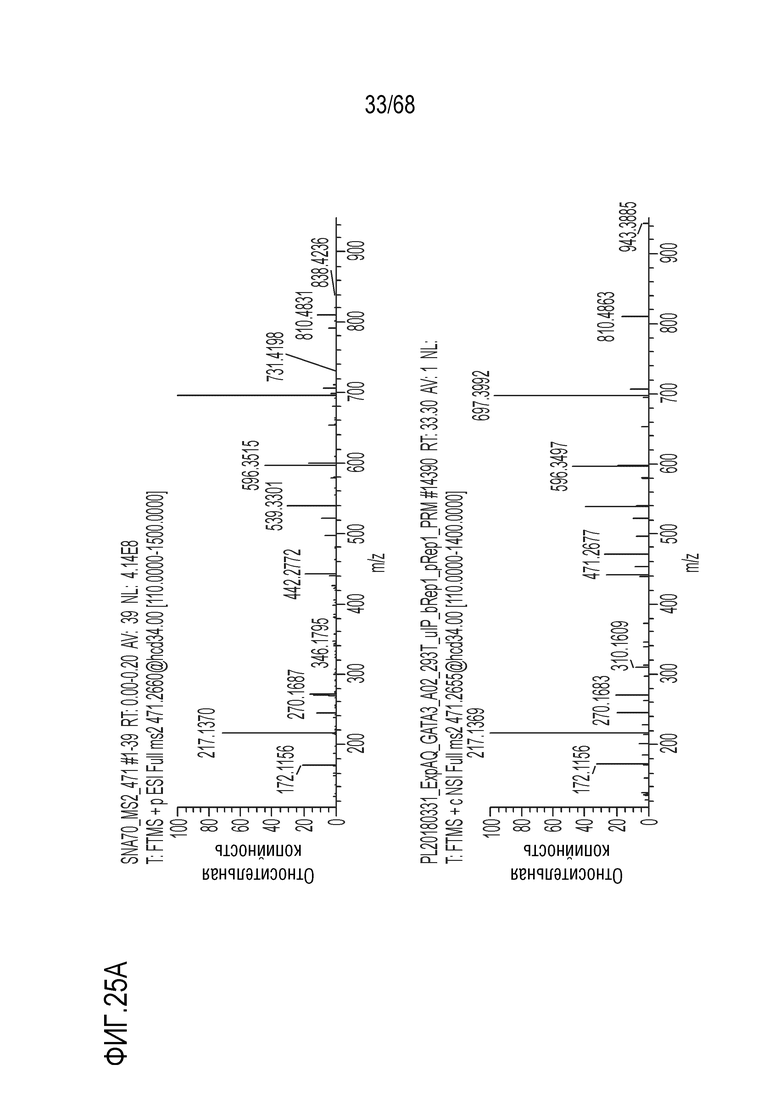
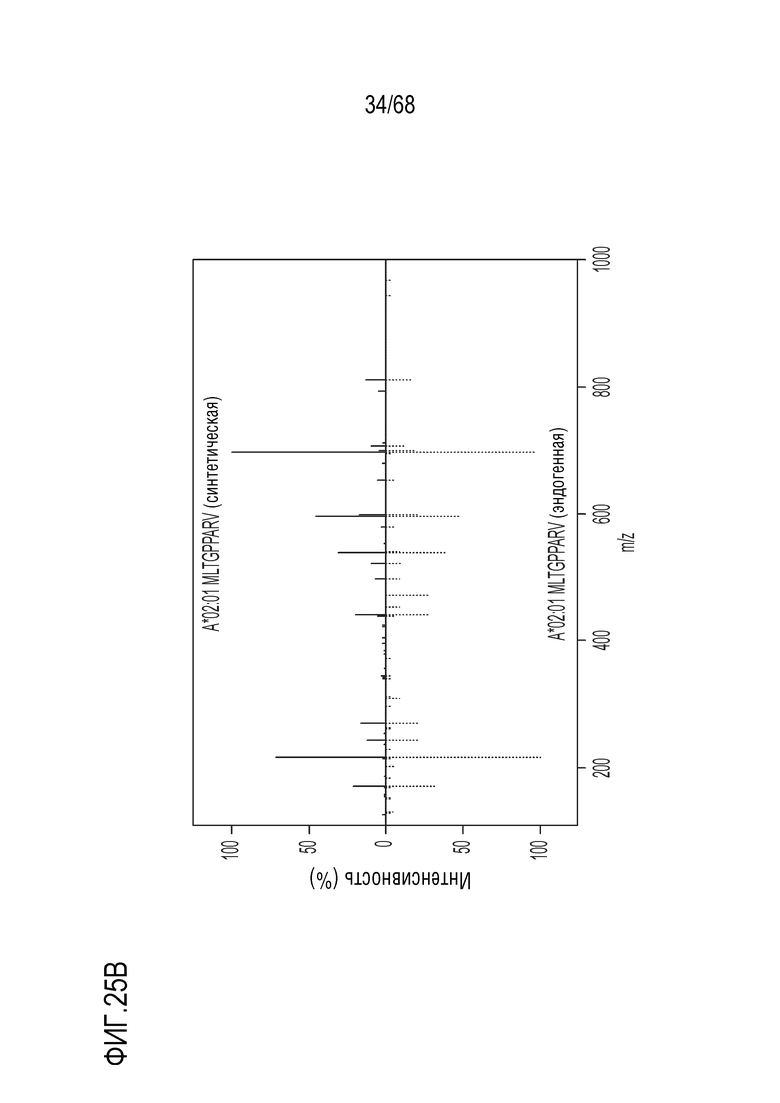
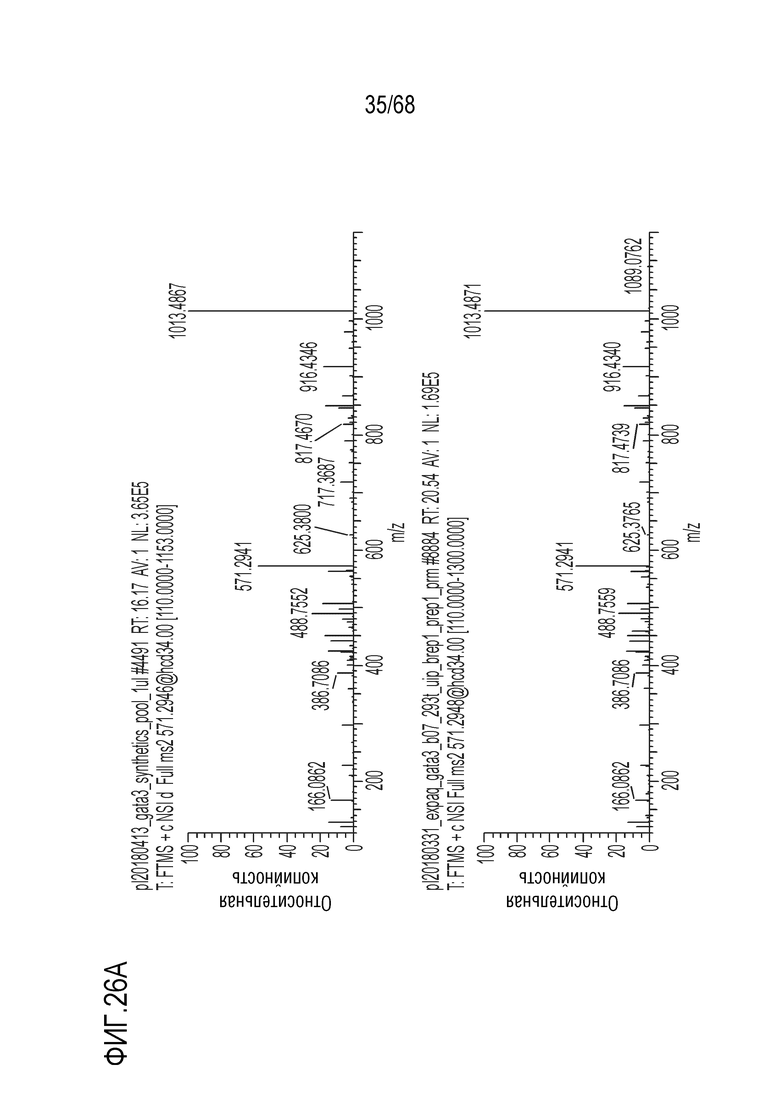
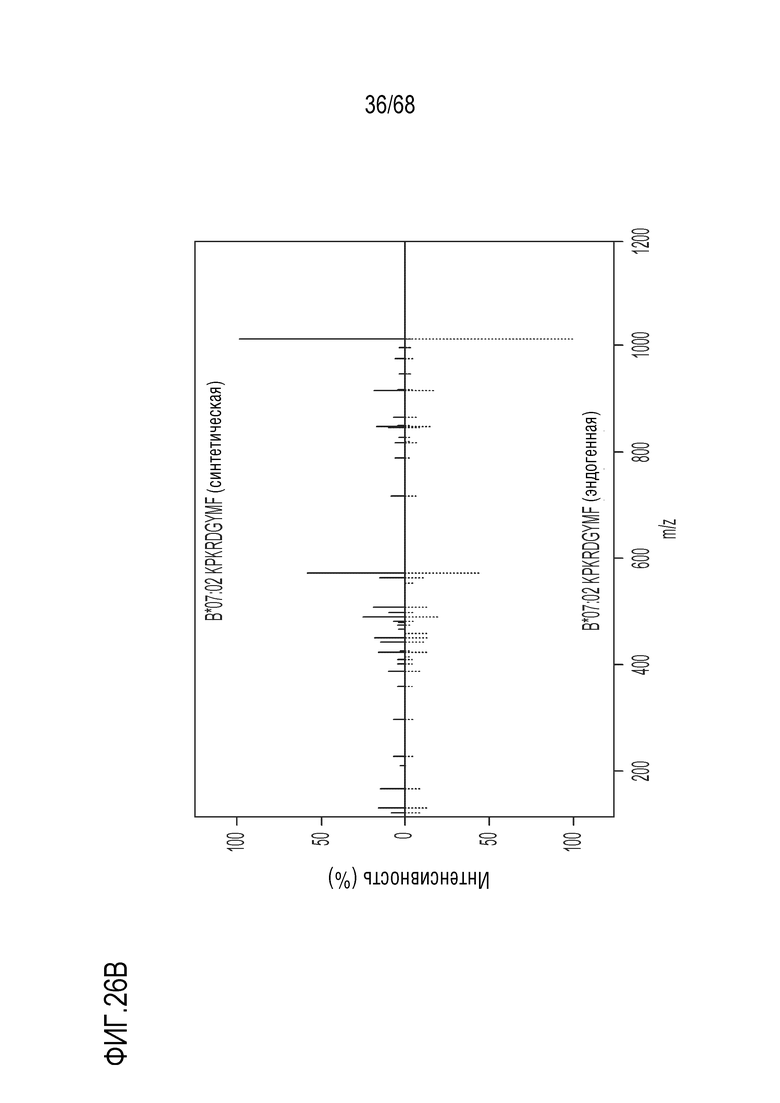
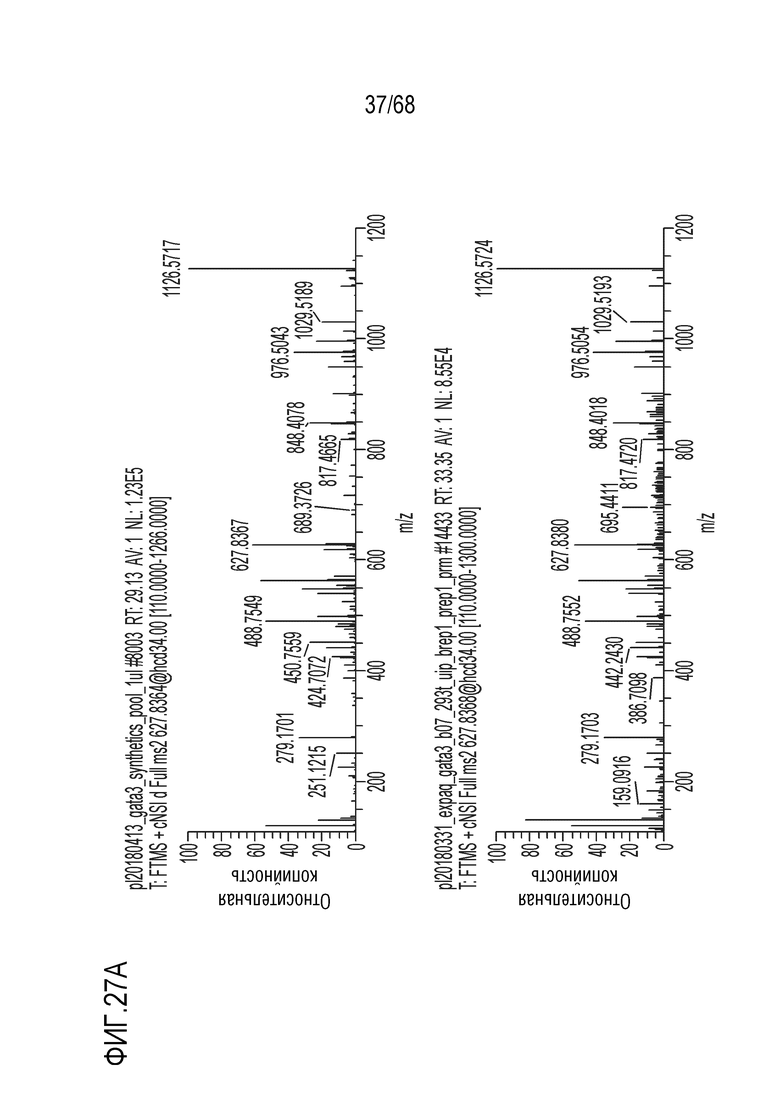
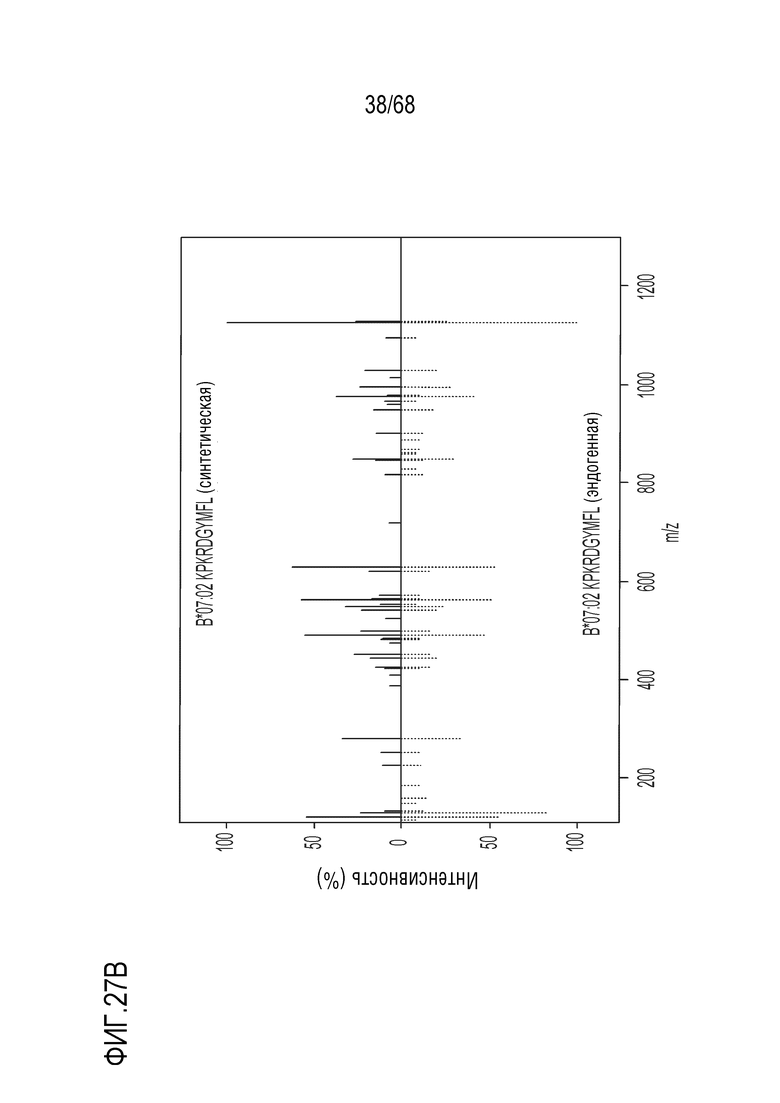
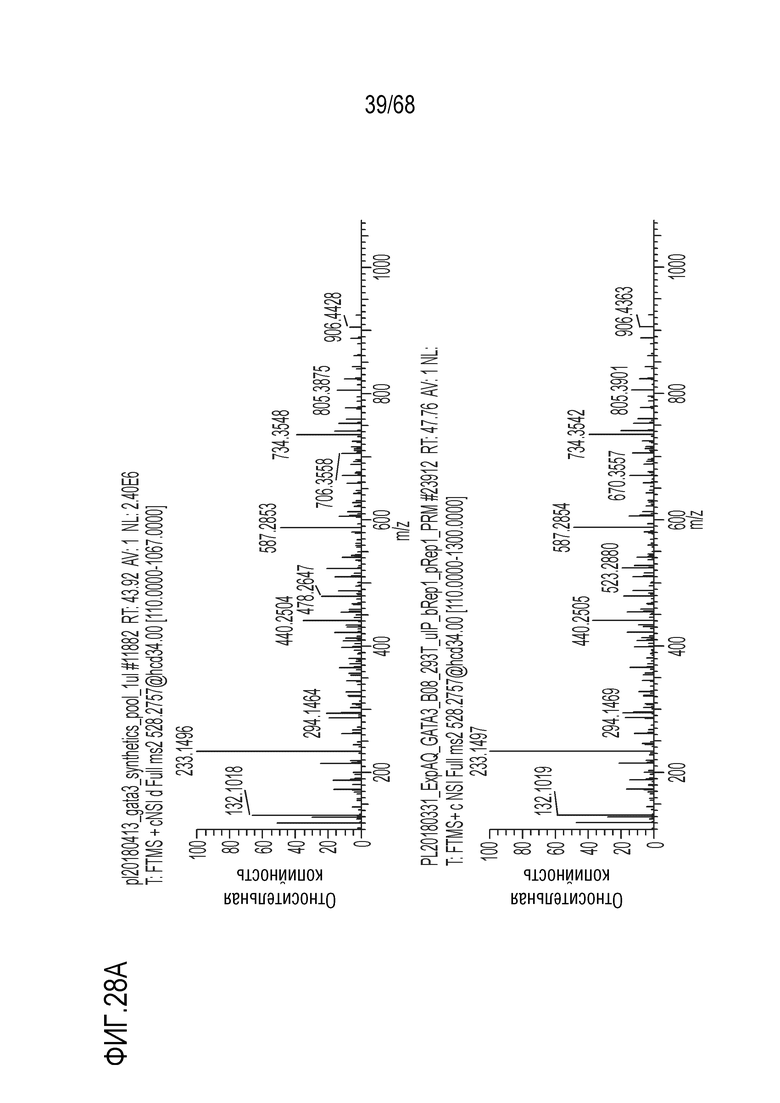
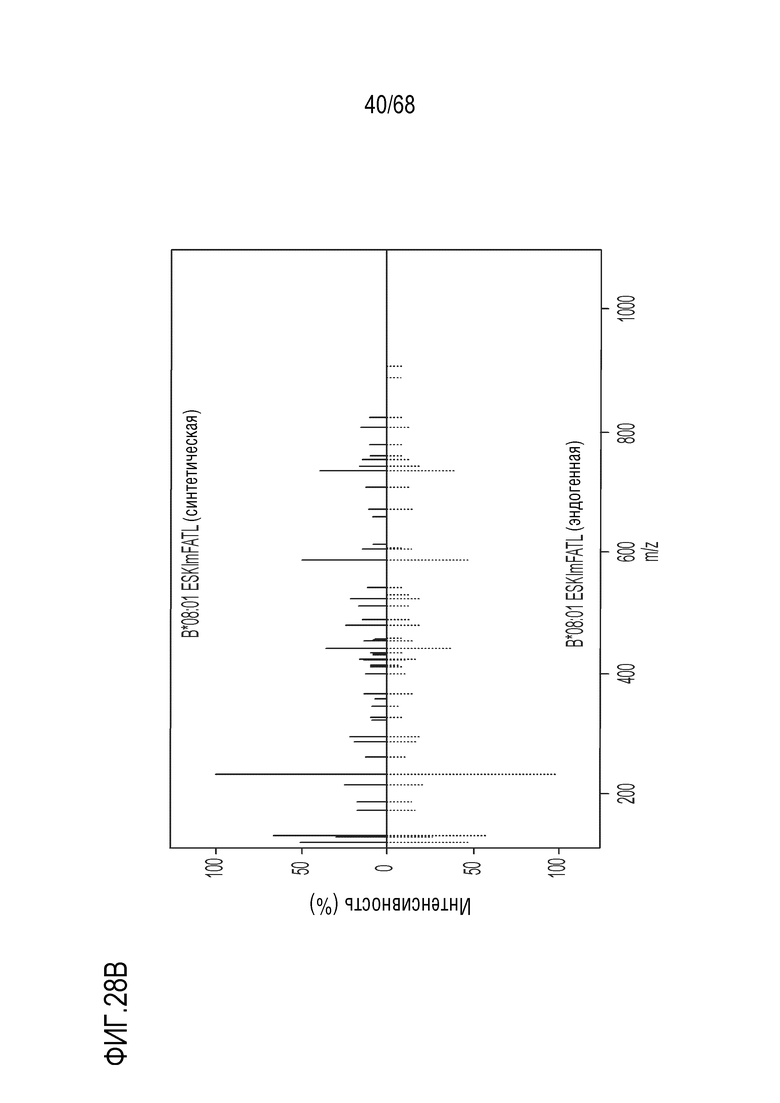
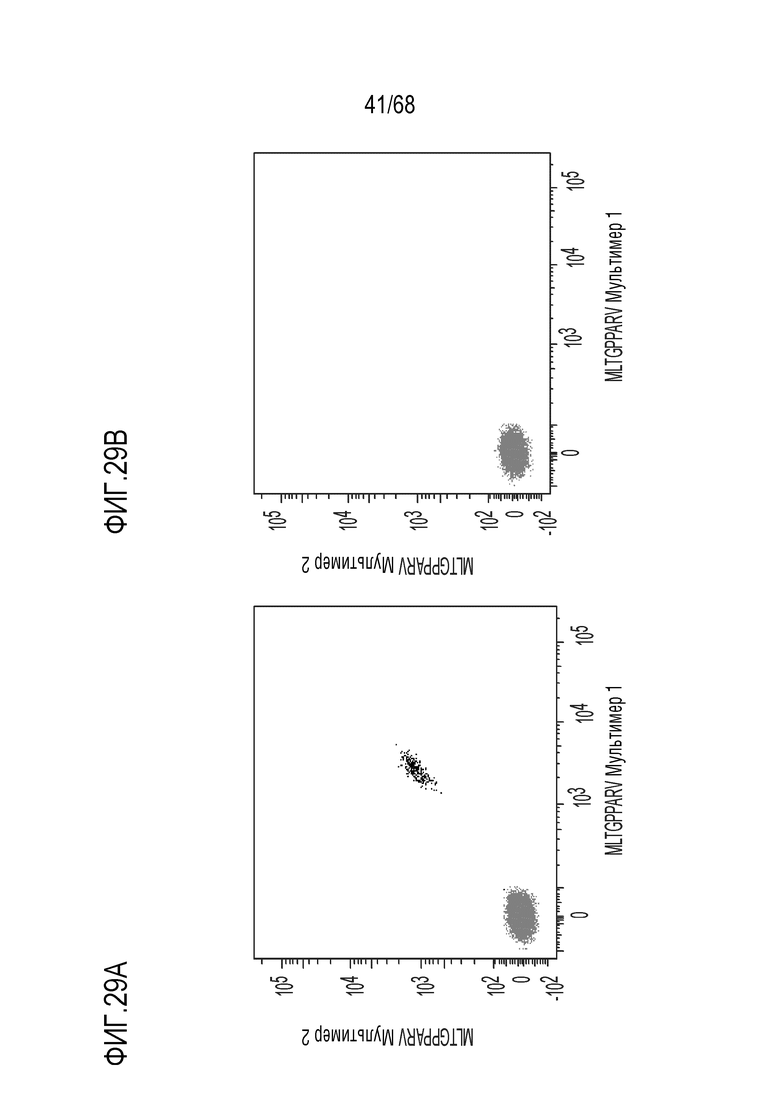
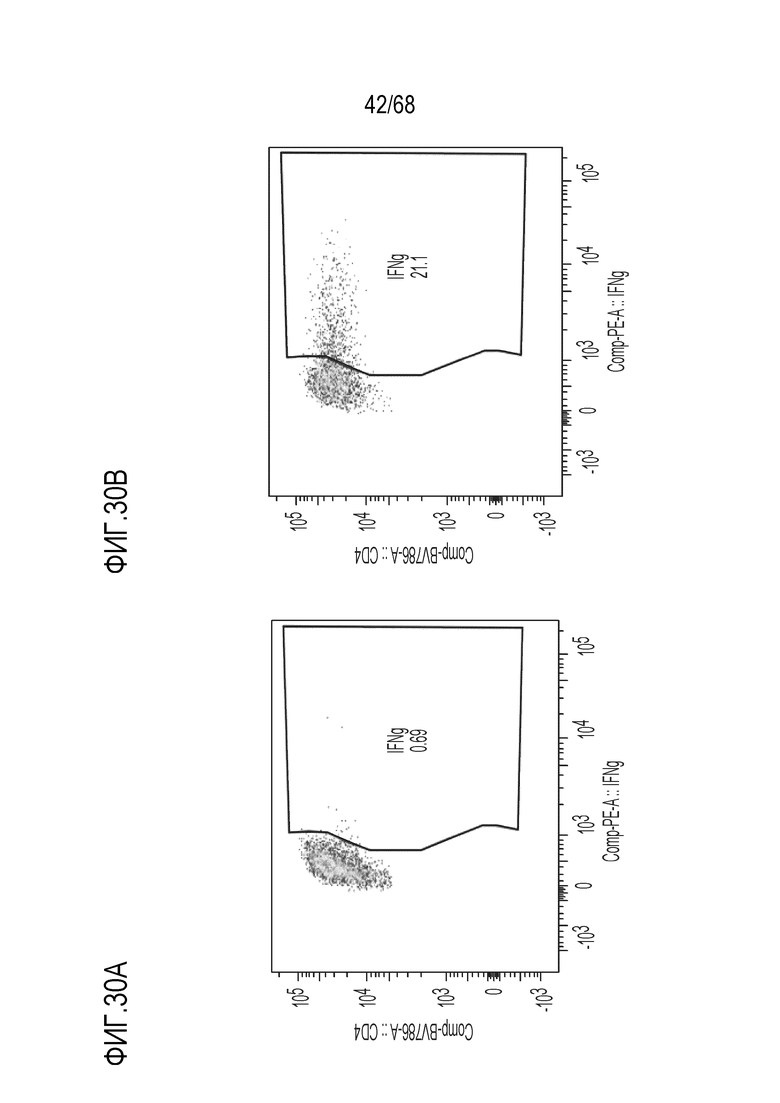
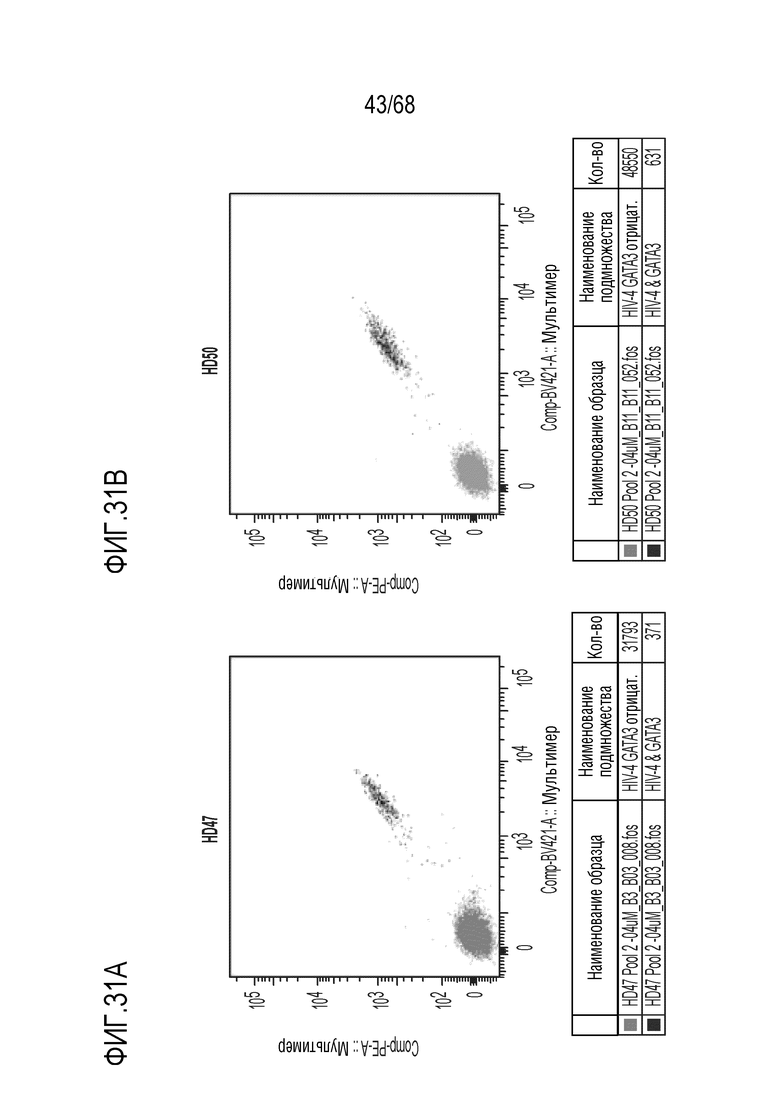
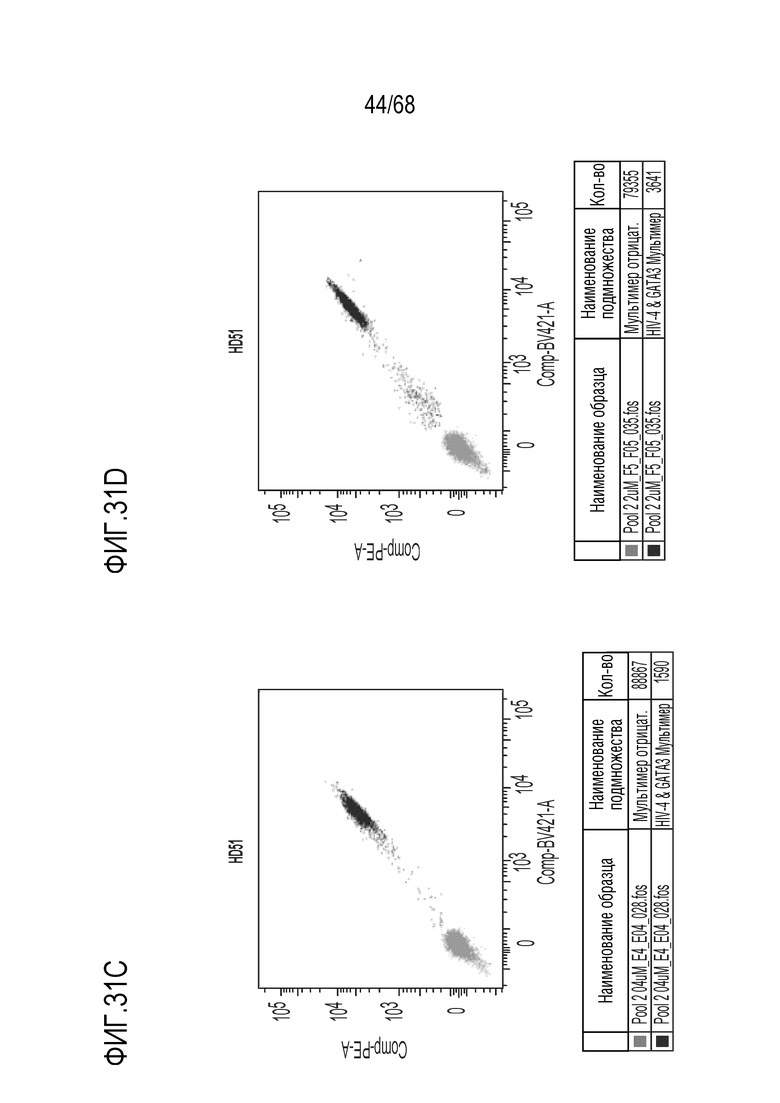
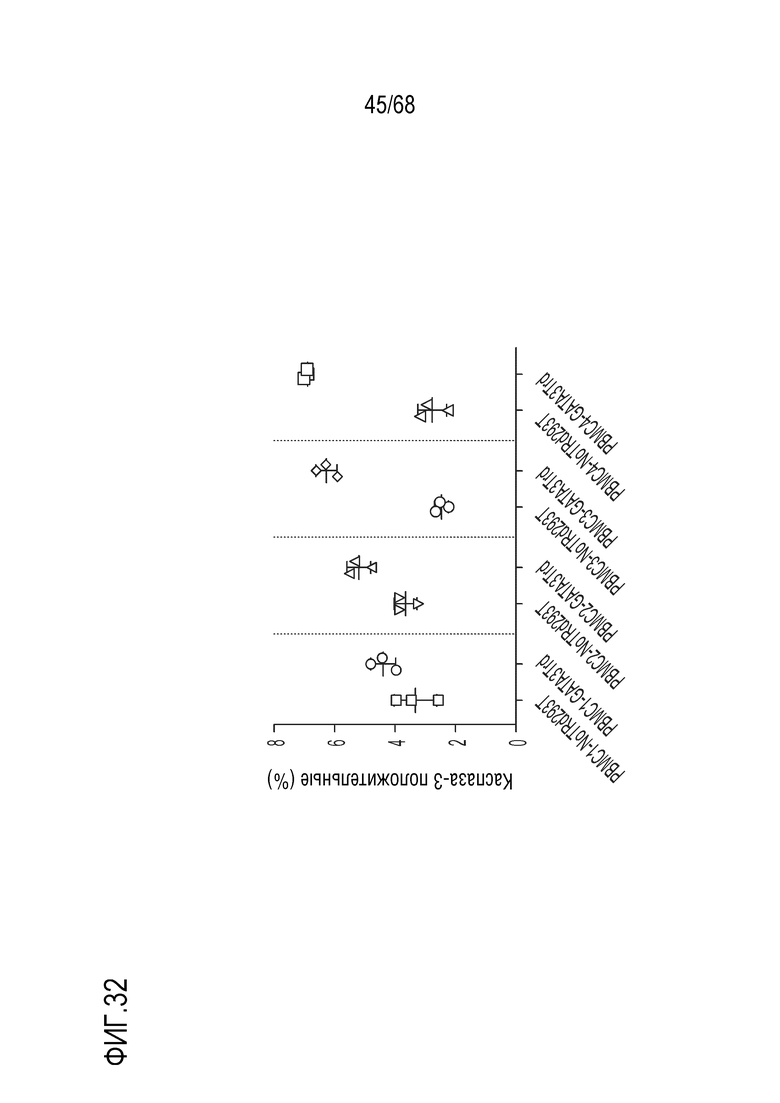
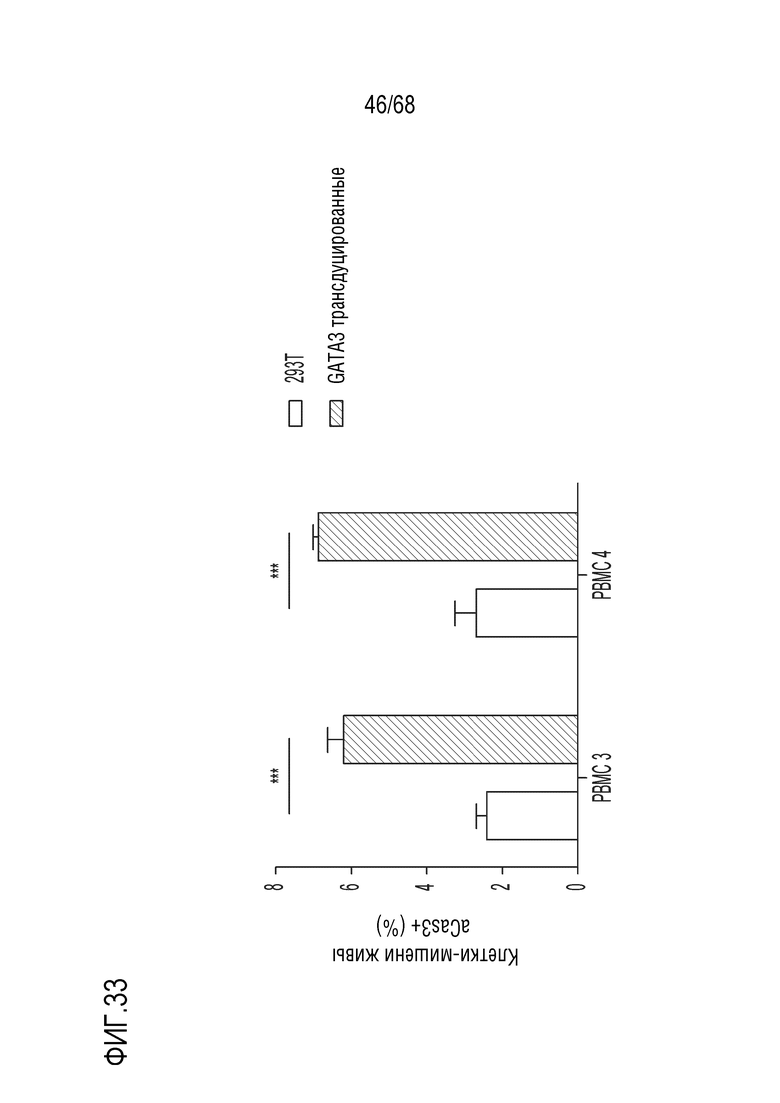
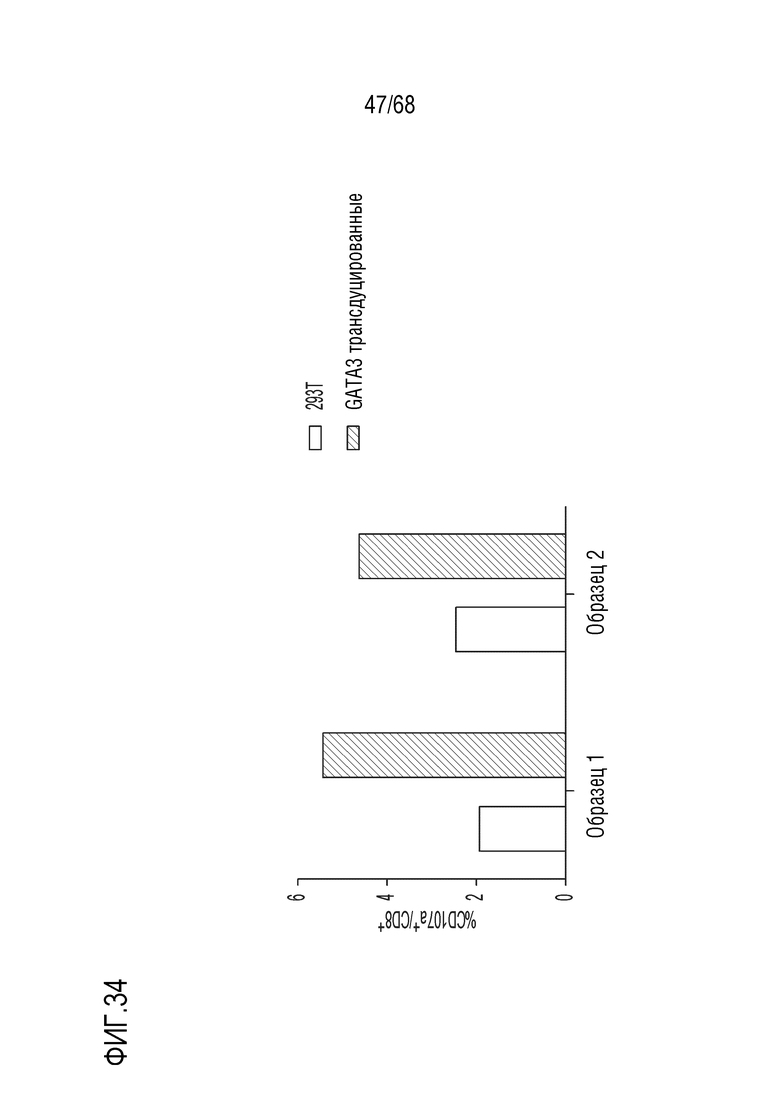
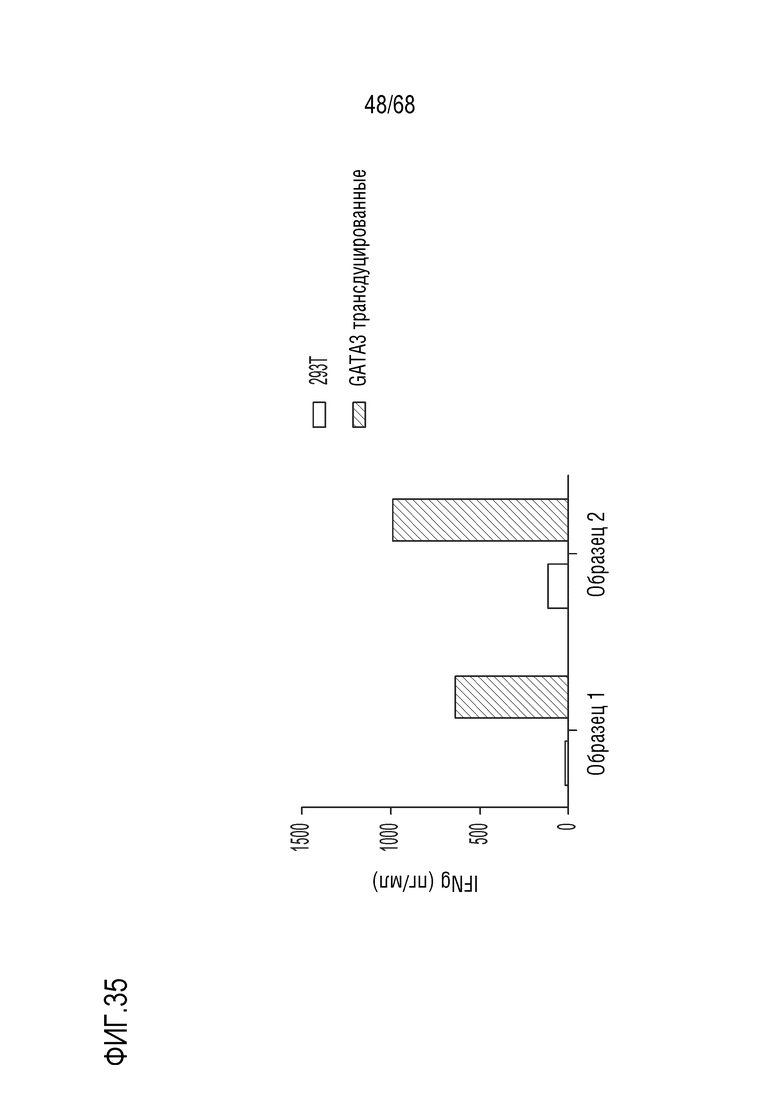
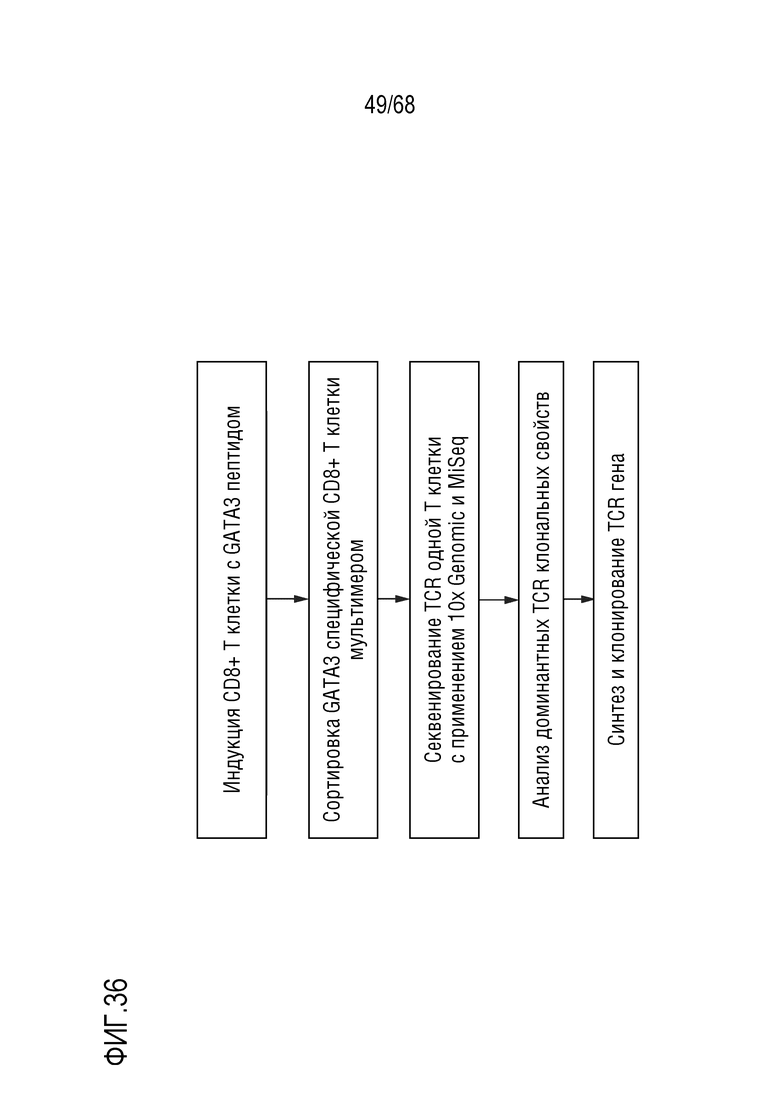
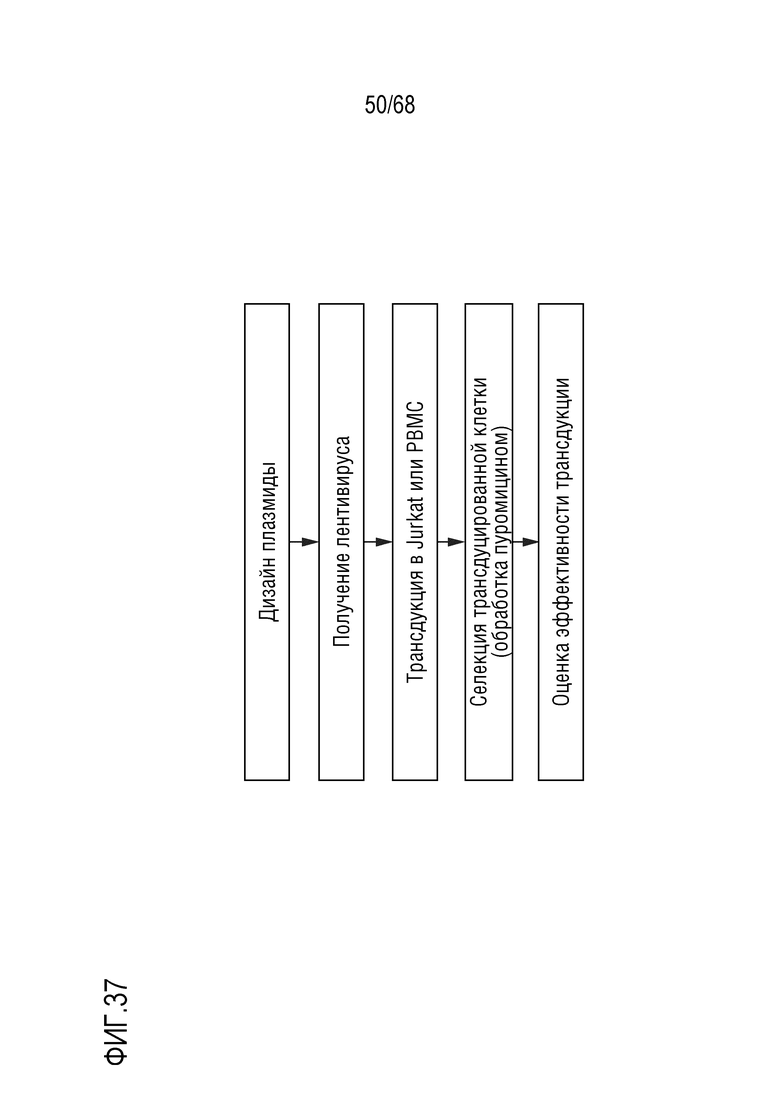
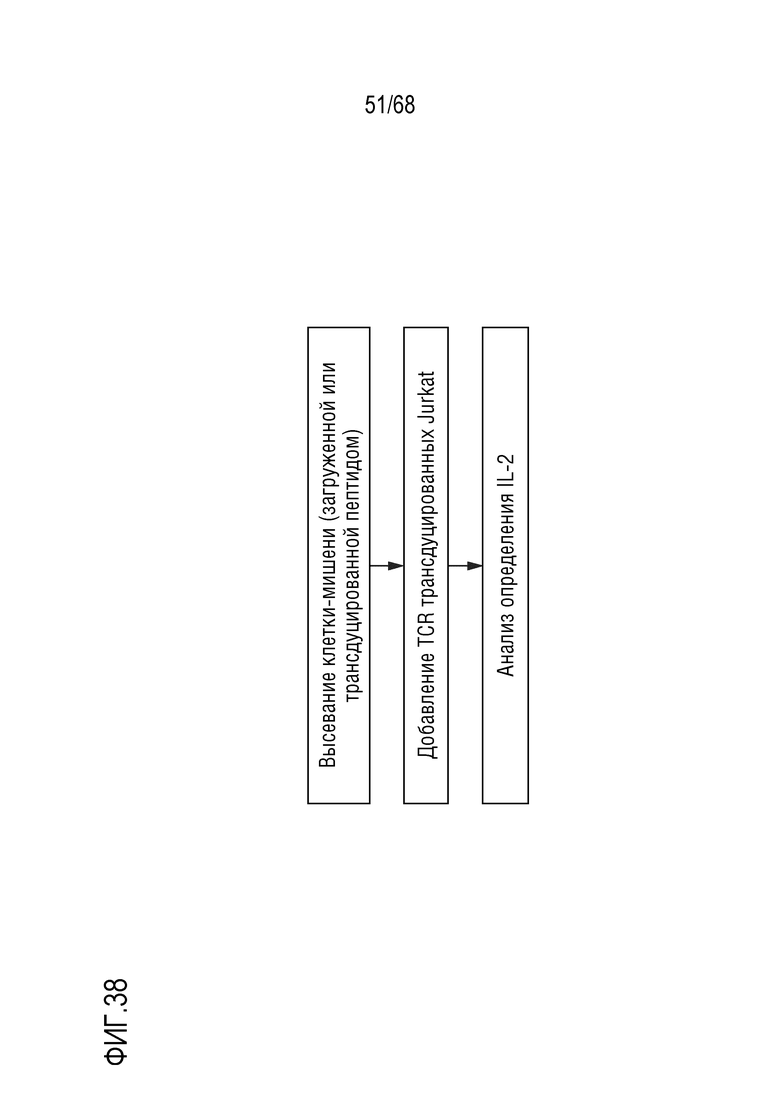
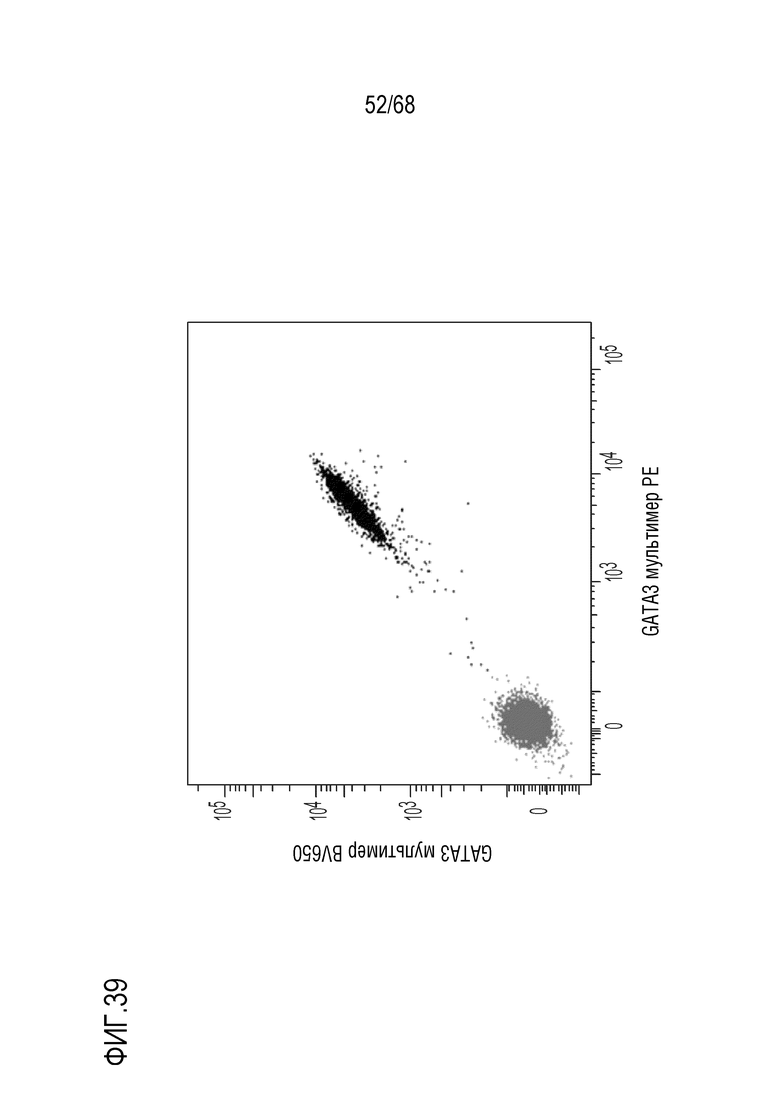
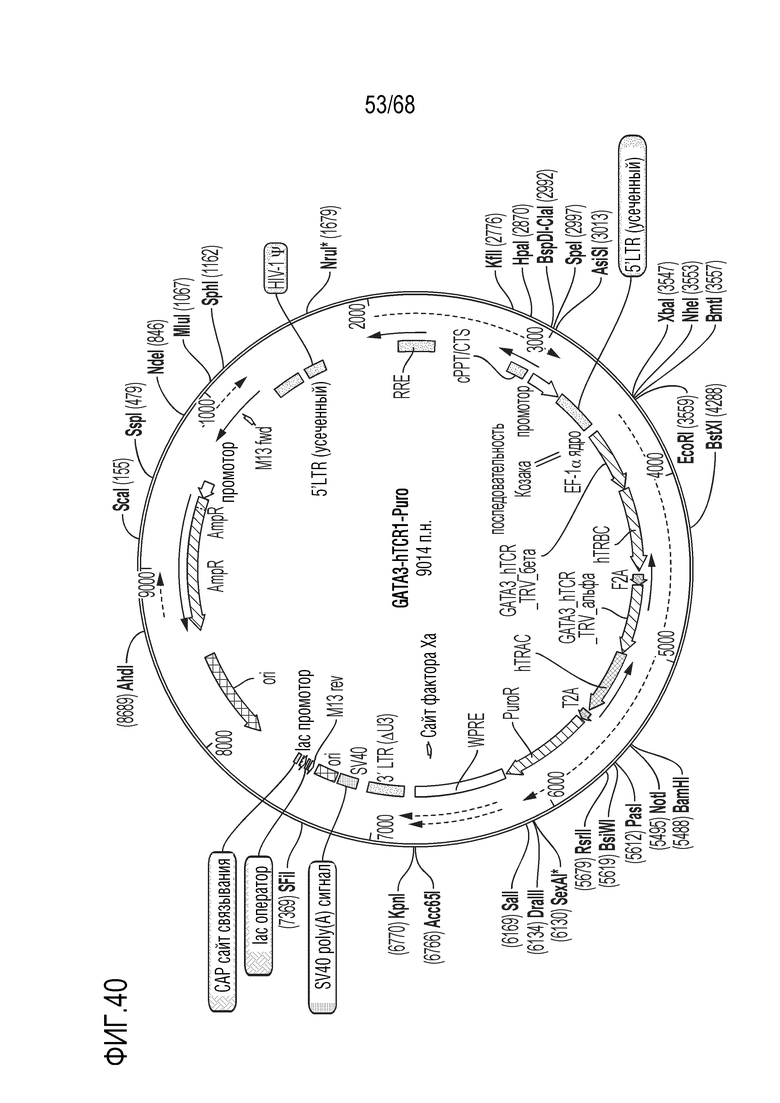
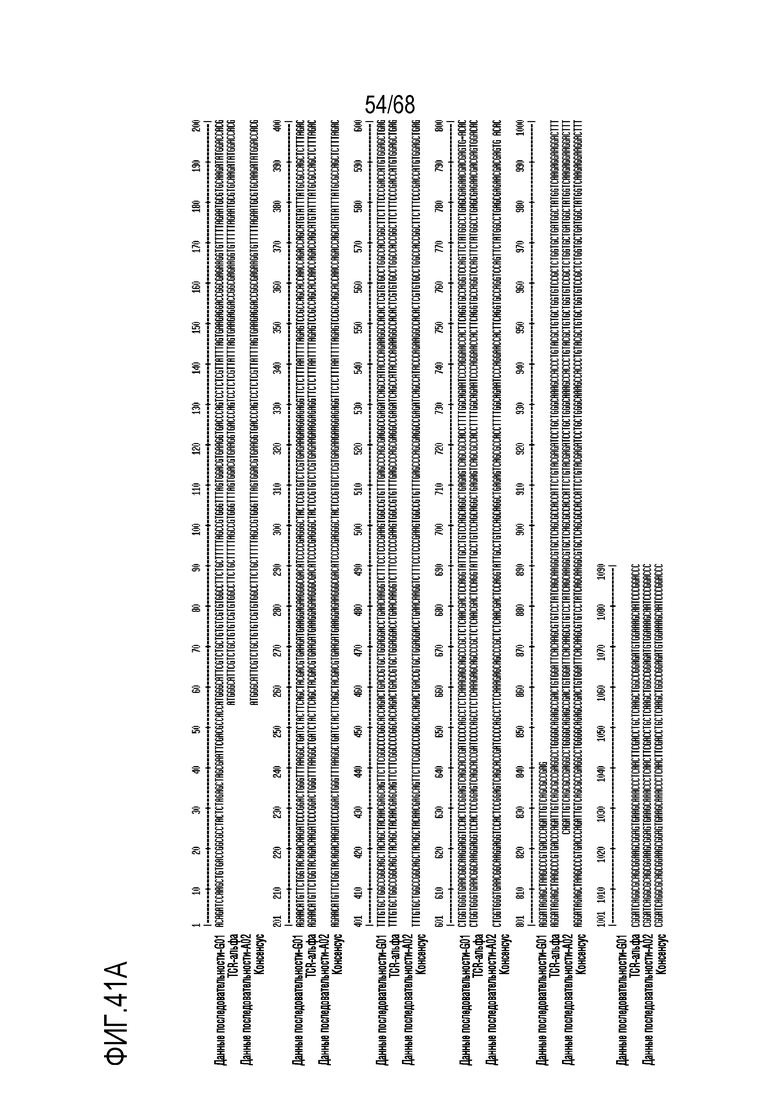
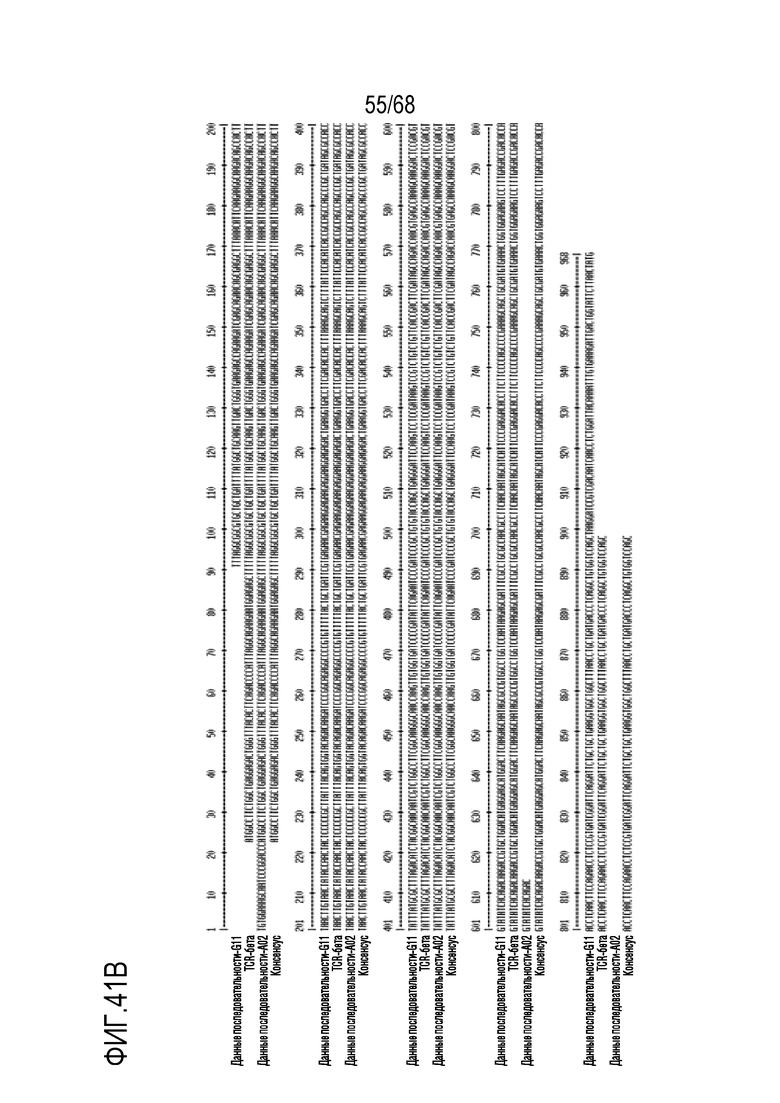
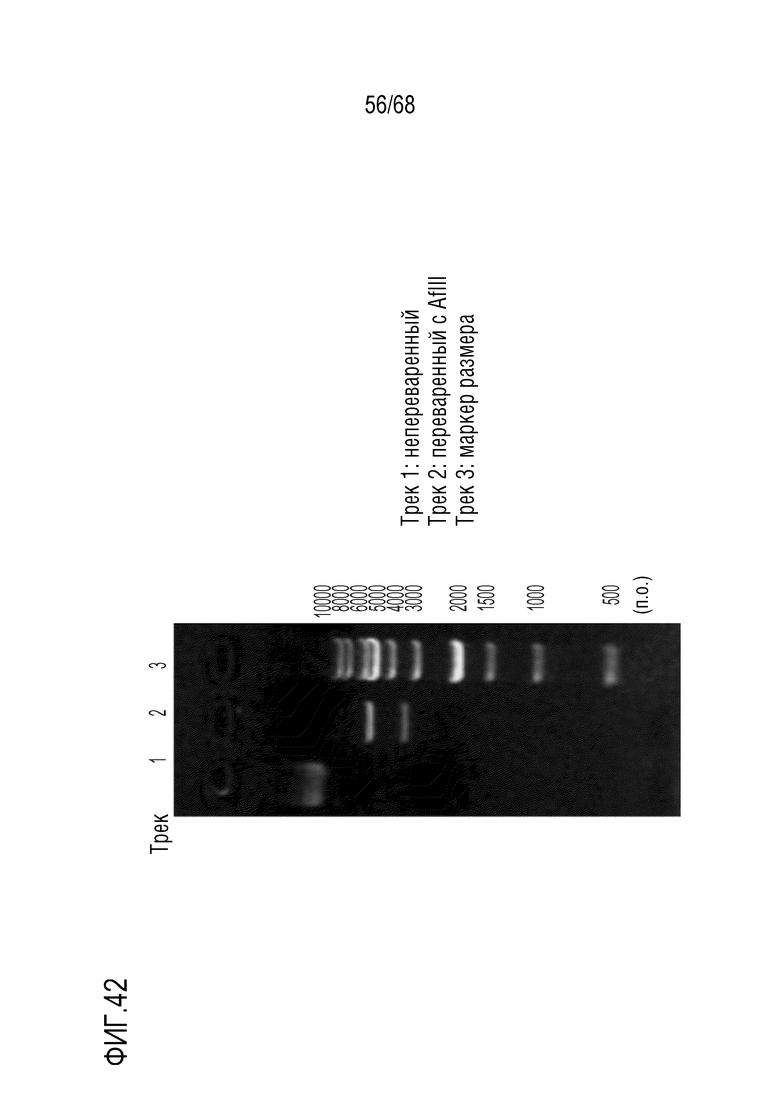
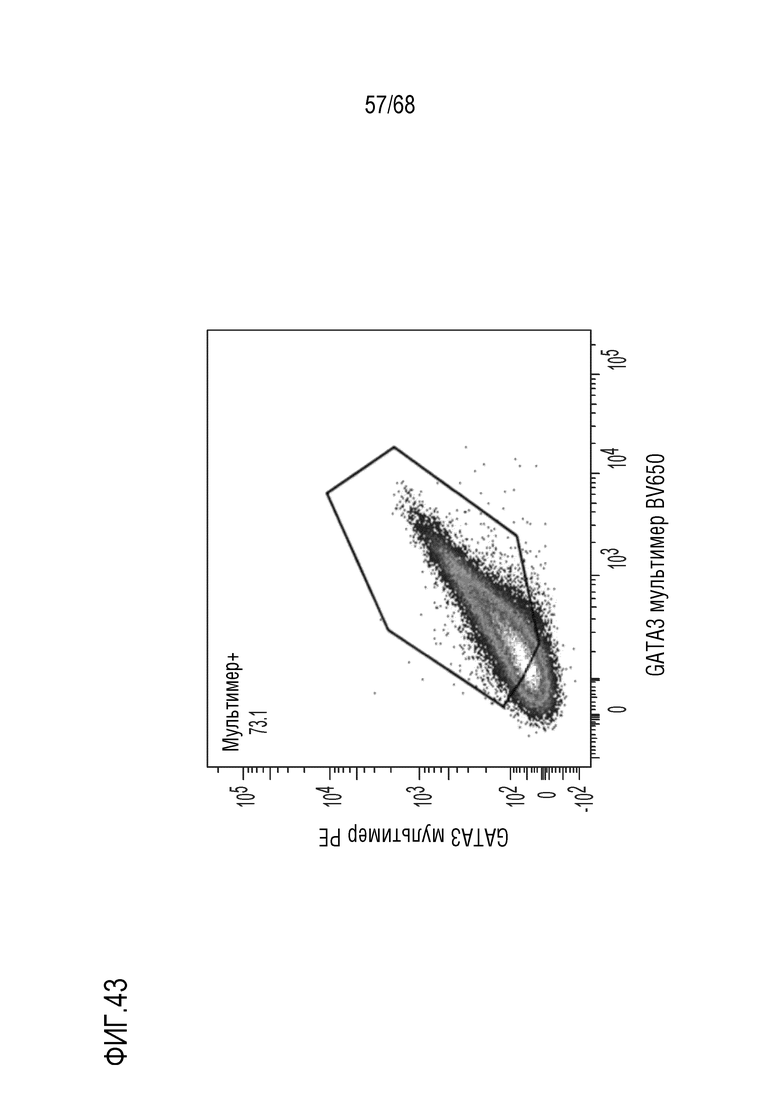

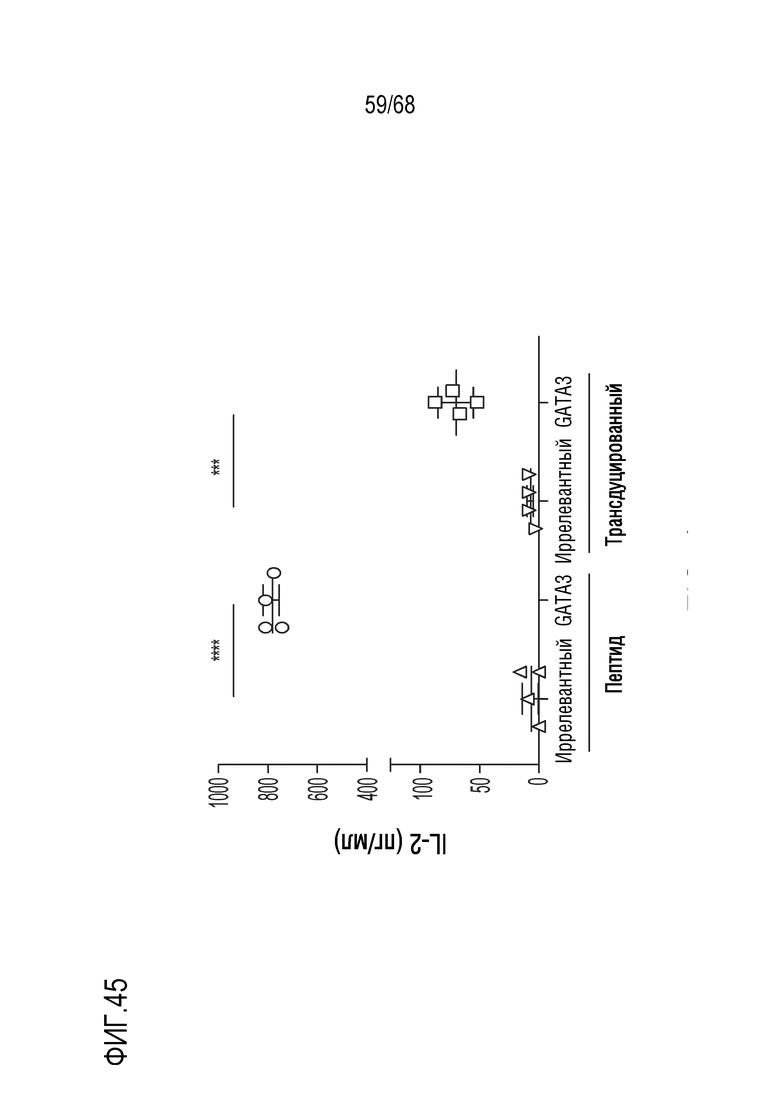
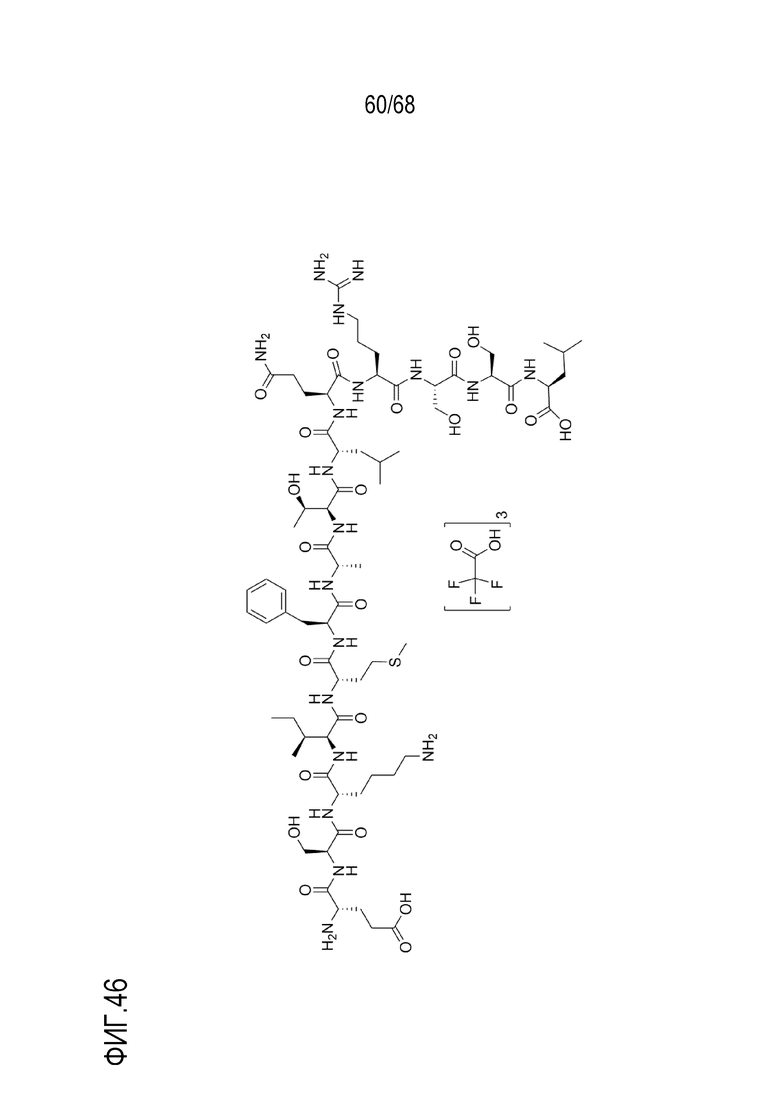
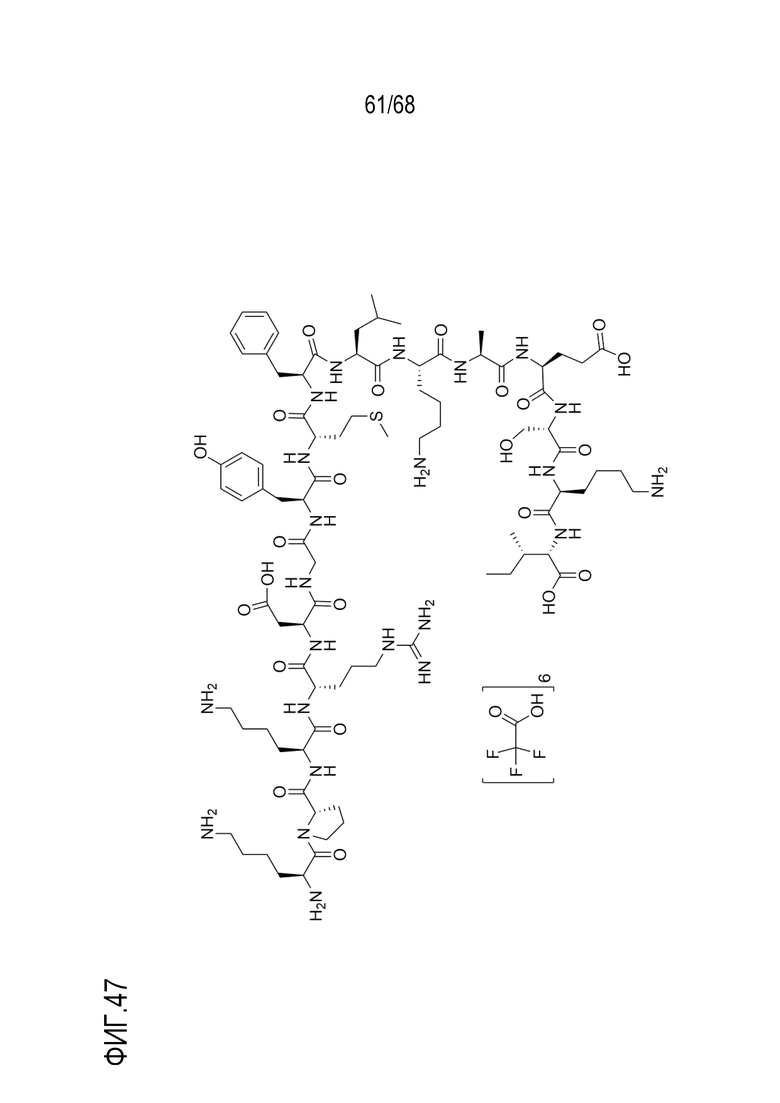
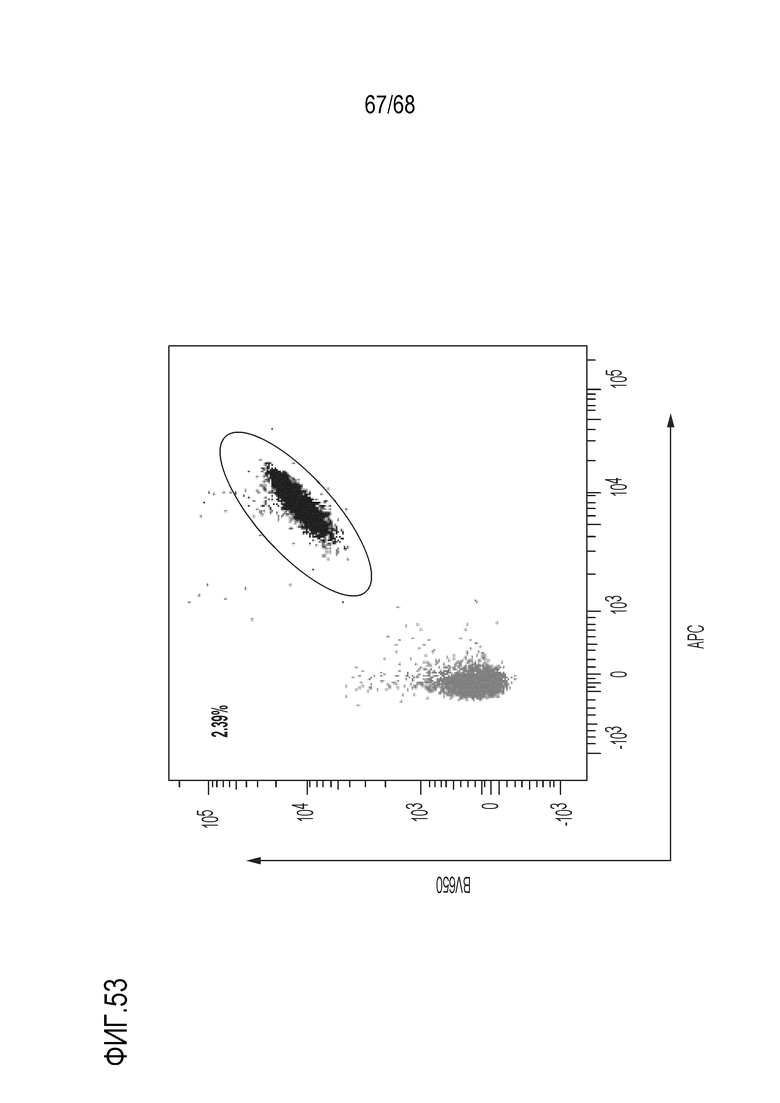

Изобретение относится к области биотехнологии, а именно к способу получения популяции иммунореактивных Т-клеток, содержащих Т-клеточный рецептор (TCR), специфичный к комплексу пептид:MHC, где пептид комплекса пептид:MHC представляет собой мутантную пептидную последовательность GATA3. Указанный способ предусматривает приведение популяции иммунных клеток в контакт с полинуклеотидом, содержащим последовательность, кодирующую полипептид, содержащий указанную мутантную пептидную последовательность GATA3, или полипептидом, содержащим указанную мутантную пептидную последовательность GATA3. При этом популяция иммунных клеток представляет собой популяцию иммунных клеток, лишенных клеток, экспрессирующих CD14 и CD25, и причем популяция иммунных клеток включает популяцию FMS-подобных лигандов рецептора тирозинкиназы 3 (FLT3L), стимулированных антигенпрезентирующими клетками (АРС), и популяцию Т-клеток. Изобретение эффективно для получения популяции иммунореактивных Т-клеток для иммунотерапии рака. 8 з.п. ф-лы, 54 ил., 44 табл., 41 пр.
1. Способ получения популяции иммунореактивных Т-клеток, содержащих Т-клеточный рецептор (TCR), специфичный к комплексу пептид:MHC, где пептид комплекса пептид:MHC представляет собой мутантную пептидную последовательность GATA3, содержащую по меньшей мере 8 смежных аминокислот из PGRPLQTHVLPEPHLALQPLQPHADHAHADAPAIQPVLWTTPPLQHGHRHGLEPCSMLTGPPARVPAVPFDLHFCRSSIMKPKRDGYMFLKAESKIMFAT LQRSSLWCLCSNH (SEQ ID NO: 2), включающий:
приведение популяции иммунных клеток в контакт с (i) полинуклеотидом, содержащим последовательность, кодирующую полипептид, содержащий указанную мутантную пептидную последовательность GATA3, или (ii) полипептидом, содержащим указанную мутантную пептидную последовательность GATA3;
причем популяция иммунных клеток представляет собой популяцию иммунных клеток, лишенных клеток, экспрессирующих CD14 и CD25, и причем популяция иммунных клеток включает популяцию FMS-подобных лигандов рецептора тирозинкиназы 3 (FLT3L), стимулированных антигенпрезентирующими клетками (АРС), и популяцию Т-клеток, и
с получением, тем самым, популяции Т-клеток, содержащих TCR, специфичный к комплексу пептид:MHC.
2. Способ по п.1, где способ включает, перед приведением в контакт, удаление из популяции иммунных клеток клеток, экспрессирующих CD14 и CD25.
3. Способ по п.1 или 2, включающий стимуляцию АРС в популяции иммунных клеток с помощью FLT3L.
4. Способ по любому из пп. 1-3, в котором полинуклеотид, содержащий последовательность, кодирующую полипептид, содержащий указанную последовательность мутантного пептида GATA3, представляет собой РНК, необязательно, где РНК представляет собой мРНК.
5. Способ по любому из пп. 1-4, в котором полипептид, содержащий указанную последовательность мутантного пептида GATA3, содержит по меньшей мере одну из следующих последовательностей:
TLQRSSLWCL (SEQ ID NO: 3753), VLPEPHLAL (SEQ ID NO: 3754), HVLPEPHLAL (SEQ ID NO: 3755), ALQPLQPHA (SEQ ID NO: 3756), AIQPVLWTT (SEQ ID NO: 3757), APAIQPVLWTT (SEQ ID NO: 3758), SMLTGPPARV (SEQ ID NO: 3759), MLTGPPARV (SEQ ID NO: 3760) и/или YMFLKAESKI (SEQ ID NO: 3761); и/или
MFLKAESKI (SEQ ID NO: 3762) и/или YMFLKAESKI (SEQ ID NO: 3763)
VLWTTPPLQH (SEQ ID NO: 3764), YMFLKAESK (SEQ ID NO: 3765) и/или KIMFATLQR (SEQ ID NO: 3766); и/или
FATLQRSSL (SEQ ID NO: 3767), EPHLALQPL (SEQ ID NO: 3768), QPVLWTTPPL (SEQ ID NO: 3769), GPPARVPAV (SEQ ID NO: 3770), MFATLQRSSL (SEQ ID NO: 3771), KPKRDGYMF (SEQ ID NO: 3772) и/или KPKRDGYMFL (SEQ ID NO: 3773) и/или
IMKPKRDGYM (SEQ ID NO: 3774), MFATLQRSSL (SEQ ID NO: 3775), FLKAESKIMF (SEQ ID NO: 3776), LHFCRSSIM (SEQ ID NO: 3777), EPHLALQPL (SEQ ID NO: 3778), FATLQRSSL (SEQ ID NO: 3779), ESKIMFATL (SEQ ID NO: 3780), FLKAESKIM (SEQ ID NO: 3781) и/или YMFLKAESKI (SEQ ID NO: 3782).
6. Способ по любому из пп. 1-4, в котором полипептид, содержащий указанную последовательность мутантного пептида GATA3, содержит по меньшей мере две из следующих последовательностей:
TLQRSSLWCL (SEQ ID NO: 3783), VLPEPHLAL (SEQ ID NO: 3784), HVLPEPHLAL (SEQ ID NO: 3785), ALQPLQPHA (SEQ ID NO: 3786), AIQPVLWTT (SEQ ID NO: 3787), APAIQPVLWTT (SEQ ID NO: 3788), SMLTGPPARV (SEQ ID NO: 3789), MLTGPPARV (SEQ ID NO: 3790) и/или YMFLKAESKI (SEQ ID NO: 3791); и/или
MFLKAESKI (SEQ ID NO: 3792) и/или YMFLKAESKI (SEQ ID NO: 3793); и/или
VLWTTPPLQH (SEQ ID NO: 3794), YMFLKAESK (SEQ ID NO: 3795) и/или KIMFATLQR (SEQ ID NO: 3796); и/или
FATLQRSSL (SEQ ID NO: 3797), EPHLALQPL (SEQ ID NO: 3798), QPVLWTTPPL (SEQ ID NO: 3799), GPPARVPAV (SEQ ID NO: 3800), MFATLQRSSL (SEQ ID NO: 3801), KPKRDGYMF (SEQ ID NO: 3802) и/или KPKRDGYMFL (SEQ ID NO: 3803) и/или
IMKPKRDGYM (SEQ ID NO: 3804), MFATLQRSSL (SEQ ID NO: 3805), FLKAESKIMF (SEQ ID NO: 3806), LHFCRSSIM (SEQ ID NO: 3807), EPHLALQPL (SEQ ID NO: 3808), FATLQRSSL (SEQ ID NO: 3809), ESKIMFATL (SEQ ID NO: 3810), FLKAESKIM (SEQ ID NO: 3811) и/или YMFLKAESKI (SEQ ID NO: 3812).
7. Способ по любому из пп. 1-4, в котором полипептид, содержащий указанную последовательность мутантного пептида GATA3, содержит последовательность, выбранную из группы, состоящей из ESKIMFATLQRSSL (SEQ ID NO: 3813), KPKRDGYMFLKAESKI (SEQ ID NO: 3814), SMLTGPPARVPAVPFDLH (SEQ ID NO: 3815), EPCSMLTGPPARVPAVPFDLH (SEQ ID NO: 3816), LHFCRSSIMKPKRDGYMFLKAESKI (SEQ ID NO: 3817), GPPARVPAVPFDLHFCRSSIMKPKRD (SEQ ID NO: 3818) и KPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 819).
8. Способ по любому из пп. 1-7, в котором полипептид, содержащий указанную последовательность мутантного пептида GATA3, содержит PGRPLQTHVLPEPHLALQPLQPHADHAHADAPAIQPVLWTTPPLQHGHRHGL (SEQ ID NO: 3) или EPCSMLTGPPARVPAVPFDLHFCRSSIMKPKRDGYMFLKAESKIMFATLQRSSLWCLCSNH (SEQ ID NO: 4).
9. Способ по любому из пп. 1-8, в котором полипептид, содержащий указанную последовательность мутантного пептида GATA3, содержит SEQ ID NO: 2.
| WO 2017173321 A1, 05.10.2017 | |||
| SARA BOBISSE et al., Neoantigen-based cancer immunotherapy, Ann Transl Med, 2016, 4(14): 262 | |||
| US 2018153975 A1, 07.06.2018 | |||
| GUSTIN J.P | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2024-02-19—Публикация
2019-06-19—Подача