ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к композиции, применяемой для перорального введения, которая включает соединение глюкагонподобный пептид 1 (GLP-1) и определенные средства для доставки. Пероральное введение композиции может использоваться для лечения диабета 2 типа, а также множества других состояний.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
За последние несколько десятилетий были предприняты многочисленные попытки усовершенствовать лечение сахарного диабета. Примерно 90% людей с диабетом 2 типа, который известен как инсулиннезависимый сахарный диабет (ИНЗСД). При диабете 2 типа в целом сохраняется способность организма вырабатывать инсулин, но инсулин не может эффективно использоваться клетками организма. В основном это связано с тем, что количество инсулина, продуцируемого в ответ на повышение уровня сахара в крови, недостаточно для того, чтобы позволять клеткам эффективно поглощать глюкозу и таким образом снижать уровень сахара в крови.
Множество данных, полученных в доклинических и клинических испытаниях, позволяет считать, что соединения глюкагонподобного пептида-1 (GLP-1) представляют собой очень перспективное средство для лечения диабета 2 типа и ряда других состояний. GLP-1 индуцирует различные биологические эффекты, такие как стимуляция секреции инсулина, ингибирование секреции глюкагона, подавление опорожнения желудка, повышение утилизации глюкозы и индуцирование потери веса. Кроме того, данные доклинических исследований позволяют полагать, что GLP-1 может также действовать в плане предотвращения разрушения β-клеток, что происходит при прогрессировании заболевания. Возможно, наиболее важной характеристикой GLP-1 является его способность стимулировать секрецию инсулина без риска развития гипогликемии, которая имеет место при лечении инсулином или некоторых типов пероральных препаратов, действие которых направлено на повышение экспрессии инсулина.
Однако развитие препаратов на основе GLP-1 представляет чрезвычайную трудность. В основном это связано с нестабильностью пептида в процессе производства в композициях, имеющих вид растворов, и in vivo. Было опубликовано единственное клиническое исследование, в котором использовали GLP-1 соединение для лечения гипергликемии или других состояний с использованием такой композиции на основе соединений GLP-1, которая может быть доставлена путем подкожной инъекции, путем непрерывной подкожной инфузии или путем непрерывного внутривенного введения. Многие пациенты с диабетом 2 типа или пациенты, желающие снизить вес, не хотят проходить курс лечения, который включает несколько инъекций в день. Таким образом, существует потребность в разработке препаратов на основе соединений GLP-1, которые могли бы доставляться альтернативными неинвазивными способами, такими как пероральная доставка.
К сожалению, имеются многочисленные барьеры на пути эффективной пероральной доставки пептидов. Высокое содержание кислоты и широкое распространение пищеварительных ферментов в желудочно-кишечном тракте зачастую приводит к разложению белков и пептидов до того, как они достигнут места всасывания. Кроме того, многие пептиды не могут эффективно пройти через клетки слизистого эпителия в тонком кишечнике для того, чтобы попасть в кровоток. И, наконец, многие лекарственные средства становятся нерастворимыми при низком pH, имеющем место в желудочно-кишечном тракте, и таким образом, они не могут подвергнуться эффективному всасыванию.
Тот факт, что соединения GLP-1 относительно нестабильны в композициях растворов и представляют собой раствор лишь при соблюдении очень узкого диапазона условий, а также обладают относительно коротким периодом полувыведения in vivo, при введении в виде композиции раствора, дает основания полагать, что указанные соединения могут быть эффективно доставлены пероральным способом. Таким образом, представляется удивительным тот факт, что соединения GLP-1 могут быть введены в состав такой композиции, из которой биологически активные молекулы могут всасываться в кровоток после перорального введения.
Настоящее изобретение относится к использования молекул специфического средства для доставки, которое взаимодействует с соединениями GLP-1 нековалентным образом, позволяя соединениям проходить через слизистую кишечника, все еще сохраняя при этом терапевтическую активность. Хотя средства для доставки, используемые в настоящем изобретении, были раскрыты в серии патентов США (см. патенты США NoNo.: 5541155, 5693338, 5976569, 5643957, 5955503, 6100298, 5650386, 5866536, 5965121, 5989539, 6001347, 6071510, 5820881 и 6242495, см. также WO 02/02509, WO 01/51454, WO 01/44199, WO 01/32130, WO 00/59863, WO 00/50386, WO 00/47188 и WO 00/40203), пероральное введение композиций, включающих соединения GLP-1 в сочетании с указанными средствами для доставки, не было раскрыто и не могло быть предположено. Кроме того, многочисленные факторы влияют на способность конкретного класса соединений эффективно доставляться в сочетании с одним или более классами средств для доставки. Так, например, конформация пептида, поверхностный заряд молекулы в определенных условиях композиции, профиль растворимости, стабильность введенного в композицию компонента, чувствительность к расщеплению протеазой и стабильность in vivo- все влияет на способность соединений к пероральной доставке.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к разработке новых композиций, включающих соединения GLP-1 и средства доставки, которые могут вводиться перорально. Настоящее изобретение относится к композиции, которая может быть введена перорально, включающей соединение GLP-1 и определенное средство для доставки. Соединение GLP-1 может представлять собой нативный GLP-1, фрагменты GLP-1, аналоги GLP-1, производные нативного GLP-1, фрагментов или аналогов GLP-1, а также эксендин-3 и эксендин-4. Средство для доставки выбирают из средств для доставки, описанных в патентах США NoNo.: 5541155, 5693338, 5976569, 5643957, 5955503, 6100298, 5650386, 5866536, 5965121, 5989539, 6001347, 6071510, 5820881 и 6242495, а также в WO 02/02509, WO 01/51454, WO 01/44199, WO 01/32130, WO 00/59863, WO 00/50386, WO 00/47188 и WO 00/40203.
Предпочтительные соединения GLP-1 представляют собой аналоги или производные аналогов, имеющие модификации в одном или более из указанных положений: 8, 12, 16, 18, 19, 20, 22, 25, 27, 30, 33 и 37, и характеризуются повышенной эффективностью в сравнении с Val8-GLP-1(7-37)OH. Предпочтительные соединения GLP-1 также раскрыты в SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:8, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13 и SEQ ID NO:14. Более предпочтительные соединения GLP-1 описаны как соединения SEQ ID NO:2, SEQ ID NO:12, SEQ ID NO:13 и SEQ ID NO:14.
Предпочтительные средства для доставки приведены в Таблице 1. Более предпочтительные средства для доставки представляют собой средства для доставки, соответствующие номерам соединений в таблице 1, выбранных из группы, состоящей из 1, 2, 4, 5, 6, 9, 10, 11, 13, 14, 15, 20, 21, 22, 23, 24, 26, 28, 30, 31, 35, 36, 38, 39, 40, 41, 42, 43, 44, 46, 51, 52 и 54.
Настоящее изобретение также относится к способу стимуляции рецептора GLP-1 у субъекта, при необходимости такой стимуляции, включающему стадию введения субъекту эффективного количества пероральной композиции, описанной в настоящем изобретении. Субъекты, нуждающиеся в стимуляции рецептора GLP-1, включают субъекты с инсулин независимым диабетом и с ожирением.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Трехбуквенный код аминокислот, используемый в настоящем описании, соответствует перечню, приведенному в Таблице 3 в Приложении С, в Приложении 2 административной инструкции PCT и соответствует пункту 37 C.F.R. § 1.822 (d)(1)(2000).
Для целей настоящего изобретения в том виде, как оно раскрыто и описано, приведенные в нем термины и сокращения определяются, как указано ниже.
Термин «композиция» в контексте настоящего описания относится к сочетанию соединения GLP-1 и определенного средства для доставки, которое может вводиться перорально, так что соединение GLP-1 проходит через кишечник в системный кровоток и сохраняет способность связываться с рецептором GLP-1 и инициировать цепь сигнальной трансдукции, приводящей к появлению инсулинотропной активности. Композиция может необязательно включать другие средства, при условии, что GLP-1 сохраняет способность связываться с рецептором GLP-1.
Термин «пероральный» в контексте настоящего описания относится к доставке соединений через рот, при которой соединение проходит через желудок, тонкий кишечник или толстый кишечник, попадая в системный кровоток.
Термин «соединение GLP-1» в контексте настоящего описания включает природные полипептиды GLP-1 (GLP-1(7-37)OH и (GLP-1(7-36)NH2), фрагменты GLP-1, аналоги GLP-1, GLP-1 производные природных GLP-1 полипептидов, фрагментов GLP-1 или аналогов GLP-1, эксендин-3 и эксендин-4, которые обладают способностью связываться с рецептором GLP-1 и инициировать цепь сигнальной трансдукции, приводящей к появлению инсулинотропной активности.
Термин «инсулинотропная активность» в контексте настоящего описания относится к способности стимулировать секрецию инсулина в ответ на повышенный уровень глюкозы, что вызывает повышение поглощения глюкозы клетками и снижение уровня глюкозы в плазме. Инсулинотропная активность может быть определена, например, с использованием способа, описанного в примере 1. Молекула GLP-1 обладает инсулинотропной активностью, если островковые клетки секретируют инсулин в присутствии молекулы GLP-1 на уровне выше фонового.
Термин «ДПП IV-резистентный» в контексте настоящего описания относится к молекулам GLP-1, которые обладают улучшенной метаболической стабильностью и повышенной биологической активностью. Так, например, ДПП IV-резистентность может быть определена с использованием способа, описанного в примере 2. GLP-1-молекула представляет собой ДПП IV-резистентную молекулу, если в присутствии ДПП IV молекула GLP-1 обладает усиленной метаболической стабильностью, превышающей стабильность нативной GLP-1. ДПП IV-резистентные молекулы GLP-1 могут включать изменения аминокислотного состава в сайте распознавания ДПП IV (положение 8) или ДПП IV-резистентные пептиды могут иметь присоединенную группу, которая ограничивает доступность ДПП IV к сайту распознавания, или могут работать оба механизма.
«Фрагмент GLP-1» представляет собой полипептид, полученный после усечения молекулы путем удаления одной или более аминокислот от N-конца и/или С-конца из GLP-1(7-37)OH или его аналога или производного. Используемая для описания GLP-1(7-37)OH номенклатура также применима к фрагментам GLP-1. Например, GLP-1(9-36)OH обозначает фрагмент GLP-1, полученный при вырезании двух аминокислот с N-конца и одной аминокислоты с С-конца. Аминокислоты во фрагменте обозначаются теми же номерами, что и соответствующие аминокислоты в GLP-1(7-37)OH. Так, например, N-концевая глютаминовая кислота в GLP-1(9-37)OH находится в положении 9, положение 12 занято фенилаланином и положение 22 занято глицином, как и в GLP-1(7-37)OH. В случае GLP-1(7-36)OH глицин в положении 37 в GLP-1(7-37)OH удален.
«Аналог GLP-1» характеризуется достаточным уровнем гомологии с GLP-1(7-37)OH или фрагментом GLP-1(7-37)OH, так что указанный аналог обладает инсулинотропной активностью. Предпочтительно, аналог GLP-1 имеет аминокислотную последовательность GLP-1(7-37)OH или его фрагмент, модифицированную таким образом, что одна, две, три, четыре или пять аминокислот отличаются от аминокислот в соответствующих положениях в GLP-1(7-37)OH или во фрагменте GLP-1(7-37)OH. В номенклатуре, используемой для обозначения соединений GLP-1, замещающая аминокислота и ее положение указываются перед исходной структурой. Так, например, Glu22-GLP-1(7-37)OH обозначает соединение GLP-1, в котором глицин, в норме находящийся в положении 22 в GLP-1(7-37)OH, замещен глютаминовой кислотой; Val8-Glu22-GLP-1(7-37)OH обозначает соединение GLP-1, в котором аланин, в норме находящийся в положении 8, и глицин в норме, находящийся в положении 22 в GLP-1(7-37)OH, заменены валином и глютаминовой кислотой соответственно.
Молекулы GLP-1 также включают полипептиды, в которых одна или более аминокислот добавлены к N-концу и/или С-концу (GLP-1(7-37)OH или к его фрагментам или аналогам. Предпочтительно, чтобы молекулы GLP-1 указанного типа включали примерно до тридцати девяти аминокислот. Аминокислоты в «удлиненной» молекуле GLP-1 обозначаются теми же номерами, что и соответствующая аминокислота в GLP-1(7-37)OH. Так, например, для молекулы GLP-1, получаемой при добавлении двух аминокислот к N-концу GLP-1(7-37)OH, N-концевая аминокислота расположена в положении 5; и в случае молекулы GLP-1, полученной при добавлении одной аминокислоты к С-концу GLP-1(7-37)OH, С-концевая аминокислота расположена в положении 38. Таким образом, положение 12 занято фенилаланином и положение 22 занято глицином в обоих из указанных «удлиненных» соединениях GLP-1, как и в случае GLP-1(7-37)OH. Предпочтительно, аминокислоты 1-6 в удлиненной молекуле GLP-1 одинаковы или включают консервативное замещение аминокислоты в соответствующем положении GLP-1(7-37)OH. Аминокислоты GLP-1 38-45 в удлиненной молекуле GLP-1 предпочтительно одинаковы или включают консервативное замещение аминокислоты в соответствующем положении глюкагона или эксендина-4.
Термин «производное GLP-1» относится к молекуле, имеющей аминокислотную последовательность GLP-1, фрагмента GLP-1 или аналога GLP-1, но включающей дополнительно химическую модификацию одной или более группах боковых аминокислот, атомов α-углерода, концевой аминогруппы или концевой карбоксильной группы. Химическая модификация включает, не ограничиваясь приведенным перечнем, добавление химических фрагментов, создание новых связей и удаление химических фрагментов. Модификации групп боковых аминокислот включают, не ограничиваясь приведенным списком, ацилирование ε-аминогрупп лизина, N-алкилирование аргинина, гистидина или лизина, алкилирование карбоновых групп глютаминовой или аспарагиновой кислот, и деаминирование глютамина или аспарагина. Модификации концевой аминогруппы включает, не ограничиваясь приведенным списком, модификацию дезамино-группы, N-низшего алкила, N-ди-низшего алкила и N-ацила. Модификации концевой карбоксигруппы включают, не ограничиваясь приведенным списком, модификацию амида, низшего алкиламида, диалкиламида и низшего сложного алкильного эфира. Низший алкил представляет собой С1-С4 алкил. Кроме того, одна или более боковых групп или концевых групп могут быть защищены защитными группами, известными специалистам в области белковой химии; α-углерод аминокислоты может быть моно- или ди-метилированным.
Для целей настоящего изобретения используют тест in vitro на выявление сигнального GLP-1 рецептора, позволяющий определить, проявляет ли удлиненный GLP-1 пептид инсулинотропную активность in vivo. Удлиненные GLP-1 пептиды, описанные в настоящем изобретении, обладают эффективностью in vitro, которая составляет не менее чем одна десятая от эффективности in vitro ДПП IV-резистентного аналога GLP-1, известного как Val8-GLP-1(7-37)OH. Более предпочтительно, удлиненные GLP-1 пептиды по настоящему изобретению являются столь же эффективными или более эффективными, чем Val8-GLP-1(7-37)OH.
Термин "эффективность in vitro» в контексте настоящего описания обозначает меру способности пептида активировать рецептор GLP-1 в клеточном тесте. Эффективность in vitro выражается в виде показателя ЭК50, который представляет собой эффективную концентрацию соединения, которая приводит к достижению 50% активности в однократном эксперименте по определению зависимости доза-реакция. Для целей настоящего описания эффективность in vitro определяют с помощью флюоресцентного теста, в котором используют клетки HEK-293 Aurora CRE-BLAM, которые стабильно экспрессируют человеческий рецептор GLP-1. Указанные клетки включают стабильно интегрированный в них ДНК-вектор, содержащий реагирующий на цАМФ элемент (GRE), который направляет экспрессию гена β-лактамазы (BLAM). Взаимодействие агониста GLP-1 с рецептором инициирует сигнал, который приводит к активации элемента, реагирующего на цАМФ, и к последующей экспрессии β-лактамазы. Субстрат β-лактамазы CCF2/AM, который вызывает флюоресценцию при расщеплении β-лактамазы (Aurora Biosciences Corp.), может быть затем добавлен к клеткам, который подвергались воздействию определенного количества агониста GLP-1, для измерения агонистской эффективности GLP-1. Тест описан также Злокарником с соавт. (Zlokarnik, et al., (1998) Science 279:84-88), см. также пример 1. Значения параметров ЭК50 для соединений, перечисленных в примере 1, определяют с помощью описанного выше теста на β-лактамазу (BLAM-теста) путем построения кривой зависимости доза-реакция с использованием разбавлений в диапазоне от 0,00003 наномоля до 30 наномоля. Относительные значения эффективности in vitro устанавливают, сравнивая с данными для Val8-GLP-1(7-37)OH как контроля и полагая значение контроля, равным 1.
Термин «средство для доставки» относится к молекулам, описанным в патентах США No. 5541155, 5693338, 5976569, 5643957, 5955503, 6100298, 5650386, 5866536, 5965121, 5989539, 6001347, 6071510, 5820881 и 6242495, а также в WO 02/02509, WO 01/51454, WO 01/44199, WO 01/32130, WO 00/59863, WO 00/50386, WO 00/47188 и WO 00/40203. Средства для доставки обычно получают из аминокислот и используют в пероральных композициях согласно настоящему изобретению. Полученные аминокислоты могут также иметь вид полиаминокислот и пептидов. Аминокислота представляет собой любую карбоновую кислоту, содержащую по меньшей мере одну свободную аминогруппу, и включает природные и синтетические аминокислоты. Полиаминокислоты представляют собой либо пептиды, либо две или более аминокислот, соединенных связью, образованной другими группами, которые могут быть соединены, например, сложноэфирной и ангидридной связью. Пептиды представляют собой две или более аминокислот, соединенных пептидной связью. Пептиды могут варьировать по длине, охватывая широкий диапазон от дипептидов из двух аминокислот до полипептидов, включающих несколько сотен аминокислот. Предпочтительные пептиды включают дипептиды, трипептиды, тетрапептиды и пентапептиды.
Кроме того, средства для доставки по настоящему изобретению могут быть необязательно представлены солевой формой. Примеры солей включают натриевые соли, соли хлористоводородной кислоты, серной кислоты, фосфорной кислоты, лимонной кислоты, уксусной кислоты, сульфат, фосфат, хлорид, бромид, иодид, ацетат, пропионат, соль бромистоводородной кислоты, гидроксид натрия, гидроксид калия, гидроксид аммония и карбонат калия.
Различные пероральные композиции по настоящему изобретению могут необязательно включать фармацевтически приемлемый буфер. Примеры фармацевтически приемлемых буферов включают фосфатные буферы, такие как двуосновной фосфат натрия, ТРИС, глицилглицин, малеат, ацетат натрия, цитрат натрия, тартрат натрия, или аминокислоту, такую как глицин, гистидин, лизин или аргинин. Другие фармацевтически приемлемые буферы также известны в данной области техники. Предпочтительно, буфер выбирают из группы, состоящей из фосфата, ТРИС, малеата и глицина. Еще более предпочтительным буфером является ТРИС.
Предпочтительная концентрация ТРИС буфера составляет от 1 мМ до 100 мМ. Еще более предпочтительная концентрация составляет от примерно 10 мМ до примерно 50 мМ и наиболее предпочтительная концентрация буфера составляет 20 мМ.
Значение pH в пероральной композиции доводят до достижения стабильности и приемлемого для перорального введения состояния. Предпочтительно, pH доводят до значения от примерно 7,0 до примерно 9,0, более предпочтительно, pH составляет от примерно 7,4 до примерно 8,4. Еще более предпочтительно, pH составляет от примерно 7,8 до примерно 8,4. Наиболее предпочтительно, pH имеет значение от 7,8 до 8,1.
Различные пероральные композиции по настоящему изобретению могут необязательно включать средство, способствующее суспендированию. Некоторые средства для доставки требуют наличия средства для суспендирования в связи со свойственными им характеристиками растворимости. Примером средства, способствующего суспендированию, является гидроксипропилметилцеллюлоза. Предпочтительно, конечная концентрация гидроксипропилметилцеллюлозы составляет от примерно 2% до примерно 10% (вес./об.). Еще более предпочтительно, концентрация составляет от примерно 2% до примерно 5% (вес./об.). Наиболее предпочтительно, концентрация составляет около 3,9% (вес/объем).
Пероральные композиции по настоящему изобретению могут необязательно включать сорастворитель. В случае некоторых средств для доставки требуется наличие сорастворителей в связи со свойственными им характеристиками растворимости. Примеры сорастворителей включают этанол, N-метилпирролидон, N,N-диметилацетамид, N,N-диметилформамид, гликофурол, этоксидиол, пропиленгликоль, полиэтиленгликоль 300 и поливинилпирролидон. Предпочтительно, конечная концентрация сорастворителей составляет от примерно 5 об.% до примерно 30 об.%. Еще более предпочтительно, концентрация составляет от примерно 10 об.% до примерно 25 об.%. Наиболее предпочтительно, концентрация составляет примерно 20 об.%.
Пероральные композиции по настоящему изобретению могут необязательно включать консервант. Консервант представляет собой соединение, которое добавляют к композиции и которое действует как противомикробный агент. Среди известных в технике эффективных и приемлемых для введения в парентеральные композиции консервантов следует отметить фенольные консерванты, алкилпарабены, бензиловый спирт, хлорбутанол, резорцинол и другие аналогичные консерванты и различные их смеси. Примеры фенольных консервантов включают крезолы и фенолы или смесь крезолов и фенола. Примеры крезолов включают мета-крезол, орто-крезол, пара-крезол, хлорокрезол или их смеси. Термин «алкилпарабены» относится к С1-С4 алкилпарабенам или их смесям. Примеры алкилпарабенов включают метилпарабен, этилпарабен, пропилпарабен и бутилпарабен. Концентрации их должны быть достаточны для поддержания эффективности консерванта в плане задержки микробного роста. Предпочтительно, консервант представляет собой фенольное производное. Более предпочтительно, консервант представляет собой крезол. Еще более предпочтительно, консервант представляет собой мета-крезол.
Предпочтительная концентрация консерванта в готовой смеси составляет примерно от 1,0 мг/мл до примерно 20,0 мг/мл. Более предпочтительные диапазоны концентрации консерванта в готовой смеси составляют от примерно 2,0 мг/мл до примерно 8,0 мг/мл, от 2,5 мг/мл до примерно 4,5 мг/мл и от примерно 2,0 мг/мл до примерно 4,0 мг/мл. Наиболее предпочтительная концентрация консерванта составляет примерно 3,0 мг/мл.
Пероральные композиции по настоящему изобретению могут необязательно включать средства, способствующие поддержанию изотоничности. Средства, способствующие поддержанию изотоничности, представляют собой соединения, которые являются физиологически толерантными и придают определенный тонус композиции для предупреждения прохода жидкости через клеточные мембраны. Примеры таких соединений включают глицерин, соли, например NaCl, и сахара, например декстрозу, маннит и сахарозу. Указанные соединения обычно используют для таких целей в известных концентрациях. Могут быть добавлены одно или более средств, способствующие поддержанию изотоничности, для доведения до нужного уровня ионной силы или тонуса. Предпочтительное средство, способствующее поддержанию изотоничности, представляет собой NaCl. Концентрация NaCl составляет предпочтительно примерно от 10 мМ до 200 мМ, более предпочтительно, составляет примерно от 50 мМ до 150 мМ и наиболее предпочтительно, составляет примерно 100 мМ.
Альтернативно, введение композиций может осуществляться в виде твердой формы, такой как таблетка, капсула или препарат из частиц, такой как порошок. Твердые дозированные формы могут быть приготовлены путем смешивания твердой формы соединения с твердой формой активного средства. Альтернативно, твердая форма может быть получена из раствора соединения и активного средства с помощью известных в данной области методов, таких как лиофильная сушка, осаждение, кристаллизация и диспергирование в твердом состоянии.
Соединения GLP-1, подходящие для использования по настоящему изобретению
Соединения GLP-1 по настоящему изобретению могут быть приготовлены с помощью большого числа методов, известных в данной области, таких как методы химии твердофазного синтеза, выделения и очистки молекул GLP-1 из природных источников, технология на основе рекомбинантной ДНК или сочетание указанных методов. Например, методы получения пептидов GLP-1 описаны в патентах США NoNo. 5118666, 5120712, 5512549, 5977071 и 6191102.
По принятым в данной области правилам, аминоконцу в GLP-1(7-37)ОН присваивается номер 7 и карбоксильному концу присваивается номер 37. Другие аминокислоты в полипептиде нумеруются последовательно, как показано в SEQ ID No:1. Например, положение 12 занято фенилаланином и положение 22 занято глицином.
Два природных усеченных пептида GLP-1 описываются формулой I, как показано на SEQ ID: NO:1:
His7-Ala-Glu-Gly10-Thr-Phe-Thr-Ser-Asp-Val-Ser-Ser-Tyr-Leu20-Glu-Gly-Gln-Ala-Ala25-Lys-Glu-Phe-Ile-Ala30-Trp-Leu-Val-Lys-Gly35-Arg-Xaa37
Формула I, SEQ ID NO:1,
где Xaa37 обозначает Gly или -NH2.
Предпочтительно, соединение GLP-1 имеет аминокислотную последовательность SEQ ID NO:1 или модифицированную таким образом, что она отличается по одной, двум, трем, четырем или пяти аминокислотам от SEQ ID: NO:1.
Предпочтительная группа соединений GLP-1 состоит из аналогов GLP-1 формулы I (SEQ ID: NO:2).
His-Xaa8-Xaa9-Gly-Xaa11-Phe-Thr-Xaa14-Asp-Xaa16-Xaa17-Xaa18-Xaa19-Xaa20-Xaa21-Xaa22-Xaa23-Xaa24-Xaa25-Xaa26-Xaa27-Phe-Ile-Xaa30-Xaa31-Xaa32-Xaa33-Xaa34-Xaa35-Xaa36-Xaa37-Xaa38-Xaa39-Xaa40-Xaa41-Xaa42-Xaa43-Xaa44-Xaa45.
Формула I (SEQ ID: NO:2),
где Xaa8 обозначает Ala, Gly, Ser, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa9 обозначает Glu, Asp или Lys;
Xaa11 обозначает Thr, Ala, Gly, Ser, Leu, Ile, Val, Glu, Asp или Lys;
Xaa14 обозначает Ser, Ala, Gly, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa16 обозначает Val, Ala, Gly, Ser, Thr, Leu, Ile, Tyr, Glu, Asp, Trp или Lys;
Xaa17 обозначает Ser, Ala, Gly, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa18 обозначает Ser, Ala, Gly, Thr, Leu, Ile, Val, Glu, Asp, Trp, Tyr или Lys;
Xaa19 обозначает Tyr, Phe, Trp, Glu, Asp, Gln или Lys;
Xaa20 обозначает Leu, Ala, Gly, Ser, Thr, Ile, Val, Glu, Asp, Met, Trp, Tyr, или Lys;
Xaa21 обозначает Glu, Asp или Lys;
Xaa22 обозначает Gly, Ala, Ser, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa23 обозначает Gln, Asn, Arg, Glu, Asp или Lys;
Xaa24 обозначает Ala, Gly, Ser, Thr, Leu, Ile, Val, Arg, Glu, Asp или Lys;
Xaa25 обозначает Ala, Gly, Ser, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa26 обозначает Lys, Arg, Gln, Glu, Asp, или His;
Xaa27 обозначает Leu, Glu, Asp или Lys;
Xaa30 обозначает Ala, Gly, Ser, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa31 обозначает Trp, Phe, Tyr, Glu, Asp или Lys;
Xaa32 обозначает Leu, Gly, Ala, Ser, Thr, Ile, Val, Glu, Asp или Lys;
Xaa33 обозначает Val, Gly, Ala, Ser, Thr, Leu, Ile, Glu, Asp или Lys;
Xaa34 обозначает Asn, Lys, Arg, Glu, Asp или His;
Xaa35 обозначает Gly, Ala, Ser, Thr, Leu, Ile, Val, Glu, Asp или Lys;
Xaa36 обозначает Gly, Arg, Lys, Glu, Asp или His;
Xaa37 обозначает Pro, Gly, Ala, Ser, Thr, Leu, Ile, Val, Glu, Asp или Lys, или делетирован;
Xaa38 обозначает Ser, Arg, Lys, Glu, Asp или His, или делетирован;
Xaa39 обозначает Ser, Arg, Lys, Glu, Asp или His или делетирован;
Xaa40 обозначает Gly, Asp, Glu или Lys или делетирован;
Xaa41 обозначает Ala, Phe, Trp, Tyr, Glu, Asp или Lys или делетирован;
Xaa42 обозначает Ser, Pro, Lys, Glu или Asp или делетирован;
Xaa43 обозначает Ser, Pro, Glu, Asp или Lys или делетирован;
Xaa44 обозначает Gly, Pro, Glu, Asp или Lys или делетирован и
Xaa45 обозначает Ala, Ser, Val, Glu, Asp или Lys, Ala-NH2, Ser-NH2, Val-NH2, Glu-NH2, Asp-NH2 или Lys-NH2 или делетирован;
при условии, что если аминокислота в положениях 37, 38, 39, 40, 41, 42, 43 или 44 делетирована, то аминокислота ниже по ходу транскрипции от данной аминокислоты также делетирована.
Предпочтительно, чтобы соединения GLP-1 содержали меньше шести аминокислот, которые отличаются от соответствующей аминокислоты в GLP-1(7-37)ОН или в эксендине-4. Более предпочтительно, чтобы соединение GLP-1 формулы I содержало меньше пяти аминокислот, которые отличаются от соответствующей аминокислоты в GLP-1(7-37)ОН или в эксендине-4. Еще более предпочтительно, чтобы меньше четырех аминокислот отличалось от соответствующей аминокислоты в GLP-1(7-37)ОН или в эксендине-4.
Соединения GLP-1 по настоящему изобретению включают производные формулы I, такие как С1-6-сложный эфир или его амид или С-1-6-алкиламид или С-1-6-диалкиламид. Документ WO 99/43706, в котором описываются производные соединений GLP-1 формулы I, включен в настоящее описание в качестве ссылки. Соединения формулы I были дериватизированы, как описано в WO 99/43706, и удаление дериватизирующих группировок также входит в область настоящего изобретения.
Другая предпочтительная группа соединений GLP-1 состоит из аналогов GLP-1 формулы II (SEQ ID NO:3):
Xaa7-Xaa8-Xaa9-Gly-Xaa11-Xaa12-Thr-Ser-Asp-Xaa16-Ser-Xaa18-Xaa19-Leu-Glu-Gly-Xaa23-Xaa24-Ala-Xaa26-Xaa27-Phe-Ile-Xaa30-Xaa31-Leu-Xaa33-Xaa34-Xaa35-Xaa36-R37
Формула II (SEQ ID NO:3),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Gly, Ala, Val, Leu, Ile, Ser или Thr;
Xaa9 обозначает Thr, Ser, Arg, Lys, Trp, Phe, Tyr, Glu или His;
Xaa11 обозначает Asp, Glu, Arg, Thr, Ala, Lys или His;
Xaa12 обозначает His, Trp, Phe или Tyr;
Xaa16 обозначает Leu, Ser, Thr, Trp, His, Phe, Asp, Val, Tyr, Glu или Ala;
Xaa18 обозначает His, Pro, Asp, Glu, Arg, Ser, Ala или Lys;
Xaa19 обозначает Gly, Asp, Glu, Gln, Asn, Lys, Arg или Cys;
Xaa23 обозначает His, Asp, Lys, Glu, Gln или Arg;
Xaa24 обозначает Glu, Arg, Ala или Lys;
Xaa26 обозначает Trp, Tyr, Phe, Asp, Lys, Glu или His;
Xaa27 обозначает Ala, Glu, His, Phe, Tyr, Trp, Arg или Lys;
Xaa30 обозначает Ala, Glu, Asp, Ser или His;
Xaa31 обозначает Asp, Glu, Ser, Thr, Arg, Trp или Lys;
Xaa33 обозначает Asp, Arg, Val, Lys, Ala, Gly или Glu;
Xaa34 обозначает Glu, Lys или Asp;
Xaa35 обозначает Thr, Ser, Lys, Arg, Trp, Tyr, Phe, Asp, Gly, Pro, His или Glu;
Xaa36 обозначает Thr, Ser, Asp, Trp, Tyr, Phe, Arg, Glu или His;
R37 обозначает Lys, Arg, Thr, Ser, Glu, Asp, Trp, Tyr, Phe, His, Gly, Gly-Pro или делетирован.
Другая предпочтительная группа соединений GLP-1 состоит из аналогов GLP-1 формулы III (SEQ ID NO: 4):
Xaa7-Xaa8-Glu-Gly-Xaa11-Xaa12-Thr-Ser-Asp-Xaa16-Ser-Ser-Tyr-Leu-Glu-Xaa22-Xaa23-Xaa24-Xaa25-Lys-Xaa27-Phe-Ile-Xaa30-Trp-Leu-Xaa33-Xaa34-Xaa35-Xaa36-R37
Формула III (SEQ ID NO:4),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Gly, Ala, Val, Leu, Ile, Ser или Thr;
Xaa11 обозначает Asp, Glu, Arg, Thr, Ala, Lys или His;
Xaa12 обозначает His, Trp, Phe или Tyr;
Xaa16 обозначает Leu, Ser, Thr, Trp, His, Phe, Asp, Val, Glu или Ala;
Xaa22 обозначает Gly, Asp, Glu, Gln, Asn, Lys, Arg или Cys;
Xaa23 обозначает His, Asp, Lys, Glu или Gln;
Xaa24 обозначает Glu, His, Ala или Lys;
Xaa25 обозначает Asp, Lys, Glu или His;
Xaa27 обозначает Ala, Glu, His, Phe, Tyr, Trp, Arg или Lys;
Xaa30 обозначает Ala, Glu, Asp, Ser или His;
Xaa33 обозначает Asp, Arg, Val, Lys, Ala, Gly или Glu;
Xaa34 обозначает Glu, Lys или Asp;
Xaa35 обозначает Thr, Ser, Lys, Arg, Trp, Tyr, Phe, Asp, Gly, Pro, His или Glu;
Xaa36 обозначает Arg, Glu или His;
R37 обозначает Lys, Arg, Thr, Ser, Glu, Asp, Trp, Tyr, Phe, His, Gly, Gly-Pro или делетирован.
Другая предпочтительная группа GLP-1 соединений состоит из аналогов GLP-1 формулы IV (SEQ ID NO: 5):
Xaa7-Xaa8-Glu-Gly-Thr-Xaa12-Thr-Ser-Asp-Xaa16-Ser-Ser-Tyr-Leu-Glu-Xaa22-Xaa23-Ala-Ala-Xaa26-Glu-Phe-Ile-Xaa30-Trp-Leu-Val-Lys-Xaa35-Arg-R37.
Формула IV (SEQ ID NO:5),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Gly, Ala, Val, Leu, Ile, Ser, Met или Thr;
Xaa12 обозначает His, Trp, Phe или Tyr;
Xaa16 обозначает Leu, Ser, Thr, Trp, His, Phe, Asp, Val, Glu или Ala;
Xaa22 обозначает Gly, Asp, Glu, Gln, Asn, Lys, Arg или Cys;
Xaa23 обозначает His, Asp, Lys, Glu или Gln;
Xaa26 обозначает Asp, Lys, Glu или His;
Xaa30 обозначает Ala, Glu, Asp, Ser или His;
Xaa35 обозначает Thr, Ser, Lys, Arg, Trp, Tyr, Phe, Asp, Gly, Pro, His или Glu;
R37 обозначает Lys, Arg, Thr, Ser, Glu, Asp, Trp, Tyr, Phe, His, Gly, Gly-Pro или делетирован.
Другая предпочтительная группа соединений GLP-1 состоит из аналогов GLP-1 формулы V (SEQ ID NO: 6):
Xaa7-Xaa8-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Val-Ser-Ser-Tyr-Leu-Glu-Xaa22-Xaa23-Xaa24-Ala-Lys-Glu-Phe-Ile-Xaa30-Trp-Leu-Val-Lys-Gly-Arg-R37
Формула V (SEQ ID NO:6),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Gly, Ala, Val, Leu, Ile, Ser или Thr;
Xaa22 обозначает Gly, Asp, Glu, Gln, Asn, Lys, Arg или Cys;
Xaa23 обозначает His, Asp, Lys, Glu или Gln;
Xaa24 обозначает Ala, Glu, His, Phe, Tyr, Trp, Arg или Lys;
Xaa30 обозначает Ala, Glu, Asp, Ser или His;
R37 обозначает Lys, Arg, Thr, Ser, Glu, Asp, Trp, Tyr, Phe, His, Gly, Gly-Pro или делетирован.
Предпочтительные соединения GLP-1 формул I, II, III, IV и V включают аналоги GLP-1 или фрагменты аналогов GLP-1, причем указанные аналоги или их фрагменты включают аминокислоту, отличную от аланина в положении 8 (аналоги по положению 8). Предпочтительно, чтобы аналоги по указанному положению 8 содержали одно или более дополнительных изменений в положениях 9, 11, 12, 16, 18, 22, 23, 24, 26, 27, 30, 31, 33, 34, 35, 36 и 37 в сравнении с соответствующей аминокислотой в нативном GLP-1(7-37)OH. Предпочтительно также, чтобы указанные аналоги имели 6 или менее замен в сравнении с соответствующими аминокислотами в нативном GLP-1(7-37)OH или GLP-1(7-36)OH. Более предпочтительные аналоги содержат 5 или менее замен в сравнении с соответствующими аминокислотами в нативном GLP-(7-37)OH или GLP-1(7-36)OH или содержат 4 или менее замен в сравнении с соответствующими аминокислотами в нативном GLP-1(7-37)OH или GLP-1(7-36)OH. Еще более предпочтительно, чтобы указанные аналоги имели 3 или менее замен в сравнении с соответствующими аминокислотами в нативном GLP-1(7-37)OH или GLP-1(7-36)OH. Наиболее предпочтительно, чтобы указанные аналоги имели 2 или менее замен в сравнении с соответствующими аминокислотами в нативном GLP-1(7-37)OH.
Предпочтительные GLP-1 соединения формул II, III, IV и V включают аналоги GLP-1 или фрагменты аналогов GLP-1, в которых глицин в положении 22 и предпочтительно аланин в положении 8 замещены другой аминокислотой.
В том случае, когда положение 22 занято аспарагиновой кислотой, глютаминовой кислотой, аргинином или лизином, положение 8 представляет собой предпочтительно глицин, валин, лейцин, изолейцин, серин, треонин или метионин и более предпочтительно валин или глицин. В том случае, когда положение 22 занято сульфоновой кислотой, такой как цистеиновая кислота, положение 8 представляет собой предпочтительно глицин, валин, лейцин, изолейцин, серин, треонин или метионин и более предпочтительно валин или глицин.
Другие предпочтительные соединения GLP-1 включают аналоги GLP-1 формулы IV (SEQ ID NO: 5), причем указанные аналоги имеют последовательность GLP-1(7-37)OH, за исключением того, что аминокислота в положении 8 представляет собой предпочтительно глицин, валин, лейцин, изолейцин, серин, треонин или метионин и более предпочтительно валин или глицин, и положение 30 занято глютаминовой кислотой, аспарагиновой кислотой, серином, гистидином и более предпочтительно, глютаминовой кислотой.
Другие предпочтительные соединения GLP-1 включают аналоги GLP-1 формулы IV (SEQ ID NO: 5), причем указанные аналоги имеют последовательность GLP-1(7-37)OH, за исключением того, что аминокислота в положении 8 представляет собой предпочтительно глицин, валин, лейцин, изолейцин, серин, треонин или метионин и более предпочтительно, валин или глицин, и положение 37 занято гистидином, лизином, аргинином, треонином, серином, глютаминовой кислотой, аспарагиновой кислотой, триптофаном, тирозином, фенилаланином и более предпочтительно, гистидином.
Другие предпочтительные соединения GLP-1 включают аналоги GLP-1 формулы IV (SEQ ID NO:5), причем указанные аналоги имеют последовательность GLP-1(7-37)ОН, за исключением того, что аминокислота в положении 8 представляет собой предпочтительно глицин, валин, лейцин, изолейцин, серин, треонин или метионин и более предпочтительно валин или глицин, и положение 22 занято глютаминовой кислотой, лизином, аспарагиновой кислотой или аргинином и более предпочтительно глютаминовой кислотой или лизином, и положение 23 занято лизином, аргинином, глютаминовой кислотой, аспарагиновой кислотой и гистидином и более предпочтительно лизином или глютаминовой кислотой.
Другие предпочтительные соединения GLP-1 включают аналоги GLP-1 формулы V (SEQ ID NO:6), причем указанные аналоги имеют последовательность GLP-1(7-37)ОН, за исключением того, что аминокислота в положении 8 представляет собой предпочтительно глицин, валин, лейцин, изолейцин, серин, треонин или метионин и более предпочтительно валин или глицин, и положение 22 занято глютаминовой кислотой, лизином, аспарагиновой кислотой или аргинином и более предпочтительно глютаминовой кислотой или лизином, и положение 27 занято аланином, лизином, аргинином, триптофаном, тирозином, фенилаланином или гистидином и более предпочтительно аланином.
Другие предпочтительные соединения GLP-1 включают аналоги GLP-1 формулы II, причем указанные аналоги имеют последовательность GLP-1(7-37)ОН, за исключением того, что аминокислота в положении 8 и одна, две или три аминокислоты, выбранные из группы, состоящей из аминокислоты в положении 9, в положении 11, в положении 12, в положении 16, в положении 18, в положении 22, в положении 23, в положении 24, в положении 26, в положении 27, в положении 30, в положении 31, в положении 33, в положении 34, в положении 35, в положении 36 и в положении 37, отличаются от аминокислоты, находящейся в соответствующем положении в нативном GLP-1(7-37)ОН.
Другие предпочтительные соединения формулы II включают
Val8-GLP-1(7-37)OH, Gly8-GLP-1(7-37)OH, Glu22-GLP-1(7-37)OH, Asp22-GLP-1(7-37)OH, Arg22-GLP-1(7-37)OH, Lys22-GLP-1(7-37)OH, Cys22-GLP-1(7-37)OH, Val8-Glu22-GLP-1(7-37)OH, Val8-Asp22-GLP-1(7-37)OH, Val8-Arg22-GLP-1(7-37)OH, Val8-Lys22-GLP-1(7-37)OH, Val8-Cys22-GLP-1(7-37)OH, Gly8-Glu22-GLP-1(7-37)OH, Gly8-Asp22-GLP-1(7-37)OH, Gly8-Arg22-GLP-1(7-37)OH, Gly8-Lys22-GLP-1(7-37)OH, Gly8-Cys22-GLP-1(7-37)OH, Glu22-GLP-1(7-36)OH, Asp22-GLP-1(7-36)OH, Arg22-GLP-1(7-36)OH, Lys22-GLP-1(7-36)OH, Cys22-GLP-1(7-36)OH, Val8-Glu22-GLP-1(7-36)OH, Val8-Asp22-GLP-1(7-36)OH, Val8-Arg22-GLP-1(7-36)OH, Val8-Lys22-GLP-1(7-36)OH, Val8-Cys22-GLP-1(7-36)OH, Gly8-Glu22-GLP-1(7-36)OH, Gly8-Asp22-GLP-1(7-36)OH, Gly8-Arg22-GLP-1(7-36)OH, Gly8-Lys22-GLP-1(7-36)OH, Gly8-Cys22-GLP-1(7-36)OH, Lys23-GLP-1(7-37)OH, Val8-Lys23-GLP-1(7-37)OH, Gly8-Lys23-GLP-1(7-37)OH, His24-GLP-1(7-37)OH, Val8-His24-GLP-1(7-37)OH, Gly8-His24-GLP-1(7-37)OH, Lys24-GLP-1(7-37)OH, Val8-Lys24-GLP-1(7-37)OH, Glu30-GLP-1(7-37)OH, Val8-Glu30-GLP-1(7-37)OH, Gly8-Glu30-GLP-1(7-37)OH, Asp30-GLP-1(7-37)OH, Val8-Asp30-GLP-1(7-37)OH, Gly8-Asp30-GLP-1(7-37)OH, Gln30-GLP-1(7-37)OH, Val8-Gln30-GLP-1(7-37)OH, Gly8-Gln30-GLP-1(7-37)OH, Tyr30-GLP-1(7-37)OH, Val8-Tyr30-GLP-1(7-37)OH, Gly8-Tyr30-GLP-1(7-37)OH, Ser30-GLP-1(7-37)OH, Val8-Ser30-GLP-1(7-37)OH, Gly8-Ser30-GLP-1(7-37)OH, His30-GLP-1(7-37)OH, Val8-His30-GLP-1(7-37)OH, Gly8-His30-GLP-1(7-37)OH, Glu34-GLP-1(7-37)OH, Val8-Glu34-GLP-1(7-37)OH, Gly8-Glu34-GLP-1(7-37)OH, Ala34-GLP-1(7-37)OH, Val8-Ala34-GLP-1(7-37)OH, Gly8-Ala34-GLP-1(7-37)OH, Gly34-GLP-1(7-37)OH, Val8-Gly34-GLP-1(7-37)OH, Gly8-Gly34-GLP-1(7-37)OH, Ala35-GLP-1(7-37)OH, Val8-Ala35-GLP-1(7-37)OH, Gly8-Ala35-GLP-1(7-37)OH, Lys35-GLP-1(7-37)OH, Val8-Lys35-GLP-1(7-37)OH, Gly8-Lys35-GLP-1(7-37)OH, His35-GLP-1(7-37)OH, Val8-His35-GLP-1(7-37)OH, Gly8-His35-GLP-1(7-37)OH, Pro35-GLP-1(7-37)OH, Val8-Pro35-GLP-1(7-37)OH, Gly8-Pro35-GLP-1(7-37)OH, Glu35-GLP-1(7-37)OH, Val8-Glu35-GLP-1(7-37)OH, Gly8-Glu35-GLP-1(7-37)OH, Val8-Ala27-GLP-1(7-37)OH, Val8-His37-GLP-1(7-37)OH, Val8-Glu22-Lys23-GLP-1(7-37)OH, Val8-Glu22-Glu23-GLP-1(7-37)OH, Val8-Glu22-Ala27-GLP-1(7-37)OH, Val8-Gly34-Lys35-GLP-1(7-37)OH, Gly8-His37-GLP-1(7-37)OH, Val8-Glu22-Ala27-GLP-1(7-37)OH, Gly8-Glu22-Ala27-GLP-1(7-37)OH, Val8-Lys22-Glu23-GLP-1(7-37)OH и Gly8-Lys22-Glu23-GLP-1(7-37)OH.
Другая предпочтительная группа аналогов и производных GLP-1 для использования по настоящему изобретению состоит из молекул формулы VI (SEQ ID NO: 7)
R1-X-Glu-Gly10-Thr-Phe-Thr-Ser-Asp15-Val-Ser-Ser-Tyr-Leu20-Y-Gly-Gln-Ala-Ala25-Lys-Z-Phe-Ile-Ala30-Trp-Leu-Val-Lys-Gly35-Arg-R2
Формула VI (SEQ ID NO: 7),
где R1 выбирают из группы, состоящей из L-гистидина, D-гистидина, дезаминогистидина, 2-аминогистидина, β-гидроксигистидина, гомогистидина, α-фторметилгистидина или α-метилгистидина;
X выбирают из группы, состоящей из Ala, Gly, Val, Thr, Ile и альфа-метил-Ala;
Y выбирают из группы, состоящей из Glu, Gln, Ala, Thr, Ser и Gly;
Z выбирают из группы, состоящей из Glu, Gln, Ala, Thr, Ser и Gly, и
R2 обозначает Gly-OH.
Другая предпочтительная группа соединений GLP-1 для использования по настоящему изобретению описана в WO 91/11457, которая состоит, по существу, из GLP-1(7-34), GLP-1(7-35), GLP-1(7-36) или GLP-1(7-37), или их амидной формы или их фармацевтически приемлемых солей, включает по меньшей мере одну модификацию, выбранную из группы, состоящей из:
(а) замещения лизина в положении 26 и/или в положении 34 глицином, серином, цистеином, треонином, аспарагином, глютамином, тирозином, аланином, валином, изолейцином, лейцином, метионином, фенилаланином, аргинином или D-лизином; или замещения аргинина в положении 36 глицином, серином, цистеином, треонином, аспарагином, глютамином, тирозином, аланином, валином, изолейцином, лейцином, метионином, фенилаланином, лизином или D-аргинином;
(b) замещения триптофана в положении 31 устойчивой к окислению аминокислотой;
(c) по меньшей мере одного из следующих замещений: валина в положении 16 тирозином; серина в положении 18 лизином; глютаминовой кислоты в положении 21 аспарагиновой кислотой; глицина в положении 22 серином; глютамина в положении 23 аргинином; аланина в положении 24 аргинином и лизина в положении 26 глютамином и
(d) по меньшей мере одного из следующих замещений: аланина в положении 8 глицином, серином или цистеином; глютаминовой кислоты в положении 9 аспарагиновой кислотой, глицином, серином, цистеином, треонином, аспарагином, глютамином, тирозином, аланином, валином, изолейцином, лейцином, метионином или фенилаланином; глицина в положении 10 серином, цистеином, треонином, аспарагином, глютамином, тирозином, аланином, валином, изолейцином, лейцином, метионином или фенилаланином, а также аспарагиновой кислоты в положении 15 глютаминовой кислотой; и
(е) замещения гистидина в положении 7 глицином, серином, цистеином, треонином, аспарагином, глютамином, тирозином, аланином, валином, изолейцином, лейцином, метионином или феналаланином или D- или N-ацилированной или алкилированной формой гистидина; причем в случае замещения по пунктам (a), (b), (d) и (e) замещенные аминокислоты могут быть необязательно в D-форме и аминокислоты, замещенные по положению 7, могут быть необязательно в N-ацилированной или N-алкилированной форме. Поскольку фермент дипептидил-пептидаза IV (ДПП IV) может быть ответственен за наблюдаемую быструю инактивацию in vivo введенного GLP-1 [см., например, Mentlein, R., et al., Eur. J. Biochem., 214:829-835 (1993)], аналоги GLP-1 и их производные, которые защищены от активности ДПП-IV за счет гибридного белка, являются предпочтительными, и гибридные белки, в которых соединение GLP-1 представляет собой Gly8-GLP-1(7-37)OH, Val8-GLP-1(7-37)OH, α-метил-Ala8-GLP-1(7-37)OH или Gly8-Gln21-GLP-1(7-37)OH, являются более предпочтительными. Другая предпочтительная группа соединений GLP-1 для использования по настоящему изобретению состоит из соединений формулы VII (SEQ ID NO: 8), заявленных в патенте США No. 5512549, который включен в настоящее описание в качеств ссылки.
R1-Ala-Glu-Gly10-Thr-Phe-Thr-Ser-Asp15-Val-Ser-Ser-Tyr-Leu20-Glu-Gly-Gln-Ala-Ala25-Xaa-Glu-Phe-Ile-Ala30-Trp-Leu-Val-Lys-Gly35-Arg-R3
Формула VII (SEQ ID NO:8),
где R1 выбирают из группы, состоящей из 4-имидазопропионила, 4-имидазоацетила или 4-имидазо-α, α-диметил-ацетила;
R2 выбирают из группы, состоящей из С6-С10 неразветвленного ацила, или отсутствует;
R3 выбирают из группы, состоящей из Gly-OH или NH2; и
Xaa обозначает Lys или Arg.
Более предпочтительные соединения формулы VII по настоящему изобретению включают такие соединения, в которых Xaa обозначает Arg и R2 обозначает С6-С10 неразветвленный ацил. Еще более предпочтительные соединения формулы IV для использования по настоящему изобретению представляют собой такие соединения, в которых Xaa обозначает Arg, R2 обозначает С6-С10 неразветвленный ацил и R3 обозначает Gly-OH. Другие очень предпочтительные соединения формулы IV для использования по настоящему изобретению представляют собой такие соединения, в которых Xaa обозначает Arg, R2 обозначает С6-С10 неразветвленный ацил, R3 обозначает Gly-OH и R1 обозначает 4-имидазопропионил. Особенно предпочтительное соединение формулы IV для использования по настоящему изобретению представляет собой такое соединение, в котором Xaa обозначает Arg, R2 обозначает С8 неразветвленный ацил, R3 обозначает Gly-OH и R1 обозначает 4-имидазопропионил.
Другие предпочтительные производные GLP-1 описаны в патенте США No. 6268343 B1. Более предпочтительным производным GLP-1 является Arg34Lys26-(N-ε-(γ-Glu(N-α-гексадеканоил)))-GLP-1(7-37).
Предпочтительно соединения GLP-1 включают аналоги GLP-1, причем скелет таких аналогов или их фрагментов содержит аминокислоту, отличную от аланина в положении 8 (положение 8 аналогов). Скелет может содержать в положении 7 L-гистидин, D-гистидин или модифицированные формы гистидина, такие как дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин. Предпочтительно, чтобы указанные аналоги в положении 8 содержали одну или более дополнительных замен в положениях 12, 16, 18, 19, 20, 22, 25, 27, 30, 33 и 37 относительно соответствующей аминокислоты в нативном GLP-1(7-37)OH. Более предпочтительно, чтобы указанное положение 8 в аналогах включало одну или более дополнительных замен в положениях 16, 18, 22, 25 и 33 в сравнении с соответствующей аминокислотой в нативном GLP-1(7-37)OH.
В предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 12 выбрана из группы, состоящей из триптофана или тирозина. Более предпочтительно, чтобы, дополнительно к замещению в положении 12, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно, валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 12 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 16 выбрана из группы, состоящей из триптофана, изолейцина, лейцина, фенилаланина или тирозина. Более предпочтительно, чтобы, дополнительно к замещению в положении 16, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 16 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 16 и 8, аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 16 и 8, аминокислота в положении 37 была замещена гистидином.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 18 выбрана из группы, состоящей из триптофана, тирозина, фенилаланина, лизина, лейцина или изолейцина, предпочтительно триптофана, тирозина и изолейцина. Более предпочтительно, чтобы, дополнительно к замещению в положении 18, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 18 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 18 и 8, аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 18 и 8, аминокислота в положении 37 была замещена гистидином.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 19 выбрана из группы, состоящей из триптофана или фенилаланина, предпочтительно триптофана. Более предпочтительно, чтобы, дополнительно к замещению в положении 19, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 19 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 19 и 8, аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 19 и 8, аминокислота в положении 37 была замещена гистидином.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 20 представляет собой фенилаланин, тирозин или триптофан. Более предпочтительно, чтобы, дополнительно к замещению в положении 20, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 20 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 20 и 8, аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 20 и 8, аминокислота в положении 37 была замещена гистидином.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 25 выбрана из группы, состоящей из валина, изолейцина и лейцина, предпочтительно валина. Более предпочтительно, чтобы, дополнительно к замещению в положении 25, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы в дополнение к замещению в положениях 25 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 25 и 8, аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 25 и 8, аминокислота в положении 37 была замещена гистидином.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 27 выбрана из группы, состоящей из изолейцина или аланина. Более предпочтительно, чтобы, дополнительно к замещению в положении 27, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 27 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 27 и 8, аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 27 и 8, аминокислота в положении 37 была замещена гистидином.
В другом предпочтительном варианте осуществления настоящего изобретения аналог GLP-1 представляет собой GLP-1(7-37)OH, в котором аминокислота в положении 33 представляет собой изолейцин. Более предпочтительно, чтобы, дополнительно к замещению в положении 33, аминокислота в положении 8 была замещена глицином, валином, лейцином, изолейцином, серином, треонином или метионином и более предпочтительно валином или глицином. Еще более предпочтительно, чтобы, дополнительно к замещению в положениях 33 и 8, аминокислота в положении 22 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 33 и 8 аминокислота в положении 30 была замещена глютаминовой кислотой. Предпочтительно также, чтобы, дополнительно к замещению в положениях 33 и 8, аминокислота в положении 37 была замещена гистидином.
Соединения GLP-1 содержат модификации в одном или более из указанных положений: 8, 12, 16, 18, 19, 20, 22, 25, 27, 30, 33 и 37. Указанные соединения GLP-1 демонстрируют повышенную эффективность в сравнении с GLP-1(7-37)OH и включают аминокислотную последовательность формулы VIII (SEQ ID NO:9)
Xaa7-Xaa8-Glu-Gly-Thr-Xaa12-Thr-Ser-Asp-Xaa16-Ser-Xaa18-Xaa19-Xaa20-Glu-Xaa22-Gln-Ala-Xaa25-Lys-Xaa27-Phe-Ile-Xaa30-Trp-Leu-Xaa33-Lys-Gly-Arg-Xaa37.
Формула VIII (SEQ ID NO:9),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Ala, Gly, Val, Leu, Ile, Ser или Thr;
Xaa12 обозначает Phe, Trp или Tyr;
Xaa16 обозначает Val, Trp, Ile, Leu, Phe или Tyr;
Xaa18 обозначает Ser, Trp, Tyr, Phe, Lys, Ile, Leu, Val.
Xaa19 обозначает Tyr, Trp или Phe;
Xaa20 обозначает Leu, Phe, Tyr или Trp;
Xaa22 обозначает Gly, Glu, Asp или Lys;
Xaa25 обозначает Ala, Val, Ile или Leu;
Xaa27 обозначает Glu, Ile или Ala;
Xaa30 обозначает Ala или Glu;
Xaa33 обозначает Val или Ile; и
Xaa34 обозначает Gly, His, NH2 или отсутствует.
Некоторые предпочтительные соединения GLP-1 формулы VIII включают:
GLP-1(7-37)OH, GLP-1(7-36)NH2, Gly8-GLP-1(7-37)OH, Gly8-GLP-1(7-36)NH2, Val8-GLP-1(7-37)OH, Val8-GLP-1(7-36)NH2, Leu8-GLP-1(7-37)OH, Leu8-GLP-1(7-36)NH2, Ile8-GLP-1(7-37)OH, Ile8-GLP-1(7-36)NH2, Ser8-GLP-1(7-37)OH, Ser8-GLP-1(7-36)NH2, Thr8-GLP-1(7-37)OH, Thr8-GLP-1(7-36)NH2, Val8-Tyr12-GLP-1(7-37)OH, Val8-Tyr12 GLP-1(7-36)NH2, Val8-Tyr16-GLP-1(7-37)OH, Val8-Tyr16 GLP-1(7-36)NH2, Val8-Glu22-GLP-1(7-37)OH, Val8-Glu22-GLP-1(7-36)NH2, Gly8-Glu22-GLP-1(7-37)OH, Gly8-Glu22-GLP-1(7-36)NH2, Val8-Asp22-GLP-1(7-37)OH, Val8-Asp22-GLP-1(7-36)NH2, Gly8-Asp22-GLP-1(7-37)OH, Gly8-Asp22-GLP-1(7-36)NH2, Val8-Lys22-GLP-1(7-37)OH, Val8-Lys22-GLP-1(7-36)NH2, Gly8-Lys22-GLP-1(7-37)OH, Gly8-Lys22-GLP-1(7-36)NH2, Leu8-Glu22-GLP-1(7-37)OH, Leu8-Glu22-GLP-1(7-36)NH2, Ile8-Glu22-GLP-1(7-37)OH, Ile8-Glu22-GLP-1(7-36)NH2, Leu8-Asp22-GLP-1(7-37)OH, Leu8-Asp22-GLP-1(7-36)NH2, Ile8-Asp22-GLP-1(7-37)OH, Ile8-Asp22-GLP-1(7-36)NH2, Leu8-Lys22-GLP-1(7-37)OH, Leu8-Lys22-GLP-1(7-36)NH2, Ile8-Lys22-GLP-1(7-37)OH, Ile8-Lys22-GLP-1(7-36)NH2, Ser8-Glu22-GLP-1(7-37)OH, Ser8-Glu22-GLP-1(7-36)NH2, Thr8-Glu22-GLP-1(7-37)OH, Thr8-Glu22-GLP-1(7-36)NH2, Ser8-Asp22-GLP-1(7-37)OH, Ser8-Asp22-GLP-1(7-36)NH2, Thr8-Asp22-GLP-1(7-37)OH, Thr8-Asp22-GLP-1(7-36)NH2, Ser8-Lys22-GLP-1(7-37)OH, Ser8-Lys22-GLP-1(7-36)NH2, Thr8-Lys22-GLP-1(7-37)OH, Thr8-Lys22-GLP-1(7-36)NH2, Glu22-GLP-1(7-37)OH, Glu22-GLP-1(7-36)NH2, Asp22-GLP-1(7-37)OH, Asp22-GLP-1(7-36)NH2, Lys22-GLP-1(7-37)OH, Lys22-GLP-1(7-36)NH2, Val8-Ala27-GLP-1(7-37)OH, Val8-Glu22-Ala27-GLP-1(7-37)OH, Val8-Glu30-GLP-1(7-37)OH, Val8-Glu30-GLP-1(7-36)NH2, Gly8-Glu30-GLP-1(7-37)OH, Gly8-Glu30-GLP-1(7-36)NH2, Leu8-Glu30-GLP-1(7-37)OH, Leu8-Glu30-GLP-1(7-36)NH2, Ile8-Glu30-GLP-1(7-37)OH, Ile8-Glu30-GLP-1(7-36)NH2, Ser8-Glu30-GLP-1(7-37)OH, Ser8-Glu30-GLP-1(7-36)NH2, Thr8-Glu30-GLP-1(7-37)OH, Thr8-Glu30-GLP-1(7-36)NH2, Val8-His37-GLP-1(7-37)OH, Val8-His37-GLP-1(7-36)NH2, Gly8-His37-GLP-1(7-37)OH, Gly8-His37-GLP-1(7-36)NH2, Leu8-His37-GLP-1(7-37)OH, Leu8-His37-GLP-1(7-36)NH2, Ile8-His37-GLP-1(7-37)OH, Ile8-His37-GLP-1(7-36)NH2, Ser8-His37-GLP-1(7-37)OH, Ser8-His37-GLP-1(7-36)NH2, Thr8-His37-GLP-1(7-37)OH, Thr8-His37-GLP-1(7-36)NH2.
Некоторые предпочтительные соединения GLP-1 формулы VIII, содержащие множественные замещения, включают GLP-1(7-37)OH, в которых положение 8 занято валином или глицином, положение 22 занято глютаминовой кислотой, положение 16 занято тирозином, лейцином или триптофаном, положение 18 занято тирозином, триптофаном или изолейцином, положение 25 занято валином и положение 33 занято изолейцином. Другие предпочтительные соединения GLP-1 включают следующие:
Val8-Tyr16-GLP-1(7-37)OH, Val8-Tyr12-Glu22-GLP-1(7-37)OH, Val8-Tyr16-Phe19-GLP-1(7-37)OH, Val8-Tyr16-Glu22-GLP-1(7-37)OH, Val8-Trp16-Glu22-GLP-1(7-37)OH, Val8-Leu16-Glu22-GLP-1(7-37)OH, Val8-Ile16-Glu22-GLP-1(7-37)OH, Val8-Phe16-Glu22-GLP-1(7-37)OH, Val8-Trp18-Glu22-GLP-1(7-37)OH, Val8-Tyr18-Glu22-GLP-1(7-37)OH, Val8-Phe18-Glu22-GLP-1(7-37)OH, Val8-Ile18-Glu22-GLP-1(7-37)OH.
Соединения GLP-1 по настоящему изобретению также включают соединения эксендина. Эксендин-3 и эксендин-4 представляют собой биологически активные пептиды, впервые выделенные из яда ящерицы Helodermatidae, в отношении которых было показано, что они связываются с рецептором GLP-1 и стимулируют цАМФ-зависимое образование Н+ в обкладочных клетках млекопитающих. Эксендин-3 и эксендин-4 - оба представляют собой пептиды из 39 аминокислот, которые характеризуются примерно 53% гомологией с GLP-1. Они действуют как мощные агонисты активности GLP-1. Существенно, что усеченное по N-концу производное эксендина, известное как эксендин(9-39 аминокислот), представляет собой ингибитор эксендина-3, эксендина-4 и GLP-1.
Эксендиновое соединение включает в типичном случае полипептид, имеющий аминокислотную последовательность эксендина-3, эксендина-4 или их аналога или фрагмента. Эксендин-3 и эксендин-4 описаны в патенте США No. 5424286.
Эксендин-3 имеет аминокислотную последовательность SEQ ID NO: 10:
His7-Ser-Asp-Gly10-Thr-Phe-Thr-Ser-Asp15-Leu-Ser-Lys-Gln-Met20-Glu-Glu-Glu-Ala-Val25-Arg-Leu-Phe-Ile-Glu30-Trp-Leu-Lys-Asn-Gly35-Gly-Pro-Ser-Ser-Gly40-Ala-Pro-Pro-Pro-Ser45-NH2.
(SEQ ID NO:10)
Эксендин-4 имеет аминокислотную последовательность SEQ ID NO: 11:
His7-Gly-Glu-Gly10-Thr-Phe-Thr-Ser-Asp15-Leu-Ser-Lys-Gln-Met20-Glu-Glu-Glu-Ala-Val25-Arg-Leu-Phe-Ile-Glu30-Trp-Leu-Lys-Asn-Gly35-Gly-Pro-Ser-Ser-Gly40-Ala-Pro-Pro-Pro-Ser45-NH2.
(SEQ ID NO:11)
Соединения GLP-1 также включают фрагменты эксендина, которые представляют собой полипептиды, полученные после усечения за счет удаления одной или более аминокислот с N-конца и/или С-конца эксендина или аналога эксендина. Кроме того, соединения GLP-1 включают полипептиды эксендина, в которых одна или более аминокислот добавлены к N-концу и/или С-концу эксендина его фрагментов. Соединения эксендина указанного типа содержат примерно до сорока пяти аминокислот.
Соединения GLP-1 также включают аналоги эксендина. Аналог эксендина характеризуется достаточной степенью гомологии с эксендином-3, эксендином-4 или их фрагментом, так что указанный аналог обладает инсулинотропной активностью. Активность фрагментов и/или аналогов эксендина может быть определена в тестах in vitro, таких как тесты, описанные в примере 1.
Предпочтительно, аналог эксендина имеет аминокислотную последовательность эксендина-4 или его фрагмента, модифицированную таким образом, что одна, две, три, четыре или пять аминокислот отличается(ются) от аминокислоты, находящейся в соответствующем положении в эксендине-4 или во фрагменте эксендина-4. В номенклатуре, используемой для обозначения соединений эксендина, замещающая аминокислота и ее положение указываются перед исходной структурой. Например, Val8-эксендин-4 обозначает соединение эксендина, в котором глицин, обычно находящийся в положении 8 эксендина-4, замещен валином.
Другая предпочтительная группа соединений GLP-1 состоит из аналогов GLP-1/эксендина-4 формулы IX (SEQ ID NO:12).
Xaa7-Xaa8-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Xaa16-Ser-Xaa18-Xaa19-Xaa20-Glu-Xaa22-Xaa23-Ala-Xaa25-Xaa26-Xaa27-Phe-Ile-Xaa30-Trp-Leu-Xaa33-Xaa34-Gly-Xaa36-R37
Формула IX (SEQ ID NO:12),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Gly, Ala или Val;
Xaa16 обозначает Leu или Val;
Xaa18 обозначает Lys или Ser;
Xaa19 обозначает Gln или Tyr;
Xaa20 обозначает Met или Leu;
Xaa22 обозначает Glu или Gln;
Xaa23 обозначает Glu или Gln;
Xaa25 обозначает Val или Ala;
Xaa26 обозначает Arg или Lys;
Xaa27 обозначает Leu или Glu;
Xaa30 обозначает Glu или Ala;
Xaa33 обозначает Val или Lys;
Xaa34 обозначает Asn или Lys;
Xaa36 обозначает Gly или Arg; и
R37 обозначает Gly, Pro, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser или отсутствует.
Другие аналоги эксендина, которые используются по настоящему изобретению, описаны в патентных публикациях РСТ WO 99/25728 (Beeley et al.); WO 99/25727 (Beeley et al.); WO 98/05351 (Young et al.); WO 99/40788 (Young et al.); WO 99/07404 (Beeley et al.) и WO 99/43708 (Knudsen et al.).
Другая предпочтительная группа соединений GLP-1 имеет аминокислотную последовательность формулы X (SEQ ID NO: 13)
Xaa7-Xaa8-Glu-Gly-Thr-Xaa12-Thr-Ser-Asp-Xaa16-Ser-Xaa18-Xaa19-Xaa20-Glu-Xaa22-Gln-Ala-Xaa25-Lys-Xaa27-Phe-Ile-Xaa30-Trp-Leu-Xaa33-Xaa34-Gly-Xaa36-Xaa37-Xaa38-Xaa39-Xaa40-Xaa41-Xaa42-Xaa43-Xaa44-Xaa45-Xaa46-Xaa47
Формула X (SEQ ID NO:13),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Ala, Gly, Val, Leu, Ile, Ser или Thr;
Xaa12 обозначает Phe, Trp или Tyr;
Xaa16 обозначает Val, Trp, Ile, Leu, Phe или Tyr;
Xaa18 обозначает Ser, Trp, Tyr, Phe, Lys, Ile, Leu, Val;
Xaa19 обозначает Tyr, Trp или Phe;
Xaa20 обозначает Leu, Phe, Tyr или Trp;
Xaa22 обозначает Gly, Glu, Asp или Lys;
Xaa25 обозначает Ala, Val, Ile или Leu;
Xaa27 обозначает Glu, Ile или Ala;
Xaa30 обозначает Ala или Glu;
Xaa33 обозначает Val или Ile;
Xaa34 обозначает Lys, Asp, Arg или Glu;
Xaa36 обозначает Gly, Pro, или Arg;
Xaa37 обозначает Gly, Pro или Ser;
Xaa38 обозначает Ser, Pro или His;
Xaa39 обозначает Ser, Arg, Thr, Trp или Lys;
Xaa40 обозначает Ser или Gly;
Xaa41 обозначает Ala, Asp, Arg, Glu, Lys или Gly;
Xaa42 обозначает Pro, Ala, NH2 или отсутствует;
Xaa43 обозначает Pro, Ala, NH2 или отсутствует;
Xaa44 обозначает Pro, Ala, Arg, Lys, His, NH2 или отсутствует;
Xaa45 обозначает Ser, His, Pro, Lys, Arg, NH2 или отсутствует;
Xaa46 обозначает His, Ser, Arg, Lys, NH2 или отсутствует и
Xaa47 обозначает His, Ser, Arg, Lys, NH2 или отсутствует;
при условии, что если Xaa42, Xaa43, Xaa44, Xaa45, Xaa46 или Xaa47 отсутствует, каждая аминокислота вниз по ходу транскрипции также отсутствует, и дополнительно, при условии, что пептид GLP-1 не имеет указанную ниже С-концевую аминокислотную последовательность, начинающуюся с Xaa36: Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-NH2.
Другая предпочтительная группа соединений GLP-1 имеет аминокислотную последовательность формулы XI (SEQ ID NO: 14)
Xaa7-Xaa8-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Xaa16-Ser-Ser-Tyr-Lys-Glu-Xaa22-Gln-Ala-Xaa25-Lys-Glu-Phe-Ile-Ala-Trp-Leu-Xaa33-Xaa34-Gly-Xaa36-Xaa37-Xaa38-Xaa39-Xaa40-Xaa41-Xaa42-Xaa43-Xaa44-Xaa45-Xaa46-Xaa47
Формула XI (SEQ ID NO:14),
где Xaa7 обозначает L-гистидин, D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин или α-метилгистидин;
Xaa8 обозначает Gly, Val, Leu, Ile, Ser или Thr;
Xaa16 обозначает Val, Trp, Ile, Leu, Phe или Tyr;
Xaa22 обозначает Gly, Glu, Asp или Lys;
Xaa25 обозначает Ala, Val, Ile или Leu;
Xaa33 обозначает Val или Ile;
Xaa34 обозначает Lys, Asp, Arg или Glu;
Xaa36 обозначает Gly, Pro, или Arg;
Xaa37 обозначает Gly, Pro или Ser;
Xaa38 обозначает Ser, Pro или His;
Xaa39 обозначает Ser, Arg, Thr, Trp или Lys;
Xaa40 обозначает Ser или Gly;
Xaa41 обозначает Ala, Asp, Arg, Glu, Lys или Gly;
Xaa42 обозначает Pro или Ala;
Xaa43 обозначает Pro или Ala;
Xaa44 обозначает Pro, Ala, Arg, Lys, His, NH2 или отсутствует;
Xaa45 обозначает Ser, His, Pro, Lys, Arg, NH2 или отсутствует;
Xaa46 обозначает His, Ser, Arg, Lys, NH2 или отсутствует и
Xaa47 обозначает His, Ser, Arg, Lys, NH2 или отсутствует;
при условии, что если Xaa44, Xaa45, Xaa46 или Xaa47 отсутствует, каждая аминокислота вниз по ходу транскрипции также отсутствует, и далее, при условии, что пептид GLP-1 не имеет указанную ниже С-концевую аминокислотную последовательность, начинающуюся с Xaa36: Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-NH2.
Предпочтительные варианты формулы Х и формулы XI включают соединения GLP-1, которые в положении 8 содержат валин или глицин и в положении 22 содержат глютаминовую кислоту.
Средства для доставки, подходящие для использования по настоящему изобретению
Средства для доставки по настоящему изобретению могут быть получены методами органической химии, известными в данной области техники и описанными в WO 90/36480, WO 96/30036, патент США No. 5643957; патент США No. 6242495, которые полностью включены в настоящее описание в качестве ссылки.
Многие из средств для доставки по настоящему изобретению могут быть легко получены из аминокислот, которые включают, не ограничиваясь приведенным списком, аминокаприловую кислоту, бутирилгидроксаминовую кислоту, аминофенилмасляную кислоту, аминофенилгексановую кислоту, аминофенилпропионовую кислоту, аминосалициловую кислоту, аминофенилянтарную кислоту, аминононановую кислоту, аминоникотиновую кислоту, аминоваленовую кислоту, аминофенилуксусную кислоту, аминокапроновую кислоту, аминоундекановую кислоту, аминогептановую кислоту, аминогидроксибензойную кислоту и аминодекановую кислоту.
В качестве примера можно отметить, что указанные средства для доставки могут быть получены при взаимодействии одной кислоты с соответствующим агентом, который взаимодействует со свободной аминогруппировкой, имеющейся в аминокислотах, с образованием амидов. Могут использоваться известные специалистам в данной области защитные группы для предупреждения нежелательных побочных реакций.
Средства для доставки могут быть очищены путем рекристаллизации или путем фракционирования на колонке с твердым наполнителем. Подходящие системы растворителей для проведения рекристаллизации включают ацетонитрил, метанол и тетрагидрофуран. Фракционирование может проводиться на подходящих колонках с твердым наполнителем, таким как глинозем, с использованием смесей метанол/н-пропанол в качестве мобильной фазы; в колонках с обращением фазы с использованием смесей трифторуксусная кислота/ацетонитрил в качестве мобильной фазы; и посредством ионообменной хроматографии с использованием воды в качестве мобильной фазы. При проведении анионообменной хроматографии используют предпочтительно градиент хлорида натрия от 0 до 500 мМ.
Полезные для использования в рамках настоящего изобретения средства для доставки описаны в патентах США No. 5541155, 5693338, 5976569, 5643957, 5955503, 6100298, 5650386, 5866536, 5965121, 5989539, 6001347, 6071510, 5820881 и 6242495, а также в WO 02/02509, WO 01/51454, WO 01/44199, WO 01/32130, WO 00/59863, WO 00/50386, WO 00/47188 и WO 00/40203, которые включены в настоящее описание в качестве ссылки. Для специалиста в данной области понятно, что могут быть внесены вариации в средства для доставки с целью использования в настоящем изобретении.
Примеры средств для доставки описаны в Таблице 1. Предпочтительные средства для доставки, указанные в Таблице 1, включают средства под номерами 1, 2, 4, 5, 6, 9, 10, 11, 13, 14, 15, 20, 21, 22, 23, 24, 26, 28, 30, 31, 35, 36, 38, 39, 40, 41, 42, 43, 44, 46, 51, 52 и 54.
Таблица 1.
Средство для доставки
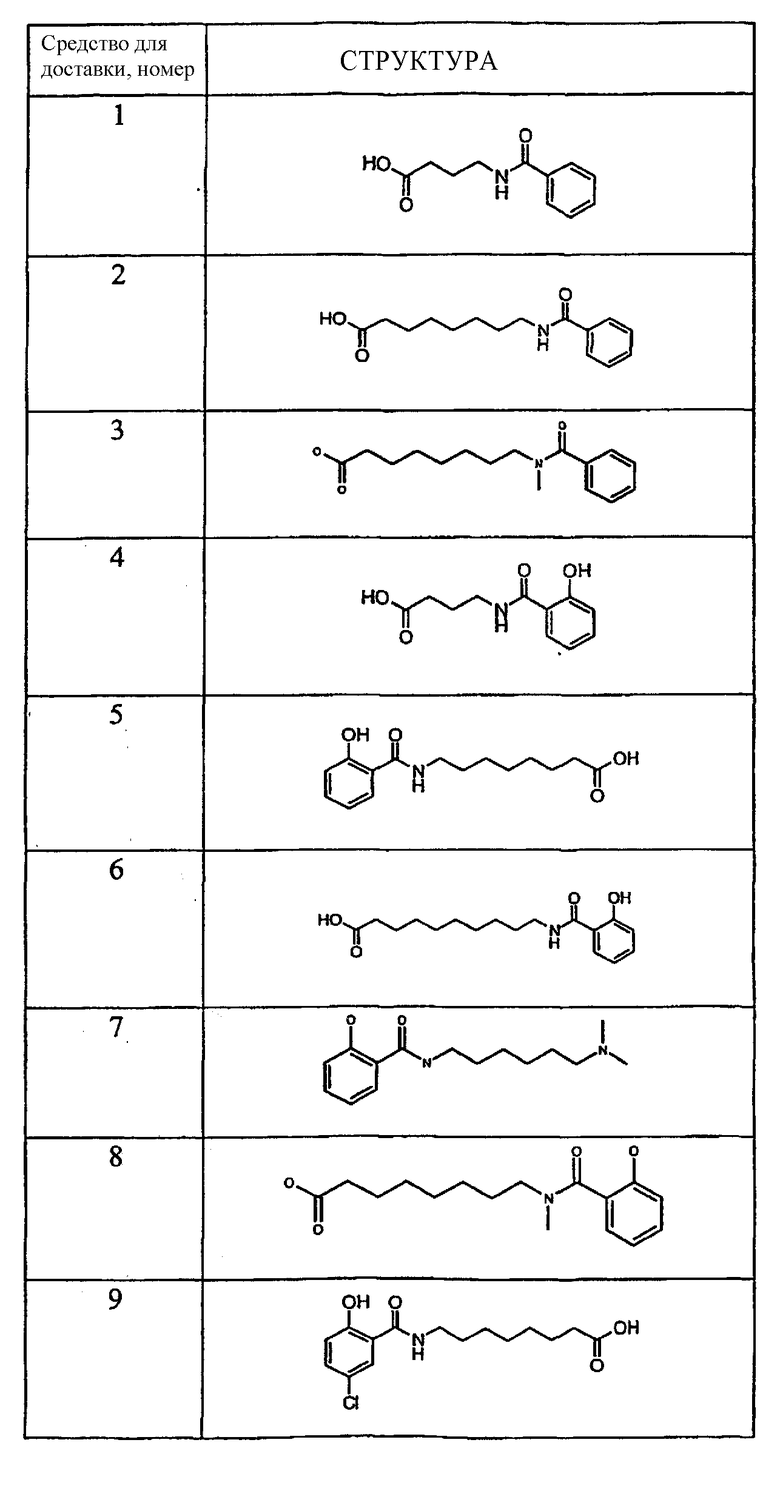
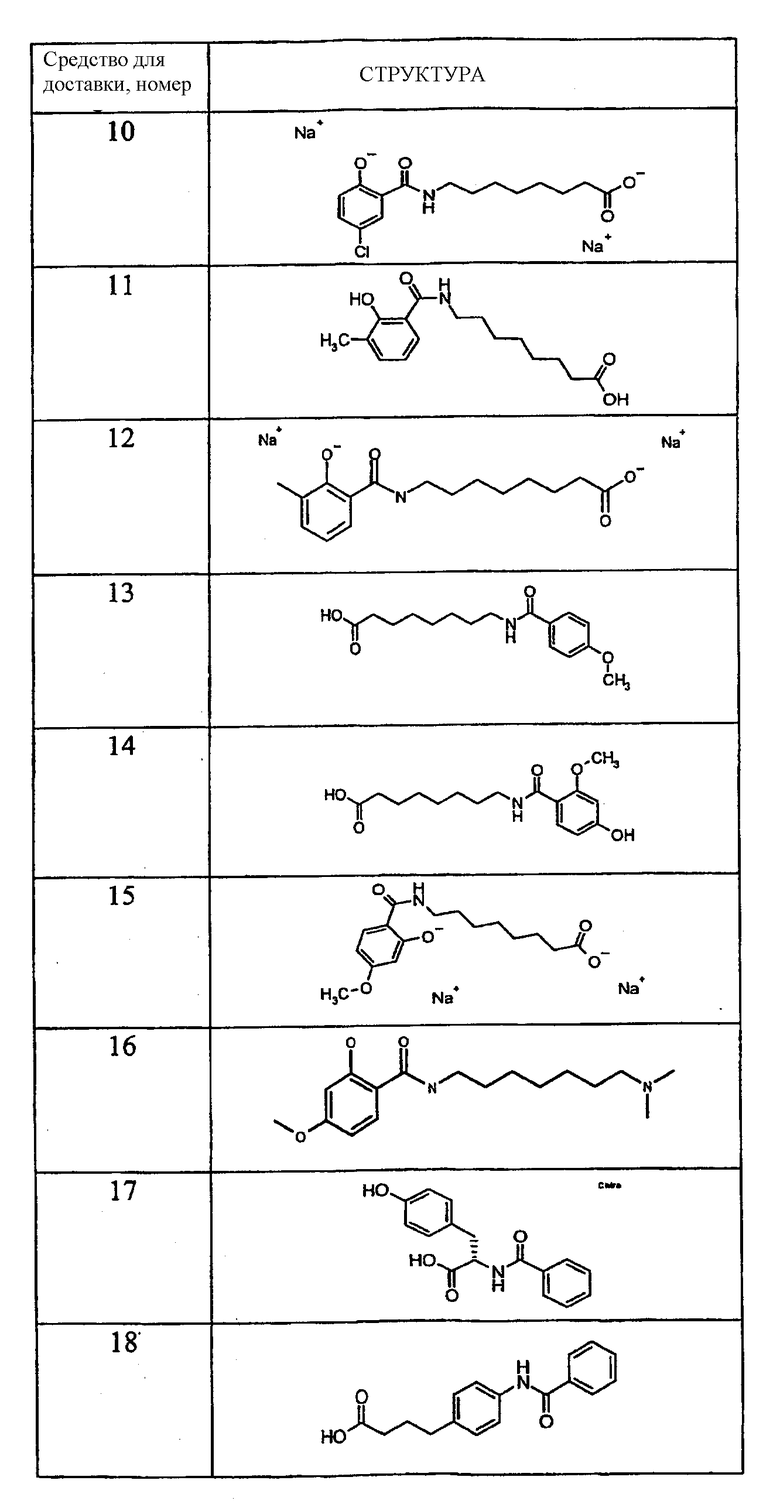
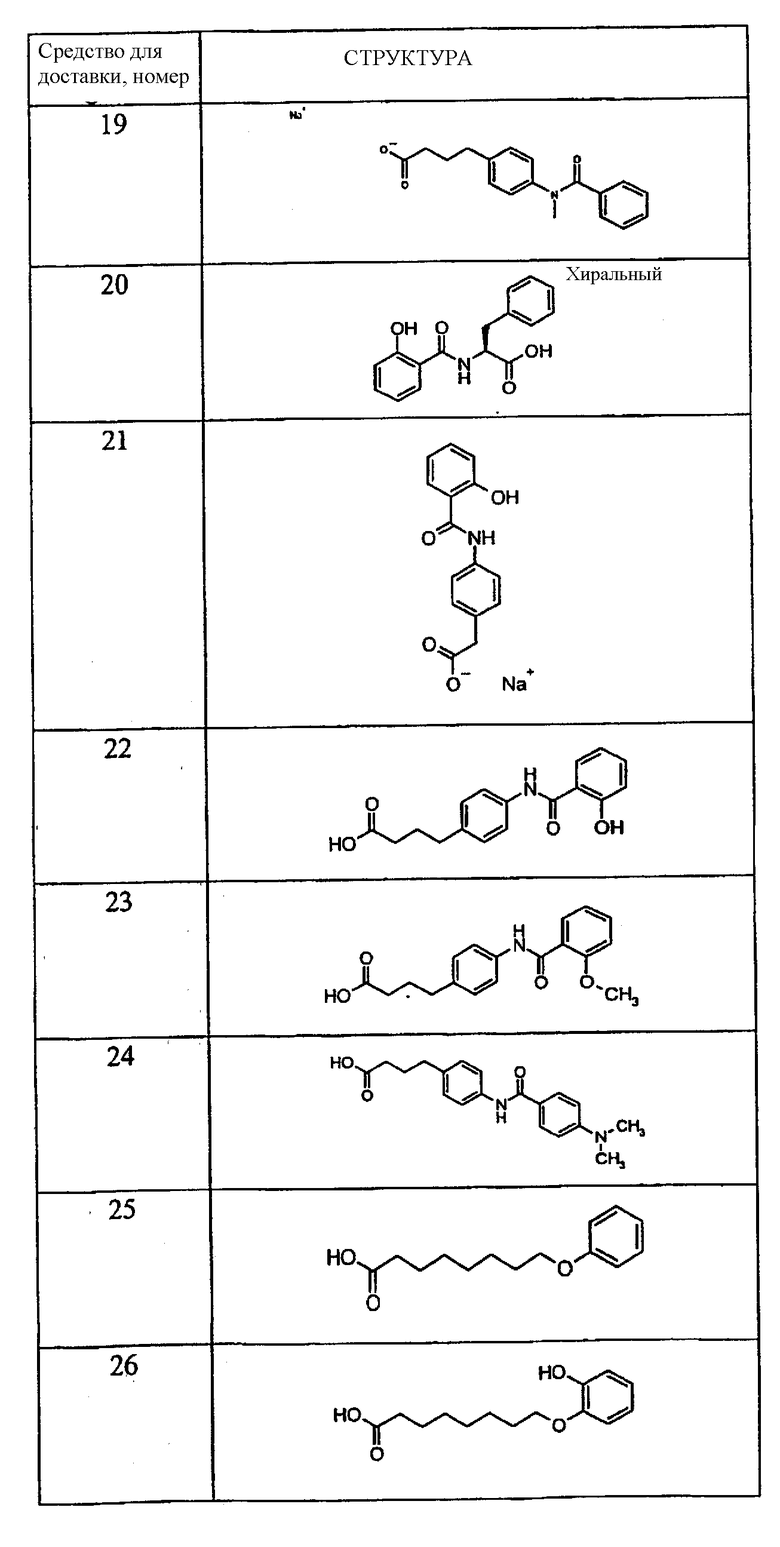
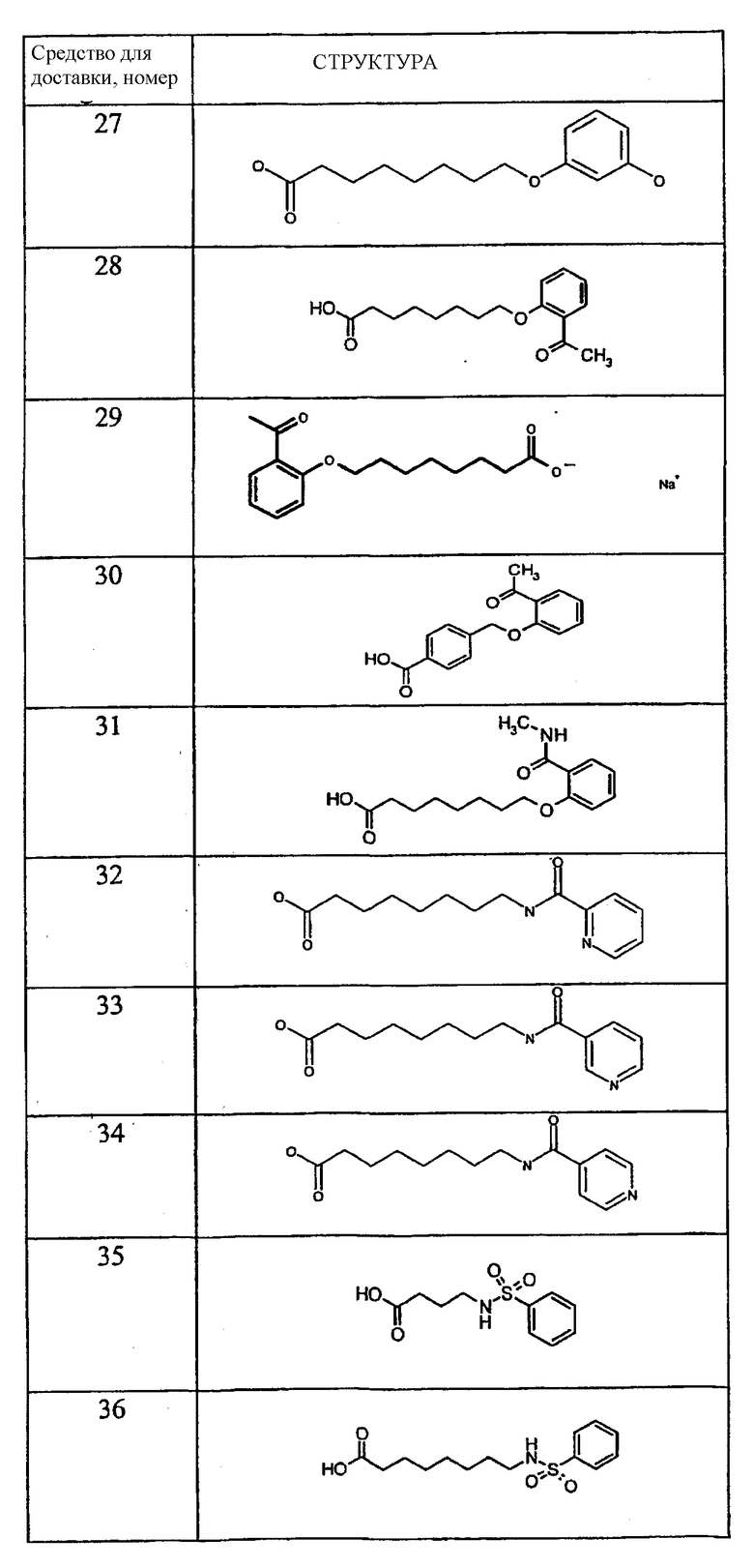
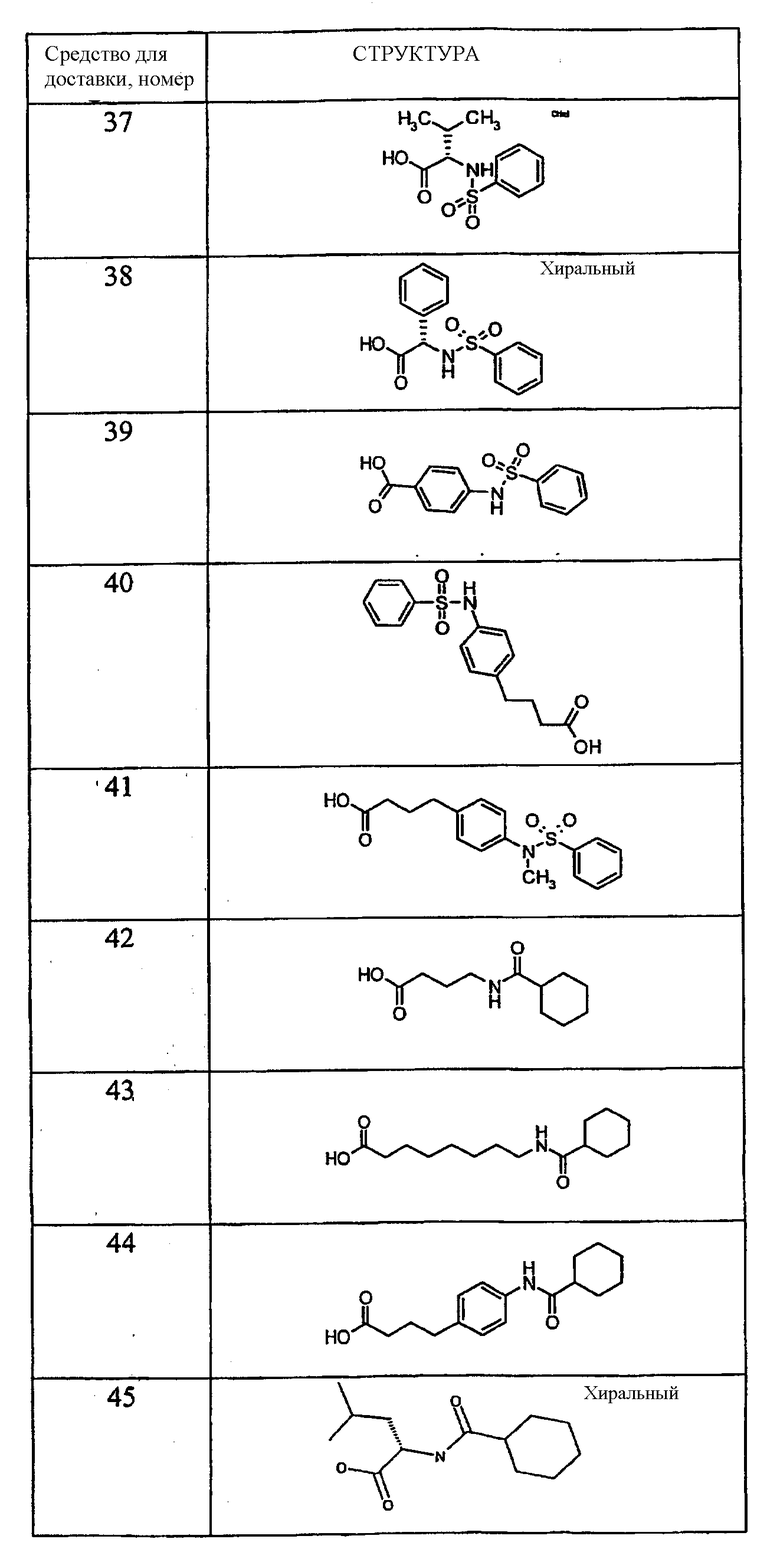
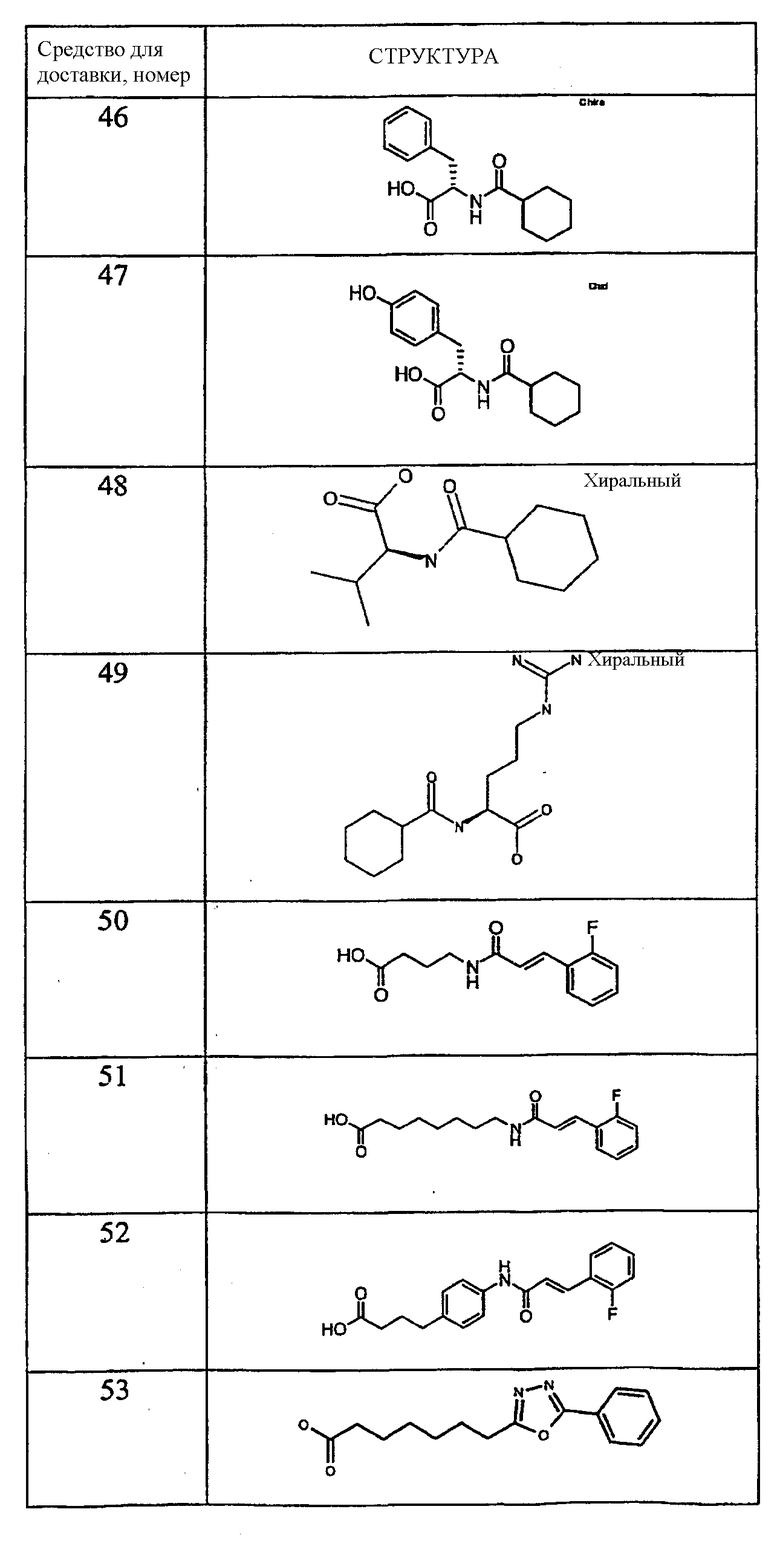
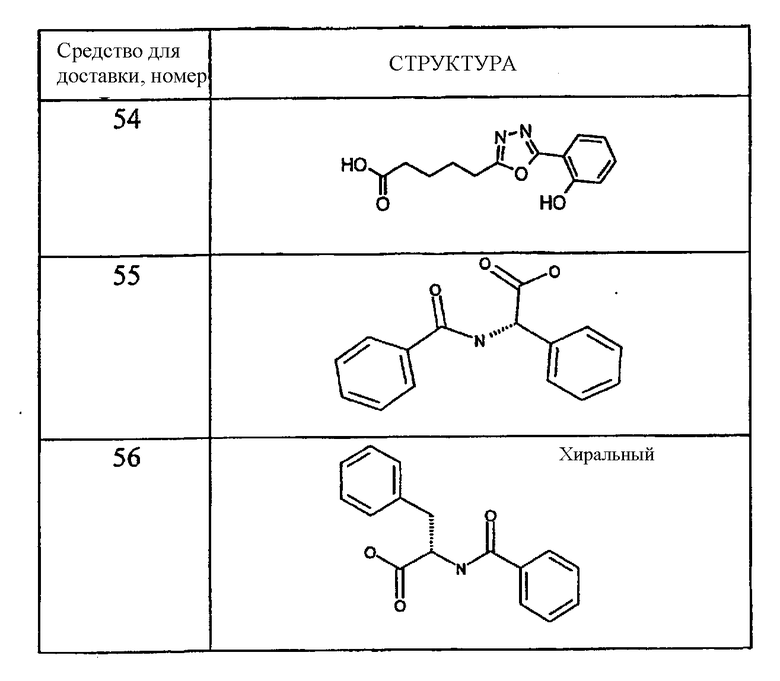
Пероральные композиции, включающие соединение GLP-1 и средство для доставки могут, использоваться для лечения широкого круга заболеваний. Соединения GLP-1 в основном проявляют биологический эффект за счет воздействия на рецептор GLP-1. Субъекты с заболеваниями и/или состояниями, которые благоприятно отвечают на стимуляцию рецептора GLP-1 или на введение соединений GLP-1, могут подвергаться лечению пероральными композициями по настоящему изобретению. Об указанных субъектах говорят, что они «нуждаются в лечении соединениями GLP-1» или «нуждаются в стимуляции рецептора GLP-1». В группы указанных субъектов входят пациенты с инсулиннезависимым диабетом, пациенты с инсулинзависимым диабетом, пациенты после перенесенного инсульта (см. WO 00/16797), пациенты после инфаркта миокарда (см. WO 98/08531), пациенты с ожирением (см. WO 98/19698), пациенты с катаболическими изменениями после проведенного хирургического вмешательства (см. патент США 6 006 753), пациенты с функциональной диспепсией и синдромом раздражения кишечника (см. WO 99/64060). В указанную группу включаются также субъекты, нуждающиеся в профилактическом лечении соединением GLP-1, то есть субъекты с риском развития инсулиннезависимого диабета (см. WO 00/07617). Субъекты с нарушенной толерантностью к глюкозе или с измененным уровнем глюкозы при анализе натощак, субъекты, вес тела которых примерно на 25% превышает нормальный вес тела субъектов их роста и телосложения, субъекты с частичной панкреатектомией, субъекты, имеющие одного или более из родителей с заболеванием инсулиннезависимым диабетом, субъекты, имевшие диабет при беременности, и субъекты с острым или хроническим панкреатитом. Все они имеют риск развития инсулиннезависимого диабета.
Настоящее изобретение может быть лучше пояснено со ссылками на приведенные ниже примеры. Указанные примеры даны для иллюстрации конкретных вариантов осуществления настоящего изобретения и не должны рассматриваться как ограничивающие область настоящего изобретения.
ПРИМЕРЫ
Пример 1
Определение инсулинотропной активности
Продукт расщепления ткани поджелудочной железы коллагеназой отделяют в градиенте Фиколла (27%, 23%, 20,5% и 11% в сбалансированном солевом растворе Хэнкса, pH 7,4). Островковые клетки собирают из промежуточного слоя с концентрацией 20,5%/11%, промывают и под стереомикроскопом освобождают от экзокринной и другой ткани. Островковые клетки инкубируют в течение ночи в среде RPMI 1640 с добавкой 10% фетальной сыворотки теленка и содержанием 11 мМ глюкозы при 37°С в атмосфере 95% воздуха/5% CO2. Исследуемое соединение GLP-1 готовят в диапазоне концентраций, предпочтительно от 3 наномолей до 30 наномолей в среде RPMI, содержащей 10% фетальной сыворотки теленка и 16,7 мМ глюкозы. Затем пипеткой переносят примерно 8-10 выделенных островковых клеток в ячейки 96-ячеечных микротитрационных планшетов, содержащих в общем объемом 250 мкл соединение GLP-1 в среде. Островковые клетки инкубируют в присутствии соединения GLP-1 при 37°С с содержанием 95% воздуха, 5% CO2 в течение 90 минут. Отбирают аликвоты среды без островковых клеток, используя по 100 мкл для определения количества имеющегося инсулина методом радиоиммуноанализа с использованием набора Equate Insulin RIA Kit (Binax, Inc., Portland, ME).
Пример 2
Стабильность GLP-1 в присутствии ДПП IV
Стабильность каждой молекулы GLP-1 может быть определена при инкубации молекулы GLP-1 в человеческой плазме. Плазму (800 мкл), полученную от здоровых добровольцев, инкубируют при 37°С с 300 пмоль/л молекулы GLP-1 в течение периода времени до шести часов. Затем проводят ВЭЖХ с обращением фаз и РИА по методу Дикона с соавт. (Deacon, et al., in J. Clin. Endocrinol. Metab. 80: 952-957 (1995).
Пример 3
Композиция средства для доставки номер 15
Примерно 600 мг средства для доставки номер 15 взвешивают в стеклянный флакон типа I, к которому добавляют 3 мл основания (0,1н NaOH, pH 12,7) до конечной концентрации 200 мг/мл. Доводят значение pH до 7,1 и определяют концентрацию, которая должна составлять 171 мг/мл. Затем средство для доставки No 15 разбавляют до концентрации 150 мг/мл с использованием воды Milli-Q®.
Пример 4
Композиция средства для доставки номер 40
Средства для доставки номера 40 и 9 являются нерастворимыми при желательной концентрации 150 мг/мл, используемой в примере 1. Дальнейшее разбавление основанием до pH 11,5 также не приводит к достижению желательной концентрации 150 мг/мл. Добавление сорастворителей также не приводит к солюбилизации с достижением желательной концентрации 150 мг/мл ни одного из средств для доставки. Исследуемые сорастворители включают этанол, N-метилпирролидон, N,N-диметилацетамид, N,N-диметилформамид, глюкофурол, этоксидиол, пропиленгликоль, полиэтиленгликоль 300 и поливинилпирролидон.
Средство для доставки номер 40 взвешивают в количестве 150 мг во флакон типа I, к которому добавляют 1 мл воды Milli-Q® и доводят значение pH до 12,7 с помощью 10 н NaOH. При использовании такой процедуры достигается концентрация 150 мг/мл в растворе средства для доставки номер 40 (pH 8,22).
Пример 5
Композиция средства для доставки номер 9
В связи с нерастворимостью в воде средства для доставки номер 9, готовят композицию в виде суспензии в 4% (вес/объем) (водном) средстве для суспендирования в гидроксипропилметилцеллюлозе (Klucel®). Примерно 1,7 мл средства для суспендирования добавляют в стеклянный флакон типа I, содержащий 300 мг средства для доставки номер 9. Препарат охлаждают на льду в течение 3 минут и затем пробу обрабатывают ультразвуком на льду в течение 30 минут с использованием устройства Misonix Sonicator® Ultrasonic Processor XL (микронаконечник 3/16 дюйма). Обработка ультразвуком приводит к снижению среднего размера частиц средства для доставки номер 9 с 48 мкм до 8 мкм (анализатор для определения размера частиц Coulter® LS) при pH 7,98. Далее композицию разбавляют средством для доставки до концентрации 150 мг/мл.
Пример 6
Другие средства для доставки
Все другие средства для доставки готовят по методике, описанной в примерах 3 и 4, за и исключением того, что средства для доставки с номерами 10, 11, 12, 16, 18, 22, 25, 27, 33 и 52 получают по методике, описанной в примере 5. Средство для доставки 46 и 54 готовят в виде двух отдельных композиций: одну по процедуре примера 3 или 4, а вторую - по процедуре примера 5.
Пример 7
Исследование стабильности
Исследование стабильности проводят с использованием средств для доставки номера 9, 15 и 40. Получают свежеприготовленное средство для доставки в соответствии с описанными выше процедурами до достижения желательной концентрации 150 мг/мл. Образцы разделяют на аликвоты по 2 мл и хранят при температуре -20°С, 4°С и при температуре окружающей среды в течение трех дней. В конце периода хранения проводят разделение методом ВЭЖХ с последующим анализом. Полученные результаты приведены в Таблице 2.
Данные по стабильности средств для доставки номеров 9, 15 и 40
Пример 8
Композиция соединения GLP-1
Получают раствор Val8-Glu22-GLP-1 при растворении соединения GLP-1 в дистиллированной воде с достижением концентрации 7 мг/мл. Значение pH медленно повышают до 10,5 посредством добавления 2н NaOH с последующим инкубированием при комнатной температуре в течение 30 минут. Добавляют объем 1М трис буфера, pH 8,0, нужный для достижения концентрации готового буфера 20 мМ трис и доводят pH до 7,8 с использованием 1н или 5н HCl. Затем раствор фильтруют через шприц-фильтр с размером пор 0,22 мкм с низким потенциалом связывания белка (Millex GV, Millipore) и концентрацию соединения GLP-1 определяют УФ, спектроскопией. Раствор разбавляют до конечной концентрации 5,5 мг/мл с использованием 290 мМ трис буфера, pH 7,8. Далее раствор пептида хранят в аликвотах по 1,0 мл при температуре -70°С до использования.
Пример 9
Готовые композиции
Готовые композиции получают примерно за 30 минут - 1 час до введения in vivo путем объединения 4,5 мл средства для доставки с 0,5 мл соединения GLP-1. Готовые композиции вводят пероральным зондом в дозе 2 мл/кг (1,1 мг/кг соединения GLP-1, 300 мг/кг средства для доставки) самцам крыс Спрэг Доли (Sprague Dawley), которых выдерживали без пищи в течение 12 часов до введения дозы. В качестве контроля используют подкожную дозу соединения GLP-1 (0,011 мг/кг) самого по себе. Среднее значение фармакокинетических параметров показано в приведенной ниже Таблице 3.
Среднее значение фармакокинетических параметров и биодоступности средств для доставки номера 9, 15 и 40
(мин)
(пг/мл)
(пг* мин/мл)
12522
b - НВ = не вычисляют в связи с низким уровнем обнаружения
На основании указанных данных вычисляют процент биодоступности в процентах при пероральном введении Val8-Glu22-GLP-1 в составе композиции со средством для доставки номер 15, равным 2,72%, Val8-Glu22-GLP-1 в составе композиции со средством для доставки номер 40, равным 1,01%, и Val8-Glu22-GLP-1 в составе композиции со средством для доставки номер 9, равным 0,3%.
Фармакокинетические данные для всех средств для доставки показаны в приведенной ниже таблице 4.
Дополнительный пример 1.
Как описано в примере 9, самцам крыс ввели GLP-1 (SEQ ID NO. 1) в составе композиции со средством доставки номер 5 (0,5 1 2 и 4 мг/кг соединения GLP-1 и 300 мг/кг средства для доставки) и IV GLP-1 (SEQ ID NO. 1) в составе композиции со средством доставки номер 5 (1 мг/кг соединения GLP-1 и 300 мг/кг средства для доставки). Данные о AUC (пг*мин/мл) приведены ниже на диаграмме 1.
На чертеже проиллюстрировано сравнение природных соединений GLP-1 (SEQ ID NO. 1) и IV GLP-1 (SEQ ID NO. 1) с использованием средства для доставки №5.
Таблица 4.
Фармакокинетические данные:
Tmax, Cmax и AUC для средств для доставки 1-56
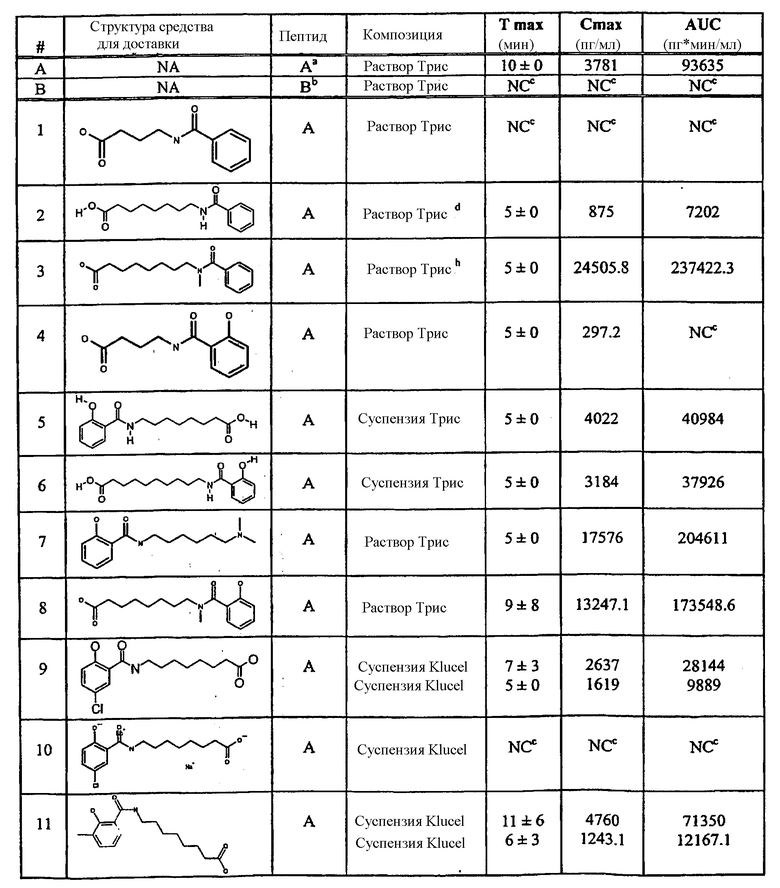
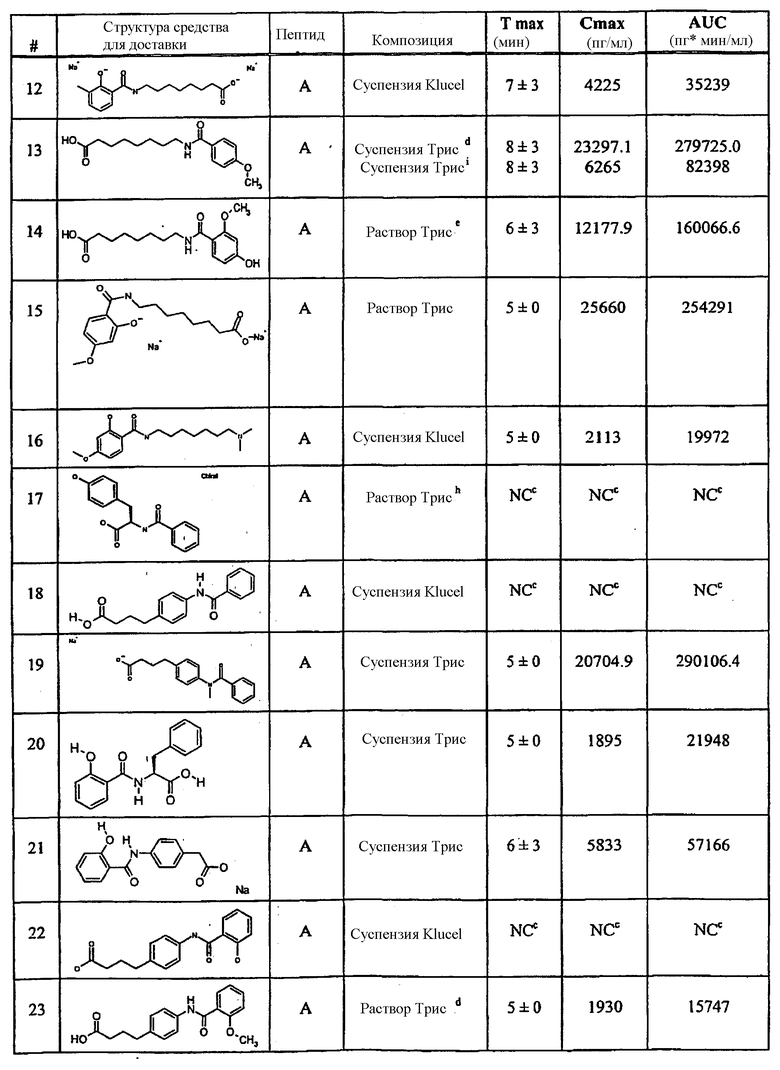
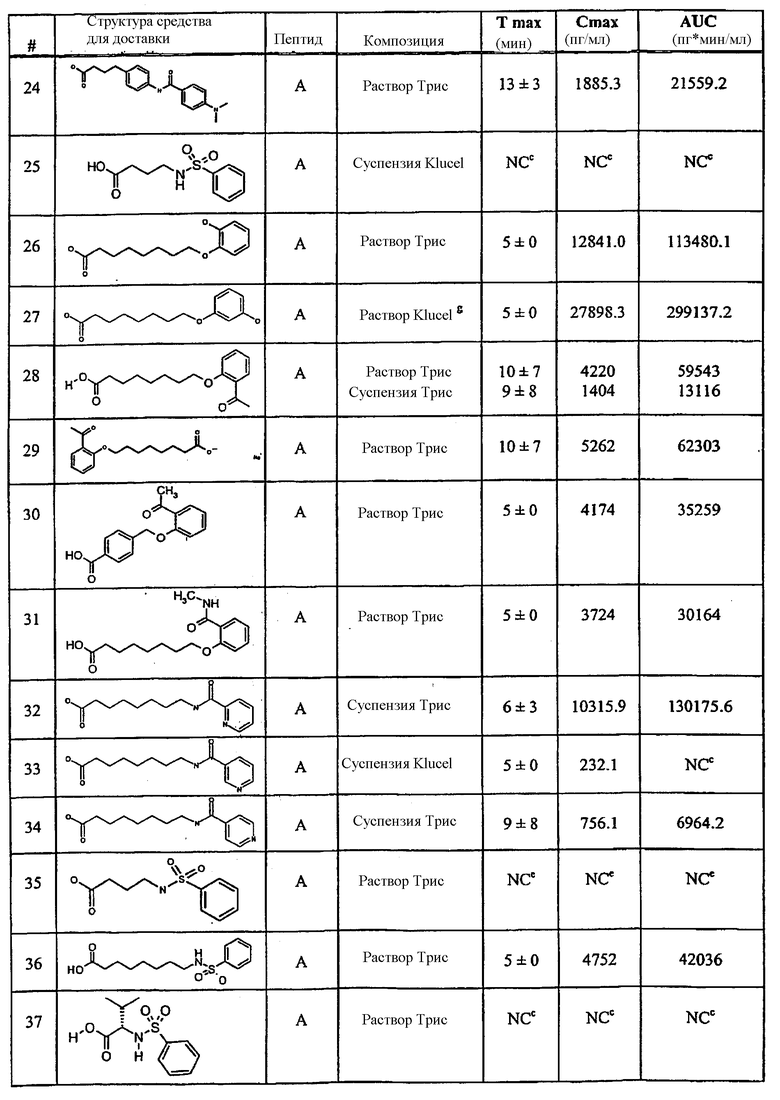
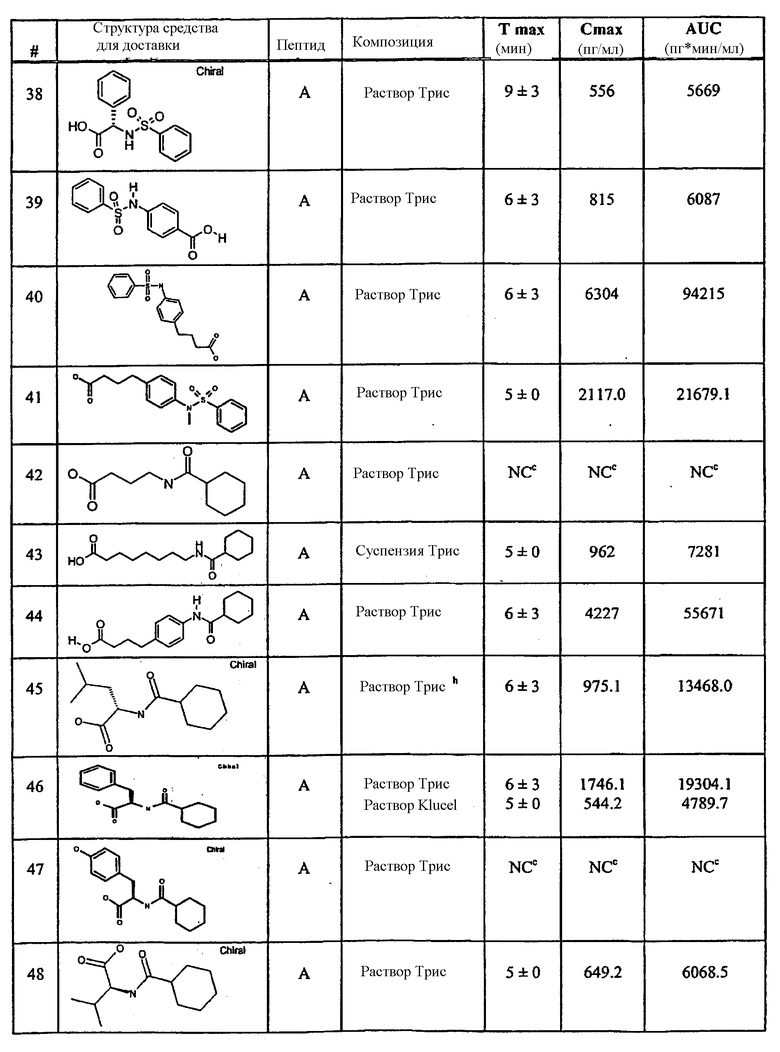
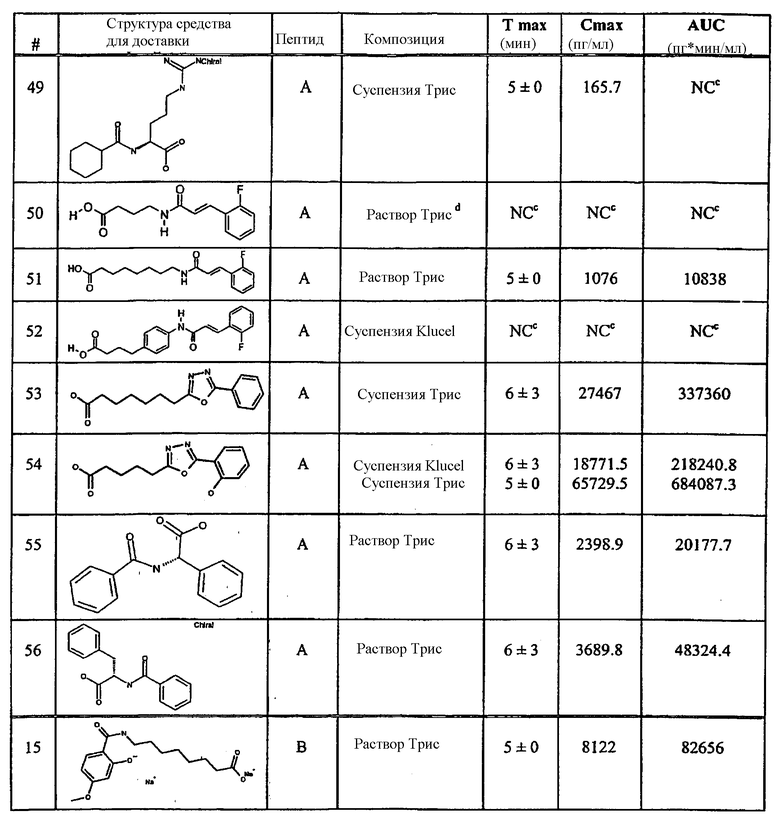
a - используемый пептид: HVEGTFTSDVSSYLEEQAAKEFIAWLVKGRG.
b - используемый пептид: HVEGTFTSDVSSYLEEQAAKEFIAWLIKGGPSSGDPPPS.
c - NC - не вычисляют в связи с недостаточностью данных.
d - дозу композиции вводят в виде раствора с нерастворенными/фиброзными частицами.
e - дозу композиции вводят в виде помутневшего раствора.
f - дозу композиции вводят в виде раствора с некоторым количеством нерастворенных частиц.
g - дозу композиции вводят в виде помутневшего вязкого раствора.
h - дозу композиции вводят в виде раствора с некоторым количеством прозрачных частиц.
i - дозу композиции вводят в виде негомогенной суспензии, содержащей комочки.





















| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ КОМПОЗИЦИИ АГОНИСТОВ ЭКСЕНДИНА И СПОСОБЫ ИХ ВВЕДЕНИЯ | 2000 |
|
RU2242244C2 |
| Производное инсулинотропного пептида с модифицированным N-концевым зарядом | 2014 |
|
RU2673179C2 |
| СПОСОБЫ ДОСТАВКИ НЕЙРОПРОТЕКТИВНОГО ПОЛИПЕПТИДА В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ | 2017 |
|
RU2790566C2 |
| ГЛИКОЗИЛИРОВАННЫЙ ПЕПТИД GLP-1 | 2009 |
|
RU2543157C2 |
| ПОЛИПЕПТИДЫ АНАЛОГА АМИЛИНА ЧЕЛОВЕКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2839688C2 |
| ДВОЙНЫЕ АГОНИСТЫ GLP1/GIP ИЛИ ТРОЙНЫЕ АГОНИСТЫ GLP1/GIP/ГЛЮКАГОНА | 2013 |
|
RU2652783C2 |
| ЛЕЧЕНИЕ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2017 |
|
RU2755997C2 |
| СПОСОБЫ ПОДАВЛЕНИЯ ГЛЮКАГОНА | 2000 |
|
RU2247575C9 |
| СЛИТЫЕ КОНСТРУКЦИИ ЛЕКАРСТВЕННОГО СРЕДСТВА И КОНЪЮГАТЫ | 2005 |
|
RU2428431C2 |
| Конъюгат, содержащий оксинтомодулин и фрагмент иммуноглобулина, и его применение | 2012 |
|
RU2733544C2 |
Изобретение относится к химико-фармацевтической промышленности и касается новых композиций, содержащих: (а) соединение GLP-1, выбранное из группы, состоящей из соединений GLP-1, представленных в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 9, SEQ ID NO: 12, SEQ ID NO: 13 и SEQ ID NO: 14; и (б) средство для доставки, выбранное из группы, состоящей из средства для доставки 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55 и 56. Такие композиции характеризуются легкостью всасывания соединения GLP-1 при пероральном введении, что позволяет вводить соединение GLP-1 перорально, исключая многократные инъекции. 17 з.п. ф-лы, 4 табл., 1 ил.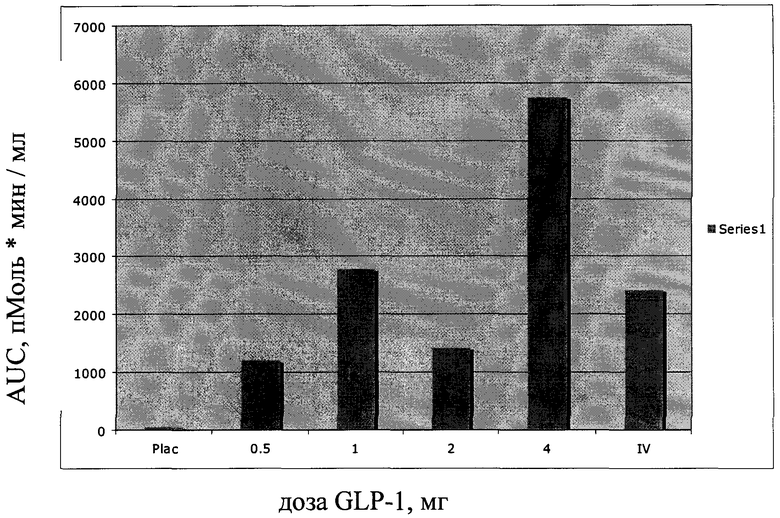
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US 6329336 B1, 11.12.2001 | |||
| ЗАМЕЩЕННЫЕ БИАРИЛЬНЫЕ СОЕДИНЕНИЯ ИЛИ ЗАМЕЩЕННЫЕ ПИРИДИНЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1997 |
|
RU2195443C2 |
| СПОСОБЫ ПОДАВЛЕНИЯ ГЛЮКАГОНА | 2000 |
|
RU2247575C9 |
Авторы
Даты
2008-08-27—Публикация
2003-02-07—Подача