Изобретение относится к области медицины, кардиохирургии, конкретно к способу прерывания проведения фронта волны возбуждения по предсердиям во время операций на "сухом" сердце и устройству для его осуществления.
Известен способ прерывания проведения фронта волны возбуждения по предсердиям, заключающийся в соединении синоатриального и атриовентрикулярного узлов полоской ткани межпредсердной перегородки с изоляцией этих участков от остальных отделов предсердий [1]. Однако применение данного способа связано со значительным количеством осложнений, обусловленных потерей предсердиями сократительной функции и сохранением риска образования внутрисосудистых тромбов, травматичностью и длительностью оперативного вмешательства.
Известен также способ, заключающийся в изоляции рядом лежащих участков миокарда предсердий специально ориентированными разрезами [2], что делает невозможным рециркуляцию волны возбуждения и снижения "критической массы" миокарда путем изоляции части участков предсердий. Однако применение указанного способа ограничено, т.к. объем операции не позволяет использовать его у тяжелобольных, для которых важным фактором, определяющим исход операции, является длительность искусственного кровообращения, а условие ее выполнения - хорошая экспозиция предсердий неприменимо у пациентов со слипчивым перикардитом в результате ревматического процесса или ранее перенесенной операции на сердце.
Известен также способ прерывания проведения фронта волны возбуждения, заключающийся в электродеструкции атриовентрикулярного соединения сердца [3, 4] . Однако у части пациентов отмечалось появление или нарастание недостаточности кровообращения на фоне искусственной полной атриовентрикулярной блокады и постоянного ритмовождения вследствие потери предсердной функции, регургитации через правый и левый предсердно-желудочковые клапаны в результате асинхронной работы предсердий и желудочков, а также нарушения нормального хода желудочковой деполяризации при VVI стимуляции, явления "ошибки", что обусловлено одновременным сокращением предсердий и желудочков при открытых атриовентрикулярных клапанах, которое ведет, в свою очередь, к рефлекторной вагусной вазодилатации в ответ на растяжение стенок предсердий (в основном правого) [5].
Наиболее близким по технической сущности к предлагаемому является способ, предложенный Л.А. Бокерия [6], заключающийся в электроизоляции левого предсердия путем отсечения с последующим восстановлением целостности медиального края левого предсердия от межпредсердной перегородки дополнительным проведением криодеструкции эпи- и эндокардиальных поверхностей заднего нижнего края разреза левого предсердия и верхней части межпредсердной борозды. Однако применение данного способа ограничено, его применение неэффективно при вовлечении в патологический процесс межпредсердной перегородки и миокарда правого предсердия, т.е. тех отделов, которые также являются субстратом фибрилляций желудочков при митральных пороках [7]. Использование данного способа связано также с длительностью оперативного вмешательства механической (при рассечении тканей) и слабо контролируемой термической травматизацией, обусловленной субъективностью воздействия (во время поочередного прикладывания криоаппликатора к поверхности сердца), отсутствием элемента контроля за объемом проводимой криодеструкции.
Известно устройство для радиочастотного воздействия - радиочастотный деструктор [8], содержащий задатчик выхода, задатчик максимума импеданса, блок регулировки выходного напряжения, радиочастотный генератор, рабочую часть, датчики напряжения и тока. Блок регулировки выходного напряжения отключает радиочастотную энергию, если импеданс, вычисленный путем деления величины выходного напряжения на величину выходного тока, превышает величину, установленную предварительно на задатчике максимума импеданса.
Данный прибор используется для радиочастотного воздействия на проводящие пути сердца, причем активный электрод вводится в область воздействия через вену и находится в потоке крови, а пассивный располагают на теле пациента. Однако применение аппарата ограничено, так, при работе на открытом сердце по методике, изложенной в предлагаемом способе, с использованием данного прибора наблюдаются искрение и вспышки в результате неплотного контакта между поверхностью активного электрода и тканью и пригорание ткани при установке на задатчике максимума импеданса величины большей, чем необходимо в данной области воздействия. Если же установленная величина импеданса меньше необходимой, то энергия на выход радиочастотного генератора не подается и воздействия нет. Импеданс между пассивным и активным электродами постоянно меняется при перемещении активного электрода, кроме того, импеданс для одной точки до момента воздействия может быть больше импеданса в момент пригорания для другой точки воздействия. Вследствие этого возникают большие неудобства в работе, ухудшается эффективность воздействия, появляются искрение, вспышки и пригорание ткани к поверхности активного электрода.
Технической задачей, решаемой данным изобретением, является повышение эффективности лечения за счет снижения числа осложнений, сокращения времени операции и расширения области применения способа.
Поставленную задачу решают применением нового способа прерывания фронта волны возбуждения по предсердиям во время операции на "сухом" сердце, заключающегося в проведении непосредственной деструкции тканей миокарда и предсердий во время выполнения, в зависимости от показания, операций фрагментации предсердия или изоляции левого предсердия, причем проводят радиочастотную деструкцию, дополнительно со стороны эпикарда по двойным непрерывно идущим параллельным линиям, при больших размерах левого предсердия радиочастотную деструкцию проводят по линии, начинающейся от заднемедиальной комиссуры митрального клапана непосредственно у фиброзного кольца и заканчивающейся у переднелатеральной комиссуры митрального клапана непосредственно у митрального кольца, идущей параллельно межпредсердной перегородке, а при больших размерах левого и правого предсердий выполняют правую атриотомию от основания ушка правого предсердия по его боковой стенке до заднего межпредсердного валика, разрез продолжают линией радиочастотной деструкции эпикардиально до устья коронарного синуса и далее до фиброзного кольца трикуспидального клапана, а с противоположной стороны эндокардиально от устья верхней полой вены до верхнего края межпредсердной перегородки у основания овальной ямки до уровня сухожилия Тодаро, далее после левой атриотомии эпикардиально вдоль задней межпредсердной борозды от нижнего угла разреза левого предсердия между нижними легочными венами и фиброзным кольцом митрального клапана, далее, огибая кнаружи устье левой нижней легочной вены к основанию ушка левого предсердия, которое отсекают, и далее от его основания линию деструкции продолжают эпикардиально вверх, соединяя с ранее выполненными линиями деструкции, также пассивный электрод располагают непосредственно под левым предсердием между правыми и левыми легочными венами, также проводят радиочастотную деструкцию с уровнем энергии от 5 до 15 Вт.
Устройство для осуществления способа состоит из задатчика выходной мощности, подключенного к блоку регулировки выходного напряжения, соединенному с радиочастотным генератором, рабочей части, состоящей из активного и пассивного электродов, подключенной через датчики тока и напряжения к радиочастотному генератору, при этом выходы датчиков соединены с блоком регулировки выходного напряжения, причем выход датчика напряжения соединен также с входом блока дифференцирования, подключенного к блоку регулировки выходного напряжения, на выходе радиочастотного генератора сформирован резонансный контур и дополнительно к блоку регулировки выходного напряжения подключен блок, выполненный с возможностью задания максимума для производной выходного напряжения, выделенной на блоке дифференцирования, также активный электрод выполнен в виде сферы или полусферы, кроме того, поверхность активного электрода должна иметь шероховатость поверхности не более 0,16 с последующей полировкой.
Способ осуществляют следующим образом.
Пациента берут в операционную. Дают вводный наркоз, интубируют, канюлируют центральные вены и лучевую артерию слева. В условиях нейролептанальгезии операционное поле обрабатывают раствором антисептика, отграничивают операционное поле. Резрезают кожу, подкожную клетчатку, выполняют срединную стернотомию, продольную Т-образную перикардиотомию. Подключают аппарат искусственного кровообращения по схеме "полые вены - аорта". Осуществляют гепаринизацию. После начала искусственного кровообращения и достижения температуры 29oС пережимают восходящую аорту, под заднюю стенку левого предсердия помещают пассивный электрод. И для осуществления изоляции левого предсердия выполняют левую атриотомию вдоль задней межпредсердной борозды. При больших размерах левого предсердия после иссечения митрального клапана с помощью активного электрода радиочастотную деструкцию проводят по линии, начинающейся от заднемедиальной комиссуры митрального клапана непосредственно у фиброзного кольца и заканчивающейся у переднелатеральной комиссуры митрального клапана также непосредственно у фиброзного кольца, идущей параллельно межпредсердной перегородке.
При больших размерах левого и правого предсердий выполняют правую атриотомию от основания ушка правого предсердия по его боковой стенке до заднего межпредсердного валика, разрез продолжают линией радиочастотной деструкции эпикардиально до устья коронарного синуса и далее до фиброзного кольца трикуспидального клапана, а с противоположной стороны эндокардиально от устья верхней полой вены до верхнего края межпредсердной перегородки к основанию овальной ямки до уровня сухожилия Тодаро, далее после левой атриотомии эпикардиально вдоль задней межпредсердной борозды от нижнего угла разреза левого предсердия между нижними легочными венами фиброзным кольцом митрального клапана, далее, огибая кнаружи устье левой нижней легочной вены к основанию ушка левого предсердия, которое отсекают, и далее от его основания линию деструкции продолжают эпикардиально вверх, к "крыше" левого предсердия, соединяя с ранее выполненными линиями деструкции.
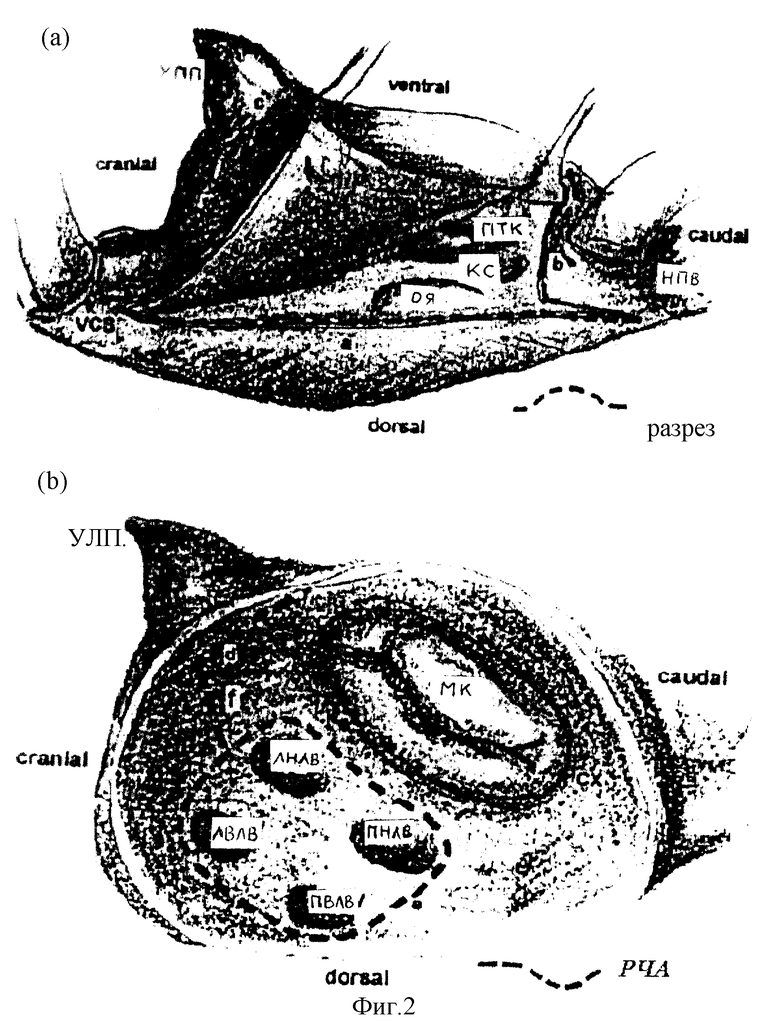
На фиг.1 приведена схема выполнения операции изоляции левого предсердия, выполняемая в случае большого размера левого предсердия, где ПЖ - правый желудочек, ПП - правое предсердие, ЛЖ - левый желудочек, НПВ - нижняя полая вена, УЛВ - утья легочных вен, МК - митральный клапан, ЛП - левое предсердие, АО - аорта, ВПВ - верхняя полая вена, РЧ - радиочастотное воздействие.
На фиг.2 приведена схема радиочастотной фрагментации предсердий, где УПП - ушко правого предсердия, ПТК - правый трикуспидальный клапан, ОЯ - овальная ямка, КС - коронарный синус, ВПВ - верхняя полая вена, НПВ - нижняя полая вена, УЛП - ушко левого предсердия, ОА - огибающая артерия, МК - митральный клапан, ЛВЛВ - левая верхняя легочная вена, ЛНЛВ - левая нижняя легочная вена, ПВЛВ - правая верхняя легочная вена, ПНЛВ - правая нижняя легочная вена.
Пример 1.
Больной Саликаев Андрей Алексеевич, 43 года, история болезни 3981, находился в отделе ССХ с 19.10.99 с диагнозом:
-осн- Ревматизм, активность 1ст. Возвратный ревмокардит. Сложный митральный порок сердца с преобладанием стеноза. Недостаточность трикуспидального клапана 1 ст. Пароксизмальная форма фибрилляции предсердий. НПА.
-соп- Хр. описторхоз. Хр. холецистит: ремиссия. Хр. бронхит, ремиссия.
Жалобы при поступлении на одышку при физической нагрузке, эпизоды неритмичных сердцебиений, слабость.
Лабораторные данные: в пределах нормы
ЭКГ: Фибрилляция предсердий, 95/мин; полувертикальное положение ЭОС, гипертрофия правого желудочка.
Спирография: дыхательная недостаточность 1 ст. по рестриктивному типу.
Рентгенография органов грудной клетки в прямой проекции (20.10.99): Легочной рисунок слегка усилен за счет интерстициального компонента. Тени корней синусы, диафрагма б/о. Сердце митральной конфигурации, слегка расширено в поперечнике. Тень аорты несколько усилена.
Эхокардиграфия (21.09.99): Увеличено левое предсердие. Фиброз створки митрального клапана, утолщение, сращение по комиссурам, подклапанные сращения, уменьшение площади митрального отверстия, градиент ЛП/ЛЖ 19/9; незначительная митральная регургитация, мягкая легочная гипертензия. Показатели сократимости левого желудочка - в норме. Диаметр предсердий: левого - 44 мм; правого - 50 мм; правого желудочка - 27 мм, левого желудочка - 55 мм; фракция выброса левого желудочка - 63%; dS - 34%.
Ультразвуковое исследование внутренних органов: дистония пр. почки (II-III ст.), нефроптоз слева (I-II ст.).
Коронаровентрикулография, зондирование правых отделов сердца (1.11.99): ЛЖ обычной конфигурации, не расширен, не утолщен, умеренный гипокинез переднебокового сегмента; фракция выброса - 57%; Рао-135/85; КДДлж-16; Рлж-143/0; dP/dT-900/1100; Рла-35-38/18; Рпж-45/4; Рпп-9/4; Рао-150/90; Левый тип кровоснабжения: ЛЖ коронарные без стенозов.
Консультация ЛОР: хронический тонзиллит.
Консультация окулиста: артериолосклероз сетчатки. Помутнение роговицы левого глаза.
1.12.99 г. выполнена операция: протезирование митрального клапана протезом "МИКС-МДМ-27" 1909-97, радиочастотная фрагментация предсердий с резекцией их ушек в условиях искусственного кровообращения и фармакохолодовой кардиоплегии.
Описание операции
Пациент взят в операционную. Вводный наркоз. Интубация. Канюляция центральных вен и лучевой артерии слева. В условиях нейролептанальгезии операционное поле обработано раствором "Кутасепт" с экспозицией 2 мин. Резрез кожи, подкожной клетчатки. Срединная стернотомия. Продольная Т-образная перикардиотомия. Подключение аппарата искусственного кровообращения по схеме "полые вены-аорта". Гепаринизация под контролем АЧТВ. Начало искусственного кровообращения. Выполнена правая атриотомия от основания ушка правого предсердия по боковой стенке правого предсердия до заднего межпредсердного валика. Разрез продолжен в двойную линию радиочастотной деструкции до устья коронарного синуса и далее до фиброзного кольца трикуспидального клапана. А с противоположной стороны - двойная полоса радиочастотной деструкции от ушка от верхней полой вены до верхнего края межпредсердной перегородки с переходом на "крышу" левого предсердия и межпредсердную перегородку книзу - к основанию овальной ямки до уровня сухожилия Тодаро.
Затем, используя стандартную левую атриотомию, вдоль задней межпредсердной борозды изолировали легочные вены, проведя двойную линию радиочастотного воздействия от нижнего угла разреза левого предсердия между нижними легочными венами и фиброзным кольцом митрального клапана, далее, обогнув кнаружи устье левой нижней легочной вены к основанию ушка левого предсердия, которое отсекается. И от его основания продолжили вверх, к "крыше" левого предсердия, соединив таким образом с ранее выполненными линиями деструкции. Перевязано ушко левого предсердия лавсановой лигатурой. Ревизия митрального клапана - выраженный стеноз клапана, кальциноз створок. Рассечена наружная комиссура, произведена папиллотомия. Однако ригидность свободного края створок митрального клапана и кальциноз комиссуры препятствуют смыканию и раскрытию створок клапана, поэтому принято решение о протезировании клапана. Клапан иссечен. В митральную позицию на 10-ти П-образных швах на прокладках имплантирован "МИКС-МДМ-27, 1909-97". Стенка левого предсердия ушита двухрядными непрерывными швами. Снятие зажима с аорты. Мероприятия по профилактике воздушной эмболии. Дефибрилляция с исходом в синусовый ритм. Остановка искусственного кровообращения. Деканюляция. Дренирование перикарда, переднего средостения. Подшивание электродов для временной электрокардиостимуляции. Гемостаз. Металлоостеосинтез грудины. Послойное ушивание раны. Додесепт. Ас. повязка.
В послеоперационном периоде сохранялся синусовый ритм. Швы сняты на 10-е сутки. Пациент выписан из клиники в удовлетворительном состоянии без приема антиаритмических препаратов.
Пример 2.
Пациентка Загромова Татьяна Петровна, 51 год, проживающая по адресу: г. Томск, ул. Кулева 31-2, находилась в отделении сердечно-сосудистой хирургии Томского НИИ кардиологии с 27.08.99 г. по 15.10.99 г.
Диагноз: Ревматизм, неактивная фаза. Комбинированный порок сердца: cложный митральный порок с преобладанием стеноза; сложный аортальный порок с преобладанием недостаточности. Состояние после операции - закрытая митральная комиссуротомия (1981 г. , г.Москва). Мерцательная аритмия, хроническая форма. Недостаточность кровообращения ПБ стадии.
При поступлении предъявляла жалобы на учащенное неритмичное сердцебиение, ноющие боли, чувство скованности в суставах кистей, быструю утомляемость, снижение работоспособности. Из анамнеза: С раннего детского возраста часто болела ангинами, ОРЗ; в 1969г. выполнена тонзиллэктомия. С юношеских лет беспокоит суставный синдром, при врачебном осмотре поставлен диагноз: Ревматизм. Проводилась сезонная противовоспалительная терапия. С конца 70-х годов ставится диагноз: Митральный порок. В 1981г. усилившаяся одышка заставила пациентку согласиться на операцию - закрытая митральная комиссуротомия в ИССХ им. А.Н. Бакулева (г.Москва), заживление первичным натяжением, после операции отмечала хороший эффект, до 1996г. чувствовала себя практически здоровой, нагрузки выполняла в полном объеме. С 1996г. отмечает появления пароксизмальной мерцательной аритмии, которые купировались приемом хинидина; в июле 1998 г. возник пароксизм мерцательной аритмии, который был купирован электроимпульсной кардиоверсией, после чего был назначен кордарон для постоянного приема. В начале августа пациентка прекратила его принимать вследствие развития аллергической реакции, 8.08.99т рецидивировала мерцательная аритмия.
При объективном осмотре общее состояние удовлетворительное. В легких дыхание везикулярное, чистое. Перкуторно границы сердца расширены влево. Тоны сердца аритмичные, тахисистолическая форма мерцательной аритмии, I тон раздвоен, систолический и диастолический шумы на верхушке, в т.Боткина. Живот мягкий, безболезненный; печень по краю реберной дуги. С-м поколачивания отр. с обеих сторон. Периферических отеков нет.
Лабораторные данные 31.08.99г.: Общий анализ крови: Э-4,ЗТ/л, Нв-132г/л, Лей-4,1Г/л, э-7%, п/я-2%, с/я-52%, лим-32%, мон-7%, СОЭ-3 мм/ч. Группа крови: О(I) Rh"+" (положительный).
Общий анализ мочи: ж. , пр., уд. вес 1015, реакция 5,0, белок и сахар отр., эп.пл.-ед. в п/зр., Лей-ед. в п/зр., соли оксалатов++.
Биохимические тесты крови: об.белок 66 г/л, холестерин 6,3 ммоль/л, ACT-0,16 ммоль/л ч, АЛТ 0,28 ммоль/л ч, сахар 4,5 ммоль/л, мочевина 6,5 ммоль/л, креатинин 84,9 мкмоль/л, билирубин общий 10,75 мкмоль/л, билирубин прямой - отрицательный, СРБ "следы", серомукоиды 0,17 ед.
Коагулограмма: ПТИ 83%, тромбиновое время 16", фибриноген "В" "-", общий фибриноген 2,6 г/л.
ЭКГ: Ритм фибрилляция предсердий, ср. ЧСС-65 в 1 мин, нормальное положение электрической оси сердца, сочетанная гипертрофия желудочков с перегрузкой.
ЭхоКГ. : Аорта на уровне створок 31 мм, на уровне фиброзного кольца 24 мм. Краевое уплотнение створок аортального клапана, пиковый градиент 9 мм рт.ст., средний 2 мм рт.ст., регургитация I-II ст. Выраженный фиброз, утолщение створок митрального клапана, створки спаяны по комиссурам, подклапанные сращения, площадь митрального отверстия 1,18 см2, пиковый градиент 24 мм рт. ст. , средний 10 мм рт. ст., регургитация I ст. Створки трикуспидального клапана тонкие, трикуспидальная регургитация I ст. Повышено систолическое давление в правом желудочке - 42 мм рт.ст. Дилатировано левое предсердие - 48 мм. Конечно-систолический размер левого желудочка 28 мм, конечно-диастолический размер левого желудочка 50 мм, передне-задний размер правого желудочка 23 мм. Стенки левого желудочка не утолщены: МЖП-9,3 мм, ЗСЛЖ-6,8 мм. Сократительная способность левого желудочка не снижена: ФВ-75%.
Левая вентрикулография, зондирование правых отделов сердца: левый желудочек обычной конфигурации, умеренно расширен - конечно-диастолический индекс левого желудочка 80 мл/м2, конечно-систолический индекс левого желудочка 28 мл/м2; стенки его не утолщены, умеренная гипокинезия верхушки, ФВ-65%. Клапанный отдел аорты 25 мм, надклапанный 37 мм, восходящая аорта 33 мм; аортальная регургитация I-IIст. Митральной регургитации не выявлено. При давлении в аорте 164/78 мм рт.ст. в момент исследования, давление в левом желудочке 170/0 мм рт.ст. (аортальный трансвальвулярный градиент 6 мм рт.ст. ). Конечно-диастолическое давление в левом желудочке 13 мм рт.ст. dР/dТмакс/мин= 1100/1300. Давление в легочной артерии 45/25 мм рт.ст., в правом желудочке 47/2 мм рт.ст., ПП-10-11/7 мм рт.ст., проба с эуфиллином не проводилась из-за мерцательной аритмии. Правый тип кровоснабжения миокарда; коронарного атеросклероза не выявлено.
Рентгенография органов грудной клетки: очаговых и инфильтративных изменений не выявлено. Умеренный диффузный пневмосклероз. Корни структурны. Сердце расширено в поперечнике, увеличен левый желудочек, талия сглажена за счет увеличения дуги левого предсердия и легочной артерии. Аорта удлинена, уплотнена. Контуры диафрагмы четкие, ровные. Синусы свободные.
Спирография: жизненная емкость легких 2,61 л при должной 2,62 л, максимальная вентиляция 52,8 л/мин при должной 65,2 л/мин, минутный объем дыхания 9,3 л/мин, дыхательный объем 0,5 л, частота дыхания 19 в 1 мин. S=1,63 м2.
УЗИ печени, желчного пузыря, почек: патологии не выявлено.
Консультация окулиста: артериолосклероз сетчатки.
15.09.99 г. проведена оперативная коррекция порока сердца - протезирование митрального клапана сердца двустворчатым искусственным клапаном сердца Model 700 "CarboMedics-29M" C383813F, протезирование аортального клапана сердца двустворчатым искусственным клапаном сердца "МЕДИНЖ-АДМ-21" 0543-1997, радиочастотная изоляция левого предсердия в условиях искусственного кровообращения. В послеоперационном периоде восстановлен синусовый ритм.
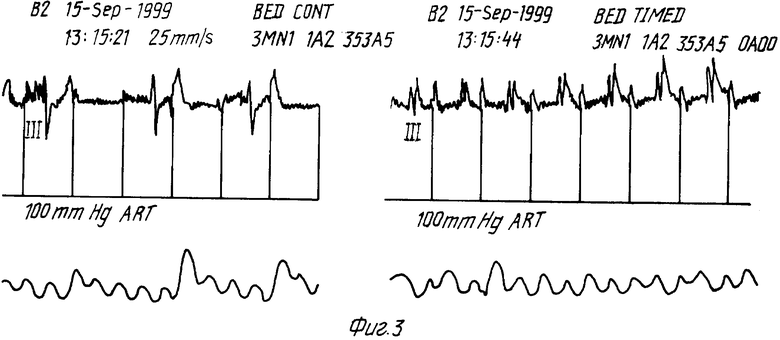
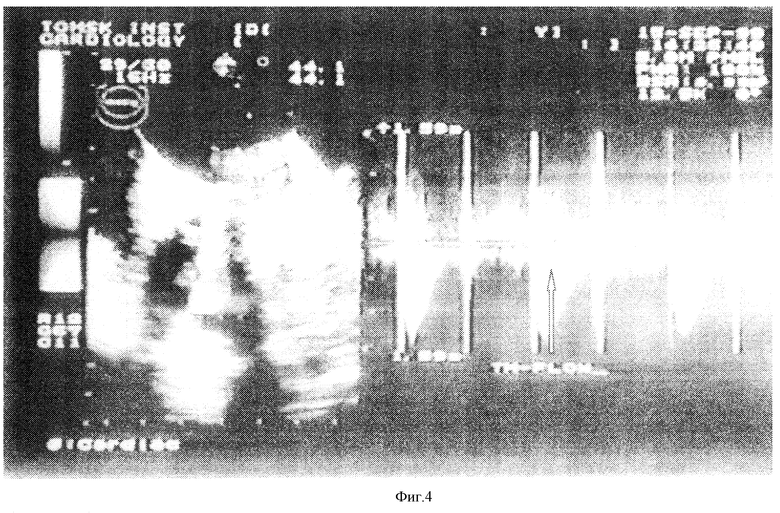
Контроль изоляции левого предсердия осуществлен интраоперационно пооследовательной электростимуляцией левого предсердия (ненавязывание ритма) и правого предсердия (ритм навязан) (фиг.3); а также трансэзофагеальной эхокардиографией - на фоне синусового ритма отмечен монопиковый поток через митральный клапан, что говорит об отсутствии активной систолы левого предсердия (фиг.4).
Течение послеоперационного периода неосложненное. Ритм на момент выписки синусовый без антиаритмиков. Выписана в удовлетворительном состоянии.
Описание операции
Пациентка взята в операционную. Вводный наркоз. Интубация. Канюляция центральных вен и лучевой артерии слева. В условиях нейролептанальгезии операционное поле обработано раствором "Кутасепт" с экспозицией 2 мин. Резрез кожи, подкожной клетчатки. Срединная стернотомия. Продольная Т-образная перикардиотомия. Частичный кардиолиз (правое предсердие, полые вены, аорта, передняя поверхность правого желудочка). Подключение аппарата искусственного кровообращения по схеме "полые вены-аорта". Гепаринизация под контролем АЧТВ. Начало искусственного кровообращения. После достижения температуры 29oС пережата восходящая аорта, под заднюю стенку левого предсердия помещен пассивный электрод. Левая атриотомия вдоль задней межпредсердной борозды. Митральный клапан иссечен. С помощью активного электрода выполнена радиочастотная деструкция миокарда предсердий от крайних точек разреза до фиброзного кольца митрального клапана в области комиссур в виде двух параллельных дорожек. На 12 П-образных швах имплантирован митральный клапан "CarboMedics-29M" C383813F. Левое предсердие ушито. Вскрыт просвет аорты, иссечен аортальный клапан и на 10 П-образных швах имплантирован "МЕДИНЖ-АДМ-21" 0543-1997. Аорта ушита. Профилактика воздушной дезаэрацией полостей, согревание, восстановление сердечной деятельности дефибрилляцией. Контроль изоляции левого предсердия методом трансэзофагеальной ЭхоКГ и предсердной ЭКС (фиг. 4, 3). Деканюляция, гемостаз. Дренирование средостения, послойное ушивание раны.
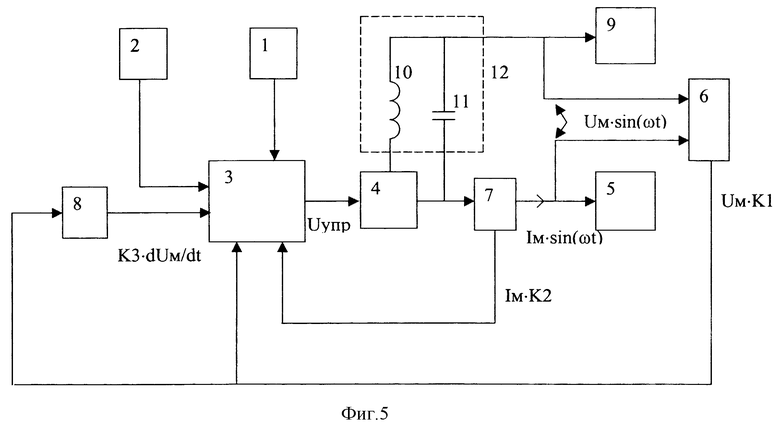
На фиг. 5 представлена блок-схема предлагаемого устройства для радиочастотного воздействия, состоящего из задатчика выходной мощности 1, соединенного с первым входом блока регулировки выходного напряжения 3, выход которого соединен с входом управления радиочастотного генератора 4. К первому выводу генератора 4 подключен первый вывод катушки индуктивности 10 резонансного контура 12, ко второму выводу генератора - первый вывод конденсатора 11 того же контура. Вторые выводы катушки индуктивности 10 и конденсатора 11 резонансного контура 12 соединены друг с другом и с активным электродом 9. Через датчик тока 7 пассивный электрод 5 соединен со вторым выходом генератора 4. Датчик напряжения 6 своими входами подключен к активному 9 и пассивному 5 электродам рабочей части. Выходы датчиков соединены со вторым (датчик тока) и третьим (датчик напряжения) входами блока регулировки выходного напряжения 3, выход датчика напряжения 6, кроме того, соединен с входом блока дифференцирования 8, выход которого соединен с четвертым входом блока регулировки выходного напряжения 3. К пятому входу блока регулировки выходного напряжения 3 подключен блок 2, выполненный с возможностью задания максимума для производной выходного напряжения, выделенной на блоке дифференцирования.
Генератор 4 настраивают на резонансную частоту резонансного контура 12. Датчик напряжения 6 измеряет напряжение между активным 9 и пассивным 5 электродами рабочей части. Датчик тока 7 и датчик напряжения 6 выдают напряжение, пропорциональное амплитуде выходного тока Iм и выходного напряжения Uм соответственно. Все приведенные на фиг.5 коэффициенты К1...К3 постоянные. Напряжение на выходе блока дифференцирования 8 пропорционально скорости изменения напряжения на его входе (производной по времени). На вход блока дифференцирования 8 подается напряжение с выхода датчика напряжения 6 (пропорциональное Uм). Таким образом, напряжение на выходе блока дифференцирования 8 пропорционально скорости изменения амплитуды выходного напряжения (его производной по времени dUм/dt). Величина напряжения на выходе блока 2 устанавливается при настройке прибора на производстве. Скорость изменения напряжения на выходе блока регулировки выходного напряжения 3 (управляющего напряжения) ограничена сверху невысоким быстродействием этого блока. Максимальная скорость изменения выходного напряжения блока регулировки выходного напряжения 3 - от нуля до максимума за 1 с. Пассивный электрод 5 находится в постоянном контакте с сердцем.
Устройство работает следующим образом.
До начала воздействия на задатчике выходной мощности 1 устанавливается требуемая величина выходной мощности. Высокочастотное напряжение поступает от генератора 4 с двух его выводов на резонансный контур 12, далее на активный электрод 9 с общей точки катушки индуктивности 10 и конденсатора 11 (вторые выводы) резонансного контура 12, а на пассивный электрод 5 через датчик тока 7 - со второго вывода генератора 4. Путем перемножения сигналов в блоке регулировки выходного напряжения 3, поступающих на его входы с датчиков 6 и 7, вычисляется текущая величина выходной мощности, которая сравнивается с величиной, установленной на задатчике выходной мощности 1, сигнал с которого подается на первый вход блока регулировки выходного напряжения 3. Напряжение на выходе блока регулировки выходного напряжения 3, поступающее на вход управления резонансного генератора 4, изменяется так, чтобы текущая величина выходной мощности была равна величине, установленной на задатчике выходной мощности 1. Пропорционально изменяется амплитуда Uм переменного напряжения на выходе генератора 4. При неизменном импедансе выходной цепи амплитуда Uм выходного напряжения (между электродами 5 и 9) также пропорциональна управляющему напряжению, но при изменении импеданса коэффициент пропорциональности существенно меняется за счет резонанса при большой добротности резонансного контура 12.
При отсутствии контакта активного электрода с тканью величина импеданса максимальна, а следовательно, и отношение амплитуды выходного напряжения к управляющему напряжению максимально. Выходная мощность при этом равна нулю, и управляющее напряжение на выходе схемы управления 3 возрастает, так как схема управления пытается поддерживать установленную на задатчике 1 величину выходной мощности. Даже при ограниченной сверху скорости нарастания управляющего напряжения скорость нарастания амплитуды выходного напряжения велика. Напряжение на выходе блока дифференцирования 8, пропорциональное скорости нарастания амплитуды выходного напряжения, больше, чем на выходе блока 2. Эти два напряжения сравниваются в блоке регулировки выходного напряжения 3, и если первое больше второго, то блок регулировки выходного напряжения 3 моментально снижает до нуля управляющее напряжение на выходе. Выходная мощность уменьшается до нуля, после чего схема управления, продолжая поддерживать установленную выходную мощность, снова увеличивает управляющее напряжение, и все процессы повторяются.
При плохом контакте активного электрода с тканью, при наличии на нем нагара импеданс больше нормы. Скорость нарастания амплитуды выходного напряжения при этом меньше, чем при полном отсутствии контакта активного электрода, но еще достаточно велика. Напряжение на выходе блока 2 устанавливается при настройке на производстве равным максимальному напряжению на выходе блока дифференцирования 8 при стабилизации мощности при выходном импедансе около 500 Ом (максимальный рабочий импеданс). Таким образом, не допускается неограниченное возрастание выходного напряжения генератора при отсутствии контакта с тканью и пригорание поверхности активного электрода при высокой величине импеданса. В начале процесса пригорания или искрения, а также при быстром уменьшении площади соприкосновения активного электрода 9 с тканью, например при отводе электрода от поверхности ткани кардиохирургом, также происходит резкое нарастание выходного напряжения Uм за счет резонанса, хотя управляющее напряжение Uyпp не изменяется и импеданс не превышает граничное значение (500 Ом). Это приводит к возрастанию напряжения на выходе блока дифференцирования 8 больше напряжения на выходе блока 2 и к снижению до нуля управляющего напряжения на выходе блока регулировки выходного напряжения 3. Таким образом, снижение до нуля управляющего напряжения Uynp произойдет уже в начале процесса, требующего немедленного снижения выходной мощности (пригорание, искрение, отвод электрода). Это выгодно отличает предложенное устройство от аналогов, в которых выходное напряжение или выходная мощность зависят от величины импеданса; в них требуется больше времени для обнаружения нежелательного процесса, необходимы дополнительное время и блок для вычисления импеданса.
Необходимо наличие резонансного контура. Это объясняется тем, что при его отсутствии зависимость выходного напряжения генератора от импеданса нагрузки должна иметь большой угол наклона к оси импеданса, что возможно при большом внутреннем сопротивлении генератора. Такая выходная характеристика генератора позволяет по резким скачкам напряжения на его выходе (при помощи датчика напряжения 6) отслеживать возникновение нежелательных явлений - искрения и пригорания ткани к активному электроду, поскольку при этом изменение напряжения происходит гораздо быстрее, чем схема управления изменяет напряжение на своем выходе.
Использование резонансного контура дает следующие существенные преимущества: 1) резонансный контур обладает свойством стабилизации выходной мощности, что упрощает требования к схеме управления; 2) форма выходного напряжения - синусоидальная, следовательно, уменьшаются уровень высокочастотного электромагнитного излучения, уровень помех в устройстве; 3) по сравнению с вышеизложенным альтернативным вариантом (генератор с большим внутренним выходным сопротивлением) при использовании резонансного контура больше КПД устройства.
Все эти свойства резонансного контура позволяют значительно улучшить качество воздействия, уменьшить травматичность операции, что является основной целью изобретения.
Воздействие по направлениям, предлагаемым авторами при выполнении операции изоляции ЛП, позволяет сохранить целостность соединительнотканного каркаса стенки предсердия, в результате повысить возможность "контролировать" сердечный ритм у пациентов после кардиохирургических операций (фиг.1).
Воздействие по схеме, предложенной авторами в случае проведения операции фрагментации (фиг. 2), позволяет провести эффективное воздействие на ткани предсердий и миокарда с учетом топографо-анатомических взаимоотношений межпредсердной перегородки и фиброзного кольца митрального клапана и также добиться прерывания фронта волны возбуждения, более надежного разделения сообщения между субстратами фибрилляции желудочков.
Воздействие токами указанного диапазона выбрано как более удобный способ в плане осуществления, контроля и качества воздействия. Режим воздействия подобран на основании экспериментальных и клинических наблюдений, его величина (5-15 Вт) необходима и достаточна для получения зоны деструкции необходимой глубины и ширины (объема). Деструкция осуществляется в виде двойной непрерывной линии с целью надежного разделения мышечных сообщений левого предсердия и межпредсердной перегородки.
Введение блока дифференцирования, блока, выполненного с возможностью задания максимума для производной выходного напряжения, выделенной на блоке дифференцирования, а также формирование резонансного контура на выходе генератора позволяет определить момент начала "подгорания" ткани к поверхности активного электрода, момент прекращения контакта активного электрода и ткани, когда возникают вспышки и искрения из-за быстрого уменьшения площади контакта и, как следствие, резкого увеличения величины энергии, приходящейся на единицу площади контакта, тем самым снижая излишнюю термическую травматизацию ткани оперируемого органа. Форма и характер поверхности активного электрода выбраны оптимальными для снижения вероятности излишнего нежелательного искрообразования между его поверхностью и поверхностью ткани оперируемого органа.
Расположение пассивного электрода связано с необходимостью плотного прилегания последнего к ткани оперируемого органа.
Таким образом, предлагаемый способ обладает следующими преимуществами: относительной технической простотой и более высокой скоростью выполнения процедуры, не требует специального хирургического навыка, высокой эффективностью проведения манипуляции, которая обусловлена возможностью исключить излишнюю механическую травматизацию тканей сердца и последующий за ним этап восстановления их целостности путем сшивания, влекущий за собой процесс рубцевания и т.д. Применение данного способа позволяет более качественно, точно и в необходимом объеме провести воздействие в условиях повышенной визуализации зоны воздействия. Критерием оценки эффективности проводимого лечения может служить снижение процента применения антиаритмических препаратов в послеоперационном периоде и снижение частоты пароксизмов мерцательной аритмии.
Источники информации
1. Guiraudon, G. , Klеin J.O., Sharma, D.A. and Yee, R., Surgical alternatives for supraventricular tachycardias.//American Journal of Cardiology.-1989.- 64.-92J-96J.
2. Cox, L.J. Schuessler, B.R. and D'Agostino, J.H. еi al... The surgical treatment of atrial fibrillation 111. Development of a definitive surgical procedure. // Journal of Thoracic and Cardiovascular Surgery. -1991.-101.- 569-583.
3. Бокeрия Л.А. Современное состояние проблемы тахиаритмий и новые направления // Матер. IV Всеc. Съезда кардиологов. Тезисы докл. М., 1986.-С. 9-10.
4. Янушкявичус З.И., Бредикис Ю.Ю., Лукошевичуте А.И., Забела П.В. Нарушения ритма и проводимости сердца // М., Медицина, 1984.-286с.
5. Cursi G., Purcado A., Viola С. Et al. Deleterious clinical and hemodynamiс effects of a V-A retroconduction in symtomatic sinus bradyarrhythmias treated with VVI pacing //Cardias pacing. - Vienna: Steinkopf Verl., 1983.
6. Бокeрия Л.А., Ревишвили А.Ш., Рыбалов А.Г., Авальяни А.Г., Марин А.Г. Электрическая изоляция левого предсердия как новый метод хирургической коррекции некоторых форм наджелудочковых тахикардий // Гр.хир. - 1981.- 6.- С. 28-33 (прототип).
7. Сох, L.J., The surgical treatment of atrial fibrillation. IV Surgical technique. //Journal of Thoracic and Cardiovascular Surgery. -1991.- 584-592.
8. Деструктор радиочастотный проводящих путей сердца РЧ-100-ТИ "Электропульс" ТГЕИ 941612.001 ТУ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ ВО ВРЕМЯ ОПЕРАЦИЙ С ИСКУССТВЕННЫМ КРОВООБРАЩЕНИЕМ БЕЗ ВСКРЫТИЯ ЛЕВЫХ ОТДЕЛОВ СЕРДЦА | 2005 |
|
RU2294155C2 |
| СПОСОБ ДОСТИЖЕНИЯ ТРАНСМУРАЛЬНОСТИ ПОВРЕЖДЕНИЯ МИОКАРДА ПРЕДСЕРДИЙ ПРИ ЛЕЧЕНИИ НАДЖЕЛУДОЧКОВЫХ АРИТМИЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2394522C2 |
| УСТРОЙСТВО ДЛЯ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ СО СЛОЖНЫМИ НАРУШЕНИЯМИ РИТМА СЕРДЦА | 1998 |
|
RU2136237C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2024 |
|
RU2833935C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2015 |
|
RU2613445C1 |
| Способ хирургического лечения фибрилляции предсердий при сопутствующей коррекции клапанной патологии в условиях искусственного кровообращения | 2023 |
|
RU2827408C1 |
| ЭЛЕКТРОКАРДИОСТИМУЛЯТОР | 2000 |
|
RU2190434C2 |
| БИПОЛЯРНЫЙ ЭЛЕКТРОХИРУРГИЧЕСКИЙ ИНСТРУМЕНТ ДЛЯ ДЕСТРУКЦИИ МИОКАРДА ПРЕДСЕРДИЙ ПРИ ЛЕЧЕНИИ НАДЖЕЛУДОЧКОВЫХ АРИТМИЙ | 2016 |
|
RU2665627C2 |
| Способ хирургического лечения гипертрофической обструктивной кардиомиопатии | 2015 |
|
RU2608705C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИНЦИЗИОННОГО ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ ПРИ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ПОРОКОВ СЕРДЦА | 2007 |
|
RU2407461C2 |
Изобретение относится к области медицины, кардиохирургии. Проводят радиочастотную деструкцию со стороны эпикарда по двойным непрерывно параллельно идущим линиям. При больших размерах левого предсердия радиочастотную деструкцию проводят по линии, начинающейся от заднемедиальной комиссуры митрального клапана и заканчивающейся у переднелатеральной комиссуры митрального клапана. Линию деструкции ведут параллельно межпредсердной перегородке. При больших размерах левого и правого предсердий выполняют правую атриотомию от основания ушка правого предсердия по его боковой стенке до заднего межпредсердного валика. Разрез продолжают линией радиочастотной деструкции эпикардиально до устья коронарного синуса и до фаброзного кольца трикуспидального клапана. С противоположной стороны деструкцию проводят эндокардиально от устья верхней полой вены до верхнего края межпредсердной перегородки к основанию овальной ямки. После левой атриотомии - эпикардиально вдоль задней межпредсердной борозды от нижнего угла разреза левого предсердия. Далее, огибая кнаружи устье левой нижней легочной вены к основанию ушка левого предсердия, которое отсекают, и от его основания линию деструкции продолжают эпикардиально вверх, соединяя с ранее выполненными линиями деструкции. Устройство для осуществления способа состоит из радиочастотного генератора, блока регулировки выходного напряжения, задатчика выхода, датчиков тока и напряжения. Рабочая часть включает активный и пассивный электроды. Задатчик выхода соединен с блоком регулировки выходного напряжения, который соединен с радиочастотным генератором, через датчики тока и напряжения. Дополнительно введены задатчик максимума производной выходного напряжения и блок дифференцирования, а на выходе генератора установлен резонансный контур. Изобретение позволяет повысить эффективность лечения за счет снижения числа осложнений и сокращения времени операции. 2 с. и 4 з.п. ф-лы, 5 ил.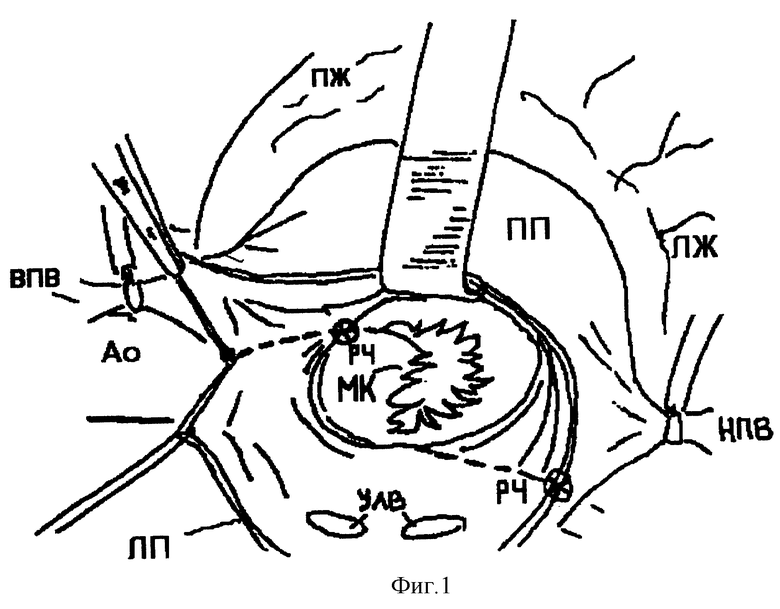
| ИЗЛУЧАТЕЛЬ | 1994 |
|
RU2089022C1 |
| СПОСОБ РАДИОЧАСТОТНОЙ ГИПЕРТЕРМИИ ЭЛЕКТРОМАГНИТНЫМ ПОЛЕМ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1993 |
|
RU2121385C1 |
| ЭЛЕКТРОХИРУРГИЧЕСКИЙ АППАРАТ | 1990 |
|
RU2008830C1 |
| ВЫСОКОЧАСТОТНОЕ ЭЛЕКТРОХИРУРГИЧЕСКОЕ УСТРОЙСТВО | 1993 |
|
RU2069990C1 |
| ЭЛЕКТРОХИРУРГИЧЕСКОЕ УСТРОЙСТВО | 1998 |
|
RU2136238C1 |
| СПОСОБ ОЦЕНКИ ПАРАМЕТРОВ СЕЛЬХОЗМАШИНЫ | 1989 |
|
RU2023359C1 |
| БОКЕРИЯ Л.А | |||
| и др | |||
| Электрическая изоляция левого предсердия как модель хирургического лечения некоторых форм нарушения ритма сердца | |||
| Гр | |||
| хир., 1981, №6, с | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| БОКЕРИЯ Л.А | |||
| Результаты радикального хирургического лечения фибрилляции предсердий | |||
| Гр | |||
| и серд.-сосуд | |||
| хир., 1996, №3, с | |||
| Шланговое соединение | 0 |
|
SU88A1 |
| НЕМКОВ А.С | |||
| и др | |||
| Презэпикальная деструкция ДАВС при синдроме WPW | |||
| Гр | |||
| и серд.-сосуд | |||
| хир., 1996, №6, с | |||
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| ВЫГОВСКИЙ А.Б | |||
| Импульсный режим - новые возможности метода радиочастотной деструкции проводящих путей сердца | |||
| Гр | |||
| и серд.-сосуд | |||
| хир., 1996, №1, с | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
Авторы
Даты
2002-07-10—Публикация
2000-02-15—Подача