Изобретение относится к новым химическим веществам, а именно к цефалоспориновым антибиотикам общей формулы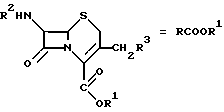
где R1=Na,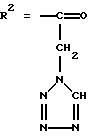
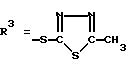
цефазолина натриевая соль (ЦФ), антибиотик первого поколения.
R1=Na,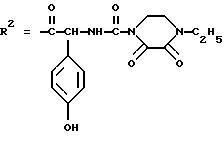

цефоперазон, цефалоспориновый антибиотик третьего поколения.
Цефалоспориновые антибиотики по структуре относятся к бета-лактамным соединениям, в основе строения которых лежит 7-амино-цефалоспориновая кислота (7-АЦК), и обладают широким спектром антибактериальной активности (Машковский М. Д. Лекарственные средства. - Харьков: Торсинг, 1997. Т. 2. - 590 с.)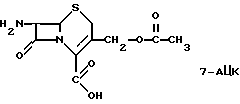
Представители четырех поколений антибиотиков этой группы используются либо в виде кислот R1=H, либо в виде натриевых солей R1=Na (кроме препарата Зиннат). Как правило, натриевые соли цефалоспоринов являются хорошо растворимыми в воде веществами. Соли или органические комплексы производных 7-АЦК с какими-либо другими катионами, кроме Na, включая катионы красителей, в литературе не описаны и в фармакологии не применяются.
Авторами предлагаются новые органические комплексы цефалоспоринов, полученные при взаимодействии с известными красителями метиленовым синим (N,N-бис- (диметил)-фенотиазоний хлоридом) или этакридина лактатом (риванолом, 2-этокси-6,9-диаминоакридина лактатом) по реакции обмена с образованием малорастворимых в воде соединений.
Полученные продукты реакции сочетают в себе и красящие свойства метиленового синего или риванола, и бактерицидную активность антибиотика и вследствие плохой растворимости в воде могут быть использованы как красители с пролонгированным антибактериальным действием для некоторых изделий медицинской техники, например хирургических нитей, искусственных сосудистых протезов и т.п.
Предлагаемое изобретение иллюстрируется следующими примерами.
Пример 1. К водному раствору цефазолина приливают водный раствор метиленового синего из расчета, чтобы в мольном отношении соблюдался небольшой избыток антибиотика. Выпавшему осадку дают сформироваться на холоду, затем отфильтровывают и несколько раз промывают осадок ледяной водой. Осадок высушивают на воздухе сначала при комнатной температуре, затем при 105oС до постоянного веса. Получают блестящие фиолетовые пластинки нового вещества, при сильном нагревании разлагающегося. Завершенность реакции метиленового синего с цефазолином контролируют по отсутствию органического хлора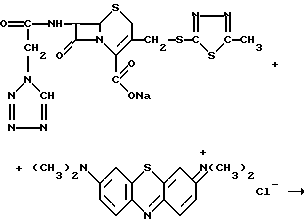
цефазолина натриевая соль (ЦФ) метиленовый синий (МС)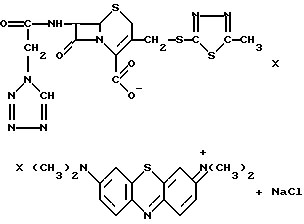
комплексное соединение цефазолина с метиленовым синим (ЦФМС)
Для установления состава образующегося комплекса ЦФМС берут точную навеску вещества, растворяют в воде и анализируют на содержание метиленового синего.
Метиленовый синий определяют по методике, утвержденной в ГФ XI и основанной на реакции осаждения бихроматом калия. Нерастворимый в воде бихромат метиленового синего отфильтровывают, а избыток бихромата калия определяют йодометрическим методом (Беликов В.Г. Учебное пособие по фармацевтической химии. - М.: Медицина. - 1979. - 552 с.).

К2Сr2O7+6KJ+7H2SO4-->Cr2(SO4)3+3J2+ +4K2SO4+7Н2O;
J2+2Na2S2O3-->2NaJ+Na2S2O6.
По результатам аналитического определения метиленового синего, входящего в состав комплексного соединения ЦФМС, взаимодействие красителя с цефазолином приводит к образованию комплекса состава ЦФ:МС=1:1.
Пример 2. Реакцию метиленового синего с цефоперазоном, цефалоспорином третьего поколения, проводят аналогично примеру 1
Комплекс цефоперазона с метиленовым синим
Пример 3. К водному раствору цефазолина приливают водный раствор этакридина лактата (ЭЛ). Выпавший осадок желтого цвета отфильтровывают, несколько раз промывают водой, затем этиловым спиртом; высушивают на воздухе. Полученный продукт реакции плохо растворяется в воде и спирте и, по результатам аналитического определения одного из компонентов (этакридина), содержит равные в мольном отношении количества красителя и антибиотика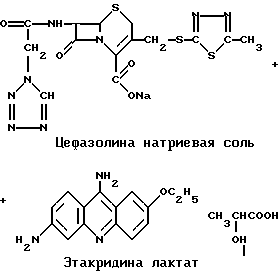
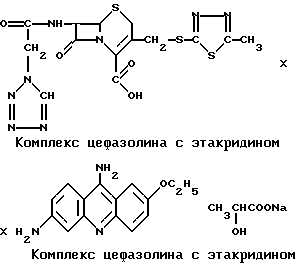
Этакридина основание определяют колориметрическим методом при 520 нм после проведения с комплексом цефазолина реакции диазотирования (Беликов В. Г. Учебное пособие по фармацевтической химии. - М.: Медицина. - 1979. - 552 с.).
Образование труднорастворимой в воде комплексной соли цефазолина с этакридином может быть использовано при получении материалов с антимикробными свойствами. При этом этакридина основание выполняет функции не только красителя, но и антисептического вещества.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МАТЕРИАЛА С АНТИМИКРОБНЫМИ СВОЙСТВАМИ | 1998 |
|
RU2157244C2 |
| СПОСОБ АНТИБАКТЕРИАЛЬНОЙ ЗАЩИТЫ АНАСТОМОЗОВ ПРИ РЕЗЕКЦИЯХ КИШЕЧНИКА | 1999 |
|
RU2184545C2 |
| СПОСОБ ФОРМИРОВАНИЯ ГЕПАРИНИЗИРОВАННОЙ ПОВЕРХНОСТИ | 1998 |
|
RU2155593C2 |
| СПОСОБ ФОРМИРОВАНИЯ АНТИКОАГУЛЯНТНОЙ ПОВЕРХНОСТИ | 1998 |
|
RU2152217C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕЗОВ КРОВЕНОСНЫХ СОСУДОВ | 2001 |
|
RU2241414C2 |
| СПОСОБ ПРОФИЛАКТИКИ РЕОККЛЮЗИЙ ПРИ ОПЕРАЦИЯХ НА МАГИСТРАЛЬНЫХ СОСУДАХ | 1999 |
|
RU2185171C2 |
| СПОСОБ ПРОФИЛАКТИКИ АСЕПТИЧЕСКОГО ВОСПАЛЕНИЯ ПРИ ОПЕРАЦИЯХ НА МАГИСТРАЛЬНЫХ СОСУДАХ | 1999 |
|
RU2180846C2 |
| СПОСОБ ФОРМИРОВАНИЯ ГЕПАРИНИЗИРОВАННОЙ ПОВЕРХНОСТИ | 1998 |
|
RU2137507C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АДАМАНТИЛАЛКИЛОВЫХ ЭФИРОВ | 1998 |
|
RU2145593C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ E3, E8-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]ДЕКАНА И E3, E9-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]ДЕКАНА | 2000 |
|
RU2188813C2 |
Изобретение относится к области медицины и касается новых органических комплексов цефалоспориновых антибиотиков с красителями метиленовым синим или этакридина лактатом. Малорастворимые в воде соединения сочетают в себе красящие свойства и бактерицидную активность антибиотиков и могут быть использованы как красители с улучшенным пролонгированным антибактериальным действием для некоторых изделий медицинской техники, например хирургических нитей, искусственных сосудистых протезов и т.д.
Органические комплексы цефалоспориновых антибиотиков общей формулы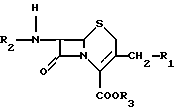

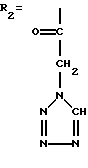

или
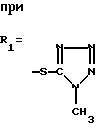
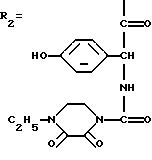
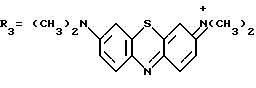
или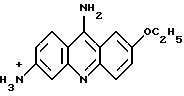
обладающие антимикробным действием.
| Лекарственные препараты в России | |||
| Справочник ВИДАЛЬ | |||
| - М.: Астра Фарм Сервис, 1995, с.451 | |||
| ПРОИЗВОДНЫЕ 8-ОКСО-4- ТИА-1- АЗАБИЦИКЛО- ОКТ-2-ЕН-2-КАРБОНОВЫХ КИСЛОТ | 1991 |
|
RU2042682C1 |
| ПРОИЗВОДНЫЕ ЦЕФАЛОСПОРИНА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2104280C1 |
Авторы
Даты
2002-07-10—Публикация
1999-02-23—Подача