Предлагаемое изобретение относится к производству диоксида хлора, используемого для обеззараживания питьевых, сточных и охлаждающих вод, а также в качестве окислителя в технологических процессах и для других целей.
Применение диоксида хлора взамен жидкого хлора для обработки питьевой воды имеет ряд преимуществ перед хлором.
В канадском патенте 543589 описывается процесс получения диоксида хлора и хлора путем взаимодействия хлората натрия, хлорида натрия и серной кислоты при высокой кислотности при температуре 30oС и атмосферном давлении. Для разбавления и удаления образующихся газообразных продуктов через реактор пропускают воздух.
Недостатками данного изобретения являются относительно невысокая скорость образования диоксида хлора и хлора вследствие неоптимальных условий протекания процесса (низкая концентрация хлората натрия и температура) и, соответственно, большой необходимый объем реактора, а также поглотительной башни, в которой производится последующее растворение диоксида хлора водой. Данные недостатки делают этот способ и аппаратуру малопригодными и трудно осуществимыми в процессах водоподготовки на автоматизированной установке.
В европейском патенте 0106503 - прототипе предлагаемого изобретения взаимодействие реагентов в реакторе осуществляют восстановлением хлорат-ионов хлорид-ионами в реакционной среде, содержащей серную кислоту с общей кислотностью 8,5-12 нормальной, путем подачи раствора хлората и хлорида натрия и серной кислоты в зону реакции и удаления отработанного реакционного раствора из зоны реакции. Для удаления газовой смеси из паров воды, двуокиси хлора и хлора из зоны реакции применяют разреженную атмосферу. Для сохранения концентрации образующейся сульфатной соли в реакционной среде ниже уровня насыщения контролируют время пребывания реакционного раствора в зоне реакции.
Процесс ведут при невысоких (0,2-0,05 моль/л) рабочих концентрациях хлората и хлорида натрия, при температуре 40-70oС в условиях кипения реакционной смеси, которое обеспечивается поддержанием большого разрежения (абсолютное давление от 60 до 160 мм рт. столба).
В качестве реактора получения диоксида хлора и хлора приводится полый цилиндрический аппарат с раздельными вводами раствора хлората и хлорида натрия и серной кислоты через стенки корпуса у днища, вертикальными стержнеобразными нагревательными элементами реакционного раствора, подведенными через днище и помещенными в вытяжные трубы, а также одним общим отверстием у верхней крышки для вывода образующихся разбавленной паром газовой смеси и отработанного реакционного раствора в эжектор. Согласно примерам за время пребывания реакционной смеси в реакторе от 30 до 60 минут достигается степень превращения хлората в диоксид хлора 87,8%. По описанию, благодаря переливу отработанного реакционного раствора из аппарата, предупреждается кристаллизация сульфата натрия из раствора в зоне реакции.
Существенными недостатками данного изобретения являются относительно невысокая практическая степень превращения хлората натрия в диоксид хлора и хлор в связи с неоптимальными условиями процесса (низкая рабочая концентрация хлората и хлорида натрия), необходимость применения нагрева реакционного раствора и глубокого разрежения.
Помимо этих недостатков, существует необходимость тонкого регулирования соотношения между количествами образующегося диоксида хлора и водяного пара, требующегося для разбавления газовой смеси. Не исключается также возможность частичных потерь диоксида хлора вследствие его самопроизвольного распада вблизи нагревательных элементов и кристаллизации кислого сульфата натрия из реакционного раствора.
Указанные недостатки прототипа устраняются предлагаемым изобретением.
Технической задачей настоящего изобретения являются: интенсификация и упрощение процесса взаимодействия и повышение выхода конечного продукта (повышение степени превращения хлората натрия в диоксид хлора и устранение потерь от распада диоксида хлора).
Техническая задача решается применением способа получения раствора диоксида хлора взаимодействием раствора хлората и хлорида натрия и серной кислоты высокой концентрации, включающего выделение диоксида хлора и хлора в газовую фазу, контроль времени пребывания реакционной среды в зоне реакции и последующее отведение газовой смеси и отработанного реакционного раствора с применением разреженной атмосферы на поглощение водой. При этом процесс взаимодействия проводят ступенчато не менее, чем в две стадии, с последовательным убыванием концентраций реагентов. Концентрации хлората и хлорида натрия в реакционной зоне первой стадии в зависимости от количества применяемых ступеней составляют от 1,5 до 0,25 моль/л по каждому из них. Выделяющийся газ разбавляют воздухом, просасываемым через реакционную среду. Отработанный раствор реагентов на последней стадии разбавляют водой до концентрации сульфата натрия меньше предельной растворимости. На первую стадию подают воздух из атмосферы как для перемешивания реагентов в зоне реакции, так и для разбавления выделяющегося газа диоксида хлора и хлора до взрывобезопасной концентрации (не более 10% объемных по диоксиду хлора).
Процесс проводят в реакторе, включающем корпус с патрубками ввода и вывода реагентов и продуктов, который содержит не менее двух переточных реакционных камер, расположенных каскадно, патрубки дозирования в верхнюю камеру растворов хлората и хлорида натрия, серной кислоты и воздуха, врезанные через верхнюю крышку корпуса; патрубок дозирования в нижнюю камеру воды; патрубок для отвода продуктов реакции из нижней камеры, расположенный на уровне зеркала поверхности.
При этом патрубок ввода раствора хлората и хлорида натрия выведен в газовоздушное пространство на поверхность реакционного пространства, а патрубок ввода серной кислоты - непосредственно в объем реакционного раствора. Патрубок ввода воздуха выведен в объем реакционного раствора со дна верхней камеры. Патрубок ввода воды выведен в объем отработанного реакционного раствора нижней камеры.
Существенные отличия предлагаемого изобретения от прототипа:
1. Процесс взаимодействия проводят ступенчато не менее, чем в две стадии, с последовательным убыванием концентраций реагентов, при этом концентрации хлората и хлорида натрия в реакционной зоне первой стадии составляют в зависимости от числа камер - от 1,5 до 0,25 моль/л. Установление максимальной целесообразной концентрации хлората натрия 1,5 моль/л возможно при осуществлении процесса в реакторе с большим числом реакционных камер. При уменьшении концентрации хлората натрия менее 0,25 моль/л падает производительность реактора.
2. Выделяющийся газ диксид хлора и хлор разбавляют воздухом, просасываемым через реакционную среду, до взрывобезопасной концентрации по диоксиду хлора.
3. Отработанный раствор реагентов на последней стадии разбавляют водой до концентрации сульфата натрия меньше предельной растворимости (20% по сульфату натрия).
4. Реактор работает без нагрева за счет теплового эффекта реакции и при меньшем разрежении. Реактор по прототипу работает при искусственном подогреве реакционной среды до температуры кипения в условиях глубокого вакуума и отсутствия разбавления воздухом, поэтому в нем не исключаются локальные перегревы и самораспад неустойчивого диоксида хлора.
5. Реактор содержит внутри корпуса:
- не менее двух переточных реакционных камер, расположенных каскадно;
- патрубки дозирования в верхнюю камеру растворов хлората и хлорида натрия, серной кислоты и воздуха, врезанные через верхнюю крышку корпуса;
- патрубок дозирования в нижнюю камеру воды;
- патрубок для отвода продуктов реакции из нижней камеры, расположенный на уровне зеркала поверхности.
Патрубок ввода раствора хлората и хлорида натрия выведен в газовоздушное пространство на поверхность реакционного раствора верхней камеры.
Патрубок ввода серной кислоты выведен в объем реакционного раствора верхней камеры, т.к. дозируемая концентрированная кислота способна разлагать диоксид хлора в газовой фазе.
Патрубок ввода воздуха выведен со дна камеры для обеспечения наилучшего перемешивания реакционной среды и взаимодействия в ней реагентов, а также отдувки растворенного диоксида хлора из раствора (отдувка интенсифицирует процесс взаимодействия реагентов). Постоянное удаление газообразных продуктов из зоны реакции систематически сдвигает равновесие реакции вправо и обеспечивает интенсификацию процесса.
Патрубок ввода воды выведен в объем отработанного раствора для обеспечения наилучшего перемешивания и разбавления раствора.
6. Организация движения в реакторе образующейся газовоздушной смеси в направлении сверху вниз, что обеспечивает лучшее усреднение ее состава, т.к. диоксид хлора и хлор соответственно в 2,30 и 2,45 раза плотнее воздуха, и более полное удаление их из реактора. Происходящая гомогенизация состава образующейся газовой смеси наряду с исключением ее дестабилизирующего локального перегрева повышает устойчивость диоксида хлора в смеси к самораспаду. Исключение потерь диоксида хлора от разложения повышает его общий выход.
Разрежение в предлагаемом реакторе необходимо для преодоления гидравлического сопротивления столба реакционного раствора в первой камере при просасывании через его толщу воздуха, а также транспортирования газовоздушной смеси и отработанного реакционного раствора из последней камеры в эжектор. Величина разрежения составляет 75-150 мм рт. столба.
Исходные реагенты подают в первую (верхнюю) реакционную камеру малого объема, в которой благодаря высокой рабочей концентрации реагентов хлората и хлорида натрия процесс протекает особенно интенсивно. Разделение зоны реакции реагентов на стадии позволяет избежать разбавления вновь поступающих исходных реагентов отработанными растворами, сохраняя высокие концентрации реагирующих веществ на первой стадии. На последующих стадиях происходит доразложение реагентов при убывающих, но больших, чем в прототипе, рабочих концентрациях, что обеспечивает также более высокие скорости реакции. Только на конечной стадии рабочие концентрации реагентов одинаковы или даже несколько меньше, чем в прототипе. Однако общая скорость реакции образования диоксида хлора и производительность реактора в целом значительно возрастают по сравнению с прототипом.
Оптимальная с точки зрения осуществления основного химического процесса образования диоксида хлора - температура 35-45oС обеспечивается за счет теплоты протекающих химических реакций в малом реакционном объеме, а также сокращения рассеивания теплоты в окружающую среду.
Благодаря стадийному осуществлению процесса в каскаде реакционных камер в условиях, наиболее отвечающих оптимальным, достигается в целом более высокая степень разложения хлората. В частности, в реакторе с тремя камерами основная химическая реакция практически завершается и достигается достаточная полнота превращения хлората в диоксид хлора и хлор уже во второй по ходу раствора реакционной камере. Степень использования хлората в оптимальном режиме составляет до 80% в первой, 90-92,5% во второй и 95% в третьей камерах.
Последняя (нижняя) камера служит для завершения реакции и разбавления прореагировавшего реакционного раствора до концентрации сульфата натрия, заведомо меньшей его предельной растворимости, что повышает надежность и безопасность работы реактора.
При осуществлении разложения хлората натрия с получением диоксида хлора в предлагаемом нами стадийном реакторе значительно сокращаются по сравнению с известным реактором его общий рабочий объем и продолжительность взаимодействия реагентов. Общее время пребывания реакционного раствора в предлагаемом реакторе составляет 6-12 минут при большей, чем в прототипе, степени превращения хлората в диоксид хлора, где время пребывания реагентов, как уже отмечалось, составляет 30-60 минут.
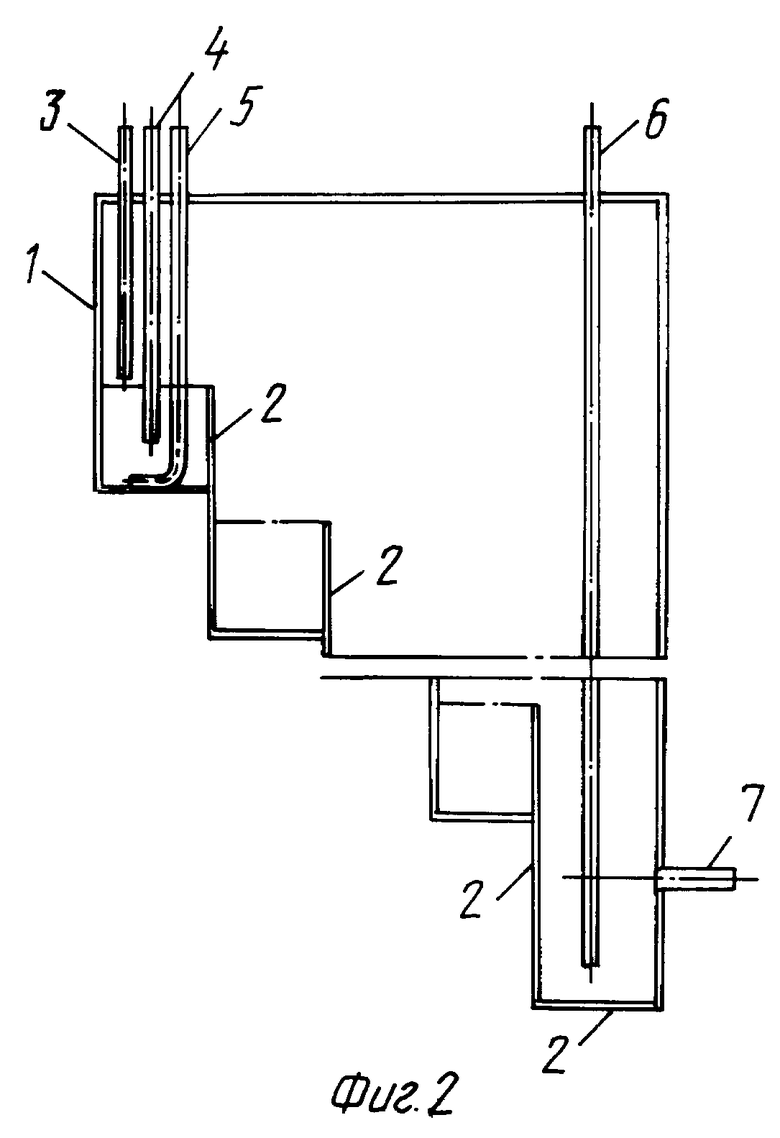
На фигурах 1 и 2 представлен реактор соответственно с двумя (фиг.1), четырьмя и более (фиг.2) реакционными камерами.
Реактор получения раствора диоксида хлора состоит из корпуса (1), реакционных камер (2), расположенных внутри корпуса каскадно, патрубков (3,4,5 и 6) для ввода соответственно раствора смеси хлората и хлорида натрия, серной кислоты, воздуха и воды и патрубка (7) для вывода газовоздушной смеси и отработанного реакционного раствора.
При работе реактора в верхнюю реакционную камеру (2), расположенную в верхней части корпуса (1), подают через патрубок (3) раствор смеси хлората и хлорида натрия на поверхность реакционного раствора и через патрубок (4) серную кислоту в объем реакционного раствора. За счет разрежения через патрубок (5) просасывают воздух из атмосферы. Образовавшаяся реакционная смесь самотеком последовательно проходит через все ниже расположенные камеры, при этом происходит доразложение исходных реагентов. В нижнюю камеру через патрубок (6) в объем прореагировавшей реакционной смеси подают воду для разбавления до концентрации сульфата натрия меньше предельной растворимости. Газовоздушная смесь диоксида хлора и разбавленный отработанный реакционный раствор через патрубок (7) выводятся из нижней камеры общим потоком за счет разрежения на поглощение водой.
Предлагаемое изобретение иллюстрируется следующими примерами его практического осуществления.
Пример 1
Производится непрерывное получение раствора диоксида хлора и хлора для обеззараживания воды в соединенном с водоструйным эжектором и работающем под разрежением вертикальном реакторе с расположенными внутри него каскадно тремя реакционными камерами при дозировании в верхнюю камеру раствора смеси хлората и хлорида натрия, серной кислоты и просасывании через реакционный раствор воздуха из атмосферы, а также подаче в нижнюю камеру части обеззараживаемой воды.
Для получения 150 г/час диоксида хлора берется 256 г/час хлората натрия, 248 г/час хлорида натрия и 767 г/час серной кислоты.
Разрежение в реакторе поддерживается 100 мм рт. столба. В реактор подсасывается 700 л/час воздуха. В нижнюю камеру вводится 400 мл/час воды.
Температура в первой и второй по ходу раствора камерах реактора составляет 40oС.
Концентрации хлората натрия и хлорида натрия в первой (верхней) камере составляют 0,4 моль/л.
Получается 150 г/час диоксида хлора и 91 г/час хлора, растворенных (поглощенных) обеззараживаемой водой вместе с переливающимся из нижней камеры разбавленным отработанным раствором в эжекторе.
Полученным раствором диоксида хлора и хлора при введении в основной поток обрабатывается (обеззараживается) 150 м3/час воды.
С водой уходит неразложившихся 13 г/час хлората натрия, 2 г/час хлорида натрия и 532 г/час серной кислоты. При общем времени взаимодействия реагентов в реакторе 9 минут степень превращения хлората натрия в хлорид натрия составляет 92,5%.
Пример 2
Процесс ведется по примеру 1, но в отличие от примера 1 процесс проводится в шестикамерном реакторе при концентрациях хлората натрия и хлорида натрия в первой камере 1,5 моль/л.
Степень превращения хлората натрия в диоксид хлора в реакторе составляет 95%.
Пример 3
Процесс ведется по примеру 1, но в отличие от примера 1 процесс проводится в двухкамерном реакторе при концентрациях хлората натрия и хлорида натрия в первой реакционной камере 0,25 моля.
Степень превращения хлората натрия в диоксид хлора в реакторе составляет 90%.
В таблице приведено сравнение основных характеристик прототипа и предлагаемого изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА ДИОКСИДА ХЛОРА И ХЛОРА В ВОДЕ И РЕАКТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2005 |
|
RU2307067C2 |
| АППАРАТ ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА ПОЛУЧЕНИЯ РАСТВОРА ДИОКСИДА ХЛОРА И ХЛОРА В ВОДЕ | 2011 |
|
RU2503614C2 |
| СПОСОБ АМПЕРОМЕТРИЧЕСКОГО КОНТРОЛЯ ПРОЦЕССА НЕЙТРАЛИЗАЦИИ ХРОМА (6+) | 1999 |
|
RU2155331C1 |
| Способ спектрофотометрического дифференциального косвенного определения концентрации диоксида хлора в питьевой воде | 2020 |
|
RU2748298C1 |
| СПОСОБ УТИЛИЗАЦИИ ОТРАБОТАННЫХ АВТОМОБИЛЬНЫХ АНТИФРИЗОВ | 2001 |
|
RU2188212C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОРАТОВ БАРИЯ | 1999 |
|
RU2146652C1 |
| УСТАНОВКА ДЛЯ ПОЛУЧЕНИЯ ДИОКСИДА ХЛОРА И ХЛОРА | 2014 |
|
RU2571006C2 |
| УСТРОЙСТВО ДЛЯ МИКРОДОЗИРОВАНИЯ ЭЛЕКТРОПРОВОДНЫХ ЖИДКОСТЕЙ | 1998 |
|
RU2153653C2 |
| СПОСОБ ПЕРЕРАБОТКИ СОДОСУЛЬФАТНОЙ СМЕСИ | 2001 |
|
RU2188794C1 |
| СОСТАВ ДЛЯ СКРЫТОЙ ЗАПИСИ ИНФОРМАЦИИ И СПОСОБ СКРЫТОЙ ЗАПИСИ ИНФОРМАЦИИ | 2001 |
|
RU2203297C1 |

Изобретение относится к производству диоксида хлора, используемого, в частности, для обеззараживания при очистке питьевой и сточной воды. Она достигается применением способа получения раствора диоксида хлора взаимодействием раствора хлората и хлорида натрия и серной кислоты высокой концентрации, включающего выделение диоксида хлора и хлора в газовую фазу, контроль времени пребывания реакционной среды в зоне реакции и последующее отведение газовой смеси и отработанного реакционного раствора на поглощение водой с применением разреженной атмосферы. Процесс проводят ступенчато не менее, чем в две стадии с последовательным убыванием концентрации реагентов, при этом рабочие концентрации хлората и хлорида натрия в реакционной зоне первой стадии составляют от 1,5 до 0,25 моль/л, выделяющийся газ разбавляют на первой стадии воздухом до взрывобезопасной концентрации по диоксиду хлора, а отработанный реакционный раствор на последней стадии разбавляют водой до концентрации сульфата натрия меньше предельной растворимости. Процесс проводят в реакторе, включающем корпус с патрубками ввода и вывода реагентов и продуктов, который содержит не менее двух переточных реакционных камер, расположенных каскадно, патрубки дозирования в верхнюю камеру растворов хлората и хлорида натрия, серной кислоты и воздуха, врезанные через верхнюю крышку корпуса, патрубок дозирования в нижнюю камеру воды, патрубок для отвода продуктов реакции из нижней камеры, расположенный на уровне зеркала поверхности. Патрубок ввода раствора хлората и хлорида натрия выведен в газо-воздушное пространство на поверхность реакционного раствора, а патрубок ввода серной кислоты - непосредственно в объем реакционного раствора. Патрубок ввода воздуха выведен в объем реакционного раствора со дна верхней камеры. Патрубок ввода воды выведен в объем реакционного раствора нижней камеры. Изобретение позволяет ускорить процесс и повысить выход конечного продукта. 2 с. и 4 з.п. ф-лы, 2 ил., 1 табл.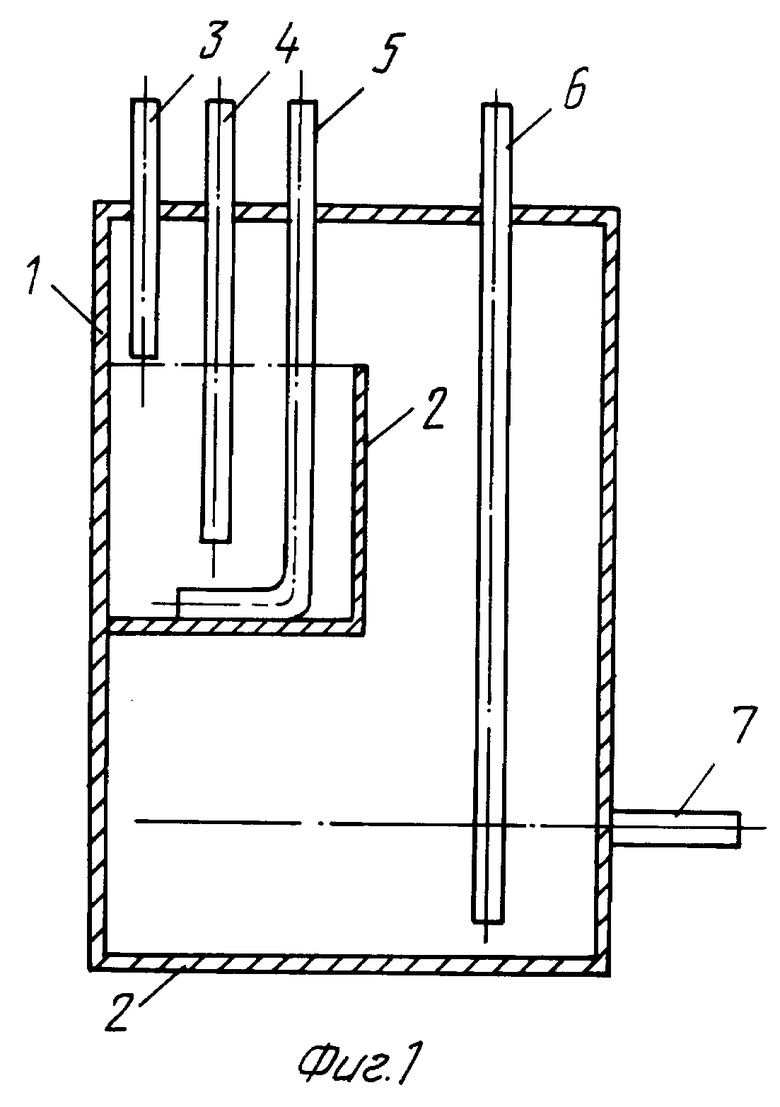
| Устройство для слива рабочей жидкости из полости гидромуфты | 1956 |
|
SU106503A1 |
| СПОСОБ НЕПРЕРЫВНОГО ПОЛУЧЕНИЯ ДВУОКИСИ ХЛОРА | 0 |
|
SU211423A1 |
| Способ получения двуокиси хлора | 1988 |
|
SU1776251A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА ХЛОРА (ВАРИАНТЫ) | 1992 |
|
RU2104247C1 |
| EP 0095199 А1, 30.11.1983 | |||
| GB 1077306 А, 26.07.1967 | |||
| US 3976758 А, 24.08.1976 | |||
| Огнетушитель | 0 |
|
SU91A1 |
Авторы
Даты
2002-09-10—Публикация
2001-02-08—Подача