Изобретение относится к новому способу лечения млекопитающего, страдающего шизофренией или острыми полиморфными расстройствами с симптомами шизофрении ("шизофрениформными расстройствами"), либо восприимчивого к указанным заболеваниям, таким как катоническая шизофрения, злокачественная (деструктивная) шизофрения, параноидная шизофрения, вялотекущая шизофрения, реактивный психоз, шизоэффективные расстройства, индуцированное психотическое расстройство, шизотипическое расстройство личности, шизоидное расстройство личности, параноидное расстройство личности, и бредовое (параноидное) расстройство.
В настоящее время существует много лекарственных средств, применяемых для лечения расстройства центральной нервной системы. Одной из известных категорий таких лекарственных средств являются антипсихотические средства, используемые для лечения серьезных психических заболеваний, таких как шизофрения и шизофрениформные расстройства. Однако для лечения таких состояний часто оказывается недостаточно имеющихся в настоящее время лекарственных средств. Лекарственные препараты могут вызывать нежелательные и серьезные побочные эффекты, такие как поздняя дискинения, нарушение двигательных функций, и другие нежелательные экстрапирамидные расстройства.
Поэтому для снижения или устранения этих эффектов необходимо разработать более безопасные и более эффективные средства. Кроме того, многие пациенты не восприимчивы или лишь частично восприимчивы к существующим лекарственным средствам. По оценкам специалистов число таких невосприимчивых или частично восприимчивых пациентов варьируется от 40% до 80% от числа всех пациентов, подвергавшихся лечению известными препаратами.
За время применения антипсихотических средств было установлено, что эти средства вызывают у пациентов экстрапирамидные расстройства, включая лекарственный паркинсонизм, острые дистонические реакции, акатизию, позднюю дискинезию и позднюю дистонию. Для оценки экстрапирамидных симптомов используются хорошо известные шкалы оценок, такие, как шкала Симпсона Ангуса, шкала оценок акатизии Бернса и шкала аномальных инволюитарных движений (AIMS). Подавляющее большинство лекарственных средств, применяемых для лечения шизофрении, способны вызвать побочные экстрапирамидные эффекты, когда они используются в дозах, оказывающих благоприятное воздействие на симптомы заболевания. Тяжесть побочных явлений и/или отсутствие положительного эффекта у значительного числа пациентов часто приводит к неудовлетворительным результатам лечения или к прекращению лечения.
Многие лекарственные препараты обладают седативным действием, а также могут оказывать нежелательное воздействие на эффективные симптомы заболевания, вызывая депрессию. В некоторых случаях длительное применение лекарственного препарата приводит к необратимым состояниям, таким, как поздняя дискенизия и поздняя дистония, упоминаемые выше.
Один из таких препаратов является широко используемое антипсихотическое средство галоперидол, которое, как уже сообщалось, очень часто вызывает экстрапирамидные симптомы и может также вызвать позднюю дискинезию. Позднее было заявлено о том, что один препарат из широкой группы трициклических антипсихотических средств, а именно клозапин, не вызывает экстрапирамидных эффектов. Однако было установлено, что у некоторых пациентов это соединение вызывает агранулоцитоз, т.е. состояние, которое приводит к снижению уровня лейкоцитов в крови, что может быть опасным для жизни, а поэтому введение указанного препарата может проводиться лишь под очень строгим наблюдением и контролем со стороны медицинского персонала.
Еще одна группа антипсихотических соединений описана в патенте Великобритании 1533235. Этими соединениями являются тиенобенздиазапины. Одно из соединений этой группы, а именно флумезапин (7-фтор-2-метил-10-(4-метил-1-пиперазинил)-4Р-тиен/2,3-b//1,5/-бенздиазепин), было разработано до стадии клинического применения для лечения пациентов, страдающих шизофренией. Лечению флузапином было подвергнуто всего 17 пациентов, а затем, после консультации с Управлением по контролю за качеством пищевых продуктов и медикаментов США, это лечение было прекращено из-за неприемлемо высокого уровня ферментов, индуцируемых у пациентов во время такого лечения. Анализы крови, взятой у этих пациентов, показали чрезмерно высокие уровни фермента креатинфосфокиназы (СЕК) и ферментов печени: глутамат-оксалацетат-трансаминазы сыворотки крови (SGOT) и глутамат-пируват-трансаминазы сыворотки крови (SGPT), что свидетельствовало о возможной токсичности. По всей способности вызвать повышение уровней ферментов печени в крови флумезапин аналогичен хлоропромазину, антипсихотическому средству, которое уже давно используется на практике, но безопасность которого вызывают сомнения.
Краткое описание изобретения
Способ настоящего изобретения предусматривает введение пациенту, страдающему шизофренией или шизофрениформными расстройствами или восприимчивому к указанным заболеваниям, эффективного количества соединения формулы I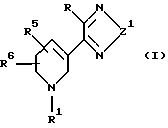
где Z1 представляет собой кислород или серу;
R представляет собой водород, галоген, аминогруппу, -NHCO-R2, С3-7 - циклоалкил, С4-10-(циклоалкилалкин);
Z2 - С3-7-циклоалкил, необязательно замещенный С1-6-алкилом;
Z2 - С4-10-(циклоалкилалкил);
Z2 - С4-10-(циклоалкенилалкил);
Z2 - С4-10-(метиленциклоалкилалкил); -NH-R2, -NR3R3, -NH-OR2;
фенил; фенокси; бензоил; бензилоксикарбонил; тетрагидронафтил; инденил; Х; R2; -Z2R2; -SOR2; -SO2R2; -Z2-R2-Z3-R3; -Z2R2-R3-Z3-R3-Z4-R4;
-Z2R2-CO-R3; -Z2R2-CO2-R3; -Z2R2-O2C-R3; -Z2R2-CONH-R3; Z2R2-NHCOR3; -Z2R2-X; -Z2R2-Z3-X; где Z2, Z3 и Z4 независимо представляют собой кислород или серу, а R2, R3 и R4 независимо представляют собой прямой или разветвленный С1-15-алкил, прямой или разветвленный С2-15-алкенил, прямой или разветвленный С2-15-алкинил, каждый из которых необязательно замещен галогеном (галогенами), -ОН, -СN, -CF3, -SH-, -COOH, -NH-R2, -NR2R3, C1-6 алкилэфирной группой, одним или двумя фенилом, фенокси, бензонилом или бензилоксикарбонилом, где каждая ароматическая группа необязательно замещена одним или двумя галогенами, -СN, C1-4-алкилом или С1-4-алкокси; а Х представляет собой 5- или 6-членную гетероциклическую группу, содержащую от 1 до 4 атомов N, О или S, либо их комбинацию; причем указанная гетероциклическая группа является необязательно замещенной у атома (атомов) углерода или азота прямым или разветвленным С1-6-алкилом, фенилом, бензилом или пиридином; либо в указанной гетероциклической группе, где атом углерода вместе с атомом кислорода образует карбонильную группу; либо указанная гетероциклическая группа является необязательно конденсированной с фенильной группой; и
R5 и R6 могут присутствовать в любом положении, включая точку присоединения тиадиозола или оксадиозолового кольца, и независимо представляют собой водород, прямой или разветвленный С1-5-алкил, прямой или разветвленный С2-5-алкенил, прямой или разветвленный С2-5-алкинил; прямую или разветвленную С1-10-алкоксигруппу; прямой или разветвленный С1-5-алкил, замещенный -ОН; -ОН; галоген; -NH2; или карбоксигруппу;
R1 представляет собой водород, прямой или разветвленный С1-5-алкил, прямой или разветвленный С2-5-алкенил, или прямой или разветвленный С2-5-алкинил; или его фармацевтически приемлемые соли.
Используемый в настоящем описании термин "пациент" относится к любому млекопитающему, которое может быть подвергнуто успешному лечению от острых полиморфных психических расстройств с симптомами шизофрении. Этот термин, в частности, относится к человеку, но не ограничивается лишь человеком.
Тиазилазоловые и оксадиазоловые соединения, используемые в способе настоящего изобретения, были раскрыты и заявлены в патентах США 5041455 и 5043345, в заявке на Европейский патент 384288, РСТ/DK 91/00234 и РСТ/DK 91/00235. Известно, что тиадиазоловые и оксадиазоловые производные могут быть использованы в качестве холинергических мускариновых средств для лечения пресенильной и сенильной декеменции. Эти соединения могут быть, очевидно, использованы для лечения болезни Альцгеймера, глаукомы и болей. В других работах было высказано предположение, что тиадиазоловые соединения могут быть использованы для лечения заболеваний, клинические проявления которых обусловлены холинергической недостаточностью (заявка на Европейский патент 307142). такими заболеваниями являются хорея Гентингтона, поздняя дискенизия, гиперкинезия, мании и синдром Туретта.
Кроме того, тиазоловые и оксадиазоловые производные, используемые в способе настоящего изобретения, обнаруживают значительную активность в моделированном анализе на условно-рефлекторное избегание. Моделированный анализ на условно-рефлекторное избегание является одним из известных способов оценки эффективности соединений для лечения шизофрении или шизофрениформных расстройств.
Острые полиморфные психические расстройства с симптомами шизофрении (шизофрениформные расстройства), очевидно, связаны с избытком допамина. Поэтому авторы настоящей заявки были особенно удивлены, обнаружив, что тиалиазоловые и оксадмазоловые соединения, используемые в данном методе, имеют низкую аффинность связывания с допаминовыми рецепторами. Еще ни одно соединение, селективное в отношении мускариновых рецепторов, не было признано клиницистами или регулятивными органами как подходящее средство для лечения шизофрении. таким образом, способ настоящего изобретения является многообещающим и неожиданным открытием, которое позволит проводить успешное лечение шизофрении и шизофрениформных расстройств.
Способ настоящего изобретения предусматривает использование раскрытых тиадиазоловых и оксадиазоловых соединений для лечения шизофрении и острых полиформных психических состояний с симптомами шизофрении. Активность этих соединений была проиллюстрирована на моделях с использованием хорошо известной техники. Например, соединения оценивали с использованием модели условно-рефлекторного избегания, т.е. стандартного поведенческого теста, способного прогнозировать антипсихотическую активность соединения. Davidson, A.B. and Veidley E. Differential Effects of Neuroleptic and other Paychotrople Agents on Acquisition of Avoidance in Rata, 18 Life Sct, 1279-1284 (1976). Кроме того, было обнаружено, что соединения, используемые в этом методе, имеют подходящий профиль активности в in vitro-анализах на связывание, проводимых для измерения степени связывания с нейтральными рецепторами.
В анализе на связывание с 3Н-оксотреморином-М эти соединения имели уровни IС50, составляющие менеt чем 1 мкм, что свидетельствует о том, что эти соединения обладают сродством к мускариновым рецепторам.
Этот профиль активности в in vitro-анализах на связывающие с рецептором так же, как и наблюдения в поведенческих тестах, указывают на то, что данные соединения являются эффективными для лечения психотических состояний, но при этом менее вероятно, что они будут вызывать побочные экстрапирамидные эффекты.
Поведение условно-рефлекторного избегания у крыс.
Одним из основных фармакологических свойств современных антипсихотических средств, используемых для лечения животных, является их способность блокировать реакцию условно-рефлекторного избегания (Cook & Davidson, 1978; Davidson & Veidley, 1976).
Активность и способность этих соединений влиять на условно-рефлекторное избегание в указанном тесте в высокой степени кореллируют с их эффективностью и действенностью в качестве антипсихотических средств (Creese и др., 1976).
В этом тесте на условно-рефректорное избегание животные при действии на них условного раздражителя усваивают соответствующую поведенческую реакцию, чтобы избежать воздействия слабого электрического тока. Термин "реакция избегания" означает ответную реакцию во время действия условного раздражителя, а термин "реакция избавления" означает ответную реакцию во время действия электрического тока; при этом реакция отсутствует в том случае, когда животное не в состоянии реагировать ни в ответ на действие условного раздражителя, ни в ответ на действие электрического тока, что указывает на двигательную недостаточность животного. В 99 случаях из ста, животные быстро обучаются указанным поведенческим реакциям. Антипсихотические средства способствуют снижению процента реакции избегания, не оказывая при этом влияния на способность животного к ответной реакции, поскольку животные остаются способными к реакции избавления. Процент отсутствия реакции является мерой двигательной недостаточности.
Методика.
От крыс, находящихся в экспериментальной камере, необходимо добиться, чтобы они нажимали рычаг для избежания или избавления от действия электрического тока, подаваемого в лапу животного. Каждый экспериментальный цикл состоял из 50 испытаний. Во время каждого испытания камеру освещали и подавали звуковой сигнал максимум на 10 с. Реакция животного во время звукового сигнала сразу прекращала подачу звука и освещения в камере, и испытание заканчивалось. При отсутствии реакции во время звукового сигнала на животное при продолжении звукового сигнала действовали слабым электрическим током (2,0 мА) максимум 1 с. Реакция крысы во время электрошока сразу прекращала подачу тока, звука и освещения, и испытание заканчивалось.
Для оценки эффективности лекарственного средства животным за 30 минут до начала экспериментального цикла подкожно вводили дозу этого средства, составляющую 3,0 мг/кг. Лекарственное средство считалось активным, если процент реакций избегания снижался, по крайней мере, на 50%, при условии, что отсутствие реакций не превышало 50%. После этого для активных лекарственных средств строили кривую зависимости "доза-эффект".
Список литературы.
Cook, L, and Davidson, A. B.: Behavioral pharmacology: Animal models involving averasive control of behavior. In Pсychopharmacology, A Generation of Progress, rd by M. A. Lipton, A.Dimsscio and K.Killman, p.p. 563-567, Raven Press, New York, 1978.
Davidson, A.B. and Weidley, K.: Differential affects of neuroleptic and other psychotropic agents on acoquisition of avoidanct in rats. Life Sci. I8: 1279-1234, 1976.
Creese, I. , Burt, D. R. and Shyder, S.H.: Dopamine Receptor binding predicts clinical and pharmacological properties of antischizophrenic drugs. Sciense (Wash. DC) 192: 481-483, 1976.
Аффиность соединений по отношению к мускариновым рецепторам определяли с использованием неселективного лиганда-агониста, 3Н-оксатреморина-М. Birdsdall N. J.V., Hulme E.C., & Burgen A.S.V., "The Character of Muscaeinic Receptors in in Differents Region of the Rat Brain", 207 Proc. Roy. Soc. I (London Series B, 1980).
Результаты анализа описаны ниже, в Таблице 1.
Для определения эффективности соединений по отношению к мускариновым рецепторам каждое соединение испытывали в соответствии с нижеследующей методикой.
Для каждого эксперимента на in vitro-связывание самцов крыс Sprague-Dawley (Harlan Sprague-Dawley, Indianapolis, IN) весом от около 100 до около 150 граммов умерщвляли путем обезглавливания, затем быстро удаляли головной мозг и извлекали из него кору головного мозга. Ткань коры головного мозга гомогенизировали в 10 объемах 0,32 М сахарозы и центрифугировали в течение примерно 10 минут при около 1000g. Супернатант центрифугировали примерно при 12000g в течение около 10 минут, и полученный осадок ресуспендировали в 120 мМ Трис-С1, рН 7,4. Ресуспендированный осадок снова центрифугировали в течение около 10 минут примерно при 50000g. Полученный гомогенат предварительно инкубировали в течение около 10 минут, приблизительно при 25oС, а затем снова центрифугировали примерно в течение 10 минут при около 50000g.
Осадок ресуспендировали в соотношении 1 грамм осадка на 3 мл буфера, и суспензию замораживали при около -80oС до ее использования.
Ингибирование связывания 3Н-оксотреморина-М, связывающего с мускариновыми рецепторами, определяли путем смешивания соединения данного Примера, 3Н-оксотреморина-М (около 87 Ки/мМ, New Ingland Nuclear, Boston MA) и цереброкортикальных мембран, эквивалентных примерно 10 мг сырой массы, которая представляла собой около 100 мкг кортикального мебранного белка, примерно в 1 мл полного объема 20 нМ Трис-С1-буфера (рН 7,4), содержащего 1 мм МnCl2. Вышеупомянутую смесь гомогенатов инкубировали примерно в течение 15 минут при около 25oС, после чего гомогенаты фильтровали через стекловолоконные фильтры (Whatman, GF/С) в вакууме. Затем фильтры 3 раза промывали примерно 2 миллилитрами холодного Трис-С1-буфера, и помещали в сцинтилляционные сосуды, содержащие около 10 мл сцинтилляционной жидкости (Ready Protein +, Beckman, Fullerton, CA). Радиоактивность, улавливаемую фильтрами, определяли с помощью жидкостно-сцинтилляционной спектрометрии. Неспецифическое связывание определяли с использованием 1 мкМ атропина. Концентрацию соединения, необходимую для 50%-ного ингибирования специфического связывания (IС50), определяли путем стандартизированных вычислений с помощью компьютера. Deleen, A. et al., Am.3. Physiol., 235, (1978).
В Таблице 1 представлены результаты испытаний некоторых соединений настоящего изобретения.
Соединения, используемые в этом месте, являются эффективными в широком диапазоне доз. Например, для лечения взрослого человека могут быть использованы дозы от около 0,05 мг до 100 мг, а предпочтительно от около 100 мг в день.
Наиболее предпочтительная лоза составляет от около 10 мг до около 70 мг в день. При выборе схемы лечения пациентов, страдающих психотическим заболеванием, часто бывает целесообразным начать с доз от около 30 до около 70 мг в день, а затем, после наступления стабилизации, дозу можно снизить примерно до 1-10 мг в день. Точная доза зависит от способа введения и формы лекарственного средства, от конкретного индивидуума, подвергающегося лечению, и его веса тела, а также от конкретного выбора и опыта лечащего врача или ветеринара.
Лекарственное средство может быть введено любым способом, обеспечивающим эффективную доставку активного соединения к соответствующим тканям-мишени, например пероральным способом или парентеральным способом, включая ректальное, чреcкожное, подкожное, внутривенное, внутримышечное или интраназальное введение; при этом предпочтительным является пероральный способ введения.
Типичные композиции включают в себя соединение формулы (I) или его фармацевтическую приемлемую кислую соль присоединения в сочетании с фармацевтически приемлемым носителем. Для изготовления таких композиций может быть использована стандартная техника получения фармацевтических композиций. Например, активное соединение обычно смешивают с носителем, или разбавляют носителем, или вводят в носитель, который может быть в виде ампулы, капсулы, саше, бумаги, или другого контейнера. Если носитель служит в качестве разбавителя, то он может быть твердым, полутвердым или жидким материалом, который действует как разбавитель, наполнитель или среда для активного соединения. Активное соединение может быть адсорбировано на гранулированной твердой емкости, например, в чаше. Некоторыми примерами подходящих носителей могут служить вода, солевые растворы, спирты, полиэтиленгликоли, полигидроксиэтоксилированное касторовое масло, желатин, лактоза, амилоза, стеарат магния, тальк, кремниевая кислота, моноглицериды и диглицериды жирных кислот, пентаэритритоловые сложные эфиры жирных кислот, гидроксиметилцеллюлоза и поливинилпирролидон.
Примерами подходящих солей, которые могут быть использованы в способе настоящего изобретения, являются неорганические и органические кислые соли присоединения, такие как гидрохлорид, гидробромид, сульфат, фосфат, ацетат, фумарат, малеиат, цитрат, лактат, тартрат, оксалат или аналогичные фармацевтически приемлемые соли присоединения неорганических или органических кислот. Особенно предпочтительными солями являются тартрат, оксалат и гидрохлорид.
Если необходимо, фармацевтические препараты могут быть стерилизованы и смешаны с добавками, эмульгаторами, солью для воздействия на осмотическое давление, буферами, и/или красителями и т.п., причем указанные дополнительные ингредиенты не должны вступать в нежелательные реакции с активными соединениями.
Для парентерального введения особенно подходящими являются инъецируемые растворы или суспензии, предпочтительно водные растворы с активным соединением, растворенным в полигидроксилированном касторовом масле.
Для перорального введения особенно подходящими являются таблетки, драже или капсулы, содержащие тальк и/или углеводный носитель, или связующее вещество, или т.п. Предпочтительными носителями для таблеток, драже или капсул являются лактоза, кукурузный крахмал и/или картофельный крахмал. В случае где используется подслащивающий наполнитель, препарат может быть изготовлен в виде сиропа или эликсира.
Обычно соединения распределяют по разовым лекарственным формам, каждая из которых содержит от около 1 до около 100 мг в фармацевтически приемлемом носителе.
Типичная таблетка, подходящая для использования в способе настоящего изобретения, может быть получена в соответствии со стандартной техникой изготовления таблеток и содержит, мг:
Активное соединение - 5,0
Лактоза - 67,8 (Евр. фарм).
Авицел (Avicel®) - 31,4
Амберлит (Amberlite®) - 1,0
Стеарат магния - 0,25 (Евр. фарм)
Соединения, используемые в этом способе, могут быть получены, в основном, известными химическими методами. Большинство соединений может быть получено с использованием методики, описанной в патентах США 5041455 и 5043345, в заявке на Европейский патент 384288, РСТ /DК 91/00234 и РСТ/DК 91/00235, которые вводятся в настоящее описание посредством ссылки. Возможные методы синтеза соединений, используемых в способе настоящего изобретения, иллюстрируются в нижеследующем описании.
Указанные соединения могут быть получены:
а) путем алкилирования соединения формулы II
где Z1, R, R5 и R6 имеют значения, определяемые выше, с использованием алкилаглогенида; и последующего восстановления образованного таким образом соединения с использованием ионов гидрида, в результате чего образуется соединение формулы I
где Z1, R, R1, R5 и R6 имеют значения, определяемые выше;
b) путем окисления соединения формулы III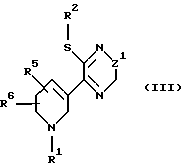
где Z1, R, R1, R2, R5 и R6 имеют значения, определяемые выше, с использованием стандартной техники, с образованием соединения формулы IV:
и последующей замены -SO2-R2 соответствующим нуклеофилом с получением соединения формулы I.
При этом следует отметить, что настоящее изобретение включает в себя все стереоизомерные формы соединений формулы I, а также их рацематы.
Получение конкретных соединений, используемых в способе настоящего изобретения, описано в нижеследующих примерах. Однако эти примеры не должны рассматриваться как некое ограничение настоящего изобретения.
Пример 1.
А. 3-(3-Хлор-1,2,5-тиадиазол-4-ил)пиридин
К раствору монохлорида серы (2,4 мл, 30 мМ) в NN- диметилформамиде (5мл) медленно добавляли альфа-аминоальфа(3-пиридил)-ацетонитрил (Archve der Pharmazie 289(4)(1956)) (1,70 г, 10 мМ). Реакционную смесь перемешивали в течение 18 часов при комнатной температуре. После добавления воды (20 мл), водную фазу экстрагировали эфиром, а эфирную фазу сливали. К водной фазе добавляли раствор 50%-ного гидроксида калия до рН 9. Затем водную фазу несколько раз экстрагировали эфиром, а эфирные фазы осушали и выпаривали. остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: смесь эилацетата/метиленхлорида 1:1)). Целевое соединение собирали. Выход: 880 мг (45%). М+: 197.
В. 3-(3-Метокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (460 мг, 20 мМ) в метаноле (10 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (750 мг, 3,8 мМ).
Полученную смесь перемешивали в течение одного часа при температуре 50oС, а затем выпаривали. Образовавшийся остаток растворяли в воде и экстрагировали метиленхлоридом. Объединенные органические фазы осушали и выпаривали, в результате чего получали целевое соединение, которое кристаллизовали из петролейного эфира.
Выход: 630 мг (86%).
С. 3-(3-Метокси-1,2,5-тиадиазол-4-ил)-1-метил-пиридиния иодид
Смесь, состоящую из метилиодида (0,37 мл, 6 мМ) и 3-(3-метокси-1,2,5-тиадиазол-4-ил)пиридина (500 мг, 2,5 мМ) в ацетоне (10 мл), перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 1,0 г (100%).
D. 1,2,5,6-Тетрагидро-3-(3-метокси-1,2,5-тиадиазол-4-ил)-1-метилпиридина оксалат
К раствору 3-(3-метокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодида (1,0 г, 3 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (460 мг, 12 мМ) и эту реакционную смесь перемешивали в течение одного часа при комнатной температуре. после выпаривания остаток растворяли в воде, а затем экстрагировали метиленхлоридом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол(4:1)). Целевое соединение кристаллизовали из ацетона в виде оксалатной соли. Выход: 390 мг (т. пл. 150 oС; М+:211; Соединение 1).
Пример 2.
А. 3-(3-Этокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (440 мг, 17 мМ) в этаноле (10 мл) добавляли 3-(3-метокси-1,2,5-тиадиазол-4-ил)пиридин (540 мг, 3,3 мМ). Полученную смесь перемешивали в течение 10 часов при температуре 40oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали метиленхлоридом. Объединенные органические фазы осушали и выпаривали, в результате чего получали 520 мг (76%) целевого соединения.
В. 3-(3-Этокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,3 мл, 5 мМ) и 3-(3-этокси-1,2,5-тиадиазол-4-ил)пиридин (520 мг, 2,5 мМ) в ацетоне (10 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,72 г (83%).
С. 3-(3-Этокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-этокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,72 г, 2 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (300 мг, 8 мМ) и реакционную смесь перемешивали при комнатной температуре в течение одного часа. После выпаривания остаток растворяли в воде и экстрагировали метиленхлоридом. Осушенные органические фазы выпаривали, а образовавшийся остаток очищали с помощью колоночной хролматографии на двуокиси кремния (элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты, а затем перекристаллизовывали из метанола с выходом 190 мг (температура плавления: 137oС, М+: 225; Соединение 2).
Пример 3.
А. 3-(3-Пропокси -1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (440 мг, 17 мМ) в 1 - пропаноле (10 мл) добавляли 3-(3-хлор-1,2,5-тиадиазол-4-ил)пиридин (650 мг, 3,3 мМ). Полученную смесь перемешивали в течение 2 часов при температуре 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали метиленхлоридом. Объединенные органические фазы осушали и выпаривали, в результате чего получали 700 мг (96%) целевого соединения.
В. 3-(3-Пропокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид.
Смесь, содержащую метилиодид (0,37 мл, 6 мМ) и 3-(3-пропокси-1,2,5-тиадиазол-4-ил)пиридин (700 мг, 3,1 мМ) в ацетоне (10 мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,98 г (88%).
С. 1,2,5,6-Тетрагидро-1-метил-3-(пропокси-1,2,5-тиадиазол-4-ил)пиридина оксалат.
К раствору иодида 3-(3-пропокси-1,2,5-тиадиазол-4-)-1- метилпиридиния (980 мг, 2,7 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (380 мг, 10 мл), и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а образовавшийся остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 440 мг (Т.пл.: 143oС; М+: 239. Соединение 3).
Пример 4.
А. 3-(3-Бутокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (290 мг, 12,5 мМ) в н-бутаноле (10 мл) добавляли 3-(3-хлоро -1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали в течение 18 часов при температуре 25oС а затем выпаривали. Остаток растворяли в воде и экстрагировали метиленхлоридом. Объединенные органические фазы осушали и выпаривали, в результате чего получали 590 мг (100%) целевого соединения.
В. 3-(3-Бутокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, состоящую их метилиодида (0,3 мл, 5 мМ) и 3-(3-бутокси -1,2,5-тиадиазол-4-ил)пиридина (580 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 0,60 г (64%).
С. 3-(3-Бутокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
К раствору иодида 3-(3-бутокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,60 г, 1,6 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (240 мг, 6,4 мМ), и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 280 мг (Т. пл. 158oС; М+: 253; Соединение 4).
Пример 5
А. 3-(3-Изопропокси -1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (290 мг, 12,5 мМ) в изопропаноле (10 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали в течение 18 часов при температуре 25oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали этилацетатом. Объединенные органические фазы осушали и выпаривали, в результате чего получали 540 мг (98%) целевого соединения.
В. 3-(3-Изопропокси -1,2,5-тиадиазол-4-ил) -1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,3 мл, 5 мМ) и 3-(3-изопропокси-1,2,5-тиадиазол-4-ил) пиридин (540 мг, 2,4 мМ) в ацетоне (5 мл), перемешивали в течение 18 часов при комнатной температуре. целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 0,68 г (77%).
С. 1,2,5,6-Тетрагидро-3-(3-изопропокси-1,2,5-тиадиазол-4-ил)-1-метилпиридина оксалат
К раствору иодида 3-(3-изопропокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (650 мг, 1,8 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (280 мг, 7,2 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток с помощью колоночной хроматографии очищали (SiO2; элюент: этилацетат/метанол; (4: 1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 280 мг (Т. пл. 164oС; М+: 239; Соединение 5).
Пример 6.
А. 3-(3-Пентилокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (230 мг, 10 мМ) в 1-пентаноле (20 мл) добавили 3-(3-хлоро-1,2,5-тиадиазол-4-ил) пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали в течение 3 часов при температуре 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали метиленхлоридом. Объединение органические фазы осушали и выпаривали, в результате чего получали нужное соединение.
В. 3-(3-Пентилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодин
Смесь, состоящую из метилиодида (0,3 мл, 5 мМ) и 3-(3-пентилокси-1,2,5-тиадиазол-4-ил)пиридина (620 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 0,81 г (84%).
С. 1,2,5,6-Тетрагидро-1-метил-3-(3-пентилокси-1,2,5-тиадиазол-4-ил)пиридина оксалат
К раствору иодида 3-3(пентилокси-3,2,5-тиадиазол-4-ил)-1-метипиридиния (0,81 г, 2 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (300 мг, 8 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали эфиром. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2); элюэент: этилацетат/метанол(4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты, затем перекристаллизовывали из метанола с выходом 220 мг (Т.пл.150oС; М+:267; Соединение 6).
Пример 7.
А. 3-(3-Изобутокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (230 мг, 10 мМ) в изобутаноле (10 мл) добавляли 3-3(хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали в течение трех часов при температуре 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали метиленхлоридом. Объединенные органические фазы осушали и выпаривали, в результате чего получали нужное соединение.
В. 3-(3-Изобутокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, состоящую из метилиодида (0,6 мл, 10 мМ) и 3-(3-изобутокси-1,2,5-тиадиазол-4-)пиридина (588 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,88 г (84%).
С. 1,2,5,6-Тетрагидро-3-(3-изобутокси-1,2,5-тиадиазол-4 ил)-1-метилпиридиния оксалат
К раствору иодида 3-(3-изобутокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,82 г, мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (160 мг, 4,3 мМ) и эту реакционную смесь перемешивали в течение 1 часа при температуре 0oС. После выпаривали остаток растворяли в воде, а затем экстрагировали этилацетатом. осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетана в виде соли щавелевой кислоты. Выход: 400 мг (Т. пл. 135oС; М+: 253; Соединение 7).
Пример 8
А. 3-(3-Изопентилокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (230 мг, 10 мМ) в изопентаноле (20 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали в течение 2 часов при температуре 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали эфиром. Объединенные органические фазы осушали и выпаривали, в результате чего получали нужное соединение.
В. 3-(3-Изопентилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,5 мл, 10 мМ) и 3-(3-изопентилокси-1,2,5-тиадиазол-4-ил)пиридин (622 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,78 г (81%).
С. 1,2,5,6-Тетрагидро-3-(3-изопентилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридина оксалат
К раствору иодида 3-(3-изопентилокси-1,25-тиадиазол-4-ил)-1-метилпиридиния (780 мг, 2 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (150 мг, 4 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент:этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 350 мг (Т.пл. 152oС; М+: 267; Соединение 8).
Пример 9.
А. 3-(3-Гексилокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (230 мг, 10 мМ) в 1-гексаноле (15 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали при температуре 50oС в течение двух часов, а затем выпаривали. Остаток растворяли в воде и экстрагировали эфиром. Объединенные органические фазы осушали и выпаривали, в результате чего получали нужное соединение.
В. 3-(3-Гексилокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,5 мл, 7,5 мМ) и 3-(3-гексилокси -1,2,5-тиадиазол-4-ил)пиридин (658 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,81 г (80%).
С. 3-(3-Гексилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
К раствору иодида 3-(3-гексилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (810 мг, 2 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (230 мг, 6 мМ) и эту реакционную смесь перемешивали при комнатной температуре в течение одного часа. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали и образовавшийся остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 350 мг (Т.пл. 148oС; М+: 281; Соединение 9).
Пример 10.
А. 3-(3-Бензилокси-1,2,5-тиадиазол-4-ил)пиридин.
К раствору натрия (490 мг, 2,5 мМ) в бензиловом спирте (15 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ). Полученную смесь перемешивали в течение 2 часов при температуре 50oС, после чего выпаривали. Остаток растворяли в воде и экстрагировали эфиром. Объединенные органические фазы осушали и выпаривали, в результате чего получали нужное соединение.
В. 3-(3-Бензилокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,5 мл, 7,5 мМ) и 3-(3-бензилокси -1,2,5-тиадиазол-4-ил)пиридин (673 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,75 г (73%).
С. 3-(3-Бензилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
К раствору, содержащему 3-(3-бензилокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния (750 мг, 1,8 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (230 мг, 6 мМ), и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты, с выходом 340 мг (Т.пл. 149oС; М+: 287; Соединение 9).
Пример 11.
А. 3-(3-Бутенилокси)-1,2,5,-тиадиазол-4-ил)пиридин.
К раствору 3-бутен-1-ол'а (540 мг, 7,5 мМ) и гидрида натрия (180 мг, 7,5 мМ) в безводном тетрагидрофуране добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение одного часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали 650 мг целевого соединения.
В.3-(3-Бутенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,5 мл, 7,5 мМ) и 3-(3-(3-бутенилокси)-1,2,5-тиадиазол-4-ил)пиридин (583 мг, 2,5 мМ) в ацетоне (5мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 890 мг (96%).
С. 3-(3-(3-Бутенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(3-бутенилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (1,03 г, 2,8 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрат натрия (210 мг, 5,5 мМ) и эту реакционную смесь перемешивали в течение 1 часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а образовавшийся остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол (4:1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 380 мг (Т.пл. 141oС; М+: 251; Соединение 11).
Пример 12.
А. 3-(3-(2-Бутинилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 2-бутин-1-ол'а (530 мг, 7,5 мМ) и гидрида натрия (180 мг, 7,5 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ) в безводном тетрагидрофуране. Реакционную смесь перемешивали в течение одного 2 часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-Бутинилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,5 мл, 7,5 мМ) и 3-(3-(2-бутинилокси)-1,2,5-тиадиазол-4-ил)пиридин (578 мг, 2,5 мМ) в ацетоне (5 мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,88 г (95%).
С. 3-(3-(2-Бутинилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-бутинилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,88 г, 2,35 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрат натрия (180 мг, 4,7 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии на двуокиси кремния. Элюент: этилацетат/метанол (4: 1). Целевое соединение кристаллизовывали из ацетона в виде соли щавелевой кислоты, а затем перекристаллизовывали из метанола. Выход: 140 мг (Т.пл.158oС; М+: 249; Соединение 12).
Пример 13.
А. 3-(3-Пропаргилокси-1,2,5-тиадиазол-4-ил)пиридин.
К раствору пропаргилового спирта (420 мг, 7,5 мМ) и гидрида натрия (180 мг, 7,5 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение 2 часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали 530 мг (98%) целевого соединения.
В. 3-(3-Пропаргилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,45 мл, 7,2 мМ) и 3-(3-пропаргилокси)-1,2,5-тиадиазол-4-ил)пиридин (430 мг, 2,4 мМ) в ацетоне (5мл), перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,58 мг (67%).
С. 1,2,3,5,6-Тетрагидро-1-метил-3-(3-пропаргилокси-1,2,5,-тиадиа-зол-4-ил)пиридина оксалат
К раствору иодида 3-(3-пропаргилокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,68 г, 1,9 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрит натрия (230 мг, 6 мМ), Реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 200 мг (Т.пл. 155oС; М+: 235; Соединение 13).
Пример 14
А. 3-(3-Циклопропилметокси -1,2,5-тиадиазол-4-ил)пиридин.
К раствору циклопропилметокси (360 мг, 5 мМ) и гидрида натрия (110 мг, 5 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридин (490 мг, 2,5 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение 3 часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали с получением 400 мг (69%) целевого соединения.
В. 3-(3-Циклопропилметокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь, содержащую метилиодид (0,25 мл, 4 мМ) и 3-(3-циклопропилметокси-1,2,5-тиадиазол-4-ил)пиридин (400 мг, 1,7 мМ) в ацетоне (5 мл), перемешивали при комнатной температуре в течение 36 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,41 мг (65%).
С. 3-(3-Циклопропилметокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
К раствору иодида 3-(3-циклопропилметокси -1,2,5-тиадиазол-4-ил)-1-метилпиридиния (410 мг, 1,1 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрит натрия (170 мг, 4,4 мМ), и реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент:этилацетат/метанол (4:1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 130 мг (Т.пл. 153oС; М+: 251; Соединение 14).
Пример 15
А. 3-(3-хлоро -1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (1,98 г, 10 мМ) и метилиодида (4,25 г, 30 мМ) в ацетоне (10 мл) перемешивали в течение 16 часов при комнатной температуре. Осадок собирали путем фильтрации и получали 3,40 г (100%) целевого соединения.
В. 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К суспензии, состоящей из борогидрида натрия (330 мл, 8,6 мМ) и этанола (20 мл), добавляли 3-(3-хлоро-1,2,5,-тиадиазол-4-ил)-1-метилпиридиния иодид (1,46 г, 4,3 мМ) при температуре 0oС. Полученную реакционную смесь перемешивали в течение одного часа при температуре 0oС. После добавления воды смесь экстрагировали этилацетатом. После осушки этилацетатную фазу выпаривали, а остаток очищали с помощью колоночной хроматографии (элюент: этилацетат/метанол (4:1). Выход: 880 мг (95%). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты (Т.пл. 124oС; М+: 215 и 217; Соединение 16).
С. 1,2,3,5,6-Тетрагидро-3-(3-метоксиэтокси-1,2,5-тиадиазол-4-ил)метилпиридина оксалат
К раствору натрия (120 мг, 5 мМ) в 2-метоксиэтаноле (10 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (310 мг, 1 мМ). Полученную смесь перемешивали в течение 18 часов при температуре 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали этилацетатом. Объединенные органические фазы осушали и выпаривали. Целевое соединение
кристаллизовывали из ацетона в виде соли щавелевой кислоты. Выход: 270 мг (Т.пл.152oС; М+: 253; Соединение 15).
D. 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина гидрохлорид.
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (670 мг, 3,1 мМ) в 1,2-дихлорэтана (20 мл) добавляли раствор 1-хлороэтил-хлороформата (440 мг, 3,1 мМ) в 1,2-дихлорэтане при температуре 0oС. Реакционную смесь перемешивали в течение одного часа при температуре 50oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Этилацетатную фазу осушали и выпаривали, в результате чего получали маслообразное вещество (200 мг). Целевое соединение кристаллизовали в виде соли щавелевой кислоты из ацетона. Выход: 170 мл (52%). (Т. пл. 173-174oС; М+: 239; Соединение 18).
Пример 16.
А. 3-(3-Хлор-1,2,5-тиадиазол-4-ил)-1-этилпиридиния иодид
Раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (1,13 г, 5,7 мМ) и этилиодида (22,65 г, 17 мМ) в ацетоне (15 мл) перемешивали в течение 16 часов при температуре 40oС. Осадок собирали путем фильтрации и получали целевое соединение. Выход: 510 мг (26%).
В. 3-(3-Хлор-1,2,5-тиадиазол-4-ил)-1-этил-1,2,5,6-тетрагидропиридина оксалат.
К суспензии, состоящей из борогидрида натрия (170 мг, 4,5 мМ) и этанола (10 мл), добавляли 3-(3-Хлор-1,2,5-тиадиазол-4-ил)-1-этилпиридиния иодид (510 мг, 1,5 мМ) при температуре 0oС. Полученную смесь перемешивали в течение одного часа при температуре 0oС. После добавления воды эту смесь экстрагировали этилацетатом. После осушали этилацетатную фазу выпаривали, а остаток очищали с помощью колоночной хроматографии (элюент: этилацетат/метанол (4:1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 70 мг (Т. пл. 143oС; М+: 229 и 231; Соединение 19).
Пример 17.
А. 3-(3-Этокси -1,2,5-тиадиазол-4-ил)-1-этилпиридиния иодид
Раствор 3-(3-этокси -1,2,5-тиадиазол-4-ил)пиридина (0,90 г, 4,3 мМ) и этилиодида (2,03 г, 13 мМ) в ацетоне (4 мл) перемешивали в течение 16 часов при температуре 40oС. Осадок собирали путем фильтрации и получали 1,34 г (86%) целевого соединения
В. 3-(3-Этокси-1,2,5-тиадиазол-4-ил)-1-этил-1,2,5,6-тетрагидропиридина оксалат.
К суспензии, состоящей из борогидрида натрия (410 мг, 10,8 мМ) и этанола (10 мл), добавляли 3-(3-этокси-1,2,5-тиадиазол-4-ил)-1-этилпиридиния иодид (1,32 г, 3,6 мМ) при 0oС. Полученную смесь перемешивали при температуре 0oС в течение одного часа. Затем добавляли воду и смесь экстрагировали этилацетатом. После осушки этилацетатную фазу выпаривали, а остаток очищали с помощью колоночной хроматографии (элюент: этилацетат/метанол (4:1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 0,49 г. (Т. пл. 120-122oС; М+: 239; Соединение 20).
Точно таким же способом были получены следующие соединения:
3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-этилпиридина оксалат из 3-(3-гексилтио-1,2,5-тиадиазол-4-ил)пиридина, т. пл. 134-135oС. Соединение 209).
3-(3-Этилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-этилпиридина оксалат из 3-(3-этилтио-1,2,5-тиадиазол-4-ил)пиридина, т. пл. 151-152oС. Соединение 210).
3-(3-Гексилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-этилпиридина оксалат из 3-(3-гексилокси -1,2,5-тиадиазол-4-ил)пиридина, т. пл. 138-139oС. Соединение 211).
Пример 18.
3-(3-Гептилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
К раствору натрия (120 мг, 5 мМ) в 1-гептаноле (10 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (310 мг, 1 мМ). Реакционную смесь перемешивали в течение 18 часов при температуре 50oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Этилацетатную фазу осушали и выпаривали, в результате чего получали маслообразное вещество. Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 270 мг (70%). (Т. пл. 152oС; М+: 295; Соединение 21).
Пример 19.
А. 3-(3-(3-Пентинилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-пентин-1-ол'а (750 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Затем реакционную смесь перемешивали при комнатной температуре в течение 1 часа. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(3-Пентинилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,6 мл, 9 мМ) и 3-(3-(3-пентинилокси)-1,2,5-тиадиазол-4-ил) пиридина (3 мМ) в ацетоне (10 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,68 г (59%).
С. 3-(3-(3-Пентинилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(3-пентинилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,68 г, 1,7 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (150 мг, 4 мМ), и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривали остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 240 мг (Т.пл. 166-167oС; М+: 263; Соединение 22).
Пример 20.
А. 3-(3-(4-Пентенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 4-пентен-1-ол'а (640 мг, 7,5 мМ) и гидрида натрия (260 мг, 7,5 мМ) в безводном тетрагидрофурана добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (490 мг, 2,5 мМ) в безводном тетрагидрофуране. Затем реакционную смесь перемешивали при комнатной температуре в течение одного часа. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(4-Пентенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид.
Смесь метилиодида (0,5 мл, 7,5 мМ) и 3-(3-(4-пентинилокси)-1,2,5-тиадиазол-4-ил)пиридина (2,5 мМ) в ацетоне (10 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,67 г (69%).
С. 3-(3-(4-Пентенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(4-пентенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,67% г, 1,7 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (150 мг, 4 мМ), и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривали остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии (SiO2; элюент:этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 150 мг (т.пл. 141-142oС; М+: 265; Соединение 23).
Пример 21.
А. 3-(3-(2-Пропенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору аллилового спирта (650 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение одного часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-Пропенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (046 мл, 6 мМ) и 3-(3-(2-пропенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,96 г (88%).
С. 3-(3-(2-Пропенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-пропенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,96 г, 2,6 мМ) в этаноле (99,9%, 25 мл) добавляли борогидрид натрия (210 мг, 5,5 мМ), и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривали остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 270 мг (температура плавления 136-137oС; М+: 237; Соединение 24).
Пример 22.
А. 3-(3-октилокси 1,2,5-тиадиазол-4-ил)пиридин
К раствору натрия (350 мг, 15 мМ) в 1 - октаноле (10 мл) добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ). Полученную смесь перемешивали в течение одного часа при температуре 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали метиленхлоридом. Объединенные органические фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-Октилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(2-октилокси-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,81 г (62%).
С. 3-(3-Октилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-октилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,81 г, 1,87 мМ) в этаноле (99,9%, 10 мл) добавляли борогидрид натрия (210 мг, 5,6 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривали остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол (4: 1)). В результате кристаллизации из ацетона получали 330 мг целевого соединения в виде соли щавелевой кислоты. (т. пл. 144-145oС; М+: 309; Соединение 25).
Пример 23.
А. 3-(3-(3-Гексинилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-гексин-1-ол'а (880 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение одного часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали с получением целевого соединения.
В. 3-(3-(3-Гексинилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(3-гексинилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,85 г (71%).
С. 3-(3-(3-Гексинилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(3-гексинилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,85 г, 2,1 мМ) в этаноле (99,9%, 10 мл) добавляли борогидрид натрия (190 мг, 5 мМ), и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метанол (4:1)). В результате кристаллизовали из ацетона целевое соединение в виде соли щавелевой кислоты: 350 мг (т. пл. 174-175oС; М+: 277; Соединение 26).
Пример 24.
А. 3-(3-(3-Метил-2-бутенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-метил-2-бутен-1-ол'а (780 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Затем реакционную смесь перемешивали при комнатной температуре в течение 0,3 часа. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(3-Метил-2-бутенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(3-метил-2-бутенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (3 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,92 г (79%).
С. 3-(3-(3-Метил-2-бутенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(3-метил-2-бутенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,92 г, 2,3 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (220 мг, 6 мМ) и реакционную смесь перемешивали при температуре -10oС в течение получаса. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии (SiO2); (элюент: этилацетат/метанол (4:1)). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 380 мг (т. пл. 150-151oС; М+: 265; Соединение 27).
Пример 25
А. 3-(3-(3-Бутенил-2-окси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-бутен-2-ол'а (650 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение 18 часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали, а затем выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(3-Бутенил-2-окси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(3-бутенил-2-окси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (3 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,73 г (65%).
С. 3-(3-(3-Бутенил-2-окси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(3-бутенил-2-окси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,73 г, 1,9 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (190 мг, 5 мМ) и эту реакционную смесь перемешивали в получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали а затем остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4:1)). F В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 270 мг (т. пл. 136-137oС; М+: 134-135o; М+: 251; Соединение 28).
Пример 26.
А. 3-(3-(4-Гексенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 4-гексен-1-ол'а (900 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь в течение 1 часа перемешивали при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали с получением целевого соединения.
В. 3-(3-(4-Гексенилокси)-2-окси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(4-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,54 г (45%).
С. 3-(3-(4-Гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(4-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,54 г, 1,3 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (150 мг, 4 мМ) и полученную реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали и остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4: 1)). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 190 мг (т. пл. 151-152oС; М+: 279; Соединение 29).
Пример 27
А. 3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору транс-3-гексен-1-ол'а (900 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Реакционную смесь перемешивали в течение одного часа при комнатной температуре. Затем добавления воду и смесь экстрагировали эфиром. После осушки и выпаривания эфирной фазы получали целевое соединение.
В. 3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,90 г (75%).
С. Транс-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида транс-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,90 г, 2,2 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (190 мг, 5 мМ) и эту реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Затем осушенные органические фазы выпаривали и остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4:1)). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 420 мг (т. пл. 163-164oС; М+: 279; Соединение 30).
Пример 28.
А. 3-(3-(2-пентенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору цис-2-центен-1-ол'а (780 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение одного часа при комнатной температуре. Затем добавления воду и смесь экстрагировали эфиром. После осушки и выпаривания эфирной фазы получали целевое соединение.
В. Цис-3-(3-(2-пентенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и цис-3-(3-(2-пентенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,53 г (46%).
С. Цис-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида цис-3-(3-(2-пентенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,53 г, 1,3 мМ) в этаноле (99,9%, 15 мл) добавляли борогидрид натрия (150 мг, 4 мМ) и эту реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Затем осушенные органические фазы выпаривали и остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 210 мг (т. пл. 143-144oС; М+: 265; Соединение 31).
Пример 29
А. Цис-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору цис-2-гексен-1-ол'а (900 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Реакционную смесь перемешивали в течение 1 часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Затем эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. Цис-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 7,5 мМ) и цис-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (4 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали.
С. Цис-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
Борогидрид натрия (150 г, 4 мМ) добавляли к раствору, содержащему цис-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид (0,6 г, 1 мМ) и этанол (99,9%, 20 мл), после чего реакционную смесь перемешивали в течение получаса при температуре -10oС. В результате выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Затем осушенные органические фазы выпаривали и остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4:1). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 150 мг (т. пл. 122-123oС; М+: 279; Соединение 32).
Пример 30
А. 3-(3-(5-Гексенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 5-гексен-1-ол'а (900 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Реакционную смесь перемешивали в течение одного часа при комнатной температуре. Затем добавляли воду и эту смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате получали целевое соединение.
В. 3-(3-(5-Гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 7,5 мМ) и 3-(3-(5-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,75 г (62%).
С. 3-(3-(5-гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида транс-3-(3-(5-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,75 г, 1,8 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (150 мг, 4 мМ) и эту реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Затем осушенные органические фазы выпаривали, а остаток очищали посредством колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 250 мг (т. пл. 137-138oС; М+: 279; Соединение 33).
Пример 31.
А. Цис-3-(3-(3-Гексенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору цис-3-гексен-1-ол'а (900 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Полученную реакционную смесь перемешивали в течение одного часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали, выпаривали и получали целевое соединение.
В. Цис-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 7,5 мМ) и цис- 3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,9 г (46%).
С. Цис-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору, содержащему цис-3-(3-(3-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,90 г. 2,2 мМ) в этаноле (99,9%, 15 мл), добавляли борогидрид натрия (230 мг, 6 мМ), и эту реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали посредством колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4: 1)). В результате кристаллизации из ацетона получали 300 мг целевого соединения в виде соли щавелевой кислоты (т. пл. 149-150oС; М+: 279; Соединение 34).
Пример 32
А. Транс-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору транс-2-гексен-1-ол'а (900 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Реакционную смесь перемешивали в течение 1 часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. Транс-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 7,5 мМ) и транс-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) оставляли при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом 0,09 г (90%).
С. Транс-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору, содержащему транс-3-(3-(2-гексенилокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид (1,09 г, 2,7 мМ) и этанол (99,9%, 20 мл), добавляли борогидрид натрия (270 мг, 4 мМ) и эту реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 400 мг (т. пл. 130-131oС; М+: 279; Соединение 35).
Пример 33
А. 3-(1,2,5-Тиадиазол-3-ил)пиридин
К раствору 1-бутантиола (2,7 г, 30 мМ) и гидрида натрия (1,2 г, 30 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (1,2 г, 6 мМ) в безводном тетрагидрофуране. Эту реакционную смесь перемешивали в течение получаса при комнатной температуре -10oС. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали. Остаток очищали с помощью колоночной хроматографии (SiO2; элюент: смесь этилацетата/метиленхлорида (1: 1)) и получали целевое соединение.
В. 3-(1,2,5-Тиадиазол-3-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(1,2,5-тиадиазол-3-ил)пиридина (6 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 1,2 г (74%).
С. 3-(1,2,5-Тиадиазол-3-ил)- 1,2,5,6- тетрагидро-1-метилпиридиния оксалат
К раствору иодида 3-(1,2,5-тиадиазол-3-ил)-1-метилпиридиния (1,2 г, 4,4 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (380 мг, 10 мМ) и эту реакционную смесь перемешивали в течение получаса при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали с помощью колоночной хроматографии (SiO2) элюент: этилацетат/метанол (4:1)). В результате кристаллизации из ацетона получали 430 мг целевого соединения в виде соли щавелевой кислоты (т. пл. 189-181oС; М+: 181; Соединение 36).
Пример 34
1,2,5,6-Тетрагидро-3-(3-гексилокси-1,2,5-тиадиазол-4-ил)пиридина оксалат
К раствору 3-(3-гексилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1- метилпиридина (0,70 г, 2,4 мМ) в 1,2-дихлорэтане (20 мл) добавляли раствор 1-хлороэтилхлороформата (0,35 г, 2,4 мМ) в 1,2-дихлорэтане при температуре 0oС. Эту реакционную смесь нагревали до температуры 40oС в течение 2 часов, а затем выпаривали. Остаток растворяли в метаноле, нагревали в течение одного часа с обратным холодильников, а затем выпаривали. После этого остаток растворяли в разведенном гидрооксиде натрия и экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали. В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты. Выход: 620 мг (72%. (Т.пл. 157-159oС; Соединение 37).
Точно таким же способом были получены следующие соединения:
3-(3-Этокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина гидрохлорид, т.пл. 217-218oС. Соединение 215.
3-(3-Этилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина гидрохлорид, т.пл. 181-182oС. Соединение 216.
3-(3-Пропилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина оксалат, т.пл. 190-191oС. Соединение 217.
3-(3-Бутилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина оксалат, т.пл. 182-183oС. Соединение 218.
3-(3-Пентилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина оксалат, т.пл. 181-182oС. Соединение 219.
3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина оксалат, т.пл. 173-175oС. Соединение 220.
3-(3-(4-Пентинилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина оксалат, т.пл. 140-142oС. Соединение 221.
3-(3-(2,2,2-Трифторэтилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина гидрохлорид, т.пл. 105-110oС. Соединение 222.
3-(3-(2,2,2-Трифторэтокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина гидрохлорид, т.пл. 149-151oС. Соединение 223.
3-(3-(2-феноксиэтилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридина оксалат, т.пл. 191-192oС. Соединение 224.
Пример 35.
А. 3-(3-(2-(2-Метоксиэтокси)этокси)-1,2,5-тиадиазол-4-ил)-пиридина
К раствору натрия (210 мг, 9 мМ) в 2-(2-метоксиэтокси)этаноле (10 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ). Полученную смесь перемешивали в течение 4 часов при 50oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали эфиром. Объединенные органические фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-(2-Метоксиэтокси) этокси)-1,2,5-тиадиазол-4-ил)-1-метилпидиния иодид
Смесь метилиодида (0,5 мл, 9 мМ) и 3-(3-(2-(2-метоксиэтокси)этокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (10 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 0,75 г (60%).
С. 3-(3-(2-(2-Метоксиэтокси) этокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-(2-метоксиэтокси) этокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (0,76 г, 1,8 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (150 мг, 4 мМ) и эту реакционную смесь перемешивали в течение одного часа при -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты. Выход: 70 мг (т.пл. 142-143oС; М+: 299; Соединение 38).
Пример 36.
А. 3-(3-(3-Этокси-1-пропокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-этокси-1-пропанола (940 мг, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ). Эту реакционную смесь перемешивали в течение 2 часов при комнатной температуре. После добавления воды экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(3-Этокси-1-пропокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 9 мМ) и 3-(3-этокси-1-пропокси-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации.
С. 3-(3-(3-Этокси-1-пропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору, содержащему 3-(3-(3-этокси-1-пропокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид (3 мМ) в этаноле (99,9%, 15 мл), добавляли борогидрид натрия (190 мг, 5 мМ), эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии (SiO2; элюент: смесь этилацетата/метанола (4:1). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 210 мг (т. пл. 149-150oС; М+: 283; Соединение 39).
Пример 37
А. 3-(3-(2-Этоксиэтокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору 2-этоксиэтанола (1,08 г, 12 мМ) и гидрида натрия (410 мг, 12 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (790 мг, 4 мМ) в безводном тетрагидрофуране. Полученную смесь перемешивали в течение двух часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-Этоксиэтокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 9 мМ) и 3-(3-этоксиэтокси)-1,2,5-тиадиазол-4-ил)пиридина (4 мМ) в ацетоне (3 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 1,45 г (92%).
С. 3-(3-(2-Этоксиэтокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-этоксиэтокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (1,45 мг, 3,7 мМ) в этаноле (99,9%, 15 мл), добавляли борогидрид натрия (350 мг, 9 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а образовавшийся остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 640 мг (т.пл. 153-156oС; М+: 269; Соединение 40).
Пример 38
А. 3-(3-(2-Бутоксиэтокси-1,2,5-тиадиазол-4-ил)пиридин
К раствору 2-этоксиэтанола (1,06 г, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Эту реакционную смесь перемешивали в течение 2 часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-Бутоксиэтокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 9 мМ) и 3-(3-бутоксиэтокси)-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (4 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 1,07 г (85%).
С. 3-(3-(2-Этоксиэтокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-бутоксиэтокси)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (1,07 мг, 2,5 мМ) в этаноле (99,9%, 20 мл), добавляли борогидрид натрия (230 мг, 6 мМ), и эту реакционную смесь перемешивали в течение 1 часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а образовавшийся остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 490 мг (т.пл. 152-153oС; М+: 297; Соединение 41).
Пример 39
А. 3-(3-(2-(2-Бутоксиэтокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 2-(2-бутоксиэтокси)этанола (1,46 г, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Эту реакционную смесь перемешивали в течение одного часа при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-(2-Бутоксиэтокси)этокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 9 мМ) и 3-(3-бутоксиэтокси)этокси-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации.
С. 3-(3-(2-(2-Бутоксиэтокси)этокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-(2-бутоксиэтокси)этокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (3 мМ) в этаноле (99,9%, 20 мл), добавляли борогидрид натрия (230 мг, 6 мМ) и эту реакционную смесь перемешивали в течение 1 часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 340 мг (т.пл. 90-91oС; М+: 341; Соединение 42).
Пример 40
А. 3-(3-(2-(2-этоксиэтокси)этокси)-1,2,5-тиадиазол-4-ил)пиридин
К раствору 2-(2-этоксиэтокси)этанола (1,21 г, 9 мМ) и гидрида натрия (310 мг, 9 мМ) в безводном тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (590 мг, 3 мМ) в безводном тетрагидрофуране. Эту реакционную смесь перемешивали в течение 2 часов при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(2-(2-Этоксиэтокси)этокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 9 мМ) и 3-(3-(2-(2-этоксиэтокси)этокси-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации.
С. 3-(3-(2-(2-Этоксиэтокси)этокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(2-(2-этоксиэтокси)этокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (3 мМ) в этаноле (99,9%, 20 мл), добавляли борогидрид натрия (230 мг, 6 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, образовавшийся остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 290 мг (т.пл. 115-116oС; М+: 313; Соединение 43).
Пример 41
А. 3-(3-(4-Метилпиперидино)-1,2,5-тиадиазол-4-ил)пиридин
Раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (10,80 г, 4 мМ) и 4-метилпиперидина (1,96 г, 20 мМ) в ДМФ (10 мл) нагревали при температуре 100oС в течение трех часов. После выпаривания к остатку добавляли воду и смесь экстрагировали эфиром. Объединенные органические фазы осушали и выпаривали. Остаток с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метиленхлорид (1:2)). Выход 0,8 г (77%).
В. 3-(3-(4-Метилпиперидино)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 8 мМ) и 3-(3-(4-метилпиперидино)-1,2,5-тиадиазол-4-ил)пиридина (0,8 г, 3,1 мМ) в ацетоне (5 мл) перемешивали при комнатной температуре в течение 18 часов. Целевое соединение осаждали из раствора и собирали путем фильтрации. Выход: 1,14 г (92%).
С. 3-(3-(4-Метилпиперидино)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(4-метилпиперидино) -1,2,5-тиадиазол-4-ил)-1-метилпиридиния (1,14 г, 2,8 мМ) в этаноле (99,9%, 20 мл), добавляли борогидрид натрия (270 мг, 7 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 450 мг (т.пл. 106-107oС; М+: 278; Соединение 44).
Пример 42.
А. 3-(3-Морфолино)-1,2,5-тиадиазол-4-ил)пиридин
Раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) и морфолино (1,3 г, 15 мМ) в ДМФ (5 мл) нагревали в течение 3 часов при 100oС. После выпаривания к остатку добавляли воду и смесь экстрагировали эфиром. Органические фазы объединяли, осушали и выпаривали. После чего остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метиленхлорид (1:1)). Выход 0,68 г (91%).
В. 3-(3-Морфолино-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 8 мМ) и 3-(3-морфолино-1,2,5-тиадиазол-4-ил)пиридина (680 мг, 2,7 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температуре. Целевое соединение осаждали из раствора и собирали путем фильтрации с выходом: 1,0 г (94%).
С. 3-(3-Морфолино-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-морфолино-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (1,53 г, 39 мМ) в этаноле (99,9%, 30 мл), добавляли борогидрид натрия (380 мг, 10 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. После выпаривания и осушки органических фаз образовавшийся остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 470 мг (т.пл. 177-178oС; М+: 266; Соединение 45).
Пример 43.
А. 3-(3-Гексиламино-1,2,5-тиадиазол-4-ил)пиридин
Раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) и гексиламина (1,52 г, 15 мМ) в ДМСО (5 мл) нагревали при температуре 100oС в течение 48 часов. После выпаривания к остатку добавляли воду и смесь экстрагировали эфиром. Объединенные органические экстракты осушали, а затем выпаривали, в результате чего получали целевое соединение.
В. 3-(3-Гексиламино -1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,6 мл, 9,6 мМ) и 3-(3-гексиламино-1,2,5-тиадиазол-4-ил)пиридина (3,2 мМ) в ацетоне (5 мл) перемешивали при комнатной температуре в течение 18 часов, а затем выпаривали.
С. 3-(3-Гексиламино-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-гексиламино-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (4,2 мМ) в этаноле (99,9%, 25 мл) добавляли борогидрид натрия (380 мг, 10 мМ) и эту реакционную смесь перемешивали в течение одного часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии (двуокись кремния; элюент: смесь этилацетата/метанола (4: 1)). В результате кристаллизации из ацетона получали 490 мг целевого соединения в виде соли щавелевой кислоты (т.пл. 103-104oС; М+: 280; Соединение 46).
Пример 44.
А. 3-(3-Пропилтио-1,2,5-тиадиазол-4-ил)пиридин
Бисульфид натрия (220 мг, 3 мМ) добавляли в течение 30 минут к раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) в ДМФ (20 мл) при комнатной температуре, затем карбонат калия (1,24 г, 9 мМ) и иодопропан (0,76 г, 4,5 мМ). Полученную реакционную смесь перемешивали в течение 30 минут при комнатной температуре. После добавления воды смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали 0,63 г (89%) целевого соединения.
В. 3-(3-Пропилтио)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (0,5 мл, 8 мМ) и 3-(3-пропилтио-1,2,5-тиадиазол-4-ил)пиридина (0,63 г, 2,6 мМ) в ацетоне (5 мл) перемешивали в течение 18 часов при комнатной температур а затем выпаривали.
С. 3-(3-Пропилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-пропилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (2,6 мМ) в этаноле (99,9%, 15 мл), добавляли борогидрид натрия (200 мг, 5 мМ) и эту реакционную смесь перемешивали в течение 1 часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. После осушки и выпаривания органических фаз остаток очищали с помощью колоночной хроматографии (двуокись кремния; элюент: смесь этилацетата/метанола (4: 1) В результате кристаллизации из ацетона получали 310 мг целевого соединения в виде соли щавелевой кислоты (т.пл. 138-139oС; М+: 255; Соединение 47).
Пример 45
А. 3-(3-Бутилтио- 1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,5 г, 2,5 мМ) в ДМФ (20 мл) при комнатной температуре добавляли бисульфат натрия (0,5 г, 6,8 мМ) и эту реакционную смесь перемешивали в течение 30 минут. После добавления карбоната калия (2 г, 14,5 мМ) и бутилиодида (1 мл, 8,8 мМ) реакционную смесь перемешивали еще 10 минут. Затем добавляли воду (50 мл) и полученную экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали целевое соединение. Выход: 0,6 г.
В. 3-(3-Бутилтио -1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-бутилтио-1,2,5-тиадиазол-4-ил)пиридина (0,6 г, 2,3 мМ) добавляли метилиодид (1 мл, 15 мМ) и эту реакционную смесь перемешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Бутилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-бутилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (2,3 мМ) в этаноле (99,9%, 20 мл), добавляли борогидрид натрия (250 мг, 6,2 мМ) и полученную реакционную смесь перемешивали в течение одного часа при 0oС. После выпаривания остаток растворяли в воде и экстрагировали эфиром. Затем осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (двуокись кремния; элюент: смесь этилацетата/метанола (4: 1)). В результате кристаллизации из ацетона получали 300 мг целевого соединения в виде соли щавелевой кислоты (т.пл. 148-150oС; М+: 269; Соединение 48).
Пример 46
А. 3-(3-Метилтио-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,5 г, 2,5 мМ) в ДМФ (20 мл) при комнатной температуре добавляли бисульфид натрия (0,5 г, 6,8 мМ), и эту реакционную смесь перемешивали в течение 30 минут. После добавления карбоната калия (2 г, 1,45 мМ) и метилиодида (1 мл, 15 мМ), реакционную смесь перемешивали еще 10 минут, затем добавляли 50 мл воды и смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали целевое соединение. Выход: 0,5 г.
В. 3-(3-Метилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-метилтио-1,2,5-тиадиазол-4-ил)пиридина (0,5 г, 2,3 мМ) добавляли метилиодид (1 мл, 15 мМ), и эту реакционную смесь перемешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Метилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-метилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (2,3 мМ) в этаноле (99,9%, 20 мл), добавляли борогидрид натрия (250 мг, 6,2 мМ) и эту реакционную смесь перемешивали в течение 1 часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Затем осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (двуокись кремния; элюент: смесь этилацетата/метанола (4:1)). В результате кристаллизации из ацетона получали 300 мг целевого соединения в виде соли щавелевой кислоты (т.пл. 169-170oС; М+: 227; Соединение 49).
Пример 47
А. Альфа-оксимидо-3-пиридилацетонитрил
3-Пиридилацетонитрил (47,2 г, 400 мМ) растворяли в растворе гидрооксида натрия (16 г, 400 мМ) и метанола (100 мл). Метилнитрит, полученный путем добавления раствора концентрированной серной кислоты (12,8 мл) и воды (26 мл) к раствору нитрита натрия (33, 2 г, 480 мМ) в воде 20 мл) и метанола (20 мл), барботировали через раствор 3-пиридилацетонитрила при 0oС. Затем реакционную смесь перемешивали в течение 1 часа при температуре 0oС, а образовавшийся осадок собирали путем фильтрации. После этого осадок промывали небольшим количество метанола и получали 41,1 г (70%) нужного продукта. М+: 147.
В. Альфа-оксимидо-3-пиридилацетамидоксим
Смесь, состоящую из альфа-оксимидо-3-пиридилацетонитрила (41,1 г, 279 мМ) гидрохлорида гидроксиламина (21,5 г, 310 мМ) и ацетата натрия (50,8 г, 62 мМ) в этаноле (99,9%, 500 мл), нагревали с обратным холодильником в течение 4 часов. После охлаждения осадок собирали путем фильтрации и осушали. Этот осадок содержал нужный продукт и ацетат натрия (85 г, 168%); М+: 180.
С.3-(3-Амино-1,2,5-оксадиазол-4-ил) пиридин
Неочищенный альфа-оксимино-3-пиридилацетамидоксим (5 г) и пентахлорид фосфора (5 г) нагревали с обратным холодильником в безводном эфире (250 мл) в течение 6 часов. Эту смесь подщелачивали путем добавления воды и карбоната калия, а затем фазы разделяли. Водную фазу экстрагировали эфиром, а объединенные эфирные фазы осушали. В результате выпаривания эфирных фаз получали целевое соединение (850 мг); М+: 162.
D. 3-(3-Амино-1,2,5-оксидиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-амино-1,2,5-оксидиазол-4-ил)пиридина (870 мг, 5,3 мМ) в ацетоне (20 мл) добавляли метилиодид (990 мкл, 16 мМ) и эту реакционную смесь перемешивали при комнатной температуре в течение ночи. Целевое соединение осаждали и собирали путем фильтрации (1,1 г, 69%).
Е. 3-(3-Амино-1,2,5-оксидиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору, содержащему 3-(3-амино-1,2,5-оксидиазол-4-ил)- 1-метилпиридиния иодид (1,05 г, 3,45 мМ) в метаноле (80 мл) при 0oС добавляли борогидрид натрия (262 мг, 6,9 мМ). Через 15 минут к смеси добавляли воду (40 мл) и эту смесь экстрагировали эфиром. Эфирную фазу осушали, выпаривали и очищали с помощью колоночной хроматографии (элюент: смесь этилацетата/метанола (2:1)). В результате кристаллизации из ацетона с использованием щавелевой кислоты получали целевое соединение (310 мг, 50%-ный выход) (т.пл. 181-183oС; М+: 180; Соединение 50).
Пример 48.
А. 3-(3-Ацетиламино -1,2,5-оксадиазол-4-ил)пиридин
Неочищенный гидроксиимино-3-пиридилметиламидоксим (4,5 г) и полифосфорную кислоту (49 г) перемешивали в течение 18 часов при температуре 100oС. После охлаждения до комнатной температуры к смеси медленно добавляли водный раствор аммиака (25%) до рН 9, а образовавшийся осадок собирали путем фильтрации. Этот осадок растворяли в воде и экстрагировали метиленхлоридом. Органические фазы осушали и выпаривали, в результате чего получали целевое соединение (430 мг).
В. 3-(3-Ацетиламино-1,2,5-оксадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-ацетиламино-1,2,5-оксадиазол-4-ил)пиридина (490 мг, 2,4 мМ) в ацетоне добавляли метилиодид (450 мкл, 7,2 мМ), Реакционную смесь перемешивали в течение 18 часов при комнатной температуре. Осадок собирали путем фильтрации. Выход: 640 мг (77%).
С. 3-(3-Ацетиламино-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-ацетиламино-1,2,5-оксадиазол-4-ил)-1-метилпиридиния (640 мг, 1,85 мМ) в метаноле (15 мл) при 0oС добавляли борогидрид натрия (140 мг, 3,7 мМ), Через 15 минут к раствору добавляли воду, и реакционную смесь и экстрагировали эфиром. Объединенные эфирные фазы осушивали и выпаривали, После кристаллизации из ацетона с щавелевой кислотой получали целевое соединение с выходом 140 мг (т.пл. 180-184oС; М+: 222; Соединение 51).
Пример 49
А. 3-(1,2,5-Оксадиазол 3-ил)пиридин и 3-(3-хлоро-1,2,5-оксадиазол-4-ил)пиридин
К раствору 3-(3-амино-1,2,5-оксадиазол-4-ил)пиридина (1,0 г, 6,2 мМ) в ледяной уксусной кислоте (16 мл) и концентрированной соляной кислоте (5,2 мл) добавляли ССl2 (938 мг, 7 мМ) и медную проволоку в виде спирали (100 мг) при 0oС. Через 10 минут по капле при 5oС добавляли раствор нитрита натрия (483 мг, 7 мМ) в воде (3 мл). После этого реакционную смесь размешивали 30 минут при 0oС. Затем для доведения рН до щелочного значения добавляли водный раствор гидроксида натрия (2 н.) и полученную смесь экстрагировали простым эфиром. Эфирные фазы осушали и выпаривали, в результате чего получали смесь целевых соединений. После разделения с помощью колоночной хроматографии (SiO2; элюент: этилацетат) получали хлоросоединение (верхнее пятно) с выходом 230 мг, и незамещенный продукт (нижнее пятно) с выходом 60 мг.
В. 3-(3-Хлоро -1,2,5-оксадиазол -4-ил)-1-метилпиридиния иодид
К раствору 3-(3-метилтио-1,2,5-тиадиазол-4-ил)пиридина (0,5 г, 2,3 мМ) добавляли метилиодид (1 мл, 15 мМ) и эту реакционную смесь перемешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Метилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору 3-(3-хлоро -1,2,5-оксадиазол-4-ил-пиридина (230 мг, 1,2 мМ) в ацетоне добавляли метилиодид (1 мл, 15 мМ) Реакционную смесь размешивали в течение 18 часов при комнатной температуре, выпаривали и получали целевое соединение.
D. 3-(3-Хлоро-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-хлоро-1,2,5-оксадиазол-4-ил)-1-метилпиридиния (1,2 мМ) в метаноле (5 мл) при 0oС добавляли боргидрид натрия (119 мг, 3,2 мМ). Через 15 минут к раствору добавляли воду и полученную смесь экстрагировали эфиром. Эфирные фазы осушали и выпаривали, После кристаллизации из ацетона со щавелевой кислотой и перекристаллизации из ацетона получали целевое соединение с выходом 60 мг (т.пл. 126-129oС; М+: 198 и 200; Соединение 52).
Пример 50
А. 3-(1,2,5-Оксадиазол-3-ил)-1-метилпиридиния иодид
К раствору 3-(1,2,5-оксадиазол-3-ил)пиридина (430 мг, 2,9 мМ) в ацетоне (20 мл) добавляли метилиодид. Реакционную смесь размешивали в течение 18 часов при комнатной температуре. Полученный продукт осаждали из раствора и целевое соединение собирали путем фильтрации с 82% выходом (700 мг).
В. 3-(1,2,5-Оксадиазол-3-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(1,2,5-оксадиазол-3-ил)-1-метилпиридиния (640 мг, 2,2 мМ) в метаноле (15 мл) и воде (2 мл) при 0oС добавляли борогидрид натрия (168 мг, 4,4 мМ). Через 15 минут к раствору добавляли воду и полученную смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, остаток кристаллизовали в виде соли щавелевой кислоты из ацетона, в результате чего получали целевое соединение с выходом 100 мг (т.пл. 238-240oС с разложением; М+:165; Соединение 53).
Пример 51
А. 3-(3-(Гексилокси-1,2,5-оксадиазол-4-ил)пиридин
К раствору натрия (100 мг, 4,3 мМ) в 1-гексаноле (10 мл) добавляли 3-(3-хлоро-1,2,5-оксадиазол-4-ил)пиридин (180 мг, 1 мМ). Полученную смесь размешивали в течение 18 часов при 25oС, а затем выпаривали, остаток растворяли в воде и экстрагировали эфиром. Объединенные органические фазы осушали, выпаривали и получали целевое соединение.
В. 3-(3-(Гексилокси-1,2,5-оксадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(Гексилокси-1,2,5-оксадиазол-4-ил)пиридина (1 мМ) в ацетоне (5 мл) размешивали в течение 18 часов при комнатной температуре и получали целевое соединение.
С. 3-(3-(Гексилокси-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(гексилокси-1,2,5-оксадиазол-4-ил)-метилпиридиния (1 мМ) в метаноле (5 мл) добавляли борогидрид натрия (76 мг, 2 мМ) и полученную реакционную смесь размешивали 15 минут при 0oС. После выпаривания остаток растворяли в воде и экстрагировали эфиром. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4: 1)). Целевое соединение кристаллизовали из ацетона и получали целевое соединение в виде соли щавелевой кислоты с выходом 60 мг (т.пл. 143-147oС; М+: 265; Соединение 54).
Пример 52
А. 3-(3-(Бутилокси-1,2,5-оксадиазол-4-ил)пиридин
К раствору натрия (150 мг, 6,5 мМ) в 1-бутаноле (5 мл) добавляли 3-(3-хлоро-1,2,5-оксадиазол-4-ил)пиридин (350 мг, 1,9 мМ). Смесь размешивали в течение 2 часов при 25oС, а затем выпаривали. Остаток растворяли в воде и экстрагировали эфиром. Объединенные органические фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(Бутилокси-1,2,5-оксадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1 мл, 15 мМ) и 3-(3-(бутилокси-1,2,5-оксадиазол-4-ил)пиридина (1,9 мМ) в ацетоне (10 мл) размешивали 18 часов при комнатной температуре и выпаривали.
С. 3-(3-(Бутилокси-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(бутилокси-1,2,5-оксадиазол-4-ил)- -метилпиридиния (1,9 мМ) в метаноле (20 мл) добавляли борогидрид натрия (140 мг, 3,8 мМ) и полученную реакционную смесь размешивали 15 минут при 0oС. После выпаривания остаток растворяли в воде и экстрагировали эфиром. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). Целевое соединение кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 120 мг (т.пл. 132-135oС; М+: 237; Соединение 55).
Пример 53
А. 3-(3-(Гексинилокси-1,2,5-оксадиазол-4-ил)пиридин
К раствору 3-гексил-1-ол а (980 мг, 10 мМ) и гидрида натрия (240 мг, 10 мМ) в сухом тетрагидрофуране добавляли раствор 3-(3-хлоро-1,2,5-оксадиазол-4-ил)пиридина (480 мг, 2,5 мМ) в сухом тетрагидрофуране. Реакционную смесь размешивали в течение 2 часа при комнатной температуре. Затем добавляли воду и полученную смесь экстрагировали эфиром. Эфирную фазу осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(Гексинилокси-1,2,5-оксадиазол-4-ил)-1-метилпиридиния иодид
Смесь метилиодида (1,5 мл, 22 мМ) и 3-(3-(3-(гексинилокси-1,2,5-оксадиазол-4-ил)пиридин (2,5 мМ) в ацетоне (20 мл) размешивали в течение 18 часов при комнатной температуре, после чего смесь выпаривали и получали целевое соединение.
С. 3-(3-(3-(Гексинилокси-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-(-(3-(гексинилокси-1,2,5-оксадиазол-4-ил)-1 -метилпиридиния (2,5 мМ) в метаноле (20 мл) добавляли борогидрид натрия (190 мг, 5 мМ) и реакционную смесь размешивали в течение 15 минут при 0oС. После выпаривания остаток растворяли в воде и экстрагировали эфиром. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). После кристализации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 50 мг (Т.пл. 159-161oС; М+: 261; Соединение 56).
Пример 54.
3-(3-Фенил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (450 мг, 1,5 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида пентилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл), а осушенные эфирные фазы выпаривали. Остаток кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 300 мг (58%). После перекристаллизации из этанола получали 125 мг целевого соединения (24%). (Т.пл. 156-157oС; М+: 251; Соединение 57).
Пример 55
3-(3-Гептил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (450 мг, 1,5 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида гептилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл), а осушенные эфирные фазы выпаривали. Остаток кристаллизовали из ацетона в виде соли щавелевой кислоты с выходом 400 мг (73%). (Т.пл. 151-152oС; М+: 274; Соединение 58).
Пример 56
3-(3-Гексенил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (450 мг, 1,5 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида 5-гексенилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл), а осушенные эфирные фазы выпаривали. Остаток очищали с помощью колоночной хроматографии (SiO2 элюент: этилацетат/метанол (4:1)). Целевое соединение получали после кристаллизации из ацетона в виде соли щавелевой кислоты с выходом 340 мг (64%). (Т.пл. 113-115oС; М+: 263; Соединение 59).
Пример 57
3-(3-Октил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (450 мг, 1,5 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида октилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл) и осушенные эфирные фазы выпаривали. Остаток очищали с помощью колоночной хроматографии (SiO2 элюент: этилацетат/метанол (4:1)). Целевое соединение получали в виде соли щавелевой кислоты после кристаллизации из ацетона с выходом 430 мг (75%). (Т.пл. 157-158oС; М+: 293; Соединение 60).
Пример 58
3-(3-Изобутил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (300 мг, 1,5 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида изобутилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл) а осушенные эфирные фазы выпаривали. Остаток очищали с помощью колоночной хроматографии (SiO2 элюент: этилацетат/метанол (4:1)). После кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 350 мг (76%). (Т. пл. 148-149oС; М+: 237; Соединение 61).
Пример 59
3-(3-Циклопропилметил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (300 мг, 1,4 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида циклопропилметилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл) и осушенные эфирные фазы выпаривали. Остаток очищали с помощью колоночной хроматографии (SiO2 элюент: этилацетат/метанол (4: 1)). После кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 380 мг (83%). (Т.пл. 147-148oС; М+: 235; Соединение 62).
Пример 60
3-(3-Пропил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридиния оксалат
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (450 мг, 1,5 мМ) в тетрагидрофуране (20 мл) медленно добавляли раствор бромида пропилмагния (1,5 мМ) в тетрагидрофуране при 0oС. Реакционную смесь размешивали в течение 10 минут, после чего добавляли воду (20 мл). Полученный продукт экстрагировали эфиром (3•100 мл) и осушенные эфирные фазы выпаривали. Остаток кристаллизовали из ацетона, получали целевое соединение в виде соли щавелевой кислоты с выходом 350 мг (75%). (Т.пл. 141-142oС; М+: 223; Соединение 63).
Пример 61
А. 3-(3-Октилтио-1,2,5-тиадиазол-4-ил)-пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) в диметилформамиде (20 мл) при комнатной температуре добавляли бисульфид натрия (0,25 г, 3,3 мМ) и полученную реакционную смесь размешивали в течение 30 минут. Затем добавляли карбонат калия (1,24 г, 9 мМ) и 1-бромоацетат (0,80 мл, 4,5 мМ) и реакционную смесь размешивали еще 10 минут. После этого добавляли воду (59 мл) и смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-Октилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-октилтио-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) добавляли метилиодид (0,5 мл, 7,5 мМ) и реакционную смесь размешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Октилтил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-октилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (3 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (270 мг, 7 мМ) и полученную реакционную смесь размешивали в течение 1 часа при 0oС. После выпаривания остаток растворяли в виде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). После кристаллизации из ацетата получали целевое соединение в виде соли щавелевой кислоты с выходом 400 мг. (Т.пл. 121-122oС; М+: 325; Соединение 64).
Пример 62
А. 3-(3-Этилтио-1,2,5-тиадиазол-4-ил)-пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) в диметилформамиде (20 мл) при комнатной температуре добавляли бисульфид натрия (0,25 г, 3,3 мМ) и реакционную смесь размешивали в течение 30 минут. Затем добавляли карбонат калия (1,24 г, 9 мМ) и этилиодид (0,36 мл, 4,5 мМ) и реакционную смесь размешивали еще 10 минут. После этого добавляли воду (50 мл) и экстрагировали эфиром. Объединенные эфирные фазы осушали, выпаривали и получали целевое соединение.
В. 3-(3-Этилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-этилтио-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) добавляли метилиодид (0,5 мл, 7,5 мМ) и реакционную смесь размешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Этилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору иодида 3-(3-этилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (3 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (270 мг, 7 мМ) и реакционную смесь размешивали в течение 1 часа при 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). После кристаллизации из ацетата получали целевое соединение в виде соли щавелевой кислоты с выходом 490 мг. (Т.пл. 145-146oС; М+: 241; Соединение 65).
Пример 63.
А. 3-(3-Пентилтио-1,2,5-тиадиазол-4-ил)-пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) в диметилформамиде (20 мл) при комнатной температуре добавляли бисульфид натрия (0,25 г, 3,3 мМ) и реакционную смесь размешивали в течение 30 минут. Затем добавляли карбонат калия (1,24 г, 9 мМ) и пентилбромид (700 мг, 4,5 мМ) и реакционную смесь размешивали еще 10 минут. После этого добавляли воду (50 мл) и смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-Пентилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-пентилтио-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) добавляли метилиодид (0,5 мл, 7,5 мМ) и полученную реакционную смесь размешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Пентилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору, содержащему 3-(3-пентилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния (3 мМ) и этанол (99,9%, 20 мл), добавляли борогидрид натрия (300 мг, 8 мМ) и полученную реакционную смесь перемешивали в течение 1 часа при 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, после чего остаток очищали с помощью колоночной хроматографии (SiO2; элюент: этилацетат/метанол (4:1)). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 430 мг. (Т.пл. 136-138oС; М+: 283; Соединение 66).
Пример 64
А. 3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3 мМ) в ДМФ (20 мл) при комнатной температуре добавляли бисульфид натрия (0,25 г, 3,3 мМ) и полученную реакционную смесь перемешивали в течение 30 минут. После добавляли карбонат калия (1,24 г, 9 мМ) и гексилбромид (0,63 мл, 4,5 мМ) реакционную смесь перемешивали еще 10 минут. Затем добавляли воду (50 мл) и эту смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-гексилтио-1,2,5-тиадиазол-4-ил)пиридина (3 мМ) добавляли метилиодид (1 мл, 15 мМ) и полученную реакционную смесь перемешивали в течение 48 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору, содержащему 3-(3-гексилтио-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид (3 мМ) и этанол (99,9%, 20 мл), добавляли борогидрид натрия (230 мг, 6 мм) и полученную реакционную смесь перемешивали в течение одного часа при температуре 0oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а затем остаток очищали с помощью колоночной хроматографии (двуокись кремния; элюент: этилацетат/метанол (4:1)). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 350 мг (т. пл. 126-127 oС; М+: 297; Соединение 67).
Пример 65
А. 3-(3-(5-Цианопентилтио)-1,2,5- тиадиазол-4-ил)пиридин
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (0,59 г, 3,0 мМ) в ДМФ (20 мл) при комнатной температуре добавляли моногидрат бисульфида натрия (0,25 г, 3,3 мМ) и полученную реакционную смесь перемешивали в течение 1 часа. После добавления карбоната калия (1,24 г, 9 мМ) и 6-бромокапронитрила (0,80 г, 4,5 мМ) реакционную смесь перемешивали еще 24 часа. Затем добавляли воду (50 мл) и эту смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали, в результате чего получали целевое соединение.
В. 3-(3-(5-Цианопентилтио)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
К раствору 3-(3-(5-цианопентилтио)-1,2,5-тиадиазол-4-ил-пиридина (3 мМ) в ацетоне добавляли метилиодид (1 мл, 15 мМ) и полученную реакционную смесь перемешивали в течение 20 часов при комнатной температуре, а затем выпаривали.
С. 3-(3-(5-Цианопентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагиро-1-метилпиридина оксалат
К раствору, содержащему 3-(3-(5-цианопентилтио)-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид (3 мМ) и этанол (99,9%, 20 мл), добавляли борогидрид натрия (290 мг, 7,5 мМ) и полученную реакционную смесь перемешивали в течение 1 часа при температуре -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Затем осушенные органические фазы выпаривали и остаток очищали с помощью колоночной хроматографии (SiO2; элюент: смесь этилацетата/метанола (4: 1)). В результате кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 410 мг, т. пл. 139-140oС (Соединение 68).
Точно таким же способом, но с использованием соответствующего алкилгалогенида были получены следующие соединения:
3-(3-(3-Хлоропропилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 136-138oС, Соединение 69.
3-(3-(3-Цианопропилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 117-118oС, Соединение 70.
3-(3-(3-Фенилпропилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 110-110,5oС, Соединение 71.
3-(3-(2-Феноксиэтилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 125-126oС, Соединение 72.
3-(3-(4-Цианобутилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 127-127,5oС, Соединение 73.
3-(3-(8-Гидроксиоктилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 112-113,5oС, Соединение 74.
3-(3-(4-Хлорбутилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 136-137oС, Соединение 75.
3-(3-(4,4-Бис-(4-фторфенил)-бутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 117,5-118oС, Соединение 76.
3-(3-(2-(1,3-Диоксолан-2-ил)-этилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 117-118oС, Соединение 77.
3-(3-(4-Цианобензилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 138-140oС, Соединение 78.
3-(3-(2-Фенилэтилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 155-156oС, Соединение 79.
3-(3-(4-Бромбензилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 196-140oС, Соединение 80.
3-(3-(4-Метилбензилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 162-165oС, Соединение 81.
3-(3-(4-Пиридилметилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 140-142oС, Соединение 82.
3-(3-(2-Бензоилэтилтио)-1,2,5-тиадиазол -4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 99-100oС, Соединение 83.
3-(3-(4-Оксо-4-(4-фторфенил)-бутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 131-132oС, Соединение 84.
3-(3-Бензилоксикарбонилметилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 179oС, Соединение 85.
3-(3-Бентилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 195-197oС, Соединение 86.
3-(3-(4,4,4-Трифторобутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 163-165oС, Соединение 87.
3-(3-(5,5,5-Трифторопентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 134-136oС, Соединение 88.
3-(3-(6,6,6-Трифторогексилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 128-129oС, Соединение 89.
3-(3-Этоксикарбонилпентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 78-81oС, Соединение 90.
3-(3-(2,2,2-Трифторэтилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро -1-метилпиридина оксалат, т.пл. 159-163oС, Соединение 225.
3-(3-Изогексилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 131-134oС. Соединение 226.
3-(3-Этоксикарбонилпропилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина гидрохлорид. Т.пл. 109-111oС. Соединение 227.
3-(3-(2-(2-Тиенилтио)этилтио))-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 112-115oС. Соединение 228.
3-(3-(5-Этил-2-тиенилметилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 106-110oС. Соединение 229.
3-(3-(6-Гидроксигексилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 108-110oС. Соединение 230.
3-(3-(3-Метил-2-тиенилметилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 184-186oС. Соединение 231.
3-(3-(2-(2-Тиенилтио)пропилтио))-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 193-196oС. Соединение 232.
3-(3-(4-Этокси-1,2,5-тиадиазол-3-илтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 173-174oС. Соединение 233.
3-(3-(5-Метил-2-тиенилметилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 148-1149С. Соединение 234.
3-(3-(4-Этилтио-1,2,5-тиадиазол-3-илтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 187-189oС. Соединение 235.
3-(3-(4-Бутилтио-1,2,5-тиадиазол-3-илтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 162-164oС. Соединение 236.
3-(3-(4-Пропокси-1,2,5-тиадиазол-3-илтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 182-183oС. Соединение 237.
Цис-3-(3-(3-гексинилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 101-102oС. Соединение 238.
3-(3-(1-Циклопропилметилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 145-146oС. Соединение 239.
3-(3-(1-Этоксикарбонилпентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 94-95oС. Соединение 240.
3-(3-(5-Гексенилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 115-116oС. Соединение 241.
3-(3-Циклопентилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 144-145oС. Соединение 242.
3-(3-(2-Метоксиэтилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 150-151oС. Соединение 243.
3-(3-(2-(2-Этоксиметокси)-этилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 117-118oС. Соединение 244.
3-(3-(4-Пентинилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 121-122oС. Соединение 245.
3-(3-Гептилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 122-123oС. Соединение 246.
3-(3-(2-Этилбутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 141-142oС. Соединение 247.
3-(3-Циклогексилметилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 153-155oС. Соединение 248.
3-(3-(7-Октенилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 115-116oС. Соединение 249.
3-(3-(3-Бутенилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 140-141oС. Соединение 250.
3-(3-(4-Пентинилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 137-138oС. Соединение 251.
3-(3-(3,3,3-Трифторпропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 131-135oС. Соединение 252.
3-(3-(1-Оксо-1-фенилпропилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 91-100oС. Соединение 253.
3-(3-(4-Фенилтиобутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 97-99oС. Соединение 254.
3-(3-Цианометилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 176-177oС. Соединение 255.
3-(3-(6-Хлоргексилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 125-126oС. Соединение 256.
3-(3-(5-Хлорпентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 106-107oС. Соединение 257.
Пример 66
А. 3-(3-(6,6,6-Трифторогексилокси)-1,2,5- тиадиазол-4-ил)пиридин
К смеси гидрида натрия (12,8 мМ) и 6,6,6-трифторо-1-гексанола (3,0 г, 19,2 мМ) в тетрагидрофуране (40 мл) добавляли 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (1,3 г, 6,4 мМ). Смесь нагревали с обратным холодильником в течение 36 часов, а затем выпаривали. После выпаривания остаток растворяли в воде и экстрагировали диэтиловым эфиром. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (силикагель; элюент: этилацетат/гексан) в результате чего получали целевое соединение с выходом 630 мг (31%).
В. 3-(3-(6,6,6-Трифторогексилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид
Раствор метилиодида (852 мг, 6,0 мМ) и 3-(3-(6,6,6-трифторгексилокси-1,2,5-тиадиазол-4-ил-пиридина (630 мг, 2,0 мМ) в ацетоне (25 мл) нагревали с обратным холодильником в течение 7 часов. Затем раствор выпаривали, а остаток использовали непосредственно в следующей стадии.
С. 1,2,5,6-Тетрагидро-1-метил-3-(3-(6,6,6-трифторгексилокси - 1,2,5-тиадиазол-4-ил)пиридина оксалат
К раствору иодида (3-(3-(6,6,6-трифторгексилокси-1,2,5-тиадиазол-4-ил)-1-метилпиридиния иодид (2,0 мМ) и этанол (15 мл) добавляли борогидрид натрия (380 мг, 10 мМ) и реакционную смесь перемешивали в течение ночи при комнатной температуре. После выпаривания остаток растворяли в воде и экстрагировали диэтиловым эфиром. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (силикагель; элюент: 25% этилацетат в гексане). После кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты с выходом 180 мг, Т. пл. 138-140oС.
Вычислено, %: С 45,17; Н 5,21; N 9,88.
Найдено, %: С 45,13; Н 5,18; N 9,62. Соединение 91.
Аналогичным способом с использованием соответствующего алкоксипроизводного были получены следующие соединения:
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-(2-тиенил)-1-пропокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 130-133oС. М+: 321. Соединение 92.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-(4-метоксифенил)-1-пропокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 166-167oС. М+: 345. Соединение 93.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-(4-метоксифенил)-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 166-167oС. М+: 331. Соединение 94.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-(2-тиенил)-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 145-146oС. М+: 306. Соединение 95.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-(3-тиенил)-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 138-140oС. Соединение 96.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-гидрокси-1-пропокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 105-107oС. М+: 256. Соединение 97.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-фенил-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 146-147oС. М+: 301. Соединение 98.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-тиенилметокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 161-162oС. М+: 294. Соединение 99.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-гидрокси-1-гексилокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 147-148oС. М+: 297. Соединение 100.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-тиенилметокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 175-176oС. М+: 293. Соединение 101.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-фенил-1-пропокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 136-138oС. М+: 315. Соединение 102.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-(2-пирролидон-1-ил)- 1-пропокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 160-161oС. М+: 322. Соединение 103.
1,2,5,6-Тетрагидро-1-метил-3-(3-(6-ацетамидо-1-гексилокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 114-116oС. М+: 338. Соединение 104.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-ацетамидо-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 145-148oС. М+: 283. Соединение 105.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-(2-пирролидон-1-ил)-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 170-171oС. М+: 309. Соединение 106.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-пропионамидо-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 142-143oС. М+: 296. Соединение 107.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-(2-оксазолидон-3-ил)-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 157-159oС. М+: 310. Соединение 108.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-бензилтио-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 133-134oС. М+: 347. Соединение 109.
1,2,5,6-Тетрагидро-1-метил-3-(3-(3-(1-пирролидил)-1-пропокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 141-142oС. М+: 308. Соединение 110.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-урендо-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат. Т. пл. 200oС (разложение). М+: 265. Соединение 111.
3-(3-(2,4-Диметилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(2,4-диметилфенил)-3-пропанола. Т. пл. 159-162oС. Соединение 161.
3-(3-(3,4-Диметилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(3,4-диметилфенил)-3-пропанола. Т. пл. 119-121oС. Соединение 162.
3-(3-(5-Этил-2-тиенилметокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-гидроксиметил-5-этилтеофена. Т.пл. 146-148oС. Соединение 163.
3-(3-Пирролидин-1-ил)пропокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1- пирролидин-1-ил-3-пропанола. Т.пл. 141oС (разложение). Соединение 164.
3-(3-(4-Фторфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(4- фторофенил)-5-пропанола. Т.пл. 143-144oС. Соединение 165.
3-(3-(4-Хлорфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(4-хлорфенил)-3-пропанола. Т.пл. 154-155oС. Соединение 166.
3-(3-(3-Метилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(3-метилфенил)-3-пропанола. Т.пл. 136-139oС. Соединение 167.
3-(3-(2,3-Дигидро-1-инденилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1- гидрокси-2,3-дегидроиндена. Т.пл. 157-159oС. Соединение 168.
3-(3-(4-Метилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(4-метилфенил)-3-пропанола. Т.пл. 155-159oС. Соединение 169.
3-(3-(1,2,3,4-Тетрагидро-2-нафтилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1,2,3,4-тетрагидро-2-нафтола. Т.пл. 100-103oС. Соединение 170.
3-(3-Фенилбутокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1- фенил-4-бутанола. Т.пл. 128-130oС. Соединение 171.
3-(3-(2-Метилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1- метилфенил-3-пропанола. Т.пл. 145-148oС. Соединение 172.
3-(3-(2,5-Диметилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(2,5-диметилфенил)-3-пропанола. Т.пл. 130-134oС. Соединение 173.
3-(3-Метилтиоэтокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и метилтиоэтанола. Т.пл. 146-147oС. Соединение 174.
3-(3-Диметиламиноэтокси -1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина диоксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-диметиламиноэтанола. Т.пл. 148-150С. Соединение 175.
3-(3-(3,4-Дихлорфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(3,4-дихлорфенил)-3-пропанола. Т.пл. 128-130oС. Соединение 176.
3-(3-Диметиламинопропокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-диметиламино-3-пропанола.. Т.пл. 144-146oС. Соединение 177.
3-(3-(4-Этилбензилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1- этил-4-гидроксиметилбензола. Т.пл. 187-190oС. Соединение 178.
3-(3-(4-Метилфенилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-(4-метилфенил)-3-пропанола. Т.пл. 147-149oС. Соединение 179.
3-(3-(4-Бутилбензилокси) -1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1- бутил-4-гидроксиметилбензола. Т.пл. 187-190oС. Соединение 180.
3-(3-(1-Этилпентилокси) -1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина фумарат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 3- октанола. Т.пл. 117-120oС. Соединение 181.
3-(3-(2-Этилбутокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина фумарат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 3-гептанола. Т.пл. 139-140oС. Соединение 182.
3-(3-(1-Метилпентилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина фумарат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 2-гексанола. Т.пл. 143-144oС. Соединение 183.
3-(3-(5-Гексинилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 3-гидрокси-1-гексина. Т.пл. 120-122oС. Соединение 184.
3-(3-(4-Циклогексилбутокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-циклогексил-4-бутанола. Т.пл. 145-147oС. Соединение 185.
3-(3-(5-Гидроксигексилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1,5-дигидроксигексина. Т.пл. 128-129oС. Соединение 186.
3-(3-(5-Оксигексилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 50-оксо-1-гексанола. Т.пл. 143-144oС. Соединение 187.
3-(3-(4-Метиленциклогексилметил)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 1-гидроксиметил-4-метиленциклогексана. Т.пл. 160-161oС. Соединение 189.
3-(3-(2,3-Диметилпентилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-гидрокси-2,3-диметилпентана. Т.пл. 160-161oС. Соединение 190.
3-(3-(3-Циклогексинилметокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-гидроксиметил-3-циклогексена. Т.пл. 138-140oС. Соединение 191.
3-(3-Изобутилтиоэтокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и изобутилтиоэтанола. Т.пл. 138-140oС. Соединение 192.
3-(3-Циклопропилпропокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-циклопропил-3-пропанола. Т.пл. 151-153oС. Соединение 193.
3-(3-(2-Метилциклопропилметокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1- гидроксиметил-2-метилциклопропана. Т.пл. 121-122oС. Соединение 194.
3-(3-Циклопентилпропокси-1,2,5-тиадиазол 4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-циклопентил-3-пропанола. Т.пл. 154-156oС. Соединение 195.
3-(3-(4-Метилгексилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 4-метил-1-гексанола. Т.пл. 136-139oС. Соединение 196.
3-(3-(1-Метилгексилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина и 2-гептанола. Т.пл. 118-119oС. Соединение 197.
3-(3-(4,4,4-Трифторобутокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 4,4,4-трифтор-1-бутанола. Т.пл. 157-160oС. Соединение 198.
3-(3-(3-Метилпентилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина фумарат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-метил-1-пентанола. Т.пл. 133-134oС. Соединение 199.
3-(3-(6,6,6-Трифторогексилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 6,6,6-трифторо-1-гексанола. Т.пл. 144-146oС. Соединение 200.
3-(3-(3-Циклобутилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 3-циклобутил-1-пропанола. Т.пл. 146-148oС. Соединение 201.
3-(3-Изопропоксиэтокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и изопропоксиэтанола. Т.пл. 142-143oС. Соединение 202.
3-(3-Изогептилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и изогептанола. Т.пл. 150-152oС. Соединение 203.
3-(3-Изогексилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина малеат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и изогексанола. Т.пл. 72-74oС. Соединение 204.
3-(3-(2,2,2-Трифтороэтокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина фумарат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 2,2,2-трифтороэтанола. Т.пл. 131-133oС. Соединение 205.
3-(3-(2-Хлорофенилпропокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-(2-хлорфенил)-3-пропанола. Т.пл. 147-149oС. Соединение 206.
3-(3-(3-Циклогексилпропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина фумарат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 1-циклопропил-3-пропанола. Т.пл. 89-90oС. Соединение 207.
3-(3-(2-Циклогексилэтокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-тиадиазол -4-ил)пиридина и 2-циклопропилэтанола. Т.пл. 134-135oС. Соединение 208.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-этилсульфинил-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат.
1,2,5,6-Тетрагидро-1-метил-3-(3-(2-этилсульфинил-1-этокси)-1,2,5-тиадиазол-4-ил)пиридина оксалат получали аналогичным способом с использованием в качестве исходного спирта 2-(этилтио)-этанол. Промежуточный 3-(4-(2-этилтио-1-этокси)-1,2,5-тиадиазол-3-ил)пиридин окисляли 1,1 эквивалентом NaIO4 и 1 эквивалентом NeSO3Н, используя воду в качестве реакционного растворителя. Через 3,5 часа раствор подщелачивали 2 н. гидроксидом натрия, а затем экстрагировали этилацетатом. Объединенные экстракты осушали сульфатом магния и выпаривали в вакууме. Полученный сульфоксид превращали в целевое соединение способом, аналогичным способу, описанному выше. 171-172oС. М+: 302; Соединение 112.
1,2,5,6-Тетрагидро-3-(3-(5-оксогексил)-1,2,5-тиадиазол-4-ил)-1-метилпиридин.
1,2,5,6-Тетрагидро-3-(3-(5-оксогексил)-1,2,5-тиадиазол-4-ил)-1-метилпиридин получали аналогичным способом с использованием 1,5-гександиола. Окисление этого соединения с получением кетона осуществляли в условиях, описанных ниже. К раствору (-70oС) оксалилхлорида (420 мкл, 4,8 мМ) в 25 мл метиленхлорида добавляли ДМСО (750 мкл, 10,6 мМ) таким образом, чтобы реакционная температура поддерживалась ниже -45oС. Через 2 минуты к смеси медленно добавляли 1,2,5-тетрагидро-3-(3-(5-гидроксигексил)-1,2,5-тиадиазол-4-ил)-1-метилпиридина (1,3 г, 4,4 мМ) в 20 мл метиленхлорида, поддерживая при этом температуру ниже -45oС. Через 15 минут к смеси добавляли 3 мл (21,8 мМ) триэтиламина и эту реакционную смесь нагревали до комнатной температуры. После добавления солевого раствора (50 мл) смесь три раза экстрагировали 50 миллилитрами метиленхлорида. Объединенные экстракты осушали сульфатом натрия и выпаривали в вакууме. Полученное маслообразное вещество хроматографировали на силикагеле (элюент: 90% СHСl3, 2% MeOH) и получали 810 мг маслообразного вещества, которое растворяли в МеОН и обрабатывали 250 миллиграммами (2,8 мМ) щавелевой кислоты. Полученную соль щавелевой кислоты перекристаллизовывали из смеси МеОН/EtOAc, в результате чего получали 860 мг целевого соединения. Т.пл. 143-144oС. М+: 295; Соединение 113.
Пример 67.
А. 3-(3-Хлоро-1,2,5-оксадиазол-4-ил)пиридин
К раствору 3-(3-амино-1,2,5-оксадиазол-4-ил)пиридина (1,0 г, 6,2 мМ) в ледяной уксусной кислоте (16 мл) и концентрированной соляной кислоте (5,2 мл) добавляли CuCl2 (938 мг, 7 мМ) и спиральную медную проволоку (100 мг) при температуре 0oС. Через 10 минут к смеси по капле добавляли раствор нитрата натрия (483 мг, 7 мМ) в воде (3 мл) при температуре 5oС. Затем реакционную смесь перемешивали еще 30 минут при температуре 0oС. Для получения щелочного значения рН к смеси добавляли водный раствор 2 н. гидроксида натрия и эту смесь экстрагировали эфиром. Эфирные фазы осушали и выпаривали, в результате чего получали смесь целевых соединений. В результате разделения с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат) получали хлоровое соединение, верхнее пятно, выход=230 мг.
В. 3-(3-(3-Фенилпропилтио)- 1,2,5-оксадиазол-4-ил)пиридин
К раствору 3-(3-хлоро -1,2,5-оксадиазол-4-ил)пиридина (1,27 г, 7,0 мМ) в ДМФ (30 мл) при комнатной температуре добавляли моногидрат бисульфида натрия (0,74 г, 10,5 мМ) и полученную реакционную смесь перемешивали в течение одного часа. После добавления карбоната калия (2,0 г, 14,5 мМ) и 1-бромо-3-фенилпропана (2,4 г, 12 мМ) реакционную смесь перемешивали еще 24 часа. Затем добавляли воду (50 мл) и смесь экстрагировали эфиром. Объединенные эфирные фазы осушали и выпаривали. В результате очистки с помощью колоночной хроматографии на двуокиси кремния (элюент: этилацетат/метиленхлорида (1:1)) получали целевое соединение.
С. 3-(3-(3-Фенилпропилтио)-1,2,5-оксадиазол-4-ил)-1-метилпиридиния иодид
3-(3-(3-Фенилпропилтио)-1,2,5-оксадиазол-4-ил)-1-метилпиридина (7 мМ) в ацетоне добавляли метилиодид (1 мл, 15 мМ) и полученную реакционную смесь перемешивали в течение 20 часов при комнатной температуре, а затем выпаривали.
D. 3-(3-(3-фенилпропилтио)-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору 3-(3-(3-фенилпропилтио)-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (7 мМ) в этаноле (99,9%, 20 мл) добавляли борогидрид натрия (650 мг, 17 мМ) и полученную реакционную смесь перемешивали в течение 1 часа при температуре -10oС. После выпаривали остаток растворяли в воде, а затем экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии на двуокиси кремния (элюент: смесь этилацетата/метанола (4:1)). Целевое соединение кристаллизовали из ацетона в виде щавелевой кислоты. После перекристаллизации получали 170 мг нужного продукта. Т.пл. 106-100oС. Соединение 114.
Точно таким же способом с использованием соответствующего алкилгалогенида были получены следующие соединения.
3-(3-(2-Феноксиэтилтио)-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 122-124oС. Соединение 115.
3-(3-Пентилтио-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-оксадиазол-4-ил)-пиридина, бисульфида натрия и 1-бромопентала. Т.пл. 123-124oС. Соединение 212.
3-(3-Гексилтио-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-оксадиазол-4-ил)-пиридина, бисульфида натрия и 1-бромгексана. Т.пл. 111-113oС. Соединение 213.
3-(3-(4-Пентинилтио)-1,2,5-оксадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат из 3-(3-хлоро-1,2,5-оксадиазол-4-ил)-пиридина, бисульфида натрия и 1-бромо-4-пентина. Т.пл. 119-120oС. Соединение 214.
Пример 68
1-(3-(3-Пиридин)-1,2,5-тиадиазол-4-ил)-4-(3-(1-метил-1,2-5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)-бутана оксалат
К раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-1-метил-1,2-5,6-тетрагидропиридина (0,43 г, 2 мМ) в ДМФ (30 мл) добавляли бисульфид натрия (0,3 г, 4 мМ). Реакционную смесь размешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат калия (1 г) и 3-(3-(4-хлоробутилтио)-1,2,5-тиадиазол-4-ил)пиридин и реакционную смесь размешивали в течение ночи при комнатной температуре. После этого добавляли воду (200 мл) и водную фазу экстрагировали эфиром (3•100 мл). Эфирные экстракты осушали сульфатом магния и выпаривали. Остаток очищали с помощью колоночной хроматографии (Элюент: этилацетат/метанол, 9:1). Полученное свободное основание кристаллизовали со щавелевой кислоты из ацетона, и получали целевое соединение с выходом 0,9 г (Соединение 116). Т.пл. 127-129oС.
Пример 69.
1-(1-Метилтетразол-5-илтио)-(1-метил-1,2-5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)-бутана оксалат
К раствору 3-(3-(4-хлоробутилтио-1,2,5-тиадиазол-4-ил)-1-метил-1,2-5,6-тетрагидропиридина (0,30 г, 1 мМ) в ДМФ (30 мл) добавляли 1-метил-5-меркаптотразол (0,35 г, 3 мМ) и карбонат калия (2 г). Реакционную смесь размешивали в течение 60 часов при комнатной температуре. Затем добавляли 1 н. соляную кислоту (200 мл), водную фазу экстрагировали эфиром (2•100 мл). Водную фазу подщелачивали твердым карбонатом калия, и экстрагировали эфиром (3•100 мл). Эфирные экстракты после щелочной экстракции объединяли и осушали сульфатом магния. Эфирную фазу выпаривали, остаток кристаллизовали из ацетона со щавелевой кислоты, в результате чего получали целевое соединение с выходом 0,4 г. (Соединение 117). Т.пл. 77-79oС.
Пример 70.
Способом, описанным в Примере 69, и с использованием указанных ниже реагентов получали следующие соединения:
1-(2-Метил-1,3,4-тиадиазол-5-илтио)-4-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)бутана оксалат из 3-(3-(4-хлорбутилтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 2-метил-5-меркапто-1,3,4- тиадиазола. Соединение 118. Т.пл. 102-104oС.
1-(2-Тиазолин-2-илтио)-4-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)бутана оксалат из 3-(4-хлорбутилтио)-1,2,5-(тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 2-тиазолин-2-тиола. Соединение 119. Т. пл. 116-117oС.
1-(2-Бензоксазолилтио)-4-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)бутана оксалат из 3-(3-илтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 2-меркаптобензоксазола. Соединение 120. Т. пл. 156-158oС.
1-(2-Метил-1,3,4-тиадиазол-5-илтио)-5-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)пентана оксалат из 3-(3-(5-хлоропентилтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 2-метил-5-меркапто-1,3,4-тиадиазола. Соединение 121. Т. пл. 69-70oС.
1-(2-Бензтиазолилтио)-5-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)пентана оксалат из 3-(3-(5-хлорпентилтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 2-меркаптобензтиазола. Соединение 122. Т. пл. 116-117oС.
1-(1-Метилтетразол-5-илтио)-5-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)пентана оксалат из 3-(3-(5-хлорпентилтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 1 -метил-5-меркаптотетразола. Соединение 123. Т. пл. 96-97oС.
1-(2-Метил-1,3,4-тиадиазол-5-илтио)-6-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)-гексана оксалат из 3-(3-(6-хлоргексилтио)-1,2,5-тиадиазол-4-илтио)-1-метил-1,2,5,6-тетрагидропиридина и 2-метил-5-меркапто-1,3,4-тиадиазола. Соединение 124. Т. пл. 85-86oС.
1-(1-Метилтетразол-5-илтио)-6-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)гексана оксалат из 3-(3-(6-хлоргексилтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 1-меркаптотетразола. Соединение 125. Т. пл. 65-66oС.
1-(2-Тиазолин-2-илтио)-6-(3-(1-метил-1,2,5,6-тетрагидропиридин-3-ил)-1,2,5-тиадиазол-4-илтио)гексана оксалат из 3-(3-(6-хлоргексилтио)-1,2,5-тиадиазол-4-ил)-1-метил-1,2,5,6-тетрагидропиридина и 2-тиазолин-2-тиола. Соединение 126. Т. пл. 61-62oС.
Пример 71.
3-(3-Метилсульфонил-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат, гемиацетон.
Раствор оксалата 3-(3-метилтио-1,2,5-тиадиазол-4-ил)-1,2-5,6-тетрагидро-1-метилпиридина (0,25 г, 0,0079 М) в воде (10 мл) охлаждали в бане из льда/воды, а затем по капле добавляли раствор оксона (0,7 г, 0,00114 М). После этого охлаждающую баню удаляли и через 5 часов добавляли избыточное количество NaHSO3. Полученный раствор охлаждали в бане из льда/воды, а затем подщелачивали и эту смесь экстрагировали метиленхлоридом (3•25 мл). Экстракты осушали, а затем растворитель выпаривали и образовавшийся остаток очищали с помощью реальной хроматографии (элюент: 5% EtOH - 0,5% NH4OH /CHCl3), в результате чего получали белое кристаллическое твердое вещество (0,2 г). Соль щавелевой кислоты перекристаллизовывали из ацетона и получали бесцветные кристаллы. (Т.пл. 96-97oС, Соединение 127). С помощью ЯМР-анализа было подтверждено, что эта соль содержала 0,2 М ацетона.
Анализ для С9Н13N3O2•C2H2O4•0,5 C3H6O
Вычислено: С 39,68; Н 4,79; N 11,10;
Найдено: С 39,52; Н 4,85; N 11,19.
3-(3-/2-(1-Пирролидинил)этокси/-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина диоксолат
Суспензию, состоящую из NaH (0,0075 М) в тетрагидрофуране (25 мл), обрабатывали 2-гидроксиэтилпирролидином (1 мл, 0,0086 М), и через 30 минут к этой суспензии добавляли свободное основание (Соединение 127) (0,6 г, 0,0023 М). Еще через один час к смеси добавляли воду (22 мл), а растворитель выпаривали. Остаток суспендировали в воде и экстрагировали метиленхлоридом (3•25 мл). После этого экстракты осушали, растворитель выпаривали, а остаток очищали с помощью радиальной хроматографии (элюент: 20% EtOH- 2% NH4OH - СНCl3), в результате чего получали 0,4 г жидкости, окрашенной в бледно-желтый цвет. Полученный диоксалат перекристаллизовывали из EtOH и получали белое твердое вещество. Т.пл. 186-188oС. Соединение 128.
Анализ для C14H22N4O - 2С2Н2О4 (С, Н, N);
Вычислено: С 45,57; Н 5,52; N 11,81;
Пример 72
3-(3-(3-(5-Метил-2-тиенил)-1-пропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат
К раствору 3-(5-метил-2-тиенил)-1-пропанола (4,0 г, 25,5 мМ) в тетрагидрофуране (40 мл) добавляли гидрид натрия (10,2 мМ). Полученную смесь перемешивали в течение одного часа при комнатной температуре, а затем к этой реакционной смеси по капле добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (1,0 г, 5,1 мМ) в тетрагидрофуране (10 мл). После перемешивали в течение ночи при комнатной температуре реакцию гасили водой и экстрагировали диэтиловым эфиром. Органическую фазу осушали смесью NaCl/Na2SO4, а затем выпаривали и получали неочищенный 3-(3-(5-метил-2-тиенил)пропокси-1,2,5-тиадиазол-4-ил)пиридин. Раствор, содержащий 3-(3-(5-метил-2-тиенил)пропокси-1,2,5-тиадиазол-4-ил)пиридин (1,0 г, 3,2 мМ) и иодометан (2,3 г, 16,0 мМ) в 60 мл ацетона, нагревали с обратным холодильником в течение ночи. После выпаривания раствора получали 1,5 г кватернизованного продукта. К этому кватернизованному продукту (1,5 г) в этаноле (30 мл) осторожно добавляли борогидрид натрия (0,6 г, 16,0 мМ). Затем реакционную смесь выпаривали и полученный остаток растворяли в воде и экстрагировали метиленхлоридом (3•100 мл). Органическую фазу осушали смесью NaCl/Na2SO4 и выпаривали. После этого остаток очищали с помощью радиальной хроматографии, используя в качестве элюента смесь 0,5% NH4OH и 5,0% EtOH в CHCl3. В результате этой процедуры получали целевое соединение в виде соли щавелевой кислоты с выходом 337 мг (Т.пл. 134-137oС. Соединение 129).
Способом, описанным выше, и с использованием вместо 3-(5-метил-2-тиенил)-1-пропанола указанного спирта, были получены следующие соединения:
3-(3-((5-Пропил-2-тиенил)метокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. (Соединение 130) из (5-пропил-2-тиенил)-метанола. Т. пл. 134-135oС.
3-(3-(3-(5-Пентил-2-тиенил)-1-пропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. (Соединение 131) из 3-(5-пентил -2-тиенил)-1-пропанола. Т. пл. 138-140oС.
3-(3-(3-(2-Тиенилтио)-1-пропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. (Соединение 132) из 3-(2-тиенилтио)-1-пропанола. Т. пл. 102-110oС.
Пример 73
3-(3-(3-(2-Тиенил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
Раствор 3-(3-хлоро-1,2,5-тиадиазол-4-ил)пиридина (2,0 г, 10,1 мМ) в ДМФ (10 мл) охлаждали до 5oС, а затем добавляли карбонат калия (2,8 г, 30,2 мМ) и моногидрат бисульфида натрия (1,5 г, 20,2 мМ). После перемешивания в течение 1 часа к реакционной смеси добавляли карбонат калия (1,4 г, 10,1 мМ) и раствор 3-(2-тиенил)-1-хлоро-пропана (1,8 г, 11,2 мМ) в ДМФ (5 мл) и эту смесь перемешивали в течение 1 часа при комнатной температуре. Затем реакцию гасили водой и экстрагировали метиленхлоридом (3•75 мл). Органическую фазу осушали смесью NaCl/Na2SO4, а затем выпаривали. остаток очищали с помощью флеш-хроматографии, используя в качестве элюента смесь этилацетата/гексана (1: 1), в результате чего получали 1,0 г 3-(3-(3-(2-тиенил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)пиридина. Кватернизацию и восстановление осуществляли способом, описанным в Примере 72. (Соединение 133; т.пл. 98-100oС).
Способом, описанным выше, и с использованием указанного алкилгалогенида получали следующие соединения:
3-(3-(2-Тиенилметилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 134) с использованием (2-тиенил)-хлорметана. Т.пл. 131-135oС.
3-(3-(3-(2-Оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 135) с использованием 3-(2-оксазолидинон-3-ил)-1-хлорпропана. Т.пл. 104-109oС.
3-(3-(3-(2-Тиазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 136) с использованием 3-(2-тиазолидинон-3-ил)-1-хлорпропана. Т.пл. 75-81oС.
3-(3-(5-Пентил-2-тиенил)метилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 137) с использованием (5-пентил-2-тиенил) 1-хлорметана. Т.пл. 143-146oС.
(R)-(+)3-(3-(3-(4-Бензил-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 138) с использованием (R)- 3-(4-бензил-2-оксазолидинон)-1-хлорпропана. Т.пл. 124-133oС.
(S)-(-) 3-(3-(3-(4-Бензил-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 139) с использованием (S)- 3-(4-бензил-2-оксазолидинон-3-ил)-1-хлорпропана. Т.пл. 132-135oС.
(4R, 5S)3-(3-(3-(4-Метил-5-фенил-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 140) с использованием (4R,5S)- 3-(4-метил-5-фенил-2-оксазолидинон-3 ил)-1-хлорпропана. Т.пл. 102-106oС.
(S)-3-(3-(3-(4-Изопропил-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 141) с использованием (S)- 3-(4-изопропил -2-оксазолидинон-3 ил)-1-хлорпропана. Т. пл. 75-79oС.
(S)-3-(3-(3-(3-(4-Этил-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 142) с использованием (S)- 3-(4-этил-2-оксазолидинон-3-ил)-1-хлорпропана. Т. пл. 69-71oС.
(S)-3-(3-(3-(3-(4-(2-Бутил)-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 143) с использованием (S)-3-(4-(2-бутил)-2-оксазолидинон-3 ил)-1-хлорпропана. Т. пл. 77-80oС.
3-(3-(3-(4-Пропил-2-оксазолидинон-3-ил)-1-пропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат (Соединение 144) с использованием 3-(4-пропил -2-оксазолидинон-3 ил)-1-хлорпропана. Т.пл. 65-68oС.
Пример 74
А. 4-Метил-1-(феноксикарбонил)-1,4-дигидропирин
Раствор иодида меди (I) (0,28 г, 1,5 мМ) и диметилсульфида (8 мл) в 30 мл безводного ТГФ, находящийся в сухой 500-миллиметровой трехгорлой колбе в атмосфере азота, размешивали 10 минут при комнатной температуре. Затем к реакционной смеси добавляли пиридин (2,43 мл, 30 мМ) в 120 мл безводного ТГФ и охлаждали до -25oС. После этого через капельную воронку добавляли фенилхлороформат 93,9 мл, 30 мМ) в 10 мл безводного ТГФ (сразу после добавления образовывался густой коричневый осадок). Полученную смесь размешивали в течение 15 минут. Затем шприцем к смеси добавляли хлорид метилмагния (10 мл, 30 мМ), после чего коричневой осадок растворялся. Реакционную смесь размешивали 20 минут при -25oС, а затем 20 минут при комнатной температуре. После этого к реакционной смеси добавляли 20% NH4Cl(вод) (70 мл). Полученную смесь экстрагировали 150 миллилитрами диэтилового эфира. Затем органический экстракт промывали 40-миллилитровыми порциями 20% NH4Cl(вод)/NH4OH (1:1), воды, 10% HCl(вод), воды и соляного раствора. Органический слой осушали NaCl/Na2SO4, фильтровали и концентрировали, в результате чего получали 5,9 г желтого маслообразного продукта. После дистилляции с использованием прибора Кюгельрора (т. пл. 150-170oС, 21 мм рт.ст.) получали 439 г (77%) целевого соединения (А).
В. 3-Формил-4-метил-1-(феноксикарбонил)-1,4-дигидропиридин
ДМФ (7,44 мл, 97 мМ) в 10 мл дихлорметана помещали в сухую 50-миллиметровую колбу в атмосфере азота и охлаждали до 0oС. Затем к раствору медленно добавляли оксихлорид фосфора (4,5 мл, 48 мМ). Полученный раствор размешивали в течение 30 минут при комнатной температуре. Соединение (А) (4,7 г, 22 мМ) в 40 мл дихлорометана размешивали в 100-миллилитровой двухгорлой колбе в атмосфере азота при 0oС. Раствор диметилфорамина/оксихлорида фосфора переносили в капельную воронку через канюлю, а затем медленно добавляли в раствор соединения (А)/дихлорометана. После этого ледяную баню удаляли и реакционную смесь перемешивали в течение 20 часов при комнатной температуре. Затем реакционную смесь охлаждали до 0oС, после чего через капельную воронку осторожно добавляли раствор ацетата калия (16 г) в 50 мл воды. Полученную смесь нагревали с обратным холодильником в течение 20 минут. Затем метиленхлоридный слой отделяли и еще раз экстрагировали 100 мл метиленхлорида. Органические фазы объединяли и промывали 40-миллилитровыми порциями воды, К2СО3(вод), воды и соляного раствора, а затем осушали NaCl/Na2SO4. Органические продукты концентрировали в роторном испарителе, в результате чего получали 4 г коричневого маслообразного продукта. После флеш-хроматографии на силикагеле (элюент: этилацетат/гексил) получали 2,0 г (37%) целевого соединения (В).
С. 4-Метил-3-пиридинкарбоксальдегид
Метанол (85 мл), триэтиламин (1,4 г) и соединение (В) (0,5 г, 20,6 мМ) помещали в 250-миллиметровую колбу в атмосферу азота. Раствор нагревали с обратным холодильником в течение 3 часов. Затем реакционную смесь концентрировали и в колбу добавляли 5% Рd/C (0,5 г) и толуол (85 мл). Полученную смесь нагревали с обратным холодильником в течение 2 часов, а затем охлаждали до комнатной температуры. После этого 5% Рd/С удаляли путем фильтрации и фильтрат концентрировали.
Полученный маслообразный продукт очищали с помощью флеш-хроматографии на силикагеле, элюируя этилацетатом/гексаном. Выход соединения (С) составлял 1,3 г (47%).
D. Альфа-амино-альфа(3-(4-метилпиридил)ацетонитрил
В 250-миллиметровой колбе в атмосфере азота растворяли цианид калия (7,3 мл, 112,6 мМ) и хлорид аммония (6,0 г, 112,6 мМ) в воде (150 мл). Затем к реакционной смеси добавляли соединение (С) (10,9 г, 90,1 мМ) и полученную смесь размешивали в течение ночи при комнатной температуре. Реакционную смесь экстрагировали этилацетатом (3•300 мл). Органические экстракты объединяли, осушали NaCl/Na2SO4, а затем концентрировали, в результате чего получали 11 г коричневого маслообразного продукта (D). Этот продукт использовали непосредственно в следующей стадии.
E. 3-(3-Хлоро-1,2,5-тиадиазол-4-ил)-4-метилпиридин
Монохлорид серы (73,5 мМ, 5,9 мл) в ДМФ (90 мл) помещали в 250-миллиметровую колбу в атмосферу азота, а затем охлаждали до -25oС. К реакционной смеси через капельную воронку добавляли соединение (D) (3,6 г, 24,5 мМ) в ДМФ (10 мл). После этого смесь оставляли на ночь для размешивания. После нагревали до комнатной температуры, к реакционной смеси добавляли воду (30 мл) и диэтиловый эфир (60 мл), затем эфирный слой отделяли и отбрасывали. После этого реакцию подщелачивали путем добавления 50%-ного NaOH (вод), а затем экстрагировали диэтиловым эфиром (4•90 мл). Органические экстракты объединяли, осушали NaCl/Na2SO4 и концентрировали, в результате чего получали коричневый маслообразный продукт. Этот продукт очищали с помощью флеш-хроматографии на 100 г силикагеля с использованием в качестве элюента 0,05% Na4OH/0, 5% этанол в хлороформе. Выход соединения (Е) составил 2 г (38%).
F. 3-(3-Метокси -1,2,5-тиадиазол-4-ил)-4-метилпиридин
Раствор натрия (0,32 г, 14 мМ) в метаноле (10 мл) получали в 25-миллиметровой колбе в атмосфере азота. Затем к реакционной смеси добавляли соединение (Е) (0,6 г, 2,8 мМ) и полученную смесь нагревали при 50oС в течение 3 часов, после чего смесь размешивали в течение ночи при комнатной температуре. Полученный после концентрирования в роторном испарителе твердый остаток растворяли в 1 н. HCl(вод) и промывали диэтиловым эфиром. Водный слой подщелачивали 5 н. NaOH (вод.), а затем экстрагировали метиленхлоридом (4•50 мл). объединенные органические экстракты осушали NaCl/Na2SO4, концентрировали, и получали 344 мг маслообразного соединения (F) (60%).
G. 3-(3-Метокси-1,2,5-тиадиазол-4-ил)-4-метилпиридиния иодид
Смесь соединения (F) (335 мг, 1,6 мМ), иодометана (1,14 г, 8,0 мМ) и ацетона (100 мМ) размешивали в 250-миллиметровой колбе в присутствии азота при комнатной температуре в течение ночи. После концентрирования реакционной смеси в роторном испарителе получали 500 мг соединения (G) в виде твердого желтого продукта. Этот продукт использовали непосредственно в следующей стадии.
Н. 1,2,5,6-Тетрагидро-3-(3-метокси-1,2,5-тиадиазол-4-ил)-1,4-диметилпиридина фумарат
К раствору соединения (G) (1,6 мМ) и этанола (15 мл) в 50-миллиметровой колбе в присутствии азота добавляли борогидрид натрия (300 мг, 8,0 мМ). Полученную реакционную смесь размешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали в роторном испарителе. Твердый остаток растворяли в 1 н HCl(вод) (75 мл), а затем промывали диэтиловым эфиром. Водный слой подщелачивали и экстрагировали метиленхлоридом (4•75 мл). Объединенные органические экстракты осушали NaCl/Na2SO4 и концентрировали, в результате чего получали маслообразный продукт, который очищали с помощью флеш-хроматографии (силикагель: элюент: NH4OH/этанол в хлороформе). выход составил 91 г. Продукт выделяли в виде соли фумаровой кислоты (130,4 мг). Т. пл. 99-105oС.
Элементный анализ С14Н19N3О5S.
Вычислено: С 49,26; Н 5,61; N 12,31.
Найдено: С 49,11; Н 5,53; N 12,03, Соединение 145.
Пример 75
Способом, описанным в Примере 74 (F-H), с использованием вместо метанола гексанола, было получено следующее соединение:
3-(3-Гексилокси -1,2,5- тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,4-диметилпиридина оксалат,Т.пл. 109-111oС.
Элементный анализ для С17Н27N3О5S.
Вычислено: С 52,97; Н 7,06; N 10,70.
Найдено: С 53,17; Н 6,88; N 10,88. Соединение 146.
Пример 76
А. Альфа-амино-альфа-(6-метил-3-пиридиния)ацетонитрил
К раствору цианида калия (6,96 г, 107 мМ) и хлорида аммония (5,72 г, 107 мМ) в воде (5 мл) добавляли 6-метил-3-пиридинкарбоксальдегид (8,68 г, 71,5 мМ) и реакционную смесь размешивали в течение 18 часов при комнатной температуре. Затем смесь подщелачивали 50%-ным NaOH и экстрагировали этилацетатом. Органическую фазу осушали сульфатом магния и выпаривали, в результате чего получали неочищенный целевой продукт с выходом 7 г. Этот продукт использовали без последующей очистки.
В. 3-(3-Хлоро-1,2,5-тиадиазол-4-ил)-6-метилпиридин
К раствору альфа-амино-альфа-(6-метил-3-пиридиния) ацетонитрила (7 г, 47 мМ) при комнатной температуре медленно добавляли раствор монохлорида серы (11,7 мл, 142 мМ) в ДМФ (50 мл). Реакционную смесь размешивали в течение 18 часов, а затем подщелачивали 50%-ным NaOH и экстрагировали эфиром. Эфирные фазы осушали сульфатом магния и выпаривали. Остаток очищали с помощью колоночной хроматографии (элюент: EtOAc/CH2Cl2 (1: 1)) и получали целевой продукт с выходом 5,30 г (54%).
С. 3-(3-Гексилтио -1,2,5-тиадиазол-4-ил)-6-метилпиридин
Моногидрат бисульфида натрия (0,33 г, 4,4 мМ) добавляли к раствору 3-(3-хлоро-1,2,5-тиадиазол-4-ил)-6-метилпиридин (0,85 г, 4 мМ) в ДМФ (20 мл) при комнатной температуре и реакционную смесь размешивали в течение 1 часа. Затем добавляли карбонат калия (1,65 г, 12 мМ) и 1-гексилбромид (0,99 г, 6 мМ) и реакционную смесь размешивали еще 24 часа. После этого добавляли 1 н. HCl и реакционную смесь один раз экстрагировали эфиром. Водную фазу подщелачивали 50%-ным NaOH и экстрагировали эфиром. Эфирные фазы осушали и выпаривали, в результате чего получали неочищенное целевое соединение.
D. 3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1,6-диметилпиридиния иодид
К раствору 3-(3-гексилтио-1,2,5-тиадиазол-4-ил)-6-метилпиридина (4 мМ) в ацетоне (5 мл) добавляли метилиодид (1 мл, 15 мМ) и полученную реакционную смесь размешивали в течение 20 часов при комнатной температуре. После выпаривания реакционной смеси получали неочищенный продукт, который использовали без последующей очистки.
Е. 3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридиния иодид
К раствору 3-(3-Гексилтио-1,2,5-тиадиазол-4-ил)-1,6-диметилпиридиния иодида (4 мМ) в этаноле (99,9%, 20 мл) при -10oС в атмосфере азота добавляли борогидрид натрия (380 мг, 10 мМ). Полученную реакционную смесь размешивали в течение 1 часа при -10oС. После выпаривания остаток растворяли в воде и экстрагировали этилацетатом. Осушенные органические фазы выпаривали, а остаток очищали с помощью колоночной хроматографии (элюент: EtOAc: MeOH (4: 1)). После кристаллизации из ацетона получали целевое соединение в виде соли щавелевой кислоты. Затем соединение перекристаллизовывали из ацетона и получали целевой продукт с выходом 700 мг. Т. пл. 127-128oС. (Соединение 147).
Пример 77.
Способом, аналогичным описанному в Примере 6 (С-Е), с использованием 1 -гексилбромид алкилбромида, получали следующие соединения:
3-(3-Пентилтио-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 112-113oС. (Соединение 148).
3-(3-(4-Цианобензилтио)-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 74-76oС. (Соединение 149).
3-(3-(4-Цианобутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 99-101oС. (Соединение 150).
3-(3-Бутилтио-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 119-120oС. (Соединение 151).
3-(3-Этилтио-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 154-155oС. (Соединение 152).
3-(3-Пентилтио-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 111-113oС. (Соединение 153).
3-(3-(3-Фенилпропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5-6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 125-126oС. (Соединение 154).
Пример 78
3-(3-Гексилокси-1,2,5-тиадиазол-4-ил)-6-метилпиридин.
Гидрид натрия (0,72 г, 15 мМ) растворяли в безводном ТГФ (20 мл) к 1-гексаноле (1,53 г, 15 мМ) и добавляли раствор 3-(3-хлоро-1,2,5-тиадиазол -4-ил)-6-метилпиридина (1,06 г, 5 мМ) в безводном ТГФ (15 мл). Полученную реакционную смесь размешивали в течение 2 часов. После добавления воды смесь экстрагировали эфиром и эфирную фазу осушали и выпаривали. Остаток, состоящий из неочищенного целевого соединения, использовали без последующей очистки.
В. 3-(3-Гексилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридина оксалат
Т. пл. 99-100oС (Соединение 155). Это соединение получали способом, описанным в Примере 76 (D-E).
Пример 79
Способом, описанным в Примере 78, с использованием соответствующего спирта вместо 1-гексанола получали следующие соединения:
3-(3-Пентилокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 122-123oС. (Соединение 156).
3-(3-Бутокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 133-134oС. (Соединение 157).
3-(3-(4-Пентенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 133-134oС. (Соединение 158).
3-(3-(3-Гексенилокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 126-128oС. (Соединение 159).
3-(3-Этокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1,6-диметилпиридина оксалат. Т.пл. 128-129oС. (Соединение 160).
Пример 80
3-(3-(3-Карбоксипропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин.
Раствор гидрохлорида 3-(3-(3-карбоксипропилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин (0,70 г, 2 мМ) в концентрированной соляной кислоте (10 мл) нагревали с обратным холодильником в течение 6 часов. Реакционную смесь выпаривали при пониженном давлении. Остаток растворяли в воде и нейтрализовали раствором гидроксида натрия, в результате чего получали целевое соединение с выходом 80%. Т.пл. 99-101oС. Соединение 258.
Точно таким же способом получали следующие соединения:
3-(3-(3-Карбоксипропокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин. Т.пл. 113-116oС. Соединение 259.
3-(3-(3-Карбоксипентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин. Т.пл. 110-120oС. Соединение 260.
Пример 81
3-(3-(3-Меркаптопентилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат.
К раствору 3-(3-(5-хлорпентилтио)- 1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина (0,31 г, 1 мМ) в диметилформамиде (5 мл) добавляли бисульфид натрия (0,35 г, 5 мМ) и полученную смесь перемешивали в течение 48 часов при комнатной температуре. После добавления воды свободное основание экстрагировали эфиром. Свободное основание кристаллизовали из ацетона в виде соли щавелевой кислоты. Выход: 50%. Т.пл. 106-107oС. Соединение 261.
Точно таким же способом были получены следующие соединения:
3-(3-(6-Меркаптогексилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 105-106oС. Соединение 262.
3-(3-(4-Меркаптобутилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридина оксалат. Т.пл. 142-144oС. Соединение 263.
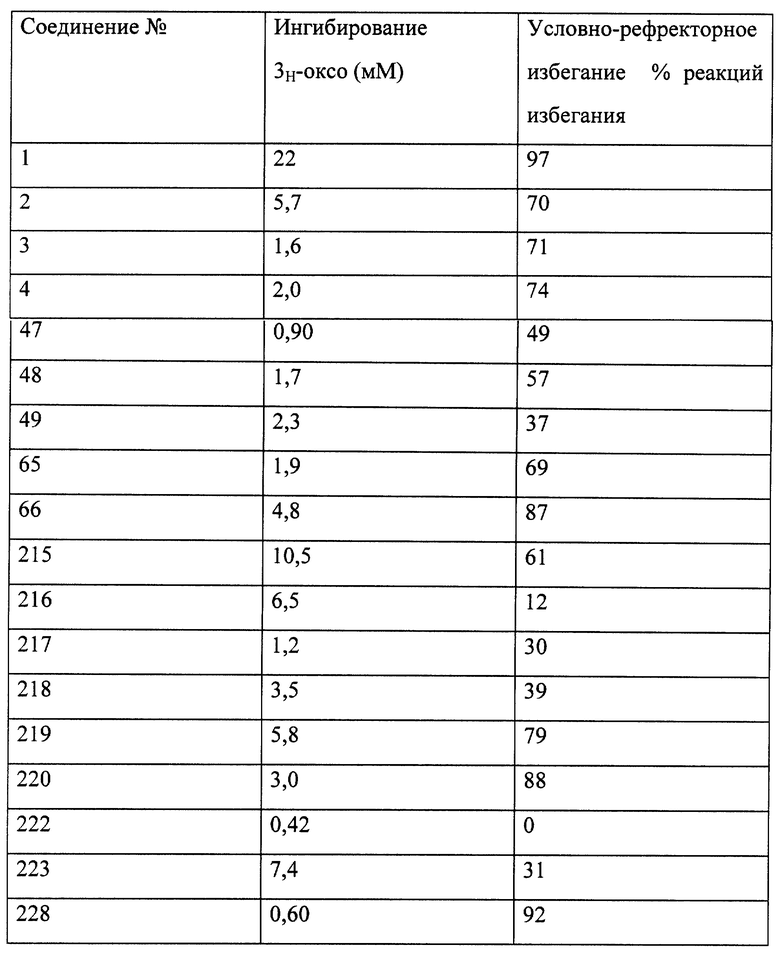
Изобретение относится к новому способу лечения психотических расстройств путем введения млекопитающему, нуждающемуся в этом, эффективного количества соединения формулы I, где Z1 - сера, Z2 - кислород или сера; R - водород или группа Z2 - R2; R1 - водород или С1-С5 алкил; R2 - С1-С15 алкил, R5, R6 - водород. 1 з.п.ф-лы, 1 табл.


где Z1 - сера;
R - водород или группа Z2 - R2, где Z2 - кислород или сера;
R2 - прямой или разветвленный С1-С15 алкил, необязательно замещенный галогеном(ами), -CF3 или тиенилтио;
R1 - водород или прямой или разветвленный С1-С5 алкил;
R5 и R6 - водород.
1,2,5,6-тетрагидро-3-(3-метокси-1,2,5-тиадиазол-4-ил)-1-метилпиридин,
3-(3-этокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
1,2,5,6-тетрагидро-1-метил-3-(3-пропокси-1,2,5-тиадиазол-4-ил)пиридин,
3-(3-бутокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
3-(3-пропилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
3-(3-бутилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
3-(3-метилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
3-(3-(этилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
3-(3-пентилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин,
3-(3-этокси-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-этилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-пропилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-бутилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-пентилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-гексилтио-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-(2,2,2-трифторэтилтио)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-(2,2,2-трифторэтокси)-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидропиридин,
3-(3-(2-(2-тиенилтио)этилтио))-1,2,5-тиадиазол-4-ил)-1,2,5,6-тетрагидро-1-метилпиридин.
| ЕР 0591027 А1 (SYNTHELABO), 06.04.1994 | |||
| ЕР 0591026 А1 (SYNTHELABO), 06.04.1994 | |||
| WO 9203430 А1 (NOVO NORDISK А/S), 05.03.1992 | |||
| Способ получения производных 1-(4-арилциклогексил)пиперидина или их фармацевтически пригодных солей или их стереоизомерных форм | 1981 |
|
SU1095878A3 |
Авторы
Даты
2002-10-27—Публикация
1994-08-15—Подача