Изобретение относится к материалам с эффектом памяти формы (ЭПФ) с модифицированной поверхностью, которые могут быть использованы в качестве имплантатов в медицине, в качестве элементов и изделий, работающих в агрессивных средах и т.д.
Известен сплав с памятью формы из никелида титана для медицинского применения [1] . Однако поверхность такого сплава содержит тонкий слой из оксидов титана (3-10 нм), который не может предотвратить диффузию ионов никеля в раствор. Наличие в поверхностном слое не связанного кислородом титана также приводит к переходу ионов титана в раствор. Таким образом, коррозионная стойкость такого сплава низкая.
Известен сплав с памятью формы для медицинского применения из никелида титана с модифицированной поверхностью [2]. Поверхность такого сплава содержит нитрид титана TiN или карбонитрид титана TiNC. Коррозионная стойкость такого сплава высокая. Недостатком этого сплава является то, что при проявлении ЭПФ нитрид титана отслаивается, TiNC - растрескивается и коррозионная стойкость резко понижается.
Наиболее близким по технической сущности и достигаемому результату к предлагаемому изобретению является сплав с эффектом памяти формы Ti - 50 ат. % Ni с модифицированной методом имплантации ионов азота поверхностью [3]. Имплантация проводилась на источнике ионов "Титан" при ускоряющем напряжении 60-80 кВ; токе - 0,2 А; длительность импульса - 400 мкс; частота - 50 Гц; доза облучения - 1016 ион•см-2. Коррозионная стойкость такого сплава высокая, однако после деформации сплава коррозионная стойкость резко понижается в результате отслоения поверхностного слоя TiN.
Необходимость использования сплавов на основе никелида титана как имплантатов обусловлена не только их функциональными возможностями, но и хорошими биомеханическими свойствами. Сверхэластичное (резиноподобное) поведение TiNi в изотермических условиях, в том числе при температуре человеческого организма, соответствует обратимой деформации, происходящей в живых тканях организма при нагрузках и разгрузках [4]. Способность никелида титана к пассивации в различных растворах с образованием на его поверхности пленки из оксидов титана делает его достаточно коррозионно-стойким. По коррозионной стойкости никелид титана приближается к титановым сплавам [4], которые широко применяются в качестве имплантатов. Однако при функциональной работе элемента с ЭПФ в результате образования на поверхности рельефа, обусловленного зарождением (или исчезновением) мартенсита, защитный слой оксидов титана разрушается, и коррозионная стойкость резко понижается. Наличие в TiNi никеля, который оказывает на организм токсическое действие [4-6] и диффундирует из материала в раствор, также сдерживает широкое использование сплавов на основе никелида титана в качестве имплантатов. Поэтому актуальной задачей является создание материала с ЭПФ и сверхэластичностью на основе TiNi, который был бы биосовместим, обладал бы высокой коррозионной стойкостью в условиях воздействия переменных нагрузок.
Указанный технический результат достигается тем, что материал на основе никелида титана с ЭПФ с поверхностным слоем, модифицированным путем ионной имплантации легирующими элементами, в качестве которых выбраны кислород, углерод, титан и/или цирконий, имеет глубину модифицированного слоя 50-300 нм, а состав модифицированного слоя имеет следующее соотношение элементов, ат.%:
Кислород - 25-75
Углерод - 5-10
Титан и/или цирконий - 20-50
Никель - 0-20
Кроме того, в качестве основы выбран никелид титана следующего состава, ат.%:
Никель - 49-51
Титан - Остальное
Материал с такими элементами и при данной их концентрации в модифицированном слое имеет высокую коррозионную стойкость как в исходном состоянии, так и после многократных циклов деформирования в режиме нагрузка - разгрузка, а также низкую растворимость ионов никеля в агрессивных средах.
Указанные свойства достигаются тем, что имплантация ионов титана и/или циркония, кислорода и углерода создает в поверхностном слое никелида титана зону с высоким содержанием оксидов и карбидов титана и/или циркония с высокими адгезионными свойствами по отношению к матрице никелида титана. При термоциклировании или после деформации в изотермических условиях обратимое образование и исчезновение мартенситных пластин не приводит к разрушению оксидокарбидного слоя титана и/или циркония и это предопределяет высокую коррозионную стойкость данного материала в условиях циклических нагрузок.
Выбор в качестве элементов для имплантации титана и/или циркония определяется тем, что матрица также содержит титан и элементы - аналоги по электронной структуре Ti и Zr не приводят к выделению каких-либо вторичных фаз. Второй особенностью выбора Ti и Zr в качестве имплантируемых элементов является то, что эти элементы легко пассивируются с образованием оксидов, биосовместимых с человеческим организмом.
Выбор в качестве элементов для имплантации кислорода и углерода обусловлен тем, что эти элементы участвуют в образовании оксидов и карбидов титана и/или циркония в поверхностном слое, которые обладают хорошей адгезией с матрицей и высокой коррозионной стойкостью.
Изобретение осуществляется следующим образом.
Материал с ЭПФ с модифицированной поверхностью готовили поэтапно. Никелид титана состава Ti - 50,5 ат.%Ni выплавляли шестикратным электродуговым переплавом в атмосфере аргона из компонентов: титан - иодидный, никель марки НО. После плавки слиток прокатывали в пластину с промежуточными отжигами, электролитически очищали поверхность и готовили образцы для имплантации размером 50•20•1 мм3. Выбор высокодозовой ионной имплантации для модификации поверхности обусловлен тем, что в результате ионной имплантации образуется поверхностный слой с измененным составом, не обладающий выраженной поверхностью раздела, характерной для осажденного слоя. Ионная обработка поверхности выполнена с помощью вакуумно-дугового частотно-импульсного источника "Диана-2". Ионы титана и/или циркония, кислорода и углерода имплангировались при ускоряющем напряжении 70 кВ с частотой импульсов 50 Гц. Расчетные дозы облучения варьировались от 1016 до 6•1017 ион•см-2.
Элементный состав поверхностных слоев определяли методом ОЖЕ-спектроскопии. Удаление верхних слоев проводили бомбардировкой поверхности образца ионами аргона.
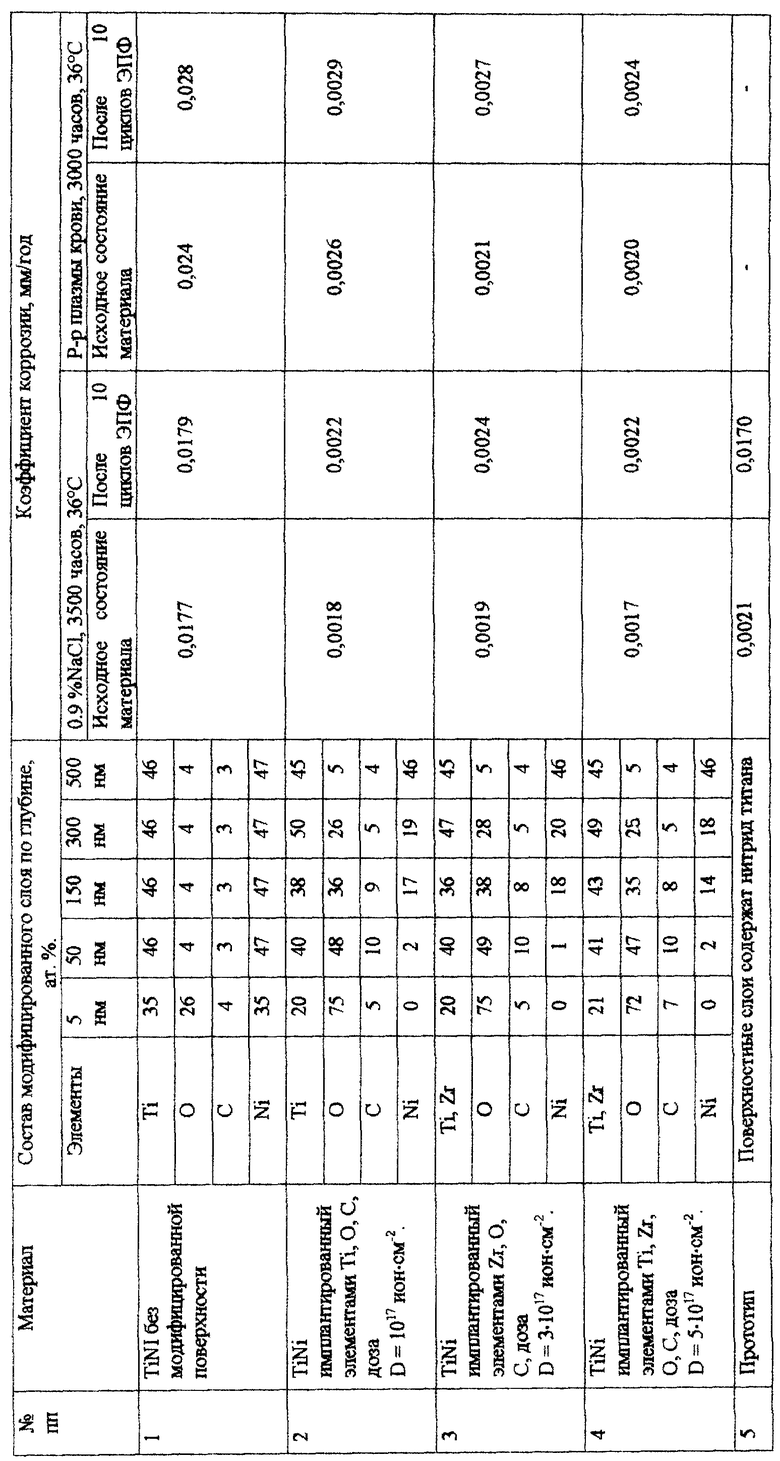
Испытания на коррозионную стойкость проводили в физиологическом растворе 0,9% NaCl, а также в солевом растворе плазмы крови состава: дистиллированая вода - 1 л, NaCl - 9 г, КСl - 0,42 г, CaCl2 - 0,21 г, NaHCO3 - 2 т, глюкоза - 2 г. Длительность нахождения образцов в растворах варьировалась от 1 ч до 6000 ч. Скорость коррозии определяли по изменению массы образцов после заданного времени их пребывания в растворах. Взвешивание проводили на аналитических весах. Показатель коррозии для исследованных образцов приведен в таблице. Из таблицы видно, что коррозионная стойкость образцов с модифицированной поверхностью высокая. Столь же высокой коррозионная стойкость остается в образцах подвергнутых десятикратному термоциклированию через интервал мартенситного превращения, в то время как в сплаве-прототипе, подвергнутому аналогичной процедуре, коррозионная стойкость снизилась на порядок.
Наряду с измерением коррозионной стойкости в предлагаемом материале проводили измерение содержания никеля в биохимических растворах. Содержание никеля в физиологическом растворе 0,9% NaCl и солевом растворе плазмы крови определяли фотометрическим методом. Исследования выполнены на двухлучевом спектрофотометре Kontron instruments Uvikon 943. Получено, что содержание никеля в физиологическом растворе 0,9% NaCl после 4000 ч выдержки составляет СNi= 0,25 мг/л, в растворе плазмы крови после 3000 ч выдержки СNi=0,04 мг/л. В образцах TiNi без модифицированной поверхности после аналогичных испытаний содержание никеля составляет более 0,5 мг/л в растворе 0,9% NaCl и СNi=0,06 мг/л в растворе плазмы крови. Таким образом, наряду с повышением коррозионной стойкости предлагаемого материала с модифицированной поверхностью в условиях циклических нагружений, предлагаемый материал обладает низкой растворимостью никеля в биохимические растворы.
Источники информации
1. Патент 0145166. Медицинские устройства, включающие сплавы с памятью формы. Опубл. 13.12.89, заявл. 12.10.84, МКИ A 61 F 5/00, A 61 F 2/00, A 61 L 27/00, B 22 F 3/00; приоритет: 14.10.83 US 541852.
2. Kimura U. , Sohmura Т. Surface coating on TiNi-shape memory implant alloys// J. Osacka Univ. Dent. Sch. - 1987, 27 (dec.), p. 211-223.
3. Налесник О.И., Ясенчук Ю.Ф., Мазуркина Н.А., Итин В.И., Гюнтер В.Э. Влияние электрополировки и ионной имплантации азота в поверхность на электрохимическое поведение титана и никелида титана в растворе NaCl // Имплантаты с памятью формы. - 1992, 4, с. 53-58.
4. Эффекты памяти формы и их применение в медицине. Под ред. А.А.Монасевича. - Новосибирск: Наука. Сиб. отделение, 1992, 742 с.
5. Chemical and electrochemichal aspects of biocompatibility of titanium and its alloys. P.Kovacs, G.A.Davidson: Medical Appl. Of Titanium and its Alloys. The Material and Biological Issues. ASTM STP 1272, S.A.Braun and J. E.Lemons Eds., American Society for Testing and Materials, 1996, p. 167-178.
6. H. Oonishi, Proc. Sec. World Congress on Biomaterials, Washington, 1984, p. 183.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ КАРДИОИМПЛАНТАТА ИЗ СПЛАВА НА ОСНОВЕ НИКЕЛИДА ТИТАНА С МОДИФИЦИРОВАННЫМ ИОННО-ПЛАЗМЕННОЙ ОБРАБОТКОЙ ПОВЕРХНОСТНЫМ СЛОЕМ | 2013 |
|
RU2508130C1 |
| ДЕНТАЛЬНЫЙ ВНУТРИКОСТНЫЙ ИМПЛАНТАТ И МАТЕРИАЛ С ЭФФЕКТОМ ПАМЯТИ ФОРМЫ ДЛЯ ЕГО ИЗГОТОВЛЕНИЯ | 2008 |
|
RU2397732C2 |
| МАТЕРИАЛ С ЭФФЕКТОМ ПАМЯТИ ФОРМЫ | 2004 |
|
RU2259415C1 |
| УСТРОЙСТВО ЗОНТИЧНОЕ (ОККЛЮДЕР) С МОДИФИЦИРОВАННЫМ ПОВЕРХНОСТНЫМ СЛОЕМ | 2013 |
|
RU2522932C9 |
| СПЛАВ С ЭФФЕКТОМ ПАМЯТИ ФОРМЫ (ВАРИАНТЫ) | 2003 |
|
RU2251584C2 |
| СПОСОБ ПЛАЗМЕННО-ИММЕРСИОННОЙ ИОННОЙ МОДИФИКАЦИИ ПОВЕРХНОСТИ ИЗДЕЛИЯ ИЗ СПЛАВА НА ОСНОВЕ НИКЕЛИДА ТИТАНА МЕДИЦИНСКОГО НАЗНАЧЕНИЯ | 2015 |
|
RU2579314C1 |
| МЕТАЛЛОКЕРАМИЧЕСКИЙ БИОИМПЛАНТАТ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ | 1996 |
|
RU2132202C1 |
| СПОСОБ ИОННО-ЛУЧЕВОЙ ОБРАБОТКИ ИЗДЕЛИЙ ИЗ ТВЕРДЫХ СПЛАВОВ | 1997 |
|
RU2155243C2 |
| СПЛАВ С ЭФФЕКТОМ ПАМЯТИ ФОРМЫ | 1996 |
|
RU2100468C1 |
| СПОСОБ ОБРАБОТКИ ДЕТАЛЕЙ И ИНСТРУМЕНТА ИЗ УГЛЕРОДИСТЫХ И ЛЕГИРУЮЩИХ СТАЛЕЙ | 1992 |
|
RU2045582C1 |
Изобретение относится к материалам с памятью формы с модифицированной поверхностью, которые могут быть использованы в качестве имплантатов в медицине, в качестве элементов и изделий, работающих в агрессивных средах и т. д. Материал на основе никелида титана с ЭПФ с поверхностным слоем, модифицированным путем ионной имплантации легирующими элементами, в качестве которых выбраны кислород, углерод, титан и/или цирконий, имеет глубину модифицированного слоя 50-300 нм, а состав модифицированного слоя имеет следующее соотношение элементов, ат.%: кислород 25-75, углерод 5-10, титан и/или цирконий 20-50, никель 0-20. Кроме того, в качестве основы выбран никелид титана следующего состава, ат.%: никель 49-51, титан остальное. Материал с такими элементами и при данной их концентрации в модифицированном слое имеет высокую коррозионную стойкость как в исходном состоянии, так и после многократных циклов деформирования в режиме нагрузка - разгрузка, а также низкую растворимость ионов никеля в агрессивных средах. 2 з.п.ф-лы, 1 табл.
Кислород - 25 - 75
Углерод - 5 - 10
Титан и/или цирконий - 20 - 50
2. Материал по п.1, отличающийся тем, что поверхностный слой дополнительно содержит до 20 ат.% никеля.
Никель - 49 - 51
Титан - Остальноел
| Имплантаты с памятью формы, 1992, № 4, с | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| МОНАСЕВИЧ А.А | |||
| Эффекты памяти формы и их применение в медицине | |||
| - Новосибирск, 1992 | |||
| Способ обработки поверхностных слоев изделий из титана | 1991 |
|
SU1828877A1 |
| JP 3093993, 18.04.1991. | |||
Авторы
Даты
2002-10-27—Публикация
2000-08-18—Подача