Изобретение относится к материалам, используемым в медицине для эндопротезирования.
Известен высокоплотный спеченный диоксид циркония (ЕP 43686/83, С 04 В 35/48, 07.03.81), содержащий стабилизатор, такой как Y2O3, полученный путем низкотемпературного спекания. При этом вязкость разрушения, полученного частично стабилизированного ZrO2, составила порядка 10-16 н/м3/2. Однако такое значение коэффициента вязкости разрушения не достаточно для безопасного функционирования имплантата в организме человека при знакопеременных нагружениях.
Известны высоковязкие спеченные изделия на основе диоксида циркония (JP 56127004, С 04 В 35/48, 35/10 81.08.13) со средним размером кристаллических зерен менее 3 мкм, состоящие из 40-99.5% ZrO2, содержащего стабилизатор, и более 90% суммарного количества тетрагональной и кубической кристаллических фаз с соотношением более 1 : 3, и 0.5-60% Al2О3, и менее 3% неизбежных примесей, однако вязкость разрушения таких керамических изделий мала для их использования в эндопротезировании. Кроме того, рядом исследований доказано неблагоприятное воздействие алюминия на биологические ткани.
Наиболее близким по технической сущности к заявляемому изобретению является имплантат (ЕP 0328041, С 04 В 35/48, A 61 L 27/00, А 61 С 8/00, 89.08.16), представляющий собой спеченное изделие из ZrO2 г с поверхностным слоем из смеси α- трикальцийфосфата и диоксида циркония или гидроксиапатита и диоксида циркония, который сформирован на поверхности изделия. Но, несмотря на хорошую биосовместимость такого материала, он достаточно хрупок и не может противостоять знакопеременным нагружениям, подобно живым тканям.
Сущность предлагаемого изобретения заключается в повышении вязкости разрушения керамического имплантата на основе диоксида циркония, содержащего гидроксиапатит, путем его армирования интерметаллическим соединением никелидом титана в виде измельченной проволоки или частиц порошка, что обеспечит его функционирование в организме при высоких знакопеременных нагрузках.
Для достижения поставленной цели биоимплантат на основе диоксида циркония, стабилизированного 3 моль.% окиси иттрия, содержащий гидроксиапатит дополнительно содержит никелид титана, с содержанием никеля порядка 50.7 ат. %, при следующем соотношении компонентов, вес.%:
Гидроксиапатит - 5 - 7;
Никелид титана - 25 - 30;
Диоксид циркония - остальное,
причем никелид титана введен в виде частиц порошка или измельченной проволоки.
Известно, что керамика на основе диоксида циркония с небольшим содержанием гидроксиапатита имеет неплохие механические характеристики, присущие ZrO2 (стабилизированного 3 моль. % Y2O3), хорошую биологическую совместимость, невысокую температуру спекания и низкое значение коэффициента трения за счет введения гидроксиапатита, однако наряду с этим материал достаточно хрупок и неспособен противостоять знакопеременным нагружениям, подобно костной ткани. Этот аспект не позволяет широко использовать керамические биоимплантаты, отдавая приоритет металлическим материалам, имеющим гораздо меньшую биосовместимость
Повышение вязкости разрушения биосовместимой керамики достигается введением интерметаллического соединения никелида титана в виде частиц порошка или измельченной проволоки. Никелид титана, NiTi, с составом незначительным обогащением никелем, порядка 50,7 ат.%, обладает аномальной эластичностью в результате низкотемпературных мартенситных превращений. Основываясь на этом, введение в керамику никелида титана позволило получить композиционный материал, способный противостоять циклическим нагружениям за счет присущего ему эффекта сверхэластичности. Эффективное использование в материалах для биоимплантации одновременно керамики на основе диоксида циркония, с высокими прочностными свойствами, и никелида титана в сверхэластичном состоянии возможно из-за незначительной разности значений коэффициентов термического расширения основных компонентов, поскольку возникающие в зоне контакта остаточные термические напряжения при охлаждении композиционного материала от температуры получения не велики и не оказывают существенного влияния на прочность металлокерамического биоимплантата.
Увеличение вязкости разрушения биоимплантата можно достигнуть двумя способами армирования диоксидциркониевой керамики. В первом случае в керамику никелид титана вводится в виде частиц порошка. Во втором случае никелид титана находится в керамике в виде измельченной тонкой проволоки с диаметром не менее 40 мкм. Как в первом, так и во втором варианте достигается повышение вязкости разрушения металлокерамического биоимплантата.
Содержание гидроксиапатита от 5 до 7 вес.% связано с тем, что уменьшение его содержания ниже 5 вес.% не позволяет добиться значительного снижения температуры спекания металлокерамического материала и значения коэффициента трения, а увеличение содержания свыше 7 вес. % приводит к охрупчиванию металлокерамики и снижению прочностных свойств.
В свою очередь, содержание никелида титана от 25 до 35 вес.% обусловлено тем, что уменьшение его содержания ниже 25 вес.% не позволяет добиться необходимого увеличения вязкости разрушения металлокерамического материала, а увеличение содержания свыше 35 вес.% уменьшает биосовместимость материала, присущую керамике.
Пример конкретного выполнения.
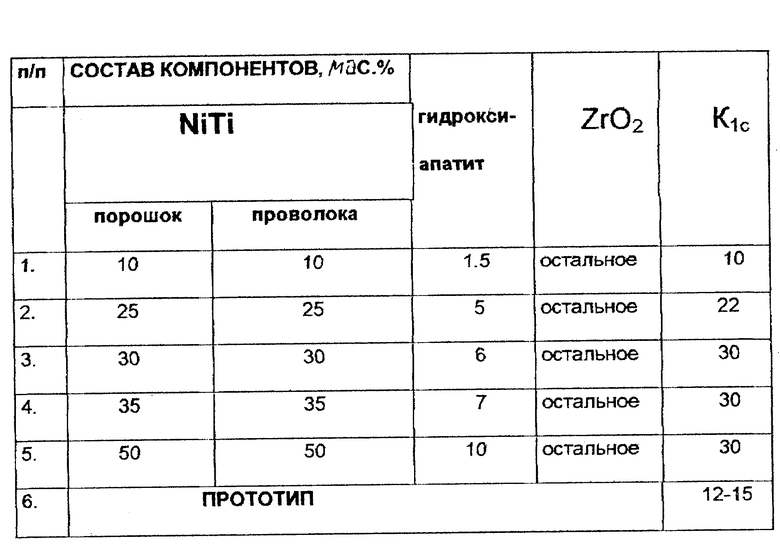
Порошки состава см. табл. смешивали в течение 64 часов. Готовую смесь прессовали на гидравлическом прессе П6324 при давлении от 1 до 1.5 т/см2. В случае использования никелида титана в виде тонкой измельченной проволоки с диаметром не менее 40 мкм ее впрессовывали в порошковую смесь из диоксида циркония и гидроксиапатита.
Прессовки спекали в вакууме (во избежание окисления никелида титана кислородом воздуха) в печи типа СНВ с вольфрамовыми нагревателями при остаточном давлении 5 • 10-5 мм рт.ст. Температура спекания 1200oC, время выдержки 4 часа. Вязкость разрушения измеряли методом индентирования полированной поверхности образцов пирамидкой Виккерса и рассчитывали по формуле
K1c= 0,035(H•a1/2)(E⊘/H)0,4(L/a)0,5/H
где E - модуль упругости;
H - твердость по Виккерсу;
⊘ - константа (≈3);
L - длина трещины из угла отпечатка;
а - диагональ отпечатка.
Кроме того, вязкость разрушения изучали на образцах с надрезом шириной 0.15-0.2 мм и глубиной 2.5 мм на испытательной машине "ИНСТРОН".
Полученные значения критического коэффициента интенсивности напряжений K1c, после армирования керамики никелидом титана превосходят вязкость разрушения прототипа примерно в два раза. Данные результатов измерений приведены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| МАТЕРИАЛ НА ОСНОВЕ НИКЕЛИДА ТИТАНА С ЭФФЕКТОМ ПАМЯТИ ФОРМЫ | 2000 |
|
RU2191842C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАЛЬЦИЙФОСФАТНОГО ПОКРЫТИЯ НА ИМПЛАНТАТЕ ИЗ БИОИНЕРТНОГО МАТЕРИАЛА (ВАРИАНТЫ) | 2012 |
|
RU2476243C1 |
| ТВЕРДЫЙ СПЛАВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2165473C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПРОЧНОЙ КЕРАМИКИ | 2004 |
|
RU2286316C2 |
| СПОСОБ ФОРМИРОВАНИЯ БИОАКТИВНОГО ПОКРЫТИЯ НА ИМПЛАНТАТ | 1999 |
|
RU2194536C2 |
| КОМПОЗИЦИОННЫЙ КЕРАМИЧЕСКИЙ МАТЕРИАЛ | 2007 |
|
RU2341494C2 |
| СПЕЧЕННЫЙ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ НА ОСНОВЕ МЕДИ | 1997 |
|
RU2112068C1 |
| ТВЕРДЫЙ СПЛАВ | 1996 |
|
RU2113532C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОЙ ПОРИСТОЙ КЕРАМИКИ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ ДЛЯ ЭНДОПРОТЕЗИРОВАНИЯ | 2020 |
|
RU2741918C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОЙ МАССЫ | 2002 |
|
RU2233816C2 |
Изобретение принадлежит к материалам, используемым в медицине для эндопротезирования. Керамический имплантат на основе диоксида циркония содержит гидроксиапатит и никелид титана при следующем соотношении компонентов, мас. %: гидроксиапатит -5-7, никелид титана -25-35, диоксид циркония - остальное. Никелид титана введен в виде частиц порошка или измельченной проволоки. Биоимплантат обладает повышенной вязкостью разрушения. 1 табл.
Металлокерамический биоимплантат на основе диоксида циркония, стабилизированного 3 мол. % окиси иттрия, содержащий гидроксиапатит, отличающийся тем, что он дополнительно содержит никелид титана с содержанием никеля порядка 50,7 ат.% при следующем соотношении компонентов, мас.%:
Гидроксиапатит - 5 - 7
Никелид титана - 25 - 35
Диоксид циркония - Остальное
причем никелид титана введен в виде частиц порошка или измельченной проволоки.
| ПДТЕНТНО-ТЕлНй':;'^БИБЛИО ТКЛ | 0 |
|
SU328041A1 |
| DE 4210801 А, 1973 | |||
| JP 56127004 А, 1981 | |||
| МНОГОСТАБИЛЬНОЕ УСТРОЙСТВО | 0 |
|
SU339004A1 |
| БИОЛОГИЧЕСКИЙ АКТИВНЫЙ КОМПЛЕКС ДЛЯ ОРГАНОГЕНЕЗА | 1990 |
|
RU2093191C1 |
Авторы
Даты
1999-06-27—Публикация
1996-08-26—Подача