Настоящее изобретение относится к предотвращению или снижению ятрогенной токсичности. В частности, оно относится к снижению токсичности, вызванной лекарственными препаратами на почечном и/или желудочно-кишечном, и/или дыхательном уровне.
Хорошо известно, что токсичность от лекарственных препаратов играет все более и более важную роль в патологии человека. Достаточно обратить внимание на гастропатию, вызванную противовоспалительными лекарственными средствами, которая подразумевает ежегодные затраты в пределах нескольких биллионов долларов для правительства США. Смотри, например, Bloom, B.S. Am. J. Medicine 84 (приложение 2А), 20, 1988, который сообщает, что ежегодные затраты на лечение артрита достигают более чем 12 биллионов долларов, из которых более чем 30% относятся к устранению побочных эффектов, связанных с противовоспалительным/противоартритным фармакологическим лечением.
Подобным образом нефропатия, вызванная антибиотиками, может означать для одного пациента потерю тысяч долларов на покрытие госпитализационных расходов. Смотри, например, Bemdt W.O. и соавт. в "Principles of Pharmacology" Munson P.L. Ed. p. 685, 1995.
Объектом настоящего изобретения являются соединения, способные к снижению токсичности, вызванной не являющимися нитро лекарственными препаратами для желудочно-кишечной и/или почечной, и/или дыхательной систем.
С удивлением и неожиданно обнаружили, что есть вероятность, если используются органические соединения, содержащие -NO группу, или неорганические соединения, содержащие -NO группу, то упомянутые соединения характеризуются как доноры окиси азота NO, то есть когда они контактируют in vitro с клетками сосудистого эндотелия, тромбоцитами и т.д., то после инкубации в течение 5 мин при температуре 37oС способны к выделению NO и активации синтеза цГМФ (циклический гуанозин 3',5'-(водород фосфат)), что определялось специфическими использованными тестами, которые будут описаны подробно в примерах.
Неожиданные и удивительные результаты заявленного изобретения также демонстрируются следующим фактом: комбинирование нитрогрупп по изобретению с лекарственными препаратами, не являющимися нитро, полезно не только для уменьшения токсичности лекарственного препарата, но также устраняет недостатки, связанные с введением нитропроизводных.
Например, нитроглицерин, который давали с эналаприлом крысам, последовательно повторяя подкожное введение дозой 1 мг/кг в день, не вызывал какой-либо толерантности в отличие от чистого нитроглицерина.
Следовательно, комбинирование в настоящем изобретении приводит к так называемой пониженной толерантности при хроническом введении фармацевтических композиций. Это является значительным достижением, так как никакой проблемы не возникает при применении нитрогрупп в течение длительного времени и поддержании одинаковой эффективности нитропрепаратов. Органические соединения, содержащие -N02 функциональные группы, которые могут быть упомянуты в качестве примера, приведены в The Merck Index 11th Ed.- 1989 и получены известными методами, например теми, которые приведены в Merck, приведены здесь в качестве ссылки и являются следующими:
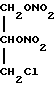
клонитрат (3-хлоро-1,2-пропандиолдинитрат) (Merck No. 2390), имеющий формулу С3Н5СlN2O6 и структурную формулу
эритритилтетранитрат (1,2,3,4 - бутантетролтетранитрат) (Merck No. 3622), имеющий формулу С4Н6N4О12 и структурную формулу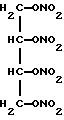
гексанитрат маннита (Merck No. 5630), имеющий формулу C6H8N6O18 и структурную формулу
никорандил ( [2-(нитроокси)этил] -3-пиридин-карбоксамид) (Merck No. 6431), имеющий формулу C8H9N304 и структурную формулу
нитроглицерин (1, 2, 3 - пропантриол тринитрат) (Merck No. 6528), имеющий формулу C3H5N3O9 и структурную формулу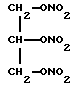
пентаэритритолтетранитрат (2,2-бис [(нитроокси) - метил] -1,3 - пропандиолдинитрат) (Merck No. 7066), имеющий формулу C5H8N4O12 и структурную формулу
пентринитрол (2,2 - бис[(нитроокси)метил] -1,3 - пропандиолмононитрат) (Merck No. 7094), имеющий формулу C5H9N3O10 и структурную формулу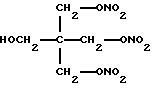
пропатилнитрат (2-этил-2-[(нитроокси)метил] -1,3-пропандаилдинитрат) (Merck No. 7821), имеющий формулу C6H11N3O9 и структурную формулу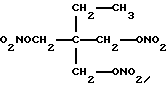
тролнитратфосфат (2,2', 2"- нитрилтрисетанолтринитратфосфат) (соль 1:2) (Merck No. 9682), имеющий формулу С6НN4O17Р2 и формулу структуры
Среди неорганических соединений, содержащих -NO группу, могут быть упомянуты нитроцианиды, такие, например, как:
нитроцианид натрия (пентакис (циано-С)нитросильферрат(2-)динатрий) (Merck No. 8600), имеющий формулу Na2[Fe(CN)5NO].
Другие соединения, содержащие -NO2 функциональную группу, представлены в патентных заявках WO 95/30641; WO 95/09831; WO 94/12463 на имя заявителя и в WO 94/04484 на другое имя. Эти патентные заявки PCT/WO приведены здесь в качестве ссылки как для соединений, так и для способов получения.
Соединения, являющиеся донорами окиси азота в этом изобретении, указаны здесь ниже обозначением DON-NO.
Среди лекарственных препаратов, не содержащих нитрогрупп, вызывающих почечную и/или желудочно-кишечного, и/или дыхательную токсичность, могут быть упомянуты следующие соединения, принадлежащие к различным терапевтическим классам, как, например:
противоопухолевые лекарственные препараты, среди которых могут быть упомянуты цисплатина 5-фтор-урацил;
иммунодепрессивные лекарственные препараты, из которых можно сослаться на циклоспорин;
противовирусные лекарственные препараты, из которых можно сослаться на ацикловир;
нестероидные противовоспалительные лекарственные препараты, среди которых ибупрофен, индометацин, диклофенак, кетеролак, напроксен, кетопрофен, мефенамоновая кислота, флуниксин, флуфенамоновая кислота; нифлумовая кислота могут быть упомянуты;
противотромботические лекарственные препараты, среди которых может быть упомянут аспирин;
стероидные противовоспалительные лекарственные препараты, среди которых могут быть упомянуты кортизон, дексаметазон, метилпреднизолон;
антибиотики, могут быть упомянуты ципрофлоксацин, гентамицин;
ингибиторы ангиотензин-превращающего фермента (АПФ), среди которых могут быть упомянуты каптоприл, эналаприл;
бета-адренергические антагонисты, например атенолол, метопролол, тимолол, пропанол и т.д. Также для этих агентов дыхательная токсичность может быть снижена введением нитрогруппы этого изобретения.
Все эти лекарственные препараты, представленные в Merck Index (смотри выше), приведены здесь как ссылки.
Предпочтительными соединениями в качестве лекарств, не содержащих нитро группу, которая желательна для предотвращения или снижения токсичности, являются противоопухолевые лекарственные препараты, в частности цисплатина (писплатина); иммунодепрессивные лекарственные препараты, в частности циклоспорин; стероидные противоопухолевые лекарственные препараты, в частности дексаметазон, метилпреднизиолон; ингибиторы ангиотензин-превращающего фермента (АПФ), в частности эналаприл, каптоприл.
Введение соединений настоящего изобретения может проводиться через кожу, оральным или парентеральным путем, и соединения в основном вводят одновременно, последовательно или предварительно по отношению к лекарству, не содержащему нитро группы, которое вызывает желудочно-кишечную, и/или почечную, и/или дыхательную токсичность. Путь через кожу является предпочтительным, и соединения изобретения вводят в форме накладок или пластырей. В частности, предпочтительны традиционные накладки, основанные на нитроглицерине, в соответствии с вариантом выполнения настоящего изобретения.
Дозировки являются общепринятыми дозировками, уже использованными для DON-NO для сердечно-сосудистых показаний в терапии человека. Коммерческая накладка обычно используется в течение одного или двух дней и затем заменяется. Медленновысвобождающие накладки могут быть использованы в течение большего числа дней, прежде чем заменяются. Также иногда могут применяться две накладки в день, каждая по двенадцать часов. Такая процедура в основном предпочтительна, если требуется большая эффективность.
Такие дозировки являются предпочтительными, поскольку они не вызывают значительных побочных эффектов, типичных для этого класса лекарственных препаратов, например сильную головную боль, заметную гипертензию и т.д.
Пределы доз для терапии человека главным образом варьируют между 5-15 мг/24 ч за 1-2 применения.
Соединения этого изобретения, содержащие -ONO2 функциональные группы или -NO группу, обеспечивающие результаты изобретения, уже упомянутые, должны подвергаться тесту in vitro, показанному здесь детально.
В частности, этот тест относится к генерации окиси азота из доноров NO настоящего изобретения, среди которых, например, нитроглицерин, никорандил, нитроцианид и т.д., когда они оцениваются в присутствии эндотелиальных клеток (метод а) или тромбоцитов (метод b).
а) Эндотелиальные клетки
Клетки пупочной вены человека, помещенные на планшет, с плотностью 103 клеток/планшет, инкубировались со скалярными концентрациями NO донора (1-100 мкг/мл) в течение 5 мин. Инкубационную среду (физиологический растворитель, например, Tyrode) затем анализировали, чтобы определить способность к генерации NO, посредством:
1) определения окиси азота хемилюминесценцией;
2) определения цГМФ (циклический ГМФ No. 2715 из вышеупомянутого Мегск).
Что касается анализа хемилюминесценцией, количество, равное 100 мкл, инжектировали в реакционную камеру хемилюминесцентного анализатора, содержащую ледяную уксусную кислоту и иодид калия. Нитриты/нитраты, присутствующие в среде, в этих условиях превращаются в NO, который затем определяют после его реакции с озоном с последующей генерацией света. Как это обычно встречается в приборах, измеряющих хемилюминесценцию, полученная люминесценция прямо пропорциональна генерированным уровням NO и может быть измерена соответствующими единицами фотоумножителя хемилюминесцентного анализатора. Фотоумножитель превращает падающий свет в электрическое напряжение, которое затем количественно записывается. По калибровочной кривой, полученной со скалярными концентрациями нитрита, можно количественно определить концентрацию выделенной NO. Например, при инкубировании 100 мкм никорандила вырабатывалось равное 10 мкм количество NO.
Что касается определения цГМФ, часть инкубационной среды, равную 100 мкл, центрифугировали при 1000 оборотах в течение 20 с. Супернатант отделяли и осадок использовали снова в ледяном фосфатном буфере (рН 7.4). Уровни полученного цГМФ тестировали специфическими иммуно-ферментными реагентами. Из таких экспериментов следовало, что инкубирование одного из различных тестируемых доноров NO вызывало значительное увеличение цГМФ по сравнению с величинами, полученными в отсутствие NO донора. Кроме того, например, при инкубировании 100 мкм нитро-цианида натрия зарегистрировали увеличение приблизительно в 20 раз значения, полученного при инкубировании только наполнителя без донора NO.
b) Тромбоциты
Использовали промытые тромбоциты человека, полученные аналогично описанному Radomski et al, (Br. J. Pharmacol. 92, 639-1987). Аликвоты по 0.4 мл инкубировали со скалярными концентрациями доноров NO (1-100 мкг/мл) в течение 5 мин. Затем инкубационную среду (физиологический растворитель Tyrode) анализировали для определения способности генерировать NO путем измерения окиси азота хемилюминесценцией или цГМФ с модальностями, описанными в предыдущем параграфе, для анализов, проведенных на эндотелиальных клетках. Что касается измерения хемилюминесценцией, в этом случае также можно было количественно определить концентрацию генерированной NO по калибровочной кривой, полученной со скалярными концентрациями нитрита. Например, после инкубирования 100 мкм никорандила вырабатывалось количество NO, равное 35 мкм.
Что касается измерения цГМФ, также в тех же экспериментальных условиях, оно привело к тому, что инкубирование с одним из различных тестируемых доноров NO вызвало значительное увеличение цГМФ по сравнению с величинами, полученными в отсутствии донора NO. Например, после инкубирования со 100 мкм нитроцианида натрия зарегистрировали увеличение приблизительно в 30 раз значения, полученного при инкубировании только наполнителя без донора NO. В заключение из вышеуказанных тестов следует, что все доноры NO согласно настоящему изобретению после инкубации с эндотелиальными клетками или тромбоцитами способны генерировать NO и активировать синтез цГМФ концетрационно-зависимым путем, как определено использованными специфическими тестами.
Следующие примеры даны для иллюстративной цели и не ограничивают настоящего изобретения.
ПРИМЕРЫ
Экспериментальные исследования комбинаций, основанных на потенциально токсичных лекарственных препаратах и на донорах NO (указанных как DON-NO)
А) Исследования на животных
1) ИЗУЧЕНИЕ ФУНКЦИОНИРОВАНИЯ ПОЧЕК ПОСЛЕ ВВЕДЕНИЯ ПРОТИВООПУХОЛЕВЫХ СОЕДИНЕНИЙ (ЦИСПЛАТИНА):
Самцов крыс Sprague-Dawley ежедневно обрабатывали наполнителем (физиологический солевой раствор, 0.9% хлорид натрия, внутрибрюшинно (в.б.)) или цисплатином (в. б. ) (5 мг/кг). Некоторые животные получали ежедневную дозу донора NO, нитроцианида натрия, 0.2-1 мг/кг подкожно (п.к.). Через пять дней животных убивали и определяли плазматическую мочевину и плазматическую концентрацию креатинина. Данные анализировали в соответствии с обычно используемыми биостатистическими методами.
Как показано в таблице 1, это привело к тому, что крысы, обработанные только цисплатиной, показывали значительные высокие уровни плазматической мочевины и креатинина по отношению к контрольным значениям (группа, получающая только наполнитель).
Наоборот, в животных, в которых вводились цисплатина и донор NO, биохимические параметры не отличались сильно от контрольных величин.
2) ИЗУЧЕНИЕ ФУНКЦИОНИРОВАНИЯ ПОЧЕК ПОСЛЕ ВВЕДЕНИЯ ИММУНО-ДЕПРЕССИВНЫХ СОЕДИНЕНИЙ (ЦИКЛОСПОРИН)
Самцов крыс Sprague-Dawley ежедневно обрабатывали наполнителем (физиологический солевой раствор, 0.9% хлорид натрия, в.б.) или внутрибрюшинно циклоспорином (5 мг/кг в. б.). Некоторые животные получали ежедневную дозу донора NO, нитроцианида натрия, 0.2-1 мг/кг п.к. Через восемнадцать дней животных убивали и измеряли плазматическую концентрацию креатинина и активность N-ацетил-бета D-глюкозаминидазы (NAG) в моче. Данные анализировали обычно используемыми биостатистическими методами.
Как показано в таблице 2, это привело к тому, что крысы, обработанные только циклоспорином, показывали довольно высокие уровни креатинина в крови и вышеупомянутой NAG в моче по сравнению с контрольными значениями (группа, получавшая только наполнитель).
Наоборот, у животных, которым вводились циклоспорин и DO-NO донор, биохимические параметры не отличались значительно от контрольных значений.
3) ИЗУЧЕНИЕ ФУНКЦИОНИРОВАНИЯ ПОЧЕК ПОСЛЕ ВВЕДЕНИЯ ПРОТИВОВИРУСНЫХ СОЕДИНЕНИЙ (АЦИКЛОВИР):
Самцов крыс Sprague-Dawley ежедневно обрабатывали наполнителем (физиологический солевой раствор, 0.9% хлорид натрия, в.б., ежедневно) или внутрибрюшинно ацикловиром (150 мг/кг в. б. в день) Некоторые животные получали ежедневную дозу DON-NO (нитроглицерин 1-10 мг/кг п.к. в день). Через пятнадцать дней животных убивали и определяли плазматическую концентрацию креатинина. Данные анализировали обычно используемыми био-статистическими методами.
Как показано в таблице 2, это привело к тому, что крысы, обработанные только ацикловиром, показывали довольно высокие уровни креатинина в крови по сравнению с контрольными значениями (группа, получавшая только наполнитель).
Наоборот, у животных, которым вводились ацикловир и DO-NO, биохимические параметры не отличались значительно от контрольных значений (группа, получавшая только наполнитель).
4) ИЗУЧЕНИЕ ФУНКЦИОНИРОВАНИЯ ПОЧЕК И ЖЕЛУДОЧНО-КИШЕЧНОЙ ТОЛЕРАНТНОСТИ У КРЫС С АРТРИТОМ ПОСЛЕ ВВЕДЕНИЯ НЕСТЕРОИДАЛЬНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СОЕДИНЕНИЙ (ИБУПРОФЕН, НАПРОКСЕН, ИНДОМЕТАЦИН, ДИКЛОФЕНАК) ИЛИ ПРОТИВОТРОБОТИЧЕСКИХ СОЕДИНЕНИЙ (АСПИРИН):
Самок крыс Sprague-Dawley превращали в страдающих артритом посредством внутрикаудальной инъекции микобактерий в масле, инактивированных теплом (0.6 мл суспендировали в 0.1 мл минерального масла). Через восемнадцать дней, когда полностью развивалась артритная патология, животных ежедневно обрабатывали наполнителем (физиологический солевой раствор, 0.9% хлорид натрия, в. б. , ежедневно) или NSAID [ибупрофен (60 мг/кг в.б. в день); индометацин (10 мг/кг в. б. в день); диклофенак (12 мг/кг в.б. в день); напроксен (12 мг/кг в.б. в день)], или аспирином (250 мг/кг в.б. в день). Некоторые животные получали ежедневную дозу DON-NO (нитроцианид натрия 0.2-1 мг/кг п.к.; нитроглицерин 1-10 мг/кг п.к. в день). Через пять дней животных убивали и определяли плазматическую концентрацию креатинина. Данные анализировали обычно используемыми био-статистическими методами.
Как показано в таблице 3, это привело к тому, что крысы, обработанные только NSAID или аспирином, показывали довольно высокие уровни креатинина в крови по сравнению с контрольными значениями (группа, получавшая только наполнитель); у таких животных обнаруживали также заметную патологию, влияющую на желудочно-кишечную систему, имеющую различную тяжесть, начиная с эрозии слизистой до язвы, затрагивающей мышечную оболочку, сращения кишечника, асцитов, перитонита. В других группах, обработанных наполнителем или сочетанием DON-NO плюс NSAID или аспирин, патология была или гораздо меньше или даже отсутствовала. Более того, у животных, которым вводились NSAID или аспирин и DO-NO, биохимические параметры не отличались значительно от контрольных значений.
5) ИЗУЧЕНИЕ ФУНКЦИОНИРОВАНИЯ ПОЧЕК И ЖЕЛУДОЧНО-КИШЕЧНОЙ ТОЛЕРАНТНОСТИ В ГИПЕРТЕНЗИВНЫХ КРЫСАХ ПОСЛЕ ВВЕДЕНИЯ НЕСТЕРОИДНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СОЕДИНЕНИЙ (ДИКЛОФЕНАК):
Самцов крыс Sprague-Dawley, самопроизвольно гипертензивных (со систолическим давлением между 180-220 мм рт.ст.), ежедневно обрабатывали наполнителем (физиологический солевой раствор, 0.9% хлорид натрия, в.б.) или NSAID [диклофенак(12 мг/кг в.б.)]. Некоторые животные получали ежедневную дозу органического нитрата (нитроглицерин 1-10 мг/кг в день п.к.). Через пять дней животных убивали и определяли плазматическую концентрацию креатинина. Данные анализировали обычно используемыми био-статистическими методами.
Как показано в таблице 4, это привело к тому, что крысы, обработанные только NSAID, показывали довольно высокие уровни креатинина в крови по сравнению с контрольными значениями (группа, получавшая только наполнитель); у таких животных также обнаруживали при изучении после вскрытия заметную патологию, влияющую на желудочно-кишечную систему, имеющую различную тяжесть, начиная с эрозии слизистой до язвы, затрагивающей мышечную оболочку, сращения кишечника, асцитов, перитонита. В других группах, обработанных наполнителем или сочетанием DON-NO плюс NSAID, патологическая картина, влияющая на желудочно-кишечную систему, была или гораздо меньше или даже отсутствовала.
Более того, у животных, которым вводились диклофенак и DO-NO, биохимические параметры не отличались значительно от контрольных значений.
6) ИЗУЧЕНИЕ ЖЕЛУДОЧНО-КИШЕЧНОЙ ТОКСИЧНОСТИ ПОСЛЕ ВВЕДЕНИЯ СТЕРОИДНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СОЕДИНЕНИЙ (МЕТИЛПРЕДНИЗОЛОН):
Самцов крыс Sprague-Dawley ежедневно обрабатывали наполнителем (физиологический солевой раствор, 0.9% хлорид натрия, в.б.) или внутрибрюшинно метилпреднизиолоном (5-10 мг/кг в.б.).
Некоторые животные получали ежедневную дозу органического нитрата (нитроцианид натрия 0.2-1 мг/кг п. к.). Через восемнадцать дней животных убивали.
Изучение после вскрытия показало (таблица 5), что у таких крыс обнаруживали также заметную патологию, влияющую на желудочно-кишечную систему, имеющую различную тяжесть, начиная с эрозии слизистой до язвы, затрагивающей мышечную оболочку, сращения кишечника, асцитов, перитонита. В других группах, обработанных наполнителем или сочетанием нитрат плюс стероид, патология была или гораздо меньшей или даже отсутствовала.
7) ИЗУЧЕНИЕ ВЛИЯНИЯ НИТРОКСИБУТИЛНАПРОКСЕНА (NO-НАПРОКСЕНА) НА БРОНХОСТЕНОЗ, ВЫЗВАННЫЙ КАПСАИЦИНОМ, В ОБРАБОТАННЫХ ЭНАЛАПРИЛОМ МОРСКИХ СВИНКАХ.
Бронхостеноз у морских свинок, вызванный капсаицином, является моделью на животных, связанную со способностью ингибиторов ангиотензин-превращающего фермента вызывать кашель у пациентов (Subissi et al., J. Cardiovasc. Pharmacol. 20/1, 139-146, 1992).
NO-напроксен (2-(6-метокси-2-нафтил)пропионат 4-гидрокси-бутила) синтезировали согласно Примеру 1 (формула V) из международного патента WO 95/09831.
Экспериментальные условия были тщательно описаны Del Soldato et al (J. Pharmacological Methods 5, 279, 1981). Самок морских свинок весом 300-400 г анестизировали посредством инъекции внутрибрюшинно 5,5-диэтилбарбитурата натрия (200 мг/кг) и поддерживали на искусственном дыхании при постоянном положительном давлении. Правая яремная вена использовалась для введения соединений. Животные получали интрадуоденально эналаприл (10 мг/кг), наполнитель (карбоксиметил целлюлозу 2% вес.) и/или NO-напроксен (10 мг/кг). Спустя 45 мин вводили внутривенно 0,1 мл капсаицина (1 мкг/мл) Перед или после инъекции капсаицина измеряли изменения дыхательного объема воздуха посредством модифицированного аппарата Konzett, подсоединенного к полиграфическому усилителю.
Результаты рассчитывали как отношение откликов, полученных перед и после проведения каждой обработки, выражали как % от отклика наполнителя (контроль) и представляли в таблице 7.
Как показано в таблице 7, NO-напроксен способен снижать бронхостеноз, вызванный капсаицином, в обработанных эналаприлом морских свинках. Эналаприл повышает отклик бронхостеноза, вызванного капсаицином, когда вводится один.
В) ИССЛЕДОВАНИЕ НА ПАЦИЕНТАХ
ИЗУЧЕНИЕ ФУНКЦИОНИРОВАНИЯ ПОЧЕК У ПАЦИЕНТОВ ПОСЛЕ ВВЕДЕНИЯ ПРОТИВООПУХОЛЕВЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ (ЦИСПЛАТИНА)
У некоторых пациентов, обследованных отдельно, и в неконтролируемых исследованиях обнаруживалось сильное влияние некоторых лекарственных препаратов, таких как цисплатина, применяемая отдельно или в составе нитроглицериновой накладки. Моно-введение цисплатина внутрибрюшинно (90 мг на м2) пациентам, которые нуждались в противоопухолевой терапии, вызывало значительное повышение количества креатинина в крови за первые 24 часа по отношению к первоначальным значениям.
Как следует из таблицы 6, если пациенты подвергались ежедневной обработке, включающей нитроглицериновую накладку, которая выделяла приблизительно 15 мг/24 ч нитроглицерина, когда накладка контактировала с кожей, то такое повышение было гораздо более ограниченно и несмотря на это значительно не отличалось от первоначальных величин.
Данные анализировали обычно используемыми био-статистическими методами.




Изобретение относится к области медицины и касается применения соединений, содержащих -ONO2 группу, для снижения токсичности, вызванной лекарственными препаратами, не содержащими нитрогрупп. Указанные соединения более эффективно снижают токсичность от лекарств. 11 з.п.ф-лы, 7 табл.
эритритилтетранитрата(1,2,3,4-бутантетролтетранитрата), имеющего структурную формулу
гексанитрата маннита, имеющего структурную формулу
никорандила(N-[2-(нитроокси)этил] -3-пиридин-карбоксамида), имеющего структурную формулу
нитроглицерина(1,2,3-пропантриолтринитрата), имеющего структурную формулу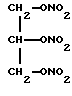
пентаэритритолтетранитрата(2,2-бис[(нитроокси)-метил] -1,3-пропандиолдинитрата), имеющего структурную формулу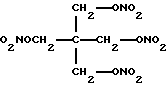
пентринитрола(2,2-бис[(нитроокси)метил] -1,3-пропандиолмононитрата), имеющего структурную формулу
пропатилнитрата(2-этил-2-[(нитроокси)метил] -1,3-пропандиолдинитрата), имеющего структурную формулу
тролнитратфосфата(2,2', 2"-нитрилтрисетанолтринитратфосфата) (соль 1: 2), имеющего формулу
3. Применение соединений по п. 1, где неорганические соединения, содержащие -NO группу, выбраны из нитроцианидов.
| WO 9600073, А1, 04.01.1996 | |||
| WALLACE JL et al., "Nitric oxide-relaxing non-steroidal anti-inflammary drugs", J.Gastroenterol Hepatol, 1994, 9 Suppl2, p.s41 | |||
| Машковский М.Д., Лекарственные средства, М | |||
| Медицина, 1986, ч.1, с.493. |
Авторы
Даты
2002-11-10—Публикация
1997-02-24—Подача