Изобретение относится к области синтеза диоксида марганца, применяемого в химических источниках тока в качестве активного компонента катодной массы, в частности к электролитическим способам синтеза.
Известен способ получения диоксида марганца, например путем электролиза из водных сернокислых растворов, содержащих 100-200 г/л сульфата марганца и 20-100 г/л свободной серной кислоты при температуре 90-98oС и плотности тока 100-300 А/м2. В качестве анода используется титан, на поверхность которого нанесен слой металла платиновой группы или двуокиси рутения, или двуокиси свинца. Катод изготовлен из хромоникелевой стали (Авторское свидетельство СССР 655764, кл. С 25 В 1/00, 1977).
Известен способ получения электролитической двуокиси марганца γ-модификации путем электролиза кислых растворов сульфата марганца при температуре 80-90oС. Электролит содержит 100-150 г/л MnSO4 и 20-50 г/л серной кислоты. Аноды изготовляются из свинца, графита, титана и др. Электролиз проводят при анодной плотности тока 80-100 А/м2. Выход по току составляет 95%, скорость осаждения диоксида марганца 0,15 кг/м2•ч (Технологический регламент производства ЭДМ на Руставском химическом заводе, фонд п/я В-8046, 4030, 1979, с.335).
Недостатком способов является то, что при использовании в качестве материала анода титана наблюдается его пассивация вследствие образования на поверхности оксидной плохо проводящей электрический ток пленки, что сопровождается повышением напряжения на ванне электролизера выше 10 В. Другим недостатком способов является сильная адсорбционная способность диоксида марганца, адсорбирующего анионы (сульфат) и катионы (железо, медь, никель), загрязняя ими продукт. Кроме того, из электролита на образование диоксида марганца идет 40-60% марганца, остальные 60-40% марганца вместе с кислым оборотным раствором возвращаются в голову технологической схемы на выщелачивание.
Наиболее близким к изобретению по технической сущности и достигаемому результату является способ получения диоксида марганца γ-модификации анодным окислением марганца в электролите, содержащем муравьиную кислоту 7,5-10 г/л и муравьино-кислый марганец 50-70 г/л. При 80-90oС и анодной плотности тока 50-100 А/м2 получают плотную, компактную двуокись марганца, прочно сцепленную с титановым анодом.
Недостатками способа является применение дефицитной дорогостоящей муравьиной кислоты, проведение электролиза при высокой температуре (80-90oС), при которой практически вся муравьиная кислота за время электролиза улетучивается (температура кипения муравьиной кислоты 100,7oС), затруднен синтез муравьино-кислого марганца, целевое использование марганца из раствора низкое (менее 50%). Муравьиная кислота обладает высоким восстановительным потенциалом, что препятствует получению монофазы γ-MnO2. В анодных осадках наряду с γ-модификацией МnО2 присутствуют малоактивные δ-MnO2, η-MnO2 модификации.
Целью изобретения является снижение температуры электросинтеза, повышение целевого использования растворенного марганца в диоксид, получение монофазы γ-MnO2.
Поставленная цель достигается применением электролиза из водного раствора уксуснокислого марганца, содержащего 110-120 г/л Мn (СН3СОО)2 и 5-10 г/л уксусной кислоты при плотности тока 50-100 А/м2, напряжении на ванне 2-3 В, при температуре 65-80oС.
Сущность способа состоит в том, что электросинтез диоксида марганца в кислых электролитах идет через промежуточную стадию образования МnООН:
Mn2++2H2O-e=МnООН+3H+-e=MnO2+4Н+
В растворах сильных кислот (НСl, H2SO4, HNO3) концентрация протонов в процессе электролиза возрастает, что тормозит реакцию синтеза, сдвигая ее влево.
Скорость процесса определяется диффузией ионов Н+, участвующих в образовании МnО2 из МnООН. Так, при электросинтезе МnО2 в сернокислых растворах на титановых анодах должна быть начальная концентрация сульфата марганца 100-150 г/л, концентрация серной кислоты 20 г/л, то начальную концентрацию серной кислоты снижать нельзя, так как уменьшился электропроводность, возможен гидролиз Mn(II), что нарушает режим электролиза. Электросинтез, таким образом, "зажат" между 20 г/л Н2SО4 (нижний предел кислотности, рН 1) и 100-150 г/л H2SO4 (верхний предел кислотности), когда тормозится скорость синтеза. Кроме того, при высокой концентрации кислоты возрастает напряжение на электролизере до 10-15 В из-за перенапряжения на титановых анодах.
Использование растворов ацетата марганца во многом исключает указанные недостатки. Процесс синтеза можно вести при температуре 65-80oС, преимущественно при 70-75oС. Образовавшаяся в процессе уксусная кислота создает рН от ≈3 до 2,2 при высоком целевом использовании растворенного марганца.
Экспериментально установлены параметры предлагаемого способа. Синтез МnО2 в ацетатных средах может быть осуществлен в широком интервале температур 65-90oС. Однако при температуре более 80oС увеличивается расход тепла на нагрев электролита, увеличивается парообразование и летучесть уксусной кислоты. При температуре ниже 65oС растет напряжение на ванне >3 В и возможно образование наряду с γ-модификацией МnО2 также нежелательных других модификаций.
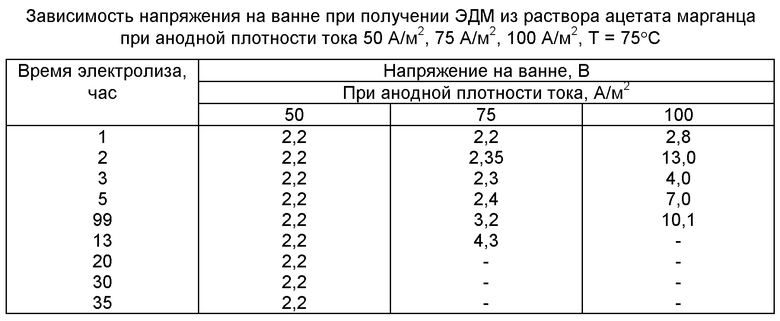
В таблице показано изменение напряжения на ванне при электролитическом синтезе диоксида марганца из ацетатных растворов при различных плотностях тока. Как следует из данных таблицы, оптимальную плотность тока при синтезе диоксида марганца в уксуснокислых средах нужно поддерживать в интервале 50-75 А/м2, при котором реализуется достаточно высокий выход по току - 95-99%.
При применении плановых анодов при плотности тока 50 А/м2 пассивации титана не наблюдается в течение 35 часов работы. Осадки получались плотные с блестящей поверхностью. Напряжение на ванне оставалось постоянным и составляло 2,2 В.
Другим важным преимуществом ацетатных растворов является возможность проведения электросинтеза в непроточном электролите с достаточно высоким срабатыванием марганца (>99%) без снижения качества МnО2.
Пример 1
Электросинтез диоксида марганца проводили из водного раствора уксуснокислого марганца. Начальная концентрация марганца составляла 108 г/л, уксусной кислоты 10 г/л. Ацетат марганца получали растворением карбоната марганца в уксусной кислоте. Аноды изготовлены из трубок титана марки ВТ1-0 с рабочей поверхностью 0,01 м2. Катоды изготовлены из стали ЭИ-943 площадью 0,005 м2. Электролиз вели в термостатированной ячейке при 65oС.
Объем электролита 300 мл. Плотность анодного тока 50 А/м2, плотность катодного тока 100 А/м2, напряжение на ванне 2,2 В, время электролиза 11 часов. Получено 13 г диоксида марганца. По данным рентгенографического анализа полученный диоксид марганца γ-модификации. Выход по току составил 92%.
Пример 2
Электросинтез МnО2 проводили в электролизере из раствора ацетата марганца с исходными концентрациями 108 г/л и уксусной кислоты 10 г/л. Аноды и катоды применяли, как в примере 1. Объем электролита 300 мл. Плотность анодного тока 75 А/м2, катодного тока 150 А/м2, температура электролита 75oС, время электролиза 13 часов. Напряжение на ванне возросло с 2,3 В до 4,2 В в конце опыта. Получено 8 г МnО2. Диоксид марганца γ-модификации. Выход по току составил 99,3%.
Пример 3
Электросинтез диоксида марганца проводили из водного раствора ацетата марганца исходной концентрации 101 г/л и 20 г/л уксусной кислоты. Объем раствора 300 мл. Аноды изготовлены из титана ВТ1-0 с работающей поверхностью 0,01 м2, катоды - из стали ЭИ-943, площадью 0,005 м2. Плотность анодного тока 100 А/м2, катодного - 200 А/м2. Температура электролита поддерживалась в течение всего опыта 80oС. Напряжение на ванне начальное 2,3 В, через 10 часов напряжение повысилось до 4,6 В. Получено 8,8 г МnО2. По данным рентгенографического анализа получен МnO2 γ-модификации.
Пример 4
В эксперименте предусматривалась максимальная выработка марганца. Электросинтез диоксида марганца проводили из водного ацетатного раствора при температуре 75oС, плотности анодного тока 75 А/м2, катодного - 150 А/м2. Аноды изготовлены из титана марки ВТ1-0, катоды - из стали ЭИ-943.
Начальное напряжение на ванне было 2,15 В. Объем раствора 330 мл, в котором исходная концентрация ацетата марганца была 120 г/л, концентрация уксусной кислоты 20 г/л.
Через 31 час концентрация марганца в растворе составила 0,3 г/л, получено 21,9 г диоксида марганца с содержанием 61,2% Мn, в диоксид марганца перешло более 99% марганца. При этом скорость синтеза МnО2 достигла 0,06 кг/м2•ч.
Таким образом, использование предлагаемого способа получения диоксида марганца позволяет проводить синтез при более низких температурах, применять титановые аноды, которые в ацетатных средах практически не пассивируются, вести электросинтез в электролизерах с непроточным электролитом с высоким срабатыванием Мn2+ в диоксид более 99%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА МАРГАНЦА γ--МОДИФИКАЦИИ | 1996 |
|
RU2115769C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА МАРГАНЦА ГАММА-МОДИФИКАЦИИ | 1997 |
|
RU2149832C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА ДЛЯ ПРОИЗВОДСТВА СОЛЕЙ СВИНЦА | 2001 |
|
RU2213698C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,1-ДИХЛОР-4-МЕТИЛПЕНТАДИЕНА-1,4 | 1991 |
|
RU2039730C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ КИСЛОТ ФОСФОРА | 2001 |
|
RU2199545C1 |
| ЛИНИЯ ПОЛУЧЕНИЯ ЭЛЕКТРОЛИТИЧЕСКОГО ДИОКСИДА МАРГАНЦА | 1996 |
|
RU2094532C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАЛЛАДИЯ, РАСТВОРИМОГО В АЗОТНОЙ КИСЛОТЕ | 2010 |
|
RU2422545C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЫШЬЯКОВОЙ КИСЛОТЫ ЭЛЕКТРОХИМИЧЕСКИМ ОКИСЛЕНИЕМ ВОДНОЙ СУСПЕНЗИИ ОКСИДА МЫШЬЯКА (III) | 2000 |
|
RU2202002C2 |
| СПОСОБ ОТДЕЛЕНИЯ РОДИЯ ОТ ИРИДИЯ И РУТЕНИЯ | 1999 |
|
RU2179193C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО КАРБОНАТА КОБАЛЬТА (II) | 2010 |
|
RU2424190C1 |
Изобретение относится к области получения диоксида марганца, в частности к электролитическим способам синтеза. Способ получения диоксида марганца включает электролитический синтез его на титановых анодах в уксуснокислых средах, при температурах 65-75oС, анодной плотности тока 50-100 А/м2, начальных концентрациях ацетата марганца 100-120 г/л и уксусной кислоты 10-20 г/л до максимально полной выработки марганца из раствора. Изобретение позволяет обеспечить высокий выход и снизить температуру синтеза. 1 з.п. ф-лы, 1 табл.
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА МАРГАНЦА γ--МОДИФИКАЦИИ | 1996 |
|
RU2115769C1 |
| МАТЕРИАЛ АНОДА ДЛЯ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ ДИОКСИДА МАРГАНЦА | 1995 |
|
RU2097449C1 |
| СПОСОБ ПЕРЕРАБОТКИ МАРГАНЦЕВОГО СЫРЬЯ | 1992 |
|
RU2054494C1 |
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| WO 00/37714 A1, 29.06.2000. | |||
Авторы
Даты
2002-11-27—Публикация
2001-04-09—Подача