Изобретение относится к области технологии производства неорганических соединений металлов, в частности солей кобальта. Полученный продукт может применяться для получения оксида двухвалентного кобальта и высших оксидов, чистых солей двухвалентного кобальта, используемых в производстве катализаторов или связующих для красок.
Известен способ получения основного карбоната кобальта (II) Со[(ОН)2]а[СО3]1-а, основанный на анодном окислении металлического кобальта в насыщенных диоксидом углерода водных растворах электролитов с последующим отделением и промывкой полученного осадка (Герге Астрид. Патент РФ №97121818, МПК6 C01G 51/06, опубликовано 1999.11.10).
Недостатком способа является необходимость дополнительных затрат, связанных с отмывкой продукта от примесных анионов и катионов, а также расход электроэнергии.
Известен способ получения основного карбоната (II) электролизом водного раствора, насыщенного диоксидом углерода под давлением 0,1-1,0 МПа, путем анодного растворения кобальта в растворе гидрокарбоната аммония с концентрацией 1 М при плотности тока 50 А/м2 (Алиев З.М. Патент РФ №2342324, C01G 51/06 (2006.01), С25В 1/00 (2006.01) опубликовано 27.12.2008).
Недостатком способа является большой расход электроэнергии, а также загрязнение конечного продукта (при получении при высоких плотностях тока) примесями оксида кобальта.
Известны способы получения основного карбоната кобальта (II), основанные на реакциях осаждения. К нагретому до 40 - 50°С раствору CoCl2 (C=1,6 моль·дм-3) при непрерывном перемешивании добавляли горячий раствор Na2CO3 (C=5 моль·дм-3) (Ю.В.Корякин, И.И.Ангелов. Чистые химические вещества. М.: Химия, 1974, с.213).
Недостатком данных способов является необходимость дополнительных затрат, связанных с отмывкой полученного продукта от примесных анионов (Сl- и др.) и катионов (Na+ и др.), содержащихся в исходных растворах.
Известен способ получения кобальта (II) основанный на реакции осаждения. Раствор хлорида кобальта заливают в раствор осадителя - гидрокарбоната щелочного металла или аммония. Реакция протекает на фоне избытка осадителя с дальнейшим снижением его концентрации до окончания реакции. Осадок фильтруют. Отмывают водой от хлорид-иона, сушат (В.Н.Андрущенко, В.П.Южаков. Патент РФ №2154029 С2, МПК7, C01G 51/06, опубликовано 10.08.2000).
Недостатком данного способа является необходимость дополнительных затрат, связанных с отмывкой полученного продукта от примесных анионов (Сl-) и катионов (Na+), содержащихся в исходных растворах.
Наиболее близким к заявленному является способ получения карбоната кобальта (II). К раствору хлорида кобальта добавляют гидрокарбонат или карбонат натрия по каплям при непрерывном перемешивании. Процесс ведут в диапазоне температур от 40 до 100°С. Осадок фильтруют. Отмывают водой, нагретой до температуры, при которой проводили синтез, сушат (Gorge Astrid, Meese-Maarktscheffel и др. Патент US 2004131530 (А1), C01G 51/04, 08.07.2004).
К недостаткам способа можно отнести значительный расход воды (нагретой до температуры от 40 до 100°С), а также расход электроэнергии.
Технический результат предлагаемого способа - получение целевого продукта высокой степени чистоты, не содержащего примесные анионы (хлорид, нитрат, сульфат) и катионы (натрия, калия), что освобождает от необходимости длительной промывки полученного осадка. При создании заявленного изобретения ставилась задача разработать ионообменный способ получения основного карбоната кобальта (II). Решение этой задачи включает выбор анионита, перевод анионита АВ-17-8 (сильноосновной анионит с полистирольной матрицей, содержащий четвертичные аммониевые основания - N+(CН3)3 (ГОСТ 20301-74)) в карбонатную форму, контакт ионита с раствором соли Со (II), отделение продукта и регенерацию анионита. Новым в этом способе является то, что в качестве реагента-осадителя используют анионит в карбонатной форме, и в связи с этим полученный продукт не загрязняется катионами-осадителя и анионами раствора.
При создании заявленного изобретения были использованы гелевые и пористые, слабоосновные и сильноосновные аниониты в СО3-форме. Полученные данные свидетельствуют, что использование пористых (слабоосновных и сильноосновных), а также гелевых слабоосновных анионитов нецелесообразно, так как значительная доля кобальта (более 50%) удерживается анионитом вследствие его осаждения в виде карбоната кобальта (II) в порах сорбента или комплексообразования ионов кобальта (II) с азотом функциональных групп. Поэтому выбор сильноосновного анионита, содержащего функциональные группы четвертичных аммониевых оснований типа АВ-17-8, является предпочтительным.
Перевод анионита в СО3-форму проводили, заливая исходный АВ-17-8 в хлоридной форме 0,5М раствором Nа2СО3 (т:ж=1:2) 5 раз, выдерживая каждую порцию в течение часа (последнюю порцию в течение суток). После чего полученный анионит хранили в набухшем состоянии под слоем воды и после определения его емкости использовали в экспериментах.
Процесс ионообменного синтеза можно описать следующим уравнением:
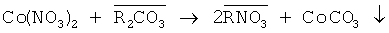
(надстрочная черта определяет фазу анионита).
СоСО3 - это упрощенная запись, на самом деле состав продукта соответствует общей формуле СоСО3·mCo(ОН)2.
Количество анионита, необходимое для синтеза, рассчитывали по формуле:
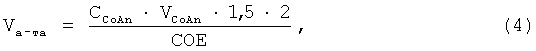
где CCoAn - концентрация исходного раствора кобальта (ммоль/мл), VCoAn - объем раствора кобальта (мл); 1,5 - избыток функциональных групп анионита; СОЕ - статическая обменная емкость анионита в набухшем состоянии (ммоль-экв мл-1).
Анионит приводили в контакт с 10 мл раствора соли Со (II) (концентрация варьировалась в интервале 0,1-0,5 М) при фиксированной температуре на определенное время при перемешивании на шейкере. Фазы разделяли, пропуская их последовательно через сито с диаметром отверстий 0,25 мм (для отделения анионита) и фильтр «синяя лента» или центрифугированием (для отделения осадка). Полученный осадок после промывания водой сушили при температуре 60-80°С.
Ниже приведены примеры предлагаемого способа.
Пример 1. Получение основного карбоната кобальта из нитратного раствора кобальта. К 10 мл 0,25 М раствора Со(NO3)2 добавляют анионит АВ-17-8 в карбонатной форме. Раствор перемешивают в течение одних суток на шейкере при температуре (20±0,2)°С, затем фазы разделяют, осадок высушивают. По данным химического анализа полученный продукт соответствует формуле Со(ОН)1,12(СО3)0,44. Выход 53%.
Пример 2. Получение основного карбоната кобальта из хлоридного раствора кобальта. К 10 мл 0,25 М раствору CoCl2 добавляют анионит АВ-17-8 в карбонатной форме. Раствор перемешивают в течение одних суток на шейкере при температуре (20±0,2)°С, затем фазы разделяют, осадок высушивают. По данным химического анализа полученный продукт соответствует формуле Со(ОН)1,04(СО3)0,48. Выход 52%.
Пример 3. Получение основного карбоната кобальта из сульфатного раствора кобальта. К 10 мл 0,25 М раствору CoSO4 добавляют анионит АВ-17-8 в карбонатной форме. Раствор перемешивают в течение 3 часов на шейкере при температуре (98±0,2)°С, затем фазы разделяют, осадок высушивают. По данным химического анализа полученный продукт соответствует формуле Co(OH)1,26(CO3)0,37. Выход 80%.
Предлагаемый способ достаточно прост, не предполагает использования агрессивных сред, высоких температур и давлений. Используя его, можно добиться получения продукта высокой степени чистоты, не содержащего примесные анионы (хлорид, нитрат, сульфат) и катионы (натрия, калия, аммония), что освобождает в дальнейшем от необходимости длительной промывки полученного осадка.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРАТА ОКСАЛАТА КОБАЛЬТА (II) | 2007 |
|
RU2384564C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРАТА ОКСАЛАТА НИКЕЛЯ(II) | 2008 |
|
RU2362763C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ЦИРКОНИЯ ТЕТРАГОНАЛЬНОЙ МОДИФИКАЦИИ ДЛЯ ПРОИЗВОДСТВА КАТАЛИЗАТОРОВ | 2008 |
|
RU2400429C2 |
| СПОСОБ ПОЛУЧЕНИЯ СИНЕГО АЛЮМОКОБАЛЬТОВОГО ПИГМЕНТА | 2011 |
|
RU2484025C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЮМОНИКЕЛЕВОГО ПИГМЕНТА | 2012 |
|
RU2482143C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА АЛЮМОИТТРИЕВОГО ГРАНАТА | 2014 |
|
RU2576271C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА КОБАЛЬТА | 2012 |
|
RU2483841C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБМИКРОННЫХ ПОРОШКОВ ФЕРРИТА КОБАЛЬТА (II) | 2017 |
|
RU2649443C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНЫХ ПОРОШКОВ ФЕРРИТА МЕДИ (II) | 2018 |
|
RU2699891C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОДИСПЕРСНЫХ ПОРОШКОВ ОКСИДА ИНДИЯ | 2015 |
|
RU2587083C1 |
Изобретение относится к технологии производства солей кобальта. Способ получения основного карбоната кобальта (II) включает приготовление реакционного водного раствора, содержащего нитрат, или хлорид, или сульфат кобальта, осаждение из раствора основного карбоната кобальта, отделение полученного осадка от раствора и его высушивание. В качестве реагента-осадителя используют сильноосновный гелевый анионит АВ-17-8 в карбонатной форме. Изобретение позволяет повысить чистоту получаемого основного карбоната кобальта (II).
Способ получения основного карбоната кобальта (II), включающий приготовление реакционного водного раствора, содержащего нитрат, или хлорид, или сульфат кобальта, осаждение из раствора основного карбоната кобальта, отделение полученного осадка от раствора и его высушивание, отличающийся тем, что в качестве реагента-осадителя используют сильноосновный гелевый анионит АВ-17-8 в карбонатной форме.
| US 2004131530 A1, 08.07.2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО КАРБОНАТА ДВУХВАЛЕНТНОГО КОБАЛЬТА | 2007 |
|
RU2342324C1 |
| ОСНОВНЫЕ КАРБОНАТЫ ДВУХВАЛЕНТНОГО КОБАЛЬТА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 1996 |
|
RU2154664C2 |
| Способ получения основного углекислого кобальта | 1975 |
|
SU709545A1 |
| CN 101323565 A, 17.12.2008 | |||
| Способ нагрева деталей из металлических порошков и устройство для его осуществления | 1986 |
|
SU1470460A1 |
Авторы
Даты
2011-07-20—Публикация
2010-02-15—Подача