Изобретение относится к области химической промышленности, в частности созданию более экономичных новых гомогенных катализаторов, позволяющих получать широкий марочный ассортимент полиэтиленов.
Известны катализаторы полимеризации этилена на основе металлгалоидных лигандов общей формулы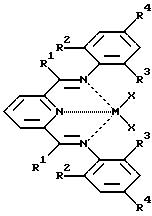
где M = Fe, Co; X = Cl, Br; R1 = H, Me; R2 = Me, i-Pr, Et, t-Bu; R3 = H, Me, Et, i-Pr; R4 = H, Me;
с подробным рассмотрением их синтеза и характеристик, а также исследование полимеризации этилена на этих катализаторах в присутствии в качестве сокатализатора метилалюмоксана (МАО) [1. Заявка WO 9623010 A2, кл. С 08 F 210/16; С 08 F 110/02; С 08 F 110/06, 1 Aug. 1996; 2. Britovsek G.J.P., Bruce M., Gibson V.C., Kimberley B.S., Maddox P.J., Mastroianni S., McTavish S. J. , Redshaw C., Solan G.A., Stromberg S., White A.J.P., and Williams D.J. "Iron and Cobalt Ethylene Polymerization Catalysts Bearing 2,6-Bis(Imino)Pyridyl Ligands: Synthesis, Structures, and Polymerization Studies", J. Amer. Chem. Soc. 1999, v.121, 38, p.8728-8740; 3. Ittel S.D. and Johnson L.K. "Late-Metal Catalysts for Ethylene Homo- and Copolymerization", Chem. Rev. 2000, v.100, 4, p.1169-1203]. Патент и обе статьи являются обзорными по всем изученным бис(имино)пиридильным и дииминным металлгалоидным катализаторам. В указанных работах отмечено, что новые каталитические системы являются высокоактивными катализаторами для синтеза ПЭВП. Однако такими особенностями обладают только бис(имино)пиридильные комплексы, содержащие кетиминные лиганды (R1=Me), а в случае альдиминных лигандов (R1=Н) их активность снижается на порядок и более. В связи с этим нами при сопоставлении результатов по исследованию полимеризации в присутствии таких каталитических систем учитываются данные, полученные на катализаторах с кетиминными лигандами.
К недостаткам всех рассмотренных в указанных публикациях катализаторов (13 образцов) следует отнести резкое снижение их активности при повышении температуры полимеризации. Так, например, для наиболее активной системы, где в качестве М=Fe; Х=Cl; R1=Me; R2=iPr; R3=iPr; R4=Н (см. общую формулу) активность падает с 10800 кг/молькат•ч•бар до 1180 кг/молькат•ч•бар соответственно, а молекулярная масса (ММ) полученного полиэтилена снижается с 386000 до 14000.
Катализаторы на основе FеСl2 более активны по сравнению с катализаторами на основе СоСl2 при температуре полимеризации 35oС в 30 раз и примерно в 8 раз - при 70oС. При использовании соединений Со с аналогичными заместителями в арильном кольце активность меняется от 360 кг/молькат•ч•бар до 150 кг/молькат•ч•бар, а ММ - от 16000 до 8800.
Наиболее близким по технической сущности является способ проведения полимеризации этилена на комплексах бис(имино)пиридинов с Fe и Со [заявка WO 98/27124 A1, кл. С 08 F 10/00, С 07 F 15/02, 1998]. Данные патента по использованию катализаторов (примеры 7, 10, 12-14, 16 и 17) подробно изучены в приведенной статье [2]. В примерах патента по полимеризации этилена при комнатной температуре на синтезированных катализаторах - комплексах на основе бис(имино)пиридинов СоСl2 и СоВr2, например 18-21, выход полиэтилена низкий (максимальный ~ 400 кг/молькат•ч•MПa, процесс проводился 16 часов при давлении этилена 0,0375 МПа с выходом ПЭ=4,3-7,25 г). MM получаемых полимеров была низкой (Мn=5094-4294). Аналогичные катализаторы на основе FeCl2, описанные в патенте, как мы отметили ранее, были активнее, их структуры и поведение при полимеризации этилена также описаны в статье [2].
Таким образом, гомогенные катализаторы, синтезированные и изученные при полимеризации этилена в патенте, не отличаются высокой термостабильностью и резко теряют свою активность при температурах выше 50oС.
Изобретение решает задачу синтеза новых гомогенных катализаторов на основе бис(имино)пиридильных лигандов и FeCl2, сохраняющих свою активность при повышенных температурах полимеризации (используемые в технологии суспензионной полимеризации температуры преимущественно 70oС и выше).
Указанная задача достигается за счет использования катализаторов на основе бис(имино)пиридильных комплексов с новыми R2: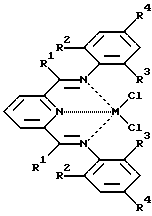
где M = Fe+2, Co+2; R1 = Me; R3 = H, Me, Et, i-Pr; R4 = H, Me.
Полимеризацию этилена проводят при давлениях 0,1-1,5 МПа и температурах 70-80oС.
В качестве углеводородных растворителей применяют, например, толуол, н-гексан, бензин и др.
В качестве сокатализатора используют алкилалюмоксаны (ААО), например метилалюмоксан (МАО), изобутилалюмоксан (ИБАО). Молекулярную массу регулируют условиями проведения реакции (температурой, концентрациями компонентов реакции).
Синтез бис(имино)пиридильных лигандов и на их основе катализаторов полимеризации этилена проводят следующим образом.
2,6-Бис(имино)пиридильные лиганды, например 2,6-бис-[1-(2-метил-6-циклоалкилфенилимино)этил] пиридины, получали при нагревании 2-метил-6-циклоалкиланилинов с 2,6-диацетилпиридином в метаноле в присутствии каталитических количеств муравьиной кислоты с выходами 80-85%, используя модификацию процедуры [4. Small B. L., Brookhart M., Bennett A.M.A. // J. Amer. Chem. Soc., 1998, v.120, 16, p.4049-4050].
Орто-циклоалкениланилины, необходимые для синтеза 2,6-бис(имино)пиридильных лигандов, например 2-метил-6-(цикло-2'-алкенил)анилины, получали при взаимодействии 3-галогенциклоалкенов с 2-метиланилином в результате аминокляйзеновской перегруппировки первоначально образующихся N-(цикло-2'-алкенил)-2-метиланилинов [5. Абдрахманов И.Б., Шарафутдинов В.М., Толстиков Г.А. Изв. АН СССР. Сер. хим., 1982, 9, 2160-2162] .
Орто-циклоалкиланилины, необходимые для синтеза 2,6-бис(имино)пиридильных лигандов, например 2-метил-6-циклоалкиланилины, получали гидрированием в мягких условиях в присутствии никеля Ренея соответствующих 2-метил-6-(цикло-2'-алкенил)анилинов с выходами 95-98%.
2,6-Бис(имино)пиридильные комплексы галогенидов металлов переменной валентности, например 2,6-бис-[1-(2-метил-6-циклоалкилфенилимино)этил]пиридин железо(II) хлориды, получены с высоким выходом взаимодействием соответствующего 2,6-бис(имино)пиридильного лиганда, например 2,6-бис-[1-(2-метил-6-циклоалкилфенилимино)этил] пиридина, с FеСl2•4Н2О или CoCl2•6H2O в ТГФ при комнатной температуре в атмосфере аргона, используя модификацию процедуры [4].
2-Метил-6-циклопентиланилин. Выход 98%. Т. кип. 98-100oС при 0.5 мм рт. ст. Найдено, %: С 82.25; Н 9.77; N 7.98. С13Н17N. Вычислено, %: С 82.23; Н 9.78; N 7.99.
2-Метил-6-циклогексиланилин. Выход 96%. Т. кип. 100-102oС при 0.5 мм рт. ст. Найдено, %: С 82.51; Н 10.15; N 7.41. C13H19N. Вычислено, %: С 82.48; Н 10.12; N 7.40.
2-Метил-6-циклооктиланилин. Выход 98%. Т. кип. 129-130oС при 0.5 мм рт. ст. Найдено, %: С 82.91; Н 10.64; N 6.41. C15H23N. Вычислено, %: С 82.89; Н 10.67; N 6.44.
2-Метил-6-циклододециланилин. Выход 95%. Т. кип. 170-172oС при 0.5 мм рт.ст. Найдено, %: С 83.48; Н 11.45; N 5.15. C19H31N. Вычислено, %: С 83.45; H 11.43; N 5.12.
2,4-Диметил-6-циклопентиланилин. Выход 98%. Т. кип. 134-136oС при 0.5 мм рт.ст. Найдено, %: С 82.48; Н 10.15; N 7.41. C13H19N. Вычислено, %: С 82.48; Н 10.12; N 7.40.
2,4-Диметил-6-циклогексиланилин. Выход 97%. Т. кип. 133-135oС при 0.5 мм рт.ст. Найдено, %: С 82.73; Н 10.45; N 6.85. C14H21N. Вычислено, %: С 82.70; H 10.41; N 6.89.
2,4-Диметил-6-циклооктиланилин. Выход 98%. Т. кип. 145-147oС при 0.5 мм рт.ст. Найдено, %: С 83.10; Н 10.92; N 6.08. C16H25N. Вычислено, %: С 83.06; Н 10.89; N 6.05.
2,4-Диметил-6-циклододециланилин. Выход 96%. Т. кип. 180-182oС при 0.5 мм рт. ст. Найдено, %: С 83.59; Н 11.60; N 4.85. С20Н33N. Вычислено, %: С 83.56; Н 11.57; N 4.87.
2,6-Бис-[1-(2-метил-6-циклопентилфенилимино)этил] пиридин. Выход 85%. Т. пл. 170-172oС. Найдено, %: С 82.94; Н 8.26; N 8.84. С33Н39N3. Вычислено, %: С 82.97; Н 8.23; N 8.80.
2,6-Бис-[1-(2-метил-6-циклогексилфенилимино)этил] пиридин. Выход 81%. Т. пл. 215-217oС. Найдено, %: С 83.15; Н 8.54; N 8.34. С35Н43N3. Вычислено, %: С 83.12; Н 8.57; N 8.31.
2,6-Бис-[1-(2-метил-6-циклооктилфенилимино)этил] пиридин. Выход 85%. Т. пл. 140-142oС. Найдено, %: С 83.39; Н 9.11; N 7.45. С39Н51N3. Вычислено, %: С 83.37; Н 9.15; N 7.48.
2,6-Бис-[1-(2-метил-6-циклододецилфенилимино)этил]пиридин. Выход 83%. Т. пл. 178-180oС. Найдено, %: С 83.78; Н 10.04; N 6.18. С47Н67N3. Вычислено, %: С 83.75; Н 10.02; N 6.23.
2,6-Бис-[1-(2,4-диметил-6-циклопентилфенилимино)этил]пиридин. Выход 81%. Т. пл. 183-185oС. Найдено, %: С 83.13; Н 8.58; N 8.30. C35H43N3. Вычислено, %: С 83.12; Н 8.57; N 8.31.
2,6-Бис-[1-(2,4-диметил-6-циклогексилфенилимино)этил]пиридин. Выход 82%. Т. пл. 234-236oС. Найдено, %: С 83.27; Н 8.85; N 7.85. C37H47N3. Вычислено, %: С 83.25; Н 8.87; N 7.87.
2,6-Бис-[1-(2,4-диметил-6-циклооктилфенилимино)этил] пиридин. Выход 80%. Т. пл. 128-130oС. Найдено, %: С 83.50; Н 9.43; N 7.10. C41H55N3. Вычислено, %: С 83.48; Н 9.40; N 7.12.
2,6-Бис-[1-(2,4-диметил-6-циклододецилфенилимино)этил] пиридин. Выход 80%. Т. пл. 168-169oС. Найдено, %: С 83.85; Н 10.22; N 5.95. C49H71N3. Вычислено, %: С 83.82; Н 10.19; N 5.98.
2,6-Бис-[1-(2-метил-6-циклопентилфенилимино)этил] пиридин железо(II) хлорид. Выход 88%. Найдено, %: С 65.32; Н 6.25; С1 11.90; N 6.51. С33Н39Сl2FеN3. Вычислено, %: С 65.57; Н 6.50; Cl 11.73; N 6.95.
2,6-Бис-[1-(2-метил-6-циклогексилфенилимино)этил] пиридин железо(II) хлорид. Выход 87%. Найдено, %: С 66.24; Н 6.75; Cl 11.45; N 6.47. С35Н43Сl2FеN3. Вычислено, %: С 66.46; Н 6.85; Cl 11.21; N 6.64.
2,6-Бис-[1-(2-метил-6-циклооктилфенилимино)этил] пиридин железо(II) хлорид. Выход 86%. Найдено, %: С 67.88; Н 7.37; Cl 10.53; N 6.01. С39Н51Сl2FеN3. Вычислено, %: С 68.03; Н 7.47; Cl 10.30; N 6.10.
2,6-Бис-[1-(2-метил-6-циклододецилфенилимино)этил] пиридин железо(II) хлорид. Выход 88%. Найдено, %: С 70.21; Н 8.24; Cl 9.03; N 5.08. С47Н67Сl2FеN3. Вычислено, %: С 70.49; Н 8.43; Cl 8.85; N 5.25.
2,6-Бис-[1-(2,4-диметил-6-циклопентилфенилимино)этил] пиридин железо(II) хлорид. Выход 85%. Найдено, %: С 66.23; Н 6.76; Cl 11.43; N 6.48. C35H43Cl2FeN3. Вычислено, %: С 66.46; Н 6.85; Cl 11.21; N 6.64.
2,6-Бис-[1-(2,4-диметил-6-циклогексилфенилимино)этил] пиридин железо(II) хлорид. Выход 88%. Найдено, %: С 67.04; Н 7.00; Cl 10.95; N 6.18. С37Н47Сl2FеN3. Вычислено, %: С 67.28; Н 7.17; Cl 10.73; N 6.36.
2,6-Бис-[1-(2,4-диметил-6-циклооктилфенилимино)этил] пиридин железо(II) хлорид. Выход 80%. Найдено, %: С 68.52; Н 7.51; Cl 9.99; N 5.68. C41H55Cl2FeN3. Вычислено, %: С 68.71; Н 7.74; Cl 9.89; N 5.86.
2,6-Бис-[1-(2,4-диметил-6-циклододецилфенилимино)этил]пиридин железо(II) хлорид. Выход 83%. Найдено, %: С 70.89; Н 8.50; Cl 8.86; N 4.91. С49Н71Сl2FеN3. Вычислено, %: С 71.00; Н 8.63; Cl 8.55; N 5.07.
2,6-Бис-[1-(2,4-диметил-6-циклогексилфенилимино)этил]пиридин кобальт(II) хлорид. Выход 85%. Найдено, %: С 67.21; Н 6.99; Cl 10.87; N 6.20. С37Н47Сl2CoN3. Вычислено, %: С 67.29; Н 7.16; Cl 10.72; N 6.35.
2,6-Бис-[1-(2-метил-6-циклооктилфенилимино)этил] пиридин кобальт(II) хлорид. Выход 76%. Найдено, %: С 67.65; Н 7.28; Cl 10.70; N 6.01. С39Н51Сl2FеN3. Вычислено, %: С 68.03; Н 7.42; Cl 10.29; N 6.09.
Структуры лигандов подтверждены ИК- и ЯМР- (1Н и 13С) спектроскопией.
В табл. 1 приведены исследованные нами образцы лигандов.
С целью упрощения восприятия используемых в данном изобретении бис(имино)пиридильных комплексов FeCl2 или CoCl2 они обозначены нами символами, приведенными в табл. 1.
Ниже приводятся примеры, иллюстрирующие данное изобретение.
Пример 1.
Полимеризацию этилена проводят в стальном автоклаве с мешалкой емкостью 150 мл, в который загружают 48 мл толуола, 1,5•10-3 моль МАО в 1 мл толуола и 2,5•10-6 моль (IV) в 1 мл толуола.
Полимеризацию проводят в течение 1 часа при температуре 70oС при давлении этилена 0,1 МПа. Процесс прерывают добавлением в реакционную смесь этилового спирта. Полученную суспензию полимера подвергают фильтрации и сушке в вакууме при 60oС. Выход полиэтилена 10,5 г; активность 42000 кг/молькат•ч•МПа; показатель текучести расплава при нагрузке 5 кг I5=0,7 г/10 мин; температура плавления полимера Тпл=138,2oС, теплота плавления ΔН= 199,3 Дж/г.
Примеры 2-13
Опыт проводят по примеру 1, но в условиях, представленных в табл. 2. Полученные результаты также отражены в табл. 2.
Примеры 14-24 (контрольные опыты)
Опыты проводят по примеру 1, но условия их осуществления описаны в табл. 3. Полученные результаты также отражены в табл. 3.
Таким образом, как показано в примерах 1-13, бис(имино)пиридильные комплексы на основе хлорида железа (примеры 1-11) и хлорида кобальта (примеры 12, 13), имеющие в качестве заместителей в орто-положении арильного кольца циклоалкильные группы с числом атомов углерода 6 или выше (в конкретных примерах - циклогексил, циклооктил, циклододецил), R3=Me, Et, i-Pr (в примерах R3= Me) и R4=Н или Me (в примерах R4=Н или Me), термостабильны с сохранением высокой активности при температурах полимеризации 70-80oС, а полученный ПЭВП имеет повышенные значения ММ.
Контрольные примеры 14-24 показали, что в том случае, когда R2=циклогексил, но R3= Н или циклогексил (см. примеры 17-20), катализаторы теряют свою активность при 70-80oС, а при 50oС дают возможность получить низкомолекулярные полимеры с низким выходом (см. примеры 23, 24). Если в качестве R2 используется циклопентильная группа (С5), а R3 и R4 аналогичны патентуемым катализаторам, то активность таких систем и молекулярные характеристики полученного полиэтилена близки к данным прототипа и [2] (см. примеры 14-18), т.е. при температурах 70-80oС резко снижается их активность и ММ полимера.
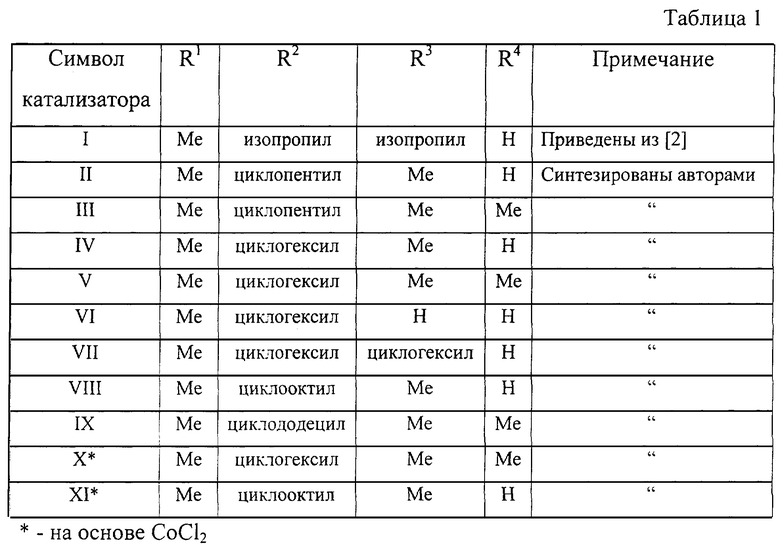

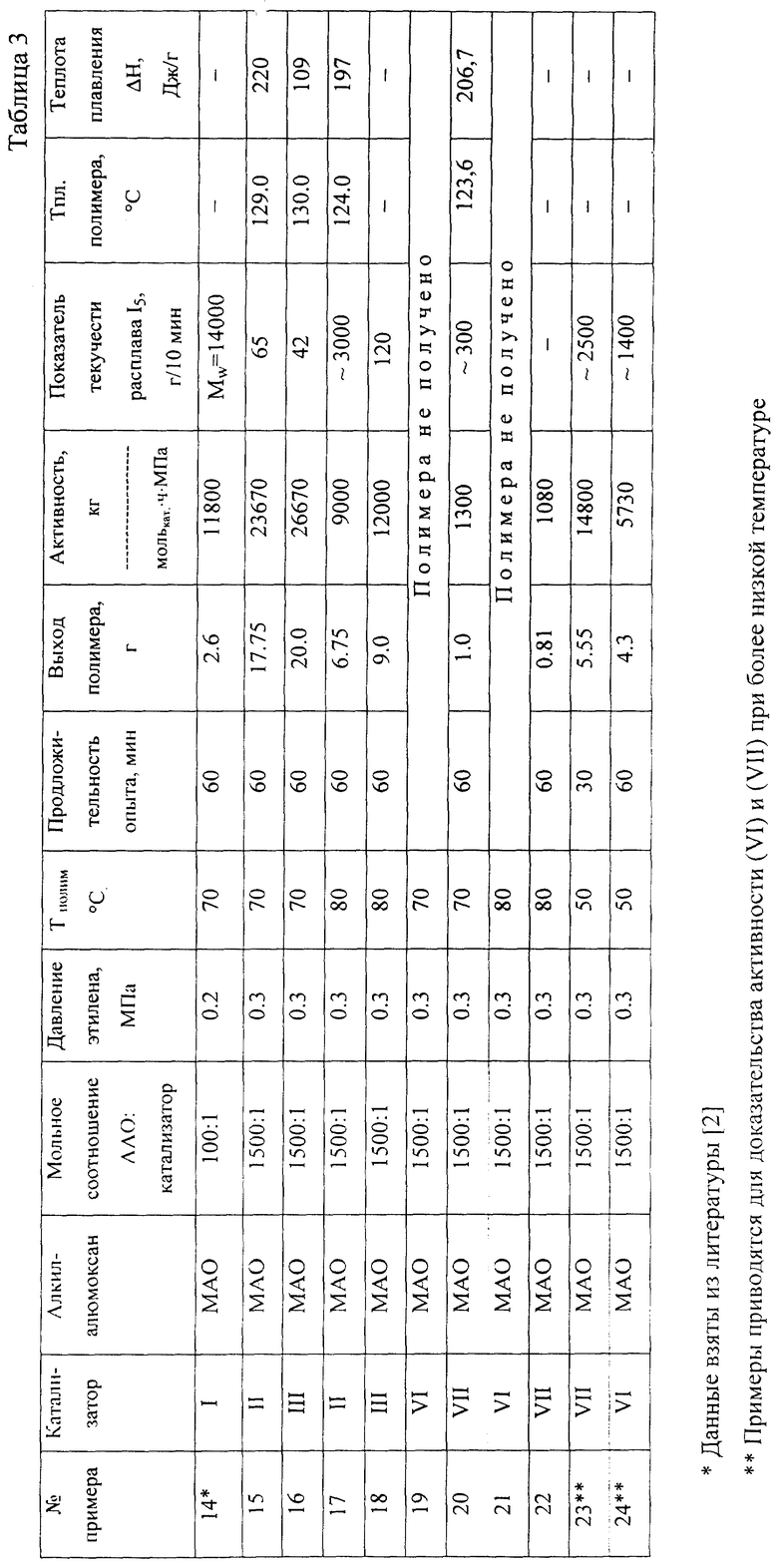
ПЭВП с различными молекулярными и термическими характеристиками получают в суспензионном режиме полимеризации при 70-80oС, давлении 0,1-1,5 МПа под действием новых 2,6-бис(имино)пиридильных комплексов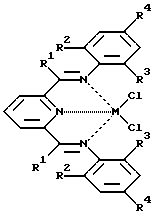
где М= Fe+2, Со+2; R1 - метил; R3 - водород, метил, этил или изопропил; R4 - водород или метил; R2 - циклоалкил с числом атомов углерода не менее 6; и алкилалюмоксана. В качестве углеводородных растворителей используют толуол, н-гексан, бензин и др. Изобретение решает задачу синтеза новых гомогенных катализаторов, сохраняющих свою активность при повышенных температурах полимеризации. 3 табл.
Катализатор полимеризации этилена, включающий бис(имино)-пиридильный комплекс общей формулы (1)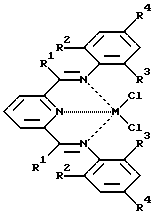
где М= Fe+2, Со+2; R1 - метил; R3 - водород, метил, этил или изопропил; R4 - водород или метил, и алкилалюмоксан, отличающийся тем, что в качестве бис(имино)пиридильного комплекса он содержит соединение общей формулы (1), где R2 - циклоалкил с числом атомов углерода не менее 6.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| WO 00/15646 А1, 23.03.2000 | |||
| DE 19741989 А1, 25.03.1999. | |||
Авторы
Даты
2002-12-10—Публикация
2001-09-25—Подача