Изобретение относится к медицине, точнее - к фармакологии, конкретно - к синтетическим биологически активным производным пиримидина.
Заявляемые вещества имеют выраженное противовирусное, иммуностимулирующее (интерферон-индуцирующее), антихламидийное, противотуберкулезное, психодепрессивное, анальгезирующее и гепатопротекторное действие.
Соединения предназначены, в основном, для использования в медицинской практике для лечения вирусных инфекций, инфекций, вызванных хламидиями, заболеваний, сопровождающихся иммунодефицитом, в частности злокачественных новообразований, а также туберкулеза. Кроме того, указанные соединения могут быть использованы для тех же целей в ветеринарии.
Как известно, одну из наиболее серьезных проблем современной медицины представляют микробные и вирусные заболевания, многие из которых крайне плохо поддаются лечению, что связано как с недостаточной эффективностью существующих препаратов, так и быстрой изменчивостью микробов, приводящей к появлению устойчивых форм [1, 2, 8].
Часто вирусные заболевания протекают на фоне снижения активности иммунной системы организма и сопровождаются вторичными инфекциями, это же относится и к онкологическим заболеваниям. Поэтому проблема разработки эффективных противовирусных и противоопухолевых препаратов тесно связана с поиском средств лечения иммунодефицитных состояний различного происхождения.
Известные противовирусные препараты можно условно разделить на 2 группы по типам механизмов их действия. Действие препаратов первой группы связано с подавлением репродукции вирусов в организме [1]. Противовирусные препараты второй группы оказывают эффект не столько за счет воздействия на сами вирусы, сколько за счет стимуляции иммунной защиты организма и усиления выработки эндогенных интерферонов [2]. Интерфероны и их индукторы используются также для лечения ряда опухолевых заболеваний [3]. Заявляемые вещества относятся к препаратам второй группы.
Химическими аналогами заявляемых соединений могут быть R-аминоурацилы нижеприведенной общей формулы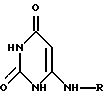
где R = фенил, 2-метилфенил, 3-метилфенил, 4-метилфенил, 4-бромфенил, 2,4-диметилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 2-хлорфенил, 3-хлорфенил, 1-нафтил, 2-нафтил, циклогексил. Они описаны, например, в работе [9].
Наиболее близким по химической природе к заявляемому является - 6-[[3-[4-(2-Метоксифенил)-1-пиперазинил] пропил] -амино] -1,3-диметилурацил. Его фармацевтическое название - урапидил.
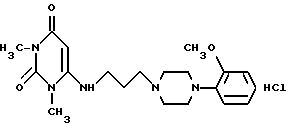
6-[[3-[4-(2-Метоксифенил)-1-пиперазинил]пропил]-амино]-1,3-диметилурацил - оказывает гипотензивное действие. В основном препарат применяют для снижения артериального давления при гипертонических кризах. Он подробно описан в работе [10].
К сожалению, спектр его биологической активности сравнительно узок.
Задачей изобретения является получение новых химических соединений, обладающих более широкой биологической активностью, в том числе противовирусной активностью (по отношению к вирусам простого герпеса), иммуностимулирующей активностью (за счет индукции выработки эндогенных интерферонов в организме), антимикробной активностью, психодепрессивным, анальгезирующим и гепатопротекторным действиями. Другими словами, задача изобретения сводится к химическому синтезу биологически активных веществ, превосходящих прототип по биологической активности, а также по широте действия.
Поставленная задача решается путем синтеза новых веществ - 2,4-диоксо-5-арилиденимино-1,3-пиримидинов общей формулы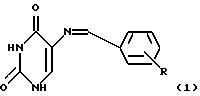
где R выбран из группы: Н, ОН, алкоксил, галоген, нитро, диалкил, арил и 3,4-диоксолано.
Перечень всех 25 синтезированных и идентифицированных веществ приведен в табл. 1.
Перечисленные в табл. 1 вещества новы, поскольку они неизвестны из доступных источников информации.
Наличие широкого спектра эффективной биологической активности заявленных веществ не вытекает явным образом из предшествующего уровня техники, т.е. неочевидно для специалиста.
Сущность изобретения поясняют приведенные далее:
- способ получения всех 25 соединений I-XXV;
- пример синтеза 2,4-диоксо-5-(2-гидрокси-3,5-дихлорбензилиден)имино-1,3-пиримидина;
- данные ПМР спектроскопии соединений I-XXV (табл. 2);
- данные экспериментов по определению биологической активности заявляемых соединений в сопоставлении с известными эффективными современными средствами того же назначения, а именно:
эксперимент 1 - определение действия заявляемых соединений на вирус простого герпеса (с табл. 3);
эксперимент 2 - определение интерферониндуцирующей активности заявляемых соединений (с табл. 4);
эксперимент 3 - определение действия заявляемых соединений на Cnlamydia_ trachomatis (с табл. 5);
эксперимент 4 - определение антимикробного действия соединений (с табл. 6);
эксперимент 5 - определение психодепрессивного действия заявляемых соединений (с табл. 7);
эксперимент 6 - оценка анальгезирующей активности заявляемых соединений (с табл. 8);
эксперимент 7 - гепатопротекторное действие заявляемых соединений (с табл. 9);
эксперимент 8 - определение максимальной переносимой дозы (с табл. 10).
Способ получения соединении I-ХХV.
Целевые 2,4-диоксо-5-арилиденимино-1,3-пиримидины получают взаимодействием 5-аминоурацила с соответствующими альдегидами (смотри R). В качестве растворителя используют смесь этанол - вода 1:1. При кипячении смеси альдегида с аминоурацилом выпадает бесцветный кристаллический осадок.
Продукты получают с выходами 45-95% от теоретического.
Пример синтеза 2,4-диоксо-5-(2-гидрокси-3,5-дихлорбензилиден)имино-1,3-пиримидина.
В колбу помещают 1.27 г 5-аминоурацила, 150 мл воды. Смесь нагревают при перемешивании до полного растворения осадка. Параллельно в 50 мл этанола растворяют 1.91 г 3,5-дихлорсалицилового альдегида и добавляют к раствору 5-аминоурацила. Сразу же выпадает осадок ярко-оранжевого цвета. Реакционная смесь кипит при перемешивании в течение 1 ч и еще 1 ч перемешивание продолжают при комнатной температуре. Затем реакционную смесь оставляют на ночь. Полученный осадок отфильтровывают, промывают теплой водой, спиртом, высушивают. Выход продукта составляет 92%.
Остальные заявляемые соединения синтезируют аналогично, используя другие R.
Заметная разница только в выходе целевого продукта.
Соединения общей формулы представляют собой бесцветные или ярко окрашенные кристаллические вещества, растворимые в диметилсульфоксиде, пиридине. Температуры плавления всех веществ превышают 300oС.
Индивидуальность веществ доказана методом тонкослойной хроматографии на пластинках Silufol UV-254, элюент четыреххлористый углерод - изопропанол = 9:1. Структура синтезированных веществ доказана методом ПMP спектроскопии.
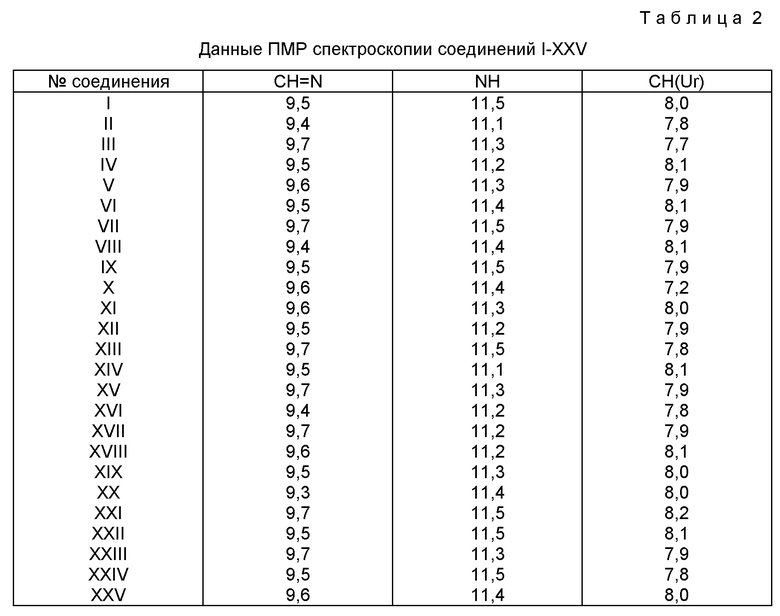
Данные ПМР спектроскопии соединений I-XXV приведены в табл. 2.
В ПМР спектрах характерен вырожденный сигнал двух протонов иминогрупп в урацильном кольце (в табл. 2 представлено усредненное значение химического сдвига).
Данные экспериментов по определению биологической активности заявляемых соединений.
Эксперимент 1. Определение действия заявляемых соединений на вирус простого герпеса.
Антивирусная активность изучалась по отношению к вирусу простого герпеса I типа (ВПГ-I /Ленинград/248/88) по общепринятому методу [5]. Вирусы выращивали на перевиваемой культуре клеток Vero, полученной из банка клеточных культур Института цитологии РАН.
Схема постановки опыта.
К клеткам, выращенным на среде RPMI-1640 с 10% сыворотки плода коровы и помещенным в лунки 96-луночного планшета, добавляли вирус в конечной концентрации 102 ТИД50/мл и заявляемые соединения, растворенные в ДМСО, в конечной концентрации 100, 10 и 1 мг/л. Для каждой испытанной концентрации препарата использовали 5 независимых лунок. Планшет инкубировали в течение 60 мин при 37oС в СO2-инкубаторе. После инкубации вирус удаляли и снова вносили свежую среду, содержащую заявляемые соединения в использованных концентрациях.
Результаты оценивали по наличию цитопатогенного действия вируса на клетки через 36 часов культивирования при 37oС в СО2-инкубаторе.
В опыте были использованы следующие контроли:
1. Контроль культуры клеток (способность к нормальному росту).
2. Контроль вируса (оценка способности к репродукции).
3. Контроль антивирусной активности противовирусного препарата - ацикловира.
4. Контроль соединений (токсичность соединений).
5. Контроль растворителя (ДМСО) на токсичность.
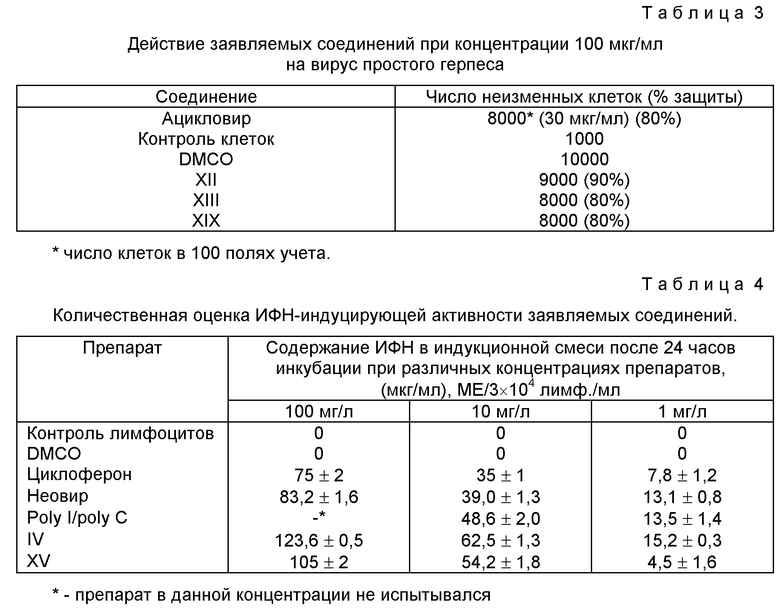
Для оценки цитопатического действия вируса подсчитывали число неизмененных клеток в 100 полях, образованных специальной сеткой окуляр-микрометра инвертированного микроскопа. Полученные результаты представлены в табл. 3.
Полученные результаты указывают, что приведенные в табл. 3 заявляемые соединения обладают антигерпетической активностью, сравнимой с таковой у стандартного препарата ацикловира. Остальные заявляемые соединения имели менее выраженную активность в подавлении репродукции вируса герпеса в выбранных условиях эксперимента.
Эксперимент 2. Определение интерферониндуцирующей активности заявляемых соединений.
Индукцию синтеза интерферонов заявляемыми препаратами проводили на первичной культуре человеческих лимфоцитов (именно данные клетки в организме человека являются основными продуцентами интерферонов). Для получения культуры лимфоцитов использовали свежую (12 часов после забора) кровь здоровых доноров (не второй группы). Для выделения лимфоцитов гепаринизированная кровь, полученная от здорового донора, подвергалась центрифугированию в градиенте плотности фиколл-верографин 1.71 г/см3 для выделения фракции иммунокомпетентных клеток. Указанная фракция отбиралась и разводилась питательной средой RPMI-1640, содержащей 5% сыворотки плода коровы, 0.3 мг/мл L-глутамина, 100 ед/мл пенициллина, 50 мг/л стрептомицина. Концентрацию лимфоцитов учитывали после окрашивания метиленовым синим и подсчета количества клеток в камере гемоцитометра. Исходные растворы заявляемых веществ разводили питательной средой RPMT-1640 так, чтобы конечные концентрации веществ составляли ряд: 100 мг/л, 10 мг/л, 1 мг/л после внесения суспензии лимфоцитов. Конечная концентрация лимфоцитов в индукционной смеси составила 3•106 клеток/мл. Параллельно с опытными пробами проставлялись следующие контроли:
1. Контроль спонтанной продукции интерферонов (ИФН) лимфоцитами.
2. Контроль протекания процесса при воздействии стандартизированного индуктора ИФН N-метил-N-(а, D-глюкопиранозил)аммоний-10-метиленкарбоксилат акридона (циклоферон).
3. Контроль протекания процесса при воздействии стандартизированного индуктора ИФН - Неовира (натрия 10-метиленкарбоксилат-9-акридон) с соответствующим содержанием DMCО в опытных пробах.
4. Контроль спонтанной продукции интерферонов в присутствии DMCO в количестве, соответствующем испытуемым образцам.
Контрольные и опытные образцы инкубировали 24 часа при 37oС. После инкубации пробы центрифугировались при 2000 g для осаждения клеточных элементов и из проб отбирался ИФН-содержащий супернатант, который анализировали на количественное содержание ИФН. Осадок клеток ресуспендировали в прежнем объеме питательной среды, окрашивали витальным красителем - трипановым синим и подсчитывали число клеток в камере гемоцитометра (как описано выше) для определения цитотоксического действия препаратов. Количественное определение содержания ИФН в контрольных и опытных образцах производили с использованием иммуноферментной тест-системы на ИФН производства ТОО "Протеиновый контур" РrоСоn IF2 plus. Для определения количества интерферона в пробе использовали твердофазный иммуноферментный метод с использованием пероксидазы хрена в качестве индикаторного фермента. Активность связанной пероксидазы измеряли с использованием автоматического фотометра для микропланшетов с микропроцессором при длине волны 450 нм.
Для подсчета результатов параллельно определяли активность ИФН у стандартных растворов ИФН, содержащих известное количество препарата. На основании полученных результатов строилась калибровочная кривая, позволяющая при использовании микропроцессора автоматического фотометра получать данные, выраженные в Международных Единицах активности (МЕ). Результаты анализа выражаются в ME активности ИФН на мл в данной индукционной системе, содержащей 3•106 лимфоцитов/мл. Каждая опытная и контрольная точка исследовалась в 4-х параллелях.
Контроли иммуноферментной реакции:
1. Контроль DMCO с питательной средой.
2. Контроль компонентов системы (согласно инструкции).
Все результаты учитывались только при соответствии контролей паспортным данным системы.
Полученные результаты подвергались статистическому анализу по t-критерию и расчетом доверительного интервала при р=0.05. Произведен анализ сходимости результатов в параллельных опытах.
В результате проведенных исследований установлено, что среди заявляемых соединений имеются пробы, обладающие способностью индуцировать синтез ИФН (табл. 4).
Остальные соединения показали меньшую активность.
Эксперимент 3. Определение действия заявляемых соединений на Chlamydia trachomatis.
Антимикробную активность заявляемых соединений изучали по отношению к C. trachomatis D323 - стандартному штамму из коллекции кафедры микробиологии С. -Петербургского Государственного медицинского университета им. ак. И.П. Павлова. Данный штамм был выделен от больного с хламидийным уретритом, имеет морфологию и физиологическую активность, характерную для представителей данного вида, чувствителен к действию препаратов, используемых для лечения хламидийной инфекции.
В работе использованы клеточные культуры МсСоу и L929, полученные из Банка клеточных культур Института цитологии РАН.
Схема постановки опыта.
Клетки выращивали во флаконах из нейтрального стекла в среде RPMI-1640 с добавлением 10% сыворотки плода коровы. Опыт ставили в стеклянных (лишенных токсичности) плоскодонных флаконах с покровными стеклами. Клетки вносили в среду в конечной концентрации 1•106 кл/мл. После получения монослоя в пробирки вносили стандартные заражающие дозы хламидий, хранящиеся в замороженном состоянии при -70oС. Одновременно к клеткам добавляли испытуемые соединения в конечной концентрации 100 мг/л. Пробу центрифугировали при 2400 g в течение 60 минут при комнатной температуре и инкубировали при 37oС в течение 2 часов. После этого меняли питательную среду на новую, содержащую 5% сыворотки плода коровы и циклогексимид (2 мкг/мл) с повторным внесением заявляемых соединений в той же концентрации. Параллельно дублировали пробы, используя среду без циклогексимида, чтобы исключить его влияние на изучаемые субстанции. Пробы инкубировали в течение 48 часов в СО2-инкубаторе при 37oС.
Контроли включали:
1. Контроль культуры клеток.
2. Контроль действия растворителей.
3. Контроль действия хламидий в отсутствие каких бы то ни было препаратов.
4. Контроль чувствительности хламидий к стандартному антимикробному препарату - ципрофлоксацину.
5. Контроль испытуемых соединений на токсичность по отношению к культурам клеток.
Оценку результатов проводили путем выявления хламидийных цитоплазматических включений с помощью метода иммунофлюоресценции (MicroТrac Chlamydia trachomatis Direct Specimen Test) и хламидийных антигенов с помощью CylaMonoScreen (Russian-British Joint Venture 66 Regent's Parс Road London NW1 7SX) [6, 7]. Эффект действия препарата определяли, анализируя состояние монослоя и число клеток с ЦПВ по сравнению с контролем (культура клеток, зараженная C. trachomatis D323) при этом учитывали число неизмененных клеток в 100 полях зрения, полученных при использовании окуляр-микрометра.
Результаты контрольных проб, удовлетворяющие требованиям эксперимента:
контроль культуры клеток - морфология клеток и состояние монослоя соответствуют данному типу клеток;
контроль роста хламидий в культуре клеток - наличие ЦПВ в монослое;
контроль действия стандартного антимикробного препарата - уменьшение числа ЦПВ в монослое по сравнению с предыдущим контролем;
контроль токсичности заявляемых соединений - токсичность отсутствует;
контроль действия растворителей - токсическое действие на клетки отсутствует.
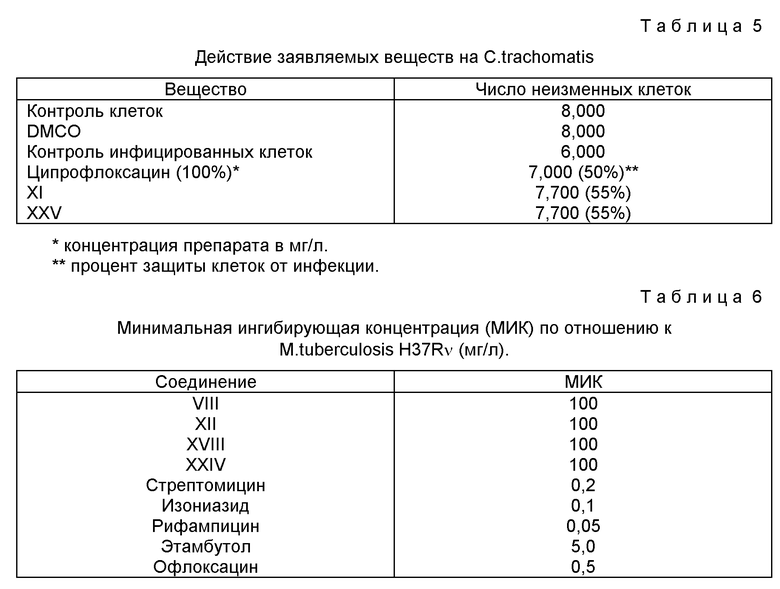
Результаты проведенных испытаний представлены в табл. 5.
Полученные данные свидетельствуют, что заявляемые соединения XI и XXV, приведенные в табл. 5, обладают выраженной активностью против хламидий, превосходящей таковую у стандартного препарата - ципрофлоксацина.
Остальные заявляемые соединения обладают менее выраженной активностью по защите клеток от хламидий в выбранных условиях эксперимента.
Эксперимент 4. Определение антимикробного действия соединений.
Для определения антимикробной активности был использован стандартный штамм Mycobacterium tuberculosis Н37Rv, чувствительный ко всем антимикробным препаратам. Оценку антимикробактериального действия проводили методом серийных разведений.
Соединения растворяли в диметилсульфоксиде (ДМСО) и титровали в среде N-1 так, что данный препарат содержался в отдельных пробирках со средой в концентрациях от 200 до 0.025 мг/л. Концентрация препарата в среде соседних пробирок отличалась в два раза. В контроле использовали ДМСО, который титровали так же, как и препарат. Результат учитывали после 72-часового культивирования бактерий при 37oС.
M. tuberculosis H37Rv выращивали на среде Сотона, содержащей 10% лошадиной сыворотки, и плотность микробной суспензии при засеве составляла 50•106 КОЕ.
В качестве контроля были использованы известные туберкулостатические препараты. Результаты, полученные для использованного штамма, приведены в табл. 6.
Приведенные в табл. 6 данные показывают, что испытанные соединения обладают антимикробной активностью по отношению к использованному штамму М. tuberculosis в концентрации 100 мг/л.
Остальные заявленные соединения показали меньшую активность.
Эксперимент 5. Определение психодепрессивного действия заявляемых соединений.
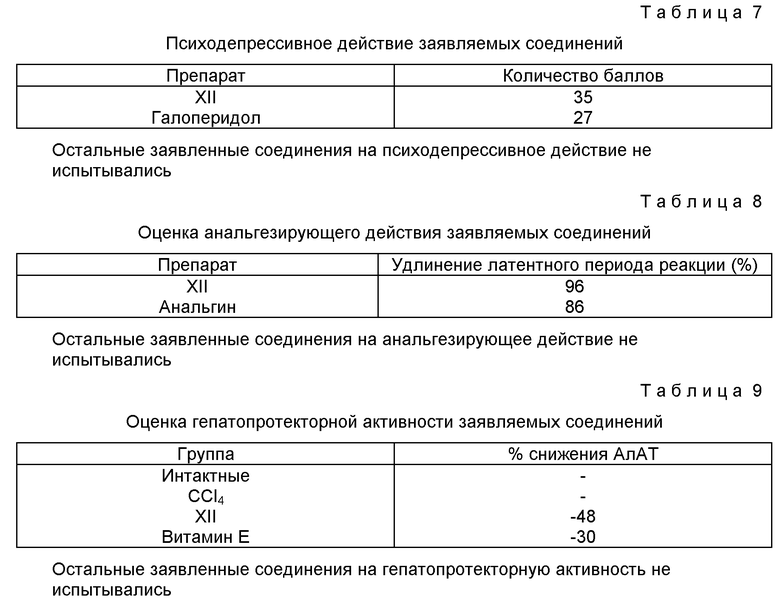
В опытах на мышах оценивали 10 параметров, указывающих на возможное развитие депрессии поведения. Каждый параметр оценивали в 2 балла для каждой мыши с неизмененным поведением. Общая сумма баллов составляла 60 (2 х 10 х 3 мыши). Уменьшение количества баллов ниже 40 через 1 час после перорального введения препарата (300 мг/кг) указывало на значимую депрессию поведения. В качестве препарата сравнения использовали галоперидол (см. табл. 7). Остальные заявленные соединения на психодепрессивное действие не испытывались.
Эксперимент 6. Оценка анальгезирующей активности заявляемых соединений.
В группе из 3 мышей оценивали время, необходимое для отдергивания хвоста, помещенного под направленный источник теплового излучения. Удлинение времени реакции более чем на 50% после внутрибрюшинного введения препарата (30 мг/кг) указывало на наличие анальгезирующей активности. В качестве препарата сравнения использовали анальгин (2 мг/кг) (см. табл. 8). Остальные заявленные соединения на анальгезирующее действие не испытывались.
Эксперимент 7. Гепатопротекторное действие заявляемых соединений.
Крысам подкожно вводили 50%-ный раствор ССl4 на оливковом масле (1 мл/кг). Исследуемые вещества применяли перорально в дозе 20 мг/кг за 30 минут до и через 7 часов после введения ССl4. Через сутки в крови животных определяли активность аланинаминотрансферазы (АлАТ) - маркерного фермента повреждения печеночной паренхимы. Уменьшение ферментемии более 30% по сравнению с группой контроля расценивали как наличие гепатопротекторных свойств препарата. В качестве препарата сравнения использовали витамин Е в дозе 100 мг/кг (см. табл. 9). Остальные заявленные соединения на гепатопротекторную активность не испытывались.
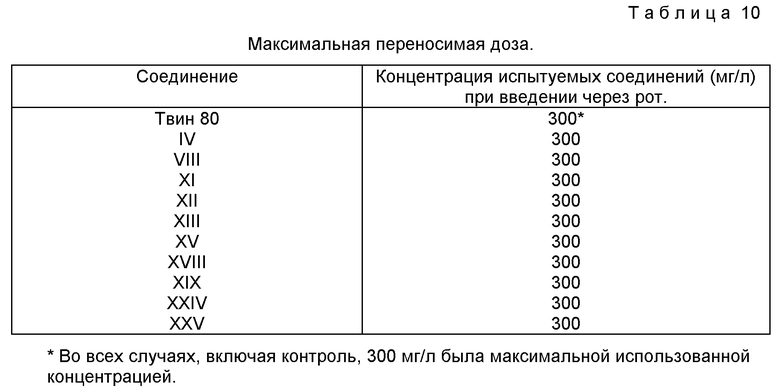
Эксперимент 8. Определение максимальной переносимой дозы.
Испытуемое соединение вводили перорально с помощью желудочного зонда (300 мг/кг) или внутрибрюшинно (100 мг/кг) белым нелинейным мышам массой 18-20 г (по 3 самца и 3 самки в каждой из испытуемых групп), после чего наблюдали за их состоянием на протяжении 72 часов. Отсутствие симптоматики, свойственной токсическим эффектам, и отсутствие гибели животных в течение указанного времени позволяет сделать вывод о низкой токсичности изучаемого соединения. При наличии острых токсических эффектов доза уменьшается до выявления максимальной переносимой дозы [4] (см. табл. 10).
Полученные результаты свидетельствуют, что при приеме через рот испытанные соединения в концентрации 300 мг/кг не обладают острой токсичностью для мышей.
Остальные заявленные соединения на токсичность не испытывались.
Промышленная применимость
Приведенные выше примеры и практические результаты синтеза и анализа заявляемых соединений подтверждают возможность лабораторного и промышленного синтеза заявляемых соединений средствами, освоенными современной фармацевтической промышленностью, а также их строгую идентификацию общепринятыми методами контроля.
Серия экспериментов по определению биологической активности, представленная в отчетах, показала, что заявляемые соединения обладают выраженными биологическими активностями - противовирусной по отношению к вирусу простого герпеса, интерферониндуцирующей и противохламидийной, а также антимикробным, психодепрессивным, анальгезирующим и гепатопротекторным действием.
Приведенные факты доказывают достижение задач, поставленных изобретением: синтезированы новые соединения, обладающие низкой токсичностью и ярко выраженным широким спектром биологического действия.
Таким образом, по нашему мнению, заявляемые вещества удовлетворяют всем требованиям, предъявляемым к изобретению: они новы, неочевидны и промышленно применимы.
Литература
1. Chatis P.A., Crumpacker C.S. Resistance of herpesviruses to antiviral drugs. Antimicrob. Agents Chemother. 1992; 36: 1589-1595.
2. Pharmaceutical microbiology, Ed. by W.B. Hugo and A.D. Russel Blackwell Scientific Publications, Oxford, 1987, 511 p.
3. Esteban M. , Раez E. Antiviral and antiproliferartive properties of interferons: mechanism of action. Prog. med. virol. 1985, 32: 159-173.
4. Irwin S., Psychopharmacology, 1968, 13, p. 222-257.
5. Gentry G.A., Lawrency N., Lushbaugh N. Isolation and differentiation of Herpes simplex virus and Trichomonas vaginalis in cell culture, J. of Clinical Microbiology 1985, Vol. 22. No. 2. P. 199-204.
6. Wang S-P., Grayston J.T. Serotyping of Clamydia tracliomatis by inderect fluorescent-antibody staining of inclusions in cell culture with monoclonal antibodies. J. of Clinical Microbiology, 1991. Vol. 29. No. 7. P. 1295-1298.
7. Judson B. A., Lambert P.P. Improved Syva MicroTrac Clamydia trachomatis direct test method, Journal of Clinical Microbiology, 1988, Vol. 26, No. 12. P. 2657-2658.
8. Grosset J., Current problems with tuberculosis treatment, Res. Microbiology. 1996, Vol. 147, No. 10-16.
9. Goldner, Dietz, Carstens // Ann. Chem, 1966, 691, p. 142; Ann. Chem., 1966, 698, р. 145, Ann. Chem., 1966, 699, р. 145.
10. Машковский М. Д. Лекарственные средства. В двух частях. Ч.1. - M.: Медицина, 1993, с. 550 - прототип.

Изобретение относится к новым 2,4-диоксо-5-арилиденимино-1,3-пиримидинам общей формулы I, где R независимо выбран из группы: Н, ОН, низший алкоксил, галоген, нитро, ди(низший)алкиламино, n = 1-3, или два близлежащих R вместе бензольным кольцом, к которому они присоединены, при n = 2, 4 образуют бензо, дибензо и при n = 2 образуют 3,4-диоксолановое кольцо. Указанные соединения обладают противовирусным, иммуностимулирующим, антихламидийным, противотуберкулезным, психодепрессивным, анальгезирующим и гепатопротекторным действием и могут найти применение в фармацевтической промышленности. Наиболее предпочтительными являются соединения общей формулы I, где R = Н, n = 1, или R = 4-Сl, n = 1, или R = 3-Сl, n = 1, или R = 2-Сl, n = 1, или R = 4-Br, n = 1, или R = 4-ОН, n = 1, или R = 2,4-(OH)2, n = 2, или R = 2-OH, 5-Br, n = 2, или R = 2-ОН,5-Сl, n = 2, или R = 4-F, n = 1, или R = 2,4-Cl2, n = 2, или R = 2-OH, 3,5-Cl2, n = 3, или R = 2-ОН, 3,5-Вr2, n = 3, или R = 4-ОСН3, n = 1, или R = 4-ОН, 3-ОСН3, n = 2, или R = 4-NO2, n = 1, или R = 3-NO2, n = 1, или R = 2-NO2, n = 1, или R = 2-OH, 5-NO2, n = 2, или R = 2-ОН, 5,6-бензо, n = 3, или R = 3,4-диоксолано, n = 2, или R = 2-NO2, 4,5-диоксолано, n = 3, или R = 2,3,5,6-дибензо, n = 4, или R = 2-OH, 3,5-I2, n = 3 или R = 4-N(СН3)2, n = 2. 25 з.п. ф-лы, 10 табл.
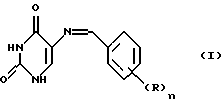
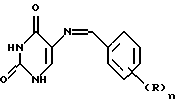
где R независимо выбран из группы: Н, ОН, низший алкоксил, галоген, нитро, ди(низший)алкиламино;
n= 1-3, или два близлежащих R вместе бензольным кольцом, к которому они присоединены, при n=2,4 образуют бензо, дибензо и при n=2 образуют 3,4-диоксолановое кольцо.
| SU 1591984 A1, 15.09.1990 | |||
| US 3361745 А, 02.01.1968 | |||
| US 3048588 A, 07.08.1962. |
Авторы
Даты
2003-02-10—Публикация
1998-12-04—Подача