Изобретение относится к медицине, а именно к внутренним болезням, и может быть использовано для объективной оценки обострения и тяжести течения хронического панкреатита с внешнесекреторной недостаточностью (ХП).
Известны следующие способы диагностики ХП.
Методы исследования экзокринной функции поджелудочной железы, которые условно можно разделить на прямые и непрямые. Прямые методы исследования основаны на определении секреции ферментов и электролитов непосредственно в дуоденальном содержимом или в чистом панкреатическом соке до и после применения раздражителей секреции, к ним относятся: тест Лунда, секретин-холецистокининовый тест, исследование дуоденального содержимого после двойной стимуляции ПЖ, исследование чистого панкреатического сока, исследование протеолитической, липолитической и амилолитической активности в содержимом двенадцатиперстной кишки; к непрямым методам можно отнести: копроскопию, панкреато-лауриновый тест, тест с ПАБК, определение активности эластазы и химотрипсина в крови, определение изоферментов в крови (Дегтярева И.И. Панкреатит. - Киев: Здоровья, 1992. - С. 64-117. Евтихов P.M. с соавт. Механическая желтуха. - Москва, 1999. - С. 196-205).Также можно выделить методы исследования внутрисекреторной функции поджелудочной железы, которые являются лишь дополнительными диагностическими тестами для выявления расстройств углеводного обмена при ХП.
К недостаткам всех вышеперечисленных методов можно отнести то, что они трудно выполнимы, инвазивны, а следовательно, это ограничивает возможность их применения в период обострения, недостаточно точны, специфичны и низко чувствительны.
Общепринятая оценка острофазовости ХП: лейкоцитоз с палочкоядерным сдвигом влево, гипербилирубинемия, увеличение в сыворотке крови щелочной фосфатазы, ГГТФ недостаточно специфичны и могут свидетельствовать о реактивном гепатите и других заболеваниях, что затрудняет дифференциальную диагностику и постановку диагноза обострения ХП.
Прототипом изобретения является способ диагностики хронического панкреатита, заключающийся в том, что в сыворотке крови определяют амилазу, липазу, трипсин, поскольку при обострении ХП наблюдается усиленное поступление панкреатических ферментов (амилазы, липазы, трипсина) в кровь, так называемое явление "уклонения" ферментов, обусловленное нарушением целостности паренхимы железы и застоем секрета в каком-либо участке системы панкреатических протоков (Под. ред. Карпищенко А.И. Медицинская лабораторная диагностика //СПб. - 1997. - С. 63-66. Дегтярева И.И. Панкреатит. -Киев: Здоровья, 1992. - С. 73-95).
Однако данный способ недостаточно точен, поскольку, например, при выраженном фиброзе поджелудочной железы, особенно при фиброзно-склеротическом ХП, уровень ферментов в сыворотке крови может быть нормальным у большей части больных даже в период обострения.
Данный способ не может считаться достаточно специфичным, поскольку амилаза и липаза не являются панкреатоспецифичными ферментами, так, амилаза содержится в слюнных железах, толстой кишке, скелетных мышцах, почках, легких, яичниках, маточных трубах (Дегтярева И.И. Панкреатит. - Киев: Здоровья, 1992. - С. 73), вследствие чего возможно повышение ее уровня при множестве заболеваний. К тому же корреляция между тяжестью панкреатита и амилаземией в ряде случаев не определяется.
Специфичность исследования по данным разных авторов составляет 5,5-99% (Руководство по гастроэнтерологии / Под общ. ред. Ф.И. Комарова, А.Л.Гребнева. - М., 1996. - Т.3; Творогова М.Г., Волкова Е.И., Коткина Е.И. и др. // Лаб. дело. - 1989. - 2. - С. 44-48.; Bockus Gastroenterology. - 5-th ed. - Philadelphia, 1995. - Vol.4. - P.2815-3001.; Meizi d'Ervil G.V., Bosoni Т., Moratti R. et al. // Eur. J. din Chem. clin. Biochem. - 1992. - Vol.30, 7. - P.439-444. Ventrucci M., Pezzilli R., Garulli R. et al. // Ital. J. Gastroent. - 1994. Vol.26, 3. - P.132-136).
Чувствительность определения амилазы связана с кратковременностью гиперамилаземии при атаках ХП, поскольку уровень амилазы начинает повышаться через 2-12 от начала заболевания (обострения), достигая максимума через 20-30 часов, нормализуется через 2-4 суток при благоприятном течении заболевания (Амелюшкина В.А., Аруказву X.Э., Творогова М.Г. и др. // Лаб. дело. - 1991. - 8. - С. 19-24).
Большое значение в диагностике панкреатитов придают определению активности трипсина в сыворотке крови, так как этот фермент продуцируется только ацинарными клетками ПЖ, т.е. является панкреатоспецифичным. Таким образом, теоретически трипсин сыворотки крови должен быть высокочувствительным и строго специфичным тестом для заболеваний ПЖ.
Однако на практике достоверность исследований оказывается ниже из-за связывания активного трипсина ингибиторами. Так, в ткани ПЖ присутствуют ингибиторы Казаля, Кунитца-Нортропа, мезотрипсин (Геллер Л.И., Пашко М.М. // Врач. дело. - 1990. - 3. - С. 86-88. Дегтярева И.И. Панкреатит/ - Кие: Здоровья, 1992. - С. 64-117), предохраняющие панкреациты от аутолиза в случае внутриорганной активации протеаз. Поступивший в сыворотку активный трипсин немедленно связывается плазменными ингибиторами, основными из которых являются α1-антитрипсин и α2-макроглобулин (Богер М.М. Методы исследования поджелудочной железы. - Новосибирск, 1982.; Бышевский A.Ш, Терсенов О. А. Биохимия для врача. - Екатеринбург, 1994).
Определение содержания этих ингибиторов в сыворотке крови также используют для диагностики ХП, однако их показатели разнонаправлены, не всегда возможна четкая трактовка результатов (Циммерман Я. С. Очерки клинической гастроэнтерологии. - Пермь, 1992. - С. 62-68). Таким образом, сывороточные протеазно-ингибиторные соотношения не отражают этих соотношений в ткани ПЖ, а следовательно, не могут ориентировать врача в отношении формы, тяжести, а в ряде случаев и диагноза панкреатита.
В крови циркулируют ферментативно неактивный трипсиноген, комплексы трипсина с α1-антитрипсином и ферментативно активные комплексы трипсина и α2-макроглобулина. Поэтому биохимические методы, основанные на расщеплении различных субстратов (БАЭЭ, БАППА, ТАМЭ и др.) недостоверны. Они отражают не активность трипсина, а суммарную активность комплексов трипсин-α2макроглобулин и других протеолитических ферментов серинового типа (плазмина, каллекреина, тромбина и др.). Это связано с тем, что у всех сериновых протеаз взаимодействие с субстратом происходит сходно - серин активного центра выступает в качестве донатора атомов водорода азоту расщепляемой пептидной связи в цепочке субстрата (Бышевский А.Ш., Терсенов О.А. Биохимия для врача. - Екатеринбург, 1994.). Следовательно, биохимические методы определения активности трипсина нельзя считать специфичными для панкреатита.
Все же некоторые авторы считают возможным применять эти методы (Le Moine O., Devaster J. M., Deviere J. et al. // Dig. Dis. Sci. -1994. - Vol.39, 12. - P. 2634-2638), так как находят сильную корреляцию между результатами теста с БАПНА и радиоиммунологического исследования трипсинемии. Наиболее достоверным методом определения уровня последней считается радиоиммунологический (Bockus Gastroenterology. - 5-th ed. - Philadelphia, 1995. - Vol. 4. - P. 2815-3001. Hedstrom J., Lemonen J., Sainio V., Stenman U.H. // Clin Chem. - 1994. - Vol.40, 9. - P.1761-1765).
При ОП, атаках ХРП уровень иммунореактивного трипсина в крови увеличивается в 20-70 раз (Hedstrom J., Leinonen J., Sainio V., Stenman U.H. // Clin Chem. - 1994. - Vol. 40, 9. - P. 1761-1765). Однако и радиоиммунологический метод также нельзя считать абсолютным, так как антитела, содержащиеся в соответствующих диагностических наборах, "узнают" 100% трипсиногена, 20% трипсина в комплексе с α1-антитрипсином и 5% трипсина в комплексе с α2-макроглобулином (Bockus Gastroenterology. - 5-th ed. - Philadelphia, 1995. - Vol.4. - P. 2815-3001).
Этим, вероятно, объясняется то, что чувствительность исследования в отношении ОП, атаки ХРП не превышает 77-97% (Губергриц Н.Б. Патогенетические аспекты клиники, диагностики, лечения и прогноза хронического панкреатита: Автореф. дис.... д-ра мед. наук. - Киев, 1994. Дегтярева И.И., Гайсенко А.В. , Пуцева П.M. // Врач. дело. - 1989. - 7. - С. 42-43), а уровень иммунореактивного трипсина (ИРТ) в ряде случаев не коррелирует с тяжестью заболевания (Гайсенко А.В. Диагностика гиперферментемических и гипоферментных форм панкреатита по определению продуктов расщепления фибриногена/фибрина и панкреатических ферментов в крови и дуоденальном содержимом: Автореф. дис.... канд. мед. наук. - Киев, 1990. Le Maine 0., Devaster J. M., Deviere J. et al. // Dig. Dis. Sci. -1994. - Vol. 39, 12. - P. 2634-2638).
Противоречивы данные литературы о диагностической ценности для панкреатитов определения активности сывороточной липазы. Так, ряд авторов считают показатель инертным, малочувствительным (Gupta A., Yuan Z.Y., Balaskas E.V. et al. // Peritoneal Dialys. int. - 1992. - Vol.12, 3. - Р. 309-316). Например, Л. И. Геллер и соавт. нашли повышение уровня липазы в крови у 34%, а Н. Б. Губергриц (Губергриц Н.Б. Патогенетические аспекты клиники, диагностики, лечения и прогноза хронического панкреатита: Автореф. дис.... д-ра мед. наук. - Киев, 1994) - у 9% больных ХРП. Другие исследователи, напротив, считают липазу высокоинформативным показателем, чувствительность которого в отношении ХРП достигает 99-100% (Meizi d'Ervil G.V., Bosoni Т., Moratti R. et al. // Eur. J. clin Chem. clin. Biochem. - 1992. - Vol. 30, 7. - P. 439-444. Ventrucci M., Pezzilli R., Garulli R. et al. // Ital. J. Gastroent. - 1994. Vol. 26, 3. - P. 132-136).
Одни авторы указывают, что определение липазы в крови предпочтительнее, чем других ферментов (Хазанов А.И. //Рос. журн. гастроэнтерол., гепатол., коло-проктол. - 1997. - 1. - С. 56-62), так как ее уровень повышается чаще, чем уровень амилазы, трипсина (Bockus Gastroenterology. - 5-th ed. - Philadelphia, 1995. - Vol. 4. - P. 2815-3001).
Однако А.В. Охлобыстин (Руководство по гастроэнтерологии / Под общ. ред. Ф.И. Комарова, А.Л. Гребнева. - M., 1996. - Т. 3) отмечает, что при хронических заболеваниях ПЖ определение липазы в сыворотке крови не имеет преимуществ перед исследованием ИРТ; эти ферменты имеют одинаковую ценность в диагностике ХП и малозначимы в установлении раннего диагноза, ни один из них не имеет прогностической значимости в отношении тяжести и течения заболевания (Viedma J.A., Pilrez-Mateo M., Agull Т. et al. // Gut. - 1994. -Vol. 35, 6. - Р. 822-827).
Противоречивы и данные о времени повышения уровня липазы в крови после атаки ХРП. Ряд авторов указывают, что гиперлипаземия в некоторых случаях опережает гиперамилаземию, развивается через 3-6 ч после болевого приступа (Gumaste V.V. // Gastroenterologist. - 1994. - Vol. 2, 2, - Р. 119-130). Чаще высказывается мнение о том, что уровень липазы в крови повышается позже, чем уровень других ферментов, достигая максимума на 5-6-е сутки развития панкреатита (Пенин В.А., Писаревский Г.Н. // Хирургия. - 1993 - 12. - С. 62-68.)
При этом гиперлипаземия удерживается дольше - до 18 сут. (Jaakkola M., Frey Т. , Sillanaukee P. et al. // Hepato-Gastro-enterology. - 1994. - Vol. 41, 5. - Р. 477-482.), т.е. изучение липолитической активности сыворотки крови нерационально для ранней диагностики, но может быть полезно через несколько суток после болевого приступа, когда активность других ферментов уже нормализовалась (Chase С. W., Barker D.Е., Russell W.L., Bums R.P. 11 Am-er. Surg. - 1996. - Vol. 62, 12. - Р. 1028-1033). Гиперлипаземия не является специфичной для панкреатитов, так как липаза синтезируется не только ацинарными клетками, но и в желудке, кишечнике.
G. Meizi (Meizi d'Ervil G.V., Bosom Т., Moratti R. et al. // Eur. J. clin Chem. clin. Biochem. - 1992. - Vol. 30, 7. - P. 439-444. M. Ventrucci с соавт.(Ventrucci M., Pezzilli R., Garulli R. et al. // Ital. J. Gastroent. - 1994. Vol. 26, 3. - P. 132-136) считают, что повышение активности липазы в крови в 2 раза специфичнее для ОП и ХРП, чем гиперамилаземия. Действительно, гиперлипаземия не встречается при аппендиците, внематочной беременности, паротите, раке легкого, но ее регистрируют у 60% больных с заболеваниями гепатобилиарной системы, при кишечной непроходимости, почечной недостаточности, раке предстательной железы и других непанкреатических заболеваниях. Более специфичным является снижение уровня липазы в крови в отношении фиброза ПЖ как исхода ХРП и муковисцидоза (Nagai К., Iguchi К., Yanaihara N. // Gastroent. Jap. - 1993. - Vol. 28, 3. - Р. 401-405).
Все перечисленные выше особенности, которые необходимо учитывать при диагностической оценке липаземии, дополняются большими колебаниями показателей не только у больных, но и у здоровых (Bockus Gastroenterology. - 5-th ed. - Philadelphia, 1995. - Vol. 4. - P. 2815-3001). Это объясняется техническими сложностями определения активности липазы. Результаты биохимических исследований зависят от площади соприкосновения фермента с жировой эмульсией.
Получение стойких эмульсий заданной дисперсности технически сложно. Кроме того, многие субстраты расщепляются и липазой, и эстеразами. Для повышения точности результатов предложены специфические субстраты, стабилизаторы эмульсий (Гайсенко А.В. Диагностика гиперферментемических и гипоферментных форм панкреатита по определению продуктов расщепления фибриногена/фибрина и панкреатических ферментов в крови и дуоденальном содержимом: Автореф. дис. . . . канд. мед. наук. - Киев, 1990. Chase С.W., Barker D.E., Russell W. L. , Bums R.P. // Amer. Surg. - 1996. - Vol. 62, 12. - P. 1028-1033. Ventrucci М., Pezzilli R., Garulli R. et al. // lta1. J. Gastroent. - 1994. Vol. 26, 3. - P. 132-136), но они малодоступны для рядовой клинической лаборатории.
В последние годы доказано большое значение участия в воспалительном процессе, в том числе в патогенезе панкреатитов, цитокинов, продуцируемымых клетками организма разных типов, в первую очередь активированными лимфоцитами, моноцитами, тканевыми макрофагами. Провоспалительными цитокинами являются интерлейкин 1 (ИЛ-1), ИЛ-6, ИЛ-8, туморнекротизирующий фактор, а их антагонистами, т.е. противовоспалительными медиаторами - ИЛ-10, антагонист рецепторов ИЛ-1 и др. При дисбалансе про- и антивоспалительных медиаторов в сторону первых воспаление, в том числе при панкреатите, усиливается (Scholmerich J. // Gut. - 1997. - Vol. 41. - Suppl. 3. - Р. А 75). В связи с этим для диагностики панкреатитов возможно определение уровня провоспалительных интерлейкинов в крови. Так, показано, что через 24 ч от начала ОП повышается содержание ИЛ-6, через 48 ч - ИЛ-8. Параллельно снижается концентрация ИЛ-10 в крови (Billi Р., Miniero R., Pezzilli R. // European Pancreatic Club and the International Association of Pancreatology. Combined Meeting, 1-st. - Mannheim, 1996. - P.1).
Цитокинами принято называть обширное семейство биологически активных пептидов, обладающих гормоноподобным действием, обеспечивающих взаимодействие клеток иммунной, кроветворной, нервной и эндокринной систем.
Интерлейкин-1 (ИЛ-1) и фактор некроза опухолевых клеток (ФНО) представляют собой биологические вещества, продуцируемые различными клетками, в том числе моноцитами и макрофагами. Было показано, что ИЛ-1 опосредует большое число видов биологической активности, которые выполняют существенную роль в иммунорегуляции, а также в случае других физиологических состояний, таких как воспаление (см. Dinarello et al., Rev Infect. Disease, 1984, 6, 51). Перечень разнообразной биологической активности, присущей ИЛ-1, включает в том числе активацию Т-хелперных клеток, индукцию развития лихорадочного состояния, стимуляцию образования простагландина или коллагеназы, хемотаксис нейтрофилов, индукцию белков острой фазы и супрессию уровня железа в плазме крови. Было продемонстрировано существование множества болезненных состояний, в ходе которых избыточное или нерегулируемое образование ИЛ-1 приводит к обострению и/или индуцированию заболевания (Dinarello et al., 1985, 5, 5, 287-297; Dinarello, С. A; Wotff. a M.; New Engl. J Med., 1993, 32B 106). Результаты последних исследований выявляют также очевидную связь активности ИЛ-1 с диабетом и панкреатическими β-клетками).
Чтобы продемонстрировать посредничество IL-1β при некоторых заболеваниях человека и некоторых видов животных, используют встречающийся в природе антагонист IL-1β рецептора (Hannum. С.К.: Wilcox С.J.: Arend W.Р.: Joslin G.G.; Dripps. D.J.: Heimdal. P.L.: Armes. L.G.; Sommer. A; Eisenberg. S.P.; Thompson. R.G, Nature, 1990, 343, 336-340; Eisenberg S.P., Evans. R.J.; Arend W. P. ; Verderber E; Brewer. M.T.; Hannum. C.K: Thomson. R.G. Nature 1990. 343, 341-346; Ohlsson. К; Bjork. P.; Bergenfeldt. M.; Hageman, R,; Thompson. R.С. Nature 1990, 348, 550-552; и Wakabayashi. G. GASEB, 1991. 338-343). Специфическая роль IL-1β при воспалении и иммуномодуляции подтверждается недавними наблюдениями (Ray, С. А, и др., Cell, 1992, 69, 597-604).
Фактор некроза опухолей (ФНО) представляет собой цитокин, который продуцируется в первую очередь активированными моноцитами и весьма плейотропен по своей природе (Agier et al., 1988, Факторы некроза опухолей. Справочник по цитолитическим лимфоцитам и компонентам: Эффекторы иммунной системы, Е R. Podak, ed. , CRC Press Inc Boca Raton, Fla., p. 105; Goeddel et al., 1987, Факторы некроза опухолей: Структура генов и биологическая активность In: Coldspring Harbor Sumposia on Quantative Biology (1, 597). ФНО иигибирует рост самых разнообразных опухолевых клеток в культуре, но стимулирует рост фибробластов, В-клеток и тимоцитов. Известна также антипролиферативная активность ФНО в отношении большого числа различных клеточных элементов.
Избыточное или нерегулируемое образование ФНО опосредует течение или обострение множества заболеваний. Было показано, что монокины, такие как ФНО, активируют ВИЧ репликацию в моноцитах и/или макрофагах (Poll et al., Proc. Natl. Acad. Sci., 1990, 87, 782-784).
Интерлейкин-8 (ИЛ-8) представляет собой фактор хемотаксиса, впервые идентифицированный и охарактеризованный в 1987 г. ИЛ-8 продуцируют несколько типов клеток, в том числе моноядерные клетки, фибробласты, эндотелиальные клетки и кератиноциты. Его образование эндотелиальными клетками индуцируется ИЛ-1, ФНО или липополисахаридом (ЛПС). Было показано, что человеческий ИЛ-8 действует на нейтрофилы мыши, морской свинки, крысы, кролика и ответственен за хемотаксис нейтрофилов в место воспаления.
Учитывая вышеизложенное, нами разработан способ оценки тяжести течения ХП с использованием определения уровня цитокинов: интерлейкина 1β, интерлейкина 8, фактора некроза опухоли α, антагониста к рецепторам интерлейкина 1β человека в сыворотке крови больного хроническим панкреатитом.
Технический результат - повышение точности диагностики за счет определения степени тяжести заболевания.
Способ осуществляется следующим образом. Проводят определение уровня цитокинов: интерлейкина 1β (ИЛ1β), интерлейкина 8 (ИЛ 8), фактора некроза опухоли α (ФНОα), антагониста к рецепторам интерлейкина 1β человека(А/ИЛ1β) в сыворотке крови у следующих групп - контроля (практически здоровые лица) и больных - легкой, средней и тяжелой степени ХП мужчин и женщин. Определение проводят радиоиммунным методом, наборами пр-ва ООО "Протеиновый контур", г. Санкт-Петербург, "Набор реагентов ProConIL-1β", код К050; и пр-ва OOO "Цитокин" тест системой иммуноферментной для определения ИЛ1β (серия 004), А/ИЛ1β (серия 005), ИЛ 8 (серия 007), ФНО (серия 005) согласно инструкциям, прилагаемым к наборам.
При повышении уровня ИЛ1β в 7,8 раза при норме 20,62±0,87 пг/мл, повышении уровня А/ИЛ1β в 5 раз при норме 14±0,19 пг/мл, повышении уровня ИЛ 8 в 3,4 раза при норме 19,33±1,39 пг/мл, повышении ФНОα в 2,6 раза при норме 28,70±0,99 пг/мл у мужчин, а при повышении уровня ИЛ1β в 9,6 раза при норме 20,81±0,97 пг/мл, повышении А/ИЛ1β в 13 раз при норме 13,22±0,15 пг/мл, повышении ИЛ8 в 2,3 раза при норме 28,88±0,82 пг/мл, повышении ФНОα в 2,4 раза при норме 28,33±1,03 пг/мл у женщин определяют легкую степень хронического панкреатита;
при повышении уровня ИЛ1β в 12,5 раз при норме 20,62±0,87 пг/мл, повышении уровня А/ИЛ 1β в 10,4 раз при норме 14±0,19 пг/мл, повышении уровня ИЛ 8 в 3,9 раза при норме 19,33±1,39 пг/мл, повышении ФНОα в 2,6 раза при норме 28,70±0,99 пг/мл у мужчин, а при повышении уровня ИЛ 1β в 12,9 раза при норме 20,81±0,97пг/мл, повышении А/ИЛ1β в 13 раз при норме 13,22±0,15 пг/мл, повышении ИЛ 8 в 2,7 раза при норме 28,88±0,82 пг/мл, повышении ФНОα в 2,3 раза при норме 28,33±1,03 пг/мл у женщин определяют среднюю степень хронического панкреатита;
при повышении уровня ИЛ 1β в 14,2 раз при норме 20,62±0,87 пг/мл, повышении уровня А/ИЛ1β в 15 раз при норме 14±0,19, повышении уровня ИЛ 8 в 11,8 раза при норме 19,33±1,39 пг/мл, повышении ФНОα в 3,8 раза при норме 28,70±0,99 пг/мл у мужчин, а при повышении уровня ИЛ1β в 13,8 раз при норме 13,22±0,15 пг/мл, повышении А/ИЛ1β в 15 раз при норме 20,81±0,97 пг/мл, повышении ИЛ 8 в 16,3 раз при норме 28,88±0,82 пг/мл, повышении ФНОα в 3,3 раз при норме 28,33±1,03 пг/мл у женщин определяют тяжелую степень хронического панкреатита.
Данным способом нами было обследовано 254 больных ХП в возрасте от 17 до 72 лет. Мужчин с легкой формой ХП было 28, женщин - 43; мужчин с ХП средней степени тяжести - 88, женщин - 47; мужчин с ХП тяжелой степени - 27, женщин - 21. Результаты показали умеренное повышение уровня цитокинов при легкой степени ХП, значительное повышение уровня цитокинов при средней и тяжелой степени ХП, что отражает степень остроты процесса. Уровень цитокинов сыворотки крови находится в прямой зависимости от тяжести течения заболевания (см. табл 1).
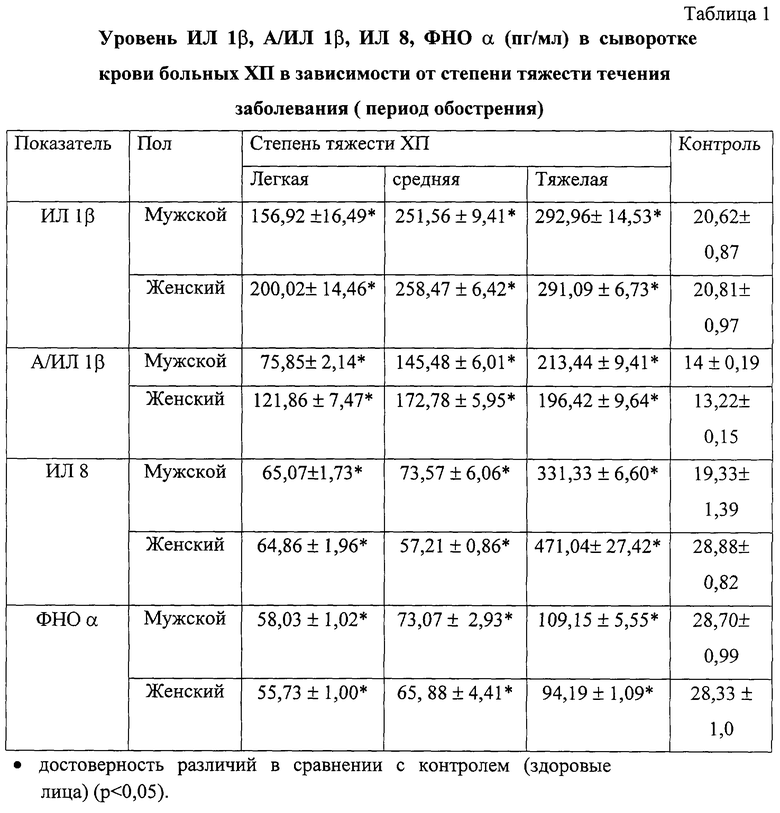
В связи с тем, что клиническая картина ХП отличается периодичностью течения, динамику изменений цитокинов (ИЛ 1β, А/ИЛ 1β, ИЛ 8, ФНО α) изучали по периодам заболевания. Так, снижение содержания цитокинов наблюдалось у пациентов (мужчин и женщин) с легкой степенью ХП уже в фазе ремиссии, которая достигалась в ходе лечения и наблюдалась при выписке больного из стационара. При ХП средней степени тяжести - в фазе ремиссии уровень цитокинов был повышен в 2,5-3,3 раза в сравнении с контрольной группой. При тяжелом ХП уровень цитокинов в фазе ремиссии оставался выше показателей контрольной группы в 3-4,5 раза, что свидетельствовало о незавершенности патологического процесса (см. табл 2).
Предлагаемый нами способ дает возможность более точно определить течение ХП по фазам и степени тяжести, так как уровень цитокинов свидетельствует о наличии ответной реакции на воспаление и ее длительность характеризует тяжесть поражения.
Пример 1. Больной П., 50 лет, история болезни 00113 поступил в стационар с диагнозом: Хронический панкреатит, фаза обострения, с жалобами на слабость, утомляемость, тошноту, однократную рвоту, выраженные боли в животе опоясывающего характера, интенсивные давящие боли в левом подреберье; чередование поносов с запорами, зловонный, жирный, плохо смываемый стул, похудание.
При поступлении состояние тяжелое, субфебрильная температура, при пальпации боли в области проекции поджелудочной железы, симптомы Губергрица, Дежардена, Мейо-Робсона положительны.
Общий анализ крови:
эритроциты 4,2•1012/л; гемоглобин 133 г/л; цветной показатель 0,9; СОЭ 31 мм/ч; лейкоциты 12,2•109/л; лейкоцитарная формула пал. 2, сег. 52, лим. 39, мон. 4, эоз. 3; тромбоциты, 250•109/л/
Биохимическое исследование крови:
щелочная фосфатаза - 101 ед/л; холестерин - 5,6 ммоль/л; аспартатаминотрансфераза - 31 ед/л; аланинаминотрансфераза - 23 ед/л; амилаза - 107,7 ед/л (норма 80 ед/л); липаза - 163 ед/л (норма 160 ед/л); общий белок - 67,1 г/л; билирубин общий - 15 мкмоль/л; креатинин - 91,4 мкмоль/л; тимоловая проба - 1,26 ед/л; глюкоза - 5 ммоль/л; ПТИ,% - 95; триглицериды - 2,4 ммоль/л ИЛ1β - 256 пг/мл; А/ИЛ1β - 174,3 пг/мл; ФНОα - 57,2 пг/мл; ИЛ8 - 58,1 пг/мл.
Гликемический профиль: 4,3; 5,8; 4,6 ммоль/л
Общий анализ мочи:
цвет: сол/желт; реакция кис.; удельный вес 1005; прозрачность; белок: отр.; сахар отр.; плоский эпителий: 4-6-4; лейкоциты: 3-2-3;
диастаза мочи, 80 г/л•ч
Эластаза-1 кала 45 мгЕ1/г (норма >200 мгЕ1/г)
Копрологическое исследование:
неоформ. ; мышечные волокна измененные ++, нейтральный жир +++; крахмал внеклеточный +++; клетчатка переваримая ++, непереваримая ++.
Ультразвуковое исследование органов брюшной полости.
Поджелудочная железа: головка, тело увеличены, контуры: неровные; вирсунгов проток расширен; эхогенность паренхимы повышенная, структура неоднородная.
ФЭГДС: Рубцовая деформация луковицы 12-перст. кишки, поверхностный бульбит, хронический эрозивный гастрит. Косвенные признаки панкреатита.
Учитывая клинику заболевания и данные дополнительных методов исследования, выставлен клинический диагноз: Хронический паренхиматозный панкреатит с выраженным болевым синдромом, с нарушением внешнесекреторной функции поджелудочной железы, фаза обострения, тяжелое течение.
Проводилась интенсивная терапия. Выписан на 26-й день лечения при клиническом выздоровлении и нормализации общеклинических анализов. Однако уровень цитокинов оставался повышенным: ИЛ1β 90,5 пг/мл (в 4,3 раза), А/ИЛ1β - 52 пг/мл (в 3,6 раза), ИЛ8 - 62 пг/мл (в 3,2 раза), ФНОα - 71 пг/мл (в 2,1 раза), что подтверждает незавершенность патологического процесса в поджелудочной железе.
Пример 2. Больная А., 38 лет, история болезни 00241 поступила в стационар с диагнозом: Хронический панкреатит, фаза обострения, с жалобами на слабость, утомляемость:, тошноту, боли в животе опоясывающего характера.
При поступлении состояние средней тяжести, субфебрильная температура, опоясывающие боли постоянного характера с локализацией в эпигастрии, левом подреберье.
Данные клинического исследования:
Общий анализ крови:
эритроциты 4,2•1012 /л; гемоглобин 133 г/л; цветной показатель 0,9; СОЭ 21 мм/ч; лейкоциты 9,2•109/л; лейкоцитарная формула пал. 2, сег. 48, лим. 43, мон. 4, эоз. 3; тромбоциты 250•109/л
Биохимическое исследование крови:
щелочная фосфатаза - 81 ед/л; холестерин - 5,6 ммоль/л; аспартатаминотрансфераза - 21 ед/л; аланинаминотрансфераза - 3 ед/л; амилаза - 87,7 ед/л; липаза 80 ед/л; общий белок - 80,1 г/л; билирубин общий - 15 мкмоль/л; креатинин - 91,4 мкмоль/л; тимоловая проба - 1,26 ед/л; глюкоза - 5 ммоль/л; ПТИ,% - 95; триглицериды - 2,2 ммоль/л;
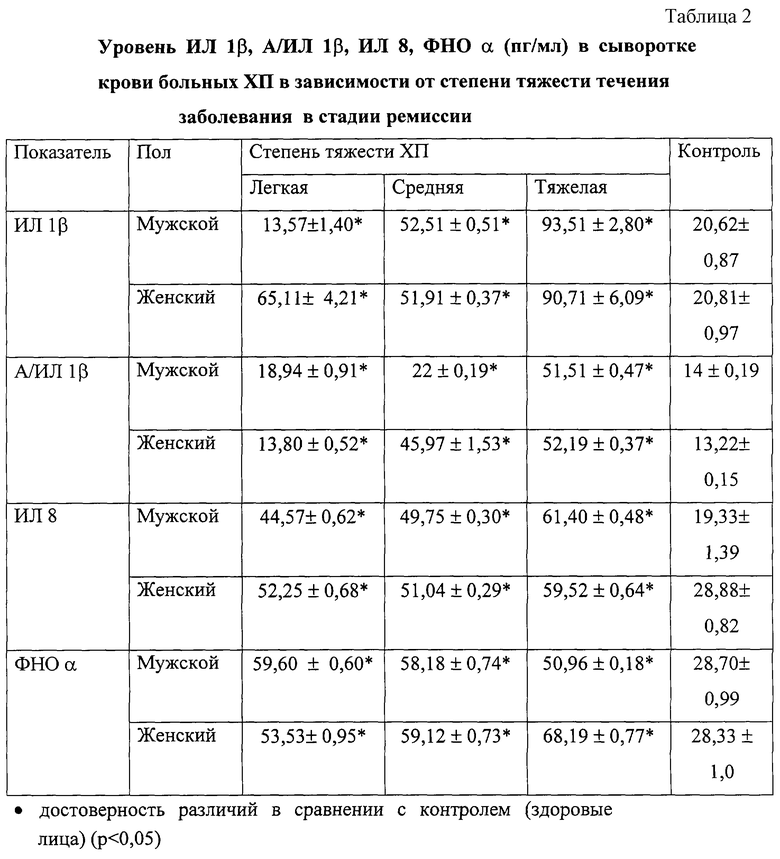
ИЛ1β - 256 пг/мл, А/ИЛ1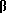 - 174,3 пг/мл, ИЛ8 - 78,1 пг/мл, ФНОα - 67,2 пг/мл;
- 174,3 пг/мл, ИЛ8 - 78,1 пг/мл, ФНОα - 67,2 пг/мл;
Гликемический профиль: 3,3; 5,8; 4,0 ммоль/л
Общий анализ мочи:
цвет: сол/желт; реакция кис.; удельный вес 1005; прозрачность; белок: отр. ; сахар отр.; плоский эпителий: 2-3-2; лейкоциты: 2-1-3; диастаза мочи, 40 г/л•ч.
Эластаза-1 кала 145 мгЕ1/г (норма >200 мгЕ1/г)
Копрологическое исследование:
форма: оформ. ; консистенция: твердая; цвет: кор.; крахмал внеклеточный +++; клетчатка переваримая ++, непереваримая ++ нейтральный жир ++.
Ультразвуковое исследование органов брюшной полости.
Поджелудочная железа: головка увеличена, контуры: неровные; эхогенность паренхимы: повышенная, структура: неоднородная
ФЭГДС: Атрофический гастит, косвенные признаки панкреатита.
Учитывая клинику заболевания и данные дополнительных методов исследования, выставлен клинический диагноз: Хронический паренхиматозный панкреатит с внешнесекреторной недостаточностью, средней тяжести течения, фаза обострения.
Проводилась интенсивная терапия. Выписана на 24-й день лечения при клиническом выздоровлении и нормализации общеклинических анализов. Однако уровень цитокинов оставался повышенным: ИЛ1β - 51 пг/мл (в 2,5 раза), А/ИЛ1β - 46 пг/мл (в 3,5 раза), ИЛ8 - 52 пг/мл (в 1,8 раза), ФНОα - 59 пг/мл (в 2,1 раза).
Из приведенного примера видно, что у больной на фоне обострения синдрома уклонения ферментов в кровь не отмечалось, но выявлялось значительное повышение цитокинов, уровень которых даже при нормализации клинических и лабораторных показателей оставался выше значений, определяемых у практически здоровых людей.
Преимущество предлагаемого метода состоит в том, что определение цитокинов сыворотки крови позволяет объективно и своевременно оценить тяжесть течения хронического панкреатита и внести коррективы в лечение.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ПАНКРЕАТИТА | 2001 |
|
RU2178304C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ХРОНИЧЕСКОГО ПАНКРЕАТИТА АЛКОГОЛЬНОЙ И БИЛИАРНОЙ ЭТИОЛОГИИ | 2005 |
|
RU2302003C1 |
| СПОСОБ ДИАГНОСТИКИ ХРОНИЧЕСКОГО ПАНКРЕАТИТА АЛКОГОЛЬНОЙ ЭТИОЛОГИИ | 2016 |
|
RU2618401C1 |
| Способ диагностики профессиональной хронической обструктивной болезни легких, сформировавшейся в условиях действия токсических промаэрозолей | 2016 |
|
RU2613164C1 |
| СПОСОБ ОЦЕНКИ АКТИВНОСТИ ЛОКАЛЬНОГО ВОСПАЛЕНИЯ ПРИ ФОНОВЫХ ЗАБОЛЕВАНИЯХ ШЕЙКИ МАТКИ | 2009 |
|
RU2405145C1 |
| Способ диагностики профессиональной хронической обструктивной болезни легких, сформировавшейся в условиях действия пылей | 2016 |
|
RU2619861C1 |
| Способ прогнозирования исходов беременности у женщин с сахарным диабетом 1 типа во время беременности | 2021 |
|
RU2770106C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ГАСТРОЭЗОФАГЕАЛЬНОЙ РЕФЛЮКСНОЙ БОЛЕЗНЬЮ | 2012 |
|
RU2495687C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ | 2013 |
|
RU2556577C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВНУТРИУТРОБНОГО ИНФИЦИРОВАНИЯ ПЛОДА | 2008 |
|
RU2382361C1 |
Изобретение относится к медицине, а именно к внутренним болезням, и может быть использовано для объективной оценки обострения и тяжести течения хронического панкреатита с внешнесекреторной недостаточностью (ХП). Способ обеспечивает повышение точности диагностики за счет определения степени тяжести заболевания. В сыворотке крови определяют уровень цитокинов: интерлейкина 1β (ИЛ1β), антагониста к рецепторам интерлейкина 1β (А/Ил1β), интерлейкина 8 (ИЛ8), фактора некроза опухоли α (ФНО α) и при повышении уровней ИЛ1β в 7,8 раза при норме 20,62±0,87 пг/мл, А/ИЛ1β человека в 5 раз при норме 14±0,19 пг/мл, ИЛ 8 в 3,4 раза при норме 19,33±1,39 пг/мл, ФНОα в 2,6 раза при норме 28,70±0,99 пг/мл у мужчин, при повышении уровней ИЛ1β в 9,6 раза при норме 20,81±0,97 пг/мл, А/ИЛ1β в 13 раз при норме 13,22±0,15 пг/мл, ИЛ8 в 2,3 раза при норме 28,88±0,82 пг/мл, ФНОα в 2,4 раза при норме 28,33±1,03 пг/мл у женщин - определяют легкую степень ХП, а при повышении уровней ИЛ1β в 12,5 раз при норме 20,62±0,87 пг/мл, А/ИЛ1β в 10,4 раз при норме 14±0,19 пг/мл, ИЛ 8 в 3,9 раза при норме 19,33±1,39 пг/мл, ФНОα в 2,6 раза при норме 28,70±0,99 пг/мл у мужчин, при повышении уровней ИЛ1β в 12,9 раза при норме 20,81±0,97 пг/мл, А/ИЛ1β в 13 раз при норме 13,22±0,15 пг/мл, ИЛ 8 в 2,7 раза при норме 28,88±0,82 пг/мл, ФНОα в 2,3 раза при норме 28,33±1,03 пг/мл у женщин - определяют среднюю степень ХП, а при повышении уровней ИЛ1β в 14,2 раз при норме 20,62±0,87 пг/мл, А/ИЛ1β в 15 раз при норме 14±0,19 пг/мл, ИЛ 8 в 11,8 раза при норме 19,33±1,39 пг/мл, ФНОα в 3,8 раза при норме 28,70±0,99 пг/мл у мужчин, при повышении уровней ИЛ1β в 13,8 раз при норме 13,22±0,15 пг/мл, А/ИЛ1β в 15 раз при норме 20,81±0,97 пг/мл, ИЛ 8 в 16,3 раз при норме 28,88±0,82 пг/мл, ФНОα в 3,3 раз при норме 28,33±1,03 пг/мл у женщин - определяют тяжелую степень ХП. 2 табл.
Способ диагностики хронического панкреатита путем исследования сыворотки крови, отличающийся тем, что определяют уровень цитокинов, а именно интерлейкина 1β (ИЛ1β), антагониста к рецепторам интерлейкина 1β (А/Ил1β), интерлейкина 8 (ИЛ 8), фактора некроза опухоли α (ФНОα) и при повышении уровней ИЛ1β в 7,8 раза при норме 20,62±0,87 пг/мл, А/ИЛ1β человека в 5 раз при норме 14±0,19 пг/мл, ИЛ 8 в 3,4 раза при норме 19,33±1,39 пг/мл, ФНО α в 2,6 раза при норме 28,70±0,99 пг/мл у мужчин, при повышении уровней ИЛ1β в 9,6 раза при норме 20,81±0,97 пг/мл, А/ИЛ1β в 13 раз при норме 13,22±0,15 пг/мл, ИЛ8 в 2,3 раза при норме 28,88±0,82 пг/мл, ФНОα в 2,4 раза при норме 28,33±1,03 пг/мл у женщин - определяют легкую степень хронического панкреатита, а при повышении уровней ИЛ1β в 12,5 раз при норме 20,62±0,87 пг/мл, А/ИЛ1β в 10,4 раз при норме 14±0,19 пг/мл, ИЛ 8 в 3,9 раза при норме 19,33±1,39 пг/мл, ФНОα в 2,6 раза при норме 28,70±0,99 пг/мл у мужчин, при повышении уровней ИЛ1β в 12,9 раза при норме 20,81±0,97 пг/мл, А/ИЛ1β в 13 раз при норме 13,22±0,15 пг/мл, ИЛ 8 в 2,7 раза при норме 28,88±0,82 пг/мл, ФНОα в 2,3 раза при норме 28,33±1,03 пг/мл у женщин - определяют среднюю степень хронического панкреатита, а при повышении уровней ИЛ1β в 14,2 раз при норме 20,62±0,87 пг/мл, А/ИЛ1β в 15 раз при норме 14±0,19 пг/мл, ИЛ 8 в 11,8 раза при норме 19,33±1,39 пг/мл, ФНОα в 3,8 раза при норме 28,70±0,99 пг/мл у мужчин, при повышении уровней ИЛ1β в 13,8 раз при норме 13,22±0,15 пг/мл, А/ИЛ1β в 15 раз при норме 20,81±0,97 пг/мл, ИЛ 8 в 16,3 раз при норме 28,88±0,82 пг/мл, ФНОα в 3,3 раз при норме 28,33±1,03 пг/мл у женщин - определяют тяжелую степень хронического панкреатита.
| Медицинская лабораторная диагностика | |||
| / Под ред | |||
| КАРПИЩЕНКО А.И | |||
| - СПб., 1997, с | |||
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| УСТРОЙСТВО ДЛЯ РАЗМЕЩЕНИЯ КОНТЕЙНЕРОВ НА ДВИЖУЩИЙСЯ КОНВЕЙЕР (ВАРИАНТЫ) | 1995 |
|
RU2133703C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕННОГО ТЕЧЕНИЯ ОСТРОГО ПАНКРЕАТИТА | 1992 |
|
RU2102764C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ДЕСТРУКТИВНОГО ПАНКРЕАТИТА | 1996 |
|
RU2126159C1 |
| Способ определения формы острого панкреатита | 1990 |
|
SU1798697A1 |
Авторы
Даты
2003-02-27—Публикация
2001-05-21—Подача