Как известно, рефлюксная болезнь в значительной степени обусловлена снижением барьерных функций естественных клапанов желудка. В частности, известно [4] , что после приема пищи давление в желудке повышается и недостаточное функционирование входного сфинктера желудка приводит к наличию пищи в пищеводе и, как следствие, появлению рефлюкса (отрыжки). Поэтому важным является оценка состоятельности (качества) формирования клапанов хирургическим способом. Формирование клапанов может быть осуществлено различными способами с применением разнообразных методик и средств. Оценка состоятельности искусственно созданных клапанов на стадии разработки технологии операции позволяет надежно прогнозировать отдаленные и ближайшие перспективы операций и избежать (минимизировать) травмирование больных, связанное с оперативным вмешательством. Оценить состоятельность искусственно созданных клапанов можно на моделях путем измерения внутреннего давления до появления разрыва клапана или жидкости "за" клапаном. В момент прорыва клапана давление в полости резко падает.
Изобретение относится к медицине, а именно к абдоминальной хирургии.
Известен способ оценки барьерной функции кардии и терапии рефлюкс-эзофагита с помощью повторного определения интраэзофагеального и интрагастрального протеолиза, заключающийся в прямом определении интенсивности переваривания белкового субстрата в нижней части пищевода в течение длительного срока (12-24 ч) до лечения и после него.
Известен способ определения барьерной функции клапанов полых органов и желудочно-пищеводного рефлюкса зондированием с применением раствора метиленового синего, заключающийся во введении через тонкий зонд в желудок раствора красителя и последующей аспирации содержимого нижней трети пищевода через несколько подтянутый вверх зонд.
Недостатком этих способов является невозможность объективной цифровой оценки барьерной функции восстановленного (после хирургического лечения) пищеводно-желудочного перехода.
Цель изобретения - объективная цифровая оценка барьерной функции различных видов антирефлюксных операций путем точного измерения максимального внутрижелудочного давления в момент появления желудочно-пищеводного рефлюкса и/или прорезывания швов фундопликационной манжеты.
Цель достигается тем, что согласно способу оценки барьерной функции клапанов полых органов в полость желудка через введенную в начальный отдел двенадцатиперстной кишки инфузионную систему осуществляют нагнетание жидкости до появления желудочно-пищеводного рефлюкса и регистрируют давление, при котором он возникает, отличающийся тем, что после этого осуществляют наложение фундопликационной манжеты, осуществляют повторное нагнетание жидкости и регистрируют внутрижелудочное давление в сантиметрах водяного столба до разрыва клапана или прорезывания швов, причем регистрацию давления осуществляют при помощи устройства, включающего электромеханический датчик, подключенный к желудку через гастротомическое отверстие диаметром 1,5 см.
На фиг.1 показано устройство в собранном виде.
Характеристика используемого средства (т.е. "устройства").
Устройство состоит из специального стенда-подставки, под которым располагается датчик давления, датчика давления, регистрирующего блока, представленного цифровым вольтметром типа В7-35, инфузионной системы для нагнетания изотонического раствора.
Специальный стенд-подставка предназначен для размещения исследуемого образца полого органа и изоляции от воздействия жидкости датчика давления, датчик давления предназначен для фиксации давления и инфузионная система для нагнетания раствора и увеличения давления в полости исследуемого органа. Стенд-подставка представляет собой лабораторный стол с технологическим отверстием в центре. Отверстие позволяет разместить датчик давления под столом и тем самым в значительной степени избежать неблагоприятного воздействия жидкости (в момент разрыва клапана) на электромеханический датчик. Датчик давления описан ниже. Инфузионная система для нагнетания раствора широко используется в физиологических процедурах и исследованиях в различных клиниках и лабораториях.
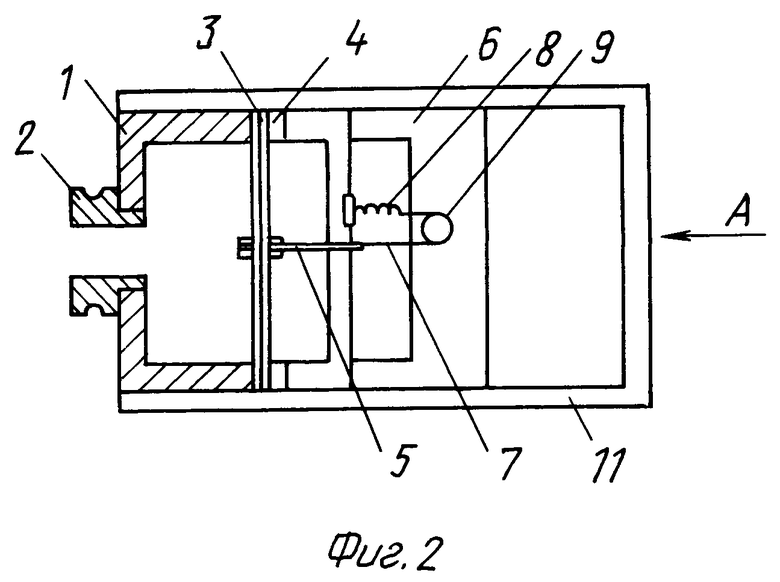
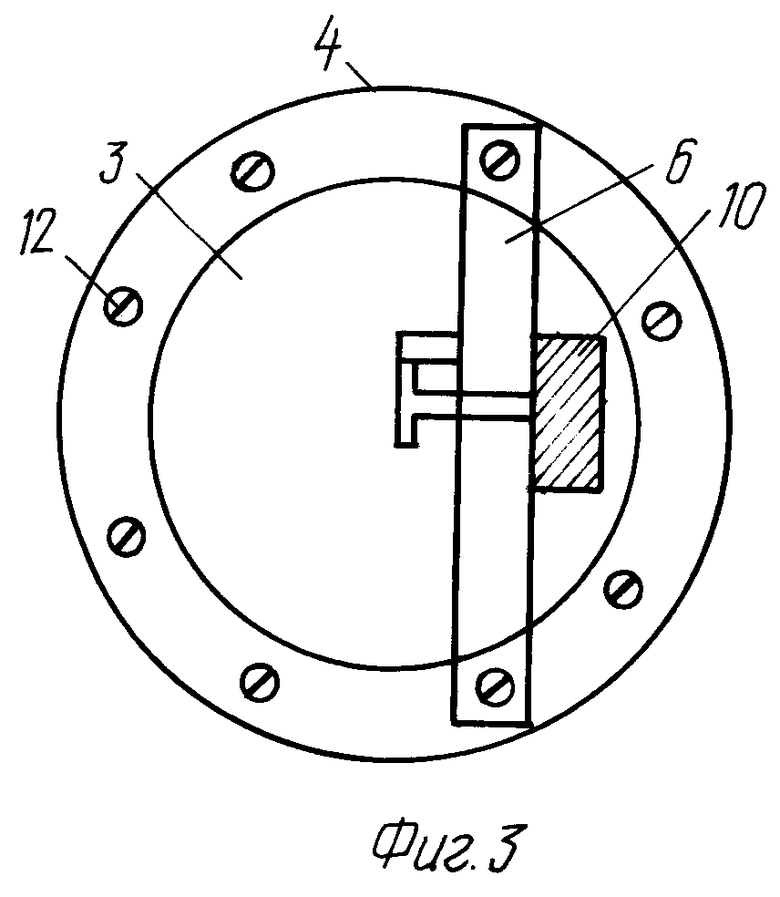
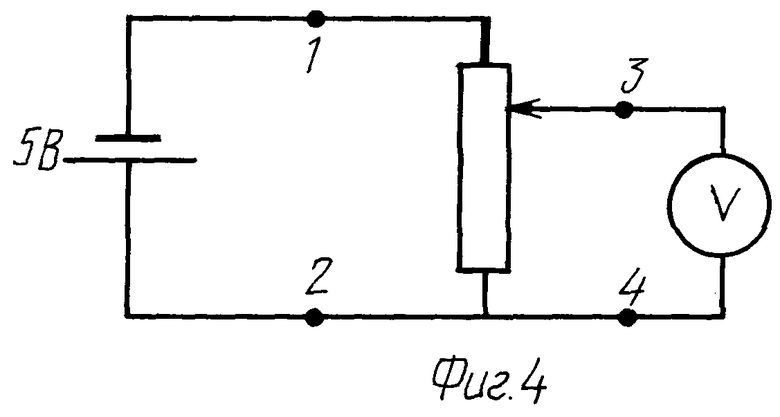
Датчик давления изображен на фиг.2 и фиг.3. Он состоит из цилиндрического корпуса 1, втулки 2, мембраны 3, кольца 4, штока 5, стойки 6, тросика 7, пружины 8, шкива 9, многооборотного проволочного потенциометра 10, кожуха 11. Электрическая схема измерений приведена на фиг.4. На потенциометр к выводам 1 и 2 подается напряжение 5В со стабилизированного источника питания. Напряжение с движка потенциометра (выводы 3 и 4) измеряется цифровым вольтметром типа В7-35. Для того чтобы жидкость и растворы не влияли на результаты измерений, источник 5В и цифровой вольтметр подключаются через специальные провода снаружи датчика давления. Цилиндрический корпус 1 датчика выполнен из органического стекла. В качестве мембраны 3 использована упругая авиационная резина, пружина 8 закреплена в стойке 6 и обеспечивает натяжение тросика 7 при изгибе мембраны 3. Упругость пружины подобрана так, чтобы она не изменяла бы заметным образом положение мембраны 3 и обеспечивала натяжение тросика 7 при перемещении мембраны. Кольцо 4 с помощью винтов 12 прижимает мембрану 3 к корпусу датчика 1. На стойке 6 закреплены потенциометр 10 и один конец пружины 8. Другой конец пружины 8 прикреплен к тросику 7. На роторе потенциометра жестко закреплен шкив 9, который преобразует поступательное перемещение тросика во вращательное движение ротора потенциометра. Кожух датчика герметизирован специальным герметиком.
Элементы датчика давления, как показал эксперимент, доступны и сравнительно просты в изготовлении. Так, в частности, многооборотные проволочные потенциометры широко используются в прецизионной электронной аппаратуре. Перемещение движка в них может осуществляться с помощью электрического моторчика. Шкив 9 представляет собой колесико с желобком, по которому движется тросик 7. Механические элементы конструкции сравнительно просто изготавливаются на токарном и фрезерном станках.
Конструктивные данные датчика:
диаметр корпуса 1-100 мм;
высота корпуса 1-120 мм;
сопротивление потенциометра 4.7 ком. тип СП5-21, число оборотов ротора 250000;
диаметр блока 9-20 мм;
диаметр штока 5-2 мм;
диаметр отверстия втулки 2-15 мм.
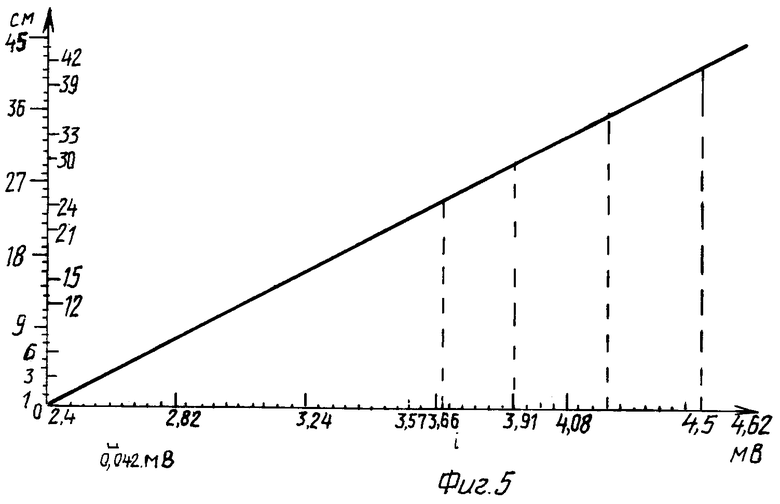
Датчик работает следующим образом. При поступлении жидкости в полость, закрытую мембраной 3, мембрана 3 под давлением столба жидкости изгибается, вызывая перемещение штока 5, что через тросик 7 и шкив 9 перемещает движок потенциометра. Это приводит к изменению напряжения на выводах 3 и 4, которое измеряется цифровым вольтметром. При уменьшении столба жидкости мембрана перемещается в противоположную сторону, вызывая противоположное изменение напряжения. Для пересчета напряжения в высоту водяного столба датчик был откалиброван на стенде. Градуировочная кривая приведена на фиг.5.
Способ осуществляют следующим образом.
Препарат, включающий 6-8 см дистального отдела пищевода, желудок и начальный отдел двенадцатиперстной кишки, через гастротомическое отверстие диаметром 1,5 см подключают к устройству и через начальный отдел двенадцатиперстной кишки к инфузионной системе. Далее нагнетают в желудок изотонический раствор хлорида натрия со скоростью 75 мл/мин до появления желудочно-пищеводного рефлюкса и регистрируют давление, при котором он возник. Выполняют оперативное вмешательство - фундопликацию тем или иным методом. Затем нагнетают в желудок изотонический раствор хлорида натрия со скоростью 75 мл/мин и регистрируют величину внутрижелудочного давления до появления желудочно-пищеводного рефлюкса или прорезывания швов.
Пример 1. Препарат от трупа больного 65 лет, умершего в стационаре от цереброваскулярной болезни, геморрагического инсульта. Начальный рефлюкс был индуцирован при внутрижелудочном давлении 4,3 см вод. ст. Далее выполнили фундопликацию по Ниссену. После оперативного вмешательства желудочно-пищеводный рефлюкс не был индуцирован, а при давлении 35,8 см вод. ст. произошло прорезывание швов стенки желудка.
Пример 2. Препарат от трупа больной 63 лет, умершей в стационаре от цереброваскулярной болезни, геморрагического инсульта. Начальный рефлюкс был индуцирован при давлении 3,5 см вод.ст. Далее выполнили фундопликацию по Тоупу в классическом варианте (фиксация задней стенки дна желудка к правой боковой стенке пищевода и передней стенки дна желудка к передней стенке пищевода). После оперативного вмешательства рефлюкс не был индуцирован, а при давлении 35,2 см вод.ст. произошел разрыв стенки желудка.
Пример 3. Препарат от трупа больного 71 года, умершего в стационаре от цереброваскулярной болезни, геморрагического инсульта. Начальный рефлюкс был индуцирован при давлении 2,8 см вод.ст. Далее выполнили фундопликацию по Тоупу (заднюю парциальную - фиксация задней стенки фундального отдела желудка к правой боковой стенке пищевода). После вмешательства рефлюкс был индуцирован при внутрижелудочном давлении 18,9 см вод.ст.
Методика апробирована в клинике кафедры хирургии с курсом эндоскопической хирургии постдипломного образования ММА им. И.М. Сеченова и в клинике кафедры хирургии и общеврачебной подготовки с курсом эндохирургии Рязанского государственного медицинского университета им. акад. И.П. Павлова на базе отделения лапароскопической хирургии и гинекологии (хирургическое отделение 2) ОКБ г. Рязани.
Всего нами проведено 30 исследований: по 10 в каждой группе ( 1 - фундопликация по Ниссену, 2 - фундопликация по Тоупу (задняя парциальная), 3 - фундопликация по Тоупу (классический вариант))
До формирования манжеты во всех группах рефлюкс возникал практически сразу при поступлении жидкости и уровне давления 3,3±2,5* см водного столба. В 1 и 3 группах рефлюкс не был индуцирован ни в одном случае, а прорезывание швов или разрыв стенки желудка наступали при внутрижелудочном давлении 35,47±2,84* см вод.ст. и 34,78±3,06* см вод.ст. соответственно. Во 2 группе желудочно-пищеводный рефлюкс возникал при давлении 21,39±3,45* см вод.ст. (* р≤0,05).
При повышении внутрижелудочного давления манжета раздувалась, и при восстановленном угле Гиса начинал функционировать клапан Губарева. К тому же наполненная манжета сдавливала дистальный отдел пищевода с силой, увеличивающейся пропорционально росту давления в желудке, выполняя функцию нижнего пищеводного сфинктера.
Таким образом, фундопликации по Nissen и Toupet (задняя парциальная и в классическом варианте) предупреждают развитие рефлюкса даже в отсутствие функциональных компонентов нижнего пищеводного сфинктера. Учитывая, что нормальное давление в желудке составляет 5-7 см вод.ст. (Я.Д. Витебский, 1988), метод Toupet с использованием только задней стенки желудка (задняя парциальная фундопликация), нам представляется также достаточно состоятельным.
Данные эксперимента полностью согласуются с клиническими. На базе отделения лапароскопической хирургии и гинекологии ОКБ г. Рязани нами выполнено 153 антирефлюксных операций, в т.ч. 28 по Ниссену, 60 по Тоупу (задняя парциальная фундопликация) и 65 по Тоупу (классический, двусторонний вариант). Все больные проходят комплексное обследование в отдаленном послеоперационном периоде в сроки 3, 6 месяцев, 1, 1,5, 2 года с момента вмешательства.
Транзиторные дисфагии (главным образом, нарушение проглатывания твердой пищи) наблюдались через 1 месяц у 18,5% больных, оперированных по Ниссену и у 9,1% - по Тоупу (задняя парциальная фундопликация), через 3 мес и через 1 год - у 11,1% и 3,0% соответственно; купировались 1-2 двухнедельными курсами прокинетических препаратов per os (церукал, мотилиум, препульсид). Отрыжка наблюдалась у 8,3% больных после фундопликации по Ниссену, у 9,5% - по Тоупу (задняя парциальная фундопликация) и у 1,4% по Тоупу (классический вариант); диарея в течение 1 месяца - у 3,7% и 3,0% больных соответственно. Боли в эпигастрии беспокоили 3,3% и 2,9% больных через 1 месяц после операции и в дальнейшем исчезали.
В течение 1 года после операции выявлен 1 рецидив ГПОД у больной, оперированной по методике Ниссена, а также по одному рецидиву патологического гастроэзофагеального рефлюкса группах. В одном случае было выявлено нарушение эвакуации из желудка после фундопликации по Ниссену.
Таким образом, группы сопоставимы по количеству рецидивов, но фундопликации по Тоупу (задняя парциальная и классическая) имеют лучшие функциональные результаты.
Предлагаемый способ и устройство позволяют объективно оценить барьерную функцию после антирефлюксных операций на органах желудочно-кишечного тракта в условиях, максимально приближенных к естественным, что позволяет в некоторой степени прогнозировать клинический эффект предлагаемых вмешательств.
Предложенный способ и устройство позволяют объективно оценивать барьерную функцию клапанов полых органов и не требуют дорогостоящего оборудования.
Поскольку проблема лечения больных гастроэзофагеальной рефлюксной болезнью на сегодняшний день является чрезвычайно актуальной (рост заболеваемости, трудность медикаментозного лечения, обилие методик хирургической коррекции и в то же время отсутствие полностью безопасной операции) предполагает интенсивное развитие и разработку лапароскопических технологий при этом заболевании. Формирование клапанов в антирефлюксной хирургии пищеводно-желудочного перехода может быть осуществлено различными способами с применением разнообразных методик и средств. Оценка состоятельности искусственно созданных клапанов с использованием способа оценки барьерной функции клапанов полых органов в абдоминальной хирургии на стадии разработки технологии операции позволяет надежно прогнозировать отдаленные и ближайшие перспективы операций и избежать (минимизировать) травмирование больных, связанное с оперативным вмешательством.
Источники информации
1. Е.В. Краевский. - Труды Ленинград. Сан.-гиг. Мед. ин-та, 1981, Т 137. С.30-33.
2. Г.С. Аржакова. Значение протеолитической агрессии в развитии рефлюкс-эзофагита. // Советская медицина, 1983, 12. C.11-14.
3. Г.С. Аржакова. Оценка терапии рефлюкс-эзофагита с помощью определения протеолиза. // Клиническая медицина, 1984, Т62, 6. С. 102-103.
4. Василенко В.Х., Гребенев А.Л. Грыжи пищеводного отверстия диафрагмы. - М.: Медицина, 1978. - 223с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФЛЮКС-ЭЗОФАГИТА | 1996 |
|
RU2132159C1 |
| Способ фиксации дна желудка при выполнении робот-ассистированной лапароскопической фундопликации | 2023 |
|
RU2813330C1 |
| Способ профилактики повреждения сердца и перикарда при лапароскопической пластике грыжи пищеводного отверстия диафрагмы сетчатым имплантом. | 2018 |
|
RU2714087C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГРЫЖ ПИЩЕВОДНОГО ОТВЕРСТИЯ ДИАФРАГМЫ | 2005 |
|
RU2281703C1 |
| Тренажер для отработки оперативных этапов методик лапароскопической фундопликации при лечении грыжи пищеводного отверстия диафрагмы | 2021 |
|
RU2768579C1 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОЙ ГАСТРОФУНДОПЛИКАЦИИ ПРИ ЛЕЧЕНИИ ЖЕЛУДОЧНО-ПИЩЕВОГО РЕФЛЮКСА У ДЕТЕЙ | 2013 |
|
RU2535607C1 |
| СПОСОБ ФУНДОПЛИКАЦИИ | 2008 |
|
RU2371108C1 |
| СПОСОБ КЛЕЕВОЙ ФУНДОПЛИКАЦИИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1995 |
|
RU2132648C1 |
| Способ хирургического лечения грыжи пищеводного отверстия диафрагмы и пищевода Барретта | 2020 |
|
RU2751739C1 |
| Способ хирургического лечения ожирения в сочетании с грыжей пищеводного отверстия диафрагмы и гастроэзофагеальной рефлюксной болезнью | 2022 |
|
RU2794406C1 |
Изобретение относится к медицине, а именно к абдоминальной хирургии. Способ оценки барьерной функции клапанов полых органов заключается в том, что в полость желудка через введенную в начальный отдел двенадцатиперстной кишки инфузионную систему осуществляют нагнетание жидкости до появления желудочно-пищеводного рефлюкса и регистрируют давление, при котором он возникает. После этого осуществляют наложение фундопликационной манжеты, осуществляют повторное нагнетание жидкости и регистрируют внутрижелудочное давление в сантиметрах водяного столба до разрыва клапана или прорезывания швов. Регистрацию давления при этом осуществляют электромеханическим датчиком, подключенным к желудку через гастротомическое отверстие диаметром 1,5 см. Это позволяет объективно оценивать барьерную функцию клапанов полых органов и не требует дорогостоящего оборудования. 5 ил.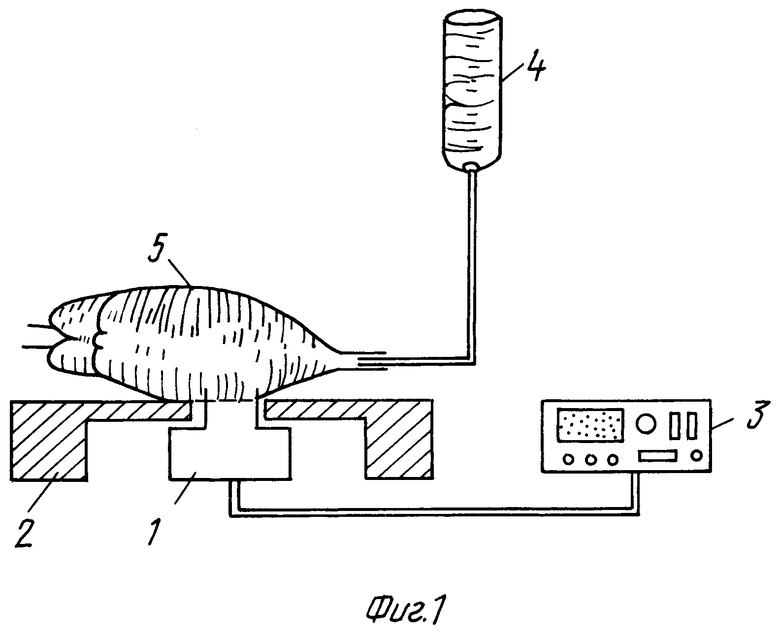
Способ оценки барьерной функции клапанов полых органов, заключающийся в том, что в полость желудка через введенную в начальный отдел двенадцатиперстной кишки инфузионную систему осуществляют нагнетание жидкости до появления желудочно-пищеводного рефлюкса и регистрируют давление, при котором он возникает, отличающийся тем, что после этого осуществляют наложение фундопликационной манжеты, осуществляют повторное нагнетание жидкости и регистрируют внутрижелудочное давление в сантиметрах водяного столба до разрыва клапана или прорезывания швов, причем регистрацию давления осуществляют электромеханическим датчиком, подключенным к желудку через гастротомическое отверстие диаметром 1,5 см.
| Способ исследования рефлюкса в лимфангионе | 1989 |
|
SU1695879A1 |
| Устройство для измерения давления в полых органах | 1987 |
|
SU1697722A1 |
| Способ диагностики дуоденогастрального рефлюкса | 1989 |
|
SU1725824A1 |
| АРЖАКОВА Г.С | |||
| Оценка терапии рефлюкс-эзофагита с помощью определения протеолиза | |||
| - Клиническая медицина, 1984, т.62, №6, с.102-103. | |||
Авторы
Даты
2003-03-20—Публикация
1999-07-19—Подача