Низин является бактериоцином, антимикробным соединением, продуцируемым содержащимся в пищевых продуктах организмом, и относится к группе родственных веществ, обозначаемых как лантибиотики (или здесь - лантоцины). Указанная группа включает также субтилин, эпидермин, галлидермин, pep 5, циннамицин, дурамицин и анковенин.
Низин продуцируется Lactococcus lactis subsp. lactis, принадлежащим к серологической группе N Lancefield [Mattic A.T.R. and Hirsch A., 1947 Lancet, 2, 5]. Низин является пептидом, состоящим из 34 аминокислотных остатков, и содержит пять кольцевых структур, перекрестно связанных тиоэфирными мостиками, которые образуют лантионин или β-метиллантионин. Эти тиоэфирные группы формируются в результате конденсации сульфгидрильных групп цистеина с дегидробоковыми цепями, образованными из остатков серина, либо треонина в результате посттрансляционных модификаций пептида - предшественника низина.
Было показано, что низин действует как катионный поверхностно-активный агент, его активность может быть нейтрализована анионными детергентами [Ramseier H.R., 1960, Arch. Mikrobiol., 37, 57] и на молекулярном уровне низин действует на цитоплазматическую мембрану и ингибирует биосинтез пептидогликана [Raisinger et al. , 1980, Arch. Mikrobiol., 127. 187]. Действие низина на вегетативных бактерий скорее всего является результатом зависимой от напряжения деполяризации плазматической мембраны с последующим проникновением пептида в липидный бислой, возможно, вследствие взаимодействия соседних молекул низина с образованием временной поры или канала. Молекулярные свойства низина и механизм его биосинтеза широко обсуждаются в недавних обзорах [Jung G. and Sahl H. - G., 1991, Nisin and Novel Lantibiotics ESCOM Science Publishers, Leiden].
Низин, как считают, имеет узкий спектр активности и в основном он активен только в отношении грамположительных бактерий за исключением тех случаев, когда его комбинируют с хелатирующим агентом, и низин проявляет неожиданную активность в отношении грамотрицательных бактерий и повышенную активность в отношении грамположительных бактерий (Патенты США 5135910; 5217950 и 5260271, выданные Blackburn et al.). Низин использовался как антимикробный консервант для пищевых продуктов и сертифицирован как безопасный препарат JEFCA различными национальными учреждениями, регулирующими использование пищевых добавок, включая таковые США, Объединенного королевства и ЕЭС.
Сущность изобретения
Изобретение относится к способам профилактики и лечения заболеваний, обусловленных инфицированием устойчивых к антибиотикам патогенов. В способах используют низин и другие лантионинсодержащие бактериоцины (лантоцины), а также их структурные варианты, полученные методами генетической инженерии или химическим синтезом (полусинтетические соединения). Способы, заявленные согласно изобретению, могут быть соответствующим образом использованы наряду с другими для контроля устойчивых к антибиотикам штаммов родов Staphylococcus, Streptococcus и Enterococcus.
Сведения, подтверждающие возможность осуществления изобретения
Бактериальные инфекции, особенно те, которые приобретаются в больницах, стали более трудно поддающимися лечению частично в результате селекции клинических изолятов, устойчивых к тем антибиотикам, которые постоянно используются для терапии. В частности, метициллин-резистентный Staphylococcus aureus (MRSA) и метициллин-резистентные коагулазоотрицательные стафилококки (MRSE) приобрели устойчивость к большинству постоянно применяемых антибиотиков, за исключением гликопептидных антибиотиков ванкомицина и тейкопланина.
Несмотря на то, что ванкомицин является лекарственным препаратом выбора для этих инфекций, он не всегда клинически эффективен [Karchmer A.W., 1991, Annals of Internal Medicine, 115:739]. Энтерококковые инфекции всегда трудно поддавались лечению отчасти потому, что энтерококки по своей природе устойчивы ко многим антибактериальным агентам и частично, вследствие своей толерантности (устойчивости к уничтожению), к агентам, которые в норме бактерицидны для других видов бактерий [Murrey B.E., 1990, Clin. Microbio. Rev., 3: 46] . Недавно энтерококки приобрели резистентность к ванкомицину, и частота инфекций, вызванных ванкомицинустойчивыми изолятами энтерококков, возрастает до тревожного уровня, особенно в отделениях интенсивной терапии [Emori T.G. and R.P. Gaynes. 1993, Clin. Microbio. Rev., 6:428]. Возможен конъюгационный перенос генетической информации между энтерококками и стафилококками, и перенос устойчивости к ванкомицину осуществлен в лабораторных условиях [Noble W. C. et al., 1992, FEMS Microbiol. Lett. 72:195]; вследствие этого, вероятно, появление устойчивых к ванкомицину стафилококков является только вопросом времени. С точки зрения передающихся контактным путем инфекций возникающая среди стрептококков устойчивость имеет отношение, в частности, к пневмококкам [Thornsberry С. et al., 1993, Infections in Medicine 10 Suppl. D: 15; Stutman H.R., 1993, Infections in Medicine 10 Suppl. D: 51]. Высокотоксигенные штаммы стрептококков группы A [Anonymous, 1994, Morbidity Mortality Weekly report 43:401] и стафилококки (вызывающие некротизирующий фасцит и синдром токсического шока и подобные им заболевания) трудно поддаются контролю и часто приводят к быстрой смерти пациента. Ясно, что для борьбы с этими инфекциями требуются новые, более эффективные и быстродействующие антимикробные агенты.
Несмотря на то, что в принципе низин можно было бы использовать в определенных случаях, когда необходимы антимикробные агенты, и бактериоцин, как было показано в предварительных исследованиях на животных моделях, является эффективным [Mattic A.T.R. and Hirsch, 1947, Lancet. 2, 5; Bavin E. M. , et al., Lancet 1, 127; Gowans J.L, et al., 1952, Brit J. Pharmacol., 7: 438; Hirsch A. and Mattick A.T.R., 1949, Lancetii: 190], низин, как было обнаружено, является недостаточно действенным для терапевтического применения в медицине и ветеринарии. Актагардин и мерсацидин являются более современными лантионинсодержащими антимикробными пептидами, но обладают только умеренной активностью в отношении стафилококков и энтерококков по сравнению с используемыми в настоящее время терапевтическими агентами [Arioli V.etal., 1976, J. Antibiotics, 29: 511; Somma et al., 1977, Antimicrob. Ад. Chemother; Barrett M. S., et al., 1992, Diagn. Microbiol. Infect. Dis. 15: 641] и, маловероятно, чтобы они обладали терапевтической ценностью.
Однако авторы изобретения обнаружили, что низин является сильным бактерицидным агентом в отношении патогенных штаммов грамотрицательных бактерий. В частности, авторы установили, что низин является бактерицидным в отношении современных изолятов Staphylococcus aureus с множественной лекарственной устойчивостью, метициллин-резистентных коагулазоотрицательных стафилококков, некротизирующего штамма стрептококков группы А и пневмококков с множественной лекарственной устойчивостью. Более того, авторы обнаружили, что низин является эффективным бактерицидным агентом в отношении энтерококков, включая ванкомицин-резистентные энтерококки. Поскольку энтерококки, как известно, устойчивы к антимикробным агентам, это наблюдение удивительно и оно решительно предполагает, что низин может иметь необыкновенную терапевтическую ценность. Поскольку считается, что повсеместное применение антимикробных агентов широкого спектра действия, особенно при пероральном введении и в низких дозах, приводит к массовому возникновению патогенов с множественной лекарственной устойчивостью, удивительно, что хотя низин вводят в низких дозах в пищевые продукты, устойчивость к низину и перекрестная устойчивость к другим антимикробным агентам не возникает. Несмотря на то, что при ранних исследованиях низина как антимикробного консерванта для пищевых продуктов не было обнаружено, что он селектирует перекрестную резистентность к кругу современных ему антибиотиков [Hossak D.J.N., April 6, 1988, Federal Register, Vol. 53, No 66; Szybalsky W., April 6, 1988, Federal Register, Vol. 53, No 66], активность низина в отношении современных ему патогенов с множественной лекарственной устойчивостью после многих лет его бесконтрольного применения в качестве консерванта пищевых продуктов не была до сих пор оценена.
Эти исследования демонстрируют, что не только низин, но и другие родственные соединения класса лантоциновых антимикробных пептидов, включая субтилин, эпидермин, галлидермин, pep 5, циннамицин, дурамицин и анковенин, а также их структурные варианты, полученные методами генетической инженерии или химическим синтезом (полусинтетические соединения), могли бы быть использованы для профилактики или терапии инфекций, вызываемых устойчивыми к антибиотикам бактериями у человека и животных.
К эффективным фармацевтическим препаратам указанных пептидов относятся простые водные растворы, пригодные для парентерального введения активного агента внутривенным (i.v.), внутримышечным (i.m.), подкожным (s.c.) или внутрибрюшинным (i. p. ) способами, таким образом, чтобы в крови и ткани были достигнуты уровни, превышающие минимальную ингибирующую концентрацию (MIC) активного агента, и был обеспечен эффект снижения титра бактерий с целью профилактики, лечения или ослабления инфекции. Принято, что лантоциновый антимикробный агент может вводиться совместно (одновременно или последовательно) с другими антимикробными агентами для того, чтобы эффективнее обеспечить более широкое лечение, особенно специфического диагноза до начала терапии. Считается, что диапазон доз, равный приблизительно 2-200 мг/кг/сутки, обеспечивает эффективное снижение титров бактерий.
Кроме того, полагают, что фармацевтические препараты, пригодные для нанесения на кожу и/или слизистые оболочки, такие как мази, лосьоны, эмульсии или гели на водной или вазелиновой основе, будут полезны для борьбы с устойчивыми к антибиотикам организмами. Например, препарат для наружного применения на основе лантоцина, пригодный для введения в ноздри с концентрацией активного агента, превышающей МIC, и вследствие этого достаточной для снижения титров бактерий, как можно ожидать, будет особенно полезным для контроля MRSA-колонизации у больных и персонала лечебных учреждений, что таким образом уменьшит риск угрожающего жизни инфицирования устойчивыми к антибиотикам микроорганизмами.
Примеры
Штаммы бактерий. Метициллин-резистентный Staphylococcus aureus (MRSA) и Staphylococcus epidermidis (MRSE) являются клиническими изолятами, предоставленными различными европейскими больницами, тогда как высокотоксигенный штамм Streptococcus pyogenes и ванкомицин-резистентные штаммы Enterococcus faecalis являются клиническими изолятами, полученными в США. В отдельных экспериментах тестируют штаммы MRSA из 4 различных стран, штаммы MRSE из Испании, пенициллин-резистентные штаммы Streptococcus pneumoniae из 6 различных стран и ванкомицин-резистентные энтерококки из двух больниц Нью-Йорка. Другие тестируемые изоляты получают из коллекций культур.
Минимальная ингибирующая концентрация (МIC).
МIC определяют, используя способ микроразведений бульона, разработанный NCCLS (Национальный Комитет клинических лабораторных стандартов). В экспериментах с клиническими изолятами MRSA и MRSE и ванкомицин-резистентным Enterococcus faecium используют бульон Мюллера-Хинтона без добавок. В экспериментах с клиническими изолятами MRSA и MRSE из различных европейских больниц и с клиническими изолятами Streptococcus pyogenes и ванкомицин-резистентного Enterococcus faecalis используют триптический соевый бульон. В последних тестах используют 0,02% бычий сывороточный альбумин (конечная концентрация 0,01%) в разбавителе для предотвращения адсорбции низина на пластмассовых лунках для микротитрования.
Минимальная бактерицидная концентрация (МВС).
После определения MIC из лунок, в которых отсутствует рост, отбирают образцы и помещают в счетчик колоний. МВС определяют как самую низкую концентрацию, при которой 99,9% первичного инокулюма погибает после 24 ч контакта.
Лизис бактериальных культур и быстрая бактерицидная активность.
Используемая среда содержит бульон "C+Y" для S. pneumoniae, триптический соевый бульон для стафилококков и бульон с экстрактом сердцевины мозга и сердца для энтерококков. Различные виды бактерий инкубируют при 37oС в течение различных периодов времени с неодинаковыми фиксированными концентрациями низина, как указано в таблицах ниже. Степень лизиса определяют как процент снижения оптической плотности при 600 нм относительно таковой у культуры перед обработкой низином. Кроме того, в некоторых эксперимента образцы удаляют и число живых колоний определяют в основном, как указано выше для МВС.
Модель интраперитонеальной инфекции на мышах, Staphylococcus aureus NCTC 8325 выращивают в бульоне с телячьим эстрактом и инфицируют каждую из мышей внутрибрюшинно дозой, составляющей 103 колониеобразующих единиц (КОЕ), разведенных в бульоне, содержащем 10% бактериологического муцина (Difco). Группы по 5 мышей в каждой либо не получают лечения, либо получают по 10 мг/кг низина, который вводят внутривенно (через хвостовую вену в 0,5 мл водного раствора рН 5,0) через 10 мин после инфицирования. За мышами наблюдают 48 ч с целью регистрации гибели или неблагоприятных симптомов.
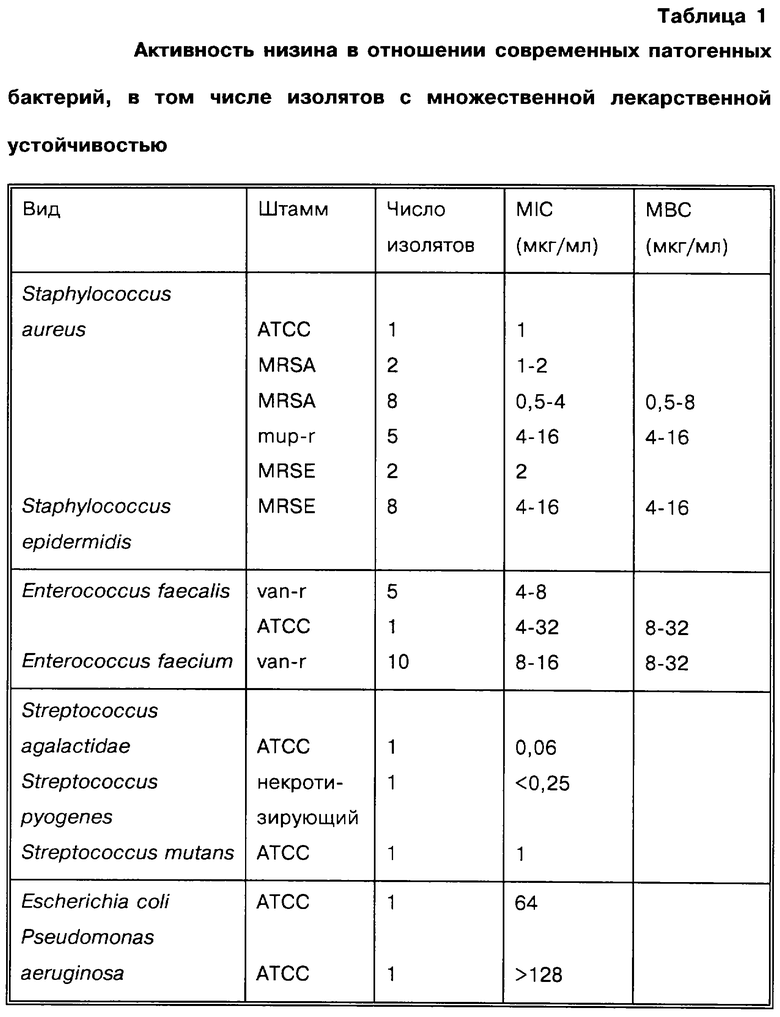
Пример 1. Определение MIC и МВС низина в отношении современных патогенов с множественной лекарственной устойчивостью.
Как показано в табл. 1, низин проявляет высоко эффективную ингибирующую активность (MIC) в отношении как лабораторных штаммов АТСС, так и клинических изолятов различных видов стафилококков, энтерококков и стрептококков, тогда как грамотрицательные бактерии [Escherichia coli и Pseudomonas aeruginosa} являются значительно менее чувствительными. Клинические изоляты включают метициллин-резистентные Staphylococcus aureus (MRSA) и Staphylococcus epidermidis (MRSE), мупироцин-резистентные (mup-r) S. aureus и MRSA и ванкомицин-резистентные (van-r) Enterococcus faecalis и Enterococcus faecium.
Для всех тестированных организмов МВС (та концентрация антибиотика, которая убивает по меньшей мере 99,9% бактерий в течение 24 ч) равна или в нескольких случаях вдвое превышает МIC, указывая на то, что низин является высокобактерицидным агентом для этих микроорганизмов. Наблюдение, что низин бактерициден для энтерококков, в том числе ванкомицин-резистентных штаммов, является неожиданным, поскольку энтерококки устойчивы к бактерицидной активности большинства антибактериальных агентов.
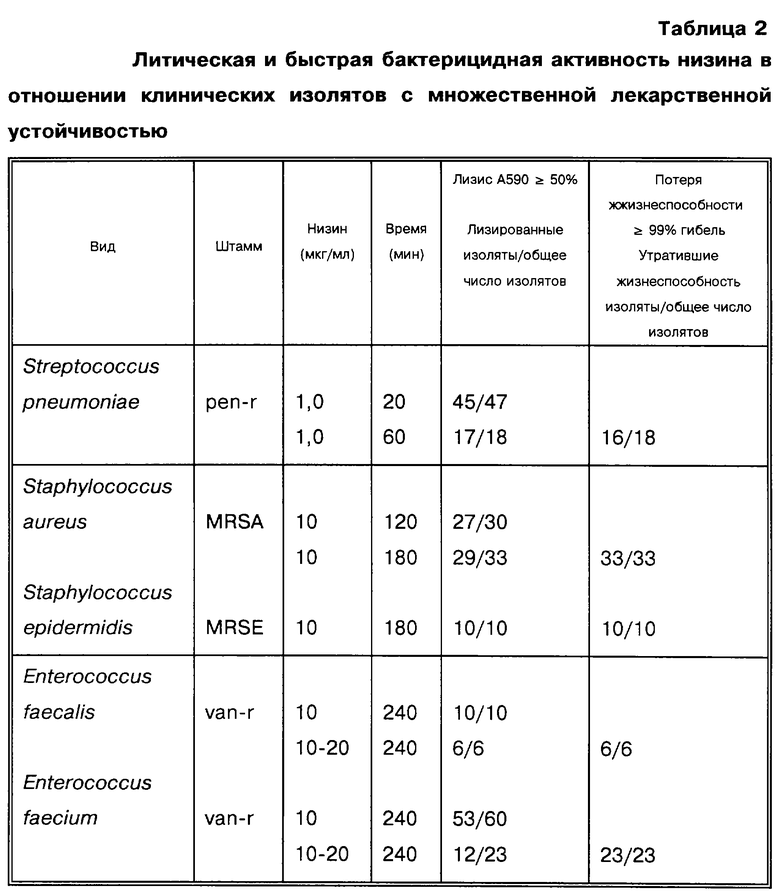
Пример 2. Определение бактерицидной активности низина по отношению к патогенам с множественной лекарственной устойчивостью.
Результаты, полученные в примере 1, подтверждают и расширяют в дополнительных экспериментах, в которых многочисленные клинические изоляты стафилококков и энтерококков с множественной лекарственной устойчивостью, а также пневмококков с множественной лекарственной устойчивостью обрабатывают фиксированными концентрациями низина в течение периодов времени, составляющих от 20 до 240 мин. В конце этих коротких периодов обработки измеряют два параметра: выживаемость клеток (в одной серии экспериментов) и лизис клеток (в обеих сериях экспериментов). Как показано в табл. 2, большинство изолятов обнаруживают лизис, превышающий 50%, определенный по снижению оптической плотности культуры при 600 нм; многие из оставшихся штаммов обнаруживают выявляемый лизис, но не превышающий 50%. Кроме того, образцы обработанных низином изолятов оценивают на жизнеспособность, что также показано в табл. 2. Отмечают, что процент снижения жизнеспособных колоний превышает процент снижения оптической плотности и некоторые изоляты, которые обнаруживают сравнительно небольшое снижение оптической плотности, тем не менее обнаруживают значительное снижение жизнеспособности.
Таким образом, бактерицидное действие низина в отношении этих бактерий не приводит к лизису клеток, хотя лизис, как считают, является поздним событием в реакции бактерий на антибиотик. Все изоляты за исключением двух (оба представлены пневмококками, обработанными низкой концентрацией низина в течение короткого периода времени) интенсивно уничтожаются в течение коротких периодов обработки в экспериментах. Быстрое бактерицидное действие низина в отношении всех изолятов энтерококков (≥ 99% в течение 4 ч) действительно представляет собой значительный результат, полученный для этих организмов.
Пример 3. Эффективность низина при внутрибрюшинной инфекции Staphvlococcus aureus у мышей.
Эффективность низина при инфекции демонстрируют на модельной системе с использованием мышей. В этом случае внутрибрюшинная инфекция приводит к гибели нелеченых животных в течение 18 ч после инфицирования. Как показано в табл. 3, пять из пяти нелеченых животных погибают, тогда как все пять инфицированных животных, которых лечат внутривенным введением 10 мг/кг низина, выживают после инфекции. Этот результат позволяет предположить, что низин является противоинфекционным агентом.
Нелеченые мыши погибают в течение 18 ч.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРЕОДОЛЕНИЯ УСТОЙЧИВОСТИ К ГЕНТАМИЦИНУ У МЕТИЦИЛЛИНОРЕЗИСТЕНТНЫХ ШТАММОВ СТАФИЛОКОККА | 2013 |
|
RU2553601C2 |
| СПОСОБ ЛЕЧЕНИЯ СТАФИЛОКОККОВЫХ ИНФЕКЦИЙ У МЛЕКОПИТАЮЩЕГО (ВАРИАНТЫ) | 1998 |
|
RU2234940C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2666605C2 |
| СПОСОБЫ ЛЕЧЕНИЯ МЕСТНЫХ МИКРОБНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2675360C2 |
| СПОСОБЫ ЛЕЧЕНИЯ МИКРОБНЫХ ИНФЕКЦИЙ, В ТОМ ЧИСЛЕ МАСТИТА | 2014 |
|
RU2662300C2 |
| Гемостатическое антибактериальное средство, способ его получения, медицинское изделие на основе гемостатического антибактериального средства | 2016 |
|
RU2665950C2 |
| КОМБИНАЦИИ ЛИЗИНА БАКТЕРИОФАГА И АНТИБИОТИКА ПРОТИВ ГРАМ-ПОЛОЖИТЕЛЬНЫХ БАКТЕРИЙ | 2013 |
|
RU2659208C2 |
| СОЕДИНЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИЙ | 2018 |
|
RU2779024C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ БЕЛКА РВР2-А И ГОМОЛОГИЧНЫХ ПОСЛЕДОВАТЕЛЬНОСТЕЙ ДЛЯ ЛЕЧЕНИЯ ЗАРАЖЕНИЯ БАКТЕРИЯМИ И ИММУНОДИАГНОСТИКИ БАКТЕРИЙ ТИПА Firmicutes | 2010 |
|
RU2575070C2 |
| КОМПОЗИЦИИ ДЛЯ УСИЛЕНИЯ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТИ МИЕЛОПЕРОКСИДАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2529799C2 |

Предложено: способ лечения инфекции, вызываемой штаммами рода Staphylococcus, Streptococcus, Enterococcus с множественной лекарственной устойчивостью лантоцином типа А из группы: низин, субтилин, эпидермин, галлидермин, рер-5. Лантоцин, в частности низин, обнаруживал литическую и быструю бактерицидную активность в отношении клинических штаммов перечисленных возбудителей. Изобретение расширяет арсенал средств указанного назначения. 4 з.п. ф-лы, 3 табл.
| Навашин С.М | |||
| и др | |||
| Рациональная антибиотикотерапия | |||
| - М.: Медицина, 1982, с | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Солесос | 1922 |
|
SU29A1 |
| Реферат из АБД Medline: Israil A | |||
| Lantibiotics | |||
| Bacteriol-Virusol-Parasitol-Epidemiol | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Реферат из АБД Medline: Bierbaum G, Sahl HG | |||
| Lantibiotics-unusually modified bacteriocin-like peptides from gram-positive bacteria | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| Егоров Н.С | |||
| Основы учения об антибиотиках | |||
| - М.: Высшая школа, 1969, с | |||
| Приспособление для подвешивания тележки при подъемках сошедших с рельс вагонов | 1920 |
|
SU216A1 |
| "Bacteriocins, microcins and Lantibiotics" NATO ASI Series 1995 v.65 p.71 | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
| US 4980163 (PUBLIC HEALT RESEARCH INSTITUTE OF THE CITY OF NEW YORK), Dec 25, 1990 | |||
| Jay P | |||
| Sandford et al | |||
| Guide to antimicrobial therapy | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2003-04-20—Публикация
1996-06-21—Подача