Изобретение относится к новым замещенным 6 и 7-аминотетрагидроизохинолин-карбоновым кислотам, к способу их получения и их применению в качестве лекарственных средств.
В заявках ЕР 0 606 046, WO 95/35276 и WO 96/27583 описываются арилсульфониламиногидроксамкислоты и их действие в качестве ингибиторов матрикс металлопротеиназы. Специальные арилсульфониламинокарбоновые кислоты служат в качестве промежуточных продуктов для представления ингибиторов тромбина (ЕР 0 468 231) и ингибиторов альдозе-редуктазы (ЕР 0 305 947). В заявке ЕР 0757 037 описывается также действие производных сульфониламинокислоты в качестве ингибиторов металлопротеиназы.
В процессе стремления найти эффективные соединения для лечения системного заболевания соединительной ткани было обнаружено, что карбоновые кислоты согласно изобретению являются сильными ингибиторами матрикс металлопротеиназ. При этом особое значение придавалось торможению стромелизина (матрикс металлопротеиназы 3) и нейтрофилов коллагеназы (ММР-8), так как оба энзима, в частности, при разложении протеоглюканов принимали существенное участие как важные составные части хрящевой ткани (A.J.Fosang et al. J.Clin. Invest. 98 (1996) 2292-2299).
Поэтому изобретение относится к соединению формулы I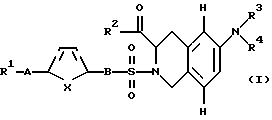
и/или стереоизомерной формы соединения формулы I и/или физиологически переносимой соли соединения формулы I, при этом R1 представляет
1. фенил
2. фенил, который однократно или двукратно замещен
2.1. (С1-С6)-алкилом, неразветвленным, цикличным или разветвленным,
2.2. -ОН,
2.3. (С1-С6)-алкил-С(O)-O-,
2.4. (С1-С6)-алкил-O-,
2.5. (С1-С6)-алкил-O-(С1-С4)-алкил-O-,
2.6. галоген,
2.7. -СF3,
2.8. -CN,
2.9. -NO2,
2.10. НО-С(О)-,
2.11. (С1-С6)-алкил-O-С(O)-,
2.12. метилендиоксо,
2.13. R5-(R6) N-C(O)-, где R5 и R6 являются одинаковыми или различными и представляют собой атом водорода или (С1-С6)-алкил, или
2.14. R5-(R6)N-, где R5 и R6 одинаковые или различные и представляют собой атом водорода или (С1-С6)-алкил,
3. гетероаромат из последующей группы 3.1.-3.15, который является незамещенным или замещен так, как описано в пунктах 2.1-2.14.
3.1. пиррол
3.2. пиразол
3.3. имидазол
3.4. триазол
3.5. тиофен
3.6. тиазол
3.7. оксазол
3.8. изоксазол
3.9. пиридин
3.10. пиримидин
3.11. индол
3.12. бензотиофен
3.13. бензимидазол
3.14. бензоксазол или
3.15. бензотиазол
4. -ОН, а А означает ковалентную связь,
5. -O-R14, а А означает ковалентную связь,
-СН=СН- или -С=С- и где R14 означает
1) (С1-С6)-алкил,
2) (С3-С6)-циклоалкил,
3) бензил или
4) фенил
6. -СООН и А означает ковалентную связь, -СН-СН- или -С≡С-,
7. (С1-С6)-алкил,
8. (С3-С6)-циклоалкил-O-(С1-С4)-алкил,
9. галоген, и А означает ковалентную связь, -СН=СН- или -С≡С-,
10. -CN, и А означает ковалентную связь, -СН=СН- или -C≡C-,
11. -NO2, и А означает ковалентную связь, -СН=СН- или -С≡С-, или
12. -СF3, и
R представляет собой
для 1. HO(H)N- или
2. R7-O, где R7 означает
2.1. атом водорода,
2.2. (С1-С6)-алкил,
2.3. аллил или
2.4. бензил,
R3 и R4 являются одинаковыми или различными и представляют собой
1. атом водорода,
2. (С1-С6)-алкил,
3. фенил-(СН2)m, гдe фенил является незамещенным или однократно или двукратно замещенным, как это описано в пунктах 2.1-2.14, a m означает целое число нуль, 1,2 или 3,
4. R8-(CO)-, где R8 представляет собой
4.1. (С1-С8)-алкил,
4.2. фенил-(СН2)m-, где фенил является незамещенным или однократно или двукратно замещенным, как это описано в пунктах 2.1-2.14, а m представляет собой целое число нуль, 1, 2 или 3,
4.3. R7-O-C(O)-(CH2)n-, гдe R7, как это определено выше, а n означает целое число нуль, 1,2,3,4,5 или 6,
4.4. R7-N(H)-(R9)-C(H)-, где R7, как это определено выше, а R9 означает характерный радикал протеиногенной α-аминокислоты и где R9 является незамещенным или на атоме кислорода или серы однократно или двукратно замещенным (C1-C4)-алкилом, бензилом, аллилом или замещен защитной N-группой,
4.5. R7-C(O)-N(H)-(R9)-C(H)-, где R7 и R9, как это определено в пункте 4.4 или
4.6. R10-O-C(O)-N(H)-(R9)-C(H)-, R9 как определено в пункте 4.4 и где R10 означает
4.6.1 (С1-С6)-алкил,
4.6.2 аллил,
4.6.3 бензил или
4.6.4 (9-фторенил)-метил;;
5. R10-О-С(О)-, где R10 имеет определение, как приведено в п.4.6.1 4.6.4,
6. R15-SO2-, где R15
6.1 (С1-С6)-алкил,
6.2 аллил или
6.3 фенил-(СН2)m- где фенил является незамещенным или однократно или двукратно замещенным, как это описано в пунктах 2.1-2.14, a m является целым числом нуль, 1,2 или 3, или
7. представляет собой Н2N-С(=NН)- или R3 и R4 вместе с атомом N образуют радикал формулы Xa или Хb,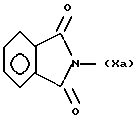

или
R3 и R4 вместе с атомом N образуют нитрорадикал, А представляет собой:
а) ковалентную связь,
б)-О-,
в) -СН=СН- или
г) г) -C≡C-,
В представляет собой a) -(CH2)m-, где m имеет указанное выше значение,
б) -O-(CH2)q, где q означает целое число 1,2,3,4 или 5, или
в) представляет -СН=СН-, и Х представляет собой -СН=СН-, атом кислорода или атом серы.
Под выражением "галоген" понимают фтор, хлор, бром или йод. Под понятием "алкил" или "алкенил" понимают углеводородные радикалы, углеводородные цепочки которых являются прямыми или разветвленными. Цикличными алкильными радикалами являются, например, 3-6-членные моноциклы, такие как циклопропил, циклобутил, циклопентил или циклогексил. Под понятием "R9 характерного радикала протеиногенной аминокислоты" понимают радикалы R формулы Хс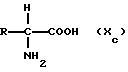
где R происходит от аминокислот: глицин, аланин, валин, лейцин, изолейцин, фенилаланин, тирозин, триптофан, серин, треонин, цистеин, метионин, аспарагин, глутамин, лизин, гистидин, аргинин, глутаминовой кислоты и аспаргиновой кислоты, и могут быть использованы обе энантиомерные формы, а также рацемат или любая смесь. В качестве подходящей N-защитной группы Е используются предпочтительным образом употребляемые для этих целей в пептидной химии N-защитные группы, например защитные группы типа уретана, как, например, бензилоксикарбонил(Z), t-бутилоксикарбонил(Вос), 9-фторенилметоксикарбонил(Fmос) и аллилоксикарбонил(Аlос) или тип кислотного амида, в частности формил, ацетил или трифторацетил алкил-типа, такой как, например, бензил. Особенно хорошо показала себя также группа (триметил-силил)этоксикарбонил (Теос) (P. Kocienski, Protecting Groups, Thieme Verlag, 1994). Далее алкениловые радикалы могут содержать также множество двойных связей.
Исходные вещества для химических преобразований известны, их легко можно получать по методике, известной из литературы.
Далее изобретение касается способа получения соединения формулы I и/или стереоизомерной формы соединения формулы I и/или физиологически приемлемой соли соединения формулы I, который отличается тем, что
а) соединение формулы II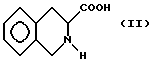
переводят в соединение формулы III,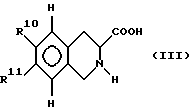
где R10 и R11 означают -NO2 или атом водорода, a R10 и R11 являются неодинаковыми и
б) полученное в пункте а) соединение формулы III вводят в реакцию взаимодействия с соединением формулы IV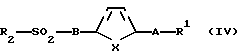
где В, X, А и R1 имеют такие же определения, что и в формуле I, a R2 обозначает атом хлора, имидазолил или -ОН, в присутствии основания или при необходимости обезвоживающего средства, с образованием соединения формулы V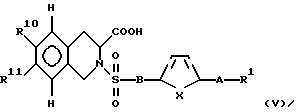
где R10 и R11 означают -NО2 или атом водорода, a R10 и R11 являются неодинаковыми, и
в) полученное в пункте б) соединение формулы V подвергают изомерному разделению и получают соединение формулы I, в
которой R3 и R4 вместе с атомом N образуют радикал NO2, который в позиции 6 или 7 связан с фенильным радикалом, или
г) полученное в пункте в) соединение восстанавливают до соединения формулы I, в которой R3 и R4 означают атом водорода, или
д) полученное в пункте г) соединение ацилируют хлоридами карбоновой или сульфоновой кислоты, имидазолидами карбоновой или сульфоновой кислоты, сложными эфирами хлормуравьиной кислоты, активными сложными эфирами или ангидридами или
е) полученное в пункте д) соединение вводят в реакцию взаимодействия с соответствующей аминокислотой, карбоновой кислотой, альдегидом или, при необходимости с замещенным гуаиндином,
или ж) полученное в пункте е) соединение алкилируют или
з) полученное в пункте а) соединение вводят в реакцию взаимодействия с образованием соединения формулы VI,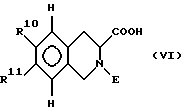
в которой Е представляет собой защитную N-группу, a R10 и R11 имеют указанные выше определения, и
соединение формулы VI разделяют в региоизомеры формул VII и VIII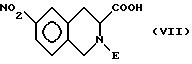
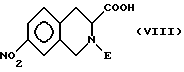
и нитрогруппу вводят в реакцию взаимодействия так, как описано в пункте г), и полученное соединение вводят в реакцию взаимодействия так, как это указано в пунктах д), е) или ж), или
и) соединение, полученное в соответствии со способами з), ж), е), д) или г), вводят в реакцию взаимодействия с получением соответствующих эфиров карбоновой кислоты (R2=O-R7) или с гидроксиламином (R2=-N(H)-ОН).
Изобретение относится также к лекарственному средству, которое отличается эффективным содержанием, по меньшей мере, одного соединения формулы I и/или физиологически переносимой соли соединения формулы I и/или стереоизомерной формы соединения формулы I, вместе с фармацевтически пригодным носителем, вспомогательным веществом и/или другими активными и вспомогательными веществами.
На основе фармакологических свойств соединения согласно изобретению пригодны для профилактики и терапии таких заболеваний, в протекании которых принимает участие усиленная активность металлопротеиназ, разлагающих матрикс. Сюда относятся дегенеративные заболевания суставов, такие как остеоартрозы, спондилезы, атрофия хряща после травмы сустава или после длительного нахождения сустава в состоянии покоя после повреждений мениска и надколенной чашечки или после разрыва связок. Далее сюда же относятся также заболевания соединительной ткани, как например, коллагенозов, периодонтальных заболеваний, незаживление ран и хронические заболевания двигательного аппарата, как например, воспалительные, обусловленные иммунологически или обменом веществ, острые и хронические артриты, артропатии, миальгии и нарушения обмена веществ в костях. Далее соединения формулы I пригодны для лечения язвенной болезни, атеросклероза и стенозов. Далее соединения формулы I пригодны для лечения воспалений, онкологических заболеваний, образования метастазов опухоли, кахексии, анорексии и септического шока.
Лекарственные средства согласно изобретению принимают в основном орально или парентерально. Возможно также ректальный и трансдермальный прием препарата.
Изобретение касается также способа получения лекарственного средства, которое отличается тем, что, по меньшей мере, одно соединение формулы I с помощью фармацевтически пригодного и физиологически приемлемого носителя и при необходимости с помощью других пригодных активных, дополнительных или вспомогательных веществ переводят в соответствующую форму применения.
Соответствующими твердыми или галеновыми формами приготовления являются, например, грануляты, порошки, драже, таблетки (микро)капсулы, суппозитории, сиропы, соки, суспензии, эмульсии, капли или инициируемые растворы, а также препараты с затяжной дачей лекарства, при изготовлении которого находят применение прочие вспомогательные средства, такие как носители, средства взрывания, связующие средства, покрывные средства, средства, вызывающие набухание, средства для улучшения скольжения, вкусовые добавки, сластители и агенты растворения. В качестве часто используемых вспомогательных веществ следует назвать карбонат магния, двуокись титана, лактозу, маннит и другие сахара, тальк, молочный белок, желатин, крахмал, целлюлоза и их производные, животные и растительные жиры, как например, рыбий жир, растительное масло, ореховое масло или сесамовое масло, полиэтиленгликоль и растворители, такие как стерильная вода и одноатомные или многоатомные спирты, как например, глицерин.
Предпочтительным образом фармацевтические препараты приготавливают и дают в дозировочных единицах, причем каждая единица в качестве активной составной части содержит определенную дозу соединения формулы I согласно изобретению. В случае твердых дозировочных единиц, как например, таблетки, капсулы, драже или суппозитории, эта доза может составлять приблизительно до 1000 мг, но предпочтительным образом около 50-300 мг, а в случае инъекционных растворов в форме ампул приблизительно до 300 мг, преимущественно около 10-100 мг.
Для лечения взрослого пациента, весящего около 70 кг - в зависимости от эффективности соединений согласно формулы I - дневные дозы составляют около 20 -1000 мг, предпочтительным образом около 100 -500 мг. Однако при определенных обстоятельствах могут даваться более высокие или более низкие дозы. Прием дневной дозы может происходить однократно в форме отдельной дозирующей единицы или же в форме множественных мелких дозирующих единиц, либо как следствие многократного приема разделенной дозы через определенные интервалы.
1H-NMR-спектры принимались с помощью прибора фирмы ВАРИАН (Varian), работающего на 200 МГц или с помощью прибора фирмы БРУКЕР (Bruker), работающего на 400 МГц, как правило, тетраметилсиланом (TMS) в качестве внутреннего стандарта и при комнатной температуре (RT). В качестве растворителя был использован DMSO-de, если в примечании не указано ничего другого. Конечные продукты определяются, как правило, с помощью методов массоспектроскопии (FAB-, ESI-MS). Температурные данные даются в градусах Цельсия. RT означает комнатная температура (20oС-26oС). Использованные сокращения либо поясняются, либо соответствуют обычным условиям.
Пример 1:
(6/7)-Нитро-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновая кислота
100 г 1,2,3,4-Тетрагидроизохинолин-3-карбоновой кислоты (564 ммоль) растворяют или же суспендируют при -10oС в 500 мл серной кислоты (98%-ная d 1,84) и охлаждают до -30oС. После этого по каплям добавляют 59 г (584 ммоль) нитрата калия, растворенного в 200 мл серной кислоты, и охлаждают до 0oС в пределах 1,5 ч (h). Внутренняя температура повышается при этом снова до -10oС. После окончания добавки нитрата перемешивают еще в течение 10 мин при -10oС и 1 ч без специального охлаждения. Полученный продукт выливают на лед, нейтрализуют при охлаждении концентрированным водным раствором аммиака: расход около 1,8 л 25%-ного раствора. Перед отфильтровыванием аминокислоты производят разбавление таким же объемом воды. Полученное твердое вещество снова суспендируют в воде и очищают фильтрованием от оставшихся растворимых солей аммония. Производят промывку большим количеством холодной воды и высушивают при пониженном давлении при 60oС.
Выход: 110,1 г (88% от теории)
Точка плавления: начиная с 245oС (медленное окрашивание),
272-275oС (при разложении плавится)
1H-NMR: (400 МГц, DCI/D2O) 3,05(dd, 1H 7-изомер);
3,30 (2dd, гетеродинировано, 2 Н, 6- и 7-изомер);
3,44 (dd, "1Н", 6-изомер); 4,25 (m, 2H); 7,20;
7,80 (2m, 3H); доля 6-изомера: 13%
Элементарный анализ: С 53,9 (теор. 54,06), Н 4,50 (теор. 4,55), N 12,6 (теор. 12,61)
IR: 1640 (s), 1540 (s), 1400 (s), 1350 (s) см-1
Пример 2:
Трет-бутилоксикарбонил-(6/7)-нитро-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновая кислота
13,3 г (59,9 ммоль) Соединения из примера 1 растворяют или же суспендируют с 13,1 г (60 ммоль) ди-трет-бутилдикарбоната и 12, 72 г (120 ммоль) карбоната натрия в 300 мл смеси диоксан/вода 1:1 и перемешивают в течение 16 ч при комнатной температуре. После этого диоксан удаляют отгонкой на ротационном испарителе, а оставшуюся водную суспензию покрывают 200 мл уксусного эфира. Производят охлаждение до 5oС, подкисляют с помощью 1н. HCl до рН 3 и отделяют органическую фазу. Она промывается два раза насыщенным раствором NaCl и высушивается над сульфатом натрия. После фильтрации сушильного агента производят упаривание при уменьшенном давлении.
Выход: 18,1 г (94% от теории)
Чистота/распределение изомеров: определение HPLC:
Nucleosil RP 18, 125 х 4 мм, 254 нм, ацетонитрил-0,1 М фосфорной кислоты 5: 95 до 70:30; 6-изомер: время удерживания 14,19 мин, 7-изомер: время удерживания 14,72 мин. Соотношение около 1:9; чистота 99,0%
1H-NMR: (200 МГц) 1,4 (2s, 9H); 3,3 (m, 2H); 4,4-5,0(3 m, 3Н); 7,4-8,2 (5 m, 2H); 12,7 (s, 1H)
Пример 3:
Дициклогексиламмониевая соль 2-трет-бутилоксикарбонил-7-нитро-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновой кислоты
Для отделения региоизомеров 10 г соединения из примера 2 растворяют в 300 мл уксусного эфира и при комнатной температуре смешивают с 1 эквивалентом (6,2 мл) дициклогексиламина в 10 мл уксусного эфира.
В холоде после добавления n-гептана медленно кристаллизуют дициклогексиламмониевую соль, которую спустя 16 часов отфильтровывают и высушивают. После двух последующих перекристаллизации доля 6-изомера составляет менее чем 1,0% при общей чистоте более 99%. Из маточного раствора можно получать дальнейший материал.
Выход: 6,1 г (первая фракция)
Чистота/распределение изомеров: определение HPLC:
Nucleosil RP 18, 125 х 4 мм, 254 нм, ацетонитрил-0,1 М фосфорной кислоты 5:95 до 70:30; 6-изомер: время удерживания 13,51 мин, 7-изомер: время удерживания 14,23 мин. Соотношение >1:99
1H-NMR: (200 МГц) 0,9-1,9 (множество m, ok. 30 Н); 2,7-3,05; 3,4; 4,6 (5 около 5 Н); 7,4; 8,0 (2m, 3H);
Значение завихрения: -23,6o (МеОН, С=1)
Пример 4:
2-Трет-бутилоксикарбонил-7-нитро-1,2,3,4-тетрагидро-изохинолин-(R)-3-карбоновая кислота
Для освобождения защищенной аминокислоты соль DCHA из примера 3 растворяют в уксусном эфире и встряхивают с избытком водного 10%-ного раствора лимонной кислоты. Органическая фаза встряхивается с насыщенным раствором NaCl, высушивается над сульфатом натрия и упаривается при уменьшенном давлении.
Выход: между 87 и 95%
1H-NMR: Характерные сигналы дициклогексиламина отсутствуют. Освобожденное соединение подвергают непосредственной дальнейшей переработке.
Пример 5:
Гидрохлорид 7-нитро-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновой кислоты 0,5 г соединения из примера 4 (1,55 ммоль) смешивают и 19 мл НСl в простом эфире и перемешивают в течение 30 мин при RT, упаривают досуха, многократно коэваполируют с помощью толуола и при пониженном давлении.
Выход: 0,385 г (96% от теории)
1H-NMR: (200 МГц) 3,2 3,6 (m, 2 Н); 4,3-4,6 (m, 3Н); 7,6 (d, 1 Н); 8,1 (dd, 1H); 8,3 (d, Ih); 10,5 (s, br., 3H) MS: 223,1 (M+H)
Значение завихрения: +143,5o (с=1, МеОН)
Пример 6:
2-Трет-бутилоксикарбонил-7-амино-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновая кислота
38 г нитросоединения из примера 4 (117 ммоль) гидрируют с помощью 2 г 10% Pd на С в метаноле 7 ч при RT и легком повышенном давлении на Parr-аппаратуре. После выпаривания растворителя остаток промывают диизопропиловым эфиром и перекристаллизовывают из смеси вода/этанол, а затем высушивают при уменьшенном давлении.
Выход: 33 г (95% от теории)
1H-NMR: (200 МГц) 1,4 (2s, 9H); 2,9; (m, 2Н); 4,2-4,8 (множество m, 3Н); 6,4(m, 2Н); 6,8 (m,1H).
MS: 293,1 (M+Н)
Значение завихрения: +28,33o (с=1, Метанол)
Пример 7:
2-Трет-бутилоксикарбонил-(6/7)-амино-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновая кислота
Для восстановления аминокислоты из примера 2 выполняют все действия, какие описаны в примере 6. Сырой продукт упаривают при пониженном давлении.
1H-NMR: (200 МГц) 1,4 (2s, 9Н); 2,9(m, 2Н); 4,2-4,8 (множество m, 3Н); 6,4(т, широкая, 2Н); 6,8 (m, 1Н).
MS: 293,1 (М+Н)
Пример 8:
2-Трет-бутилоксикарбонил-7-амино-1,2,3,4-тетрагидро-изохинолин-(R)-3-карбоновая кислота (альтернативный способ)
Смесь изомеров из примера 7 обрабатывают при жаре кипения ацетонитрилом. После охлаждения производят фильтрацию. Эту обработку проводят 2-3 раза.
1H-NMR: (200 МГц) 1,4 (2s, 9H); 2,9; (m, 2H); 4,2-4,8 (множество m, 3Н); 6,4 (m, 2H);6,8 (m, 1H). Разницы по отношению к примеру 6 нет.
MS: 293,1 (M+Н)
Значение завихрения: +28,13o (с=1, Метанол)
Пример 9:
Дигидрохлорид 7-амино-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновой кислоты
0,5 г (1,7 ммоль) Соединения из примера 8 обрабатывают при RT в течение 30 мин. НСl в простом эфире. После упаривания при пониженном давлении упаривают совместно с толуолом и освобождают продукт от остатков растворителя в вакууме, создаваемом масляным насосом.
Выход: 0,41 г (91% от теории)
1H-NMR: (200 МГц) 3,0-3,5 (m, 2H); 4,2-4,5 (m, 3Н); 7,1-7,4 (2m, 3Н); 10,0 (s, широкая, 1H)
MS: 193,0 (M+Н)
Значение завихрения: +86,3o (С=1, Метанол)
Пример 10:
2-(4-Метоксибензолсульфонил)-7-амино-1,2,3,4-тетрагидроизохинолин-(R)-3-(N-гидрокси)-карбоксамид
2-(4-Метоксибензолсульфонил)-7-(трет-бутоксикарбонил)-амино-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновую кислоту получают в стандартных условиях, которые известны специалисту, из соединения, приведенного в примере 1, путем, приведенным в варианте способа а) (образование сульфонамида с помощью хлорида 4-метоксибензолсульфоновой кислоты, хроматографическая очистка 6/7-изомеров (пример 13), восстановление нитрогруппы до аминогруппы (пример 12) и введение защитной группы Вос).
Для получения гидроксамовой кислоты растворяют 10 г (22 ммоля) 2-(4-метоксибензолсульфонил)-7-(трет- бутоксикарбонил)-амино-1,2,3,4-тетрагидроизохинолин-(R)-3-карбоновой кислоты в 100 мл тетрагидрофурана (THF), охлаждают до температуры -15oС и по очереди смешивают с 2,1 мл (22 ммоля) этилового эфира хлормуравьиной кислоты, 4,8 мл (44 ммоля) N-метилморфолина и спустя 45 мин при этой температуре с 13,5 мл (110 ммоль) O-триметилсилил гидроксиламина. Перемешивают еще 3 ч при RT, удаляют растворитель при пониженном давлении, поглощают уксусным эфиром и встряхивают по очереди с 10%-ным раствором лимонной кислоты, 10%-ным раствором карбоната натрия и насыщенным раствором NaCl, высушивают над сульфатом натрия, выпаривают на ротационном упаривателе и удаляют остатки растворителя в вакууме, создаваемом масляным насосом.
2,6 г Этого приведенного в качестве примера 11 соединения (общий выход 9,1 г) смешивают после хроматографической очистки с 50 мл НСl в диэтиловом эфире и перемешивают 30 мин при RT. После этого при пониженном давлении производят упаривание, а остаток упаривают совместно с толуолом.
Выход: 1,97 г (89% от теории)
1H-NMR: 2,75 (m, 2H); 3,8(s, 3Н); 4,40(m, 3Н); 6,9 7,3(m, 3Н); 7,0; 7,7(2d, 4H); 8,8; 9,3; 10,7 (3s, 3Н)
Соединения, названные в таблице 1, получены аналогично предшествующим примерам.
Фармакологические примеры
Получение и определение энзиматической активности каталитических доменов человеческого стромелизина и нейтрофиленовой коллагеназы.
Оба энзима - стромелизин (ММР-3) и нейтрофиленколлагеназа (ММР-8) - были получены по Ye et al. (Biochemistry; 31 (1992), стр. 11231-11235). Для замерения энзиматической активности или энзиматического ингибиторного действия в течение 15 мин инкубируют 70μ1 буферного раствора и 10μ1 ферментного раствора с 10μ1 10%-ного (v/v) водного раствора диметилсульфоксида, который при необходимости содержит энзиматический ингибитор. После добавления 10μ1 10%-ного (v/v) водного раствора диметилсульфоксида, который содержит 1 ммоль/л субстрата, с помощью флуоресценцескопии отслеживается ферментная реакция (328 нм(ех)/393 нм(еm)).
Энзиматическую активность определяют как увеличения поглощения (экстинции) в минуту. Приведенные в таблице 2 значения IC50 определяют в виде таких концентраций ингибитора, которые соответственно ведут к 50%-ному ингибированию энзима.
Буферный раствор содержит 0,05% Brij (Sigma, Deisenhofen, Deutschland), а также 0,1 моль/л Tris/HCl, 0,1 моль/л NaCl, 0,01 моль/л CaCl2 и 0,1 моль/л пиперазин-N,N'-бис/2-этан-сульфоновой кислоты/ (рН 6,5).
Раствор энзима содержит 5μ1/мл одного из полученных по Ye et al энзимных доменов. Раствор субстрата содержит 1 ммоль/л флуорогенного субстрата (7-метоксикумарин-4-ил)ацетил-Рro-Lеu-Gly-Leu-3-(2', 4'-динитрофенил)-L-2,3-диаминопропионил-Ala-Arg-NH2 (Bachem, Heidelberg, Deutschland).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЦИКЛИЧЕСКИЕ И ГЕТЕРОЦИКЛИЧЕСКИЕ N-ЗАМЕЩЕННЫЕ α-ИМИНОГИДРОКСАМОВЫЕ И КАРБОНОВЫЕ КИСЛОТЫ | 1996 |
|
RU2164914C2 |
| ЗАМЕЩЕННЫЕ ДИАМИНОКАРБОНОВЫЕ КИСЛОТЫ | 1998 |
|
RU2196768C2 |
| ЗАМЕЩЕННЫЕ АЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2047604C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПУРИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1997 |
|
RU2228335C2 |
| НОВЫЕ ЦИКЛОАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕЗОРБЦИИ КОСТИ И АНТАГОНИСТОВ РЕЦЕПТОРА ВИТРОНЕКТИНА | 1997 |
|
RU2180331C2 |
| АНТАГОНИСТЫ ВИТРОНЕКТИНОВОГО РЕЦЕПТОРА, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 1997 |
|
RU2198892C2 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОИЗОХИНОЛИНА, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ СИНАПТИЧЕСКОГО ЗАХВАТА ДОПАМИНА И СПОСОБ ЛЕЧЕНИЯ | 2000 |
|
RU2293728C2 |
| ПРОИЗВОДНЫЕ ГИДРОКСИМЕТИЛФУРАЗАНКАРБОНОВОЙ КИСЛОТЫ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1994 |
|
RU2134687C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОЛЕФИНОВ | 1992 |
|
RU2111211C1 |
| Производные фосфиновых и фосфоновых кислот, способ их получения и фармацевтическая композиция на их основе | 1999 |
|
RU2224762C2 |
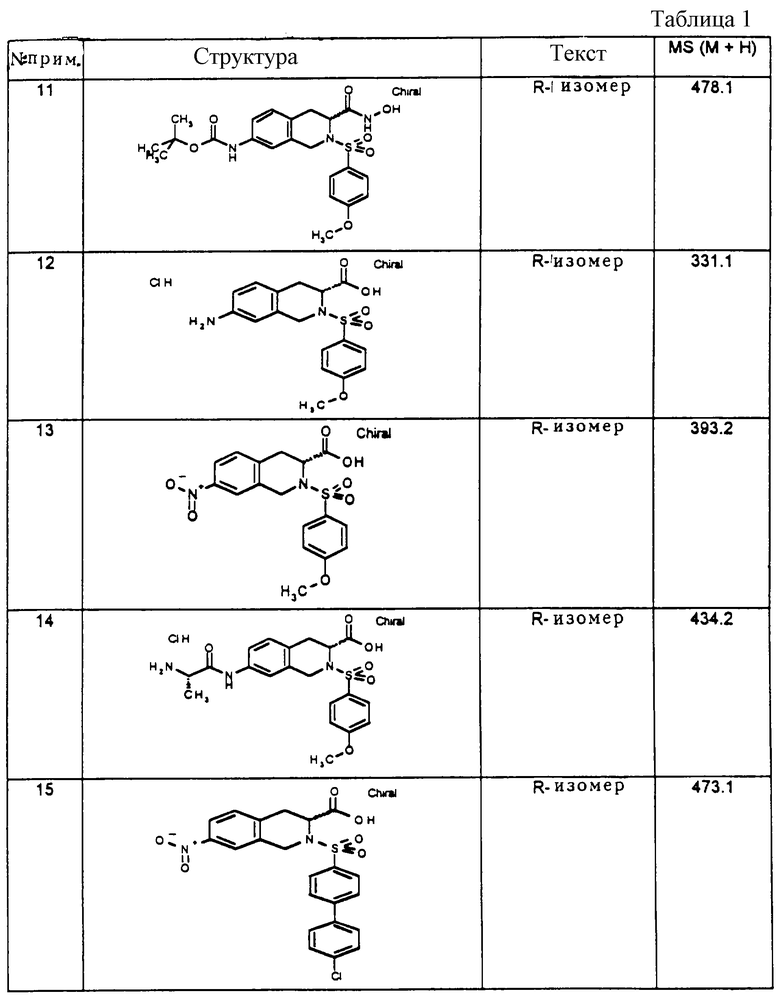
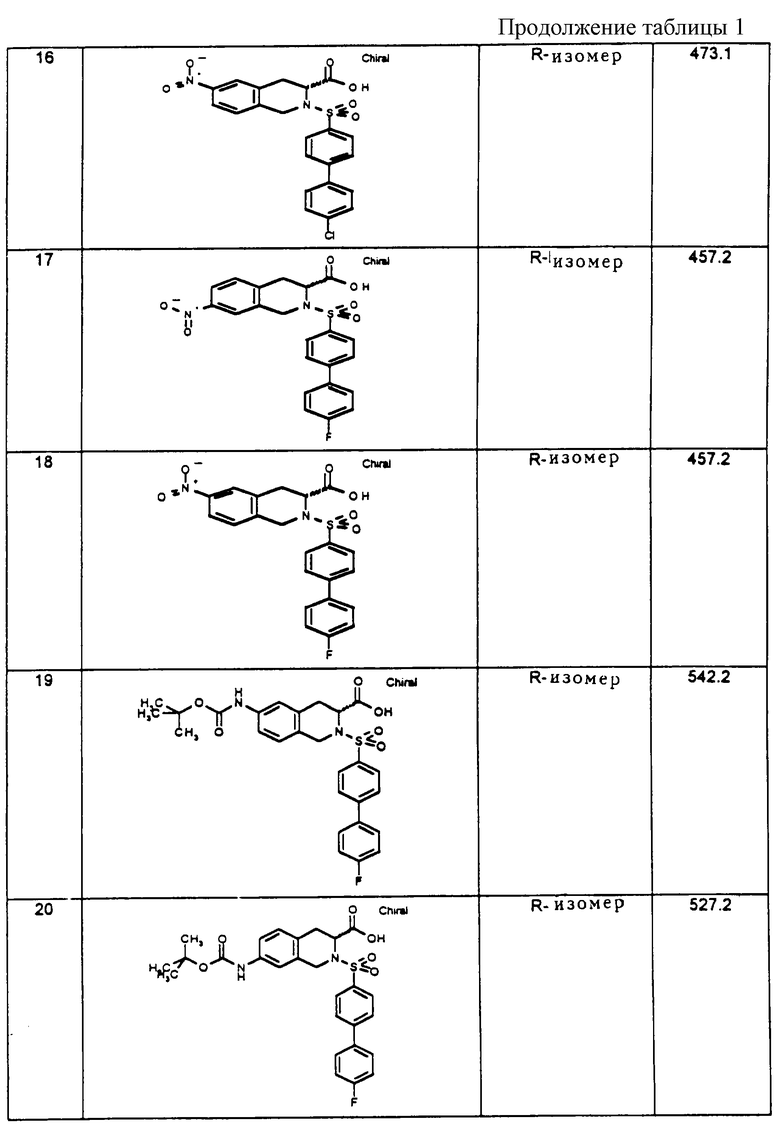
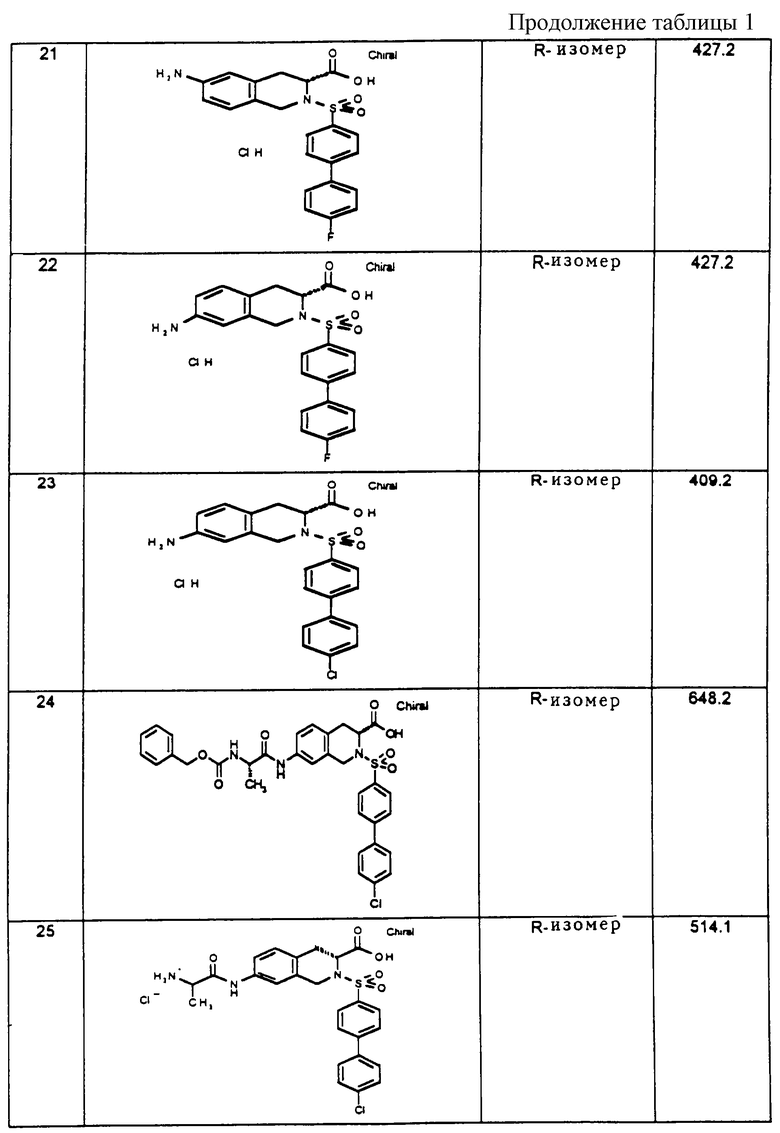
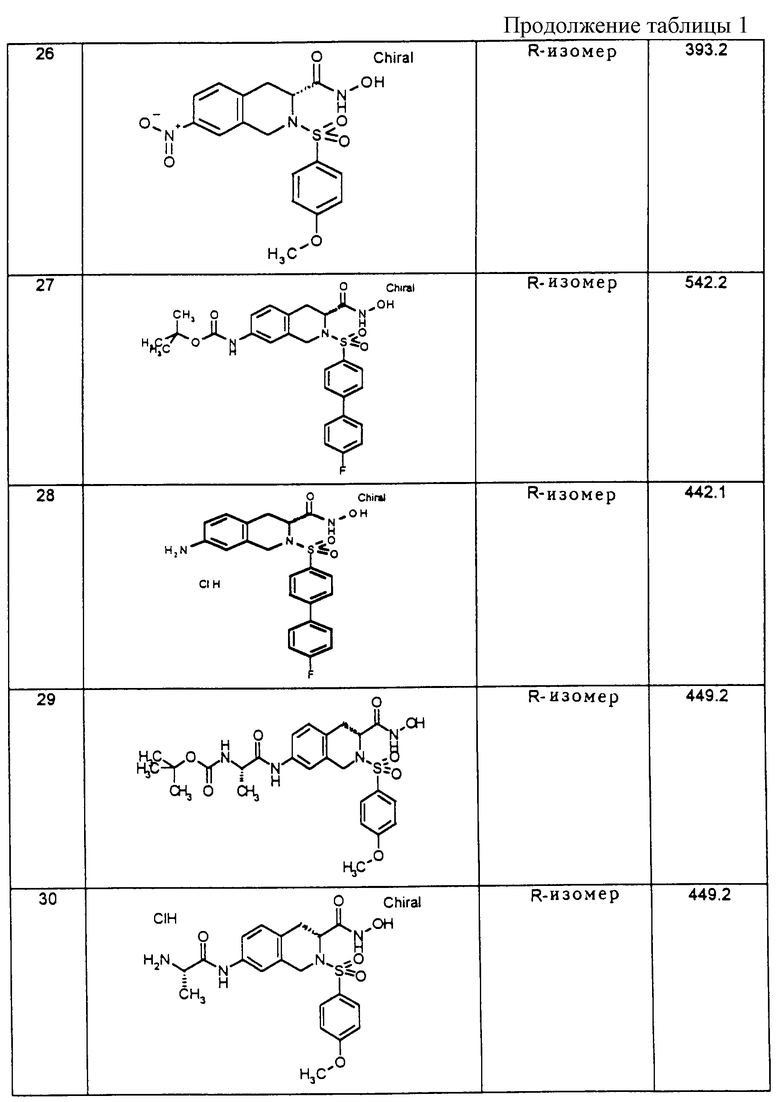


Описываются замещенные 6- и 7-аминотетрагидроизохинолинкарбоновые кислоты формулы (1) и/или ее R-изомерная форма, и/или ее физиологически переносимые соли, где R1 фенил, однократно замещенный (С1-С6)-алкил-O-, галогеном; -OR14, где R14 - (С1-С6)-алкил; R2 - НО(Н)N- или R7-O-, где R7 - атом водорода или (С1-С6)-алкил; R3 и R4 - одинаковые или различные и означают атом водорода, R8-(СО)-, где R8 представляет собой R7-О-С(О)-(СН2)n -, n= 0, R7-N(H)-(R9)-C(H)-, где R9 означает характерный радикал протеиногенной 2-аминокислоты аланин, R10-O-C(O)-N(H)-(R9)-C(H)-, где R10 -(С1-С6)-алкил или бензил ; R3 и R4 вместе с атомом N образуют нитрорадикал, А - ковалентная связь, В - (СН2)m, где m=0, х - CH=CH-. Технический результат заключается в том, что соединения являются ингибиторами матрикс металлопротеиназ. 1 з.п.ф-лы, 2 табл.
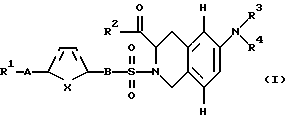
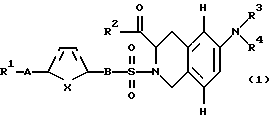
и/или ее R-изомерная форма и/или ее физиологически переносимые соли, при этом R1 представляет фенил, который однократно замещен (C1-С6)-алкил-О-, галогеном, -OR14, где R14 означает (C1-С6)-алкил;
R2 означает HO(H)N- или R7-О-, где R7 означает атом водорода или (С1-С6)-алкил;
R3 и R4 являются одинаковыми или различными и означают атом водорода;
R8-(CO)-, где R8 представляет собой R7-O-C(O)-(CH2)n-, где R7, как это определено выше, а n= 0;
R7-N(Н)-(R9)-C(H)-, где R7, как это определено выше, а R9 означает характерный радикал протеиногенной α-аминокислоты аланин;
R10-O-C(O)-N(H)-(R9)-C(H)-, R9, как определено, и где R10означает (C1-C6)-алкил или бензил;
R3 и R4 вместе с атомом N образуют нитрорадикал;
А представляет собой ковалентную связь;
В представляет собой -(СН2)m-, где m= 0;
Х представляет собой -СН= СН-.
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Турбохолодильник для системы кондиционирования воздуха | 1976 |
|
SU606046A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Способ получения арилсульфонамидных производных 1,2-дигидрохинолина | 1975 |
|
SU575349A1 |
Авторы
Даты
2003-09-20—Публикация
1998-05-12—Подача