Предпосылки создания изобретения.
Область, к которой относится изобретение.
Настоящее изобретение в общих чертах относится к области технологии липидов/липосом и доставки ДНК. Более конкретно настоящее изобретение относится к стабилизации композиций "липид:ДНК" в процессе распыления.
Описание предшествующего уровня техники
Разработка липосомных композиций, совместимых с аэрозольной доставкой, дает возможность с помощью аэрозольного распылителя осуществлять доставку препаратов нуклеиновых кислот, биологическая активность которых поддерживается на уровне, достаточном для терапевтического использования. Использование липосом для аэрозольной доставки имеет много преимуществ, а именно их совместимость с водой; возможность поддерживать пролонгированное поступление терапевтических количеств лекарственного средства в легкие; и кроме того, облегчение доставки липосом вовнутрь клеток, а в частности в эпителиальные клетки дыхательных путей.
Эффективность локальной, местной терапии посредством аэрозольного введения определяется количеством лекарственного средства, доставляемого в пораженные участки легких; и существует несколько различных ключевых параметров, определяющих уровень доставки, который влияет на обеспечение терапевтической эффективности аэрозольных композиций. Так, например, важными факторами являются конструкция ингалятора, скорость потока, объем потока, размер частиц, гигроскопичность и наличие вспомогательного оборудования (систем трубок, соединителей, наконечников для рта, масок для лица и т.п.). Поэтому эффективный выход аэрозольных частиц соответствующего размера может быть увеличен посредством правильной эксплуатации соответствующего устройства для распыления. Неправильная эксплуатация этого устройства и/или неточные параметры могут приводить к нежелательному изменению доз вдыхаемого лекарственного препарата и участков доставки этих доз, а также негативно влиять на терапевтический эффект.
Состав лекарственной композиции также является существенным фактором, регулирующим эффективный выход аэрозоля и аэродинамические свойства липосом, содержащих лекарственное средство. Было обнаружено, что эффективный выход липосом, содержащих лекарственное средство, может быть увеличен путем использования липосом, изготовленных в условиях низких температур фазового перехода (см., Wal.drep et al., J. of Aerosol Med. 7:1994 (1994) и Wal.drep et al. , Int'l J. of Pharmaceutics 97: 205-12 (1993)). Дополнительным способом увеличения аэрозольного выхода липосом, содержащих лекарственное средство, является повышение концентраций лекарственного средства и фосфолипидного резервуара. Распыление некоторых липосомных композиций, содержащих лекарственное средство, при концентрации выше 50 мг/мл приводит к засорению распыляющего сопла; тогда как композиции с пустыми липосомами при концентрации вплоть до 150 мг/мл успешно поддавались распылению (см., Thomas et al., Chest 99: 1268-70 (1941)). Кроме того, характеристики аэрозолей (выход и размер частиц) определяются частично их физико-химическими свойствами, такими как вязкость и поверхностное натяжение. Эти свойства влияют на максимальные концентрации липосом с лекарственным средством, которые могут быть доставлены с помощью аэрозольного распылителя.
Проблема, связанная с аэрозольной доставкой композиций "катионный липид: плазмидная ДНК", осуществляемой в целях проведения направленной генной терапии легких, заключается в том, что этот способ распыления приводит к значительному снижению трансфекционной эффективности композиций. Это является главной причиной относительно низкой эффективности in vivo-переноса генов, доставляемых с помощью аэрозольных композиций. Быстрая потеря активности обусловлена большим разнообразием аэрозольных распылителей и композиций "липид:ДНК".
В предшествующем уровне техники отсутствовали какие-либо эффективные способы увеличения уровня стабилизации композиций "липид:ДНК" в процессе распыления. Настоящее изобретение удовлетворяет уже давно ставшим актуальными требованиям и целям в данной области техники.
Краткое описание изобретения
В одном из вариантов своего осуществления настоящее изобретение относится к липосомной аэрозольной композиции, содержащей: (1) фармацевтическое соединение, (2) катионный липид, (3) нейтральный колипид и (4) триптон.
В другом варианте своего осуществления настоящее изобретение относится к липосомной аэрозольной композиции, содержащей: (1) фармацевтическое соединение, (2) катионный липид, (3) нейтральный колипид и (4) глутаминовую кислоту.
В другом варианте своего осуществления настоящее изобретение относится к распыляемой суспензии катионного липида:колипида:ДНК, используемой для липид-ДНК-трансфекции, где указанным катионным липидом является бис(гуанидиний)-трен-холестерин (BGTC).
В еще одном варианте осуществления настоящего изобретения аэрозольную обработку делают более продуктивной и более эффективной путем помещения мышей в закрытую камеру с их последующей обработкой аэрозольным составом, который распыляют в течение одной минуты через каждые 10 минут. В этом устройстве для обеспечения более глубокого дыхания животных, а следовательно, оседания композиций для трансфекции в легких вместо воздуха, имеющегося в помещении, используют сжатый воздух, содержащий 5%-ную двуокись углерода.
Другие и дополнительные аспекты, отличительные признаки и преимущества настоящего изобретения будут очевидны из нижеследующего описания предпочтительных вариантов осуществления настоящего изобретения, приведенных в целях раскрытия сущности изобретения.
Краткое описание чертежей
Для осуществления настоящего изобретения и более глубокого понимания его сущности, где вышеупомянутые отличительные признаки, преимущества и цели, а также другие факторы будут очевидными из дальнейшего описания, ниже приводится более детальное описание кратко изложенного выше изобретения со ссылками на некоторые конкретные варианты его осуществления, проиллюстрированные в прилагаемых чертежах. Эти чертежи являются частью описания настоящего изобретения. Однако при этом следует отметить, что прилагаемые чертежи иллюстрируют предпочтительные варианты осуществления изобретения, а поэтому не должны рассматриваться как некое ограничение изобретения.
На фиг.1 показано, что добавление 1,3%-ного триптона к распыляемому раствору давало аналогичный, но промежуточный уровень защиты от потерь, ассоциированных с распылителем.
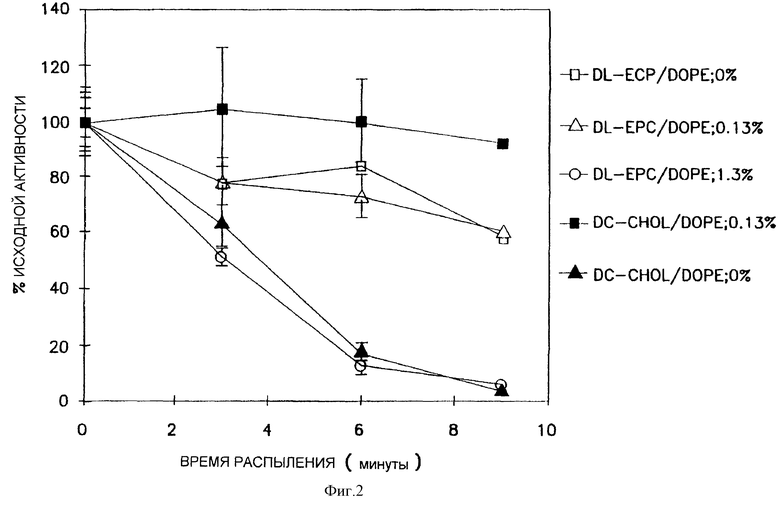
На фиг.2 проиллюстрировано сравнительное действие триптона на ассоциированные с распылителем потери с использованием различных липидов.
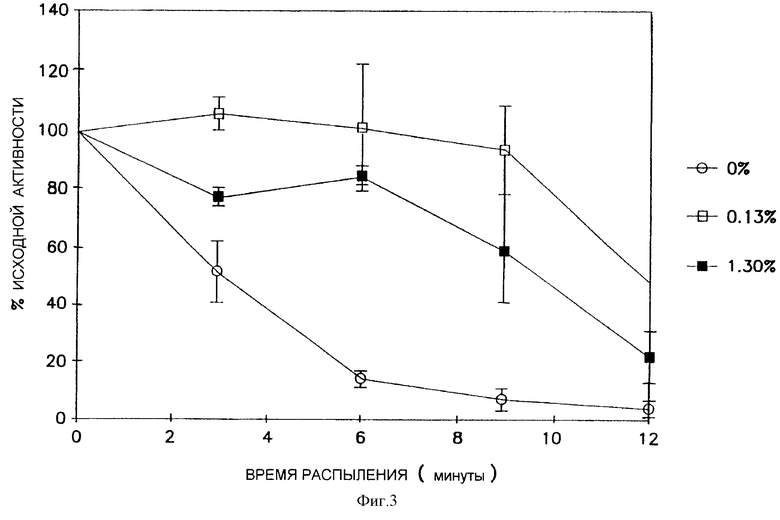
На фиг.3 показано, что глутаминовая кислота также обеспечивает значительную степень защиты от ассоциированных с распылителем потерь в активности трансфекции клеток в случае, если эта глутаминовая кислота присутствует в концентрации, эквивалентной ее концентрациям в триптоне.
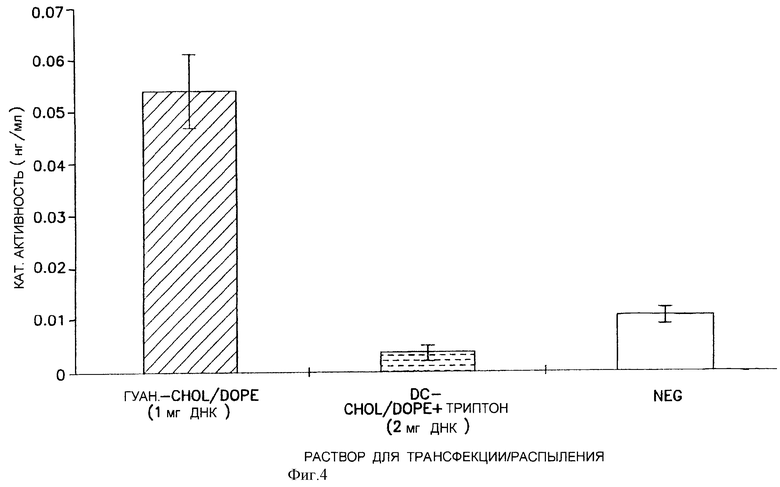
На фиг.4 проиллюстрирована аэрозольная In vivo-обработка мышей Bal.b/C. В этом эксперименте животных подвергают либо периодической аэрозольной обработке указанными композициями "липид: ДНК" (ген хлорамфеникол-ацетилтрансферазы), либо неаэрозольной обработке (NEG). Эту обработку осуществляют путем помещения животных в закрытую камеру, подсоединенную к распылителю с одним соплом Puritan Bennett 1600, и введения в течение 1 минуты аэрозоля с последующим прекращением его введения на 9 минут для того, чтобы дать возможность этим животным вдыхать распыленный аэрозоль перед началом следующего цикла. Для обеспечения глубокого дыхания аэрозольный распылитель приводится в действие сжатым воздухом, содержащим 5% двуокись углерода. Эту процедуру повторяют до тех пор, пока не израсходуется вся жидкость в распылителе (прибл. 16 часов). Затем через 48 часов после окончания аэрозольной обработки животных умерщвляют, легкие удаляют, а ткани экстрагируют и анализируют (с помощью ELISA) на САТ-активность.
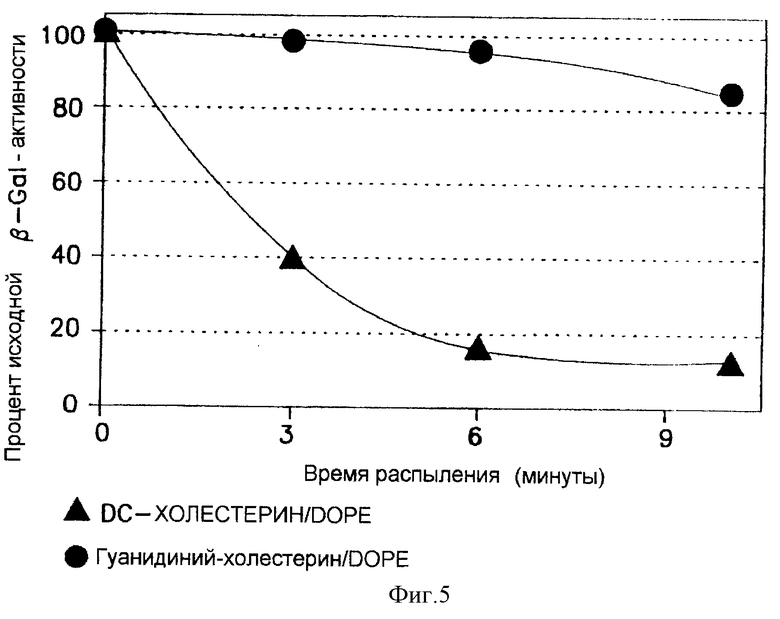
На фиг. 5 проиллюстрировано влияние катионного липида на стабильность трансфекции в процессе распыления. Как подробно описано ниже, композиции "липид: ДНК" были подвергнуты процессу распыления с вышеуказанной продолжительностью, при этом из резервуара распылителя брали образцы и подвергали количественному мониторингу в анализе на in vitro-трансфекцию с использованием клеток А549 (рака легких человека) в культуре. Активность гуанидиний-холестерина/DOPE представлена в виде средних значений от двух экспериментов и является гораздо более стабильной в процессе распыления, чем активность DС-холестерина/DОРЕ (показано) и ряд других обычно используемых липидов, который на этом графике не показан.
Подробное описание изобретения
Настоящее изобретение относится к липосомной аэрозольной композиции, содержащей: (1) фармацевтическое соединение, (2) катионный липид, (3) нейтральный колипид и (4) триптон. В одном из вариантов этой липосомной аэрозольной композиции указанным фармацевтическим соединением является геном в форме плазмидной ДНК. Характерными примерами используемых фосфолипидов являются фосфатидилхолин яичного желтка, гидрогенизированный фосфатидилхолин сои, димиристоилфосфатидилхолин, дилауроилфосфатидилхолин, диолеолилдипальмитоилолеилфосфатидилхолин, бис(гуанидиний)-трен-холестерин и дипальмитоилфосфатидилхолин. Этот колипид обычно представляет собой нейтральный фосфолипид. Характерными примерами подходящих колипидов являются диолеоилфосфотидилэтаноламин (DOPE), аналоги диолеоилфосфотидилэтаноламина и холестерин. Обычно в этой композиции триптон присутствует в количестве, достаточном для усиления трансфекции суспензии "ДНК:липида" после ее распыления. Такие концентрации, в основном, составляют от около 0,1% до около 5%.
Настоящее изобретение также относится к липосомной аэрозольной композиции, содержащей: (1) фармацевтическое соединение, (2) катионный липид, (3) нейтральный колипид и (4) глутаминовую кислоту. В одном из вариантов этой липосомной аэрозольной композиции указанным фармацевтическим соединением является ген. Характерными примерами подходящих фосфолипидов являются фосфатидилхолин яичного желтка, гидрогенизированный фосфатидилхолин сои, димиристоилфосфатидилхолин, дилауроилфосфатилхолин, диолеолилдипальмитоилолилфосфатидилхолин, бис(гуанидиний)-трен-холестерин и дипальмитоилфосфатидилхолин. Обычно в этой композиции глутаминовая кислота присутствует в количестве, достаточном для усиления трансфекции суспензией "ДНК:липида" после ее распыления. Эти концентрации, в основном, составляют от около 0,1% до около 5%.
Настоящее изобретение также относится к распыляемой суспензии катионного липида: ДНК, используемой для липид-ДНК-трансфекции, где указанным катионным липидом является бис-(гуанидиний)-трен-холестерин, а нейтральным колипидом является DOPE. В указанной суспензии концентрацию бис(гуанидиний)-трен-холестерина/DOPE по отношению к плазмидной ДНК предпочтительно определяют так, чтобы она была оптимальной для трансфекции. Концентрация стабильной композиции зависит от относительных концентраций трех компонентов, т.е. плазмидной ДНК, катионного липида бис(гуанидиний)-трен-холестерина и нейтрального колипида DOPE. Предпочтительное количество плазмидной ДНК составляет от около 40 мкг/мл до около 400 мкг/мл. Оптимальное отношение плазмидной ДНК к объединенным липидам (липидная композиция включает катионный липид и нейтральный колипид в отношении 1:1) составляет приблизительно 1:3. Однако в целях оптимизации для различных применений или для различных плазмид часто допустимы различные небольшие отклонения от указанных соотношений, так, например, более крупные плазмиды имеют более высокий суммарный заряд, а следовательно, для нейтрализации этого заряда требуется большее количество липида. Поэтому, для концентрации ДНК в 400 мкг/мл необходимо использовать приблизительно 600 мкг/мл бис(гуанидиний)-трен-холестерина и 600 мкг/мл DOPE. В композиции с плазмидной ДНК концентрации бис(гуанидиний)-трен-холестерина вплоть до около 1,5 мг/мл (присутствующего в сочетании с DOPE в отношении 1:1) должны быть стабильными. В одном из вариантов распыляемой суспензии катионного липида: ДНК настоящего изобретения отношение количества ДНК к количеству объединенных катионного липида и нейтрального колипида составляет от около 1:1 до около 1:4.
Нижеследующие примеры приводятся в целях иллюстрации различных вариантов осуществления настоящего изобретения и не должны рассматриваться как некое ограничение настоящего изобретения.
Пример 1
Плазмида
Для оценки экспрессии в клетках млекопитающих был использован промотор цитомегаловируса (CMV) вместе с геном E.coli (репортерным геном β-галактозидазы (pCMVβ-gal.). pCMVβ-gal. (Clonetech Laboratories, Inc., Pal. o Alto, CA) получали в виде бактериальной пасты, поставляемой фирмой Genzyme. Inc. и очищали на колонках Qiagen (Qiagen Inc., Chatsworth, CA).
Пример 2
Катионные липиды
DL-EPC/DOPE, 1:1-смесь 1,2-дилауроил-sn-глицеро-3-этилфосфохолина (DL-EPC) и диолеоилфосфатидилэтаноламина (DOPE; Avanti Polar Lipids, Alabaster, AL) получали путем смешивания DL-EPC (5 мг/мл в хлороформе) и DOPE (5 мг/мл в хлороформе) и сушили в атмосфере азота. Затем этот липид растворяли в т-бутаноле при 37oС, замораживали при -80oС и лиофилизовали в течение, по крайней мере, 24 часов. DC-CHOL/DOPE, 1:1-смесь 3β-[N-[(N',N'-диметиламино)этан] -карбамоил] холестерина (DC-CHOL) и DOPE получали путем растворения DC-CHOL в хлороформе с последующим объединением с DOPE. Затем этот липид получали тем же способом, что и DL-EPC/DOPE. Эти липиды хранили при -20oС вплоть до их использования. Затем этот липид нагревали до комнатной температуры и подвергали набуханию с использованием воды для орошения (WFI) в течение, по крайней мере, 30 минут, после чего получали комплекс с ДНК.
Пример 3
Оптимизация отношений ДНК:липид
Оптимальное отношение ДНК:липид определяли с помощью гель-электрофореза. При полной нейтрализации отрицательного заряда ДНК катионным липидом трансфекция культуры тканей максимизируется. Путем изменения отношения ДНК:липид от 1:1 до 1:10 и электрофореза этого комплекса на 1%-ном агарозном ТАЕ-геле может быть достигнуто оптимальное соотношение, поскольку комплекс "нейтральный липид:ДНК" не мигрирует.
Пример 4
Культура тканей
Клетки А549 (клетки карциномы легких человека с морфологией, подобной морфологии эпителиальных клеток) культивировали в модифицированной по способу Дульбекко поддерживающей среде (DMEM), в которую были добавлены очищенная 10%-ная фетальная телячья сыворотка (FBS), 2 мМ L-глутамина и 50 мкг/мл гентамицина.
Пример 5
Трансфекция
За один день до трансфекции клетки А549 засевали при концентрации 1,5•105 клеток на 35-мм чашку. Во время трансфекции эти клетки имели ~80%-ную сплошность. К каждой 175-мкл-аликвоте, взятой из резервуара распылителя, добавляли равный объем Среды с пониженным содержанием сыворотки 2•Opti-mem I (Opti-mem I; Gibco BRL, Grand Island, NY), a затем доводили до конечного объема 3,5 мл с использованием Opti-mem (lx). Среда Opti-mem представляет собой модифицированную минимальную поддерживающую среду Игла, в которую были добавлены факторы роста, и эта среда является идеальной для трансфекции композицией "катионный липид-ДНК". Непосредственно перед трансфекцией клетки дважды промывали средой Opti-mem, а затем покрывали сверху 1 мл трансфецирующего раствора на лунку (для каждого периода времени были трансфецированы 3 лунки). Через 24 часа раствор удаляли, клетки два раза промывали средой Opti-mem и добавляли 1 мл среды с клетками А549. Затем эти клетки инкубировали еще в течение 24 часов, два раза промывали PBS, после чего подвергали лизису.
Пример 6
Количественный анализ эффективности трансфекции с использованием β-галактозидазы
Клетки А549 подвергали лизису с использованием 500 мкл 0,1М Трис-HCl, содержащего 0,5% тритона Х-100. Клеточный дебрис удаляли путем центрифугирования, и концентрацию белка в лизате определяли с помощью анализа на содержание белка с использованием бицинхроновой кислоты (ВСА Protein Assay; Pierce, Rockford, IL). β-Галактозидазную активность количественно оценивали с использованием раствора хлорфенолового кpacного-β-D-галактопиранозида (CPRG; Boehringer Mannheim, Indianapolis, IN), содержащего хлорид магния и β-меркаптоэтанол в забуференном фосфатом физиологическом растворе (PBS). 100 мкл-аликвоту лизата добавляли в лунку 96-луночного планшета, а затем добавляли равный объем раствора CPRG. Эти образцы и стандарты инкубировали при 37oС, а затем считывали на планшет-ридере для микротитрационных планшетов Dynatech MR5000 (Dynatech Laboratories, Inc., Chantilly, VA).
Пример 7
Результаты
При добавлении суспензии "липид:ДНК" до ее распыления некоторые компоненты способствуют значительной стабилизации транфекцирующей способности этих композиций. Это приводит к многократному увеличению количества доставляемого биологически активного генного терапевтического агента.
В нескольких экспериментах добавление 0,13%-ного триптона, ферментного (трипсинового) гидролизата казеина к раствору для распыления приводило к 105%-, 100%- и 93%-ному сохранению трансфекционной активности контрольного (нераспыляемого) материала в in vitro-анализе, проводимом с использованием клеток опухоли легких человека А549 при взятии аликвот периодически подаваемого распылителем материала из резервуара распылителя через 3, 6 и 9 минут распыления соответственно со скоростью потока 15 л/мин и при исходном объеме 5 мл. В отличие от этого, сохранение трансфекционной активности для контроля (без добавления триптона) составляло 51%, 13% и 6%. Добавление 1,3%-ного триптона давало аналогичный, но промежуточный уровень защиты от потерь, ассоциированных с распылителем (см. фиг.1).
Эти результаты были получены для композиции, состоящей из DL-EPC/DOPE в комплексе с плазмидной ДНК pCMVβ-GAL (для экспрессии β-галактозидазы). При повторении эксперимента более двух раз достигалась аналогичная стабилизация трансфекционной активности. Используемым распылителем являлся модифицированный распылитель Puritan Bennett 1600 (Carlsbad, CA), где одна трубка из двойного сопла была удалена, и этот распылитель называют распылителем с одним соплом Puritan Bennett 1600 (РВ sj). Контрольный раствор для распыления состоял из 200 мкг pCMVβ-GAL и 700 мкг DL-EPC/DOPE в комплексе с водой для орошения (WFI; Baxter) с полным объемом 5 мл. Раствор для распыления с 0,13%-ным триптоном содержал то же самое количество плазмидной ДНК и липида. После образования комплекса ДНК и липида в течение 15 минут (конечный объем поддерживался при 5 мл) к раствору для распыления добавляли 50 мкл-аликвоту 13%-ного триптонового маточного раствора (13% мас./об. в WFI). Раствор для распыления с 1,3%-ным триптоном также содержал то же самое количество плазмидной ДНК и липида. После образования комплекса ДНК и липида в течение 15 минут (конечный объем после добавления триптона составлял 5 мл) к раствору для распыления добавляли 0,5 мл-аликвоту 13%-ного триптонового маточного раствора (13% мас./об. в WFI).
Кроме того, аналогичная стабилизация достигалась с использованием композиции, состоящей из DC-CHOL/DOPE и pCMVβ-GAL, что свидетельствовало о том, что этот эффект очевидно не зависит от конкретного катионного липида, выбранного для липидной композиции. Контрольный раствор для распыления состоял из 200 мкг pCMVβ-GAL и 800 мкг DC-CHOL/DOPE в комплексе с WFI с полным объемом 5 мл. Раствор для распыления с 0,13%-ным триптоном содержал то же самое количество плазмидной ДНК и липида. После образования комплекса ДНК и липида в течение 15 минут (конечный объем поддерживали при 5 мл) к раствору для распыления добавляли 50 мкл-аликвоту 13%-ного триптонового маточного раствора (13% мас./об. в WFI). Раствор для распыления с 1,3%-ным триптоном также содержал то же самое количество плазмидной ДНК и липида. После образования комплекса ДНК и липида в течение 15 минут (конечный объем после добавления составлял 5 мл) к раствору для распыления добавляли 0,5 мл-аликвоту 13%-ного триптонового маточного раствора (13% мас./об. в WFI). Сравнительное действие триптона на потери, ассоциированные с данным распылителем при использовании обоих липидов, проиллюстрировано на фиг.2.
Поскольку триптон состоит из ряда компонентов, то был проведен анализ для того, чтобы определить, является ли один или несколько конкретных компонентов ответственными за наблюдаемую стабильность аэрозоля. Глутаминовая кислота, главный аминокислотный компонент триптона, также обеспечивает значительный уровень защиты от ассоциированных с распылителем потерь трансфецирующей активности по отношению к клеткам в том случае, если указанная глутаминовая кислота присутствует в концентрации, эквивалентной концентрациям глутаминовой кислоты, которые должны присутствовать в триптоне и которые являлись эффективными в вышеуказанных экспериментах (см. фиг.3). Этот эксперимент проводили тем же способом, что и ранее описанные эксперименты, с использованием композиции "DC-холестерин:DOPE:pCMVβ-GAL" и глутаминовой кислоты в концентрациях 0,221 мг/мл и 0,975 мг/мл, и этот эксперимент был проведен в дубликатах. Контрольный раствор для распыления состоял из 200 мкг pCMVβ-GAL и 800 мкг DC-Chol/DOPE в комплексе с WFI в полном объеме 5 мл. Раствор для распыления, включающий 0,221 мг/мл глутаминовой кислоты, также содержал то же самое количество плазмидной ДНК и липида.
После образования комплекса ДНК и липида в течение 15 минут к раствору для распыления добавляли 0,227 мл-аликвоту 4,875 мг/мл маточного раствора глутаминовой кислоты (в WFI) (после добавления глутаминовой кислоты конечный объем составлял 5 мл). Раствор для распыления, содержащий 0,975 мг/мл глутаминовой кислоты, также содержал то же самое количество плазмидной ДНК и липида. После образования комплекса ДНК с липидом в течение 15 минут к раствору для распыления добавляли 1 мл-аликвоту 4,875 мл маточного раствора глутаминовой кислоты (в WFI) (после добавления глутаминовой кислоты конечный объем составлял 5 мл).
Пример 7
Плазмида
Для оценки экспрессии в клетках млекопитающих был использован промотор цитомегаловируса (CMV) вместе с геном E.coli (репортерным геном β-галактозидазы (pCMVβ-gal.)) pCMVβ-gal. (Clontech Laboratories, Inc., Pal.o Alto, CA) получали в виде бактериальной пасты, поставляемой фирмой Genzyme, Inc. и очищали на колонках Qiagen (Qiagen Inc., Chatsworth, CA).
Пример 8
Катионные липиды
BGTC/DOPE, 1: 1-смесь бис(гуанидиний)-трен-холестерина и диолеоилфосфатидилэтаноламина (DOPE; Avanti Polar Lipids, Alabaster, AL) получали путем смешивания DL-ЕРС (5 мг/мл в хлороформе) и DOPE (5 мг/мл в хлороформе) и сушили в атмосфере азота. Затем этот липид растворяли в т-бутаноле при 37oС, замораживали при -80oС и лиофилизовали в течение, по крайней мере, 24 часов. DC-CHOL/DOPE, 1:1-смесь 3β-[N-[(N',N'-диметиламино)этан]карбамоил]холестерина (DC-CHOL) и DOPE получали путем растворения DC-CHOL в хлороформе с последующим объединением с DOPE. Затем этот липид получали тем же способом, что и BGTC/DOPE. Полученные липиды хранили при -20oС вплоть до их использования. Затем перед образованием комплекса с ДНК липид нагревали до комнатной температуры и подвергали набуханию с использованием воды для орошения (WFI) в течение, по крайней мере, 30 минут.
Пример 9
Оптимизация отношений ДНК:липид
Оптимальное отношение ДНК:липид определяли с помощью гель-электрофореза. При полной нейтрализации отрицательного заряда ДНК катионным липидом трансфекция культуры тканей максимизируется. Путем изменения отношения ДНК: липид от 1:1 до 1:10 и электрофореза этого комплекса на 1%-ном агарозном ТАЕ-геле может быть достигнуто оптимальное соотношение, поскольку комплекс "нейтральный липид:ДНК" не мигрирует.
Пример 10
Культура тканей
Клетки А549 (клетки карциномы легких человека с морфологией, подобной морфологии эпителиальных клеток) культивировали в модифицированной по способу Дульбекко поддерживающей среде (DMEM), в которую были добавлены 10%-ная очищенная телячья фетальная сыворотка (FBS), 2 мМ L-глутамин и 50 мкг/мл гентамицина.
Пример 11
Трансфекция
Клетки А549 засевали при концентрации 1,5•105 клеток на 35-мм чашку за один день до трансфекции. Во время трансфекции эти клетки имели ~80%-ную сплошность. К каждой 175-мкл-аликвоте, взятой из резервуара распылителя, добавляли равный объем среды с пониженным содержанием сыворотки 2•Opti-mem I (Opti-mem I; Gibco BRL, Grand Island, NY), a затем доводили до конечного объема 3,5 мл с использованием среды Opti-mem (1х). Среда Opti-mem представляет собой модифицированную минимальную поддерживающую среду Игла, в которую были добавлены факторы роста, и эта среда является идеальной для трансфекции композицией "катионный липид-ДНК". Непосредственно перед трансфекцией клетки дважды промывали средой Opti-mem, а затем покрывали сверху 1 мл трансфецирующего раствора на лунку (для каждого периода времени были трансфецированы 3 лунки). Через 24 часа раствор удаляли, клетки два раза промывали средой Opti-mem и добавляли 1 мл среды с клетками А549. Затем эти клетки инкубировали еще в течение 24 часов, два раза промывали PBS, после чего подвергали лизису.
Пример 12
Количественный анализ эффективности трансфекции с использованием β-галактозидазы
Клетки А549 подвергали лизису с использованием 500 мкл 0,1М Трис-HCl, содержащего 0,5% тритона Х-100. Клеточный дебрис удаляли путем центрифугирования, и концентрацию белка в лизате определяли с помощью анализа на содержание белка с использованием бицинхроновой кислоты (ВСА Protein Assay; Pierce, Rockford, IL). β-Галактозидазную активность количественно оценивали с использованием раствора хлорфенолового кpacнoro-β-D-галактопиранозида (CPRG; Boehringer Mannheim, Indianapolis, IN), содержащего хлорид магния и β-меркаптоэтанол в забуференном фосфатом физиологическом растворе (PBS). 100 мкл-аликвоту лизата добавляли в лунку 96-луночного планшета, а затем добавляли равный объем раствора CPRG. Эти образцы и стандарты инкубировали при 37oС, а затем считывали на планшет-ридере для микротитрационных планшетов Dynatech MR5000 (Dynatech Laboratories, Inc., Chantilly, VA).
Пример 13
Стабилизация трансфекции бис(гуанидиний)-трен-холестерином
Настоящее изобретение показало, что некоторые компоненты при их добавлении к суспензии "липид: ДНК" перед распылением в значительной степени стабилизируют трансфекцирующую возможность этих композиций. Более конкретно композиции, содержащие один конкретный катионный липид, оказались значительно более стабильными в процессе распыления, чем ранее протестированные липиды. Этот липид, бис(гуанидиний)-трен-холестерин (BGTC), был отмечен ранее (Оudrhiri et al.., 1997) как возможный кандидат для генной терапии. Однако для введения композиций "липид:ДНК", Oudrhiri и др. использовали лишь метод внутритрахеальной инстилляции и не проводили оценку уровня доставки аэрозоля. Эти композиции при их распылении являются эффективными in vivo (в легких мышей) в качестве агента для генной терапии. Результаты проиллюстрированы на фиг.4.
В двух экспериментах использование бис(гуанидиний)-трен-холестерина приводило к 98%, 95% и 84%-ному сохранению трансфецирующей активности контрольного (нераспыляемого) материала в in vitro-анализе, проводимом с использованием клеток опухоли легких человека А549 при взятии аликвот периодически подаваемого распылителем материала из резервуара распылителя через 3, 6 и 10 минут распыления соответственно со скоростью потока 15 л/мин и при исходном объеме 5 мл. В отличие от этого сохранение трансфецирующей активности для другого, обычно используемого катионного липида (DC-CHOL/DOPE) составляло 40%, 15,7% и 13,5%.
Уровень потерь, наблюдаемый при использовании DC-CHOL/DOPE/, в основном аналогичен уровню, наблюдаемому для ряда катионных липидов, обычно используемых в генной терапии, а в настоящее время и в клинических испытаниях. Эти данные систематизированы на фиг.5. Используемым распылителем является модифицированный распылитель Puritan Bennett 1600 (Carlsbad, CA), где одна трубка от одного из двойных сопел была удалена. Этот распылитель называют распылителем с одним соплом Puritan Bennett 1600 (РВ sj). Контрольный раствор для распыления состоял из 200 мкг pCMVβ-GAL и 700 мкг композиции "катионный липид/колипид" в комплексе с водой для орошения (WFI; Baxter) в полном объеме 5 мл.
Все патенты или публикации, упомянутые в этом описании, отражают известный уровень техники в области, к которой относится настоящее изобретение. Все указанные патенты и публикации вводятся в настоящее описание посредством ссылки так, как если бы каждая отдельная публикация была конкретно и индивидуально введена в настоящее описание посредством ссылки.
Для каждого специалиста в данной области техники очевидно, что настоящее изобретение может быть хорошо адаптировано для осуществления конкретных целей и достижения конечных результатов и вышеупомянутых преимуществ, а также других преимуществ, присущих настоящему изобретению. Примеры настоящего изобретения наряду с методами, процедурами, обработками, молекулами и конкретными соединениями, описанными в настоящей заявке, представляют собой репрезентативные предпочтительные варианты осуществления настоящего изобретения и приводятся лишь в иллюстративных целях, а поэтому не должны рассматриваться как некое ограничение объема изобретения. Модификации и другие применения, которые могут потребоваться специалисту и которые не выходят за рамки сущности изобретения, входят в объем настоящего изобретения, определенный в нижеприведенной формуле изобретения.
Изобретение относится к медицине и биотехнологии и касается стабилизации композиций "липид: ДНК" в процессе распыления. Сущность изобретения включает фармацевтическое соединение, содержащее плазмидную ДНК, несущую ген, катионный липид, нейтральный колипид и триптон или глутаминовую кислоту, а также распыляемую суспензию, включающую катионный липид - бис(гуанидиний)-тренхолестерин, нейтральный колипид - диолеоилфосфотидилэтаноламин или его аналог, а также плазмидную ДНК, несущую ген. Преимущество изобретения заключается в разработке лекарственной формы для генной терапии. 3 с. и 8 з.п.ф-лы, 5 ил.
| US 5641662 А, 24.01.1997 | |||
| US 5211955 А, 18.05.1993 | |||
| JUDRHIRI et al | |||
| Gene transfer by gyanudinium-cholesterol cationic lipids into airway epithelial cells in vitro and in vivo, Pros | |||
| Natl., Acad | |||
| Sci USA, 1997, v.94, р.1651-1656 | |||
| DEBS R.J | |||
| et al | |||
| Regulation of gene expression in vivo by liposome-mediated delivery of purified transcription factor, J | |||
| Biol | |||
| Chem., 1990, v.265, р.10189. |
Авторы
Даты
2003-10-10—Публикация
1999-01-08—Подача