Изобретение относится к области аналитической химии, а именно исследованию способов извлечения, приемов стабилизации проб почвы, зараженных микроколичествами пинаколинового эфира фторангидрида метилфосфоновой кислоты (зомана), и последующего биохимического анализа.
Известны исследования по извлечению микроколичеств зомана из почвы водой с последующей сорбцией вещества смолой XAD - 4 (Trace analysis of chemical warfare agents. 1. An approach to the environmental monitoring of nerve agents. The ministri for foreign affairs of Finland. Helsinki, 1981, p.121.). Анализ проводился на газовом хроматографе с биохимическим детектором.
Существенным недостатком описанного метода является то, что низкие значения коэффициента экстракции не позволяют проводить количественное определение зомана при заражении ниже 0,06 мг•кг-1 (коэффициент экстракции составил 45,0±12,0%). Этот метод был взят нами за ближайший аналог, так как в предлагаемом нами методе для извлечения зомана тоже используется жидкостная экстракция, а для анализа - биохимический метод определения.
Применяемый авторами газовый хроматограф с биохимическим детектором является малодоступным специальным оборудованием. Поэтому мы разрабатываем метод, основанный на биохимическом определении зомана с использованием доступного фотометрического оборудования.
Описан способ извлечения зомана из почвы путем жидкостной экстракции (Харечко А. Т. и др. Оценка влияния микроорганизмов на динамику разложения зомана в почве // ЖРХО им. Менделеева. - 1995 - Т.39. - 4. - С.104-107). В данной работе проводились исследования по оценке динамики убыли содержания зомана в почве. Экстракцию проводили изопропанолом. Степень извлечения в диапазоне концентраций от 200 до 10 мг•кг-1 составила 89%. Сведения об эффективности извлечения зомана этим методом при заражении почвы менее 1 мг•кг-1 в данной работе отсутствуют. Поэтому этот метод нельзя отнести к методу определения микроколичеств зомана в почве.
Задачей настоящего изобретения являлось снижение предела определяемых концентраций зомана в почве биохимическим методом до микроколичеств (n•10-2 мг•кг-1) при сохранении коэффициента экстракции не ниже 80%.
Основной причиной низкого коэффициента экстракции, по нашему мнению, является то, что зоман как при внесении в почву, так и при его извлечении подвержен быстропротекающим процессам деструкции. Поэтому перед внесением зомана в почву для создания модельных заражений почву необходимо стабилизировать. Литературные сведения о способе стабилизации проб почвы, зараженных зоманом, отсутствуют.
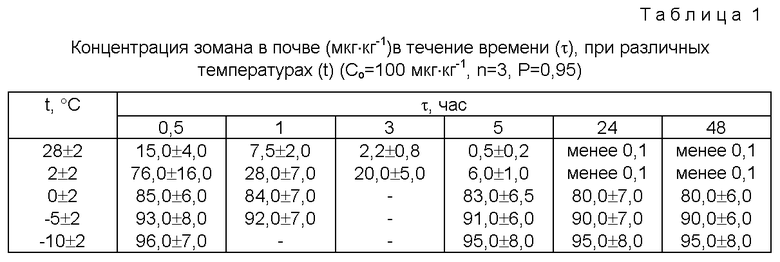
Известно, что снижение температуры уменьшает скорость химических процессов, в том числе и процессов деструкции. Поэтому была исследована возможность стабилизации проб почвы, зараженных зоманом, посредством их охлаждения. Экспериментальные результаты представлены в табл.1.
Как видно из результатов, представленных в табл. 1, снижение температуры действительно замедляет процессы деструкции зомана. Поэтому для создания модельных заражений почву охлаждали до температуры -5...0oС и вносили стартовый раствор зомана. Экстракцию проводили через 20 мин после заражения. При промораживании почвы процессы деструкции практически прекращаются, и в таком виде пробы можно хранить длительное время.
Нестойкость зомана не позволяет проводить его длительную экстракцию, поэтому экстракцию проводили при ультразвуковом воздействии. Необходимо было провести оптимизацию времени ультразвуковой экстракции, так как при длительной экстракции возможны потери вещества в результате химической деструкции, а при короткой - неполный выход вещества.
В соответствии с вышеприведенными условиями стабилизации и извлечения было проведено определение оптимального времени ультразвукового воздействия. Исследовали зависимость коэффициента экстракции от времени. Экспериментальные результаты представлены в табл.2.
Оптимальное время экстракции составило 8-12 мин.
Для достижения максимальной чувствительности методики разбавления экстрактов должны быть минимальными, но в этом случае присутствующие остатки органических растворителей и коэкстрактивных веществ в растворах могут мешать биохимическому определению зомана, поэтому необходимо было изучить влияние этих веществ для выбора оптимальных условий анализа.
В ходе исследований оценивали ингибирующее действие растворителя и коэкстрактивных веществ на фермент. Известно, что для проведения биохимических анализов содержание спиртов в растворах проб не должно превышать 5-10%, а ацетона - 2%.
Экспериментально установлено, что для достижения приемлемой величины неспецифического угнетения холинэстераз необходимо разбавление не менее чем в 20-50 раз в зависимости от растворителя.
Была проведена экспериментальная оценка влияния веществ, присутствующих в метанольном или этанольном экстракте почвы на биохимическое определение зомана. Установлено, что калибровочные зависимости концентрации зомана от степени угнетения бутирилхолинэстеразы (БХЭ) в почвенных вытяжках и водных растворах характеризуются значительными отличиями, кроме того, калибровочные зависимости концентрации зомана в почвенных вытяжках характеризуются большими различиями в разных опытах, что, видимо, обусловлено непостоянным составом коэкстрактивных веществ.
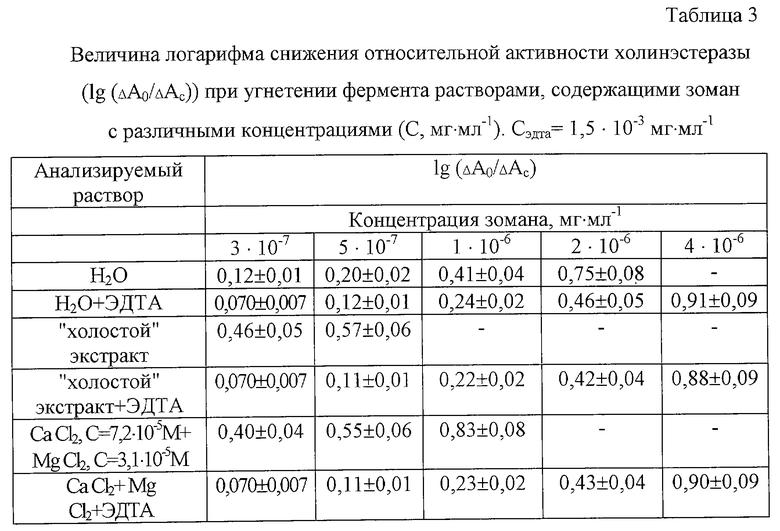
Установлено, что эффекты изменения сродства холинэстеразы к зоману вызывают соли кальция, магния и железа. Были исследованы возможности устранения искажающего влияния солей на ход биохимического определения с помощью комплексона динатриевой соли -N,N,N',N' этилендиаминтетрауксусной кислоты (ЭДТА). Результаты представлены в табл.3.
Анализ результатов, представленных в табл.3, показывает, что добавление ЭДТА полностью устраняет мешающее влияние солей кальция и магния на биохимическое определение зомана.
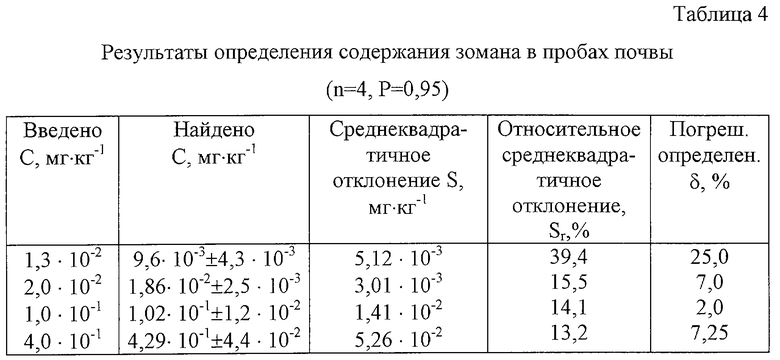
Правильность количественного определения зомана в пробах почвы разработанной методикой определяли методом введено-найдено. Расчет найденного количества зомана проводили с учетом установленного коэффициента экстракции. Результаты представлены в табл.4.
Результаты, представленные в табл.4, показывают, что погрешность определения содержания зомана при концентрациях ниже 2,0•10-2 мг•кг-1 сильно возрастает. При этом возрастает также и относительное среднеквадратичное отклонение. Поэтому предел определяемых концентраций зомана в почве биохимическим методом с использованием БХЭ составляет 2,0•10-2 мг•кг-1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ МИКРОКОЛИЧЕСТВ ИЗОПРОПИЛОВОГО ЭФИРА ФТОРАНГИДРИДА МЕТИЛФОСФОНОВОЙ КИСЛОТЫ В ПОЧВЕ | 2001 |
|
RU2213349C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА КИСЛЫХ МОНОЭФИРОВ МЕТИЛФОСФОНОВОЙ КИСЛОТЫ | 2006 |
|
RU2308030C1 |
| СПОСОБ РАЗДЕЛЬНОГО ОПРЕДЕЛЕНИЯ α-, β-ЛЮИЗИТА, ИХ ОКСИДОВ И ХЛОРВИНИЛАРСОНОВЫХ КИСЛОТ ПРИ СОВМЕСТНОМ ПРИСУТСТВИИ В ПОЧВЕ | 2000 |
|
RU2201780C2 |
| ПРИМЕНЕНИЕ N,N-ДИЭТИЛАНИЛИНА В КАЧЕСТВЕ ИМИТАТОРА ЗОМАНА В ВОДНОЙ СРЕДЕ | 2009 |
|
RU2404160C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА МЕТИЛФОСФОНОВОЙ КИСЛОТЫ ТИТРИМЕТРИЧЕСКИМ МЕТОДОМ | 2007 |
|
RU2365914C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА ДИАЛКИЛОВЫХ ЭФИРОВ АЛКИЛФОСФОНОВЫХ КИСЛОТ | 2006 |
|
RU2320989C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА О-АЛКИЛМЕТИЛФОСФОНАТОВ | 2008 |
|
RU2354661C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ О-АЛКИЛОВЫХ ЭФИРОВ МЕТИЛФОСФОНОВОЙ КИСЛОТЫ В ВОДНЫХ МАТРИЦАХ МЕТОДОМ РЕАКЦИОННОЙ ГАЗОВОЙ ХРОМАТОГРАФИИ С АТОМНО-ЭМИССИОННЫМ ДЕТЕКТИРОВАНИЕМ | 2001 |
|
RU2213959C2 |
| СПОСОБ ЭКСТРАКЦИИ МИКРОКОЛИЧЕСТВ β,β′-ДИХЛОРДИЭТИЛСУЛЬФИДА ИЗ ВОДНЫХ ПРОБ | 1998 |
|
RU2157272C2 |
| СОСТАВ ЭКСТРАГЕНТА ДЛЯ ИЗВЛЕЧЕНИЯ β-ХЛОРВИНИЛАРСИНОКСИДА ИЗ ПРОБ ПОЧВЫ | 1996 |
|
RU2129454C1 |

Изобретение относится к области аналитической химии, а именно исследованию способов извлечения, приемов стабилизации проб почвы, зараженных микроколичествами пинаколинового эфира фторангидрида метилфосфоновой кислоты, и последующего биохимического анализа. При проведении анализа для извлечения микроколичеств пинаколинового эфира фторангидрида метилфосфоновой кислоты необходима предварительная стабилизация проб почвы посредством их охлаждения до 0-5oС. Для достижения наибольшего извлечения данного вещества необходимо применение ультразвукового воздействия, время проведения которого составляет 8-12 мин. Для устранения мешающего воздействия солей металлов на биохимическое определение пинаколинового эфира фторангидрида метилфосфоновой кислоты в почвенных экстрактах необходимо применение диаммонийной или динатриевой соли N, N,N',N' - этилендиаминтетрауксусной кислоты. Достигается повышение чувствительности анализа. 1 з.п.ф-лы, 4 табл.
| Trace analysis of chemical warfare agents | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| The ministri for foreign affairs of Finland | |||
| - Helsinki, 1981, p.121 | |||
| ИЗМЕРИТЕЛЬ СОДЕРЖАНИЯ ПЫЛИ В СЫПУЧИХ МАТЕРИАЛАХ | 1994 |
|
RU2084866C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ В ПОЧВЕ ПОДВИЖНОГО ФОСФОРА, СПОСОБ ДИАГНОСТИКИ И РЕГУЛИРОВАНИЯ ФОСФОРНОГО ПИТАНИЯ РАСТЕНИЙ И СПОСОБ ОЦЕНКИ СИСТЕМЫ УДОБРЕНИЯ ФОСФОРОМ | 1997 |
|
RU2133465C1 |
| SU 214875 А, 27.06.1968 | |||
| SU 1785572 А3, 30.12.1992 | |||
| US 4842746 А, 27.06.1989 | |||
| ХАРЕЧКО А.Т | |||
| и др | |||
| ЖРХО им | |||
| Менделеева, 1995, т.39, №4, с.104-107. | |||
Авторы
Даты
2003-10-20—Публикация
2001-01-15—Подача