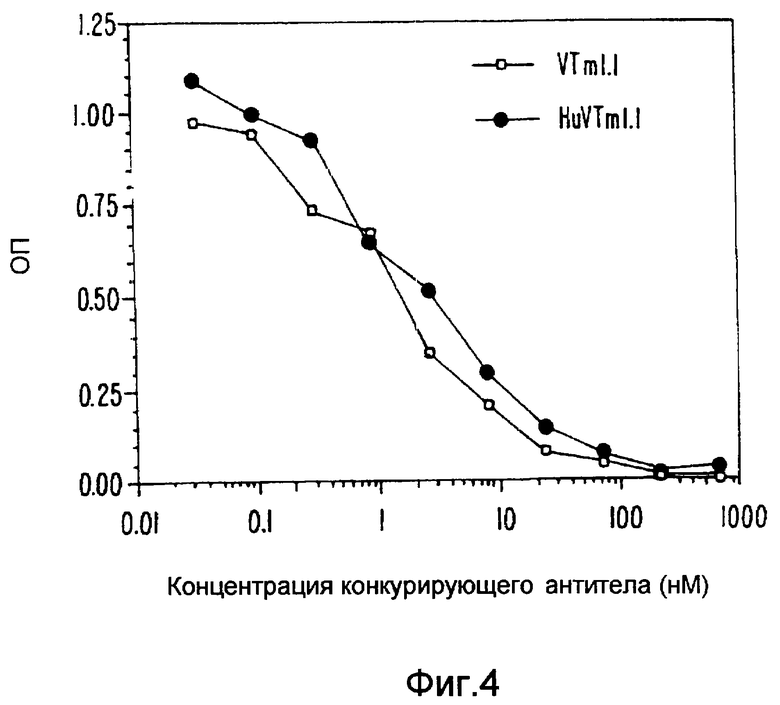
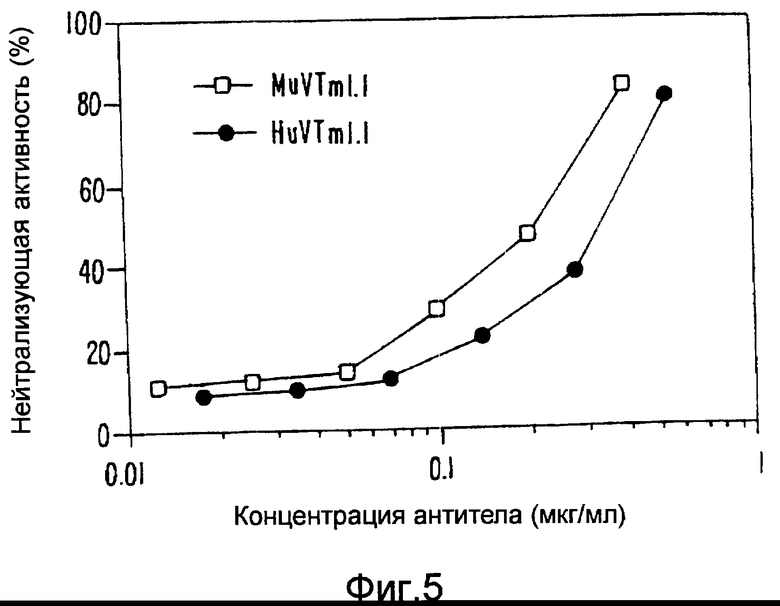
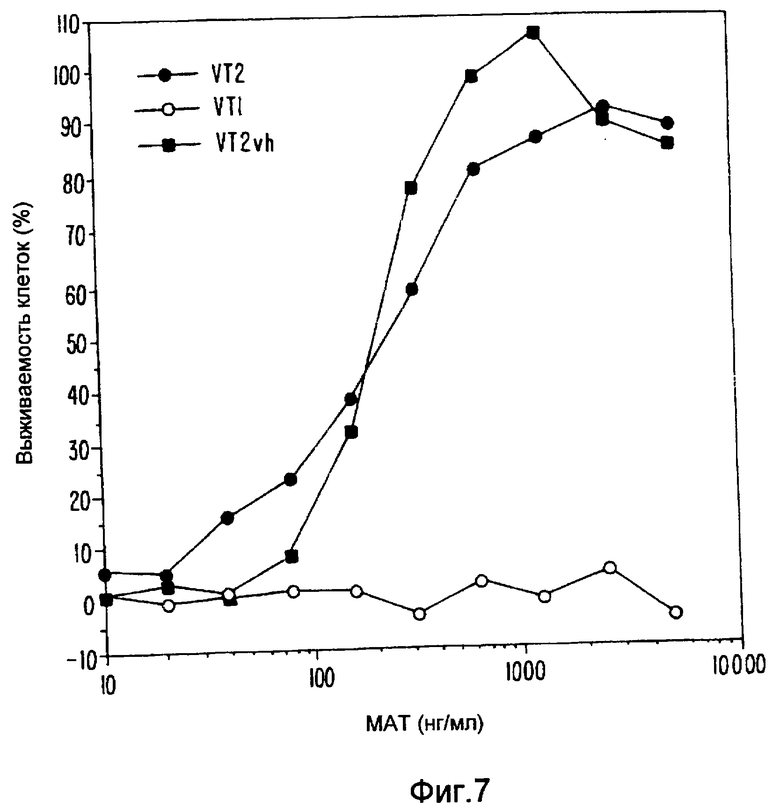
Изобретение относится к медицине и касается гуманизированных антител, которые распознают веротоксин II, и продуцирующей их линии клеток. Сущность изобретения заключается в создании гуманизированного антитела, представляющего собой гуманизированную форму антитела VTm.1 мыши, которое характеризуется вариабельной областью легкой цепи и вариабельной областью тяжелой цепи и которое специфически связывает и нейтрализует VT2 или его вариант, а также касается фармацевтических композиций и способов лечения с применением указанных антител. Преимущество изобретения заключается в получении антител, не иммуногенных для человека, но обладающих свойствами антитела мыши, которые могут быть получены способами, пригодными для терапевтического использования. 5 с. и 20 з.п.ф-лы, 6 табл., 7 ил.
1. Гуманизированное антитело, представляющее собой гуманизированную форму антитела VTm1-1 мыши, причем указанное антитело мыши характеризуется вариабельной областью легкой цепи, представленной на фиг.1В, и вариабельной областью тяжелой цепи, представленной на фиг.1А, где указанное гуманизированное антитело специфически связывает и нейтрализует VT2 и/или вариант VT2.2. Гуманизированное антитело по п.1, которое конкурирует с антителом VTm1-1 мыши за специфическое связывание с VT2 и/или вариантом VT2.3. Гуманизированное антитело по п.1, которое специфически связывает субъединицу В VT2 и/или субъединицу В варианта VT2.4. Гуманизированное антитело по п.1 или 2, включающее области, определяющие комплементарность, от антитела VTm1-1 мыши, а каркасы вариабельных областей тяжелой и легкой цепей от каркасов тяжелой и легкой цепей антитела GF4 человека, при условии, что, по меньшей мере, одно положение, выбранное из группы, состоящей из L49, Н29, Н30, Н49 и Н98, занято аминокислотой, присутствующей в соответствующем положении каркаса вариабельной области тяжелой или легкой цепи антитела VTm1-1 мыши, причем указанное гуманизированное антитело специфически связывает веротоксин II с константой сродства между 107 М-1 и в десять раз большим сродством, чем таковое антитела VTm1-1 мыши.5. Гуманизированное антитело по п.4, где каждое положение, выбранное из группы, состоящей из L49, Н29, H30, Н49 и Н98, занято аминокислотой, присутствующей в соответствующем положении каркаса вариабельной области тяжелой или легкой цепи антитела VTm1-1 мыши.6. Гуманизированное антитело по п.5, где, по меньшей мере, одно положение, выбранное из группы L3, L4, L19, L76, L79, L85, H1, Н4, Н5, Н79, Н89 и Н93, занято аминокислотой, присутствующей в соответствующем положении консенсусной последовательности тяжелой или легкой цепи антитела человека.7. Гуманизированное антитело по п.6, где каждое положение, выбранное из группы L3, L4, L19, L76, L79, L85, H1, Н4, Н5, Н79, Н89 и Н93, занято аминокислотой, присутствующей в соответствующем положении консенсусной последовательности тяжелой или легкой цепи антитела человека.8. Гуманизированное антитело по п.1 или 2, содержащее вариабельную область тяжелой цепи, представленную на фиг.2А, и вариабельную область легкой цепи, представленную на фиг.2В, при условии, что одно или несколько положений, выбранных из группы, состоящей из L49, Н29, Н30, Н49, Н98, L3, L4, L19, L76, L79, L85, H1, Н4, Н5, Н79, Н89 и Н93, может быть заменено, как показано в таблицах 2 и 3.9. Гуманизированное антитело по п.1 или 2, содержащее вариабельную область тяжелой цепи, представленную на фиг.2А, и вариабельную область легкой цепи, представленную на фиг.2В.10. Гуманизированное антитело по п.1 или 2, содержащее гуманизированную тяжелую цепь, имеющую последовательность, по меньшей мере, на 85% идентичную гуманизированной тяжелой цепи, представленной на фиг.2А, и гуманизированную легкую цепь, имеющую последовательность, по меньшей мере, на 85% идентичную гуманизированной легкой цепи, представленной на фиг.2В, при условии, что, по меньшей мере, одно положение, выбранное из группы, состоящей из L49, Н29, Н30, Н49 и Н98, занято аминокислотой, присутствующей в соответствующем положении каркаса вариабельной области тяжелой или легкой цепи антитела мыши VTm1-1.11. Гуманизированное антитело по п.1 или 2, где антитело содержит две пары димеров легких/тяжелых цепей, где каждая цепь содержит вариабельную область и константную область.12. Гуманизированное антитело по п.1 или 2, которое представляет собой Fab-фрагмент или F(ab')2.13. Гуманизированное антитело по п.1 или 2 в очищенной форме.14. Гуманизированное антитело по п.1 или 2, которое имеет иммуноглобулиновый изотип IgG1.15. Способ получения гуманизированного антитела VTm1-1, предусматривающий культивирование клеточной линии, которая кодирует тяжелую и легкую цепи гуманизированного антитела, охарактеризованного в любом из пп.1-14, в результате чего экспрессируется гуманизированное антитело, и выделение гуманизированного антитела, экспрессируемого указанной клеточной линией.16. Способ по п.15, дополнительно предусматривающий смешивание антитела с фармацевтически приемлемым носителем для получения фармацевтической композиции.17. Фармацевтическая композиция для лечения инфекции, вызванной Е.соli, продуцирующей веротоксин, и гемолитико-уремического синдрома, содержащая гуманизированное антитело, охарактеризованное в любом из пп.1-14, и фармацевтически приемлемый носитель.18. Фармацевтическая композиция по п.17, содержащая гуманизированное антитело, содержащее вариабельную область тяжелой цепи, представленную на фиг.2А, и вариабельную область легкой цепи, представленную на фиг.2В.19. Способ лечения пациента, подвергающегося риску или страдающего от токсических эффектов веротоксина, включающий введение пациенту эффективной дозы гуманизированного антитела, представляющего собой гуманизированную форму антитела VTm1-1 мыши, причем указанное антитело мыши характеризуется вариабельной областью легкой цепи, представленной на фиг.1В, и вариабельной областью тяжелой цепи, представленной на фиг.1А, где указанное гуманизированное антитело специфически связывает и нейтрализует субъединицу В VT2 и/или субъединицу В варианта VT2.20. Способ по п.19, в котором антитело конкурирует с антителом VTm1-1 мыши за специфическое связывание с веротоксином II или вариантом веротоксина II.21. Способ по п.19, в котором антитело представляет собой гуманизированное антитело, содержащее вариабельную область тяжелой цепи, представленную на фиг.2А, и вариабельную область легкой цепи, представленную на фиг.2В.22. Способ по п.19, в котором указанный пациент инфицирован Е.coli, продуцирующей веротоксин, и антитело вводят терапевтически.23. Способ по п.22, дополнительно предусматривающий мониторинг состояния пациента на предмет восстановления от токсических эффектов веротоксина II или варианта веротоксина II.24. Способ по п.19, в котором указанный пациент подвержен риску инфекции Е.coli, продуцирующей веротоксин, и антитело вводят профилактически.25. Клеточная линия миеломы мыши, продуцирующая антитело, охарактеризованное в любом из пп.1-14.