ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0001] Настоящее изобретение в целом относится к новым анти-CLDN18.2 антителам, которые специфически связываются с CLDN18.2 человека.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Молекула клаудина-18 (CLDN18) (инвентарный номер Genbank: сплайс-вариант 1 (CLDN18A1 или CLDN18.1): NP_057453, NM_016369 и сплайс-вариант 2 (CLDN18A2 или CLDN18.2): NM_001002026, NP_001002026) представляет собой соединение трансмембранный белок с молекулярной массой примерно 27,9/27,72 кДа. Белки CLDN18 расположены в пределах плотных контактов эпителия и эндотелия, которые организуют сеть взаимосвязанных нитей внутримембранных частиц между соседними клетками. CLDN18 и окклюдин являются наиболее известными трансмембранными белковыми компонентами в плотных соединениях. Из-за своих сильных свойств межклеточной адгезии эти белки плотных контактов создают первичный барьер для предотвращения и контроля парацеллюлярного транспорта растворенных веществ, а также ограничивают латеральную диффузию мембранных липидов и белков для поддержания клеточной полярности. Следовательно, они критически вовлечены в организацию архитектуры эпителиальной ткани.
[0003] CLDN18 является членом семейства тетраспанинов и имеет 4 гидрофобных участка. CLDN18 имеет несколько различных конформаций, которые могут избирательно воздействовать на антитела (см. Sahin U, Koslowski M, Dhaene K, et al. Claudin-18 splice variant 2 is a pan-cancer target suitable for therapeutic antibody development[J]. Clinical Cancer Research, 2008, 14(23): 7624-7634). CLDN18-конформация-1 имеет все четыре гидрофобных участка, служащих трансмембранными доменами (ТМ), и формируются две внеклеточные петли (петля 1, охваченная гидрофобным участком 1 и гидрофобным участком 2; петля 2, охваченная гидрофобным участком 3 и 4), как описано для подавляющее большинство членов семьи CLDN. Вторая конформация (CLDN18-конформация-2) подразумевает, что, как описано для PMP22, второй и третий гидрофобные домены не полностью пересекают плазматическую мембрану, так что часть (петля D3) между первым и четвертым трансмембранными доменами является внеклеточной. Третья конформация (CLDN18-конформация-3) демонстрирует большой внеклеточный домен с двумя внутренними гидрофобными областями, окруженными первой и четвертой гидрофобными областями. Из-за классического сайта N-гликозилирования в петле D3 варианты топологии CLDN-18 CLDN18 топология-2 и CLDN18 топология-3 содержат дополнительный внеклеточный сайт N-гликозилирования.
[0004] CLDN18 имеет два различных варианта сплайсинга, которые присутствуют как у мыши, так и у человека. Варианты сплайсинга CLDN18.1 и CLDN18.2 различаются по первой 21 аминокислоте на N-конце, который включает первый TM и петлю 1, тогда как белковые последовательности на C-конце идентичны (см. Niimi T, Nagashima K, Ward J M, et al. Claudin-18, a novel downstream target gene for the T/EBP/NKX2. 1 homeodomain transcription factor, encodes lung-and stomach-specific isoforms through alternative splicing[J]. Molecular and cellular biology, 2001, 21(21): 7380-7390).
[0005] CLDN18.1 избирательно экспрессируется на нормальных эпителиях легких и желудка, тогда как CLDN18.2 экспрессируется только на клетках желудка. Что наиболее важно, экспрессия CLDN18.2 ограничена дифференцированными короткоживущими клетками эпителия желудка, но лишена области стволовых клеток желудка. При использовании чувствительной RT-PCR оба варианта не обнаруживаются ни в одном другом нормальном органе человека. Однако они сильно экспрессируются при некоторых типах рака, включая опухоли желудка, пищевода, поджелудочной железы и легких, а также в линиях раковых клеток человека (см. Matsuda Y, Semba S, Ueda J, et al. Gastric and intestinal claudin expression at the invasive front of gastric carcinoma[J]. Cancer science, 2007, 98(7): 1014-1019).
[0006] Существует значительная потребность в новых анти-CLDN18.2 антителах, которые можно использовать для лечения заболеваний, позитивных по экспрессии CLDN18.2, таких как злокачественные новообразования.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0007] Во всем настоящем описании указание в единственном числе используется в настоящем документе для обозначения одного или более чем одного (то есть по меньшей мере одного) грамматического объекта. Например, «антитело» означает одно антитело или более одного антитела.
[0008] В настоящем изобретении предложены, среди прочего, новые моноклональное анти-CLDN18.2 антитела, кодирующие их нуклеотидные последовательности и их применение.
[0009] В одном аспекте в настоящем изобретении предложено выделенное антитело против CLDN18.2 человека или его антигенсвязывающий фрагмент, способным связываться с эпитопом, содержащим по меньшей мере один, два или три аминокислотных остатка в положениях D28, W30, V43, N45, Y46, L49, W50, R51, R55, E56, F60, E62, Y66, L72, L76, V79 и R80 в аминокислотной последовательности SEQ ID NO: 30.
[0010] В некоторых вариантах осуществления изобретения эпитоп содержит аминокислотный остаток в положении E56. В некоторых вариантах осуществления изобретения эпитоп не содержит по меньшей мере один из следующих остатков: A42 или N45. В некоторых вариантах осуществления изобретения эпитоп содержит аминокислотный остаток в положении W30, L49, W50, R55 и E56. В некоторых вариантах осуществления изобретения эпитоп дополнительно содержит один или несколько аминокислотных остатков: T41, N45, Y46, R51, F60, E62, и R80. В некоторых вариантах осуществления изобретения эпитоп дополнительно содержит один или несколько аминокислотных остатков: D28, V43, N45, Y46, Y66, L72, L76 и V79.
[0011] В одном аспекте в настоящем изобретении предложено выделенное антитело или его антигенсвязывающий фрагмент, которые способны специфически связываться с CLDN18.2 человека и обладают по меньшей мере одной из следующих характеристик:
a) связывание с клеткой, экспрессирующей CLDN18.2 человека со значением Kd не более чем 2,5 нМ (или не более чем 2,4, 2,3, 2,2, 2,1, 2,0, 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4 нМ), как определено анализом KinExA;
b) связывание с клеткой, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 70 мкг/мл (или не более чем 65, 60, 55, 50, 45, 40, 35, 30, 25, 20, 15, 12, или 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 мкг/мл), как определено анализом проточной цитометрии;
c) индуцирование комплемент-зависимой цитотоксичности (CDC) на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 1 мкг/мл (или не более чем 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2, 0,1, 0,05, или 0,01 мкг/мл), как определено анализом цитотоксичности;
d) индуцирование антителозависимой цитотоксичности (ADCC) на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 2 мкг/мл (или не более чем 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2, или 0,1 мкг/мл) как определено анализом с использованием репортерного гена ADCC.
[0012] В некоторых вариантах осуществления изобретения клетка содержит клетку NUGC4, клетку SNU-620, клетку SNU-601, клетку KATOIII или сравнимую с ними клетку, имеющую уровень экспрессии человеческого белка CLDN18.2, сравнимый или не превышающий таковой у клетки NUGC4, клетки SNU-620, клетки SNU-601 или клетки KATOIII.
[0013] В некоторых вариантах осуществления изобретения клетка содержит клетку CLDN18.2 человека с высокой степенью экспрессии, клетку CLDN18.2 человека со средней степенью экспрессии или клетку CLDN18.2 человека с низкой степенью экспрессии.
[0014] В некоторых вариантах осуществления изобретения клетка CLDN18.2 человека с высокой степенью экспрессии экспрессирует CLDN18.2 человека с интенсивностью по меньшей мере 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 40% (например, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, 40-100%, 50-100%, 60-100%, 70-100%, 80-100%, 90-100%, 40-90%, 50-90%, 60-90%, 70-90%, 80-90%, 40-80%, 40-70%, 40-60%, 40-50%, 50-80%, 50-70%, 50-60%, 60-80%, 60-70%, или 70-80%) клеток окрашиваются положительно при иммуногистохимическом исследовании (IHC); клетка CLDN18.2 человека со средней степенью экспрессии экспрессирует CLDN18.2 человека с интенсивностью по меньшей мере 1+ и ниже 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 30% (или по меньшей мере 35%), но ниже 40% клеток окрашиваются положительно при IHC; и клетка CLDN18.2 человека с низкой степенью экспрессии экспрессирует CLDN18.2 человека с интенсивностью около 0, но ниже 1+, как определено с помощью IHC, и на уровне, где около 0, но ниже 30% (например, 5%, 10%, 15%, 20%, 25%, 5-25%, 10-25%, 15-25%, 20-25%, 5-20%, 5-15%, 5-10%, 10-20% или 10-15%) клеток окрашиваются положительно при IHC.
[0015] В некоторых вариантах осуществления изобретения значение EC50 для связывания с клетками NUGC4 составляет не более чем 70 мкг/мл (или не более чем 65, 60, 55, 50, 45, 40, 35, 30, 25, 20, 15, 12 или 10 мкг/мл).
[0016] В некоторых вариантах осуществления изобретения ADCC на клетках NUGC4 при значении EC50 не более чем 2 мкг/мл (или не более чем 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2 или 0,1 мкг/мл), как определено анализом с использованием репортерного гена ADCC.
[0017] В одном аспекте в настоящем изобретении предложено выделенное антитело или его антигенсвязывающий фрагмент, которые способны специфически связываться с CLDN18.2 человека и обладают по меньшей мере одной из следующих характеристик:
a) связывание с CLDN18.2 человека со значением Kd не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15% от такового для IMAB362, как определено анализом KinExA;
b) связывание с клеткой, экспрессирующей CLDN18.2 человека или мыши при значении EC50 не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15% или 10% от такового для IMAB362, как определено анализом проточной цитометрии;
c) индуцирование комплемент-зависимой цитотоксичности (CDC) на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10% или 5% от такового для IMAB362, как определено анализом цитотоксичности; и
d) индуцирование антителозависимой цитотоксичности (ADCC) на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, 5% или 1% от такового для IMAB362, как определено анализом с использованием репортерного гена ADCC,
где IMAB362 представляет собой антитело, содержащее вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 72, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 73.
[0018] В некоторых вариантах осуществления изобретения клетка содержит клетку NUGC4, клетку SNU-620, клетку SNU-601, клетку KATOIII или клеточную линию, имеющую уровень экспрессии человеческого белка CLDN18.2, сравнимый или не превышающий уровень экспрессии клетки NUGC4, клетки SNU-620, клетки SNU-601 или клетки KATOIII.II. В некоторых вариантах осуществления изобретения клетка содержит клетку CLDN18.2 человека с высокой степенью экспрессии, клетку CLDN18.2 человека со средней степенью экспрессии, или клетку CLDN18.2 человека с низкой степенью экспрессии.
[0019] В некоторых вариантах осуществления изобретения клетка CLDN18.2 человека с высокой степенью экспрессии экспрессирует CLDN18.2 человека с интенсивностью по меньшей мере 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 40% (например, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, 40-100%, 50-100%, 60-100%, 70-100%, 80-100%, 90-100%, 40-90%, 50-90%, 60-90%, 70-90%, 80-90%, 40-80%, 40-70%, 40-60%, 40-50%, 50-80%, 50-70%, 50-60%, 60-80%, 60-70% или 70-80%) клеток окрашиваются положительно при IHC; клетка CLDN18.2 человека со средней степенью экспрессии экспрессирует CLDN18.2 человека с интенсивностью по меньшей мере 1+ и ниже 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 30% (или по меньшей мере 35%), но ниже 40% клеток окрашиваются положительно при IHC; и клетка CLDN18.2 человека с низкой степенью экспрессии экспрессирует CLDN18.2 человека с интенсивностью около 0, но ниже 1+, как определено с помощью IHC, и на уровне, где около 0, но ниже 30% (например, 5%, 10%, 15%, 20%, 25%, 5-25%, 10-25%, 15-25%, 20-25%, 5-20%, 5-15%, 5-10%, 10-20%, или 10-15%) клеток окрашиваются положительно при IHC.
[0020] В некоторых вариантах осуществления изобретения выделенные антитела или их антигенсвязывающие фрагменты способны связываться с эпитопом, содержащим по меньшей мере один, два или три аминокислотных остатка в положениях D28, W30, V43, N45, Y46, L49, W50, R51, R55, E56, F60, E62, Y66, L72, L76, V79 и R80 в аминокислотной последовательности SEQ ID NO: 30. В некоторых вариантах осуществления изобретения эпитоп содержит аминокислотный остаток в положении E56. В некоторых вариантах осуществления изобретения эпитоп не содержит по меньшей мере один из следующих остатков: A42 или N45. В некоторых вариантах осуществления изобретения эпитоп содержит аминокислотный остаток в положении W30, L49, W50, R55 и E56. В некоторых вариантах осуществления изобретения эпитоп дополнительно содержит один или несколько аминокислотных остатков: T41, N45, Y46, R51, F60, E62 и R80. В некоторых вариантах осуществления изобретения эпитоп дополнительно содержит один или несколько аминокислотных остатков: D28, V43, N45, Y46, Y66, L72, L76 и V79.
[0021] В одном аспекте в настоящем изобретении предложено анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, содержащие последовательности тяжелых цепей HCDR1, HCDR2 и HCDR3 и/или легких цепей LCDR1, LCDR2 и LCDR3, где
последовательность HCDR1 содержит GYNMN (SEQ ID NO: 1), или TYFIGVG (SEQ ID NO: 13), или гомологическую последовательность с по меньшей мере 80% идентичностью ее последовательностей;
последовательность HCDR2 содержит X1IDPYYX2X3TX4YNQKFX5G (SEQ ID NO: 32), или HIWWNDNKYYNTALKS (SEQ ID NO: 15), или гомологическую последовательность с по меньшей мере 80% (или по меньшей мере 85%, 90%, 95%) идентичностью ее последовательностей;
последовательность HCDR3 содержит X6X7X8GNAFDY (SEQ ID NO: 33), или MGSGAWFTY (SEQ ID NO: 17), или гомологическую последовательность с по меньшей мере 80% идентичностью ее последовательностей;
последовательность LCDR1 содержит KSSQX9LX10NX11GNX12KNYLT (SEQ ID NO: 34) или гомологическую последовательность с по меньшей мере 80% (или по меньшей мере 85%, 90%, 95%) идентичностью ее последовательностей;
последовательность LCDR2 содержит WASTRX13S (SEQ ID NO: 35) или гомологическую последовательность с по меньшей мере 80% идентичностью ее последовательностей;
последовательность LCDR3 содержит QNDYX14X15PX16T (SEQ ID NO: 36) или гомологическую последовательность с по меньшей мере 80% идентичностью ее последовательностей;
где X1 представляет собой N или Y или H, X2 представляет собой G или V, X3 представляет собой A или G или T, X4 представляет собой R или T или S, X5 представляет собой K или R, X6 представляет собой S или M, X7 представляет собой Y или F, X8 представляет собой Y или H, X9 представляет собой S или N, X10 представляет собой L или F, X11 представляет собой S или N, X12 представляет собой Q или L, X13 представляет собой E или K, X14 представляет собой S или Y, X15 представляет собой F или Y и X16 представляет собой F или L.
[0022] В одном аспекте в настоящем изобретении предложено анти-CLDN18.2 в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где вариабельная область тяжелой цепи содержит:
a) HCDR1 содержит последовательность, выбранную из SEQ ID NO: 1 и SEQ ID NO: 13,
b) HCDR2 содержит последовательность, выбранную из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 15, SEQ ID NO: 19 и SEQ ID NO: 22, и
c) HCDR3 содержит последовательность, выбранную из SEQ ID NO: 5, SEQ ID NO: 11, SEQ ID NO: 17 и SEQ ID NO: 21, и/или
вариабельная область легкой цепи содержит:
d) LCDR1 содержит последовательность SEQ ID NO: 2, SEQ ID NO: 10, SEQ ID NO: 14 и SEQ ID NO: 20,
e) LCDR2 содержит последовательность SEQ ID NO: 4 и SEQ ID NO: 16, и
f) LCDR3 содержит последовательность, выбранную из SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 12 и SEQ ID NO: 18.
[0023] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где вариабельная область тяжелой цепи выбрана из группы, включающей:
a) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 3, и HCDR3, содержащую последовательность SEQ ID NO: 5;
b) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 7, и HCDR3, содержащую последовательность SEQ ID NO: 5;
c) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 9, и HCDR3, содержащую последовательность SEQ ID NO: 11;
d) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 13, HCDR2, содержащую последовательность SEQ ID NO: 15, и HCDR3, содержащую последовательность SEQ ID NO: 17;
e) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 19, и HCDR3, содержащую последовательность SEQ ID NO: 21; и
f) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 22, и HCDR3, содержащую последовательность SEQ ID NO: 5.
[0024] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где вариабельная область легкой цепи выбрана из группы, включающей:
a) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
b) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 8;
c) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 10, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
d) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 12;
e) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 14, LCDR2, содержащую последовательность SEQ ID NO: 16, и LCDR3, содержащую последовательность SEQ ID NO: 18; и
f) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 20, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6.
[0025] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где:
a) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 3, и HCDR3, содержащую последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
b) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 7, и HCDR3, содержащую последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 8;
c) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 9, и HCDR3, содержащую последовательность SEQ ID NO: 11; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 10, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
d) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 13, HCDR2, содержащую последовательность SEQ ID NO: 15, и HCDR3, содержащую последовательность SEQ ID NO: 17; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 12;
e) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 19, и HCDR3, содержащую последовательность SEQ ID NO: 21; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 14, LCDR2, содержащую последовательность SEQ ID NO: 16, и LCDR3, содержащую последовательность SEQ ID NO: 18; или
f) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 22, и HCDR3, содержащую последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 20, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6.
[0026] В некоторых вариантах осуществления изобретения вариабельная область тяжелой цепи содержит последовательность, выбранную из группы, включающей SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 29, SEQ ID NO: 37, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 43, SEQ ID NO: 45 и SEQ ID NO: 47, и ее гомологичную последовательность с по меньшей мере 80%-ной (например, по меньшей мере 85%, 90%, 95%, 96%, 97%, 98%, или 99%) идентичностью последовательностей, сохраняя при этом аффинность специфического связывания с CLDN18.2.
[0027] В некоторых вариантах осуществления изобретения, где вариабельная область легкой цепи содержит последовательность, выбранную из группы, включающей SEQ ID NO: 26, SEQ ID NO: 28, SEQ ID NO: 38, SEQ ID NO: 40, SEQ ID NO: 42, SEQ ID NO: 44, SEQ ID NO: 46, SEQ ID NO: 48, и ее гомологичную последовательность с по меньшей мере 80%-ной (например, по меньшей мере 85%, 90%, 95%, 96%, 97%, 98%, или 99%) идентичностью последовательностей, сохраняя при этом аффинность специфического связывания с CLDN18.2.
[0028] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где:
a) вариабельная область тяжелой цепи, содержащая последовательность SEQ ID NO: 23 и вариабельная область легкой цепи, содержащая последовательность SEQ ID NO: 24;
b) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 25 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 26;
c) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 27 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 28;
d) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 29 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 26, или 28;
e) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 37 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 38;
f) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 39 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 40;
g) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 41 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 42;
h) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 43 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 44;
i) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 45 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 46; или
j) вариабельная область тяжелой цепи содержит последовательность SEQ ID NO: 47 и вариабельная область легкой цепи содержит последовательность SEQ ID NO: 48.
[0029] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, содержат, кроме того, одну или несколько тяжелых цепей HFR1, HFR2, HFR3 и HFR4, и/или одну или несколько легких цепей LFR1, LFR2, LFR3 и LFR4, где:
HFR1 содержит QVQLVQSGAEVKKPGASVKVSCKASGYX17FT (SEQ ID NO: 54) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей,
HFR2 содержит WVX18QAPGQGLEWX19G (SEQ ID NO: 55) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 90%) идентичностью последовательностей,
HFR3 содержит RVTX20TIDKSTSTVYMELSSLRSEDTAVYYCAR (SEQ ID NO: 56) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей,
HFR4 содержит WGQGTTVTVSS (SEQ ID NO: 57) или гомологическую последовательность с по меньшей мере 80%-ной идентичностью последовательностей,
LFR1 содержит DIVMTQSPDSLAVSLGERATX21NC (SEQ ID NO: 58) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей,
LFR2 содержит WYQQKPGQPPKLLIY (SEQ ID NO: 59) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%) идентичностью последовательностей,
LFR3 содержит GVPDRFX22GSGSGTDFTLTISSLQAEDVAVYYC (SEQ ID NO: 60) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей, и
LFR4 содержит FGGGTKVEIK (SEQ ID NO: 61) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 90%) идентичностью последовательностей,
где X17 представляет собой T или S, X18 представляет собой R или K, X19 представляет собой M или I, X20 представляет собой M или L, X21 представляет собой I или M, и X22 представляет собой S или T.
[0030] В некоторых вариантах осуществления изобретения
HFR1 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 62 и 63,
HFR2 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 64 и 65,
HFR3 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 66 и 67,
HFR4 содержит последовательность SEQ ID NO: 57,
LFR1 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 68 и 69,
LFR2 содержит последовательность SEQ ID NO: 59,
LFR3 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 70 и 71, и
LFR4 содержит последовательность SEQ ID NO: 61.
[0031] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, дополнительно содержат одну или несколько замен или модификаций аминокислотных остатков, сохраняют при этом аффинность специфического связывания с CLDN18.2. В некоторых вариантах осуществления изобретения по меньшей мере одна из замен или модификаций находится в одной или нескольких последовательностях CDR и/или в одной или нескольких не-CDR областях последовательностей VH или VL.
[0032] В некоторых вариантах осуществления изобретения антитело связывается с эпитопом, содержащим по меньшей мере один, два или три аминокислотных остатка в положениях D28, W30, V43, N45, Y46, L49, W50, R51, R55, E56, F60, E62, Y66, L72, L76, V79 и R80 CLDN18.2 человека, имеющим аминокислотную последовательность SEQ ID NO: 30.
[0033] В некоторых вариантах осуществления изобретения антитела или их антигенсвязывающие фрагменты содержат константную область иммуноглобулина, необязательно константную область Ig человека или необязательно константную область IgG человека. В некоторых вариантах осуществления изобретения константная область содержит константную область IgG1, IgG2, IgG3 или IgG4 человека. В некоторых вариантах осуществления изобретения константная область IgG1 человека содержит SEQ ID NO: 49, или гомологичную последовательность, содержащую по меньшей мере 80% (например, по меньшей мере 85%, 90%, 95%, 96%, 97%, 98% или 99%) идентичностью последовательностей.
[0034] В некоторых вариантах осуществления изобретения константная область содержит одну или несколько замен или модификаций аминокислотных остатков, придающих повышенную CDC или ADCC по сравнению с константной областью дикого типа. В некоторых вариантах осуществления изобретения константная область содержит одну или несколько замен аминокислотных остатков относительно SEQ ID NO: 49, выбранных из группы, включающую: L235V, F243L, R292P, Y300L, P396L или любую их комбинацию. В некоторых вариантах осуществления изобретения константная область содержит последовательность SEQ ID NO: 51.
[0035] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент являются афукозилированными.
[0036] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент является гуманизированным. В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент представляет собой верблюжье однодоменное антитело, диатело, scFv, димер scFv, BsFv, dsFv, (dsFv)2, фрагмент Fv, Fab, Fab', F(ab')2, ds-диатело, нанотело, доменное антитело или бивалентное доменное антитело.
[0037] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент является биспецифическим. В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент способно специфически связываться с первым эпитопом на CLDN18.2, и вторым эпитопом на CLDN18.2 или на втором антигене, отличном от CLDN18.2. В некоторых вариантах осуществления изобретения второй антиген представляет собой иммунную мишень, необязательно выбранную из группы, включающей: PD-L1, PD-L2, PD-1, CLTA-4, TIM-3, LAG3, CD160, 2B4, TGF β, VISTA, BTLA, TIGIT, LAIR1, OX40, CD2, CD27, ICAM-1, NKG2C, SLAMF7, NKp80, CD160, B7-H3, LFA-1, 1COS, 4-1BB, GITR, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, IL-2, IL-15, CD3, CD16 и CD83.
[0038] В некоторых вариантах осуществления изобретения второй антиген содержит опухолевый антиген. В некоторых вариантах осуществления изобретения опухолевый антиген присутствует в клетке, экспрессирующей CLDN18.2.
[0039] В вариантах осуществления изобретения опухолевый антиген содержит CA-125, ганглиозиды G(D2), G(M2) и G(D3), CD20, CD52, CD33, Ep-CAM, CEA, бомбезин-подобные пептиды, PSA, HER2/neu, рецептор эпидермального фактора роста (EGFR), erbB2, erbB3/HER3, erbB4, CD44v6, Ki-67, рако-ассоциированный муцин, VEGF, VEGFR (например, VEGFR3), рецепторы эстрогена, антиген Льюиса-Y TGFβ1, Рецептор IGF-1, EGFα, рецептор c-Kit, рецептор трансферрина, IL-2R или CO17-1A.
[0040] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент способны специфически связываться с CLDN18.2 мыши. В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент не связывается с CLDN18.1 человека.
[0041] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент связан с одним или несколькими фрагментами конъюгата. В некоторых вариантах осуществления изобретения фрагмент конъюгата содержит агент, модифицирующий клиренс, химиотерапевтический агент, токсин, радиоактивный изотоп, лантанид, люминесцентную метку, флуоресцентную метку, фермент-субстратную метку, алкилаторы ДНК, ингибитор топоизомеразы, средства, связывающие тубулин или другие противоопухолевые лекарственные средства.
[0042] В одном аспекте в настоящем изобретении предложено антитело или его антигенсвязывающий фрагмент, которое конкурирует за связывание с CLDN18.2 с антителом или его антигенсвязывающим фрагментом, предложенными в настоящем документе.
[0043] В одном аспекте в настоящем изобретении предложена фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, и один или несколько фармацевтически приемлемых носителей.
[0044] В одном аспекте в настоящем изобретении предложен выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе. В одном аспекте в настоящем изобретении предложен вектор, содержащий выделенный полинуклеотид, предложенный в настоящем документе. В одном аспекте в настоящем изобретении предложена клетка-хозяин, содержащая вектор, предложенный в настоящем документе.
[0045] В одном аспекте в настоящем изобретении предложены способы экспрессии антитела или его антигенсвязывающего фрагмента, предложенных в настоящем документе, включающие культивирование клетки-хозяина, предложенной в настоящем документе, в условиях, при которых экспрессируется вектор, предложенный в настоящем документе.
[0046] В одном аспекте в настоящем изобретении предложены способы лечения заболевания или состояния у субъекта, при которых было бы полезно модулировать активность CLDN18.2, включающие введение субъекту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента, предложенных в настоящем документе, и/или фармацевтической композиции, предложенной в настоящем документе. В некоторых вариантах осуществления изобретения заболевание или состояние представляет собой заболевание или состояние, связанное с CLDN18.2. В некоторых вариантах осуществления изобретения заболевание или состояние представляет собой рак, необязательно рак, экспрессирующий CLDN18.2. В некоторых вариантах осуществления изобретения у субъекта идентифицирована раковая клетка, экспрессирующая CLDN18.2. В некоторых вариантах осуществления изобретения субъект идентифицирован как имеющий раковую клетку с высоким уровнем экспрессии CLDN18.2, раковую клетку со средним уровнем экспрессии CLDN18.2 или раковую клетку с низким уровнем экспрессии CLDN18.2. В некоторых вариантах осуществления изобретения раковая клетка с высоким уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью по меньшей мере 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 40% (например, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, 40-100%, 50-100%, 60-100%, 70-100%, 80-100%, 90-100%, 40-90%, 50-90%, 60-90%, 70-90%, 80-90%, 40-80%, 40-70%, 40-60%, 40-50%, 50-80%, 50-70%, 50-60%, 60-80%, 60-70% или 70-80%) клеток окрашиваются положительно при IHC; раковая клетка со средним уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью по меньшей мере 1+ и ниже 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 30% (или по меньшей мере 35%), но ниже 40% клеток окрашиваются положительно при IHC, и раковая клетка с низким уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью около 0, но ниже 1+, как определено с помощью IHC, и на уровне, где около 0, но ниже 30% (например, 5%, 10%, 15%, 20%, 25%, 5-25%, 10-25%, 15-25%, 20-25%, 5-20%, 5-15%, 5-10%, 10-20%, или 10-15%) клеток окрашиваются положительно при IHC.
[0047] В некоторых вариантах осуществления изобретения способ включает, кроме того, введение терапевтически эффективного количества второго терапевтического агента. В некоторых вариантах осуществления изобретения заболевание или состояние представляет собой заболевание или состояние, связанное с CLDN18.2. В некоторых вариантах осуществления изобретения заболевание или состояние представляет собой рак, необязательно рак, экспрессирующий CLDN18.2.
[0048] В некоторых вариантах осуществления изобретения субъектом является человек.
[0049] В некоторых вариантах осуществления изобретения введение осуществляют перорально, назально, внутривенно, подкожно, сублингвально или внутримышечно.
[0050] В некоторых вариантах осуществления изобретения способы включают, кроме того, введение терапевтически эффективного количества второго терапевтического агента. В некоторых вариантах осуществления изобретения второй терапевтический агент выбран из химиотерапевтического агента, противоопухолевого лекарственного средства, лучевой терапии, иммунотерапевтического агента, антиангиогенного агента, таргетного терапевтического агента, клеточного терапевтического агента, генотерапевтического агента, гормонального терапевтического агента или цитокинов.
[0051] В одном аспекте в настоящем изобретении предложено набор, содержащий антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, и второй терапевтический агент.
[0052] В одном аспекте в настоящем изобретении предложены способы модулирования активности CLDN18.2 в клетках, экспрессирующих CLDN18.2, включающие воздействие на клетки, экспрессирующие CLDN18.2, антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе.
[0053] В одном аспекте в настоящем изобретении предложены способы обнаружения присутствия или количества CLDN18.2 в образце, включающие приведение образца в контакт с антителом или его антигенсвязывающим фрагментом, предложенными в настоящем документе, и определение присутствия или количества CLDN18. .2 в образце.
[0054] В одном аспекте в настоящем изобретении предложены способы диагностики заболевания или состояния, связанного с CLDN18.2, у субъекта, включающие: a) приведение в контакт образца, полученного от субъекта, с антителом или его антигенсвязывающим фрагментом, предложенными в настоящем документе; b) определение наличия или количества CLDN18.2 в образце; и c) сопоставление наличия или количества CLDN18.2 с наличием или статусом связанного с CLDN18.2 заболевания или состояния у субъекта.
[0055] В одном аспекте в настоящем изобретении предложено применение антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе, при изготовлении медицинского препарата для лечения у субъекта заболевания или состояния, связанного с CLDN18.2.
[0056] В одном аспекте в настоящем изобретении предложено применение антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе, при изготовлении диагностического реагента для диагностики заболевания или состояния, связанного с CLDN18.2.
[0057] В одном аспекте в настоящем изобретении предложено набор, содержащий антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, который можно использовать для обнаружения CLDN18.2.
[0058] В одном аспекте в настоящем изобретении предложено химерный антигенный рецептор (CAR), содержащий антигенсвязывающий домен, трансмембранный домен, костимуляторную сигнальную область и сигнальный домен TCR, где антигенсвязывающий домен специфически связывается с CLDN18.2 и содержит его антигенсвязывающий фрагмент, предложенный в настоящем документе.
[0059] В некоторых вариантах осуществления изобретения антигенсвязывающий фрагмент представляет собой Fab или scFv.
[0060] В некоторых вариантах осуществления изобретения CAR является биспецифическим. В некоторых вариантах осуществления изобретения CAR способен специфически связываться с первым эпитопом на CLDN18.2, и вторым эпитопом. В некоторых вариантах осуществления изобретения второй эпитоп находится на CLDN18.2. В некоторых вариантах осуществления изобретения второй эпитоп находится на а втором антигене, отличном от CLDN18.2. В некоторых вариантах осуществления изобретения второй антиген содержит опухолевый антиген.
[0061] В одном аспекте в настоящем изобретении предложена последовательность нуклеиновой кислоты, кодирующая химерный антигенный рецептор (CAR), предложенный в настоящем документе. В одном аспекте в настоящем изобретении предложена клетка, содержащая последовательность нуклеиновой кислоты, предложенную в настоящем документе. В одном аспекте в настоящем изобретении предложено клетка, генетически модифицированная для экспрессии CAR.
[0062] В одном аспекте в настоящем изобретении предложен вектор, содержащий последовательность нуклеиновой кислоты, предложенную в настоящем документе.
[0063] В одном аспекте в настоящем изобретении предложены способы стимуляции опосредованного Т-клетками иммунного ответа на клетки или ткани, экспрессирующие CLDN18.2, у млекопитающего, где способ включает введение млекопитающему эффективного количества клеток, генетически модифицированных для экспрессии CAR, предложенного в настоящем документе.
[0064] В одном аспекте в настоящем изобретении предложены способы лечения млекопитающего, страдающего заболеванием или состоянием, связанным с CLDN18.2, включающие введение млекопитающему эффективного количества клеток, предложенных в настоящем документе, и тем самым лечение млекопитающего.
[0065] В некоторых вариантах осуществления изобретения клетка представляет собой аутологичную Т-клетку. В некоторых вариантах осуществления изобретения заболевание или состояние, связанное с CLDN18.2, представляет собой рак. В некоторых вариантах осуществления изобретения млекопитающим является человек. В некоторых вариантах осуществления изобретения млекопитающее идентифицировано как имеющее раковую клетку, экспрессирующую CLDN18.2, необязательно, млекопитающее идентифицировано как имеющее раковую клетку с высоким уровнем экспрессии CLDN18.2, раковую клетку со средним уровнем экспрессии CLDN18.2, или раковую клетку с низким уровнем экспрессии CLDN18.2.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0066] Фигура 1A представляет собой график рассеяния, показывающий аффинности связывания 7C12, 11F12, 12E9 и 26G6 с клетками HEK293-CLDN18.2, которые экспрессируют CLDN18.2 человека. Фигура 1B представляет собой график рассеяния, показывающий аффинности связывания 59A9, 18B10, 7C12, 12C12 и 11F12 с клетками HEK293-CLDN18.2. Фигура 1C представляет собой график рассеяния, показывающий аффинности связывания 7C12, 11F12, 12E9 и 26G6 с клетками NUGC4. Фигура 1D представляет собой график рассеяния, показывающий аффинности связывания 59A9, 18B10, 7C12, 12C12 и 11F12 с клетками NUGC4. Названия клеточных линий, содержащих «CLDN18.2», описанные в настоящем документе, а также указанные на фигурах и примерах, относятся к CLDN18.2 человека, если не указано иное. CLDN18.2 мыши обозначается аббревиатурой «mCLDN18.2».
[0067] Фигура 2A представляет собой график рассеяния, показывающий, что химерное антитела 7C12-C, 11F12-C, 12E9-C связываются с клеткой HEK293-CLDN18.2 при EC50 около 0,6 мкг/мл, и 26G6-C связывается с клеткой HEK293-CLDN18.2 при EC50 около 1 мкг/мл. Фигура 2B представляет собой график рассеяния, показывающий, что эффективность CDC антител 7C12-C, 11F12-C, 12E9-C и 26G6-C более чем в 2 раза выше, чем у IMAB362. Фигура 2C представляет собой график рассеяния, показывающий, что 59A9-C имеет немного более высокую EC50 (1,3 мкг/мл) чем 18B10-C (1,0 мкг/мл). Фигура 2D представляет собой график рассеяния, показывающий, что антитела 59A9-C и 18B10-C имеют более чем 3-кратное увеличение эффективности CDC по сравнению с IMAB362.
[0068] Фигура 3A представляет собой график рассеяния, показывающий, что 18B10-C связывается с клетками MKN45 с высоким уровнем CLDN18.2 со значительно более высокой аффинностью, чем IMAB362. Фигура 3B представляет собой график рассеяния, показывающий, что при использовании клеток MKN45-CLDN18.2 две кривые свидетельствуют о том, что 18B10-C имеет лучшую ADCC-активность, чем IMAB362. Фигура 3C представляет собой график рассеяния, показывающий, что 18B10-C связывается с клетками MKN45 со средним уровнем CLDN18.2 со значительно более высокой аффинностью, чем IMAB362. Фигура 3D представляет собой график рассеяния, показывающий, что, в клетке MKN45 со средним уровнем CLDN18.2 18B10-C имеет более чем 50-кратное увеличение активности ADCC, как определено EC50, по сравнению с IMAB362.
[0069] Фигура 4A представляет собой график рассеяния, показывающий, что 3 из 4 химерных антител связываются с клеткой NUGC4 с ЕС50 около 10 мкг/мл, за исключением 26G6-C. Фигура 4B представляет собой график рассеяния, показывающий, что ADCC активность химерных антител 7C12-C, 11F12-C, 12E9-C и 26G6-C против клеток NUGC4. Фигура 4C представляет собой график рассеяния, показывающий, что химерное антитело 18B10-C связывается с клеткой NUGC4 с EC50 около 10 мкг/мл, но не для 59A9-C. Фигура 4D представляет собой график рассеяния, показывающий, что ADCC активность химерных антител 59A9-C и 18B10-C против клеток NUGC4 в отдельном эксперименте.
[0070] Фигура 5 представляет собой гистограмму, показывающую селективное связывание 18B10-C и IMAB362 с клетками HEK293, экспрессирующими CLDN18.2 или CLDN18.1.
[0071] Фигуры 6A и 6B представляют собой диаграммы рассеяния, показывающие аффинность связывания, когда гибридомное антитело 18B10 конкурирует с 10 мкг/мл IMAB362 на клетках MKN45 с высоким уровнем CLDN18.2 и 5 мкг/мл 18B10-C на клетках MKN45 с высоким уровнем CLDN18.2, соответственно. Гибридомное антитело 18B10 может полностью блокировать связывание IMAB362 с клетками MKN45 с высоким уровнем CLDN18.2.
[0072] Фигура 7A-B представляет собой гистограммы, показывающие сигнал связывания химерных антител с мутантными вариантами hCLDN 18.2 с использованием картирования эпитопов. Связывание 18B10-C было полностью утрачено, когда E56 был заменен на Q. Это изменение также относилось к IMAB362 и другим химерным антителам, за исключением 59A9-C. Другие аминокислоты, такие как A42, N45, также в некоторой степени способствовали связыванию IMAB362 и других антител, но не для 18B10-C.
[0073] Фигура 8A представляет собой график рассеяния, показывающий связывающую способность всех гуманизированных вариантов вместе с их химерными аналогами. Фигура 8B представляет собой график рассеяния, показывающий связывающую способность гуманизированного антитела 18B10-HaLa по сравнению с IMAB362 и контрольным hlgG1. 18B10-HaLa хорошо связывается с CLDN18.2 мыши с большей активностью и более высоким MFI, чем IMAB362.
[0074] Фигура 9 представляет собой график рассеяния, показывающий влияние CDC гуманизированного антитела 18B10-HaLa на HEK293-CLDN18.2. 18B10-HaLa имеет более чем в 20 раз более высокую CDC-активность, чем IMAB362.
[0075] Фигура 10A представляет собой график рассеяния, показывающий аффинность связывания гуманизированных вариантов 18В10 по сравнению с химерным 18В10 для клеток MKN45, экспрессирующих промежуточные уровни белка CLDN18.2 (MKN45 со средним уровнем CLDN18.2). Все гуманизированные варианты 18B10 связываются с клетками среды MKN45-CLDN18.2 с аффинностью, сравнимой с химерным 18B10. Фигура 10B представляет собой график рассеяния, показывающий анализ с использованием репортерного гена ADCC 18B10-HaLa и IMAB362 на клетках со средним уровнем MKN45-CLDN 18.2. 18B10-HaLa имеет намного более низкую EC50(0,05 мкг/мл), чем IMAB362, что согласуется с химерным 18B10.
[0076] Фигура 11A представляет собой график рассеяния, показывающий результат аффинности связывания 18B10-HaLa с клетками NUGC4. Фигура 11B представляет собой график рассеяния, показывающий эффект ADCC 18B10-HaLa по сравнению с IMAB362. 18B10-HaLa обладает гораздо большей активностью ADCC, чем IMAB362.
[0077] Фигура 12 представляет собой график рассеяния, показывающий результаты анализа ADCC с использованием PBMC (ID донора: A18Z017017) в качестве эффекторной клетки. 18B10-HaLa демонстрирует гораздо лучшую активность ADCC, чем IMAB362.
[0078] Фигура 13A представляет собой гистограмму, показывающую результат картирования эпитопа 18B10-HaLa (концентрация антител: 10 мкг/мл). Фигура 13B представляет собой гистограмму, показывающую результат картирования эпитопа 59A9-C (концентрация антител: 10 мкг/мл).
[0079] Фигура 14A представляет собой график рассеяния, показывающий цитотоксичность ADC как 18B10-HaLa-vcMMAE, так и IMAB362-vcMMAE на клетке HEK293-CLDN18.2. И 18B10-HaLa-vcMMAE, и IMAB362-vcMMAE, но не контрольный hIgG1-vcMMAE, индуцировали цитотоксичность в отношении клеток HEK293-CLDN18.2. Фигура 14B представляет собой график рассеяния, показывающий результат цитотоксического действия ADC 18B10-HaLa-MMAE и IMAB362-MMAE на NUGC-4. 18B10-HaLa-vcMMAE продемонстрировал дозозависимое ингибирование роста клеток, начиная с концентрации 0,03 мкг/мл, тогда как IMAB362-vcMMAE ингибировал рост клеток только при 10 мкг/мл, что является гораздо более высокой концентрацией. Фигура 14C представляет собой график рассеяния, показывающий цитотоксичность ADC 18B10-HaLa-MMAE и IMAB362-MMAE на клетке MKN45 с высоким уровнем CLDN18.2. 18B10-HaLa-vcMMAE достигает максимального уничтожения клеток 86%, что также выше, чем у IMAB362 (60%).
[0080] Фигура 15 представляет собой график рассеяния, показывающий изменение объема опухоли в зависимости от времени для изотипического контроля, IMAB362 и 18B10-HaLa. 18B10-HaLa демонстрирует значительно лучшую противоопухолевую активность, чем IMAB362 или изотипический контроль, что измеряется размером опухоли и TGI (ингибирование роста опухоли).
[0081] Фигура 16 представляет собой график рассеяния, показывающий изменение объема опухоли по времени в модельной группе (без РВМС), изотипическом контроле, 18B10-HaLa 3 мг/кг (мг/кг) и 18B10-HaLa 10 мг/кг, соответственно. 18B10-HaLa либо при дозе 3, либо при 10 мг/кг обладал значительным ингибированием роста опухоли по сравнению с изотипическим контролем или контролем РВМС.
[0082] Фигура 17 представляет собой график рассеяния, показывающий изменение объема опухоли по времени изотипического контроля, 18B10-HaLa 0,1 мг/кг, 18B10-HaLa 0,3 мг/кг и 18B10-HaLa 1 мг/кг, соответственно. Результаты показывают, что противоопухолевая активность 18B10-HaLa зависит от дозы.
[0083] Фигуры 18 A-I представляют собой графики рассеяния, показывающие связывание 18B10-HaLa hIgG1 с hFcRI-his, hFcγRIIB-his, hFcγRIIIA(F176)-his, hFcγRIIIA(V176)-his, FcγRI-his мыши, FcγRIIB-his мыши, FcγRIIIA-his мыши, FcγRIV-his и FcγRIII-his яванского макака, FcγRIIIA-his мыши, FcγRIV-his и FcγRIII-his яванского макака. Не было обнаружено существенной разницы между 18B10-HaLa_VLPYLL и 18B10-HaLa-wt в связывании с человеческим FcγRI или FcγRIIB. Однако 18B10-Hala_VLPYLL показал 10-кратное увеличение связывания с человеческим FcγRIIIA (F176) и FcγRIIIA (V176) по сравнению с его диким типом (wt). Аналогичные результаты были получены с FcγR мыши и FcγR яванского макака.
[0084] Фигуры 19A-19B представляют собой графики рассеяния, показывающие аффинность связывания 18B10 HaLa hlgG1 с huFcRn- биотином и C1q человека, соответственно. Результаты, представленные на фигуре 19A, показывают, что нет существенной разницы в связывании FcRn между 18B10-HaLa_VLPYLL и 18B10-HaLa wt. Результаты, представленные на фигуре 19B, показывают, что 18B10-HaLa_VLPYLL имеет несколько лучший сигнал связывания при более низкой концентрации C1q, чем 18B10-HaLa wt.
[0085] Фигура 20A представляет собой график рассеяния, показывающий результат репортерного анализа 18B10-HaLa hlgG1 на NUGC-4 (соотношение E/T=6:1) с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток. 18B10-HaLa-VLPYLL показывает 3-кратное увеличение активности ADCC (EC50~0,0097 мкг/мл) по сравнению с 18B10-HaLawt (EC50~0,032 мкг/мл). Фигура 20B представляет собой график рассеяния, показывающий результат анализа ADCC NUGC-4 с использованием PBMC (ID донора: A18Z017017) в качестве эффекторных клеток. 18B10-HaLa-VLPYLL показывает 3-кратное увеличение эффективности ADCC по сравнению с 18B10-HaLawt и 100-кратное увеличение активности ADCC по сравнению с IMAB362.
[0086] На Фигуре 21 показано сравнение уровня экспрессии CLDN18.2 в различных клеточных линиях рака желудка.
[0087] Фигура 22A-22D представляют собой графики рассеяния, показывающие анализы ADCC различных клеточных линий рака желудка с различными уровнями экспрессии CLDN18.2.
[0088] Фигура 23 представляет собой график рассеяния, показывающий результат репортерного анализа ADCC на NUGC4 (отношение E/T=6:1). Антитело, полученное с использованием процесса с добавлением 50 мкМ 2F-OF, повышало активность ADCC более чем в 30 раз по сравнению с эталонным образцом, полученным с использованием процесса без добавления 2F-OF, или более чем в 1000 раз выше активность ADCC, чем IMAB362.
[0089] Фигуры 24A-24C представляют собой графики рассеяния, показывающие связывание FACS различных клеточных линий рака желудка с использованием 18B10-HaLa с низким содержанием фукозы.
[0090] Фигуры 25A-25E представляют собой графики рассеяния, показывающие результаты анализа с использованием репортерного гена ADCC на различных клеточных линиях рака желудка с использованием 18B10-HaLa с низким содержанием фукозы.
[0091] Фигуры 26A-26D представляют собой графики рассеяния, показывающие результат анализа ADCC на различных клеточных линиях рака желудка с использованием PBMC (ID донора: A19028011) в качестве эффекторной клетки и 50 мкМ образца 2F-O-F 18B10-HaLa.
[0092] На фигуре 27 показана специфическая цитотоксичность 18B10-HaLa с низким содержанием фукозы в анализе ADCC на клетках NUGC-4.
[0093] На фигурах с 28A по 28B показано ингибирование роста опухоли 18B10-HaLa с низким содержанием фукозы в различных дозах в ксенотрансплантатной модели опухоли с совместной инокуляцией MKN45-CLDN18.2 и hPBMC.
[0094] На фигуре 29 показано ингибирование роста опухоли 18B10-HaLa с низким содержанием фукозы комбинацией 18B10-HaLa с низким содержанием фукозы с оксалиплатином и 5-FU на модели опухоли с MKN45 с высоким уровнем CLDN18.2.
[0095] На фигурах 30A и 30B показано ингибирование роста опухоли антителами в ксенотрансплантатной модели опухоли с MKN45 с высоким уровнем CLDN18.2.
[0096] На фигурах 31A, 31B и 31C показана эффективность 18B10-HaLa с низким содержанием фукозы в сочетании с паклитакселом в модели опухоли GC02-0004 PDX у голых мышей.
[0097] На фигурах 31D и 31E показано ингибирование роста опухоли антителами в модели опухоли GC02-0004 PDX.
[0098] На фигуре 32 показано ингибирование роста опухоли (TGI) антителами в ксенотрансплантатной модели MKN45-CLDN18.2.
[0099] На фигурах 33A и 33B показан FACS связывание с клеточными линиями рака поджелудочной железы с использованием 18B10-HaLa с низким содержанием фукозы.
[00100] На фигурах 34A и 34B показан анализ с использованием репортерного гена ADCC на клеточных линиях рака поджелудочной железы с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток.
[00101] На фигуре 35 показано ингибирование роста опухоли (TGI) антител в ксенотрансплантатной модели MIA PaCa-2-CLDN18.2.
[00102] На фигуре 36 показано ингибирование роста опухоли (TGI) антител в ксенотрансплантатной модели BxPC-3-CLDN18.2.
[00103] На фигурах 37A и 37B показано связывание FACS с клеточными линиями рака легкого с использованием 18B10-HaLa с низким содержанием фукозы.
[00104] На фигуре 38 показан анализ с использованием репортерного гена ADCC на NCI-H146 с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток.
[00105] На фигуре 39 показан анализ ADCC на NCI-H460-CLDN18.2 с использованием PBMC в качестве эффекторных клеток.
[00106] На фигурах 40A и 40B показано ингибирование роста опухоли (TGI) антител в модели совместной инокуляции NCI-H146 и PBMC.
[00107] На фигуре 41 показано ингибирование роста опухоли (TGI) антител в модели опухоли NCI-H460-CLDN18.2.
[00108] На фигуре 42 показан FACS связывание с клеточными линиями рака толстой кишки с использованием 18B10-HaLa с низким содержанием фукозы.
[00109] На фигуре 43 показан анализ с использованием репортерного гена ADCC на клеточных линиях рака толстой кишки с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00110] Следующее описание изобретения предназначено только для иллюстрации различных вариантов осуществления изобретения. Как таковые, обсуждаемые конкретные модификации не следует рассматривать как ограничение объема изобретения. Специалисту в данной области техники очевидно, что могут существовать различные эквиваленты, изменения и модификации, не выходя за рамки объема изобретения, и понятно, что такие эквивалентные варианты осуществления должны быть включены в настоящий документ. Все цитируемые в настоящем документе ссылки, включая публикации, патенты и патентные заявки, полностью включены в настоящий документ.
Определения
[00111] Как используется в настоящем документе, термины, используемые в контексте настоящего изобретения (особенно в контексте формулы изобретения) в единственном числе, следует толковать как охватывающие как единственное, так и множественное число, если в настоящем документе не указано иное или это явно не противоречит контексту.
[00112] Термин «антитело», как используется в настоящем документе, включает иммуноглобулин, моноклональное антитело, поликлональное антитело, поливалентное антитело, бивалентное антитело, моновалентное антитело, мультиспецифическое антитело или биспецифическое антитело которое связывается со специфическим антигеном. Нативное интактное антитело содержит две тяжелые (Н) цепи и две легкие (L) цепи. Тяжелые цепи млекопитающих классифицируются как альфа, дельта, эпсилон, гамма и мю, каждая тяжелая цепь состоит из вариабельной области (VH) и первой, второй и третьей константных областей (CH1, CH2, CH3, соответственно); легкие цепи млекопитающих классифицируются как λ или κ, при этом каждая легкая цепь состоит из вариабельной области (VL) и константной области. Антитело имеет Y-образную форму со стержнем Y, состоящим из второй и третьей константных областей двух тяжелых цепей, связанных вместе дисульфидной связью. Каждое плечо Y включает вариабельную область и первую константную область одиночной тяжелой цепи, связанные с вариабельной и константной областями одиночной легкой цепи. Вариабельные области легкой и тяжелой цепей отвечают за связывание антигена. Вариабельные области в обеих цепях обычно содержат три высоковариабельные петли, называемые областями, определяющими комплементарность (CDR) (CDR легкой цепи, включая LCDR1, LCDR2 и LCDR3, CDR тяжелой цепи, включая HCDR1, HCDR2, HCDR3). Границы CDR для антител и антигенсвязывающих доменов, раскрытых в настоящем документе, могут быть определены или идентифицированы в соответствии с конвенциями Кабата, IMGT, AbM, Chothia или Al-Lazikani (Al-Lazikani, B., Chothia, C., Lesk, A. M., J. Mol. Biol., 273(4), 927 (1997); Chothia, C. et al., J Mol Biol. Dec 5;186(3):651-63 (1985); Chothia, C. and Lesk, A.M., J.Mol.Biol., 196,901 (1987); N. R. Whitelegg et al. Protein Engineering, v13(12), 819-824 (2000); Chothia, C. et al., Nature. Dec 21-28;342(6252):877-83 (1989); Kabat E.A. et al., National Institutes of Health, Bethesda, Md. (1991); Marie-Paule Lefranc et al. Developmental and Comparative Immunology, 27: 55-77 (2003); Marie-Paule Lefranc et al. Immunome Research, 1(3), (2005); Marie-Paule Lefranc, Molecular Biology of B cells (second edition), chapter 26, 481-514, (2015)). Три CDR расположены между фланкирующими участками, известными как каркасные области (FR), которые являются более консервативными, чем CDR, и образуют каркас для поддержки гипервариабельных петель. Константные области тяжелой и легкой цепей не участвуют в связывании антигена, но выполняют различные эффекторные функции. Антитела относятся к классам на основании аминокислотной последовательности константной области их тяжелой цепи. Пятью основными классами или изотипами антител являются IgA, IgD, IgE, IgG и IgM, которые характеризуются наличием тяжелых цепей альфа, дельта, эпсилон, гамма и мю, соответственно. Некоторые основные классы антител делятся на подклассы, такие как IgG1 (тяжелая цепь гамма1), IgG2 (тяжелая цепь гамма2), IgG3 (тяжелая цепь гамма3), IgG4 (тяжелая цепь гамма4), IgA1 (тяжелая цепь альфа1) или IgA2 (тяжелая цепь альфа2). В некоторых вариантах осуществления изобретения антитело, предложенное в настоящем документе, включает любые его антигенсвязывающие фрагменты.
[00113] Как используется в настоящем документе, термин «антигенсвязывающий фрагмент» относится к фрагменту антитела, образованному из фрагмента антитела, содержащего одну или несколько CDR, или любой другой части антитела, которая связывается с антигеном, но не содержит интактного нативного структура антитела. Примеры антигенсвязывающего фрагмента включают, без ограничения, диатело, Fab, Fab', F(ab')2, Fd, фрагмент Fv, стабилизированный дисульфидом фрагмент Fv (dsFv), (dsFv)2, биспецифическое dsFv (dsFv-dsFv'), дисульфид-стабилизированное диатело (ds диатело), молекулу одноцепочечного антитела (scFv), димер scFv (бивалентное диатело), полиспецифическое антитело, верблюжье однодоменное антитело, нанотело, доменное антитело и бивалентное доменное антитело. Антигенсвязывающий фрагмент способен связываться с тем же антигеном, с которым связывается исходное антитело. В некоторых вариантах осуществления изобретения антигенсвязывающий фрагмент может содержать одну или несколько CDR конкретного человеческого антитела.
[00114] «Fab» в отношении антитела относится к моновалентному антигенсвязывающему фрагменту антитела, состоящему из одной легкой цепи (как вариабельной, так и константной областей), связанной с вариабельной областью и первой константной областью
[00115] одиночной тяжелой цепи дисульфидной связью. Fab можно получить расщеплением антитела папаином по остаткам, проксимальным к N-концу дисульфидной связи между тяжелыми цепями шарнирной области.
[00116] «Fab'» относится к Fab-фрагменту, который включает часть шарнирной области, который может быть получен расщеплением пепсином антитела по остаткам, проксимальным к С-концу дисульфидной связи между тяжелыми цепями шарнирной области и, таким образом, отличается от Fab небольшим количеством остатков (включая один или несколько цистеинов) в шарнирной области.
[00117] «F(ab')2» относится к димеру Fab', который содержит две легкие цепи и часть двух тяжелых цепей.
[00118] «Fc» в отношении антитела относится к части антитела, состоящей из второй и третьей константных областей первой тяжелой цепи, связанных со второй и третьей константными областями второй тяжелой цепи посредством дисульфидной связи. Fc-области IgG и IgM содержат три константные области тяжелой цепи (вторая, третья и четвертая константные области тяжелой цепи в каждой цепи). Его можно получить путем расщепления антитела папаином. Часть Fc антитела отвечает за различные эффекторные функции, такие как ADCC, ADCP и CDC, но не участвует в связывании антигена.
[00119] «Fv» в отношении антитела относится к наименьшему фрагменту антитела, имеющему полный сайт связывания антигена. Фрагмент Fv состоит из вариабельной области одной легкой цепи, связанной с вариабельной областью одной тяжелой цепи. «dsFv» относится к стабилизированному дисульфидом фрагменту Fv, в котором связь между вариабельной областью одиночной легкой цепи и вариабельной областью одиночной тяжелой цепи представляет собой дисульфидную связь.
[00120] «Одноцепочечное Fv-антитело» или «scFv» относится к сконструированному антителу, состоящему из вариабельной области легкой цепи и вариабельной области тяжелой цепи, соединенных друг с другом непосредственно или через пептидную линкерную последовательность (Huston JS et al. Proc Natl Acad Sci USA, 85:5879(1988)). «Димер scFv» относится к одиночной цепи, содержащей две вариабельные области тяжелой цепи и две вариабельные области легкой цепи с линкером. В некоторых вариантах осуществления «димер scFv» представляет собой двухвалентное диатело или двухвалентный ScFv (BsFv), содержащий VH-VL (связанный пептидным линкером), димеризованный с другим фрагментом VH-VL, так что VH одного фрагмента координируются с VL другого фрагмент и образуют два сайта связывания, которые могут быть нацелены на одни и те же антигены (или эпитопы) или на разные антигены (или эпитопы). В других вариантах осуществления изобретения «димер scFv» представляет собой биспецифическое диатело, содержащее VH1-VL2 (связанные пептидным линкером), связанные с VL1-VH2 (также связанные пептидным линкером), так что VH1 и VL1 координируются, а VH2 и VL2 координируются, и каждый координированная пара имеет различную антигенную специфичность.
[00121] «Одноцепочечное антитело Fv-Fc» или «scFv-Fc» относится к сконструированному антителу, состоящему из scFv, соединенного с Fc-областью антитела.
[00122] «Верблюжье однодоменное антитело», «антитело с тяжелой цепью», «нанотело» или «HCAb» относится к антителу, которое содержит два домена VH и не содержит легких цепей (Riechmann L. and Muyldermans S., J Immunol Methods. Dec 10;231(1-2):25-38 (1999); Muyldermans S., J Biotechnol. Jun; 74(4):277-302 (2001); WO 94/04678; WO 94/25591; патент США № 6005079). Антитела с тяжелой цепью первоначально были получены от Camelidae (верблюды, дромадеры и ламы). Несмотря на отсутствие легких цепей, верблюжьи антитела обладают аутентичным репертуаром связывания антигена (Hamers-Casterman C. et al., Nature. Jun 3; 363(6428):446-8 (1993); Nguyen VK. et al. «Heavy-chain antibodies in Camelidae; a case of evolutionary innovation», Immunogenetics. Apr; 54(1):39-47 (2002); Nguyen VK. et al. Immunology. May; 109(1):93-101 (2003)). Вариабельный домен тяжелой цепи антитела (домен VHH) представляет собой наименьшую известную антигенсвязывающую единицу, генерируемую адаптивными иммунными реакциями (Koch-Nolte F. et al., FASEB J. Nov; 21(13):3490-8. Epub 2007 Jun 15 (2007)). «Диатела» включают небольшие фрагменты антител с двумя антигенсвязывающими сайтами, где фрагменты содержат домен VH, соединенный с доменом VL в одной полипептидной цепи (VH-VL или VL-VH) (см., например, Holliger P. et al., Proc Natl Acad Sci U S A. Jul 15;90(14):6444-8 (1993); EP404097; WO 93/11161). Два домена в одной цепи не могут быть спарены, потому что линкер слишком короткий, поэтому домены вынуждены соединяться с комплементарными доменами другой цепи, тем самым создавая два антигенсвязывающих сайта. Антигенсвязывающие сайты могут быть нацелены на одни и те же различные антигены (или эпитопы).
[00123] «Домен антитела» относится к фрагменту антитела, содержащему только вариабельную область тяжелой цепи или вариабельную область легкой цепи. В некоторых вариантах осуществления два или более домена VH ковалентно соединены с пептидным линкером с образованием антитела с двухвалентным или поливалентным доменом. Два домена VH двухвалентного домена антитела могут быть нацелены на один и тот же или разные антигены.
[00124] В некоторых вариантах осуществления изобретения «(dsFv)2» содержит три пептидные цепи: две части VH, связанные пептидным линкером, и связанные дисульфидными мостиками с двумя частями VL.
[00125] В некоторых вариантах осуществления изобретения «биспецифическое ds диатело» содержит VH1-VL2 (связанные пептидным линкером), связанные с VL1-VH2 (также связанные пептидным линкером) через дисульфидный мостик между VH1 и VL1.
[00126] В некоторых вариантах осуществления изобретения «биспецифическое dsFv» или «dsFv-dsFv'» содержит три пептидные цепи: часть VH1-VH2, в которой тяжелые цепи связаны пептидным линкером (например, длинным гибким линкером) и спарены через дисульфидные мостики к фрагментам VL1 и VL2, соответственно. Каждая дисульфидная пара тяжелой и легкой цепи имеет различную антигенную специфичность.
[00127] Термин «гуманизированное», как используется в настоящем документе, означает, что антитело или его антигенсвязывающий фрагмент содержит CDR, полученные от животных, отличных от человека, области FR, полученные от человека, и, когда это применимо, константные области, полученные от человека. В некоторых вариантах осуществления изобретения аминокислотные остатки каркаса вариабельной области гуманизированного антитела CLDN18.2 заменены для оптимизации последовательности. В некоторых вариантах осуществления каркасные последовательности вариабельной области гуманизированной цепи антитела CLDN18.2 по меньшей мере на 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентичны соответствующим последовательностям каркаса вариабельной области человека.
[00128] Термин «химерный», используемый в настоящем документе, относится к антителу или его антигенсвязывающему фрагменту, которые имеют часть тяжелой и/или легкой цепи, полученную из одного вида, и остальная часть тяжелой и/или легкой цепи получена из другого вида. В иллюстративном примере химерное антитело может содержать константную область, полученную от человека, и вариабельную область, полученную от вида, отличного от человека, такого как мышь.
[00129] Термин «последовательность зародышевой линии» относится к последовательности нуклеиновой кислоты, кодирующей аминокислотную последовательность или подпоследовательность вариабельной области, которая имеет наивысшую определенную идентичность аминокислотной последовательности с эталонной аминокислотной последовательностью или подпоследовательностью вариабельной области по сравнению со всеми другими известными аминокислотными последовательностями вариабельной области, кодируемыми последовательностями вариабельной области иммуноглобулина зародышевой линии. Последовательность зародышевой линии может также относиться к аминокислотной последовательности или субпоследовательности вариабельной области с наивысшей идентичностью аминокислотной последовательности с эталонной аминокислотной последовательностью или субпоследовательностью вариабельной области по сравнению со всеми другими оцениваемыми аминокислотными последовательностями вариабельной области. Последовательность зародышевой линии может быть только каркасными областями, только определяющими комплементарность областями, каркасными и определяющими комплементарность областями, вариабельным сегментом (как определено выше) или другими комбинациями последовательностей или субпоследовательностей, которые составляют вариабельную область. Идентичность последовательности можно определить с использованием способов, описанных в настоящем документе, например, путем выравнивания двух последовательностей с использованием BLAST, ALIGN или другого алгоритма выравнивания, известного в данной области. Последовательность нуклеиновой кислоты или аминокислоты зародышевой линии может иметь по меньшей мере около 90%, 91, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичности последовательности с эталонной последовательностью нуклеиновой кислоты или аминокислоты вариабельной области. Последовательности зародышевой линии можно определить, например, с помощью общедоступной международной базы данных ImMunoGeneTics (IMGT) и V-base.
[00130] «Анти-CLDN18.2 антитело» или «антитело против CLDN18.2», как используется в настоящем документе, относится к антителу, которое способно специфически связываться с CLDN18.2 (например, CLDN18.2 человека или не человека) с достаточной аффинностью, например, для обеспечения диагностического и/или терапевтического применения.
[00131] Термин «аффинность», как используется в настоящем документе, относится к силе нековалентного взаимодействия между молекулой иммуноглобулина (то есть антителом) или ее фрагментом и антигеном.
[00132] Термин «специфическое связывание» или «специфически связывает», как используется в настоящем документе, относится к реакции неслучайного связывания между двумя молекулами, например, между антителом и антигеном. В некоторых вариантах осуществления изобретения антитела или антигенсвязывающие фрагменты, предложенные в настоящем документе, специфически связываются с CLDN18.2 человека и/или не человека с аффинностью связывания (KD) ≤10-6 M (например, ≤5×10-7 M, ≤2×10-7 M, ≤10-7 M, ≤5×10-8 M, ≤2×10-8 M, ≤10-8 M, ≤5×10-9 M, ≤4×10-9M, ≤3×10-9M, ≤2×10-9 M или ≤10-9 M. KD, используемый в настоящем документе, относится к отношению скорости диссоциации к скорости ассоциации (koff/kon), которое может быть определено с использованием любого обычного метода, известного в данной области техники, включая, помимо прочего, метод поверхностного плазмонного резонанса, метод микромасштабного термофореза, метод ВЭЖХ-МС и метод проточной цитометрии (например, FACS). В некоторых вариантах осуществления значение KD может быть надлежащим образом определено с помощью метода проточной цитометрии. Для выбора антител, специфически иммунореактивных с конкретным белком, можно использовать различные форматы иммунологических анализов. Например, твердофазные иммунологические анализы ELISA обычно используются для выбора антител, специфически иммунореактивных с белком (см., например, Harlow & Lane, Using Antibodies, A Laboratory Manual (1998), описание форматов и условий иммуноанализа, которые можно использовать для определения специфической иммунореактивности). Обычно реакция специфического или селективного связывания будет давать сигнал, по меньшей мере, в два раза превышающий фоновый сигнал, а более типично, по меньшей мере, в 10-100 раз превышающий фоновый сигнал.
[00133] «Процент (%) идентичности последовательности» по отношению к аминокислотной последовательности (или последовательности нуклеиновой кислоты) определяется как процент аминокислотных (или нуклеиновых) остатков в последовательности-кандидате, которые идентичны остаткам аминокислоты (или нуклеиновой кислоты) в эталонной последовательности, после выравнивания последовательностей и, при необходимости, введения гэпов для достижения максимального соответствия. Выравнивание с целью определения процентной идентичности аминокислотной (или нуклеиновой кислоты) последовательности может быть достигнуто, например, с использованием общедоступных инструментов, таких как BLASTN, BLASTp (доступны на веб-сайте Национального центра биотехнологической информации США (NCBI), см. также, Altschul S.F. et al. J. Mol. Biol., 215:403-410 (1990); Stephen F. et al. Nucleic Acids Res., 25:3389-3402 (1997)), ClustalW2 (доступны на сайте Европейского института биоинформатики, см. также Higgins D.G. et al. Methods in Enzymology, 266:383-402 (1996); Larkin M.A. et al. Bioinformatics (Oxford, England), 23(21): 2947-8 (2007)), и программное обеспечение ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут использовать параметры по умолчанию, предоставляемые прибором, или могут настраивать параметры в соответствии с настройками, например, путем выбора подходящего алгоритма. В некоторых вариантах осуществления изобретения неидентичные положения остатков могут отличаться консервативными аминокислотными заменами. «Консервативная аминокислотная замена» представляет собой замену аминокислотного остатка другим аминокислотным остатком, имеющим боковую цепь (группу R) с аналогичными химическими свойствами (например, зарядом или гидрофобностью). В общем, замена консервативной аминокислоты существенно не изменит функциональные свойства белка. В случаях, когда две или более аминокислотных последовательностей отличаются друг от друга консервативными заменами, процент или степень сходства можно скорректировать в сторону увеличения, чтобы скорректировать консервативный характер замены. Средства для выполнения этой регулировки хорошо известны специалистам в данной области техники. См., например, работу Pearson (1994) Methods Mol. Biol. 24: 307-331, которая включена в настоящий документ в качестве ссылки..
[00134] Как используется в настоящем документе, «гомологическая последовательность» и «гомологичная последовательность» взаимозаменяемы и относятся к полинуклеотидным последовательностям (или их комплементарным цепям) или аминокислотным последовательностям, которые имеют идентичность последовательностей по меньшей мере на 85%, 88%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%) к другим последовательностям при необязательном выравнивании.
[00135] «Выделенное» вещество было изменено руками человеком из естественного состояния. Если «изолированная» композиция или вещество встречаются в природе, они были изменены или удалены из исходной среды, или и то, и другое. Например, полинуклеотид или полипептид, естественно присутствующий в живом организме, не является «выделенным», но тот же самый полинуклеотид или полипептид является «выделенным», если он был достаточно отделен от сосуществующих материалов в своем естественном состоянии, чтобы существовать в практически чистом состоянии. Выделенная «нуклеиновая кислота» или «полинуклеотид» используются взаимозаменяемо и относятся к последовательности выделенной молекулы нуклеиновой кислоты. В некоторых вариантах осуществления изобретения «выделенное антитело или его антигенсвязывающий фрагмент» относится к антителу или его антигенсвязывающим фрагментам, имеющим чистоту по меньшей мере 60%, 70%, 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% как определено электрофоретическими методами (такими как SDS-PAGE, изоэлектрическое фокусирование, капиллярный электрофорез) или хроматографическими методами (такими как ионообменная хроматография или ВЭЖХ с обращенной фазой).
[00136] Способность «блокировать связывание» или «конкурировать за один и тот же эпитоп», как используется в настоящем документе, относится к способности антитела или антигенсвязывающего фрагмента ингибировать связывающее взаимодействие между двумя молекулами (например, CLDN18.2 человека и анти-CLDN18.2 антитело) в любой обнаруживаемой степени. В некоторых вариантах осуществления изобретения антитело или антигенсвязывающий фрагмент, блокирующие связывание между двумя молекулами, ингибируют связывающее взаимодействие между двумя молекулами по меньшей мере на 50%. В некоторых вариантах осуществления изобретения то ингибирование может составлять более 60%, более 70%, более 80% или более 90%.
[00137] Термин «конъюгат антитело-лекарственное средство», как используется в настоящем документе, относится к связыванию антитела или его антигенсвязывающего фрагмента с другим агентом, таким как химиотерапевтический агент, токсин, иммунотерапевтический агент, визуализирующий зонд и тому подобное. Связь может представлять собой ковалентные связи или нековалентные взаимодействия, такие как электростатические силы. Для образования конъюгата антитело-лекарственное средство можно использовать различные линкеры, известные в данной области. Кроме того, конъюгат антитело-лекарственное средство может быть предоставлен в форме слитого белка, который может быть экспрессирован из полинуклеотида, кодирующего конъюгат. Как используется в настоящем документе, термин «слитый белок» относится к белкам, созданным путем соединения двух или более генов или фрагментов генов, которые первоначально кодировали отдельные белки (включая пептиды и полипептиды). Трансляция гена слияния приводит к одному белку с функциональными свойствами, полученными от каждого из исходных белков.
[00138] Термин «субъект» включает человека и животных, отличных от человека. К животным, отличным от человека, относятся все позвоночные, например, млекопитающие и не млекопитающие, такие как приматы, мыши, крысы, кошки, кролики, овцы, собаки, коровы, куры, земноводные и рептилии. Если не указано иное, термины «пациент» или «субъект» используются в настоящем документе взаимозаменяемо.
[00139] Термин «противоопухолевая активность» означает снижение пролиферации, жизнеспособности или метастатической активности опухолевых клеток. Например, противоопухолевая активность может проявляться снижением скорости роста аномальных клеток, возникающим во время терапии, или стабильностью или уменьшением размера опухоли, или более длительной выживаемостью благодаря терапии по сравнению с контролем без терапии. Такую активность можно оценить с использованием общепринятых моделей опухолей in vitro или in vivo, включая, помимо прочего, ксенотрансплантатные модели, модели аллотрансплантатов, модели вируса опухоли молочной железы мыши (MMTV) и другие известные в данной области модели для исследования противоопухолевой активности.
[00140] «Эффекторные функции» или «эффекторные функции антитела», используемые в настоящем документе, относятся к биологической активности, связанной со связыванием Fc-области антитела с его эффекторами, такими как комплекс C1 и Fc-рецептор. Примеры эффекторных функций включают: комплементзависимую цитотоксичность (CDC), индуцированную взаимодействием антител и C1q на комплексе C1; антителозависимую клеточно-опосредованную цитотоксичность (ADCC), индуцированную связыванием Fc-области антитела с Fc-рецептором на эффекторной клетке; и антителозависимый клеточно-опосредованный фагоцитоз (ADCP), при котором неспецифические цитотоксические клетки, экспрессирующие FcγR, распознают связанное антитело на клетке-мишени и впоследствии вызывают фагоцитоз клетки-мишени. Эффекторные функции включают как те, которые действуют после связывания антигена, так и те, которые действуют независимо от связывания антигена.
[00141] «Лечение» или «излечение» состояния, используемое в настоящем документе, включает предотвращение или облегчение состояния, замедление начала или скорости развития состояния, снижение риска развития состояния, предотвращение или задержку развития симптомов, связанных с состоянием, уменьшением или прекращением симптомов, связанных с состоянием, созданием полной или частичной регрессии состояния, излечением состояния или некоторой их комбинацией.
[00142] Термин «вектор», используемый в настоящем документе, относится к носителю, в который может быть функционально встроен генетический элемент, чтобы вызвать экспрессию этого генетического элемента, например, для продукции белка, РНК или ДНК, кодируемых генетическим элемента или для репликации генетического элемента. Вектор можно использовать для трансформации, трансдукции или трансфекции клетки-хозяина, чтобы вызвать экспрессию генетического элемента, который он несет в клетке-хозяине. Примеры векторов включают плазмиды, фагемиды, космиды, искусственные хромосомы, такие как искусственная хромосома дрожжей (YAC), искусственная хромосома бактерий (BAC) или искусственная хромосома, полученная из P1 (PAC), бактериофаги, такие как фаг лямбда или фаг M13, и вирусы животных. Вектор может содержать множество элементов для контроля экспрессии, включая промоторные последовательности, последовательности инициации транскрипции, энхансерные последовательности, селектируемые элементы и репортерные гены. Кроме того, вектор может содержать точку начала репликации. Вектор может также включать материалы, способствующие его проникновению в клетку, включая, помимо прочего, вирусную частицу, липосому или белковое покрытие. Вектор может быть вектором экспрессии или вектором клонирования. В настоящем изобретении предложены векторы (например, векторы экспрессии), содержащие представленную в настоящем документе последовательность нуклеиновой кислоты, кодирующую антитело или его антигенсвязывающий фрагмент, по меньшей мере один промотор (например, SV40, CMV, EF-1α), функционально связанный с последовательностью нуклеиновой кислоты, и хотя бы один маркер выбора.
[00143] Термин «клетка-хозяин», как используется в настоящем документе, относится к клетке, в которую введен экзогенный полинуклеотид и/или вектор.
[00144] Термин «CLDN18.2» относится к варианту 2 сплайсинга клаудина-18, полученному от млекопитающих, таких как приматы (например, люди, обезьяны) и грызуны (например, мыши). В некоторых вариантах осуществления CLDN18.2 представляет собой CLDN18.2 человека. Типовая последовательность CLDN18.2 человека включает белок CLDN18.2 человека (NCBI Ref Seq No. NP_001002026.1, или SEQ ID NO: 30). Типичная последовательность CLDN18.2 включает белок CLDN18.2 Mus musculus (мышь) (NCBI Ref Seq No. NP_001181852.1), белок CLDN18.2 Macaca fascicularis (крабоядная макака) (NCBI Ref Seq No. XP_015300615.1). CLDN18.2 экспрессируется в раковой клетке. В одном варианте осуществления указанный CLDN18.2 экспрессируется на поверхности раковой клетки.
[00145] Термин «CLDN18.1» относится к варианту 1 сплайсинга клаудина-18, полученному от млекопитающих, таких как приматы (например, люди, обезьяны) и грызуны (например, мыши). В некоторых вариантах осуществления CLDN18.1 представляет собой CLDN18.1 человека. Типовая последовательность CLDN18.1 человека включает белок CLDN18.1 человека (NCBI Ref Seq No. NP_057453.1 или SEQ ID NO: 31), белок CLDN18.2 Mus musculus (мыши) (NCBI Ref Seq No. NP_001181851.1) , Macaca fascicularis (крабоядная макака) белок CLDN18.2 (NCBI Ref Seq No. XP_005545920.1).
[00146] «Связанное с CLDN18.2» заболевание или состояние, как используется в настоящем документе, относится к любому заболеванию или состоянию, вызванному, усугубленному или иным образом связанным с повышенной или пониженной экспрессией или активностью CLDN18.2. В некоторых вариантах осуществления состояние, связанное с CLDN18.2, представляет собой, например, рак.
[00147] «Рак» в контексте настоящего документа относится к любому медицинскому состоянию, характеризующемуся злокачественным ростом клеток или новообразованиями, аномальной пролиферацией, инфильтрацией или метастазированием, и включает как солидные опухоли, так и несолидные виды рака (например, гематологические злокачественные новообразования), такие как лейкемия. Как используется в настоящем документе, термин «солидная опухоль» относится к солидной массе неопластических и/или злокачественных клеток. Термин «фармацевтически приемлемый» означает, что указанный носитель, носитель, разбавитель, эксципиент(ы) и/или соль, как правило, химически и/или физически совместимы с другими ингредиентами, входящими в состав, и физиологически совместимы с их реципиентом.
[00148] Ссылка на «около» значения или параметра в данном документе включает (и описывает) варианты осуществления, которые направлены на это значение или параметр как таковой. Например, описание, относящееся к «около X», включает в себя описание «X». Числовые диапазоны включают числа, определяющие диапазон. Вообще говоря, термин «около» относится к указанному значению переменной и ко всем значениям переменной, которые находятся в пределах экспериментальной ошибки указанного значения (например, в пределах 95% доверительного интервала для среднего значения) или в пределах 10 процентов от указанного значения, в зависимости от того, что больше. Когда термин «около» используется в контексте периода времени (годы, месяцы, недели, дни и т.д.), термин «около» означает этот период времени плюс или минус одно значение следующего подчиненного периода времени (например, около 1 года означает 11-13 месяцев; около 6 месяцев означает 6 месяцев плюс или минус 1 неделя; около 1 недели означает 6-8 дней и т.д.) или в пределах 10 процентов от указанного значения, в зависимости от того, что больше.
[00150] В настоящем изобретении предложены анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты. Анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, способны специфически связываться с CLDN18.2 (например, CLDN18.2 человека) или клетками, экспрессирующими CLDN18.2. «Специфическое связывание», как используется в настоящем документе, означает аффинность связывания (например, KD) ≤10-6 M (например, ≤5×10-7 М, ≤2×10-7 М, ≤10-7 М, ≤5×10-8 М, ≤2×10-8 М, ≤10-8 М, ≤5×10-9 М, ≤4×10-9 М, ≤3×10-9М, ≤2×10-9 М или ≤10-9 М).
i. Аффинность связывания
[00151] Аффинность связывания анти-CLDN18.2 антител и антигенсвязывающих фрагментов, предложенных в настоящем документе, может быть представлена значением KD, которое представляет собой отношение скорости диссоциации к скорости ассоциации (koff/kon), когда связывание между антигеном и связывающей антиген молекулой достигает равновесия. Антитела с низкой аффинностью обычно медленно связывают антиген и легко диссоциируют, в то время как антитела с высокой аффинностью обычно связывают антиген быстрее и дольше остаются связанными. Аффинность связывания антигена (например, KD) можно надлежащим образом определить с использованием любых подходящих способов, известных в данной области, включая, например, анализ кинетического исключения (KinExA) или проточную цитометрию.
[00152] В некоторых вариантах осуществления изобретения «Kd» или «значение Kd» в соответствии с настоящим изобретением определяется с помощью анализа KinExA, проводимого с анти-CLDN18.2 антителом и CLDN18.2, как описано в следующем анализе, в котором определяется аффинность связывания раствора анти-CLDN18.2 антитело. Как правило, KinExA работает, уравновешивая постоянное количество одного партнера по связыванию (CBP) с различной концентрацией другого партнера по связыванию (титрант), а затем захватывая часть свободного CBP с помощью флуоресцентно-меченого вторичного антитела за короткое время контакта, которое меньше времени, необходимого для диссоциации предварительно образованного комплекса СВР-титрант. Сигналы флуоресценции, генерируемые захваченным CBP, прямо пропорциональны концентрации свободного CBP в уравновешенных образцах и используются для построения кривой связывания (процент свободного CBP по сравнению с общей концентрацией титранта) при измерении в серии. Более подробную информацию можно получить в работе Schreiber, G., Fersht, A.R. Nature Structural Biology. 1996, 3(5), 427-431. Когда анти-CLDN18.2 антитело используется в качестве CBP в постоянном количестве, тогда в качестве титранта можно использовать клетки, экспрессирующие CLDN18.2, или наоборот. Клетки, экспрессирующие CLDN18.2 или CLDN18.2, можно использовать для определения Kd с помощью KinExA. В некоторых вариантах осуществления Kd анти-CLDN18.2 антитело или его антигенсвязывающих фрагментов определяют в соответствии со способом, описанным в разделе 3 примера 10 настоящего описания.
[00153] Другие способы, подходящие для измерения Kd, также могут быть использованы при соответствующих обстоятельствах, например, анализ связывания антигена с радиоактивной меткой (см., например, Chen, et al., (1999) J. Mol Biol 293:865-881), или анализы поверхностного плазмонного резонанса, такие как BIAcore, с использованием иммобилизованных чипов CLDN18.2 CM5 в соответствующих единицах ответа (RU).
[00154] В некоторых вариантах осуществления изобретения аффинность связывания анти-CLDN18.2 антитела определяют с помощью проточной цитометрии. Как правило, клетки, экспрессирующие CLDN18.2, инкубируют с рядом концентраций анти-CLDN18.2 антитело, затем инкубируют с флуоресцентно меченым вторичным антителом, а затем анализируют на интенсивность флуоресцентного сигнала. В некоторых вариантах осуществления изобретения аффинность связывания анти-CLDN18.2 антитела или их антигенсвязывающие фрагменты определяют в соответствии со способом, описанным в примере 5 настоящего описания.
[00155] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, специфически связываются с CLDN18.2 человека (или клеткой, экспрессирующей CLDN18.2 человека) со значением Kd не более чем 2.5 нМ (или не более чем 2,4, 2,3, 2,2, 2,1, 2,0, 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4 нМ), как определено анализом KinExA.
[00156] Альтернативно, аффинность связывания анти-CLDN18.2 антител и антигенсвязывающих фрагментов, предложенных в настоящем документе, с CLDN18.2 человека также может быть представлена значением «полумаксимальной эффективной концентрации» (EC50), которое относится к концентрации антитела, при которой 50% наблюдается его максимальный эффект (например, связывание). Величину EC50 можно определить способами, известными в данной области, например, сэндвич-анализом, таким как ELISA, вестерн-блоттингом, анализом проточной цитометрии и другим анализ связывания. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, специфически связываются с CLDN18.2 человека (например, клеткой, экспрессирующей CLDN18.2 человека) при значении EC50 не более чем 70 мкг/мл (или не более чем 65, 60, 55, 50, 45, 40, 35, 30, 25, 20, 15, 12, или 10, 9, 8, 7, 6, 5, 4, 3, 2, или 1 мкг/мл), как определено анализом проточной цитометрии.
[00157] Аффинность связывания можно определить в отношении рекомбинантных CLDN18.2 или экспрессирующих CLDN18.2 клеточных линий. Антитело и его антигенсвязывающий фрагмент, предложенные в настоящем документе, способны связываться с клетками, экспрессирующими различные уровни CLDN18.2 человека, в частности с клетками, экспрессирующими относительно средние или низкие уровни CLDN18.2 человека.
[00158] В некоторых вариантах осуществления изобретения аффинность связывания определяют с помощью клетки, экспрессирующей CLDN18.2 человека, такой как клетка NUGC4, клетка SNU-620, клетка SNU-601, клетка KATOIII или их сравнимых клеток, имеющих уровень экспрессии человеческого белка CLDN18.2, сравнимый или не превышающий уровень экспрессии клеток NUGC4, клеток SNU-620, клеток SNU-601 или клеток KATOIII.
[00159] Клетка NUGC4 представляет собой клеточную линию, полученную из парагастрального лимфатического узла больного раком (см. Akiyama S et al. Jpn J Surg. 1988 Jul;18(4):438-46). Клеточная линия NUGC4 доступна в банке клеток JCRB под регистрационным номером JCRB0834.
[00160] Клетки SNU-601 и клетки SNU-620 представляют собой клеточные линии карциномы желудка человека, полученные из асцита онкологических больных Сеульским национальным университетом (SNU) (KU JL et al. Cancer Res Treat. 2005 Feb; 37(1): 1-19; Park et al., Int J Cancer. 1997 Feb 7; 70(4):443-449). Клетка SNU-601 и клетка SNU-620 доступны в банке клеточных линий Кореи под регистрационными номерами 00601 и 00620, соответственно.
[00161] Клетка KATO III представляет собой клеточную линию, полученную из метастатического участка больного раком желудка (см. Sekiguchi M, et al. Jpn. J. Exp. Med. 48: 61-68, 1978.). Клеточная линия KATO III доступна в ATCC под регистрационным номером ATCC HTB-103.
[00162] Линии клеток, рекомбинантно экспрессирующие белок CLDN18.2 человека, также могут быть получены, например, путем трансфекции и экспрессии ДНК, кодирующей CLDN18.2 человека, в клеточной линии, такой как клетки яичника китайского хомячка (CHO), HEK или клеточная линия MKN45 (National Infrastructure of Cell Line Resource, № по каталогу 3111C0001CCC000229), среди прочего.
[00163] В некоторых вариантах осуществления изобретения аффинность связывания определяют с помощью клетки CLDN18.2 человека с высокой степенью экспрессии, клетки CLDN18.2 человека со средней степенью экспрессии или клетки CLDN18.2 человека с низкой степенью экспрессии.
[00164] Уровни экспрессии человеческого белка CLDN18.2 могут различаться в разных клеточных линиях. Уровень экспрессии белка CLDN18.2 в клетке можно измерить любыми подходящими способами, известными в данной области, например, количественной флуоресцентной цитометрией или иммуногистохимией (IHC). В некоторых вариантах осуществления уровень экспрессии белка CLDN18.2 человека на данной клетке определяют в соответствии с IHC. IHC включает обнаружение антигенов (например, CLDN18.2) в клетках или тканях путем визуализации антигена при взаимодействии антиген-антитело. Обычно антиген выявляют с помощью первичных антител против антигена. Первичное антитело может быть помечено для прямого обнаружения антигена. В качестве альтернативы, первичное антитело может быть немеченым и дополнительно контактировать со вторичным антителом, конъюгированным с обнаруживаемой меткой, для обеспечения непрямого обнаружения антигена. Первичное антитело может представлять собой любое антитело, способное специфически связываться с CLDN18.2 человека, например, без ограничений, любое из предложенных в настоящем документе анти-CLDN18.2 антител, или любое из анти-CLDN18.2 антител, известных в данной области. В некоторых вариантах осуществления изобретения клетки или ткани можно фиксировать, например, с помощью параформальдегида.
[00165] Термин «высокоэкспрессирующие», как используется в настоящем документе, в отношении клеток, экспрессирующих CLDN18.2 человека, означает, что клетки экспрессируют CLDN18.2 человека с интенсивностью по меньшей мере 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 40% (например, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, 40-100%, 50-100%, 60-100%, 70-100%, 80-100%, 90-100%, 40-90%, 50-90%, 60-90%, 70-90%, 80-90%, 40-80%, 40-70%, 40-60%, 40-50%, 50-80%, 50-70%, 50-60%, 60-80%, 60-70% или 70-80%) клеток окрашиваются положительно при IHC. Аналогичным образом, термин «среднеэкспрессирующие», как используется в настоящем документе, означает, что клетки экспрессируют CLDN18.2 человека с интенсивностью по меньшей мере 1+ и ниже 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 30% (или по меньшей мере 35%), но ниже 40% клеток окрашиваются положительно при IHC. Кроме того, термин «низкоэкспрессирующие», как используется в настоящем документе, означает, что клетки экспрессируют CLDN18.2 человека с интенсивностью около 0, но ниже 1+, как определено с помощью IHC, и на уровне, где около 0, но ниже 30% (например, 5%, 10%, 15%, 20%, 25%, 5-25%, 10-25%, 15-25%, 20-25%, 5-20%, 5-15%, 5-10%, 10-20%, или 10-15%) клеток окрашиваются положительно при IHC. Определение также показано в приведенной ниже таблице А.
Таблица A. Категория экспрессирующих клеток
HEK293-CLDN18.2
SNU-620;
KATO III;
MKN45-CLDN18.2-средне
[00166] В некоторых вариантах осуществления изобретения уровень экспрессии CLDN18.2 человека определяют с помощью IHC, как описано в разделе 6 и разделе 7 примера 15. Вкратце, клетки, экспрессирующие CLDN18.2 человека, фиксируют в парафине и обнаруживают с помощью IHC с использованием анти-CLDN18.2 антитела человека, с последующим определением относительной доли положительно окрашенных клеток и интенсивности окрашивания клеточной мембраны. В некоторых вариантах осуществления изобретения клетки окрашивают биотинилированным анти-CLDN18.2 антителом GC182 в процессе IHC. Антитело GC182 имеет последовательность вариабельной области тяжелой цепи SEQ ID NO: 74 и последовательность вариабельной области легкой цепи SEQ ID NO: 75 (см. также WO2013167259).
[00167] На основании результатов иммуногистохимического (IHC) определения, представленных в настоящем документе (таблица 13), клетки NUGC4 можно охарактеризовать как клеточную линию человека со средним уровнем экспрессии CLDN18.2, в то время как клетки SNU-620, SNU-601 и KATOIII как клеточная линия с низким уровнем экспрессии. Кроме того, рекомбинантные клеточные линии могут быть созданы для высокой экспрессии человеческого CLDN18.2. Примеры клеток с высоким уровнем экспрессии включают, без ограничения, клеточную линию MKN45 с высоким уровнем CLDN18.2 и клеточную линию HEK293-CLDN18.2, описанные в настоящем документе в разделе 3 примера 1.
[00168] Авторы изобретения неожиданно обнаружили, что анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, обладают высокой аффинностью к клеточным линиям человека со средним уровнем экспрессии CLDN18.2 (например, клеткам NUGC4), клеточным линиям с низким уровнем экспрессии (например, клетки SNU-620, SNU-601 и KATOIII). Это отличается от существующих антител, таких как IMAB362, которые не проявляют специфического или сравнимого связывания с клетками человека с низким уровнем экспрессии CLDN18.2. Химерное антитело IgG1 IMAB362 представляет собой анти-CLDN18.2 антитело человека, разработанное Ganymed Pharmaceuticals AG, имеющее аминокислотную последовательность, описанную в заявке на патент США US2009169547A1 (последовательности вариабельных областей тяжелой и легкой цепей IMB362 включены в настоящий документ как SEQ ID NO: 72 и SEQ ID NO: 73), и номер CAS 1496553-00-4. IMAB362 распознает первый внеклеточный домен (ECD1) CLDN18.2 и не связывается с каким-либо другим членом семейства клаудинов, включая близкородственный вариант сплайсинга 1 клаудина 18 (CLDN18.1).
[00169] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, специфически связываются с клеткой, экспрессирующей CLDN18.2 человека (например, клеточной линией NUGC4 или клеточной линией KATOIII) со значением Kd не более чем 2,5 нМ (или не более чем 2,4, 2,3, 2,2, 2,1, 2,0, 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4 нМ), как определено анализом KinExA. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, специфически связываются с клеткой, экспрессирующей CLDN18.2 человека со значением Kd не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15% от такового для IMAB362, как определено анализом KinExA. В некоторых вариантах осуществления изобретения значение KD определяют с помощью клетки NUGC4, клетки KATOIII, клетки SNU-601, клетки SNU-620 или их сопоставимых клеток, имеющих уровень экспрессии человеческого белка CLDN18.2, сравнимый или не превышающий таковой у клетки NUGC4, клетки KATOIII, клетки SNU-601 или клетки SNU-620. В некоторых вариантах осуществления изобретения значение KD определяют с помощью клеточной линии с высоким уровнем экспрессии CLDN18.2 человека или клеточная линия со средним уровнем экспрессии CLDN18.2 человека.
[00170] В некоторых вариантах осуществления изобретения антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, имеют значение EC50 для связывания с клеткой, экспрессирующей CLDN18.2 человека (или CLDN18.2 мыши) не более чем 70 мкг/мл (или не более чем 65, 60, 55, 50, 45, 40, 35, 30, 25, 20, 15, 12, или 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 мкг/мл), как определено анализом проточной цитометрии. В некоторых вариантах осуществления изобретения антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, специфически связываются с клеткой, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15%, 10%, 1% или 0,1% от такового для IMAB362, как определено анализом проточной цитометрии. В некоторых вариантах осуществления изобретения EC50 определяют с помощью клеточной линии NUGC4, клеточной линии KATOIII, клеточной линии SNU-601, клеточной линии SNU-620 или их сопоставимых клеток, имеющих уровень экспрессии человеческого белка CLDN18.2, сравнимый или не превышающий уровень экспрессии клеточной линии NUGC4, клеточной линии KATOIII, клеточной линии SNU-601 или клеточной линии SNU-620, например, клеточной линии с низким уровнем экспрессии CLDN18.2 человека или клеточной линии со средним уровнем экспрессии CLDN18.2 человека. В некоторых вариантах осуществления изобретения EC50 определяют с помощью клеточной линии с высоким уровнем экспрессии CLDN18.2 человека.
[00171] В некоторых вариантах осуществления изобретения антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, имеют значение EC50 не более чем 5, 4, 3 или 2 мкг/мл для связывания с клеточной линией с высоким уровнем экспрессии CLDN18.2 человека или с клеточной линией со средним уровнем экспрессии CLDN18.2 человека.
[00172] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, имеют значение EC50 для связывания с клетками NUGC4 не более чем 70 мкг/мл (или не более чем 65, 60, 55, 50, 45, 40, 35, 30, 25, 20, 15, 12, или 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 мкг/мл), как определено анализом проточной цитометрии.
[00173] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты не связываются с CLDN18.1 (например, CLDN18.1 человека или CLDN18.1 мыши).
[00174] В некоторых вариантах осуществления изобретения антитела и их антигенсвязывающие фрагменты способны специфически связываться с CLDN18.2 мыши (например, клетка, экспрессирующая CLDN18.2 мыши) при значении EC50 не более чем 1,5 мкг/мл, как определено проточной цитометрией. В некоторых вариантах осуществления изобретения антитела и их антигенсвязывающие фрагменты связываются с CLDN18.2 мыши при EC50 0,1 мкг/мл-1,5 мкг/мл (например, 0,1 мкг/мл-1,2 мкг/мл, 0,2 мкг/мл-1 мкг/мл, 0,5 мкг/мл-1 мкг/мл, 0,6 мкг/мл-1 мкг/мл, 0,6 мкг/мл-0,8 мкг/мл, или 0,67 мкг/мл), как определено проточной цитометрией.
1. Активность ADCC и CDC
[00175] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, способны индуцировать активность антителозависимой клеточной цитотоксичности (ADCC) и/или активность CDC в клетках, экспрессирующих различные уровни CLDN18.2 человека.
[00176] Как используется в настоящем документе, «антителозависимая клеточная цитотоксичность» или «ADCC» относится к клеточно-опосредованному взаимодействию, при котором неспецифические цитотоксические клетки, экспрессирующие Fc-рецепторы (FcR) (например, естественные клетки-киллеры (NK), нейтрофилы и макрофаги) распознают связанное антитело на клетке-мишени и впоследствии вызывают лизис клетки-мишени. Лизис клетки-мишени является внеклеточным, требует прямого межклеточного контакта и не включает комплемент. ADCC можно рассматривать как механизм, непосредственно вызывающий немедленную деструкцию опухоли различной степени, что приводит к презентации антигена и индукции Т-клеточного ответа, направленного против опухоли. Считается, что индукция ADCC in vivo приводит к ответу Т-клеток, направленному против опухоли, и ответу антител хозяина.
[00177] Способы проведения ADCC известны в данной области техники. Как правило, клетки-мишени, такие как клетки, экспрессирующие CLDN18.2, инкубируют с антителом против CLDN18.2 в диапазоне концентраций, и после промывания добавляют эффекторные клетки, такие как клетки, экспрессирующие рецептор Fc, чтобы обеспечить ADCC. Цитотоксичность или жизнеспособность клеток определяют в один момент времени через несколько часов после смешивания клеток-мишеней с эффекторными клетками для количественного определения уровня ADCC. Цитотоксичность можно обнаружить по высвобождению метки (например, радиоактивных субстратов, флуоресцентных красителей или природных внутриклеточных белков, таких как лактатдегидрогеназа (LDH)) из лизированных клеток-мишеней. В другом варианте жизнеспособность клеток определяют с помощью индикатора (такого как АТФ) метаболически активных клеток (см., например, Crouch, S.P. et al. (1993) J. Immunol. Methods 160, 81-8), с использованием репортерного гена люциферазы, который генерирует люминесцентный сигнал, пропорциональный количеству живых клеток в культуре (то есть анализ с использованием репортерного гена ADCC). Примерами эффекторных клеток являются NK-клетки, РВМС или FcγRIII-экспрессирующие клетки. В некоторых вариантах осуществления изобретения ADCC активность анти-CLDN18.2 антитела или его антигенсвязывающего фрагмента, предложенных в настоящем документе, определяют в соответствии со способами, описанными в разделе 2 примера 7.
[00178] «Комплемент-зависимая цитотоксичность» или «CDC» представляет собой другой метод уничтожения клеток, который может быть направлен антителами путем лизиса мишени в присутствии комплемента. IgM является наиболее эффективным изотипом для активации комплемента. IgG1 и IgG3 также очень эффективны в управлении CDC посредством классического пути активации комплемента. В этом каскаде образование комплексов антиген-антитело приводит к раскрытию множества сайтов связывания Clq в непосредственной близости от доменов CH2 участвующих молекул антител, таких как молекулы IgG (Clq является одним из трех субкомпонентов комплемента C1), связанных с родственным антиген. Эти незамаскированные сайты связывания Clq преобразуют ранее низкоаффинное взаимодействие Clq-IgG во взаимодействие с высокой авидностью, что запускает каскад событий с участием ряда других белков комплемента и приводит к протеолитическому высвобождению хемотаксических/активирующих агентов эффекторных клеток C3a. и С5а. Каскад комплемента заканчивается образованием мембраноатакующего комплекса (MAC), который создает поры в клеточной мембране, облегчающие свободный проход воды и растворенных веществ в клетку и из нее.
[00179] Активность CDC может быть определена способом, аналогичным методу ADCC-активности, как обсуждалось выше, за исключением того, что не используются эффекторные клетки, требуется присутствие комплемента, полученного из сыворотки человека. Вкратце, образцы антител серийно разводили в среде для анализа и инкубировали с клетками-мишенями, экспрессирующими CLDN18.2, в присутствии комплемента сыворотки человека. После инкубации цитотоксичность или жизнеспособность клеток определяют по высвобождению метки из лизированных клеток-мишеней или по индикатору (например, АТФ) метаболически активных клеток. Можно использовать реагент CellTiter-Glo, который анализирует АТФ в метаболически активных клетках, а степень лизиса клеток можно количественно определить путем измерения интенсивности люминесценции с помощью соответствующего ридера. В некоторых вариантах осуществления CDC-активность антитела против CLDN18.2 или его антигенсвязывающего фрагмента, предложенных в настоящем документе, определяют в соответствии со способами, описанными в разделе 1 примера 7.
[00180] В некоторых вариантах осуществления изобретения ADCC или CDC, индуцированные гибелью клеток с помощью антител против CLDN18.2 и их антигенсвязывающих фрагментов, представленных в настоящем документе, можно определить по потере целостности мембраны, оцениваемой по поглощению йодида пропидия (PI), трипанового синего (см. Moore et al. Cytotechnology 17:1-11 (1995)), или 7AAD можно оценивать относительно необработанных клеток.
[00181] Авторы изобретения неожиданно обнаружили, что анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, способны индуцировать ADCC, и/или CDC в клеточной линии человека со средним уровнем экспрессии CLDN18.2 (например, клетке NUGC4) или в клеточной линии человека с низким уровнем экспрессии CLDN18.2 (например, клетки SNU-620, SNU-601 и клетки KATOIII). Это отличается от существующих антител, таких как IMAB362, которые не могут индуцировать ADCC или CDC в такой линии клеток человека со средним или низким уровнем экспрессии CLDN18.2.
[00182] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, способны индуцировать комплемент-зависимую цитотоксичность (CDC) на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 1 мкг/мл (или не более чем 0,9, 0,8, 0,7, 0,6, 0,5 мкг/мл), как определено анализом цитотоксичности. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, способны индуцировать CDC на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, или 5% от такового для IMAB362, как определено анализом цитотоксичности. В некоторых вариантах осуществления изобретения CDC определяли с помощью клеточной линии со средним уровнем экспрессии CLDN18.2 человека или клеточной линии с высоким уровнем экспрессии CLDN18.2 человека.
[00183] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, способны индуцировать антителозависимую цитотоксичность (ADCC) на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 2 мкг/мл (или не более чем 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2 или 0,1 мкг/мл), как определено анализом с использованием репортерного гена ADCC. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, индуцируют ADCC на клетке, экспрессирующей CLDN18.2 человека при значении EC50 не более чем 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, 5%, или 1% от такового для IMAB362, или при общей емкости ADCC (например, как показано максимальным уровнем активности ADCC, наблюдаемым на графике зависимости концентрации антител от уровня активности ADCC) по меньшей мере 120%, 150%, 180%, или 200% от такового для IMAB362, как определено анализом с использованием репортерного гена ADCC. В некоторых вариантах осуществления изобретения ADCC определяют с помощью клеточной линии NUGC4, клеточной линии KATOIII, клеточной линии SNU-601, клеточной линии SNU-620 или их сопоставимых клеток, имеющих уровень экспрессии человеческого белка CLDN18.2, сравнимый или не превышающий уровень экспрессии клеточной линии NUGC4, клеточной линии KATOIII, клеточной линии SNU-601 или клеточной линии SNU-620, например, клеточной линии со средним уровнем экспрессии CLDN18.2 человека или клеточной линии с низким уровнем экспрессии CLDN18.2 человека.
[00184] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело и антигенсвязывающий фрагмент, предложенные в настоящем документе, способны индуцировать ADCC на клетках NUGC4 при значении EC50 не более чем 2 мкг/мл (или не более чем 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 1,0, 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2 или 0,1 мкг/мл) как определено анализом с использованием репортерного гена ADCC.
[00185] Эпитоп
[00186] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, связываются с эпитопом, содержащим по меньшей мере одну или несколько (например, один, два, три или более) аминокислотных остатков в положениях D28, W30, V43, N45, Y46, L49, W50, R51, R55, E56, F60, E62, Y66, L72, L76, V79 и R80 CLDN18.2 человека, имеющим аминокислотную последовательность SEQ ID NO: 30.
[00187] Термин «эпитоп», как используется в настоящем документе, относится к конкретной группе атомов или аминокислот на антигене, с которой связывается антитело. Эпитоп может включать определенные аминокислоты, боковые цепи сахаров, фосфорильные или сульфонильные группы, которые непосредственно контактируют с антителом. Специалистам в данной области понятно, что можно определить без излишнего экспериментирования, связывается ли антитело с тем же или перекрывающимся или соседним эпитопом, что и антитело по настоящему изобретению (например, гибридомные/химерные или гуманизированные антитела 7C12, 11F12, 26G6, 59A9, 18B10 и любые их химерные и гуманизированные варианты, представленные в настоящем документе), путем определения того, конкурируют ли они за связывание с антигенным полипептидом CLDN18.2.
[00188] Термин «конкурировать за связывание», как используется в настоящем документе, по отношению к двум антигенсвязывающим белкам (например, антителам), означает, что один антигенсвязывающий белок блокирует или снижает связывание другого с антигеном (например, CLDN18.2 человека/мыши), как определено анализом конкурентного связывания. Анализы конкурентного связывания хорошо известны в данной области и включают, например, прямой или непрямой радиоиммуноанализ (RIA), прямой или непрямой иммуноферментный анализ (EIA) и сэндвич-конкурентный анализ (см., например, Stahli et al., 1983, Methods in Enzymology 9:242-253). Как правило, такой анализ включает использование очищенного антигена, связанного с твердой поверхностью или клетками, несущими антиген, немеченого тестируемого антитела и меченого эталонного антитела. Конкурентное ингибирование измеряют путем определения количества метки, связанной с твердой поверхностью или клетками в присутствии тестируемого антитела. Обычно тестируемое антитело присутствует в избытке. Если два антитела конкурируют за связывание с CLDN18.2, то два антитела связываются с одним и тем же или перекрывающимся эпитопом или соседним эпитопом, достаточно проксимальным по отношению к эпитопу, связанному другим антителом, для возникновения стерических затруднений. Обычно, когда конкурирующее антитело присутствует в избытке, оно будет ингибировать (например, снижать) специфическое связывание тестируемого антитела с общим антигеном по крайней мере на 5 50-55%, 55-60%, 60-65%, 65-70%, 70-75% 75-80%, 80-85%, 85-90% или более.
[00189] В некоторых вариантах осуществления изобретения эпитоп или аминокислотный остаток в эпитопе, связанном с антителом, можно определить путем мутации определенных остатков в антигене, то есть CLDN18.2. Если антитело связывается с мутантным CLDN18.2, имеющим мутантный аминокислотный остаток, например, до аланина, на значительно сниженном уровне по сравнению с его связыванием с CLDN18.2 дикого типа, то это указывает на то, что мутантный остаток непосредственно участвует в связывание антитела с антигеном CLDN18.2 или находится в непосредственной близости от антитела, когда оно связано с антигеном. Считается, что такой мутантный остаток находится внутри эпитопа, и считается, что антитело специфически связывается с эпитопом, содержащим этот остаток. Значительно сниженный уровень связывания, как используется в настоящем документе, означает, что аффинность связывания (например, EC50, Kd или связывающая способность) между антителом и мутантным CLDN18.2 снижена более чем на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более по сравнению со связыванием между антителом и CLDN18.2 дикого типа. Такое измерение связывания можно проводить с использованием любых подходящих способов, известных в данной области техники и раскрытых в настоящем документе, например, без ограничения, анализа KinExA и проточной цитометрии.
[00190] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, демонстрируют значительно более низкое связывание с мутантным CLDN18.2, в котором остаток в CLDN18.2 дикого типа заменен аланином, и остаток выбран из группы, включающей: D28, W30, V43, N45, Y46, L49, W50, R51, R55, E56, F60, E62, Y66, L72, L76, V79 и R80 CLDN18.2 человека. В некоторых вариантах осуществления изобретения остаток представляет собой E56. В некоторых вариантах осуществления изобретения остаток выбран из группы, включающей: W30, L49, W50, R55 и E56. В некоторых вариантах осуществления изобретения остаток выбран из группы, включающей: T41, N45, Y46, R51, F60, E62 и R80. В некоторых вариантах осуществления изобретения остаток выбран из группы, включающей: D28, V43, N45, Y46, Y66, L72, L76 и V79.
[00191] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, демонстрируют по меньшей мере 80%, 90%, 95% или 99% или более снижение связывания мутантного CLDN18.2, содержащего E56A CLDN18.2 человека, по сравнению со связыванием между антителом и CLDN18.2 дикого типа.
[00192] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, демонстрируют по меньшей мере 50%, 60%, 70%, 80% или 90% снижение связывания мутантного CLDN18.2, содержащего один или несколько мутантных остатков, выбранных из группы, включающей: W30A, L49A, W50A, R55A и E56A CLDN18.2 человека, по сравнению со связыванием между антителом и CLDN18.2 дикого типа.
[00193] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, демонстрируют по меньшей мере 30%, 35%, 40%, 45% или 50% снижение связывания мутантного CLDN18.2, содержащего один или несколько мутантных остатков, выбранных из группы, включающей: D28, V43, N45, Y46, Y66, L72, L76 и V79 CLDN18.2 человека, по сравнению со связыванием между антителом и CLDN18.2 дикого типа.
[00194] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, демонстрируют по меньшей мере 10%, 15%, 20%, 25% или 30% снижение связывания мутантного CLDN18.2, содержащего одну или несколько мутантных остатков, выбранных из группы, включающей: T41A, N45A, Y46A, R51A, F60A, E62A и R80A CLDN18.2 человека, по сравнению со связыванием между антителом и CLDN18.2 дикого типа.
[00195] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, не связываются с A42 и/или N45.
[00196] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, способны связываться с эпитопом, предложенным в настоящем документе, и индуцировать активность ADCC или CDC в клеточной линии со средним уровнем экспрессии CLDN18.2 человека или в клеточной линии с низким уровнем экспрессии CLDN18.2 человека.
[00197] Последовательности антител
[00198] В другом аспекте в настоящем изобретении предложены анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, содержащие последовательности тяжелых цепей HCDR1, HCDR2 и HCDR3 и/или легких цепей LCDR1, LCDR2 и LCDR3, где
последовательность HCDR1 содержит GYNMN (SEQ ID NO: 1), или TYFIGVG (SEQ ID NO: 13), или гомологическую последовательность с по меньшей мере 80%-ной идентичностью последовательностей;
последовательность HCDR2 содержит X1IDPYYX2X3TX4YNQKFX5G (SEQ ID NO: 32), или HIWWNDNKYYNTALKS (SEQ ID NO: 15), или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей;
последовательность HCDR3 содержит X6X7X8GNAFDY (SEQ ID NO: 33), или MGSGAWFTY (SEQ ID NO: 17), или гомологическую последовательность с по меньшей мере 80%-ной идентичностью последовательностей;
последовательность LCDR1 содержит KSSQX9LX10NX11GNX12KNYLT (SEQ ID NO: 34) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей;
последовательность LCDR2 содержит WASTRX13S (SEQ ID NO: 35) или гомологическую последовательность с по меньшей мере 80%-ной идентичностью последовательностей; и
последовательность LCDR3 содержит QNDYX14X15PX16T (SEQ ID NO: 36) или гомологическую последовательность с по меньшей мере 80%-ной идентичностью последовательностей;
где X1 представляет собой N или Y или H, X2 представляет собой G или V, X3 представляет собой A или G или T, X4 представляет собой R или T или S, X5 представляет собой K или R, X6 представляет собой S или M, X7 представляет собой Y или F, X8 представляет собой Y или H, X9 представляет собой S или N, X10 представляет собой L или F, X11 представляет собой S или N, X12 представляет собой Q или L, X13 представляет собой E или K, X14 представляет собой S или Y, X15 представляет собой F или Y и X16 представляет собой F или L.
[00199] В одном аспекте в настоящем изобретении предложено анти-CLDN18.2 или его антигенсвязывающий фрагмент, представленные в настоящем документе, где вариабельная область тяжелой цепи содержит:
a) HCDR1 содержит последовательность, выбранную из SEQ ID NO: 1 и SEQ ID NO: 13,
b) HCDR2 содержит последовательность, выбранную из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 15, SEQ ID NO: 19 и SEQ ID NO: 22, и
c) HCDR3 содержит последовательность, выбранную из SEQ ID NO: 5, SEQ ID NO: 11, SEQ ID NO: 17 и SEQ ID NO: 21, и/или
вариабельную область легкой цепи, содержащую:
d) LCDR1 содержит последовательность SEQ ID NO: 2, SEQ ID NO: 10, SEQ ID NO: 14 и SEQ ID NO: 20,
e) LCDR2 содержит последовательность SEQ ID NO: 4 и SEQ ID NO: 16, и
f) LCDR3 содержит последовательность, выбранную из SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 12 и SEQ ID NO: 18.
[00200] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где вариабельная область тяжелой цепи выбрана из группы, включающей:
a) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 3, и HCDR3, содержащую последовательность SEQ ID NO: 5;
b) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 7, и HCDR3, содержащую последовательность SEQ ID NO: 5;
c) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 9, и HCDR3, содержащую последовательность SEQ ID NO: 11;
d) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 13, HCDR2, содержащую последовательность SEQ ID NO: 15, и HCDR3, содержащую последовательность SEQ ID NO: 17;
e) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 19, и HCDR3, содержащую последовательность SEQ ID NO: 21; и
f) вариабельную область тяжелой цепи, содержащую HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 22, и HCDR3, содержащую последовательность SEQ ID NO: 5.
[00201] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где вариабельная область легкой цепи выбрана из группы, включающей:
a) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
b) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 8;
c) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 10, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
d) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 12;
e) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 14, LCDR2, содержащую последовательность SEQ ID NO: 16, и LCDR3, содержащую последовательность SEQ ID NO: 18; и
f) вариабельную область легкой цепи, содержащую LCDR1, содержащую последовательность SEQ ID NO: 20, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6.
[00202] В некоторых вариантах осуществления изобретения в настоящем документе предложены антитело или его антигенсвязывающий фрагмент, где:
a) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 3, и HCDR3, содержащую последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
b) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 7, и HCDR3, содержащую последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 8;
c) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 9, и HCDR3, содержащую последовательность SEQ ID NO: 11; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 10, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6;
d) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 13, HCDR2, содержащую последовательность SEQ ID NO: 15, и HCDR3, содержащую последовательность SEQ ID NO: 17; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 2, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 12;
e) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 19, и HCDR3, содержащую последовательность SEQ ID NO: 21; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 14, LCDR2, содержащую последовательность SEQ ID NO: 16, и LCDR3, содержащую последовательность SEQ ID NO: 18; или
f) вариабельная область тяжелой цепи содержит HCDR1, содержащую последовательность SEQ ID NO: 1, HCDR2, содержащую последовательность SEQ ID NO: 22, и HCDR3, содержащую последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит LCDR1, содержащую последовательность SEQ ID NO: 20, LCDR2, содержащую последовательность SEQ ID NO: 4, и LCDR3, содержащую последовательность SEQ ID NO: 6.
[00203] В некоторых вариантах осуществления изобретения антитела, предложенные в настоящем документе, содержат одну или несколько (например, 1, 2, 3, 4, 5, или 6) последовательностей CDR CLDN18.2 антител 7C12, 11F12, 26G6, 59A9, 18B10 и 12E9.
[00204] «7C12», как используется в настоящем документе, относится к мышиному антителу, имеющему вариабельную область тяжелой цепи SEQ ID NO: 37 и вариабельную область легкой цепи SEQ ID NO: 38.
[00205] «11F12», как используется в настоящем документе, относится к мышиному антителу, имеющему вариабельную область тяжелой цепи SEQ ID NO: 39, и вариабельную область легкой цепи SEQ ID NO: 40.
[00206] «26G6», как используется в настоящем документе, относится к мышиному антителу, имеющему вариабельную область тяжелой цепи SEQ ID NO: 41, и вариабельную область легкой цепи SEQ ID NO: 42.
[00207] «59A9», как используется в настоящем документе, относится к мышиному антителу, имеющему вариабельную область тяжелой цепи SEQ ID NO: 43, и вариабельную область легкой цепи SEQ ID NO: 44.
[00208] «18B10», как используется в настоящем документе, относится к мышиному антителу, имеющему вариабельную область тяжелой цепи SEQ ID NO: 45, и вариабельную область легкой цепи SEQ ID NO: 46.
[00209] «12E9», как используется в настоящем документе, относится к мышиному антителу, имеющему вариабельную область тяжелой цепи SEQ ID NO: 47, и вариабельную область легкой цепи SEQ ID NO: 48.
[00210] В Таблице 1 показаны последовательности CDR этих антител CLDN18.2. Последовательности вариабельных областей тяжелой цепи и легкой цепи также представлены ниже в таблице 2.
[00211] Таблица 1. Последовательности области CDR антител CLDN18.2
[00212] Таблица 2. Последовательности мышиного/химерного антитела VH/VL
EFQLQQSGPELEKPGASVRISCKTSGYSFTGYNMNWVKQSNGESLEWIGNIDPYYGGTRYNQKFKGKATLTVDKSSSTAYMQLKSLTSEDSAVYYCARSYYGNAFDYWGQGTTLTVSS
DIVMTQSPSSLTVTAGEKVTMSCKSSQNLLNNGNQKNYLTWYQQKPGQPPKLLIYWASTRESGVPDRFTGSGSGTDFILTISSVQAEDLAVYYCQNDYSFPFTFGAGTKLELK
[00213] Анти-CLDN18.2 антитела или их антигенсвязывающие фрагменты, предложенные в настоящем документе, могут представлять собой моноклональное антитело, поликлональное антитело, гуманизированное антитело, химерное антитело, рекомбинантное антитело, биспецифическое антитело, меченое антитело, бивалентное антитело или антиидиотипическое антитело. Рекомбинантное антитело представляет собой антитело, полученное in vitro с использованием рекомбинантных методов, а не на животных.
[00214] Известно, что CDR ответственны за связывание антигена, однако было обнаружено, что не все из 6 CDR обязательно незаменимы или неизменны. Другими словами, можно заменить, изменить или модифицировать 1, 2 или 3 CDR в анти-CLDN18.2 антителах 7C12, 11F12, 26G6, 59A9, 18B10 или 12E9 (соответствует любой из SEQ ID NO: 1-22), но в значительной степени сохраняют аффинность специфического связывания с CLDN18.2.
[00215] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, содержат последовательность CDR3 тяжелой цепи одного из анти-CLDN18.2 антител 7C12, 11F12, 26G6, 59A9, 18B10 или 12E9. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, содержат последовательность CDR3 тяжелой цепи SEQ ID NO: 5, 11, 17 и 21. Области CDR3 тяжелой цепи расположены в центре сайта связывания антигена, и поэтому считается, что они в наибольшей степени контактируют с антигеном и обеспечивают наибольшую свободную энергию для аффинности антитела к антигену. Также считается, что CDR3 тяжелой цепи представляет собой наиболее разнообразный CDR сайта связывания антигена с точки зрения длины, аминокислотного состава и конформации за счет множественных механизмов диверсификации (Tonegawa S. Nature. 302:575-81). Разнообразия в CDR3 тяжелой цепи достаточно для обеспечения большей специфичности антител (Xu JL, Davis MM. Immunity. 13:37-45), а также желаемой антигенсвязывающей аффинности (Schier R, etc. J Mol Biol. 263:551-67).
[00216] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, содержат весь или часть вариабельного домена тяжелой цепи и/или весь или часть вариабельного домена легкой цепи. В одном варианте осуществления изобретения анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, представляют собой однодоменное антитело, которое состоит из всего или части вариабельного домена тяжелой цепи, предложенное в настоящем документе. Дополнительная информация о таком однодоменном антителе доступна в данной области (см., например, патент США № 6248516).
[00217] В некоторых вариантах осуществления изобретения антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, содержат подходящие последовательности каркасной области (FR), при условии, что антитела и их антигенсвязывающие фрагменты могут специфически связываться с CLDN18.2. Последовательности CDR, представленные в таблице 1, получены из мышиных антител, но они могут быть привиты к любым подходящим последовательностям FR любых подходящих видов, таких как мышь, человек, крыса, кролик, среди прочих, с использованием подходящих способов, известных в данной области, таких как рекомбинантный методы.
[00218] В некоторых вариантах осуществления изобретения антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, являются гуманизированными. Гуманизированное антитело или антигенсвязывающий фрагмент являются желательными из-за их пониженной иммуногенности у человека. Гуманизированное антитело является химерным в своих вариабельных областях, поскольку нечеловеческие последовательности CDR привиты к человеческим или по существу человеческим последовательностям FR. Гуманизацию антитела или его антигенсвязывающего фрагмента можно по существу осуществить путем замены генов CDR нечеловеческого происхождения (например, мышиных) на соответствующие гены CDR человека в гене человеческого иммуноглобулина (см., например, Jones et al. (1986) Nature 321:522-525; Riechmann et al. (1988) Nature 332:323-327; Verhoeyen et al. (1988) Science 239:1534-1536).
[00219] Подходящие вариабельные домены тяжелой и легкой цепей человека могут быть выбраны для достижения этой цели с использованием способов, известных в данной области. В иллюстративном примере можно использовать подход «наилучшего соответствия», когда последовательность вариабельного домена антитела не человека (например, грызуна) подвергается скринингу или BLAST против базы данных известных последовательностей зародышевой линии вариабельного домена человека, и последовательность человека, наиболее близкая к запрашиваемой последовательности, отличной от человека, идентифицируется и используется в качестве каркаса человека для прививки последовательностей CDR, не принадлежащих человеку (см., например, Sims et al. (1993) J. Immunol. 151:2296; Chothia et al. (1987) J. Mot. Biol. 196:901). Альтернативно, каркас, полученный из консенсусной последовательности всех антител человека, можно использовать для наращивания CDR, не принадлежащих человеку (см., например, Carter et al. (1992) Proc. Natl. Acad. Sci. USA, 89:4285; Presta et al. (1993) J. Immunol., 151:2623).
[00220] В некоторых вариантах осуществления изобретения гуманизированное антитела или антигенсвязывающие фрагменты, предложенные в настоящем документе, состоят практически из всех последовательностей человека, за исключением последовательностей CDR, которые не принадлежат человеку. В некоторых вариантах осуществления изобретения FR вариабельной области и константные области, если они присутствуют, полностью или по существу происходят из последовательностей иммуноглобулина человека. Последовательности FR человека и последовательности константной области человека могут быть получены из разных генов иммуноглобулина человека, например, последовательности FR получены из одного антитела человека, а последовательности константной области - из другого антитела человека. В некоторых вариантах осуществления изобретения гуманизированное антитело или антигенсвязывающий фрагмент содержат FR1-4 тяжелой/легкой цепи человека.
[00221] В некоторых вариантах осуществления изобретения области FR, полученные от человека, могут содержать ту же аминокислотную последовательность, что и иммуноглобулин человека, из которого они получены. В некоторых вариантах осуществления изобретения один или несколько аминокислотных остатков FR человека замещены соответствующими остатками исходного нечеловеческого антитела. В некоторых вариантах осуществления может быть желательным сделать гуманизированное антитело или его фрагмент максимально приближенным к структуре родительского антитела нечеловеческого происхождения, чтобы уменьшить или избежать иммуногенности и/или улучшить или сохранить активность связывания или аффинность связывания.
[00222] В некоторых вариантах осуществления изобретения гуманизированное антитело или антигенсвязывающий фрагмент, предложенные в настоящем документе, содержат не более чем 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 замен аминокислотных остатков в каждой из последовательностей FR человека, или не более чем 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 замен аминокислотных остатков во всех FR вариабельного домена тяжелой или легкой цепи. В некоторых вариантах осуществления изобретения такое изменение аминокислотного остатка может присутствовать только в FR-областях тяжелой цепи, только в FR-областях легкой цепи или в обеих цепях. В некоторых вариантах осуществления изобретения один или несколько аминокислотных остатков мутированы, например, обратно мутированы до соответствующего остатка, обнаруженного в нечеловеческом исходном антителе (например, в мышиной каркасной области), из которого получены последовательности CDR. Подходящие положения для мутаций могут быть выбраны специалистом в данной области в соответствии с принципами, известными в данной области. Например, положение для мутации может быть выбрано, когда: 1) остаток в каркасе последовательности зародышевой линии человека встречается редко (например, менее чем в 20% или менее чем в 10% в последовательности вариабельной области человека); 2) положение непосредственно примыкает к одному или нескольким из 3 CDR в первичной последовательности цепи зародышевой линии человека, поскольку оно, вероятно, взаимодействует с остатками в CDR; или 3) положение близко к CDR в 3-мерной модели и, следовательно, может иметь хорошую вероятность взаимодействия с аминокислотами в CDR. Остаток в выбранном положении может быть мутирован обратно в соответствующий остаток в исходном антителе или в остаток, который не является соответствующим остатком ни в последовательности зародышевой линии человека, ни в исходном антителе, а в остаток, типичный для последовательностей человека, то есть который чаще встречается в этом положении в известных последовательностях человека, принадлежащая к той же подгруппе, что и последовательность зародышевой линии человека (см. патент США № 5693762).
[00223] В некоторых вариантах осуществления изобретения гуманизированные легкие и тяжелые цепи по настоящему изобретению являются по существу неиммуногенными для человека и сохраняют по существу такую же аффинность или даже более высокую аффинность, чем исходное антитело к CLDN18.2.
[00224] В некоторых вариантах осуществления изобретения гуманизированные антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, содержат одну или несколько последовательностей FR легкой цепи каркасной последовательности VK/4-1 зародышевой линии человека и/или одну или несколько последовательностей FR тяжелой цепи зародышевой линии человека каркасная последовательность VH/1-46, без или без обратных мутаций. При необходимости в каркасную последовательность зародышевой линии человека могут быть введены обратные мутации. В некоторых вариантах осуществления изобретения гуманизированное антитело 18B10 может содержать одну или несколько обратных мутаций, выбранных из группы, включающей: R71I, T73K, T28S, M69L, R38K и M48I, все на основе нумерации Kabat, в последовательности каркаса тяжелой цепи VH/1-46. Гуманизированное антитело 18B10 может содержать одну или несколько обратных мутаций, выбранных из группы, включающей: S63T и I21M, все основанные на нумерации Kabat, в последовательности каркаса легкой цепи VK/4-1.
[00225] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, содержат вариабельную область тяжелой цепи, содержащую последовательность, выбранную из группы, включающей SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 29, SEQ ID NO: 37, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 43, SEQ ID NO: 45 и SEQ ID NO: 47, и ее гомологичную последовательность с по меньшей мере 80%-ной (например, по меньшей мере 85%, 90%, 95%, 96%, 97%, 98% или 99%) идентичностью последовательностей, сохраняя при этом аффинность специфического связывания с CLDN18.2, в частности, CLDN18.2 человека.
[00226] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, антитело или его антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, содержащую последовательность, выбранную из группы, включающей SEQ ID NO: 26, SEQ ID NO: 28, SEQ ID NO: 38, SEQ ID NO: 40, SEQ ID NO: 42, SEQ ID NO: 44, SEQ ID NO: 46, SEQ ID NO: 48, и ее гомологичную последовательность с по меньшей мере 80%-ной (например, по меньшей мере 85%, 90%, 95%, 96%, 97%, 98% или 99%) идентичностью последовательностей, сохраняя при этом аффинность специфического связывания с CLDN18.2, в частности, CLDN18.2 человека.
[00227] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, включают:
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 25 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 26;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 27 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 28;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 29 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 26, или 28;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 37 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 38;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 39 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 40;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 41 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 42;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 43 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 44;
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 45 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 46; или
вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 47 и вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 48.
[00228] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, дополнительно содержит одну или несколько тяжелых цепей HFR1, HFR2, HFR3 и HFR4, и/или одну или несколько легких цепей LFR1, LFR2, LFR3 и LFR4, где:
HFR1 содержит QVQLVQSGAEVKKPGASVKVSCKASGYX17FT (SEQ ID NO: 54) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей,
HFR2 содержит WVX18QAPGQGLEWX19G (SEQ ID NO: 55) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 90%) идентичностью последовательностей,
HFR3 содержит RVTX20TIDKSTSTVYMELSSLRSEDTAVYYCAR (SEQ ID NO: 56) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей,
HFR4 содержит WGQGTTVTVSS (SEQ ID NO: 57) или гомологическую последовательность с по меньшей мере 80%-ной-ной идентичностью последовательностей,
LFR1 содержит DIVMTQSPDSLAVSLGERATX21NC (SEQ ID NO: 58) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей,
LFR2 содержит WYQQKPGQPPKLLIY (SEQ ID NO: 59) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%) идентичностью последовательностей,
LFR3 содержит GVPDRFX22GSGSGTDFTLTISSLQAEDVAVYYC (SEQ ID NO: 60) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 85%, 90%, 95%) идентичностью последовательностей, и
LFR4 содержит FGGGTKVEIK (SEQ ID NO: 61) или гомологическую последовательность с по меньшей мере 80%-ной (или по меньшей мере 90%) идентичностью последовательностей,
где X17 представляет собой T или S, X18 представляет собой R или K, X19 представляет собой M или I, X20 представляет собой M или L, X21 представляет собой I или M, и X22 представляет собой S или T.
[00229] В некоторых вариантах осуществления изобретения HFR1 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 62 и 63, HFR2 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 64 и 65, HFR3 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 66 и 67, HFR4 содержит последовательность SEQ ID NO: 57, LFR1 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 68 и 69, LFR2 содержит последовательность SEQ ID NO: 59, LFR3 содержит последовательность, выбранную из группы, включающей SEQ ID NO: 70 и 71, и LFR4 содержит последовательность SEQ ID NO: 61.
[00230] Таблица 3-1. Каркасные (FR) последовательности гуманизированных CLDN18.2 антител 18B10
[00231] Таблица 3-2 иллюстрирует последовательности вариабельных областей гуманизированных антител 18B10.
[00232] Таблица 3-2. Последовательности гуманизированного 18B10
[00233] В некоторых вариантах осуществления изобретения гуманизированное антитела, предложенные в настоящем документе, могут содержать вариабельную область тяжелой цепи, слитую с константной областью изотипа IgG1 человека, и вариабельную область легкой цепи, слитую с константной областью каппа-цепи человека.
[00234] Гуманизированные анти-CLDN18.2 антитела, предложенные в настоящем документе, сохраняли аффинность специфического связывания с клетками, экспрессирующими CLDN18.2, и в этом аспекте по меньшей мере сравнимы с исходными антителами или даже превосходят их. Гуманизированные антитела, предложенные в настоящем документе, также могут сохранять свое функциональное взаимодействие с клетками, экспрессирующими CLDN18.2, такими как клетки NUGC4, клетки SNU-620, клетки SNU-601 или клетки KATOIII, поскольку все антитела могут опосредовать уничтожение клеток с помощью ADCC, CDC и индукцию апоптоза, вызванного поперечным связыванием мишени на поверхности опухолевых клеток и прямым ингибированием пролиферации. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, содержат константную область иммуноглобулина, необязательно константную область Ig человека или необязательно константную область IgG человека. В некоторых вариантах осуществления изобретения константная область иммуноглобулина содержит константную область тяжелой цепи и/или легкой цепи. Константная область тяжелой цепи включает области СН1, шарнирную область и/или области СН2-СН3. В некоторых вариантах осуществления изобретения константная область тяжелой цепи содержит Fc-область. В некоторых вариантах осуществления изобретения константная область легкой цепи содержит Cκ или Cλ.
[00235] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их фрагменты, предложенные в настоящем документе, дополнительно содержат константную область IgG1, IgG2, IgG3 или IgG4 человека. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, содержат константную область изотипа IgG1. В некоторых вариантах осуществления изобретения константная область IgG1 человека содержит SEQ ID NO: 49, или гомологичную последовательность, содержащую по меньшей мере 80% (например, по меньшей мере 85%, 90%, 95%, 96%, 97%, 98%, или 99%) идентичностью последовательностей.
[00236] Константная область изотипа IgG1 может индуцировать эффекторные функции, такие как ADCC или CDC. Эффекторные функции анти-CLDN18.2 антител и их антигенсвязывающих фрагментов, предложенных в настоящем документе, могут приводить к цитотоксичности в отношении клеток, экспрессирующих CLDN18.2. Эффекторные функции можно оценить с помощью различных анализов, таких как анализ связывания Fc-рецептора, анализ связывания C1q и анализ лизиса клеток, а также любого из описанных выше анализов для определения ADCC или CDC.
[00237] Варианты антител
[00238] Анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, также охватывают различные типы вариантов последовательностей антител, представленных в настоящем документе.
[00239] В некоторых вариантах осуществления изобретения варианты содержат одну или несколько модификаций или замен в 1, 2 или 3 последовательностях CDR, как представлено в таблице 1, в одной или нескольких последовательностях FR, в последовательностях вариабельной области тяжелой или легкой цепи, представленных в настоящем документе, и/или в константной области (например, Fc-области). Такие варианты антител сохраняют аффинность специфического связывания с CLDN18.2 своих исходных антител, но обладают одним или несколькими желательными свойствами, придаваемыми модификацией(ями) или заменой(ами). Например, варианты антител могут обладать улучшенной антигенсвязывающей аффинностью, улучшенным характером гликозилирования, сниженным риском гликозилирования, сниженным дезаминированием, сниженной или повышенной эффекторной(ыми) функцией(ями), улучшенным связыванием с рецептором FcRn, увеличенным фармакокинетическим периодом полужизни, чувствительностью к рН и/или совместимостью с конъюгацией (например, одним или несколькими введенными остатками цистеина), и это лишь некоторые из них.
[00240] Последовательность исходного антитела может быть подвергнута скринингу для идентификации подходящих или предпочтительных остатков, подлежащих модификации или замене, с использованием методов, известных в данной области техники, например, «сканирующим аланином мутагенезом» (см., например, Cunningham and Wells (1989) Science, 244:1081-1085). Короче, остатки-мишени (например, заряженные остатки, такие как Arg, Asp, His, Lys и Glu) могут быть идентифицированы и заменены нейтральной или отрицательно заряженной аминокислотой (например, аланином или полиаланином), после чего получают модифицированные антитела и подвергают скринингу на интересующие свойство. Если замена в определенном аминокислотном положении демонстрирует интересующее функциональное изменение, то это положение может быть идентифицировано как потенциальный остаток для модификации или замены. Потенциальные остатки можно дополнительно оценить путем замены остатком другого типа (например, цистеиновым остатком, положительно заряженным остатком и т.д.).
1. Вариант аффинности
[00241] Вариант аффинности сохраняет аффинность специфического связывания с CLDN18.2 исходного антитела или даже обладает улучшенной аффинностью специфического связывания с CLDN18.2 по сравнению с исходным антителом. Для достижения этой цели можно использовать различные способы, известные в данной области техники. Например, библиотека вариантов антител (таких как варианты Fab или scFv) может быть создана и экспрессирована с помощью технологии фагового дисплея, а затем проверена на аффинность связывания с CLDN18.2 человека. В качестве другого примера можно использовать компьютерное программное обеспечение для виртуального моделирования связывания антител с CLDN18.2 человека и идентификации аминокислотных остатков на антителах, которые образуют интерфейс связывания. Таких остатков можно либо избегать при замене, чтобы предотвратить снижение аффинности связывания, либо нацеливаться на замену, чтобы обеспечить более сильное связывание.
[00242] В некоторых вариантах осуществления изобретения по меньшей мере одна (или все) замена(и) в последовательностях CDR, последовательностях FR или последовательностях вариабельной области содержит консервативную замену. «Консервативная замена» по отношению к аминокислотной последовательности относится к замене аминокислотного остатка другим аминокислотным остатком, имеющим боковую цепь со сходными физико-химическими свойствами. Например, консервативные замены могут быть сделаны среди аминокислотных остатков с гидрофобными боковыми цепями (например, Met, Ala, Val, Leu и Ile), среди остатков с нейтральными гидрофильными боковыми цепями (например, Cys, Ser, Thr, Asn и Gln), среди остатков с кислотными боковыми цепями (например, Asp, Glu), среди аминокислот с основными боковыми цепями (например, His, Lys и Arg) или среди остатков с ароматическими боковыми цепями (например, Trp, Tyr и Phe) Как известно специалистам, консервативная замена обычно не вызывает существенного изменения конформационной структуры белка и, следовательно, может сохранять биологическую активность белка.
[00243] В некоторых вариантах осуществления изобретения антитело или антигенсвязывающий фрагмент, предложенные в настоящем документе, содержит одну или несколько замен аминокислотных остатков в одной или нескольких последовательностях CDR последовательности, и/или одной или нескольких последовательностях FR. В некоторых вариантах осуществления изобретения вариант аффинности содержит не более чем 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 замены в одной или нескольких последовательностях CDR и/или последовательностях FR в целом.
[00244] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты содержат 1, 2 или 3 последовательности CDR с по меньшей мере 80%-ной (например, по меньшей мере 85%, 88%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%) идентичности последовательности с той (или теми), которые перечислены в таблице 1, и при этом сохраняют аффинность связывания с CLDN18.2 на уровне аналогичен или даже выше, чем его родительское антитело.
[00245] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты содержат одну или несколько вариабельных областей последовательности с по меньшей мере 80%-ной (например, по меньшей мере 85%, 88%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%) идентичностью последовательностей с той (или теми) SEQ ID NO: 23-29 и 37-48, и при этом сохраняют аффинность связывания с CLDN18.2 на уровне, аналогичном или даже превышающем уровень исходного антитела. В некоторых вариантах осуществления изобретения в последовательности, выбранной из SEQ ID NO: 25-29 и 37-48, были заменены, вставлены или делетированы в общей сложности от 1 до 10 аминокислот. В некоторых вариантах осуществления замены, вставки или делеции происходят в областях за пределами CDR (то есть в FR).
2. Вариант гликозилирования
[00246] Анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, также охватывают вариант гликозилирования, который может быть получен либо для увеличения, либо для уменьшения степени гликозилирования антитела или антигенсвязывающего фрагмента. Термин «гликозилирование», как используется в настоящем документе, относится к ферментативному процессу, при котором гликаны, такие как фукоза, ксилоза, манноза или фосфосерингликан GlcNAc, присоединяются к белкам, липидам или другим органическим молекулам. В зависимости от углерода, связанного с гликаном, гликозилирование можно разделить на пять классов, включая: N-гликозилирование, O-гликозилирование, фосфогликозилирование, C-гликозилирование и глипирование.
[00247] Гликозилирование антител обычно является N-связанным или O-связанным. N-связанное относится к присоединению углеводного фрагмента к боковой цепи остатка аспарагина, например, остатка аспарагина в трипептидной последовательности, такой как аспарагин-X-серин и аспарагин-X-треонин, где X представляет собой любую аминокислоту, кроме пролина. О-связанное гликозилирование относится к присоединению одного из сахаров N-ацеилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, чаще всего к серину или треонину.
[00248] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, охватывают вариант гликозилирования, обладающий улучшенными эффекторными функциями, такими как ADCC или CDC.
[00249] В некоторых вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, являются афукозилированными. Термин «афукозилирование» или «афукозилированные» относится к уменьшенной или элиминированной сердцевинной фукозе на N-гликане, присоединенном к антителу. Большинство гликанов человеческих антител IgG известны как G0, G1 и G2, которые представляют собой сложные биантеннарные молекулы с остатком фукозы в сердцевине, несущим ноль, одну или две концевые галактозы.
[00250] Варианты афукозилированных антител могут быть получены с использованием способов, известных в данной области, например, как описано в US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO2005/053742; WO2002/031140; Okazaki et al. J. Mol. Biol. 336:1239-1249 (2004); Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004).
[00251] В некоторых вариантах осуществления изобретения вариант гликозилирования антитело афукозилирован на участке Asn297 области CH2 в Fc антитела. Asn297 относится к остатку аспарагина, расположенному примерно в положении 297 в Fc-области (нумерация ЕС остатков Fc-области); однако Asn297 также может быть расположен примерно на ±3 аминокислоты выше или ниже положения 297, то есть между положениями 294 и 300, из-за незначительных вариаций последовательности в антителах.
[00252] В некоторых вариантах осуществления изобретения варианты гликозилирования антител могут быть получены, например, путем удаления нативного сайта гликозилирования (например, путем замены N297A), так что последовательности трипептидов для сайтов N-связанного гликозилирования или остатки серина или треонина для сайтов O-связанного гликозилирования больше не присутствуют в последовательности антитела или Fc. Альтернативно, в некоторых вариантах осуществления варианты гликозилирования антитела могут быть получены путем продуцирования антитела в линии клеток-хозяев, дефектных по добавлению выбранной(ых) сахарной(ых) группы(групп) к зрелой сердцевинной углеводной структуре в антителе.
3. Вариант, сконструированный с цистеином
[00253] Анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, также охватывают вариант, сконструированный с цистеином, который содержит один или несколько введенных аминокислотных остатков свободного цистеина.
[00254] Свободный остаток цистеина представляет собой остаток, который не является частью дисульфидного мостика. Вариант, сконструированный с цистеином, может использоваться для конъюгации, например, с цитотоксическим и/или визуализирующим соединением, меткой или радиоактивным изотипом, среди прочего, на участке сконструированного цистеина, например, через малеимид или галоацетил. Способы конструирования антител или антигенсвязывающих фрагментов для введения свободных остатков цистеина известны в данной области, см., например, WO2006/034488.
4. Варианты Fc
[00255] Анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, также охватывают вариант Fc, который включает одну или несколько модификаций или замен аминокислотных остатков в своей Fc-области и/или шарнирной области.
[00256] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела или их антигенсвязывающие фрагменты содержат константную область, содержащую одну или несколько замен или модификаций аминокислотных остатков, придающих повышенную CDC или ADCC по сравнению с константной областью дикого типа. Некоторые аминокислотные остатки в домене CH2 Fc-области могут быть заменены для обеспечения повышенной активности ADCC, например, путем повышения аффинности Fc-домена к FcγRIIIA. Способы изменения активности ADCC с помощью инженерии антител описаны в данной области, см., например, Shields RL. et al., J Biol Chem. 2001. 276(9): 6591-604; Idusogie EE. et al., J Immunol. 2000.164(8):4178-84; Steurer W. et al., J Immunol. 1995, 155(3): 1165- 74; Idusogie EE. et al., J Immunol. 2001, 166(4): 2571-5; Lazar GA. et al., PNAS, 2006, 103(11): 4005-4010; Ryan MC. et al., Mol. Cancer Ther., 2007, 6: 3009-3018; Richards JO,. et al., Mol Cancer Ther. 2008, 7(8): 2517-27; Shields R. L. et al. J. Biol. Chem, 2002, 277: 26733-26740; Shinkawa T. et al. J. Biol. Chem, 2003, 278: 3466-3473.
[00257] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела или антигенсвязывающие фрагменты содержат одну или несколько аминокислотных замен, которые изменяют комплемент-зависимую цитотоксичность (CDC), например, улучшая или уменьшая связывание C1q и/или комплемент-зависимую цитотоксичность (CDC) (см., например, WO99/51642; Duncan & Winter Nature 322:738-40 (1988); патент США № 5648260; патент США № 5624821; и WO94/29351 в отношении других примеров вариантов Fc-области).
[00258] В некоторых вариантах осуществления изобретения константная область антител или их антигенсвязывающих фрагментов, представленных в настоящем документе, содержит одну или несколько замен аминокислотных остатков относительно SEQ ID NO: 49 (то есть последовательности дикого типа), выбранных из группы, включающей: L235V, F243L, R292P, Y300L, P396L или любую их комбинацию. В некоторых вариантах осуществления изобретения константная область содержит последовательность SEQ ID NO: 51.
[00259] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела или антигенсвязывающие фрагменты содержат одну или несколько минокислотных замен, которые улучшают pH-зависимое связывание с неонатальным Fc-рецептором (FcRn). Такой вариант может иметь увеличенный фармакокинетический период полужизни, поскольку он связывается с FcRn при кислом рН, что позволяет ему избежать деградации в лизосоме, а затем перемещаться и высвобождаться из клетки. Способы конструирования антитела и его антигенсвязывающего фрагмента для улучшения аффинности связывания с FcRn хорошо известны в данной области, см., например, Vaughn, D. et al. Structure, 6(1): 63-73, 1998; Kontermann, R. et al. Antibody Engineering, Volume 1, Chapter 27: Engineering of the Fc region for improved PK, published by Springer, 2010; Yeung, Y. et al. Cancer Research, 70: 3269-3277 (2010); и Hinton, P. et al. J. Immunology, 176:346-356 (2006).
[00260] Антигенсвязывающие фрагменты
[00261] В настоящем документе предложены также анти-CLDN18.2 антигенсвязывающие фрагменты. В данной области техники известны различные типы антигенсвязывающих фрагментов, и их можно разработать на основе анти-CLDN18.2 антител, предложенных в настоящем документе, включая, например, типичные антитела, последовательности CDR которых показаны в таблицах 1, и их различные варианты (такие как как аффинные варианты, варианты гликозилирования, варианты Fc, варианты с модифицированным цистеином и так далее).
[00262] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антигенсвязывающий фрагмент, предложенный в настоящем документе, представляет собой диатело, Fab, Fab', F(ab')2, Fd, фрагмент Fv, стабилизированный дисульфидом фрагмент Fv (dsFv), (dsFv)2, биспецифический dsFv (dsFv-dsFv'), дисульфид-стабилизированное диатело (ds диатело), молекулу одноцепочечного антитела (scFv), димер scFv (бивалентное диатело), полиспецифическое антитело, верблюжье однодоменное антитело, нанотело, доменное антитело или бивалентное доменное антитело.
[00263] Для получения таких антигенсвязывающих фрагментов можно использовать различные методики. Иллюстративные способы включают ферментативное расщепление интактных антител (см., например, Morimoto et al., Journal of Biochemical and Biophysical Methods 24:107-117 (1992); и Brennan et al., Science, 229:81 (1985)), рекомбинантную экспрессию клетками-хозяевами, такими как E. Coli (например, для фрагментов антител Fab, Fv и ScFv), скрининг из библиотеки фагового дисплея, как обсуждалось выше (например, для ScFv), и химическое связывание двух фрагментов Fab'-SH с образованием фрагментов F(ab')2 (Carter et al., Bio/Technology 10:163-167 (1992)). Специалисту в данной области техники будут очевидны и другие способы получения фрагментов антител.
[00264] В некоторых вариантах осуществления изобретения антигенсвязывающий фрагмент представляет собой scFv. Создание scFv описано, например, в WO 93/16185; патентах США №№ 5571894 и 5587458. scFv может быть слит с эффекторным белком либо на амино-, либо на карбоксильном конце, чтобы получить слитый белок (см., например, Antibody Engineering, ed. Borrebaeck).
[00265] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, являются бивалентными, четырехвалентными, шестивалентными или поливалентными. Термин «валентный», как используется в настоящем документе, относится к наличию определенного количества антигенсвязывающих сайтов в данной молекуле. Как таковые, термины «бивалентный», «тетравалентный» и «шестивалентный» обозначают наличие двух сайтов связывания, четырех сайтов связывания и шести сайтов связывания, соответственно, в антигенсвязывающей молекуле. Любая молекула, являющаяся более чем бивалентной, считается поливалентной, включая, например, трехвалентную, четырехвалентную, шестивалентную и так далее.
[00266] Бивалентная молекула может быть моноспецифической, если оба сайта связывания специфичны для связывания с одним и тем же антигеном или одним и тем же эпитопом. В некоторых вариантах осуществления изобретения это обеспечивает более сильное связывание с антигеном или эпитопом, чем моновалентный аналог. Аналогично, поливалентная молекула также может быть моноспецифичной. В некоторых вариантах осуществления изобретения в бивалентном или поливалентном антигенсвязывающем фрагменте первая валентность сайта связывания и вторая валентность сайта связывания являются структурно идентичными (то есть имеющими одинаковые последовательности) или структурно разными (то есть имеющими разные последовательности, хотя и с одинаковой специфичностью).
[00267] Бивалентная молекула также может быть биспецифической, если два сайта связывания специфичны для разных антигенов или эпитопов. Это относится и к поливалентной молекуле. Например, трехвалентная молекула может быть биспецифичной, когда два сайта связывания моноспецифичны для первого антигена (или эпитопа), а третий сайт связывания специфичен для второго антигена (или эпитопа).
[00268] Биспецифические антитела
[00269] В некоторых вариантах осуществления изобретения антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, являются биспецифичными. Термин «биспецифическое», как используется в настоящем документе, включает молекулы, обладающие более чем двумя специфичностями, и молекулы, обладающие более чем двумя специфичностями, то есть мультиспецифические. В некоторых вариантах осуществления изобретения биспецифическое антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, способны специфически связываться с первым и вторым эпитопами CLDN18.2 или способны специфически связываться с CLDN18.2 и вторым антигеном. В некоторых вариантах осуществления изобретения первый эпитоп и второй эпитоп CLDN18.2 отличаются друг от друга или не перекрываются. В некоторых вариантах осуществления изобретения биспецифическое антитела и их антигенсвязывающие фрагменты могут одновременно связываться как с первым эпитопом, так и со вторым эпитопом. В некоторых вариантах осуществления изобретения второй антиген отличается от CLDN18.2.
[00270] В некоторых вариантах осуществления изобретения второй антиген представляет собой иммунологическую мишень. В некоторых вариантах осуществления изобретения биспецифическое антитела и их антигенсвязывающие фрагменты специфически связываются с CLDN18.2 и иммунологической мишенью, и способны нацеливать иммунные клетки на экспрессирующие CLDN18.2 клетки (например, экспрессирующие CLDN18.2 опухолевые клетки) и/или активировать специфический иммунный ответ CLDN18.2 на экспрессирующие CLDN18.2 клетки-мишени. Иммунологическая мишень, как используется в настоящем документе, охватывает биологическую молекулу, которая участвует в генерации или модуляции иммунного ответа, необязательно, клеточного иммунного ответа. Примером связанной с иммунитетом мишени является молекула иммунной контрольной точки и поверхностная молекула цитолитической иммунной клетки, такой как Т-клетка или естественная киллерная (NK) клетка.
[00271] Молекула иммунной контрольной точки может опосредовать костимулирующий сигнал для усиления иммунного ответа или может опосредовать ко-ингибирующие сигналы для подавления иммунного ответа. Примеры молекулы иммунной контрольной точки включают, например, PD-L1, PD-L2, PD-1, CLTA-4, TIM-3, LAG3, A2AR, CD160, 2B4, TGF β, VISTA, BTLA, TIGIT, LAIR1, OX40, CD2, CD27, CD28, CD30, CD40, CD122, ICAM-1, IDO, NKG2C, SLAMF7, SIGLEC7, NKp80, CD160, B7-H3, LFA-1, 1COS, 4-1BB, GITR, BAFFR, HVEM, CD7, LIGHT, IL-2, IL-15, CD3, CD16 и CD83.
[00272] Цитолитические иммунные клетки могут запускаться своей поверхностной молекулой для атаки и опосредования лизиса клетки-мишени, такой как опухолевая клетка. Примеры поверхностного антигена Т-клеток включают, без ограничения, антиген, выбранный из группы, включающей CD3, CD2, CD4, CD5, CD6, CD8, CD28, CD40L и/или CD44, предпочтительно, CD3. В некоторых вариантах осуществления изобретения указанный второй антиген представляет собой эпсилон-цепь CD3. В некоторых вариантах осуществления изобретения связывание указанного биспецифического антитела с CD3 на Т-клетках приводит к пролиферации и/или активации указанных Т-клеток, что индуцирует высвобождение цитотоксических факторов, например, перфоринов и гранзимов, а также цитолиз и апоптоз клеток-мишеней В некоторых вариантах осуществления изобретения второй антиген представляет собой антиген поверхности NK-клеток, такой как CD16 (FcγRIII) или CD56. В некоторых вариантах осуществления изобретения связывание биспецифического антитела к CD16 на NK-клетках приводит к дегрануляции NK-клеток и перфорин-зависимому лизису (ADCC) клеток-мишеней.
[00273] В некоторых вариантах осуществления изобретения второй антиген содержит опухолевый антиген. «Опухолевый антиген», как используется в настоящем документе, относится к опухолеспецифическим антигенам (например, антигенам, уникальным для опухолевых клеток и обычно не обнаруживаемым в неопухолевых клетках), опухолеассоциированным антигенам (например, обнаруживаемым как в опухолевых, так и в неопухолевых клетках, но по-разному экспрессирующимся в опухолевых клетках) и опухолевым неоантигенам (например, которые экспрессируются в раковых клетках из-за соматических мутаций, которые изменяют последовательность белка или создают слитые белки между двумя неродственными последовательностями).
[00274] Примеры опухолевых антигенов включают, без ограничения, EpCAM, HER2/neu, HER3/neu, C250, CEA, MAGE, протеогликаны, VEGF, EGFR, αVβ3-интегрин, HLA, HLA-DR, ASC, CD1, CD2, CD4, CD6, CD7, CD8, CD11, CD13, CD14, CD19, CD20, CD21, CD22, CD23, CD24, CD30, CD33, CD37, CD40, CD41, CD47, CD52, c-erb-2, CALLA, MHCII, CD44v3, CD44v6, p97, ганглиозид GM1, GM2, GM3, GD1a, GD1b, GD2, GD3, GT1 b, GT3, GQ1, NY-ESO-1, NFX2, SSX2, SSX4, Trp2, gp100(Pmel 17), тирозиназу, Muc-1, теломеразу, сурвивин, G250, p53, CA125 MUC, антиген Wue, антиген Y Льюиса, HSP-27, HSP-70, HSP-72, HSP-90, Pgp, MCSP, EpHA2 и мишени клеточной поверхности GC1 82, GT468 или GT512, PD-L1, эпитоп арбовирусного белка Е, ассоциированный с глиомой антиген, карциноэмбриональный антиген (СЕА), β-хорионический гонадотропин человека, альфафетопротеин (AFP), лектин-реактивный AFP, тиреоглобулин, RAGE-1, MN-CA IX, теломеразную обратную транскриптазу человека, RU1, RU2 (AS), кишечную карбоксиэстеразу, мутант hsp70-2, M-CSF, простазу, простатспецифический антиген (PSA), PAP, NY-ESO-1, LAGE-1a, p53, prostein, PSMA, сурвивин и теломеразу, антиген-1 опухоли карциномы предстательной железы (PCTA-1), MAGE, ELF2M, эластазу нейтрофилов, эфрин-B2, CD22, фактор роста инсулина (IGF)-I, IGF-II, IGF-I рецептор и мезотелин, ART-l/MelanA (MART-1), тирозиназу, TRP-1, TRP-2 и опухолеспецифические мультилинейные антигены, такие как MAGE-1, MAGE-3, BAGE, GAGE- 1, GAGE-2, pi 5; Ras, уникальные опухолевые антигены, возникающие в результате хромосомных транслокаций; такие как BCR-ABL, E2A-PRL, H4-RET, 1GH-IGK, MYL-RAR; и вирусные антигены, такие как антигены вируса Эпштейна-Барр EBVA и антигены вируса папилломы человека (HPV) E6 и E7; антигены на основе белков включают TSP-180, MAGE-4, MAGE-5, MAGE- 6, RAGE, NY-ESO, pl 85erbB2, pl 80erbB-3, c-met, nm-23H l, PSA, TAG-72, CA19-9, CA72-4, CAM 17.1, NuMa, K-ras, бета-катенин, CDK4, Mum-1, p15, p16, 43-9F, 5T4(791Tgp72), α-фетопротем, бета-HCG, BCA225, BTAA, CA 125, CA 15-3\CA 27.29\BCAA, CA 195, CA 242, CA-50, CAM43, CD68\I, CO-029, FGF-5, G250, Ga733VEpCAM, HTgp-175, M344, MA-50, MG7-Ag, MOV 18, NB/70K, NY-CO-1, RCAS 1, SDCCAG16, белок, связывающий TA-90\Mac-2, белок, ассоциированный с циклофилином С, TAAL6, TAG72, TLP и TPS.
[00275] В некоторых вариантах осуществления изобретения опухолевый антиген связан с раком желудка, раком пищевода, раком поджелудочной железы, раком легких, раком яичников, раком толстой кишки, раком печени, раком головы и шеи, раком желчного пузыря и их метастазами. Примеры такого опухолевого антигена включают, но не ограничиваются ими, CA-125, ганглиозиды G(D2), G(M2) и G(D3), CD20, CD52, CD33, Ep-CAM, CEA, бомбезин-подобные пептиды, PSA, HER2/neu, рецептор эпидермального фактора роста (EGFR), erbB2, erbB3/HER3, erbB4, CD44v6, Ki-67, рако-ассоциированный муцин, VEGF, VEGFR (например, VEGFR3), рецепторы эстрогена, антиген Льюиса-Y TGFβ1, рецептор IGF-1, EGFα, рецептор c-Kit, рецептор трансферрина, IL-2R или CO17-1A, CAl9-9, и CA72-4. В некоторых вариантах осуществления изобретения опухолевый антиген присутствует в клетке, экспрессирующей CLDN18.2, например, раковой клетке, экспрессирующей CLDN18.2.
[00276] Биспецифическое антитела и их антигенсвязывающие фрагменты, предложенные в настоящем документе, могут быть представлены в подходящем формате, известном в данной области. Например, иллюстративным биспецифическим форматом могут быть биспецифические диатела, биспецифические форматы на основе scFv, слияния IgG-scFv, двойной вариабельный домен (DVD)-Ig, квадрома, выступы-во-впадины, общая легкая цепь (например, общая легкая цепь с выступами-во-впадины и т.д.), BiTE, CrossMab, CrossFab, Duobody, SEEDbody, лейциновая молния, Fab (DAF)-IgG двойного действия и биспецифические форматы Mab2 (см., например, Brinkmann et al. 2017, Mabs, 9(2): 182-212). Биспецифические молекулы могут иметь симметричную или асимметричную архитектуру.
[00277] Биспецифическое антитела и антигенсвязывающие фрагменты, предложенные в настоящем документе, могут быть получены любыми подходящими способами, известными в данной области.
[00278] В одном варианте осуществления изобретения две пары тяжелых и легких цепей иммуноглобулина, обладающие различной антигенной специфичностью, коэкспрессируются в клетке-хозяине с образованием биспецифических антител рекомбинантным способом (см., например, Milstein and Cuello, Nature, 305: 537 (1983)) с последующей очисткой аффинной хроматографией.
[00279] В другом варианте осуществления изобретения последовательности, кодирующие вариабельные домены тяжелой цепи антитела для двух специфичностей соответственно сливают с последовательностями константного домена иммуноглобулина с последующей вставкой в один или несколько векторов экспрессии, ко-трансфицированных вектором экспрессии для последовательностей легкой цепи, в подходящую клетку-хозяин для рекомбинантной экспрессии биспецифического антитела (см., например, WO 94/04690; Suresh et al., Methods in Enzymology, 121:210 (1986)). Подобным образом димеры scFv также могут быть рекомбинантно сконструированы и экспрессированы из клетки-хозяина (см., например, Gruber et al., J. Immunol., 152:5368 (1994)).
[00280] В другом способе пептиды лейциновой молнии из белков Fos и Jun могут быть связаны с частями Fab' двух разных антител путем слияния генов. Связанные антитела восстанавливаются в шарнирной области до четырех полуантител (то есть мономеров) и затем повторно окисляются с образованием гетеродимеров (Kostelny et al., J. Immunol., 148(5):1547-1553 (1992)).
[00281] Два антигенсвязывающих домена также могут быть конъюгированы или сшиты с образованием биспецифического антитела или антигенсвязывающего фрагмента. Например, одно антитело может быть связано с биотином, тогда как другое антитело может быть связано с авидином, и сильная связь между биотином и авидином может привести к образованию комплекса двух антител вместе с образованием биспецифического антитела (см., например, патент США № 4676980; WO 91/00360, WO 92/00373 и EP 03089). В другом примере два антитела или антигенсвязывающие фрагменты могут быть сшиты обычными способами, известными в данной области техники, например, как описано в патенте США № 4676980.
[00282] Биспецифическое антигенсвязывающие фрагменты могут быть получены из биспецифического антитела, например, путем протеолитического расщепления или химического связывания. Например, антигенсвязывающий фрагмент (например, Fab') антитела можно получить и преобразовать в Fab'-тиоловое производное, а затем смешать и ввести в реакцию с другим преобразованным Fab'-производным, имеющим другую антигенную специфичность, с образованием биспецифического антигенсвязывающего фрагмента (см., например, Brennan et al., Science, 229: 81 (1985)).
[00283] В некоторых вариантах осуществления изобретения биспецифическое антитело или его антигенсвязывающие фрагменты, предложенные в настоящем документе, могут быть сконструированы на поверхности раздела таким образом, что может образовываться ассоциация выступы-во-впадины для стимуляции гетеродимеризации двух разных антигенсвязывающих сайтов. Это может максимизировать процент гетеродимеров, которые выделяются из рекомбинантной клеточной культуры. Термин «выступы-во-впадины», как используется в настоящем документе, относится к взаимодействию между двумя полипептидами (такими как Fc), где один полипептид имеет выпуклость (то есть «выступ») из-за присутствия аминокислотного остатка, имеющего объемную боковую цепь (например, тирозин или триптофан), а другой полипептид имеет полость (т.е. «впадину»), в которой находится небольшой аминокислотный остаток боковой цепи (например, аланин или треонин), и выпуклость может располагаться в полости таким образом, чтобы способствовать взаимодействию двух полипептидов с образованием гетеродимера или комплекса. Способы получения полипептидов с выступами-во-впадины известны в данной области техники, например, как описано в патенте США № 5731168.
[00284] Конъюгаты
[00285] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты связаны с одним или несколькими фрагментами конъюгата. Конъюгат представляет собой часть, которая может быть присоединена к антителу или его антигенсвязывающему фрагменту. Предполагается, что различные конъюгаты могут быть связаны с антителами или антигенсвязывающими фрагментами, представленными в настоящем документе (см., например, «Conjugate Vaccines», Contributions to Microbiology and Immunology, J. M. Cruse and R. E. Lewis, Jr. (eds.), Carger Press, New York, (1989)). Эти конъюгаты могут быть связаны с антителами или антигенсвязывающими фрагментами путем ковалентного связывания, аффинного связывания, интеркаляции, координированного связывания, комплексообразования, ассоциации, смешивания или добавления среди других способов. В некоторых вариантах осуществления изобретения антитела или их антигенсвязывающие фрагменты связаны с одним или несколькими конъюгатами через линкер. В некоторых вариантах осуществления изобретения линкер представляет собой гидразоновый линкер, дисульфидный линкер, бифункциональный линкер, дипептидный линкер, глюкуронидный линкер, тиоэфирный линкер.
[00286] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела и антигенсвязывающие фрагменты, описанные в настоящем документе, могут быть сконструированы таким образом, чтобы они содержали специфические сайты за пределами части, связывающей эпитоп, которые можно использовать для связывания с одним или несколькими конъюгатами. Например, такой сайт может включать один или несколько реакционноспособных аминокислотных остатков, таких как, например, остатки цистеина или гистидина, для облегчения ковалентной связи с конъюгатом.
[00287] Конъюгат может представлять собой агент, модифицирующий клиренс, терапевтический агент (например, химиотерапевтический агент), токсин, радиоактивный изотоп, обнаруживаемую метку (например, лантанид, люминесцентную метку, флуоресцентную метку или фермент-субстратную метку), фрагмент, модифицирующий фармакокинетику, алкилаторы ДНК, ингибитор топоизомеразы, средства, связывающие тубулин, другие противоопухолевые лекарственные средства, или очищающий компонент (такой как магнитный шарик или наночастица).
[00288] Примеры обнаруживаемой метки могут включать флуоресцентные метки (например, флуоресцеин, родамин, дансил, фикоэритрин или техасский красный), фермент-субстратные метки (например, пероксидаза хрена, щелочная фосфатаза, люцериферазы, глюкоамилаза, лизоцим, сахаридоксидазы или β-D-галактозидаза), радиоизотопы, другие лантаниды, люминесцентные метки, хромофорную группу, дигоксигенин, биотин/авидин, молекулу ДНК или золото для обнаружения.
[00289] Примеры радиоизотопов могут включать 123I, 124I, 125I, 131I, 35S, 3H, 111In, 112In, 14C, 64Cu, 67Cu, 86Y, 88Y, 90Y, 177Lu, 211At, 186Re, 188Re, 153Sm, 212Bi и 32P. Антитела, меченные радиоизотопом, могут быть использованы в экспериментах по визуализации, ориентированных на рецепторы.
[00290] В некоторых вариантах осуществления изобретения конъюгат может представлять собой фармакокинетический модифицирующий фрагмент, такой как ПЭГ, который способствует увеличению времени полужизни антитела. Другие подходящие полимеры включают, например, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, сополимеры этиленгликоля/пропиленгликоля и тому подобное.
[00291] В некоторых вариантах осуществления изобретения конъюгат может представлять собой очищающий компонент, такой как магнитный шарик или наночастица.
[00292] Конъюгаты антитело-лекарственное средство
[00293] В некоторых вариантах осуществления изобретения в настоящем изобретении предложены конъюгаты антитело-лекарственное средство (ADC), содержащие любое из указанных выше анти-CLDN18.2 антител или антигенсвязывающих фрагментов, конъюгированных с цитотоксическим агентом.
[00294] ADC может быть полезен для местной доставки цитотоксических агентов, например, при лечении рака. Это позволяет целенаправленно доставлять цитотоксические агенты к опухолям и накапливать их внутри клетки, что особенно полезно, когда системное введение этих неконъюгированных цитотоксических агентов может привести к неприемлемым уровням токсичности нормальных клеток, а также опухолевых клеток, которые необходимо уничтожить (Baldwin et al., (1986) Lancet pp. (Mar. 15, 1986):603-05; Thorpe, (1985) «Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review», in Monoclonal Antibodies ʼ84: Biological And Clinical Applications, A. Pinchera et al. (ed.s), pp. 475-506; Syrigos and Epenetos (1999) Anticancer Research 19:605-614; Niculescu-Duvaz and Springer (1997) Adv. Drg Del. Rev. 26:151-172; патент США № 4975278).
[00295] В некоторых вариантах осуществления изобретения цитотоксический агент может представлять собой любой агент, который вреден для клеток или может повреждать или убивать клетки. В некоторых вариантах осуществления изобретения цитотоксический агент, необязательно, представляет собой, токсин, химиотерапевтический агент (такой как алкилаторы ДНК, ингибитор топоизомеразы, средства, связывающие тубулин, агент, ингибирующий рост, или другие противоопухолевые лекарственные средства) или радиоактивный изотоп.
[00296] Примеры токсинов включают бактериальные токсины и растительные токсины, такие как, например, дифтерийный токсин, цепь экзотоксина А (из Pseudomonas aeruginosa), рицин, абрин, модекцин, альфа-сарцин, белки Aleurites fordii, диантиновые белки, белки Phytolaca americana (PARI, PAPII и PAP-S), ингибитор момордики харанции, курцин, кротин, ингибитор сапаонарии лекарственной, гелонин, рестриктоцин, феномицин, эномицин и трикотецены (см., например, WO 93/21232). Такая крупная молекула токсина может быть конъюгирована с антителами или антигенсвязывающими фрагментами, представленными в настоящем документе, с использованием способов, известных в данной области, например, как описано в работе Vitetta et al (1987) Science, 238:1098.
[00297] Цитотоксический агент также может представлять собой низкомолекулярные токсины и химиотерапевтические агенты, такие как гелданамицин (Mandler et al (2000) Jour. of the Nat. Cancer Inst. 92(19):1573-1581; Mandler et al (2002) Bioconjugate Chem. 13:786-791), майтанзин и майтанзиноиды (EP 1391213; Liu et al., (1996) Proc. Natl. Acad. Sci. USA 93:8618-8623; патент США № 5208020), калихимицин (Lode et al (1998) Cancer Res. 58:2928; Hinman et al (1993) Cancer Res. 53:3336-3342), таксол, цитохалазин B, грамицидин D, бромид этидия, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, виндезин, колхицин, доксорубицин, даунорубицин, дигидрокси антрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, новокаин, тетракаин, лидокаин, пропранолол, пуромицин и их аналоги, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацил декарбазин), алкилирующие агенты (например, мехлорэтамин, тиоэпахлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклотофосфамид, бусульфан, дибромманнитол, стрептозотоцин, митомицин С и цис-дихлордиамин платины (II) (DDP) цисплатин), антрациклины (например, даунорубицин (ранее дауномицин) и доксорубицин), антибиотики (например, дактиномицин (ранее актиномицин), блеомицин, митрамицин и антрамицин (АМС)) и антимитотические агенты (например, винкристин и винбластин), калихеамицин, майтанзиноиды, доластатины, ауристатины, такие как MMAE и MMAF (патенты США №№ 5635483, 5780588), долостатины, трихотецен и CC1065 и их производные, обладающие цитотоксической активностью.
[00298] Цитотоксический агент также может представлять собой высокорадиоактивный изотоп. Примеры включают At211, I131, I125, Y90, Re186, Sm153, Bi212, P32, Pb212 и радиоактивные изотопы Lu. Способы конъюгации радиоизотопа с антителом известны в данной области, например, с помощью подходящего лигандного реагента (см., например, WO94/11026; Current Protocols in Immunology, Volumes 1 и 2, Coligen et al. Ed. Wiley-Interscience, New York, N.Y., Pubs. (1991)). Реагент-лиганд имеет хелатирующий лиганд, который может связывать, хелатировать или иным образом образовывать комплексы с радиоактивным изотопом металла, а также имеет функциональную группу, которая вступает в реакцию с тиолом цистеина антитела или антигенсвязывающего фрагмента. Примеры хелатирующих лигандов включают DOTA, DOTP, DOTMA, DTPA и TETA (Macrocyclics, Dallas, Tex.).
[00299] Цитотоксические агенты могут быть связаны с антителом или антигенсвязывающим фрагментом с помощью любых подходящих линкеров, известных в данной области, см., например, патенты США №№ 5208020, 6441163 или патент EP 0425235 B1, Chari et al., Cancer Research 52:127-131 (1992), и US 2005/0169933 A1, описание которых настоящим включено посредством ссылки.
[00300] В некоторых вариантах осуществления изобретения the линкер расщепляется в определенных физиологических условиях, тем самым способствуя высвобождению цитотоксического лекарственного средства в клетке. Например, линкер может представлять собой кислотолабильный линкер, пептидазо-чувствительный линкер, фотолабильный линкер, диметиллинкер или дисульфид-содержащий линкер, тиоэфирный линкер и эстеразолабильный линкер (Chari et al., Cancer Research 52:127-131 (1992); патент США № 5208020). В некоторых вариантах осуществления изобретения линкер может содержать аминокислотные остатки, такие как дипептид, трипептид, тетрапептид или пентапептид. Аминокислотные остатки в линкере могут быть природными или неприродными аминокислотными остатками. Примеры таких линкеров включают: валин-цитруллин (ve или val-cit), аланин-фенилаланин (af или ala-phe), глицин-валин-цитруллин (gly-yal-cit), глицин-глицин-глицин (gly-gly-gly), валин-цитруллин-п-аминобензилоксикаронил («vc-PAB»). Аминокислотные линкерные компоненты могут быть разработаны и оптимизированы по их селективности в отношении ферментативного расщепления конкретными ферментами, например, ассоциированной с опухолью протеазой, катепсином B, C и D или плазминовой протеазой.
[00301] В некоторых вариантах осуществления изобретения цитотоксические агенты могут быть связаны с антителом или его антигенсвязывающим фрагментом, представленным в настоящем документе, с помощью бифункционального линкерного реагента, включая, например, N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP), сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (SMCC), N-сукцинимидил-4-(2-пиридилтио)пентаноат (SPP), иминотиолан (IT), бифункциональные производные имидоэфиров (такие как диметиладипимидат HCl), активные сложные эфиры (такие как дисукцинимидилсуберат), альдегиды (такие как глутаровый альдегид), бис-азидосоединения (такие как бис(п-азидобензоил)гександиамин), производные бис-диазония (такие как бис(п-диазонийбензоил)этилендиамин), диизоцианаты (такие как толуол 2,6-диизоцианат), бисактивные фтор соединения (такие как 1,5-дифтор-2,4-динитробензол), BMPS, EMCS, GMBS, HBVS, LC-SMCC, MBS, MPRH, SBAP, SIA, SIAB, SMPB, SMPH, сульфо-EMCS, сульфо-GMBS, сульфо-KMUS, сульфо-MBS, сульфо-SIAB, сульфо-SMCC и сульфо-SMPB, и SVSG (сукцинимидил-(4-винилсульфон)бензоат). Эти линкерные реагенты коммерчески доступны (например, от компании Pierce Biotechnology, Inc., Rockford, Ill., U.S.A, см. стр. 467-498, 2003-2004 Applications Handbook and Catalog).
[00302] В некоторых вариантах осуществления изобретения в ADC, представленном в настоящем документе, антитело (или его антигенсвязывающий фрагмент) конъюгировано с одним или несколькими цитотоксическими агентами при соотношении антитело: агент от около 1 до около 20, от около 1 до около 6, от около 2 до около 6, от около 3 до около 6, от около 2 до около 5, от около 2 до около 4 или от около 3 до около 4.
[00303] ADC, представленный в настоящем документе, может быть получен любыми подходящими способами, известными в данной области техники. В некоторых вариантах осуществления изобретения нуклеофильная группа антитела (или его антигенсвязывающего фрагмента) сначала реагирует с бифункциональным линкерным реагентом, а затем связывается с цитотоксическим агентом или наоборот, то есть сначала взаимодействие нуклеофила цитотоксического агента с бифункциональным линкером, а затем связывание с антителом.
[00304] В некоторых вариантах осуществления изобретения цитотоксический агент может содержать (или быть модифицированным, чтобы содержать) функциональную группу, реагирующую с тиолом, которая может реагировать с цистеиновым тиолом свободного цистеина антител или антигенсвязывающих фрагментов, представленных в настоящем документе. Типичные тиол-реактивные функциональные группы включают, например, малеимид, йодацетамид, пиридилдисульфид, галогенацетил, сукцинимидиловый эфир (например, NHS, N-гидроксисукцинимид), изотиоцианат, сульфонилхлорид, 2,6-дихлортриазинил, пентафторфениловый эфир или фосфорамидит (Haugland, 2003, Molecular Probes Handbook of Fluorescent Probes and Research Chemicals, Molecular Probes, Inc.; Brinkley, 1992, Bioconjugate Chem. 3:2; Garman, 1997, Non-Radioactive Labelling: A Practical Approach, Academic Press, London; Means (1990) Bioconjugate Chem. 1:2; Hermanson, G. in Bioconjugate Techniques (1996) Academic Press, San Diego, pp. 40-55, 643-671).
[00305] Цитотоксический агент или антитело могут реагировать со связывающим реагентом перед конъюгированием с образованием ADC. Например, N-гидроксисукцинимидиловый эфир (NHS) цитотоксического агента может быть получен, выделен, очищен и/или охарактеризован, или он может быть образован in situ и прореагировать с нуклеофильной группой антитела. Обычно карбоксильная форма конъюгата активируется реакцией с некоторой комбинацией карбодиимидного реагента, например, дициклогексилкарбодиимида; диизопропилкарбодиимид или урониевый реагент, например, TsTu (O-(N-сукцинимидил)-N,N,N',N'-тетраметилурония тетрафторборат, HBTU (O-бензотриазол-1-ил)-N, N,N'N'-тетраметилурония гексафторфосфат) или HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат), активатор, такой как 1-гидроксибензотриазол (HOBt), и N-гидроксисукцинимид для получения сложного эфира NHS. В некоторых случаях цитотоксический агент и антитело могут быть связаны активацией in situ и реакцией с образованием ADC в одну стадию. Другие активирующие и связывающие реагенты включают TBTU (2-(1H-бензотриазо-1-ил)-1-1,3,3-тетраметилурония гексафторфосфат), TFFH (N,N',N'',N'''-тетраметилуроний 2-фторгексафторфосфат), PyBOP (гексафторфосфат бензотриазол-1-ил-окси-трис-пирролидинофосфония, EEDQ (2-этокси-1-этоксикарбонил-1,2-дигидрохинолин), DCC (дициклогексилкарбодиимид); DIPCDI (диизопропилкарбодиимид), MSNT (1-(мезитилен-2-сульфонил)-3-нитро-1H-1,2,4-триазол и арилсульфонилгалогениды, например, триизопропилбензолсульфонилхлорид. В другом примере антитело или антигенсвязывающие фрагменты могут быть конъюгированы с биотином, а затем непрямым образом конъюгированы со вторым конъюгатом, который конъюгирован с авидином.
[00306] Композиция химерного антигенного рецептора (CAR)
[00307] В настоящем изобретении также предложены химерные антигенные рецепторы (CAR), содержащие антигенсвязывающий домен против CLDN18.2, предложенные в настоящем документе, и домен активации Т-клеток. Химерные антигенные рецепторы (CAR) представляют собой сконструированные химерные рецепторы, которые объединяют антигенсвязывающий домен антитела с одним или несколькими сигнальными доменами для активации Т-клеток. Иммунные клетки, такие как Т-клетки и клетки Nature Killer (NK), могут быть генетически модифицированы для экспрессии CAR. Т-клетки, экспрессирующие CAR, называются CAR-T-клетками. CAR может опосредовать антигенспецифическую клеточную иммунную активность в Т-клетках, позволяя CAR-T-клеткам элиминировать клетки (например, опухолевые клетки), экспрессирующие антиген-мишень. В одном варианте осуществления изобретения связывание CAR-T-клеток, представленных в настоящем документе, с CLDN18.2, экспрессируемым на клетках, таких как раковые клетки, приводит к пролиферации и/или активации указанных CAR-T-клеток, при этом указанные активированные CAT-T-клетки могут высвобождать цитотоксические факторы, например, перфорин, гранзимы и гранулизин, и инициируют цитолиз и/или апоптоз раковых клеток.
[00308] В некоторых вариантах осуществления изобретения домен активации Т-клеток CAR содержит костимулирующий сигнальный домен и сигнальный домен TCR, которые могут быть связаны друг с другом в случайном порядке или в указанном порядке, необязательно с помощью короткого пептидного линкера, имеющего длину, например, от 2 до 10 аминокислот (например, двойной глицин-сериновый линкер).
[00309] В некоторых вариантах осуществления изобретения CAR дополнительно содержит трансмембранный домен. При экспрессии в клетках антигенсвязывающий домен анти-CLDN18.2 является внеклеточным, а домен активации Т-клеток является внутриклеточным.
[00310] В некоторых вариантах осуществления изобретения CAR содержит анти-CLDN18.2 антигенсвязывающий домен, трансмембранный домен, костимулирующий сигнальный участок и сигнальный домен TCR, где антигенсвязывающий домен специфически связывается с CLDN18.2 и содержит антигенсвязывающий фрагмент антител, предложенные в настоящем документе.
1. Антигенсвязывающий домен
[00311] В некоторых вариантах осуществления изобретения анти-CLDN18.2 антигенсвязывающий домен CAR содержит одну или несколько последовательностей CDR, представленных в настоящем документе, один или несколько вариабельных доменов тяжелой цепи или вариабельных доменов легкой цепи, представленных в настоящем документе, или один или несколько антигенсвязывающих фрагментов, полученный из любого из анти-CLDN18.2 антител, предложенных в настоящем документе.
[00312] В некоторых вариантах осуществления изобретения предпочтительно, чтобы антигенсвязывающий домен был получен из тех же видов, у которых в конечном итоге будет использоваться CAR. Например, для применения у людей может быть удобно иметь антигенсвязывающий домен, используемый в CAR, полученный из человеческого антитела или гуманизированного антитела. В некоторых вариантах осуществления антигенсвязывающий домен содержит одноцепочечный вариабельный фрагмент (scFv). В некоторых вариантах осуществления антигенсвязывающий домен может существовать во множестве других форм, включая, например, Fv, Fab, и (Fab')2, а также бифункциональные (то есть биспецифические) гибридные фрагменты антител (например, Lanzavecchia et al., Eur. J. Immunol. 17, 105 (1987)). В некоторых вариантах осуществления изобретения антигенсвязывающий домен содержит Fab или scFv.
2. Трансмембранный домен
[00313] В некоторых вариантах осуществления изобретения CAR содержит трансмембранный домен, слитый с внеклеточным антигенсвязывающим доменом CAR. В одном варианте осуществления изобретения трансмембранный домен может быть выбран таким образом, чтобы он естественным образом был связан с одним из доменов в CAR. В некоторых случаях трансмембранный домен можно выбрать или модифицировать, чтобы избежать связывания с трансмембранными доменами других членов комплекса Т-клеточного рецептора.
[00314] Трансмембранный домен CAR по настоящему изобретению может быть получен из трансмембранных доменов любого природного мембраносвязанного или трансмембранного белка, такого как, например, альфа-, бета- или дзета-цепь Т-клеточного рецептора, CD28, эпсилон CD3, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137 и CD154. В некоторых вариантах осуществления изобретения трансмембранный домен CAR также может использовать множество шарнирных областей человека, таких как шарнирная область человеческого Ig (иммуноглобулина).
[00315] Альтернативно, трансмембранный домен CAR, представленный в настоящем документе, может быть синтетическим, например, содержащим преимущественно гидрофобные остатки, такие как лейцин и валин. В одном варианте осуществления изобретения a триплет фенилаланина, триптофана и валина включен на каждом конце синтетического трансмембранного домена. Необязательно, короткий олиго- или полипептидный линкер длиной от 2 до 10 аминокислот может образовывать связь между трансмембранным доменом и внутриклеточным сигнальным доменом CAR. Особенно подходящий линкер обеспечивает дублет глицин-серин.
3. Сигнальный домен TCR
[00316] Домен активации Т-клеток CAR по настоящему изобретению содержит сигнальный домен TCR. Сигнальный домен TCR может активировать Т-клетку, которая экспрессирует CAR, для проявления по меньшей мере одной из нормальных эффекторных функций TCR Т-клетки, например, цитолитическую активность или хелперную активность, включая секрецию цитокинов. Сигнальный домен TCR может представлять собой либо полноразмерный домен передачи естественного внутриклеточного сигнала, либо его фрагмент, достаточный для передачи сигнала эффекторной функции TCR.
[00317] Примеры внутриклеточных сигнальных доменов, применимых в CAR, представленных в настоящем документе, включают цитоплазматические последовательности Т-клеточного рецептора (TCR) и корецепторов, которые действуют согласованно, инициируя трансдукцию сигнала после взаимодействия с антигенным рецептором, а также любые производные или варианты из этих последовательностей и любой синтетической последовательности, обладающей такой же функциональной способностью.
[00318] Сигнальный домен TCR, который действует стимулирующим образом, может содержать сигнальные мотивы, которые известны как мотивы активации иммунорецептора на основе тирозина или ITAM. Примеры ITAM, содержащих сигнальные домены TCR, применимые в CAR, представленные в настоящем документе, включают домены, полученные из TCR дзета, FcR гамма, FcR бета, CD3 гамма, CD3 дельта, CD3 эпсилон, CD5, CD22, CD79a, CD79b и CD66d. В некоторых вариантах осуществления изобретения сигнальный домен TCR содержит цитоплазматическую сигнальную последовательность, полученную из CD3-дзета.
4. Костимулирующая сигнальная область
[00319] Домен активации Т-клеток CAR по настоящему изобретению дополнительно содержит костимулирующий сигнальный участок. Костимулирующая сигнальная область действует антиген-независимым образом, опосредуя активацию TCR, и может быть получена из костимулирующей молекулы, необходимой для эффективного ответа лимфоцитов на антиген. Примеры костимулирующих молекул включают CD27, CD28, 4-1BB (CD137), OX40, CD30, CD40, PD-1, ICOS, антиген-1, ассоциированный с функцией лимфоцитов (LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3 и лиганд, который специфически связывается с CD83 и тому подобное.
5. Биспецифический CAR
[00320] В некоторых вариантах осуществления изобретения CAR является биспецифическим. В некоторых вариантах осуществления изобретения биспецифический CAR, предложенный в настоящем документе, специфически связывается с первым и вторым эпитопом CLDN18.2, или способен специфически связываться с CLDN18.2 и вторым антигеном.
[00321] В одном варианте осуществления изобретения указанный CAR связывается с нативным эпитопом CLDN18.2, присутствующим на поверхности живых клеток.
6. Полинуклеотидная последовательность, кодирующая CAR
[00322] В одном аспекте в настоящем изобретении предложены, кроме того, последовательности нуклеиновых кислот, кодирующие CAR, представленные в настоящем документе, содержащие первую полинуклеотидную последовательность, кодирующую антигенсвязывающий домен CAR, представленного в настоящем документе, и необязательно вторую полинуклеотидную последовательность, кодирующую трансмембранный домен и T -домен активации клеток, представленный в настоящем документе. В некоторых вариантах осуществления изобретения последовательность, кодирующая антигенсвязывающий домен, функционально связана с последовательностью, кодирующей трансмембранный домен и домен активации Т-клеток. Последовательности нуклеиновых кислот, кодирующие желаемые молекулы, могут быть получены с использованием рекомбинантных методов, известных в данной области, таких как, например, путем скрининга библиотек из клеток, экспрессирующих ген, путем получения гена из вектора, который, как известно, его содержит, или путем выделения непосредственно из клеток и тканей, содержащих их, с использованием стандартных методов. В качестве альтернативы интересующий ген может быть получен синтетическим путем, а не клонирован.
[00323] В одном аспекте в настоящем изобретении предложены векторы, содержащие последовательность нуклеиновой кислоты, кодирующую CAR, представленный в настоящем документе. В некоторых вариантах осуществления изобретения вектор представляет собой ретровирусную и лентивирусную векторную конструкцию, экспрессирующую CAR по настоящему изобретению, которая может быть непосредственно трансдуцирована в клетку, или РНК-конструкцию, которая может быть непосредственно трансфицирована в клетку.
[00324] В одном аспекте в настоящем изобретении предложены выделенные клетки, которые содержат последовательность нуклеиновой кислоты, кодирующую CAR и/или экспрессирующую CAR по настоящему изобретению.
[00325] В некоторых вариантах осуществления изобретения клетка, содержащая нуклеиновую кислоту, кодирующую CAR или экспрессирующую CAR, выбрана из группы, состоящей из Т-клетки, NK-клетки, цитотоксического Т-лимфоцита (CTL) и регуляторной Т-клетки. В одном варианте осуществления изобретения клетка, содержащая нуклеиновую кислоту, кодирующую CAR или экспрессирующую CAR, проявляет противоопухолевый иммунитет, когда антигенсвязывающий домен CAR связывается с соответствующим антигеном. Цитотоксические лимфоциты, предпочтительно, представляют собой аутологичные клетки, хотя можно использовать гетерологичные клетки или аллогенные клетки. Как используется в настоящем документе, «аутологичный» означает любой материал, полученный от того же индивидуума, которому он позднее будет повторно введен индивидууму.
[00326] В одном аспекте в настоящем изобретении предложены, кроме того, способы стимуляции опосредованного Т-клетками иммунного ответа на клетки или ткани, экспрессирующие CLDN18.2, где способ включает введение субъекту эффективного для субъекта количества клеток, генетически модифицированных для экспрессии CAR, предложенного в настоящем документе.
[00327] В одном аспекте в настоящем изобретении предложены, кроме того, способы лечения млекопитающего, имеющего заболевание, нарушение или состояние, связанное с повышенной экспрессией CLDN18.2, включающие введение млекопитающему эффективного количества клеток, генетически модифицированных для экспрессии CAR, предложенные в настоящем документе, и тем самым лечение млекопитающего. В некоторых вариантах осуществления изобретения клетка представляет собой аутологичную Т-клетку. В некоторых вариантах осуществления изобретения у млекопитающего диагностировано заболевание, нарушение или состояние, связанное с повышенной экспрессией CLDN18.2.
[00328] Полинуклеотиды и рекомбинантные способы
[00329] В настоящем изобретении предложены выделенные полинуклеотиды, которые кодируют анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты. Термин «нуклеиновая кислота» или «полинуклеотид», как используется в настоящем документе, относится к дезоксирибонуклеиновым кислотам (ДНК) или рибонуклеиновым кислотам (РНК) и их полимерам либо в одноцепочечной, либо в двухцепочечной форме. Если не указано иное, конкретная полинуклеотидная последовательность также неявно включает ее консервативно модифицированные варианты (например, замены вырожденных кодонов), аллели, ортологи, SNP и комплементарные последовательности, а также явно указанную последовательность. В частности, замен вырожденных кодонов можно добиться путем создания последовательностей, в которых третье положение одного или нескольких выбранных (или всех) кодонов заменено остатками смешанного основания и/или дезоксиинозина (см. Batzer et al., Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al., J. Biol. Chem. 260:2605-2608 (1985); и Rossolini et al., Mol. Cell. Probes 8:91-98 (1994)).
[00330] ДНК, кодирующую моноклональное антитело, легко выделяют и секвенируют с использованием обычных процедур (например, с использованием олигонуклеотидных зондов, которые способны специфически связываться с генами, кодирующими тяжелые и легкие цепи антитела). Кодирующая ДНК также может быть получена синтетическими методами.
[00331] В настоящем изобретении предложены векторы (например, векторы экспрессии), содержащие выделенный полинуклеотид, представленный в настоящем документе. В некоторых вариантах осуществления изобретения вектор экспрессии, представленный в настоящем документе, содержит полинуклеотид, кодирующий антитела или их антигенсвязывающие фрагменты, представленные в настоящем документе, по меньшей мере один промотор (например, SV40, CMV, EF-1α), функционально связанный с полинуклеотидной последовательностью, и по меньшей мере один селективный маркер. Примеры векторов включают, но не ограничиваются ими, ретровирус (включая лентивирус), аденовирус, аденоассоциированный вирус, герпесвирус (например, вирус простого герпеса), поксвирус, бакуловирус, папилломавирус, паповавирус (например, SV40), фаг лямбда и фаг М13, плазмиды, такие как pcDNA3.3, pMD18-T, pOptivec, pCMV, pEGFP, pIRES, pQD-Hyg-GSeu, pALTER, pBAD, pcDNA, pCal, pL, pET, pGEMEX, pGEX, pCI, pEGFT, pSV2, pFUSE, pVITRO, pVIVO, pMAL, pMONO, pSELECT, pUNO, pDUO, Psg5L, pBABE, pWPXL, pBI, p15TV-L, pPro18, pTD, pRS10, pLexA, pACT2.2, pCMV-SCRIPT.RTM., pCDM8, pCDNA1,1/amp, pcDNA3.1, pRc/RSV, PCR 2.1, pEF-1, pFB, pSG5, pXT1, pCDEF3, pSVSPORT, pEF-Bos и т. д.
[00332] Векторы, содержащие полинуклеотидную последовательность, кодирующую антитело или его антигенсвязывающий фрагмент, можно вводить в клетку-хозяин для клонирования или экспрессии гена. Подходящими клетками-хозяевами для клонирования или экспрессии ДНК в векторах по настоящему изобретению являются клетки прокариот, дрожжей или высших эукариот, описанные выше. Подходящие для этой цели прокариоты включают эубактерии, такие как грамотрицательные или грамположительные организмы, например, Enterobacteriaceae, такие как Escherichia, например, E. coli, Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella, например, Salmonella typhimurium, Serratia, например, Serratia marcescans, и Shigella, а также Bacilli, такие как B. subtilis и B. licheniformis, Pseudomonas, такие как P. aeruginosa, и Streptomyces.
[00333] Помимо прокариот, эукариотические микробы, такие как мицелиальные грибы или дрожжи, являются подходящими хозяевами для клонирования или экспрессии векторов, кодирующих антитело против CLDN18.2. Saccharomyces cerevisiae, или обычные пекарские дрожжи, наиболее часто используются среди низших эукариотических микроорганизмов-хозяев. Однако ряд других родов, видов и штаммов обычно доступны и применимы в настоящем документе, такие как Schizosaccharomyces pombe; Kluyveromyces hosts, такие как, например, K. lactis, K. fragilis (ATCC 12424), K. bulgaricus (ATCC 16045), K. wickeramii (ATCC 24178), K. waltii (ATCC 56500), K. drosophilarum (ATCC 36906), K. thermotolerans, и K. marxianus; yarrowia (EP 402226); Pichia pastoris (EP 183070); Candida; Trichoderma reesia (EP 244234); Neurospora crassa; Schwanniomyces, такие как Schwanniomyces occidentalis; и нитчатые грибы, такие как, например, Neurospora, Penicillium, Tolypocladium и Aspergillus hosts, такие как A. nidulans и A. niger.
[00334] Клетки-хозяева, подходящие для экспрессии гликозилированных антител или фрагмента антигена по настоящему изобретению, получены из многоклеточных организмов, таких как клетки беспозвоночных, например, клетки растений и насекомых. Были идентифицированы многочисленные бакуловирусные штаммы и варианты и соответствующие пермиссивные клетки насекомых-хозяев, таких как Spodoptera frugiperda (гусеница), Aedes aegypti (комар), Aedes albopictus (комар), Drosophila melanogaster (плодовая муха) и Bombyx mori. Общедоступны различные вирусные штаммы для трансфекции, например, вариант L-1 Autographa californica NPV и штамм Bm-5 Bombyx mori NPV, и такие вирусы могут быть использованы в качестве вируса по настоящему изобретению, в частности, для трансфекции клеток Spodoptera frugiperda. В качестве хозяев также можно использовать культуры клеток растений хлопка, кукурузы, картофеля, сои, петунии, помидоров и табака.
[00335] Однако наибольший интерес вызывают клетки позвоночных, и размножение клеток позвоночных в культуре (тканевой культуре) стало рутинной процедурой. Примерами пригодных линий клеток-хозяев млекопитающих являются линия CV1 почки обезьяны, трансформированная SV40 (COS-7, ATCC CRL 1651); линия эмбриональной почки человека (клетки 293 или 293, субклонированные для роста в суспензионной культуре, Graham et al., J. Gen Virol. 36:59 (1977)); клетки почек детенышей хомячков (BHK, ATCC CCL 10); клетки яичника китайского хомячка/-DHFR (CHO, Urlaub et al., Proc. Natl. Acad. Sci. USA 77:4216 (1980)); мышиные клетки Сертоли (TM4, Mather, Biol. Reprod. 23:243-251 (1980)); клетки почки обезьяны (CV1 ATCC CCL 70); клетки почки африканской зеленой мартышки (VERO-76, ATCC CRL-1587); клетки карциномы шейки матки человека (HELA, ATCC CCL 2); клетки почек собак (MDCK, ATCC CCL 34); клетки печени крысы-буйвола (BRL 3A, ATCC CRL 1442); клетки легкого человека (W138, ATCC CCL 75); клетки печени человека (Hep G2, HB 8065); опухоль молочной железы мыши (MMT 060562, ATCC CCL51); клетки TRI (Mather et al., Annals N.Y. Acad. Sci. 383:44-68 (1982)); клетки MRC 5; клетки FS4 и линия гепатомы человека (Hep G2). В некоторых предпочтительных вариантах осуществления клетка-хозяин представляет собой культивируемую клеточную линию млекопитающих, такую как CHO, BHK, NS0, 293 и их производные.
[00336] Клетки-хозяева трансформируют описанными выше экспрессионными или клонирующими векторами для продукции антител против CLDN18.2 и культивируют в обычных питательных средах, модифицированных соответствующим образом для индукции промоторов, отбора трансформантов или амплификации генов, кодирующих желаемые последовательности. В другом варианте осуществления антитело может быть получено путем гомологичной рекомбинации, известной в данной области.
[00337] Клетки-хозяева, используемые для продукции антител или антигенсвязывающих фрагментов, предложенных в настоящем документе, можно культивировать в различных средах. Для культивирования клеток-хозяев подходят коммерчески доступные среды, такие как Hamʼs F10 (Sigma), минимальная основная среда (MEM), (Sigma), RPMI-1640 (Sigma) и модифицированная Дульбекко среда Игла (DMEM), Sigma). Кроме того, в качестве питательной среды для клеток-хозяев можно использовать любую из сред, описанных в работах Ham et al., Meth. Enz. 58:44 (1979), Barnes et al., Anal. Biochem. 102:255 (1980), патентах США №№ 4767704, 4657866, 4927762, 4560655 или 5122469; WO 90/03430; WO 87/00195; или патенте США Re. 30985. Любая из этих сред при необходимости может быть дополнена гормонами и/или другими факторами роста (такими как инсулин, трансферрин или эпидермальный фактор роста), солями (такими как хлорид натрия, кальция, магния и фосфата), буферами (такими как HEPES), нуклеотидами (такими как аденозин и тимидин), антибиотиками (такими как препарат GENTAMYCINT), микроэлементами (определяемыми как неорганические соединения, обычно присутствующими в конечных концентрациях в микромолярном диапазоне) и глюкозой или эквивалентным источником энергии. Также в соответствующих концентрациях могут быть включены любые другие необходимые добавки, которые известны специалистам в данной области. Условия культивирования, такие как температура, рН и тому подобное, являются такими, которые ранее использовались с клеткой-хозяином, выбранной для экспрессии, и будут очевидны для обычного специалиста в данной области.
[00338] При использовании рекомбинантных методик антитело можно продуцировать внутриклеточно, в периплазматическом пространстве или непосредственно секретировать в среду. Если антитело продуцируется внутриклеточно, то на первом этапе частицы дебриса, либо клетки-хозяева, либо лизированные фрагменты, удаляют, например, центрифугированием или ультрафильтрацией. Carter et al., Bio/Technology 10:163-167 (1992) описывают процедуру выделения антител, которые секретируются в периплазматическое пространство E.coli. Вкратце, клеточную пасту оттаивают в присутствии ацетата натрия (рН 3,5), EDTA и фенилметилсульфонилфторида (PMSF) в течение примерно 30 минут. Клеточный дебрис можно удалить центрифугированием. Когда антитело секретируется в среду, надосадочные жидкости из таких систем экспрессии обычно сначала концентрируют с использованием имеющегося в продаже фильтра для концентрирования белка, например, устройства для ультрафильтрации Amicon или Millipore Pellicon. Для ингибирования протеолиза на любой из вышеперечисленных стадий может быть включен ингибитор протеазы, такой как PMSF, и для предотвращения роста посторонних примесей могут быть включены антибиотики.
[00339] Анти-CLDN18.2 антитела и их антигенсвязывающие фрагменты, полученные из клеток, могут быть очищены с использованием, например, хроматографии на гидроксилапатите, гель-электрофореза, диализа, ионообменной хроматографии на DEAE-целлюлозе, осаждения сульфатом аммония, высаливания и аффинной хроматографии, при этом аффинная хроматография является предпочтительным методом очистки.
[00340] В некоторых вариантах осуществления изобретения для иммуноаффинной очистки антитела и его антигенсвязывающего фрагмента используют белок А, иммобилизованный на твердой фазе. Пригодность белка А в качестве аффинного лиганда зависит от вида и изотипа любого домена Fc иммуноглобулина, присутствующего в антителе. Белок А можно использовать для очистки антител, основанных на тяжелых цепях гамма1, гамма2 или гамма4 человека (Lindmark et al., J. Immunol. Meth. 62:1-13 (1983)). Для всех изотипов мыши и для гамма-3 человека рекомендуется белок G (Guss et al., EMBO J. 5:1567 1575 (1986)). Матрица, к которой присоединен аффинный лиганд, чаще всего представляет собой агарозу, но доступны и другие матрицы. Механически стабильные матрицы, такие как стекло с регулируемыми порами или поли(стиролдивинил)бензол, обеспечивают более высокую скорость потока и более короткое время обработки, чем при использовании агарозы. Если антитело содержит домен СН3, для очистки может быть использована смола Bakerbond ABX.TM. (J. T. Baker, Phillipsburg, N.J.). Также в зависимости от восстанавливаемого антитела доступны другие методы очистки белка, такие как фракционирование на ионообменной колонке, осаждение этанолом, ВЭЖХ с обращенной фазой, хроматография на силикагеле, хроматография на гепарине SEPHAROSETM, хроматография на анионообменной или катионообменной смоле (такой как колонка с полиаспарагиновой кислотой), хроматофокусирование, SDS-PAGE и осаждение сульфатом аммония.
[00341] После любой предварительной(ых) стадии(й) очистки смесь, содержащая представляющее интерес антитело и примеси, может быть подвергнута хроматографии с гидрофобным взаимодействием при низком рН с использованием элюирующего буфера при рН примерно 2,5-4,5, предпочтительно проводимой при низких концентрациях соли (например, примерно от 0 до 0,25 М соли).
[00342] Композиция
[00343] В другом аспекте в настоящем изобретении предложена композиция, содержащая анти-CLDN18.2 антитела или их антигенсвязывающие фрагменты.
[00344] В другом аспекте в настоящем изобретении предложена композиция, содержащая анти-CLDN18.2 антитела или их антигенсвязывающие фрагменты, которые афукозилированы. В некоторых вариантах осуществления изобретения анти-CLDN18.2 антитела в композиции имеют количество фукозы 60% или менее (например, менее чем 55%, 50%, 45%, 40%, 35%, 30%, 25%, 20%, 15% или 10%) от общего количества олигосахаридов (сахаров) по Asn297 согласно системе нумерации ЕС. Количество фукозы, присоединенной к домену CH2 Fc-области, можно определить путем расчета среднего количества фукозы в цепи сахара в Asn297 по отношению к сумме всех гликоструктур, присоединенных к Asn 297 (например, сложных, гибридных и структур с высоким содержанием маннозы). Количество фукозы можно измерить способами, известными в данной области техники, например, масс-спектрометрией. В иллюстративном варианте осуществления антитело обрабатывают N-гликозидазой (PNGaseF) для гидролиза олигосахарида цепи N-сахара из антитела. Гидролизованный олигосахарид метят реагентом флуоресцентного маркера RapiFluor-MS, разделяют с помощью сверхвысокоэффективной жидкофазной гидрофильной хроматографии и обнаруживают с помощью флуоресцентного детектора (UPLC-HILIC-FLR). Метод нормализации площади использовали для расчета доли различных олигосахаридов. В другом иллюстративном примере количество фукозы можно измерить масс-спектрометрией MALDI-TOF, как описано в WO 2008/077546.
[00345] Фармацевтическая композиция
[00346] В настоящем изобретении предложены, кроме того, фармацевтические композиции, содержащие анти-CLDN18.2 антитела или их антигенсвязывающие фрагменты (необязательно, афукозилированные) и один или несколько фармацевтически приемлемых носителей.
[00347] Фармацевтически приемлемые носители для применения в фармацевтических композициях, описанных в настоящем документе, могут включать, например, фармацевтически приемлемые жидкие, гелевые или твердые носители, водные носители, неводные носители, антимикробные агенты, изотонические агенты, буферы, антиоксиданты, анестетики, суспендирующие/диспергирующие агенты, связывающие или хелатирующие агенты, разбавители, адъюванты, эксципиенты или нетоксичные вспомогательные вещества, другие компоненты, известные в данной области, или их различные комбинации.
[00348] Подходящие компоненты могут включать, например, антиоксиданты, наполнители, связующие вещества, разрыхлители, буферы, консерванты, смазывающие вещества, ароматизаторы, загустители, красители, эмульгаторы или стабилизаторы, такие как сахара и циклодекстрины. Подходящие антиоксиданты могут включать, например, метионин, аскорбиновую кислоту, EDTA, тиосульфат натрия, платину, каталазу, лимонную кислоту, цистеин, тиоглицерин, тиогликолевую кислоту, тиосорбит, бутилированный гидроксанизол, бутилированный гидрокситолуол и/или пропилгаллат. Как описано в настоящем документе, включение одного или нескольких антиоксидантов, таких как метионин, в композицию, содержащую антитело или антигенсвязывающий фрагмент и конъюгаты, как предусмотрено в настоящем документе, снижает окисление антитела или антигенсвязывающего фрагмента. Это снижение окисления предотвращает или уменьшает потерю аффинности связывания, тем самым повышая стабильность антител и максимально увеличивая срок хранения. Таким образом, в некоторых вариантах осуществления предусмотрены композиции, которые содержат одно или несколько антител или антигенсвязывающих фрагментов, описанных в настоящем документе, и один или несколько антиоксидантов, таких как метионин. Кроме того, предложены способы предотвращения окисления, продления срока годности и/или повышения эффективности антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе, путем смешивания антитела или антигенсвязывающего фрагмента с одним или несколькими антиоксидантами, такими как метионин.
[00349] Для дополнительной иллюстрации, фармацевтически приемлемые носители могут включать, например, водные носители, такие как инъекция хлорида натрия, инъекция Рингера, инъекция изотонической декстрозы, инъекция стерильной воды или инъекция декстрозы и лактата Рингера, неводные носители, такие как нелетучие масла растительного происхождения, хлопковое масло, кукурузное масло, кунжутное масло или арахисовое масло, противомикробные агенты в бактериостатических или фунгистатических концентрациях, изотонические агенты, такие как хлорид натрия или декстроза, буферы, такие как фосфатные или цитратные буферы, антиоксиданты, такие как бисульфат натрия, местные анестетики, такие как гидрохлорид прокаина, суспендирующие и диспергирующие агенты, такие как карбоксиметилцеллюлоза натрия, гидроксипропилметилцеллюлоза или поливинилпирролидон, эмульгаторы, такие как полисорбат 80 (TWEEN-80), секвестрирующие или хелатирующие агенты, такие как EDTA (этилендиаминтетрауксусная кислота) или EGTA (этиленгликольтетрауксусная кислота), этиловый спирт, полиэтиленгликоль, пропиленгликоль, гидроксид натрия, соляная кислота, лимонная кислота или молочная кислота. К фармацевтическим композициям в многодозовых контейнерах могут быть добавлены антимикробные агенты, используемые в качестве носителей, которые включают фенолы или крезолы, ртутные соединения, бензиловый спирт, хлорбутанол, метил- и пропил-п-гидроксибензойные эфиры, тимеросал, хлорид бензалкония и хлорид бензетония. Подходящие эксципиенты могут включать, например, воду, физиологический раствор, декстрозу, глицерин или этанол. Подходящие нетоксичные вспомогательные вещества могут включать, например, смачивающие или эмульгирующие агенты, рН-буферные агенты, стабилизаторы, усилители растворимости или такие агенты, как ацетат натрия, монолаурат сорбитана, олеат триэтаноламина или циклодекстрин.
[00350] Фармацевтические композиции могут представлять собой жидкий раствор, суспензию, эмульсию, пилюлю, капсулу, таблетку, состав с замедленным высвобождением или порошок. Пероральные составы могут включать стандартные носители, такие как маннит фармацевтической степени чистоты, лактозу, крахмал, стеарат магния, поливинилпирролидон, сахарин натрия, целлюлозу, карбонат магния и т.д.
[00351] В некоторых вариантах осуществления изобретения фармацевтические композиции составляют в виде инъекционной композиции. Фармацевтические композиции для инъекций могут быть приготовлены в любой традиционной форме, такой как, например, жидкий раствор, суспензия, эмульсия или твердые формы, подходящие для получения жидкого раствора, суспензии или эмульсии. Препараты для инъекций могут включать стерильные и/или не вызывающие жара растворы, готовые для инъекций, стерильные сухие растворимые продукты, такие как лиофилизированные порошки, готовые для смешивания с растворителем непосредственно перед применением, включая таблетки для подкожных инъекций, стерильные суспензии, готовые для инъекций, стерильные сухие нерастворимые продукты, готовые к смешиванию с носителем непосредственно перед использованием, а также стерильные и/или непиретические эмульсии. Растворы могут быть как водными, так и неводными.
[00352] В некоторых вариантах осуществления изобретения парентеральные препараты с разовой дозой упакованы в ампулу, флакон или шприц с иглой. Все препараты для парентерального введения должны быть стерильными, а не пиретическими, как это известно и практикуется в данной области.
[00353] В некоторых вариантах осуществления изобретения стерильный лиофилизированный порошок получают путем растворения антитела или его антигенсвязывающего фрагмента, как описано в настоящем документе, в подходящем растворителе. Растворитель может содержать вспомогательное вещество, улучшающее стабильность, или другие фармакологические компоненты порошка или восстановленного раствора, приготовленного из порошка. Эксципиенты, которые могут быть использованы, включают, но не ограничиваются ими, воду, декстрозу, сорбитал, фруктозу, кукурузный сироп, ксилит, глицерин, глюкозу, сахарозу или другой подходящий агент. Растворитель может содержать буфер, такой как цитрат, фосфат натрия или калия, или другой подобный буфер, известный специалистам в данной области техники, в одном варианте осуществления с примерно нейтральным рН. Последующая стерильная фильтрация раствора с последующей лиофилизацией в стандартных условиях, известных специалистам в данной области, дает желаемый состав. В одном варианте полученный раствор распределяют по флаконам для лиофилизации. Каждый флакон может содержать одну дозу или несколько доз анти-CLDN18.2 антитела или его антигенсвязывающего фрагмента или их композиции. Допускается переполнение флаконов небольшим количеством сверх необходимого для дозы или набора доз (например, около 10%), чтобы облегчить точный отбор пробы и точное дозирование. Лиофилизированный порошок можно хранить в соответствующих условиях, например, при температуре от примерно 4°C до комнатной температуры.
[00354] Восстановление лиофилизированного порошка водой для инъекций дает состав для применения при парентеральном введении. В одном варианте осуществления для восстановления к лиофилизированному порошку добавляют стерильную и/или апиретическую воду или другой жидкий подходящий носитель. Точное количество зависит от выбранной терапии и может быть определено эмпирически.
[00355] Способы применения
[00356] В настоящем изобретении также предложены терапевтические способы, включающие: введение терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента, предложенного в настоящем документе (необязательно афукозилированного), и/или фармацевтической композиции, представленного в настоящем документе, субъекту, нуждающемуся в этом, тем самым осуществляя лечение или предотвращение заболевания или состояния, связанного с CLDN18.2.
[00357] В другом аспекте способы предложены способы лечения заболевания или состояния у субъекта, для которых было бы полезно модулировать активность CLDN18.2, включающие введение терапевтически эффективного количества антитела или антигенсвязывающего фрагмента, как предусмотрено в настоящем документе (необязательно афукозилированного) и/или фармацевтической композиции, предоставленной в настоящем документе субъекту, нуждающемуся в этом. В некоторых вариантах осуществления изобретения заболевание или состояние представляет собой заболевание или состояние, связанное с CLDN18.2. В некоторых вариантах осуществления изобретения заболевание или состояние, связанное с CLDN18.2, представляет собой рак.
[00358] В некоторых вариантах осуществления изобретения рак выбран из рака желудка, рака легких, рака бронхов, рака костей, рака печени и желчных протоков, рака поджелудочной железы, рака молочной железы, рака печени, рака яичников, рака яичка, рака почки, рака мочевого пузыря, рака головы и шеи, рака позвоночника, рака головного мозга, рака шейки матки, рака матки, рака эндометрия, рака толстой кишки, колоректального рака, рака прямой кишки, рака анального канала, рака пищевода, рака желудочно-кишечного тракта, рака кожи, рака предстательной железы, рака гипофиза, рака желудка, рака влагалища, рака щитовидной железы, глиобластомы, астроцитомы, меланомы, миелодиспластического синдрома, саркомы, тератомы и аденокарциномы.
[00359] Примеры рака включают, но не ограничиваются ими, немелкоклеточный рак легкого (плоскоклеточный/неплоскоклеточный), мелкоклеточный рак легкого, почечно-клеточный рак, колоректальный рак, рак толстой кишки, рак яичников, рак молочной железы (включая базальную карциному молочной железы, протоковую карциному и лобулярную карциному молочной железы), рак поджелудочной железы, карциному желудка, рак мочевого пузыря, рак пищевода, мезотелиому, меланому, рак головы и шеи, рак щитовидной железы, саркому, рак предстательной железы, глиобластому, рак шейки матки, карциному тимуса, меланому, миелому, грибовидные микозы, рак из клеток Меркеля, гепатоцеллюлярную карциному (HCC), фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому и другие саркомы, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, лимфоидную злокачественную опухоль, базально-клеточную карциному, аденокарциному, карциному потовых желез, медуллярную карциному щитовидной железы, папиллярную карциному щитовидной железы, феохромоцитомы, карциному сальных желез, папиллярную карциному, папиллярную аденокарциному, медуллярную карциному, бронхогенную карциному, гепатому, карциному желчных протоков, хориокарциному, опухоль Вильмса, рак шейки матки, опухоль яичка, семиному, классическую лимфому Ходжкина (CHL), медиастинальную крупноклеточную В-клеточную лимфому, Т-клеточную/богатую гистиоцитами В-клеточную лимфому, острый лимфоцитарный лейкоз, острый миелоцитарный лейкоз, острый миелогенный лейкоз, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический миелогенный лейкоз, хронический лимфолейкоз, истинную полицитемию, опухоли, происходящие из тучных клеток, EBV-положительные и -отрицательные PTLD и диффузную крупноклеточную B-клеточную лимфому (DLBCL), плазмобластную лимфому, экстранодальную NK/T-клеточную лимфому, назофарингеальную карциному, первичную выпотную лимфому, ассоциированную с HHV8, неходжкинскую лимфому, множественную миелому, макроглобулинемию Вальденстрема, болезнь тяжелых цепей, миелодиспластический синдром, волосатоклеточный лейкоз и миелодисплазию, первичную лимфому ЦНС, опухоль оси позвоночника, глиому ствола головного мозга, астроцитому, медуллобластому, краниофариому, эпендимому, пинеалому, гемангиобластому, акустическую неврому, олигодендроглиому, менангиому, меланому, нейробластому и ретинобластому.
[00360] В некоторых вариантах осуществления изобретения рак представляет собой рак, экспрессирующий CLDN18.2. Термин «рак, экспрессирующий CLDN18.2», используемый в данном документе, относится к любому раку или опухоли, включающей раковые клетки, экспрессирующие CLDN18.2.
[00361] В некоторых вариантах осуществления изобретения у субъекта идентифицирована раковая клетка, экспрессирующая CLDN18.2. Присутствие и/или уровень экспрессии CLDN18.2 в раковой клетке можно определить различными способами, известными в данной области. Биологический образец, содержащий или предположительно содержащий раковую клетку, может быть получен от субъекта. В некоторых вариантах осуществления изобретения биологический образец может быть получен из раковой клетки или раковой ткани, или иммунных клеток, инфильтрирующих опухоль. В некоторых вариантах осуществления изобретения биологический образец может быть дополнительно обработан, например, для выделения анализируемого вещества, такого как нуклеиновые кислоты или белки. Присутствие и/или уровень экспрессии CLDN18.2 можно определить, например, с помощью количественной флуоресцентной цитометрии, иммуногистохимии (IHC) или методов на основе нуклеиновых кислот. Например, биологический образец от субъекта может подвергаться воздействию антитела против CLDN18.2 или его антигенсвязывающего фрагмента, которые связываются с экспрессированным белком CLDN18.2 и обнаруживают его. Альтернативно, CLDN18.2 также можно обнаружить на уровне экспрессии нуклеиновой кислоты с использованием таких методов, как количественная PCR, PCR с обратной транскриптазой, микрочип, SAGE, FISH и тому подобное.
[00362] В некоторых вариантах осуществления изобретения экспрессию CLDN18.2 в биологическом образце или раковой клетке определяют или измеряют с помощью IHC. В некоторых вариантах осуществления изобретения уровень экспрессии человеческого белка CLDN18.2 на раковой клетке субъекта можно определить в соответствии со способами, описанными в разделе 6 и разделе 7 примера 15, приведенного в настоящем документе.
[00363] В некоторых вариантах осуществления изобретения субъект идентифицирован как имеющий раковые клетки, высэкспрессирующие CLDN18.2, раковые клетки, среднеэкспрессирующие CLDN18.2, или раковые клетки, низкоэкспрессирующие CLDN18.2. В некоторых вариантах осуществления изобретения раковая клетка с высоким уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью по меньшей мере 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 40% (например, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, 40-100%, 50-100%, 60-100%, 70-100%, 80-100%, 90-100%, 40-90%, 50-90%, 60-90%, 70-90%, 80-90%, 40-80%, 40-70%, 40-60%, 40-50%, 50-80%, 50-70%, 50-60%, 60-80%, 60-70% или 70-80%) клеток окрашиваются положительно при IHC; среднеэкспрессирующие раковые клетки экспрессируют CLDN18.2 с интенсивностью по меньшей мере 1+ и ниже 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 30% (или по меньшей мере 35%), но ниже 40% клеток окрашиваются положительно при IHC; и низкоэкспрессирующие раковые клетки экспрессируют CLDN18.2 с интенсивностью около 0, но ниже 1+, как определено с помощью IHC, и на уровне, где около 0, но ниже 30% (например, 5%, 10%, 15%, 20%, 25%, 5-25%, 10-25%, 15-25%, 20-25%, 5-20%, 5-15%, 5-10%, 10-20%, или 10-15%) клеток окрашиваются положительно при IHC.
[00364] Примеры рака, экспрессирующего CLDN18.2, включают, без ограничения, рак желудка, рак пищевода, рак поджелудочной железы, рак легких, такой как немелкоклеточный рак легкого (NSCLC) и мелкоклеточный рак легкого (SCLC), рак яичников, рак толстой кишки, колоректальный рак, стромальные опухоли желудочно-кишечного тракта (GIST), карциноидные опухоли желудочно-кишечного тракта, рак прямой кишки, рак анального канала, рак желчных протоков, рак тонкой кишки, рак аппендикса; рак предстательной железы, рак почки (например, почечно-клеточная карцинома), рак печени, рак головы и шеи и рак желчного пузыря и его метастазы, например, метастазы рака желудка, такие как опухоли Крукенберга, метастазы в брюшную полость и метастазы в лимфатические узлы.
[00365] В некоторых вариантах осуществления изобретения рак, экспрессирующий CLDN18.2, может представлять собой аденокарциному, например, запущенную аденокарциному. В некоторых вариантах осуществления изобретения рак выбран из аденокарциномы желудка, пищевода, протока поджелудочной железы, желчных протоков, легкого и яичника. В некоторых вариантах осуществления изобретения рак, экспрессирующий CLDN18.2, включает рак желудка, рак пищевода, в частности, нижнего отдела пищевода, рак пищеводно-желудочного перехода и гастроэзофагеальный рак.
[00366] Без привязки к каким-либо теориям считается, что молекулярные и функциональные характеристики CLDN18 делают его очень интересной мишенью для терапии рака на основе антител. К ним относятся (i) отсутствие CLDN18 в большинстве нормальных тканей, имеющих отношение к токсичности, (ii) ограничение экспрессии варианта CLDN18.2 замещающей клеточной популяцией в виде дифференцированных клеток желудка, которые могут быть восполнены за счет негативных по мишеням стволовых клеток желудка, (iii) потенциальное дифференциальное гликозилирование между нормальными и неопластическими клетками и (iv) наличие различных конформационных топологий.
[00367] Было обнаружено, что молекулярная масса белка CLDN18 различается между опухолями и соседними нормальными тканями. Белок CLDN18 с более высокой молекулярной массой наблюдается в здоровых тканях, который может быть снижен до той же молекулярной массы, что и в опухоли, путем обработки лизатов нормальных тканей дегликозилирующим соединением PNGase F. Это предполагает, что CLDN18 менее N-гликозилирован в опухоли, чем по сравнению с аналогом из нормальной ткани. Классический мотив N-гликозилирования находится в аминокислотном остатке 116 в домене петли D3 молекулы CLDN18. Разница в молекулярной массе и предполагаемая структурная разница могут представлять собой измененный эпитоп для связывания антител.
[00368] Кроме того, CLDN18 в качестве белка с плотными контактами также может способствовать хорошему терапевтическому диапазону. Поскольку опухолевые клетки экспрессируют CLDN, но часто не образуют классических плотных контактов за счет гомотипической и гетеротипической ассоциации CLDN, обнаруженной в нормальной эпителиальной ткани, они, вероятно, имеют значительный пул свободных CLDN, которые поддаются связыванию внеклеточных антител и иммунотерапии. Возможно, что связывающие эпитопы CLDN в здоровом эпителии защищены плотными соединениями от доступа к связыванию антител.
Терапевтически эффективное количество антитела или антигенсвязывающего фрагмента, как предусмотрено в настоящем документе, будет зависеть от различных факторов, известных в данной области техники, таких как, например, масса тела, возраст, история болезни в прошлом, принимаемые лекарства, состояние здоровья субъекта и возможность перекрестная реакция, аллергия, чувствительность и неблагоприятные побочные эффекты, а также путь введения и степень развития заболевания. Дозы могут быть пропорционально уменьшены или увеличены специалистом в данной области (например, врачом или ветеринаром) в зависимости от этих и других обстоятельств или требований.
[00370] В некоторых вариантах осуществления изобретения антитело или антигенсвязывающий фрагмент, представленные в настоящем документе, можно вводить в терапевтически эффективной дозе от примерно 0,01 мг/кг до примерно 100 мг/кг. В некоторых вариантах осуществления доза введения может меняться в течение курса лечения. В некоторых вариантах осуществления доза введения может меняться в течение курса лечения в зависимости от реакции субъекта.
[00371] Режимы дозирования могут быть скорректированы для обеспечения оптимального желаемого ответа (например, терапевтического ответа). Например, можно вводить одну дозу или можно вводить несколько разделенных доз в течение времени.
[00372] Антитела и антигенсвязывающие фрагменты, описанные в настоящем документе, можно вводить любым путем, известным в данной области, таким как, например, парентеральный (например, подкожный, внутрибрюшинный, внутривенный, включая внутривенную инфузию, внутримышечную или внутрикожную инъекцию) или не-парентеральный (например, пероральный, интраназальный, внутриглазной, сублингвальный, ректальный или местный) пути введения.
[00373] В некоторых вариантах осуществления изобретения антитела или антигенсвязывающие фрагменты, описанные в настоящем документе, можно вводить отдельно или в комбинации с одним или несколькими дополнительными терапевтическими средствами или агентами. Например, антитела или антигенсвязывающие фрагменты, описанные в настоящем документе, можно вводить в комбинации со вторым терапевтическим средством, например, химиотерапевтическим средством, противоопухолевым средством, лучевой терапией, иммунотерапией, средством против ангиогенеза, таргетной терапией, клеточной терапией, генной терапией, гормональной терапией, паллиативным лечением, хирургическим вмешательством для лечения рака (например, опухолеэктомия) или одним или несколькими противорвотными средствами или другими средствами для лечения осложнений, возникающих в результате химиотерапии.
[00374] Термин «иммунотерапия», как используется в настоящем документе, относится к типу, который стимулирует иммунную систему для борьбы с таким заболеванием, как рак, или который укрепляет иммунную систему в целом. Иммунотерапия включает пассивную иммунотерапию путем доставки агентов с установленной опухолеиммунной реактивностью (таких как эффекторные клетки), которые могут прямо или косвенно опосредовать противоопухолевые эффекты и не обязательно зависят от интактной иммунной системы хозяина (например, терапия антителами или терапия CAR-T-клетками). Иммунотерапия может дополнительно включать активную иммунотерапию, при которой лечение основано на стимуляции in vivo эндогенной иммунной системы хозяина, чтобы она реагировала на больные клетки введением агентов, модифицирующих иммунный ответ.
[00375] Примеры иммунотерапии включают, без ограничения, модуляторы контрольных точек, адоптивный перенос клеток, цитокины, онколитический вирус и терапевтические вакцины.
[00376] Модуляторы контрольных точек могут препятствовать способности раковых клеток избегать атаки иммунной системы и помогать иммунной системе более сильно реагировать на опухоль. Молекула иммунной контрольной точки может опосредовать костимулирующий сигнал для усиления иммунного ответа или может опосредовать ко-ингибирующие сигналы для подавления иммунного ответа. Примеры модуляторов контрольных точек включают, без ограничения, модуляторы PD-1, PD-L1, PD-L2, CLTA-4, TIM-3, LAG3, A2AR, CD160, 2B4, TGFβ, VISTA, BTLA, TIGIT, LAIR1, OX40, CD2, CD27, CD28, CD30, CD40, CD122, ICAM-1, IDO, NKG2C, SLAMF7, SIGLEC7, NKp80, CD160, B7-H3, LFA-1, 1COS, 4-1BB, GITR, BAFFR, HVEM, CD7, LIGHT, IL-2, IL-15, CD3, CD16 и CD83.
[00377] Адаптивный перенос клеток, который представляет собой лечение, направленное на усиление естественной способности Т-клеток бороться с раком. При этом лечении Т-клетки берутся у пациента, размножаются и активируются in vitro. В некоторых вариантах осуществления Т-клетки in vitro модифицируют до CAR-T-клеток. Т-клетки или CAR-T-клетки, наиболее активные в отношении рака, культивируют большими партиями in vitro в течение от 2 до 8 недель. В течение этого периода пациенты будут проходить такие процедуры, как химиотерапия и лучевая терапия, чтобы снизить иммунитет организма. После этих процедур культивированные in vitro Т-клетки или CAR-T-клетки будут возвращены пациенту. В некоторых вариантах осуществления иммунотерапия представляет собой терапию CAR-T.
[00378] Цитокиновую терапию также можно использовать для усиления представления опухолевого антигена иммунной системе. Двумя основными типами цитокинов, используемых для лечения рака, являются интерфероны и интерлейкины. Примеры цитокиновой терапии включают, без ограничения, интерфероны, такие как интерферон-α, -β и -γ, колониестимулирующие факторы, такие как макрофагальный-CSF, гранулоцитарный-макрофагальный CSF и гранулоцитарный-CSF, фактор роста инсулина (IGF-1), фактор роста эндотелия сосудов (VEGF), трансформирующий фактор роста (TGF), фактор роста фибробластов (FGF), интерлейкины, такие как IL-1, IL-1α, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11 и IL-12, факторы некроза опухоли, такие как TNF-α и TNF-β, или любая их комбинация.
[00379] Онколитические вирусы представляют собой генетически модифицированные вирусы, способные убивать раковые клетки. Онколитический вирус может специфически инфицировать опухолевые клетки, тем самым приводя к лизису опухолевых клеток с последующим высвобождением большого количества опухолевых антигенов, которые запускают иммунную систему для нацеливания и уничтожения раковых клеток, содержащих такие опухолевые антигены. Примеры онколитического вируса включают, без ограничения, талимоген лахерпарепвек.
[00380] Терапевтические вакцины действуют против рака, усиливая реакцию иммунной системы на раковые клетки. Терапевтические вакцины могут содержать непатогенный микроорганизм (например, Mycobacterium bovis Bacillus Calmette-Guérin, BCG), генетически модифицированный вирус, нацеленный на опухолевую клетку, или один или несколько иммуногенных компонентов. Например, BCG может быть введена непосредственно в мочевой пузырь с помощью катетера и может вызвать иммунный ответ против клеток рака мочевого пузыря.
[00381] Средство против ангиогенеза может блокировать рост кровеносных сосудов, поддерживающих рост опухоли. Некоторые антиангиогенные агенты нацелены на VEGF или его рецептор VEGFR. Примеры средства против ангиогенеза включают, без ограничения, акситиниб, бевацизумаб, кабозантиниб, эверолимус, леналидомид, ленватиниба мезилат, пазопаниб, рамуцирумаб, регорафениб, сорафениб, сунитиниб, талидомид, вандетаниб и зив-афлиберцепт.
[00382] «Таргетная терапия» представляет собой тип терапии, который воздействует на определенные молекулы, связанные с раком, такие как определенные белки, которые присутствуют в раковых клетках, но не в нормальных клетках, или которые более распространены в раковых клетках, или молекулы-мишени в микроокружение рака, которое способствует росту и выживанию рака. Таргетная терапия направляет терапевтический агент на опухоль, тем самым защищая нормальную ткань от эффектов терапевтического агента.
[00383] Таргетная терапия может быть нацелена, например, на тирозинкиназные рецепторы и ядерные рецепторы. Примеры таких рецепторов включают erbB1 (EGFR или HER1), erbB2 (HER2), erbB3, erbB4, FGFR, рецептор тромбоцитарного фактора роста (PDGFR) и рецептор инсулиноподобного фактора роста-1 (IGF-1R), эстрогеновые рецепторы (ER), ядерные рецепторы (NR) и PR.
[00384] Таргетная терапия может быть нацелена на молекулы тирозинкиназы или сигнального каскада ядерных рецепторов, такие как Erk и PI3K/Akt, AP-2α, AP-2β, AP-2γ, митоген-активируемая протеинкиназа (MAPK), PTEN, p53, p19ARF, Rb, Apaf-1, CD-95/Fas, TRAIL-R1/R2, каспаза-8, Forkhead, Box 03A, MDM2, IAP, NF-kB, Myc, P13K, Ras, FLIP, херегулин (HRG) (также известный как gp30), Bcl-2, Bcl-xL, Bax, Bak, Bad, Bok, Bik, Blk, Hrk, BNIP3, BimL, Bid и EGL-1.
[00385] Таргетная терапия может также воздействовать на ассоциированные с опухолью лиганды, такие как эстроген, эстрадиол (E2), прогестерон, эстроген, андроген, глюкокортикоид, пролактин, гормон щитовидной железы, инсулин, белок киназы P70 S6 (PS6), сурвивин, факторы роста фибробластов (FGF), EGF, фактор дифференцировки Neu (NDF), трансформирующий фактор роста альфа (TGF-α), IL-1A, TGF-бета, IGF-1, IGF-II, IGFBP, IGFBP протеазы и IL-10.
[00386] В некоторых из этих вариантов осуществления антитело или его антигенсвязывающий фрагмент, описанные в настоящем документе, которые вводят в комбинации с одним или несколькими дополнительными терапевтическими средствами, можно вводить одновременно с одним или несколькими дополнительными терапевтическими средствами, и в некоторых из этих вариантов осуществления антитело или его антигенсвязывающий фрагмент и дополнительное(ые) терапевтическое(ие) средство(а) можно вводить как часть одной и той же фармацевтической композиции. Однако антитело или его антигенсвязывающий фрагмент, вводимые «в комбинации» с другим терапевтическим средством, не обязательно вводить одновременно с этим средством или в той же композиции, что и это средство. Антитело или его антигенсвязывающий фрагмент, вводимые до или после другого агента, считаются вводимыми «в комбинации» с этим агентом, как используется в данном документе, даже если антитело или антигенсвязывающий фрагмент и второй агент вводятся разными путями. По возможности, дополнительные терапевтические средства, вводимые в комбинации с антителами или антигенсвязывающими фрагментами, описанными в настоящем документе, вводят в соответствии со схемой, приведенной в информационном листке дополнительного терапевтического средства, или в соответствии со справочником Physicians' Desk Reference 2003 (Physicians' Desk Reference, 57th Ed; Medical Economics Company; ISBN: 1563634457; 57th edition (November 2002)) или протоколами, хорошо известными в данной области техники.
[00387] В настоящем изобретении предложены, кроме того, способы применения анти-CLDN18.2 антител или их антигенсвязывающие фрагменты. В некоторых вариантах осуществления изобретения в настоящем изобретении предложены способы подавления роста клеток, экспрессирующих CLDN18.2 in vivo или in vitro, включающий: приведение в контакт клеток, экспрессирующих CLDN18.2, с антителом или его антигенсвязывающим фрагментом, предложенными в настоящем документе. В некоторых вариантах осуществления изобретения в настоящем изобретении предложены способы модулирования активности CLDN18.2 в клетках, экспрессирующих CLDN18.2, включающие воздействие на клетки, экспрессирующие CLDN18.2, антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе.
[00388] В некоторых вариантах осуществления изобретения в настоящем изобретении предложены способы обнаружения присутствия или количества CLDN18.2 в образце, полученном от субъекта, включающие приведение образца в контакт с антителом или его антигенсвязывающим фрагментом, и определение присутствия или количества CLDN18.2 в образце. В некоторых вариантах осуществления изобретения биологический образец содержит раковую клетку.
[00389] В некоторых вариантах осуществления изобретения в настоящем изобретении предложены способы диагностики заболевания или состояния, связанного с CLDN18.2, у субъекта, включающие: a) приведение в контакт образца, полученного от субъекта, с антителом или его антигенсвязывающим фрагментом, предложенными в настоящем документе; b) определение наличия или количества CLDN18.2 в образце; и c) сопоставление наличия или количества CLDN18.2 с наличием или статусом связанного с CLDN18.2 заболевания или состояния у субъекта. В некоторых вариантах осуществления изобретения биологический образец содержит раковую клетку. В некоторых вариантах осуществления изобретения уровень экспрессии CLDN18.2 в раковой клетке определяют с помощью IHC (например, в соответствии со способами, описанными в разделе 6 и разделе 7 примера 15, представленного в настоящем документе). В некоторых вариантах осуществления изобретения субъект идентифицирован как имеющий раковую клетку с высоким уровнем экспрессии CLDN18.2, раковую клетку со средним уровнем экспрессии CLDN18.2 или раковую клетку с низким уровнем экспрессии CLDN18.2.
[00390] В некоторых вариантах осуществления изобретения способ включает, кроме того, введение субъекту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе. В некоторых вариантах осуществления изобретения субъект имеет раковую клетку со средним уровнем экспрессии CLDN18.2, или раковую клетку с низким уровнем экспрессии CLDN18.2.
[00391] В некоторых вариантах осуществления изобретения в настоящем изобретении предложены наборы, содержащие антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, необязательно, конъюгированные с обнаруживаемым фрагментом. Наборы могут быть использованы для обнаружения присутствия или количества CLDN18.2 в биологическом образце или могут быть использованы в способах диагностики, представленных в настоящем документе.
[00392] В некоторых вариантах осуществления изобретения в настоящем изобретении предложено наборы, содержащие антитело или его антигенсвязывающий фрагмент, предложенные в настоящем документе, и второй терапевтический агент. Наборы могут быть использованы для лечения, профилактики и/или облегчения заболевания, связанного с CLDN18.2.
[00393] В некоторых вариантах осуществления изобретения в настоящем изобретении предложено также применение антитела или его антигенсвязывающего фрагмента, предложенные в настоящем документе, при изготовлении медицинского препарата для лечения у субъекта заболевания или состояния, связанного с CLDN18.2.
Примеры
[00395] Хотя изобретение было конкретно показано и описано со ссылкой на конкретные варианты осуществления (некоторые из которых являются предпочтительными вариантами осуществления), специалистам в данной области должно быть понятно, что в них могут быть внесены различные изменения в форме и деталях, не отступая от сущности и объема настоящего изобретения, описанного в настоящем документе.
Пример 1: Получение клеточных линий, экспрессирующих CLDN18.2 или CLDN18.1
[00395] 1. Получение клеточных линий HEK293-CLDN18.2 человека, HEK293-CLDN18.1 человека и HEK293-CLDN18.2 мыши
[00396] Клетка HEK293-CLDN18.2 человека (именуемая далее как HEK293-CLDN18.2) и клетка HEK293-CLDN18.2 мыши (именуемая далее HEK293-mCLDN18.2) были сконструированы компанией MabSpace Biosciences (Suzhou) Co., Limited. Вкратце, клетку HEK293 (Shanghai Institutes for Biological Sciences, кат. № GNhu43) трансфицировали плазмидами pcDNA3.1/hCLDN18.2 или pcDNA3.1/mCLDN18.2 и отбирали с помощью G418 с получением стабильно экспрессирующей клеточной линии HEK293-CLDN18.2 или HEK293-mCLDN18.2. Уровень экспрессии hCLDN18.2 или mCLDN18.2 определяли с помощью антитела IMAB362, которое может связываться с CLDN18.2 как человека, так и мыши. IMAB362 экспрессировали в соответствии с последовательностью, описанной в US2009169547A1. Клон одной клетки с самым высоким сигналом отбирали и амплифицировали для банка клеток.
[00397] Вариабельная область тяжелой цепи IMAB362 (SEQ ID NO: 72)
QVQLQQPGAELVRPGASVKLSCKASGYTFTSYWINWVKQRPGQGLEWIGNIYPSDSYTNYNQKFKDKATLTVDKSSSTAYMQLSSPTSEDSAVYYCTRSWRGNSFDYWGQGTTLTVSS
[00398] Вариабельная область легкой цепи IMAB362 (SEQ ID NO: 73)
DIVMTQSPSSLTVTAGEKVTMSCKSSQSLLNSGNQKNYLTWYQQKPGQPPKLLIYWASTRESGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCQNDYSYPFTFGSGTKLEIK
[00399] Клетки HEK293-CLDN18.1 человек (именуемые далее как HEK293-CLDN18.1) также конструировали, как описано выше. Экспрессию CLDN18.1 определяли с помощью анти-CLDN18 антитела (Abcam, кат. № ab222513), которое распознает как CLDN18.1, так и CLDN18.2.
[00400] 2. Получение клетки CHO-CLDN18.2, транзиентно экспрессирующей
[00401] Клетка, экспрессирующая CHO-CLDN18.2Ю была сконструюрована следующим образом: клетки CHO транзиентно трансфицировали с помощью pcDNA3.1/CLDN18.2 без реагента для селекции. Белок клеточной мембраны экстрагировали с использованием набора Mem-PER™ Plus Membrane Protein Extraction Kit и использовали для бустерной иммунизации животных.
[00402] 3. Получение клетки MKN45-CLDN18.2, транзиентно экспрессирующей
[00403] Клетка MKN45-CLDN18.2 была сконструирована компанией MabSpace Biosciences (Suzhou) Co., Limited. Вкратце, клетку MKN45 (National Infrastructure of Cell Line Resource, кат. № 3111C0001CCC000229) трансфицировали плазмидами pcDNA3.1/CLDN18.2 и отбирали с помощью G418 с получением стабильно экспрессирующей клеточной линии MKN45-CLDN18.2. Уровень экспрессии CLDN18.2 определяли с помощью антитела IMAB362 с использованием метода FACS. Моноклональные клетки с самым высоким, средним и низким сигналом отбирали и амплифицировали для банка клеток.
[00404] В следующих экспериментах использовали указанные выше клеточные линии.
Пример 2: Получение антител
[00405] 1. Иммунизация
[00406] Для иммунизации готовили иммуноген как ДНК, так и клеточный. 6-8 недельных мышей разных линий разделяли на 2 группы. Одну инициировали и стимулировали с помощью внутривенной инъекции 100 мкг/мышь плазмиды pVAC2-mcs/CLDN18.2 и 100 мкг/мышь CpG. Другой внутримышечно инъецировали те же ДНК и CpG. Обеим группам на 1-й и 10-й день вводили инъекции и на 18-й день определяли титр антител с помощью FACS-связывания с клеткой HEK293-CLDN18.2. В планшет, содержащий клетки HEK293-CLDN18.2 или рака желудка NUGC4 (JCRB, кат. № JCRBB0834) добавляли 100 мкл/лунку разбавленной мышиной сыворотки и затем инкубировали при температуре 4°C в течение 30 мин. После промывки буфером при температуре 4°C в течение 30 мин для повторной инкубации добавляли 100 мкл/лунку козьего анти-mIgG-FITC (разведение 1:500). После промывки буфером для промывки FACS клетки анализировали с помощью проточной цитометрии. Мышей с более высоким сигналом связывания и титром отбирали для следующих процедур слияния.
[00407] 2. Слияния
[00408] За четыре дня до слияния каждую мышь стимулировали внутрибрюшинным введением 5×107 клеток HEK293-CLDN18.2. В день слияния селезенки удаляли в асептических условиях и затем перерабатывали в суспензию отдельных клеток. Жизнеспособные клетки миеломы логарифмической фазы (SP2/0) смешивали с мышиными спленоцитами в соотношении 1:1 в среде для слияния с последующим электрослиянием в течение 1 мин. Клетки ресуспендировали и культивировали в 96-луночных культуральных планшетах по 200 мкл/лунку в инкубаторе при температуре 37°C, 5% CO2. После 7-дневного культивирования питательную среду заменяли на свежую питательную среду с последующим скринингом супернатантов гибридом через 2-3 дня.
Пример 3: Скрининг антител
[00409] 1. Скрининг положительных связующих CLDN18.2 человека с помощью анализа FACS
[00410] Клетки CLDN18.2, экспрессирующие HEK293-CLDN18.2 в логарифмической фазе, ресуспендировали в PBS при плотности 105/100 мкл на лунку. После 3-кратного промывания клеток буфером для промывки FACS (PBS+2% FBS) в каждую лунку добавляли 100 мкл/лунку супернатанта гибридомы для инкубации при температуре 4°C в течение 30 мин. Клетки снова промывали 3 раза, используя промывочный буфер FACS, и затем инкубировали со 100 мкл/лунку козьего анти-mIgG-FITC (разведение1:400) при температуре 4°C в течение еще 30 мин. После последней 3-кратной промывки с использованием промывочного буфера FACS клетки анализировали с помощью проточной цитометрии.
[00411] 2. Скрининг отрицательных связующих CLDN18.1 с помощью анализа FACS
[00412] Клетки CLDN18.1 в логарифмической фазе , экспрессирующие HEK293-CLDN18.1, ресуспендировали в PBS при плотности 105/100 мкл на лунку. После 3-кратного промывания клеток буфером для промывки FACS (PBS+2% FBS) в каждую лунку добавляли 100 мкл/лунку супернатанта гибридомы для инкубации при температуре 4°C в течение 30 мин. Клетки снова промывали 3 раза, используя промывочный буфер FACS, и затем инкубировали со 100 мкл/лунку козьего анти-mIgG-FITC (разведение 1:400) при температуре 4°C в течение еще 30 мин. После последней 3-кратной промывки с использованием промывочного буфера FACS клетки анализировали с помощью проточной цитометрии.
[00413] Отбирали клоны с высоким уровнем сигнала связывания CLDN18.2, но без связывания CLDN18.1, для последующего субклонирования с получением моноклонов, включая 7C12, 11F12, 12E9, 26G6, 59A9, 18B10 и 12C12.
Пример 4: Субклонирование положительных гибридомных клонов и производство антител в небольших масштабах
[00414] 1. Субклонирование положительных гибридомных клонов
[00415] Клетки из лунок FACS-положительной гибридомы с желаемым профилем связывания отбирали для ограниченного разведения в 96-луночных планшетах. Этим клеткам давали расти в течение 7 дней. После достижения адекватной клеточной массы супернатант из каждой лунки собирали и подвергали повторному скринингу с использованием анализа связывания клеток (см. пример 3).
[00416] Из каждого 96-луночного планшета клон с самой высокой активностью связывания клеток размножали для 2-го раунда ограниченного разведения в 96-луночном планшете с 200 мкл ростовой среды гибридомы на лунку. Через 7 дней супернатант клеток из 96-луночных планшетов анализировали с помощью анализа FACS. Субклонирование проводили более 2 раз, пока более чем в 90/96 лунках не появился положительный сигнал связывания. Клоны с самой высокой связывающей активностью идентифицировали, дополнительно размножали и культивировали для продукции антител. Изотипы определяли стандартным методом.
[00417] 2. Маломасштабное производство антител
[00418] Клетки гибридомы инокулировали и культивировали в течение 14 дней. Моноклональные антитела (mAb) CLDN18.2 очищали из культуры клеток гибридомы с помощью аффинной хроматографии с использованием хроматографической колонки с протеином А (Protein A Высоко Performance (Bio-Rad)).
[00419] После очистки mAb CLDN18.2 готовили в PBS путем диализа с использованием мембран 10000 MWCO (Pierce Slide-A-Lyzer или диализных трубок) с последующей стадией фильтрации.
Пример 5: Анализ связывания клеток с очищенным гибридомным антителом CLDN18.
[00420] Клетки HEK293-CLDN18.2 и NUGC4 в логарифмической фазе ресуспендировали в PBS. После 3-кратного промывания клеток буфером для промывки FACS (PBS+2% FBS) в каждую лунку добавляли по 100 мкл/лунку разбавленных гибридомных антител в диапазоне от 400 нМ до 0,002 нМ для инкубации при температуре 4°C в течение 30 мин. Клетки снова промывали 3 раза, используя промывочный буфер FACS, и затем инкубировали со 100 мкл/лунку козьего анти-mIgG-FITC (разведение 1:400) при температуре 4°C в течение еще 30 мин. После последней 3-кратной промывки с использованием промывочного буфера FACS клетки анализировали с помощью проточной цитометрии.
[00421] Большинство гибридомных антител демонстрировали высокую аффинность связывания с клетками HEK293-CLDN18.2, но меньшее связывание с клетками NUGC4. Разница в связывании, вероятно, связана с разной плотностью экспрессии, конформацией и/или статусом гликозилирования белка CLDN18.2 в этих двух клеточных линиях. Интересно, что 7C12, 11F12, 59A9 и 18B10 имели сравнимую аффинность связывания как с клетками HEK293-CLDN18.2, так и с клетками NUGC4 (фигуры 1A-1D, таблица 4). Эти гибридомные антитела отбирают для клонирования генов и экспрессии химерных антител для дальнейшей функциональной характеристики ADCC/CDC.
[00422] ТАБЛИЦА 4
Пример 6: Получение химерных антител
[00423] Последовательности вариабельных областей легкой цепи и тяжелой цепи мышиного антитела против человеческого CLDN18.2 были получены с помощью амплификации полимеразной цепной реакции (PCR) из клеточных линий гибридомы-кандидата. После анализа последовательности и подтверждения, указанные выше гены вариабельной области, включая последовательность вариабельной области легкой цепи (VL), слитую с константной областью каппа IgG человека, и последовательность вариабельной области тяжелой цепи (VH), слитую с константной областью IgG1 человека, клонировали в рекомбинантный вектор экспрессии pcDNA3.1(+) для продукции и очистки антител.
[00424] Клетки ExpiCHO трансфицировали с использованием набора для трансфекции ExpiCHO с равным количеством ДНК из вектора тяжелой цепи и вектора легкой цепи. Трансфицированные клетки культивировали во встряхиваемых колбах при 125 об/мин в инкубаторе с 8% CO2 и при температуре 37°C. Культуру клеток собирали на 10-й день, а собранные антитела очищали аффинной хроматографией. Полученное антитело анализировали для определения уровня чистоты с помощью SDS-PAGE и эксклюзионной хроматографии (TSKgel G3000SWXL, TOSOH). Химерные антитела были обозначены как: 7C12-C, 11F12-C, 12E9-C, 26G6-C, 59A9-C, 18B10-C, и 12C12-C.
Пример 7: Характеристика очищенных химерных антител CLDN18.2
[00425] 1. Связывание и цитотоксическое действие на клетку HEK293-CLDN18.2
[00426] Связывание химерных антител с клеткой определяли в соответствии со способом, описанным в примере 5.
[00427] Как показано на фигуре 2A, 7C12-C, 11F12-C и 12E9-C, которые имели очень похожие CDR (отличаются только 2-3 аминокислотами), связывались с клеткой HEK293-CLDN18.2 при EC50 около 0,6 мкг/мл. 26G6-C имел EC50 1,1 мкг/мл. 59A9-C и 18B10-C выпускались позже, так что их испытывали отдельно. Как показано на фигуре 2C, 59A9-C с другой зародышевой линией и CDR имел несколько более высокую EC50 (1,3 мкг/мл), чем 18B10-C (1,0 мкг/мл).
[00428] CDC (комплемент-зависимая цитотоксичность) представляла собой важный механизм иммунной защиты. Таким образом, для оценки биологической активности антител в настоящем документе использовали анализ CDC. Вкратце, клетки HEK293-CLDN18.2 в логарифмической фазе ресуспендировали в RPMI1640 с 10% FBS. Эти клетки высевали по 8×103/100 мкл на лунку. Химерные анти-CLDN18.2 антитела и контрольное антитело IMAB362 разводили, используя 60% RPMI1640 с 20 мМ HEPES и 40% сыворотки человека, и затем добавляли в планшет для культуры клеток в конечной концентрации от 10 до 0,0012 мкг/мл, 100 мкл/лунку. Планшеты инкубировали при температуре 37°C в течение 80 мин. Затем планшетам с клеточными культурами давали уравновеситься до комнатной температуры в течение 30 минут. Для анализа жизнеспособности клеток при комнатной температуре использовали набор для анализа люминесцентной жизнеспособности клеток CellTiter-Glo с применением устройства для считывания микропланшетов (Thermo VARIOSKAN FLASH 3001).
[00429] Как показано на фигурах 2B и 2D, все 6 химерных антител CLDN18.2 индуцировали CDC-эффект при более низкой концентрации по сравнению с IMAB362. Эффективность 4 антител (7C12-C, 11F12-C, 12E9-C и 26G6-C) была более чем в 2 раза выше, чем у IMAB362. 59A9-C и 18B10-C имели более чем 3-кратное увеличение активности по сравнению с IMAB362.
[00430] 2. Связывание и цитотоксическое действие на клетку MKN45-CLDN18.2
[00431] MKN45 представляет собой низкодифференцированную аденокарциному желудка и подходит для оценки противоопухолевой эффективности in vivo. Однако клетка MKN45 не экспрессирует CLDN18.2 человека, если только не проводится трансфекция. Авторами изобретения было обнаружено, что разный уровень экспрессии человеческого CLDN18.2 на клетках MKN45 обусловливает разную чувствительность к антителам CLDN18.2. Затем для следующего исследования отобрали клетки MKN45 с высоким и средним уровнем экспрессии (см. фигуру 21).
[00432] Анализ клеточного связывания химерных антител проводили, как описано в примере 5, с использованием клеток MKN45 с высоким и средним уровнем экспрессии CLDN18.2. Как показано на фигурах 3A (верхняя) и 3C (средняя), 18B10-C связывался с клетками, экспрессирующими как с высоким, так и со средним уровнем hCLDN18.2 со значительно более высокой аффинностью, чем IMAB362. В клетках MKN45 с высоким уровнем CLDN18.2, активность 18B10-C была примерно в 2 раза выше, чем у IMAB362. Гораздо более значительная разница наблюдалась в клетке MKN45 со средним уровнем CLDN18.2, 18B10-C показал EC50 на уровне 0,96 мкг/мл, в то время как IMAB362 не связывался.
[00433] Активность ADCC оценивали с использованием клеток Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток и клеток MKN45-CLDN18.2 в качестве клеток-мишеней. Клетка Jurkat-NFAT-luc-FcγRIIIA-V176 была сконструирована в компании Mabspace Biosciences (Suzhou) Co., Limited. Вкратце, клетку Jurkat (Shanghai Institutes for Biological Sciences, кат. № SCSP-513) трансфицировали плазмидами pGL4.30-luc/NFAT-RE/Hygro и отбирали с помощью гигромицина для получения стабильно экспрессирующей клеточной линии Jurkat-NFAT-luc. Линию клеток Jurkat-NFAT-luc дополнительно трансфицировали плазмидами pcDNA3.1-FcγRIIIA-V176 и отбирали с помощью антибиотика G418 для получения линии клеток со стабильной экспрессией Jurkat-NFAT-luc-FcγRIIIA-V176.
[00434] Затем клетки-мишени в логарифмической фазе повторно суспендировали в RPMI1640 с 10% FBS, а затем высевали по 1×104 клеток на лунку для инкубации при температуре 37°C в течение 30 мин. Химерные анти-hCLDN18.2 антитела и контрольное антитело IMAB362 разводили, используя RPMI1640 с 10%FBS, и затем добавляли в планшет с клетками-мишенями в конечной концентрации от 100 до 0,0017 мкг/мл. Клетки Jurkat-NFAT-luc-FcγRIIIA-V176 в логарифмической фазе также добавляли в указанный выше планшет в количестве 6×104 клеток на лунку. Планшеты инкубировали при температуре 37°C в течение 6 часов. Затем планшетам с клеточными культурами давали уравновеситься до комнатной температуры в течение 30 минут. Для анализа жизнеспособности клеток при комнатной температуре использовали набор для анализа люминесцентной жизнеспособности клеток Cell Titer-Glo с применением устройства для считывания микропланшетов (Thermo VARIOSKAN FLASH 3001).
[00435] На основании кривой считывания репортера можно рассчитать EC50 и использовать для оценки эффекта ADCC. Как показано на фигуре 3B с использованием клетки MKN45 с высоким уровнем CLDN18.2, хотя у IMAB362 было мало точек для расчета EC50, две кривые предполагали, что 18B10-C имел лучшую ADCC-активность, чем IMAB362. Как показано на фигуре 3D в клетке MKN45 со средним уровнем CLDN18.2 18B10-C имел более чем 50-кратное увеличение эффективности ADCC, измеренной по EC50, по сравнению с IMAB362. Эти результаты предполагают, что клетка со средней экспрессией CLDN18.2 может дифференцировать антитело 18B10-C от IMAB362 лучше, чем клетка с высокой экспрессией. На клетках MKN45-hCLDN18.2 активности CDC не наблюдалось (данные не показаны).
[00436] 3. Связывание и цитотоксическое действие на клетку NUGC4
[00437] NUGC4 представляет собой линию клеток желудка с таким же уровнем экспрессии hCLDN18.2, как у пациентов с раком желудка.
[00438] Анализ связывания клеток и анализ с использованием репортерного гена ADCC проводили с использованием того же способа, что и выше (см. раздел 2 этого примера). Как показано на фигурах 4А и 4С, 5 из 6 химерных антител связывались с клеткой NUGC4 с EC50 около 10 мкг/мл (см. таблицу 5), за исключением 26G6-C и 59A9-C. 26G6-C связывался с NUGC4 с более высокой ЕС50 (67 мкг/мл), что указывает на более низкую аффинность. 59A9-C показал как более высокую ЕС50 (19 мкг/мл), так и более низкий максимальный сигнал. Кроме того, на фигурах 4B и 4D показана аналогичная тенденция активности ADCC в отношении клеток NUGC4. Из-за двух отдельных экспериментов EC50 и максимальные сигналы могут различаться между фигурой 4B и фигурой 4D. Важно отметить, что все испытанные химерные антитела продемонстрировали лучшую ADCC-активность, чем IMAB362, особенно 18B10-C с более чем 40-кратным увеличением, чем IMAB362. На клетках NUGC4 активности CDC не наблюдалось (данные не показаны).
[00439] В таблице 5 обобщены данные FACS по связыванию всех химерных антител и IMAB362 с клетками HEK293-CLDN18.2 и NUGC4.
[00440] ТАБЛИЦА 5
[00441] 4. Специфичность химерных антител CLDN18.2
[00442] CLDN18.2 имеет только несколько аминокислот, отличных от CLDN18.1, который существует во многих нормальных тканях и органах. Специфичность связывания антител с CLDN18.2 очень важна. Анализ связывания клеток был таким же, как указано выше (см. раздел 1 этого примера). На фигуре 5 показано связывание 18B10-C и IMAB362 с клетками HEK293, экспрессирующими CLDN18.2 или CLDN18.1. Оба антитела связывались только с клетками, экспрессирующими CLDN18.2, но не с клетками, экспрессирующими CLDN18.1. Другие химерные антитела также обладали аналогичной хорошей селективностью (данные не показаны).
Пример 8: Биннинг эпитопа
[00443] Гибридомные антитела конкурируют за связывание эталонных антител с клетками, экспрессирующими CLDN18.2
[00444] Клетки MKN45 с высоким уровнем CLDN18.2 в логарифмической фазе ресуспендировали в промывочном буфере FACS (PBS с 2% BSA), и затем добавляли в 96-луночный планшет с V-образным дном при плотности 1×105 клеток на лунку. В планшет добавляли разведенные гибридомные антитела или IMAB362-mIgG2a (конечная концентрация: от 100 до 0,01 мкг/мл). Планшет инкубировали при температуре 4°C в течение 1 часа чтобы позволить антителу полностью занять антиген на поверхности клетки. Клетки промывали 2 раза буфером для промывки FACS и к клеткам добавляли 10 мкг/мл IMAB362 или 5 мкг/мл 18B10-C для дальнейшей инкубации при температуре 4°C в течение 1 часа. Затем клетки промывали 3 раза и инкубировали с козьим анти-hIgG (H+L)-FITC (разведение 1:200). Наконец, клетки промывали 3 раза буфером для промывки FACS и анализировали с помощью проточной цитометрии.
[00445] Как показано на фигурах 6A и 6B, гибридомное антитело 18B10 может полностью блокировать связывание IMAB362 с клетками MKN45-CLDN18.2, что указывает на то, что 18B10 может иметь более высокую аффинность связывания, чем IMAB362, но опираясь на аналогичные или близкие аминокислоты (таблица 6).
[00446] ТАБЛИЦА 6
ная
ная
ная
 : полная блокада; частичная: частичная блокада; -: необнаруженная
: полная блокада; частичная: частичная блокада; -: необнаруженная
Пример 9: Картирование эпитопов выбранных антител с помощью сайт-направленного мутагенеза на аминокислотах CLDN18.2, отличающихся от CLDN18.1
[00447] 1. Создание конструкций CLDN18.2-mRFP человека и CLDN18.1-mRFP человека
[00448] кДНК, кодирующая CLDN18.1 человека (аминокислота 1-261, SEQ ID NO: 31)-mRFP1 (аминокислота 1-225) и CLDN18.2 человека (аминокислота 1-261, SEQ ID NO: 30)-mRFP1 (аминокислота 1-225) была синтезирована in vitro (SEQ ID NO: 52 и SEQ ID NO: 53 представляют собой аминокислотные последовательности, соответственно). Затем продукт PCR клонировали в вектор pcDNA3.1 (+) методом гомологичной рекомбинации с использованием реагента Syno Assembly Mix (Synbio) в соответствии с инструкциями производителя. Плазмиду очищали с использованием QIAGEN Plasmid Mega Kit (QIAGEN).
[00449] В соответствии с последовательностью человеческих CLDN18.1 и CLDN18.2 (инвентарный номер Genbank: сплайс-вариант 1 (CLDN18.1): NP_057453, NM_016369 и сплайс-вариант 2 (CLDN18.2): NM_001002026, NP_001002026), 8 разные аминокислоты расположены между 28-70, что может быть детерминантой специфического связывания с CLDN18.2 человека, а не с CLDN18.1. Используя человеческую плазмиду CLDN18.2-mRFP дикого типа, полученную выше, в качестве матрицы, с помощью праймеров были созданы два сегмента интегрированной последовательности. Варианты CLDN18.2-mRFP человека с заменой одной аминокислоты на аминокислоту CLDN18.1 человека в указанном положении амплифицировали с помощью перекрывающейся PCR с использованием праймеров. Специфические мутации относятся к Q29M, N37D, A42S, N45Q, Q47E, E56Q, G65P и L69I. Варианты человеческого CLDN18.1-mRFP с заменой одной аминокислоты в указанном положении амплифицировали с помощью перекрывающейся PCR с использованием праймеров. Специфические мутации относятся к M29Q, D37N, S42A, Q45N, E47Q, Q56E, P65G, I69L. Затем продукт PCR клонировали в вектор pcDNA3.1(+) методом гомологичной рекомбинации. Варианты CLDN18.2-mRFP человека были идентифицированы и подтверждены секвенированием отдельных положительных клонов.
[00450] Впоследствии эти плазмиды мутантов и CLDN18.2-mRFP человека дикого типа или CLDN18.1-mRFP человека трансфицировали в клеточную линию HEK293. Сначала 5×106 леток HEK293 высевали в чашку диаметром 60 мм в соотношении 60%~80% для трансфекции. 10 мкг ДНК в 400 мкл 1×HBS и 10 мкл линейного трансфекционного реагента PEI 25 кДа (растворенного в 1×HBS, исходный раствор 1 мг/мл) смешивали для достижения соотношения ДНК/PEI 1:2,5. Затем смесь по каплям добавляли в культуру клеток HEK293. Через 6-8 часов трансфицированные клетки заменяли полной DMEM на ночь. Через 24 часа после трансфекции клетки собирали для анализа FACS с использованием химерных антител.
[00451] Аминокислотная последовательность CLDN18.1 человека (SEQ ID NO: 31)
MSTTTCQVVAFLLSILGLAGCIAATGMDMWSTQDLYDNPVTSVFQYEGLWRSCVRQSSGFTECRPYFTILGLPAMLQAVRALMIVGIVLGAIGLLVSIFALKCIRIGSMEDSAKANMTLTSGIMFIVSGLCAIAGVSVFANMLVTNFWMSTANMYTGMGGMVQTVQTRYTFGAALFVGWVAGGLTLIGGVMMCIACRGLAPEETNYKAVSYHASGHSVAYKPGGFKASTGFGSNTKNKKIYDGGARTEDEVQSYPSKHDYV
[00452] Аминокислотная последовательность CLDN18.1 человека-mRFP1 (SEQ ID NO: 52):
MSTTTCQVVAFLLSILGLAGCIAATGMDMWSTQDLYDNPVTSVFQYEGLWRSCVRQSSGFTECRPYFTILGLPAMLQAVRALMIVGIVLGAIGLLVSIFALKCIRIGSMEDSAKANMTLTSGIMFIVSGLCAIAGVSVFANMLVTNFWMSTANMYTGMGGMVQTVQTRYTFGAALFVGWVAGGLTLIGGVMMCIACRGLAPEETNYKAVSYHASGHSVAYKPGGFKASTGFGSNTKNKKIYDGGARTEDEVQSYPSKHDYVMASSEDVIKEFMRFKVRMEGSVNGHEFEIEGEGEGRPYEGTQTAKLKVTKGGPLPFAWDILSPQFQYGSKAYVKHPADIPDYLKLSFPEGFKWERVMNFEDGGVVTVTQDSSLQDGEFIYKVKLRGTNFPSDGPVMQKKTMGWEASTERMYPEDGALKGEIKMRLKLKDGGHYDAEVKTTYMAKKPVQLPGAYKTDIKLDITSHNEDYTIVEQYERAEGRHSTGA
[00453] Аминокислотная последовательность CLDN18.2 человека (SEQ ID NO: 30)
MAVTACQGLGFVVSLIGIAGIIAATCMDQWSTQDLYNNPVTAVFNYQGLWRSCVRESSGFTECRGYFTLLGLPAMLQAVRALMIVGIVLGAIGLLVSIFALKCIRIGSMEDSAKANMTLTSGIMFIVSGLCAIAGVSVFANMLVTNFWMSTANMYTGMGGMVQTVQTRYTFGAALFVGWVAGGLTLIGGVMMCIACRGLAPEETNYKAVSYHASGHSVAYKPGGFKASTGFGSNTKNKKIYDGGARTEDEVQSYPSKHDYV
[00454] Аминокислотная последовательность CLDN18.2 человека-mRFP1 (SEQ ID NO: 53):
MAVTACQGLGFVVSLIGIAGIIAATCMDQWSTQDLYNNPVTAVFNYQGLWRSCVRESSGFTECRGYFTLLGLPAMLQAVRALMIVGIVLGAIGLLVSIFALKCIRIGSMEDSAKANMTLTSGIMFIVSGLCAIAGVSVFANMLVTNFWMSTANMYTGMGGMVQTVQTRYTFGAALFVGWVAGGLTLIGGVMMCIACRGLAPEETNYKAVSYHASGHSVAYKPGGFKASTGFGSNTKNKKIYDGGARTEDEVQSYPSKHDYVMASSEDVIKEFMRFKVRMEGSVNGHEFEIEGEGEGRPYEGTQTAKLKVTKGGPLPFAWDILSPQFQYGSKAYVKHPADIPDYLKLSFPEGFKWERVMNFEDGGVVTVTQDSSLQDGEFIYKVKLRGTNFPSDGPVMQKKTMGWEASTERMYPEDGALKGEIKMRLKLKDGGHYDAEVKTTYMAKKPVQLPGAYKTDIKLDITSHNEDYTIVEQYERAEGRHSTGA
[00455] 2. Связывание химерных антител CLDN18.2 с клетками HEK293-CLDN18.2 или HEK293-CLDN18.1 с сайт-мутацией
[00456] Трансфицированные клетки HEK293-CLDN18.2 или HEK293-CLDN18.1 ресуспендировали в PBS с 2% BSA при плотности 10 5/лунка, 100 мкл/лунка. Клетки промывали 3 раза буфером для промывки FACS (PBS+2% FBS) и инкубировали со 100 мкл/лунку 10 мкг/мл химерных антител и IMAB362 в каждой лунке при температуре 4°C в течение 30 мин. Затем клетки промывали 3 раза буфером для промывки FACS и инкубировали со 100 мкл/лунку козьего анти-hIgG(H+L)-FITC (1 разведение:200) при температуре 4°C в течение еще 30 мин. Наконец, клетки промывали 3 раза буфером для промывки FACS и анализировали с помощью проточной цитометрии. При анализе связывания с клетками, трансфицированными CLDN18.2, для контроля гейтинга использовали RFP-положительные клетки.
[00457] Процент сигнала связывания этих химерных антител с мутантными вариантами CLDN18.2 по сравнению с сигналом дикого типа был рассчитан и суммирован в таблице 7. Как показано на фигурах 7A-7B, связывание 18B10-C было полностью утрачено, когда E56 был заменен на Q. Это изменение также относилось к IMAB362 и другим химерным антителам, за исключением 59A9-C. Кроме того, авторами изобретения было обнаружено, что другие аминокислоты, такие как A42, N45, также в некоторой степени способствовали связыванию IMAB362 и других антител, но не 18B10-C.
[00458] ТАБЛИЦА 7
Пример 10: Получение и характеристика гуманизированных антител
[00459] 1. Получение, экспрессия и очистка гуманизированных антител
[00460] 18B10
[00461] Для пришивки CDR использовали последовательности каркасной области человеческой зародышевой линии для легкой цепи и VH/1-46 для тяжелой цепи, соответственно.
[00462] Варианты тяжелой цепи (HC) 1, 2 и 3 были получены путем прямой пришивки трех CDR к последовательности зародышевой линии (зародышевой линии 18B10 HC, SEQ ID NO: 23), обратной мутации R71I, T73K для варианта 1 HC (Hu18B10_Ha, SEQ ID NO: 25), обратной мутации R71I, T73K, T28S, M69L для варианта HC 2 (Hu18B10_Hb, SEQ ID NO: 27) и обратной мутации R71I, T73K, T28S, M69L, R38K, M48I для варианта 3 HC (Hu18B10_Hc, SEQ ID NO: 29) соответственно.
[00463] (1) Зародышевая последовательность для 18B10 HC:
[00464] VH/1-46(18B10-зародышевая последовательность, SEQ ID NO: 23):
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYYMHWVRQAPGQGLEWMGIINPSGGSTSYAQKFQGRVTMTRDTSTSTVYMELSSLRSEDTAVYYCAR
[00465] VH/1-46 вариант 1 (Hu18B10_Ha, SEQ ID NO: 25):
QVQLVQSGAEVKKPGASVKVSCKASGYTFTGYNMNWVRQAPGQGLEWMGNIDPYYGGTSYNQKFKGRVTMTIDKSTSTVYMELSSLRSEDTAVYYCARMYHGNAFDYWGQGTTVTVSS
[00466] VH/1-46 вариант 2 (Hu18B10_Hb, SEQ ID NO: 27):
QVQLVQSGAEVKKPGASVKVSCKASGYSFTGYNMNWVRQAPGQGLEWMGNIDPYYGGTSYNQKFKGRVTLTIDKSTSTVYMELSSLRSEDTAVYYCARMYHGNAFDYWGQGTTVTVSS
[00467] VH/1-46 вариант 3 (Hu18B10_Hc, SEQ ID NO: 29):
QVQLVQSGAEVKKPGASVKVSCKASGYSFTGYNMNWVKQAPGQGLEWIGNIDPYYGGTSYNQKFKGRVTLTIDKSTSTVYMELSSLRSEDTAVYYCARMYHGNAFDYWGQGTTVTVSS
[00468] Варианты легкой цепи (LC) 1 и 2 были получены путем прямой пришивки трех CDR к последовательности зародышевой линии (18B10 LC зародышевой линии, SEQ ID NO: 24) и без обратной мутации для варианта 1 (Hu18B10_La, SEQ ID NO: 26) и S63T, I21M для варианта 2 LC (Hu18B10_Lb, SEQ ID NO: 28), соответственно.
[00469] (2) Зародышевая последовательность для 18B10 LC:
[00470] VK/4-1 (18B10 LC зародышевая последовательность, SEQ ID NO: 24)
DIVMTQSPDSLAVSLGERATINCKSSQNNKNYLAWYQQKPGQPPKLLIYWASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQYYSTP
[00471] VK/4-1 вариант 1 (Hu18B10_La, SEQ ID NO: 26)
DIVMTQSPDSLAVSLGERATINCKSSQSLLNSGNLKNYLTWYQQKPGQPPKLLIYWASTRKSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQNDYSYPLTFGGGTKVEIK
[00472] VK/4-1 вариант 2 (Hu18B10_Lb, SEQ ID NO: 28)
DIVMTQSPDSLAVSLGERATMNCKSSQSLLNSGNLKNYLTWYQQKPGQPPKLLIYWASTRKSGVPDRFTGSGSGTDFTLTISSLQAEDVAVYYCQNDYSYPLTFGGGTKVEIK
[00473] Комбинация вышеуказанных вариабельных областей тяжелой цепи и вариабельных областей легкой цепи дает следующие гуманизированные антитела: 18B10-HaLa (имеющее VH SEQ ID NO: 25 и VL SEQ ID NO: 26), 18B10-HbLa (имеющее VH SEQ ID NO: 27 и VL SEQ ID NO: 26), 18B10-HcLa (имеющее VH SEQ ID NO: 29 и VL SEQ ID NO: 26), 18B10-HaLb (имеющее VH SEQ ID NO: 25 и VL SEQ ID NO: 28), 18B10-HbLb (имеющее VH SEQ ID NO: 27 и VL SEQ ID NO: 28), 18B10-HcLb (имеющее VH SEQ ID NO: 29 и VL SEQ ID NO: 28).
[00474] Гуманизированные варианты тяжелой цепи и легкой цепи 18B10 связаны с константной областью тяжелой цепи IgG1 человека и константной областью легкой каппа-цепи, как показано ниже:
[00475] Константная область тяжелой цепи IgG1 человека (SEQ ID NO: 49):
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
[00476] Константная область легкой каппа-цепи человека (SEQ ID NO: 50):
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
[00477] Вариабельные области вышеуказанных кДНК тяжелой и легкой цепей синтезировали и сливали с константной областью IgG1 человека и каппа-цепи человека. Тяжелую цепь и легкую цепь выбранных генов антител клонировали в экспрессионный вектор, и крупномасштабную ДНК получали с использованием системы Plasmid Maxiprep от компании Qiagen. Трансфекцию проводили с использованием реагента ExpiFectamine™ CHO от компании Invitrogen в соответствии с протоколом производителя. Супернатанты собирали, когда жизнеспособность клеток составляла около 60%. Супернатант клеточной культуры фильтровали через фильтрующую капсулу 0,22 мкм для удаления клеточного дебриса. Супернатант загружали на предварительно уравновешенную колонку сродства с белком-А. Затем смолу с белком А внутри колонки промывали уравновешивающим буфером (PBS) и для элюирования антитела использовали 25 мМ цитрата (рН 3,5). рН доводили примерно до 6,0-7,0 с помощью 1М трис-основания (рН 9,0). Уровень эндотоксина контролировался ниже 1EU/мг. Затем очищенное антитело характеризовали с помощью SDS-PAGE и SEC-HPLC.
[00478] 2. Связывание с CLDN18.2 человека и мыши
[00479] Связывание гуманизированных антител тестировали в соответствии с тем же способом, который описан в Примере 5.
[00480] Как показано на фигуре 8A, все гуманизированные варианты были протестированы на равных с химерным вариантом, чтобы отобрать наилучший вариант. Все варианты полностью сохраняли свое связывание. Затем 18B10-HaLa, который имел только одну обратную мутацию, тестировали на его связывание с клетками CLDN18.2 мыши HEK293 (фигура 8B). 18B10-HaLa может хорошо связываться с мышиным CLDN18.2 с большей активностью и более высоким MFI, чем IMAB362, что указывает на хорошую перекрестную реактивность 18B10-HaLa с мышами.
[00481] 3. Аффинный анализ гуманизированных антител CLDN18.2 с помощью KinExA
[00482] 18B10-HaLa и IMAB362 оценивали напрямую с помощью KinExA на предмет их аффинного связывания с клетками, экспрессирующими CLDN18.2. Следуя инструкциям KinExA 4000 (Sapidyne Instruments Inc.), 200 мг твердых шариков из PMMA (Sapidyne, #440176) покрывали 30 мкг козьего антитела против IgG Fc человека на 2 часа, а затем блокировали 10 мг/мл BSA на 1 час. Две линии клеток желудка, NUGC4 и KATOIII (ATCC, кат. № HTB-103), собирали в логарифмической фазе и смешивали с 0,2 нМ 18B10-HaLa или IMAB362. Смесь клеток и антител разбавляли в 2 раза с использованием 0,2 нМ 18B10-HaLa или IMAB362 и инкубировали при комнатной температуре в течение 3 часов. Количество свободных антител увеличивалось по мере разведения. Эти свободные антитела были захвачены шариками, покрытыми Fc козьего антитела против IgG человека, и затем помечены 1 мкг/мл Alexa Fluor 647 против IgG человека для считывания.
[00483] Аффинность связывания каждого антитела суммирована в таблице 8. Kd связывания 18B10-HaLa с клеткой NUGC4 и KATOIII составлял приблизительно 0,3 нМ, что более чем в 8 раз выше, чем у IMAB362. Это согласуется с приведенными выше результатами связывания FACS.
ТАБЛИЦА 8. Kd антител CLDN18.2 к клеточным линиям желудка
[00485] 4. Анализ CDC на клетках HEK293-CLDN18.2
[00486] Аналогично способу, описанному выше (см. раздел 1 примера 7), 18B10-HaLa тестировали напрямую с IMAB362 в анализе активности CDC. Как показано на фигуре 9, 18B10-HaLa имел более чем в 20 раз более высокую CDC-активность, чем IMAB362. Процент 18B10-HaLa-зависимого специфического уничтожения клеток достигал 86% при концентрации 0,3 мкг/мл, в то время как IMAB362 не вызывал уничтожения клеток при той же концентрации
[00487] 5. Связывание и цитотоксическое действие на клетку MKN45-CLDN18.2
[00488] Анализ связывания клеток был таким же, как описано выше. Как показано на фигуре 10А, все гуманизированные варианты 18В10 связывались с клетками с аффинностью, сравнимой с химерным 18В10. Для дальнейшего изучения активности ADCC был выбран 18B10-HaLa, имеющий только одну обратную мутацию.
[00489] Активность ADCC тестировали с использованием клеток Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток и клеток MKN45-CLDN18.2 в качестве клеток-мишеней. Протокол анализа был таким же, как указано выше (см. раздел 2 примера 7). Как показано на фигуре 10B, 18B10-HaLa имеет намного более низкую ЕС50 (0,05 мкг/мл), чем IMAB362, что соответствует таковому для химерного 18B10.
[00490] 6. Связывание и цитотоксическое действие на клетку NUGC4
[00491] Анализы связывания клеток и ADCC были такими же, как указано выше. На фигуре 11А показаны результаты аффинности связывания 18B10-HaLa с клетками NUGC4. На фигуре 11B показана гораздо лучшая ADCC-активность 18B10-HaLa (EC50~0,59 мкг/мл) по сравнению с IMAB362.
[00492] 7. Анализ ADCC с использованием NUGC4 в качестве клетки-мишени и PBMC в качестве эффекторной клетки
[00493] Клетки NUGC4 в логарифмической фазе ресуспендировали в RPMI1640 с 10% FBS. Клетки предварительно высевали в 96-луночный планшет с U-образным дном из расчета 1×104 клеток на лунку. Анти-CLDN18.2 антитела и IMAB362 градиентно разводили в RPMI1640 с 10% FBS и добавляли в вышеуказанный планшет в конечной концентрации от 200 до 0,2 мкг/мл и инкубировали при температуре 37°C в течение 30 мин. Извлекали из жидкого азота замороженные РВМС от компании Miao Shun (Shanghai) Biological & Technology Co., Ltd и немедленно помещали в водяную баню при температуре 37°C. После центрифугирования клетки ресуспендировали в RPMI1640 плюс 10% FBS и высевали в упомянутый выше 96-луночный планшет с U-образным дном в количестве 40×104 клеток на лунку. Затем планшет на 5 часов помещали в инкубатор при температуре 37°С.
[00494] После инкубации планшет уравновешивали до температуры 22°C. LDH определяли с помощью антитела с использованием набора для анализа целостности и однородности мембран Promega CytoTox-ONE (G7892) или набора реагентов для нерадиоактивной оценки цитотоксичности CytoTox 96® (G1780). После добавления лизирующего раствора, реагента и стоп-раствора в соответствии с инструкциями производителя измеряли флуоресценцию при длине волны возбуждения 560 нм и длине волны испускания 590 нм (G7892) или поглощение при 490 нм или 492 нм (G1780).
[00495] а Фигуре 12 показаны репрезентативные данные с использованием РВМС в качестве эффекторной клетки. 18B10-HaLa показал гораздо лучшую активность ADCC, чем IMAB362. Из-за несоответствия кривой регрессии EC50 не может быть рассчитана точно.
[00496] 8. Картирование эпитопов выбранных антител с использованием сайт-направленного мутагенеза на CLDN18.2 человека
[00497] Используя тот же способ и плазмиду CLDN18.2-mRFP человека, что и в примере 9, 42 аминокислоты между CLDN18.2 человека 28-80, как указано ниже, заменяли аланином по одной за раз. Эти варианты амплифицировали путем перекрывающейся PCR с использованием праймеров. Специфическими мутациями являются Q28A, Q29A, W30A, S31A, T32A, Q33A, D34A, L35A, Y36A, N37A, N38A, V40A, T41A, V43A, F44A, N45A, Y46A, Q47A, L49A, W50A, R51A, S52A, V54A, R55A, E56A, E56A, S57A, S58A, F60A, T61A, E62A, R64A, Y66A, F67A, T68A, L69A, L70A, L72A, M75A, L76A, Q77A, V79A, R80A. Затем продукт PCR клонировали в вектор pcDNA3.1 (+) методом гомологичной рекомбинации с использованием реагента Syno Assembly Mix (Synbio) в соответствии с инструкциями производителя. Плазмиду очищали с использованием набора QIAGEN Plasmid Mega Kit (QIAGEN).
[00498] Впоследствии эти плазмиды мутантов и CLDN18.2-mRFP дикого типа трансфицировали в клетки HEK293. Как и в примере 9, клетки анализировали с помощью проточной цитометрии через 24 часа после трансфекции.
[00499] Как показано на фигуре 13A, связывание 18B10-HaLa было полностью утрачено (процент связывания <10%), когда W30, L49, W50, E56 были заменены на A, что указывает на то, что эти 4 аминокислоты имеют решающее значение для его связывания с CLDN18.2 человека. В частности, E56 является наиболее важным для образования связывающего эпитопа. Помимо этих 4 важнейших аминокислот, на связывание также влияет несколько других аминокислот (процент связывания от 10% до 25%), когда их заменяют аланином, например, R51, F60, E62, R80. На фигуре 13В показано связывание 59A9-C с мутантным сайтом CLDN18.2, которое лишь частично зависело от Е56 (процент связывания около 22%). Процент связывания мутантного CLDN18.2 в сравнении с антителами дикого типа суммирован в таблице 9.
[00500] ТАБЛИЦА 9
Пример 11: Интернализация и цитотоксичность конъюгата антитело-лекарственное средство (ADC)
[00501] 18B10-HaLa и контрольный hIgG1 конъюгировали с vcMMAE с использованием набора MC-vc-PAB-MMAE KIT (Levena Biopharma, кат. № SET0201). Соотношение лекарство-антитело (DAR) химерного 18B10-HaLa составляло 4,05, тогда как соотношение IMAB362 и контрольного hIgG1 составляло 2,9 и 4,96, соответственно. Влияние 18B10-HaLa-vcMMAE на жизнеспособность клеток оценивали с помощью колориметрического анализа, определяющего клеточную метаболическую активность.
[00502] Клетки HEK293-CLDN18.2, NUGC4 или клетки MKN45 с высоким уровнем CLDN18.2 в логарифмической фазе ресуспендировали в соответствующей культуральной среде, а затем добавляли в планшет для культивирования клеток в количестве 1×104 клеток на лунку, 50 мкл/лунку для инкубации при температуре 37°C в течение ночи. Далее Ab-vcMMAE, контроль hIgG1-vcMMAE и Ab градиентно разбавляли и добавляли в каждую лунку по 50 мкл/лунка. В качестве положительного контроля цитотоксичности использовали конечную концентрацию vcMMAE 4,75 нМ. Через 72 часа в каждую лунку добавляли 100 мкл/лунку реагента для детекции из набора для анализа люминесцентной жизнеспособности клеток CellTiter-Glo на 10 минут при комнатной температуре, затем считывали данные с помощью устройства для считывания микропланшетов.
[00503] Как показано на фигуре 14A, как 18B10-HaLa-vcMMAE, так и IMAB362-vcMMAE, но не контрольный hIgG1-vcMMAE, индуцировали цитотоксичность в отношении клеток HEK293-CLDN18.2, указывая на то, что цитотоксичность была специфичной для hCLDN18.2. Хотя 18B10-HaLa и IMAB362 по отдельности не проявляли цитотоксичности в отношении клеток-мишеней (данные не показаны), это указывает на то, что наблюдаемая цитотоксичность была опосредована vcMMAE. На фигуре 14В показано цитотоксическое действие на NUGC4, клетку рака желудка. 18B10-HaLa-vcMMAE продемонстрировал дозозависимое ингибирование роста клеток, начиная с концентрации 0,03 мкг/мл. Напротив, IMAB362-vcMMAE ингибировал рост клеток только при 10 мкг/мл, что является гораздо более высокой концентрацией. В другой клетке рака желудка MKN-45, трансфицированной CLDN18.2 (высокая экспрессия), 18B10-HaLa-vcMMAE достигла максимального уничтожения клеток 86%, что также было выше, чем у IMAB362 (60%) (как показано на фигуре 14C).
[00504] Хорошо изучено, что ADC функционирует посредством связывания антигена и его интернализации в клетки-мишени. Лекарственное средство, конъюгированное с антителом, не может высвобождаться и убивать клетки до тех пор, пока оно не интернализуется и не переносится в лизосому для деградации. Авторы изобретения использовали этот анализ в качестве предварительной оценки свойства интернализации 18B10-HaLa. Результаты показывают, что он обладает потенциальной активностью интернализации и может быть разработан в качестве терапевтического препарата ADC.
Пример 12: Оценка эффективности in vivo гуманизированных антител CLDN18.2 в ксенотрансплантатной модели с MKN45 с высоким уровнем CLDN18.2
[00505] 1. Противоопухолевая эффективность в ксенотрансплантатной модели с MKN45 с высоким уровнем CLDN18.2 с использованием голых мышей
[00506] Исследование in vitro (пример 10) показало, что гуманизированные антитела CLDN18.2 могут индуцировать ADCC-эффект на клетках с MKN45 с высоким уровнем CLDN18.2 (пример 1). Поэтому была создана модель in vivo, которую использовали для оценки противоопухолевой активности. Вкратце, каждой самке голых мышей Balb/c инокулировали 5×106 клеток MKN45 с высоким уровнем CLDN18.2 с 50% матригелем (BD) путем подкожной инъекции в правый бок. Через 12 дней после инокуляции были отобраны 24 мыши с размером опухоли около 70 мм3, которые были случайным образом разделены на 3 группы (n=8). Затем мышам дважды в неделю в течение 3 недель путем внутрибрюшинной инъекции вводили изотипический контроль или гуманизированные антитела CLDN18.2 в дозе 0,3 мг/кг. В конце исследования животных забивали ингаляцией СО2. Размер и объем опухоли измеряли 2-3 раза в неделю. Результаты были проанализированы с использованием Prism GraphPad и выражены как среднее±SEM.
[00507] Как показано на фигуре 15, 18B10-HaLa продемонстрировал немного лучшую противоопухолевую активность, чем IMAB362, по измерению размера опухоли и TGI, в то время как оба были значительно лучше, чем изотипический контроль (таблица 10).
[00508] ТАБЛИЦА 10. Ингибирование роста опухоли (TGI) 18B10-HaLa и IMAB362 в ксенотрансплантатной модели с MKN45 с высоким уровнем CLDN18.2 (среднее±SEM, n=8)
День 28
День 28
[00509] 2. Противоопухолевая эффективность в ксенотрансплантатной модели с совместной инокуляцией MKN45 с высоким уровнем CLDN18.2 и hPBMC с использованием мышей NOD-SCID
[00510] Клетки РВМС человека были приобретены у компании Allcells. 24 самки мышей NOD-SCID класса SPF были случайным образом разделены на 3 группы (n=8), 6 мышам инокулировали 5×106 клеток MKN45 с высоким уровнем CLDN18.2 и 50% матригель (BD) путем подкожной инъекции в правый бок в качестве модельной группы (без РВМС), и 18 мышам инокулировали 5×106 клеток MKN45 с высоким уровнем CLDN18.2 и 5×106 клеток РВМС человека с 50% матригелем (BD) в качестве терапевтической группы. Через 4 часа после инокуляции мышам вводили 10 мг/кг изотипического контроля, 3 мг/кг и 10 мг/кг 18B10-HaLa два раза в неделю в течение 4 недель путем внутрибрюшинной инъекции. В конце исследования животных забивали ингаляцией СО2. Размер и объем опухоли измеряли 2-3 раза в неделю. Результаты были проанализированы с помощью Prism GraphPad и выражены как среднее±SEM.
[00511] Как показано на фигуре 16, рост опухоли в группе 18B10-HaLa полностью ингибировался в течение периода обработки. После терапии опухоль в группе 3 мг/кг начала расти через 20 дней, в то время как в группе 10 мг/кг этого не произошло. Отсутствие существенной разницы между группой без РВМС и группой PBS с РВМС позволяет предположить, что РВМС сами по себе в качестве эффекторных клеток без антител не могут ингибировать рост опухоли. Ингибирование роста опухоли (TGI) суммировано в таблице 11. 18B10-HaLa не влиял на массу животного (данные не представлены).
[00512] Таблица 11. Ингибирование роста опухоли 18B10-HaLa в ксенотрансплантатной модели опухоли с совместной инокуляцией MKN45 с высоким уровнем CLDN18.2 и hPBMC (среднее±SEM, n=6)
День 29
День 29
[00513] 3. 18B10-HaLa дозозависимо ингибирует рост ксенотрансплантатной опухоли с MKN45 с высоким уровнем CLDN18.2 у голых мышей
[00514] Каждой самке голых мышей Balb/c инокулировали 5×106 клеток с 50% матригелем (BD) путем подкожной инъекции в правый бок. Через 9 дней после инокуляции были отобраны 32 мыши с размером опухоли около 100 мм3 и случайным образом разделяли на 4 группы (n=8). Затем мышам вводили изотипический контроль, 0,1 мг/кг, 0,3 мг/кг и 1 мг/кг 18B10-HaLa, два раза в неделю в течение 3 недель путем внутрибрюшинной инъекции. В конце исследования животных забивали ингаляцией СО2. Размер и объем опухоли измеряли 2-3 раза в неделю. Результаты были проанализированы с помощью Prism GraphPad и выражены как среднее±SEM.
[00515] Как показано на фигуре 17, противоопухолевая активность 18B10-HaLa является дозозависимой. Группа 1 мг/кг показала наилучшую активность ингибирования роста опухоли (таблица 12).
[00516] Таблица 12. Дозозависимое ингибирование роста опухоли 18B10-HaLa в ксенотрансплантатной модели опухоли MKN45 с высоким уровнем CLDN18.2 (среднее±SEM, n=8)
День 13
День 13
Пример 13: Получение, экспрессия, очистка и характеристика мутанта 18B10-HaLa-VLPYLL с усиленным ADCC-эффектом
[00517] 1. Получение мутанта 18B10-HaLa-VLPYLL
[00518] Согласно исследованию, проведенному Futa Mimoto et al., мутации L235V/F243L/R292P/Y300L/ P396L могут повышать аффинность связывания с FcγRIIIA в 10 раз без каких-либо изменений в отношении FcγRIIB, который является ингибирующей изоформой FcγR. Для проверки этой гипотезы был сконструирован и получен мутант 18B10-HaLa-L235V/F243L/R292P/Y300L/P396L (18B10-HaLa-VLPYLL) для усиления его эффекта ADCC. Этот вариант Fc подвергали временной трансфекции, экспрессии и очистке в соответствии с теми же методами, что и в разделе 1 примера 12.
[00519] Сообщалось, что пять мутаций L235V/F243L/R292P/Y300L/P396L в Fc могут повышать аффинность связывания с обоими аллелями CD16A человека (FcγRIIIA) без каких-либо изменений в отношении FcγRIIB, который является ингибирующей изоформой FcγR i (Futa Mimoto et al., Novel asymmetrically engineered antibody Fc variant with superior FcγR binding affinity and specificity compared with afucosylated Fc variant[C]//MAbs. Taylor & Francis, 2013, 5(2): 229-236). Чтобы проверить эту гипотезу, эти мутации были введены в Hu18B10_Ha_hIgG1 с использованием PCR удлинения перекрытия, и новая конструкция названа Hu18B10_Ha_hIgG1_L235V/F243L/R292P/Y300L/P396L. Конечные продукты PCR характеризовали электрофорезом в агарозном геле. Фрагмент нужного размера извлекали из геля и клонировали в вектор экспрессии. Правильная конструкция Hu18B10_Ha_hIgG1_P330S была затем подтверждена анализом секвенирования. Плазмиды Hu18B10_Ha_hIgG1_L235V/F243L/R292P/Y300L/P396L и Hu18B10_La_hKappa получали с использованием системы Plasmid Maxi-prep System от компании Qiagen. Затем плазмиды тяжелой цепи и легкой цепи совместно трансфицировали в клетку Expi-CHO для экспрессии и очистки, как описано выше, с использованием тех же методов, что и в разделе 1 примера 10.
[00520] Последовательности сконструированного Fc L235V/F243L/R292P/Y300L/P396L(SEQ ID NO: 51):
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELVGGPSVFLLPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPPEEQYNSTLRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPLVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
[00521] 2. Связывание с гамма-рецепторами Fc
[00511] Futa Mimoto et сравнили мутант Fc VLPYLL с мутантом дикого типа и обнаружили, что мутации могут повышать его аффинность связывания как с FcγRIIIA F176 (в 63 раза), так и c FcγRIIIA V176 в 33 раза), не затрагивая другие FcgR. Чтобы подтвердить это открытие, тестировали связывание антител с этими FcγRs. Вкратце, на планшет наносили антитело 18B10-HaLa-VLPYLL или 18B10-HaLa-wt в концентрации 1 мкг/мл. После блокировки и промывки добавляли последовательно разбавленные (5 мкг/мл~0,02 мкг/мл) FcγR, меченные His-меткой, и инкубировали в течение 1 часа. Затем добавляли анти-His-HRP и TMB для обнаружения связывания FcγR при OD450 нм.
[00523] Как показано на фигурах 18A и 18B, не было существенной разницы между 18B10-HaLa_VLPYLL и 18B10-HaLa-wt в связывании с человеческим FcγRI или FcγRIIB. Однако 18B10-HaLa_VLPYLL продемонстрировал 10-кратное увеличение связывания с человеческим FcγRIIIA (F176) и FcγRIIIA (V176) по сравнению с их диким типом (wt) (фигура 18C и 18D). Сходные результаты были показаны с FcγR мыши и FcγR яванского макака (фигуры 18E-18I).
[00524] 3. Связывание с FcRn и C1q
[00525] Связывание FcRn оценивали методом ELISA. Вкратце, на планшете иммобилизовали 18B10-HaLa_VLPYLL или дикий тип. Биотинализированный FcRn серийно разбавляли в буфере для разведения pH 6,0 (1 мкг/мл~0,0002 мкг/мл), и затем добавляли для инкубации в течение 1 часа. Затем добавляли Streptavidin-HRP и TMB для обнаружения связывания при OD450 нм.
[00526] Анализ связывания C1q проводили следующим способом. На планшете иммобилизовали два антитела. Добавляли серийно разведенный C1q (20 мкг/мл~0,31 мкг/мл) для инкубации в течение 1 часа. Затем добавляли анти-C1q-HRP и TMB для обнаружения при OD450 нм.
[00527] Как показано на фигуре 19A, нет существенной разницы в связывании FcRn между 18B10-HaLa_VLPYLL и дикого типа, что указывает на отсутствие влияния мутаций VLPYLL на связывание FcRn. На фигуре 19В показано, что 18B10-HaLa_VLPYLL достигает такого же сигнала связывания при более низкой концентрации C1q, чем у дикого типа, что может привести к повышенной активности CDC.
[00528] 4. Анализ ADCC на клетках NUGC4 с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток
[00529] Анализ с использованием репортерного гена ADCC выполняли в соответствии с описанным выше способом (см. раздел 2 примера 7). Как показано на фигуре 20A, 18B10-HaLa_VLPYLL имел 3-кратное увеличение активности ADCC (EC50~0,0097 мкг/мл) по сравнению с таковой у дикого типа (EC50~0,032 мкг/мл).
[00530] 5. Анализ ADCC на клетках NUGC4 с использованием PBMC человека в качестве эффекторных клеток
[00531] Анализ ADCC с использованием РВМС человека проводили в соответствии с описанным выше способом (см. раздел 7 примера 10). Как показано на фигуре 20B, 18B10-HaLa_VLPYLL также имел 3-кратное увеличение активности ADCC по сравнению с таковой у дикого типа, хотя максимальная цитотоксичность обоих была сходной (~45%). По сравнению с IMAB362, 18B10-HaLa_VLPYLL имел 100-кратное увеличение активности.
[00532] 6. MESF экспрессии CLDN18.2 на панели клеточных линий рака желудка
[00533] Наборы микросфер Quantum™ MESF (молекулы эквивалентного растворимого флуорохрома) позволяют стандартизировать единицы интенсивности флуоресценции для применения в количественной флуоресцентной цитометрии. Панель клеток рака желудка (GC) окрашивали с использованием 30 мкг/мл 18B10-HaLa и козьего античеловеческого IgG-FITC. Клетки выявляли с помощью гранул Quantum™ MESF на проточном цитометре с фиксированной настройкой флуоресценции. Вкратце, добавляли одну каплю эталонного бланка «В» к 400 мкл суспендирующего раствора, затем объединяли по 1 капле каждой популяции интенсивности флуоресценции с 400 мкл того же буфера для анализа. Микросферы анализировали на проточном цитометре. Для анализа данных использовали загруженный шаблон количественного анализа Bangs Laboratories, QuickCal® v. 2.3, с использованием калибровочной кривой и значения коэффициента регрессии (r2). Для точных назначений MESF была обеспечена линейность инструментов и достигнут коэффициент регрессии ≥0,9995. Кроме того, параллельно проводили соответствующие контроли (например, неокрашенные клетки, изотипические контроли).
[00534] Как показано на фигуре 21, две трансфицированные клеточные линии HEK293-CLDN18.2 и MKN45 с высоким уровнем CLDN18.2 имели гораздо более высокий уровень экспрессии CLDN18.2, чем другие клеточные линии, которые могут не представлять опухолевые клетки от пациентов с GC. Среди клеток GC NUGC4 имел самую высокую экспрессию CLDN18.2. SNU-601 (Cobioer, кат. № CBP60507) и SNU-620 (Cobioer, кат. № CBP60508) имели умеренный уровень экспрессии, в то время как KATOIII и OCUM-1 (Cobioer, кат. № CBP60494) имели более низкий уровень экспрессии. Следовательно, CLDN18.2 имеет различный уровень экспрессии среди клеток рака желудка.
[00535] 7. IHC-обнаружение экспрессии CLDN18.2 на панели клеточных линий рака желудка
[00536] Линии клеток рака желудка собирали в логарифмической фазе роста и после промывки фосфатно-солевым буфером (PBS), соответственно, фиксировали в 4% нейтральном забуференном параформальдегиде (PFA) в течение 30 минут при комнатной температуре. После центрифугирования клетки повторно суспендировали в PBS с плотностью примерно 2-5×107, затем смешивали с 200 мкл расплавленного агара, затем дегидратировали в градиентном спирте, очищали ксилолом, а затем заливали парафином для срезов. Уровень экспрессии CLDN18.2 в этих клетках определяли с помощью иммуногистохимии (IHC) с использованием 3 мкг/мл GC182-биотина, произведенного компанией Mabspace Bioscience в соответствии с последовательностью, описанной в WO2013167259, и биотинилированного собственными силами, которое представляет собой доступное моноклональное антитело для IHC-обнаружения CLDN18.2. Результаты IHC оценивали по относительной доле положительных клеток и интенсивности окрашивания клеточной мембраны. В соответствии с рекомендациями по подсчету баллов IMAB362 в клинических испытаниях эти клеточные линии характеризовали и оценивали (таблица 13). Для включения в исследование FAST IMAB362 подходили только пациенты с умеренным (2+) и сильным (3+) окрашиванием не менее 40% опухолевых клеток. Следовательно, критериям соответствуют NUGC4, MKN45 с высоким уровнем CLDN18.2 и HEK293-CLDN18.2. Результаты соответствовали результатам примера 13, раздел 6 (метод Quantum™ MESF).
[00537] Вариабельная область тяжелой цепи GC182 (SEQ ID NO:74):
QIQLVQSGPELKKFGETVKISCKASGYTFTDYSIHWVKQAPGKGLKWMGWINTETGVPTYADDFKGRFAFSLETSASTAYLQINNLKNEDTATYFCARRTGFDYWGQGTTLTVSS
[00538] Вариабельная область легкой цепи GC182 (SEQ ID NO:75):
DIVMTQAAFSIPVTLGTSASISCRSSKNLLHSDGITYLYWYLQRPGQSPQLLIYRVSNLASGVPNRFSGSESGTDFTLRISRVEAEDVGVYYCVQVLELPFTFGGGTKLEIK
[00539] ТАБЛИЦА 13. Анализ экспрессии CLDN18.2 в клеточных линиях рака желудка методом IHC
[00540] 8. Анализ ADCC на клеточных линиях рака желудка (GC) с другим уровнем экспрессии CLDN18.2 с использованием PBMC человека в качестве эффекторных клеток
[00541] Для дальнейшей проверки гипотезы о том, что ADCC-активность антител CLDN18.2 регулируется уровнем экспрессии CLDN18.2 на клетках GC, анализ ADCC с использованием PBMC человека в качестве эффекторных клеток проводили в соответствии с описанным выше способом (см. раздел 7 примера 10). В качестве клеток-мишеней использовали 4 линии клеток желудка с разным уровнем экспрессии CLDN18.2. Как показано на фигурах 22A-22D, клетка NUGC4 индуцировала самую высокую ADCC-активность (максимальная цитотоксичность ~40%) среди всех антител CLDN18.2. Из трех протестированных антител 18B10-HaLa-VLPYLL продемонстрировал гораздо лучшую активность, чем 18B10-HaLa-wt и IMAB362. Клетки SNU-601 и SNU-620 индуцировали умеренную активность ADCC (максимальная цитотоксичность 30% и 15%, соответственно), в то время как клетка OCUM-1 имела самую низкую цитотоксичность (ниже 10%). Эти результаты позволяют предположить, что активность ADCC коррелирует с уровнем экспрессии CLDN18.2 в этих клеточных линиях.
Пример 14: Оптимизация процесса 18B10-HaLa и характеристика эффекта ADCC
[00542] 1. Оптимизация процесса получения 18B10-HaLa
[00543] Хорошо известно, что афукозилирование или дефукозилирование селективно и значительно увеличивает аффинность связывания с FcγRIII и приводит к усилению функции ADCC. Ниже описывается оптимизация процесса для снижения уровня фукозы и повышения ADCC.
[00544] Вкратце, после того, как посев банка клеток был извлечен и культивирован в среде CD-CHO (Gibco) в течение 3 дней, клетки размножались в базовой среде (Hyclone, ActiPro+4 мМ Gln+1=HT) в течение 6 дней. Затем в биореактор добавляли 0 (в качестве эталонного образца) или 50 мкМ 2F-O-F (2-дезокси-2-фтор-L-фукоза) и количество DO (растворенный кислород) контролировали на уровне около 40%. Добавляли питательную среду 1/2 (HyClone, Cell Boost 7a, Cell Boost 7b) и собирали клеточную суспензию, когда VCD (переменная плотность клеток) была ниже 80% или на 13-й день.
[00545] Титры антител как эталонного образца, так и 50 мкМ образца 2F-O-F измеряли с помощью ВЭЖХ после сбора клеточной суспензии. Титр 50 мкМ образца 2F-O-F составлял 4,73 г/л на 13-й день, что было даже выше, чем у эталонного образца, что указывает на то, что на него не влиял 2F-O-F.
[00546] Качество антител определяли с помощью ВЭЖХ после очистки, и 50 мкМ образца 2F-O-F имели такую же чистоту (98,3%), что и эталонный образец (98,2%). Не было значительного влияния 2F-O-F на качество антител.
[00547] В то же время N-гликан анализировали с помощью ВЭЖХ, и результат показан в таблице 14. По сравнению с эталонным образцом добавление 2F-OF снижало процентное содержание G0F (FA2) (с 61,6% до 1,9%) и фукозы (с 87,7% до 13,7%), но увеличилось процентное содержание G0 (А2) (с 8,1% до 69,8%). Следовательно, 50 мкМ 2F-O-F было достаточно для контроля содержания фукозы ниже 15%, что может привести к усилению эффекта ADCC. Продукт в этом процессе (с 50 мкМ 2F-O-F) был назван 18B10-HaLa с низким содержанием фукозы.
ТАБЛИЦА 14. Анализ N-гликанов образцов 18B10-HaLa
[00549] Чтобы продемонстрировать, что 18B10-HaLa с низким содержанием фукозы повышает аффинность эффективного рецептора FcγIIIa, сохраняя при этом сродство к FcRn, авторы изобретения сравнили сродство 18B10-HaLa с низким содержанием фукозы и аналога IMAB362 с помощью метода биослоевой интерферометрии (BLI) системы Fortebio. В качестве контроля был взят аналог IMAB362 с изотипом IgG1 человека и нормальным гликозилированием.
[00550] В этом исследовании FcγRI, FcγRIIa-H167, FcγRIIa-R167, FcγRIIb, FcγRIIIa-V176, FcγRIIIa-F176, FcγRIIIb-NA1, FcγRIIIb-NA2 и FcRn наносили на биосенсоры и погружали в IMAB362-аналог и 18B10- HaLa с низким содержанием фукозы в растворе с различной концентрацией. Все данные по связыванию собирали при температуре 30°C. При измерении аффинности 18B10-HaLa с низким содержанием фукозы или IMAB362-аналог к C1q биотинилированные антитела загружали на биосенсоры, а затем инкубировали с C1q в растворе. Когда аффинность антител к FcRn измеряли с помощью BLI, pH составлял 6,0, а для анализа связывания с другими рецепторами Fc pH равнялся 7,4. Эксперименты состояли из 5 этапов: 1. Определение исходного уровня; 2. Загрузка гамма-рецепторов Fc человека на биосенсор; 3. Определение второго исходного уровня; 4. Ассоциация 18B10-HaLa с низким содержанием фукозы и IMAB362-аналог для определения koff; и 5. Диссоциация антител для определения koff. 18B10-HaLa с низким содержанием фукозы и IMAB362-аналог имеют схожую аффинность к FcγRI, FcRn или C1q, в то время как 18B10-HaLa с низким содержанием фукозы демонстрирует несколько более высокое сродство, чем IMAB362-аналог к другим рецепторам. Эти результаты показывают, что в клинических испытаниях 18B10-HaLa с низким содержанием фукозы будет проявлять повышенную активность ADCC и аналогичный период полужизни с нормальными гликозилированными антителами.
[00551] ТАБЛИЦА 15. Данные по аффинности 18B10-HaLa с низким содержанием фукозы и IMAB362-аналога к Fc-рецептору человека, обнаруженные с помощью ForteBio Octet
[00552] Как показано в Таблице 15, аффинность 18B10-HaLa с низким содержанием фукозы к человеческому FcγRIIIa-V176 и человеческому белку FcγRIIIa-F176 была немного выше, чем сродство IMAB362, что может быть вызвано более низким фукозилированием. Как показано в таблице 15, на аффинность 18B10-HaLa с низким содержанием фукозы к белку FcRn человека не влияло более низкое фукозилирование, даже немного выше, чем у IMAB362. Как показано в таблице 15, аффинность 18B10-HaLa с низким содержанием фукозы к человеческому белку C1q не совсем аналогична аффинности IMAB362.
[00553] 2. Анализ с использованием репортерного гена ADCC на NUGC4 с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток.
[00554] Тест ADCC проводили по тому же протоколу, что и выше (см. раздел 2 примера 7). Как показано на фигуре 23, антитело, полученное с использованием процесса с добавлением 50 мкМ 2F-OF (18B10-HaLa с низким содержанием фукозы), повышало активность ADCC более чем в 30 раз по сравнению с эталонным образцом, полученным с использованием процесса без добавления 2Ф-ОФ. Кратковременно экспрессированный 18B10-HaLa также был включен в это сравнение, и благодаря оптимизации процесса максимальный сигнал также был увеличен, что представляет активность ADCC.
[00555] 3. Связывание FACS с различными клеточными линиями рака желудка с использованием 18B10-HaLa с низким содержанием фукозы
[00556] Связывание FACS осуществляли в соответствии с тем же протоколом, что и в разделе 2 примера 7. Как показано на фигурах 24A-24C, 18B10-HaLa с низким содержанием фукозы может связываться с этими клеточными линиями с более высокой эффективностью, чем у IMAB362. EC50 18B10-HaLa с низким содержанием фукозы составляла 0,5~1,6 мкг/мл, в то время как IMAB362 практически не имел сигнала связывания при концентрации 1 мкг/мл.
[00557] 4. Анализ с использованием репортерного гена ADCC на различных клеточных линиях рака желудка с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток
[00558] Тест ADCC проводили по тому же протоколу, что и выше (см. раздел 2 примера 7). Как показано на фигурах 25A-E, при использовании клеточных линий рака желудка с различными уровнями экспрессии CLDN18.2 EC50 ADCC-активности 18B10-HaLa с низким содержанием фукозы составляла около 0,008 мкг/мл. По сравнению с IMAB362, 18B10-HaLa с низким содержанием фукозы имел по крайней мере в 100 раз более высокую активность ADCC.
[00559] 5. Анализ с использованием репортерного гена ADCC на различных клеточных линиях рака желудка с использованием РВМС в качестве эффекторных клеток
[00560] Тест ADCC проводили по тому же протоколу, что и выше (см. раздел 7 примера 10). Как показано на фигурах 26A-26D, 18B10-HaLa с низким содержанием фукозы на различных клеточных линиях рака желудка значительно индуцировал более высокий ADCC-эффект, чем IMAB362. IMAB362 практически не индуцировал какую-либо цитотоксичность при низкой концентрации (0,01~0,1 мкг/мл). Однако при концентрации 0,1 мкг/мл цитотоксичность 18B10-HaLa с низким содержанием фукозы была почти насыщенной.
[00571] 6. Оптимизированный анализ ADCC на NUGC4 с использованием РВМС в качестве эффекторных клеток
[00562] Для дальнейшего изучения был разработан оптимизированный анализ ADCC с использованием РВМС человека в качестве эффекторных клеток. Вкратце, извлекали замороженные РВМС из жидкого азота и ресуспендировали клетки с RPMI1640+10% FBS при плотности 5×106/мл и перед использованием инкубировали их в инкубаторе при температуре 37°C и 5% CO2 в течение 5 часов. Клетки-мишени NUGC4 метили с помощью CellTrace™ Far Red (Invitrogen, кат. № C34564), следуя инструкциям. В 96-луночный планшет добавляли меченые клетки NUGC4 и разбавленное антитело и инкубировали в инкубаторе при температуре 37°C и 5% CO2 в течение 30 минут. Затем в соответствующие лунки добавляли клетки РВМС и инкубировали клетки в инкубаторе в течение 15 часов. В конце культивирования добавляли окрашивающий раствор йодистого пропидия (PI), чтобы пометить мертвые клетки NUGC4. Анализировали процентное содержание PI-положительных клеток в CellTrace™ Far Red положительных клетках с помощью проточной цитометрии. Специфическую цитотоксичность рассчитывали путем вычитания процента неспецифического уничтожения.
[00563] Как показано на фигуре 27, репрезентативные данные, максимальная удельная цитотоксичность 18B10-HaLa с низким содержанием фукозы достигала более 60% при концентрации 1,2 мкг/мл, а ее ЕС50 составляла 0,014 мкг/мл, в то время как максимум IMAB362-аналога составляла только 40% при самой высокой концентрации (30 мкг/мл), а его EC50 составляла 0,54 мкг/мл, что более чем в 30 раз больше, чем у 18B10-HaLa с низким содержанием фукозы.
[00564] Пример 15: Противоопухолевая активность of 18B10-HaLa с низким содержанием фукозы in vivo
[00565] 1. Противоопухолевая эффективность MKN45 с высоким уровнем CLDN18.2 и hPBMC в ксенотрансплантатной модели с совместной инокуляцией с использованием мышей NOD-SCID
[00566] Клетки РВМС человека были приобретены у компании Allcells. 60 самок мышей NOD-SCID класса SPF случайным образом разделяли на 6 групп (n=10), 10 мышам инокулировали 5×106 клеток MKN45 с высоким уровнем CLDN18.2 и 50% матригель (BD) путем подкожной инъекции в правый бок в качестве модельной группы (без РВМС), и 50 мышам инокулировали 5×106 клеток MKN45 с высоким уровнем CLDN18.2 и 5×106 клеток РВМС человека с 50% матригелем (BD) в качестве терапевтической группы. Через 4 часа после инокуляции два раза в неделю в течение 5 недель путем внутрибрюшинной инъекции мышам вводили 10 мг/кг изотипического контроля, 1 мг/кг, 3 мг/кг и 10 мг/кг 18B10-HaLa с низким содержанием фукозы. В конце исследования животных забивали ингаляцией СО2. Размер и объем опухоли измеряли 2-3 раза в неделю. Результаты были проанализированы с помощью Prism GraphPad и выражены как среднее±SEM.
[00567] Как показано на фигуре 28A, рост опухоли значительно ингибировался 18B10-HaLa с низким содержанием фукозы дозозависимым образом. В частности, при приеме 10 мг/кг 18B10-HaLa с низким содержанием фукозы большинство опухолей (7/10) исчезало в конце исследования (фигура 28В). Скорость ингибирования роста опухоли 18B10-HaLa с низким содержанием фукозы также зависела от дозировки, и TGI группы, получавшей 10 мг/кг, достигал 95,86% (таблица 16). По сравнению с аналогом IMAB362, 1810-HaLa с низким содержанием фукозы обладает гораздо более мощной противоопухолевой активностью. При этом 18B10-HaLa с низким содержанием фукозы не влиял на вес животных (данные не представлены).
[00568] Ингибирование роста опухоли антителами в ксенотрансплантатной модели опухоли с совместной инокуляцией MKN45 с высоким уровнем CLDN18.2 и hPBMC на 36-й день (среднее±SEM, n=10)
(±SEM, мм3)
[00569] 2. Эффективность 18B10-HaLa с низким содержанием фукозы в сочетании с оксалиплатином и 5-Fu на модели опухоли с MKN45 с высоким содержанием CLDN18.2 у голых мышей
[00570] Самкам голых мышей класса SPF инокулировали смесь 5×106 клеток MKN45 с высоким уровнем CLDN18.2 с 50% матригелем. Когда размер опухоли составлял около 90мм3, мышей отбирали и случайным образом разделяли на 4 группы (n=8). Животных обрабатывали 10 мг/кг изотипического контроля и носителя, 10 мг/кг 18B10-HaLa с низким содержанием фукозы, 2,5 мг/кг оксалиплатина и 30 мг/кг 5-FU, и 10 мг/кг 18B10-HaLa с низким содержанием фукозы в сочетании с 2,5 мг/кг оксалиплатина и 30 мг/кг 5-FU, 18B10-HaLa с низким содержанием фукозы вводили дважды в неделю в течение 4 недель путем внутрибрюшинной инъекции, тогда как оксалиплатин и 5FU вводили один раз в неделю в течение 4 недель путем внутривенной инъекции. Размер опухоли измеряли дважды или трижды в неделю в двух измерениях с помощью штангенциркуля (INSIZE), а объем выражали в мм3 по формуле: V=0,5a×b2, где a и b обозначают диаметры опухоли по длинной и короткой части, соответственно. Результаты были проанализированы с использованием Prism GraphPad и выражены как среднее±SEM. Сравнения между двумя группами были сделаны с помощью Т-критерия, и разница считается значимой, если р составляет*<0,05 и **<0,01.
[00571] Как показано на фигуре 29 и в таблице 17, без РВМС группы с одним агентом 18B10-HaLa с низким содержанием фукозы и оксалиплатин+5-FU имели только умеренное ингибирование роста опухоли с TGI 47% и 52%, соответственно. Но их комбинация имела усиленное ингибирование опухоли на 69% со значительной разницей по сравнению с группами с одним агентом.
[00572] ТАБЛИЦА 17. Ингибирование роста опухоли комбинацией 18B10-HaLa с низким содержанием фукозы с оксалиплатином и 5-FU на модели опухоли с MKN45 с высоким содержанием CLDN18.2 на 28-й день (среднее±SEM, n=8)
(±SEM, мм3)
[00573] 3. Эффективность 18B10-HaLa с низким содержанием фукозы в сочетании с паклитакселом на модели опухоли с MKN45 с высоким содержанием CLDN18.2 у голых мышей
[00574] Клетки MKN45 с высоким содержанием CLDN18.2 держали in vitro в виде монослойной культуры в среде RPMI1640 (Thermo Fisher) с добавлением 10% инактивированной нагреванием эмбриональной бычьей сыворотки (ExCell Biology), 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина (Hyclone) при температуре 37°C и 5% CO2. Для инокуляции опухоли собирали и подсчитывали клетки в фазе экспоненциального роста. Каждой самке голых мышей Balb/c подкожно вводили 5×106 клеток с 50% матригелем (BD) путем инъекции в правый бок. Через 8-11 дней после инокуляции отбирали 24 мыши с размером опухоли около 100 мм3, случайным образом делили на 3 группы (n=8). Затем мышам вводили изотипический контроль или 18B10-HaLa с низким содержанием фукозы в дозе 10 мг/кг два раза в неделю в течение 3 недель путем внутрибрюшинной инъекции. Раз в неделю внутривенно вводили 5 мг/кг паклитаксела. В конце исследования животных забивали ингаляцией СО2. Размер опухоли измеряли в двух измерениях с помощью штангенциркуля (INSIZE), а объем выражали в мм3 по формуле: V=0,5a×b2 ((где a и b представляют собой длину и ширину опухоли, соответственно). Коэффициент ингибирования роста опухоли (TGI%) рассчитывали по формуле: TGI%=(1-(TVDt (терапевтическая группа)/TVDt(контрольная группа))×100%. TVDt представляет собой объем опухоли при каждом последующем измерении. Гистограммы были созданы с помощью Prism GraphPad (среднее±SEM), и для статистического анализа использовали Т-анализ. p<0,05 представляет собой достоверную разницу между группами; p <0,01 представляет собой высокозначимую разницу между группами.
[00575] Как показано на фигуре 30A, по сравнению с изотипическим контролем, 18B10-HaLa с низким содержанием фукозы значительно ингибирует рост опухоли, начиная с 5-го дня, и его TGI составлял около 43%. Точно так же паклитаксел, как широко используемый химиотерапевтический агент второй линии для лечения рака желудка, также имел около 45% TGI. Но когда они были объединены, степень ингибирования опухоли достигла 61% со значительным отличием от групп с одним агентом (фигура 30В, таблица 18). Однако без инокулированных опухолью РВМС человека объем опухоли был значительно больше, чем у РВМС человека. Значимого изменения массы тела во всех группах не наблюдалось.
[00576] ТАБЛИЦА 18. Ингибирование роста опухоли антителами на ксенотрансплантатной модели опухоли с MKN45 с высоким содержанием CLDN18.2 на день 29 (среднее±SEM, n=10)
(±SEM, mm3)
[00577] 4. Эффективность 18B10-HaLa с низким содержанием фукозы в сочетании с паклитакселом в модели опухоли GC02-0004 PDX у голых мышей
[00578] Опухолевая ткань рака желудка ксенографта человеческой опухоли (PDX) была получена от пациента с аденокарциномой/раком желудка (№: GC-02-004) из Пекинской онкологической больницы и проанализирована после 6 пассажей на бестимусных мышах. Экспрессию CLDN18.2 определяли с помощью иммуногистохимии (IHC) с использованием 3 мкг/мл GC182-биотина, который является общепринятым антителом IHC для обнаружения CLDN18.2. GC182 был создан Mabspace Bioscience в соответствии с последовательностью, описанной в WO2013167259. Относительная доля положительных клеток в этой опухолевой ткани составляла от 40% до 70% (фигура 31А, 200-кратное увеличение). Экспрессию HER2 и PD-L1 также определяли с помощью IHC с использованием кроличьего mAb D8F12 (Cell Signaling Technology, кат. № по 4290) и SP263 (производимого MabSpace Bioscience в соответствии с последовательностью, описанной в WO2016124558), соответственно. В результате эта опухолевая ткань была как HER2-отрицательной (Фигура 31B), так и PD-L1-отрицательной (Фигура 31C).
[00579] Каждой мыши подкожно инокулировали небольшой блок опухолевой ткани диаметром приблизительно 3 мм, который отделяли от интегрированного участка опухолевого отростка мыши с опухолью. Через 2 недели после инокуляции отбирали животных с размером опухоли около 50 мм3 и случайным образом разделяли на 3 группы, каждая из которых состояла из 8 мышей. Два раза в неделю внутрибрюшинно в дозе 10 мг/кг вводили 18B10-HaLa с низким содержанием фукозы и контрольное антитело. Раз в неделю внутривенно вводили 5 мг/кг паклитаксела. Лечение продолжалось в течение 5 недель после первой инъекции. Объем опухоли и массу мыши измеряли 2-3 раза в неделю. В конце исследования животных забивали ингаляцией СО2. Размер опухоли измеряли в двух измерениях с помощью штангенциркуля (INSIZE), а объем выражали в мм3 по формуле: V=0,5a×b2 ((где a и b представляют собой длину и ширину опухоли, соответственно). Коэффициент ингибирования роста опухоли (TGI%) рассчитывали по формуле: TGI%=(1-(TVDt (терапевтическая группа)/TVDt(контрольная группа))×100%. TVDt представляет собой объем опухоли при каждом последующем измерении. Гистограммы были созданы с помощью Prism GraphPad (среднее±SEM), и для статистического анализа использовали Т-анализ. p<0,05 представляет собой достоверную разницу между группами; p <0,01 представляет собой высокозначимую разницу между группами.
[00580] Как показано на фигуре 31D, 18B10-HaLa с низким содержанием фукозы приводил к степени ингибирования опухоли на 48%. Точно так же паклитаксел, как широко используемый химиотерапевтический агент второй линии для лечения рака желудка, также имел только 45% степень ингибирования опухоли. Но когда они были объединены, степень ингибирования опухоли достигала 68% со значительным отличием от групп с одним агентом (таблица 19). Как показано на фигуре 31E, 5 мг/кг паклитаксела, по-видимому, оказывали незначительное токсическое действие на массу тела мышей, в то время как другие виды лечения не оказывали такого влияния.
[00581] ТАБЛИЦА 19. Ингибирование роста опухоли антителами в модели опухоли GC02-0004 PDX на день 36 (среднее±SEM, n=10)
(±SEM, mm3)
[00582] 5. Комбинация с DC101 в ксенотрансплантатной модели опухоли с MKN45 с высоким содержанием CLDN18.2
[00583] DC101 представляет собой моноклональное антитело, реагирующее с мышиным VEGFR-2 (рецептором 2 фактора роста эндотелия сосудов), также известным как CD309, KDR и Flk-1. VEGFR-2 является членом семейства тирозиновых протеинкиназ. После связывания со своим лигандом VEGF, VEGFR-2 играет ключевую роль в развитии и проницаемости сосудов. Доказано, что DC101 конкурентно блокирует связывание VEGF и VEGFR-2, что приводит к снижению плотности микрососудов опухоли и росту опухоли. Это антитело было произведено MabSpace Biosciences (Suzhou) Co., Limited в соответствии с последовательностью, описанной в US5840301.
[00584] Самкам голых мышей класса SPF инокулировали смесью 5×106 клеток MKN45-CLDN18.2-high с 50% матригелем. Когда размер опухоли составлял около 90 мм3, мышей с опухолью отбирали и случайным образом разделяли на 4 группы (n=8). Животных лечили 10 мг/кг изотипического контроля, 10 мг/кг 18B10-HaLa с низким содержанием фукозы, 3 мг/кг DC101 и 10 мг/кг 18B10-HaLa с низким содержанием фукозы в сочетании с 3 мг/кг DC101. Все антитела вводили дважды в неделю в течение 4 недель путем внутрибрюшинной инъекции. Размер опухоли измеряли дважды или трижды в неделю в двух измерениях с помощью штангенциркуля (INSIZE), а объем выражали в мм3 по формуле: V=0,5a×b2, где a и b обозначают длинный и короткий диаметры опухоли, соответственно. Результаты были проанализированы с использованием Prism GraphPad и выражены как среднее±SEM. Сравнения между двумя группами были сделаны с помощью Т-критерия, и разница считается значимой, если р составляет *<0,05 и **<0,01.
[00585] Как показано на фигуре 32 и в таблице 20, без РВМС группы с одним агентом (18B10-HaLa с низким содержанием фукозы или DC101) имели некоторую степень ингибирования опухоли с TGI 47% и 35% соответственно. При их сочетании рост опухоли почти остановился со степенью ингибирования 75%, что значительно отличается от групп с одним агентом.
[00586] TABLE 20. ТАБЛИЦА 20. Ингибирование роста опухоли (TGI) антителами в ксенотрансплантатной модели с MKN45-CLDN18.2 на день 22 (среднее±SEM, n=6)
(±SEM, мм3)
[00587] Пример 18: Противоопухолевая активность 18B10-HaLa с низким содержанием фукозы в отношении клеток рака поджелудочной железы in vitro
[00588] 1. Получение клеточных линий MIA PaCa-2-CLDN18.2 и BxPC-3-CLDN18.2
[005899] Клеточные линии MIA PaCa-2-CLDN18.2 и BxPC-3-CLDN18.2 были сконструированы компанией MabSpace Biosciences (Suzhou) Co., Limited. Вкратце, клетки MIA PaCa-2 (Шанхайский институт биологических наук, кат. № SCSP-568) и клетки BxPC-3 (Шанхайский институт биологических наук, кат. № TCHu12) трансфицировали плазмидами pcDNA3.1/hCLDN18.2 и отбирали с G418 для получения стабильно экспрессирующих клеточных линий MIA PaCa-2-CLDN18.2 и BxPC-3-CLDN18.2. Уровень экспрессии CLDN18.2 определяли с помощью антитела 18B10-HaLa с низким содержанием фукозы. Клон одной клетки с самым высоким сигналом отбирали и амплифицировали для банка клеток.
2. [00590] Связывание FACS с клеточными линиями рака поджелудочной железы с использованием 18B10-HaLa с низким содержанием фукозы
[00591] Связывание FACS осуществляли в соответствии с тем же протоколом, что и в разделе 2 примера 7. Как показано на Фигурах 33A-33B, 18B10-HaLa с низким содержанием фукозы может связываться с двумя клеточными линиями с более высокой эффективностью, чем у IMAB362. Максимальный сигнал 18B10-HaLa с низким содержанием фукозы был значительно выше, чем у IMAB362. EC50 18B10-HaLa с низким содержанием фукозы составлял около 0,53 мкг/мл, что также было значительно ниже, чем у IMAB362.
[00592] 3. Анализ с использованием репортерного гена ADCC на клеточных линиях рака поджелудочной железы с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток
[00593] Тест ADCC проводили по тому же протоколу, что и выше (см. раздел 2 примера 7). Как показано на фигуре 34A-34B, EC50 ADCC-активности 18B10-HaLa с низким содержанием фукозы составляла около 0,001 мкг/мл. По сравнению с IMAB362, 18B10-HaLa с низким содержанием фукозы имел примерно в 4 раза более высокую активность ADCC.
[00594] Пример 19: Противоопухолевая активность 18B10-HaLa с низким содержанием фукозы в отношении клеток рака поджелудочной железы in vivo
[00595] 1. Эффективность на ксенотрансплантатной модели MIA PaCa-2-CLDN18.2 с использованием голых мышей
[00596] Каждые 5-6 недель самкам голых мышей Balb/c инокулировали 5×106 клеток MIA PaCa-2-CLDN18.2 с 50% матригелем (BD) путем подкожной инъекции в правый бок. Через 12 дней после инокуляции были отобраны 24 мыши с размером опухоли около 70 мм3, которые были случайным образом разделяли на 4 группы (n=6). Затем мышам в течение 5 недель два раза в неделю путем внутрибрюшинной инъекции вводили изотипический контроль или 18B10-HaLa с низким содержанием фукозы, или IMAB362 в дозе 10 мг/кг, или PBS в том же объеме. В конце исследования животных забивали ингаляцией СО2. Размер и объем опухоли измеряли 2-3 раза в неделю. Результаты были проанализированы с использованием Prism GraphPad и выражены как среднее±SEM.
[00597] Как показано на фигуре 35, 18B10-HaLa с низким содержанием фукозы продемонстрировал лучшую противоопухолевую активность, чем IMAB362, при измерении размера опухоли и TGI, при этом оба показателя были значительно лучше, чем изотипический контроль (таблица 21). Значимого изменения массы тела во всех группах не наблюдалось.
[00598] ТАБЛИЦА 21. Ингибирование роста опухоли (TGI) антителами в ксенотрансплантатной модели MIA PaCa-2-CLDN18.2 на день 36 (среднее±SEM, n=6)
(±SEM, мм3)
[00599] 2. Эффективность в ксенотрансплантатной модели BxPC-3-CLDN18.2 с использованием голых мышей
[00600] Создавали ксенотрансплантатную модель BxPC-3-CLDN18.2 и обрабатывали антителами, следуя той же процедуре, что и модель MIA PaCa-2-CLDN18.2 (раздел 1 примера 19).
[00601] Как показано на фигуре 36, IMAB362 вообще не мог ингибировать рост опухоли, в то время как 18B10-HaLa с низким содержанием фукозы проявлял некоторую степень противоопухолевой активности (таблица 22). Значимого изменения массы тела во всех группах не наблюдалось.
[00602] ТАБЛИЦА 22. Ингибирование роста опухоли (TGI) антителами в ксенотрансплантатной модели BxPC-3-CLDN18.2 на день 34 (среднее±SEM, n=6)
(±SEM, мм3)
[00603] Пример 20: Противоопухолевая активность 18B10-HaLa с низким содержанием фукозы в отношении клеток рака легких in vitro
[00604] 1. FACS с клеточными линиями рака легких с использованием 18B10-HaLa с низким содержанием фукозы
[00605] NCI-H146 был приобретен в ATCC (кат. № ATCC® HTB-173). NCI-H460-CLDN18.2 был приобретен у Kyinno (кат. № KC-1450) и был стабильно трансфицирован CLDN18.2. Связывание FACS осуществляли в соответствии с тем же протоколом, что и в разделе 2 примера 7. Как показано на фигурах 37A-37B, 18B10-HaLa с низким содержанием фукозы может связываться с двумя клеточными линиями дозозависимым образом. Для гораздо более высокого уровня экспрессии CLDN18.2 в клетке NCI-H460-CLDN18.2, чем в клетке NCI-H146, максимальный сигнал связывания первой клетки также был значительно выше, чем у более поздней.
[00606] 2. Анализ с использованием репортерного гена ADCC на NCI-H146 с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток
[00607] Тест ADCC проводили по тому же протоколу, что и выше (см. раздел 2 примера 7). Как показано на Фигуре 38, 18B10-HaLa с низким содержанием фукозы мог индуцировать ADCC на клетках NCI-H146, а EC50 составляла около 0,003 мкг/мл. По сравнению с IMAB362, 18B10-HaLa с низким содержанием фукозы имел примерно в 150 раз более высокую активность ADCC.
[00608] 3. Анализ ADCC на NCI-H460-CLDN18.2 с использованием PBMC в качестве эффекторных клеток
[00609] Тест ADCC, опосредованной первичными РВМС, проводили в соответствии с аналогичным протоколом, описанным выше (раздел 6 примера 16). Вкратце, замороженные РВМС извлекали из жидкого азота и ресуспендировали клетки с RPMI1640+10% FBS при плотности 5×106/мл и перед использованием инкубировали в инкубаторе при температуре 37°C и 5% CO2 в течение 5 часов. Клетки-мишени клеток NCI-H460-CLDN18.2 или клеток NCI-H292 метили с помощью CellTrace™ Far Red, следуя инструкциям. Добавляли меченые клетки-мишени и разбавленное антитело в 24-луночный планшет для культивирования клеток и инкубировали их в инкубаторе при температуре 37°C и 5% CO2 в течение 30 минут. Затем в соответствующие лунки добавляют клетки РВМС при соотношении E:T 40:1 и инкубировали клетки в инкубаторе в течение 15 часов. В конце культивирования из каждой лунки в соответствующую пробирку объемом 15 мл собирали суспензионные клетки и прикрепленные клетки (с мягким расщеплением трипсином). Пробирки центрифугировали для удаления супернатанта. Чтобы ресуспендировать клетки-мишени и пометить мертвые клетки-мишени добавляли PBS с раствором для окрашивания йодидом пропидия (PI). Анализировали процентное содержание PI-положительных клеток в CellTrace™ Far Red положительных клетках с помощью проточной цитометрии. Специфическую цитотоксичность рассчитывали путем вычитания процента неспецифического уничтожения.
[00610] Как показано на фигуре 39, 18B10-HaLa с низким содержанием фукозы проявляла ADCC-активность только в отношении клеток NCI-H460-CLDN18.2, а не NCI-H292, которая является CLDN18.2-отрицательной клеткой аденокарциномы легкого человека.
[00611] Пример 21: Противоопухолевая активность 18B10-HaLa с низким содержанием фукозы в отношении клеток рака легких in vivo
[00612] 1. Эффективность на модели опухоли при совместной инокуляции NCI-H146 и РВМС человека с использованием голых мышей
[00613] Создавали модель опухоли с совместной инокуляцией NCI-H146 и РВМС человека и обрабатывали антителами в соответствии с той же процедурой, что и модель MKN45 с высоким содержанием CLDN18.2 (раздел 1 примера 17). 30 мышам NOD-SCID инокулировали 5×106 клеток NCI-H146+1,5×106 клеток РВМС человека и 50% матригель. Через 4 часа после инокуляции животных случайным образом разделяли на 3 группы (n=10).
[00614] Как показано на фигурах 40A-40B и в таблице 23, при обработке РВМС человека и 18B10-HaLa с низким содержанием фукозы опухоли NCI-H146 практически не росли, и между группами была очень небольшая разница.
[00615] ТАБЛИЦА 23. Ингибирование роста опухоли (TGI) антителами в модели совместной инокуляции NCI-H146 и PBMC на день 32 (среднее±SEM, n=10)
(±SEM, мм3)
[00616] 2. Эффективность на модели опухоли с совместной инокуляцией NCI-H460-CLDN18.2 и РВМС человека с использованием мышей NOD-SCID
[00617] Клетки РВМС человека были приобретены у Allcells. 20 самок мышей NOD-SCID класса SPF случайным образом разделяли на 2 группы (n=10). Мышей инокулировали 3×106 клетками NCI-H460-CLDN18.2 и 5×106 клетками РВМС человека с 50% матригелем (BD) путем подкожной инъекции на правом фланге в качестве модельной группы. Через 4 часа после инокуляции мышам путем внутрибрюшинной инъекции два раза в неделю в течение 5 недель вводили 10 мг/кг изотипического контроля и 10 мг/кг 18B10-HaLa с низким содержанием фукозы. В конце исследования животных забивали ингаляцией СО2. Размер и объем опухоли измеряли 2-3 раза в неделю. Результаты были проанализированы с помощью Prism GraphPad и выражены как среднее±SEM.
[00618] Как показано на фигуре 41 и в таблице 24 с РВМС человека, рост опухоли в группе 18B10-HaLa с низким содержанием фукозы был медленнее, чем в группе изотипического контроля, с 36% TGI.
[00619] ТАБЛИЦА 24. Ингибирование роста опухоли (TGI) антителами в модели опухоли NCI-H460-CLDN18.2 на день 25 (среднее±SEM, n=10)
(±SEM, мм3)
[00620] Пример 22: Противоопухолевая активность 18B10-HaLa с низким содержанием фукозы в отношении клеток рака толстой кишки in vitro
[00621] 1. Связывание FACS с клеточными линиями рака толстой кишки с использованием 18B10-HaLa с низким содержанием фукозы
[00622] SK-CO-1 был приобретен в ATCC (кат. №, ATCC® HTB-39). Связывание FACS осуществляли в соответствии с тем же протоколом, что и в разделе 2 примера 7. Как показано на фигуре 42, 18B10-HaLa с низким содержанием фукозы может связываться с клеткой SK-CO-1 дозозависимым образом. EC50 составляла примерно 1,78 мкг/мл.
[00623] 2. Анализ с использованием репортерного гена ADCC на клеточных линиях рака толстой кишки с использованием Jurkat-NFAT-luc-FcγRIIIA-V176 в качестве эффекторных клеток
[00624] Тест ADCC проводили по тому же протоколу, что и выше (см. раздел 2 примера 7). Как показано на фигуре 43, 18B10-HaLa с низким содержанием фукозы может индуцировать ADCC на клетке SK-CO-1. По сравнению с IMAB362, 18B10-HaLa с низким содержанием фукозы обладала гораздо более высокой активностью ADCC.
[00625] Пример 23: Анализ взаимодействия 18B10-HaLa с низким содержанием фукозы с Fc-рецепторами человека с использованием ForteBio Octet RED96
[00626] 1. Взаимодействие с белками FcγRIIIa
[00627] Биотинилированный белок FcγRIIIa-V176 человека или биотинилированный белок FcγRIIIa-F176 человека с His-меткой в концентрации 100 нМ в 1× кинетическом буфере (1× PBS, pH 7,4, 0,002% Tween 20) наносили на 7 предварительно влажных биосенсоров SA (PALL, ForteBio, кат. № 18-5019) и инкубировали с различными концентрациями 18B10-HaLa с низким содержанием фукозы или IMAB362 в растворе. Все данные по связыванию собирали при температуре 30°C. Эксперименты состояли из 5 стадий: 1. Определение исходного уровня (60 с); 2. Загрузка биотинилированного белка FcγRIIIa-V176 человека или биотинилированного белка FcγRIIIa-F176 человека на биосенсор SA (120 с); 3. Определение второго исходного уровня (60 с); 4. Ассоциация 18B10-HaLa с низким содержанием фукозы или IMAB362 для определения kon (60 с); и 5. Диссоциация антител для определения koff (60 с). Использовали 7 различных концентраций антител, включая 1000 нМ, 500 нМ, 250 нМ, 125 нМ, 62,5 нМ, 31,3 нМ и 0 нМ, и. Стадии основного уровня и диссоциации проводили только в 1× кинетическом буфере. Отношение koff к kon определяет KD. Биосенсоры регенерируют в течение 5 с в буфере для регенерации (10 мМ глицин-HCL, pH 1,5) с последующей нейтрализацией в течение 5 с в буфере для нейтрализации (1×PBS, pH 7,4, 0,002% Tween 20), этот процесс повторяют 3 раза.
[00628] Как показано в таблице 25, аффинность 18B10-HaLa с низким содержанием фукозы к человеческому FcγRIIIa-V176 и человеческому белку FcγRIIIa-F176 было немного выше, чем у IMAB362, что может быть вызвано более низким фукозилированием.
[00629] Таблица 25. Кинетическая константа связывания антител CLDN18.2 с белком FcγRIIIa человека
[00630] 2. Взаимодействие с белком FcRn (FCGRT&B2M)
[00631] Белок FcRn человека (FCGRT&B2M) с His-меткой при 50 нМ в FcRn в 1× кинетическом буфере (1× PBS, pH 6,0, 0,002% Tween 20) наносили на 7 предварительно смоченных биосенсоров Ni-NTA и инкубировали с различными концентрациями 18B10-HaLa с низким содержанием фукозы или IMAB362 в растворе. Все данные по связыванию собирали при температуре 30°C. Эксперименты состояли из 5 стадий: 1. Определение исходного уровня (60 с); 2. Загрузка белка Fc-гамма-FcRn человека (FCGRT&B2M) на биосенсор Ni-NTA (150 с); 3. Определение второго исходного уровня (80 с); 4. Ассоциация 18B10-HaLa с низким содержанием фукозы или IMAB362 для определения kon (60 с); и 5. Диссоциация антител для определения koff (60 с). Использовали 7 различных концентраций антител, включая 500 нМ, 250 нМ, 125 нМ, 62,5 нМ, 31,3 нМ, 15,6 нМ и 0 нМ, и антитела разбавляли FcRn кинетическим буфером (pH 6,0). Основную стадию проводили только в 1× кинетическом буфере, основную2 и стадии диссоциации проводили в FcRn кинетическом буфере (pH 6,0). Отношение koff к kon определяет KD. Биосенсоры регенерировали в течение 5 секунд в буфере регенерации, после чего проводили нейтрализацию в течение 5 секунд в буфере нейтрализации, этот процесс повторяли 3 раза.
[00632] Как показано в таблице 26, на аффинность 18B10-HaLa с низким содержанием фукозы к человеческому белку FcRn не влияло более низкое фукозилирование, даже немного более высокое, чем у IMAB362.
[00633] Таблица 26. Кинетическая константа связывания антител CLDN18.2 с белком FcRn человека
[00634] 3. Взаимодействие с белком C1q человека
[00635] 18B10-HaLa с низким содержанием фукозы или IMAB362 биотинилировали путем смешивания с N-гидроксисукцинимидным эфиром биотинамидогексановой кислоты (Sigma) в ДМФА. Биотинилированный 18B10-HaLa с низким содержанием фукозы или IMAB362 в концентрации 100 нМ в 1× кинетическом буфере наносили на 7 предварительно смоченных биосенсоров SA и инкубировали с различными концентрациями C1q человека в растворе. Все данные по связыванию собирали при 30°C. Эксперименты состояли из 5 стадий: 1. Определение исходного уровня (60 с); 2. Загрузка биотинилированной 18B10-HaLa с низким содержанием фукозы или IMAB362 на биосенсор SA (150 с); 3. Определение второго исходного уровня (60 с); 4. Ассоциация C1q человека для измерения kon (30 с); и 5. Диссоциация C1q человека для измерения koff (30 с). Использовали 7 различных концентраций антител, включая 50 нМ, 25 нМ, 12,5 нМ, 6,25 нМ, 3,13 нМ, 1,56 нМ и 0 нМ, и C1q человека разбавляли 1× кинетическим буфером. Стадии базовой линии и диссоциации проводили только в 1× кинетическом буфере. Отношение koff к kon определяет KD. Биосенсоры используются только один раз..
[00636] Как показано в таблице 27, аффинность 18B10-HaLa с низким содержанием фукозы к человеческому белку C1q не совсем аналогична аффинности IMAB362.
[00637] Таблица 27. Кинетическая константа связывания антител CLDN18.2 с белком C1q человека
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Сучжоу трансента терапьютикс Ко., Лтд.
<120> НОВЫЕ АНТИ-CLDN18.2 АНТИТЕЛА
<130> 063694-8003WO04
<150> PCT/CN2019/101563
<151> 2019-08-20
<150> PCT/CN2020/097559
<151> 2020-06-22
<160> 75
<170> PatentIn version 3.5
<210> 1
<211> 5
<212> БЕЛОК
<213> Mus musculus
<400> 1
Gly Tyr Asn Met Asn
1 5
<210> 2
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 2
Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 3
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 3
Asn Ile Asp Pro Tyr Tyr Gly Ala Thr Arg Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 4
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 4
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 5
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 5
Ser Tyr Tyr Gly Asn Ala Phe Asp Tyr
1 5
<210> 6
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 6
Gln Asn Asp Tyr Ser Phe Pro Phe Thr
1 5
<210> 7
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 7
Tyr Ile Asp Pro Tyr Tyr Gly Gly Thr Arg Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 8
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 8
Gln Asn Asp Tyr Ser Tyr Pro Phe Thr
1 5
<210> 9
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 9
His Ile Asp Pro Tyr Tyr Val Thr Thr Thr Tyr Asn Gln Lys Phe Arg
1 5 10 15
Gly
<210> 10
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 10
Lys Ser Ser Gln Ser Leu Phe Asn Ser Gly Asn Gln Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 11
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 11
Ser Phe Tyr Gly Asn Ala Phe Asp Tyr
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 12
Gln Asn Asp Tyr Tyr Tyr Pro Leu Thr
1 5
<210> 13
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 13
Thr Tyr Phe Ile Gly Val Gly
1 5
<210> 14
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 14
Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Leu Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 15
<211> 16
<212> БЕЛОК
<213> Mus musculus
<400> 15
His Ile Trp Trp Asn Asp Asn Lys Tyr Tyr Asn Thr Ala Leu Lys Ser
1 5 10 15
<210> 16
<211> 7
<212> БЕЛОК
<213> Mus musculus
<400> 16
Trp Ala Ser Thr Arg Lys Ser
1 5
<210> 17
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 17
Met Gly Ser Gly Ala Trp Phe Thr Tyr
1 5
<210> 18
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 18
Gln Asn Asp Tyr Ser Tyr Pro Leu Thr
1 5
<210> 19
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 19
Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 20
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 20
Lys Ser Ser Gln Asn Leu Leu Asn Asn Gly Asn Gln Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 21
<211> 9
<212> БЕЛОК
<213> Mus musculus
<400> 21
Met Tyr His Gly Asn Ala Phe Asp Tyr
1 5
<210> 22
<211> 17
<212> БЕЛОК
<213> Mus musculus
<400> 22
Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Arg Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 23
<211> 98
<212> БЕЛОК
<213> Homo sapiens
<400> 23
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg
<210> 24
<211> 95
<212> БЕЛОК
<213> Homo sapiens
<400> 24
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Asn Asn Lys Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr Tyr Ser Thr Pro
85 90 95
<210> 25
<211> 118
<212> БЕЛОК
<213> Homo sapiens
<400> 25
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ile Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Met Tyr His Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 26
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 26
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Leu Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 27
<211> 118
<212> БЕЛОК
<213> Homo sapiens
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ile Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Met Tyr His Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 28
<211> 113
<212> БЕЛОК
<213> Homo sapiens
<400> 28
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Met Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Leu Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 29
<211> 118
<212> БЕЛОК
<213> Homo sapiens
<400> 29
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ile Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Met Tyr His Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 30
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 30
Met Ala Val Thr Ala Cys Gln Gly Leu Gly Phe Val Val Ser Leu Ile
1 5 10 15
Gly Ile Ala Gly Ile Ile Ala Ala Thr Cys Met Asp Gln Trp Ser Thr
20 25 30
Gln Asp Leu Tyr Asn Asn Pro Val Thr Ala Val Phe Asn Tyr Gln Gly
35 40 45
Leu Trp Arg Ser Cys Val Arg Glu Ser Ser Gly Phe Thr Glu Cys Arg
50 55 60
Gly Tyr Phe Thr Leu Leu Gly Leu Pro Ala Met Leu Gln Ala Val Arg
65 70 75 80
Ala Leu Met Ile Val Gly Ile Val Leu Gly Ala Ile Gly Leu Leu Val
85 90 95
Ser Ile Phe Ala Leu Lys Cys Ile Arg Ile Gly Ser Met Glu Asp Ser
100 105 110
Ala Lys Ala Asn Met Thr Leu Thr Ser Gly Ile Met Phe Ile Val Ser
115 120 125
Gly Leu Cys Ala Ile Ala Gly Val Ser Val Phe Ala Asn Met Leu Val
130 135 140
Thr Asn Phe Trp Met Ser Thr Ala Asn Met Tyr Thr Gly Met Gly Gly
145 150 155 160
Met Val Gln Thr Val Gln Thr Arg Tyr Thr Phe Gly Ala Ala Leu Phe
165 170 175
Val Gly Trp Val Ala Gly Gly Leu Thr Leu Ile Gly Gly Val Met Met
180 185 190
Cys Ile Ala Cys Arg Gly Leu Ala Pro Glu Glu Thr Asn Tyr Lys Ala
195 200 205
Val Ser Tyr His Ala Ser Gly His Ser Val Ala Tyr Lys Pro Gly Gly
210 215 220
Phe Lys Ala Ser Thr Gly Phe Gly Ser Asn Thr Lys Asn Lys Lys Ile
225 230 235 240
Tyr Asp Gly Gly Ala Arg Thr Glu Asp Glu Val Gln Ser Tyr Pro Ser
245 250 255
Lys His Asp Tyr Val
260
<210> 31
<211> 261
<212> БЕЛОК
<213> Homo sapiens
<400> 31
Met Ser Thr Thr Thr Cys Gln Val Val Ala Phe Leu Leu Ser Ile Leu
1 5 10 15
Gly Leu Ala Gly Cys Ile Ala Ala Thr Gly Met Asp Met Trp Ser Thr
20 25 30
Gln Asp Leu Tyr Asp Asn Pro Val Thr Ser Val Phe Gln Tyr Glu Gly
35 40 45
Leu Trp Arg Ser Cys Val Arg Gln Ser Ser Gly Phe Thr Glu Cys Arg
50 55 60
Pro Tyr Phe Thr Ile Leu Gly Leu Pro Ala Met Leu Gln Ala Val Arg
65 70 75 80
Ala Leu Met Ile Val Gly Ile Val Leu Gly Ala Ile Gly Leu Leu Val
85 90 95
Ser Ile Phe Ala Leu Lys Cys Ile Arg Ile Gly Ser Met Glu Asp Ser
100 105 110
Ala Lys Ala Asn Met Thr Leu Thr Ser Gly Ile Met Phe Ile Val Ser
115 120 125
Gly Leu Cys Ala Ile Ala Gly Val Ser Val Phe Ala Asn Met Leu Val
130 135 140
Thr Asn Phe Trp Met Ser Thr Ala Asn Met Tyr Thr Gly Met Gly Gly
145 150 155 160
Met Val Gln Thr Val Gln Thr Arg Tyr Thr Phe Gly Ala Ala Leu Phe
165 170 175
Val Gly Trp Val Ala Gly Gly Leu Thr Leu Ile Gly Gly Val Met Met
180 185 190
Cys Ile Ala Cys Arg Gly Leu Ala Pro Glu Glu Thr Asn Tyr Lys Ala
195 200 205
Val Ser Tyr His Ala Ser Gly His Ser Val Ala Tyr Lys Pro Gly Gly
210 215 220
Phe Lys Ala Ser Thr Gly Phe Gly Ser Asn Thr Lys Asn Lys Lys Ile
225 230 235 240
Tyr Asp Gly Gly Ala Arg Thr Glu Asp Glu Val Gln Ser Tyr Pro Ser
245 250 255
Lys His Asp Tyr Val
260
<210> 32
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (1)..(1)
<223> Xaa может представлять собой Asn, Tyr или His
<220>
<221> прочий_признак
<222> (7)..(7)
<223> Xaa может представлять собой Gly или Val.
<220>
<221> прочий_признак
<222> (8)..(8)
<223> Xaa может представлять собой Ala, Gly или Thr.
<220>
<221> прочий_признак
<222> (10)..(10)
<223> Xaa может представлять собой Arg, Thr или Ser.
<220>
<221> прочий_признак
<222> (16)..(16)
<223> Xaa может представлять собой Lys или Arg.
<400> 32
Xaa Ile Asp Pro Tyr Tyr Xaa Xaa Thr Xaa Tyr Asn Gln Lys Phe Xaa
1 5 10 15
Gly
<210> 33
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (1)..(1)
<223> Xaa может представлять собой Ser или Met.
<220>
<221> прочий_признак
<222> (2)..(2)
<223> Xaa может представлять собой Tyr или Phe.
<220>
<221> прочий_признак
<222> (3)..(3)
<223> Xaa может представлять собой Tyr или His.
<400> 33
Xaa Xaa Xaa Gly Asn Ala Phe Asp Tyr
1 5
<210> 34
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (5)..(5)
<223> Xaa может представлять собой Ser или Asn.
<220>
<221> прочий_признак
<222> (7)..(7)
<223> Xaa может представлять собой Leu или Phe.
<220>
<221> прочий_признак
<222> (9)..(9)
<223> Xaa может представлять собой Ser или Asn.
<220>
<221> прочий_признак
<222> (12)..(12)
<223> Xaa может представлять собой Gln или Leu.
<400> 34
Lys Ser Ser Gln Xaa Leu Xaa Asn Xaa Gly Asn Xaa Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 35
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (6)..(6)
<223> Xaa может представлять собой Glu или Lys.
<400> 35
Trp Ala Ser Thr Arg Xaa Ser
1 5
<210> 36
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (5)..(5)
<223> Xaa может представлять собой Ser или Tyr.
<220>
<221> прочий_признак
<222> (6)..(6)
<223> Xaa может представлять собой Phe или Tyr.
<220>
<221> прочий_признак
<222> (8)..(8)
<223> Xaa может представлять собой Phe или Leu.
<400> 36
Gln Asn Asp Tyr Xaa Xaa Pro Xaa Thr
1 5
<210> 37
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 37
Glu Phe Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Ile Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Lys Gln Ser Asn Gly Glu Ser Leu Glu Trp Ile
35 40 45
Gly Asn Ile Asp Pro Tyr Tyr Gly Ala Thr Arg Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Lys Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Tyr Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 38
<211> 113
<212> БЕЛОК
<213> Mus musculus
<400> 38
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 39
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 39
Glu Phe Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Ile Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Lys Gln Ser Asn Gly Glu Ser Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Tyr Gly Gly Thr Arg Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Lys Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Tyr Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 40
<211> 113
<212> БЕЛОК
<213> Mus musculus
<400> 40
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 41
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 41
Glu Phe Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Lys Gln Ser Asn Gly Gln Ser Leu Glu Trp Ile
35 40 45
Gly His Ile Asp Pro Tyr Tyr Val Thr Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Lys Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Tyr Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 42
<211> 113
<212> БЕЛОК
<213> Mus musculus
<400> 42
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Phe Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 43
<211> 119
<212> БЕЛОК
<213> Mus musculus
<400> 43
Gln Ile Thr Gln Lys Glu Ser Gly Pro Gly Ile Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Leu Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Phe Ile Gly Val Gly Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Ala His Ile Trp Trp Asn Asp Asn Lys Tyr Tyr Asn Thr Ala
50 55 60
Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Asn Asn Gln Val
65 70 75 80
Phe Leu Lys Ile Ala Ser Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Met Gly Ser Gly Ala Trp Phe Thr Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ala
115
<210> 44
<211> 113
<212> БЕЛОК
<213> Mus musculus
<400> 44
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Tyr Tyr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 45
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 45
Glu Phe Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Ile Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Lys Gln Ser Asn Gly Glu Ser Leu Glu Trp Ile
35 40 45
Gly Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Lys Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Met Tyr His Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 46
<211> 113
<212> БЕЛОК
<213> Mus musculus
<400> 46
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Leu Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Leu Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu
100 105 110
Lys
<210> 47
<211> 118
<212> БЕЛОК
<213> Mus musculus
<400> 47
Glu Phe Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Ile Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Asn Met Asn Trp Val Lys Gln Ser Asn Gly Glu Ser Leu Glu Trp Ile
35 40 45
Gly Asn Ile Asp Pro Tyr Tyr Gly Gly Thr Arg Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Lys Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Tyr Gly Asn Ala Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 48
<211> 113
<212> БЕЛОК
<213> Mus musculus
<400> 48
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Asn Leu Leu Asn Asn
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Phe Pro Phe Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu
100 105 110
Lys
<210> 49
<211> 330
<212> БЕЛОК
<213> Homo sapiens
<400> 49
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 50
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 50
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 51
<211> 330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<400> 51
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Val Gly Gly Pro Ser Val Phe Leu Leu Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Pro Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Leu Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Leu Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 52
<211> 486
<212> БЕЛОК
<213> Homo sapiens
<400> 52
Met Ser Thr Thr Thr Cys Gln Val Val Ala Phe Leu Leu Ser Ile Leu
1 5 10 15
Gly Leu Ala Gly Cys Ile Ala Ala Thr Gly Met Asp Met Trp Ser Thr
20 25 30
Gln Asp Leu Tyr Asp Asn Pro Val Thr Ser Val Phe Gln Tyr Glu Gly
35 40 45
Leu Trp Arg Ser Cys Val Arg Gln Ser Ser Gly Phe Thr Glu Cys Arg
50 55 60
Pro Tyr Phe Thr Ile Leu Gly Leu Pro Ala Met Leu Gln Ala Val Arg
65 70 75 80
Ala Leu Met Ile Val Gly Ile Val Leu Gly Ala Ile Gly Leu Leu Val
85 90 95
Ser Ile Phe Ala Leu Lys Cys Ile Arg Ile Gly Ser Met Glu Asp Ser
100 105 110
Ala Lys Ala Asn Met Thr Leu Thr Ser Gly Ile Met Phe Ile Val Ser
115 120 125
Gly Leu Cys Ala Ile Ala Gly Val Ser Val Phe Ala Asn Met Leu Val
130 135 140
Thr Asn Phe Trp Met Ser Thr Ala Asn Met Tyr Thr Gly Met Gly Gly
145 150 155 160
Met Val Gln Thr Val Gln Thr Arg Tyr Thr Phe Gly Ala Ala Leu Phe
165 170 175
Val Gly Trp Val Ala Gly Gly Leu Thr Leu Ile Gly Gly Val Met Met
180 185 190
Cys Ile Ala Cys Arg Gly Leu Ala Pro Glu Glu Thr Asn Tyr Lys Ala
195 200 205
Val Ser Tyr His Ala Ser Gly His Ser Val Ala Tyr Lys Pro Gly Gly
210 215 220
Phe Lys Ala Ser Thr Gly Phe Gly Ser Asn Thr Lys Asn Lys Lys Ile
225 230 235 240
Tyr Asp Gly Gly Ala Arg Thr Glu Asp Glu Val Gln Ser Tyr Pro Ser
245 250 255
Lys His Asp Tyr Val Met Ala Ser Ser Glu Asp Val Ile Lys Glu Phe
260 265 270
Met Arg Phe Lys Val Arg Met Glu Gly Ser Val Asn Gly His Glu Phe
275 280 285
Glu Ile Glu Gly Glu Gly Glu Gly Arg Pro Tyr Glu Gly Thr Gln Thr
290 295 300
Ala Lys Leu Lys Val Thr Lys Gly Gly Pro Leu Pro Phe Ala Trp Asp
305 310 315 320
Ile Leu Ser Pro Gln Phe Gln Tyr Gly Ser Lys Ala Tyr Val Lys His
325 330 335
Pro Ala Asp Ile Pro Asp Tyr Leu Lys Leu Ser Phe Pro Glu Gly Phe
340 345 350
Lys Trp Glu Arg Val Met Asn Phe Glu Asp Gly Gly Val Val Thr Val
355 360 365
Thr Gln Asp Ser Ser Leu Gln Asp Gly Glu Phe Ile Tyr Lys Val Lys
370 375 380
Leu Arg Gly Thr Asn Phe Pro Ser Asp Gly Pro Val Met Gln Lys Lys
385 390 395 400
Thr Met Gly Trp Glu Ala Ser Thr Glu Arg Met Tyr Pro Glu Asp Gly
405 410 415
Ala Leu Lys Gly Glu Ile Lys Met Arg Leu Lys Leu Lys Asp Gly Gly
420 425 430
His Tyr Asp Ala Glu Val Lys Thr Thr Tyr Met Ala Lys Lys Pro Val
435 440 445
Gln Leu Pro Gly Ala Tyr Lys Thr Asp Ile Lys Leu Asp Ile Thr Ser
450 455 460
His Asn Glu Asp Tyr Thr Ile Val Glu Gln Tyr Glu Arg Ala Glu Gly
465 470 475 480
Arg His Ser Thr Gly Ala
485
<210> 53
<211> 486
<212> БЕЛОК
<213> Homo sapiens
<400> 53
Met Ala Val Thr Ala Cys Gln Gly Leu Gly Phe Val Val Ser Leu Ile
1 5 10 15
Gly Ile Ala Gly Ile Ile Ala Ala Thr Cys Met Asp Gln Trp Ser Thr
20 25 30
Gln Asp Leu Tyr Asn Asn Pro Val Thr Ala Val Phe Asn Tyr Gln Gly
35 40 45
Leu Trp Arg Ser Cys Val Arg Glu Ser Ser Gly Phe Thr Glu Cys Arg
50 55 60
Gly Tyr Phe Thr Leu Leu Gly Leu Pro Ala Met Leu Gln Ala Val Arg
65 70 75 80
Ala Leu Met Ile Val Gly Ile Val Leu Gly Ala Ile Gly Leu Leu Val
85 90 95
Ser Ile Phe Ala Leu Lys Cys Ile Arg Ile Gly Ser Met Glu Asp Ser
100 105 110
Ala Lys Ala Asn Met Thr Leu Thr Ser Gly Ile Met Phe Ile Val Ser
115 120 125
Gly Leu Cys Ala Ile Ala Gly Val Ser Val Phe Ala Asn Met Leu Val
130 135 140
Thr Asn Phe Trp Met Ser Thr Ala Asn Met Tyr Thr Gly Met Gly Gly
145 150 155 160
Met Val Gln Thr Val Gln Thr Arg Tyr Thr Phe Gly Ala Ala Leu Phe
165 170 175
Val Gly Trp Val Ala Gly Gly Leu Thr Leu Ile Gly Gly Val Met Met
180 185 190
Cys Ile Ala Cys Arg Gly Leu Ala Pro Glu Glu Thr Asn Tyr Lys Ala
195 200 205
Val Ser Tyr His Ala Ser Gly His Ser Val Ala Tyr Lys Pro Gly Gly
210 215 220
Phe Lys Ala Ser Thr Gly Phe Gly Ser Asn Thr Lys Asn Lys Lys Ile
225 230 235 240
Tyr Asp Gly Gly Ala Arg Thr Glu Asp Glu Val Gln Ser Tyr Pro Ser
245 250 255
Lys His Asp Tyr Val Met Ala Ser Ser Glu Asp Val Ile Lys Glu Phe
260 265 270
Met Arg Phe Lys Val Arg Met Glu Gly Ser Val Asn Gly His Glu Phe
275 280 285
Glu Ile Glu Gly Glu Gly Glu Gly Arg Pro Tyr Glu Gly Thr Gln Thr
290 295 300
Ala Lys Leu Lys Val Thr Lys Gly Gly Pro Leu Pro Phe Ala Trp Asp
305 310 315 320
Ile Leu Ser Pro Gln Phe Gln Tyr Gly Ser Lys Ala Tyr Val Lys His
325 330 335
Pro Ala Asp Ile Pro Asp Tyr Leu Lys Leu Ser Phe Pro Glu Gly Phe
340 345 350
Lys Trp Glu Arg Val Met Asn Phe Glu Asp Gly Gly Val Val Thr Val
355 360 365
Thr Gln Asp Ser Ser Leu Gln Asp Gly Glu Phe Ile Tyr Lys Val Lys
370 375 380
Leu Arg Gly Thr Asn Phe Pro Ser Asp Gly Pro Val Met Gln Lys Lys
385 390 395 400
Thr Met Gly Trp Glu Ala Ser Thr Glu Arg Met Tyr Pro Glu Asp Gly
405 410 415
Ala Leu Lys Gly Glu Ile Lys Met Arg Leu Lys Leu Lys Asp Gly Gly
420 425 430
His Tyr Asp Ala Glu Val Lys Thr Thr Tyr Met Ala Lys Lys Pro Val
435 440 445
Gln Leu Pro Gly Ala Tyr Lys Thr Asp Ile Lys Leu Asp Ile Thr Ser
450 455 460
His Asn Glu Asp Tyr Thr Ile Val Glu Gln Tyr Glu Arg Ala Glu Gly
465 470 475 480
Arg His Ser Thr Gly Ala
485
<210> 54
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (28)..(28)
<223> Xaa может представлять собой Thr или Ser.
<400> 54
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Xaa Phe Thr
20 25 30
<210> 55
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (3)..(3)
<223> Xaa может представлять собой Arg или Lys.
<220>
<221> прочий_признак
<222> (13)..(13)
<223> Xaa может представлять собой Met или IIe.
<400> 55
Trp Val Xaa Gln Ala Pro Gly Gln Gly Leu Glu Trp Xaa Gly
1 5 10
<210> 56
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (4)..(4)
<223> Xaa может представлять собой Met или Leu.
<400> 56
Arg Val Thr Xaa Thr Ile Asp Lys Ser Thr Ser Thr Val Tyr Met Glu
1 5 10 15
Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 57
<211> 11
<212> БЕЛОК
<213> Homo sapiens
<400> 57
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 58
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (21)..(21)
<223> Xaa может представлять собой Ile или Met.
<400> 58
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Xaa Asn Cys
20
<210> 59
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 59
Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr
1 5 10 15
<210> 60
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<220>
<221> прочий_признак
<222> (7)..(7)
<223> Xaa может представлять собой Ser или Thr.
<400> 60
Gly Val Pro Asp Arg Phe Xaa Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys
20 25 30
<210> 61
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 61
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 62
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 62
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
20 25 30
<210> 63
<211> 30
<212> БЕЛОК
<213> Homo sapiens
<400> 63
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr
20 25 30
<210> 64
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 64
Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
1 5 10
<210> 65
<211> 14
<212> БЕЛОК
<213> Homo sapiens
<400> 65
Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly
1 5 10
<210> 66
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 66
Arg Val Thr Met Thr Ile Asp Lys Ser Thr Ser Thr Val Tyr Met Glu
1 5 10 15
Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 67
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 67
Arg Val Thr Leu Thr Ile Asp Lys Ser Thr Ser Thr Val Tyr Met Glu
1 5 10 15
Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 68
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 68
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys
20
<210> 69
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 69
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Met Asn Cys
20
<210> 70
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 70
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys
20 25 30
<210> 71
<211> 32
<212> БЕЛОК
<213> Homo sapiens
<400> 71
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys
20 25 30
<210> 72
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<400> 72
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asn Ile Tyr Pro Ser Asp Ser Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser Trp Arg Gly Asn Ser Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 73
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетическая
<400> 73
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 74
<211> 115
<212> БЕЛОК
<213> Mus musculus
<400> 74
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Phe Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Gly Val Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Arg Thr Gly Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 75
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 75
Asp Ile Val Met Thr Gln Ala Ala Phe Ser Ile Pro Val Thr Leu Gly
1 5 10 15
Thr Ser Ala Ser Ile Ser Cys Arg Ser Ser Lys Asn Leu Leu His Ser
20 25 30
Asp Gly Ile Thr Tyr Leu Tyr Trp Tyr Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Val Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asn Arg Phe Ser Gly Ser Glu Ser Gly Thr Asp Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Val
85 90 95
Leu Glu Leu Pro Phe Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ ЛЕКАРСТВЕННЫХ СРЕДСТВ, СОДЕРЖАЩИЕ АНТИТЕЛА ПРОТИВ КЛАУДИНА 18.2 | 2016 |
|
RU2841168C2 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18A2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2811431C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ ПРОТИВ КЛАУДИНА 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2014 |
|
RU2792932C2 |
| ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ РАКА, ВКЛЮЧАЮЩАЯ АНТИТЕЛА ПРОТИВ КЛАУДИНА 18.2 | 2014 |
|
RU2832015C2 |
| АНТИТЕЛА ПРОТИВ КЛАУДИНА И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2815926C2 |
| АНТИ-CLDN АНТИТЕЛО, ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕГО ОБНАРУЖЕНИЯ | 2020 |
|
RU2801315C2 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18.2 И ЕГО КОНЪЮГАТ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2022 |
|
RU2814164C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПРОГНОЗИРОВАНИЯ ТЕРАПЕВТИЧЕСКОЙ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И ПРОГНОЗА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2016 |
|
RU2785291C2 |
| ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ROR2 | 2018 |
|
RU2784586C2 |
| АНТИТЕЛА К ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРАМ, ПОЛУЧЕННЫМ ИЗ 4G7 | 2020 |
|
RU2826051C2 |
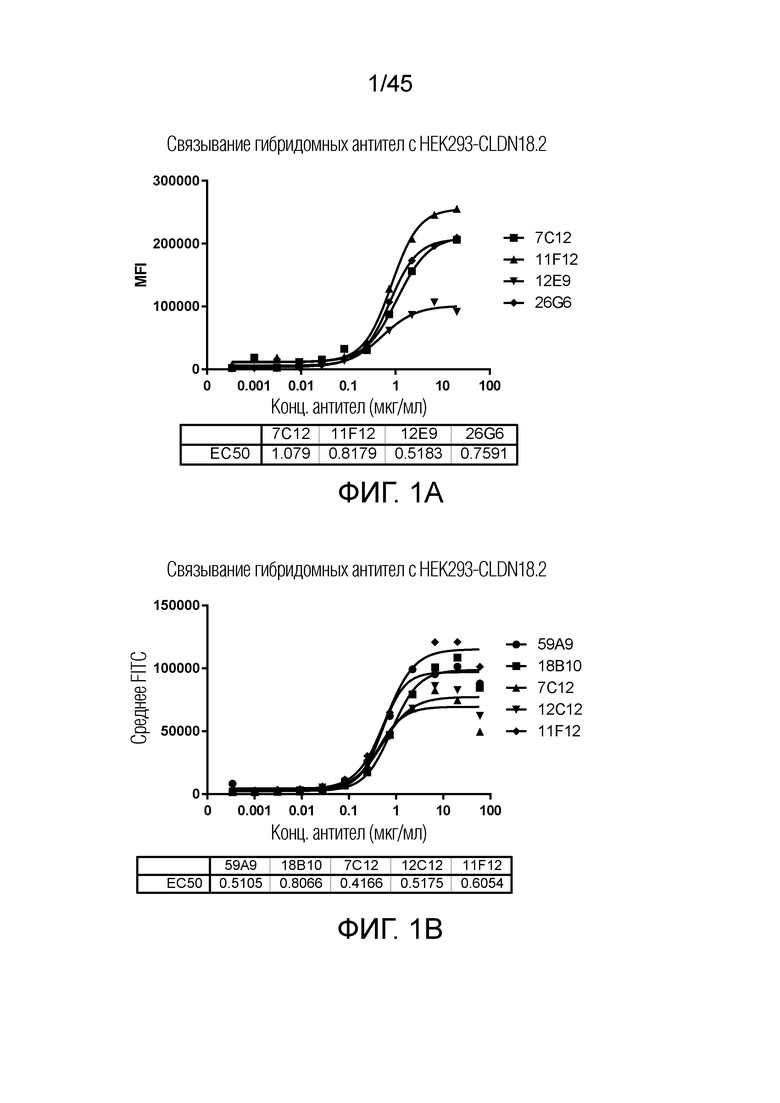
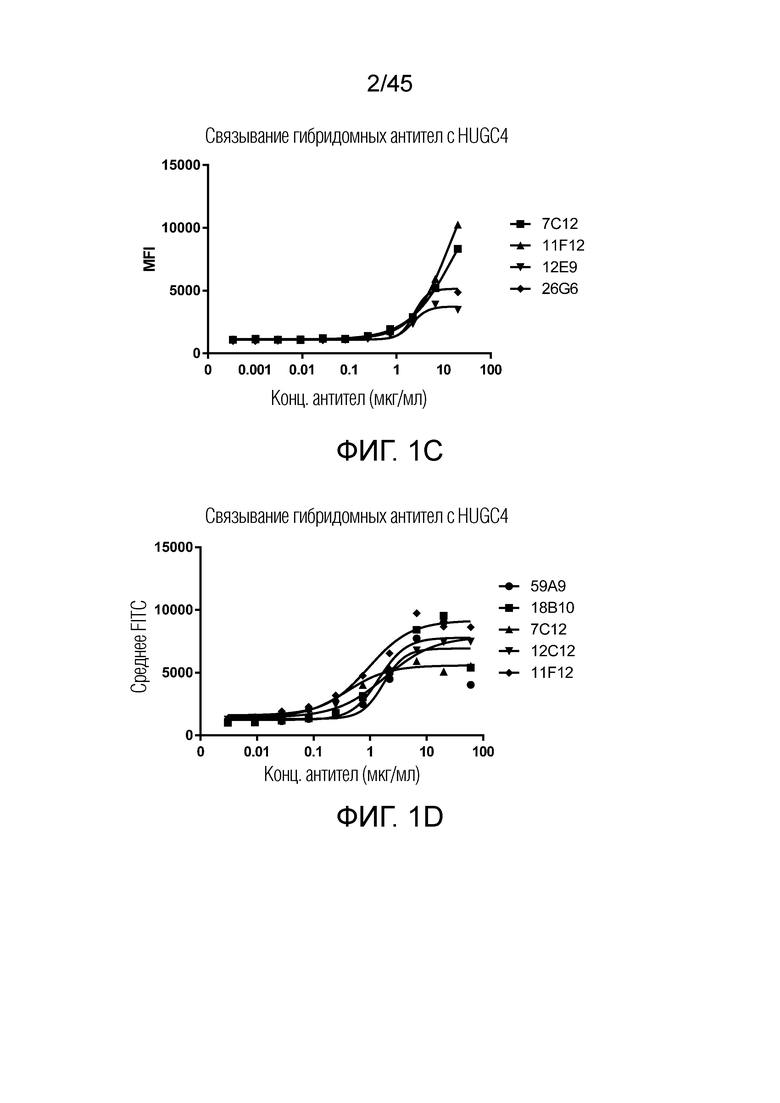
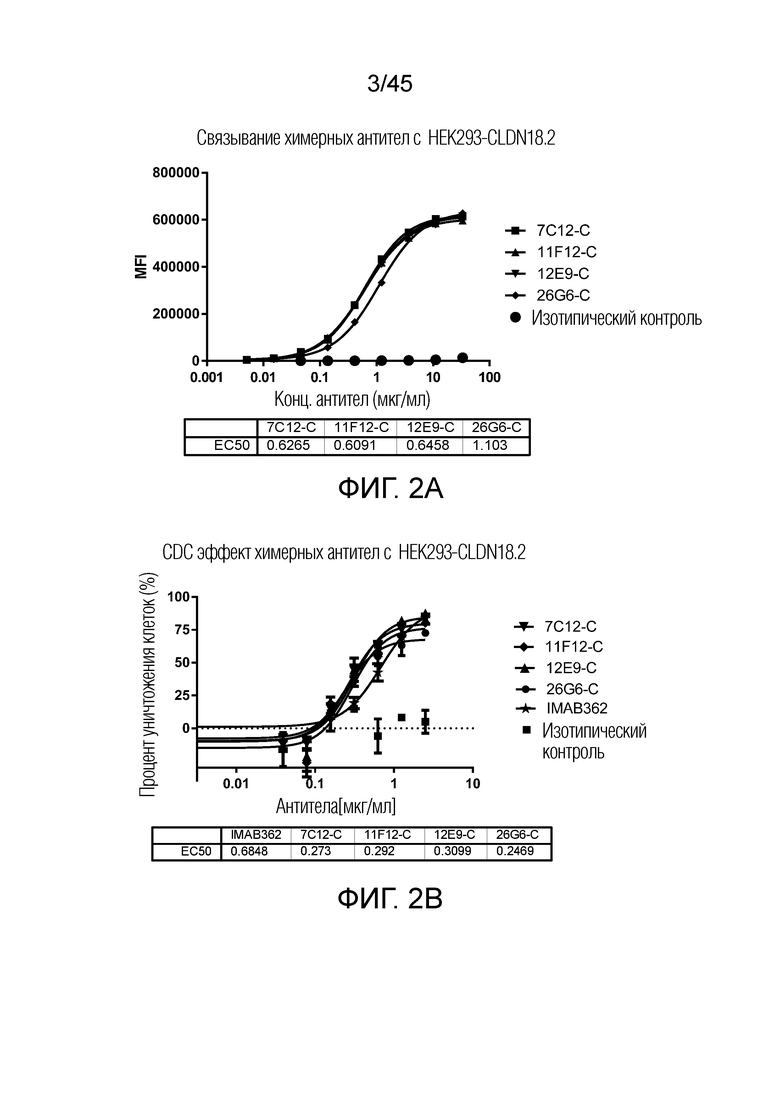
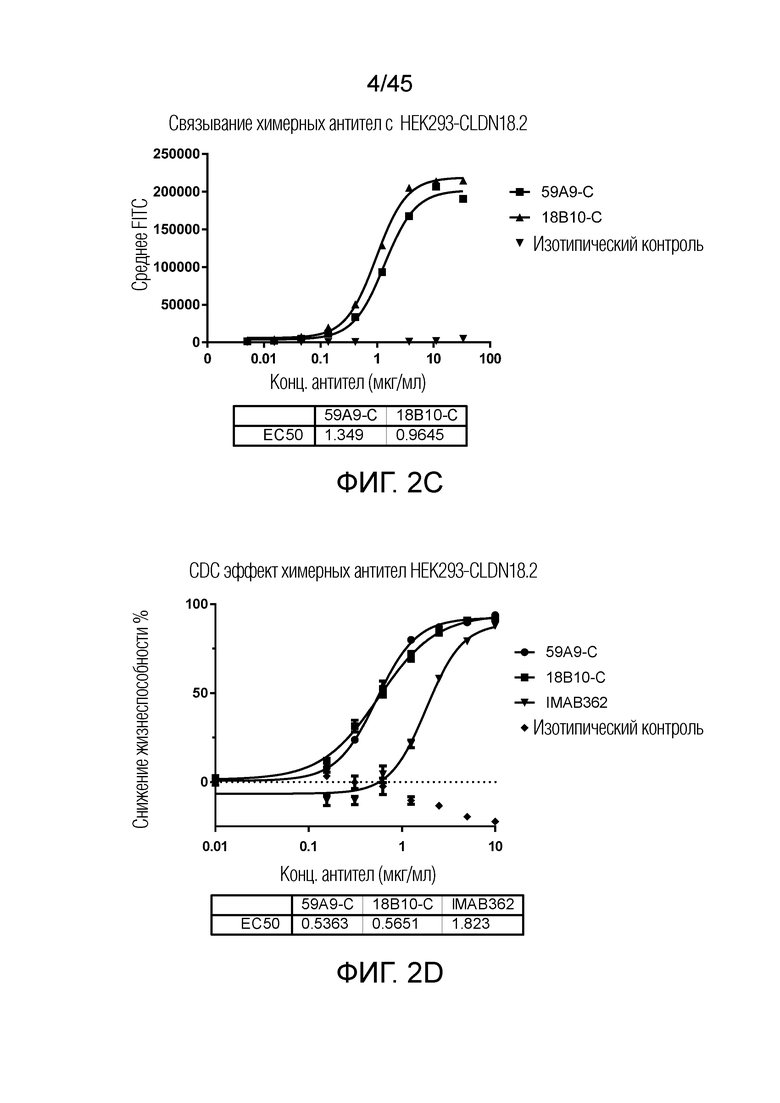
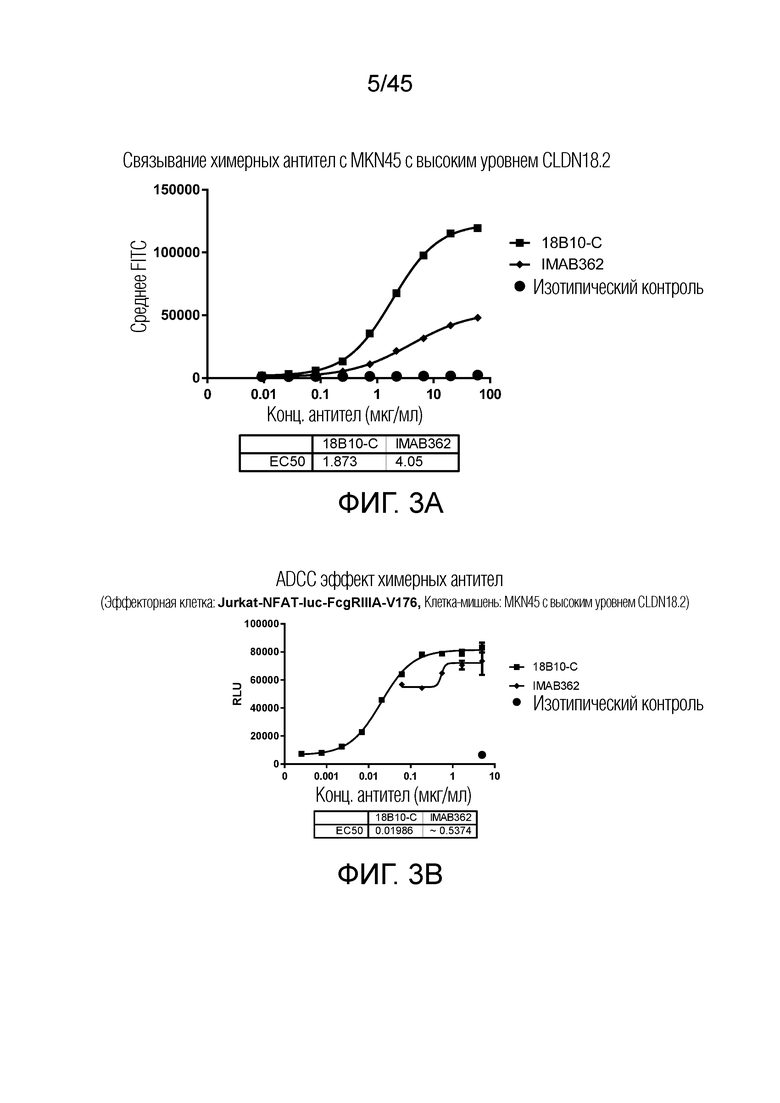
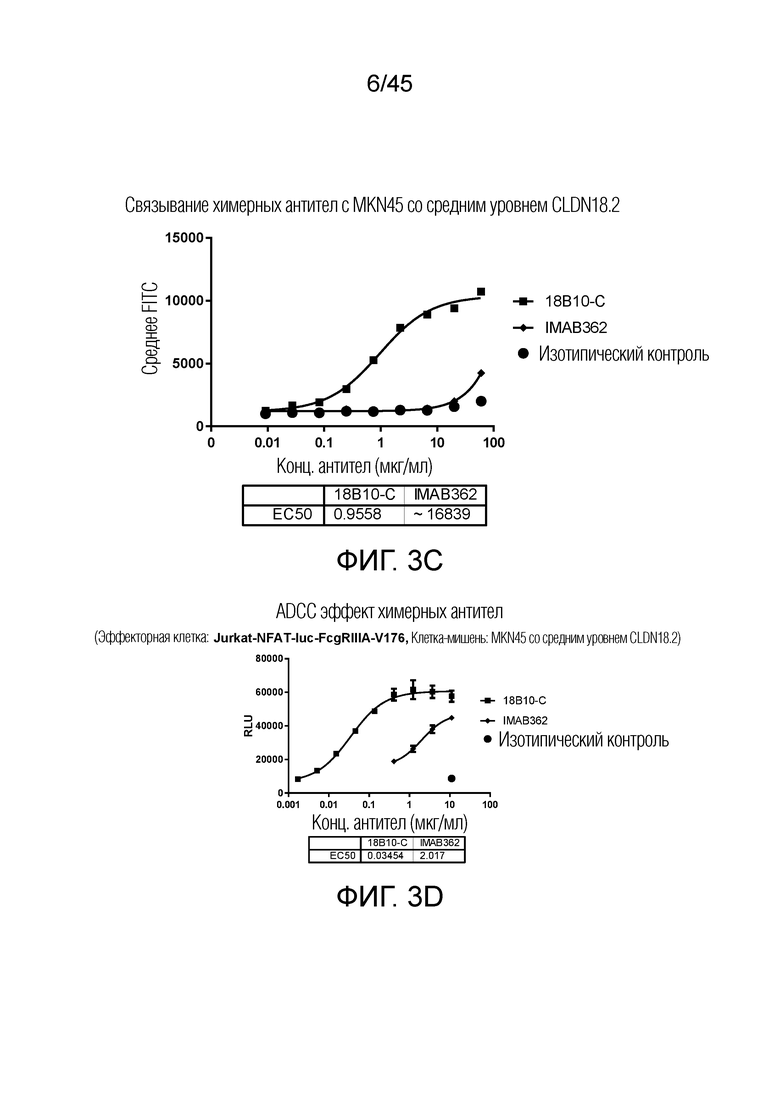
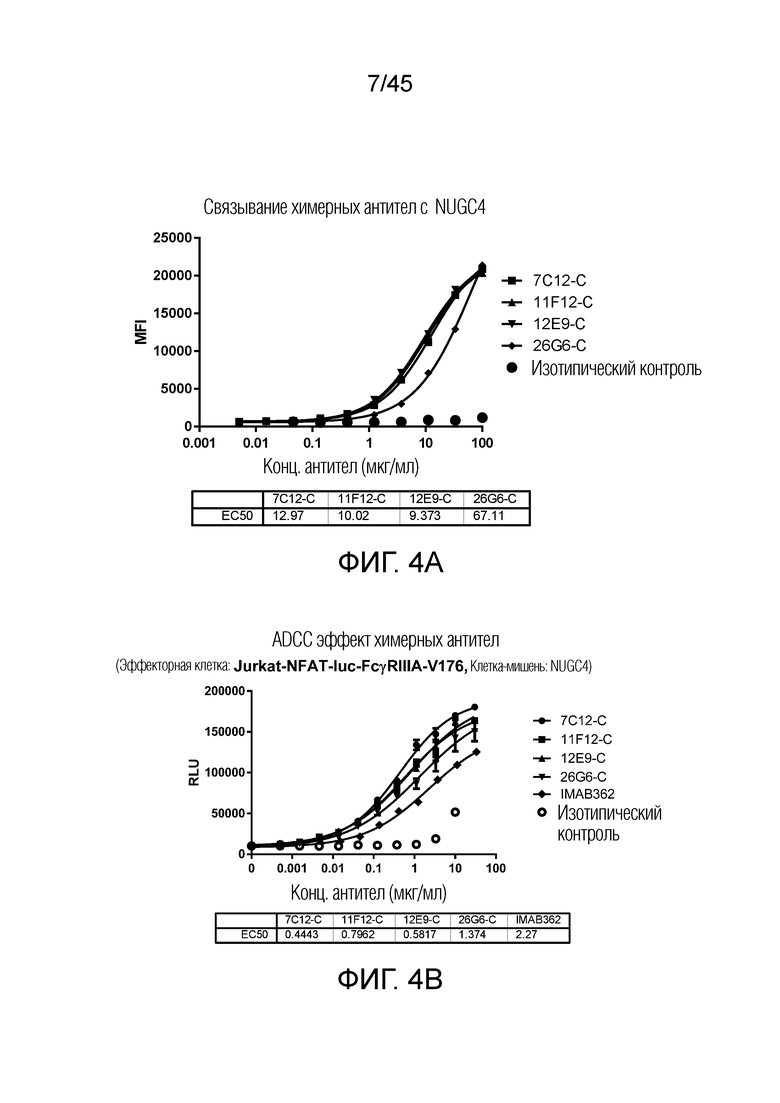
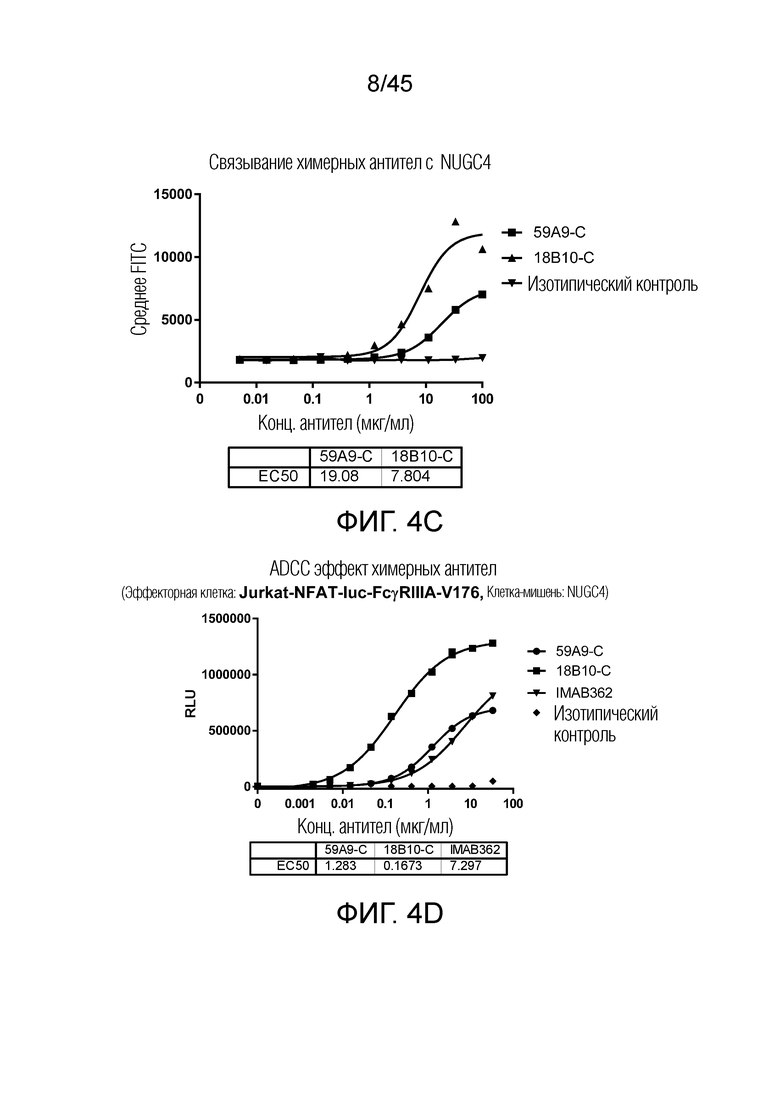
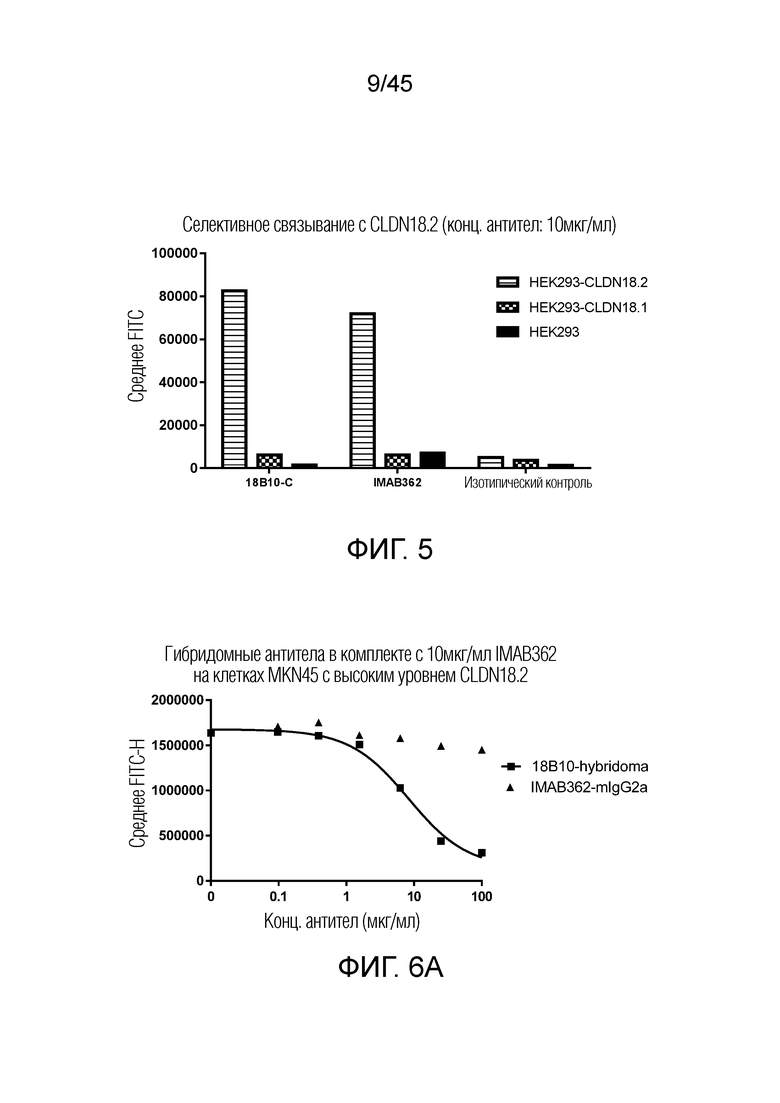
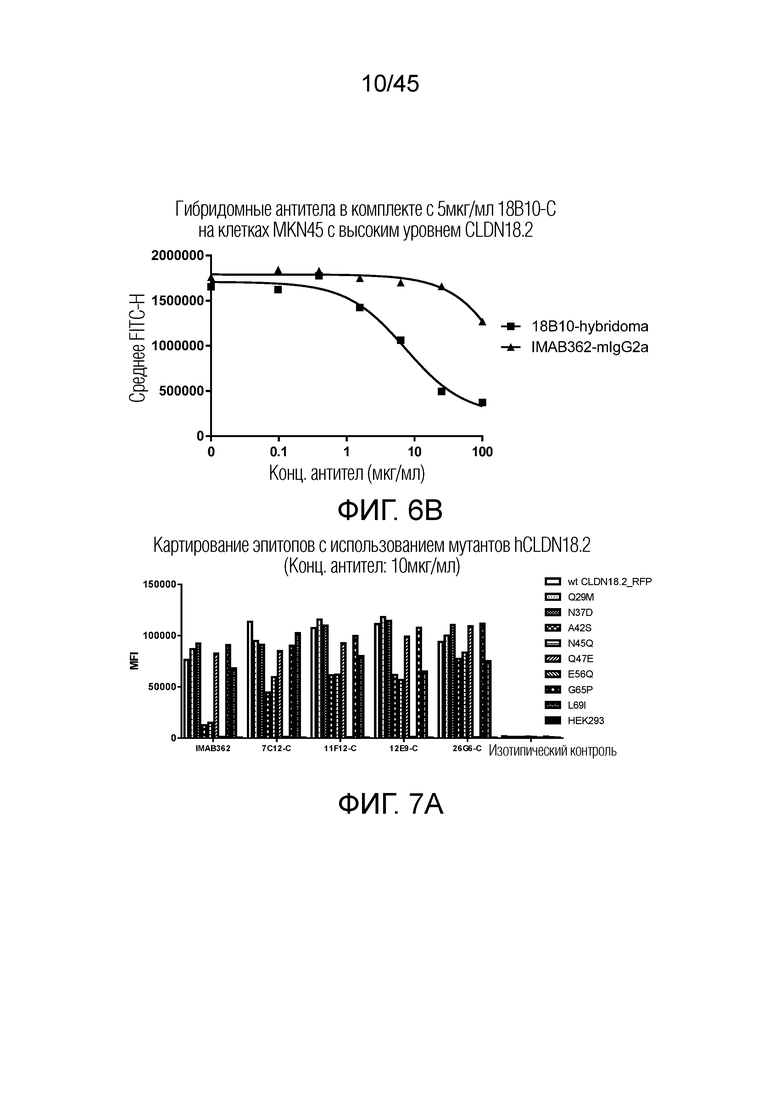
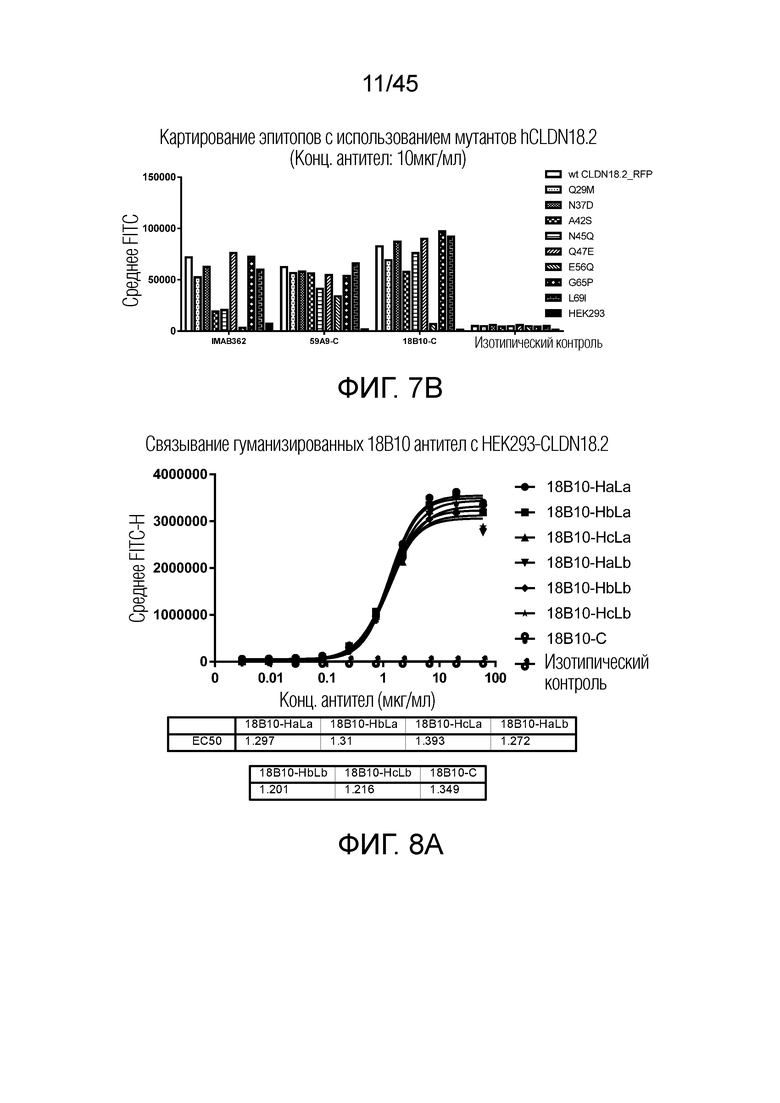
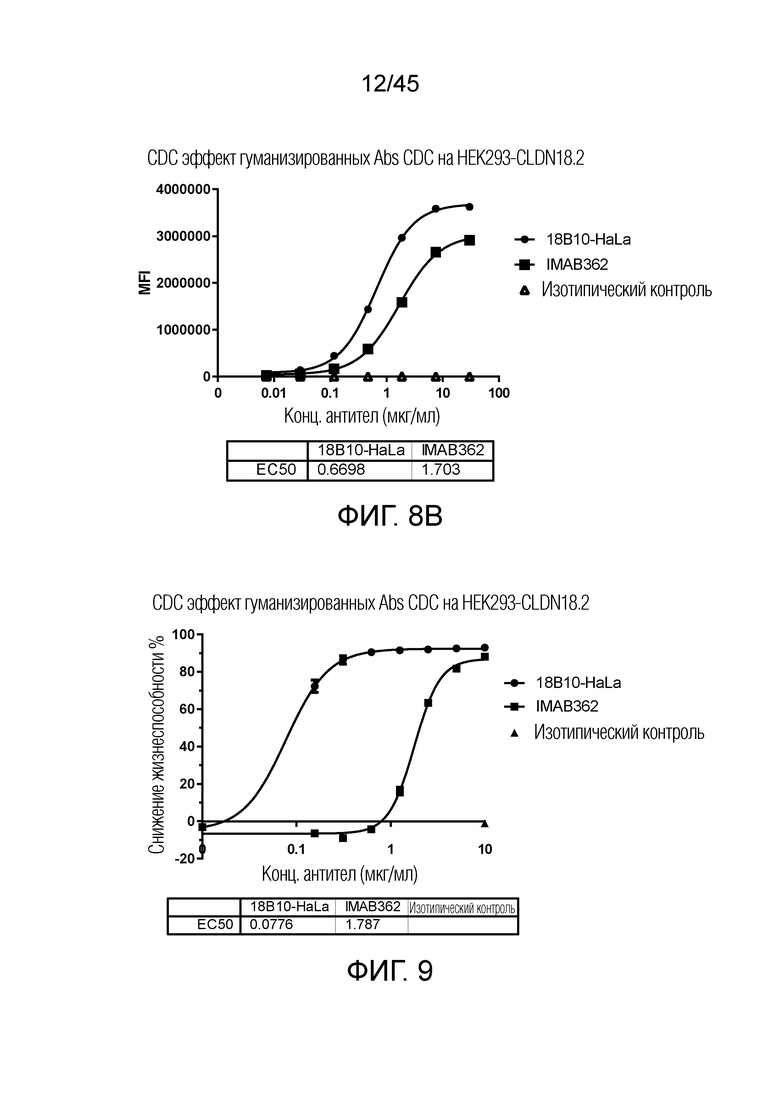
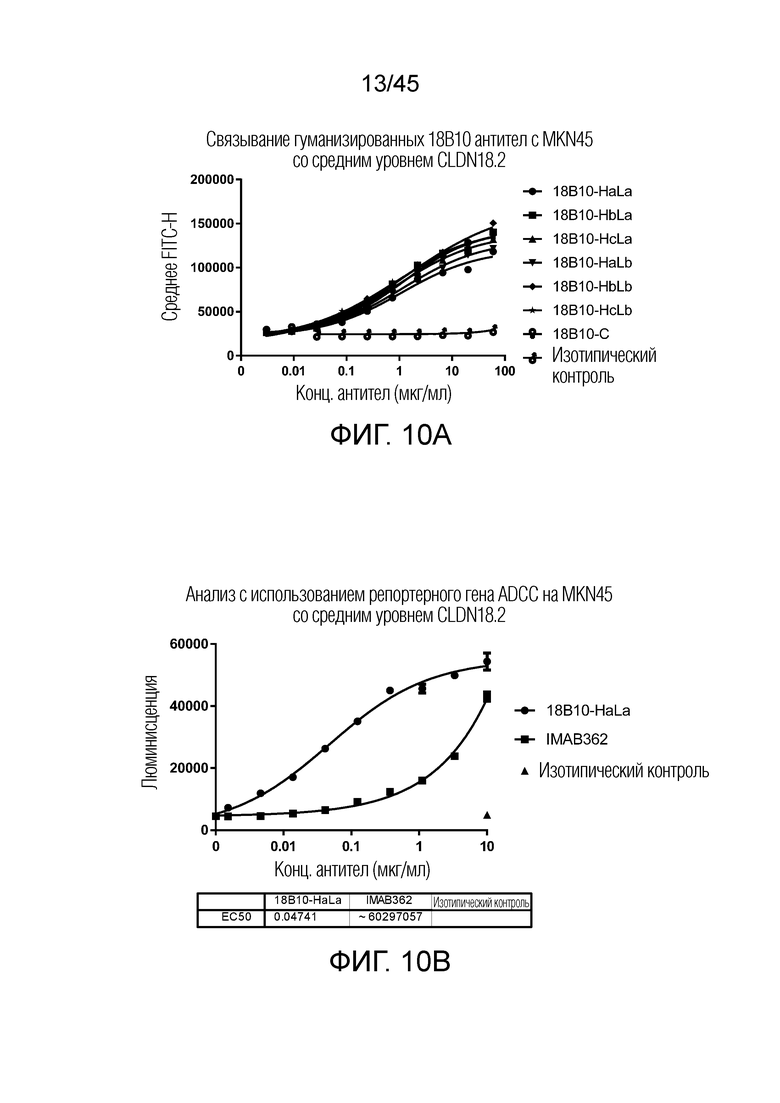
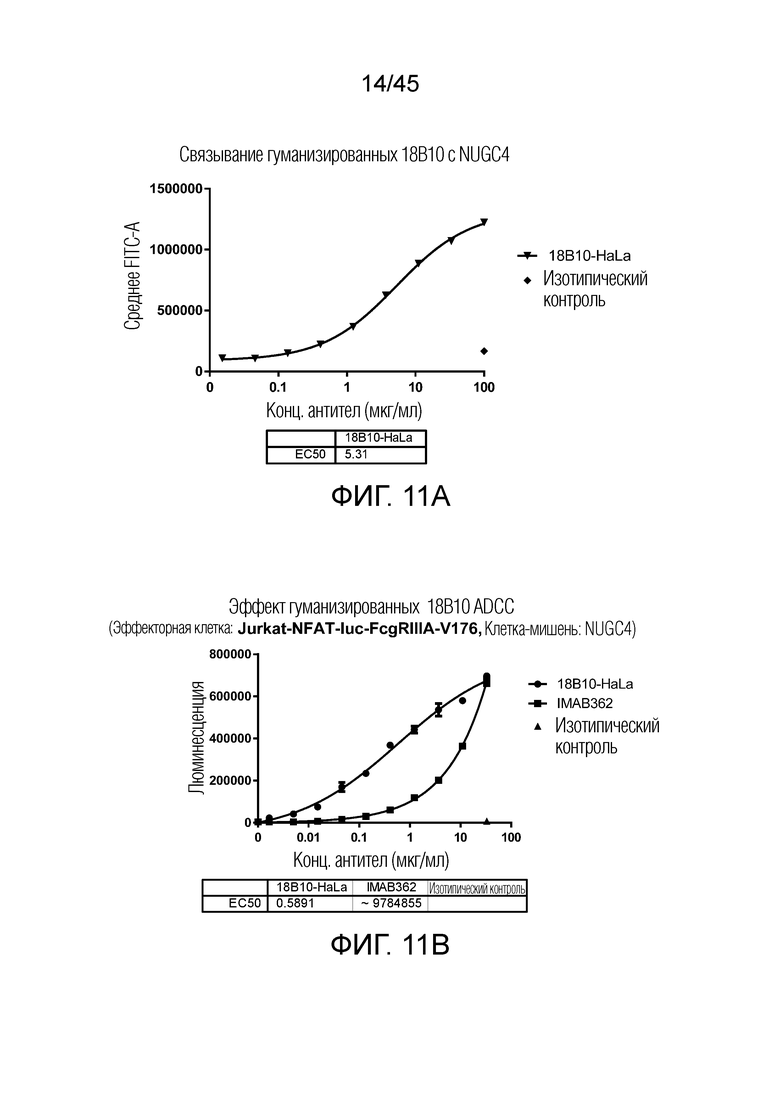
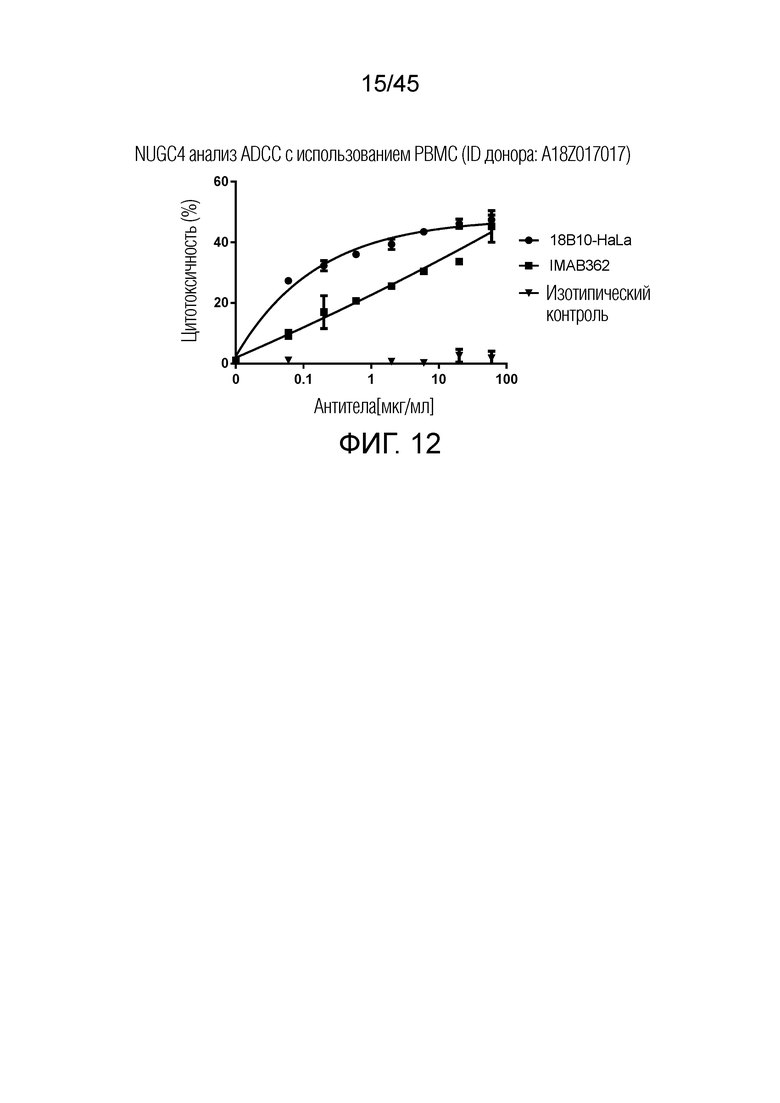
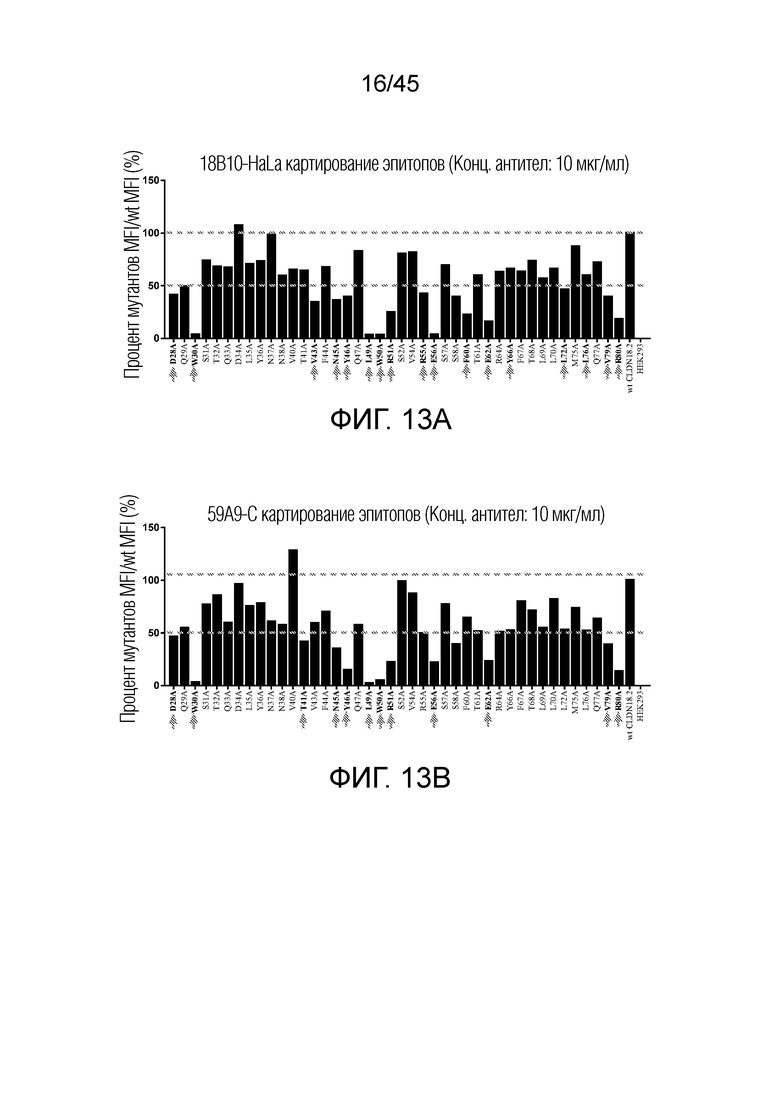
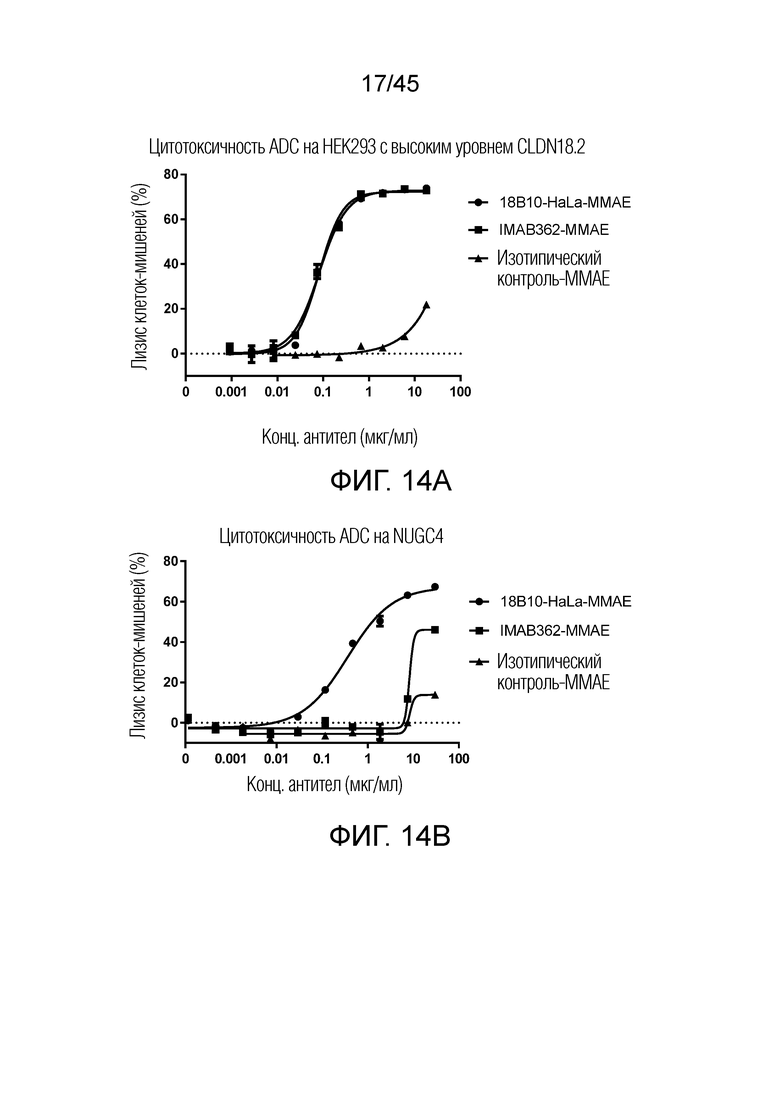
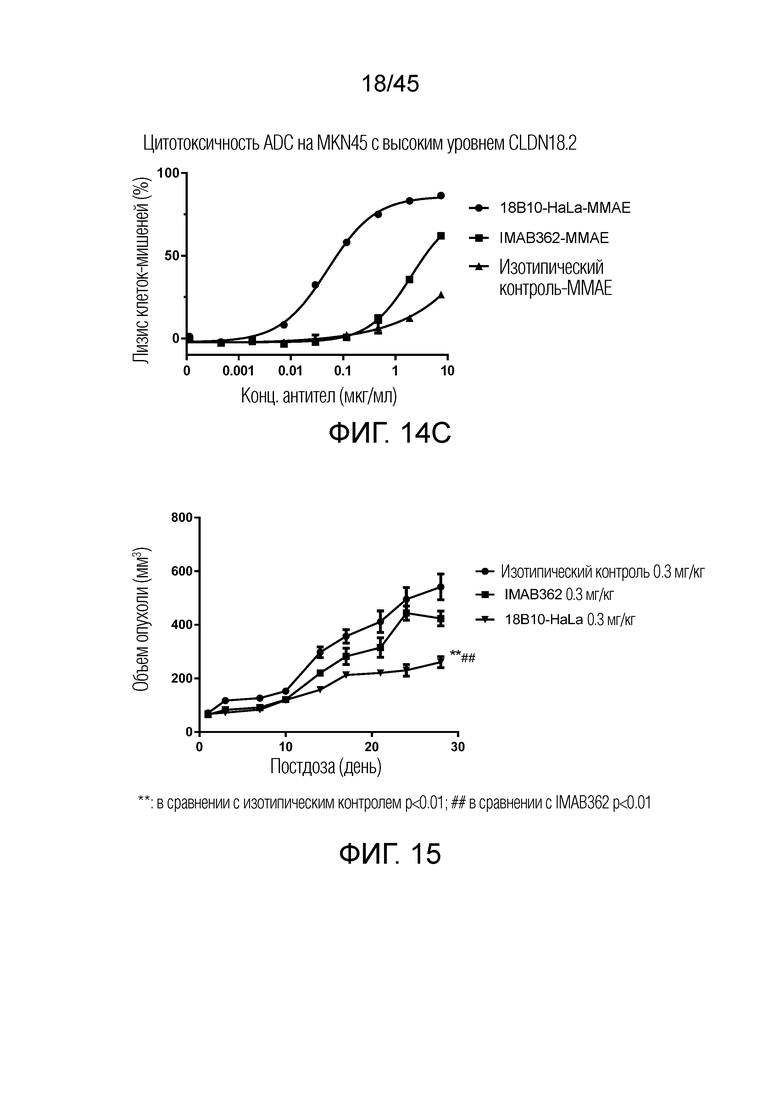
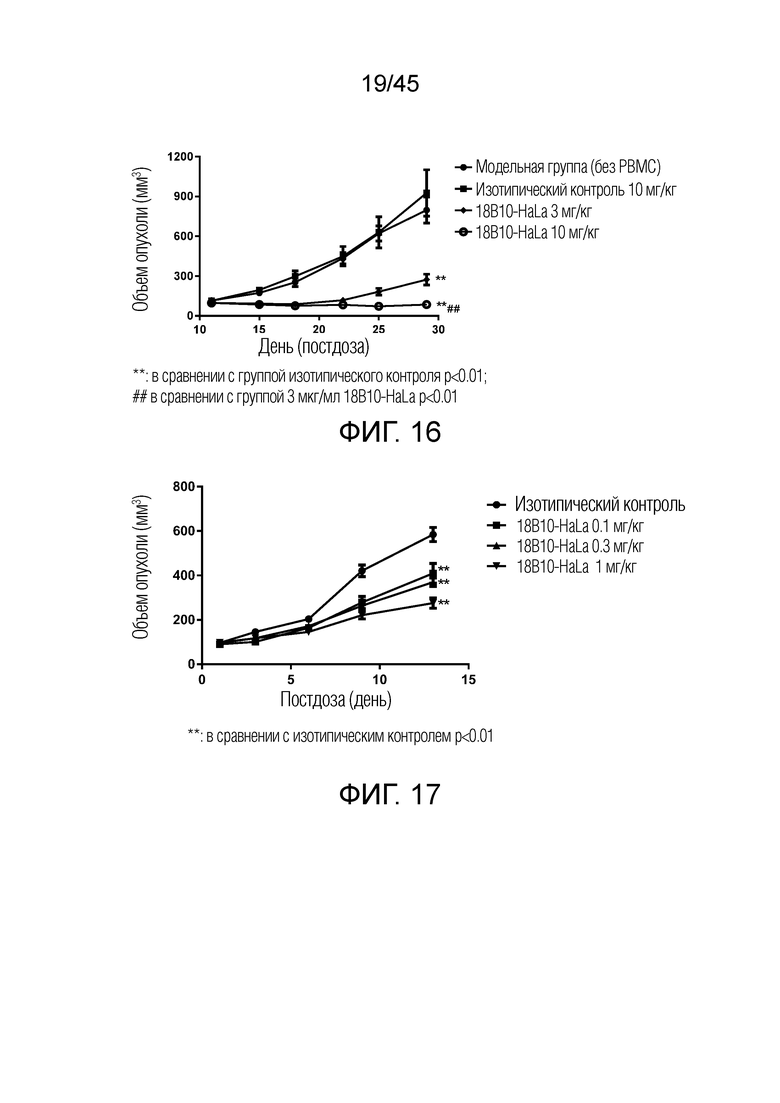
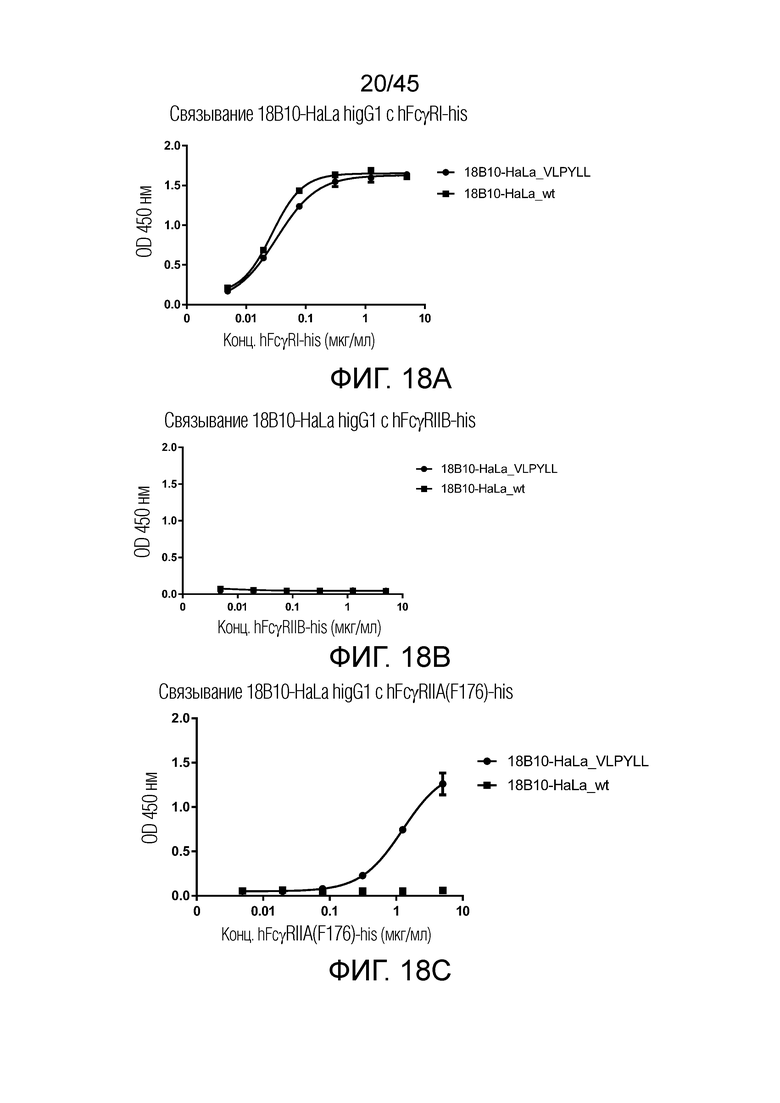
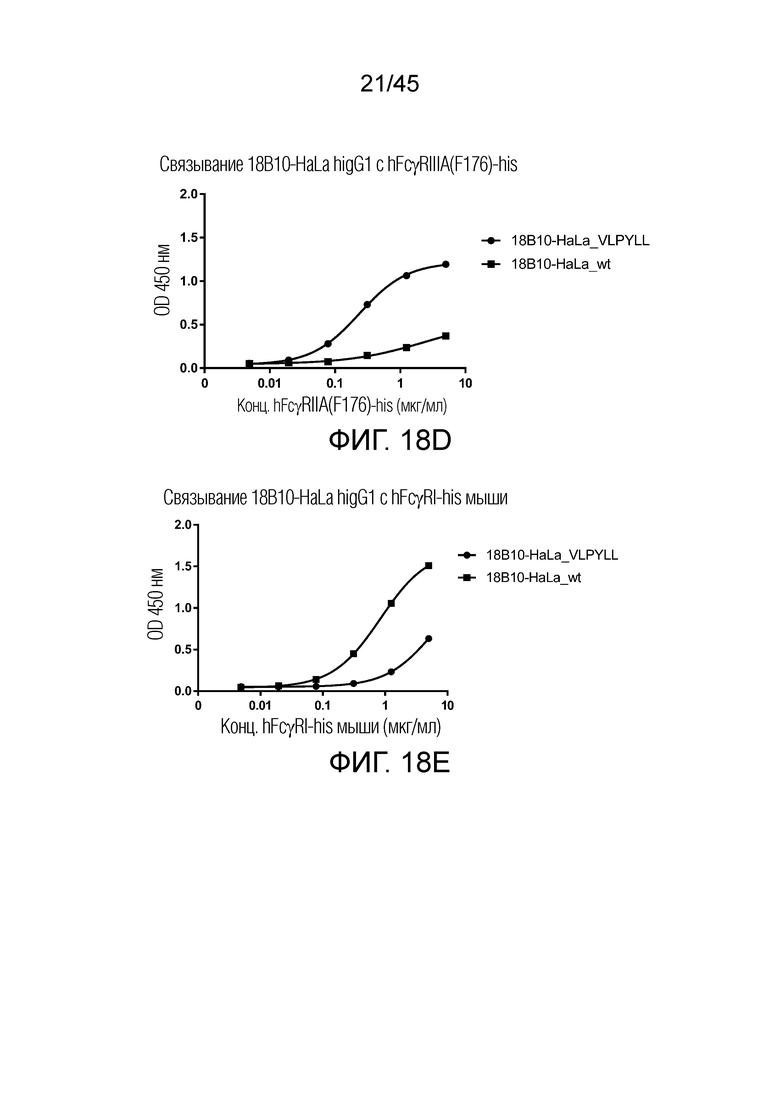
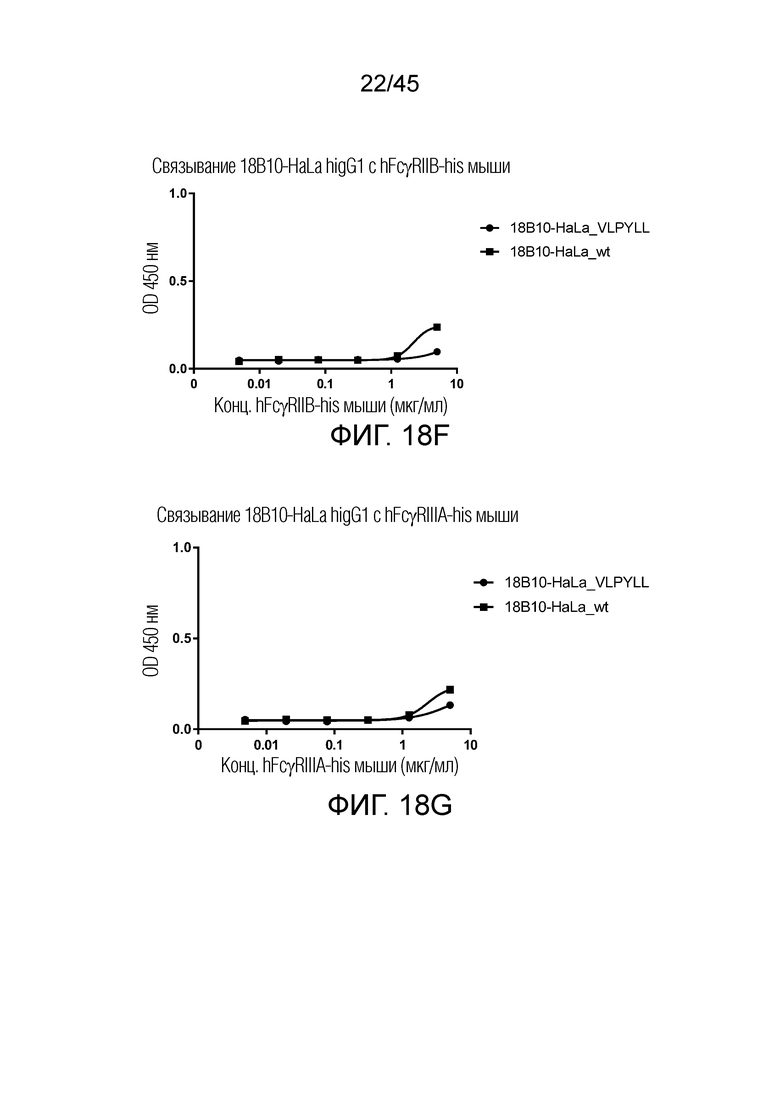
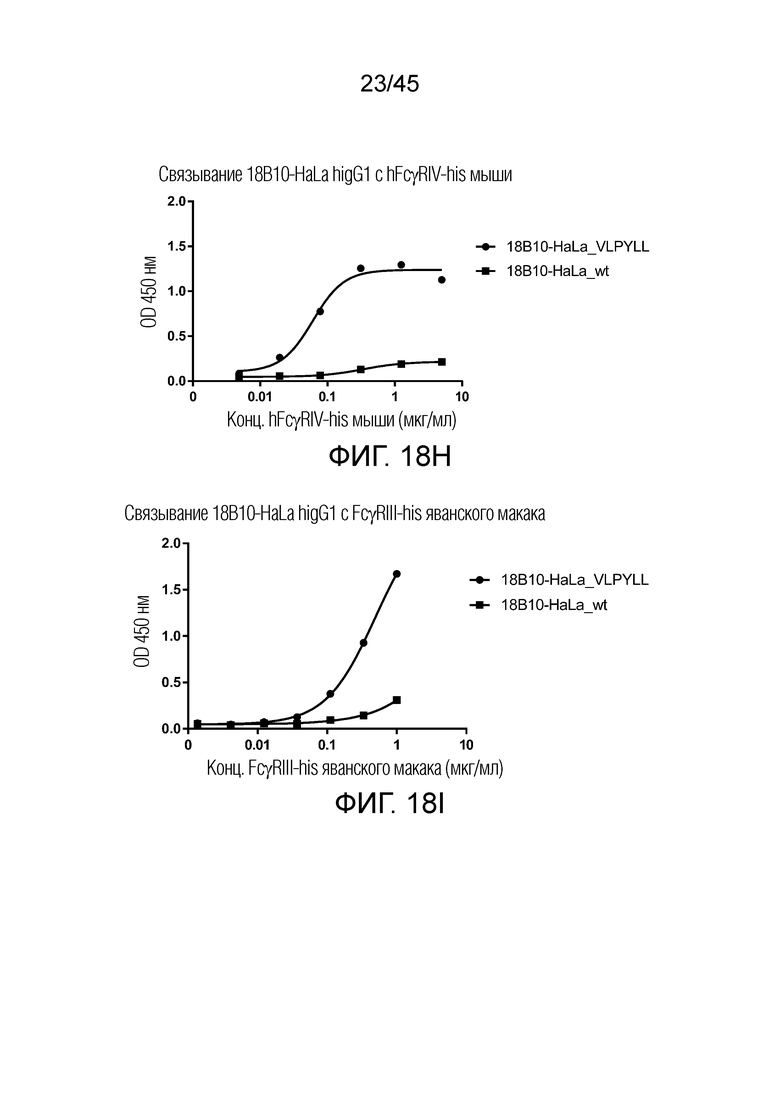
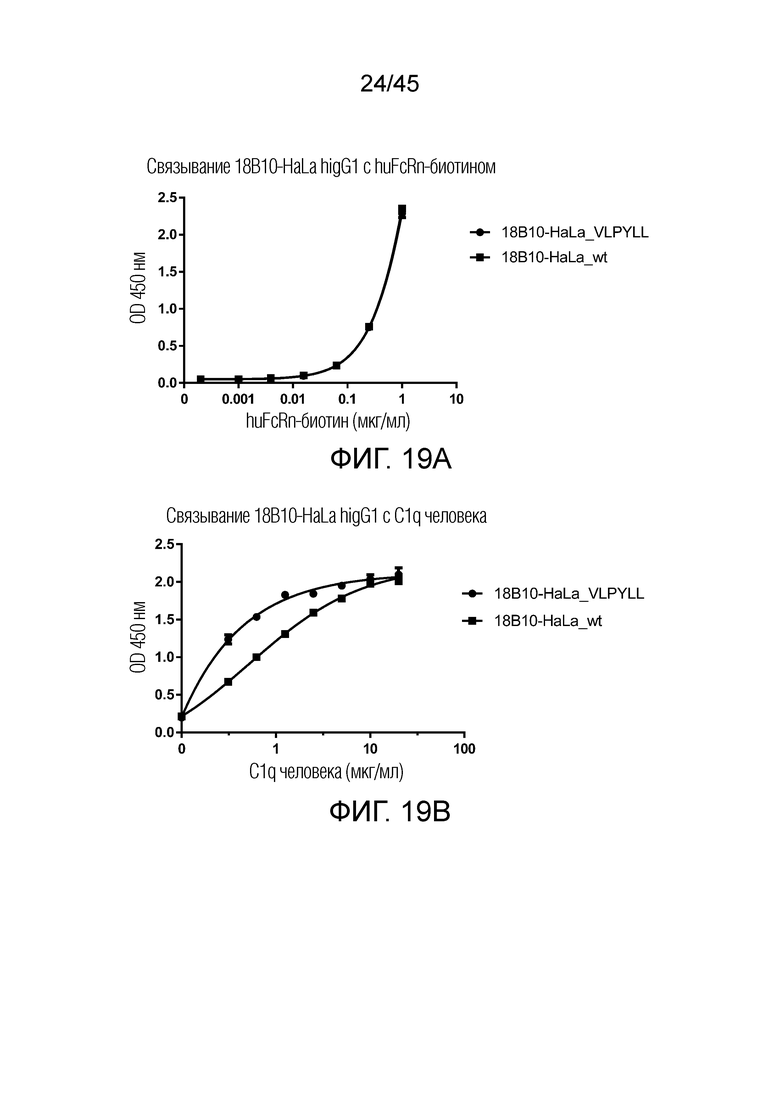
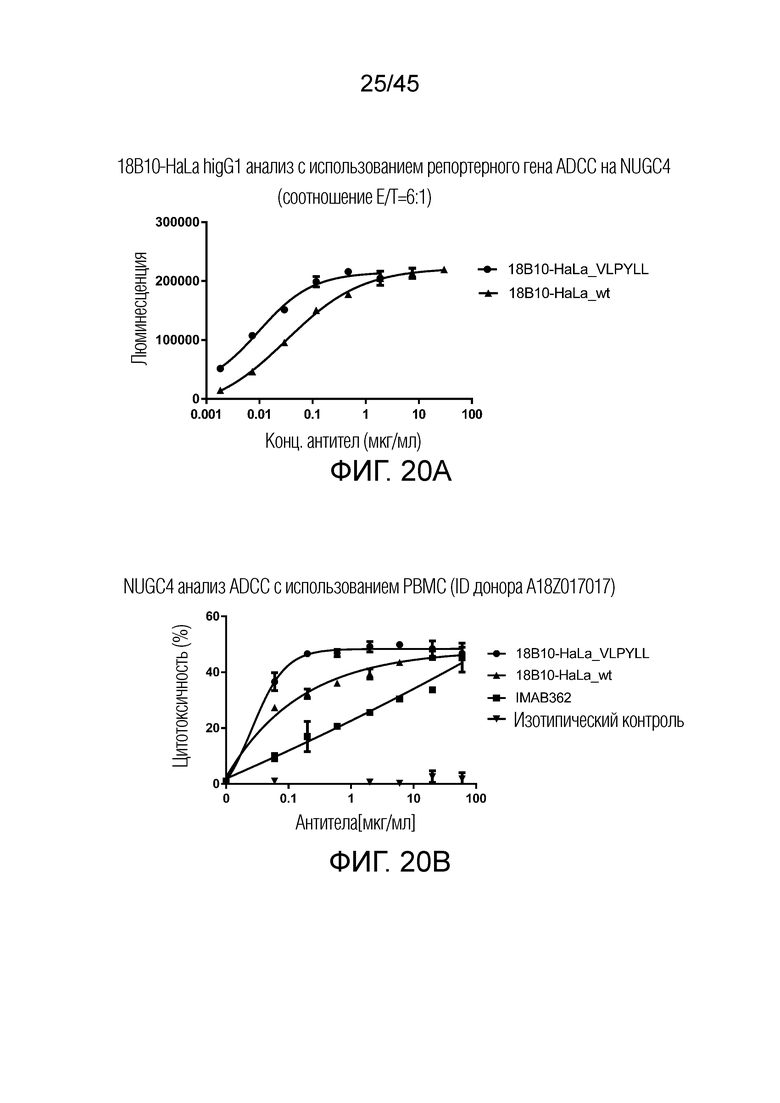
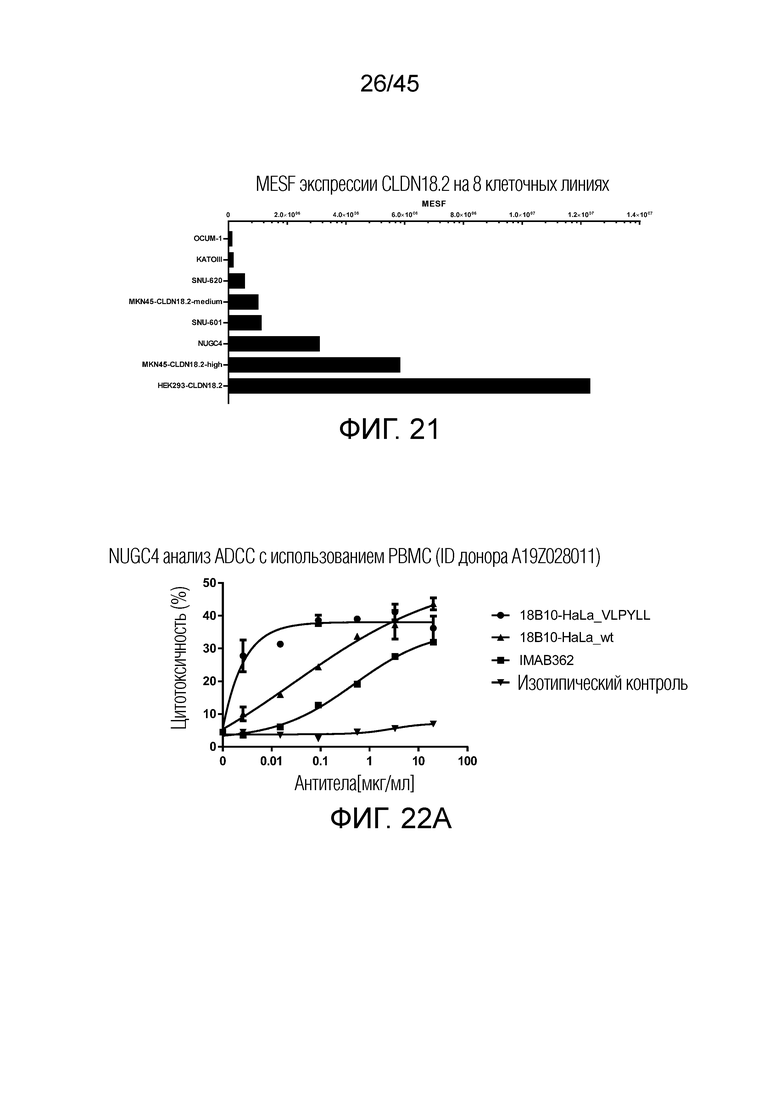
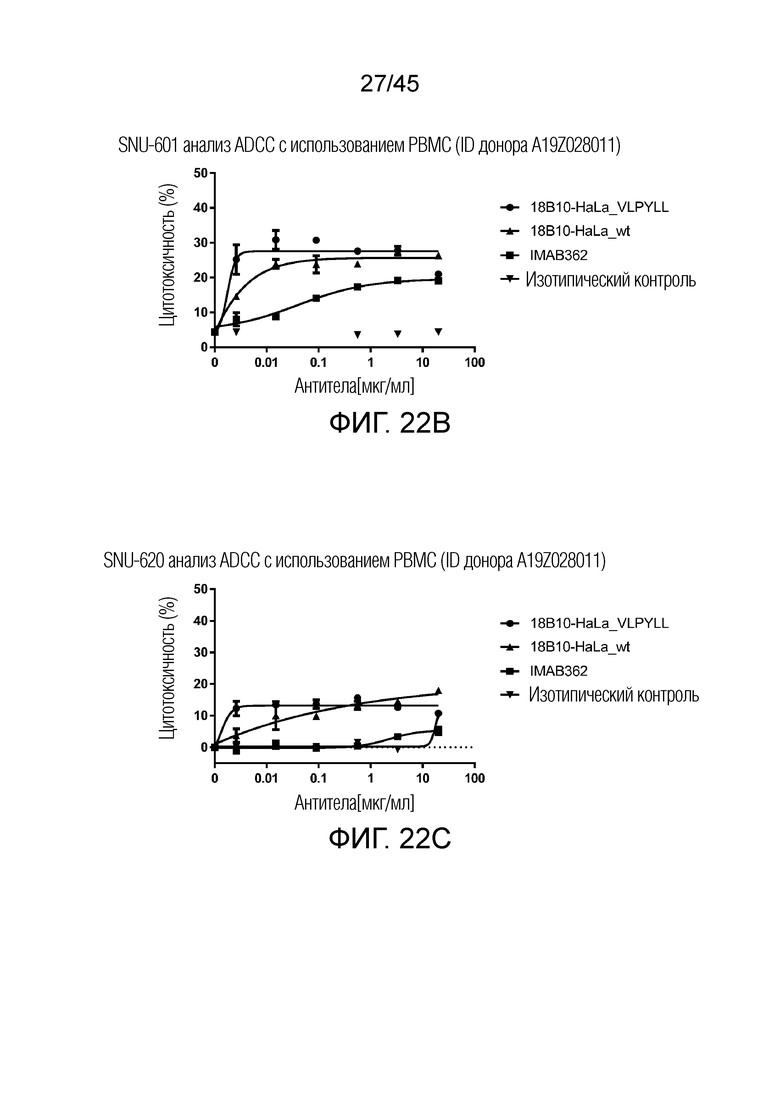
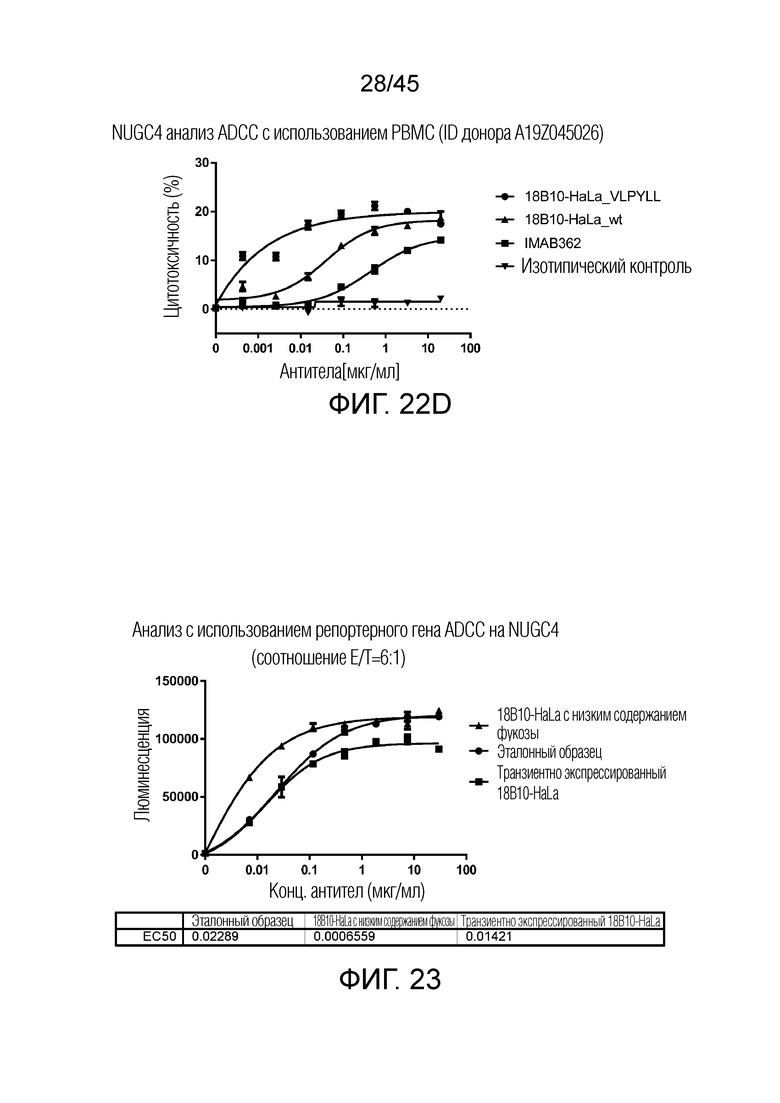
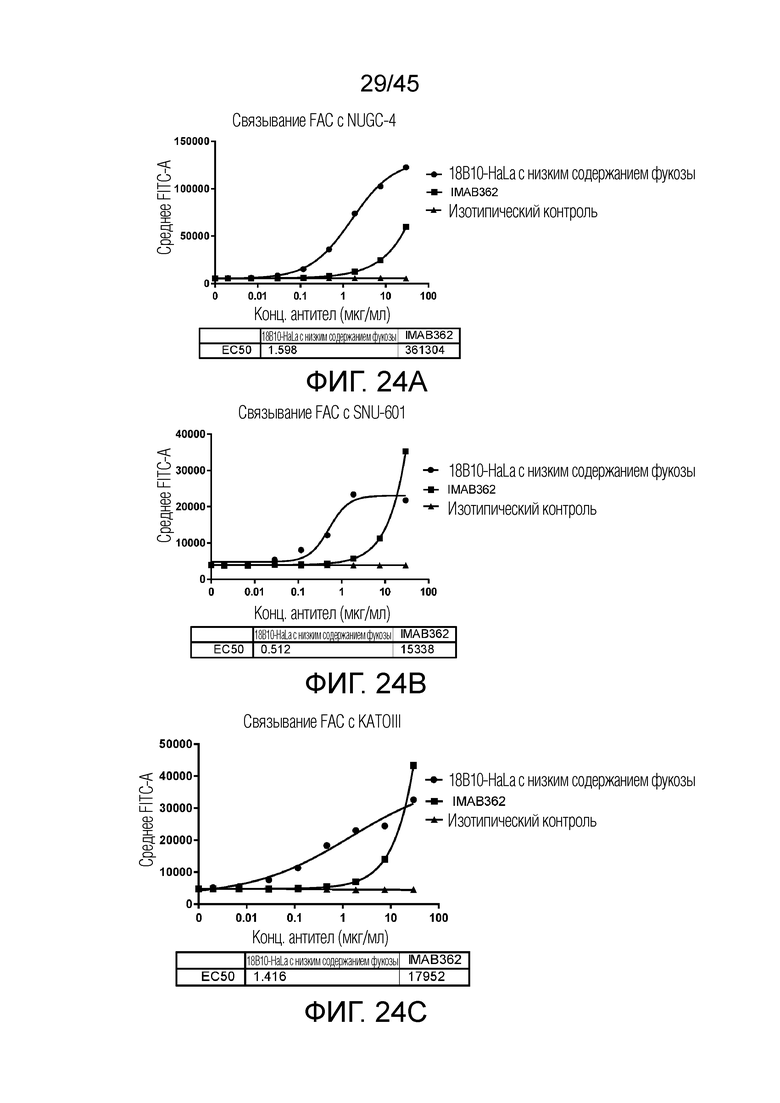
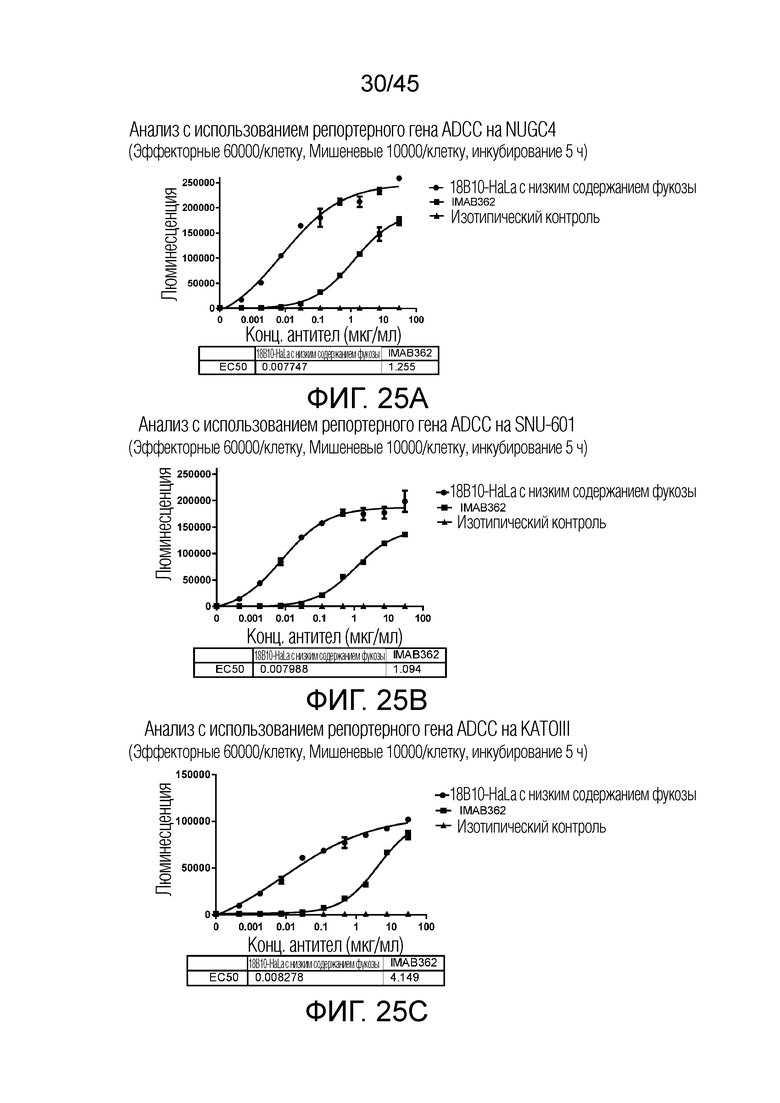
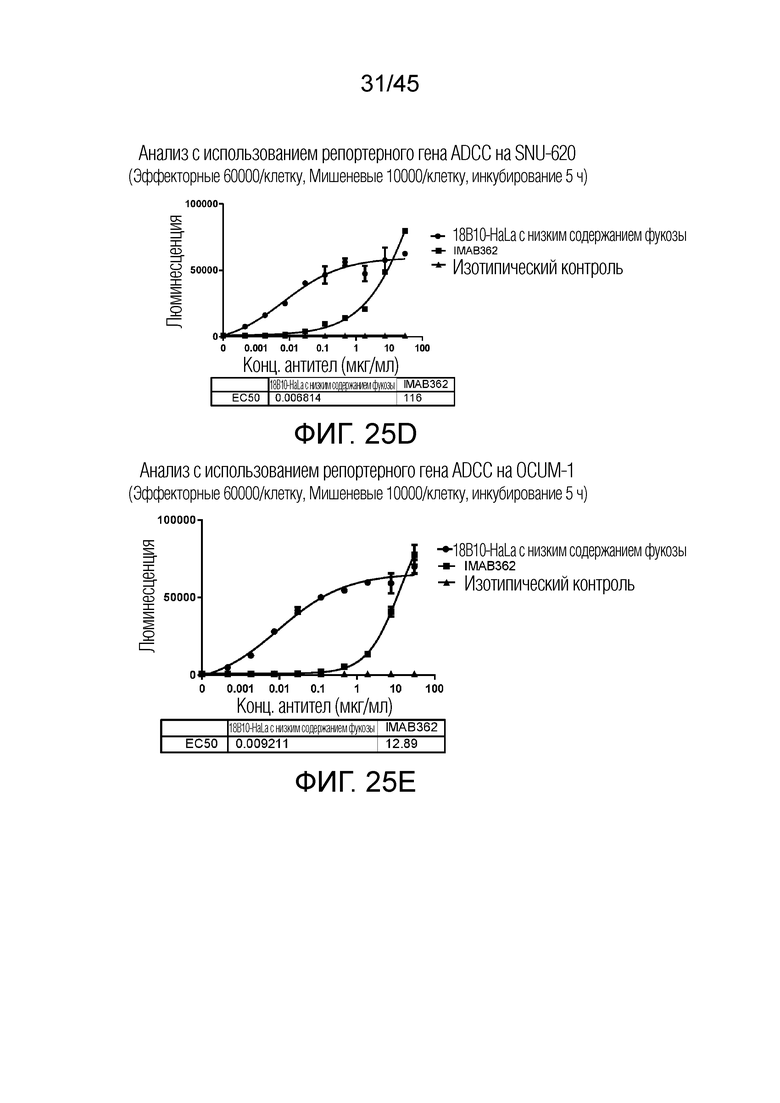
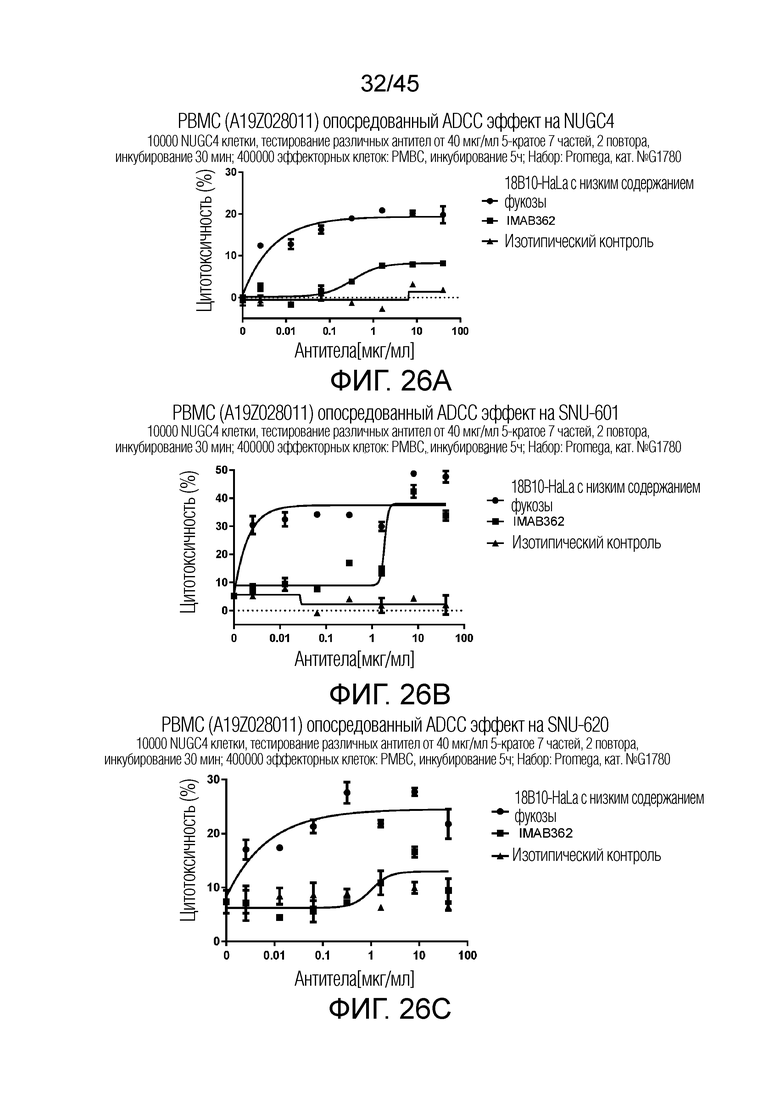
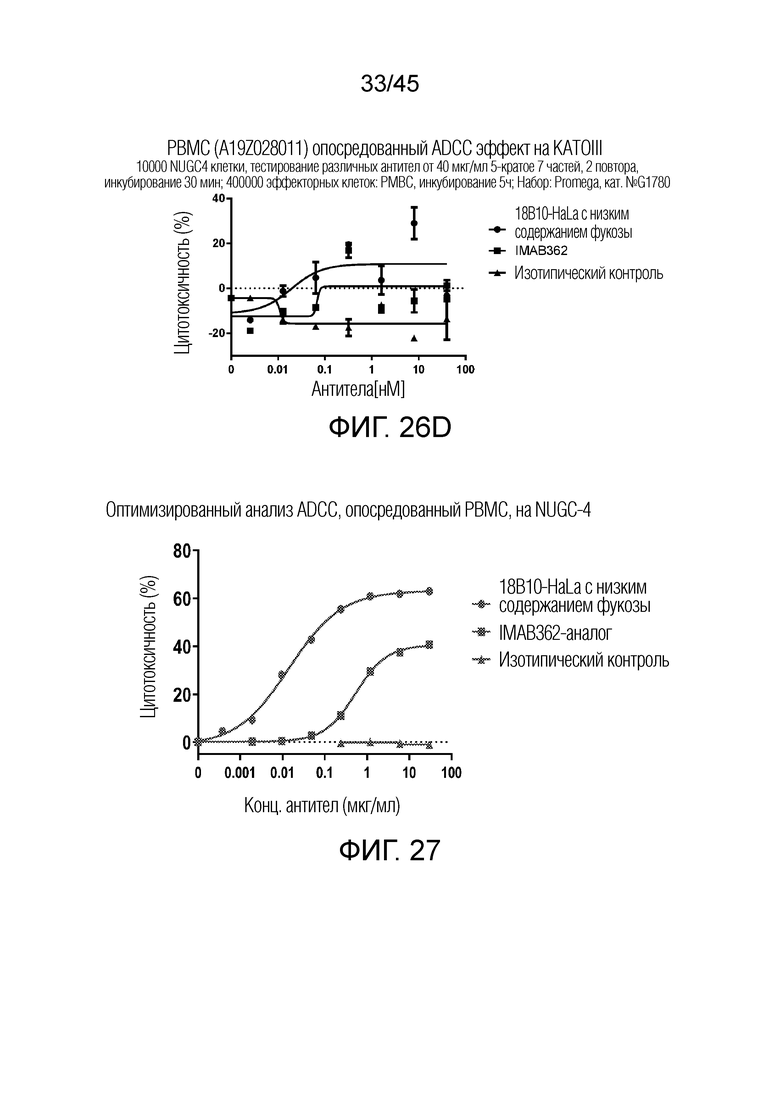
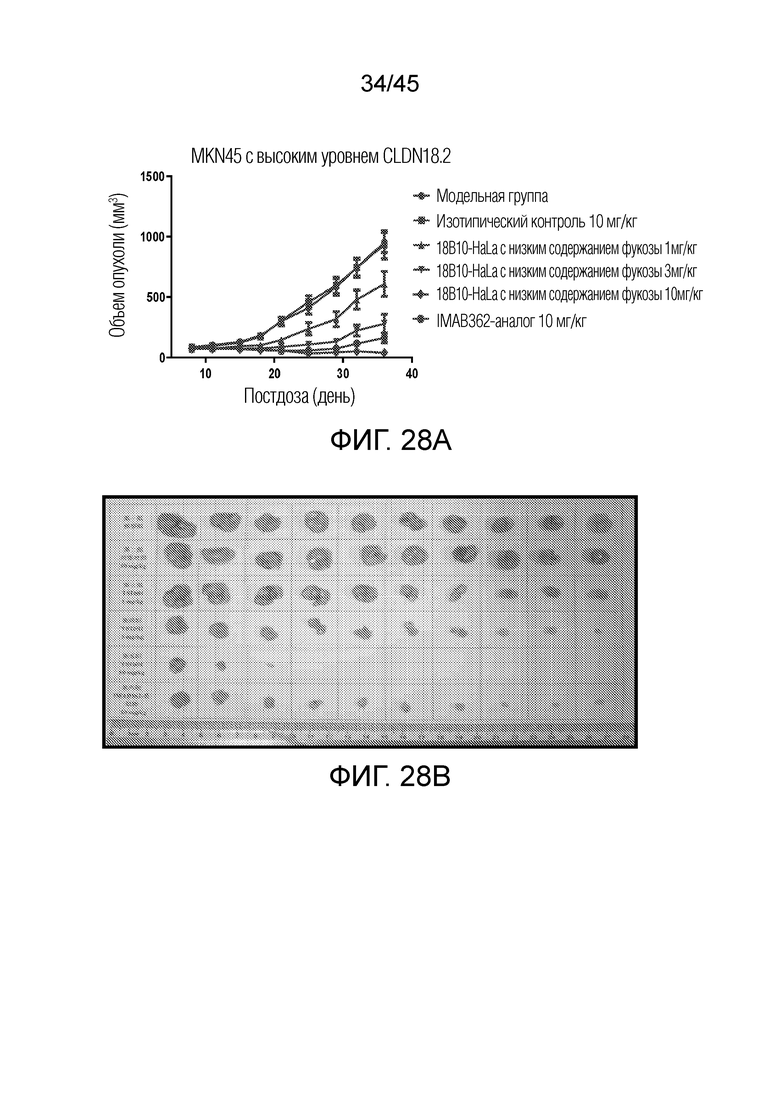
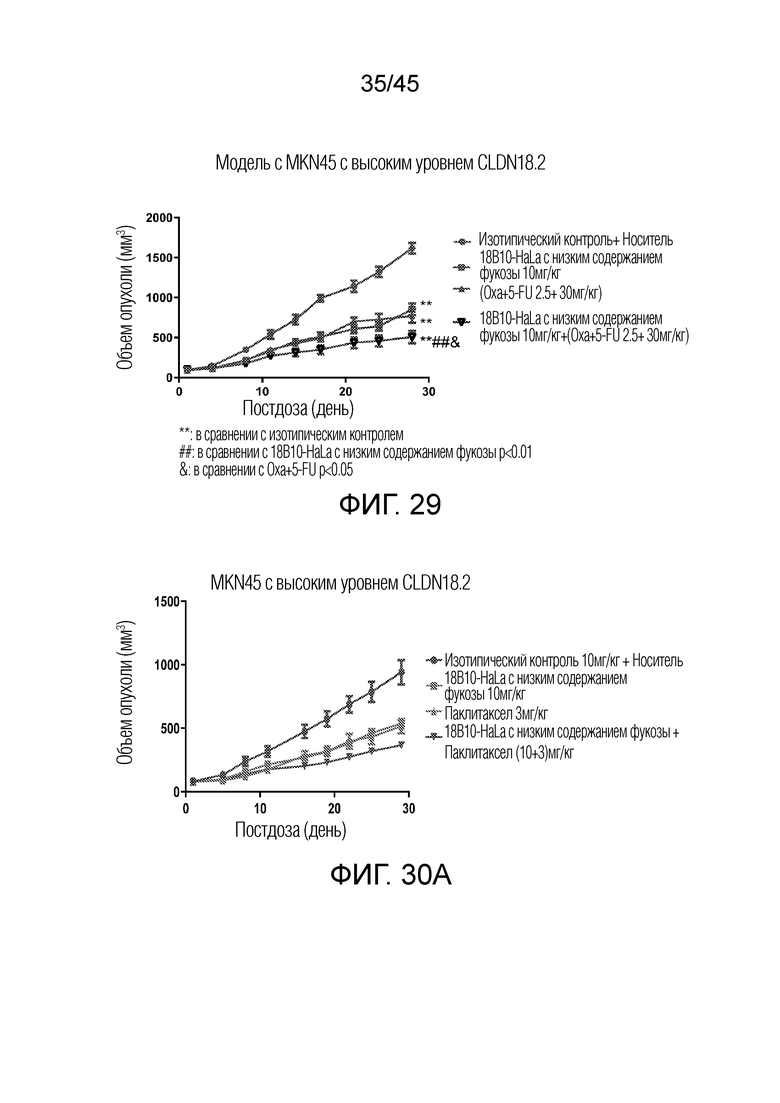
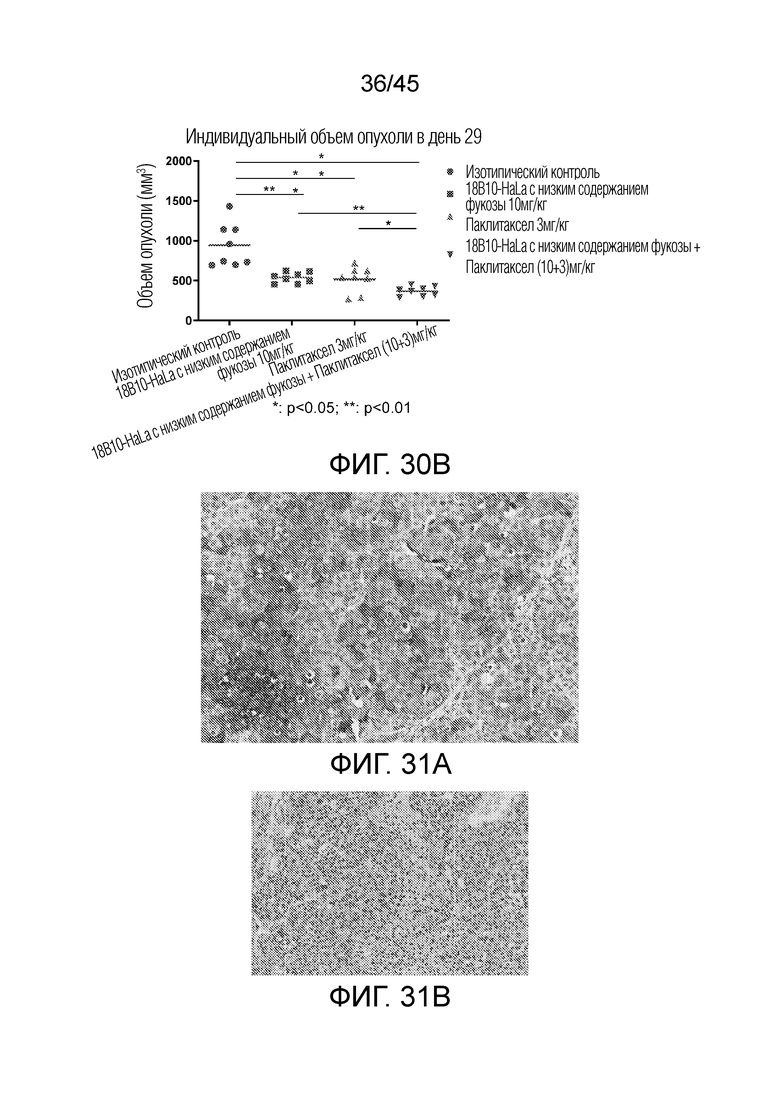
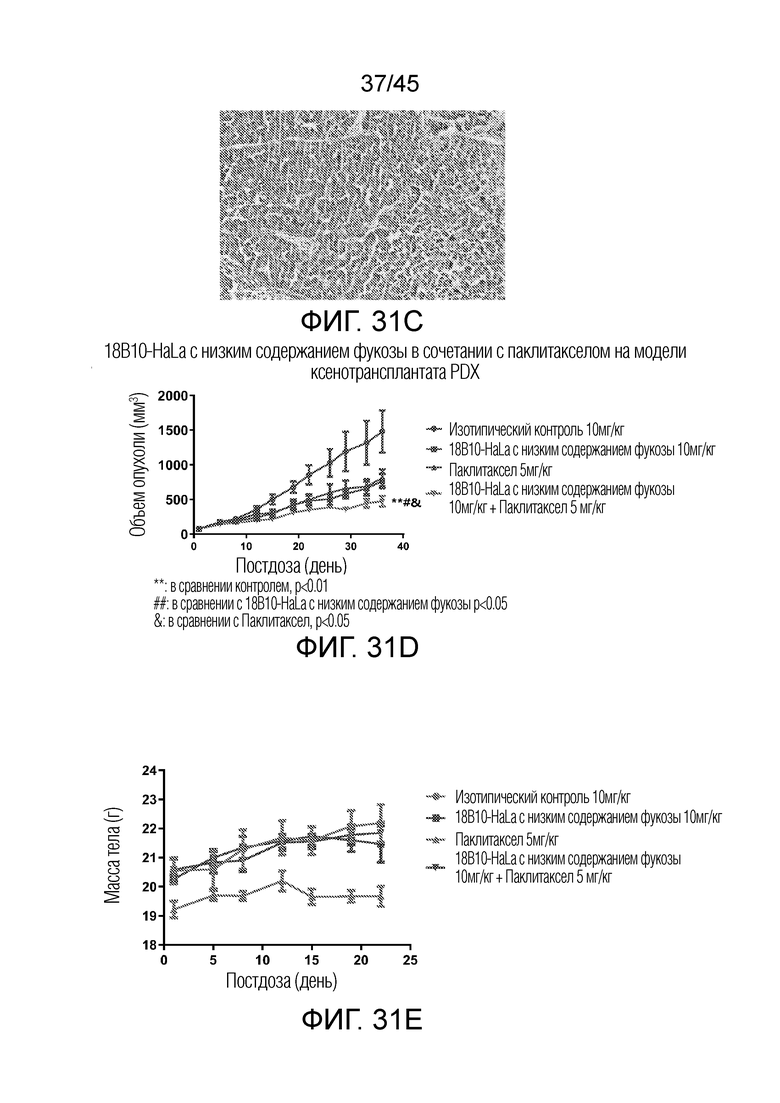
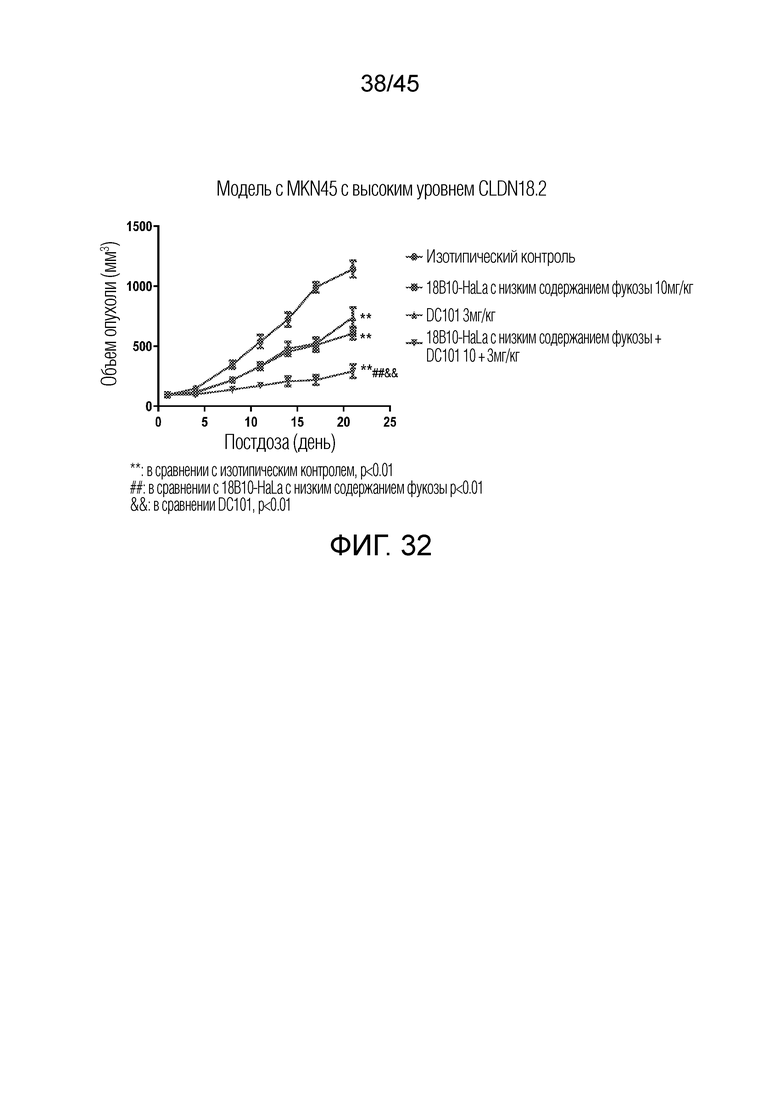
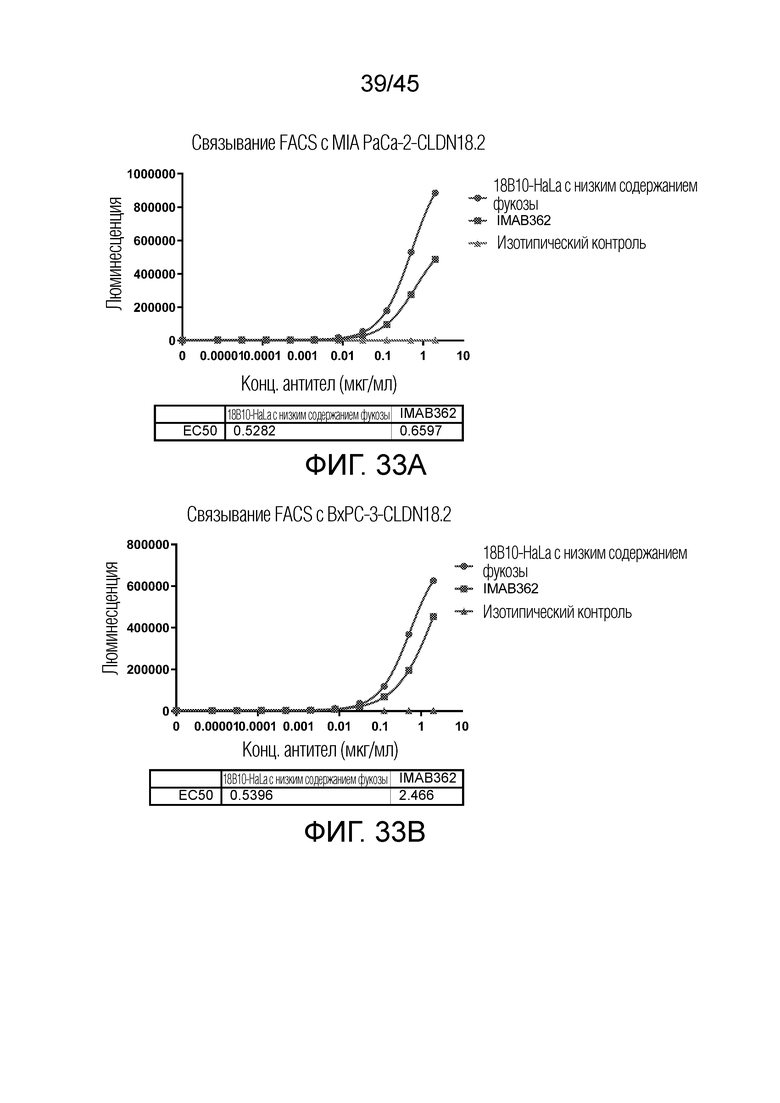
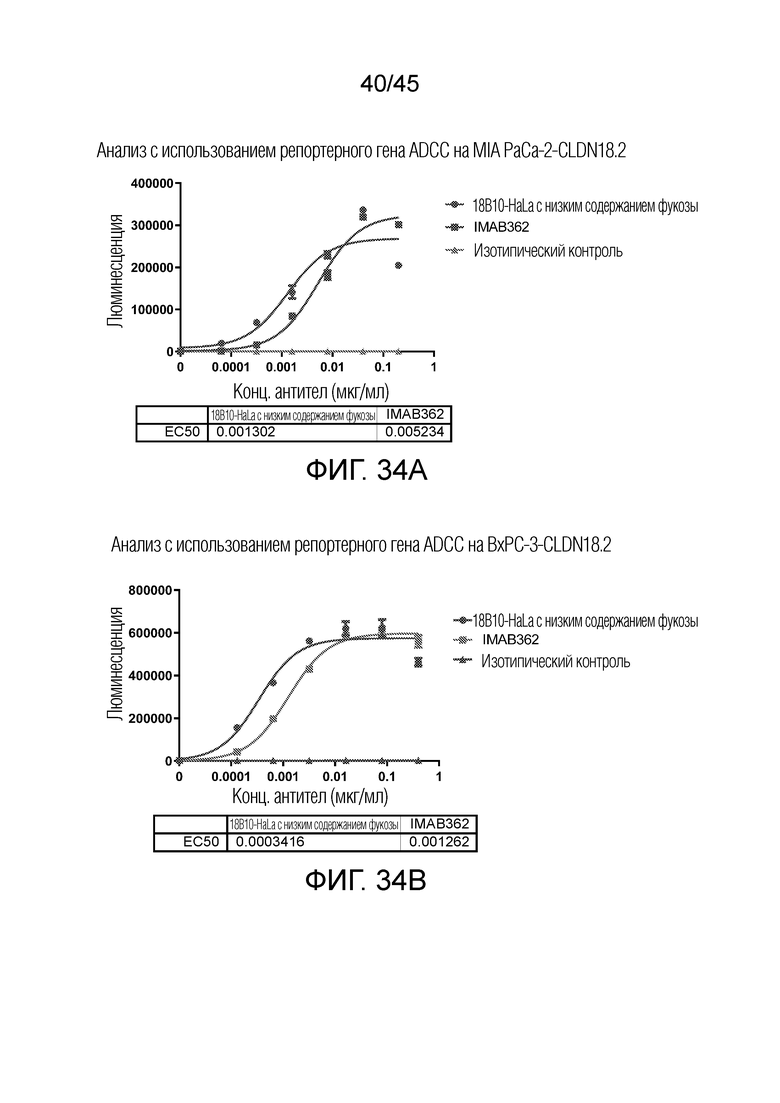
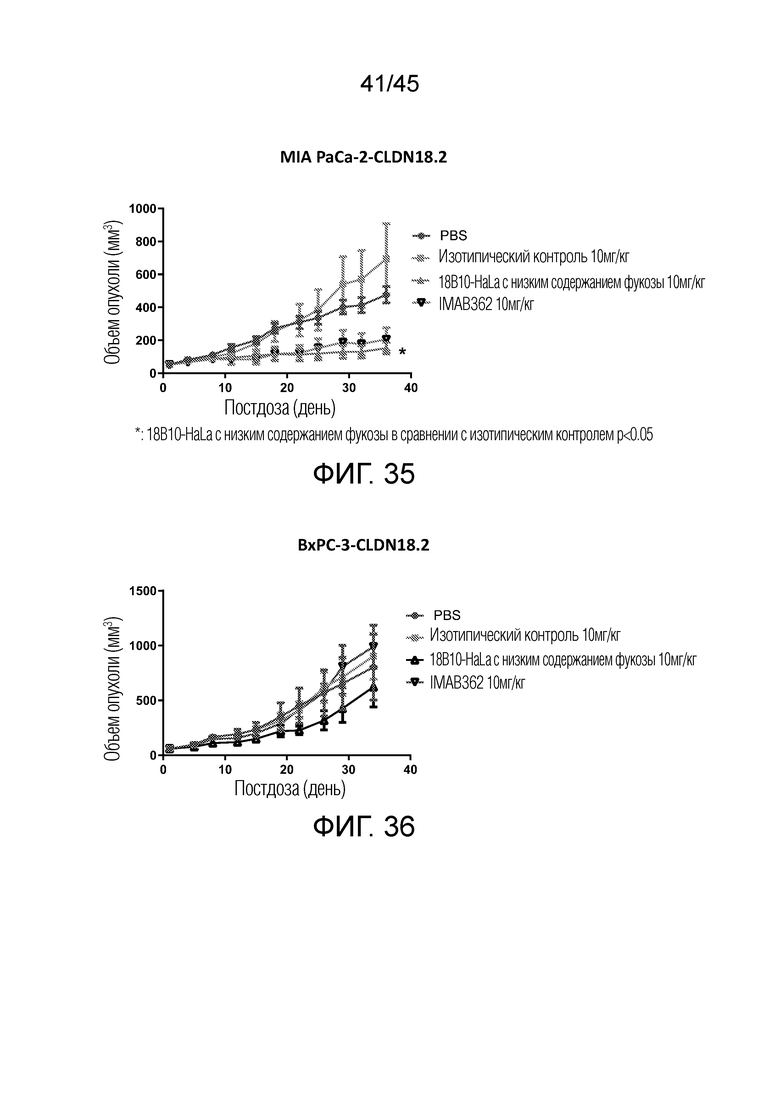
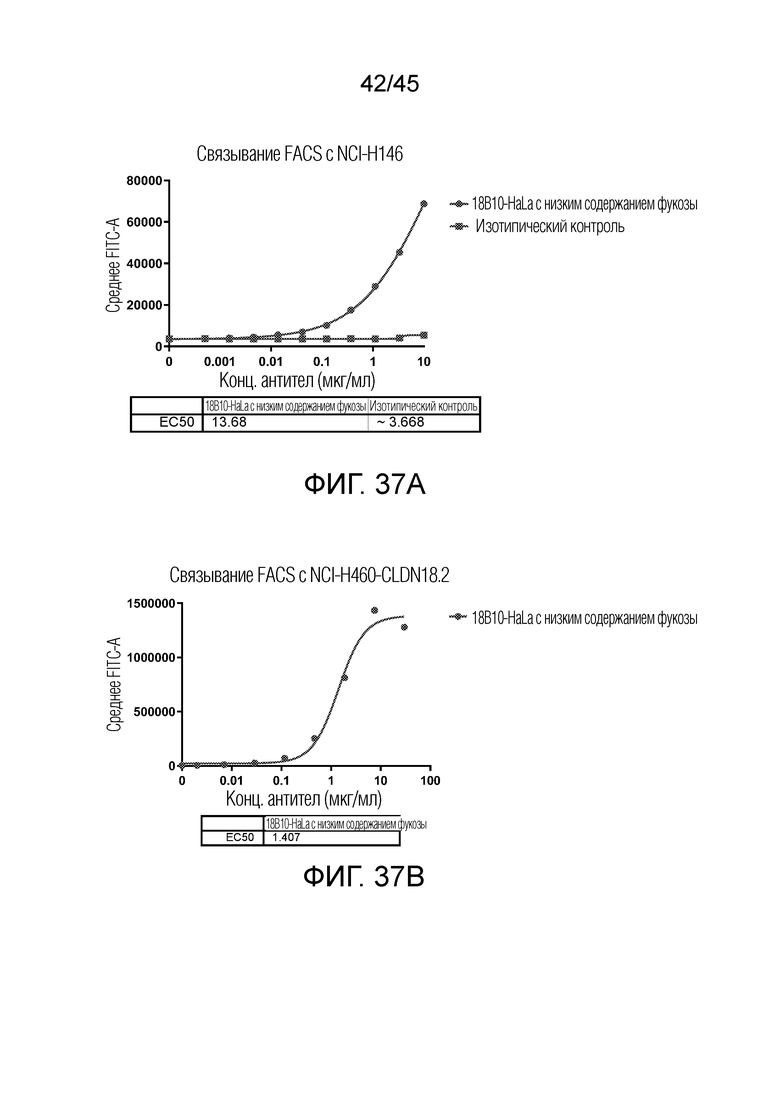
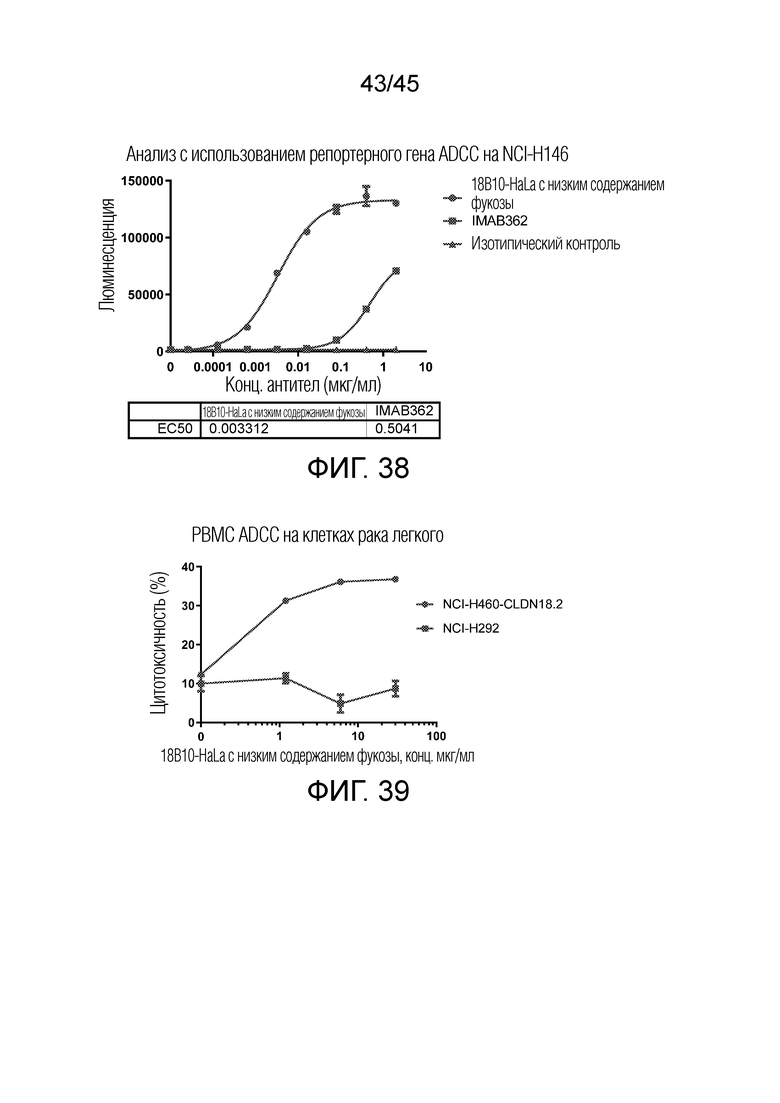
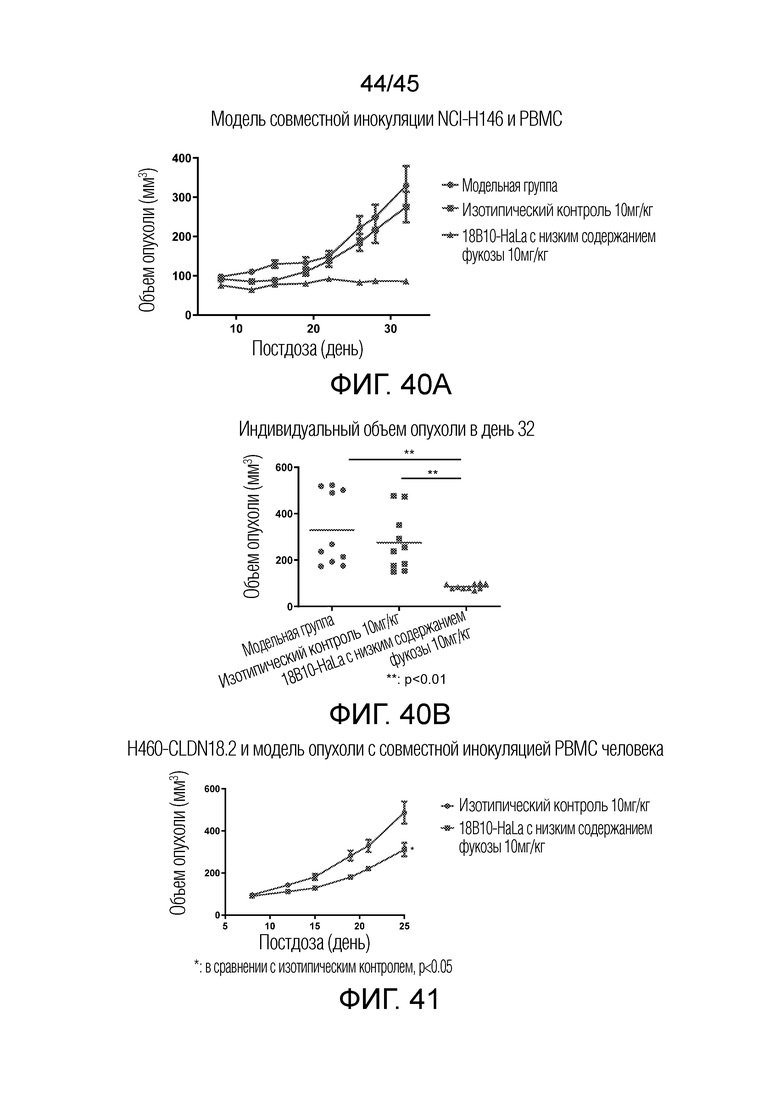
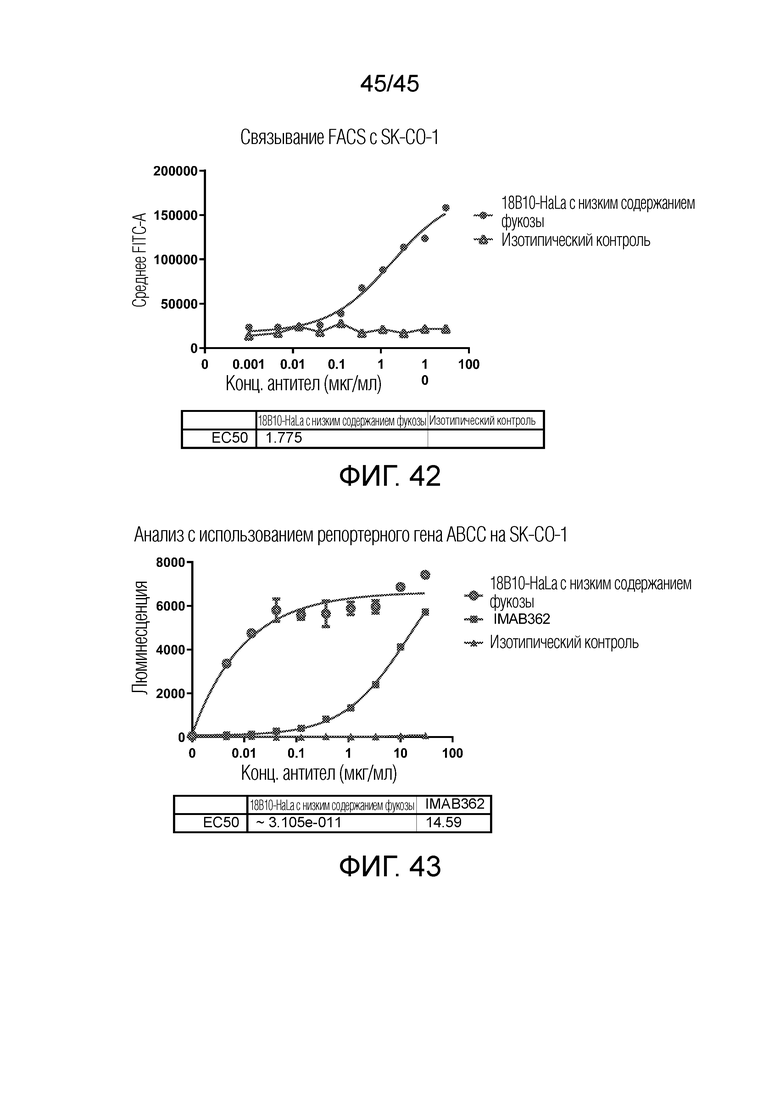
Изобретение относится к области биохимии, в частности к анти-CLDN18.2 антителу или его антигенсвязывающему фрагменту, а также к фармацевтической композиции, конъюгату и набору, его содержащим. Также раскрыты выделенный полинуклеотид, кодирующий вышеуказанное антитело или его фрагмент, а также вектор и клетка, его содержащие. Изобретение эффективно для лечения заболевания или состояния, связанного с CLDN18.2. 12 н. и 15 з.п. ф-лы, 43 ил., 27 табл., 23 пр.
1. Анти-CLDN18.2 антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи и вариабельную область легкой цепи, где
вариабельная область тяжелой цепи содержит последовательности тяжелых цепей HCDR1, HCDR2 и HCDR3 и
вариабельная область легкой цепи содержит последовательности легких цепей LCDR1, LCDR2 и LCDR3, где:
последовательность HCDR1 содержит GYNMN (SEQ ID NO:1), или TYFIGVG (SEQ ID NO:13);
последовательность HCDR2 содержит X1IDPYYX2X3TX4YNQKFX5G (SEQ ID NO:32), или HIWWNDNKYYNTALKS (SEQ ID NO:15);
последовательность HCDR3 содержит X6X7X8GNAFDY (SEQ ID NO:33), или MGSGAWFTY (SEQ ID NO:17);
последовательность LCDR1 содержит KSSQX9L×10NX11GNX12KNYLT (SEQ ID NO:34);
последовательность LCDR2 содержит WASTRX13S (SEQ ID NO:35);
последовательность LCDR3 содержит QNDYX14X15PX16T (SEQ ID NO:36);
где X1 представляет собой N или Y или H,
X2 представляет собой G или V,
X3 представляет собой A или G или T,
X4 представляет собой R или T или S,
X5 представляет собой K или R,
X6 представляет собой S или M,
X7 представляет собой Y или F,
X8 представляет собой Y или H,
X9 представляет собой S или N,
X10 представляет собой L или F,
X11 представляет собой S или N,
X12 представляет собой Q или L,
X13 представляет собой E или K,
X14 представляет собой S или Y,
X15 представляет собой F или Y и
X16 представляет собой F или L, и
где
а) HCDR1 содержит последовательность SEQ ID NO:1,
HCDR2 содержит последовательность SEQ ID NO:19,
HCDR3 содержит последовательность SEQ ID NO:21,
LCDR1 содержит последовательность SEQ ID NO:14;
LCDR1 содержит последовательность SEQ ID NO:16 и
LCDR1 содержит последовательность SEQ ID NO:18;
b) HCDR1 содержит последовательность SEQ ID NO:1,
HCDR2 содержит последовательность SEQ ID NO:3,
HCDR3 содержит последовательность SEQ ID NO:5;
LCDR1 содержит последовательность SEQ ID NO:2,
LCDR1 содержит последовательность SEQ ID NO:4 и
LCDR1 содержит последовательность SEQ ID NO:6;
с) HCDR1 содержит последовательность SEQ ID NO:1,
HCDR2 содержит последовательность SEQ ID NO:7,
HCDR3 содержит последовательность SEQ ID NO:5;
LCDR1 содержит последовательность SEQ ID NO:2,
LCDR1 содержит последовательность SEQ ID NO:4 и
LCDR1 содержит последовательность SEQ ID NO:8;
d) HCDR1 содержит последовательность SEQ ID NO:1,
HCDR2 содержит последовательность SEQ ID NO:9,
HCDR3 содержит последовательность SEQ ID NO:11;
LCDR1 содержит последовательность SEQ ID NO:10,
LCDR1 содержит последовательность SEQ ID NO:4 и
LCDR1 содержит последовательность SEQ ID NO:6; или
e) HCDR1 содержит последовательность SEQ ID NO:13,
HCDR2 содержит последовательность SEQ ID NO:15,
HCDR3 содержит последовательность SEQ ID NO:17;
LCDR1 содержит последовательность SEQ ID NO:2,
LCDR1 содержит последовательность SEQ ID NO:4 и
LCDR1 содержит последовательность SEQ ID NO:12;
f) HCDR1 содержит последовательность SEQ ID NO:1,
HCDR2 содержит последовательность SEQ ID NO:22,
HCDR3 содержит последовательность SEQ ID NO:5;
LCDR1 содержит последовательность SEQ ID NO:20,
LCDR1 содержит последовательность SEQ ID NO:4 и
LCDR1 содержит последовательность SEQ ID NO:6.
2. Антитело или его антигенсвязывающий фрагмент по п.1, содержащие одну или несколько тяжелых цепей HFR1, HFR2, HFR3 и HFR4, и/или одну или несколько легких цепей LFR1, LFR2, LFR3 и LFR4, где:
HFR1 содержит QVQLVQSGAEVKKPGASVKVSCKASGYX17FT (SEQ ID NO:54),
HFR2 содержит WVX18QAPGQGLEWX19G (SEQ ID NO:55),
HFR3 содержит RVTX20TIDKSTSTVYMELSSLRSEDTAVYYCAR (SEQ ID NO:56),
HFR4 содержит WGQGTTVTVSS (SEQ ID NO:57),
LFR1 содержит DIVMTQSPDSLAVSLGERATX21NC (SEQ ID NO:58),
LFR2 содержит WYQQKPGQPPKLLIY (SEQ ID NO:59),
LFR3 содержит GVPDRFX22GSGSGTDFTLTISSLQAEDVAVYYC (SEQ ID NO:60), и
LFR4 содержит FGGGTKVEIK (SEQ ID NO:61),
где X17 представляет собой T или S,
X18 представляет собой R или K,
X19 представляет собой M или I,
X20 представляет собой M или L,
X21 представляет собой I или M, и
X22 представляет собой S или T.
3. Антитело или его антигенсвязывающий фрагмент по п.2, где:
HFR1 содержит последовательность, выбранную из группы, включающей SEQ ID NO:62 и 63,
HFR2 содержит последовательность, выбранную из группы, включающей SEQ ID NO:64 и 65,
HFR3 содержит последовательность, выбранную из группы, включающей SEQ ID NO:66 и 67,
HFR4 содержит последовательность SEQ ID NO:57,
LFR1 содержит последовательность, выбранную из группы, включающей SEQ ID NO:68 и 69,
LFR2 содержит последовательность SEQ ID NO:59,
LFR3 содержит последовательность, выбранную из группы, включающей SEQ ID NO:70 и 71, и
LFR4 содержит последовательность SEQ ID NO:61.
4. Антитело или его антигенсвязывающий фрагмент по п.1, где
вариабельная область тяжелой цепи содержит последовательность, выбранную из группы, включающей SEQ ID NO:25, SEQ ID NO:27, SEQ ID NO:29, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:41, SEQ ID NO:43, SEQ ID NO:45 и SEQ ID NO:47; и
вариабельная область легкой цепи содержит последовательность, выбранную из группы, включающей SEQ ID NO:26, SEQ ID NO:28, SEQ ID NO:38, SEQ ID NO:40, SEQ ID NO:42, SEQ ID NO:44, SEQ ID NO:46 и SEQ ID NO:48.
5. Антитело или его антигенсвязывающий фрагмент по п.1, где:
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:25 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:26;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:27 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:28;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:29 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:26 или 28;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:37 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:38;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:39 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:40;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:41 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:42;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:43 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:44;
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:45 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:46; или
вариабельная область тяжелой цепи содержит последовательность SEQ ID NO:47 и вариабельная область легкой цепи содержит последовательность SEQ ID NO:48.
6. Антитело или его антигенсвязывающий фрагмент по п.1, содержащие константную область иммуноглобулина, содержащие константную область Ig человека или содержащие константную область IgG человека.
7. Антитело или его антигенсвязывающий фрагмент по п.6, где константная область содержит одну или несколько замен аминокислотных остатков относительно SEQ ID NO:49, выбранных из группы, включающей: L235V, F243L, R292P, Y300L, P396L или любую их комбинацию.
8. Антитело или его антигенсвязывающий фрагмент по п.7, где константная область содержит последовательность SEQ ID NO:51.
9. Антитело или его антигенсвязывающий фрагмент по п.1, которые являются гуманизированными или афукозилированными.
10. Антитело или его антигенсвязывающий фрагмент по п.1, где антигенсвязывающий фрагмент выбран из группы, состоящей из диатела, Fab, Fab', F(ab')2, Fd, фрагмента Fv, стабилизированного дисульфидом фрагмента Fv (dsFv), (dsFv)2, стабилизированного дисульфидом диатела (ds диатело), молекулы одноцепочечного антитела (scFv), димера scFv (бивалентное диатело), верблюжьего однодоменного антитела, нанотела, доменного антитела и бивалентного доменного антитела.
11. Биспецифическое антитело или его антигенсвязывающий домен для связывания с CLDN18.2 и второго антигена, которые содержат антигенсвязывающий домен анти-CLDN18.2 антитела, или его антигенсвязывающего фрагмента, по п.1 и второй антигенсвязывающий домен,
где второй антиген представляет собой иммунную мишень или опухолевый антиген,
где иммунная мишень выбрана из группы, состоящей из: PD-L1, PD-L2, PD-1, CLTA-4, TIM-3, LAG3, CD160, 2B4, TGF β, VISTA, BTLA, TIGIT, LAIR1, OX40, CD2, CD27, ICAM-1, NKG2C, SLAMF7, NKp80, CD160, B7-H3, LFA-1, 1COS, 4-1BB, GITR, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, IL-2, IL-15, CD3, CD16 и CD83; и
где опухолевый антиген содержит CA-125, ганглиозиды G(D2), G(M2) и G(D3), CD20, CD52, CD33, Ep-CAM, CEA, бомбезин-подобные пептиды, PSA, HER2/neu, рецептор эпидермального фактора роста (EGFR), erbB2, erbB3/HER3, erbB4, CD44v6, Ki-67, опухоле-ассоциированный муцин, VEGF, VEGFR, рецепторы эстрогена, антиген Льюиса-Y, TGFβ1, рецептор IGF-1, EGFα, рецептор c-Kit, рецептор трансферрина, IL-2R или CO17-1A.
12. Конъюгат антитела-лекарственного средства для доставки цитотоксических средств в опухоли, содержащий антитело или его антигенсвязывающий фрагмент по п.1, связанные с одним или несколькими фрагментами конъюгата,
где фрагмент конъюгата содержит средство, модифицирующее клиренс, химиотерапевтическое средство, токсин, радиоактивный изотоп, лантанид, люминесцентную метку, флуоресцентную метку, фермент-субстратную метку, алкилаторы ДНК, ингибитор топоизомеразы, средства, связывающие тубулин, или другие противоопухолевые лекарственные средства.
13. Фармацевтическая композиция для лечения заболевания или состояния, связанного с CLDN18.2, у пациента, содержащая антитело или его антигенсвязывающий фрагмент по п.1, и один или несколько фармацевтически приемлемых носителей.
14. Выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по п.1.
15. Вектор экспрессии, содержащий выделенный полинуклеотид по п.14.
16. Клетка-хозяин, экспрессирующая антитело или его антигенсвязывающий фрагмент по п.1, содержащая вектор по п.15.
17. Способ экспрессии антитела или его антигенсвязывающего фрагмента по п.1, включающий культивирование клетки-хозяина, содержащий вектор экспрессии, содержащий выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по п.1, в условиях, при которых экспрессируется вектор.
18. Способ лечения заболевания или состояния, связанного с CLDN18.2, у пациента, включающий введение пациенту терапевтически эффективного количества антитела или его антигенсвязывающего фрагмента по п.1,
где заболевание или состояние представляет собой рак, необязательно рак, экспрессирующий CLDN18.2.
19. Способ по п.18, где рак, экспрессирующий CLDN18.2, представляет собой раковую клетку с высоким уровнем экспрессии CLDN18.2, раковую клетку со средним уровнем экспрессии CLDN18.2 или раковую клетку с низким уровнем экспрессии CLDN18.2.
20. Способ по п.19, где
раковая клетка с высоким уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью по меньшей мере 2+, как определено с помощью IHC, и на уровне, где по меньшей мере 70% клеток окрашиваются положительно при IHC;
раковая клетка со средним уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью по меньшей мере 1+, как определено с помощью IHC, и на уровне, где по меньшей мере 40%, но ниже 70% клеток окрашиваются положительно при IHC, и
раковая клетка с низким уровнем экспрессии CLDN18.2 экспрессирует CLDN18.2 с интенсивностью по крайней мере 1+, как определено с помощью IHC, и на уровне, где около 0, но ниже 40% клеток окрашиваются положительно при IHC.
21. Способ по любому из пп.18-20, где рак представляет собой рак желудка, рак легкого, рак бронхов, рак кости, рак печени и желчных протоков, рак поджелудочной железы, рак молочной железы, рак печени, рак яичников, рак яичка, рак почки, рак мочевого пузыря, рак головы и шеи, рак позвоночника, рак головного мозга, рак шейки матки, рак матки, рак эндометрия, рак толстой кишки, колоректальный рак, рак прямой кишки, рак анального канала, рак пищевода, рак желудочно-кишечного тракта, рак кожи, рак предстательной железы, рак гипофиза, рак желудка, рак влагалища, рак щитовидной железы, глиобластому, астроцитому, меланому, миелодиспластический синдром, саркому, тератому и аденокарциному.
22. Способ по п.18, где пациентом является человек.
23. Способ по п.18, дополнительно включающий введение терапевтически эффективного количества второго терапевтического агента.
24. Набор для лечения заболевания или состояния, связанного с CLDN18.2, у пациента, содержащий антитело или его антигенсвязывающий фрагмент по п.1, и второй терапевтический агент.
25. Способ диагностики заболевания или состояния, связанного с CLDN18.2, у пациента, включающий:
a) приведение в контакт образца, полученного у пациента, с антителом или его антигенсвязывающим фрагментом по п.1;
b) определение наличия или количества CLDN18.2 в образце; и
c) сопоставление наличия или количества CLDN18.2 с наличием или статусом связанного с CLDN18.2 заболевания или состояния у пациента.
26. Набор для обнаружения CLDN18.2, отличающийся тем, что набор содержит антитело или его антигенсвязывающий фрагмент по п.1.
27. Химерный антигенный рецептор (CAR), который специфически связывается с CLDN18.2, содержащий антигенсвязывающий домен, трансмембранный домен, костимуляторную сигнальную область и сигнальный домен TCR,
где антигенсвязывающий домен содержит антигенсвязывающий фрагмент по п.1.
| WO 2008145338 A2, 04.12.2008 | |||
| US 2009169547 A1, 02.07.2009 | |||
| EP 3170842 A1, 24.05.2017 | |||
| PRABHSIMRANJOT SINGH et al | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К КЛАУДИНУ-18 ДЛЯ ЛЕЧЕНИЯ РАКА | 2006 |
|
RU2445319C2 |
Авторы
Даты
2024-11-26—Публикация
2020-08-20—Подача