Изобретение относится к медицине, конкретно к области хирургического лечения постинтубационных и посттрахеостомических стенозов шейного отдела трахеи.
В современном мире сохраняется отчетливая тенденция к росту общего травматизма. В последние годы с бурным развитием автотранспорта, современных высокоэнергетических технологий на производстве и непрекращающимися локальными войнами травмы стали носить все более тяжелый характер. Кроме того, довольно широко стали выполняться операции на сердце и центральной нервной системе, чаще стали оперировать пожилых больных и пациентов с сопутствующими заболеваниями; частота токсических поражений, сопровождающихся острой дыхательной недостаточностью, также не уменьшается. Все это ведет к увеличению количества больных, которым по различным причинам требуется проведение длительной искусственной вентиляции легких. Это, в свою очередь, приводит к увеличению числа пациентов с постинтубационными и посттрахеостомическими стенозами трахеи. Рост числа реконструктивно-пластических операций, трансплантаций легких вносит свою лепту в увеличение числа пациентов с рубцовыми стенозами трахеи. Нарастающая в России эпидемия туберкулеза, которой способствует увеличение лекарственно-резистентных форм микобактерий, приведет в том числе к увеличению посттуберкулезных стенозов трахеи.
Таким образом, несмотря на прогресс медицины количество больных с рубцовыми стенозами дыхательных путей не снижается.
Уровень техники
Лечение рубцовых стенозов трахеи до настоящего времени остается одной из наиболее сложных проблем хирургии легких и средостения. Наиболее радикальным методом их лечения является циркулярная резекция трахеи с иссечением пораженного сегмента и анастомозом по типу "конец в конец". Однако у части больных такие операции невыполнимы из-за распространенности поражения или связаны с большим операционным риском, а частота послеоперационных осложнений и рестенозов остается довольно высокой. В качестве альтернативы используют пролонгированную дилатацию просвета дыхательных путей различными трубками, что довольно травматично, многоэтапно, при этом на длительный срок сохраняется трахеостома, инвалидизирующая пациента.
Известные устройства для лечения рубцового стеноза условно делят на дилататирующие и иссекаюшие. К дилатирующим устройствам, обеспечивающим расширение места сужения, относят жесткий бронхоскоп, фибробронхоскоп, интубационые трубки, пластмассовые и ламинарные бужи, катетер Фогарти и т.д. Операции одномоментного эндоскопического расширения просвета при рубцовых стенозах дают лишь временный эффект, так что вышеперечисленным средствам чаще отводится роль подготовительных, обеспечивающих адекватную подготовку к основному вмешательству. К иссекающим относится ряд устройств, таких как электронож, электрокаутеры, биопсийные кусачки, лазерные фотокоагуляторы, ультразвуковые и криогенные деструкторы.
Применение для иссечения стеноза тубусов жесткого бронхоскопа, специальных циркулярных ножей и биопсийных щипцов чревато прободением деформированной стенки гортани и развитием серьезных кровотечений.
Электрохирургическое оборудование по сравнению с лазерным обладает преимуществами дешевизны и доступности - всю необходимую аппаратуру легко приобрести и разместить в операционной, а ее стоимость составляет лишь ничтожную часть стоимости лазерной установки. Однако применение средств иссечения токами высокой частоты и лазерным излучением опасно высокой вероятностью повреждения прилежащих неизмененных участков трахеи с последующим развитием в них воспалительного процесса и увеличением протяженности стеноза. Серьезным недостаткам электрохирургического оборудования является также наличие контакта электрода с тканью. Из-за этого происходит образование нагара и приваривание электрода к тканям, а при извлечении электрода часто происходит отрыв струпа, что может привести к кровотечению.
Средства ультразвукового воздействия на рубцовую ткань не получили широкого распространения в хирургии рубцовых стенозов трахеи из-за малой интенсивности оказываемого воздействия.
Одним из перспективных средств лечения рубцовых стенозов трахеи является криохирургическое воздействие [1, гл. 1]. Важным достоинством его является то, что, вызывая некроз и отторжение промороженной ткани рубца, оно почти не приводит к разрушению неизмененной стенки трахеи или бронха. Измененные ткани ввиду их поверхностного расположения, повышенной плотности и морфологической неполноценности наиболее подвержены деструкции при переохлаждении. Криовоздействие радикально отличается от других форм воздействия отсутствием явных травматических изменений, таких как механическое раздавливание, химические или термические ожоги, сопровождающиеся денатурацией биологического вещества и последующий реакцией на уровне макроорганизма.
Как показали экспериментальные исследования, хрящи трахеи при промораживании повреждаются минимально и восстанавливаются полностью в течение 1-6 мес [2] . Необратимо погибают и замещаются рубцовой тканью только гладкие мышечные волокна. Но в хрящевой части стенки трахеи количество их невелико, а ограниченное рубцевание только мембранной части не может привести к развитию рубцового стеноза. К недостаткам способа относится то, что эффект лечения наступает только через 8-10 дней после вмешательства. В качестве хладагента применительно к отоларингологии и хирургии трахеи используют углекислоту, закись азота и жидкий азот.
Известен ряд устройств для подведения хладагента к патологическому очагу [1, гл.2]. К ним относятся: аппараты А.И. Шальникова, С.Е. Сладковича, криокаутер Лоратта-Джакоба, криоэкстракторы Крвавича, А.М. Водовозова, аппараты "Криотом-1" и "Пингвин" (Россия), аппараты типа "СЕ" фирмы "Linde Division of Union Carbide Corporation", типа "ACU" фирмы "Spembly Technical Products". Различаясь по сложности, надежности и стоимости, они, по-видимому, не всегда могут удовлетворить хирургов, в связи с чем и не получили широкого распространения, а используются лишь некоторыми специализированными клиниками. Косвенным свидетельством этого может служить небольшое количество публикаций по их применению в отечественной и зарубежной литературе. Кроме того, все перечисленные аппараты имеют жесткие наконечники, проведение которых к стенозированному участку трахеи затруднено и сопряжено с риском дополнительной травматизации, вызывающей вторичное развитие грануляции и стеноза. Еще одним недостатком известных аппаратов является несоответствие формы контактной поверхности наконечника форме дефекта, что вынуждает проводить в ходе одного сеанса многократные манипуляции с наконечником. Таким образом, при достигнутом уровне техники средства криовоздействия не обеспечивают радикальности при лечении рубцовых стенозов трахеи.
Наиболее близким к предлагаемому устройству является криогенный аппликатор [3] , содержащий цилиндрический рабочий элемент с закрепленным на одном из его торцов деформируемым держателем. Рабочий элемент выполнен из пористого проницаемого никелида титана, а держатель выполнен из пластичного никелида титана. Криовоздействие осуществляется следующим образом. Аппликатор погружают в хладагент, как правило, жидкий азот, который удерживается в порах капиллярными силами, после чего подводят рабочей поверхностью к подлежащему криодеструкции патологическому очагу. Криовоздействие продолжают до испарения хладагента из пор рабочего элемента. Пластичность держателя позволяет придавать ему форму, удобную для подведения к месту воздействия.
Недостатком устройства является неудобство его применения для лечения рубцового стеноза трахеи. Этому препятствует ряд факторов: сложность проведения к участку воздействия, трудность манипуляции в узком просвете, испарение значительной части хладагента за время проведения. В значительной степени эти факторы обусловлены сложностью конфигурации области вмешательства: входное отверстие трахеостомы ориентировано приблизительно под прямым углом к оси трахеи. Криоаппликатор приходится проводить по сильно искривленной траектории. Кроме того, существует большая вероятность примораживания по пути проведения. При случайном касании ткани прилипают к боковой поверхности аппликатора, что вынуждает или дожидаться отогревания, или производить отрыв; в обоих случаях ткани получают дополнительное повреждение. Постепенное и осторожное подведение апликатора к участку воздействия влечет потерю значительной части хладагента, в результате манипуляцию приходится повторять многократно, что повышает риск вышеуказанного прилипания,
Сущность изобретения
Технический результат, достигаемый предлагаемым изобретением, состоит в повышении удобства подведения криоаппликатора к области криовоздействия и снижении травматизма за счет исключения прилипания аппликатора к тканям в процессе подведения к дефекту.
Указанный технический результат достигается тем, что известное устройство для хирургического лечения стеноза трахеи в виде криоаппликатора, содержащего закрепленный на держателе из пластичного никелида титана цилиндрический контактный наконечник, выполненный из пористого проницаемого никелида титана с коэффициентом пористости 30-70%, снабжено направителем в виде жесткой трубки, плавно изогнутой на угол 80-100o с отношением радиуса изгиба по средней линии к внутреннему диаметру в пределах 2,5-5, при этом торцы контактного наконечника сферически сглажены, а на его боковой поверхности имеется слой с коэффициентом пористости 3-5% и шероховатостью не менее 2,5.
На чертеже показано устройство для хирургического лечения стеноза трахеи
Сведения, подтверждающие возможность осуществления изобретения.
Снабжение криоаппликатора трубчатым направителем обеспечивает его проведение к зоне криовоздействия без риска примораживания к тканям при случайном касании. Это исключает дополнительную травматизацию тканей в результате примораживания при случайном касании.
Изгиб направителя под углом 80-100o обеспечивает его соответствие анатомическому строению области воздействия, поскольку трахеостомическое отверстие своей осью ориентировано приблизительно перпендикулярно оси трахеи.
Жесткость направителя обеспечивает адекватную конфигурацию пути проведения криоаппликатора за счет того, что пластичный держатель изгибается соответственно кривизне направителя именно благодаря жесткости последнего. Кроме того, решение в пользу жесткого направителя обусловлено тем, что, например, эластичный направитель под действием сверхнизких температур способен к неконтролируемой деформации.
Выбор отношения радиуса изгиба трубчатого направителя по его средней линии к внутреннему диаметру в пределах 2,5-5 обусловлен следующими соображениями. Внутренний диаметр и радиус изгиба направителя должны обеспечивать свободное прохождение контактного наконечника внутри направителя. Математически соотношение радиуса изгиба по средней линии R и внутреннего диаметра D должно соответствовать формуле
R2≥L2/8(D-d),
где L - длина, d - диаметр контактного наконечника. Типичные размеры наконечника составляют: диаметр 8 мм, длина 20 мм. Типичная величина внутреннего диаметра трубчатого направителя составляет 10 мм. При этих условиях радиус изгиба согласно формуле должен быть не менее 25 мм, или 2,5D. Выбор верхнего предела радиуса изгиба определяется требованием удобства применения. При радиусе, превышающем 50 мм, то есть 5D, направитель не вписывается в область перехода от трахеостомы к трахее, что создает излишнее давление на ее стенки, кроме того, увеличение общей длины направителя замедляет процесс проведения наконечника к области воздействия, тем самым снижая ресурс криовоздействия.
Выполнение торцов контактного наконечника сферически сглаженными исключает заклинивание контактного наконечника при его проведении по направителю, а также предотвращает травматизацию стенки трахеи при любых манипуляциях с наконечником.
Наличие на боковой поверхности аппликатора слоя с уменьшенной до 3-5% пористстью обеспечивает замедленное испарение хладагента, увеличивая продолжительность криовоздействия. Это существенно для проведения аппликатора к труднодоступной зоне. Верхний предел диапазона пористости поверхностного слоя определяется достижением достаточного для целей операции замедления испарения. Нижний предел диапазона обеспечивает скорость поступления хладагента к поверхности, достаточную для осуществления криовоздействия на заданный участок.
Выбор шероховатости покрытия боковой поверхности не менее 2,5 обеспечивает беспрепятственное скольжение аппликатора вдоль направителя.
Таким образом, сочетание заявленных признаков повышает удобство проведения криоаппликатора, сокращает время манипуляции, что имеет существенное значение, так как операция связана с блокированием дыхательных путей, и значительно снижает травматичность.
На чертеже изображено устройство для хирургического лечения стеноза трахеи. Устройство содержит криоаппликатор в виде цилиндрического пористого контактного наконечника 1, выполненного из пористого никелида титана с закрепленным на торце пластичным держателем 2 и жесткий направитель 3 в виде изогнутой под углом 80-100 градусов трубки. Торцы 4 пористого никелид-титанового наконечника 1 выполнены сферически сглаженными. На боковой поверхности наконечника 1 имеется слой 5 с пониженной в сравнении с материалом наконечника пористостью - в диапазоне 3-5% - и с уменьшенной шероховатостью - не менее 2,5. Внутренний диаметр и радиус изгиба направителя 3 согласованы с размерами контактного наконечника, так чтобы последний при продольном продвижении вписывался в сечение направителя. Типичные размеры наконечника составляют: диаметр 8 мм, длина 20 мм. При этом, например, если внутренний диаметр трубчатого направителя составляет D=10 мм, радиус изгиба согласно вышеприведенной формуле должен превышать 25 мм, или 2,5D. В то же время для удобства применения радиус изгиба выбран не более 50 мм, то есть не более 5D.
Устройство применяют следующим образом. Держатель 2 деформируют при комнатной температуре до придания ему необходимой для работы формы, отвечающей предполагаемой анатомической области криовоздействия. Трубчатый направитель 3 устанавливают в отверстие трахеостомы, помещая его край на уровне дистальной границы стенозированного участка. В качестве направителя может быть использована подходящая по размерам трахеостомическая трубка. Цилиндрический контактный наконечник 1 погружают в хладагент, например жидкий азот. Пористость материала обеспечивает наполнение его в течение 3-5 с, критерием чего является прекращение выделения пузырьков над поверхностью наконечника. После этого, манипулируя держателем, цилиндрический контактный наконечник вводят через направитель на необходимую глубину и прижимают к стенке трахеи в области грануляций, локализацию и распространение которых устанавливают во время предварительной трахеобронхоскопии. Стенки направителя препятствуют контакту наконечника с тканями на пути проведения, исключая случайное примораживание. Продолжительность криовоздействия определяется скоростью испарения хладагента из пор наконечника и, как правило, составляет 8-10 с. Время воздействия определяется испарением хладагента и отогреванием тканей, после чего криоаппликатор легко вынимается. Оттаивание определяется появлением подвижности при попытке смещения инструмента (при попытке извлечения аппликатора раньше наступления оттаивания происходит механическое повреждение тканей в месте примораживания, сопровождающееся нежелательным кровотечением). Зона промораживания может контролироваться макроскопически при помощи трахеобронхоскопии. При необходимости манипуляцию повторяют в указанной последовательности, подвергая криовоздействию последовательно всю поверхность грануляционного стеноза. Манипуляции повторяют через день в количестве 5-8 раз, что зависит от степени выраженности и распространенности стеноза, а также макроскопической картины динамики течения заболевания.
Дополнительным преимуществом предлагаемого устройства является возможность применения его не только для лечения сформировавшегося стеноза, но и для профилактики стеноза путем криообработки проблемных участков трахеи, например участков, подвергавшихся механической травматизации во время оперативного вмешательства.
Клинический пример.
Больной М., 31 года, история болезни 259, с 24.02.99 по 02.04.99 находился на лечении в госпитальной хирургической клинике им. А.Г. Савиных Сибирского государственного медицинского университета по поводу субкомпенсированного (В.К. Трутнев, А.И. Юнина, 1960 г.) постинтубационного стеноза шейного отдела трахеи. В анамнезе тяжелая сочетанная черепно-мозговая травма, полученная в результате ДТП в одном из районов области около 1 года назад. В период лечения травмы потребовалось проведение продленной искусственной вентиляции легких, для чего была наложена трахеостома. В дальнейшем дважды производилась реконструкция трахеостомы, несмотря на это предотвратить развитие стеноза трахеи не удалось. При поступлении: одышка при минимальной физической нагрузке, во время разговора вынужден многократно останавливаться, для предотвращения удушья во время сна приспособился самостоятельно вводить укороченную интубационную трубку с наружным диаметром до 5 мм. При попытке выполнения фибротрахеобронхоскопии ниже дистального края трахеостомического отверстия отмечено концентрическое сужение трахеи, которое явилось препятствием для дальнейшего осмотра бронхофиброскопом диаметром 5,5 мм. На выполненных рентгенотомограммах протяженность стеноза составила 4,5-5 см. Далее в течение 10 дней 1 раз в день проводилось бужирование стеноза набором стандартных пищеводных бужей номерами от 10 до 34, ежедневно увеличивая размер бужа на 2-4 номера. Каждый раз бужирование заканчивалось установлением специально укороченной интубационной трубки соответствующего диаметра. Максимальный диаметр последней после завершения бужирования равнялся 10,5 мм. При повторной трахеобронхоскопии установлено, что имеет место рубцово-грануляционный стеноз, циркулярно поражающий стенку трахеи ниже дистального края трахеостомического отверстия протяженностью на длине до 5 см. С использованием вышеописанного устройства проведено 8 сеансов криовоздействия, каждый из которых завершался установлением укороченной интубационной трубки с наружным диаметром 10 мм, обработанной снаружи с противовоспалительной целью 0,5% преднизолоновой мазью. Повторная госпитализация для контрольного обследования осуществлена 06.04.99, история болезни 435. При проведении трахеобронхоскопии на переднелевой стенке трахеи выявлен участок грануляций размером 0,5х1,5 см, располагавшийся на расстоянии около 1,5 см от нижнего края отверстия трахеостомы. Во всех остальных отделах стенки трахеи покрыты эпителием. Проведено дополнительно 5 сеансов криовоздействия по описанной выше методике и в удовлетворительном состоянии 23.04.99 больной был выписан из клиники. При проведении контрольных амбулаторных осмотров через 3, 6 и 12 месяцев признаков рецидива заболевания выявлено не было, и в мае 2000 года в ЛОР-отделении клиник НИИ онкологии ТФ СО РАМН выполнено пластическое закрытие трахеостомического отверстия.
Источники информации
1. Потапов И.И., Рудня ПК., Тарлычева Л.С., Шеврыгин Б.В. Криохирургия в отоларингологии. М.: Медицина, 1975 - 168 с.
2. Русаков М. А. Криохирургия трахеи и бронхов (обзор литературы). Грудная хирургия, 1981, 5, с. 66-71.
3. Авторское свидетельство СССР 1616628, МКИ А 61 В 17/36. Криогенный аппликатор. Малеткина Т.Ю., Староха А.В., Гюнтер В.Э., Сысолятин П.Г., Котенко В.В., Пархоменко Г.С., Миргазизов М.З., Зиганьшин Р.В., Попович В.И.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РУБЦОВОГО СТЕНОЗА ТРАХЕИ С ПОМОЩЬЮ ВЫСОКОЧАСТОТНОГО ХИРУРГИЧЕСКОГО АППАРАТА С ЭФФЕКТОМ РАДИОВОЛНЫ И АРГОН-УСИЛЕННОЙ ПЛАЗМЕННОЙ КОАГУЛЯЦИИ | 2009 |
|
RU2442547C2 |
| СПОСОБ ОБРАБОТКИ КУЛЬТИ ГЛАВНОГО БРОНХА | 2004 |
|
RU2271155C2 |
| КРИОХИРУРГИЧЕСКИЙ ЭПИКАРДИАЛЬНЫЙ АППЛИКАТОР | 2012 |
|
RU2514726C1 |
| КОСТНЫЙ ИМПЛАНТАТ | 1998 |
|
RU2157151C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭКСПИРАТОРНОГО СТЕНОЗА ТРАХЕИ И ГЛАВНЫХ БРОНХОВ | 2009 |
|
RU2376949C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ПРОТЯЖЕННОГО ЦИРКУЛЯРНОГО ДЕФЕКТА ТРАХЕИ | 2011 |
|
RU2449740C1 |
| ЭНДОСКОПИЧЕСКИЙ КРИОАППЛИКАТОР | 2011 |
|
RU2462208C1 |
| СПОСОБ ЗАКРЫТИЯ ДЕФЕКТА ТРАХЕИ И УСТРОЙСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ ПЕРВОГО ЭТАПА СПОСОБА | 2002 |
|
RU2230529C2 |
| СПОСОБ КРИОДЕСТРУКЦИИ ОПУХОЛЕЙ НАДПОЧЕЧНИКОВ | 2011 |
|
RU2477625C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ЦИРКУЛЯРНЫХ ДЕФЕКТОВ ТРАХЕИ | 2010 |
|
RU2445008C1 |
Изобретение относится к медицине, а именно к области хирургического лечения постинтубационных и посттрахеостомических стенозов шейного отдела трахеи при помощи криовоздействия. Устройство содержит криоаппликатор в виде закрепленного на держателе из пластичного никелида титана цилиндрического контактного наконечника, выполненный из пористого проницаемого никелида титана с коэффициентом пористости 30-70%, направитель в виде жесткой трубки, плавно изогнутой на угол 80-100o с отношением радиуса изгиба по средней линии к внутреннему диаметру в пределах 2,5-5. Торцы контактного наконечника сферически сглажены, а на его боковой поверхности имеется слой с пористостью 3-5% и шероховатостью не менее 2,5. Изобретение позволяет повысить удобство проведения криоаппликатора к области криовоздействия и снизить травматизм за счет исключения прилипания аппликатора к тканям в процессе подведения к дефекту. 1 ил.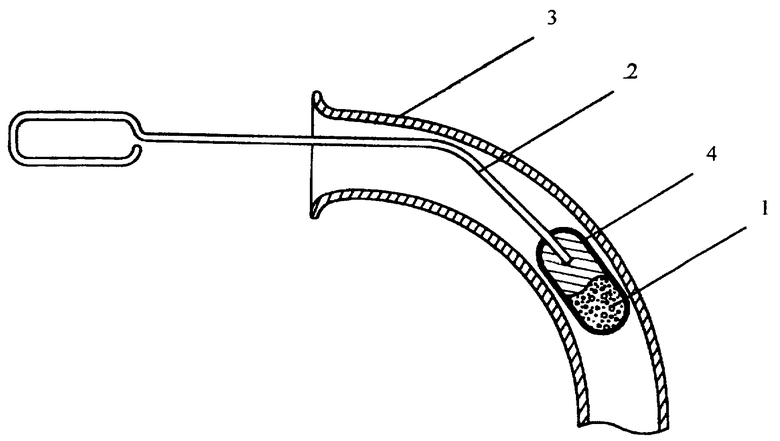
Устройство для хирургического лечения стеноза трахеи, содержащее криоаппликатор в виде закрепленного на держателе из пластичного никелида титана цилиндрического контактного наконечника, выполненного из пористого проницаемого никелида титана с коэффициентом пористости 30÷70%, отличающееся тем, что оно снабжено направителем в виде жесткой трубки, плавно изогнутой на угол 80÷100°с отношением радиуса изгиба по средней линии к внутреннему диаметру в пределах 2,5÷5, при этом торцы контактного наконечника сферически сглажены, а на его боковой поверхности имеется слой с пористостью 3÷5% и шероховатостью не менее 2,5.
| SU 1616628 A1, 30.12.1990 | |||
| Грудная хирургия | |||
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| Потапов И.И | |||
| и др | |||
| Криохирургия в отоларингологии | |||
| - М.: Медицина, 1975, с.44-52. | |||
Авторы
Даты
2004-01-20—Публикация
2001-10-08—Подача