Изобретение относится к биотехнологии и, в частности, к генетической инженерии и представляет собой фрагмент ДНК, кодирующий полную аминокислотную последовательность L-аспарагиназы Erwinia carotovora, и рекомбинантную плазмидную ДНК pBADLANS, обуславливающую синтез L-аспарагиназы Erwinia carotovora (ECAR-LANS) в клетках Escherichia coli.
Изобретение может найти применение в микробиологической промышленности и медицине, в частности для создания новых противоопухолевых средств.
Бактериальные аспарагиназы - хорошо известные ферментные препараты, которые на протяжении более 30 лет используются в противоопухолевой терапии для лечения острых лимфобластных лейкозов /1/. Эффективность применения аспарагиназ в противоопухолевой терапии ограничена развитием иммунного ответа на вводимые препараты /2/. В этой связи, для проведения необходимых курсов комбинированной химио- и энзимотерапии лейкозов целесообразно располагать набором L-аспарагиназ, обладающих высокой ферментативной активностью, но отличающихся по своим антигенным свойствам. Дополнительные возможности для направленного изменения ферментативных и иммунологических свойств L-аспаргиназ открываются с применением методов генетической инженерии /3/. Этими обстоятельствами определяется интерес к клонированию новых генов бактериальных L-аспарагиназ и их модификации путем сайт-направленного мутагенеза и гетерологичной экспресии.
К настоящему времени известны первичные структуры генов бактериальных Erwinia chryzantemi /4/, Escherichia coli /5/, Wolinella succinogenes /6/ и ряда других микроорганизмов, а также описаны рекомбинантные плазмидные ДНК, обеспечивающие синтез L-аспарагиназ в клетках бактерий Escherichia coli /7/ и Erwinia carotovora /8/. Первичная структура гена L-аспарагиназы Erwinia carotovora ранее не была известна, равно как и не описано получение рекомбинантных штаммов, обуславливающих синтез этого фермента.
Целью предлагаемого изобретения является клонирование гена ECAR-LANS и получение рекомбинантного штамма бактерий, продуцирующего биологически активную ECAR-LANS с высоким выходом. Поставленная цель достигается тем, что осуществлено выделение фрагмента ДНК штамма Erwinia carotovora, кодирующего полную аминокислотную последовательность гена ECAR-LANS, а также тем, что сконструирована рекомбинантная плазмидная ДНК pBADLANS, обеспечивающая синтез ECAR-LANS в клетках кишечной палочки.
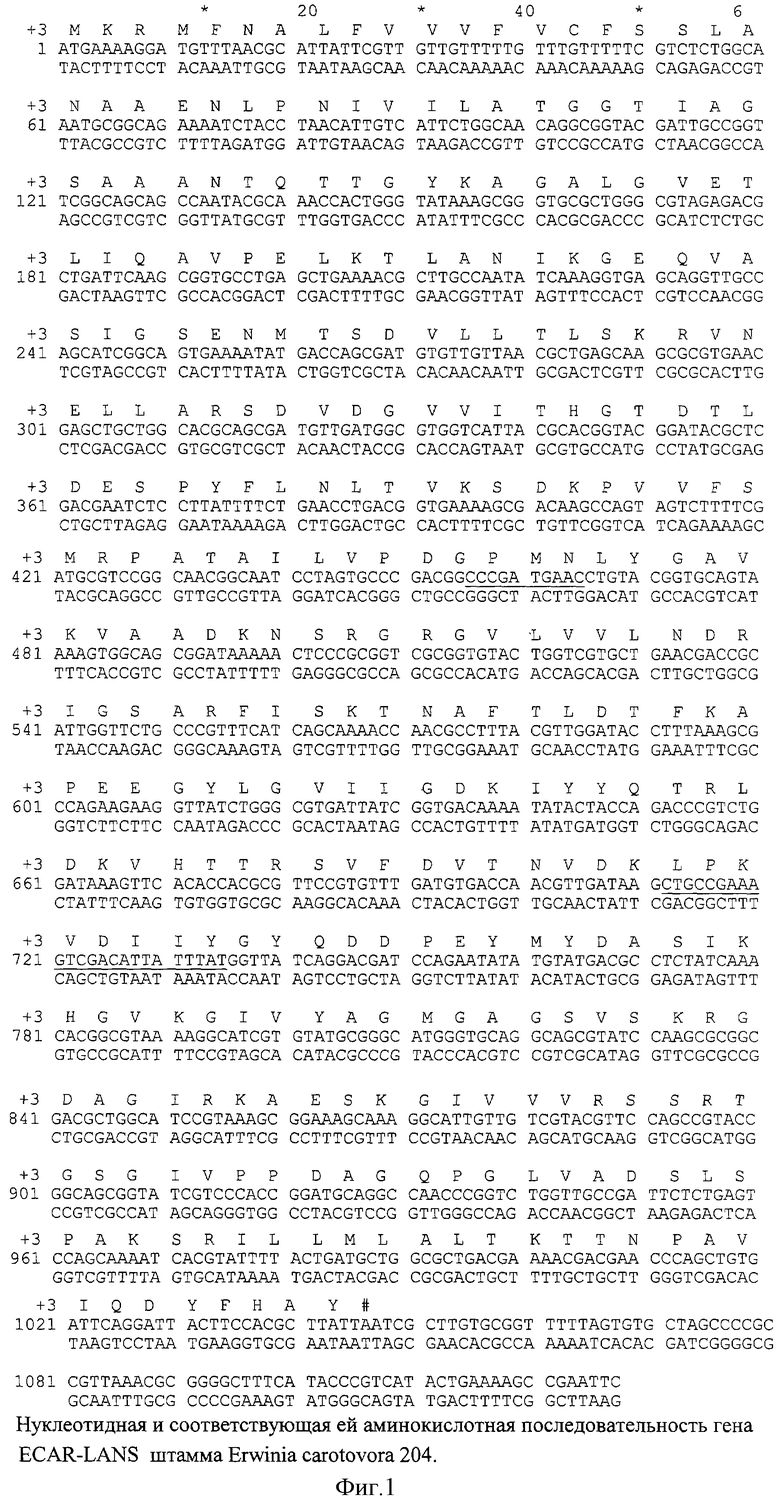
Сущность модифицированного гена ECAR-LANS состоит в том, что он имеет нуклеотидную последовательность, указанную на фиг.1, которая кодирует синтез белка ECAR-LANS с аминокислотной последовательностью, указанной на той же фигуре.
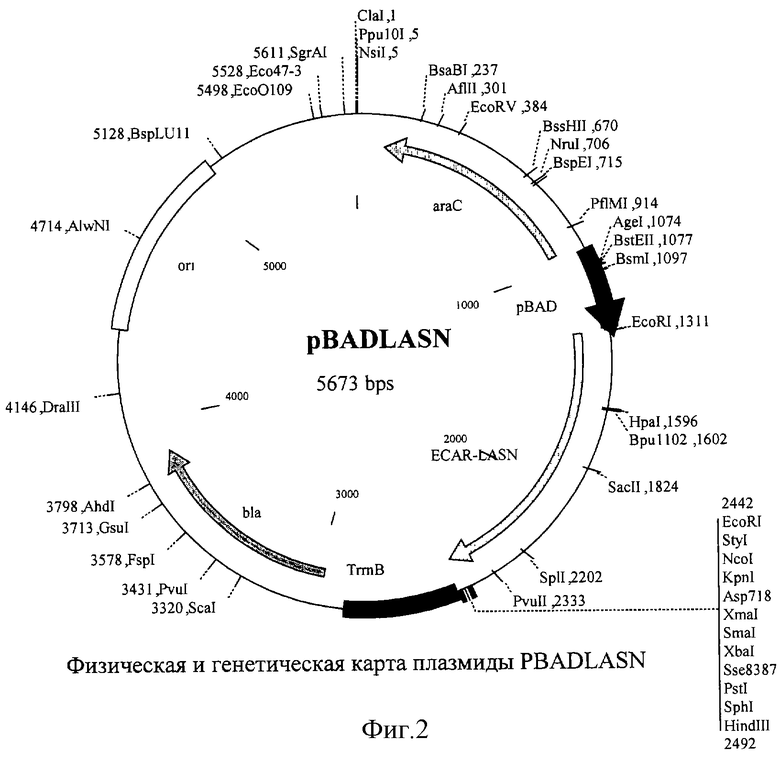
Сущность рекомбинантной плазмиды pBADLANS, чья рестрикционная и генетическая карта представлена на фиг.2, состоит в том, что она содержит фрагмент природного гена ECAR-LANS, встроенный в состав экспрессионного дрожжевого вектора pBAD24. Плазмида pBADLANS состоит из следующих элементов:
- фрагмента EcoRI размером 4,5 тпн плазмиды pBAD24 /9/,
- фрагмента EcoRI размером 1,1 тпн, несущего ген ECAR-LANS.
Молекулярный вес плазмиды pBADLANS составляет 3,5 Мд, что соответствует размеру в 5,6 тпн.
Число копий полученной плазмиды составляет 50-100 на клетку кишечной палочки.
Плазмида pBADLANS реплицируется в клетках E. coli за счет репликона pUC18. Синтез ECAR-LANS в клетках в трансформированных плазмидой pBADLANS штаммах E. coli осуществляется под контролем регулируемого промотора pBAD и терминатора rrnBTIT Escherichia coli и достигается при культивировании трансформированного штамма на обычных селективных средах при добавлении L-арабинозы до концентрации 0,2%.
Плазмида PBADLANS содержит гены:
- модифицированный природный ген ECAR-LANS, который кодирует синтез этого белка в бактериальной клетке. Этот ген, введенный по месту расщепления EcoRI, имеет нуклеотидную последовательность, показанную на фиг.2. Эта последовательность кодирует полноразмерный предшественник ECAR-LANS с собственным сигнальным пептидом для экспорта белка в периплазму и последующего процессинга;
- blа-ген, обеспечивающий синтез b-лактамазы и влияющий на устойчивость штаммов E.coli, несущих плазмиду, к ампициллину;
- аrаС-ген, являющийся регулятором промотора pBAD.
Штамм-продуцент ECAR-LANS получают трансформацией клеток Escherichia coli BL21(DE3) /10/ [F-, ompT, hsdSB (rв-, mв-), dcm, gal, λ (DE3), AmpR] предложенной рекомбинантной плазмидной ДНК. Выбор штамма обусловлен тем, что он несет, а также тем, что он дефектен по синтезу протеаз, что существенно влияет на выход синтезируемых гетерологичных белков.
Полученный после селекции трансформированный клон BL21/pBADLANS способен при культивировании продуцировать ECAR-LANS. Уровень синтеза ECAR-LANS в сконструированном штамме составляет мг/л при титре культуры 1х109 кл/мл, что следует из данных определения ECAR-LANS в образцах биомассы штамма-продуцента с помощью специфической ферментативной реакции.
Полученный штамм бактерий, несущий плазмиду PBADLANS, характеризуется следующими общими признаками.
Морфологические признаки: Клетки имеют продолговатую палосковидную форму, при делении не почкуются.
Культуральные признаки: Клетки хорошо растут на обычно используемых питательных средах. Время генерации около 30 мин в жидкой LB-среде. На 2-2,5% питательном агаре "Difco" образуются круглые, гладкие, желтоватые колонии с ровными краями. При выращивании на жидких LB- и YT-средах образуется интенсивная ровная мутность.
Физиолого-биохимические признаки: Оптимальная температура культивирования - от 35 до 37oС, оптимум рН 7,6.
Источником азота служат органические соединения (в виде триптона, дрожжевого экстракта).
Штамм депонирован во Всероссийской коллекции промышленных микроорганизмов под номером ВКПМ.
Способ клонирования гена ECAR-LANS и получения рекомбинантной плазмиды pBADLANS иллюстрируется следующими примерами.
Пример 1. Выделение центрального фрагмента гена ECAR-LANS
Для клонирования гена ECAR-LANS использовали стратегию, основанную на методе инвертированной полимеразной цепной реакции" ("инвертированной ПЦР, 1) и схематически приведенную на фиг.3.
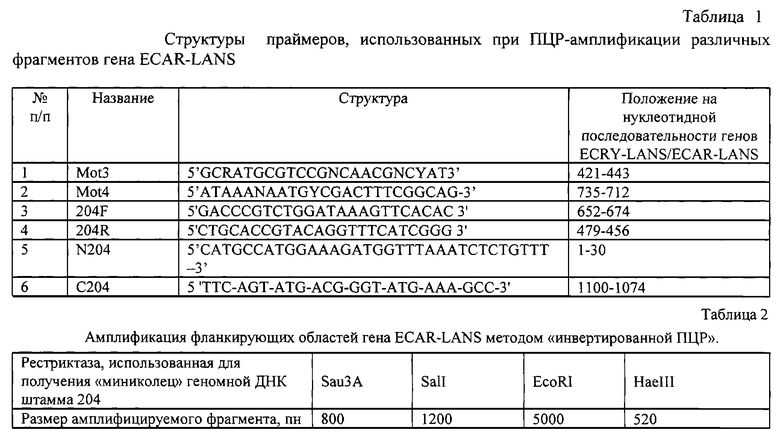
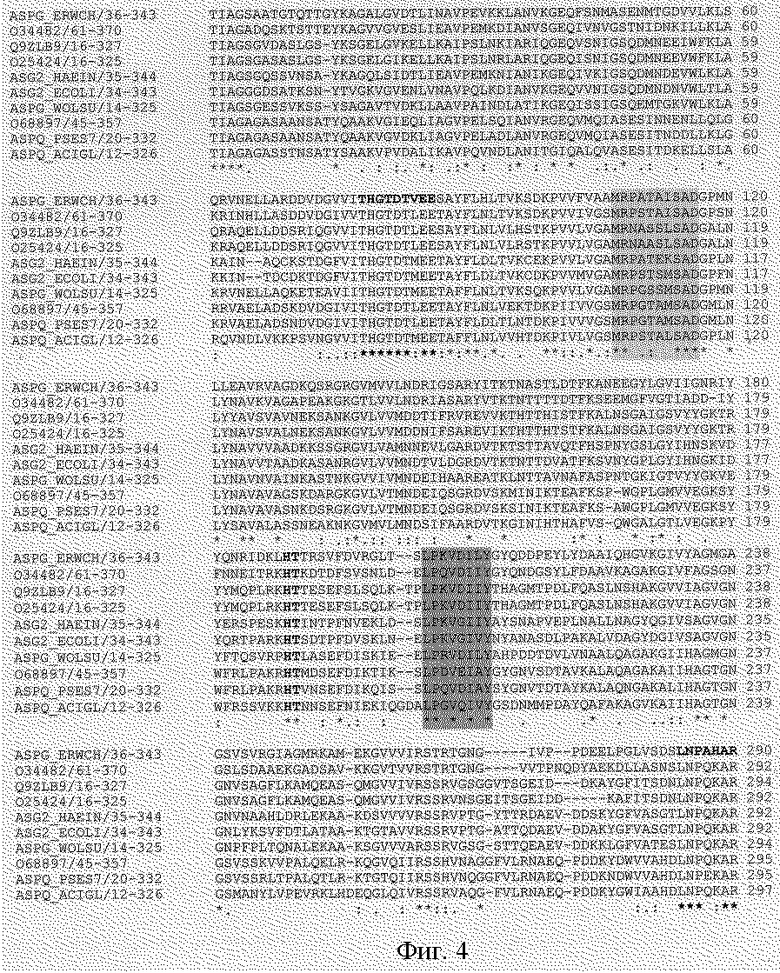
На первом этапе проводили сравнение аминокислотных и нуклеотидных последовательностей бактериальных L-аспарагиназ с использованием информации, доступной с помощью Интернет на сайте Сэнгер Центра в Великобритании /11/, а также на сайте Национального Центра Биотехнологической Информации США /12/. С помощью программы CLUSTAL Х /13/ были выявлены наиболее консервативные участки L-аспарагиназ бактериального происхождения (фиг.4) и синтезированы два синтетических олигонуклеотида Mot3 и Mot4, структура и свойства которых приведены в таблице 1. Эти олигонуклеотиды использовали в качестве праймеров в ПЦР с образцами геномной ДНК, выделенными общепринятым способом /14/ из различных штаммов ервиний, находившихся в лабораторной коллекции. ПЦР проводили с помощью Taq-ДНК полимеразы производства Fermentas (Вильнюс) в соответствии с инструкциями фирмы-изготовителя на приборе MJ-Research в следующих условиях: первоначальный прогрев - 2 мин, 94, затем 25 циклов амплификации - 94, 40". 50, 40". 72, 40". Объем реакционной смеси составлял 50 мкл, концентрация праймеров - 0,5 мкм, концентрация ДНК - 20 нг/мкл. В образцах ДНК, выделенных из штаммов ервиний, условно обозначенных 1А, 2А, 204, идентифицировали продукт реакции размером около 300 пн. ПЦР фрагмент, полученный на ДНК штамма 204, использовали в дальнейшей работе. Фрагмент был клонирован в вектор pT-Adv (Clontech, USA) в соответствии с инструкциями фирмы-изготовителя и его нуклеотидная последовательность определена путем автоматического секвенирования на приборе ABI 373 DNA Sequencer с использованием набора Perkin-Elmer "fluorescent dye Cycle sequencing kit". Сравнение полученной нуклеотидной последовательности с последовательностью ДНК гена LANS Erw. chrysanthemi (GenBank Acc# A 14577, ECRY-LANS) показало, что уровень гомологии между выделенным фрагментом и соответствующим центральным фрагментом гена ECRY-LANS составляет 85% (фиг.4). Таким образом, полученный фрагмент с высокой вероятностью соответствует центральной части искомого гена ECAR-LANS.
Пример 2. Определение кодирующей последовательности гена ECAR-LANS
Для выделения и определения первичной структуры фланкирующих участков гена ECAR-LANS, перекрывающих кодирующую аминокислотную последовательность данного белка, использовали стратегию "инвертированной ПЦР". На основании данных секвенирования центральной части гена ECAR-LANS штамма 204 провели дизайн двух праймеров - 204F и 204R, структура и положение которых указаны в таблице 2 и на фиг.5.
Препараты геномной ДНК штамма 204 в количестве 2-4 мкг гидролизовали различными рестрикционными эндонуклеазами - BamHI, BglII, Bspl201, EcoRI, НаеIII, HindIII, KpnI, PstI, SalI, Sau3A, SpeI, Xba, XhoI по отдельности либо в комбинации двух ферментов, образующих после расщепления ДНК с идентичными "липкими концами", например BamHI+BglII, SalI+XhoI, XbaI+SpeI. После инкубации в течение 10-16 часов при нужной температуре присутствующие в смеси рестрикционные эндонуклеазы инактивировали прогреванием (10-15 мин при 65 градусах), добавляли 1/10 объема раствора, содержащего 100 мМ ДТТ и 10 мМ АТФ, 1-2 единицы Т4 ДНК-лигазы и инкубировали еще 10-12 часов при +4 градусах. Полученные образцы депротеинизировали обработкой смесью фенола с хлороформом (1: 1) и осаждали спиртом по общепринятым методикам /14/. ДНК растворяли в объеме 50 мкл и 10-15 мкл использовали в реакции ПЦР с праймерами 204F/204R, которую проводили с использованием Taq-полимеразы, либо набора Expand Long Template PCR system (Roche Diagnostics GmBh, Mannheim, Германия). Условия ПЦР и характеристики полученных продуктов приведены в таблице 2.
Образцы, полученные на матрицах Sau3A, HaeIII, EcoRI, SalI выделяли из агарозного геля с помощью набора "Wizard PCR prep purification system" производства Promega (США) в соответствии с инструкцией фирмы изготовителя и определяли их нуклеотидную последовательность путем автоматического секвенирования на приборе ABI 373. DNA Sequencer. В качестве праймеров использовали синтетические олигонулеотиды 204F и 204R. Полная последовательность была восстановлена путем построения "контига" с использованием программы Oligo /15/. Сравнение полученной последовательности со структурой гена ECRY-LANS показало, что уровень гомологии между данными последовательностями составляет 85% (фиг.6). На фиг.1 приведены нуклеотидная последовательность и выведенная из нее полная аминокислотная последовательность гена ECAR-LANS. Сравнение аминокислотных последовательностей ECAR-LANS и ECRY-LANS (фиг.7) подтвердило высокую степень гомологии между двумя белками. Степень идентичности составила 72%, степень сходства - 87%.
Пример 3. Выделение и клонирование фрагмента нуклеотидной последовательности гена ECAR-LANS, кодирующего полную аминокислотную последовательность этого белка.
Препарат геномной ДНК штамма 204 использовали в ПЦР реакции с олигонуклеотидами N204 и С204, структура и специфичность которых приведены в таблице 1. Использованные праймеры ограничивают фрагмент гена ECAR-LANS, включающий инициаторный кодон трансляции ATG, расположенный в положении + 1 последовательности, указанной на фиг.6, и терминаторный кодон ТАА, расположенный в положении + 1045 той же последовательности. Таким образом, полноразмерный специфичный продукт реакции амплификации должен включать полную кодирующую последовательность гена ECAR-LANS. Использовали следующие условия амплификации: начальная денатурация - 94, 2 мин, затем 30 циклов амплификации - 94, 40 с, 50, 40 с, 72,1 мин 30 с. Реакционную смесь разделяли электрофорезом в 1% агарозном геле и выявляли продукт реакции - единичный фрагмент размером около 1100 пн. Фрагмент выделяли из геля с помощью набора "Wizard PCR preps Purification System" (Promega, США) и клонировали в вектор pT-AdV (Clontech, США), как описано в примере 1. Из полученных индивидуальных клонов трансформантов выделяли плазмидную ДНК по стандартной методике и анализировали ее путем гидролиза рестриктазой EcoRI и разделения продуктов реакции в 1% агарозном геле. Поскольку сайты рестриктазы EcoRI фланкируют с двух сторон место клонирования ПЦР-фрагмента в векторе pT-AdV, то появление в EcoRI-гидролизатах исследуемых плазмидных ДНК фрагмента размером около 1 тпн свидетельствует о наличии в рекомбинантных клонах нужной вставки. Всего отобрали 12 клонов, "положительных" по этому тесту, и использовали их в дальнейшей работе. Для доказательства того, что полученные клоны содержат фрагмент гена ECAR-LANS плазмидную ДНК использовали в "проверочных ПЦР-реакциях" с использованием комбинаций праймеров, указанных в таблице 3. Наличие продуктов ПЦР-реакции с характерными размерами, указанным в таблице 3, подтвердило, что полученные клоны содержат искомый фрагмент.
Пример 4. Конструирование рекомбинантной плазмиды pBADLANS для экспрессии ECAR-LANS в клетках Escherichia coli.
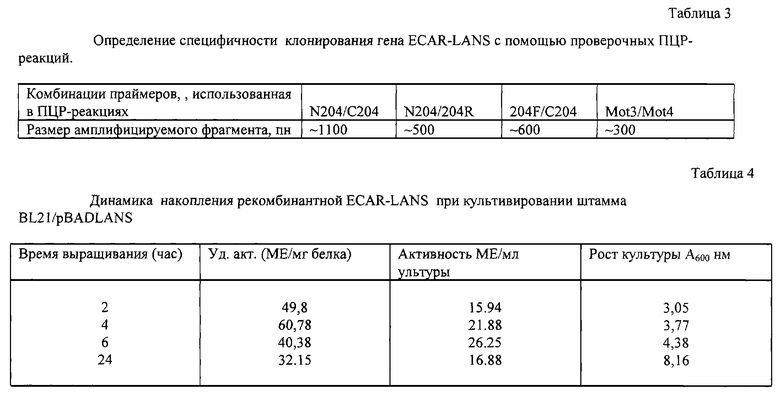
Для доказательства того, что клонированные в п.3. фрагменты ДНК способны направлять синтез функционально-активной ECAR-LANS в клетках кишечной палочки, осуществляли конструирование плазмид, содержащих фрагмент гена ECAR-LANS под контролем промотора PBAD вектора pBAD24. Для получения "вставки" по 2 мкг ДНК каждого из 12 "положительных" клонов, отобранных согласно процедуре, описанной в п. 3., объединяли в одной пробирке и проводили гидролиз суммарной ДНК рестриктазой EcoRI. Выделяли из агарозного геля "суммарный" EcoRI-фрагмент размером около 1 тпн, соответствующий фрагменту гена ECAR-LANS. Для получения "вектора" 2 мкг плазмидной ДНК pBAD24 линеаризовали по сайту EcoRI, обрабатывали фосфатазой кишки теленка для предотвращения замыкания вектора "сам на себя" и выделяли из агарозного геля фрагмент размером 4,5 тпн. 20 нг "вектора" лигировали с 50 нг "фрагмента" с помощью Т4 ДНК лигазы в стандартных условиях и смесью трансформировали компетентные клетки штамма E.coli XL1. Индивидуальные клоны трансформантов анализировали на способность направлять синтез функционально-активной ECAR-LANS. Для этого отдельные колонии (30 штук) выращивали на LB-среде, содержащей 100 мкг/мл ампициллина до ОП600 ~ 1,0 в объеме 5 мл. После этого в культуры вносили L-арабинозу до конечной концентрации 0,2% для индукции промотора pBAD и продолжали инкубацию в течение 2 часов. Аликвоты суспензии клеток выросших индивидуальных культур трансформантов использовали для определения L-аспарагиназной активности с помощью разработанного для этой цели микрометода. В основе данного метода лежит периплазматическая локализация экспрессируемой в клетках E.coli ECAR-LANS, благодаря чему субстрат (аспарагин) свободно проникает в клетку и взаимодействует с ферментом. Суспензии клеток (50 мкл) помещали в ячейку 96-луночной плашки и инкубировали (37oС; 20 мин) с 50 мкл L-аспарагина (30 мг/мл в 0,0125 М боратном буфере, рН 9,5). По окончании инкубации в лунки добавляли 50 мкл реактива Несслера. Активность аспарагиназы оценивается визуально по интенсивности развивающегося окрашивания. Контрольные пробы содержат либо бактериальные клетки, либо раствор L-аспарагина. Таким образом, из 30 проанализированных клонов было выявлено 5 "положительных". Отобранные положительные клоны дополнительно анализировали на наличие вставки с фрагментом гена ECAR-LANS. Для этого выделяли плазмидную ДНК, гидролизовали ее рестриктазой EcoRI и выявляли наличие продуктов гидролиза размером 4.5 тпн ("вектор") и 1.1 тпн ("фрагмент"). Один из отобранных клонов вводили путем трансформации в штамм E.coli BL21(DE3). Для количественного определения уровня экспрессии ECAR-LANS в полученных рекомбинантных штаммах отдельные клоны трансформантов BL21(DE3)/pBADLANS выращивали на LB среде в объеме 50 мл в колбах объемом 500 мл при температуре 37oС А600 = 0,6-0,7 ОЕ. Далее вносили индуктор - L-арабинозу до концентрации 0,2% и проводили инкубацию еще в течение 22 часов, отбирая периодически пробы культуральной жидкости для определения роста культуры и активности фермента в бактериальных клетках /16/. Полученные данные обобщены в таблице 4. Как видно из представленных данных, удельная активность фермента достигает максимума около 55 МЕ/мг белка через 4 часа инкубации, что примерно в 50-60 раз выше, чем у исходного дикого штамма Erw.carotovora 204. Таким образом, в этих экспериментах был достигнут достаточно высокий уровень экспрессии рекомбинантной аспарагиназы Erw.carotovora (8-10%) от тотального белка клетки. Сопоставление полученных данных с известными ранее литературными сведениями о характеристиках рекомбинантных штаммов E.coli, продуцирующих бактериальные аспарагиназы, позволяет утверждать, что уровень продукции рекомбнантной ECAR-LANS в созданном нами штамме примерно в 1,5 раза превышает продуктивность лучших из ранее разработанных образцов /8/. Физическая и генетическая карта полученной плазмиды приведена на фиг.2.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PACYCLANS ДЛЯ ПЕРЕНОСА И ЭКСПРЕССИИ В КЛЕТКАХ ESCHERICHIA COLI ГЕНА L-АСПАРАГИНАЗЫ ERWINIA CAROTOVORA (ECAR-LANS) И СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОЙ ECAR-LANS ИЗ БИОМАССЫ ШТАММА E.COLI-ПРОДУЦЕНТА | 2002 |
|
RU2224797C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pACYC-LANS(KM), ШТАММ Escherichia coli BL21(DE3), ТРАНСФОРМИРОВАННЫЙ РЕКОМБИНАНТНОЙ ДНК pACYC-LANS(KM), И СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОЙ L-АСПАРАГИНАЗЫ Erwinia carotovora | 2010 |
|
RU2441916C1 |
| Модифицированный ген рас бактерий Escherichia coli, кодирующий предшественник фермента с активностью пенициллин G ацилазы, рекомбинантный штамм Escherichia coli - продуцент пенициллин G ацилазы и способ микробиологического синтеза этого фермента | 2015 |
|
RU2624022C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБСТАНЦИИ РЕКОМБИНАНТНОЙ L-АСПАРАГИНАЗЫ ERWINIA CAROTOVORA | 2010 |
|
RU2441914C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА pETTvDAO2, ОБЕСПЕЧИВАЮЩАЯ СИНТЕЗ ОКСИДАЗЫ D-АМИНОКИСЛОТ (DAO) ДРОЖЖЕЙ Trigonopsis variabilis В КЛЕТКАХ Escherichia coli И РЕКОМБИНАНТНЫЙ ШТАММ Escherichia coli C41(DE3)/pETTvDAO2 - ПРОДУЦЕНТ DAO | 2006 |
|
RU2310687C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА pSVH0106, ОБЕСПЕЧИВАЮЩАЯ СИНТЕЗ Gl7ACA-АЦИЛАЗЫ В КЛЕТКАХ Escherichia coli, И РЕКОМБИНАНТНЫЙ ШТАММ Escherichia coli BL21(DE3)/pSVH0106-ПРОДУЦЕНТ Gl7ACA-АЦИЛАЗЫ | 2005 |
|
RU2300566C2 |
| РЕКОМБИНАНТНАЯ ДНК, КОДИРУЮЩАЯ ФУНКЦИОНАЛЬНО АКТИВНЫЙ ГИБРИДНЫЙ БЕЛОК ОКСИДАЗЫ D-АМИНОКИСЛОТ С ХИТИНСВЯЗЫВАЮЩИМ ДОМЕНОМ (DAOcbd) РЕКОМБИНАНТНАЯ ПЛАЗМИДА pVR1, ОБЕСПЕЧИВАЮЩАЯ ЕГО СИНТЕЗ В КЛЕТКАХ Escherichia coli, И РЕКОМБИНАНТНЫЙ ШТАММ Escherichia coli С 41(DE3)/pVR1 - ПРОДУЦЕНТ DAOcbd | 2006 |
|
RU2310688C1 |
| ПРОДУЦЕНТ L-АСПАРАГИНАЗЫ E. COLI И ЭКСПРЕССИОННАЯ ПЛАЗМИДА PET28A-ASNSYN, КОДИРУЮЩАЯ L-АСПАРАГИНАЗУ | 2023 |
|
RU2817891C1 |
| РЕКОМБИНАНТНАЯ ДНК, КОДИРУЮЩАЯ ФУНКЦИОНАЛЬНО АКТИВНЫЙ ГИБРИДНЫЙ БЕЛОК G17ACA-АЦИЛАЗЫ С ХИТИН-СВЯЗЫВАЮЩИМ ДОМЕНОМ (BrdG17ACA-cbd), РЕКОМБИНАНТНАЯ ПЛАЗМИДА pSVH0108, ОБЕСПЕЧИВАЮЩАЯ ЕГО СИНТЕЗ В КЛЕТКАХ Escherichia coli, И РЕКОМБИНАНТНЫЙ ШТАММ Escherichia coli BL21(DE3)/pSVH0108-ПРОДУЦЕНТ BrdG17ACA-cbd | 2006 |
|
RU2388826C2 |
| МОДИФИЦИРОВАННЫЙ ГЕН tsA, КОДИРУЮЩИЙ ТЕРМОСТАБИЛЬНУЮ L-АСПАРАГИНАЗУ ИЗ АРХЕИ THERMOCOCCUS SIBIRICUS, РЕКОМБИНАНТНЫЙ ШТАММ ESCHERICHIA COLI - ПРОДУЦЕНТ ТЕРМОСТАБИЛЬНОЙ L-АСПАРАГИНАЗЫ И СПОСОБ ОЧИСТКИ ЭТОГО ФЕРМЕНТА | 2022 |
|
RU2794225C1 |










Изобретение относится к области биотехнологии, в частности к генетической инженерии, и может быть использовано в медицинской практике. Выделен и охарактеризован фрагмент ДНК, кодирующий полную аминокислотную последовательность L-аспарагиназы Erwinia carotovora (ECAR-LANS). Сконструирована плазмидная ДНК рBADLANS, в которой кодирующий фермент фрагмент ДНК находится под контролем регулируемого промотора рBAD. В результате трансформации штамма Е. coli предложенной рекомбинантной плазмидой и селекции трансформированных клонов получен новый штамм - продуцент ECAR - LANS (Е.coli ВКПМ B-8174), обеспечивающий высокий выход рекомбинантного фермента, основным назначением которого является применение в качестве основного компонента при получении известных и создании новых противоопухолевых препаратов. 2 с.п. ф-лы, 7 ил., 4 табл.
| MINTON et al | |||
| Gene, 46, 25-35, 1986 | |||
| TIWARI et al | |||
| Jndian Journal of Biochem | |||
| and Biophys, 33, 371-376, 1996 | |||
| GILBERT et al | |||
| J | |||
| Gen | |||
| Microbiol, 132, 151-160, 1986 | |||
| US 6140101, 31.10.00. |
Авторы
Даты
2004-01-20—Публикация
2001-08-22—Подача