Изобретение относится к области биоорганической химии, а именно к новым биологически активным веществам (БАВ), способам их получения и применения.
Известна многочисленная группа веществ, обладающих антиоксидантным (АО) и/или антигипоксантным (АГ) действием. К их числу, в частности, относятся цитохром С, убихинон, метилфеназин, ионол и другие (М.Д. Машковский. Лекарственные средства. - М.: Медицина, т. 2, с. 73-76; Энциклопедия лекарств. Изд. 8, М. : РЛС. 2001, 1503 с.; Справочник ВИДАЛЬ. М.: Астра-ФармСервис, 2001, 725 с. ; Виноградов В.М. Фармакология и токсикология. Сб. Киев: Здоровье, 1972, 7, с. 163). Так, в частности, убихинон (коэнзим Q) в дозе 200 мг/кг живого веса оказывает нормализующее воздействие на клетки в условиях некоторых гипоксий, являясь природным переносчиком электронов и занимая центральное место в цепи ферментов электронного транспорта, реагируя с тремя ферментными системами: НАД, Н-оксидазой, сукцинат KoQ-редуктазой, и системой цитохромов (патент РФ 1746886, 1991, кл. С 08 Р 32/06; заявка РСТ 96/08527, 1996, кл. С 08 G 61/10).
Недостатками большинства указанных веществ является узкий спектр действия, обусловленный значительным числом противопоказаний, недостаточная эффективность, сложная технология получения.
Аналогами по структуре являются полиариленовые эфиры типа С6Н5O(С6Н4O)6С6Н5, используемые в качестве компонентов сополимеров с полипропиленами или в качестве добавок, повышающих термоустойчивость смол и получаемые окислением фенолов (патент США 3257357, 1966, НКл. 260-47; патент США 3306874, 1967, НКл. 260-47; патент США 4645787, 1987, НКл. 260-47).
Отличием данных аналогов от заявляемых веществ является наличие иных радикалов, олигомерная или полимерная природа соединения, принципиально иные физико-химические свойства.
Наиболее близким по свойствам к заявляемой группе изобретений являются производные олиго-окси-фениленов - препараты Олифен и другие (заявка РСТ 96/08527, кл. С 08 G 61/10, 1996), нашедшие применение в качестве антигипоксантов при шоке, эпилепсии и хронических заболеваний легких, в качестве антиоксиданта при лечении саркоидоза и в составе кормовых добавок (патент РФ 2082397, кл. А 61 К 31/095, 1997; авт. св. СССР 1660701, кл. А 61 К 31/745, 1991; патент РФ 2076611, кл. А 23 К 1/16, 1997; патент РФ 2043765, кл. А 61 К 31/095, 1995).
Соединения данного типа получали полимеризацией пара-бензохинона в присутствии щелочных агентов в водно-ацетоновой среде с добавками веществ, обеспечивающих введение в полимер замещающих групп, например тиосульфата натрия или гуанидина, и последующим выделением целевого продукта с помощью экстракции, как правило, эфиром.
Недостатком соединений данного типа является получение в ходе реакции смеси олигомеров, что приводит к плохой стандартизуемости препарата, плохая растворимость соединений в воде, наличие неприятного привкуса, недостаточно высокой эффективности при некоторых патологиях, наличие осложнений особенно при внутривенном введении.
Задачей, решаемой авторами, являлось создание новых более эффективных препаратов, обладающих сочетанными антиоксидантными и антигипоксантными свойствами.
Было выдвинуто предположение, что свойства препарата должны улучшиться при замене связей -С-С- между фенильными группами олигомера на связь -С-О-С-. Появление между гибридизованными фенильнымн ядрами (ФЯ) атома кислорода, обладающего свободной электронной парой и обеспечивающего сближение фенольных ядер за счет расположения индивидуальных связей О-(ФЯ) под острым углом друг к другу должно было обеспечивать переход от отдельных гибридизованных фрагментов структур к гибридизации всего олигомера.
При этом новая структура должна была бы иметь более плотное электронное облако, быть более стабильной в отношении внешних условий, что делало ее перспективной для работы с биосистемами.
Указанная задача была успешно решена созданием полиоксифениленовых эфиров (ПДФЭ) общей формулы (фиг.1):
где R-ОН, -S-SO2-ONa; х=1; 2 М=-ОН, -О-С6Н4-ОН
В качестве таких соединений, в частности, были получены:
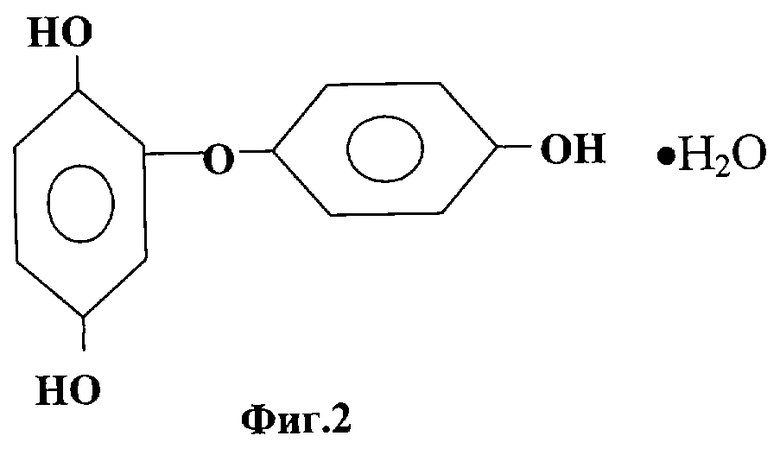
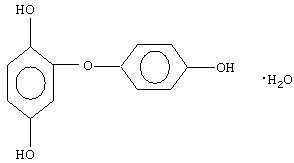
(1)4-гидроксифенилен-2,4-диоксибензол, кристаллогидрат - "ДФД" (базовая структура). Брутто-формула C12H12O4. Молекулярная масса 237 к.е. (анализ 240±5). Массовая доля углерода - 58,7%; массовая доля водорода - 5,4%.
Формула: (НО)2С6Н3ОС6Н4OНхН2O (фиг.2).
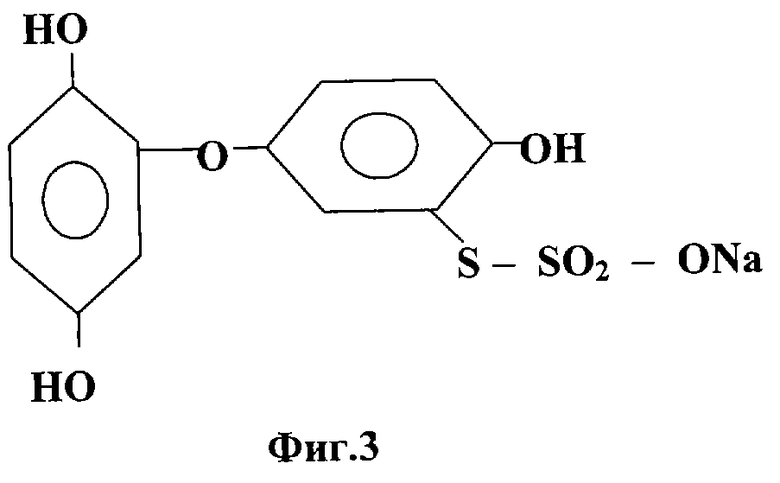
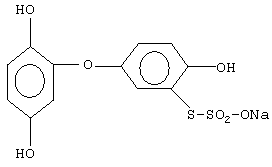
(2)2-(1-окси-4-гидроксибензол)-5-(натрийсульфотио)-1,4-гидроксифенилен - "ДФС"
Брутто-формула C12H9O7S2Na. Молекулярная масса 311 к.е. (анализ 302±8).
Предполагаемая структурная формула
(НO)2С6Н3-О-С6Н3(ОН)(-S-SO2ONa) (фиг.3).
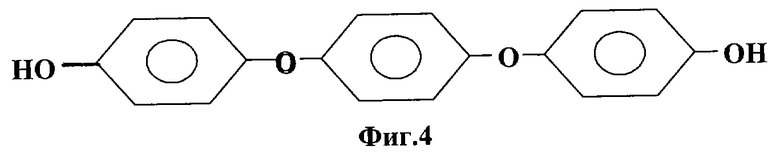
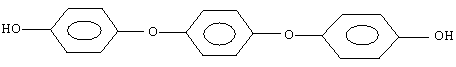
(3)ди-(1,4-гидроксифенилен)-1,4-диоксибензол или п-диокси-п-дифенил-п-оксихинон - "ДФТ".
Брутто-формула С18Н14O4. Молекулярная масса 294 к.е. (анализ 292±6).
Предполагаемая структурная формула:
НО-С6Н4-O-С6Н4-O-С6Н4-ОН (фиг.4).
Все указанные структуры при обезвоживании образуют игольчатые кристаллы серого (1) или темно-серого (2-3) цвета, хорошо растворимые в воде и практически нерастворимые в органических растворителях: бензоле, дихлорметилене, хлороформе, этилацетате, ацетоне, органических спиртах (метиловом, этиловом, изопропиловом).
Соединения (1) и (3), слабо растворимы в кислотах, соединение (2) среднерастворимо в сильных кислотах. рН водного раствора 7,3-7,6, плотность 0,93-0,94 г/см3.
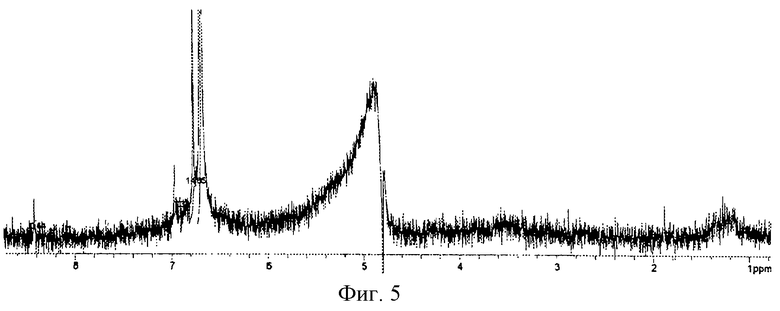
Оценка химической структуры "ПДФЭ" осуществлялась с использованием методов инфракрасной (ИК) и ультрафиолетовой спектроскопии, ядерного магнитного (ЯМР) резонанса и рядом других методов (ИК- и УФ-спектры всех трех соединений были близки между собой и имели одинаковые характеристические полосы, характеризующие базовую структуру). Для оценки структуры препарата методом ЯМР образцы препарата растворяли в 2Н2О ("Изотоп", 98% 2H) до конечной концентрации 10 вес. %. Спектры 1Н-ЯМР измеряли на частоте 300 МГц. Отнесение линии в спектрах производили по сигналу резонанса остаточных протонов воды (δ 4,8). Спектры ЯМР снимали при комнатной температуре 20±2oС. Спектр ЯМР приведен на фиг.5.
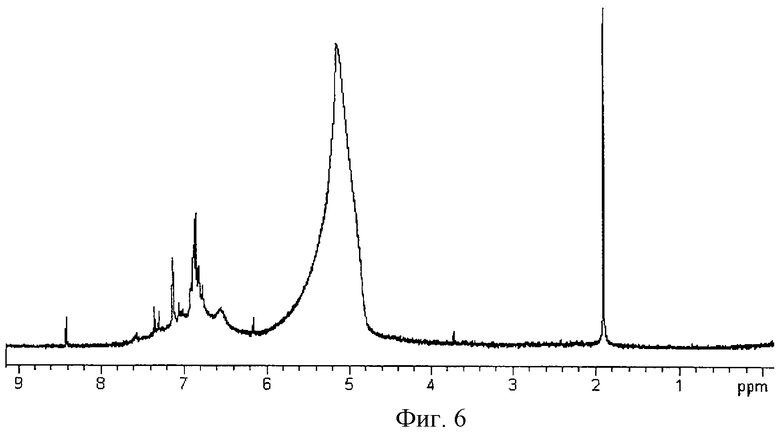
Анализ спектра показал, что в области резонанса ароматических протонов обнаружен мультиплет с положением δ=6,57 м.д., принадлежащий протонам гидрохинона, что подтверждают наличие его структуры в соединении, как и предполагалось для структур данного типа. Сопоставление полученного спектра со спектром "Олифена" (фиг. 6) показало наличие определенного сходства между спектрами, что обусловлено определенным сходством их структур (основным отличием является замена -С-С- связи между бензольными ядрами на связь -С-О-С-).
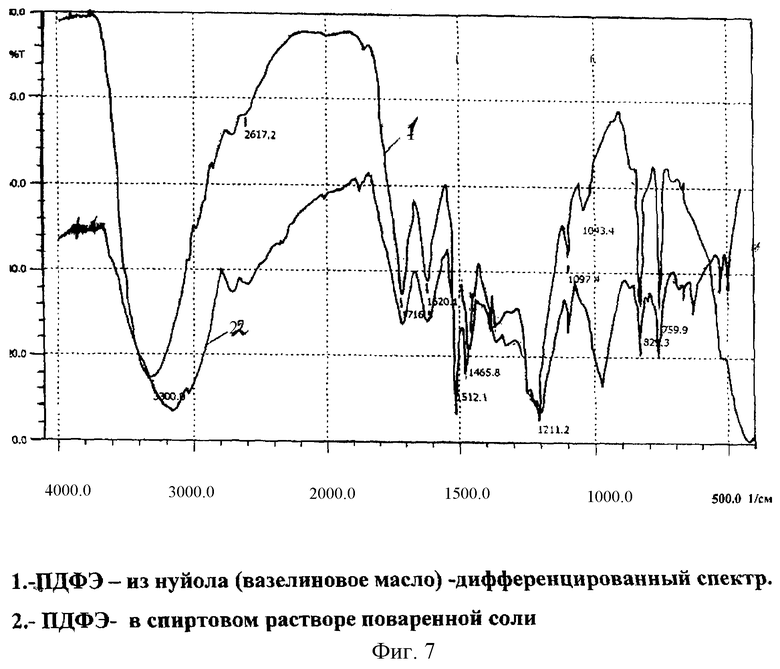
Анализ "ПДФЭ" методами ПК-спектроскопии выявил характеристические линии, соответствующие наличию гидроксильных групп, замещению ароматического кольца в пара-положении, наличия связей -С-O- и -С=С- (фиг.7, табл.1), что подтверждает предполагаемую вторичную структуру заявляемой группы соединений.
Исследование УФ-спектра выявило наличие характеристической полосы поглощения с максимумом 289 нм, характерной для гидрохиноидной структуры.
Исследование ЭПР показало наличие мощного сигнала для вещества (1), связанного с наличием неспаренных электронов на фенильной группе. Величина сигнала уменьшается более чем вдвое при переходе к соединению (2), что связано с присоединением к фенильному ядру тиосерной группы в пара-положении по отношению к структуре гидрохинона и повышенной гибридизации электронного облака всего соединения.
Приведенные данные наряду с механизмом образования соединений достаточно однозначно показывают особенности вторичной структуры "ПДФЭ". Способ получения соединений "ПДФЭ" включает в себя:
- на первой стадии- получение "ДФД" в результате взаимодействия гидрохинона с перекисью водорода в присутствии солей двухвалентного железа по реакции:
НО-С6Н4-ОН+Н2О2-->О=С6Н4=О+е--->
О=С6Н4-О-->(НО)2С6Н3-О-С6Н4ОН (а)
на второй стадии - введение в структуру (1) тиосульфо- и иных групп по стандартным схемам, например
(НО)2С6Н3-О-С6Н4ОН+Na2S2O3-->
НО-С6Н4-О-С6Н2(ОН)2(-S-SO2ONа) (б)
или
(НО)2С6Н3-О-С6Н4ОН+НО-С6Н4-ОН+Н2О2
-->НО-С6Н4-О-С6Н4-О-С6Н4-ОН (в)
Реакция (а) протекает путем взаимодействия гидрохинона с избытком перекиси водорода (оптимально мольное соотношение 1:1,5-2,0) с введением в реакцию 0,01-0,02 мас. % хлористого железа. Избыток образующихся кислот нейтрализуют щелочью. При меньшем соотношении скорость реакции уменьшается и возможно неполное превращение гидрохинона, что потребует введения дополнительно очистки целевого продукта от непрореагировавших соединения.
Реакция (б) протекает при между "ДФД" и тиосульфатом натрия в весовом соотношении 1:0,2-0,5 при температуре 40-60oС и интенсивном перемешивании в течение 20-60 мин.
Реакция (в) протекает при между "ДФД" и гидрохиноном в мольном соотношении 1:0,8-1,5 в присутствии 0,5-0,8 моль перекиси водорода в виде 3% раствора и 0,3-0,8 мас.% хлористого железа.
Реакции (а) и (б) являются экзотермическими и не требуют для своего протекания повышенной температуры.
Анализ химических структур, проведенный путем просмотра Beilsteins Handhuch с 1941 г. по настоящее время с целью поиска аналогичных соединений, выявил в качестве аналогов производные бензохинонов, например фенилмеркантобензохинон и 2-фенил-5-сульфотио-пара-бензохинон (Helvetica Chimica Acta, v. XXX, Fsaciculus 11, 1947, p. 578-584// Beil Bd. 08/03/70 p. 2635-2637). Все выявленные соединения имели связи между ядрами С-С или -S-S-, т.е. заявляемые соединения в научно-технической литературе не описаны.
Свойства полученных соединений иллюстрируются следующими примерами.
Пример 1. Способ получения субстанции "ДФД". К 500 г гидрохинона (ГХ), помещенного в фарфоровую чашку, добавляют 200 мл 30% Н2O2 (ПВ) и 15 мг железного купороса (ЖК) и тщательно перемешивают, после чего в смесь еще 4 раза вводят по 200 мл 30% Н2О2 и по 2 г едкого натра. По окончании реакции образуется черное твердое вещество, которое помещают на 14-16 часов в сушильный шкаф при температуре 60-70oС до исчезновения запаха. Выход 506 г, рН 5% водного раствора 6,8. После перекристаллизации из водного раствора по молекулярной массе и спектральных характеристиками вещество соответствует свойствам "ДФД".
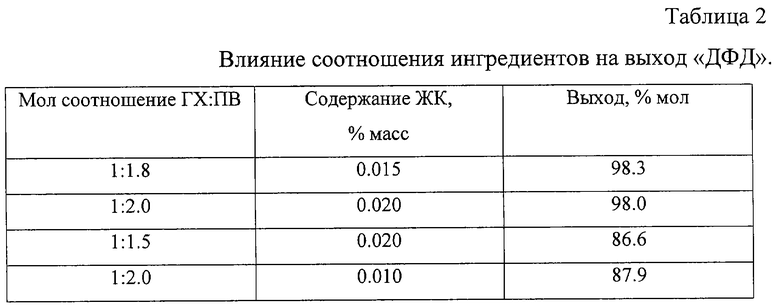
Влияние соотношения ингредиентов на выход конечного продукта приведено в таблице 2.
Пример 2. Способ получения субстанции "ДФС". К 500 г "ДФД", помещенного в фарфоровую чашку, добавляют 150 г тиосульфата натрия (ТСН) и тщательно перемешивали при 60oС в течение 30 мин. По окончании реакции образуется черное твердое вещество, которое затем перекристаллизовывают. Выход 780 г. После перекристаллизации из водного раствора по молекулярной массе и спектральным характеристиками оно соответствует свойствам "ДФС".
Влияние соотношения ингредиентов на выход конечного продукта приведено в таблице 3.
Пример 3. Способ получения субстанции "ДФТ".
К 500 г гидрохинона (ГХ) и 1000 г "ДФД", помещенных в фарфоровую чашку, добавляют 100 мл 30% перекиси водорода (ПВ) и 7,5 г хлористого железа (ЖХ), тщательно перемешивают, после чего в смесь еще 14 раз вносят по 100 мл 30% ПВ и по 4 г едкого натра. По окончании реакции образуется черное твердое вещество, которое помещают на 10 часов в сушильный шкаф при температуре 60-70oС до исчезновения запаха. Выход: 506 г.
После перекристаллизации из водного раствора вещество по молекулярной массе и спектральным характеристикам вещество соответствует свойствам "ДФТ".
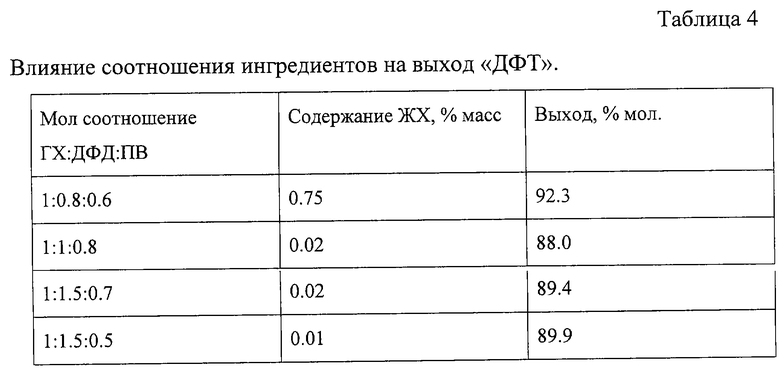
Влияние соотношения ингредиентов на выход конечного продукта приведено в таблице 4.
Пример 4. Исследование биологических свойств препаратов. Исследование биологических свойств препаратов типа "ПДФЭ" проводили в соответствии с методическими указаниями (Методические указания к постановке исследований для обоснования санитарных стандартов вредных веществ в воздухе рабочей зоны. 2163. М., 1980, 19 с.; Определение безопасности и эффективности биологически активных добавок к пище МУК 2.3.2.721-98. МЗ РФ., М. 1999, 87 с.) В экспериментах использовали белых мышей, крыс, морских свинок и кроликов стандартной массы. Для внутрижелудочного введения из порошков субстанций "ПДФЭ" и Олифена ex tempore готовили водные взвеси.
Динамику веса крыс и относительной массы внутренних органов к весу тела определяли на весах ВЛР-500.
Суточную мочу собирали с помощью обменных клеток для крыс итальянской фирмы "Texnoplast". Кровь для биохимических исследований получали пункцией хвостовой вены крыс или из орбитального синуса морских свинок.
Активность АлТ, АсТ, ЩФ, тимоловую пробу, содержание общего белка и липидного фосфора сыворотки крови, а также белка мочи определяли с помощью наборов "Био-Лат-Тест" чешской фирмы "Лахема".
СПП определяли по С.В. Сперанскому (Сперанский С.В. Фармакология и токсикология, 1965, 1, с. 123), а остальные показатели общепринятыми методами.
В условиях свободного поведения методом "открытого поля" изучали поведение животных (Я. Буреш, О. Бурешова, Дж.П. Хьюстон Методики и основные эксперименты по изучению мозга и поведения. - М.: Высшая школа, 1991, 450 с.). Забитые декапитацией животные подвергались патологоанатомическому вскрытию. Для гистологического исследования брали легкие, сердце, печень, почки, желудок и кожу. Материал фиксировали в 15% формалине и заливали в парафин. Срезы окрашивали гематоксилин-эозином и cуданом IV на жир.
Изучение гонадотоксического эффекта Эпофена проводилось по показателям, обязательным при первичной оценке химических веществ. Изучение мутагенной активности проводили по частоте образования микроядер в полихроматофильных эритроцитах костного мозга (из бедренной кости) белых мышей в соответствии с методическими рекомендациями. (Методы экспериментального исследования по установлению порога действия промышленных ядов на генеративную функцию. МЗ СССР, М. , 1969, 25 с.; Методы экспериментального исследования по установлению порогов действия промышленных ядов на генеративную фикцию с целью гигиенического нормирования. Методические рекомендации. МЗ СССР, 1744, М., 1978, 35 с. ; Оценка мутагенной активности химических веществ микроядерным методом. Методические рекомендации. МЗ СССР 28/10. М., 1984. 21 с.; Критерии оценки и методы прогнозирования отдаленных последствий действия на организм вредных веществ в воздухе вследствие действия на организм вредных веществ в воздухе рабочей зоны. Информационное письмо. НИИ гиг. труда и проф. забол., М., 1985, 15 с.).
Статистическую обработку результатов экспериментов проводили по Стьюденту-Фишеру.
Определение показателей острой токсичности включало эксперименты на грызунах (мышах, крысах). Животные распределялись по группам случайным образом методом рандомизании. В качестве критериев приемлемости рандомизации считали отсутствие внешних признаков заболеваний и гомогенность групп по весу тела (±20%).
Субстанции растирали в порошок, из которого готовили водные растворы (взвеси) для внутрижелудочного (в/ж) введения. Введение осуществляли перорально через металлический атравматический зонд в возрастающих дозах но Литчфилду-Унлкоксону.
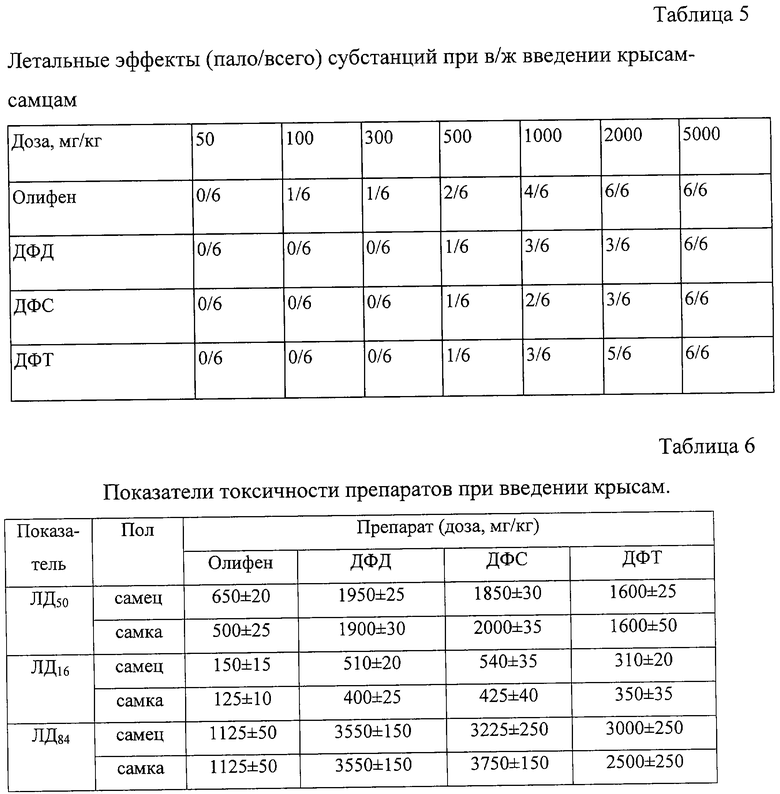
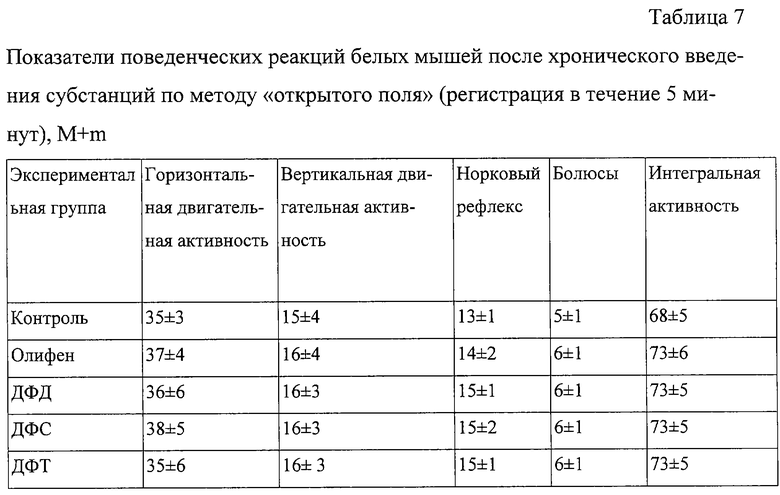
Для исследования каждой дозы препарата использовались группы по 6 животных одного пола. Кроме того, имелись аналогичные по численности группы контрольных животных каждого пола, которым по тому же пути вводили эквивалентные объемы растворителя - дистиллированной воды. Период наблюдения составлял 14 суток. Полученные результаты приведены в таблицах 5-7.
Как видно из таблиц, препараты типа "ПДФЭ" существенно менее токсичны, чем "Олифен". Введение субстанций в токсических дозах через 20-30 мин сопровождалось развитием заторможенности, гиподинамии, атаксии, тремором, взъерошенностью шерсти, гиперсаливацией. В течение часа развивались приступы клонико-тонических судорог с нарушением акта дыхания. Гибель животных наблюдалась в течение 3-5 часов при явлениях одышки и паралича. Выжившие животные были заторможены, гиподинамичны, имели неопрятный вид.
При вскрытии через день после острого введения выявлено следующее. Листки плевры и органы грудной клетки не изменены. Легкие бледно-розовые, воздушные, без уплотнении на ощупь. Размеры сердца в пределах нормы. В полостях сердца содержится небольшое количество жидкой крови. Мышца сердца плотная, коричневой окраски. Желудок заполнен небольшим количеством плотной пищи. Слизистая оболочка блестящая, складчатая, слегка розоватой окраски. Слизистая тонкого кишечника блестящая, гладкая, розоватой окраски.
Размеры и форма печени не отличаются от контроля. Поверхность печени гладкая. Капсула тонкая, прозрачная. Рисунок печени на разрезе не изменен. Ткань печени умеренно полнокровна. Почки обычной величины и формы, коричневатого цвета, плотные, с отчетливыми корковым и мозговым веществом на разрезе. Щитовидная железа, надпочечники и поджелудочная железа по внешнему виду не отличаются от контроля. При осмотре гистологических препаратов желудка и паренхиматозных органов отличий в структуре между опытными и контрольными группами не обнаружено.
Сосуды легких были умеренно полнокровны. Эпителий альвеол и внутрилегочных бронхов изменений не представлял. Альвеолы были заполнены воздухом. Отека либо воспаления легочной ткани не наблюдалось. Миобифриллы левого желудочка сердца и межжелудочковой перегородки имели отчетливую поперечную исчерченность, ядра кардиомиоцитов были светлыми. Сосуды миокарда умеренно полнокровные. Дольчатое строение печени сохранялось. Границы гепатоцитов были четкими, цитоплазма гепатоцитов была слабобазофильной, зернистой, ядра с достаточным содержанием хроматина и тонкой ядерной мембраной.
Эпителий извитых канальцев почек изменений не представлял. Цитоплазма его была зернистой, оксифильной, ядра светлыми. Сосуды клубочков умеренно полнокровные.
Строение слизистой оболочки фундальной части желудка не отличалось от контроля. Ядра эпителия слизистой и желез были светлыми. В базальных отделах желез сохранилась зернистость в цитоплазме. Эпителий ворсинок и крипт слизистой тонкой кишки был сохранен, в криптах присутствовали митозы.
При окраске замороженных срезов печени Суданом IV признаков жировой дистрофии не наблюдалось. В головном мозге наблюдались субдуральные и периваскулярные кровоизлияния.
Анализ величин массовых коэффициентов внутренних органов крыс не выявил каких-либо достоверных отличий как между группами животных, получавших сравниваемые субстанции, так и по отношению к контрольной группе.
По результатам исследований субстанции препаратов "ПДФЭ" относятся к IV классу малотоксичных лекарственных веществ (Н. Hodge et al. Clinical Toxicology of Commercial Products. Acute Poisoning. Ed. IV, Baltimore, 1975, 427 p.).
При хроническом ежедневном (на протяжении 30 дней) в/ж введении субстанций крысам в дозе 100 мг/кг (доза, превышающая максимальную терапевтическую для человека в 2 раза) (Энциклопедия лекарств, изд. 7. Под ред. Ю.Ф. Крылова, М., 2000, с. 678) летальных эффектов не наблюдалось. Данные таблиц свидетельствуют, что ни по одному из использованных показателей не было выявлено статистически значимых различий с контролем (вода) (р>0,05 при 95% уровне вероятности) или патологических отклонений за пределы варьирования физиологической нормы.
При вскрытии крыс, забитых на следующий день после последнего введения субстанций, размеры, форма и окраска внутренних органов макроскопических изменений по сравнению с контролем не имели. Слизистая оболочка желудка и тонкого кишечника были блестящими, бледно-розовыми, без признаков раздражения или воспаления.
При гистологическом исследовании препаратов легких, миокарда, печени, почек и слизистой желудка подопытных животных дистрофических, воспалительных или некробиотических изменений указанных выше органов не наблюдалось.
Эпителий альвеол и внутрилегочных бронхов изменений не представлял, альвеолы были воздушными. Ателектазов либо отека легочной ткани не наблюдалось. Поперечная исчерченность миофибрилл миокарда была отчетливой. Строение печени нарушений не представляло. Границы гепатоцитов были отчетливые, цитоплазма зернистая, слабобазофильная, ядра светлые с тонкой мембраной и отчетливыми ядрышками. Некроэпителий с оксифильной зернистой цитоплазмой и светлыми четкими ядрами. Эпителий слизистой желудка сохранен, главные и обкладочные клетки желез желудка не изменены.
Хроническое поступление субстанций ПДФЭ в организм мышей и крыс через желудок не вызывает дистрофических или деструктивных измерений паренхиматозных органов и не сопровождается раздражением слизистых оболочек желудочно-кишечного тракта.
Пример 5. Оценка антигипоксических и антиоксидантных свойств препаратов.
Оценка эффективности новых БАВ оценивалась на модели острой гипоксии. (Руководство по физиологии. Экологическая физиология человека. Адаптация человека к экстремальным условиям среды, под ред. О.Г. Газенко. М.: Наука, 1979, с. 333-336; Руководство к практическим занятиям по патологической физиологи. Под ред. О.М. Павленко. М.: Медицина, 1974. С. 174-175).
Животные помещались в банку объемом 250 мл, плотно закрытую стеклянной крышкой, смазанной герметиком. Фиксировали с помощью секундомера максимальную продолжительность жизни и симптомы танатогенеза. Банки с животными во время исследования находились в кондиционере, обеспечивающем постоянство условий эксперимента (температура 20oС, влажность 65-70%, атмосферное давление). Контролем служили интактные животные.
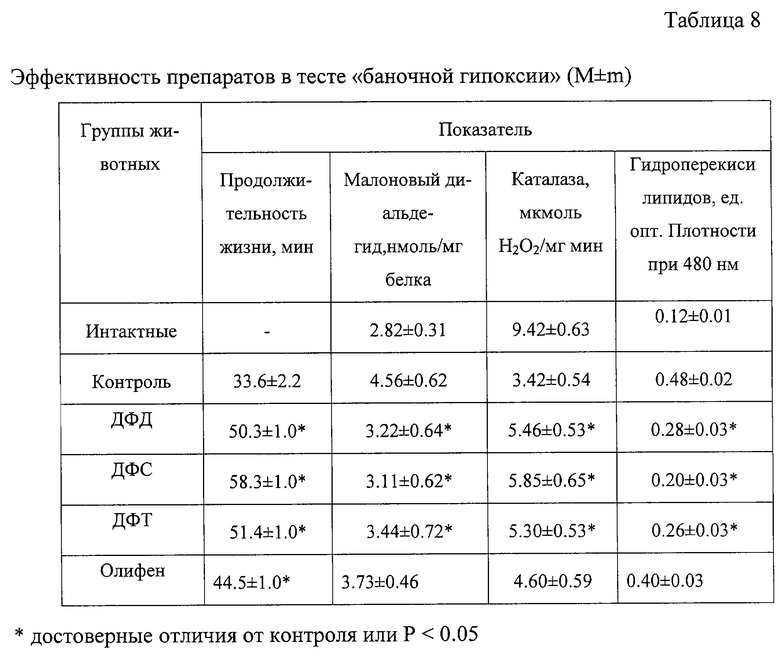
После гибели у каждого животного ex tempore получали головной мозг, проводили его гомогенезацню (400 об/мин, 10 ходов пестика) и определяли в гомогенате активность каталазы, уровень диеновых конъюгатов и гидроперекисей липидов (Tyson C. A. , Luman K.O., Stephens R.J., Arch. Env. Health, 1982, Vol. 37., 3, p. 167-176; Современные методы в биохимии. Под ред. В.Н. Ореховича. М. : Медицина, 1977. С. 62-64). Указанные показатели позволяют оценивать антиоксидантные свойства препарата (табл.8)
Оказалось, что препараты достоверно увеличивают время жизни мышей, при этом стабилизировались показатели перекисного окисления липидов (снижались уровни малонового диальдегида и гидроперекисей липидов мозга) и восстанавливалась антиокислительная (каталазная) активность, что свидетельствует об увеличении резервной антиокислительной активности мозга.
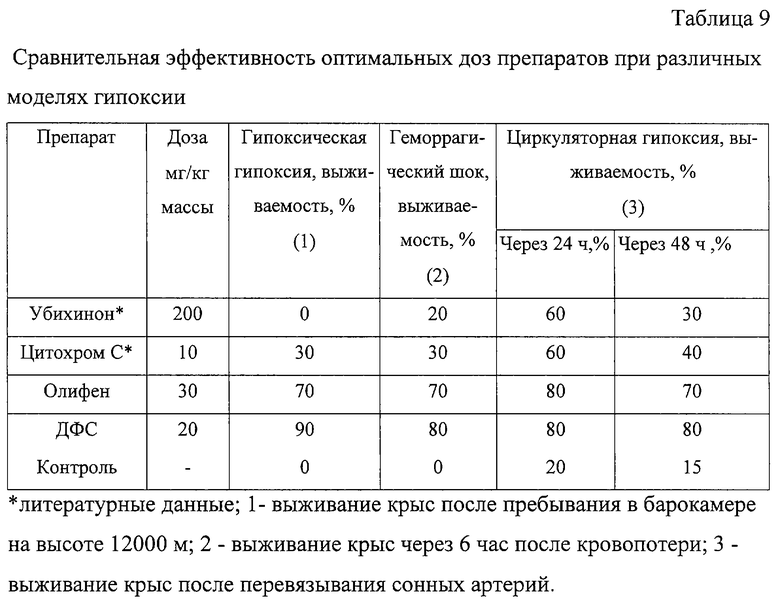
Препарат "ДФС", сопоставляли по эффективности антигипоксического воздействия с убихиноном, цитохромом и Олифеном при различных видах гипоксии на крысах с использованием экспериментальных и литературных данных. Результаты испытаний приведены в таблице 9.
Полученные данные показывают, что соединения типа "ПДФЭ" практически нетоксичны и обладают ярковыраженными антигипоксантными и антиоксидантными свойствами, что делает их перспективными для дальнейшего применения в медицинской, пищевой и косметической промышленности, а также в ветеринарии и сельском хозяйстве.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДОБАВКА К ПИЩЕВЫМ ПРОДУКТАМ, БИОЦИДНЫЙ ПРЕПАРАТ, 2-(1-ОКСИ-4-ГИДРОКСИФЕНИЛЕН)-БЕНЗОХИНОН (ВАРИАНТЫ) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2230467C1 |
| ПРЕПАРАТ ДЛЯ СТИМУЛЯЦИИ ПРОРАЩИВАНИЯ СЕМЯН И ПОВЫШЕНИЯ УСТОЙЧИВОСТИ ПРОРОСТКОВ К ДЕФИЦИТУ ВЛАГИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2337543C2 |
| ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО | 2005 |
|
RU2309735C2 |
| ЛЕЧЕБНО-КОСМЕТИЧЕСКОЕ СРЕДСТВО И ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЙ НАРУЖНЫХ ТКАНЕЙ ОРГАНИЗМА | 2005 |
|
RU2309750C2 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО "КАРСИЛИН" | 2002 |
|
RU2205637C1 |
| СМЕСЬ ПОЛИ (1,4-ДИГИДРОКСИ)-ФЕНИЛЕНОВ (ПОЛИГИДРОХИНОНОВ) | 2005 |
|
RU2294918C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНАЛЬГЕЗИРУЮЩИМ, УЛУЧШАЮЩИМ КРОВОСНАБЖЕНИЕ, СТИМУЛИРУЮЩИМ РЕГЕНЕРАЦИЮ НЕРВНОЙ ТКАНИ И ПРОТИВОАЛЛЕРГИЧЕСКИМ ДЕЙСТВИЕМ | 2003 |
|
RU2225707C1 |
| АНТИДОТ ОКИСИ УГЛЕРОДА И ГЕПАТОТОКСИЧЕСКИХ ВЕЩЕСТВ | 2015 |
|
RU2584586C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ | 2013 |
|
RU2552006C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ПЕДИФЕНА ДЛЯ ЛЕЧЕНИЯ ПОРАЖЕНИЯ НЕЛЕТАЛЬНЫМИ РАЗДРАЖАЮЩИМИ СРЕДСТВАМИ | 2012 |
|
RU2496485C1 |


Изобретение относится к области биоорганической химии, а именно к новым биологически активным веществам и способам их получения. Синтезированы новые полиоксифениленовые эфиры общей формулы I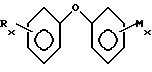
где R = -OH, -S-SO2-ONa; x = 1,2; M = -OH, -O-C6H4-OH. Способ получения полиоксифениленовых эфиров включает окисление гидрохинона перекисью водорода в присутствии солей двухвалентного железа с последующим введением дополнительных функциональных групп в соединение (НО)2С6Н3-О-С6Н4(ОН)•Н2О. Новые биологически активные вещества практически нетоксичны, обладают выраженным сочетанным антиоксидантным и антигипоксантным действием. 2 с. и 7 з.п.ф-лы, 9 табл., 7 ил.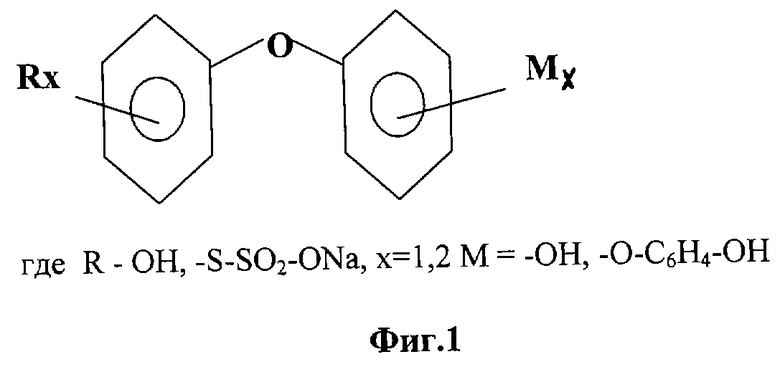
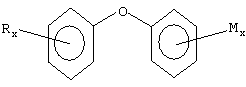
где R=-ОН, -S-SO2-ONa;
х=1, 2;
М=-ОН, -О-С6Н4-ОН.
| US 3306874 А, 28.02.1967 | |||
| US 4645787 А, 24.02.1987 | |||
| US 3257357 А, 21.06.1966 | |||
| Способ получения олигомерных полиоксифениленов | 1975 |
|
SU576325A1 |
| НАТРИЕВАЯ СОЛЬ [ПОЛИ-(2,5-ДИГИДРОКСИ-ФЕНИЛЕН)]-4-ТИОСУЛЬФОКИСЛОТЫ КАК РЕГУЛЯТОР МЕТАБОЛИЗМА КЛЕТКИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2105000C1 |
| НАТРИЕВАЯ СОЛЬ ПОЛИ(ПАРА-ДИГИДРОКСИ-ПАРА-ФЕНИЛЕН)ТИОСУЛЬФОКИСЛОТЫ, ОБЛАДАЮЩАЯ СУПЕРОКСИДАЗНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2000 |
|
RU2175317C1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства, 14-е издание | |||
| - М.: ООО "Новая волна", 2001, т.2, с.182-188. | |||
Авторы
Даты
2004-02-27—Публикация
2002-04-11—Подача