Изобретение относится к области медицины и касается получения обладающего гепатопротекторным действием средства, активное начало которого - силимарин является флавоноидным соединением, выделенным из плодов расторопши пятнистой.
Флавоноидные соединения имеют фенилхроманоновую структуру. Их гепатозащитное действие объясняется антиоксидантной активностью, стимуляцией синтеза белка, нормализацией обмена фосфолипидов.
Известно средство, содержащее соли полигидроксифенилхроманонов (US п. 4061765, А 61 К 31/335, 1977 г.). Оно представлено в различных лекарственных формах, в том числе в виде таблеток, покрытых оболочкой.
Наиболее близкими к предлагаемому лекарственному средству по технической сущности и достигаемому результату являются средства, содержащие в качестве активного вещества сумму флавоноидов из плодов расторопши пятнистой. Эти средства выполнены в форме драже, таблеток "Силибор", "Легален", "Карсил" (М.Д. Машковский. Лекарственные средства, М., 1993, т. 1, с. 611-612).
Целью настоящего изобретения является получение отечественной лекарственной формы силимарина в виде покрытых оболочкой таблеток с биодоступностью, улучшенной благодаря увеличению скорости высвобождения действующего вещества.
Поставленная цель достигается с помощью предлагаемого гепатопротекторного средства, названного "Карсилин". Средство выполнено в виде таблеток, содержащих ядро, покрытое многослойной оболочкой. Ядро таблеток содержит действующее вещество силимарин в количестве 10-20% от массы ядра, а также вспомогательные вещества: микрокристаллическую целлюлозу, лактозу, крахмал кукурузный, кросповидон, поливинилпирролидон, натрия бикарбонат, тальк и кислоту стеариновую и/или ее соли.
Для получения ядер таблеток "Карсилин" используют следующие компоненты, % от массы ядра:
Силимарин - 10-20
Микрокристаллическая целлюлоза - 15-30
Крахмал кукурузный - 15-30
Кросповидон - 1-5
Поливинилпирролидон - 5-15
Натрия бикарбонат - 0,1-1
Тальк - Не более 3
Кислота стеариновая и/или ее соли - Не более 1
Лактоза - Остальное
Для получения ядер таблеток "Карсилин" перемешивают активное вещество, микрокристаллическую целлюлозу, лактозу, часть крахмала, кросповидона и проводят грануляцию в установке с псевдоожиженным слоем. В качестве гранулирующей жидкости используют раствор натрия бикарбоната в водном растворе поливинилпирролидона. Полученный гранулят сушат, подвергают сухой грануляции и опудривают оставшимися кросповидоном и крахмалом, тальком, кислотой стеариновой и/или ее солями. Полученную смесь таблетируют. Ядра таблеток имеют среднюю массу 0,25 г.
Ядра таблеток покрывают оболочкой, имеющей следующий состав, % от общей массы оболочки:
I слой
Этацел - 0,05-0,4
Полиэтиленгликоль 6000 - 0,05-0,5
II слой
Сахар - 70,0-90,0
Поливинилпирролидон - 0,2-0,6
Натрий карбоксиметилцеллюлоза - 0,3-1,2
Твин 80 - 0,08-0,3
Тальк - 5,0-9,0
Титана диоксид - 0,3-3,0
Аэросил - 0,15-0,5
III слой
Сахар - 4,0-9,0
Opalux AS 9840 Brown - 1,0-3,0
IV слой
Полиэтиленгликоль 6000 - 0,06-0,2
Глицерин - 0,005-0,03
Процесс покрытия проводят в дражировальном котле. Получают таблетки "Карсилин" с оболочкой коричневого цвета и со средней массой 0,45 г.
Проведено изучение опытного препарата - таблеток "Карсилин" в сравнении с драже "Карсил" фирмы "Софарма", Болгария.
Изучение биодоступности сравниваемых препаратов провели на белых крысах-самцах Wistar с массой тела 190-210 г. Крысам вводили в виде суспензии растертую массу сравниваемых таблеток и драже в дозе 600 мг/кг в пересчете на активное вещество. Суспензию готовили непосредственно перед введением животным. Пробы крови отбирали после декапитации крыс под эфирным наркозом через 1, 2, 3, 4, 5, 6 и 8 ч после введения препарата. Для каждой временной точки использовали 8 животных.
Подготовленные соответствующим образом пробы крови анализировали на жидкостном хроматографе "Милихром-5" с колонкой, наполненной "Диасорб C16". В качестве подвижной фазы использовали систему растворителей ацетонитрил-вода-ледяная уксусная кислота (49:50:1). Детектирование осуществляли при длине волны 280 нм. Расчет содержания препарата в сыворотке крови проводили по градуировочному графику. Так как силимарин представляет собой сумму различных флавонолигнанов, которые имеют различные растворимость в воде, скорость и степень всасывания и элиминации, то при проведении данного исследования в расчет брали только один из пиков на хроматограммах раствора рабочего стандарта силимарина (максимальный), результаты по которому отличались большей воспроизводимостью.
Результаты количественной оценки содержания силимарина в сыворотке крови при пероральном введении сравниваемых лекарственных форм представлены на чертеже. В таблице 1 приведены основные фармакокинетические параметры, рассчитанные с учетом двухкамерной модели, которой описываются полученные концентрационные кривые.
Для оценки фармакокинетики и биодоступности рассчитывали константы скоростей всасывания, распределения, элиминации, максимальную концентрацию препарата в крови и время ее достижения, периоды полувсасывания и полувыведения, среднее время удерживания. Из полученных результатов следует, что концентрационные профили силимарина для двух лекарственных форм различаются незначительно. Максимальное количество препарата в крови при применении обеих лекарственных форм наблюдается через 3 ч. Применение таблеток "Карсилин" обеспечивает несколько больший уровень концентраций действующих веществ в крови через 3 и 4 ч по сравнению с "Карсилом". Однако уровни концентраций достоверно не отличаются (Р>0,05) и составляют через 3 ч (19,1±3,8) и (16,5±2,9) мкг/мл, через 4 ч - (16,2±2,3) и (11,3±1,7) мкг/мл соответственно. Константы скоростей всасывания и время полувсасывания составляют K01= 0,735 ч-1, T0,5;01= 0,94 ч и К01=0,557 ч-1, T0,5;0,1=1,2 ч соответственно. Полученные результаты позволяют сделать вывод, что применение таблеток "Карсилин" обеспечивает 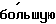 скорость всасывания, чем применение драже "Карсил".
скорость всасывания, чем применение драже "Карсил".
После достижения максимальной концентрации силимарин распределяется в органах и тканях также с примерно одинаковой скоростью. Значение среднего времени удерживания для сравниваемых лекарственных форм также практически одинаково - 5,8 и 5,5 ч. Расчет констант перехода препарата в периферическую камеру из центральной и обратно показывает, что силимарин не накапливается в организме.
В то же время площади под фармакокинетическими кривыми различаются. Относительная биодоступность силимарина при применении опытной лекарственной формы составляет 126% по сравнению с препаратом сравнения. Увеличение биодоступности связано с тем, что при применении таблеток "Карсилин" обеспечивается более быстрое поступление препарата в системный кровоток и, как следствие этого, поступление большего количества препарата в кровь.
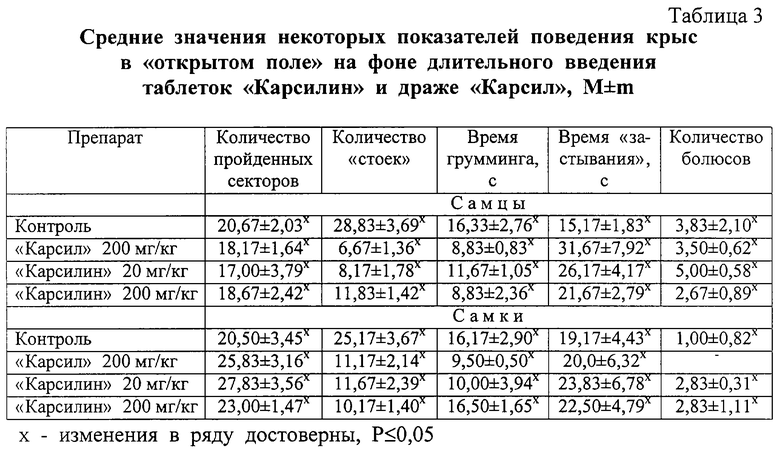
Для подтверждения полученных данных была изучена фармацевтическая доступность силимарина из изучаемых лекарственных форм методом "вращающейся корзинки" в соответствии с требованиями ГФ XI. Полученные данные представлены в таблице 2. Из таблицы видно, что скорость высвобождения силимарина из опытной лекарственной формы на 30% больше скорости его высвобождения из препарата сравнения (за 3 ч наблюдения). Это согласуется с результатами фармакокинетического эксперимента.
Таким образом, проведенное сравнительное изучение фармакокинетики и биологической доступности двух лекарственных форм, содержащих сумму флаволигнанов расторопши пятнистой, - таблеток "Карсилин" и драже "Карсил" показало, что по степени биологической доступности таблетки "Карсилин" незначительно превосходят препарат сравнения. В то же время при применении таблеток "Карсилин" препарат быстрее всасывается в кровь, что обеспечивает более высокие уровни его концентрации в крови и несколько большую биологическую доступность. Увеличение относительной биологической доступности связано с тем, что таблетки "Карсилин" обеспечивают большую скорость высвобождения действующих веществ. Однако в связи с тем, что различия в биодоступности незначительны, можно считать данные лекарственные формы биоэквивалентными.
Изучение специфической гепатозащитной активности таблеток "Карсилин" и драже "Карсил" проводили на 84 рандомбредных взрослых белых крысах обоего пола массой 143,3-215,0 г. Все животные были разделены на 7 групп, в каждой по 6 самок и 6 самцов. Препараты вводили животным перорально с помощью зонда в виде суспензии в дозе 200 мг/кг.
Специфическую гепатозащитную активность таблеток "Карсилин" и драже "Карсил" изучали путем лечебно-профилактического введения препаратов крысам с использованием модели острого гепатита. В качестве гепатотропного яда использовали 50% раствор четыреххлористого углерода (ССl4) в вазелиновом масле в дозе 3 мл/кг массы тела животного. Препараты вводили в течение 6 дней до введения гепатотоксина, а затем параллельно с исследуемыми средствами через день троекратно вводили перорально четыреххлористый углерод через час после введения препарата.
Модель лекарственного гепатита создавали введением парацетамола в дозе 700 мг/кг через день в течение 2 дней.
Четыреххлористый углерод является промышленным гепатотропным ядом. Парацетамол широко используется как жаропонижающее, болеутоляющее и противовоспалительное средство, в том числе в детской практике. Его побочный эффект - гепатотоксичность.
Контролем служили группы крыс, которым вводили четыреххлористый углерод и парацетамол в тех же дозах. Интактные животные получали 1 мл воды.
Животных забивали через сутки после введения последней дозы токсиканта. При вскрытии крыс взвешивали печень с целью определения относительной массы. Известно, что при остром гепатите размеры печени могут резко увеличиться. Поэтому представляло интерес частично оценить по изменению данного показателя гепатозащитное действие "Карсилина" в сравнении с "Карсилом".
С целью оценки влияния на функциональную активность печени сравниваемых препаратов были проведены следующие биохимические исследования:
- общий белок определяли унифицированным способом с биуретовым реактивом;
- альбумины определяли реакцией с бромкрезоловым зеленым;
- мочевину определяли по цветной реакции с диацетилмонооксимом;
- тимоловую пробу проводили методом Хуэрго и Поппера;
- холестерин определяли методом Илька;
- билирубиновые фракции определяли диазометодом по Йендрашику, Клеггорну, Грофу;
- активность наиболее важных аминотрансфераз - аланинаминотрансферазы (АлАТ) и аспартатаминотрансферазы (АсАТ) определяли методом Райтмана-Френкеля;
- активность щелочной фосфатазы (ЩФ) в сыворотке крови определяли реакцией гидролиза с п-нитрофенилфосфатом.
Относительная масса печени у животных с ССl4-гепатитом была на 27,59% у самцов и на 30,25% у самок больше, чем у интактных крыс.
Парацетамоловый гепатит дал увеличение печени по отношению к массе тела на 12,53% у самок и на 10,88% у самцов в сравнении со здоровыми крысами.
Применение "Карсила" у животных с моделью CCl4-гепатита привело к снижению относительной массы печени в сравнении с животными контрольной группы на 4,69% у самок и на 3,91% у самцов. На фоне таблеток "Карсилин" в тех же условиях относительная масса печени снизилась на 13,03% у крыс-самок и на 12,27% у крыс-самцов. То есть "Карсилин" при токсическом гепатите снизил размеры печени на 8,3% больше, чем "Карсил".
На фоне парацетамолового гепатита по отношению к интактным животным "Карсилин" и "Карсил" повысили относительную массу печени в среднем на 10%, а в сравнении с контрольными крысами - в среднем на 2%.
Таким образом, измерение относительной массы печени показало, что четыреххлористый углерод по сравнению с парацетамолом дает более выраженный гепатит, на фоне которого эффект от таблеток "Карсилин" на 8% выше, чем от драже "Карсил".
Установлено, что четыреххлористый углерод снижал содержание общего белка в сыворотке крови на 36% у самок и 39,9% у самцов. "Карсилин" и "Карсил" увеличивали содержание белка в крови крыс-самок соответственно на 12,68 и 15,81% в сравнении с содержанием белка в крови контрольных крыс-самок (с моделью ССl4-гепатита). У крыс-самцов в аналогичных условиях белок крови повышался на 17,54% при применении "Карсилина" и на 17,79% при применении "Карсила".
Уровень альбуминов в крови самок, получавших с лечебно-профилактической целью "Карсил", был на 30,59%, а у получавших "Карсилин" на 24% выше, чем у контрольных групп крыс (ССl4-гепатит). У самцов данный показатель "Карсилин" повысился на 29,73%, "Карсил" - на 20,7% в сравнении с группой нелеченных крыс-самцов.
Содержание глобулинов в крови самок повысилось на 3,3% при применении как "Карсилина", так и "Карсила". У самцов уровень глобулинов увеличился на фоне "Карсила" на 14,9%, на фоне "Карсилина" - на 7,14%, то есть у самцов глобулиновая фракция белков была несколько выше, чем у самок в сравнении с контрольной группой животных (ССl4-гепатит). Аналогично изменялся коэффициент альбумины/глобулины.
Таким образом, "Карсилин" и "Карсил" давали близкий, но не очень выраженный эффект по восстановлению общего белка и его фракций в крови как самок, так и самцов.
На фоне парацетамолового гепатита у крыс-самцов альбуминовая фракция на фоне "Карсила" возросла на 17,6%, на фоне "Карсилина" - на 28,4%, уровень глобулинов вырос на 2,7-5,3%, у самок уровень альбуминов и глобулинов изменялся таким же образом.
Следовательно, на фоне парацетамолового гепатита восстановление уровня белка в крови при применении "Карсилина" в среднем выше на 10%, чем при использовании "Карсила".
При парацетамоловом гепатите лечебно-профилактическое воздействие на белково-синтетическую функцию печени как у "Карсилина", так и у "Карсила", было выше, чем на фоне ССl4-гепатита.
Показатель тимоловой пробы при ССl4-гепатите вырос у самок на 560%, у самцов на 448%, а на фоне парацетамолового гепатита - на 437,5% и на 342% соответственно у самок и самцов в сравнении с интактными крысами.
"Карсил" снижал пробу на фоне парацетамолового гепатита до 115%, а "Карсилин" до 128,8%, то есть оба препарата работали практически одинаково. На фоне ССl4-гепатита "Карсил" снизил показатель тимоловой пробы всего на 24%, а "Карсилин" на 22% в сравнении с контролем, то есть почти в равной степени, но в сравнении со здоровыми крысами этот показатель был довольно высоким как у самок (402,5 и 413,75%), так и у самцов (318 и 300%). В целом показатель тимоловой пробы оба препарата снижали в среднем на 20-25%.
Содержание мочевины при токсическом гепатите снизилось на 41,7% у самок и на 46,1% у самцов. На фоне парацетамола детоксикационная функция печени снижалась в меньшей степени. "Карсил" и "Карсилин" повысили содержание мочевины в сыворотке крови крыс с моделью ССl4-гепатита на 38-40% у самок и на 43,7-42,3% у самцов. На фоне парацетамолового гепатита содержание мочевины в крови увеличилось по сравнению с контролем на 23,3 и 22,5% у самок и на 31,2 и 29,0% у самцов при применении "Карсила" и "Карсилина" соответственно.
Оба препарата незначительно повысили уровень холестерина на фоне CCl4-гепатита (на 1-3%), несколько больше - на фоне парацетамолового гепатита (на 13-14%), то есть при лекарственном гепатозе оба препарата в большей степени нормализовали показатель жирового обмена.
Содержание общего билирубина при острых гепатитах увеличилось на 105,9-154,9% у самок и самцов. Введение "Карсила" и "Карсилина" уменьшило уровень билирубина у животных обоих полов с обеими моделями гепатита в среднем на 50%. Концентрация прямого билирубина при CCl4-гепатите выросла на 400,0 и 278,3% у самок и самцов соответственно. "Карсил" и "Карсилин" уменьшили его в 2 раза как у самок, так и у самцов. На фоне парацетамолового гепатита эффект обоих препаратов проявился аналогично.
Таким образом, концентрация общего и прямого билирубина в сыворотке крови крыс, получавших "Карсил" и "Карсилин", снизилась практически в равной мере, что говорит о восстановлении пигментного обмена под влиянием препаратов.
Активность трансаминаз на фоне ССl4-гепатита повысилась. Для АсАТ это увеличение составило 200,0% у самок и 184,0% у самцов, для АлАТ - 452,6% у самок и 430,0% у самцов соответственно. При применении обоих препаратов на фоне ССl4-гепатита активность АсАТ снизилась незначительно, а на фоне лекарственного гепатита - в 3,5-4 раза у самок и в 5-17 раз у самцов. "Карсилин" снижал уровень АсАТ в большей степени. Уровень АлАТ снизился на 1/3 при введении "Карсила" и "Карсилина" у крыс обоих полов с моделью ССl4-гепатита. На фоне парацетамолового гепатита уровень АлАТ снизился в 3-4 раза у самок и самцов при применении обоих препаратов. Коэффициент де Ритиса (соотношение АсАТ/АлАТ) у самок всех подопытных групп был ниже нормы (1,33). Аминокислотный баланс значительно возрастал при введении "Карсила" и "Карсилина" крысам с парацетамоловым гепатитом, но не полностью.
Лечебно-профилактическое применение препаратов уменьшало активность щелочной фосфатазы в среднем в 2 раза как у самок, так и у самцов.
Результаты биохимических исследований сыворотки крови показали, что влияние таблеток "Карсилин" и драже "Карсил" на обменные, метаболические, синтетические, дезинтоксикационные, холеретические функции печени почти равноценно, хотя на фоне ССl4-гепатита оно выражено в меньшей степени, чем на фоне парацетамолового гепатита. Различия в действии препаратов по многим показателям недостоверны и указывают на небольшое снижение процессов цитолиза и холестаза в печени.
При вскрытии животных визуально оценивали состояние печени. У интактных крыс печень была темно-красного цвета, упругая, с гладкой блестящей поверхностью, капсула печени прозрачная. Ткань печени на срезе была однородная, сосуды заполнены кровью.
У крыс с моделью острого ССl4-гепатита печень была светло-бурого цвета, тусклая, рыхлая. Ткань печени легко травмировалась.
У животных с моделью острого парацетамолового гепатита ткань печени была довольно плотная, темно-красного цвета, на срезе были видны бурые вкрапления в виде точек разной величины.
У крыс, которым вводили "Карсилин" и "Карсил" на фоне острого ССl4-гепатита, ткань печени была более плотная, чем у крыс с чистой моделью ССl4-гепатита. Цвет печени был красно-бурый.
Печень животных, которые получали препараты на фоне острого парацетамолового гепатита, внешне была похожа на здоровую, но местами на поверхности виднелись бурые пятнышки, говорящие о частичном токсическом воздействии больших доз (700 мг/кг) парацетамола.
Провели микроскопические исследования при применении "Карсилина" и "Карсила" в дозе 200 мг/кг на фоне последующего введения парацетамола в дозе 700 мг/кг. Установлено, что в печени сохраняются признаки подострого медикаментозного очажкового гепатита с преимущественно портальной локализацией. В то же время обращает на себя внимание появление микроструктурных эквивалентов развития компенсаторно-приспособительных процессов в печени. Они заключаются в увеличении размеров клеток, активизации пластической их функции, гиперхромии ядер, контурируемости хроматина, набухании ядрышек, появлении двуядерных гепатоцитов, активизации клеточных коопераций.
Провели микроскопические исследования при использовании "Карсилина" и "Карсила" в дозе 200 мг/кг с последующим введением четыреххлористого углерода в виде 50% раствора в вазелиновом масле в дозе 3,0 мл/кг. Установлено, что при применении "Карсила" с последующим введением черыреххлористого углерода в печени крыс диагностирован диффузный подострый токсический альтеративно-экссудативный паренхиматозно-интерстициальный гепатит с частичной узелковой трансформацией и гиперплазией отдельных групп гепатоцитов. В данной серии опытов не обнаружено гепатопротекторное действие "Карсила", но некоторой тенденцией к этому можно считать, с известной долей условности, наличие узелковой трансформации и очаговой гиперплазии клеток печени.
Во всех сериях опытов не обнаружено принципиальных различий в патологии печени и развитии репаративных процессов (они протекали по типу субституции) у крыс обоего пола как при применении "Карсилина", так и на фоне "Карсила".
Кроме того, было проведено сравнительное изучение "острой" и хронической токсичности таблеток "Карсилин" и драже "Карсил".
Исследования общетоксического действия препаратов провели на 72 нелинейных белых мышах обоего пола массой по 25-30 г и на 80 беспородных белых крысах обоего пола массой по 150-220 г.
"Острую" токсичность препаратов определяли методом Кербера.
Суспензию препаратов вводили мышам перорально с помощью иглы с оливой в дозах 4000, 4500, 4600, 4700, 4800, 5000 мг/кг. Препараты вводили в течение суток через каждые 3-4 ч. Животные были разделены на 6 групп по 6 мышей в каждой. Часть мышей получала суспензию опытного препарата, другая часть - суспензию препарата сравнения. В течение первых суток за мышами вели тщательное наблюдение, отмечая поведение, потребление пищи, воды, а также общее состояние. Погибших мышей вскрывали и обследовали макроскопически. За выжившими животными наблюдали в течение 2-х недель.
При изучении хронической токсичности препаратов все крысы были разделены на 4 группы по 20 крыс в каждой (10 самок и 10 самцов). Две группы животных получали ежедневно в течение 2-х месяцев за час до кормления водную суспензию таблеток "Карсилин": первая группа в дозе 20 мг/кг, вторая группа - 200 мг/кг. Третьей группе вводили при тех же условиях суспензию драже "Карсил" в дозе 200 мг/кг. Четвертой группе вливали в желудок через зонд по 1 мл воды. Количество корма и воды для крыс не ограничивали. Ежедневно визуально оценивали состояние животных.
Общетоксическое действие таблеток "Карсилин" оценивали по их влиянию на различные показатели и функции организма. В течение первого месяца животных еженедельно взвешивали до кормления. Последний контроль веса провели перед забоем. По ходу опыта следили за внешним видом животных, работой сердца, дыхательной системы, состоянием волосяного покрова, двигательной активностью. Влияние таблеток "Карсилин" на ЦНС оценивали методом "открытого поля". Полученные при этом показатели поведения животных позволили судить о влиянии "Карсилина" на двигательную активность, исследовательскую и эмоциональную деятельность, отражающие работу ЦНС. Каждое животное тестировалось один раз.
Характер и степень токсического действия таблеток "Карсилин" в сравнении с драже "Карсил" при длительном применении оценивали путем гематологических, биохимических и патологоанатомических исследований.
Патоморфологические исследования проводили макроскопически при забое, для микроскопических исследований органы соответствующим образом подготавливали.
При введении первых порций токсических доз "Карсилина" и "Карсила" поведение белых мышей несколько угнеталось на 2-5 мин, в последующие 3-4 ч их двигательная активность, поведение, внешний вид не отличались от данных показателей у мышей контрольной группы. Ритм сердечных сокращений до введения препаратов составлял от (450,0±10,2х) до (500±12,5x) уд/мин (x - изменения в ряду достоверны, Р≤0,05). Через 5-10 мин после интрагастрального введения суспензий "Карсилина" и "Карсила" в объеме 0,5 мл ритм увеличивался от (560,0±8,5х) до (640,0±16,6х) уд/мин, а через 40-60 мин ритм восстанавливался. Число исходных дыхательных движений составляло до введения препаратов в среднем 146,7±14,8х, через 5-10 мин после введения - 160,0±5,4x, затем ритм дыхания восстанавливался. Потребление мышами пищи и воды уменьшалось. Наклон волосяного покрова не изменялся, судорог не наблюдалось, координация движений не нарушалась.
При введении суспензий препаратов в объеме 0,5 мл 4-6 раз с интервалами в 3-4 ч (максимальная доза) поведение животных изменялось. Уменьшалась их двигательная активность, постепенно снижались ритм сердечных сокращений и число дыхательных движений до их полного прекращения. За выжившими мышами наблюдали в течение 2-х недель. Через сутки после введения токсических доз их внешний вид и поведение не отличались от внешнего вида и поведения контрольных мышей. Погибших мышей вскрывали. Во внутренних органах была видна гиперемия, кишечник содержал препарат и был значительно расширен из-за большого объема введенных изучаемых средств. Из мышей, получивших токсические дозы "Карсилина", погибло 16, причем 11 из них погибли в первые сутки после введения последней порции токсической дозы - в основном через 5-8 ч. Остальные 5 мышей погибли на вторые сутки. При расчете LD50 для таблеток "Карсилин" получен результат 4666,67 мг/кг.
При введении токсических доз драже "Карсил" из 36 мышей погибло 12. Картина их гибели была схожа с картиной смерти мышей от максимальных доз "Карсилина". Расчет показал, что для "Карсила" значение LD50 составляет 4775,0 мг/кг, то есть токсичность у "Карсила" несколько меньше, чем у "Карсилина". Токсическое действие таблеток и драже на самок и самцов было одинаковым, то есть половая чувствительность к препаратам отсутствовала.
Таким образом, изучение "острой" токсичности таблеток "Карсилин" в сравнении с драже "Карсил" показало, что по классификации опасности оба лекарственных препарата могут быть отнесены к умеренно опасным веществам (III класс), а по классификации токсичности - к относительно безвредным средствам (VI класс токсичности).
При изучении хронической токсичности препаратов в течение 2-х месяцев запаивания животных не погибла ни одна крыса ни в контрольной, ни в опытных группах. Первые 7-10 дней крысы во время введения суспензии "Карсилина" и "Карсила" проявляли некоторое беспокойство, настороженность, на боль отвечали гиперреакцией. В дальнейшем, по ходу исследования, данные явления уменьшались, животные вели себя спокойно и в момент работы с ними, и в течение всего дня. Агрессивности не отмечалось ни среди самок, ни среди самцов. Внешний вид подопытных крыс был обычным, не отмечалось изменения цвета шерстки, наклона волосяного покрова. Цвет носов и лапок в сравнении с животными контрольных групп был одинаковым. Корм животные употребляли в неограниченном количестве, отправления были в несколько больших количествах, чем у контрольных крыс, и в целом почти всегда оформленными. Воду животные потребляли в количестве от 200 до 300 мл в сутки на группу, состоящую из 10 крыс.
В первую неделю эксперимента животные практически не прибавляли в весе, к концу первого месяца прибавка в весе составила 11-17%, в течение второго месяца применения препаратов вес животных стабилизировался, в то время как в контрольных группах он увеличился на 7-10%.
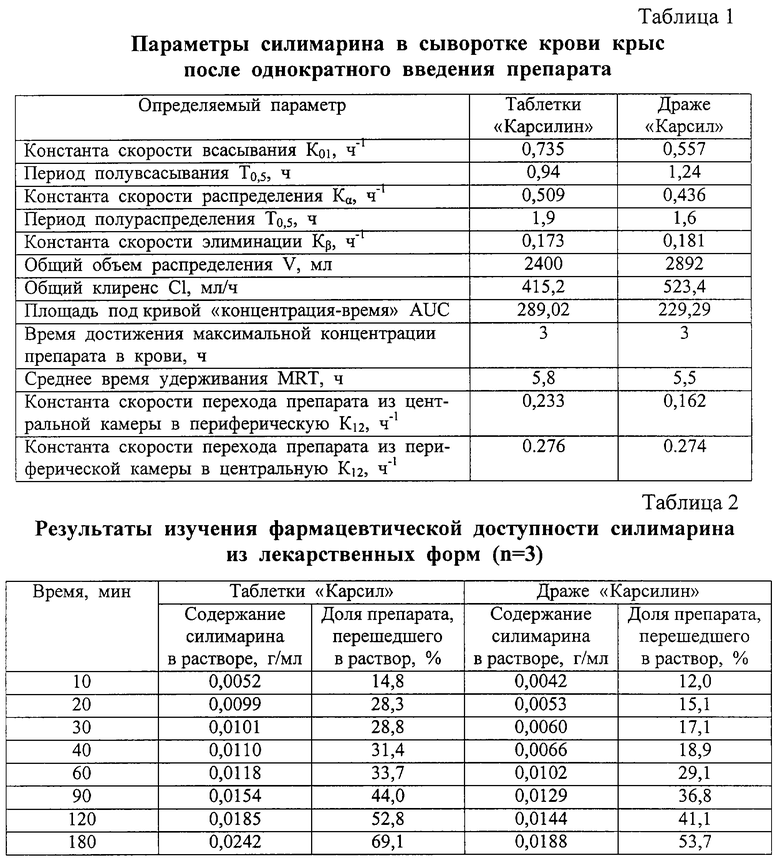
Результаты контроля влияния препаратов на ЦНС отражены в табл.3.
Двигательная активность самцов при введении "Карсилина" и "Карсила" снизилась в отличие от контрольных групп в среднем на 15%, а у самок количество пройденных секторов увеличилось на 12-30%. В обеих группах животных снизилась ориентировочно-познавательная деятельность. Число стоек на фоне введения обоих препаратов уменьшилось на 60-75%.
Время умывания (грумминга) в контрольных группах составило у самцов и самок соответственно (16,33±2,76x) и (16,17±2,9x) с. При применении "Карсила" этот показатель составил (8,83±0,83x) с (самцы) и (9,50±0,5x) с (самки). При введении "Карсилина" в той же дозе самцы умывались (8,83±2,36) с, а самки (16,5±1,65) с. Время застывания на фоне обоих препаратов у самцов увеличилось в большей степени (на 43-100%), а у самок - в меньшей степени (на 4-24%).
В связи с этим можно сказать, что в использованных дозах оба препарата уменьшали эмоциональную деятельность. Общая оценка тестирования крыс в "открытом поле" позволяет предположить, что "Карсилин" так же, как и "Карсил", действует на ЦНС крыс угнетающе (успокаивающе).
Результаты клинических анализов крови показали, что содержание эритроцитов у самцов и самок, получавших "Карсилин" и "Карсил", практически не отличалось ни в опытных, ни в контрольной группах животных. Гемоглобин (Hb) у животных, которым вводили "Карсилин" в дозе 20 мг/кг, был на 20 г/л выше, чем у крыс других групп, как опытных, так и контрольных. Скорость оседания эритроцитов (СОЭ) у всех животных не отклонялась от нормы, но у самцов "Карсилин" увеличивал СОЭ в 2,2 раза в сравнении с "Карсилом", хотя данные изменения были недостоверны. Процент ретикулоцитов в крови, а также гематокрит находились в допустимых пределах при применении обоих препаратов, но их число было в рамках допустимого как у самцов, так и у самок. Осмотическая резистентность эритроцитов составила 0,35-0,45 ед., причем ее увеличение на фоне "Карсилина" у крыс-самцов (в обеих дозах) до 0,45 ед. было достоверно в сравнении с контролем и "Карсилом" и не выходило за пределы нормы. У самок осмотическая резистентность эритроцитов изменялась незначительно. Увеличение числа тромбоцитов на фоне "Карсила" и "Карсилина" было незначительным (на 2-3%) и не выходило за рамки нормы (у животных (522,0±33,0)109/л). Число лейкоцитов составило (4,10±0,19x)109/л - (4,46±0,19x)109/л у самцов и (4,02±0,08х)109/л - (4,52±0,47x)109/л у самок, в том числе на фоне "Карсилина" в дозе 200 мг/кг число лейкоцитов было на (0,18-0,22)109/л больше, чем при применении "Карсила". В сравнении с контролем изменения числа лейкоцитов были недостоверны. В лейкоцитарной формуле изменения недостоверны за исключением процента изменения содержания эозинофиллов при введении "Карсилина". Содержание эозинофиллов в крови у самцов и самок на фоне "Карсилина" увеличилось достоверно в отношении "Карсила", но не выходило за рамки нормы. Количество сегментноядерных нейрофиллов колебалось у самцов от (20,69±0,46х)% (на фоне "Карсилина" в дозе 20 мг/кг) до (22,06±0,75х)% (на фоне "Карсила"). Процент содержания лимфоцитов был от 65,56±2,17х (у самцов на фоне "Карсила") до 70,54±1,42х (у самок на фоне "Карсила"). Грубых сдвигов в лейкограмме в сравнении с контрольной группой крыс применение обоих препаратов не давало. При этом изменения клинических показателей крови животных при применении "Карсилина" и "Карсила" отличались незначительно и, в основном, кроме количества эозинофиллов, недостоверно. Все клинические показатели крови при длительном применении "Карсилина" и "Карсила" не выходили за пределы нормы.
В ходе исследования состава мочи белок, глюкоза, кетоны, гемоглобин, желчные пигменты не определялись ни в контрольных, ни в подопытных группах животных. Удельный вес мочи составил в среднем (1,006±0,0005x) г/мл. Значение рН мочи в контрольной группе составило 6,34±0,16х, на фоне "Карсила" (200 мг/кг) у самок - 6,65±0,21х, у самцов - 7,45±0,11. При применении "Карсилина" в дозе 20 мг/кг рН равнялся 6,98±0,08х и 7,05±0,14х у самок и самцов соответственно. При увеличении дозы "Карсилина" до 200 мг/кг рН мочи у самок повышался до 7,07±0,19х, а у самцов до 7,45±0,15х.
К 3-му часу сбор мочи под водной нагрузкой у крыс, получавших таблетки "Карсилин", составил (4,5±0,05х) мл (самки) и (4,3±0,04х) мл (самцы).
На фоне драже "Карсил" диурез в сравнении с "Карсилином" был почти одинаковым как у самок, так и у самцов. Мочеотделение у контрольных крыс составило (3,6±0,05х) и (3,8±0,04х) мл у самок и самцов соответственно.
Таким образом, установлено, что длительное применение обоих исследованных препаратов несколько увеличивало диурез, причем практически в равной мере.
Микроскопический анализ осадка мочи показал отсутствие в ней эритроцитов, гиалиновых и зернистых цилиндров, почечного эпителия, микрофлоры. В осадке мочи некоторых крыс во всех группах (и контрольных, и подопытных) определялся единичный эпителий мочевыводящих путей - не более 3-4 клеток в поле зрения. Лейкоциты в осадке мочи присутствовали в количестве 1-4 у животных всех групп. Количество слизи в моче было незначительным или умеренным. Из солей встречались в основном оксалаты и кое-где ураты.
Таким образом, клинический анализ состава мочи показал, что таблетки "Карсилин" так же, как и драже "Карсил", не вызывают почечной патологии, способны сдвигать рН мочи в щелочную сторону и оказывать небольшой диуретический эффект.
Введение "Карсилина" в сравнении с "Карсилом" в незначительной степени и недостоверно понижало уровень глюкозы как у самок, так и у самцов, в отличие от контрольной группы. Изменения содержания общего белка и белковых фракций имели тенденцию к увеличению при введении как "Карсила", так и "Карсилина", а отличия в их действии были недостоверны (P2>0,05). Показатель тимоловой пробы у самок, получавших "Карсил", снижался на 46,25% в сравнении с контролем, а на фоне "Карсилина" в той же дозе - на 23,75%. Уменьшение дозы "Карсилина" в 10 раз приводило к снижению тимоловой пробы на 10%. У самцов данный показатель понижался в меньшей степени и почти однозначно (в среднем на 20%). При сравнительной оценке обоих препаратов на показатель тимоловой пробы значения носили характер недостоверности.
Оба препарата достоверно (Р≤0,05) повышали дезинтоксикационную функцию печени, что видно по приросту уровня мочевины в крови, но "Карсилин" делал это в большей степени и достоверно по отношению к "Карсилу". Холестерин в сыворотке крови снижался при применении "Карсила" у самок на 13,25%, у самцов на 10,59%. "Карсилин" в обеих дозах (20 и 200 мг/кг) снижал данный показатель на 7% в среднем. По отношению к контролю изменения были достоверны.
Содержание билирубина общего и прямого в сыворотке крови крыс снижалось, причем процент уменьшения общего билирубина как у самок, так и у самцов, при введении "Карсилина" был ниже на 4-5%, чем на фоне "Карсила". В целом показатели свидетельствуют о благоприятном влиянии препаратов на липидный обмен.
При введении "Карсилина" в дозе 200 мг/кг активность трансаминаз снижалась у самок на 4,40% для АcАТ и 6,72% для АлАТ, а у самцов - на 7,88 и 11,96% соответственно. На фоне "Карсила" в той же дозе активность АcАТ была ниже на 8,75%, АдАТ - на 10,45%, а у самцов - соответственно на 4,25 и 8,22%. При введении "Карсилина" в дозе 20 мг/кг изменения были менее выражены или отсутствовали. Активность щелочной фосфатазы в сыворотке крови крыс на фоне "Карсилина" снижалась у самок на 23-30%, у самцов на 15,66-23,14%. При введении "Карсила" этот показатель снижался на 36,77% (самки) и 25,63% (самцы).
При сравнении активности "Карсилина" и "Карсила" изменения недостоверны, то есть их активность в отношении холеретической и антихолеретической функции печени близка.
Таким образом, биохимические исследования сыворотки крови крыс, получавших в течение двух месяцев в виде суспензии таблетки "Карсилин" в сравнении с драже "Карсил", показали, что в метаболических, дезинтоксикационных, обменных функциях жизненно важных органов (печени, почек) на их фоне произошли положительные изменения (активация функций), причем изменения на фоне "Карсилина" по отношению к "Карсилу" были недостоверны по многим показателям, то есть очень близкими.
Проведены макро- и микроскопические исследования внутренних органов животных после длительного введения им таблеток "Карсилин".
При забое производили вскрытие животных, осматривали внутренние органы. Некоторые органы были взвешены. Значительного отклонения массы органов в процентном отношении от массы тела не выявлено.
По расположению внутренних органов у животных всех групп констатирована норма. Ткани грудной клетки, брюшной полости бледно-розовые, блестящие, гладкие, мест сращения нет. Сердце темно-красного цвета с небольшим количеством крови. В полостях сердца видимой патологии нет. Перикард легко отделяется и имеет нормальную влажность. Ткань легкого с пенистым содержимым. Желудок заполнен небольшим количеством пищи. При разрезе по большой кривизне видна складчатая серо-розовая слизистая желудка. Проходимость желудочно-кишечного тракта не нарушена. Кишечник частично заполнен пищевыми массами, его тонус снижен у всех крыс в равной степени.
Печень имеет красно-бурую окраску, ее поверхность гладкая, покрыта серозной блестящей оболочкой. Ткань печени плотная, в разрезе однородная, темно-красного цвета с умеренным кровенаполнением сосудов. Поджелудочная железа серовато-красного цвета, дольчатая, зернистая, покрыта блестящей капсулой. Желчь у подопытных крыс более прозрачная и светлая, чем у животных контрольных групп.
Форма почек правильная, бобовидная. Почки темно-красного цвета, плотной консистенции. Снаружи фиброзная капсула, которая легко снимается с почек всех животных. Практически у всех крыс почки окружены жировой клетчаткой в виде капсулы. На разрезах почек видны корковый и мозговой слои. Лоханки почек свободные. Мочевой пузырь у некоторых животных слегка заполнен. При разрезе слизистая складчатая, чистая.
Почти у всех крыс селезенка темно-вишневого цвета, поверхность зернистая, на разрезе определяются белая и красная пульпа, сосуды расширены.
Провели изучение микроморфологии внутренних органов крыс после 2-месячного введения им "Карсилина" и "Карсила" в дозе 20 и 200 мг/кг массы тела животного.
Печень. Центральные вены умеренно полнокровные. Балочное строение печеночных долек сохранено. Клетки имеют четкие границы, хорошо контурируемые ядра с зернами хроматина. Полнокровие наблюдается лишь в тех участках синусоидальных капилляров, которые прилежат к центральным венам. Эндотелиальные клетки вытянутой формы. Пространства Диссе не определяются. Топология Pit-cells, звездчатых ретикулоэндотелиоцитов, в структуре печеночной дольки не изменена. В цитоплазме как светлых гепатоцитов, так и темных, обнаруживается зернистость. Клетки в состоянии гидропической белковой дистрофии, а также в состоянии жирового метаморфоза, отсутствуют. Сосуды триад с умеренным полнокровием в просветах. В строме портальных трактов - обычный клеточный состав. Среди гепатоцитов можно встретить двухядерные клетки.
Желудок. Покровный эпителий сохранен. Он равномерно выстилает желудочные валики, распространяясь на желудочные ямки. Обращает на себя внимание несколько увеличенное содержание муцина в клетках покровного эпителия и на его поверхности. Формула железы, то есть соотношение между отдельными гландулоцитами фундальных желез, не изменена. Сосуды собственной пластинки слизистой оболочки умеренно полнокровные.
Тонкий кишечник. Ворсинки тонкие, выстланы преимущественно каемчатыми энтероцитами. Количество бокаловидных клеток не увеличено. Эпителий ворсин, крипт сохранен во всех наблюдениях. Клеточные составляющие лимфоидных фолликулов (пейеровы бляшки) не изменены ни количественно, ни качественно. Сосуды микроциркуляторного русла слизистой пластинки умеренно полнокровные.
Почки. Капилляры клубочков умеренно полнокровные. Просветы капсул свободные. Синехий между висцеральным и париетальным листками капсулы не обнаружено. Пролиферации эндотелия, мезангиальных клеток не наблюдается. Эпителий всех отделов канальцевого аппарата нефрона сохранен. Сосуды кортикального и юкстамедуллярного отделов почки умеренно полнокровные. Следует отметить активное функционирование в юкстамедуллярных отделах перитубулярных интеркапиллярных анастомозов.
Надпочечники. Подразделение структур на корковый и мозговой слои не нарушено. В корковом слое отчетливо дифференцируются клубочковая, пучковая и сетчатая зоны. В двух последних сохраняются "пустоты" в цитоплазме клеток, что наблюдалось и у интактных животных. Хромаффинные клетки мозгового слоя крупные, с хорошо контурируемыми ядрами. Между ними видны синусоидные капилляры.
Селезенка. Трабекулярные сосуды красной пульпы полнокровные. Они окружены муфточками лимфоцитов. В белой пульпе лимфоидные фолликулы четко ограничены. Реактивные центры не выражены. Плазматизации в них не обнаружено. Гиперпластических процессов в тимусзависимых и тимуснезависимых зонах не выявлено.
Легкие. Эпителий во всех подразделах бронхиального древа сохранен. Количество бокаловидных клеток в бронхиолах среднего калибра не увеличено. Просветы терминальных бронхиол, респираторных отделов легких свободные. Межальвеолярные перегородки тонкие. Разрывов, эмфизематозных вздутий в них не обнаружено. Сосуды межальвеолярных перегородок умеренно полнокровные.
Сердце. Волокнистые компоненты эпикарда тонкие. Отчетливо заметна поперечная исчерченность миокардиоцитов. Смещения темных и светлых дисков друг относительно друга, а также по отношению к вставочным пластинкам не обнаружено. Более отчетливо выявляются межмышечные анастомозы. Межмышечные соединительнотканные прослойки - тонкие без очагов базофиллии. Артериолы, венулы, капилляры полнокровные. Просветы их округлой формы без признаков манифестной дилатации или дистонии.
Таким образом, двухмесячное введение "Карсилина" и "Карсила" в дозах 20 и 200 мг/кг не выявило, судя по микроморфологическим данным, деструктивных процессов во внутренних органах. Изменения, обнаруженные в печени (внутриклеточная гиперплазия гепатоцитов, бинуклеарные гепатоциты, активизация пластического обмена в клетках, гиперхроматоз ядер), гастрогипермукоидизация покровного эпителия, функционирование перитубулярных интеркапиллярных ренальных анастомозов, а также межмышечных интракардиальных анастомозов свидетельствуют о формировании адаптационных процессов при длительном применении "Карсилина" и "Карсила" в равной степени.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГЕПАТОЗАЩИТНЫМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2009 |
|
RU2406496C1 |
| НОВЫЙ КОМПЛЕКС БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ ИЗ КОРЫ ЛИСТВЕННИЦЫ-ПИКНОЛАР | 2003 |
|
RU2252028C2 |
| Гепатопротекторное средство | 2015 |
|
RU2614691C2 |
| СБОР ГЕПАТОПРОТЕКТОРНОГО ДЕЙСТВИЯ | 2012 |
|
RU2500418C1 |
| Средство, обладающее гепатопротекторной активностью | 2018 |
|
RU2701567C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНАЛЬГЕЗИРУЮЩИМ, УЛУЧШАЮЩИМ КРОВОСНАБЖЕНИЕ, СТИМУЛИРУЮЩИМ РЕГЕНЕРАЦИЮ НЕРВНОЙ ТКАНИ И ПРОТИВОАЛЛЕРГИЧЕСКИМ ДЕЙСТВИЕМ | 2003 |
|
RU2225707C1 |
| ПРИМЕНЕНИЕ 6-ГИДРОКСИ-2,2,4-ТРИМЕТИЛ-1,2-ДИГИДРОХИНОЛИНА В КАЧЕСТВЕ ГЕПАТОПРОТЕКТОРА | 2017 |
|
RU2677883C1 |
| ЭЛИКСИР, ОБЛАДАЮЩИЙ ОБЩЕУКРЕПЛЯЮЩИМ И АДАПТОГЕННЫМ ДЕЙСТВИЕМ | 2000 |
|
RU2171113C1 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО | 2003 |
|
RU2244553C1 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ПЕЧЕНИ У ЖИВОТНЫХ | 2012 |
|
RU2504347C1 |
Изобретение относится к медицине и касается средства, обладающего гепатозащитным действием. Предложено гепатопротекторное средство, выполненное в виде таблеток, содержащих ядро, покрытое многослойной оболочкой. Ядро таблеток, помимо действующего вещества силимарина, в количестве 10-20% от массы ядра содержит вспомогательные вещества. Таблетки обладают высокой скоростью высвобождения действующего вещества. 3 табл., 1 ил.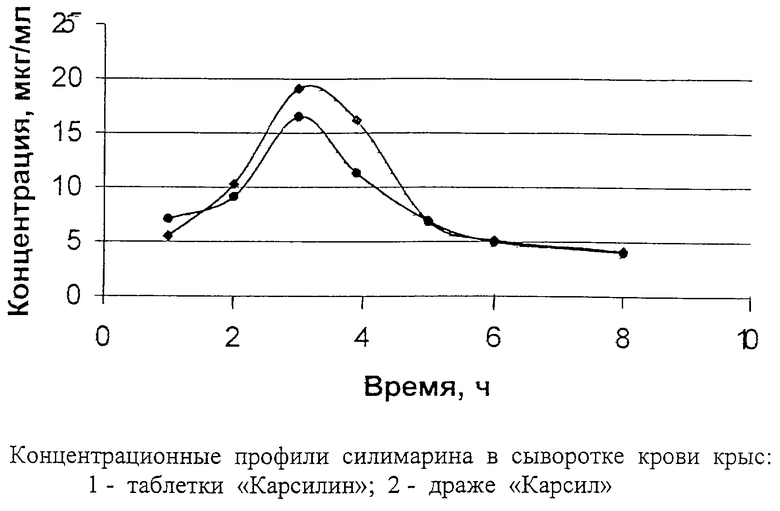
Гепатопротекторное средство, характеризующееся тем, что оно выполнено в таблетированной форме и содержит в качестве активного вещества силимарин в количестве 10-20% от массы ядра таблетки и целевые добавки: микрокристаллическую целлюлозу, лактозу, крахмал кукурузный, кросповидон, поливинилпирролидон, натрия бикарбонат, тальк и кислоту стеариновую и/или ее соли, при этом ядро таблеток покрыто многослойной оболочкой, ингредиенты которых от общей массы оболочки составляют, мас.%:
I слой
Этацел - 0,05 - 0,4
Полиэтиленгликоль 6000 - 0,05 - 0,5
II слой
Сахар - 70,0 - 90,0
Поливинилпирролидон - 0,2 - 0,6
Натрий карбоксиметилцеллюлоза - 0,3 - 1,2
Твин 80 - 0,08 - 0,3
Тальк - 5,0 - 9,0
Титана диоксид - 0,3 - 3,0
Аэросил - 0,15 - 0,5
III слой
Сахар - 4,0 - 9,0
Opalux AS 9840 Brown - 1,0 - 3,0
IV слой
Полиэтиленгликоль 6000 - 0,06 - 0,2
Глицерин - 0,005 - 0,03и
| US 4061765 А, 06.12.1977 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч.1, с.611-612 | |||
| ФЛАВАНО-ЛИГНАНОВАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ЕЕ ОСНОВЕ | 1996 |
|
RU2157225C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА СИЛИБИНИНА С ЦИКЛОДЕКСТРИНОМ, КОМПЛЕКС ВКЛЮЧЕНИЯ СИЛИБИНИНА С ЦИКЛОДЕКСТРИНОМ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНТИГЕПАТОТОКСИЧЕСКОЙ АКТИВНОСТИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1991 |
|
RU2108109C1 |
Авторы
Даты
2003-06-10—Публикация
2002-04-24—Подача