Изобретение относится к медицине, а именно к ультразвуковым исследованиям в онкологии, и может быть использовано при эхокардиографической диагностике у больных в процессе химиотерапии для выявления кардиотоксического эффекта на доклиническом уровне и выбора адекватной тактики лечения и своевременного назначения сопроводительного лечения.
Известно, что антрациклиновые антибиотики, введенные в клиническую практику с начала 70-х годов, стали обязательной составной частью большинства современных противоопухолевых режимов и показали высокую эффективность при лечении гемобластозов, неходжкинских и ходжкинских лимфом, рака молочной железы, легких, костей, мягкотканных сарком (Гершанович Л.М. Проблема кардиозащиты в детской онкологии при лечении антрациклинами. Саттелитный симпозиум в рамках 28-го заседания Международного общества детской онкологии. Вена. Австрия. - Журнал "Вопросы онкологии", 1997, т.43, 2, с.243-247).
Основное побочное действие адриамицина, жестко ограничивающее его суммарную дозу, - кардиотоксический эффект, ведущий к диффузному поражению миокарда, так называемой "кардиомиопатии". В наиболее тяжелых случаях развиваются дилатация полостей сердца, застойная сердечная недостаточность, аритмии, высока вероятность летального исхода несмотря на лечение сердечными гликозидами и диуретиками. С учетом того, что антрациклины входят в очень большое количество программ химиотерапии, в том числе комбинированной, возникновение кардиотоксичности в среднем у 4-5% больных при обычных дозах и до 10% и более в так называемой группе риска (пожилой возраст, сопутствующая сердечно-сосудистая патология, предыдущее облучение левой половины грудной клетки, предшествующая химиотерапия алкилирующими препаратами), то это осложнение может сказаться на значительном контингенте лиц, страдающих злокачественными опухолями.
Несмотря на то, что реализация кардиотоксического эффекта в результате химиолечения происходит чаще у лиц с факторами риска, зависит от суммарной дозы препарата, тем не менее в клинической практике отмечено развитие кардиомиопатии даже при небольших суммарных дозах антрациклинов (100 мг/м2), а также у лиц молодого возраста, не имеющих сопутствующих заболеваний.
Ситуация осложняется также тем, что застойная сердечная недостаточность чаще развивается в сроки от 1 до 231 дня (в среднем 33 дня) после введения последней дозы доксорубицина. Другим неблагоприятным фактором является то, что застойная сердечная недостаточность резистентна к проводимой терапии и носит фатальный характер.
Таким образом, вопросы ранней диагностики возникших кардиотоксических осложнений, являются высоко актуальными в клинической практике.
Современная диагностика кардиотоксичности по клиническим симптомам у онкологических больных затруднена в связи с тем, что они неспецифичны и бывают мало выражены. К тому же такие симптомы как одышка, тахикардия, могут быть обусловлены прогрессированием опухолевого процесса. Потому клиническую картину важно рассматривать в совокупности с данными неинвазивных методов функционального исследования кровообращения.
Известен способ электрокардиографии для функционального исследования сердечно-сосудистой системы с целью оценки кардиотоксичности в процессе химиотерапии (Шхвацабая Л.В., Неклюдова В.И. Дифференциальная диагностика поражения сердца у онкологических больных. - Журнал "Клиническая медицина", 1985, 2, с.73-78).
Изменения на ЭКГ при развитии кардиотоксичности регистрируются у 1-41% больных. Электрокардиографическими признаками кардиотоксического действия антрациклинов являются синусовая тахикардия, экстрасистолия (предсердная и желудочковая), снижение амплитуды зубцов R и Т, формирование отрицательного зубца Т, появление дистрофических изменений миокарда. Однако, такие проявления кардиотоксичности, как кардиалгии, признаки недостаточности кровообращения могут не сопровождаться отрицательной динамикой ЭКГ. Кроме того, у больных с исходной коронарной патологией (ИБС, артериальная гипертония) появление изменений сегмента S-T и отрицательного Т при наличии клинических симптомов этих заболеваний в процессе химиотерапии затрудняет диагностику кардиотоксичности вследствие неспецифичности изменений на ЭКГ.
Известно, что наиболее информативным, неинвазивным и безопасным методом мониторинга сердечно-сосудистой системы у больных, получающих лечение доксорубицином, является эхокардиография (Гершанович М.Л. Кардиотоксичность противоопухолевых антрациклиновых антибиотиков и возможности ее предупреждения кардиосканом (декстразоксаном) в онкологической практике. - Журнал "Вопросы онкологии", т. 47, 2001, 1, с.119-122).
Этот способ выбран нами в качестве прототипа.
Наиболее информативной является двухмерная эхокардиография, позволяющая визуализировать структуру сердечной мышцы (фиброз стенок левого желудочка, наличие выпотного перикардита). Двухмерная эхокардиография позволяет производить количественное измерение объемов левого желудочка и, соответственно, оценивать сократительную способность миокарда, что важно в диагностике субклинической левожелудочковой недостаточности. Сведения же о применении в диагностике кардиотоксичности доплерографии крайне немногочислены.
Исследование динамики диастолической функции левого желудочка в процессе химиотерапии на наш взгляд перспективно в плане ранней диагностики кардиотоксичности, изменение показателей диастолической функции могут быть выявлены уже после первого введения химиопрепарата.
Целью изобретения является ультразвуковая оценка показателей трансмитрального кровотока (диастолической функции левого желудочка) в процессе химиотерапии для ранней доклинической диагностики кардиотоксичности и дальнейшей адекватной коррегирующей сопроводительной терапии.
Поставленная цель достигается тем, что на разных этапах противоопухолевой химиотерапии проводят ультразвуковой мониторинг состояния миокарда методом трансторакальной эхокардиографии с доплерографией. При этом устанавливают, что у некоторых больных уже при первом введении химиопрепарата происходит изменение характеристик трансмитрального потока. Регистрируется появление диастолической дисфункции - преобладание скорости трансмитрального потока во время предсердной систолы - пик Е над скоростью раннего диастолического наполнения - пик А с изменением соотношения Е/А <1,0, у пациентов с исходно неизмененными показателями диастолической функции левого желудочка. Появление диастолической дисфункции у пациенток, получающих химиотерапию после первого введения химиопрепаратов, представляется зарегистрированным проявлением кардиотоксического эффекта на доклиническом уровне, что является ранней диагностикой кардиотоксичности и требует проведения индивидуализированной коррегирующей сопроводительной терапии.
Изобретение "Способ УЗ-оценки кардиотоксичности, индуцированной антрациклинами у онкологических больных" является новым, так как оно неизвестно из уровня медицины, в области ультразвукового исследования в онкологии.
Новизна изобретения заключается в том, что на разных этапах противоопухолевой XT (исходно, до лечения, после первого введения XT, после первого курса XT и перед последующими курсами) проводят ультразвуковой мониторинг состояния миокарда методом эхокардиографии с доплерографией, сопоставляя данные клиники и ультразвукового исследования сердца. В частности, клинически определяют распространенность опухолевого процесса, локализацию и стадию заболевания, наличие фоновых сердечно-сосудистых заболеваний и связанные с ними жалобы, данные ЭКГ и исходной Эхо-КГ и отслеживают динамические изменения ультразвуковых характеристик диастолической функции левого желудочка в процессе химиотерапии.
Используют следующие УЗ-критерии для диагностики ранних проявлений кардиотоксического эффекта:
- максимальная скорость раннего диастолического наполнения - пик Е (м/с);
- максимальная скорость трансмитрального потока во время предсердной систолы - пик А (м/с);
- соотношение максимальных скоростей диастолических потоков Е/А;
- время ускорения кровотока раннего диастолического наполнения левого желудочка Та (мс);
- время замедления кровотока раннего диастолического наполнения левого желудочка Тд (мс);
- время изоволюметрического расслабления левого желудочка IVRT (мс).
Изобретение имеет изобретательский уровень, так как для врача-терапевта, специалиста УЗИ, онколога явным образом не следует из уровня медицины в области УЗИ в онкологии - ультразвуковой прогностической диагностики развития кардиотоксичности и ранней диагностики кардиотоксических проявлений.
Известные прогностические факторы развития кардиотоксичности (пожилой возраст больных, наличие сердечно-сосудистых заболеваний, суммарная доза XT, превышающая 550 мг/м2), характерны не для всех групп больных и могут указывать на степень агрессивности кардиотоксического эффекта, требующего индивидуализированной коррегирующей терапии и нуждаются в дальнейшем исследовании.
Значение исследования гемодинамических показателей сердца в процессе XT (динамика показателей трансмитрального кровотока) с точки зрения ранней доклинической диагностики в медицинской литературе не рассматривалось.
Авторами разработан способ ультразвуковой оценки трансмитрального кровотока в ранней диагностике кардиотоксичности, индуцированной антрациклинами на разных этапах противоопухолевой терапии.
Таким образом, предлагаемое изобретение является новым, не очевидным, не следующим из уровня современной медицины, не известного в мировой медицинской литературе ни в СНГ, ни в России.
Изобретение является промышленно применимым, так как может быть воспроизведено в Здравоохранении, в медицинских учреждениях, занимающихся УЗИ в онкологии, НИИ-онкологических институтах, онкодиспансерах, оснащенных необходимым современным ультразвуковым оборудованием.
Способ УЗ-оценки кардиотоксичности, индуцированной антрациклинами у онкологических больных выполняется следующим образом.
До проведения XT больным выполняют УЗИ сердца стандартизованно трансторакально в положении больного "лежа на левом боку", в режимах В- и М-сканирования датчиком Р4-2 МГц с тканевым гармоническим изображением миокарда и использованием триплексной доплерографии. При выполнении эхокардиографии в B-режиме производят стандартные измерения: размеров аортального кольца, левого предсердия, правого желудочка, толщины свободной стенки правого желудочка, дуги аорты. Отмечают состояние клапанного аппарата и фиброзных колец, наличие гипертрофии стенок желудочков и дилатацию полостей сердца, оценивают локальную сократимость желудочков (по 16 сегментам). Изучают состояние нижней полой вены (размеры, реакция на вдох), брюшного отдела аорты, состояние листков перикарда и полости перикарда, состояние плевральных полостей. Далее выполняют ЦДК в стандартизованном режиме настройки аппарата для регистрации и оценки степени выраженности регургитации и градиента давления на клапанах (с помощью постоянно-волнового доплера). Оценку систолической функции левого желудочка производят в М-режиме. С помощью встроенного компьютера по методу Teinchhols производится автоматический расчет систолического и диастолического объемов левого желудочка, используемых для оценки систолической функции левого желудочка: фракции выброса и фракции укорочения волокон левого желудочка. Оценку диастолической функции левого желудочка производят при сканировании в В-режиме из четырехкамерной позиции, располагая контрольный объем импульсно-волнового доплера в полости левого желудочка за створками митрального клапана. Измеряют максимальную скорость раннего диастолического наполнения (пик Е), максимальную скорость диастолического потока в фазе предсердной систолы (пик А), вычисляют соотношение максимальных скоростей диастолических потоков (Е/А), отмечают время ускорения и замедления кровотока раннего диастолического наполнения левого желудочка. Время изоволюметрического расслабления левого желудочка измеряют в пятикамерной позиции с использованием постоянно-волнового доплера. Все УЗИ выполняются по общепринятым доступам в акустических окнах (парастернальное, супрастернальное, субкостальное, апикальное). Результаты Эхо-КГ регистрируют в протокол УЗИ, сопоставляют с жалобами, анамнестическими данными и клиническими проявлениями сопутствующих сердечно-сосудистых заболеваний.
Далее на разных этапах XT (после первого введения, после первого курса, перед каждым очередным курсом) проводят УЗ-мониторинг функциональных показателей методом Эхо-КГ, сопоставляя исходные параметры УЗИ сердца и клиники. В частности, клинически определяют появление кардиалгий, сердцебиений, нарушений ритма, признаки имеющейся или появившейся сердечной недостаточности. Сопоставляют клинические проявления с динамикой ЭКГ. Используют следующие УЗ-критерии: показатели систолической функции левого желудочка (фракция выброса левого желудочка, фракция укорочения волокон левого желудочка, конечно-диастолический и конечно-систолические объемы и размеры левого желудочка) и показатели диастолической функции левого желудочка (максимальная скорость трансмитрального потока во время раннего диастолического наполнения - пик Е, максимальная скорость диастолического потока во время предсердной систолы - пик А, соотношение Е/А, время ускорения раннего диастолического потока, время замедления раннего диастолического потока, время изоволюметрического расслабления). Все доплеровские исследования проводятся стандартизированно в режимах импульсно-волнового доплера из четырехкамерной позиции при расположении контрольного объема в полости левого желудочка за створками митрального клапана, IVRT вычисляется в режиме постоянно-волнового доплеровского исследования в пятикамерной позиции.
Далее устанавливают, что у больных при появлении и идентификации диастолической дисфункции после первого введения XT и сохраняющейся по окончании первого курса XT диагностируются ранние проявления кардиотоксичности, индуцированные XT, что требует назначения коррегирующей индивидуализированной сопроводительной терапии. При появлении клинических проявлений кардиотоксичности у больных, с появившейся диастолической дисфункцией, рекомендуется назначение кардиопротектора - кардиоксана еще до достижения рекомендуемой "безопасной" суммарной дозы доксорубицина в 330-550 мг на м2.
Пример конкретного применения "Способа ультразвуковой оценки кардиотоксичности, индуцированной антрациклинами у онкологических больных"
Больная З. , история болезни 15758-н, 1946 года рождения, поступила на лечение в отделение химиогормонотерапии РНИОИ 01.12.2001 г. Диагноз: Рак правой молочной железы, экзофитная форма с вторичным отеком (гиперемия за пределами молочной железы с переходом на спину), метастазы в правые подмышечные лимфоузлы. Т4 N2 M1 (Стадия 4, группа 4).
Из анамнеза выяснено, что около 5 лет больная страдает артериальной гипертонией. АД повышается до 150/90 мм рт.ст. при постоянном приеме эднита в дозе 5 мг в течение последних 2-х месяцев, а также во время проведения химиолечения АД 130/80 мм рт.ст.
ЭКГ от 02.12.2001 г. Снижены восстановительные процессы в миокарде левого желудочка.
Эхо КГ от 06.12.2001 г. Аорта 26 мм, стенка уплотнена. Открытие аортального клапана 19,9 мм, скорость на аортальном клапане 117 см/сек. Левое предсердие 40 мм. Правый желудочек 22 мм, толщина стенки 5 мм. Митральный клапан - движение створок М-образное, разнонаправленное, створки несколько уплотнены. Конечный диастолический размер левого желудочка 49,9 мм, конечный систолический размер 31,1 мм. Конечный диастолический объем левого желудочка 118 см3. Конечный систолический объем 51 см3. Ударный объем 67 мл. Минутный объем 4,7 л. Фракция выброса 65,2%. Фракция укорочения 30%. Толщина межжелудочковой перегородки 11 мм. Толщина задней стенки левого желудочка 11 мм. Признаков нарушения локальной сократимости левого желудочка не выявлено. Легочная артерия 19 мм, кровоток не ускорен. Качественные признаки легочной гипертензии отсутствуют. Доплерография - максимальная скорость раннего диастолического наполнения (пик Е) 61 см/сек, максимальная скорость кровотока во время предсердной систолы (пик А) 42 см/сек. Соотношение Е/А=1,45. Время ускорения раннего диастолического наполнения (Тасс) 70 мс. Время замедления раннего диастолического наполнения (Тдес) 140 мс. Время изоволюметрического расслабления левого желудочка 70 мс (фиг.1).
Больной начато проведение химиотерапии. В первый день лечения введено винбластина 1 мг, метотрексата 25 мг, циклофосфана 200 мг, 5-фторурацила 500 мг и доксорубицина 30 мг внутривенно капельно.
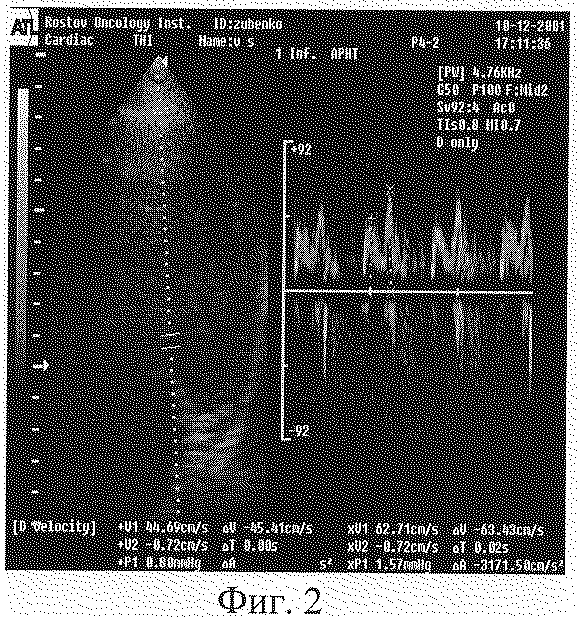
В тот же день через 2 часа после окончании введения химиопрепаратов больной выполнена эхокардиография с доплерометрией (10.12.2001). Получены следующие данные. Максимальная скорость трансмитрального кровотока в фазе раннего диастолического наполнения (пик Е) 44,69 см/сек. Максимальная скорость во время предсердной систолы 62,71 см/сек. Соотношение Е/А=0,71. Время ускорения раннего диастолического наполнения 50 мс. Время замедления раннего диастолического наполнения 150 мс. Время изоволюметрического расслабления 120 мс. ЧСС 70 мс. Таким образом, у больной зафиксировано появление диастолической дисфункции уже после первого введения химиопрепаратов (фиг.2).
В дальнейшем проводилось эхокардиографическое исследование перед проведением каждого курса химиотерапии. Результаты исследования сопоставлялись с клиническими проявлениями и данными ЭКГ.
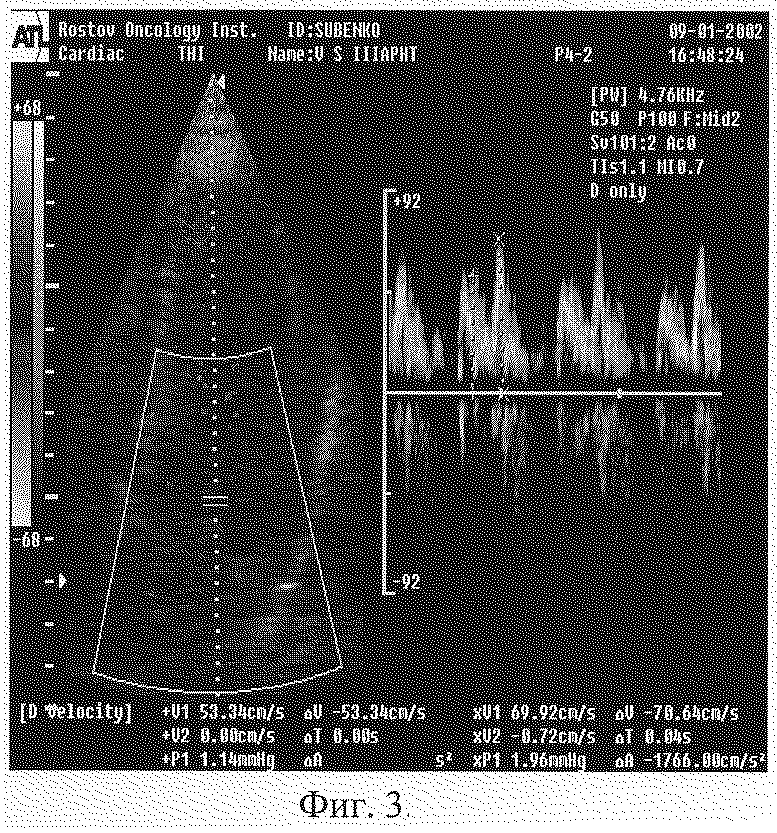
Так, отмечено сохранение диастолической дисфункции перед вторым неоадьювантным курсом химиотерапии. ЭхоКГ от 09.01.2002 г. Доплерометрия: максимальная скорость раннего диастолического потока (пик Е) 53,34 см/сек, максимальная скорость во время предсердной систолы (пик А) 69,92 см/сек. Соотношение Е/А= 0,76. Тасс 60 мс. Тдес 140 мс. Время изоволюметрического расслабления 90 мс. ЧСС 80 (фиг.3).
Во время проведения второго курса химиотерапии у больной впервые появились боли в области сердца, постоянного характера, не связанные с физической нагрузкой. На ЭКГ появились очаговые дистрофические изменения верхушки, передне-боковой стенки.
Таким образом, появление диастолической дисфункции во время первого курса неоадъювантного химиолечения может рассматриваться как проявление раннего кардиотоксического действия химиотерапии на доклиническом этапе.
Технико-экономическая эффективность "Способа ультразвуковой оценки кардиотоксичности, индуцированной антрациклинами у онкологических больных" заключается в том, что ранняя доклиническая диагностика кардиотоксического эффекта позволяет назначать своевременное лечение, профилактируя развитие последующей кардиомиопатии. Кроме того, в зависимости от динамики диастолических параметров в сочетании с данными фонового состояния пациента, а также клиническими проявлениями можно рекомендовать изменение схемы XT, снижение дозы препарата либо замену традиционной XT на нетрадиционную XT (аутогемо, аутолимфо XT), обладающую менее выраженными общетоксическими эффектами под прикрытием кардиотропных препаратов и кардиопротекторов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования развития кардиотоксичности у больных HER2 позитивным раком молочной железы исходно низкого/умеренного сердечно-сосудистого риска, получающих таргетную терапию трастузумабом после антрациклин-содержащей химиотерапии | 2020 |
|
RU2741371C1 |
| СПОСОБ ДИАГНОСТИКИ НАЧАЛЬНЫХ ПРОЯВЛЕНИЙ ДИАСТОЛИЧЕСКОЙ ДИСФУНКЦИИ МИОКАРДА ЛЕВОГО ЖЕЛУДОЧКА У ДЕТЕЙ, НАХОДЯЩИХСЯ НА РАЗНЫХ ЭТАПАХ ПОЛИХИМИОТЕРАПИИ | 2010 |
|
RU2440032C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАРДИОТОКСИЧЕСКИХ ОСЛОЖНЕНИЙ У БОЛЬНЫХ ХРОНИЧЕСКИМ ЛИМФОЛЕЙКОЗОМ | 2010 |
|
RU2450791C1 |
| СПОСОБ УЛЬТРАЗВУКОВОЙ ДИАГНОСТИКИ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ РЕЗИДУАЛЬНЫХ ОПУХОЛЕЙ ЯИЧНИКОВ К ХИМИОТЕРАПИИ | 2002 |
|
RU2239362C2 |
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ МИОКАРДА ЛЕВОГО ЖЕЛУДОЧКА С ПОМОЩЬЮ ОПРЕДЕЛЕНИЯ ИНДЕКСА ДИСФУНКЦИИ СЕРДЕЧНОЙ МЫШЦЫ | 2000 |
|
RU2182459C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ГРУППЫ РИСКА ДИАСТОЛИЧЕСКОЙ ДИСФУНКЦИИ ЛЕВОГО ЖЕЛУДОЧКА У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2007 |
|
RU2356499C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ С ИБС В ПОСТИНФАРКТНЫЙ ПЕРИОД | 2004 |
|
RU2269922C1 |
| СПОСОБ ДИАГНОСТИКИ ИНСУЛИНОРЕЗИСТЕНТНОСТИ | 2014 |
|
RU2553943C1 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ ТЯЖЕСТИ ДИАСТОЛИЧЕСКОЙ ДИСФУНКЦИИ ЛЕВОГО ЖЕЛУДОЧКА У БОЛЬНЫХ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2006 |
|
RU2325850C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КУМУЛЯТИВНОЙ КАРДИОТОКСИЧНОСТИ ХИМИОТЕРАПЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2012 |
|
RU2510240C2 |
Изобретение относится к медицине, кардиологии, онкологии и может быть использовано в комплексной диагностике кардиотоксичности на доклиническом уровне у больных в процессе химиотерапии. На разных этапах химиотерапии проводят ультразвуковой мониторинг состояния миокарда методом трансторакальной эхокардиографии с доплерографией. Сопоставляют данные клиники и ультразвукового исследования сердца. В случае отсутствия изменений показателей диастолической функции левого желудочка в процессе химиотерапии делают вывод об отсутствии кардиотоксических проявлений. Ранние признаки кардиотоксичности выявляют при изменении в процессе химиотерапии показателей трансмитрального потока. Способ позволяет выбрать адекватную тактику химиотерапии и своевременно назначить сопроводительную кардиальную терапию. 3 ил.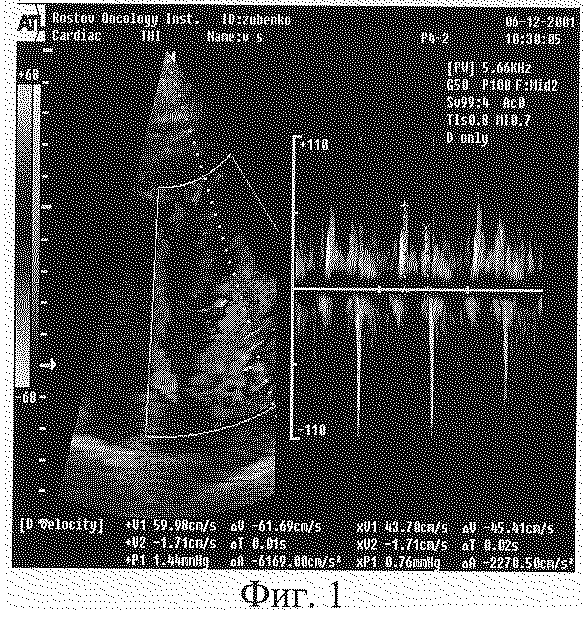
Способ ультразвуковой оценки кардиотоксичности, индуцированной антрациклинами, у онкологических больных, включающий клиническое обследование, электрокардиографию, эхокардиографию с доплерографией, отличающийся тем, что на разных этапах противоопухолевой химиотерапии проводят ультразвуковой мониторинг состояния миокарда методом трансторакальной эхографии с доплерографией, сопоставляют данные клиники и диастолической функции левого желудочка и устанавливают изменение характеристики трансмитрального потока после первого введения химиопрепарата - регистрируют диастолическую дисфункцию - преобладание скорости трансмитрального потока во время предсердной систолы (пик Е) над скоростью раннего диастолического наполнения (пик А) с изменением соотношения Е/А<1,0 у пациентов с исходно неизмененными показателями диастолической функции левого желудочка, появление диастолической дисфункции является зарегистрированным проявлением кардиотоксического эффекта, ранней диагностикой кардиотоксичности на доклиническом уровне, однако, если у больных в процессе химиотерапии не изменяются характеристики трасмитрального потока - это свидетельствует об отсутствии ранних кардиотоксических проявлений.
| ГЕРШАНОВИЧ М.Л | |||
| Кардиотоксичность противоопухолевых антрациклиновых антибиотиков и возможности ее предупреждения кардиосканом (декстразоканом) в онкологической практике | |||
| - Вопросы онкологии, 2001, т | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Способ получения камфоры | 1921 |
|
SU119A1 |
| СПОСОБ ДИНАМИЧЕСКОГО КОНТРОЛЯ СОСТОЯНИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ТЯЖЕЛЫХ БОЛЬНЫХ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1993 |
|
RU2071269C1 |
| ШХВАЦАБАЯ Л.В., НЕКЛЮДОВА В.И | |||
| Дифференциальная диагностика поражения сердца у онкологических больных | |||
| - Клиническая медицина, 1985, № 2, с | |||
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
Авторы
Даты
2004-03-10—Публикация
2002-04-08—Подача