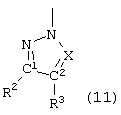Текст описания в факсимильном виде (см. графическую часть).
Непротеиногенные L-аминокислоты получают путем непосредственной ферментации с использованием широко известного штамма микроорганизма, характеризующегося нарушенной регуляцией метаболизма цистеина, которую осуществляют согласно широко известному методу. Данный способ отличается от известного тем, что в процессе ферментации в среду для ферментации добавляют нуклеофильное соединение, которое представляет собой 1,2,3,4-тетразолил-L-аланин, или его производные, или S-гетероарил-L-цистеин. Использование такого нуклеофильного соединения в определенных количествах приводит к продуцированию непротеиногенных L-аминокислот штаммом микроорганизма. 2 с. и 16 з.п. ф-лы.
1. Способ получения непротеиногенных L-аминокислот, предусматривающий ферментацию с использованием штамма микроорганизма с нарушенной регуляцией метаболизма цистеина и выделение L-аминокислот, отличающийся тем, что в процессе ферментации в среду для ферментации добавляют нуклеофильное соединение в количестве 10 - 1000 ммолей на 1 л начального объема ферментационной среды после начала ферментации, что приводит к продуцированию непротеиногенных L-аминокислот.2. Способ по п.1, отличающийся тем, что добавляют нуклеофильное соединение, содержащее фрагмент, выбранный из группы, включающей



3. Способ по п.1 или 2, отличающийся тем, что нуклеофильное соединение выбирают из группы соединений, включающей тиол общей формулы (1):
где R1 обозначает одновалентный замещенный или незамещенный алкил, алкоксигруппу, арил или гетероарил, имеющий максимум 15 атомов углерода; азол общей формулы (2) или (3):


а также его сложные и простые эфиры или соли,
где Х и Y имеют одинаковые или различные значения и обозначают CR4 или N, где R4 обозначает –Н, –СООН, –ОН, –NH2, –NO-
2
, –SH, –SO-
3
, –F, –Cl, –Br, –I, С1-С5алкилкарбонил- или R1, где R1 имеет значения, указанные для формулы (1), при этом R2 и R3 имеют одинаковые или различные значения и обозначают R4, или С1 и С2 в формуле (3) вместо заместителей R2 и R3 присоединены к кольцу с помощью мостика [–CR5R6–]а, где а равно 1, 2, 3 или 4, при этом R5 и R6 имеют одинаковые или различные значения и обозначают R4, и одна или несколько групп [–CR5R6–], которые не являются соседними, могут быть замещены атомом кислорода, серы или при необходимости иминофрагментом, замещенным С1-С5 алкилом, и две соседние группы [–CR5R6–] могут быть заменены группой [–CR5=R6–] или группой [–CR5=N–], - изоксазолинон общей формулы (4) или (5):


а также его сложные и простые эфиры или соли,
где Х, R1, R2 и R3 имеют указанные выше значения, С1 и С2 в формуле (5) вместо заместителей R2 и R3 могут быть присоединены к кольцу с помощью указанного для формулы (3) мостика.
4. Способ по любому из пп.1-3, отличающийся тем, что в способе по изобретению применяют штамм микроорганизмов, выбранный из группы, включающей следующие штаммы: штаммы с модифицированными cysЕ-аллелями; штаммы, содержащие гены экспорта; штаммы с измененной CysB-активностью; штаммы, которые получают с помощью методов неспецифического мутагенеза в сочетании с методами скрининга с целью сверхпроизводства цистеина или уменьшения разложения цистеина.5. Способ по любому из пп.1-4, отличающийся тем, что в качестве штамма микроорганизмов применяют штамм Escherichia coli.6. Способ по пп.1, 4 или 5, отличающийся тем, что культивирование штамма микроорганизма в ферментере осуществляют непрерывно, периодически (культивирование партий) либо с использованием периодического процесса с подпиткой.7. Способ по любому из пп.1-6, отличающийся тем, что источник углерода и нуклеофильное соединение добавляют непрерывно в процессе ферментации.8. Способ по любому из пп.1-7, отличающийся тем, что добавление нуклеофильного соединения начинают через 6-8 ч после начала ферментации и продолжают до окончания ферментации.9. Способ по любому из пп.1-8, отличающийся тем, что количество добавляемого нуклеофильного соединения составляет 10 - 1000 ммолей на 1 л начального объема среды для ферментации.10. Способ по любому из пп.1-9, отличающийся тем, что в качестве источника углерода для ферментации применяют сахар, многоатомный спирт, дающий при окислении моносахарид, или органические кислоты.11. Способ по п.10, отличающийся тем, что источники углерода вносят таким образом, что содержание глюкозы в ферментере составляет 0,1-50 г/л.12. Способ по любому из пп.1-11, отличающийся тем, что в качестве источника азота применяют аммиак, соли аммония или протеиновые гидролизаты.13. Способ по любому из пп.1-12, отличающийся тем, что значение рН среды для ферментации составляет 4-10 и температура инкубации составляет 15-45°С.14. Способ по любому из пп.1-13, отличающийся тем, что его осуществляют в аэробных условиях для роста.15. Способ по любому из пп.1-14, отличающийся тем, что после удаления биомассы из среды для ферментации путем фильтрации или центрифугирования непротеиногенные L-аминокислоты выделяют из надосадочной жидкости культуры с помощью экстракции, адсорбции, ионообменной хроматографии, осаждения или кристаллизации.16. Способ по любому из пп.1-15, отличающийся тем, что непротеиногенная L-аминокислота представляет собой аминокислоту общей формулы (6), имеющую L-конфигурацию: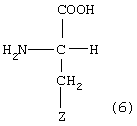
где Z обозначает одновалентный радикал, выбранный из группы, включающей радикалы формул (7)-(13)




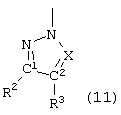
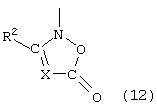

а также их сложные эфиры, простые эфиры или соли,
где R1, R2, R3, R4, Х и Y имеют значения, указанные для формул (1) - (5).
17. Соединение, выбранное из группы, включающей 1,2,3,4-тетразолил-L-аланин и его производные, 1,2,3-триазолил-L-аланин и его производные и S-гетероарил-L-цистеин.18. Соединение по п.17, выбранное из группы, включающей 1,2,3,4-тетразол-1-ил-L-аланин, 1,2,3,4-тетразол-2-ил-L-аланин, 1,2,3-бензотриазол-1-ил-L-аланин, 1,2,3-бензотриазол-2-ил-L-аланин, 5-карбокси-1,2,3-бензотриазол-1-ил-L-аланин, 5-карбокси-1,2,3-бензотриазол-2-ил-L-аланин, 1,2,4-триазол-3-ил-L-цистеин, тиазол-2-ил-L-цистеин, имидазол-2-ил-L-цистеин, тиен-2-ил-L-цистеин, пиридин-2-ил-L-цистеин, пиримидин-2-ил-L-цистеин, бензотиазол-2-ил-L-цистеин и бензоксазол-2-ил-L-цистеин.