Объектом настоящего изобретения являются простые эфиры, являющиеся производными тетрагидроизохинолина и тетрагидробензо[h]изохинолина, способ их получения и их применение в терапии.
В WO 02/076925 описаны антагонисты рецепторов Н3 гистамина. Некоторые эти соединения являются простыми эфирами - производными изохинолинов или бензоизохинолинов, с которыми соединены линейные или циклические алкиламины.
Целью заявителей являются новые соединения, модулирующие активность рецептора Н3 гистамина.
Таким образом, первым объектом настоящего изобретения являются новые соединения формулы I
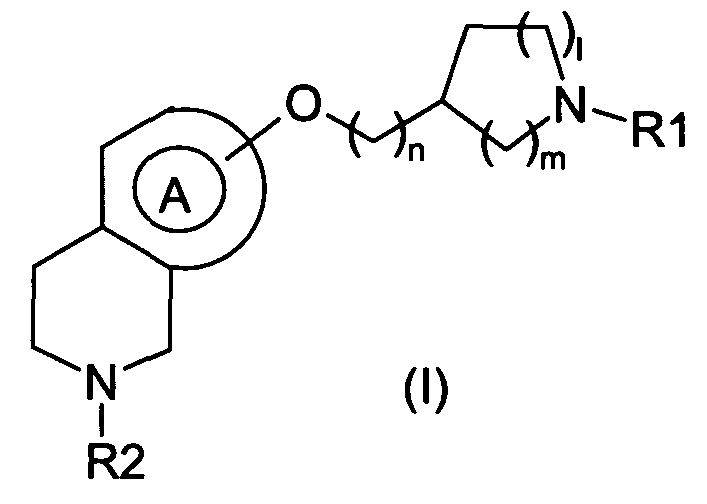
в которой
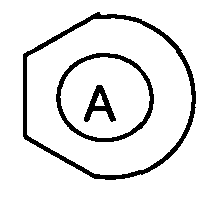
обозначает ненасыщенный карбоцикл с двойными связями, такой как фенил или нафтил, при этом карбоцикл возможно замещен одним или несколькими заместителями, выбранными независимо друг от друга из атома галогена, гидрокси, группы нитро, циано,
(С1-2)пергалогеналкила, (С1-3)алкила или фенила;
l может принимать значение от 0 до 4;
m может принимать значение от 0 до 3;
n может принимать значение от 0 до 6;
-(С)l-, -(С)m- и (С)n- обозначают независимо друг от друга группу (Сx-z)алкилидена, возможно замещенную 1-4 заместителями, выбранными из атома галогена, группы гидрокси, нитро, циано, амино, (С1-2)пергалогеналкила, (С1-3)алкила или фенила; и кроме того, если l, m и/или n равно 0, -(С)0 обозначает связь;
R1 обозначает атом водорода, (С1-3)алкильную группу,
(С1-6)алкилкарбонил, (С1-6)алкоксикарбонил, которые могут быть замещены, эти группы (С1-3)алкил, (С1-6)алкилкарбонил,
(С1-6)алкоксикарбонил, атомом галогена, группой гидрокси,
(С1-3)алкокси, нитро, циано, амино или арилом, таким как бензилоксикарбонил; (С1-3)алкиларил, такой как бензил или фенетил, моноциклический гетероарил, такой как тиенил, фурил или пирролил, или арил, такой как фенил или нафтил; при этом группы арильная и гетероарильная возможно замещены 1-4 заместителями, выбранными из атома галогена, группы гидрокси, нитро, циано, амино, (С1-3)моноалкиламино, (С2-6)диалкиламино, (С1-3)алкила,
(С1-2)пергалогеналкила, (С1-3)галогеналкила, (С1-3)алкокси или группы (С1-3)алкилидендиокси;
R2 обозначает атом водорода, (С1-6)алкильную группу или
(С3-6)циклоалкильную группу, возможно замещенные 1-4 заместителями, выбранными из атома галогена, группы гидрокси, нитро, циано, амино, (С1-3)моноалкиламино, (С2-6)диалкиламино,
(С1-2)пергалогеналкила, (С1-3)галогеналкила, (С1-3)алкокси,
(С3-6)циклоалкила, моноциклический гетероарил, такой как тиенил, фурил или пирролил, бициклический гетероарил, такой как бензотриазолил, или арильную группу, такую как фенил или нафтил; при этом арил возможно замещен 1-4 заместителями, выбранными из атома галогена, группы гидрокси, нитро, циано, амино,
(С1-3)моноалкиламино, (С2-6)диалкиламино, (С1-3)алкила,
(С1-2)пергалогеналкила, (С1-3)галогеналкила, (С1-3)алкокси, или группы (С1-3)алкилидендиокси.
В рамках настоящего изобретения понимают под
Сx-z, где x и z могут принимать значения от 0 до 6, углеродную цепочку, которая может содержать от x до z атомов углерода, однако если х равен 0, С0 обозначает связь, например, С1-6 обозначает углеродную цепочку, которая может содержать от 1 до 6 атомов углерода; С0-6 обозначает связь или углеродную цепочку, которая может содержать от 1 до 6 атомов углерода;
алкилом - алифатическую насыщенную линейную или разветвленную цепочку; например, (С1-6)алкил обозначает насыщенную линейную или разветвленную углеродную цепочку с 1-6 атомами углерода, более конкретно, радикал метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил и т.д;
при этом термин (Сx-z)алкилиден обозначает (Сx-y)алкил, линейный или разветвленный, двухвалентный; термин (С2-8)алкенилиден обозначает (Сx-y)алкил, ненасыщенный линейный или разветвленный, двухвалентный;
(Сx-y)алкокси - группу алкилокси с алифатической насыщенной линейной или разветвленной цепочкой, содержащей от х до y атомов углерода;
атом галогена - фтор, хлор, бром или йод;
(С1-3)моноалкиламино - моноамино, замещенный (С1-3)алкильной группой;
(С2-6)диалкиламино - амино, двузамещенный двумя
(С1-3)алкильными группами, одинаковыми или разными;
(С1-2)пергалогеналкил - (С1-2)алкильную группу, в которой все атомы водорода замещены атомами галогена;
(С1-3)галогеналкил -(С1-3)алкильную группу, в которой по меньшей мере один атом водорода замещен атомом галогена.
Соединения формулы I могут содержать один или несколько асимметрических атомов углерода. Таким образом, они могут быть в виде энантиомеров или диастереоизомеров. Эти энантиомеры, диастереоизомеры, а также их смеси, включая рацемические смеси, относятся к изобретению.
Соединения общей формулы I могут быть в виде свободных оснований или солей присоединения с кислотами, которые также относятся к изобретению. К этим солям по настоящему изобретению относятся соли с фармацевтически приемлемыми кислотами, а также соли с неорганическими или органическими кислотами, которые обеспечивают соответствующее отделение или кристаллизацию соединений формулы I. Эти соли можно получить методами, известными специалисту, например, путем взаимодействия соединения формулы I в виде основания с кислотой в соответствующем растворителе, таком как спиртовой раствор или органический растворитель, с последующим отделением среды, его содержащей, путем выпаривания растворителя или путем фильтрования.
Соединения формулы I могут также быть в виде гидратов или сольватов, а именно в виде ассоциаций или комбинаций с одной или несколькими молекулами воды или с растворителем. Такие гидраты или сольваты также относятся к изобретению.
Объектом настоящего изобретения являются также соединения, выбранные из следующих подгрупп, рассматриваемых отдельно или в комбинации, в которых
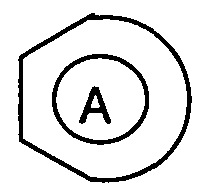
обозначает ненасыщенный карбоцикл, такой как фенил или нафтил, при этом карбоцикл возможно замещен одним или двумя заместителями, выбранными независимо друг от друга из атома галогена, группы гидрокси, нитро, циано, (С1-2)пергалогеналкила или (С1-3)алкила;
l может принимать значение 1, 2 или 3;
m может принимать значение 0, 1 или 2;
n может принимать значение 0, 1, 2 или 3;
-(С)l- и -(С)m- образуют вместе с группой -NR1- аминоцикл, связанный атомом углерода с группой -О-(С)n, такой как азетидин, пирролидин, пиперидин или азепин и/или
-(С)n- обозначают -(С0-3)алкилиден, возможно замещенный 1-4 заместителями, выбранными из атома галогена, группы гидрокси, нитро, циано, амино, (С1-2)пергалогеналкила, тем не менее если n равно 0, -(С)0 обозначает связь;
R1 обозначает атом водорода, группу: (С1-3)алкил,
(С1-6)алкилкарбонил, (С1-6)алкоксикарбонил; (С1-3)алкиларил, такой как бензил, гетероарил, такой как тиенил или фурил, арильную группу, такую как фенил или нафтил; причем арильная и гетероарильная группы могут быть замещены 1-4 заместителями, выбранными из атома галогена, группы гидрокси, циано, амино,
(С1-3)моноалкиламино, (С1-3)алкила, (С1-2)пергалогеналкила,
(С1-3)галогеналкила, (С1-3)алкокси или (С1-3)алкилидендиокси.
Более конкретно, если аминоцикл, частью которого являются
-(С)l-, -(C)m и -NR1-, и который связан атомом углерода с группой -O-(С)n-, выбирают из следующих групп:
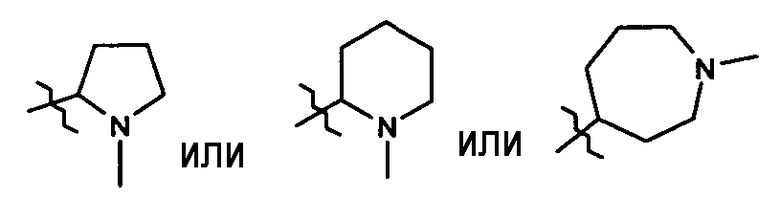
R2 обозначает атом водорода, (С1-3)алкил или (С5-6)циклоалкил, возможно замещенные 1-4 заместителями, выбранными из фенила, моноциклического гетероарила, такого как тиенил, бициклического гетероарила, такого как бензотриазолил, (С3-6)циклоалкила,
(С1-2)пергалогеналкила, (С1-3)галогеналкила или (С1-3)алкокси; при этом фенил и гетероарил возможно замещены 1-4 заместителями, выбранными из атома галогена, группы гидрокси, нитро, циано, амино, (С1-3)моноалкиламино, (С2-6)диалкиламино, (С1-3)алкила,
(С1-2)пергалогеналкила, (С1-3)галогеналкила, (С1-3)алкокси или группы (С1-3)алкилидендиокси.
Другим объектом изобретения являются следующие соединения и их фармацевтически приемлемые соли:
Соединение 1: 7-{2-[1-метилпиперидин-2-ил]этокси}-2-пропил-1,2,3,4-тетрагидроизохинолин;
Соединение 2: 2-изобутил-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
Соединение 3: 2-(3-метилбутил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
Соединение 4: 7-[(1-метилазепан-4-ил)окси]-2-(3-метилбутил)-1,2,3,4-тетрагидроизохинолин;
Соединение 5: (2-циклогексилметил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
Соединение 6: (2-циклогексилметил)-7-{2-[(2R)-1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидроизохинолин;
Соединение 7: (2-циклогексилметил)-7-{2-[(2S)-1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидроизохинолин;
Соединение 8: (2-циклогексилметил)-7-[(1-метилазепан-4-ил])окси]-1,2,3,4-тетрагидроизохинолин;
Соединение 9: (2-циклогексилметил)-7-[2(1-метилпиперидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
Соединение 10: 2-бензил-7-[2(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
Соединение 11: 2-бензил-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолин;
Соединение 12: 7-[(1-метилазепан-4-ил)окси]-2-(2-тиенилметил)-1,2,3,4-тетрагидроизохинолин;
Соединение 13: (2-циклогексилметил)-8-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидробензо[h]изохинолин;
Соединение 14: (2-циклогексилметил)-8-{2-[(2R)-(1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидробензо[h]изохинолин;
Соединение 15: (2-циклогексилметил)-8-{2-[(2S)-(1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидробензо[h]изохинолин;
Соединение 16: (2-циклогексилметил)-8-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидробензо[h]изохинолин;
Соединение 17: (2-циклогексилметил)-8-[2-(1-метилпиперидин-2-ил)этокси]-1,2,3,4-тетрагидробензо[h]изохинолин;
Соединение 20: 2-бутил-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолин;
Соединение 21: 2-бутил-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
Соединение 22: 7-[(1-метилазепан-4-ил)окси]-2-пропил)-1,2,3,4-тетрагидроизохинолин;
Соединение 23: 7-[2-(1-метилпирролидин-2-ил)этокси]-2-пропил-1,2,3,4-тетрагидроизохинолин.
С другой стороны, в рамках настоящего изобретения под защитной группой Pg понимают группу, которая позволяет, с одной стороны, защищать реакционноспособную функциональную группу, такую как гидрокси, или амин в процессе синтеза и, с другой стороны, регенерировать целую реакционноспособную функциональную группу в конце синтеза. Примеры защитных групп, а также методы защиты и снятия защиты приведены в “Protective groups in Оrganic Synthesis 3 Ed”, Green et Wuts (John Wiley and Sons, Inc., New York, 1999).
Вторым объектом изобретения является способ получения соединений формулы I по изобретению.
Так, соединения формулы I можно получать способом, изображенным на схеме 1.
Схема 1
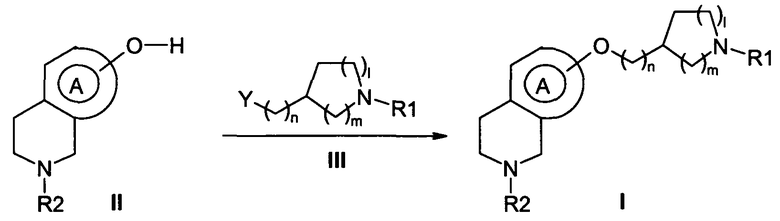
В соответствии со способом, изображенным на схеме 1, соединения формулы I, в которой R1, R2, l, m, n и цикл А такие, как определены по формуле I, получают нуклеофильным замещением путем взаимодействия фенола формулы II, в которой R2 и цикл А такие, как определены по формуле I, с амином формулы III, в которой R1, l, m и n такие, как определены по формуле I, и Y обозначает атом галогена, такой, например, как хлор, йод или бром, или обозначает «псевдо-галоген», такой как мезилат, трифлат, тозилат, бросилат или нозилат. Взаимодействие можно осуществлять в протонном или апротонном растворителе, таком как вода, метанол, ацетон, бутанон, этилацетат, толуол, N,N-диметилформамид, ацетонитрил или смесь этих растворителей при температуре от 0 до 110°С в присутствии основания, такого как, например, гидроксид натрия или калия, карбонат натрия или калия, триэтиламин или диизопропилэтиламин, для получения соединения формулы I. В случае несмешивающихся растворителей можно использовать катализатор фазового превращения, такой как соль аммония или фосфония, предпочтительно бромид тетрабутиламмония или хлорид тетраэтиламмония в смеси толуола и воды при температуре от 20 до 110°С. В случае необходимости соединения формулы II и III можно предварительно защитить до того, как провести взаимодействие методами, известными специалисту. Затем, возможно, с соединения формулы I снимают защиту в условиях, известных специалисту.
В варианте соединения формулы I можно получать путем реакции типа Mitsunobu. В соответствии с этим вариантом вводят во взаимодействие фенол формулы II, в которой R2 и цикл А такие, как определены по формуле I, с амином формулы III, в которой R1, l, m и n такие, как определены по формуле I, но Y обозначает группу гидрокси, полученную методами, известными специалисту. Взаимодействие можно проводить традиционным методом в присутствии реагентов Mitsunobu, таких как азопроизводное, например диэтилазодикарбоксилат, диизопропилазодикарбоксилат, ди-трет-бутилазодикарбоксилат, 1,1′-(азодикарбонил)дипиперидин или N,N,N',N'-тетраметилазодикарбоксамид, и фосфин, например трифенилфосфин или трибутилфосфин. Взаимодействие можно осуществлять в апротонном растворителе, таком как тетрагидрофуран или диоксан, или смеси этих растворителей, при температуре от 0 до 100°С для получения соединения формулы I. Если реагенты были предварительно защищены до проведения взаимодействия, с соединения формулы I снимают защиту в условиях, известных специалисту.
Защищенные (формула VI) или незащищенные (формула II) исходные соединения можно получать по схеме 2 или можно синтезировать традиционными методами, известными специалисту, такими, как описаны в Journal of Medicinal Chemistry 40, 3997-4005 (1997) или Тetrahedron Assymmetry 12, 2427-2434 (2001).
Схема 2
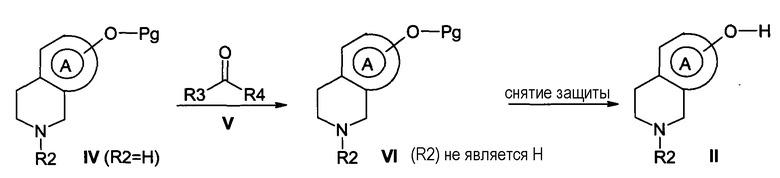
В соответствии со способом, изображенным на схеме 2, соединения формулы II, в которой R2 такой, как определен по формуле I, но не является атомом водорода, получают амино-восстановлением путем взаимодействия вторичного амина формулы IV, в которой R2 обозначает Н, с альдегидом или кетоном формулы V, в которой R3 и R4 после взаимодействия образуют вместе R2, такой, как определен по формуле I, и не являющийся водородом. Соединения формулы IV, в которой R2 обозначает атом водорода, можно получить традиционными методами, известными специалисту, такими, как описаны в Journal of Medicinal Chemistry 40, 3997-4005 (1997). Соединения формулы II можно затем получить из соединений формулы VI, с которых снята защита, в условиях, известных специалисту. Например, если Pg является метильной группой, защиту с соединений формулы VI можно снять в присутствии кислоты, такой как бромистоводородная кислота, в протонном растворителе, таком как вода или уксусная кислота, или смесь этих растворителей при температуре от 0 до 100°С в присутствии или в отсутствие катализатора фазового превращения, такого как соль аммония или фосфония, для получения фенола формулы II. Способ иллюстрируют примеры.
В варианте в способе по схеме 3 соединения формулы II, в которой R2 такой, как определен по формуле I, но не является атомом водорода, можно получить путем взаимодействия защищенного соединения формулы VI, в которой R2 обозначает бензотриазолилметильную группу, полученную, например, способом, описанным в Тetrahedron Assymmetry 12, 2427-2434 (2001), с агентом алкилирования, таким как соответствующий реагент Гриньяра.
Схема 3
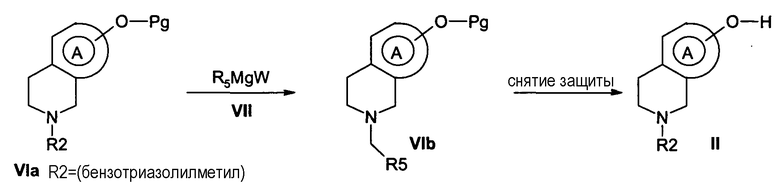
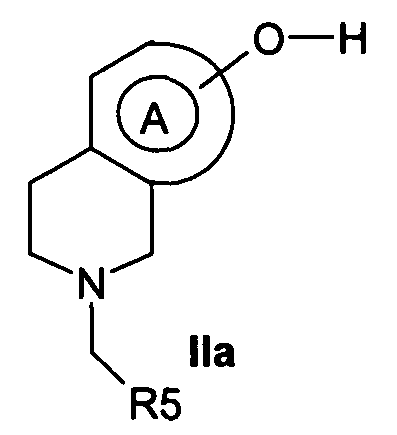
В соответствии с этим вариантом соединения формулы II, в которой R2 такой, как определен по формуле I, можно получить путем нуклеофильного замещения взаимодействием соединения формулы VIа, в которой R2 обозначает бензотриазолилметильную группу, с реагентом Гриньяра формулы VII, в которой W обозначает атом галогена, такой, например, как хлор, йод или бром, и R5 обозначает (С1-5)алкил, (С1-2)пергалогеналкил, (С1-3)галогеналкил, (С3-6)циклоалкил, моноциклический гетероарил, такой как тиенил или фурил или арильную группу, такую как фенил или нафтил; после взаимодействия получают соединение формулы II, в которой R2 такой, как определен по формуле I, и не является водородом. Взаимодействие можно осуществлять в апротонном растворителе, таком как простой диэтиловый эфир, тетрагидрофуран или диоксан или смесь этих растворителей при температуре от -70 до 100°С для получения соединения формулы VI. Затем соединения формулы II можно получить из соединений формулы VI, с которых снята защита в условиях, известных специалисту. Например, если Pg является метильной группой, защиту с соединений формулы VI можно снять в присутствии кислоты, такой как бромистоводородная кислота, в протонном растворителе, таком как вода или уксусная кислота, или смесь этих растворителей, при температуре от 0 до 100°С в присутствии или в отсутствие катализатора фазового превращения, такого как соль аммония или фосфония, для получения фенола формулы II. Способ иллюстрируют примеры.
Исходные соединения II и амины формулы III имеются в продаже, или их можно синтезировать методами, описанными выше, методами, известными специалисту или известными из литературы.
В соответствии с другим аспектом объектом изобретения являются лекарственные средства, содержащие соединение формулы I или соль присоединения последнего с фармацевтически приемлемой кислотой или гидрат или сольват соединения формулы I.
Эти соединения по настоящему изобретению применяются в терапии, в частности, для лечения нарушений, при которых улучшение наступает при модулировании рецептора Н3 гистамина, и для лечения патологий, при которых терапевтический эффект достигается за счет антагониста рецептора гистамина типа Н3. В частности, такими патологиями являются ожирение и диабет.
Эти соединения, обладающие свойствами антагониста и обратного агониста рецептора Н3 гистамина, используют в лечении заболеваний центральной нервной системы.
Также эти соединения можно использовать в лечении заболеваний центральной нервной системы, таких как нарушение сна, нарколепсия, болезнь Альцгеймера и другие виды деменции, болезнь Паркинсона, нарушения внимания у гиперкинетических детей, нарушения памяти и трудности в обучении, эпилепсия, шизофрения, умеренные нарушения психических процессов, ведуших к познанию и действию, депрессия и тревога. К состояниям депрессии и тревоги относятся, например, состояние тревоги, вызванное ожиданием (перед хирургическим вмешательством, перед лечением зубов и т.д.), тревога, вызванная алкогольной, наркотической зависимостью, мания, сезонные эмоциональные нарушения, мигрень и тошнота. Их можно также использовать при лечении сексуальных дисфункций, головокружения и тошноты при укачивании.
Применение соединений по изобретению для получения лекарственного средства, предназначенного для лечения указанных выше патологий, является частью изобретения.
В соответствии с другим из его аспектов настоящее изобретение относится к фармацевтическим композициям, содержащим в качестве действующего вещества по меньшей мере одно соединение по изобретению. Эти фармацевтические композиции содержат эффективную дозу по меньшей мере одного соединения по изобретению или фармацевтически приемлемую соль или гидрат или сольват указанного соединения, а также по меньшей мере один или несколько фармацевтически приемлемых эксципиентов. Указанные эксципиенты выбирают в зависимости от лекарственной формы и требуемого способа введения из традиционных эксципиентов, известных специалисту.
В составе фармацевтических композиций по настоящему изобретению для перорального, сублингвального, подкожного, внутримышечного, внутривенного, местного, локального, интратрахеального, интраназального, чрескожного или ректального введения действующее вещество указанной формулы I или его соль, сольват или гидрат можно вводить в виде разовой формы введения в смеси с традиционными фармацевтическими эксципиентами животным или людям для профилактики или лечения указанных выше нарушений или заболеваний.
К соответствующим стандартным лекарственным формам относятся формы для перорального введения, такие как таблетки, мягкие или твердые желатиновые капсулы, порошки, гранулы и растворы или суспензии для перорального введения, формы для сублингвального, буккального, интратрахеального, интраназального введения, введения путем ингаляции, формы для топического, чрескожного, подкожного, внутримышечного или внутривенного введения, формы для ректального введения и имплантаты. Для топического нанесения можно использовать соединения по изобретению в составе кремов, гелей, мазей или лосьонов.
Для получения требуемого профилактического или терапевтического эффекта доза действующего вещества может варьировать от 0,1 мкг до 50 мг на 1 кг веса тела в день. Каждая разовая доза может содержать от 0,1 до 1000 мг, предпочтительно от 0,1 до 500 мг действующего вещества в сочетании с фармацевтически приемлемым эксципиентом. Эту разовую дозу можно вводить от 1 до 5 раз в день с тем, чтобы вводить суточную дозу от 0,5 до 5000 мг, предпочтительно от 1 до 2500 мг.
В отдельных случаях доза может быть более высокой или более низкой. Такие дозы также относятся к изобретению. В обычной практике дозировку для каждого пациента определяет врач в зависимости от способа введения, веса и ответа пациента.
В качестве примера стандартная лекарственная форма соединения по изобретению содержит:
Соединение по изобретению 50,0 мг
Маннит 223,75 мг
Кроскармеллоза натрия 6,0 мг
Кукурузный крахмал 15,0 мг
Гидроксипропилметилцеллюлоза 2,25 мг
Стеарат магния 3,0 мг.
В соответствии с другим аспектом настоящее изобретение относится также к способу лечения указанных выше патологий, который включает в себя введение пациенту эффективной дозы соединения по изобретению или одной из его фармацевтически приемлемых солей или гидратов или сольватов.
Следующие примеры иллюстрируют способы и технологии осуществления этого изобретения, не ограничивая его объем.
Пример 1: Оксалат (2:1) (2-циклогексилметил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолина
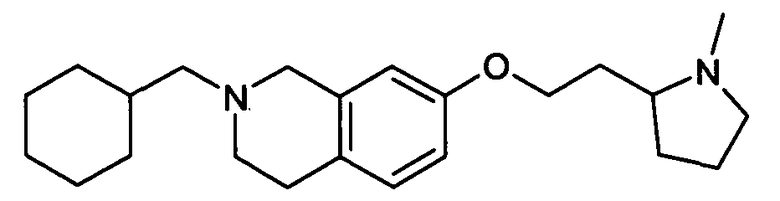
1.1. 2-(циклогексилметил)-7-метокси-1,2,3,4-тетрагидроизохинолин
В раствор 10,41 г (0,035 моль) 2-(1Н-1,2,3-бензотриазол-1-илметил)-7-метокси-1,2,3,4-тетрагидроизохинолина в 150 мл тетрагидрофурана, охлажденный до -40°С, вводят 35 мл (0,070 моль) раствора 2N циклогексилмагнезия хлорида в тетрагидрофуране. Перемешивают в течение двух часов при 40°С, затем смесь выдерживают в течение одной ночи при комнатной температуре. Добавляют раствор 2N гидроксида натрия (50 мл). Водную фазу экстрагируют 3 раза при помощи 20 мл простого этилового эфира и органические фазы сушат и выпаривают в вакууме. Получают 8,20 г масла, которое используют без дополнительной очистки.
Rdt: 90%
PF = масло
1.2. Гидробромид 2-(циклогексилметил)-1,2,3,4-тетрагидроизохинолин-7-ола
Раствор 8,20 г (0,032 моль) 2-(циклогексилметил)-7-метокси-1,2,3,4-тетрагидроизохинолина в 80 мл водного бромида водорода (48%) нагревают в течение 6 часов до 120°С. Смесь охлаждают, концентрируют досуха и осадок обрабатывают 60 мл смеси этанол/простой этиловый эфир. Образовавшееся твердое вещество фильтруют, промывают простым этиловым эфиром и сушат. Получают 9,70 г целевого продукта в виде чистого вещества белого цвета.
Rdt: 94%
PF=210-214°С
1.3. Оксалат (2:1) (2-циклогексилметил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолина
В смесь 5,00 г (0,020 моль) соединения, полученного на стадии 1.2, 11,2 г (0,0061 моль) 2-(2-хлорэтил)-1-метилпирролина и 0,41 г (0,002 моль) триэтиламмония хлорида в 125 мл толуола вводят смесь 9,7 г (0,244 моль) гидроксида натрия в 125 мл воды. Реакционную смесь нагревают с обратным холодильником в течение 8 часов. Фазы разделяют и водную фазу экстрагируют дважды 20 мл толуола. Органические фазы сушат, затем выпаривают досуха. Получают 7 г (97%) необработанного масла, которое очищают хроматографией на колонке силикагеля смесью дихлорметан/метанол (98:2), используемой в качестве элюента. Целевой продукт (0,70 г; 10%) получают в виде масла с наиболее высоким Rf.
1H-ЯМР (CDCl3) δ (ppm): 7,1 (1H, д), 6,7 (1H, д), 6,5 (1H, с), 4,0 (2H, м), 3,5 (2H, с), 3,0 (1H, м), 2,7 (2H, м), 2,6 (2H, м), 2,4 (3H, с), 2,2 (2H, д), 2,1 (2H, м) 2,0 (1H, м), 1,7 (11H, м), 1,1 (3H, м), 0,9 (2H, м).
Полученное выше масло (0,65 г; 0,002 моль) растворяют в 10 мл этанола, затем вводят 0,36 г (0,004 моль) щавелевой кислоты, растворенной в 10 мл этанола. Осадок фильтруют и промывают холодным этанолом. Получают 0,46 г целевого продукта в виде твердого вещества белого цвета.
Rdt: 47%
PF=78-98°С
Пример 2: Оксалат (2:1) (2-циклогексилметил)-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолина
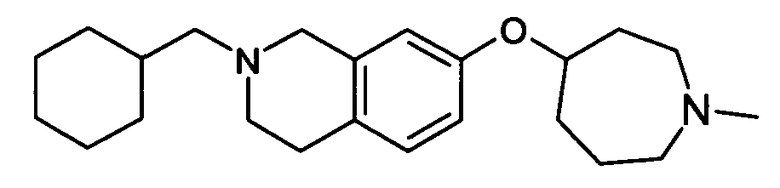
В соответствии со способом, описанным выше на стадии 1.3, получают масло с наиболее низким полученным Rf (1,30 г, 0,002 моль), которое соответствует структуре (2-циклогексилметил)-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолина.
1H-ЯМР (CDCl3) δ (ppm): 7,1 (1H, д), 6,7 (1H, д), 6,5 (1H, с), 4,5 (1H, м), 3,5 (2H, с), 2,7 (2H, м), 2,6-2,4 (5H, м), 2,3 (3H, с), 2,2 (2H, д), 2,0 (2H, м), 1,7 (11H, м), 1,1 (3H, м), 0,9 (2H, м).
Масло растворяют в 12 мл этанола, затем вводят 0,24 г (0,003 моль) щавелевой кислоты, растворенной в 12 мл этанола. Осадок фильтруют и промывают холодным этанолом. Получают 0,46 г целевого продукта в виде твердого вещества белого цвета.
Rdt: 86%
PF=110-112°С
Пример 3: Оксалат (2:1) (2-циклогексилметил)-8-[(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидробензо[h]изохинолина
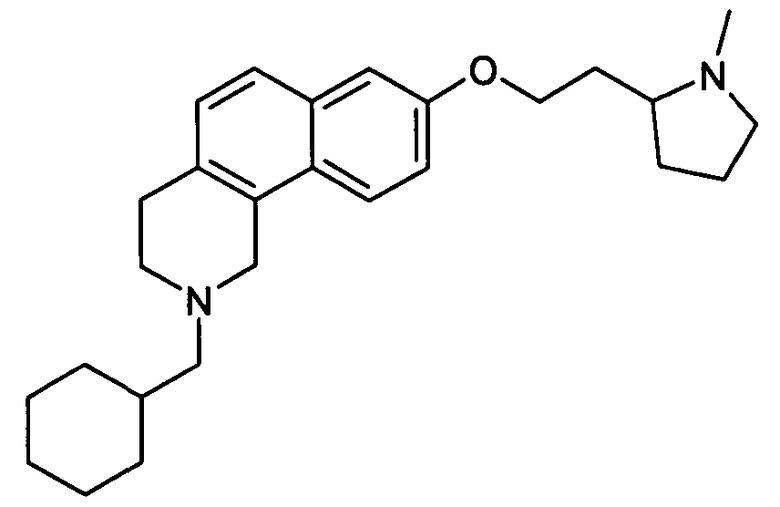
3.1. (2-циклогексилметил)-8-метокси-1,2,3,4-тетрагидроизобензо[h]хинолин
В раствор 3 г (0,014 моль) 8-метокси-1,2,3,4-тетрагидроизобензо[h]хинолина и 1,6 г (0,014 моль) циклогексанкарбоксальдегида в 70 мл метанола вводят 0,32 г (0,0003 моль) 10%-ного палладия на угле. Раствор гидрируют в течение 24 часов в гидрирующем средстве Paar под давлением 45 Psi. Катализатор устраняют фильтрованием и отфильтрованный раствор выпаривают досуха. Получают 4 г целевого продукта в виде масла.
Rdt: 93%
PF=масло
3.2. (2-циклогексилметил)-1,2,3,4-
тетрагидробензо[h]изохинолин-7-ола гидробромид
Раствор 2 г (0,006 моль) (2-циклогексилметил)-8-метокси-1,2,3,4-тетрагидроизобензо[h]хинолина в 30 мл водного бромида водорода (48%) нагревают в течение 6 часов до 120°С. Смесь охлаждают, концентрируют досуха и осадок обрабатывают 20 мл смеси этанол/простой этиловый эфир. Образовавшееся твердое вещество фильтруют, промывают простым этиловым эфиром и сушат. Получают 2,3 г целевого продукта в виде чистого твердого вещества белого цвета.
Rdt: 96%
PF=270-276°С
3.3. Оксалат (2:1) (2-циклогексилметил)-8-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидробензо[h]изохинолина
В смесь 2,00 г (0,005 моль) соединения, полученного на стадии 3.2, 2,4 г (0,014 моль) 2-(2-хлорэтил)-1-метилпирролина и 0,11 г (0,0006 моль) триэтиламмония хлорида в 75 мл толуола вводят в смесь 2,5 г (0,064 моль) гидроксида натрия в 75 мл воды. Реакционную смесь нагревают с обратным холодильником в течение восьми часов. Фазы разделяют и водную фазу экстрагируют 2 раза 20 мл толуола. Органические фазы сушат, затем выпаривают досуха. Получают 3 г (>100%) неочищенного масла, которое очищают хроматографией на колонке силикагеля при помощи смеси дихлорметан/метанол (98:2), используемой в качестве элюента. Целевой продукт (0,70 г; 10%) получают в виде масла с наиболее высоким Rf.
1H-ЯМР (CDCl3) δ (ppm): 7,7 (1H, д), 7,5 (1H, д), 7,1-7,0 (3H, м), 4,2 (2H, м), 4,0 (2H, с), 3,0 (1H, м), 2,9 (2H, м), 2,7 (2H, м), 2,4 (2H, д), 2,3 (3H, с), 2,2-2,0 (3H, м), 1,7 (11H, м), 1,1 (3H, м), 0,9 (2H, м).
Полученное выше масло (0,5 г; 0,001 моль) растворяют в 10 мл этанола, затем вводят 0,24 г (0,003 моль) щавелевой кислоты, растворенной в 10 мл этанола. Осадок фильтруют и промывают холодным этиловым эфиром, получают 0,50 г целевого продукта в виде твердого вещества белого цвета.
Rdt: 70%
PF=127-135°С
Пример 4: Оксалат (2:1) (2-циклогексилметил)-8-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидробензо[h]изохинолина
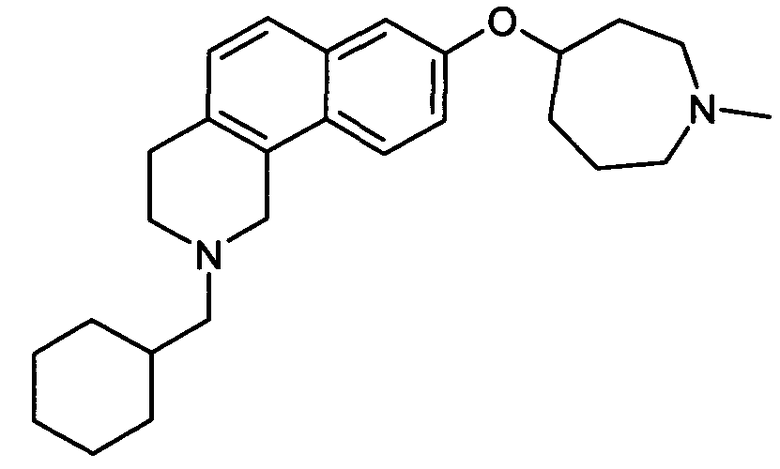
В соответствии со способом, описанным выше на стадии 3.3, получают масло с наиболее низким полученным Rf (0,67 г, 0,002 моль), которое соответствует структуре (2-циклогексилметил)-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолина.
1H-ЯМР (CDCl3) δ (ppm):), 7,8 (1H, д), 7,6 (1H, д), 7,2-7,0 (3H, м), 4,7 (1H, м), 4,0 (2H, с), 3,0 (2H, м), 2,9 (2H, м), 2,7 (2H, м), 2,4 (2H, д), 2,3 (3H, с), 2,3-1,7 (14H, м), 1,1 (3H, м), 0,9 (2H, м).
Масло растворяют в 10 мл этанола, затем вводят 0,37 г (0,004 моль) щавелевой кислоты, растворенной в 10 мл этанола. Осадок фильтруют и промывают холодным этиловым спиртом и получают 0,25 г целевого продукта в виде твердого вещества белого цвета.
Rdt: 31%
PF=77-101°С
Пример 5: Гидрохлорид (2:1) (2-циклогексилметил)-7-{2-[(2S)-(1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидроизохинолина
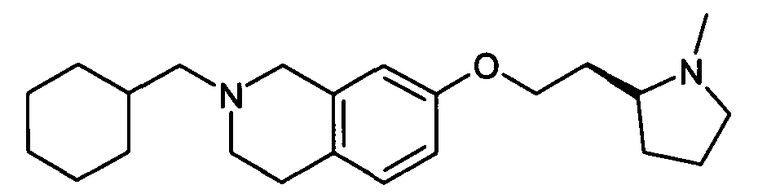
В смесь 7,3 г (0,030 моль) 2-(циклогексилметил)-1,2,3,4-тетрагидроизохинолин-7-ола, полученного выше на стадии 1.2, 3,5 г (0,027 моль) (S)-2-(2-гидроксиэтил)-1-метилпирролина и 9,2 г (0,036 моль) трифенилфосфина в 150 мл тетрагидрофурана, охлажденного до -5°С, вводят 6,6 г (0,032 моль) диизопропилазодикарбоксилата. Перемешивают в течение ночи при комнатной температуре. Раствор выпаривают досуха и получают неочищенное масло, которое очищают хроматографией на колонке силикагеля при помощи смеси дихлорметан/метанол (95:5), используемой в качестве элюента. Целевой продукт (1,4 г; 15%) получают в виде масла.
1H-ЯМР (CDCl3) δ (ppm): 7,1 (1H, д), 6,7 (1H, д), 6,5 (1H, с), 4,0 (2H, м), 3,5 (2H, с), 3,0 (1H, м), 2,7 (2H, м), 2,6 (2H, м), 2,4 (3H, с), 2,2 (2H, д), 2,1 (2H, м) 2,0 (1H, м), 1,7 (11H, м), 1,1 (3H, м), 0,9 (2H, м).
Масло растворяют в 25 мл изопропанола, затем изопропанола, насыщенного HCl. Осадок фильтруют и промывают 1 мл холодного изопропанола. Получают 1 г целевого продукта в виде твердого вещества белого цвета.
Rdt: 59%
PF=238-241°С
Пример 6: Гидрохлорид (2:1) (2-циклогексилметил)-8-[(2S)-(1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидробензо[h]изохинолина
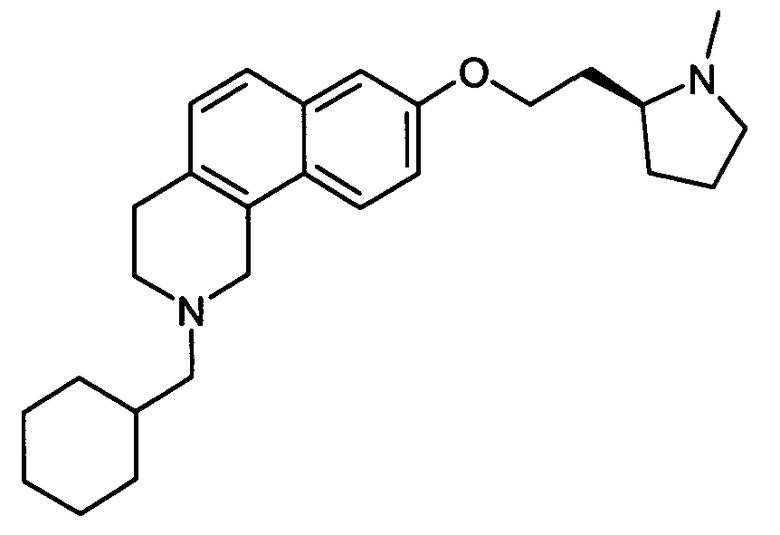
В смесь 2,2 г (0,007 моль) 2-(циклогексилметил)-1,2,3,4-тетрагидробензо[h]изохинолин-7-ола, полученного выше на стадии 3.2, 0,95 г (0,007 моль) (S)-2-(2-гидроксиэтил)-1-метилпирролина и 2,14 г (0,008 моль) трифенилфосфина в 150 мл тетрагидрофурана, охлажденного до -5°С, вводят 1,88 г (0,008 моль) диизопропилазодикарбоксилата. Перемешивают в течение ночи при комнатной температуре. Раствор выпаривают досуха и получают неочищенное масло, которое очищают хроматографией на колонке силикагеля при помощи смеси дихлорметан/метанол (95:5), используемой в качестве элюента. Целевой продукт (1,1 г; 36%) получают в виде масла.
1H-ЯМР (CDCl3) δ (ppm):), 7,7 (1H, д), 7,5 (1H, д), 7,1-7,0 (3H, м), 4,2 (2H, м), 4,0 (2H, с), 3,0 (1H, м), 2,9 (2H, м), 2,7 (2H, м), 2,4 (2H, д), 2,3 (3H, с), 2,2-2,0 (3H, м), 1,7 (11H, м), 1,1 (3H, м), 0,9 (2H, м).
Масло растворяют в 15 мл изопропанола, затем изопропанола, насыщенного HCl. Осадок фильтруют и промывают 1 мл холодного изопропанола. Получают 0,8 г целевого продукта в виде твердого вещества белого цвета.
Rdt: 62%
PF=260°С
Нижеследующая таблица иллюстрирует химические структуры и физические свойства нескольких соединений по изобретению. Элементарные микроанализы и спектры ЯМР, инфракрасной и масс-спектрометрии подтверждают структуры полученных соединений.
В таблице “P.F.” соединений формулы I соответствует точке плавления, а “Config” указывает на стереохимическую конфигурацию, а именно (R), (S) или рацемическую смесь (R,S) атома углерода, обозначенного звездочкой (*).
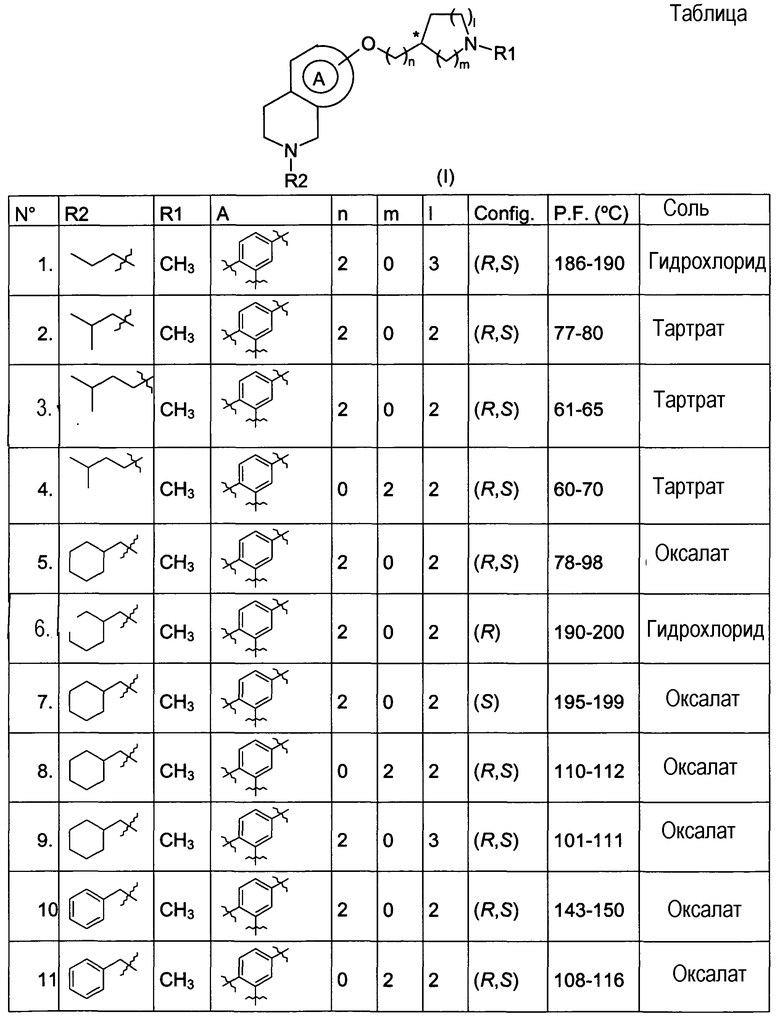
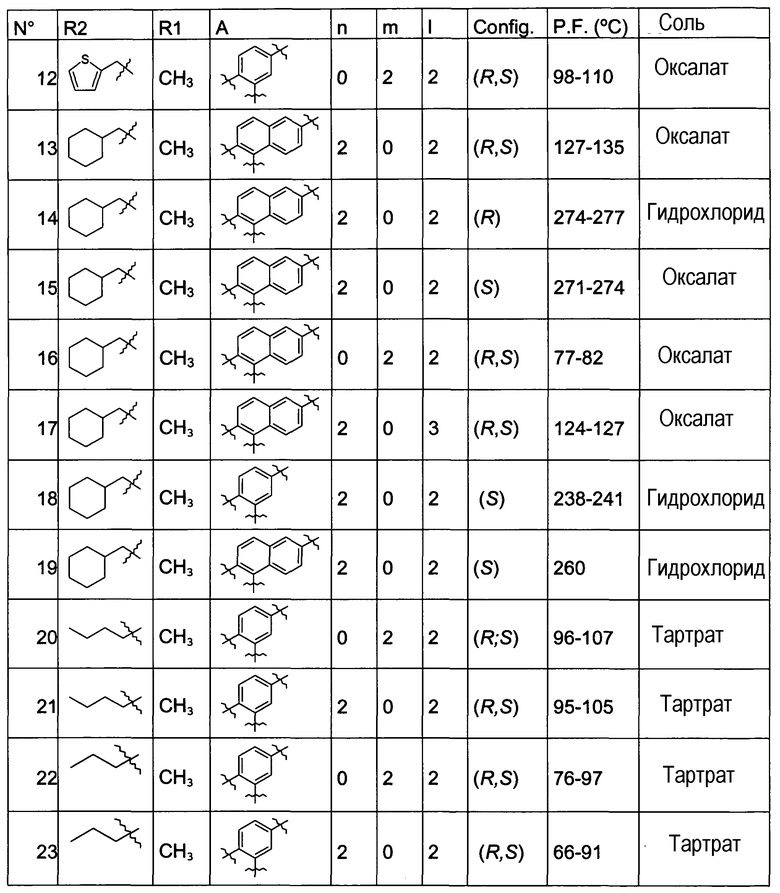
Соединения по изобретению, соответствующие формуле I, являлись объектом фармакологических испытаний, которые показали, что соединения представляют интерес в качестве активных веществ в терапии.
Более конкретно, соединения по изобретению являются антагонистами рецептора гистамина типа Н3. Рецепторы типа Н3 известны специалисту, и интерес, который они представляют в терапии, описан в литературе («Histamine Н3 receptor antagonists» Еxp. Opinion Ther. Patents (2000) 10 (7): 1045-1055). Таким образом, соединения по изобретению формулы I подвергли испытанию на сродство in vitro к природному рецептору гистамина типа Н3 в мембранном препарате мозга взрослой крысы путем специфической связи [3H]-N-α-метилгистамина с этим рецептором методами, описанными Korte A et al. в Biochem. Biophys. Res. Commun. 168, 979-986(1990) и West, R.E.Jr et al. в Mol. Pharmacol. 38, 610-613(1990).
Ki соединений по изобретению по отношению к рецепторам Н3 находится в диапазоне от 0,1 нM до 50 мкм, и более конкретно (2-циклогексиметил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин (см. соединение 5 в таблице) имеет Ki 0,1 нM.
Соединения по изобретению формулы I подвергали испытанию на образование сАМР на человеческом рецепторе гистамина типа Н3, перемещенного в клетки СНО путем ингибирования агонизма, вызванного специфической связью R-α-метилгистамина с этим рецептором методами, описанными Lovenberg, Т.W. et al., в J.Pharmacol. Exp. Ther. 293, 771-778 (2000).
CI50 соединений по изобретению по отношению к рецепторам Н3 составляет от 0,1 нM до 5,0 мкм.
В качестве примера соединение 5, включенное в таблицу, имеет CI50<10 нM, при этом измерение образования сАМР проводили при помощи прибора EIA (Amersham) на человеческом рецепторе гистамина типа Н3, перемещенного в клетки СНО путем ингибирования агонизма, вызванного специфической связью R-α-метилгистамина с этим рецептором.
Соединения по изобретению обладают селективной активностью в отношении рецептора гистамина типа Н3. Действительно, соединения имеют Ki выше 7,0 мкм в тесте на сродство in vitro к природному рецептору гистамина типа Н3 в мембранном препарате мозга взрослой крысы путем специфической связи [3H]-N-пириламина с этим рецептором методом, описанным Liu Y.Q. et al. в J. Pharmacol. Еxp. Ther 268, 959 (1994).
Настоящее изобретение относится к соединению формулы I, в которой цикл А обозначает ненасыщенный карбоцикл с двойными связями, который выбирают из фенила или нафтила; 1 может принимать значение от 1 до 3; m может принимать значение 0, 2 или 3; n может принимать значение 0 или 2; R1 обозначает атом водорода, (С1-3)алкильную группу; R2 обозначает (С1-6)алкильную группу, которая возможно замещена заместителем, выбранными из С6-циклоалкила, моноциклического гетероарила, выбранного из тиофена, арильной группы, выбранной из фенила, в виде основания или соли присоединения с кислотой. Также изобретение относится к фармацевтической композиции на основе соединения формулы I, к применению соединения формулы I для получения лекарственного средства, к способу получения соединения формулы I и к применению соединения формулы II для получения соединения формулы I. Технический результат: получены новые производные изохинолина и бензо[h]изохинолина, обладающие свойствами антагониста рецептора гистамина типа Н3. 6 н. и 3 з.п. ф-лы, 1 табл.

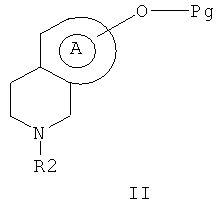
1. Соединения формулы I
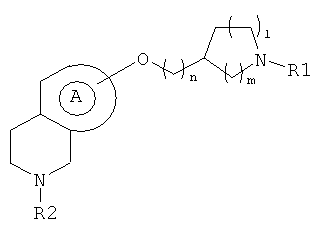
в которой
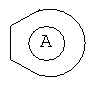
обозначает ненасыщенный карбоцикл с двойными связями, который выбирают из фенила или нафтила;
l может принимать значение от 1 до 3;
m может принимать значение 0, 2 или 3;
n может принимать значение 0 или 2;
R1 обозначает атом водорода,
(С1-3)алкильную группу;
R2 обозначает
(С1-6)алкильную группу, которая возможно замещена заместителем, выбранным из С6-циклоалкила, моноциклического гетероарила, выбранного из тиофена, арильной группы, выбранной из фенила,
в виде основания или соли присоединения с кислотой.
2. Соединения формулы I по п.1, имеющие следующие названия:
1: 7-{2-[1-метилпиперидин-2-ил]этокси}-2-пропил-1,2,3,4-тетрагидроизохинолин;
2: 2-изобутил-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
3: 2-(3-метилбутил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
4: 7-[(1-метилазепан-4-ил)окси]-2(3-метилбутил)-1,2,3,4-тетрагидроизохинолин;
5: (2-циклогексилметил)-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
6: (2-циклогексилметил)-7-{2-[(2R)-1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидроизохинолин;
7: (2-циклогексилметил)-7-{2-[(2S)-1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидроизохинолин;
8: (2-циклогексилметил)-7-[(1-метилазепан-4-ил])окси]-1,2,3,4-тетрагидроизохинолин;
9: (2-циклогексилметил)-7-[2(1-метилпиперидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
10: 2-бензил-7-[2(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
11: 2-бензил-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолин;
12: 7-[(1-метилазепан-4-ил)окси]-2-(2-тиенилметил)-1,2,3,4-тетрагидроизохинолин;
13: (2-циклогексилметил)-8-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидробензо[h]изохинолин;
14: (2-циклогексилметил)-8-{2-[(2R)-1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидробензо[h]изохинолин;
15: (2-циклогексилметил)-8-{2-[(2S)-1-метилпирролидин-2-ил]этокси}-1,2,3,4-тетрагидробензо[h]изохинолин;
16: (2-циклогексилметил)-8-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидробензо[h]изохинолин;
17: (2-циклогексилметил)-8-[2-(1-метилпиперидин-2-ил)этокси]-1,2,3,4-тетрагидробензо[h]изохинолин;
20: 2-бутил-7-[(1-метилазепан-4-ил)окси]-1,2,3,4-тетрагидроизохинолин;
21: 2-бутил-7-[2-(1-метилпирролидин-2-ил)этокси]-1,2,3,4-тетрагидроизохинолин;
22: 7-[(1-метилазепан-4-ил)окси]-2-пропил)-1,2,3,4-тетрагидроизохинолин;
23: 7-[2-(1-метилпирролидин-2-ил)этокси]-2-пропил-1,2,3,4-тетрагидроизохинолин;
и их фармацевтически приемлемые соли.
3. Фармацевтическая композиция, обладающая свойствами антагониста рецептора гистамина типа Н3, содержащая соединение формулы I по любому из пп.1, 2 или его соль в эффективном количестве, и меньшей мере один фармацевтический эксципиент.
4. Применение соединения формулы I по любому из пп.1, 2 или его соли, для получения лекарственного средства, предназначенного для лечения ожирения и/или диабета.
5. Применение соединения формулы I по любому из пп.1, 2 или его соли, для получения лекарственного средства, предназначенного для лечения заболевания, выбранного из заболеваний центральной нервной системы, нарушения сна, нарколепсии, болезни Альцгеймера и других видов деменции, болезни Паркинсона, нарушения внимания у гиперкинетических детей, нарушения памяти и трудностей в обучении, эпилепсии, шизофрении, умеренных нарушений психических процессов, ведущих к познанию и действию, депрессии и тревоги, состояния тревоги, вызванного ожиданием или алкогольной, наркотической зависимостью, мании, сезонных эмоциональных нарушений, мигрени и тошноты.
6. Применение соединений формулы II
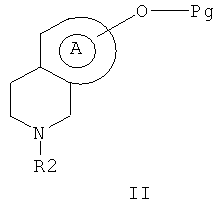
в которой Pg обозначает атом водорода или защитную группу и R2 и А такие, как определены по любому из пп.1, 2, для получения соединений формулы I по любому из пп.1, 2.
7. Способ получения соединений формулы I, в которой R1, R2, l, m, n и цикл А такие, как определены по формуле I по любому из пп.1, 2, путем проведения следующей реакции:
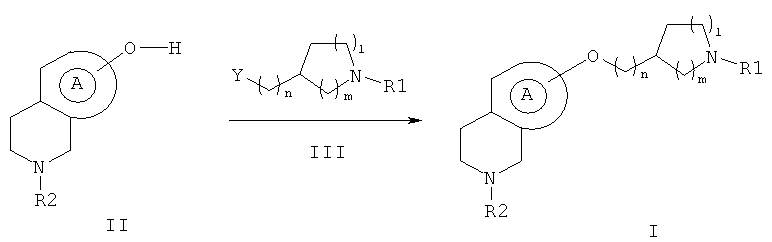
в которой происходит нуклеофильное замещение путем взаимодействия фенола формулы II, в которой R2 и цикл А такие, как определены по формуле I, с амином формулы III, в которой R1, l, m и n такие, как определены по формуле I, и Y обозначает атом галогена или обозначает псевдогалоген, такой как мезилат, трифлат, тозилат, бросилат или нозилат, или обозначает группу гидрокси.
8. Способ получения по п.7, в котором соединение формулы II получают амино-восстановлением путем взаимодействия вторичного амина формулы IV, в которой R2 обозначает Н,
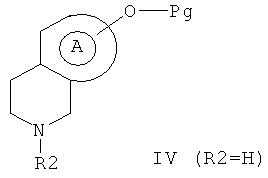
с альдегидом или кетоном формулы V (R3R4C(0)), где R3 и R4 образуют вместе в результате реакции R2, такой как определен по формуле I и неявляющийся водородом, по формуле VI
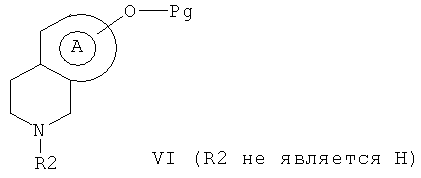
возможно с последующим снятием защиты.
9. Способ получения по п.7, в котором соединение формулы II получают нуклеофильным замещением путем взаимодействия соединения формулы VIa, в которой R2 обозначает бензотриазолилметильную группу,
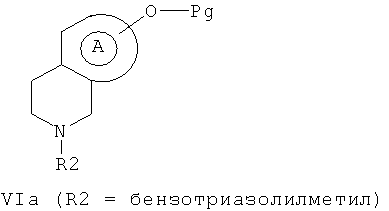
с реактивом Гриньяра формулы VII R5MgW, где W обозначает атом галогена, выбранный из хлора, йода и брома, и R5 обозначает С6-циклоалкил, моноциклический гетероарил, выбранный из тиофена, или арильную группу, выбранную из фенила; после взаимодействия получают соединение формулы VIb, в которой R2 обозначает CH2R5
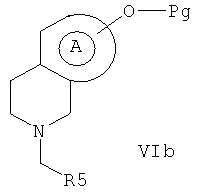
возможно с последующим снятием защиты.
| ЕР 1070714 А, 24.01.2001 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОИЗОХИНОЛИНА И ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2000 |
|
RU2256661C2 |
Авторы
Даты
2011-05-20—Публикация
2006-11-22—Подача