Изобретение относится к биотехнологии, предназначено для оптимизации процесса получения регенерантных растений в культуре регенерирующих в течение длительного периода времени каллусных тканей и может быть использовано в селекции при клонировании ценных, в том числе и рекомбинантных, генотипов проса.
Известный способ получения регенерантных растений проса в культуре пыльников и сегментов незрелых соцветий включает три важных этапа: 1) дедифференциацию клеток эксплантов и формирование эмбриогенных каллусных тканей; 2) стимулирование регенерационного процесса; 3) длительное культивирование регенерирующих каллусных тканей на среде без регуляторов роста с последовательным переводом корнесобственных регенерантов в нестерильные условия [1, 2]. Получение клонов регенерантных растений происходит, в основном, на третьем этапе. Его продолжительность достаточно велика и может исчисляться годами.
Особенность биологии каллусных тканей, заключающаяся в сочетании процессов пролиферации клеток каллусной массы и регенерации корнесобственных растений, позволяет переводить регенераты в нестерильные условия и переносить регенерирующие участки ткани на свежие среды в один и тот же момент времени. Тем не менее, несмотря на достаточную простоту кло-нирования проса, в литературе не приведены рациональные способы осуществления этого процесса.
Цель изобретения состоит в установлении последовательности технологических операций для получения заданного числа регенерантных растений в любой удобный для их массового клонирования период времени.
Регенерирующие каллусные ткани проса получают в культурах соматических тканей и пыльников. Изолирование эксплантов происходит в различное время года у растений, растущих летом в полевых условиях и в осенний, зимний и весенний периоды в тепличных боксах. Однако потребность в регенерантах не всегда соотносится со временем получения регенерирующих каллусных тканей. Напротив, она имеет смысл только тогда, когда известно, что существуют условия выращивания регенерантов в тепличных боксах или полевых условиях, с жестко регламентированным сезонным сроком посева или высадки. Учитывая способность регенерирующих каллусных тканей к длительному субкультивированию in vitro целесообразно поддерживать их в малых объемах до наступления благоприятного для массового клонирования периода.
Для получения запланированного числа регенерантных растений и определения времени клонирования предложена технология, включающая ряд существенных этапов:
А. В процессе субкультивирования каллусных тканей в малых объемах определяют оптимальный интервал пересадок. Его величину находят путем пересчета числа регенерантов, пригодных для перевода в нестерильные условия, на 1 сутки культивирования. Максимальное число регенерантов указывает на оптимальный интервал пересадок.
Б. Определяют число участков регенерирующих каллусных тканей (q) в пересчете на единицу культуральной посуды для переноса на свежие среды. Затем с учетом первоначального числа регенерантов в каллусных тканях определяют число регенерантных растений на различных этапах клонирования и количество пересадок, необходимое для получения запланированного числа регенерантных растений.
Формула определения числа регенерантов на любом этапе клонирования представляет собой геометрическую прогрессию
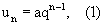
где а - число регенерантных растений, пригодных к переводу в нестерильные условия, в начале клонирования;
q - число участков одной регенерирующей каллусной ткани, пересаживаемых на свежие среды;
un - число регенерантов на на n-м этапе клонирования.
По правилу суммирования членов геометрической прогрессии определяют общее число получаемых регенерантных растений
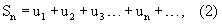
или
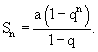
Формулу 2 преобразуют с целью определения необходимого числа этапов клонирования при запланированном суммарном числе регенерантных растений
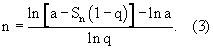
Этапы клонирования представляют все члены геометрической прогрессии, включая начальный клоновый материал. Следовательно, число пересадок на единицу меньше числа членов. Число пересадок (р), необходимых для получения запланированного числа регенерантных растений (Sp) находят по формуле
р=n-1,
или
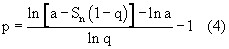
В. Проводят определение числа регенерантов и единиц культуральной посуды для последней неполной пересадки.
Расчетное число пересадок, как правило, не является целым числом. Поэтому для получения заданного числа регенерантных растений выполняют все полные пересадки, а для последней берут только часть имеющегося в наличии материала. Исходное число регенерантных растений (a1) для проведения последней неполной пересадки вычисляют по формуле
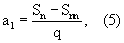
где Sn - запланированное число регенерантных растений на этапе клонирования n=p+1;
Snn - сумма регенерантных растений на последнем полном этапе клонирования n=р+1, где р = целое число.
Следует отметить, что вычисление величины Snn производится по формуле 2. Для последней пересадки берут столько единиц культуральной посуды, чтобы в ней было представлено число регенерантных растений, равное a1.
Для определения суммарного времени получения заданного числа регенерантов длительность интервала пересадок умножают на их число.
Пример. Изучали три длительно культивируемых каллусных клона, полученных в культуре пыльников гибридов проса F3: Могарообразное 2009 × Соргообразный карлик 2010 - клон gm 1, Регенерант 20 №10 × Соргообразный карлик 1959 - клон gm 1, Соргообразный карлик 2010 × Могарообразное 2009 - am26. Каллусные клоны получены на средах, содержащих соли MS [3], витамины В5 [4], L-глутамин (L-глутаминовую кислоту) - 500 мг/л, глицин - 2 мг/л, мио-инозитол - 500 мг/л, 2,4-Д (2,4-дихлорфеноксиуксусная кислота) - 2 мг/л. Стимулирование регенерационного процесса проведено на среде R1, включающей соли MS, витамины В5, мио-инозитол - 100 мг/л, глицин – 2 мг/л, 6-БАП (6-бензиламинопурин) - 10 мг/л, α-НУК (α-нафтилуксусная кислота) - 0,5 мг/л. Регенерирующие каллусные ткани культивировали с последовательным переводом регенератных растений в нестерильные условия на среде МС (МС=R1 без регуляторов роста) [1].
На всех этапах эксперимента использовали в качестве химической посуды стаканчики 60×35 см. В каждом стаканчике представлена 1 регенерирующая каллусная ткань. В условиях среды МС клон gml культивировали 895 суток, аm129 - 775, am26 - 805.
В процессе культивирования изучали изменение числа регенерантных растений выше 1,5 см, выделяемых в нестерильные условия на 5, 10, 15, 20, 25, 35, 40, 50 сутки культивирования in vitro.
Экспериментальные данные обрабатывали с использованием компьютерной программы двухфакторного дисперсионного анализа.
Установили, что существенное увеличение числа регенерантных растений наблюдалось на 20 сутки культивирования каллусных тканей (табл.1). Однако наибольшее число регенерантов получено на 35 сутки культивирования. После этого периода отмечалось уменьшение их числа.
Оптимальное время пересадок каллусных тканей, удовлетворяющее требованиям получения наибольшего выхода регенерантов при наименьших затратах времени и реактивов, определяли путем перерасчета числа регенерантных растений на одни сутки культивирования in vitro (табл.1)
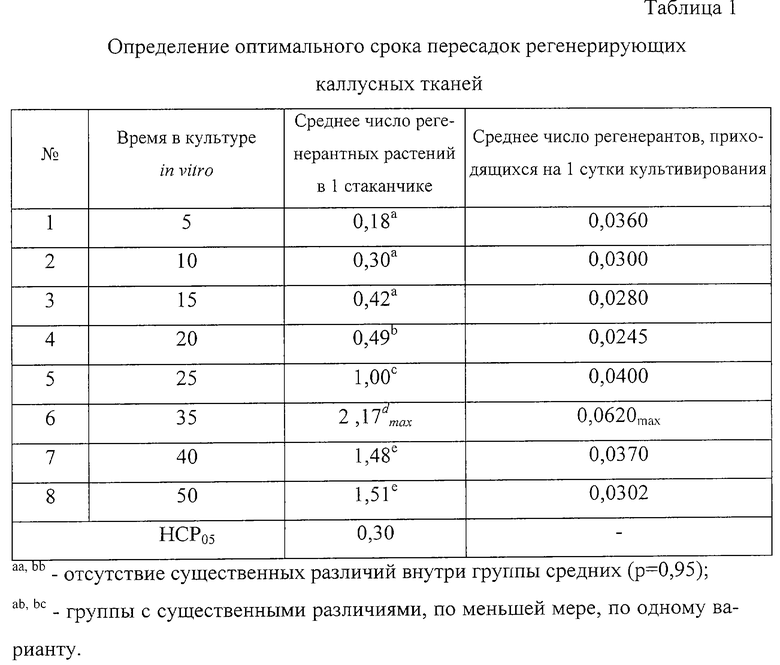
Для анализа использовали усредненные значения чисел регенерантных растений трех каллусных клонов: gml, am29 и am26. Максимальное число регенерантных растений, приходящееся на одни сутки культивирования, указывало на оптимальный срок пересадок. В данном опыте оптимальным временем пересадок являются 35 сутки культивирования каллусных тканей.
Из таблицы 1 видно, что на 35 сутки культивирования среднее число регенерантных растений в 1 стаканчике равно 2,17.
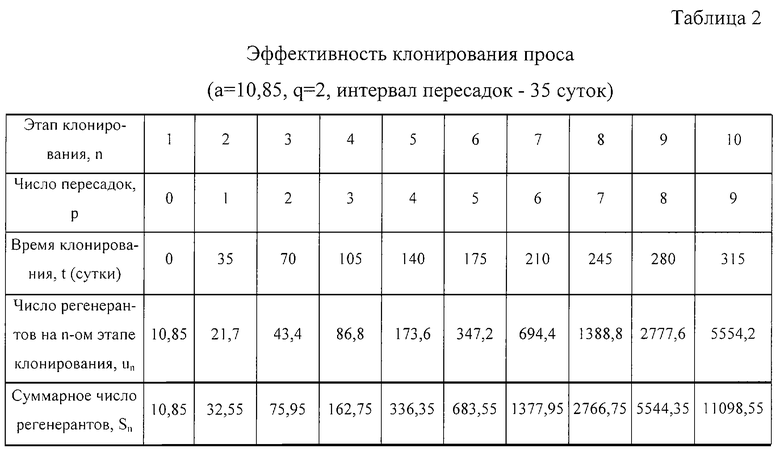
Если принять, что на начало клонирования имеются в наличии 5 стаканчиков, то исходное число регенерантов а=2,17×5=10,85. Если число участков одной регенерирующей ткани, переносимых на свежие среды q=2, то можно рассчитать количество регенерантных растений (un) на отдельных этапах (n) клонирования, их суммы (Sn) и согласовать полученные данные с числом пересадок (р) и длительностью (t) клонирования (табл.2).
Из таблицы 2 следует, что предложенный способ получения клонов регенерантных растений обеспечивает получения регенерантных клонов в больших количествах и, поэтому, достаточно эффективен для использования в практической селекции.
Формула 4 для расчета числа пересадок при заданном объеме регенерантов позволяет гибко управлять процессом клонирования. Например, если необходимо получить 1000 регенерантных растений при условии, что а=10,85 и q=2, то число пересадок, вычисленное по формуле 4, будет равно:
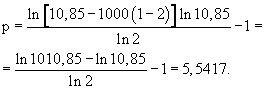
Это означает, что проводятся 5 полных пересадок. Затем вычисляют суммарное число регенерантных растений Snn на n=р+1=5+1=6 этапе клонирование по формуле 2
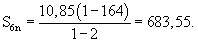
Используя формулу 5, получают исходное число регенерантов для последней неполной пересадки
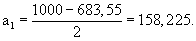
Учитывая, что в одном стаканчике, в среднем, находится 2,17 регенерантных растений, вычисляют число используемых стаканчиков
158,225:2,17≈73.
ЛИТЕРАТУРА
1. Бобков С.В. Вестник РАСХН. 2000. - №5. - С.41-43.
2. Бобков С.В. Регенерация корнесобственных растений в культурах незрелых соцветий и пыльников проса (Panicum miliaceum L.) // Вопросы физиологии, селекции и технологии возделывания сельскохозяйственных культур. - Орел: Орелиздат, 2001. - С.134-141.
3. Murashige Т., Skoog F. A revised medium for rapid growth and bioassays with tobacco tissue cultures // Physiology of plant. - 1962. - V.15. - №13. - Р.473-497.
4. Gamborg O., Evelegh D.E. Culture methods and detection of gluconases in cultures of wheat and barley // Can.J. Biochem. - 1968. - №5. - P.417-421.
Изобретение предназначено для использования в области сельского хозяйства. Способ включает длительное непрерывное культивирование регенерирующих каллусных тканей. Для реализации технологического процесса получения заданного числа регенерантов к необходимому моменту времени устанавливают оптимальный интервал пересадок. Для этого определяют максимальное число регенерантов, пригодных для перевода в нестерильные условия в пересчете на 1 сутки культивирования. Определяют число участков одной каллусной ткани с сочетанием процессов пролиферации и регенерации для переноса на свежие среды и исходное число регенерантов, пригодных для перевода в нестерильные условия. При этом для определения числа регенерантов на любом этапе клонирования используют математическую зависимость, представляющую собой геометрическую прогрессию 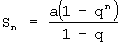 , где а - число регенерантных растений, пригодных к переводу в нестерильные условия, в начале клонирования; q - число участков одной регенерирующей каллусной ткани, пересаживаемых на свежие среды, число пересадок находят по формуле
, где а - число регенерантных растений, пригодных к переводу в нестерильные условия, в начале клонирования; q - число участков одной регенерирующей каллусной ткани, пересаживаемых на свежие среды, число пересадок находят по формуле 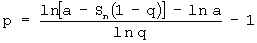 , число регенерантов для участия в последней неполной пересадке вычисляют, используя формулу
, число регенерантов для участия в последней неполной пересадке вычисляют, используя формулу 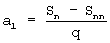 , a1 - исходное число регенерантных растений; Sn - запланированное число регенерантных растений на этапе клонирования n=p+1; Snn - сумма регенерантных растений на последнем полном этапе клонирования n=р+1, где р - целое число, а для развертывания массового клонирования регенерантов в любой удобный период времени каллусные ткани длительное время поддерживают in vitro в малом количестве. Изобретение позволяет установить последовательность технологических операций для получения заданного числа регенерантных растений в любой удобный для их массового клонирования период времени. 2 табл.
, a1 - исходное число регенерантных растений; Sn - запланированное число регенерантных растений на этапе клонирования n=p+1; Snn - сумма регенерантных растений на последнем полном этапе клонирования n=р+1, где р - целое число, а для развертывания массового клонирования регенерантов в любой удобный период времени каллусные ткани длительное время поддерживают in vitro в малом количестве. Изобретение позволяет установить последовательность технологических операций для получения заданного числа регенерантных растений в любой удобный для их массового клонирования период времени. 2 табл.
Способ оптимизации клонирования проса (Panicum miliaceum L.), включающий длительное непрерывное культивирование регенерирующих каллусных тканей, отличающийся тем, что для реализации технологического процесса получения заданного числа регенерантов к необходимому моменту времени устанавливают оптимальный интервал пересадок, для чего определяют максимальное число регенерантов, пригодных для перевода в нестерильные условия в пересчете на 1 сутки культивирования, определяют число участков одной каллусной ткани с сочетанием процессов пролиферации и регенерации для переноса на свежие среды и исходное число регенерантов, пригодных для перевода в нестерильные условия, при этом для определения числа регенерантов на любом этапе клонирования используют математическую зависимость, представляющую собой геометрическую прогрессию
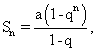
где а - число регенерантных растений, пригодных к переводу в нестерильные условия, в начале клонирования;
q - число участков одной регенерирующей каллусной ткани, пересаживаемых на свежие среды, число пересадок находят по формуле
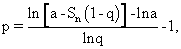
число регенерантов для участия в последней неполной пересадке вычисляют, используя формулу
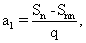
где a1 - исходное число регенерантных растений;
Sn - запланированное число регенератных растений на этапе клонирования n=p+1;
Snn - сумма регенерантных растений на последнем полном этапе клонирования n=р+1, где р - целое число, а для развертывания массового клонирования регенерантов в любой удобный период времени каллусные ткани длительное время поддерживают in vitro в малом количестве.
| БОБКОВ С.В | |||
| Регенерация корнесобственных растений в культурах незрелых соцветий и пыльников проса (Panicum miliaceum L.) | |||
| Вопросы физиологии, селекции и технологии возделывания сельскохозяйственных культур | |||
| -Орел: Орелиздат, 2001, с.134-141 | |||
| Вестник РАСХН, 2000, №5, с.41-43 | |||
| MURASHIGE Т | |||
| et al | |||
| A revised medium for rapid growth and bioassays with tobacco tissue cultures | |||
| Phisiology of plant, 1962, v.15, №13, p.417-421. |
Авторы
Даты
2004-04-20—Публикация
2001-11-08—Подача