Область изобретения
Настоящее изобретение относится к усовершенствованному и экономичному способу получения 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазина, который также известен как ламотригин. Он представляет новый структурный класс противоэпилептического лекарственного средства.
Обоснование изобретения
Всегда существует потребность в лекарственных средствах, которые будут эффективными для пациентов, которые неудовлетворительно реагируют на общепринятые противоэпилептические средства. Кроме того, селективность специфического механизма действия снижает бремя побочного действия, как в случае с ламотригином, то есть 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазином (I). Ламотригин, селективный блокатор натриевых каналов, который ингибирует высвобождение синаптосомальных возбуждающих нейротрансмиттеров, представляет собой зависимый от использования и вольтажа или напряжения ингибитор пресинаптических натриевых каналов.
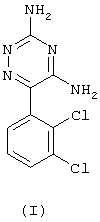
Ламотригин может быть получен в соответствии с известным из литературы способом, описанным в патенте США 4602017, который включает взаимодействие 2,3-дихлор-ацилхлорида с цианидом меди и йодидом калия в среде сухого ксилола, взаимодействие полученного в результате дихлорацилцианида с бикарбонатом аминогуанидина и циклизацию продукта реакции в присутствии 10% метанольного КОН или н-пропанола с получением ламотригина.
В патенте США 4602017 хлорангидрид кислоты (II) (1 моль эквивалент) превращали в ацилцианид (III) (реакция 1) с использованием цианида металла, а именно цианида меди (~2,4 моль эквивалента), и йодида калия (~2,4 моль эквивалента), в сухом ксилоле (~20 объем/вес хлорангидрида кислоты) в качестве растворителя.
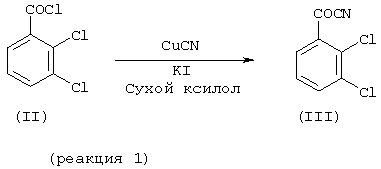
При реакции превращения хлорангидрида кислоты (II) в ацилцианид (III), как в реакции 1, объемные количества растворителя - сухого ксилола, требуется реактор крупного размера для относительно небольших количеств хлорангидрида кислоты.
Использование йодида калия, кроме того, увеличивает стоимость процесса. На конечной стадии циклизации спиртовой растворитель, то есть спиртовой КОН, дополнительно увеличивает стоимость.
Конечно заслуживает внимания активирование цианида меди использованием йодида металла.
Однако, принимая во внимание стоимость йодида металла, а именно йодида калия, настоящее изобретение исследует возможность избежания его использования с целью снижения стоимости производства. Кроме того, использование растворителя, а именно ксилола, в таких больших количествах увеличивает стоимость продукта.
Изложение сущности изобретения
Целью настоящего изобретения является предоставление способа получения ламотригина, который является эффективным по стоимости.
Еще одной целью настоящего изобретения является предоставление способа получения ламотригина, который не использует йодида калия или спиртового гидроксида калия и требует меньшего количества растворителя, такого как толуол или ксилол, которые используются только как сорастворители.
Еще одной целью изобретения является предоставление способа получения ламотригина высокой степени чистоты, в высокой степени удовлетворительного профиля по примесям, белого цвета, свободно текущего, с более низким содержанием влаги, который действенно и эффективно сушится и может легко превращаться в фармацевтические композиции.
Соответственно, настоящее изобретение предоставляет усовершенствованный способ получения 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазина формулы I, который включает стадии:
(а) взаимодействия 2,3-дихлорбензоилхлорида (II) с цианидом меди в присутствии ацетонитрила и сорастворителя с получением дихлорбензоилцианида (III)
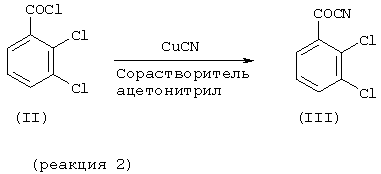
(b) взаимодействия дихлорбензоилцианида (III), полученного на стадии (а), с бикарбонатом аминогуанидина с получением промежуточного продукта формулы (IV)
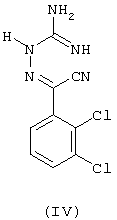
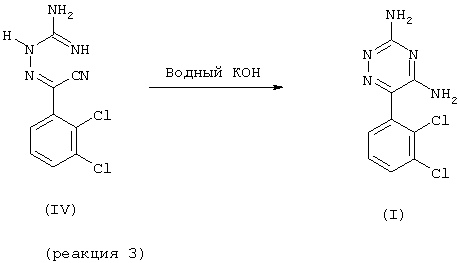
(с) циклизации названного промежуточного продукта формулы IV в присутствии водного гидроксида калия с получением 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазина
Подробное описание изобретения
Настоящее изобретение направлено на снижение стоимости ламотригина, обеспечивает промышленно экономичный способ получения ламотригина, то есть 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазина (I).
В данном изобретении 2,3-дихлорбензоилхлорид (II) трансформируется в 2,3-дихлорбензоилцианид (III), который представляет строительный блок для гетероциклического кольца, как показано выше в реакции 2. Ацетонитрил используется для образования комплекса с цианидом меди. Цианид меди, закомплексованный с ацетонитрилом в качестве растворителя, дает хороший выход. Ацетонитрил также образует часть системы растворителя, например ацетонитрил : толуол или ацетонитрил : ксилол. Таким образом, использование избытка сухого ксилола заменяется смесью ацетонитрила и толуола/ксилола в соотношении от 1:6 до 1:3 и более предпочтительно 1,2:6. Использование толуола помогает увеличить температуру реакции. Использование йодида калия также исключается. Благодаря данной модификации также снижены требования к размеру реактора. В другом аспекте циклизацию промежуточного продукта (IV) (получаемого по реакции ацилцианида (III) с бикарбонатом аминогуанидина) для образования гетероароматической кольцевой системы ламотригина можно осуществлять, используя 0,5 - 1,5% водный КОН, предпочтительно 0,95 - 1,06% водный КОН (как показано в реакции 3), вместо 10% метанольного КОН или только н-пропанола, что является дорогостоящим.
В то время, как реакция стадии (b) осуществляется при комнатной температуре, предпочтительный температурный интервал для реакции стадии (а) составляет от 40°С до температуры кипения с обратным холодильником, и температура циклизации стадии (с) составляет от 80°С до температуры кипения с обратным холодильником.
С помощью данного пути проведения реакции выход ламотригина улучшается примерно на 5%.
С целью получения ламотригина высокой степени чистоты, высоко удовлетворительного профиля в смысле примесей, белого по цвету, свободно текучего, имеющего более низкое содержание влаги, который может действенно и эффективно сушиться и может легко превращаться в фармацевтические композиции, осуществляют обработку активированным углем в спирте, таком как метанол.
Примеры получения
Изобретение подробно поясняется в следующих примерах, которые предоставляются только с целью иллюстрации, и, следовательно, не должны рассматриваться как ограничивающие объем изобретения.
Пример 1
К смеси 128 грамм цианида меди, 120 мл ацетонитрила и 200 мл толуола добавляют раствор 200 грамм 2,3-дихлорбензоилхлорида (II) в 250 мл толуола. Реакционную смесь кипятят с обратным холодильником в течение 16 часов. После фильтрования растворитель удаляют при пониженном давлении, получая 200 мл маслянистого 2,3-дихлорбензоилцианида (III).
Пример 2
К раствору 2,28 кг серной кислоты в 1,2 л воды добавляют 260 г аминогуанидинбикарбоната. Туда же добавляют 2,3-дихлорбензоилцианид, то есть соединение III (из примера 1) в 800 мл ацетонитрила и перемешивают в течение 60 часов. Твердое вещество отфильтровывают. Затем твердое вещество добавляют к водному NaOH. Смесь перемешивают в течение 1 часа при рН 11-12. Вещество, полученное после фильтрования, то есть соединение IV, используют в примере 3.
Пример 3
Соединение IV, полученное из 2,3-дихлорбензоилцианида (III), кипятят с обратным холодильником в 1,5 л 1% водного раствора КОН в течение 1,5 ч, получая белое твердое вещество. Его отфильтровывают и промывают водой, получая 107 г ламотригина, т.пл. 216-218°С.
ИК (КВr): 3450, 3315, 1646, 1619, 1557, 1490, 792 см-1.
1Н ЯМР (ДМСО, 400 МГц) δ: 7,61 (д, 1Н, J=1,5 Гц), 7,35 (т, 1Н, J=7,9 Гц), 7,26 (дхд, 1Н, J1=l,6 Гц, J2=7,6 Гц).
Масса 256,4 (100%).
Пример испытаний
20,4 кг ламотригина, полученного в результате проведения последующих стадий, указанных в примерах 1-3, растворяют в 700 литрах метанола путем нагревания в интервале температур 60-65°С в течение одного часа и добавляют 3 кг активированного угля. Полученную смесь фильтруют, концентрируют до 200 литров и охлаждают до 5-10°С. Ламотригин, полученный после фильтрации, сушат и проводят анализ с целью определения его физических свойств и чистоты. Данные испытаний приведены в таблице.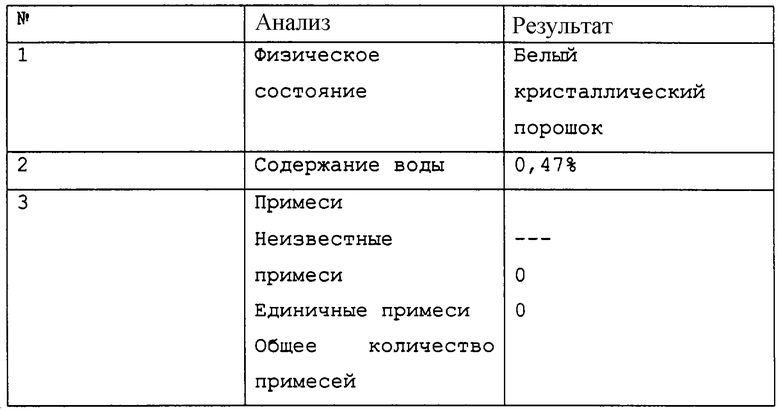
Как видно из таблицы, ламотригин получают в виде кристаллического порошка высокой степени чистоты, белого по цвету, свободно текучего, имеющего более низкое содержание влаги.
Описывается усовершенствованный способ получения 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазина, который включает стадии взаимодействия 2,3-дихлорбензоилхлорида с цианидом меди в присутствии ацетонитрила и сорастворителя с получением дихлорбензоилцианида, взаимодействия названного дихлорбензоилцианида с бикарбонатом аминогуанидина с получением промежуточного продукта, который циклизуют в присутствии водного гидроксида калия с получением 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазина. Данный способ позволяет упростить процесс и повысить выход целевого продукта. 1 н. и 8 з.п., ф-лы, 1 табл.
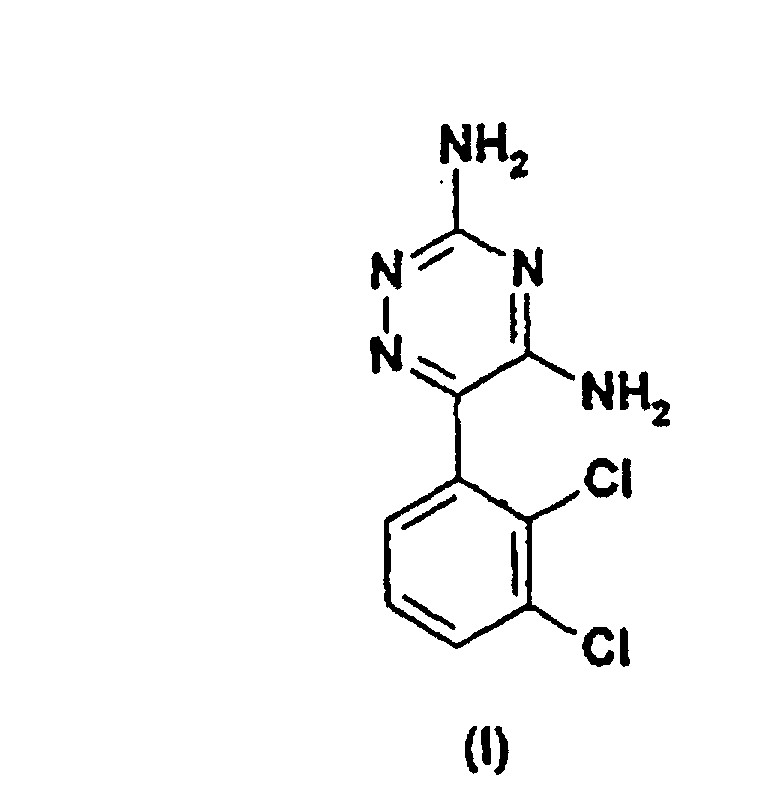
путем взаимодействия 2,3-дихлорбензоилхлорида (II)
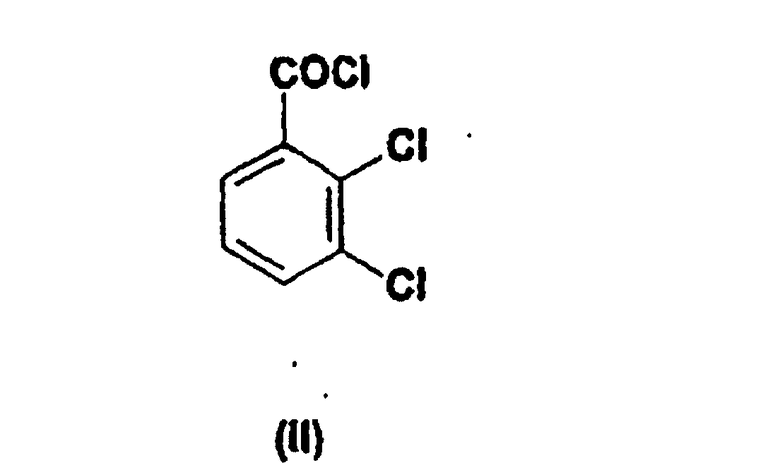
с цианидом меди CuCN в присутствии растворителя с получением дихлорбензоилцианида (III)
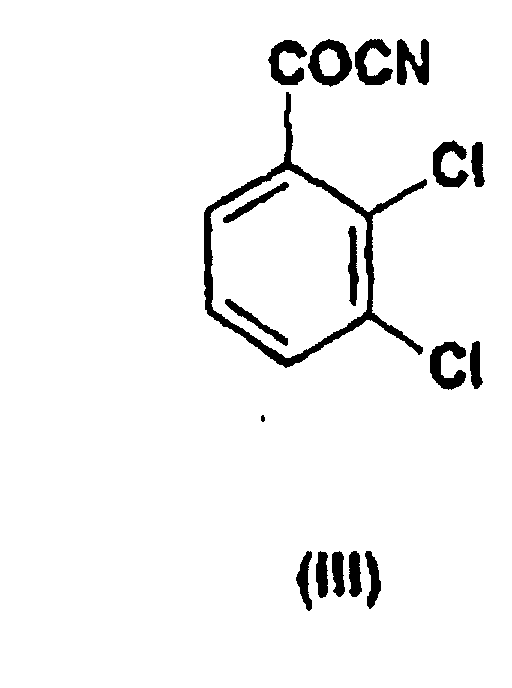
который подвергают взаимодействию с бикарбонатом аминогуанидина с получением промежуточного продукта формулы (IV)
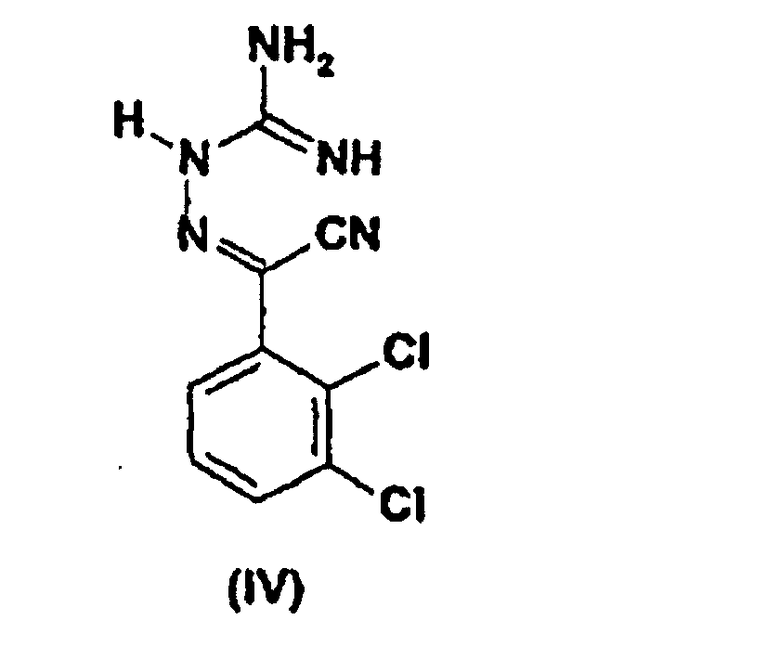
с последующей его циклизацией в присутствии раствора гидроксида калия и выделением целевого продукта, отличающийся тем, что в качестве растворителя на первой стадии процесса используют ацетонитрил и сорастворитель, а циклизацию соединения IV осуществляют в присутствии водного раствора гидроксида калия.
| US 4602017 A, 22.07.1986.FR 2741879 A, 06.06.1997.RU 97112881 C1, 15.04.1997.SU 799651 A, 08.05.1981. |
Авторы
Даты
2004-06-27—Публикация
1999-12-07—Подача