Изобретение относится к биохимической фармакологии и фармакодинамики, биохимической медицины, клеточной и молекулярной биологии, иммунофармакологии и прикладной медицины и может быть использовано в клинической медицине как противовоспалительное, ранозаживляющее, кровоостанавливающее, противораковое, антигельминтное и кардиотоническое средство. Данное вещество может использоваться как для стимуляции иммунной системы, так и для регуляции разнообразных метаболических процессов.
В настоящее время в клинической медицине для коррекции иммунных и метаболических процессов, а также для регуляции сердечно-сосудистых механизмов используются органические вещества природного происхождения. Это, как правило, препараты из экстрактов зобной железы, лимфатических узлов, соединительной ткани и селезенки. К таким лекарственным средствам относятся хорошо известные в клинической практике вещества - тимоген, Т-активин, миелопид, тимоптин и т.д. (Машковский М.Д. Препараты, корригирующие процессы иммунитета. В кн. Лекарственные средства, Харьков, “Торсинг”, т.2, 1997, с 199-207).
В последнее время внимание многочисленных исследователей привлек селен и его соединения, так называемые селеносодержащие белки, потому что именно биохимические функции селена определяются не самим микроэлементом, а селенопротеиновыми органическими веществами. Недостаток этого микроэлемента может приводить к нарушению клеточной целостности, изменению метаболизма тиреоидных гормонов, активности биотрансформирующих ферментов, усилению токсического действия тяжелых металлов, повышению концентрации глутатиона в плазме. Характерной особенностью селеносодержащих белков млекопитающих является то, что они связаны с окислительно-восстановительными процессами, происходящими внутри клетки и вне нее. К настоящему времени охарактеризованы двенадцать селеносодержащих белков, к числу которых относятся ферменты - глутатионпероксидаза, йодтирониндейодиназа, тиоредоксинредуктаза, селенфосфатсинтетаза и другие. Данные изотопного анализа и результаты теоретических исследований позволяют предполагать, что в организме млекопитающих может насчитываться от 20 до 100 селеносодержащих белков (В.А.Тутельян и др. в кн. Селен в организме человека, М., 2002 г., с.18-34).
К настоящему времени достаточно хорошо изучены биологические функции селена, в том числе механизм действия глутатионпероксидазы, процесс восстановления пероксинитритов под действием селеносодержащих белков, механизм взаимодействия селена с антиоксидантами, особенно с витаминами С, Е и А. Изучены также роль селена в возникновении и развитии кардиологических заболеваний, влияние селена на биосинтез простагландинов, влияние селена на репродукцию, а также роль селена в метаболизме ксенобиотиков (В.А.Тутельян и др. в кн. Селен в организме человека. М., 2002 г., с.88-117).
Представленные данные показывают, что селен и селеносодержащие белки являются необходимыми биологическими компонентами и регуляторами в осуществлении сложнейших метаболических процессов, в том числе окислительно-восстановительных, сосудистых, нейрогуморальных и других. В связи с этим особенно актуален вопрос получения таких биологически активных соединений селена, которые могли бы принимать непосредственное участие в нормализации и восстановлении целого ряда гомеостатических процессов. Однако полученные к настоящему времени лекарственные вещества селенового ряда представляют собой либо сам микроэлемент, или его соединения с витаминами, в том числе и аминокислотами, например цистеином или метионином. В связи с этим создаваемые лекарственные вещества нового класса должны в какой то мере по своему строению и механизму действия соответствовать селеносодержащим белкам, непосредственно осуществляющим разнообразные физиологические процессы - метаболические, иммунобиологические, репродуктивные, генопротекторные и другие.
Для решения поставленной задачи предлагаются лекарственные вещества, обладающие действием селеносодержащих белков. Они включают низкомолекулярный компонент - протеин, полученный экстракцией из протеиносодержащего растительного сырья органическими растворителями, селен, сесквитерпеновый лактон, туйон, анионы брома, терпингидрат, пинен и вербенол, азулен.
Полученные средства названы селенотерпенопротеиновыми органическими веществами. Сущность изобретения поясняется фиг.1-13.
Получение селенотерпенопротеинового органического вещества - СТП
В качестве исходных продуктов используют зеленую массу белковосодержащих растений, например злаковых, бобовых, листья кукурузы. Экстракцией из растительной массы извлекают протеин. Экстракцию осуществляют эфиром, этиловым спиртом, димексидом. Полученный экстракт выпаривают и производят лиофильную сушку. Порошок растворяют в 60-90%-ном растворе этилового спирта. В раствор вводят селен, полученный термолизом селеномочевины (из расчета 6-12 мкг на 1 мл раствора). Затем к смеси добавляют определенное количество сесквитерпенового лактона и помещают ее в электромагнитное высокочастотное поле (мощность 5·10-3 Вт/см, частота 20-30 МГц).
1. Вещество селенотерпенопротеин - СТП
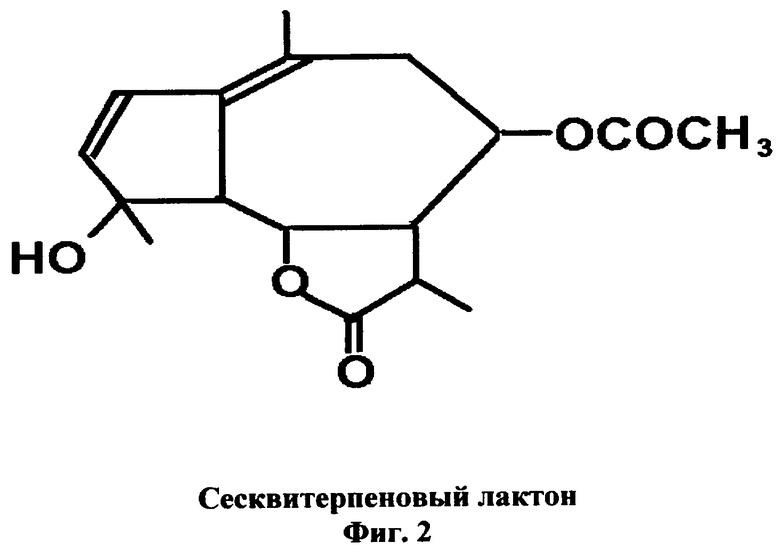
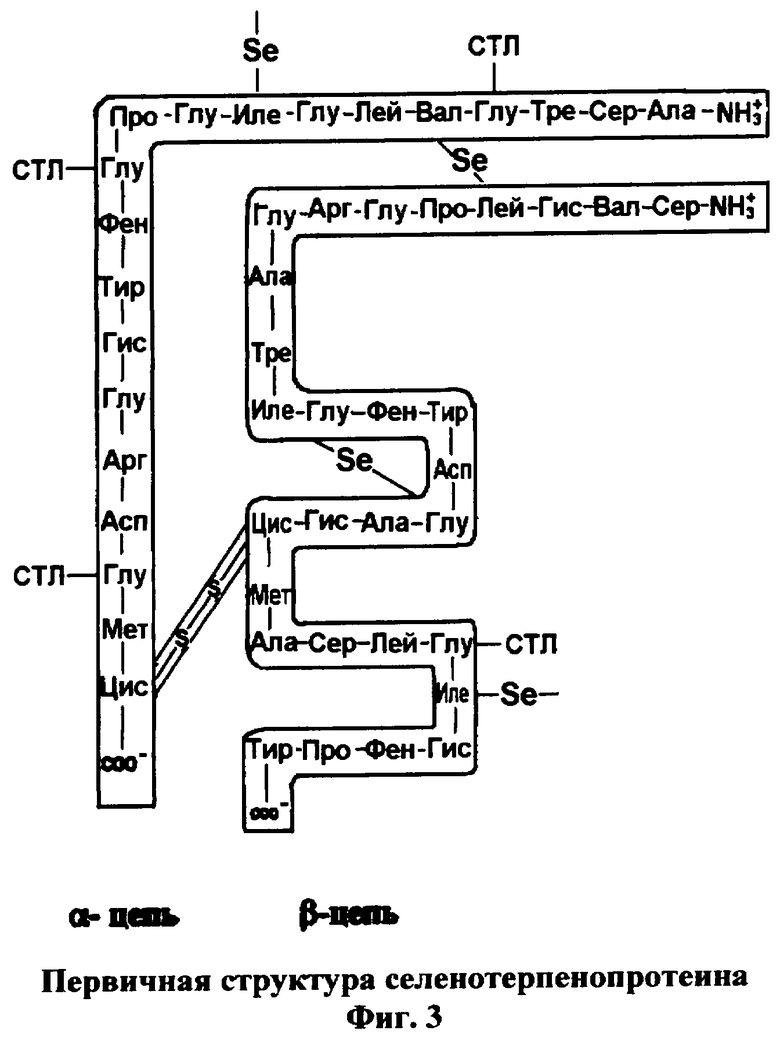
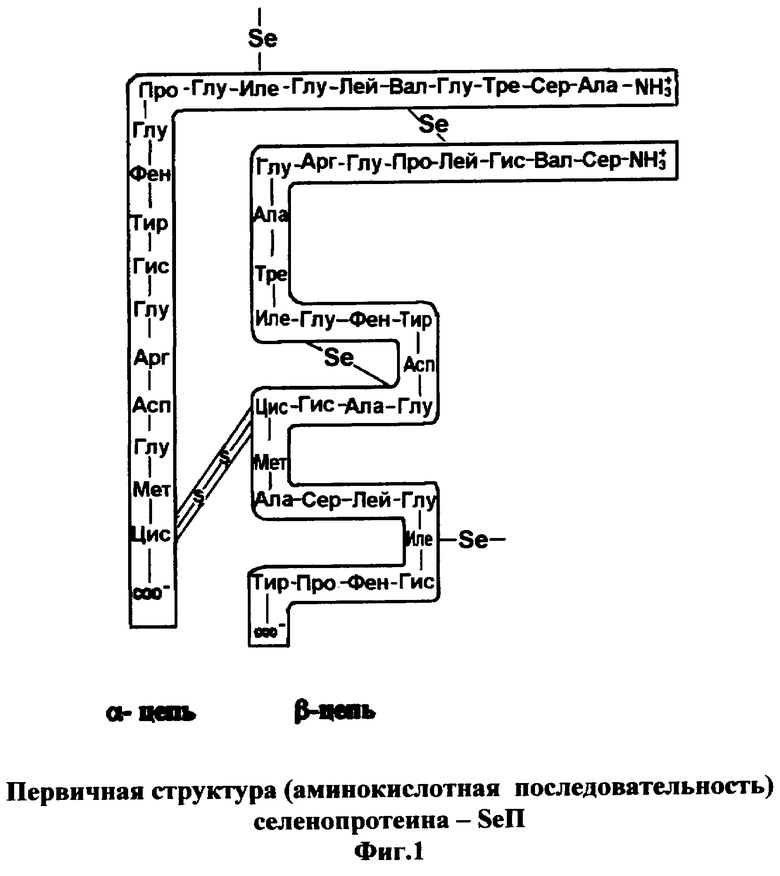
Вещество включает в себя молекулу селенопротеина (фиг.1), к которой присоединен сесквитерпеновый лактон - СТЛ (фиг.2), к карбоксильным группам боковых цепей - остаткам глутаминовой и/или аспарагиновой кислот и/или к С-концевым карбоксильным группам через сложно-эфирную связь (фиг.3). Молекула селенотерпенопротеина представляет собой две полипептоидные альфа- и бета-цепи, соединенные дисульфидным мостиком по остаткам цистеина (α-цепь состоит из остатков 20 аминокислот). Селен, полученный путем термолиза селеномочевины, входит в боковые алкильные радикалы аминокислот, соединяя некоторые звенья альфа- и/или бета-цепей одной или двух соседних молекул протеина, тем самым дополнительно “сшивая” их.
При всех физиологических значениях рН молекула селенотерпенопротеина ионизирована. Заряженными являются С- и N-концевые группы и связанные с α-углеродными атомами боковые цепи, содержащие карбоксильную или аминогруппу (-COO-, -NH
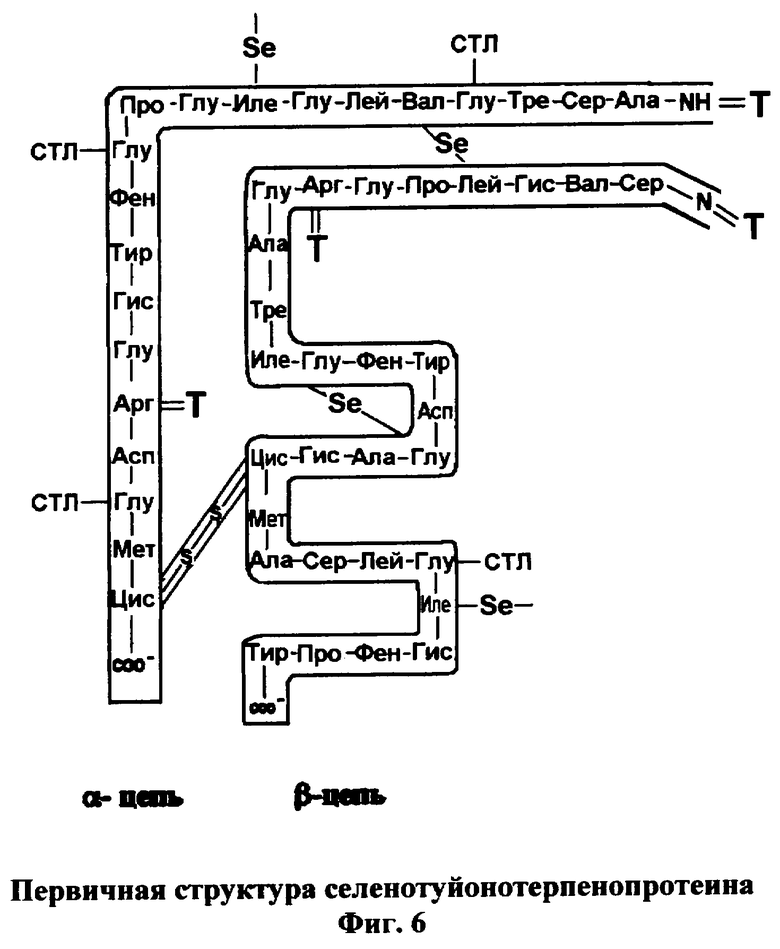
2. Вещество селенотуйонотерпенопротеин (фиг.6)
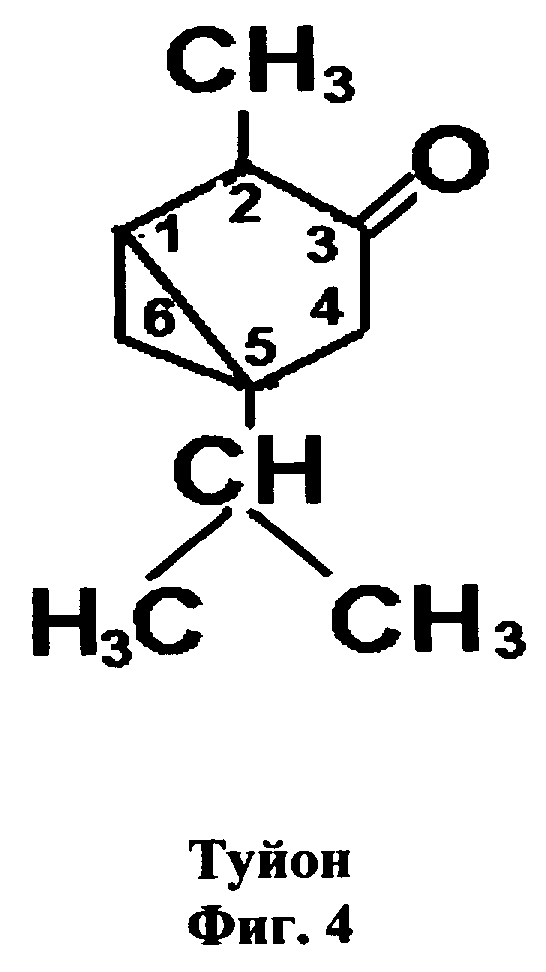
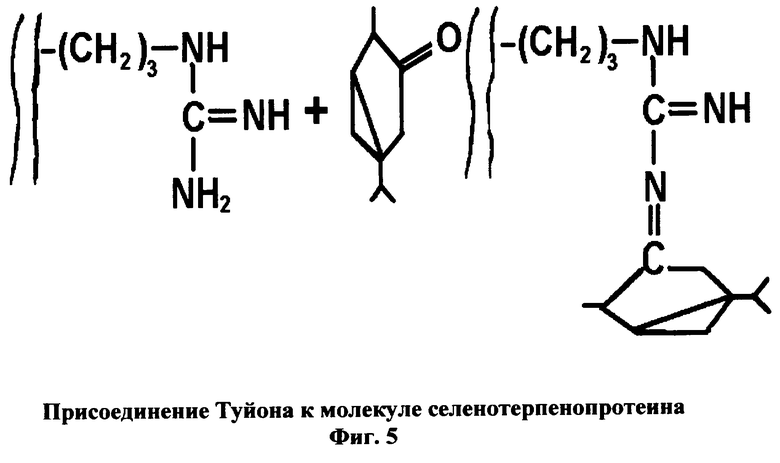
Вещество включает ионизированную молекулу селенотерпенопротеина (фиг.3), к которой присоединен кетон туйон - Т (фиг.4) через аминогруппы боковых цепей остатков аргинина и/или концевые аминогруппы (фиг.5).
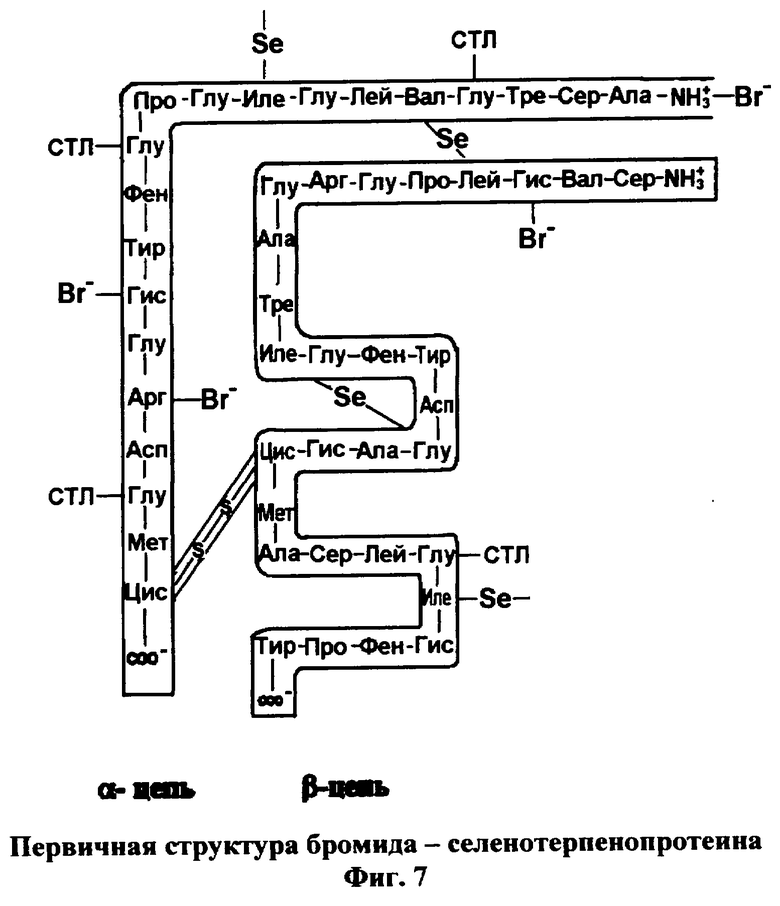
3. Вещество бромида-селенотерпенопротеин (фиг.7)
Вещество включает ионизированную молекулу селенотерпенопротеина, к которому по аминогруппам боковых цепей остатков аргинина и/или гистидина и/или концевым аминогруппам присоединены анионы брома (Вr-).
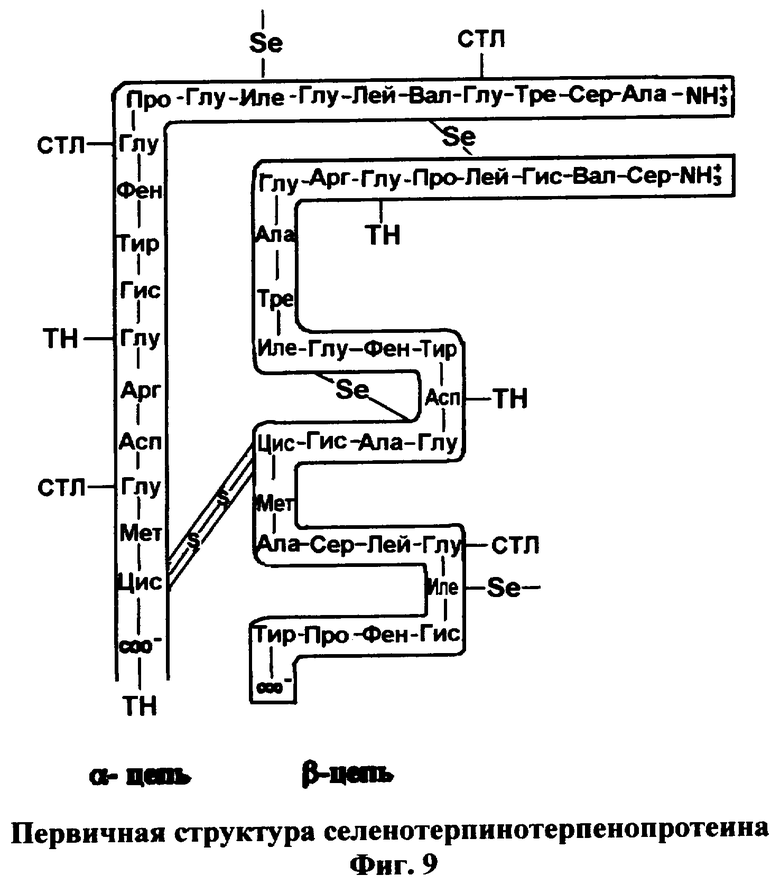
4. Вещество селенотерпинотерпенопротеин (фиг.9)
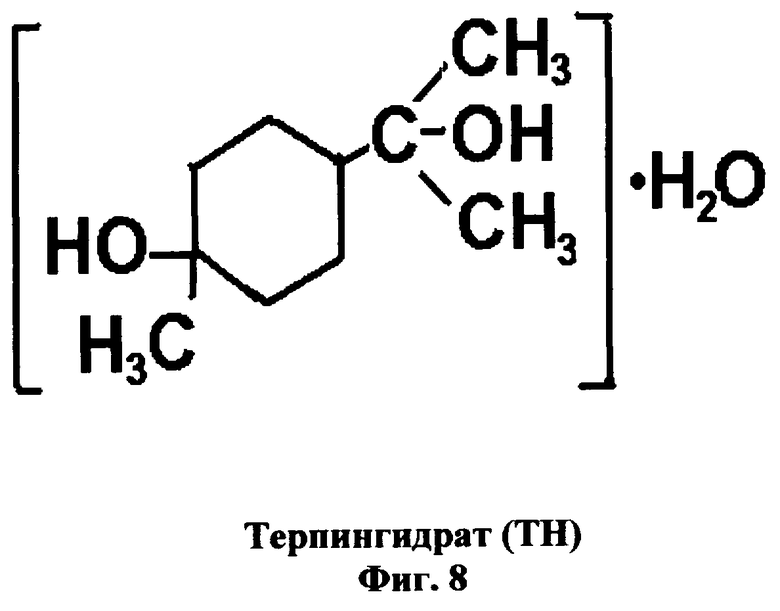
Вещество включает ионизированную молекулу селенотерпенопротеина, к которой присоединен терпингидрат - ТН (фиг.8) к карбоксильным группам боковых цепей остатков глутаминовой и/или аспарагиновой кислот и/или к С-концевым карбоксильным группам через сложно-эфирную связь.
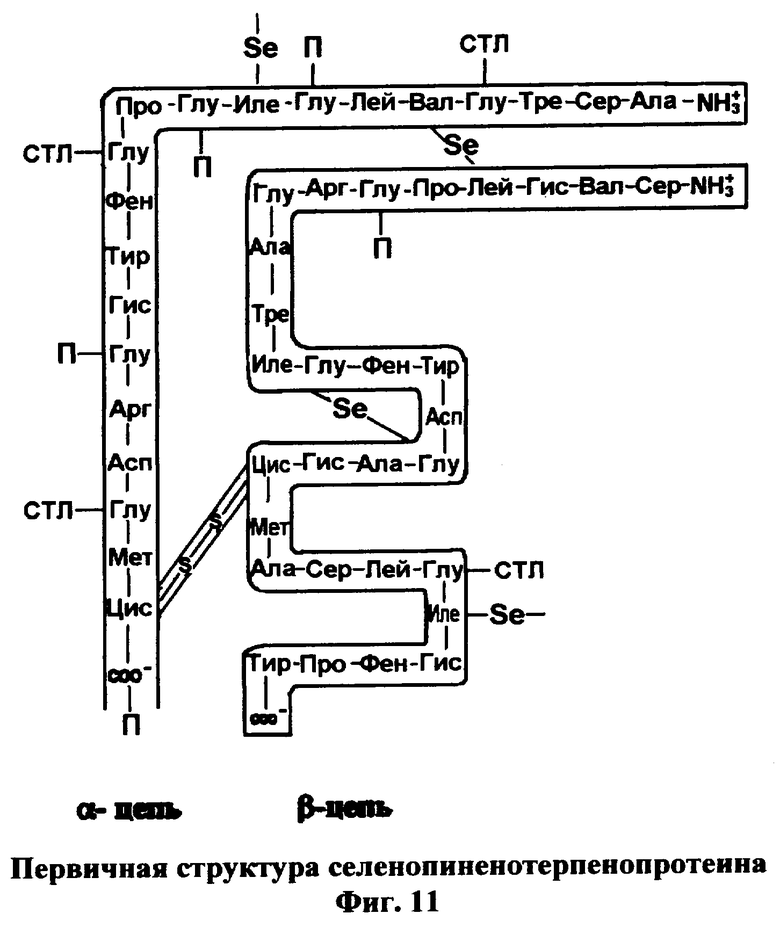
5. Вещество селенопиненотерпенопротеин (фиг.11)
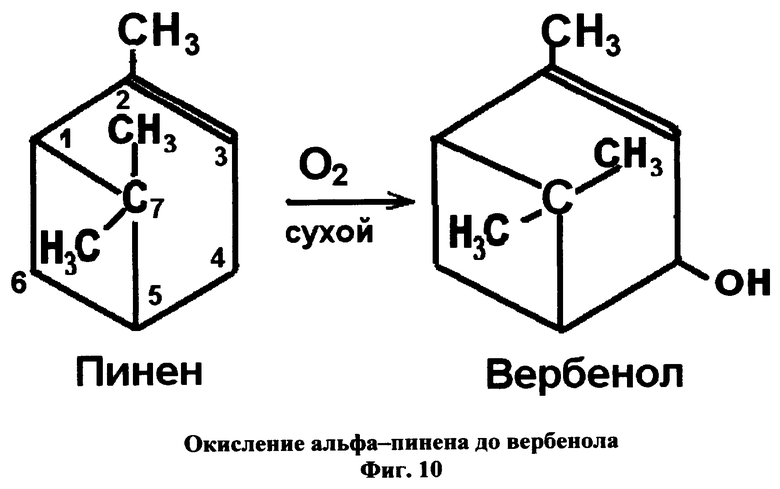
Вещество включает ионизированную молекулу селенотерпенопротеина (фиг.3), к которой присоединен альфа-пинен (П), предварительно окисленный до вербенола (фиг.10), к карбоксильным группам боковых цепей остатков глутаминовой и/или аспарагиновой кислот и/или к С-концевым карбоксильным группам через сложно-эфирную связь.
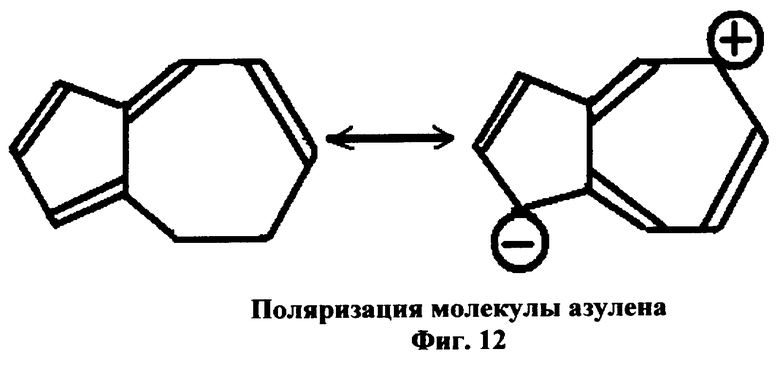
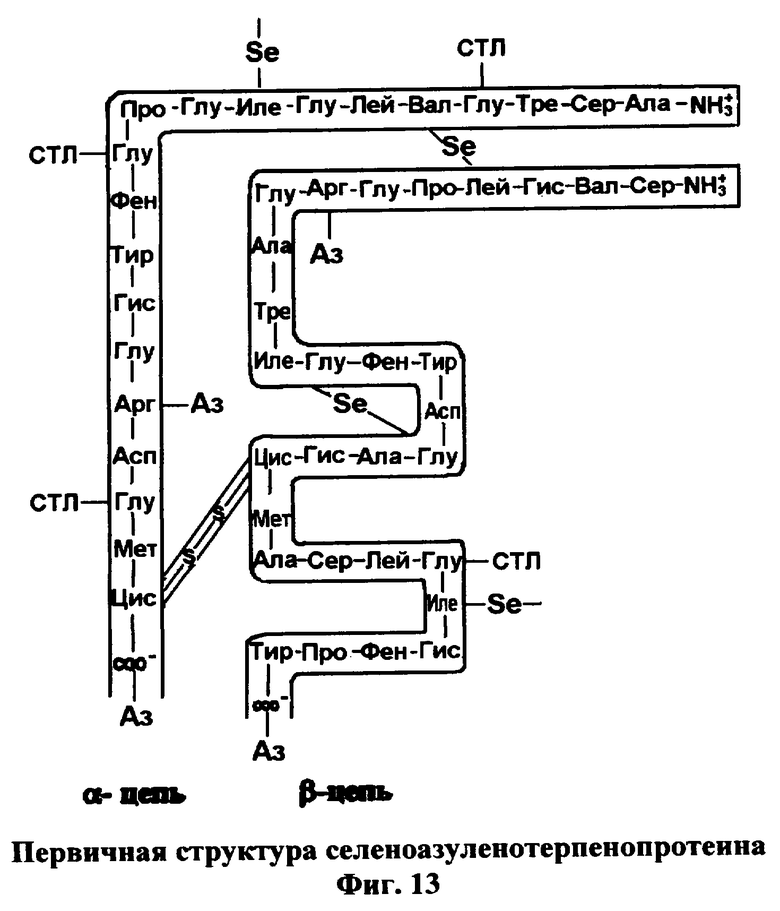
6. Вещество селеноазуленотерпенопротеин (фиг.13)
Вещество включает ионизированную молекулу селенотерпенопротеина (фиг.3), к которой присоединен азулен (Аз), в значительной степени поляризованный (фиг.12) по концевым карбоксильным (-) и амино-(+) группам и/или по боковым цепям аргинина (+), и/или гистидина (+), и/или глутаминовой кислоты(-), и/или аспарагиновой кислоты(-) (фиг.13).
Примеры получения селенотерпенопротеиновых органических веществ
Пример 1
Способ получения селенотерпенопротеина
К ионизированной молекуле селенопротеина добавляют необходимое количество сесквитерпенового лактона. Смесь выдерживают в электромагнитном высокочастотном поле (мощность 5·10-3 Вт/см, частота 20-30 МГц). Молярные соотношения СТЛ:селенопротеин 4:1.
Пример 2
Способ получения селенотуйонотерпенопротеина
К ионизированной молекуле селенотерпенопротеина добавляют необходимое количество кетона туйона. Смесь выдерживают в электромагнитном высокочастотном поле (мощность 5·10-3 Вт/см, частота 20-30 МГц). Молярные соотношения Т:селенотерпенопротеин 4:1.
Пример 3
Способ получения бромида-селенотерпенопротеина
К ионизированной молекуле селенотерпенопротеина добавляют необходимое количество анионов брома, полученных путем электролиза NaBr. Смесь выдерживают в электромагнитном высокочастотном поле (мощность 5·10-3 Вт/см, частота 20-30 МГц). Молярные соотношения Вr:селенотерпенопротеин 4:1.
Пример 4
Способ получения селенотерпинотерпенопротеина
К ионизированной молекуле селенотерпенопротеина добавляют необходимое количество терпингидрата. Смесь выдерживают в электромагнитном высокочастотном поле (мощность 5·10-3 Вт/см, частота 20-30 МГц). Молярные соотношения ТН:селенотерпенопротеин 4:1.
Пример 5
Способ получения селенопиненотерпенопротеина
К ионизированной молекуле селенотерпенопротеина добавляют необходимое количество пинена, предварительно окисленного до вербенола. Смесь выдерживают в электромагнитном высокочастотном поле (мощность 5·10-3 Вт/см, частота 20-30 МГц). Молярные соотношения П:селенотерпенопротеин 4:1.
Пример 6
Способ получения селеноазуленотерпенопротеина
К ионизированной молекуле селенотерпенопротеина добавляют необходимое количество азулена. Смесь выдерживают в электромагнитном высокочастотном поле (мощность 5·10-3 Вт/см, частота 20-30 МГц). Молярные соотношения Аз:селенотерпенопротеин 4:1.
Острую токсичность препарата исследовали при внутрибрюшинном введении Se-ТП в дозе 250 мг/кг мышам (возраст 6 недель, вес 28-30 г). Значение ЛД составило 700 мг/кг.
При исследовании общей токсичности мышам вводили Se-ТП в дозе 100 мг/кг в день внутрибрюшинно непрерывно в течение 10 дней. Снижение веса и каких-либо других нарушений при этом не отмечали, в последующем при наблюдении этих мышей в течение трех месяцев отклонений от нормы не выявлено.
В результате проведенных исследований установлено, что Se-ТП является органическим соединением, обладает выраженным биологическим действием, нетоксичен, полностью растворим в воде и биологических жидкостях - крови, лимфе и ликворе. В 1 мл Se-ТП содержится в зависимости от количества аминокислот в лиганде от 20 до 30 мг субстанции и 8-10 мкг селена.
Доза вводимого препарата зависит от клинического состояния больного, его возраста, веса, а также способа введения. Эффективная терапевтическая суточная доза для больного составляет от 6 до 150 мг активного вещества, которое вводят одномоментно или дробно.
Способ активации и стимуляции метаболических и иммунных процессов осуществляют следующим образом.
Полученный препарат Se-ТП представляет собой раствор активного вещества в 60-90%-ном этиловом спирте, 1 мл которого содержит 20-30 мг лекарственной субстанции. Se-ТП вводят перорально, внутримышечно, внутривенно, внутриартериально, а также наружно в виде суспензии в масляном растворе или в виде мази с масляно-спиртовым наполнителем.
При пероральном введении необходимую дозу рассчитывают следующим образом:
в 20 каплях раствора содержится 20-30 мг лекарственной субстанции;
в 10 каплях (1/2 мл) содержится 10-15 мг препарата;
в 5 каплях (1/4 мл) содержится 5 -7,5 мг препарата;
в 3 каплях (1/7 мл) содержится 3,3 мг препарата.
При внутримышечном, внутривенном или внутриартериальном введении препарат растворяют в физиологическом растворе для лучшей диссоциации в соотношении 1:10-1:20 при использовании 60%-ного спирта или 1:15 при 90%-ном спирте.
Например, при клинической патологии средней степени тяжести препарат вводят однократно в виде инъекции от 0,1 до 0,5 мл в день, при тяжелой степени патологии указанную дозу вводят два раза в день. При проведении интенсивной терапии препарат вводят внутримышечно или внутривенно (внутриартериально) по 1,0-2,0 мл соответственно с добавлением 10 или 20 мл физиологического раствора. В случае перорального введения в зависимости от возраста, веса и степени поражения - от 0,5 до 3,0 мл, причем препарат растворяют в 1/3 стакана кипяченой слегка теплой воды (36-38°С). Длительность лечения может колебаться от 1 до 3 месяцев, в случае тяжело протекающей патологии курс лечения повторяют с интервалом в 1-2 месяца до выраженного клинического эффекта. В период проведения лечения контролируют эффект терапии исследованием биохимических показателей и иммунологического статуса.
Изобретение относится к биохимической фармакологии и может быть использовано в клинической медицине как противовоспалительное, ранозаживляющее, кровоостанавливающее, противораковое, антигельминтное и кардиотоническое средство. Вещество с широким спектром биологического действия - селенотерпенопротеин. Оно содержит селенопротеин, селен и сесквитерпеновый лактон и получено под действием электромагнитного высокочастотного поля мощностью 5·10-3 Вт/см при частоте 20-30 МГц. Селенотерпенопротеин дополнительно содержит кетон туйон - селенотуйонотерпенопротеин; или анион брома - бромида-селенотерпенопротеин; или терпингидрат - селенотерпинотерпенопротеин или альфа-пинен - селенопиненотерпенопротеин; или азулен - селеноазуленотерпенопротеин. Предложенные вещества обеспечивают использование их как для стимуляции иммунной системы, так и для регуляции разнообразных метаболических процессов. 5 з.п.ф-лы, 13 ил.
| ТУТЕЛЬЯН В.А | |||
| и др | |||
| Селен в организме человека | |||
| - М., 2002, с.88-117.RU 2177323 С1, 27.12.2001.RU 2176916 С1, 20.12.2001.US 6545129 А, 08.04.2003. |
Авторы
Даты
2004-08-10—Публикация
2003-09-03—Подача